JP5426554B2 - ドネペジル塩、その多形体、その製造方法、応用方法および組成物 - Google Patents
ドネペジル塩、その多形体、その製造方法、応用方法および組成物 Download PDFInfo
- Publication number
- JP5426554B2 JP5426554B2 JP2010526129A JP2010526129A JP5426554B2 JP 5426554 B2 JP5426554 B2 JP 5426554B2 JP 2010526129 A JP2010526129 A JP 2010526129A JP 2010526129 A JP2010526129 A JP 2010526129A JP 5426554 B2 JP5426554 B2 JP 5426554B2
- Authority
- JP
- Japan
- Prior art keywords
- donepezil
- acid
- solution
- compound represented
- chemical formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- ADEBPBSSDYVVLD-UHFFFAOYSA-N COc(cc(CC(CC1CCN(Cc2ccccc2)CC1)C1=O)c1c1)c1OC Chemical compound COc(cc(CC(CC1CCN(Cc2ccccc2)CC1)C1=O)c1c1)c1OC ADEBPBSSDYVVLD-UHFFFAOYSA-N 0.000 description 1
- GXYXSFSEAKATQB-UHFFFAOYSA-N COc(cc(c(CC1CC2CCN(Cc3ccccc3)CC2)c2)C1=O)c2[O]=C Chemical compound COc(cc(c(CC1CC2CCN(Cc3ccccc3)CC2)c2)C1=O)c2[O]=C GXYXSFSEAKATQB-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/08—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms
- C07D211/18—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D211/30—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms with hydrocarbon radicals, substituted by doubly bound oxygen or sulfur atoms or by two oxygen or sulfur atoms singly bound to the same carbon atom
- C07D211/32—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms with hydrocarbon radicals, substituted by doubly bound oxygen or sulfur atoms or by two oxygen or sulfur atoms singly bound to the same carbon atom by oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C57/00—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms
- C07C57/02—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms with only carbon-to-carbon double bonds as unsaturation
- C07C57/13—Dicarboxylic acids
- C07C57/145—Maleic acid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C65/00—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C65/01—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing hydroxy or O-metal groups
- C07C65/03—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing hydroxy or O-metal groups monocyclic and having all hydroxy or O-metal groups bound to the ring
- C07C65/05—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing hydroxy or O-metal groups monocyclic and having all hydroxy or O-metal groups bound to the ring o-Hydroxy carboxylic acids
- C07C65/10—Salicylic acid
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Psychology (AREA)
- Anesthesiology (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Hydrogenated Pyridines (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
日本国特開昭64-79151(US4895841、EP296560) では、いくつかのドネペジル塩が開示され、特に老人性認知症の予防・治療薬として良好な薬効を有する塩酸塩がアルツハイマー病の予防・治療薬としての応用およびこれらの薬物の産業的製造方法が開示された。中国特許出願CN1874998Aではドネペジルシュウ酸塩の製造方法及び結晶多形が開示された。
老人性認知症は主に高齢者で発生する一般的な疾病であり、進行性認知障害と記銘力障害を主とする中枢神経系の変性であり、主な症状としては記銘障害、計算力の低下、視空間失認、言語障害、理解力や判断力の低下、感情障害、行動障害などが取上げられる。ADを治療するために長期間に渡って薬物を投与する必要があり、また従来、国内で販売されるドネペジル製剤は常規の経口投与製剤であるため、嚥下困難な高齢者にとって非常に不便である。
(a)ドネペジルを適宜な甲溶媒に溶解して溶液Aを調製する、
(b)対応する酸XHを適宜な乙溶媒に溶解して溶液Bを調製する、
(c)溶液Aを溶液Bに加え、或いは、溶液Bを溶液Aに加えることによって混合溶液を調製し、混合溶液から分離してドネペジル塩(即ち化合式(I)に示される化合物)を得る。
(a)ネペジルを適宜な丙溶媒に溶解して溶液Cを調製する、
(b)対応する酸 XHを適宜な丁溶媒に溶解して溶液Dを調製する、
(c)溶液Cを溶液Dに加え、又は溶液Dを溶液Cに加えることによって混合溶液を調製する、
(d)混合溶液EにはЖ溶媒を加えても加えなくても良い。
これらの塩から形成される十四種類の新規な結晶多形は、
ドネペジルメタンスルホン酸塩 (I)の一種の結晶多形 (I-A)、
ドネペジルパラトルエンスルホン酸塩 (II)の一種の結晶多形 (II-A)、
ドネペジル琥珀酸塩 (III)の一種の結晶多形 (III-A)、
ドネペジル酒石酸塩 (IV)の一種の結晶多形 (IV-A)、
ドネペジル硫酸塩 (V)の二種の結晶多形 (V-A and V-B)、
ドネペジル硝酸塩 (VI)の一種の結晶多形 (VI-A)、
ドネペジルリン酸塩 (VII)の一種の結晶多形 (VII-A)、
ドネペジルサリチル酸塩 (VIIII)の一種の結晶多形 (VIII-A)、
ドネペジルフマル酸塩 (IX)の一種の結晶多形 (IX-A)、
ドネペジルマレイン酸塩 (X)の二種の結晶多形 (X-AとX-B)、
ドネペジルリンゴ酸塩 (XI)の一種の結晶多形 (XI-A)、と
ドネペジルベンゼンスルホン酸塩 (XII)の一種の結晶多形 (XII-A)とを含む。
試料量:約100 mg
ターゲッ卜:Cu
フィルター:単色
電圧/電流:40kV/100mA
スリット:SS/DS 1°、RS 0.3 mm
走査速度:8 °/min
赤外吸収の測定条件:
解像度:4 cm-1
走査回数:20
スペクトル領域:4000-400 cm-1
熱重量-示差熱分析(TG-DTA) の測定条件:
試料量:約6 mg
参照:Al2O3
昇温速度:10 ℃/min
注入:0.7 秒
上限:250 ℃
下限:室温
ドネペジルメタンスルホン酸塩(I)の結晶多形(I-A)の融点:179.1〜182.6 ℃
ドネペジルパラトルエンスルホン酸塩(II)の結晶多形(II-A):170.3〜171.0 ℃
ドネペジル琥珀酸塩(III)の結晶多形 (III-A):168.9〜170.2 ℃
ドネペジル酒石酸塩 (IV)の結晶多形 (IV-A):160.3〜164.5 ℃
ドネペジル硫酸塩 (V)の結晶多形 (V-A):175.1 ℃
ドネペジル硫酸塩 (V)の結晶多形 (V-B):130.0 ℃
ドネペジル硝酸塩 (VI)の結晶多形 (VI-A):213.5〜216.3 ℃
ドネペジルリン酸塩 (VII)の結晶多形 (VII-A):156.5 ℃
ドネペジルサリチル酸塩 (VIIII)の結晶多形 (VIII-A):174.8〜175.5 ℃
ドネペジルフマル酸塩 (IX)の結晶多形 (IX-A):170.0〜171.8 ℃
ドネペジルマレイン酸塩 (X)の結晶多形 (X-A):130.1〜132.4 ℃
ドネペジルマレイン酸塩 (X)の結晶多形 (X-B):131.1 ℃
ドネペジルリンゴ酸塩 (XI)の結晶多形 (XI-A):142.4〜144.7 ℃ ドネペジルベンゼンスルホン酸塩 (XII)の結晶多形 (XII-A):175.8 ℃
(1) ドネペジルメタンスルホン酸塩 (I)の一種の結晶多形 (I-A)
III-Aの赤外吸収スペクトル波数(KBr) (cm-1):532.3、572.8、669.2、717.4、773.3、819.6、877.5、935.3、960.4、997.0、1053.0、1141.7、1186.0、1232.3、1294.0、1353.8、1411.7、1483.0、1535.1、1641.2、2183.1、2615.0、2688.3、2815.6、2850.3、2877.3、2985.3、3052.8、3147.3、3698.9.
VI-Aの赤外吸収スペクトル波数(KBr) (cm-1):478.3、522.6、574.7、630.6、665.3、721.3、771.4、815.8、896.8、933.4、987.4、1054.9、1141.7、1238.1、1280.5、1351.9、1394.3、1442.5、1486.9、1546.7、1629.6、1805.1、1851.4、2028.8、2082.8、2456.9、2642.0、2690.3、2792.5、2883.1、2987.2、3151.2、3716.2、3791.4、3845.4、3876.3、3997.8。
VII-Aの赤外吸収スペクトル波数(KBr) (cm-1):480.2、518.8、570.8、661.5、736.7、775.3、833.1、900.6、987.4、1053.0、1093.5、1162.9、1238.1、1288.2、1388.5、1446.4、1483.0、1535.1、1637.3、1947.8、2032.6、2105.9、2580.3、2649.8、2773.2、2863.8、2989.2、3022.0、3176.2、3847.4、3876.3、3988.1。
ドネペジルメタンスルホン酸塩 (I) の製造方法としては
(I-1)ドネペジルの酢酸エチル溶液にメタンスルホン酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(I-2)ドネペジルの酢酸エチル溶液にメタンスルホン酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(I-3)ドネペジルの酢酸エチル溶液にメタンスルホン酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる;
(I-4)ドネペジルのアセトン溶液にメタンスルホン酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジルメタンスルホン酸塩 (I)の一種の結晶多形 (I-A) の製造方法としては
(I-A-1)ドネペジルメタンスルホン酸塩を無水エタノールに溶解し、澄明な溶液が得られ、その後冷却し結晶が得られる;
(I-A-2) ドネペジルメタンスルホン酸塩を無水エタノールに溶解し、澄明な溶液が得られ、その後2-プロピルエーテルを加え、次に冷却し結晶が得られる;
(I-A-3) ドネペジルメタンスルホン酸塩を無水エタノールに溶解し、澄明な溶液が得られ、その後n-ヘキサンを加え、次に冷却し結晶が得られる;
(I-A-4) ドネペジルの酢酸エチル溶液にメタンスルホン酸のアセトン溶液を加え澄明な溶液が得られ、その後冷却し結晶が得られる;
(I-A-5) ドネペジルの無水エタノール溶液にメタンスルホン酸の無水エタノール溶液を加え、澄明な溶液が得られ、その2-プロピルエーテルを加え、室温で撹拌し結晶が得られる;
(I-A-6) ドネペジルの無水エタノール溶液にメタンスルホン酸の無水エタノールと2-プロピルエーテルの混合溶液を加え、澄明な溶液が得られ、室温で撹拌し結晶が得られる。
(II-1) ドネペジルの酢酸エチル溶液にパラ-トルエンスルホン酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(II-2) ドネペジルの酢酸エチル溶液にパラ-トルエンスルホン酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(II-3) ドネペジルの酢酸エチル溶液にパラ-トルエンスルホン酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジルパラ-トルエンスルホン酸塩 (II) の一種の結晶多形 (II-A)の製造方法としては
(II-A-1) ドネペジルパラ-トルエンスルホン酸塩を無水エタノールに溶解し、冷却し結晶が得られる;
(II-A-2) ドネペジルパラ-トルエンスルホン酸塩を無水エタノールに溶解し、その後2-プロピルエーテルを加え、冷却し結晶が得られる。
ドネペジル琥珀酸塩 (III)の製造方法としては
(III-1)ドネペジルの酢酸エチル溶液にコハク酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(III-2) ドネペジルの酢酸エチル溶液にコハク酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(III-3)ドネペジルの酢酸エチル溶液にコハク酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる;
(III-4) コハク酸の無水エタノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(III-5) コハク酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(III-6) コハク酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジル琥珀酸塩 (III)の一種の結晶多形 (III-A)の製造方法としては:
(III-A-1) ドネペジル琥珀酸塩を無水エタノールに溶解して、冷却する;
(III-A-2) ドネペジル琥珀酸塩を無水エタノールに溶解して、その後n-ヘキサンを加え、冷却する;
(III-A-3) ドネペジル琥珀酸塩を無水エタノールに溶解して、その後蒸留水を加え、冷却する;
(III-A-4)ドネペジル琥珀酸塩をアセトンと水の混合液に溶解し、冷却する;
(III-A-5)ドネペジル琥珀酸塩を2-プロパノールに溶解して、冷却する。
ドネペジル酒石酸塩 (IV)の製造方法としては
(IV-1)ドネペジルの酢酸エチル溶液に酒石酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(IV-2) ドネペジルの酢酸エチル溶液に酒石酸のアセトン-水溶液を加え、室温で撹拌し、固体を析出させる;
(IV-3) ドネペジルの酢酸エチル溶液に酒石酸の2-プロパノール-水溶液を加え、濃縮する;
(IV-4) 酒石酸の無水エタノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(IV-5) 酒石酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(IV-6) 酒石酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、濃縮する。
ドネペジル酒石酸塩 (IV)の一種の結晶多形 (IV-A)の製造方法としては
(IV-A-1) ドネペジル酒石酸塩をアセトンに溶解して、冷却する;
(IV-A-2) ドネペジル酒石酸塩を2-プロパノールに溶解して、冷却する。
ドネペジル硫酸塩 (V)の製造方法としては
(V-1) ドネペジルの酢酸エチル溶液に硫酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(V-2) ドネペジルの酢酸エチル溶液に硫酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(V-3) ドネペジルの酢酸エチル溶液に硫酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジル硫酸塩 (V)の第一の結晶多形 (V-A)の製造方法は(V-A-1)ドネペジル硫酸塩を無水エタノールに溶解して、冷却することである。
ドネペジル硫酸塩 (V)の第二の結晶多形 (V-B)の製造方法は (V-B-1)ドネペジル硫酸塩を2-プロパノールに溶解して、冷却することである。
ドネペジル硝酸塩 (VI)の製造方法としては、
(VI-1) ドネペジルの酢酸エチル溶液に硝酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(VI-2) ドネペジルの酢酸エチル溶液に硝酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(VI-3) ドネペジルの酢酸エチル溶液に硝酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジル硝酸塩 (VI)の一種の結晶多形 (VI-A)の製造方法としては、
(VI-A-1) ドネペジル硝酸塩を無水エタノール-水に溶解して、冷却する;
(VI-A-2) ドネペジル硝酸塩をアセトン-水に溶解して、冷却する;
(VI-A-3) ドネペジル硝酸塩を2-プロパノール-水に溶解して、冷却する。
ドネペジルリン酸塩 (VII)の製造方法としては、
(VII-1) ドネペジルの酢酸エチル溶液にリン酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(VII-2) ドネペジルの酢酸エチル溶液にリン酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる;
(VII-3) リン酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(VII-4) リン酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジルリン酸塩(VII)の一種の結晶多形 (VII-A)の製造方法は (VII-A-1) ドネペジルリン酸塩を2-プロパノールに溶解し、その後2-プロピルエーテルを加え、冷却することである。
実施例52は方法 (VII-A-1)を説明する。
本発明はドネペジルサリチル酸塩 (VIII)及びその一種の結晶多形(VIII-A)を製造するための複数の製造方法が開示される。
ドネペジルサリチル酸塩 (VIII)の製造方法としては、
(VIII-1) ドネペジルの酢酸エチル溶液にサリチル酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(VIII-2) ドネペジルの酢酸エチル溶液にサリチル酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(VIII-3) ドネペジルの酢酸エチル溶液にサリチル酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる。
実施例53〜55は方法 (VIII-1)〜(VIII-3)を説明する。
ドネペジルサリチル酸塩 (VIII)の一種の結晶多形 (VIII-A)の製造方法としては、
(VIII-A-1) ドネペジルサリチル酸塩をアセトン-水に溶解して、冷却する;
(VIII-A-2)ドネペジルサリチル酸塩を2-プロパノール-水に溶解して、冷却する。
ドネペジルフマル酸塩 (IX)の製造方法としては、
(IX-1) ドネペジルの酢酸エチル溶液にフマル酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(IX-2) ドネペジルの酢酸エチル溶液にフマル酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(IX-3) ドネペジルの酢酸エチル溶液にフマル酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる;
(IX-4) フマル酸の無水エタノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(IX-5) フマル酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(IX-6) フマル酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる。
(IX-A-1) ドネペジルフマル酸塩を無水エタノールに溶解して、冷却する;
(IX-A-2) ドネペジルフマル酸塩を2-プロパノールに溶解して、冷却する。
実施例64〜65は方法 (IX-A-1)〜(IX-A-2) を説明する。
ドネペジルマレイン酸塩 (X)の製造方法としては、
(X-1) ドネペジルの酢酸エチル溶液にマレイン酸の無水エタノール溶液を加え、濃縮する;
(X-2) ドネペジルの酢酸エチル溶液にマレイン酸のアセトン溶液を加え、濃縮する;
(X-3) ドネペジルの酢酸エチル溶液にマレイン酸の2-プロパノール溶液を加え、濃縮する;
(X-4) マレイン酸の無水エタノール溶液にドネペジルの酢酸エチル溶液を加え、濃縮する;
(X-5) マレイン酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、濃縮する;
(X-6) マレイン酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、濃縮する;
(X-7) ドネペジルの酢酸エチル溶液にマレイン酸の無水エタノール溶液を加え、室温で撹拌し、固体を析出させる;
(X-8) ドネペジルの酢酸エチル溶液にマレイン酸のアセトン溶液を加え、室温で撹拌し、固体を析出させる;
(X-9) ドネペジルの酢酸エチル溶液にマレイン酸の2-プロパノール溶液を加え、室温で撹拌し、固体を析出させる;
(X-10) マレイン酸の無水エタノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(X-11) マレイン酸のアセトン溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる;
(X-12) マレイン酸の2-プロパノール溶液にドネペジルの酢酸エチル溶液を加え、室温で撹拌し、固体を析出させる。
ドネペジルマレイン酸塩 (X)の一種の結晶多形 (X-A)の製造方法としては、
(X-A-1) ドネペジルマレイン酸塩を無水エタノールに溶解して、冷却する;
(X-A-2) ドネペジルマレイン酸塩をアセトンに溶解して、冷却する;
(X-A-3) ドネペジルマレイン酸塩を2-プロパノールに溶解して、冷却する;
(X-A-4) ドネペジルマレイン酸塩 (1/2 酸) を無水エタノールに溶解して、冷却する。
実施例78〜81は方法 (X-A-1)〜(X-A-4)を説明する。
ドネペジルマレイン酸塩 (X)の一種の結晶多形 (X-B)の製造方法としては
(X-B-1) ドネペジルマレイン酸塩 (1/2 酸)をアセトンに溶解して、冷却する;
(X-B-1) ドネペジルマレイン酸塩 (1/2 酸)を2-プロパノールに溶解して、冷却する。
a)ドネペジルを適宜な甲溶媒に溶解して溶液Aを調製する工程、
b)対応する酸XHを適宜な乙溶媒に溶解して溶液Bを調製する工程、
c)溶液Aを溶液Bに加え、或いは、溶液Bを溶液Aに加え、混合溶液を調製する工程、
d)工程cで得られた混合溶液を濃縮又は室温で撹拌することによって、対応するドネペジル塩の固体を得る工程。
a)ドネペジルを適宜な丙溶媒に溶解して溶液Cを調製する工程。
b)対応する酸 XHを適宜な丁溶媒に溶解して溶液Dを調製する工程。
c)溶液Cを溶液Dに加え、又は溶液Dを溶液Cに加えることによって澄明な溶液Eを調製する工程。
d)上記工程cで得られた溶液Eを室温で撹拌しドネペジル塩の結晶を析出させ、又は溶液Eを濃縮又は冷却し、対応するドネペジル塩の結晶多形を得、或いは、溶液Eに戊溶媒を加えて冷却又は濃縮することによって、対応するドネペジル塩の結晶多形を得る工程。
本発明に係る化学式(I)に示される化合物、化学式(I)に示される化合物の溶媒和物、化学式(I)に示される化合物の結晶多形又は化学式(I)に示される化合物の溶媒和物の結晶多形は薬物活性成分として種々の疼痛を治療改善でき、すべての痛覚がある不快、機能性疼痛症候群又は器質性疼痛症候群が含まれ、上記の痛み、機能性疼痛症候群及び器質性疼痛症候群は神経障害性頭痛、特に片頭痛(migraine)、線維筋肉痛(primary fibromyalgia)、切断傷による疼痛(amputation)、腫瘍神経傷害による疼痛(tumoral denervation)、外傷性神経傷害による疼痛(traumatic denervation)又は自己免疫機序(autoimmune mechanism)の病理学的変化による疼痛が含まれるが、これに限定されない。
1)化学式(XX)に示される化合物を適宜な辛溶媒に溶解して溶液Fを調製する工程;
3)溶液Fを溶液Gに加え、或いは溶液Gを溶液Fに加え、混合溶液を調製し、混合溶液からドネペジル塩(即ち化学式(II)に示される化合物)を分離する工程。
1)化学式(XX)に示される化合物を適宜な辛溶媒に溶解して溶液Hを調製する工程;
2)対応する酸YHを適宜な壬溶媒に溶解して溶液Jを調製する工程;
3)溶液Hを溶液Jに加え、溶液Jを溶液Hに加え、溶液Kを調製する工程;
4)溶液Kを室温で撹拌し、化学式(II)に示される化合物の結晶多形又は化学式(II)に示される化合物の溶媒和物の結晶多形を析出させ、或いは溶液Kを濃縮又は冷却し化学式(II)に示される化合物の結晶多形又は化学式(II)に示される化合物の溶媒和物の結晶多形を得、或いは溶液Kに癸溶媒を加え、撹拌し、冷却又は濃縮し化学式(II)に示される化合物の結晶多形又は化学式(II)に示される化合物の溶媒和物の結晶多形を得る工程。
ドネペジル硝酸塩: 0.1〜20 %
充填剤: 35〜90 %
崩壊剤: 1〜30 %
矯味剤: 0.0〜5 %
滑剤: 0.1〜10 %
流動促進剤: 0.01〜5 %
着色剤: 0.0〜1 %
結合剤: 0〜5 %
好ましい処方:
ドネペジル硝酸塩: 1〜15 %
充填剤: 50〜80 %
崩壊剤: 4〜25 %
矯味剤: 0.1〜2 %
滑剤: 0.4〜8 %
流動促進剤: 0.1〜3 %
着色剤: 0.0〜1%
結合剤: 0〜5 %
さらに好ましい処方:
ドネペジル硝酸塩: 5〜13%
充填剤: 65〜75 %
崩壊剤: 8〜20 %
矯味剤: 0.5〜1 %
滑剤: 0.5〜5 %
流動促進剤: 0.2〜1.5 %
着色剤: 0.0〜1%
結合剤: 0〜5 %
本発明に係る口腔内崩壊錠の処方に用いられる崩壊剤は低置換度ヒドロキシプロピルセルロース (L-HPC)、クロスポリビニルピロリドン (PVPP)、クロスカルボキシメチルセルロースナトリウム (CCNa)、クロスカルボキシメチルデンプンナトリウム (CCMS-Na)、処理寒天 (TAG) からなる群より選ばれる一種又は一種以上である。
本発明に係る口腔内崩壊錠の処方に用いられる矯味剤は天然又は人工甘味料、例えばステビオシド、キシリトール、アスパルテーム、オレンジ固体エッセンス、シクラミン酸ナトリウム、ソルボースからなる群より選ばれる一種又は一種以上である。
本発明に係る口腔内崩壊錠の処方に用いられる滑剤はステアリン酸マグネシウム、タルク粉末、ラウリル硫酸マグネシウムからなる群より選ばれる一種又は一種以上である。
本発明に係る口腔内崩壊錠の処方に用いられる流動促進剤はシリカゲル微粉末、Cab-O-sil (Cabot社)、Arosil (Degussa社)、アルミノケイ酸ナトリウム水和物からなる群より選ばれる一種又は一種以上である。
本発明に係る口腔内崩壊錠の処方に用いられる結合剤は水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
上記の無苦味ドネペジル塩の口腔内崩壊錠の処方にはさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無苦味ドネペジル塩の口腔内崩壊錠の処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、口腔内崩壊錠の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無苦味ドネペジル塩の口腔内崩壊錠の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれにに限定されないものである。従って、口腔内崩壊錠の製造に適する他の方法も本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 0.05〜1 %
充填剤: 92〜99.9 %
矯味剤: 0.0〜5 %
着色剤: 0.0〜2 %
結合剤: 0.01〜3 %
本発明に係る顆粒剤の処方に用いられる結合剤は水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
本発明に係る顆粒剤の処方に用いられる矯味剤は天然又は人工甘味料、例えばステビオシド、アスパルテーム、オレンジ固体エッセンス、シクラミン酸ナトリウム、ソルボース、スクロース、グルコースからなる群より選ばれる一種又は一種以上である。
上記の無苦味ドネペジル塩の顆粒剤処方にさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無苦味ドネペジル塩の顆粒剤処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、顆粒剤の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩の顆粒剤の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、顆粒剤の製造に適する他の方法も本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 1〜20 %
充填剤: 30〜80 %
発泡剤: 5〜40 %
崩壊剤: 1〜30 %
矯味剤: 0.0〜5 %
結合剤: 0.1〜3 %
滑剤:0.1〜10 %
着色剤: 0〜1 %
本発明に係る発泡錠の処方において、発泡剤における酸源はクエン酸、酒石酸、テトラヘキサン酸、リジン、アルギニンからなる群より選ばれる一種又は一種以上である。
本発明に係る発泡錠の処方において、発泡剤におけるアルカリ源は重炭酸ナトリウム、炭酸ナトリウム、重炭酸カリウム、炭酸カリウムからなる群より選ばれる一種又は一種以上である。
本発明に係る発泡錠の処方に用いられる崩壊剤はデンプン、低置換度ヒドロキシプロピルセルロース (L-HPC)、カルボキシメチルデンプンナトリウム、クロスポリビニルピロリドン (PVPP)、クロスカルボキシメチルセルロースナトリウム (CCNa)、クロスカルボキシメチルデンプンナトリウム (CCMS-Na)、処理寒天(TAG)からなる群より選ばれる一種又は一種以上である。
本発明に係る発泡錠の処方に用いられる結合剤は水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
本発明に係る発泡錠の処方に用いられる矯味剤は天然又は人工甘味料、例えばステビオシド、アスパルテーム、オレンジエッセンス、シクラミン酸ナトリウム、ソルボース、からなる群より選ばれる一種又は一種以上である。
本発明に係る発泡錠の処方に用いられる滑剤はステアリン酸マグネシウム、タルク粉末、ラウリル硫酸マグネシウムからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の発泡錠の処方にさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の発泡錠処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、発泡錠の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩の発泡錠の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、発泡錠の製造に適する他の方法も本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 1〜20 %
充填剤: 70〜95 %
滑剤: 0.05〜5 %
結合剤: 0.1〜3 %
矯味剤: 0.0〜5 %
着色剤: 0.0〜1 %
本発明に係る口腔錠の処方に用いられる結合剤は水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
本発明に係る口腔錠の処方に用いられる矯味剤はステビオシド、アスパルテーム、果実精、シクラミン酸ナトリウム、ソルボース、スクロース、グルコース、メントール、クエン酸、アスコルビン酸からなる群より選ばれる一種又は一種以上である。
本発明に係る口腔錠の処方に用いられる滑剤はステアリン酸マグネシウム、タルク粉末、ステアリン酸カルシウム、ステアリン酸、ポリエチレングリコール 4000、ポリエチレングリコール 6000、ラウリル硫酸マグネシウムからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の口腔錠の処方にはさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の口腔錠の処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、口腔錠の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩の口腔錠の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、口腔錠の製造に適するその他の方法はいずれも本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 1〜20 %
充填剤: 65〜95 %
矯味剤: 0.0〜5 %
結合剤: 0.1〜3 %
滑剤: 0.1〜10 %
崩壊剤: 0〜10 %
着色剤: 0〜1 %
本発明に係るチュアブル剤の処方に用いられる結合剤チュアブル剤は水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
本発明に係るチュアブル剤の処方に用いられる矯味剤はステビオシド、アスパルテーム、果実精、オレンジエッセンス、シクラミン酸ナトリウム、ソルボース、スクロース、グルコース、メントール、クエン酸、アスコルビン酸からなる群より選ばれる一種又は一種以上である。
本発明に係るチュアブル剤の処方に用いられる滑剤はステアリン酸マグネシウム、タルク粉末、ステアリン酸カルシウム、ステアリン酸、ポリエチレングリコール 4000、ポリエチレングリコール 6000、ラウリル硫酸マグネシウムからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩のチュアブル剤の処方にはさらに適宜な崩壊剤を加えてもよく、崩壊剤はデンプン、低置換度ヒドロキシプロピルセルロース (L-HPC)、カルボキシメチルデンプンナトリウム、クロスポリビニルピロリドン (PVPP)、クロスカルボキシメチルセルロースナトリウム (CCNa)、クロスカルボキシメチルデンプンナトリウム (CCMS-Na)、処理寒天 (TAG) からなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩のチュアブル剤の処方にはさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩のチュアブル剤の処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、チュアブル剤の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩のチュアブル剤の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、チュアブル剤の製造に適するその他の方法はいずれも本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 1〜20 %
充填剤: 78〜96 %
矯味剤: 0.0〜5 %
本発明に係る凍結乾燥速溶錠の処方に用いられる矯味剤はステビオシド、アスパルテーム、果実精、シクラミン酸ナトリウム、メントール、クエン酸、アスコルビン酸からなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の凍結乾燥速溶錠の処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、凍結乾燥速溶錠の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩の凍結乾燥速溶錠の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、凍結乾燥速溶錠の製造に適するその他の方法はいずれも本発明の保護範囲に含まれる。
ドネペジル硝酸塩: 0.05〜0.5 %
溶解補助剤: 0.2〜10 %
防腐剤: 0.01〜1 %
矯味剤: 0.0〜5 %
溶媒: 85〜99.5 %
着色剤: 0〜1 %
本発明に係る経口液の処方に用いられる溶解補助剤はポロキサマー、エタノール、1,2-プロピレングリコール、グリセロール、ポリエチレングリコール 200〜600からなる群より選ばれる一種又は一種以上である。
本発明に係る経口液の処方に用いられる防腐剤はニパギン系、安息香酸、安息香酸ナトリウム、ソルビン酸からなる群より選ばれる一種又は一種以上であり、その中ニパギン系はメチルパラベン、エチルパラベン、プロピルパラベン、ブチルパラベンからなる群より選ばれる一種又は一種以上である。
本発明に係る経口液の処方に用いられる矯味剤は天然又は人工甘味料、例えばステビオシド、アスパルテーム、オレンジ固体エッセンス、シクラミン酸ナトリウム、ソルボース、スクロース、グルコースからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の経口液の処方にはさらに適宜な着色剤を加えてもよく、着色剤はカロチン、サンセットイエロー、タートラジン、カーミン、クロロフィルからなる群より選ばれる一種又は一種以上である。
上記の無味ドネペジル塩の経口液の処方はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、経口液の製造に適する他の処方も本発明の保護範囲に含まれる。
上記の無味ドネペジル塩の経口液の製造方法はただ本発明の主旨を説明するための特定の実施例だけであり、本発明は特にこれに限定されないものである。従って、経口液の製造に適するその他の方法はいずれも本発明の保護範囲に含まれる。
化学式(II)に示される化合物と、化学式(II)に示される化合物の結晶多形と、化学式(II)に示される化合物の溶媒和物と、化学式(II)に示される化合物の溶媒和物の結晶多形との少なくとも一つを含有する経口液、顆粒剤、口腔錠、発泡錠、チュアブル剤、口腔内崩壊錠又は凍結乾燥速溶錠はアセチルコリンエステラーゼ抑制剤に応用される場合、最適な単位投与量は5 mg、10 mg又は20 mgのドネペジル塩酸塩に相当する投与量である。
化学式(I)に示される化合物: 1〜20 %
充填剤: 35〜90 %
崩壊剤: 1〜30 %
矯味剤: 0.01〜5 %
滑剤: 0.1〜10 %
流動促進剤: 0.01〜5 %
結合剤: 0〜5 %
本発明に係る、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤の処方に用いられる結合剤は、水、デンプン、ヒドロキシプロピルメチルセルロース (HPMC)、カルボキシメチルセルロースナトリウム (CMC-Na)、ヒドロキシプロピルセルロース (HPC)、メチルセルロース (MC)、エチルセルロース (EC)、ポリビニルピロリドン (PVP)、エタノールからなる群より選ばれる一種又は一種以上である。
本発明に係る、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤に用いられる崩壊剤は、デンプン、改質デンプン、セルロース、アルギン酸カルボキシメチルデンプンナトリウム、微結晶性セルロース、低置換度ヒドロキシプロピルセルロース (L-HPC)、カルボキシメチルデンプンナトリウム、クロスポリビニルピロリドン (PVPP)、クロスカルボキシメチルセルロースナトリウム (CCNa)、クロスカルボキシメチルデンプンナトリウム (CCMS-Na)、処理寒天 (TAG) からなる群より選ばれる一種又は一種以上である。
本発明に係る、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤に用いられる矯味剤は、ステビオシド、アスパルテーム、果実精、シクラミン酸ナトリウム、ソルボース、スクロース、グルコース、メントール、クエン酸、アスコルビン酸からなる群より選ばれる一種又は一種以上である。
本発明に係る、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤に用いられる滑剤は、ステアリン酸マグネシウム、タルク粉末、ステアリン酸カルシウム、ステアリン酸、硬化植物油、ポリオキシエチレンモノステアレート、軽油、ワックス、トリアセチン、ポリエチレングリコール 4000、ポリエチレングリコール 6000、ラウリル硫酸マグネシウムからなる群より選ばれる一種又は一種以上である。
本発明に係る、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤に用いられる流動促進剤は、シリカゲル微粉末、Cab-O-sil、Arosil、アルミノケイ酸ナトリウム水和物からなる群より選ばれる一種又は一種以上である。
また、化学式(I)に示される化合物と、化学式(I)に示される化合物の結晶多形と、化学式(I)に示される化合物の溶媒和物と、化学式(I)に示される化合物の結晶多形との少なくとも一つを含有する錠剤またはコート錠は、アセチルコリンエステラーゼ抑制剤に応用される場合、最適な単位投与量は5 mg、10 mg又は20 mgのドネペジル塩酸塩に相当する投与量である。
総合評価する場合、七人のボランティアがいずれも無味と評価すれば、無味と表記する。四人以下のボランティアは僅かに苦いと評価し、その他は無味と評価すれば、僅かに苦いと表記する。評価結果は表22に記す。
錠剤の製造プロセス:
処方:化合物 I-A 1.14g; 水溶性デンプン 6g; 微結晶性セルロース 4g; ラクトース 7.46g; 低置換度HPMC 0.8g; 1% HPMC 10ml; ステアリン酸マグネシウム 0.6g。
製造プロセス:
薬物と補助材料は80目の篩を通過した後、処方に基づいて主薬と補助材料を称り、均一に混合し、1% HPMCを数回に分けて加え、軟質材料を製造し、軟質材料は24目の篩を通過して造粒する。粒子を60℃のオーブンで2.5時間乾燥した後、30目の篩で整粒する。粒子の実際測定量に比例してステアリン酸マグネシウムを添加し、均一に混合し、打錠して錠剤が得られる。
杵径:6 mm、錠剤重量:100±2 mg。
溶出試験:RC806 溶出テスター
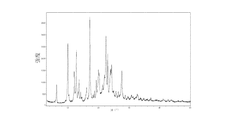
試料を6錠取り、米国薬局方溶出試験法第二法に従って測定する。溶出媒体は900ml 脱気水であり、温度は37℃であり、回転速度は100 rpmである。5 min、10 min、15 min、20 minにそれぞれ1ml試料を取り、溶出媒体を補充しない。0.45 ミクロ細孔フィルムにより試料を濾過した後、90 μl試料を注入し、測定する。結果は図面13に示す。
本発明において、特に記述がない限り、核磁気共鳴測定に用いられる溶媒はいずれもD2Oである。
ドネペジル3.79gを酢酸エチル70mlに溶解し、室温で撹拌しながらメタンスルホン酸 (0.65ml) の無水エタノール (35ml)溶液を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:181.9℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にメタンスルホン酸 (0.65ml;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:181.1℃。
室温で撹拌しながらドネペジル(3.79g) の酢酸エチル (70ml)溶液にメタンスルホン酸 (0.65ml;2-プロパノール 35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:182.2℃。
ドネペジル3.79gをアセトン80mlに溶解し、メタンスルホン酸の無水エタノール溶液10mlを徐々に加える。固体が析出し、濾過して表題化合物が得られる。55℃で真空乾燥する。融点:181.6℃。
加熱しながら、ドネペジルメタンスルホン酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。徐々に冷却し、析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:182.6℃。
加熱しながら、ドネペジルメタンスルホン酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量の2-プロピルエーテルを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:182.6℃。
加熱しながら、ドネペジルメタンスルホン酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量のn-ヘキサンを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:181.5℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にメタンスルホン酸 (0.65ml;アセトン35mlに溶解されている)を徐々に加える。室温で撹拌し固体が析出した後、すぐに析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:180.1℃。
室温で撹拌しながら、ドネペジル(3.79g) の無水エタノール (38ml)溶液にメタンスルホン酸 (1.3ml;無水エタノール11mlに溶解されている)を徐々に加え、さらに2-プロピルエーテル 50mlを加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:180.3℃。
室温で撹拌しながら、ドネペジル(3.79g) の無水エタノール (38ml)の溶液にメタンスルホン酸 (1.3ml;無水エタノール11ml と2-プロピルエーテル50mlに溶解されている)を徐々に加える。室温で撹拌し固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:177.4℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にパラ-トルエンスルホン酸 (1.902g;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.8℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にパラ-トルエンスルホン酸 (1.902g;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.8℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にパラ-トルエンスルホン酸 (1.902g;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.8℃。
加熱しながら、ドネペジルパラ-トルエンスルホン酸塩 (いかなる形態)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:171.0℃。
加熱しながら、ドネペジルパラ-トルエンスルホン酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量の2-プロピルエーテルを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.3℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に琥珀酸 (1.18g;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.1℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に琥珀酸 (1.18g;アセトン35mlと水5mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.0℃。
室温で撹拌しながら、ドネペジル(3.79g)のテトラヒドロフラン (70ml)溶液に琥珀酸 (1.18g;アセトン35mlと水5mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.7℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に琥珀酸 (1.18g;2-プロパノール35mlと水5mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:165.7℃。
室温で撹拌しながら、コハク酸 (0.59g) の無水エタノール (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.5℃。
室温で撹拌しながら、コハク酸 (0.59g) のアセトン(35ml)と水 (5ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.2℃。
室温で撹拌しながら、コハク酸 (0.59g)の2-プロパノール(35ml) と水 (5ml)の溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:167.5℃。
加熱しながら、ドネペジル琥珀酸塩 (いかなる形態)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.6℃。
加熱しながら、ドネペジル琥珀酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量のn-ヘキサンを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.4℃。
加熱しながら、ドネペジル琥珀酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量の蒸留水を加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.8℃。
加熱しながら、ドネペジル琥珀酸塩 (いかなる形態)を適宜量のアセトン-水混合液に溶解し、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.2℃。
加熱しながら、ドネペジル琥珀酸塩 (いかなる形態)を適宜量の2-プロパノールに溶解し、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.3℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に酒石酸 (1.5g;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:169.6℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (200ml)溶液に酒石酸 (1.5g;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に酒石酸 (1.5g;2-プロパノール-水混合液35mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、酒石酸 (0.75g) の無水エタノール (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.0℃。
室温で撹拌しながら、酒石酸のアセトン(35ml)溶液にドネペジル(3.79g;酢酸エチルの200mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g) の無水エタノール (70ml)溶液に酒石酸 (1.18g;水7mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、酒石酸 (0.75g)の2-プロパノール(35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
加熱しながら、ドネペジル酒石酸塩 (いかなる形態)を適宜量のアセトンに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:164.5℃。
加熱しながら、ドネペジル酒石酸塩 (いかなる形態)を適宜量の2-プロパノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:161.6℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硫酸 (0.53ml;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硫酸 (0.53ml;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硫酸塩 (0.53ml;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
加熱しながら、ドネペジル硫酸塩 (いかなる形態)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:175.1℃。
加熱しながら、ドネペジル硫酸塩 (いかなる形態)を適宜量の無水エタノールに溶解する。適宜量の2-プロピルエーテルを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:130.5℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硝酸 (0.45ml;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:213.7℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硝酸 (0.45ml;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:212.8℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液に硝酸塩 (0.45ml;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:213.7℃。
加熱しながら、ドネペジル硝酸塩 (いかなる形態)を適宜量の無水エタノール-水混合液に溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:215.8℃。
加熱しながら、ドネペジル硝酸塩 (いかなる形態)を適宜量のアセトン-水混合液に溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:213.5℃。
加熱しながら、ドネペジル硝酸塩 (いかなる形態)を適宜量の2-プロパノール-水混合液に溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:216.3℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にリン酸 (0.58ml;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にリン酸 (0.58ml;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、リン酸 (0.29ml) のアセトン(35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、リン酸 (0.29ml)の2-プロパノール(35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
加熱しながら、ドネペジルリン酸塩 (いかなる形態)を適宜量の2-プロパノールに溶解し、適宜量の2-プロピルエーテルを加え、僅かに懸濁させる。さらに加熱し、澄明な溶液にした後、徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:156.5℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にサリチル酸 (1.38g;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:176.5℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にサリチル酸 (1.38g;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:175.8℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にサリチル酸 (1.38g;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:174.5℃。
加熱しながら、ドネペジルサリチル酸塩 (いかなる形態)を適宜量のアセトン-水混合液に溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:175.5℃。
加熱しながら、ドネペジルサリチル酸塩 (いかなる形態)を適宜量の2-プロパノール-水混合液に溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:174.8℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にフマル酸 (1.16g;無水エタノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:167.7℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にフマル酸 (1.16g;アセトン35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.1℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にフマル酸塩 (1.16g;2-プロパノール35mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:168.5℃。
室温で撹拌しながら、フマル酸 (0.58g) の無水エタノール (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:166.9℃。
室温で撹拌しながら、フマル酸 (0.58g)のアセトン (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:167.4℃。
室温で撹拌しながら、フマル酸 (0.58g)の2-プロパノール (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:173.1℃。
加熱しながら、ドネペジルフマル酸塩 (いかなる形態)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.4℃。
加熱しながら、ドネペジルフマル酸塩 (いかなる形態)を適宜量の2-プロパノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:170.0℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にマレイン酸 (1.161g;無水エタノール35mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にマレイン酸 (1.161g;アセトン35mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にマレイン酸 (1.161g;2-プロパノール35mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、マレイン酸 (0.58g) の無水エタノール (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、マレイン酸 (0.58g) のアセトン (35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、マレイン酸 (0.58g)の2-プロパノール(35ml)溶液にドネペジル(3.79g;酢酸エチル70mlに溶解されている)を徐々に加える。室温で3時間撹拌した後、真空濃縮し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (20ml)溶液にマレイン酸 (1.161g;無水エタノール10mlに溶解されている)を徐々に加え、さらに2-プロピルエーテル 10mlを加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:132.2℃。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (20ml)溶液にマレイン酸 (1.161g;アセトン10mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (20ml)溶液にマレイン酸 (1.161g;2-プロパノール10mlに溶解されている)を徐々に加え、さらに2-プロピルエーテル 10mlを加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:126.8℃。
室温で撹拌しながら、マレイン酸 (0.58g) の無水エタノール (5ml)溶液にドネペジル(3.79g;酢酸エチル20mlに溶解されている)を徐々に加え、さらに2-プロピルエーテル 10mlを加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:127.8℃。
室温で撹拌しながら、マレイン酸 (0.58g) のアセトン (5ml)溶液にドネペジル(3.79g;酢酸エチル20mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:130.3℃。
室温で撹拌しながら、マレイン酸 (0.58g)の2-プロパノール(5ml)溶液にドネペジル(3.79g;酢酸エチル20mlに溶解されている)を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:129.5℃。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=1:1である)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:130.1℃。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=1:1である)を適宜量のアセトンに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:132.4℃。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=1:1である)を適宜量の2-プロパノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=2:1である)を適宜量の無水エタノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:130.5℃。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=2:1である)を適宜量のアセトンに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:131.1℃。
加熱しながら、ドネペジルマレイン酸塩 (モル比はドネペジル:マレイン酸=2:1である)を適宜量の2-プロパノールに溶解し、溶液を徐々に冷却する。析出した結晶を濾過し、55℃で真空乾燥し、表題化合物が得られる。
ドネペジル1.901g を酢酸エチル15mlに溶解し、リンゴ酸 (0.679g) の無水エタノール溶液(4ml)を徐々に滴下し、溶液を撹拌する。固体を析出した後、析出した固体を吸引ろ過し、目的化合物が得られる。
ドネペジルリンゴ酸塩3.206gを無水エタノール10mlに溶解し、溶液を加熱し、澄明になり、溶液を冷却し、固体を析出させ、目的化合物が得られる。
ドネペジル3.790g を酢酸エチル70mlに溶解し、ベンゼンスルホン酸 (1.852g) の無水エタノール溶液(35ml)を徐々に滴下する。固体が析出した後、析出した固体を吸引濾過し、目的化合物が得られる。
ドネペジル3.790gを酢酸エチル70mlに溶解し、ベンゼンスルホン酸 (1.852g) のアセトン溶液(35ml)を徐々に滴下する。固体が析出した後、析出した固体を吸引濾過し、目的化合物が得られる。
ドネペジル3.790gを酢酸エチル70mlに溶解し、ベンゼンスルホン酸 (1.852g)のイソプロパノール溶液(35ml) を徐々に滴下する。固体が析出した後、析出した固体を吸引濾過し、目的化合物が得られる。
ドネペジル3.790gをエタノール20mlに溶解し、ベンゼンスルホン酸 (1.852g)のアセトン溶液(35ml)を徐々に滴下する。固体が析出した後、析出した固体を吸引ろ過し、目的化合物が得られる。
ドネペジル3.790gを酢酸エチル70mlに溶解し、ベンゼンスルホン酸 (1.852g)のアセトン溶液(35ml)を徐々に滴下する。固体が析出した後、析出した固体を吸引濾過し、目的化合物が得られる。
室温で撹拌しながら、ドネペジル(3.79g)の酢酸エチル (70ml)溶液にマロン酸 (1.18g;2-プロパノール35mlと水5mlに溶解されている) を徐々に加える。固体が析出した後、析出した固体を濾過し、55℃で真空乾燥し、表題化合物が得られる。融点:165.7℃。
ドネペジル3.79gを酢酸エチル70mlに溶解し、室温で撹拌しながら、アセチルサリチル酸 (1.80g)のアセトン(35ml)溶液を徐々に加える。固体が析出した後、析出した固体を濾過する。融点:173〜176℃。
実施例92に記載される製造方法により得られるドネペジル安息香酸。
1H NMR(D2O):δ 7.33〜7.28 (m、5H)、6.87 (s、1H)、6.84 (s、1H)、4.07 (s、2H)、3.70 (s、3H)、3.62 (s、3H)、3.35〜3.28 (m、2H)、3.05〜2.98 (m、1H)、2.83〜2.75 (m、2H)、2.63 (d、2H、J = 16 Hz)、2.53 (s、2H)、2.49 (s、2H)、1.88〜1.82 (m、1H)、1.72〜1.67 (m、1H)、1.53〜1.48 (m、2H)、1.25〜1.13 (m、3H)
実施例92に記載される製造方法により得られるドネペジルアスパラギン酸塩。
1H NMR(D2O):δ 7.30〜7.28 (m、5H)、6.68 (s、1H)、6.66 (s、1H)、4.08 (s、2H)、3.66 (dd、1H、J = 4Hz、J =16Hz)、3.62 (s、3H)、3.54 (s、3H)、3.34〜3.28 (m、2H)、2.89〜2.76 (m、3H)、2.58 (dd、1H、J =4Hz、J = 16Hz)、2.47〜2.33 (m、3H)、1.82〜1.79 (m、1H)、1.70〜1.66 (m、1H)、1.57〜1.51 (m、2H)、1.21〜1.09(m、3H)
実施例92に記載される製造方法により得られるドネペジルクエン酸塩。
1H NMR(D2O):δ 7.33〜7.28 (m、5H)、6.87 (s、1H)、6.84 (s、1H)、4.07 (s、2H)、3.70 (s、3H)、3.62 (s、3H)、3.35〜3.28 (m、2H)、3.05〜2.98 (m、1H)、2.83〜2.75 (m、2H)、2.63 (d、2H、J = 16Hz)、2.53 (s、2H)、2.49 (s、2H)、1.88〜1.82 (m、1H)、1.72〜1.67 (m、1H)、1.53〜1.48 (m、2H)、1.25〜1.13 (m、3H)
実施例92に記載される製造方法により得られるドネペジルアスコルビン酸塩。
実施例92に記載される製造方法により得られるドネペジルギ酸塩。
1H NMR(D2O):δ 8.21 (s、1H)、7.30〜7.28 (m、5H)、6.71 (s、2H)、4.07 (s、2H)、3.64 (s、3H)、3.56 (s、3H)、3.35〜3.28 (m、2H)、2.93〜2.86 (m、1H)、2.82〜2.75 (m、2H)、2.38 (d、2H、J = 16Hz)、1.84〜1.80 (m、1H)、1.70〜1.66 (m、1H)、1.55〜1.45 (m、2H)、1.24〜1.08 (m、3H)
実施例92に記載される製造方法により得られるドネペジル没食子酸塩。
1H NMR(D2O):δ 7.28〜7.24 (m、5H)、6.74 (s、2H)、6.72 (s、1H)、6.69 (s、1H)、4.03 (s、2H)、3.63 (s、3H)、3.56 (s、3H)、3.31〜3.23 (m、2H)、2.89〜2.83 (m、1H)、2.77〜2.70 (m、2H)、2.35 (d、2H、J = 16 Hz)、2.53 (s、2H)、2.49 (s、2H)、1.88〜1.77 (m、1H)、1.67〜1.63 (m、1H)、1.49〜1.45 (m、2H)、1.24〜1.05 (m、3H)
実施例92に記載される製造方法により得られるドネペジル塩酸塩。
実施例92に記載される製造方法により得られるドネペジル酢酸塩。
実施例92に記載される製造方法により得られるドネペジル乳酸塩。
1H NMR(D2O):δ 7.30〜7.28 (m、5H)、6.78 (s、1H)、6.77 (s、1H)、4.07 (s、2H)、3.91〜3.85 (m、1H)、3.66 (s、3H)、3.59 (s、3H)、3.31〜3.23 (m、2H)、2.97〜2.91 (m、1H)、2.84〜2.74 (m、2H)、2.43 (d、2H、J = 16 Hz)、1.84〜1.78 (m、1H)、1.70〜1.66 (m、1H)、1.58〜1.46 (m、2H)、1.23〜1.13 (m、3H)、1.09 (d、3H、J = 3.0)
実施例92に記載される製造方法により得られるドネペジルソルビン酸塩。
1H NMR(D2O):δ 7.22 (s、5H)、6.79 (s、1H)、6.78 (s、1H)、6.69〜6.62 (m、1H)、5.92〜5.86 (m、1H)、5.82〜5.74 (m、1H)、5.48 (d、1H、J = 16 Hz)、4.01 (s、2H)、3.63 (s、3H)、3.55 (s、3H)、3.23〜3.16 (m、2H)、2.93 (d、2H、J = 16 Hz)、2.74〜2.68 (m、2H)、2.41 (d、2H、J = 16 Hz)、1.74 (d、1H、J = 14 Hz)、1.63 (d、1H、J = 14 Hz)、1.53〜1.46 (m、2H)、1.49 (d、3H、J = 4 Hz)、1.28〜1.12 (m、3H)
実施例92に記載される製造方法により得られるドネペジルグルタミン酸塩。
1H NMR(D2O):δ 7.28〜7.23 (m、5H)、6.67 (s、2H)、4.03 (s、2H)、3.59 (s、3H)、3.52 (s、3H)、3.48〜3.45 (m、2H)、3.29〜3.22 (m、2H)、2.88〜2.68 (m、3H)、2.34 (d、2H、J = 16 Hz)、2.09〜2.06 (m、2H)、1.85〜1.73 (m、3H)、1.66〜1.62 (m、1H)、1.50〜1.39 (m、2H)、1.10〜1.03 (m、3H)
処方:
ドネペジルサリチル酸塩:5 %
ラクトース:15 %
MCC:25 %
PVPP:10 %
マンニトール:40 %
シリカゲル微粉末:3 %
ステアリン酸マグネシウム:1 %
アスパルテーム:1 %
製造工程:各成分を称り、主薬、充填剤、崩壊剤と矯味剤をそれぞれ微粉砕し、80目の篩を通過させ、均一に混合し、さらに流動促進剤と滑剤を加え、均一に混合した後、粉末の含有量を測定し、錠剤重量を確定した後、打錠し、口腔内崩壊錠が得られる。
得られた錠剤は純水での崩壊時間が25sであり、砂利感がなく、味が甘く、清涼感がある。
処方:
ドネペジル硝酸塩:5 %
MCC:30 %
CCMs-Na:7 %
マンニトール:50 %
シリカゲル微粉末:5 %
タルク粉末:1 %
ステビオシド:2 %
製造方法は実施例26と同じである。
得られた錠剤は純水での崩壊時間が49sであり、砂利感がなく、味が甘く、清涼感がある。
処方:
ドネペジル硝酸塩:10 %
粉砂糖:10 %
MCC:28 %
L-HPC :7 %
PVPP:5%
マンニトール:35 %
シリカゲル微粉末:3 %
ステアリン酸マグネシウム:1 %
キシリトール:1 %
製造方法は実施例104と同じである。
得られた錠剤は純水での崩壊時間が37sであり、砂利感がなく、味が甘く、清涼感がある。
処方:
ドネペジルメタンスルホン酸塩:5 %
ラクトース:15 %
MCC:25 %
CCNa:6 %
マンニトール:46.5 %
シリカゲル微粉末:2 %
ステアリン酸マグネシウム:0.5 %
製造方法は実施例104と同じである。
得られた錠剤は純水での崩壊時間が21sである。
処方:
ドネペジル没食子酸塩:5 %
ラクトース:15 %
MCC:25 %
CCNa:6 %
マンニトール:31 %
エリトリトール:15 %
シリカゲル微粉末:2 %
ステアリン酸マグネシウム:0.5 %
アスパルテーム:0.5 %
製造方法は実施例104と同じである。
実施例106に記載される処方と口腔内崩壊錠の製造方法(方法B)により、ドネペジルの塩酸塩、硝酸塩、重硫酸塩、リン酸二水素塩、琥珀酸塩、マレイン酸塩、フマル酸塩、パラ-トルエンスルホン酸塩、酒石酸塩、アセチルサリチル酸塩、安息香酸塩、アスパラギン酸塩、クエン酸塩、アスコルビン酸塩、ニコチン酸塩、フタル酸塩の口腔内崩壊錠を製造する。
処方:
ドネペジル硝酸塩:5.3 %
ラクトース:29 %
マンニトール:40 %
エリトリトール:23.15 %
メントール:0.5 %
タートラジン:0.05 %
4 % PVP-50 % エタノール 溶液:適量
ポリエチレングリコール 4000:1 %
製造工程:主薬、充填剤と矯味剤をそれぞれ微粉砕し、80目の篩を通過し、均一に混合し、結合剤を逐次に加えて軟質材料を製造し、軟質材料は25目の篩を通過させ、 粒子を60℃で1〜2時間乾燥し、30目の篩で整粒し、さらに滑剤と着色剤を加え、均一に混合した後、粒子の含有量を測定し、錠剤重量を確定した後打錠し、口腔錠が得られる。
得られた錠剤は砂利感がなく、味が甘く、清涼感がある。
処方:
ドネペジル硝酸塩:5.3 %
クエン酸:15 %
重炭酸ナトリウム:9 %
クロスカルボキシメチルセルロースナトリウム:6 %
ラクトース:15 %
デンプン:27.7 %
微結晶性セルロース:20 %
オレンジエッセンス:0.5 %
1 % HPMC 溶液:適量
ステアリン酸マグネシウム:0.5 %
製造工程:主薬、充填剤、崩壊剤と矯味剤をそれぞれ微粉砕し、80目の篩を通過し、均一に混合し、結合剤を逐次に加えて軟質材料を製造し、軟質材料は25目の篩を通過させ、粒子を60℃で1〜2時間乾燥し、30目の篩で整粒し、さらに滑剤を加え、均一に混合した後、粒子の含有量を測定し、錠剤重量を確定した後打錠し、口腔錠が得られる。
得られた錠剤は2分間で純水にすべて崩壊し、味が甘く、清涼感がある。
処方:
ドネペジル硝酸塩:0.2 %
デンプン:34 %
微結晶性セルロース:27 %
ラクトース:38.7 %
ステビオシド:0.05 %
サンセットイエロー:0.05 %
80 % エタノール :適量
製造工程:主薬、充填剤と矯味剤をそれぞれ微粉砕し、80目の篩を通過し、均一に混合し、着色剤を結合剤に溶解し、結合剤を逐次に加えて軟質材料を製造し、軟質材料は14目の篩を通過させ製粒し、粒子を60℃で1〜2時間乾燥し、16目の篩で整粒し、顆粒剤が得られる。
得られた顆粒剤は熱水で5分間以内すべて溶解し、味が甘く、清涼感がある。
処方:
ドネペジル硝酸塩:0.1 %
ポロキサマー:0.5 %
アスパルテーム:0.2 %
メチルヒドロキシ安息香酸塩:0.05 %
蒸留水:99.15 %
製造工程:ポロキサマーを蒸留水に溶解し、ドネペジル硝酸塩を加え、完全に溶解するまで撹拌し、メチルヒドロキシ安息香酸塩を加え、均一に混合し、濾過し、1000mlになるように蒸留水を加え、滅菌して経口液が得られる。
処方:
ドネペジル硝酸塩:5.3 %
ラクトース:40 %
ソルビトール:22 %
マンニトール:30 %
メントール:0.1 %
オレンジエッセンス:0.1 %
カロチン:0.5 %
1 % HPMC 溶液:適量
ステアリン酸マグネシウム:1 %
製造工程:主薬、充填剤、矯味剤をそれぞれ微粉砕し、80目の篩を通過し、均一に混合し、結合剤を逐次に加えて軟質材料を製造し、軟質材料は25目の篩を通過させ; 粒子を60℃で1〜2時間乾燥し、30目の篩で整粒し、さらに滑剤と着色剤を加え、均一に混合した後、粒子の含有量を測定し、錠剤重量を確定した後、打錠し、チュアブル剤が得られる。
得られたチュアブル剤は果物のような甘さを持ち、砂利感がない。
処方:
ドネペジル硝酸塩:10.6 %
マンニトール:49.4 %
グルコース:30 %
ゼラチン:2.5 %
ヒドロキシエチルセルロース:7.5 %
水:適量
製造工程:主薬と充填剤をそれぞれ微粉砕し、80目の篩を通過し、主薬をヒドロキシエチルセルロース溶液に懸濁させ、他の補助材料を溶解して溶液を調製し、両溶液を混合し、モールドに入れ、低温で凍結させ、凍結乾燥機中で真空にして材料を完全に乾燥させ、シールして凍結乾燥速溶錠が得られる。
得られた凍結乾燥速溶錠は口で5秒以内速やかに溶解し、味が甘い。
処方:
ドネペジル硝酸塩:5 %
ラクトース:16 %
MCC:25 %
CCNa:6 %
マンニトール:31 %
エリトリトール:15 %
シリカゲル微粉末:1.5 %
アスパルテーム:0.5 %
製造工程:上記の各成分を称り、主薬、充填剤、崩壊剤と矯味剤をそれぞれ微粉砕し、80目の篩を通過し、均一に混合し、さらに流動促進剤と滑剤を加え、均一に混合した後、粉末の含有量を測定し、錠剤重量を確定した後打錠し、錠剤が得られる。
ドネペジル塩酸塩 1 g (2.5mmol)を250ml フラスコに投入し、エタノール20 mlを加える。65℃の水浴に混合液を撹拌し、澄明になる直前、水1 mlを加え、澄明になった後、マレイン酸 5 mmolを加え、さらに65℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液に酢酸エチル20 mlと石油エーテル20 mlを加える。固体はなお析出しない。溶媒が回転除去され、エタノール 10 mlを加え、70℃で加熱し溶解させ、次に室温で撹拌する。固体が析出された。吸引濾過後のケーキを洗浄し、得られた白い固体を真空乾燥する。
融点測定:試料は167℃の時から灰色になり、196℃の時からブラウンになり、203℃の時からすべて黒くなって気泡が現れ始めた。
三つの測定値は212.6〜212.7℃、213.3〜212.2℃、211.1〜211.7℃である。注入チューブでの測定値は208.1℃である。
ドネペジル塩酸塩 1g (2.5mmol)を250ml フラスコに投入し、エタノール20mlを加える。60℃の水浴に混合液を撹拌し、澄明になった後、フマル酸2.5mmolを加え、さらに65℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体が析出する。吸引濾過後のケーキを洗浄し、得られた白い固体を真空乾燥する。
融点測定:試料は168℃の時から黄色になり、185℃の時からトップは黒くなり、逐次に分解する。
三つの測定値は211.8〜214.8℃、213.8〜217.1℃、217.0〜217.1℃。注入チューブでの測定値は204.3℃である。
ドネペジル塩酸塩 1g (2.5mmol)を250ml フラスコに投入し、エタノール20mlを加える。65℃の水浴に混合液を撹拌し、澄明になる直前、水1mlを加え、澄明になった後、フマル酸 5mmolを加え、さらに65℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液に酢酸エチル20mlと石油エーテル20mlを加えた後、固体が析出する。続いて徹夜で撹拌する。翌日、吸引濾過後のケーキを洗浄し、得られた白い固体を真空乾燥する。
融点測定:試料は159℃の時から黄色になり、且つ僅かに融解し、185℃の時からトップは融解し、195℃の時からガス化し始まり、試料は若干膨張する。
三つの測定値は211.3℃、211.9℃、208.6℃である。注入チューブでの測定値は199.1℃である。
ドネペジル塩酸塩 1g (2.5mmol)を250ml フラスコに投入し、エタノール5mlと水1mlを加える。70℃の水浴に混合液を撹拌し、澄明になった後、クエン酸5 mmolを加え、さらに70℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液にジエチルエーテルを加え、続いて徹夜で撹拌する。翌日、吸引濾過後のケーキを洗浄し、得られた白い固体を真空乾燥する。
融点測定:試料は135℃の時から黄色になり、208℃の時から黒くなりはじめ、210の時黒くなり、且つ試料は僅かに融解し、212のとき気泡が生成する。
三つの測定値は219.4℃、216.3℃、216.1℃である。平均値は217.3℃である。
ドネペジル塩酸塩 1g (2.5 mmol)を250ml フラスコに投入し、エタノール5mlと水1mlを加える。70℃の水浴に混合液を撹拌し、澄明になった後、サリチル酸5mmolを加え、さらに70℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液にジエチルエーテルを加え、続いて徹夜で撹拌する。翌日、吸引濾過後のケーキを洗浄し、白い固体が得られる。
融点測定:試料は167℃のときから灰色になり、180℃のとき銀白色であり、且つトップは黄色であり、193℃のとき銀白色になった部分はガス化し、透明になり、トップの黄色物は膨張し、元の銀白色部分を代替する。200℃のときトップは黒くなり、且つ気泡が生成する。202℃のとき灰黒色になり、206℃のとき黒くなり、試料はほとんど分解する。
三つの測定値は204.5℃、208.1℃、206.1℃である。平均値は206.2℃である。
ドネペジル塩酸塩 1g (2.5mmol)を250ml フラスコに投入し、エタノール5mlと水1mlを加える。70℃の水浴に混合液を撹拌し、澄明になった後、酒石酸5 mmolを加え、さらに70℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液にジエチルエーテルを加え、続いて徹夜で撹拌する。翌日、吸引濾過後のケーキを洗浄し、白い固体が得られる。
融点測定:試料は180℃のときから黄色になり、198℃のときブラウンになり、且つ僅かに膨張し、206℃のときトップは黒くなり、210℃のとき膨張し始まり、且つ試料は黒くなり、212℃のとき気泡は生成し始まる。
三つの測定値は215.2℃、215.5℃、214.9℃である。平均値は215.2である。
ドネペジル塩酸塩 1g (2.5mmol)を250ml フラスコに投入し、エタノール5mlと水1mlを加える。70℃の水浴に混合液を撹拌し、澄明になった後、コハク酸5 mmolを加え、さらに70℃の水浴に混合液を0.5時間撹拌し、次に室温で20時間撹拌する。固体は析出しない。混合液にジエチルエーテルを加え、続いて徹夜で撹拌する。翌日、吸引濾過後のケーキを洗浄し、白い固体が得られる。
融点測定:試料は173℃のときから黄色になり、215℃のとき気泡は生成し始まり、219℃のときトップは黒くなり、気泡は生成し、分解してブラウンブラックの溶液が得られる。
三つの測定値は228.2℃、229.0℃、225.7℃である。平均値は227.6である。
試料は219℃のときトップは黒くなり、222℃のときすべて黒くなり、気泡は生成する。
Claims (9)
- 請求項1または2に記載の前記式(I)に示される化合物または式(I)に示される化合物の多形体と、薬的に許容可能な賦形剤とを含有し、経口液、顆粒剤、口腔錠、発泡錠、口腔内崩壊錠、凍結乾燥速溶錠、普通の錠剤又はチュアブル錠の形式となることを特徴とする医薬用組成物。
- 式(I)に示される化合物(式中、XHが硝酸を示す):1〜20%
充填剤:35〜90%
崩壊剤:1〜30%
矯味剤:0.00〜5%
滑剤:0.1〜10%
流動促進剤:0.01〜5%
着色剤:0〜1%
結合剤:0〜5%
重量%で表される上記組成で製造され、口腔内崩壊錠の形式となることを特徴とする請求項3に記載の医薬用組成物。 - アセチルコリンレベルの低下に起因する疾病、生理機能低下または各種疼痛の治療および/または改善のための薬物の製造における請求項1または2に記載の式(I)に示される化合物または式(I)に示される化合物の多形体の応用方法であって、
アセチルコリンレベルの低下に起因する前記疾病または生理機能低下が、老人性認知症(AD)、若年性注意欠陥障害、記銘力低下、振戦麻痺(demeritia)、脳損傷(brain injury)、多発性硬化(multiple sclerosis)、ダウン症候群(Down’s Syndrome)、狂乱状態(delirium)、気分障害(mood disorder)、ハンチントン病(Huntington’s disease)および睡眠障害(sleep disorder)からなる群より独立して選ばれることを特徴とする応用方法。 - 前記式(I)に示される化合物または式(I)に示される化合物の多形体の単位投与量が、0.5mg〜50mgであることを特徴とする、請求項5に記載の応用方法。
- 化学式(I)に示される化合物を適宜の溶媒に溶解して溶液を調製し、式(I)の化合物の溶液を濃縮又は冷却し、相応の式(I)に示される化合物の多形体が得られ、若しくは、前記式(I)に示される化合物の溶液に他の溶媒を添加し、さらに冷却して相応の式(I)に示される化合物の多形体が得られることを特徴とする請求項1または2の式(I)の化合物の多形体の製造方法。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN200710061212 | 2007-09-28 | ||
| CN200710061212.0 | 2007-09-28 | ||
| CN200810052067.4 | 2008-01-15 | ||
| CN200810052067 | 2008-01-15 | ||
| PCT/CN2008/001646 WO2009049479A1 (en) | 2007-09-28 | 2008-09-24 | Polymorphs of donepezil salts, preparation methods and uses thereof |
| CN200810211731.5 | 2008-09-24 | ||
| CN2008102117315A CN101397270B (zh) | 2007-09-28 | 2008-09-24 | 多奈哌齐盐的多晶型物及其制备和应用 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010540470A JP2010540470A (ja) | 2010-12-24 |
| JP2010540470A5 JP2010540470A5 (ja) | 2013-12-05 |
| JP5426554B2 true JP5426554B2 (ja) | 2014-02-26 |
Family
ID=40566980
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010526129A Expired - Fee Related JP5426554B2 (ja) | 2007-09-28 | 2008-09-24 | ドネペジル塩、その多形体、その製造方法、応用方法および組成物 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US8501779B2 (ja) |
| EP (1) | EP2204364B1 (ja) |
| JP (1) | JP5426554B2 (ja) |
| CN (2) | CN101397270B (ja) |
| DK (1) | DK2204364T3 (ja) |
| ES (1) | ES2415166T3 (ja) |
| WO (1) | WO2009049479A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007108011A2 (en) * | 2006-03-20 | 2007-09-27 | Ind-Swift Laboratories Limited | Process for the preparation of highly pure donepezil |
| JP5563841B2 (ja) * | 2010-02-05 | 2014-07-30 | 沢井製薬株式会社 | 薬物の不快な味をマスキングした経口医薬組成物 |
| GB201411802D0 (en) | 2014-07-02 | 2014-08-13 | Univ Bradford | Effervescent compositions |
| CN104958254A (zh) * | 2015-06-27 | 2015-10-07 | 万特制药(海南)有限公司 | 一种盐酸多奈哌齐口服溶液及其制备方法 |
| KR102318249B1 (ko) * | 2018-11-26 | 2021-10-27 | 에바바이오 주식회사 | 도네페질 이온성 액체 및 이의 용도 |
| CN113164392A (zh) * | 2018-11-26 | 2021-07-23 | 益霸生物公司 | 多奈哌齐共熔混合物及其用途 |
| WO2021142210A1 (en) * | 2020-01-10 | 2021-07-15 | President And Fellows Of Harvard College | Methods for inducing biostasis in a cell, tissue or organ |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FI95572C (fi) | 1987-06-22 | 1996-02-26 | Eisai Co Ltd | Menetelmä lääkeaineena käyttökelpoisen piperidiinijohdannaisten tai sen farmaseuttisen suolan valmistamiseksi |
| JPH1053576A (ja) * | 1996-06-07 | 1998-02-24 | Eisai Co Ltd | 塩酸ドネペジルの多形結晶およびその製造法 |
| SK285312B6 (sk) * | 1996-06-07 | 2006-10-05 | Eisai Co., Ltd. | Polymorf (III) donepezil hydrochloridu, spôsob jeho výroby a terapeutický prostriedok s jeho obsahom |
| US7439365B2 (en) | 2003-11-17 | 2008-10-21 | Usv, Ltd. | Pharmaceutical salt of (1-benzyl-4-[(5,6-dimethoxy-1-indanone)-2-yl] methyl piperidine (Donepezil) |
| US20050288330A1 (en) * | 2004-06-29 | 2005-12-29 | Avinash Naidu | Process for producing a polymorphic form of (1-Benzyl-4-[(5,6-dimethoxy-1-indanone)-2-yl] methyl piperidine hydrochloride (donepezil hydrochloride) |
| HUP0401850A3 (en) | 2004-09-15 | 2008-03-28 | Egis Gyogyszergyar Nyilvanosan | Donepezil salts for producing pharmaceutical composition |
| DE102004046497A1 (de) * | 2004-09-23 | 2006-04-06 | Helm Ag | Donepezil-Salze |
| CA2581926A1 (en) * | 2004-09-29 | 2006-04-06 | Chemagis Ltd. | Use of purified donepezil maleate for preparing pharmaceutically pure amorphous donepezil hydrochloride |
| CN1759836A (zh) * | 2004-10-12 | 2006-04-19 | 天津和美生物技术有限公司 | 多奈哌齐及其衍生物的舌下含片 |
| US20090171094A1 (en) * | 2005-07-15 | 2009-07-02 | Kazuhide Ashizawa | 1-benzyl-4-[(5, 6-dimethoxy- 1- indanon)- 2- yl]-methyl piperidine p-toluenesulfonate or crystal thereof |
| HU227474B1 (en) * | 2005-12-20 | 2011-07-28 | Richter Gedeon Nyrt | Process for industrial scale production of high purity donepezil hydrochloride polymorph i. |
-
2008
- 2008-09-24 CN CN2008102117315A patent/CN101397270B/zh active Active
- 2008-09-24 EP EP08800639A patent/EP2204364B1/en not_active Not-in-force
- 2008-09-24 JP JP2010526129A patent/JP5426554B2/ja not_active Expired - Fee Related
- 2008-09-24 CN CN2012100165448A patent/CN102603612A/zh active Pending
- 2008-09-24 ES ES08800639T patent/ES2415166T3/es active Active
- 2008-09-24 DK DK08800639.0T patent/DK2204364T3/da active
- 2008-09-24 WO PCT/CN2008/001646 patent/WO2009049479A1/zh not_active Ceased
-
2010
- 2010-03-26 US US12/748,248 patent/US8501779B2/en not_active Expired - Fee Related
-
2013
- 2013-07-05 US US13/935,927 patent/US20130296283A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN102603612A (zh) | 2012-07-25 |
| US20100311793A1 (en) | 2010-12-09 |
| US20130296283A1 (en) | 2013-11-07 |
| EP2204364A4 (en) | 2011-08-10 |
| HK1146047A1 (en) | 2011-05-13 |
| DK2204364T3 (da) | 2013-06-03 |
| JP2010540470A (ja) | 2010-12-24 |
| ES2415166T3 (es) | 2013-07-24 |
| EP2204364B1 (en) | 2013-03-20 |
| US8501779B2 (en) | 2013-08-06 |
| CN101397270B (zh) | 2012-03-28 |
| EP2204364A1 (en) | 2010-07-07 |
| CN101397270A (zh) | 2009-04-01 |
| WO2009049479A1 (en) | 2009-04-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5426554B2 (ja) | ドネペジル塩、その多形体、その製造方法、応用方法および組成物 | |
| AU2016358448B2 (en) | Salts of tetracyclines | |
| WO2010130139A1 (zh) | 芳基(乙)丙酸抗坏血酸酯,其制备方法及含有它们的药物 | |
| TWI322147B (en) | Crystalline mycophenolate sodium | |
| EP3480200B1 (en) | Optically active pyranochromenyl phenol derivative and pharmaceutical composition comprising same | |
| TW200536845A (en) | Crystalline polymorph of bazedoxifene acetate | |
| JPH0251540B2 (ja) | ||
| JP2010540470A5 (ja) | ||
| KR100339115B1 (ko) | 결정성3-(4-헥실옥시-1,2,5-티아디아졸-3-일)-1,2,5,6-테트라하이드로-1-메틸피리딘(+)l-하이드로겐타르트레이트,이의제조방법및이를포함하는약제학적조성물 | |
| JP5562337B2 (ja) | ドネペジルの多形結晶及びその製造方法 | |
| KR20250081156A (ko) | L-세린 염산염의 제조 방법 및 이의 용도 | |
| HK1146047B (en) | Polymorphs of donepezil salts, preparation methods and uses thereof | |
| TWI267511B (en) | Process for preparing 10,11-methanobenzosuberane derivatives | |
| WO2022050385A1 (ja) | フェノール誘導体 | |
| JP2020189888A (ja) | キノロン類似体及びその塩の結晶形 | |
| JP3864991B2 (ja) | (±)2−(ジメチルアミノ)−1−{〔O−(m−メトキシフェネチル)フェノキシ〕メチル}エチル水素サクシナート塩酸塩の結晶 | |
| CN112778201B (zh) | 一种苯并[b]氮杂䓬-查尔酮杂合物及其制备方法和用途 | |
| JP2010077155A (ja) | (±)2−(ジメチルアミノ)−1−{〔O−(m−メトキシフェネチル)フェノキシ〕メチル}エチル水素サクシナート塩酸塩の結晶 | |
| RU2802964C2 (ru) | Твердые формы 2-(5-(4-(2-морфолиноэтокси)фенил)пиридин-2-ил)-n-бензилацетамида | |
| JPH0466568A (ja) | 中枢性抗酸化剤化合物 | |
| JP2006160766A (ja) | (±)2−(ジメチルアミノ)−1−{〔O−(m−メトキシフェネチル)フェノキシ〕メチル}エチル水素サクシナート塩酸塩の結晶 | |
| JP2008504369A (ja) | 1,24(s)−ジヒドロキシビタミンd2の結晶形態 | |
| CN117986143A (zh) | 含有多环结构的γ-氨基丁酸衍生物及其制备方法和用途 | |
| JPH0459792A (ja) | ジエチレントリアミン三酢酸オキシアルキルエステル化合物及びそれらの製造法 | |
| TW201720832A (zh) | 喹諾酮類似物及其鹽的結晶形式 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100927 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100927 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121120 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130128 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130523 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130723 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20131017 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131119 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131128 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |