JP5313660B2 - Hgf/hgfr活性の観察と調節 - Google Patents
Hgf/hgfr活性の観察と調節 Download PDFInfo
- Publication number
- JP5313660B2 JP5313660B2 JP2008504520A JP2008504520A JP5313660B2 JP 5313660 B2 JP5313660 B2 JP 5313660B2 JP 2008504520 A JP2008504520 A JP 2008504520A JP 2008504520 A JP2008504520 A JP 2008504520A JP 5313660 B2 JP5313660 B2 JP 5313660B2
- Authority
- JP
- Japan
- Prior art keywords
- hgf
- hgfr
- antibody
- protein
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1833—Hepatocyte growth factor; Scatter factor; Tumor cytotoxic factor II
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/16—Emollients or protectives, e.g. against radiation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/10—Antioedematous agents; Diuretics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/4753—Hepatocyte growth factor; Scatter factor; Tumor cytotoxic factor II
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/5064—Endothelial cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/475—Assays involving growth factors
- G01N2333/4753—Hepatocyte growth factor; Scatter factor; Tumor cytotoxic factor II
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/04—Screening involving studying the effect of compounds C directly on molecule A (e.g. C are potential ligands for a receptor A, or potential substrates for an enzyme A)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Gastroenterology & Hepatology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Urology & Nephrology (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- General Physics & Mathematics (AREA)
- Biophysics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Microbiology (AREA)
- Pathology (AREA)
- Biotechnology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Genetics & Genomics (AREA)
- Physics & Mathematics (AREA)
- Oncology (AREA)
- Diabetes (AREA)
Description
当該出願は、2005年3月31日に出願された米国特許出願番号第60/667,463号に対する優先権を主張する。この出願の内容全体を本明細書中に援用する。
1つの側面において、開示は、望ましくない皮膚の症状、例えば、皮膚の構造を損なう症状、を有する対象の治療方法を特徴とする。その方法は、治療的有効量のHGF/HGFRモジュレーターを対象に投与するステップを含む。1つの側面において、開示は、医薬品の製造における治療的有効量のHGF/HGFRモジュレーター(例えば、作動薬又は拮抗薬)の使用を特徴とする。
作動薬は、増強されたリンパ管形成が望まれる症状を治療するために、又はその症状を治療するための医薬品の製造において使用されてもよい。そのような症状には、リンパ浮腫、例えば、後天性リンパ水腫が含まれた。後天性リンパ水腫の例には、外科処置又は放射線療法後になったリンパ浮腫、又は、例えば、病原菌による感染、例えば、フィラリア症などの感染、によって少なくとも部分的に引き起こされたリンパ浮腫が含まれる。増強されたリンパ管形成が望まれる他の症状には、老化した皮膚又は痛んだ皮膚、例えばUVBによって痛んだ皮膚、が含まれる。更なる他の症状には、遺伝的又は環境要因、例えば、紫外線、によって部分的に引き起こされたものが含まれる。例えば、前記症状は、表皮剥離、例えば、老化又は紫外線への過度の暴露によって引き起こされた表皮剥離である。
1つの側面において、開示は、腫瘍性疾患、例えば、転移性癌、特に、リンパ管内への細胞転移を伴うもの、又はリンパ節に転移する可能性を持った癌、を患うか、又はそうした危険性がある対象の治療方法を特徴とする。前記方法は、前記対象においてHGF/HGFR活性を低下させる治療的有効量のHGF/HGFR拮抗薬をその対象に投与するステップを含む。HGF/HGFR拮抗薬の治療的有効量は、腫瘍性疾患、例えば、転移性癌を患うか、又はそうした危険性がある対象を治療するための医薬品の製造において使用できる。
前記細胞又は生物体は、通常、哺乳動物、例えば、ヒト、又はヒト以外、例えば、マウス、ラット、ハムスター、モルモット、サルなど、である。
我々は、特に、リンパ系のリンパ内皮細胞(LEC)において、肝細胞増殖因子受容体(HGFR)が高度に発現されることを見つけ出した。HGFでのLECの処理は、脈管内のLECsの増殖、遊走、及び組織化を促進する。加えて、マウスへのHGFの投与は、新しいリンパ管形成を強力に促進した。更に、LEC遊走の誘導は、α9インテグリンを介して主に媒介された。
従って、HGF/HGFR活性を調節することによって、リンパ系に影響を受けた病状を治療することが可能である。対象は、また、HGF/HGFR活性を評価するパラメーターを評価することによっても診断できる。HGF/HGFR活性を調節する作用物質は、例えば、本明細書中に記載のアッセイ及びスクリーニング方法を使用して同定できる。
ヒト血清から精製される主形態に該当する成熟型のヒトHGF(hHGF)は、アミノ酸R494とV495の間の、ヒト・プロホルモンのタンパク質分解的開裂によって得られたジスルフィド結合ヘテロ二量体である。この開裂過程は、440個のアミノ酸から成るαサブユニット(M.W. 69kDa)及び234個のアミノ酸から成るβサブユニット(M.W. 34kDa)で構成された分子を生じる。αとβ鎖は、プレプロ前駆体タンパク質をコードする単一のオープン・リーディング・フレームから産生される。代表的な成熟hHGFの予測される一次構造において、鎖間S-S架橋が、α鎖のCys487とβ鎖内のCys604の間で形成される。(例えば、Nakamuraら、Nature 342:440-443ページ(1989年)を参照のこと)。α鎖のN末端は、メチオニン基で始まる54個のアミノ酸によって先行される。このセグメントは、31残基の特徴的な疎水性リーダー(シグナル)配列、及びプロ配列を含む。α鎖は、第55アミノ酸(aa)にて始まり、そして、4つのクリングル・ドメインを含む。クリングル1ドメインは約第128aa〜約第206aaに広がり、クリングル2ドメインは約第211aa〜約第288aaにあり、クリングル3ドメインは約第303aa〜約第383aaと規定され、そして、クリングル4ドメインはα鎖の約第391aa〜約第464aaに広がる。代表的なHGFは、α鎖の294位及び402位、並びにβ鎖の566位及び653位に位置する4つの推定グリコシル化部位を含む。
様々な作用物質が、例えば、誘発性リンパ浮腫、リンパ管腫、腫瘍リンパ管新生、又は腫瘍転移を含めたリンパ系に関連する病状を治療するためにHGF/HGFRモジュレーターとして使用できる。前記作用物質は、対象に投与することができるあらゆるタイプの化合物であってよい(例えば、抗体、タンパク質、ペプチド、糖タンパク質、糖ペプチド、糖脂質、多糖、オリゴ糖、核酸、生体有機分子、ペプチド模倣薬、薬理学的物質及びその代謝産物、転写及び翻訳制御配列など)。1つの態様において、HGF/HGFRモジュレーターは、生物学的な、例えば、5〜300kDaの分子量を有するタンパク質、である。
代表的なHGF/HGFRモジュレーターには、HGF、及び/又はHGFRに結合する抗体が含まれる。1つの態様において、抗体は、例えば、相互作用を物理的に遮断することによって、そのカウンターパートに対するHGF、及び/又はHGFRの親和性を低下させることによって、HGF複合体を崩壊させるか又は不安定化させることによって、HGF又はHGFRを隔離することによって、あるいは分解のためにHGF又はHGFRを標的化することによって、HGFとHGFRの間の相互作用を抑制する。1つの態様において、抗体は、HGF/HGFR結合界面に関与する1つ以上のアミノ酸残基を含むエピトープにてHGF又はHGFRに結合することができる。そのようなアミノ酸残基は、例えば、アラニン走査によって、同定できる。他の態様において、抗体は、HGF/HGFR結合に関与しない残基に結合することができる。例えば、抗体は、HGF又はHGFRの立体構造を変更し、その結果、結合親和性を低下させることができるか、あるいは抗体は、HGF/HGFR結合を立体的に妨げ得る。前記抗体は、HGFのαサブユニット又はβサブユニットに結合し得る。
抗体との関連で記載される方法は、他のタンパク質、例えば、Fc融合体及び可溶性受容体断片、に適合されてもよい。
いくつかの態様において、HGFタンパク質は、HGFの2鎖形態への生体内における変換ができる酵素によるタンパク質分解的開裂に抵抗性であるHGF変異体であってよい。前記変異体は、好ましくは、HGFを2鎖形態に変換できる酵素によって認識される領域内の部位特異的突然変異誘発によって一本鎖形態を安定させる。これらのHGF変異体は、対応する野生型HGFの実質的に完全な受容体結合親和性を保持するが、HGFRを活性化しない。1つの態様において、HGF変異体は、対応する野生型HGFと比べて受容体結合親和性は強化されていてよいが、HGFRを活性化することができない。そのような化合物は、対応する野生型HGFの競合的拮抗薬であり、そして、十分な濃度で存在している時、HGFRへの野生型HGFの結合を抑制することができる。例えば、Lokkerら、EMBO J., 11(7):2503-2510ページ(1992年)、及びGodowskiらに対する米国特許番号第5,316,921号を参照のこと。従って、それらをHGF/HGFR拮抗薬として使用できる。
いくつかの態様において、HGF/HGFRモジュレーターは、標的分子(例えば、HGFR)に独立に結合するが、それを活性化しない32個以下のアミノ酸から成るペプチドであっててよい。そのようなペプチドのいくつかは、1つ以上のジスルフィド結合を含んでよい。いわゆる「線状ペプチド」である他のペプチドは、システインを欠いている。1つの態様において、ペプチドは、人工、すなわち、天然に存在しないか、又は1つ以上の着目のゲノム、例えば、ヒトゲノム、によってコードされたタンパク質の状態で存在しない。合成ペプチドは、溶液中でほとんど構造がない(例えば、非構造化)か、不均一な構造(例えば、選択的な立体構造、又は「ゆるい」構造化)か、あるいは特異的天然構造(例えば、協調的な折り畳み)を持ってよい。いくつかの合成ペプチドは、標的分子に結合した時に、特定構造をとる。いくつかの代表的な合成ペプチドは、少なくとも1つのジスルフィド結合、及び、例えば、約4〜12個の非システイン残基から成るループを持つ、いわゆる「環状ペプチド」である。代表的なペプチドは、28、24、20、又は18アミノ酸以下の長さである。
特定の実施において、核酸拮抗薬が、HGF、HGFR、インテグリンα9、又はスタニオカルシン1をコードする内在性遺伝子の発現を低下させるために使用される。1つの態様において、核酸拮抗薬は、HGF又はHGFRをコードするmRNAを標的とするsiRNAである。他のタイプの拮抗核酸、例えば、dsRNA、リボザイム、三重らせん形成体、又はアンチセンス核酸、もまた、使用されてよい。いくつかの態様において、核酸拮抗薬は、HGFR活性化の下流エフェクタ標的(例えば、ヒトα9インテグリン、ジェンバンク番号NM 002207の下で一覧に記載される代表的な配列)に向けられてよい。
人工転写因子もまた、HGF、HGFR、インテグリンα9、又はスタニオカルシン1の発現を調節するために使用できる。人工転写因子は、例えば、HGF又はHGFRをコードする内在性遺伝子内、例えば、調節領域内の配列に、例えば、プロモーターに、結合する能力に関して、設計されるか、又はライブラリから選択されてもよい。例えば、人工転写因子は、(例えば、ファージ・ディスプレイ、米国特許番号第6,534,261号を使用して)試験管内若しくは生体内における選択によって、又は認識コードに基づいた設計(例えば、WO 00/42219及び米国特許番号第6,511,808号を参照のこと)によって製造されてもよい。特に、様々なジンク・フィンガー・ドメインのライブラリを作り出す方法に関して、例えば、Rebarら(1996年)Methods Enzymol 267:129ページ;Greisman及びPabo(1997年)Science 275:657ページ;Isalanら(2001年)Nat. Biotechnol 19:656ページ;及びWuら(1995年)Proc. Natl. Acad. Sci. USA 92:344ページを参照のこと。
HGF/HGFRモジュレーター(例えば、抗体又は可溶性HGFRタンパク質、例えばFcに融合させたHGFR細胞外領域)は、例えば、リンパ系に関連する病状(例えば、リンパ浮腫、リンパ性フィラリア症、リンパ管腫、腫瘍リンパ管新生、又は腫瘍転移などの本明細書中に記載の障害)に対する対象への投与のために、医薬組成物として処方されてもよい。通常、医薬組成物は、医薬として許容される担体を含む。本明細書中では、「医薬として許容される担体」には、生理的に適合しうる、いずれか又はあらゆる溶剤、分散媒質、コーティング、抗菌剤、抗カビ剤、等張剤、及び吸収遅延化剤などが含まれる。前記組成物は、医薬として許容される塩、例えば、酸付加塩又は塩基付加塩、を含んでもよい(例えば、Berge, S. M.ら(1977年)J. Pharm. Sci. 66:1-19ページを参照のこと)。
HGF/HGFRモジュレーター(例えば、抗体又は可溶性HGFRタンパク質)又は他の作用物質は、様々な方法によって対象、例えば、ヒト対象に投与されてもよい。多くの適用に関して、投与経路は、以下の:静脈内注射若しくは注入(IV)、皮下注射(SC)、腹腔内注射(IP)、又は筋肉内注射、の中の1つである。HGF/HGFRモジュレーターは、固定用量、又は対象の体重について調節された用量(例えば、mg/kg用量)として投与されてよい。
それらの投与経路、及び/又は様式は、また、例えばトモグラフィー像、リンパ管造影、及び特定の疾患に関連する標準的なパラメーター、例えば、リンパ管若しくはリンパ系関連障害を評価するための基準、を使用して、例えば、対象を観察することによって、個々の症例に合わせられてもよい。
HGF/HGFRモジュレーター(例えば、抗体又は可溶性HGFR)を含む医薬組成物は、医療器具を用いて投与されてもよい。前記器具は、例えば、訓練を受けていない対象によって、又は医療設備及び他の医療装置と離れた、現場の救急隊員によって、緊急事態で使用できるように、例えば、携帯性、室温保存、使いやすさなどの特徴を考慮して設計されることができる。前記器具には、例えば、HGF/HGFRモジュレーターを含む医薬調剤を保存するための1つ以上のハウジング、を含んでもよく、且つ、HGF/HGFRモジュレーターの1つ以上の単位用量をデリバリーするように構成されてもよい。
HGF/HGFR経路(例えば、HGF、HGFR、インテグリンα9、及びスタニオカルシン1)の発現に関する推定上のモジュレーターのスクリーニングは、試験管内又は生体内におけるHGF又はHGFRプロモーター活性に対するモジュレーターの効果を測定することによって実施されることができる。例えば、HGFRプロモーター(例えば、ヒト、サル、又はマウスHGFR遺伝子)若しくはその調節領域、例えば、Gambarottaら(1994年)、J. Biol. Chem., 269(17):12852-12857ページ;又は、例えば、HGFプロモーター(例えば、ヒト、サル、又はマウスHGF遺伝子)若しくはその調節領域、例えば、Bellら(1998年)、J. Biol. Chem., 273(12);6900-6908ページを含む核酸は、レポーター・ポリペプチド、例えば、以下で説明したレポーター・ポリペプチド(例えば、高感度緑色蛍光タンパク質)、の1つをコードする核酸に作動できるように連結されてもよい。使用できる他のプロモーターには、例えば、インテグリンα9、及びスタニオカルシン1といったHGF/HGFR経路活性によって調節される他の遺伝子のものが含まれる。レポーター核酸に作動できるように連結された標的プロモーターを含む核酸は、培養細胞内に導入されても、及び/又は生体内におけるプロモーター活性の評価を許容する、トランスジェニック動物を作り出すために使用されてもよい。いくつかの態様において、トランスジェニック動物は、また、HGF/HGFRモジュレーターの投与によって影響を受ける他の表現型(例えば、皮膚における遺伝子発現の誘導又は抑制)についても評価されてよい。
本明細書中に開示した方法は、実験の対象におけるHGF、HGFR、又は他の標的遺伝子の発現に対する効果について化合物を評価することを可能にする。いくつかの態様において、皮膚に対する化合物(例えば、皮膚の状態のための治療的な化合物)の効果は、発現が測定された同じ実験の対象において評価されてもよい。皮膚に対する効果は、通常、皮膚代謝関連プロモーターの制御下の遺伝子の発現に対する効果として測定される。そのようなプロモーターには、以下の:皮膚の成分である生成物、例えば、真皮又は表皮;皮膚の水和又は栄養に影響する生成物;皮膚の成分の合成又は分解を促進する生成物;皮膚の脈管構造に影響する生成物;毛嚢代謝に影響する生成物;皮膚の腺状構造に影響する生成物;皮下筋系に影響する生成物;脂肪組織に影響する生成物;又は、皮神経に影響する生成物、の発現、及び/又は合成を制御するものが含まれる。
本発明の方法で使用できるトランスジェニック動物には、ヒト以外の哺乳動物、例えば、ブタ、例えば、ミニ・ブタ;又は、齧歯動物、例えば、マウス、ラット、又はモルモット、例えば、(例えば、Begona M.ら(1994年)Proc. Natl. Acad. Sci. 91:7717-7721ページに記載の)無毛マウス、ヌード・マウス、(例えば、Takedaら(1991年)L. Am. Geriatr. Soc. 39:911-19ページに記載の)老化促進マウス、又は促進された老化の表現型を示すトランスジェニック突然変異マウスなどが含まれる。1つ以上、そして、好ましくは基本的に全ての動物細胞が導入遺伝子を含む。トランスジェニック動物は、導入遺伝子に関してホモ接合であっても、ヘテロ接合であってもよい。マウスは好ましい対象動物である。
胚操作及びマイクロインジェクションの手順は、例えば、Manipulating the Mouse Embryo(Cold Spring Harbor Laboratory Press、Cold Spring Harbor, NY.、1986年、上記文献の内容を本明細書中に援用する)に記載されている。妊馬血清(PMS)と、それに続いて48時間後にヒト絨毛性ゴナドトロピンで過剰排卵させた6週齢の雌からマウス接合体を採集することができる。準備刺激された雌は、雄と一緒に置かれて、そして、翌朝、腟栓がないかどうか調べられる。疑似妊娠雌は、発情期に関して選択されて、不妊パイプカット雄と一緒に置かれ、そして、受容者として使用される。接合体は採集され、そして、卵丘細胞が取り除かれる。更に、胚盤胞が採取されてもよい。前核胚が、雄と交尾した雌マウスから回収される。雌は、卵胞成長を誘発するために妊馬血清、PMSで処理され、そして、排卵を誘発するためにヒト絨毛性ゴナドトロピン、hCGで処理される。胚を、ダルベッコ変性リン酸緩衝生理食塩水(DPBS)中で回復させ、10%のウシ胎仔血清が補われたダルベッコ変性基本培地(DMEM)中で維持する。
トランスジェニック動物は、出生後に標準的なプロトコールによって特定できる。尾部組織からのDNAが、サザン・ブロット法、及び/又はPCR法を使用した標的構築物の存在についてスクリーニングされてもよい。それらが生殖細胞系に標的構築物を保有すると考えられる場合、ホモ接合トランスジェニック動物を生み出すために、次に、モザイクであるように見える子孫が互いに交配される。子孫が生殖細胞系伝播を持つかどうか不明瞭である場合、それらは親又は他の系統と交配されて、そして、子孫がヘテロ接合性についてスクリーニングされてよい。ヘテロ接合体は、DNAのサザン・ブロット、及び/又はPCR増幅によって特定される。
プロモーター活性は、レポーター遺伝子を着目のプロモーター(例えば、HGF、HGFR、インテグリンα9、又はスタニオカルシン1プロモーター)と対にすることによってアッセイできる。レポーター遺伝子は、検出可能な生成物、好ましくは、比較的容易に検出できるもの、例えば、蛍光性である遺伝子産物か、又は有色、蛍光性、若しくは発光性の生成物の形成によって測定することができる反応を触媒する遺伝子産物、をコードするいずれかの遺伝子であってよい。例えば、レポーター遺伝子は、酵素、例えば、検出可能な生成物、例えば、有色、蛍光性、若しくは発光性の生成物、を産生する酵素、をコードすることができる。レポーター遺伝子は、当該技術分野で知られており、そして、β-ガラクトシダーゼ遺伝子、ルシフェラーゼ遺伝子、緑色蛍光タンパク質遺伝子、シアン蛍光タンパク質、黄色蛍光タンパク質、赤色蛍光タンパク質、アルカリ・ホスファターゼ遺伝子、西洋ワサビ・ペルオキシダーゼ遺伝子、β-ラクタマーゼ遺伝子、又はクロラムフェニコール・アセチル・トランスフェラーゼ遺伝子を含む。レポーター遺伝子は、例えば、Sambrook, J, Fritsh, E. F及びManiatis, T.、Molecular Cloning:A Laboratory Manual.第2版、Cold Spring Harbor Laboratory, Cold Spring Harbor Laboratory Press、Cold Spring Harbor, NY、1989年、に記載されている。
A. 核酸及びタンパク質の検出
アレイは、サンプル、例えば、対象からのサンプル、を特徴づけするための有用な分子ツールである。例えば、アレイは、HGF、HGFR、インテグリンα9、及びスタニオカルシン1核酸に対するプローブを含めた複数の遺伝子に対する、あるいは複数のタンパク質に対する捕獲プローブがある。アレイは、基板上に多くのアドレス、例えば、位置を特定できる部位、を持ってよい。紹介されるアレイは、様々な形式で構成されることができ、その制限されることのない例を以下に説明する。
遺伝情報を提供するための遺伝物質を評価するための多数の方法が存在する。これらの方法は、HGFをコードする遺伝子又はHGFRをコードする遺伝子、並びに他の座位を含めた遺伝子座を評価するために使用できる。前記方法は、1つ以上のヌクレオチド、例えば、調節領域(例えば、プロモーター、非翻訳領域又はイントロンをコードする領域など)内の、例えば、遺伝子のコードすること又は非コード領域、を評価するために使用できる。
HGF/HGFR結合物質(例えば、抗体)は、それぞれ、生体内におけるHGF、及び/又はHGFRの存在の検出(例えば、対象における生体内造影)に使用できる。前記方法は、本明細書中に記載の症状、例えば、リンパ障害、又はそのような障害の危険性、を評価する(例えば、診断する、部位を特定する、又は病期分類する)ために使用できる。前記方法は、以下のステップ:(i)結合物質とHGF又はHGFRの相互作用が起こるのを許容する条件下で、対象(及び必要に応じて、対照対象)にHGF/HGFR結合物質(例えば、HGF又はHGFRに結合する抗体)を投与し;そして、(ii)上記結合物質を検出して、例えば、HGF又はHGFR発現細胞の位置を特定するか、又はその他の方法で識別する、を含む。基準(例えば、対照対象又は対象のベースライン)に対する対象における複合体量の統計的に有意な増加は、リンパ管、又はリンパ系関連障害、あるいはそのような障害の危険性の診断につながりお得る要因となり得る。
定量的リアルタイムRT-PCR法(QPCR)は、3つの独立に確立された初代LEC株が、血管内皮細胞(BVEC)と比較して、主要なリンパ系統マーカーであるProx1及びLYVE-1のmRNAを高いレベルで発現したが、血管系統マーカーであるFlt-1を低いレベルでしか発現しなかったことを確認した(図1A〜C)。LECのHGFR mRNAレベルをQPCRによって計測し、そして、BVECのレベルに比べて、2倍よりも高いことがわかった(図1D)。加えて、免疫沈降反応、及びウエスタン・ブロット分析では、HGFRタンパク質の発現が、BVECに比べて、LECにおいてより高かったことが実証された(図1E)。30ng/mlのHGFでのLEC処理がHGFRのリン酸化の増加をもたらしたので(図1F)、HGFRはLEC内において機能的である。要するに、HGFRは、BVEC内に比べて、LEC内で高いレベルで発現されており、且つ、LECがHGFで処理される時に、活性化される。
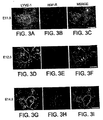
HGFR、及びリンパ特異的ヒアルロナン受容体のLYVE-1に対する抗体を使用して、正常なマウス皮膚の示差的免疫蛍光分析を実施した。HGFRの発現は、正常な皮膚中の静止状態のリンパ管においてほとんど検出されなかった。HGFRが生理学的過程中にリンパ内皮によって上方制御される可能性があるかどうかを測定するために、我々は、リンパ管の膨大及び増殖を特徴とするVEGF-Aトランスジェニック(VEGF-TG)マウス(Kunstfeldら(2004年)Blood, 104(4):1048-1057ページ)において実験的に誘発した遅延型過敏症から得られた慢性的な炎症マウス皮膚のサンプルを免疫染色した。皮膚炎誘導の7日後に、拡大したLYVE-1陽性リンパ管がVEGF-TGマウスにおいて検出されたが、野生型マウスにおいて検出されなかった(図2A、D)。LYVE-1陽性リンパ管がHGFRを強く発現したのに対して、野生型マウスの正常なリンパ管においてHGFR発現はほとんど検出されなかった(図2A〜F)。
HGFは、唯一知られているHGFRのリガンドであり、そして、ヒト血管内皮細胞(HVEC)の増殖と遊走を引き起こすことを示した、例えば、Bussolinoら(1992年)、J. Cell Biol., 119:629-641ページ。LEC対BVECによるHGFRの示差的な発現レベルがHGF刺激に関してそれらの示差的な応答をもたらすかどうか調査するために、我々は、次に、試験管内におけるLEC対BVECの増殖に対するHGFの効果を調査した。HGFは、未処理対照培養物と比べた場合に、1ng/ml(p<0.01)の最小有効濃度でLECの増殖を強力に誘導した。HGFもまた、この濃度にてBVEC増殖を誘導したが、増殖刺激の程度は、BVECと比べて、LECにおいてより高かった(図4A)。これまでのところ、VEGF-C及びVEGF-Dが、VEGF受容体-3(VEGFR-3)の活性化を介して直接的にLEC増殖を促進する唯一知られている増殖因子であり(例えば、Jussila及びAlitalo(2002年)、Physiol Rev, 82:673-700ページ)、そして、それらがVEGFR-3経路のブロックによって抑制され得るので、リンパ管新生に対するFGF-2の効果が、VEGFR-3リガンドの上方制御の結果であることが提案された(例えば、Changら(2004年)、PNAS, 101:11658-11663ページ;Kuboら(2002年)、PNAS, 99:8868-8873ページ)。HGFが直接的又は間接的にLEC増殖を刺激するかどうか調査するために、我々は、次に、VEGFR-3又はHGFRに対するブロッキング抗体の存在下又は不存在下、HGFでLECを処理した。HGFRブロッキング抗体と一緒のLECのインキュベーションが、HGFによるLEC増殖の刺激を強力に遮断したが(p<0.001)、その一方で、−VEGF-CによるLEC増殖の刺激を効果的に遮断した用量(データ未掲載)における−、VEGFR-3ブロッキング抗体と一緒の、又は対照IgGと一緒のインキュベーションは、HGF誘発増殖に影響を与えなかった(図4B)。これらの結果は、HGF誘発LEC増殖が、VEGF-R3経路の活性化から独立して起こり、且つ、HGFのその受容体への効果的な結合に依存していることを示唆している。
HGFが、また、生体内においてリンパ管新生も誘導するかどうか調査するために、我々は、Hirakawaら(2003年)、Am. J. Pathol., 162:575-586ページに記載のとおり、HGFを含むか又は含まないマトリゲルをFVBマウスの皮下に埋め込んだ。リンパ管特異的糖タンパク質であるポドプラニン、例えば、Schachtら(2003年)、EMBO J., 22:3546-3556ページ、についての免疫染色が、埋め込み後7日目のHGF含有マトリゲル内の新しいリンパ管の顕著な形成を明らかにしたが、その一方で、対照マトリゲル内にリンパ管は観察されなかった(図5C、D)。
我々はマウスにおいて実験的な皮膚炎中に膨大したリンパ管によってHGFRが強く発現されることを発見したので、我々は、次に、HGFが、生体内におけるリンパ管膨大に直接的に貢献するかどうか調査した。遅延型過敏反応を、Kunstfeldら(2004年)、Blood, 104(4):1048-1057ページに記載のとおり、マウス耳部への局部塗付によって誘導した。実験的炎症の誘導の1日前に、100μgのHGFRに対するブロッキング抗体、又は等量の対照免疫グロブリンGを、腹腔内に注射した。炎症誘導の24時間後の免疫蛍光分析は、対照IgGを受けたマウスと比べて、HGF-Rブロッキング抗体での処理を受けたマウスにおいてリンパ管のサイズの大幅な減少を明らかにした(図6A、B)。LYVE-1及びCD31について染色した切片のコンピュータを利用した形態計測による分析は、リンパ管の平均サイズ、及びリンパ管によって覆われている組織領域のパーセンテージが、対照IgG処理マウスと比較して、HGF-Rブロッキング抗体の注射後に有意に減少した(P<0.01)ことを実証した(図6C、D)。リンパ管の密度は、2つの処理群の間で有意に異なっていなかった(図6E)。
LECに対するHGFの効果を媒介し得る可能性のある分子機序を規定するために、LECの独立した2種類の系統を30ng/mlのHGFと一緒に、又はそれなしに6時間、インキューベートし、それに続いて、Affymetrix HU133v2(商標)アレイを使用してマイクロアレイ分析をした。我々は、スタニオカルシン1がHGF処理後に最も高く上方制御された遺伝子の1つであったことを発見した。そのうえ、インテグリンα9の発現もまた、HGF処理後に有意に上方制御された。これらの結果を、QPCR分析によって確認した(図7A)。
インテグリンα9の存在下、又は不存在下のHGFとLECの同時インキュベーションは、インテグリンα9遮断は、HGF誘導性遊走を部分的にしか遮断しなかったが(p=0.0143)、その一方で、HGF-Rブロッキング抗体とのインキュベーションは、LEC遊走に対するHGFの効果を完全に抑制する(p=0.0074)ことを明らかにした(図7B)。
生体内におけるHGF過剰発現の効果を測定するために、リンパ管構造を、先に確立したメタロチオネインIプロモーター駆動HGFトランスジェニック・マウスにおいて調査した(Takayamaら(1996年)Proc. Natl. Acad. Sci. USA, 93:5866-5871ページ)。分析は、リンパ管が最も豊富であり、且つ、遺伝的マウス・モデルにおいてリンパ系の異常が最も容易に検出される皮膚及び小腸に注目した。脈管の膨大を、野生型マウスと比べて(図8A)、HGFトランスジェニック・マウス(図8B)の粘液と回腸の粘膜下組織において検出した。リンパ特異的マーカーであるポドプラニンについての免疫蛍光染色が、HGFトランスジェニック・マウスの回腸の粘膜下組織の中心乳び腔の顕著な拡張と、リンパ管の膨大を明らかにした(図8C、D)。ポドプラニン染色は、また、HGFトランスジェニック・マウスの皮膚においてリンパ管の数の増加と膨大が明らかになったが(図8G、H)、その一方で、主要な組織学的異常は観察されなかった(図8E、F)。増強されたリンパ管形成と膨大は、また、HGFトランスジェニック・マウスの十二指腸及び肝臓においても観察された。
これらに実施例において示された結果は、HGFがリンパ管新生を制御するためのタンパク質標的であることを示唆している。
本発明の多数の態様を説明した。それにもかかわらず、様々な修飾が本発明の趣旨及び範囲から逸脱することなく作られ得ることは理解される。例えば、核酸、及びHGFとHGFR活性の抗体モジュレーターの組み合わせが、想定される。従って、他の態様は、添付の請求項の範囲内にある。
Claims (1)
- 肝細胞増殖因子を含有するリンパ管形成促進剤。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US66746305P | 2005-03-31 | 2005-03-31 | |
| US60/667,463 | 2005-03-31 | ||
| PCT/US2006/012389 WO2006105511A1 (en) | 2005-03-31 | 2006-03-30 | Monitoring and modulating hgf/hgfr activity |
Related Child Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010109852A Division JP4664441B2 (ja) | 2005-03-31 | 2010-05-12 | Hgf/hgfr活性の観察と調節 |
| JP2012090431A Division JP2012149087A (ja) | 2005-03-31 | 2012-04-11 | Hgf/hgfr活性の観察と調節 |
| JP2013043836A Division JP5801835B2 (ja) | 2005-03-31 | 2013-03-06 | Hgf/hgfr活性の観察と調節 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008538551A JP2008538551A (ja) | 2008-10-30 |
| JP5313660B2 true JP5313660B2 (ja) | 2013-10-09 |
Family
ID=36638370
Family Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008504520A Expired - Fee Related JP5313660B2 (ja) | 2005-03-31 | 2006-03-30 | Hgf/hgfr活性の観察と調節 |
| JP2010109852A Expired - Fee Related JP4664441B2 (ja) | 2005-03-31 | 2010-05-12 | Hgf/hgfr活性の観察と調節 |
| JP2012090431A Pending JP2012149087A (ja) | 2005-03-31 | 2012-04-11 | Hgf/hgfr活性の観察と調節 |
| JP2013043836A Expired - Fee Related JP5801835B2 (ja) | 2005-03-31 | 2013-03-06 | Hgf/hgfr活性の観察と調節 |
| JP2013149577A Active JP5722960B2 (ja) | 2005-03-31 | 2013-07-18 | Hgf/hgfr活性の観察と調節 |
Family Applications After (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010109852A Expired - Fee Related JP4664441B2 (ja) | 2005-03-31 | 2010-05-12 | Hgf/hgfr活性の観察と調節 |
| JP2012090431A Pending JP2012149087A (ja) | 2005-03-31 | 2012-04-11 | Hgf/hgfr活性の観察と調節 |
| JP2013043836A Expired - Fee Related JP5801835B2 (ja) | 2005-03-31 | 2013-03-06 | Hgf/hgfr活性の観察と調節 |
| JP2013149577A Active JP5722960B2 (ja) | 2005-03-31 | 2013-07-18 | Hgf/hgfr活性の観察と調節 |
Country Status (11)
| Country | Link |
|---|---|
| US (4) | US20070010443A1 (ja) |
| EP (2) | EP1863519B1 (ja) |
| JP (5) | JP5313660B2 (ja) |
| KR (3) | KR20130114763A (ja) |
| CN (2) | CN102989012B (ja) |
| DK (1) | DK1863519T3 (ja) |
| ES (1) | ES2440953T3 (ja) |
| HK (1) | HK1183441A1 (ja) |
| PL (1) | PL1863519T3 (ja) |
| TW (1) | TWI362940B (ja) |
| WO (1) | WO2006105511A1 (ja) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20080260861A1 (en) * | 2004-04-07 | 2008-10-23 | The General Hospital Corporation | Modulating Lymphatic Function |
| US7713969B2 (en) | 2005-02-09 | 2010-05-11 | Arqule, Inc. | Compositions and methods for treatment of cancer |
| TWI362940B (en) * | 2005-03-31 | 2012-05-01 | Gen Hospital Corp | A use of agonist and/or antagonist of hgf/hgfr activity |
| EP1911459B1 (en) * | 2005-07-28 | 2015-12-02 | AnGes MG, Inc. | Lymphangiogenesis promoter |
| US20090169473A1 (en) * | 2005-10-24 | 2009-07-02 | Fujifilm Ri Pharma Co., Ltd. | Diagnostic agent and therapeutic agent for disease associated with hepatocyte growth factor receptor |
| EP2173724B1 (en) | 2007-06-22 | 2012-12-05 | ArQule, Inc. | Quinazolinone compounds and methods of use thereof |
| JP5425060B2 (ja) | 2007-06-22 | 2014-02-26 | アークル インコーポレイテッド | ピロリジノン、ピロリジン−2,5−ジオン、ピロリジンおよびチオスクシンイミド誘導体、癌の治療のための組成物および方法 |
| CA2912546A1 (en) | 2007-06-22 | 2008-12-31 | Arqule, Inc. | Compositions and methods for treatment of cancer |
| WO2009084671A1 (ja) * | 2007-12-28 | 2009-07-09 | Astellas Pharma Inc. | ヒト抗α9インテグリン抗体 |
| WO2011079261A2 (en) * | 2009-12-23 | 2011-06-30 | Curna, Inc. | Treatment of hepatocyte growth factor (hgf) related diseases by inhibition of natural antisense transcript to hgf |
| EP3511342B1 (en) | 2010-03-10 | 2024-01-17 | Genmab A/S | Monoclonal antibodies against c-met |
| CN105209483B (zh) * | 2013-05-31 | 2021-07-27 | 分子组合公司 | 与肝细胞生长因子结合的设计锚蛋白重复蛋白 |
| KR20170136536A (ko) | 2015-03-16 | 2017-12-11 | 셀덱스 쎄라퓨틱스, 인크. | 항-met 항체 및 그 사용 방법 |
| KR101843248B1 (ko) * | 2015-03-17 | 2018-03-29 | 고려대학교 세종산학협력단 | 흉선 기질 림프단백질 매개 신호전달을 제어하는 펩타이드 유도체 및 이를 포함하는 알러지 및 천식 질환 예방 및 치료용 약학 조성물 |
| WO2017019454A2 (en) | 2015-07-28 | 2017-02-02 | Musc Foundation For Research Development | Identification of novel anti-fibrotic peptide in c-terminal region of the met receptor tyrosine kinase |
| CN114292899B (zh) * | 2022-01-08 | 2024-03-26 | 安徽医科大学第一附属医院 | 一种肝细胞生长因子检测及信号增敏探针、引物对及其应用 |
Family Cites Families (84)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4277437A (en) | 1978-04-05 | 1981-07-07 | Syva Company | Kit for carrying out chemically induced fluorescence immunoassay |
| US4399216A (en) | 1980-02-25 | 1983-08-16 | The Trustees Of Columbia University | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US5179017A (en) | 1980-02-25 | 1993-01-12 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4634665A (en) | 1980-02-25 | 1987-01-06 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4475196A (en) | 1981-03-06 | 1984-10-02 | Zor Clair G | Instrument for locating faults in aircraft passenger reading light and attendant call control system |
| US4447233A (en) | 1981-04-10 | 1984-05-08 | Parker-Hannifin Corporation | Medication infusion pump |
| US4439196A (en) | 1982-03-18 | 1984-03-27 | Merck & Co., Inc. | Osmotic drug delivery system |
| US4447224A (en) | 1982-09-20 | 1984-05-08 | Infusaid Corporation | Variable flow implantable infusion apparatus |
| US4487603A (en) | 1982-11-26 | 1984-12-11 | Cordis Corporation | Implantable microinfusion pump system |
| US4486194A (en) | 1983-06-08 | 1984-12-04 | James Ferrara | Therapeutic device for administering medicaments through the skin |
| US4683196A (en) | 1983-12-12 | 1987-07-28 | Meru, Inc. | Method and materials for the identification of lipopolysaccharide producing microorganisms |
| US4596556A (en) | 1985-03-25 | 1986-06-24 | Bioject, Inc. | Hypodermic injection apparatus |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| US5116742A (en) | 1986-12-03 | 1992-05-26 | University Patents, Inc. | RNA ribozyme restriction endoribonucleases and methods |
| US4987071A (en) | 1986-12-03 | 1991-01-22 | University Patents, Inc. | RNA ribozyme polymerases, dephosphorylases, restriction endoribonucleases and methods |
| JP3101690B2 (ja) | 1987-03-18 | 2000-10-23 | エス・ビィ・2・インコーポレイテッド | 変性抗体の、または変性抗体に関する改良 |
| US5573933A (en) | 1987-04-14 | 1996-11-12 | Luminis Pty, Ltd. | Transgenic pigs |
| US4941880A (en) | 1987-06-19 | 1990-07-17 | Bioject, Inc. | Pre-filled ampule and non-invasive hypodermic injection device assembly |
| US4790824A (en) | 1987-06-19 | 1988-12-13 | Bioject, Inc. | Non-invasive hypodermic injection device |
| JP2650159B2 (ja) | 1988-02-24 | 1997-09-03 | アクゾ・ノベル・エヌ・ベー | 核酸増幅方法 |
| CA1340807C (en) | 1988-02-24 | 1999-11-02 | Lawrence T. Malek | Nucleic acid amplification process |
| US5130238A (en) | 1988-06-24 | 1992-07-14 | Cangene Corporation | Enhanced nucleic acid amplification process |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| US5143854A (en) | 1989-06-07 | 1992-09-01 | Affymax Technologies N.V. | Large scale photolithographic solid phase synthesis of polypeptides and receptor binding screening thereof |
| US5527681A (en) | 1989-06-07 | 1996-06-18 | Affymax Technologies N.V. | Immobilized molecular synthesis of systematically substituted compounds |
| US5545522A (en) | 1989-09-22 | 1996-08-13 | Van Gelder; Russell N. | Process for amplifying a target polynucleotide sequence using a single primer-promoter complex |
| US5064413A (en) | 1989-11-09 | 1991-11-12 | Bioject, Inc. | Needleless hypodermic injection device |
| US5312335A (en) | 1989-11-09 | 1994-05-17 | Bioject Inc. | Needleless hypodermic injection device |
| US5362716A (en) | 1989-12-27 | 1994-11-08 | The United States Of America As Represented By The Department Of Health And Human Services | Methods for stimulating hematopoietic progenitors using hepatocyte growth factor and lymphokines |
| US5648273A (en) | 1989-12-27 | 1997-07-15 | The United States Of America, As Represented By The Department Of Health And Human Services | Hepatic growth factor receptor is the MET proto-oncogene |
| US6013431A (en) | 1990-02-16 | 2000-01-11 | Molecular Tool, Inc. | Method for determining specific nucleotide variations by primer extension in the presence of mixture of labeled nucleotides and terminators |
| US5789650A (en) | 1990-08-29 | 1998-08-04 | Genpharm International, Inc. | Transgenic non-human animals for producing heterologous antibodies |
| JP3200609B2 (ja) * | 1990-12-28 | 2001-08-20 | 敏一 中村 | 上皮細胞増殖促進剤 |
| US5455166A (en) | 1991-01-31 | 1995-10-03 | Becton, Dickinson And Company | Strand displacement amplification |
| US5922854A (en) | 1991-06-14 | 1999-07-13 | Kumar; Ramesh | Purifying Human Hemogloblin from transgenic pig red cells and plasmids containing pig globin nucleic acids |
| CA2103059C (en) | 1991-06-14 | 2005-03-22 | Paul J. Carter | Method for making humanized antibodies |
| US5384261A (en) | 1991-11-22 | 1995-01-24 | Affymax Technologies N.V. | Very large scale immobilized polymer synthesis using mechanically directed flow paths |
| US5316921A (en) | 1992-05-18 | 1994-05-31 | Genentech, Inc. | Single-chain hepatocyte growth factor variants |
| WO1993025071A1 (en) | 1992-06-12 | 1993-12-23 | Dnx Corporation | Production of human hemoglobin in transgenic pigs |
| US5383851A (en) | 1992-07-24 | 1995-01-24 | Bioject Inc. | Needleless hypodermic injection device |
| US5288514A (en) | 1992-09-14 | 1994-02-22 | The Regents Of The University Of California | Solid phase and combinatorial synthesis of benzodiazepine compounds on a solid support |
| ES2112997T3 (es) | 1992-09-18 | 1998-04-16 | Us Gov Health & Human Serv | Un metodo para producir factor de crecimiento de hepatocitos y una linea celular. |
| DE69419721T2 (de) | 1993-01-12 | 2000-04-27 | Biogen Inc | Rekombinante anti-vla4 antikörpermoleküle |
| US5714320A (en) | 1993-04-15 | 1998-02-03 | University Of Rochester | Rolling circle synthesis of oligonucleotides and amplification of select randomized circular oligonucleotides |
| US5422252A (en) | 1993-06-04 | 1995-06-06 | Becton, Dickinson And Company | Simultaneous amplification of multiple targets |
| US5523226A (en) | 1993-05-14 | 1996-06-04 | Biotechnology Research And Development Corp. | Transgenic swine compositions and methods |
| US5951974A (en) | 1993-11-10 | 1999-09-14 | Enzon, Inc. | Interferon polymer conjugates |
| US5827690A (en) | 1993-12-20 | 1998-10-27 | Genzyme Transgenics Corporatiion | Transgenic production of antibodies in milk |
| AU694187B2 (en) | 1994-02-07 | 1998-07-16 | Beckman Coulter, Inc. | Ligase/polymerase-mediated genetic bit analysis TM of single nucleotide polymorphisms and its use in genetic analysis |
| EP0823941A4 (en) | 1995-04-28 | 2001-09-19 | Abgenix Inc | HUMAN ANTIBODIES DERIVED FROM IMMUNIZED XENO MOUSES |
| US5686292A (en) | 1995-06-02 | 1997-11-11 | Genentech, Inc. | Hepatocyte growth factor receptor antagonist antibodies and uses thereof |
| US5733729A (en) | 1995-09-14 | 1998-03-31 | Affymetrix, Inc. | Computer-aided probability base calling for arrays of nucleic acid probes on chips |
| DE19541844C1 (de) | 1995-11-09 | 1997-07-24 | Gsf Forschungszentrum Umwelt | Verfahren zur Herstellung von menschlichen Antikörpern und deren Verwendung |
| JP3974941B2 (ja) | 1995-11-21 | 2007-09-12 | イェール ユニバーシティ | 単分子セグメントの増幅および検出 |
| US5854033A (en) | 1995-11-21 | 1998-12-29 | Yale University | Rolling circle replication reporter systems |
| US20030143204A1 (en) | 2001-07-27 | 2003-07-31 | Lewis David L. | Inhibition of RNA function by delivery of inhibitors to animal cells |
| WO1997035033A1 (en) | 1996-03-19 | 1997-09-25 | Molecular Tool, Inc. | Method for determining the nucleotide sequence of a polynucleotide |
| ATE465257T1 (de) | 1996-07-03 | 2010-05-15 | Genentech Inc | Agonisten für den rezeptor des hepatozyten- wachstumsfaktors und deren anwendungen |
| GB9618050D0 (en) | 1996-08-29 | 1996-10-09 | Cancer Res Campaign Tech | Global amplification of nucleic acids |
| EP0942968B1 (en) | 1996-12-03 | 2008-02-27 | Amgen Fremont Inc. | Fully human antibodies that bind EGFR |
| US6534261B1 (en) | 1999-01-12 | 2003-03-18 | Sangamo Biosciences, Inc. | Regulation of endogenous gene expression in cells using zinc finger proteins |
| US6453242B1 (en) | 1999-01-12 | 2002-09-17 | Sangamo Biosciences, Inc. | Selection of sites for targeting by zinc finger proteins and methods of designing zinc finger proteins to bind to preselected sites |
| US6132997A (en) | 1999-05-28 | 2000-10-17 | Agilent Technologies | Method for linear mRNA amplification |
| KR100768023B1 (ko) * | 1999-09-21 | 2007-10-17 | 안제스에무지 가부시키가이샤 | 뇌혈관 장애를 위한 유전자 치료 |
| WO2001044294A2 (en) * | 1999-12-15 | 2001-06-21 | Entremed, Inc. | Compositions and methods for inhibiting endothelial cell proliferation |
| US20020102260A1 (en) * | 2000-03-02 | 2002-08-01 | Marc Achen | Methods for treating neoplastic disease characterized by vascular endothelial growth factor D expression, for screening for neoplastic disease or metastatic risk, and for maintaining vascularization of tissue |
| EP1272630A2 (en) | 2000-03-16 | 2003-01-08 | Genetica, Inc. | Methods and compositions for rna interference |
| US8288322B2 (en) | 2000-04-17 | 2012-10-16 | Dyax Corp. | Methods of constructing libraries comprising displayed and/or expressed members of a diverse family of peptides, polypeptides or proteins and the novel libraries |
| WO2001083819A2 (en) | 2000-04-28 | 2001-11-08 | Sangamo Biosciences, Inc. | Methods for designing exogenous regulatory molecules |
| WO2002029087A2 (en) | 2000-10-02 | 2002-04-11 | St. Elizabeth's Medical Center Of Boston, Inc. | Use of lymphangiogenic agents to treat lymphatic disorders |
| CN1150035C (zh) * | 2000-12-21 | 2004-05-19 | 中国人民解放军军事医学科学院放射医学研究所 | 一种重组质粒及其在疾病防治中的应用 |
| WO2003064621A2 (en) | 2002-02-01 | 2003-08-07 | Ambion, Inc. | HIGH POTENCY siRNAS FOR REDUCING THE EXPRESSION OF TARGET GENES |
| AU2003234336A1 (en) | 2002-05-03 | 2003-11-17 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and compositions for use in preparing sirnas |
| WO2004015062A2 (en) | 2002-08-12 | 2004-02-19 | New England Biolabs, Inc. | Methods and compositions relating to gene silencing |
| DE10242663A1 (de) * | 2002-09-13 | 2004-03-25 | Forschungszentrum Karlsruhe Gmbh | Verfahren zur Identifizierung von Inhibitoren in vivo |
| US20050026830A1 (en) * | 2003-05-14 | 2005-02-03 | Yasushi Kawaguchi | Compositions and methods for treating fibrosis |
| US20060199762A1 (en) * | 2003-09-03 | 2006-09-07 | Toshikazu Nakamura | Skin ulcer preventive curative agent containing human recombinant hgf |
| EP1588718B1 (en) * | 2004-03-31 | 2010-05-19 | AnGes MG, Inc. | Gene therapy of hepatocyte growth factor to enhance muscular and cutaneous flap survival |
| TWI362940B (en) * | 2005-03-31 | 2012-05-01 | Gen Hospital Corp | A use of agonist and/or antagonist of hgf/hgfr activity |
| JP4111993B2 (ja) * | 2006-05-29 | 2008-07-02 | アンジェスMg株式会社 | リンパ管新生促進剤 |
| JP2016031772A (ja) | 2014-07-30 | 2016-03-07 | 株式会社日立ハイテクファインシステムズ | 熱アシスト磁気ヘッド素子の検査方法及びその装置 |
-
2006
- 2006-03-30 TW TW095111167A patent/TWI362940B/zh not_active IP Right Cessation
- 2006-03-30 CN CN201210536271.XA patent/CN102989012B/zh not_active Expired - Fee Related
- 2006-03-30 PL PL06749190T patent/PL1863519T3/pl unknown
- 2006-03-30 KR KR1020137019978A patent/KR20130114763A/ko active IP Right Grant
- 2006-03-30 KR KR1020147011245A patent/KR20140068234A/ko not_active Application Discontinuation
- 2006-03-30 ES ES06749190.2T patent/ES2440953T3/es active Active
- 2006-03-30 JP JP2008504520A patent/JP5313660B2/ja not_active Expired - Fee Related
- 2006-03-30 CN CN2006800191873A patent/CN101189023B/zh not_active Expired - Fee Related
- 2006-03-30 KR KR1020077024730A patent/KR20070119710A/ko not_active Application Discontinuation
- 2006-03-30 DK DK06749190.2T patent/DK1863519T3/da active
- 2006-03-30 EP EP06749190.2A patent/EP1863519B1/en not_active Not-in-force
- 2006-03-30 EP EP13172330.6A patent/EP2674165B1/en not_active Not-in-force
- 2006-03-30 WO PCT/US2006/012389 patent/WO2006105511A1/en active Application Filing
- 2006-03-31 US US11/394,422 patent/US20070010443A1/en not_active Abandoned
-
2010
- 2010-05-12 JP JP2010109852A patent/JP4664441B2/ja not_active Expired - Fee Related
- 2010-05-20 US US12/784,272 patent/US20100227821A1/en not_active Abandoned
-
2012
- 2012-04-11 JP JP2012090431A patent/JP2012149087A/ja active Pending
- 2012-09-07 US US13/606,490 patent/US8865673B2/en active Active
-
2013
- 2013-03-06 JP JP2013043836A patent/JP5801835B2/ja not_active Expired - Fee Related
- 2013-07-18 JP JP2013149577A patent/JP5722960B2/ja active Active
- 2013-09-24 HK HK13110867.4A patent/HK1183441A1/xx not_active IP Right Cessation
-
2014
- 2014-10-07 US US14/508,576 patent/US20150030611A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| US20150030611A1 (en) | 2015-01-29 |
| US20100227821A1 (en) | 2010-09-09 |
| EP2674165A3 (en) | 2014-07-30 |
| JP4664441B2 (ja) | 2011-04-06 |
| EP2674165A2 (en) | 2013-12-18 |
| DK1863519T3 (da) | 2014-01-13 |
| JP2013216690A (ja) | 2013-10-24 |
| CN101189023A (zh) | 2008-05-28 |
| TW200722099A (en) | 2007-06-16 |
| KR20140068234A (ko) | 2014-06-05 |
| JP2010265266A (ja) | 2010-11-25 |
| KR20130114763A (ko) | 2013-10-18 |
| CN101189023B (zh) | 2013-01-30 |
| PL1863519T3 (pl) | 2014-03-31 |
| CN102989012A (zh) | 2013-03-27 |
| EP1863519B1 (en) | 2013-09-25 |
| WO2006105511A1 (en) | 2006-10-05 |
| US20070010443A1 (en) | 2007-01-11 |
| JP5801835B2 (ja) | 2015-10-28 |
| TWI362940B (en) | 2012-05-01 |
| HK1183441A1 (en) | 2013-12-27 |
| JP5722960B2 (ja) | 2015-05-27 |
| EP2674165B1 (en) | 2016-10-12 |
| CN102989012B (zh) | 2015-05-13 |
| JP2008538551A (ja) | 2008-10-30 |
| US8865673B2 (en) | 2014-10-21 |
| JP2012149087A (ja) | 2012-08-09 |
| EP1863519A1 (en) | 2007-12-12 |
| KR20070119710A (ko) | 2007-12-20 |
| US20130064833A1 (en) | 2013-03-14 |
| JP2013136622A (ja) | 2013-07-11 |
| ES2440953T3 (es) | 2014-01-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5722960B2 (ja) | Hgf/hgfr活性の観察と調節 | |
| US20210169983A1 (en) | Compositions and Methods for Treatment of Metabolic Disorders and Diseases | |
| US11066454B2 (en) | Compositions comprising variants and fusions of FGF19 polypeptides | |
| US10413590B2 (en) | Methods of using compositions comprising variants of FGF19 polypeptides for reducing body mass in a subject | |
| US20200054714A1 (en) | Methods and Compositions for the Treatment of Metabolic Disorders and Diseases | |
| US20090068102A1 (en) | Treating stroke | |
| US20110059069A1 (en) | Gapr-1 Methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090330 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111011 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120110 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120411 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20121106 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130306 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130509 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130604 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130704 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |