JP5272003B2 - 食品のグリセミック指数を決定するためのインビトロ方法 - Google Patents
食品のグリセミック指数を決定するためのインビトロ方法 Download PDFInfo
- Publication number
- JP5272003B2 JP5272003B2 JP2010515074A JP2010515074A JP5272003B2 JP 5272003 B2 JP5272003 B2 JP 5272003B2 JP 2010515074 A JP2010515074 A JP 2010515074A JP 2010515074 A JP2010515074 A JP 2010515074A JP 5272003 B2 JP5272003 B2 JP 5272003B2
- Authority
- JP
- Japan
- Prior art keywords
- test food
- vitro method
- sample
- glycemic index
- food
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/66—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood sugars, e.g. galactose
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Hematology (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Diabetes (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- General Preparation And Processing Of Foods (AREA)
- Investigating Or Analyzing Non-Biological Materials By The Use Of Chemical Means (AREA)
Description
本出願は、2008年6月23日に出願した米国特許出願第12/144,056号の継続出願であり、仮出願への変更が要請された2007年6月28日出願の米国特許出願第11/770,361号の利益を主張するものであり、これらの出願は、その全体が参照により本明細書に組み込まれる。
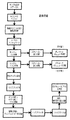
(1)試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)試験食物サンプルが得られるように、本質的に均質な微粉化された状態の試験食品を提供するステップ;
(3)消化されたサンプルが得られるように、固定期間中に、消化酵素の混合物で、標準量の利用可能な炭水化物を提供するのに十分な量の、本質的に均質な微粉化された状態にある試験食物サンプルを消化するステップ;
(4)酵素反応を停止させるため、固定期間の直後に、消化されたサンプルの全体を処理するステップ;
(5)ステップ(4)からの消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、試験食品に関するステップ(1)および(5)で得られたデータから、試験食品のグリセミック指数を計算し、但しこの較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、較正サンプルは、既知のインビボグリセミック指数値を有しているステップ
を含む方法を提供する。
(1)試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)試験食物サンプルが得られるように、本質的に均質な微粉化された状態の試験食品を提供し、但しこの試験食品は、本質的に液体窒素温度で摩砕されるステップ;
(3)消化されたサンプルが得られるように、固定期間中に、消化酵素の混合物で、標準量の利用可能な炭水化物を提供するのに十分な量の、本質的に均質な微粉化された状態にある試験食物サンプルを消化するステップ;
(4)酵素反応を停止させるため、固定期間の直後に、消化されたサンプルの全体を処理するステップ;
(5)ステップ(4)からの消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、試験食品に関するステップ(1)および(5)で得られたデータから、試験食品のグリセミック指数を計算し、但しこの較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、較正サンプルは、既知のインビボグリセミック指数値を有しているステップ
を含む方法も提供する。
(1)試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)試験食物サンプルが得られるように、本質的に均質な微粉化された状態の試験食品を提供するステップ;
(3)消化されたサンプルが得られるように、固定期間中に、消化酵素の混合物で、標準量の利用可能な炭水化物を提供するのに十分な量の、本質的に均質な微粉化された状態にある試験食物サンプルを消化するステップ;
(4)酵素反応を停止させるため、固定期間の直後に、消化されたサンプルの全体を処理するステップ;
(5)ステップ(4)からの消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、試験食品に関するステップ(1)および(5)で得られたデータから、試験食品のグリセミック指数を計算し、但しこの較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、較正サンプルは、既知のインビボグリセミック指数値を有しているステップ
を含む方法を提供する。
(1)試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)試験食物サンプルが得られるように、本質的に均質な微粉化された状態の試験食品を提供し、但しこの試験食品は、本質的に液体窒素温度で摩砕されるステップ;
(3)消化されたサンプルが得られるように、固定期間中に、消化酵素の混合物で、標準量の利用可能な炭水化物を提供するのに十分な量の、本質的に均質な微粉化された状態にある試験食物サンプルを消化するステップ;
(4)酵素反応を停止させるため、固定期間の直後に、消化されたサンプルの全体を処理するステップ;
(5)ステップ(4)からの消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、試験食品に関するステップ(1)および(5)で得られたデータから、試験食品のグリセミック指数を計算し、但しこの較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、較正サンプルは、既知のインビボグリセミック指数値を有しているステップ
を含む方法も提供する。
1.温度制御式振盪水浴(約175ストローク/分が可能);
2.ボルテックスミキサ;
3.化学天秤(±0.0001gまで正確);
4.容量フラスコ、クラスA、100ml、1000ml;
5.ピペット、クラスA、1ml、2ml、5ml、6ml、10ml;
6.ガラスボール、6mm(Fischer#11−312−Dまたは同等物)
7.スクリュキャップを備えたガラスサンプルバイアル(40ml)(VWR#66014−389または同等物);
8.スクリュキャップを備えたプラスチック遠心管(50ml)(VWR#21008−730または同等物);
9.遠心分離機;
10.Spex CertiPrep 6850フリーザミルまたは同等物;
11.1Qt.広口Masonジャー;
12.濾過漏斗;
13.Whatman#4高速濾紙、12.5cmの円、または同等物;
14.リングスタンド;
15.Anotop 10 Plus 0.2ミクロン 10mm直径シリンジフィルタ;
16.HPIC装置、および以下の「HPIC手順」という標題のセクションに列挙される試薬;および
17.JMP統計ソフトウェア、バージョン5.1、SAS Institute、または同等物。
1.0.5N塩酸(HCl)(VWR#VW3201−0);
2.酢酸ナトリウム(NaAc)(Acros#42425−5000);
3.エチルアルコールUSP、190プルーフ−95%(95%EtOH)(Aaper Alcohol & Chemical Co.);
4.パン酵母のインベルターゼ、215U/mg固体(Sigma#1−9274);
5.アミログルコシダーゼ(AMG)、300U/ml(Novozymes#$ANG300L)(注記:0〜25℃で保存し、配達日から3カ月以内に使用すべきである。);
6.ブタ胃粘膜からのペプシン、439U/mg固体(Sigma#P−7000)
7.グアーガム(Sigma#G4129−250G);
8.ブタ膵臓からのパンクレアチン(Sigma#P−7545);
9.脱イオン水(H2O);および
10.液体窒素;および
11.無水グルコース、フルクトース、スクロース、ラクトース、ガラクトース、およびマルチトールの純粋な標準(最小99%純度、Sigma Aldrich Company、または同等物;使用しないときはデシケータ内で保存すべきである。)。
1.0.05N HCl溶液(脱イオン水で、100mlの0.5N HClを1000mlに希釈する。);
2.ペプシン/グアーガム溶液(2195U/mlペプシンおよび0.5%グアーガム(W/V)、0.05N HCl中)−0.5gのペプシンおよび0.5gのグアーガムを100mlの0.05N HClに溶解する;
3.インベルターゼ原液(510.7U/ml、H2O中)−100mgのインベルターゼを42.10mlのH2Oに溶解する;
4.0.5M酢酸ナトリウム溶液(H2O中0.5M NaAc)−4.10gの酢酸ナトリウムを100mlのH2Oに溶解する;
5.66%エチルアルコール溶液(66%EtOH)(V/V)−347mlのメチルアルコールを、1クォートのメーソンジャー内で153mlの脱イオン水と混合し、キャップする;これは、1つのサンプルに十分な溶液である;および
6.酵素溶液(1つのサンプルの処方−136mg/mlパンクレアチン、13.4U/ml AMGおよび25.43U/mlインベルターゼ);
i.1.0gのパンクレアチンを50mlの遠心管に計量する;
ii.6.67ml H2Oを添加し、10分間ボルテックス混合して完全に溶解する(多数のサンプルに使用される溶液を調製する場合には、攪拌棒またはガラスボールが必要となる場合がある。);
iii.2000rpmで10分間遠心分離する;および
iv.各試験サンプルごとに、6mlの上澄みを別の50mlの遠心管に移し、296μlのAMGおよび330μlのインベルターゼ原液を添加する。
高速性能ポンプ;
液体クロマトグラフィーモジュール;
パルス式電気化学検出器;
溶離剤脱気モジュール;および
Dionex Chromeleonクロマトグラフィーワークステーション
からなるDionexクロマトグラフィーシステム。
脱イオン水、18MΩ−cm抵抗;
水酸化ナトリウム溶液、50%w/w、低カーボネート;および
ガラクトース、グルコース、フルクトース、スクロース、ラクトース、およびマルチトールの純粋標準。
カラム:CarboPacTM PA1分析(4×250mm)およびAminoTrapガード(4×50mm)カラム;
操作条件:圧力:1200〜1500psi;注入体積;10μL;
溶離剤:21mM水酸化ナトリウム(各カラムで最良の分離が実現するように調節することができる;注記:CarboPac PA1は、カラム面にカーボネートが蓄積されないように、各操作ごとに200mM NaOHで洗浄すべきである。);
流量:1mL/分;および
検出:パルス式電流測定、使い捨て可能な金の作用電極、よび標準炭水化物設定。
a)溶離剤:NaOH溶液(50%w/w、低カーボネート)1.6725gを脱イオン水1.0L(18MΩ−cm抵抗)に希釈する;
b)カラム洗浄溶液:200mM NaOH:NaOH溶液(50%w/w、低カーボネート)16gを脱イオン水(18MΩ−cm抵抗)1.0Lに希釈する。
約6種の標準(即ち、ガラクトース、グルコース、フルクトース、スクロース、ラクトース、およびマルチトールの純粋な標準)のそれぞれの約0.1000gmを、100ml容量フラスコに正確に計量して、1000ppmの混合標準を脱イオン水(18MΩ−cm抵抗)で作製する。この溶液を希釈して、以下の作用標準を生成する:
a)1mlを、66mlのエチルアルコール(195プルーフ)を含む1000mlに希釈して、1ppm標準を作製する;
b)2mlを、6.6mlのエチルアルコール(195プルーフ)を含む100mlに希釈して、20ppm標準を作製する;
c)5mlを、6.6mlのエチルアルコール(195プルーフ)を含む100mlに希釈して、50ppm標準を作製する;および
d)10mlを、6.6mlのエチルアルコール(195プルーフ)を含む100mlに希釈して、100ppm標準を作製する。
消化手順からの最終的な消化溶液を、脱イオン水で1:10に希釈し、次いで0.2ミクロンのAnotop 10 Plusシリンジフィルタに通してオートサンプラバイアルに濾過する。次いで溶液(10μl)のサンプルを、クロマトグラフに注入する。
GI=63.080214−0.974313タンパク質(%)−0.67442脂肪(%)+367.97478グルコース(%)−452.5341フルクトース(%)−191.8138ラクトース(%)−437.3615ガラクトース(%)−298.0102マルチトール(%)
になる。
このモデルに関連する統計的パラメータは、下記の通りである:
当てはめの概要:
GI=62.745005−0.986004タンパク質(%)−0.670993脂肪(%)+369.91833グルコース(%)−446.4468フルクトース(%)−195.07ラクトース(%)−425.7489ガラクトース(%)−291.9779マルチトール(%)
になる。
このモデルに関連する統計的パラメータは、下記の通りである:
当てはめの概要:
GI=26.779686−0.967251タンパク質(%)−0.385715脂肪(%)+611.60013グルコース(%)+301.95014ラクトース(%)+169.03383マルチトール(%)−18.16062[グルコース(%)−0.05718]×[タンパク質(%)−8.24967]
になる。
このモデルに関連する統計パラメータは、下記の通りである:
当てはめの概要:
GI=26.264529−1.048186タンパク質(%)−0.248138脂肪(%)+621.7824グルコース(%)−52.7993フルクトース(%)+233.67679ラクトース(%)−61.21071ガラクトース(%)+84.689245マルチトール(%)
になる。
このモデルに関連する統計パラメータは、下記の通りである:
当てはめの概要:
GI=30.502796−0.787639タンパク質(%)−0.515649脂肪(%)+573.03525グルコース(%)+275.61246ラクトース(%)+147.62386マルチトール(%)−20.39966[グルコース(%)−0.05091]×[タンパク質(%)−10.0429]。
このモデルに関連する統計パラメータは、下記の通りである:
当てはめの概要
GI=48.443999−1.003763タンパク質(%)−0.492915脂肪(%)+443.60721グルコース(%)−265.4383フルクトース(%)−33.78516ラクトース(%)−277.1671ガラクトース(%)−142.2773マルチトール(%)
になる。
このモデルに関連する統計パラメータは、下記の通りである:
当てはめの概要
Claims (20)
- 試験食品のグリセミック指数を決定するためのインビトロ方法であって、
(1)前記試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)本質的に均質かつ微粉化された状態の試験食品を提供することにより、試験食物サンプルを提供するステップ;
(3)標準量の利用可能な炭水化物を提供するのに十分な量の本質的に均質かつ微粉化された状態の前記試験食物サンプルを、一定期間、消化酵素の混合物を用いて消化することにより、消化されたサンプルを提供するステップ;
(4)前記消化されたサンプルを、前記一定期間経過直後に、そのまま処理することにより、酵素反応を停止させるステップ;
(5)ステップ(4)からの前記消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールからなる群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、前記試験食品に関するステップ(1)および(5)で得られたデータから、前記試験食品のグリセミック指数を計算するステップであって、前記較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、前記較正サンプルは、既知のインビボグリセミック指数値を有するものであるステップ;
を含むことを特徴とするインビトロ方法。 - 前記請求項1に記載のインビトロ方法であって、ステップ(5)に列挙されたすべての糖および糖アルコールの量が決定され、それがステップ(6)のグリセミック指数の計算に使用されることを特徴とするインビトロ方法。
- 前記請求項1に記載のインビトロ方法であって、前記試験食品は、前記試験食品を約−40℃よりも低い温度で摩砕することによって、本質的に均質な微粉化された状態で得られることを特徴とするインビトロ方法。
- 前記請求項2に記載のインビトロ方法であって、前記試験食品は、前記試験食品を約−78℃以下の温度で摩砕することによって、本質的に均質な微粉化された状態で得られることを特徴とするインビトロ方法。
- 前記請求項1に記載のインビトロ方法であって、前記試験食品は、前記試験食品を液体窒素温度でまたは液体窒素温度付近の温度で摩砕することによって、本質的に均質な微粉化された状態で得られることを特徴とするインビトロ方法。
- 前記請求項2に記載のインビトロ方法であって、前記試験食品は、前記試験食品を液体窒素温度でまたは液体窒素温度付近の温度で摩砕することによって、本質的に均質な微粉化された状態で得られることを特徴とするインビトロ方法。
- 前記請求項1に記載のインビトロ方法であって、ステップ(4)の前記消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールからなる群から選択された少なくとも2種の糖または糖アルコールとの量は、高速イオンクロマトグラフィーを使用して決定されることを特徴とするインビトロ方法。
- 前記請求項2に記載のインビトロ方法であって、ステップ(4)の前記消化されたサンプル中の、グルコースと糖または糖アルコールとの量は、高速イオンクロマトグラフィーを使用して決定されることを特徴とするインビトロ方法。
- 前記請求項1に記載のインビトロ方法であって、前記試験食品は、前記試験食品を約−40℃よりも低い温度で摩砕することによって、本質的に均質な微粉化された状態で得られ、ステップ(4)の消化されたサンプル中のグルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールからなる群から選択された少なくとも2種の糖または糖アルコールとの量は、高速イオンクロマトグラフィーを使用して決定されることを特徴とするインビトロ方法。
- 前記請求項2に記載のインビトロ方法であって、前記試験食品は、前記試験食品を約−40℃よりも低い温度で摩砕することによって、本質的に均質な微粉化された状態で得られ、ステップ(4)の消化されたサンプル中のグルコース、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの量は、高速イオンクロマトグラフィーを使用して決定されることを特徴とするインビトロ方法。
- 試験食品のグリセミック指数を決定するためのインビトロ方法であって、
(1)前記試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)前記試験食品を液体窒素温度でまたは液体窒素温度付近で摩砕することによって本質的かつ均質な微粉化された状態の試験食品を提供することにより、試験食物サンプルを提供するステップ;
(3)標準量の利用可能な炭水化物を提供するのに十分な量の本質的に均質かつ微粉化された状態の前記試験食物サンプルを、一定期間、消化酵素の混合物を用いて消化することにより、消化されたサンプルを提供するステップ;
(4)前記消化されたサンプルを、前記一定期間経過直後に、そのまま処理することにより、酵素反応を停止させるステップ;
(5)ステップ(4)からの前記消化されたサンプル中の、グルコースと、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの群から選択された少なくとも2種の糖または糖アルコールとの量を決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、前記試験食品に関するステップ(1)および(5)で得られたデータから前記試験食品のグリセミック指数を計算するステップであって、前記較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、前記較正サンプルは、既知のインビボグリセミック指数値を有するものであるステップ
を含むことを特徴とするインビトロ方法。 - 前記請求項11に記載のインビトロ方法であって、前記多変量解析は、多重線形回帰、部分最小二乗法、およびニューラルネットからなる群から選択された曲線当てはめ手順を使用することを特徴とするインビトロ方法。
- 前記請求項12に記載のインビトロ方法であって、前記曲線当てはめ手順は、多重線形回帰であることを特徴とするインビトロ方法。
- 前記請求項12に記載のインビトロ方法であって、前記曲線当てはめ手順は、部分最小二乗法であることを特徴とするインビトロ方法。
- 前記請求項12に記載のインビトロ方法であって、前記曲線当てはめ手順は、ニューラルネットであることを特徴とするインビトロ方法。
- 試験食品のグリセミック指数を決定するためのインビトロ方法であって、
(1)前記試験食品のタンパク質含量および脂肪含量を決定するステップ;
(2)前記試験食品を液体窒素温度または液体窒素近くの温度で摩砕して本質的に均質かつ微粉化された状態の試験食品を提供することにより、試験食物サンプルを提供するステップ;
(3)標準量の利用可能な炭水化物を提供するのに十分な量の本質的に均質かつ微粉化された状態の前記試験食物サンプルを、一定期間、消化酵素の混合物を用いて消化することにより、消化されたサンプルを提供するステップ;
(4)前記消化されたサンプルを、前記一定期間経過直後に、そのまま処理することにより、酵素反応を停止させるステップ;
(5)ステップ(4)からの前記消化されたサンプル中の、グルコース、フルクトース、ガラクトース、ラクトース、スクロース、およびマルチトールの量を高速イオンクロマトグラフィーを使用して決定するステップ;および
(6)較正サンプルに関する較正データの多変量解析から導き出された予測方程式または予測技法を使用して、前記試験食品に関するステップ(1)および(5)で得られたデータから、前記試験食品のグリセミック指数を計算するステップであって、前記較正データは、ステップ(1)および(5)で決定された試験食品に関するデータと同じタイプのものでありかつ同じ手法で得られるものであり、前記較正サンプルは、既知のインビボグリセミック指数値を有するものであるステップ;
を含むことを特徴とするインビトロ方法。 - 前記請求項16に記載のインビトロ方法であって、前記多変量解析は、多重線形回帰、部分最小二乗法、およびニューラルネットからなる群から選択された曲線当てはめ手順を使用することを特徴とするインビトロ方法。
- 前記請求項17に記載のインビトロ方法であって、前記曲線当てはめ手順は、多重線形回帰であることを特徴とするインビトロ方法。
- 前記請求項17に記載のインビトロ方法であって、前記曲線当てはめ手順は、部分最小二乗法であることを特徴とするインビトロ方法。
- 前記請求項17に記載のインビトロ方法であって、前記曲線当てはめ手順は、ニューラルネットであることを特徴とするインビトロ方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US77036107A | 2007-06-28 | 2007-06-28 | |
| US11/770,361 | 2007-06-28 | ||
| US12/144,056 | 2008-06-23 | ||
| US12/144,056 US9109247B2 (en) | 2007-06-28 | 2008-06-23 | In vitro method for the determination of glycemic index of food products |
| PCT/US2008/068176 WO2009006155A1 (en) | 2007-06-28 | 2008-06-25 | In vitro method for the determination of glycemic index of food products |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010532001A JP2010532001A (ja) | 2010-09-30 |
| JP5272003B2 true JP5272003B2 (ja) | 2013-08-28 |
Family
ID=39736991
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010515074A Expired - Fee Related JP5272003B2 (ja) | 2007-06-28 | 2008-06-25 | 食品のグリセミック指数を決定するためのインビトロ方法 |
Country Status (14)
| Country | Link |
|---|---|
| EP (1) | EP2171472B1 (ja) |
| JP (1) | JP5272003B2 (ja) |
| KR (1) | KR101138598B1 (ja) |
| CN (1) | CN101784898B (ja) |
| AT (1) | ATE537452T1 (ja) |
| AU (1) | AU2008270671B2 (ja) |
| BR (1) | BRPI0813241A2 (ja) |
| CA (1) | CA2691062C (ja) |
| DK (1) | DK2171472T3 (ja) |
| IL (1) | IL202786A (ja) |
| MX (1) | MX2009014177A (ja) |
| RU (1) | RU2451938C2 (ja) |
| WO (1) | WO2009006155A1 (ja) |
| ZA (1) | ZA200909056B (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2171472B1 (en) | 2007-06-28 | 2011-12-14 | Kraft Foods Global Brands LLC | In vitro method for the determination of glycemic index of food products |
| EP2261668A1 (en) | 2009-06-11 | 2010-12-15 | Nederlandse Organisatie voor toegepast -natuurwetenschappelijk onderzoek TNO | Method for predicting glycaemic response and use thereof |
| WO2014096184A1 (en) * | 2012-12-20 | 2014-06-26 | Roche Diagnostics Gmbh | Method for analyzing a sample of a body fluid |
| US9672331B2 (en) * | 2013-12-17 | 2017-06-06 | Alltech, Inc. | Systems and methods for computer models of animal feed |
| RU2596506C1 (ru) | 2015-03-13 | 2016-09-10 | Общество С Ограниченной Ответственностью "Хилби" | Способ определения гликемического индекса потребляемой человеком пищи |
| CN106680383A (zh) * | 2015-11-09 | 2017-05-17 | 北京工商大学 | 一种便捷的测定食品血糖生成指数的体外方法 |
| TWI574009B (zh) * | 2016-01-18 | 2017-03-11 | 醫博科技股份有限公司 | 應用於食物升糖指數評估之快速測定方法 |
| CN105911007A (zh) * | 2016-06-14 | 2016-08-31 | 安徽平唐微食疗科技有限公司 | 一种血糖生成指数体外检测方法 |
| CN106135133B (zh) * | 2016-08-02 | 2018-10-16 | 四川大学 | 验证食物血糖生成指数动物实验模型的构建方法及其构建的动物模型 |
| RU2696958C1 (ru) * | 2018-12-10 | 2019-08-07 | Федеральное государственное бюджетное учреждение науки "Институт токсикологии Федерального медико-биологического агентства" (ФГБУН ИТ ФМБА России) | Способ определения ртути в биологических материалах |
| CN112557607A (zh) * | 2020-11-09 | 2021-03-26 | 中粮营养健康研究院有限公司 | 通过仿生模拟消化吸收技术预测食物血糖生成指数的方法 |
| CN113238010B (zh) * | 2021-04-27 | 2022-06-07 | 暨南大学 | 一种体外测定碳水化合物食物的血糖生成指数的方法 |
| CN115032350B (zh) * | 2022-06-13 | 2023-08-01 | 暨南大学 | 一种体外测定面条食品血糖生成指数的方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1337765A1 (ru) * | 1985-11-29 | 1987-09-15 | Институт питания АМН СССР | Способ определени гликемического индекса пищевых продуктов по глюкозе |
| US5843786A (en) * | 1995-11-28 | 1998-12-01 | Neose Technologies, Inc. | Analysis of carbohydrates in biological fluids by high performance liquid chromatography |
| EP1660889B1 (en) * | 2003-08-13 | 2011-05-11 | Ceapro Inc. | Diagnostic composition for diabetes type-2 and impaired glucose tolerance, and methods of use |
| US20060003400A1 (en) * | 2004-06-30 | 2006-01-05 | Byrd Patricia A | Methods and compositions for characterizing a redox reagent system enzyme |
| CN100466920C (zh) * | 2005-01-28 | 2009-03-11 | 黑龙江省农业科学院食品加工研究所 | 一种低血糖生成指数营养粉及其制备方法 |
| EP2171472B1 (en) | 2007-06-28 | 2011-12-14 | Kraft Foods Global Brands LLC | In vitro method for the determination of glycemic index of food products |
-
2008
- 2008-06-25 EP EP08771919A patent/EP2171472B1/en not_active Not-in-force
- 2008-06-25 JP JP2010515074A patent/JP5272003B2/ja not_active Expired - Fee Related
- 2008-06-25 CA CA2691062A patent/CA2691062C/en not_active Expired - Fee Related
- 2008-06-25 IL IL202786A patent/IL202786A/en not_active IP Right Cessation
- 2008-06-25 RU RU2010102733/15A patent/RU2451938C2/ru not_active IP Right Cessation
- 2008-06-25 KR KR1020107001892A patent/KR101138598B1/ko not_active IP Right Cessation
- 2008-06-25 AU AU2008270671A patent/AU2008270671B2/en not_active Ceased
- 2008-06-25 CN CN200880105327.8A patent/CN101784898B/zh not_active Expired - Fee Related
- 2008-06-25 MX MX2009014177A patent/MX2009014177A/es active IP Right Grant
- 2008-06-25 BR BRPI0813241-0A2A patent/BRPI0813241A2/pt not_active IP Right Cessation
- 2008-06-25 AT AT08771919T patent/ATE537452T1/de active
- 2008-06-25 DK DK08771919.1T patent/DK2171472T3/da active
- 2008-06-25 WO PCT/US2008/068176 patent/WO2009006155A1/en active Application Filing
-
2009
- 2009-12-18 ZA ZA200909056A patent/ZA200909056B/xx unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CN101784898A (zh) | 2010-07-21 |
| JP2010532001A (ja) | 2010-09-30 |
| DK2171472T3 (da) | 2012-02-06 |
| RU2451938C2 (ru) | 2012-05-27 |
| ZA200909056B (en) | 2010-09-29 |
| RU2010102733A (ru) | 2011-08-10 |
| WO2009006155A1 (en) | 2009-01-08 |
| EP2171472B1 (en) | 2011-12-14 |
| BRPI0813241A2 (pt) | 2014-12-23 |
| MX2009014177A (es) | 2010-03-11 |
| AU2008270671A1 (en) | 2009-01-08 |
| CN101784898B (zh) | 2014-03-19 |
| IL202786A (en) | 2013-02-28 |
| EP2171472A1 (en) | 2010-04-07 |
| ATE537452T1 (de) | 2011-12-15 |
| IL202786A0 (en) | 2010-06-30 |
| CA2691062A1 (en) | 2009-01-08 |
| KR20100038401A (ko) | 2010-04-14 |
| AU2008270671B2 (en) | 2011-01-20 |
| KR101138598B1 (ko) | 2012-05-10 |
| CA2691062C (en) | 2012-11-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5272003B2 (ja) | 食品のグリセミック指数を決定するためのインビトロ方法 | |
| US9109247B2 (en) | In vitro method for the determination of glycemic index of food products | |
| Englyst et al. | Rapidly available glucose in foods: an in vitro measurement that reflects the glycemic response | |
| Kiszonas et al. | A critical assessment of the quantification of wheat grain arabinoxylans using a phloroglucinol colorimetric assay | |
| Hernández-López et al. | Quantification of reducing sugars based on the qualitative technique of Benedict | |
| US20050244910A1 (en) | Methods for determining glycemic responses of foods | |
| CN112051367A (zh) | 一种测定食品血糖生成指数的体外消化模型方法 | |
| Wei et al. | Sensitive quantification of cannabinoids in milk by alkaline saponification–solid phase extraction combined with isotope dilution UPLC–MS/MS | |
| Yu et al. | Establishing reference intervals for urine and serum iodine levels: A nationwide multicenter study of a euthyroid Chinese population | |
| TWI574009B (zh) | 應用於食物升糖指數評估之快速測定方法 | |
| Fang et al. | Simultaneous analysis of the stable carbon isotope ratios of acetoin and acetic acid by GC-C-IRMS for adulteration detection in brewed rice vinegar products | |
| Müller et al. | Quantitative saccharide release of hydrothermally treated flours by validated salivary/pancreatic on-surface amylolysis (nanoGIT) and high-performance thin-layer chromatography | |
| Ciobanu et al. | Glycated albumin is correlated with glycated hemoglobin in type 2 diabetes | |
| Yu et al. | Age-and Gender-Specific Reference Intervals for the Fasting Serum Lipid Levels in a Pediatric Population Aged 0–< 15 Years in Nanjing, China | |
| MQ et al. | The metabolic effects of two meals with the same glycaemic index but different slowly available glucose parameters determined in vitro: a pilot study | |
| Delanghe | Standardization of creatinine determination and its consequences for the clinician | |
| Sunada et al. | Clinical utility of urinary levels of catecholamines and their fraction ratios related to heart rate and thyroid function | |
| Chen | Using linear regression model to explore the relationship between testosterone and SUA in adult males: NHANES 2013–2016 | |
| El-Fahkhri | Modification and validation of a semi-automated in vitro method for predicting the glycemic index of starchy foods | |
| He et al. | Postprandial lipid profile characteristics and their influencing factors in Chinese healthy volunteers with normal fasting blood lipids | |
| Shahfiza et al. | Metabolomics for characterization of gender differences in patients infected with dengue virus | |
| Li et al. | Accuracy Evaluation of Five Blood Glucose Monitoring Systems in Patients from Different Departments | |
| CN100529043C (zh) | 蛇葡萄素保健酒 | |
| Aisha et al. | Salivary Glucose as a Potential Biomarker for Monitoring Blood Glucose Levels in Type 2 Diabetes Mellitus: Current Insights and Future Prospects | |
| Mishra et al. | Digestive analysis of processing effects on the glycaemic impact of oats in vitro. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110506 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121116 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130215 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130412 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130513 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| LAPS | Cancellation because of no payment of annual fees |