JP5017377B2 - pH及びグルコースの光学的決定 - Google Patents
pH及びグルコースの光学的決定 Download PDFInfo
- Publication number
- JP5017377B2 JP5017377B2 JP2009549167A JP2009549167A JP5017377B2 JP 5017377 B2 JP5017377 B2 JP 5017377B2 JP 2009549167 A JP2009549167 A JP 2009549167A JP 2009549167 A JP2009549167 A JP 2009549167A JP 5017377 B2 JP5017377 B2 JP 5017377B2
- Authority
- JP
- Japan
- Prior art keywords
- analyte
- optical sensor
- glucose
- quencher
- sensor according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 title claims description 111
- 239000008103 glucose Substances 0.000 title claims description 111
- 230000003287 optical effect Effects 0.000 title claims description 50
- 238000013494 PH determination Methods 0.000 title description 7
- 239000012491 analyte Substances 0.000 claims description 78
- 229920000642 polymer Polymers 0.000 claims description 74
- 239000007850 fluorescent dye Substances 0.000 claims description 70
- 230000005284 excitation Effects 0.000 claims description 66
- 239000011159 matrix material Substances 0.000 claims description 56
- 150000001875 compounds Chemical class 0.000 claims description 51
- 230000027455 binding Effects 0.000 claims description 44
- KXXXUIKPSVVSAW-UHFFFAOYSA-K pyranine Chemical group [Na+].[Na+].[Na+].C1=C2C(O)=CC(S([O-])(=O)=O)=C(C=C3)C2=C2C3=C(S([O-])(=O)=O)C=C(S([O-])(=O)=O)C2=C1 KXXXUIKPSVVSAW-UHFFFAOYSA-K 0.000 claims description 41
- 239000000017 hydrogel Substances 0.000 claims description 35
- 239000008280 blood Substances 0.000 claims description 18
- 210000004369 blood Anatomy 0.000 claims description 18
- 230000008878 coupling Effects 0.000 claims description 12
- 238000010168 coupling process Methods 0.000 claims description 12
- 238000005859 coupling reaction Methods 0.000 claims description 12
- 239000013307 optical fiber Substances 0.000 claims description 12
- 230000008859 change Effects 0.000 claims description 10
- 229920003176 water-insoluble polymer Polymers 0.000 claims description 6
- WFOTVGYJMFZMTD-UHFFFAOYSA-N 3',10'-dihydroxyspiro[2-benzofuran-3,7'-benzo[c]xanthene]-1-one Chemical compound O1C(=O)C2=CC=CC=C2C21C(C=CC=1C3=CC=C(O)C=1)=C3OC1=CC(O)=CC=C21 WFOTVGYJMFZMTD-UHFFFAOYSA-N 0.000 claims description 3
- 230000003100 immobilizing effect Effects 0.000 claims description 3
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical group OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- PBHVCRIXMXQXPD-UHFFFAOYSA-N chembl2369102 Chemical compound C1=CC(S(=O)(=O)O)=CC=C1C(C1=CC=C(N1)C(C=1C=CC(=CC=1)S(O)(=O)=O)=C1C=CC(=N1)C(C=1C=CC(=CC=1)S(O)(=O)=O)=C1C=CC(N1)=C1C=2C=CC(=CC=2)S(O)(=O)=O)=C2N=C1C=C2 PBHVCRIXMXQXPD-UHFFFAOYSA-N 0.000 claims description 2
- 239000000975 dye Substances 0.000 description 92
- 239000002253 acid Substances 0.000 description 33
- 229910052757 nitrogen Inorganic materials 0.000 description 25
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 24
- 238000000034 method Methods 0.000 description 24
- 239000000243 solution Substances 0.000 description 21
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 20
- 125000005620 boronic acid group Chemical group 0.000 description 20
- 238000001139 pH measurement Methods 0.000 description 19
- 230000004044 response Effects 0.000 description 19
- 238000010521 absorption reaction Methods 0.000 description 18
- 239000000523 sample Substances 0.000 description 15
- -1 SNARF-1 Chemical compound 0.000 description 14
- 239000000835 fiber Substances 0.000 description 14
- 238000005259 measurement Methods 0.000 description 14
- 238000010791 quenching Methods 0.000 description 14
- 230000000171 quenching effect Effects 0.000 description 14
- 239000002609 medium Substances 0.000 description 12
- 239000000178 monomer Substances 0.000 description 12
- 238000001727 in vivo Methods 0.000 description 11
- 125000003118 aryl group Chemical group 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 10
- 230000001419 dependent effect Effects 0.000 description 9
- 238000001514 detection method Methods 0.000 description 9
- 238000012544 monitoring process Methods 0.000 description 9
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 8
- 125000005647 linker group Chemical group 0.000 description 8
- GNWBLLYJQXKPIP-ZOGIJGBBSA-N (1s,3as,3bs,5ar,9ar,9bs,11as)-n,n-diethyl-6,9a,11a-trimethyl-7-oxo-2,3,3a,3b,4,5,5a,8,9,9b,10,11-dodecahydro-1h-indeno[5,4-f]quinoline-1-carboxamide Chemical compound CN([C@@H]1CC2)C(=O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](C(=O)N(CC)CC)[C@@]2(C)CC1 GNWBLLYJQXKPIP-ZOGIJGBBSA-N 0.000 description 7
- 238000000862 absorption spectrum Methods 0.000 description 7
- 230000002378 acidificating effect Effects 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 230000009977 dual effect Effects 0.000 description 6
- 239000003269 fluorescent indicator Substances 0.000 description 6
- 238000000338 in vitro Methods 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- 102100026735 Coagulation factor VIII Human genes 0.000 description 5
- 101000911390 Homo sapiens Coagulation factor VIII Proteins 0.000 description 5
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 5
- 125000002947 alkylene group Chemical group 0.000 description 5
- 125000000129 anionic group Chemical group 0.000 description 5
- 239000012736 aqueous medium Substances 0.000 description 5
- 230000007423 decrease Effects 0.000 description 5
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 238000006116 polymerization reaction Methods 0.000 description 5
- 229940124530 sulfonamide Drugs 0.000 description 5
- 150000003456 sulfonamides Chemical class 0.000 description 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 238000002835 absorbance Methods 0.000 description 4
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 239000007793 ph indicator Substances 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- DYPYMMHZGRPOCK-UHFFFAOYSA-N seminaphtharhodafluor Chemical compound O1C(=O)C2=CC=CC=C2C21C(C=CC=1C3=CC=C(O)C=1)=C3OC1=CC(N)=CC=C21 DYPYMMHZGRPOCK-UHFFFAOYSA-N 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 230000003595 spectral effect Effects 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 239000010409 thin film Substances 0.000 description 4
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 4
- MWVTWFVJZLCBMC-UHFFFAOYSA-N 4,4'-bipyridine Chemical group C1=NC=CC(C=2C=CN=CC=2)=C1 MWVTWFVJZLCBMC-UHFFFAOYSA-N 0.000 description 3
- KYARBIJYVGJZLB-UHFFFAOYSA-N 7-amino-4-hydroxy-2-naphthalenesulfonic acid Chemical compound OC1=CC(S(O)(=O)=O)=CC2=CC(N)=CC=C21 KYARBIJYVGJZLB-UHFFFAOYSA-N 0.000 description 3
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical group N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 3
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 210000004204 blood vessel Anatomy 0.000 description 3
- 238000011088 calibration curve Methods 0.000 description 3
- 239000004202 carbamide Substances 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 239000003086 colorant Substances 0.000 description 3
- 238000012937 correction Methods 0.000 description 3
- 150000004985 diamines Chemical class 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 229920001477 hydrophilic polymer Polymers 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical class [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 3
- 229920000620 organic polymer Polymers 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 150000003457 sulfones Chemical class 0.000 description 3
- 125000000542 sulfonic acid group Chemical group 0.000 description 3
- 229920001169 thermoplastic Polymers 0.000 description 3
- 239000004416 thermosoftening plastic Substances 0.000 description 3
- 229920003169 water-soluble polymer Polymers 0.000 description 3
- YAIPUKTYJXXKKF-UHFFFAOYSA-N 2-methyl-N-(3-sulfamoylpropyl)prop-2-enamide Chemical compound CC(=C)C(=O)NCCCS(N)(=O)=O YAIPUKTYJXXKKF-UHFFFAOYSA-N 0.000 description 2
- OFDVABAUFQJWEZ-UHFFFAOYSA-N 3-pyridin-3-ylpyridine Chemical group C1=CN=CC(C=2C=NC=CC=2)=C1 OFDVABAUFQJWEZ-UHFFFAOYSA-N 0.000 description 2
- ABVCMDMBWDRVAG-UHFFFAOYSA-N 4-hydroxypyrene-1,2,3-trisulfonamide Chemical class C1=CC=C2C=C(O)C3=C(S(N)(=O)=O)C(S(=O)(=O)N)=C(S(N)(=O)=O)C4=CC=C1C2=C43 ABVCMDMBWDRVAG-UHFFFAOYSA-N 0.000 description 2
- OMPGKWICGUBROA-UHFFFAOYSA-N 4-sulfamoylbutanoic acid Chemical compound NS(=O)(=O)CCCC(O)=O OMPGKWICGUBROA-UHFFFAOYSA-N 0.000 description 2
- OBJOZRVSMLPASY-UHFFFAOYSA-N 8-hydroxypyrene-1,3,6-trisulfonic acid Chemical compound C1=C2C(O)=CC(S(O)(=O)=O)=C(C=C3)C2=C2C3=C(S(O)(=O)=O)C=C(S(O)(=O)=O)C2=C1 OBJOZRVSMLPASY-UHFFFAOYSA-N 0.000 description 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 2
- GAIQIDITLZQBHB-UHFFFAOYSA-N [3,6,8-tris(chlorosulfonyl)pyren-1-yl] acetate Chemical compound C1=C2C(OC(=O)C)=CC(S(Cl)(=O)=O)=C(C=C3)C2=C2C3=C(S(Cl)(=O)=O)C=C(S(Cl)(=O)=O)C2=C1 GAIQIDITLZQBHB-UHFFFAOYSA-N 0.000 description 2
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- HBWDWGMBZIFBQE-UHFFFAOYSA-N benzylboronic acid Chemical group OB(O)CC1=CC=CC=C1 HBWDWGMBZIFBQE-UHFFFAOYSA-N 0.000 description 2
- 239000000560 biocompatible material Substances 0.000 description 2
- 229920000249 biocompatible polymer Polymers 0.000 description 2
- 210000001124 body fluid Anatomy 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000007334 copolymerization reaction Methods 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 238000000295 emission spectrum Methods 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 238000000855 fermentation Methods 0.000 description 2
- 230000004151 fermentation Effects 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 229920000592 inorganic polymer Polymers 0.000 description 2
- 230000001678 irradiating effect Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 239000012982 microporous membrane Substances 0.000 description 2
- 239000003068 molecular probe Substances 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 238000012643 polycondensation polymerization Methods 0.000 description 2
- 229920000867 polyelectrolyte Polymers 0.000 description 2
- 150000004032 porphyrins Chemical class 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 239000012048 reactive intermediate Substances 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 125000000565 sulfonamide group Chemical group 0.000 description 2
- 229920001187 thermosetting polymer Polymers 0.000 description 2
- 150000000180 1,2-diols Chemical class 0.000 description 1
- 150000000185 1,3-diols Chemical class 0.000 description 1
- BIJNHUAPTJVVNQ-UHFFFAOYSA-N 1-Hydroxypyrene Chemical class C1=C2C(O)=CC=C(C=C3)C2=C2C3=CC=CC2=C1 BIJNHUAPTJVVNQ-UHFFFAOYSA-N 0.000 description 1
- YEBQUUKDSJCPIX-UHFFFAOYSA-N 12h-benzo[a]thioxanthene Chemical class C1=CC=CC2=C3CC4=CC=CC=C4SC3=CC=C21 YEBQUUKDSJCPIX-UHFFFAOYSA-N 0.000 description 1
- VXXRMBQHVJKWIC-UHFFFAOYSA-N 2-(1-pyridin-2-ylethenyl)pyridine Chemical group C=1C=CC=NC=1C(=C)C1=CC=CC=N1 VXXRMBQHVJKWIC-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- OLYBTQCLJOBELT-UHFFFAOYSA-N 2-bromoethanamine;hydrochloride Chemical compound Cl.NCCBr OLYBTQCLJOBELT-UHFFFAOYSA-N 0.000 description 1
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 1
- MSQCQZMTRWHMFQ-UHFFFAOYSA-N 3-(2-methylprop-2-enoyloxy)propane-1-sulfonic acid;sodium Chemical compound [Na].CC(=C)C(=O)OCCCS(O)(=O)=O MSQCQZMTRWHMFQ-UHFFFAOYSA-N 0.000 description 1
- WHNPOQXWAMXPTA-UHFFFAOYSA-N 3-methylbut-2-enamide Chemical compound CC(C)=CC(N)=O WHNPOQXWAMXPTA-UHFFFAOYSA-N 0.000 description 1
- DATYUTWESAKQQM-UHFFFAOYSA-N 4,7-phenanthroline Chemical compound C1=CC=C2C3=CC=CN=C3C=CC2=N1 DATYUTWESAKQQM-UHFFFAOYSA-N 0.000 description 1
- MTYHUTYJKFVTJJ-UHFFFAOYSA-N 4-hydroxypyrene-1,2,3-trisulfonic acid Chemical class OS(=O)(=O)C1=C(S(O)(=O)=O)C(S(O)(=O)=O)=C2C(O)=CC3=CC=CC4=CC=C1C2=C34 MTYHUTYJKFVTJJ-UHFFFAOYSA-N 0.000 description 1
- NIXVAPHNPNMUIX-UHFFFAOYSA-N 6-amino-2-methylhex-2-enamide Chemical compound NC(=O)C(C)=CCCCN NIXVAPHNPNMUIX-UHFFFAOYSA-N 0.000 description 1
- STGMORHGPQLXMT-UHFFFAOYSA-N 9h-indeno[2,1-c]pyridazine Chemical compound C1=NN=C2CC3=CC=CC=C3C2=C1 STGMORHGPQLXMT-UHFFFAOYSA-N 0.000 description 1
- GWWFKWJMIKQILK-UHFFFAOYSA-N B(C1=CC(=C(C(=C1CBr)CBr)C)C)(O)O Chemical compound B(C1=CC(=C(C(=C1CBr)CBr)C)C)(O)O GWWFKWJMIKQILK-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- VTLYFUHAOXGGBS-UHFFFAOYSA-N Fe3+ Chemical compound [Fe+3] VTLYFUHAOXGGBS-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- JPBQBCTYPHBRIE-UHFFFAOYSA-N NC1=CC=C2N=CC=CC2=C1.OBO Chemical compound NC1=CC=C2N=CC=CC2=C1.OBO JPBQBCTYPHBRIE-UHFFFAOYSA-N 0.000 description 1
- 241000287462 Phalacrocorax carbo Species 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical group OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- DAKWPKUUDNSNPN-UHFFFAOYSA-N Trimethylolpropane triacrylate Chemical compound C=CC(=O)OCC(CC)(COC(=O)C=C)COC(=O)C=C DAKWPKUUDNSNPN-UHFFFAOYSA-N 0.000 description 1
- NJSSICCENMLTKO-HRCBOCMUSA-N [(1r,2s,4r,5r)-3-hydroxy-4-(4-methylphenyl)sulfonyloxy-6,8-dioxabicyclo[3.2.1]octan-2-yl] 4-methylbenzenesulfonate Chemical compound C1=CC(C)=CC=C1S(=O)(=O)O[C@H]1C(O)[C@@H](OS(=O)(=O)C=2C=CC(C)=CC=2)[C@@H]2OC[C@H]1O2 NJSSICCENMLTKO-HRCBOCMUSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- MIHJMMKHEDKTNX-UHFFFAOYSA-N [6,7,8-tris(chlorosulfonyl)pyren-1-yl] acetate Chemical compound C1=C2C(OC(=O)C)=CC=C(C=C3)C2=C2C3=C(S(Cl)(=O)=O)C(S(Cl)(=O)=O)=C(S(Cl)(=O)=O)C2=C1 MIHJMMKHEDKTNX-UHFFFAOYSA-N 0.000 description 1
- 239000000980 acid dye Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 238000012644 addition polymerization Methods 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229940124277 aminobutyric acid Drugs 0.000 description 1
- 239000003011 anion exchange membrane Substances 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 125000006615 aromatic heterocyclic group Chemical class 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- UWCPYKQBIPYOLX-UHFFFAOYSA-N benzene-1,3,5-tricarbonyl chloride Chemical compound ClC(=O)C1=CC(C(Cl)=O)=CC(C(Cl)=O)=C1 UWCPYKQBIPYOLX-UHFFFAOYSA-N 0.000 description 1
- XFOZBWSTIQRFQW-UHFFFAOYSA-M benzyl-dimethyl-prop-2-enylazanium;chloride Chemical compound [Cl-].C=CC[N+](C)(C)CC1=CC=CC=C1 XFOZBWSTIQRFQW-UHFFFAOYSA-M 0.000 description 1
- 238000010364 biochemical engineering Methods 0.000 description 1
- 238000006065 biodegradation reaction Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 125000005621 boronate group Chemical group 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229920000547 conjugated polymer Polymers 0.000 description 1
- 230000009146 cooperative binding Effects 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 239000000412 dendrimer Substances 0.000 description 1
- 229920000736 dendritic polymer Polymers 0.000 description 1
- 230000005595 deprotonation Effects 0.000 description 1
- 238000010537 deprotonation reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- STVZJERGLQHEKB-UHFFFAOYSA-N ethylene glycol dimethacrylate Chemical compound CC(=C)C(=O)OCCOC(=O)C(C)=C STVZJERGLQHEKB-UHFFFAOYSA-N 0.000 description 1
- 238000000695 excitation spectrum Methods 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 210000003722 extracellular fluid Anatomy 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 238000005562 fading Methods 0.000 description 1
- 229910001447 ferric ion Inorganic materials 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical compound NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 description 1
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000031700 light absorption Effects 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 238000012806 monitoring device Methods 0.000 description 1
- 230000002794 monomerizing effect Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 229940088644 n,n-dimethylacrylamide Drugs 0.000 description 1
- YLGYACDQVQQZSW-UHFFFAOYSA-N n,n-dimethylprop-2-enamide Chemical compound CN(C)C(=O)C=C YLGYACDQVQQZSW-UHFFFAOYSA-N 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- HUMMCEUVDBVXTQ-UHFFFAOYSA-N naphthalen-1-ylboronic acid Chemical compound C1=CC=C2C(B(O)O)=CC=CC2=C1 HUMMCEUVDBVXTQ-UHFFFAOYSA-N 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 150000005041 phenanthrolines Chemical class 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 238000007539 photo-oxidation reaction Methods 0.000 description 1
- 229920001228 polyisocyanate Polymers 0.000 description 1
- 239000005056 polyisocyanate Substances 0.000 description 1
- 229920000307 polymer substrate Polymers 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- OBJOZRVSMLPASY-UHFFFAOYSA-K pyranine(3-) Chemical compound C1=C2C(O)=CC(S([O-])(=O)=O)=C(C=C3)C2=C2C3=C(S([O-])(=O)=O)C=C(S([O-])(=O)=O)C2=C1 OBJOZRVSMLPASY-UHFFFAOYSA-K 0.000 description 1
- XMAPHCGFUPXIEN-UHFFFAOYSA-N pyren-1-yl acetate Chemical compound C1=C2C(OC(=O)C)=CC=C(C=C3)C2=C2C3=CC=CC2=C1 XMAPHCGFUPXIEN-UHFFFAOYSA-N 0.000 description 1
- 125000005581 pyrene group Chemical group 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-O pyridinium Chemical compound C1=CC=[NH+]C=C1 JUJWROOIHBZHMG-UHFFFAOYSA-O 0.000 description 1
- 239000002096 quantum dot Substances 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- RJSRSRITMWVIQT-UHFFFAOYSA-N quinolin-6-amine Chemical compound N1=CC=CC2=CC(N)=CC=C21 RJSRSRITMWVIQT-UHFFFAOYSA-N 0.000 description 1
- 238000010823 ratiometric pH measurement Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- UZNHKBFIBYXPDV-UHFFFAOYSA-N trimethyl-[3-(2-methylprop-2-enoylamino)propyl]azanium;chloride Chemical compound [Cl-].CC(=C)C(=O)NCCC[N+](C)(C)C UZNHKBFIBYXPDV-UHFFFAOYSA-N 0.000 description 1
- 238000000108 ultra-filtration Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/14532—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue for measuring glucose, e.g. by tissue impedance measurement
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/66—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood sugars, e.g. galactose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/14507—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue specially adapted for measuring characteristics of body fluids other than blood
- A61B5/1451—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue specially adapted for measuring characteristics of body fluids other than blood for interstitial fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/14539—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue for measuring pH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1455—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters
- A61B5/1459—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters invasive, e.g. introduced into the body by a catheter
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/84—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving inorganic compounds or pH
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2400/00—Assays, e.g. immunoassays or enzyme assays, involving carbohydrates
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Pathology (AREA)
- Urology & Nephrology (AREA)
- Immunology (AREA)
- Heart & Thoracic Surgery (AREA)
- Medical Informatics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Surgery (AREA)
- Optics & Photonics (AREA)
- Animal Behavior & Ethology (AREA)
- Biophysics (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Inorganic Chemistry (AREA)
- Diabetes (AREA)
- Emergency Medicine (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
センサーに関連した別の問題は、pH感受性である。pHにおけるわずかな変化は、蛍光放出を変更するか又は弱め、そして不正確な読取を引き起こし得る。この問題は、その血中pHが急速に変動し得る糖尿病患者における血中グルコースレベルをモニタリングするためには特に深刻である。正確な血中グルコースレベル測定はこれらの患者を治療するためには不可欠であるため、別個の留置型pH及び分析物センサー、又は多染料を有するセンサーを必要とせずに、pH作用の実時間補正を促すグルコースセンサーに対する有意の必要性が存在する。
したデバイスのいずれかを提供するステップと、血管内にセンサーを挿入するステップと、第一の励起波長でセンサーを照射するステップと、放出波長でセンサーの第一の蛍光放出を検出するステップと、第二の励起波長でセンサーを照射するステップと、放出波長でセンサーの第二の蛍光放出を測定するステップと、血中pHをレシオメトリック決定するステップと、pHに関して補正された血中グルコース濃度を決定するステップとを包含する。
定値が第一分析物濃度に応じて決まる場合(例えばグルコース測定値がpHに伴って変わる光学系において−この分野における共通問題)には、本発明の好ましい一実施形態に従って、測定第二分析物濃度は第一分析物濃度の寄与のために補正され得る。センサーは、好ましくは水性媒質(例えば生理学的媒質、血液、間質液等)中で安定であり、さらに好ましくは、センサーは、それが或る期間留置したままであり得る血管中に挿入されるよう設計される。したがって本発明の好ましい一実施形態に従って、血管内配置のために設計される光学センサーが開示され、このセンサーは、単一指示薬系を用いて2つの分析物(好ましくはpH及びグルコース)を測定し、そしてpHの任意の寄与に関してグルコース測定値を補正し得る。
本発明の好ましい実施形態に従って用いられる指示薬系は、分析物結合部分と操作可能的に結合されるフルオロフォアを含み、この場合、分析物結合はフルオロフォア濃度における見掛けの光学的変化(例えば放出強度)を引き起こす。さらに、レシオメトリックpH感知が可能にされ得るよう、フルオロフォアはスペクトル特性における検出可能な差を示す異なる酸形態及び塩基形態を有する、ということが望ましい。例えば、HPTS−トリLysMA(以下で詳細に記載される)のような蛍光染料と操作可能的に結合されるグルコース結合部分、例えば3,3’−oBBV(以下で詳細に記載される)は、蛍光染料の放出強度を抑制するが、この場合、消光の程度はグルコース結合時に低減され、グルコース濃度に関連した放出強度の増大を生じる。好ましい実施形態では、指示薬系は、少なくとも2つの陰イオン基を有する染料、及び少なくとも2つのボロン酸を有する消光剤を含む。さらなる好ましい実施形態では、反応(消光)するために互いに十分に物理的に近いままであるよう、指示薬系は感知部分(例えば染料−消光剤)を固定するための手段も含む。in vivo感知が望ましい場合、このような固定化手段は、好ましくは水性環境(例えば血管内)中で不溶性であり、標的分析物に対して透過性であり、そして感知部分に対して不透過性である。典型的には、固定化手段は、水不溶性有機ポリマーマトリックスを含む。例えばHPTS−トリLysMA染料及び3,3’−oBBV消光剤は、DMAA(N,N−ジメチルアクリルアミド)ヒドロゲルマトリックス(以下で詳細に記載される)内で有効に固定され、これがin vivoでのpH及びグルコース感知を可能にする。
「フルオロフォア」は、特定波長での光に照らされた場合、より長い波長での光を放出する、即ちそれが蛍光発光する物質を指す。フルオロフォアとしては有機染料、有機金属化合物、金属キレート化合物、蛍光共役ポリマー、量子ドット又はナノ粒子、並びに上記のものの組み合せが挙げられるが、これらに限定されない。フルオロフォアは、ポリマー
に結合される別個の部分又は置換基であり得る。
。HPTSは、約450nm及び約405nmの2つの励起波長を示し、これは、酸及びその共役塩基の吸収波長に対応する。励起波長におけるシフトは、HPTS上のヒドロキシル基のpH依存性イオン化のためである。pHが増大すると、HPTSは、約450nmでの吸光度の増大、及び約420nmより低い吸光度の低減を示す。吸収極大でのpH依存性シフトは、生理学的範囲での二重励起レシオメトリック検出を可能にする。この染料は500ダルトン未満の分子量を有し、したがってそれはポリマーマトリックス内に留まらないが、それは陰イオン排除膜と共に用いられ得る。
本発明の広範な態様に従って、分析物結合部分は、分析物結合の量に関連したやり方で、分析物と結合することができ且つフルオロフォアの見掛けの濃度(例えば放出シグナル強度の変化として検出される)を調整することができる少なくとも二重の機能性を提供する。好ましい実施形態では、分析物結合部分は、消光剤と会合される。「消光剤」は、その存在下で、フルオロフォアの放出を低減する化合物を指す。消光剤(Q)は、独立した化合物、例えば、第二の独立した化合物に、又は重合性化合物に転化可能である反応性中間体から選択されるか、或いはQは、上記反応性中間体又は重合性化合物から調製されるポリマー中のペンダント基又は鎖単位であって、このポリマーは水溶性又は水分散性であるか、或いは不溶性ポリマーであり、上記ポリマーは任意に架橋される。
中でグルコースと可逆的に反応して、ボロン酸エステルを形成する。反応の程度は、媒質中のグルコース濃度に関連する。ボロン酸エステルの形成は、ビオロゲンによるフルオロフォア(fluorphore)の消光を減少させて、グルコース濃度に応じた蛍光の増大を引き起こす。有用なビス−オニウム塩は分析物溶液と相溶性であり、そして検出されるべき分析物の存在下で染料の蛍光放出における検出可能な変化を生じ得る。
a)第1の芳香族部分上の反応性基は1つの窒素と結合され、そして少なくとも1つの−B(OH)2基を含有する第二芳香族基は第二窒素と結合される;
b)1つ又は複数のボロン酸基は、1つの窒素と結合される第一芳香族部分と結合され、そして1つのボロン酸及び反応性基は第二窒素と結合される第二芳香族基に結合される;
c)1つのボロン酸基及び反応性基は1つの窒素と結合される第一芳香族基の第一芳香族部分と結合され、そしてボロン酸基及び反応性基は第二窒素と結合される第二芳香族部分と結合される;そして
d)1つのボロン酸は各窒素と結合され、そして反応性基はヘテロ芳香族環と結合される。
Zは、反応性基であり;且つ
R’は、ベンジル環上のオルト−、メタ−又はパラ−位における−B(OH)2であり、そしてR’’はH−であり;或いは任意にR’’は、本明細書中で定義されるようなカップリング基、又はボロン酸の酸性を改質するために特定的に用いられる置換基、例えばフルオロ−又はメトキシ−である)。
いくつかの実施形態では、動いている流れを包含しないin vitroで用いるために、感知構成成分は個々の(別個の)構成成分として用いられる。染料及び消光剤は液体溶液中に一緒に混合され、分析物が付加され、蛍光強度における変化が測定され、そして構成成分が廃棄される。滲出を防止するために感知構成成分を閉じ込めるために用いられ得る高分子マトリックスは、存在する必要がない。任意に、感知構成成分が固定され、これが移動流中の分析物を測定するためのそれらの使用を可能にする。
る。
ー混合物を架橋して、ヒドロゲルを得る。生成物を塩基で処理して、アセトキシ・ブロッキング基を除去する。さらなる使用の前に、脱イオン水を用いた網羅的抽出により、不完全反応生成物及び非反応出発物質をヒドロゲルから濾し取る。生成物は、本明細書中に記載したような感知構成成分として用いられる場合、グルコースに対して応答性である。
レシオメトリックpH感知は知られている。例えば米国特許出願公開第2006/0105174号;同第2005/0090014号(これらの記載内容の全体は参照により本明細書中で援用される)参照。2つの形態(酸形態及び塩基形態)で存在するフルオロフォアを含む指示薬系(例えば蛍光指示薬染料)を考えると、2つの波長での放出強度の比は、フルオロフォア濃度のpH非依存性を測定するために用いられ得る。レシオメトリックpH感知に適した蛍光指示薬染料は、以下のものであり得る:(1)二重励起波長(酸形態及び共役塩基形態に対応する)及び単一放出波長を示す染料(例えばHPTS染料);(2)単一励起波長及び二重放出波長(酸形態及び塩基形態);或いは(3)二重励起−二重放出染料。いくつかの染料、例えばSNARF又はSNAFL染料は、二重放出特性及び二重励起特性の両方を有し得る。しかしながら二重−二重染料、例えばSNARFは、単一−二重又は二重−単一として用いられ得る。
Parus, et al. (1997) "High-performance fiber-optic pH microsensors for practical physiological measurements using a dual-emission sensitive dye" Analytical Chemistry 69: 863-867参照。これらの染料に関して観察される広範な光褪色はレシオメトリック・アプローチにより説明され得るが、しかしそれは依然としてセンサーの有用な寿命を限定する。
Kaの励起におけるその後のpH依存性シフトは、生理学的範囲における二重励起/単一放出レシオメトリック検出を可能にする。これは、低毒性(Lutty, G.A. (1978). "The acute intravenous toxicity of stains, dyes, and other fluorescent substances." Toxical Pharmacol. 44: 225-229)及び酸素濃度に対する非感受性(Zhujun, Z. and W.R. Seitz (1984). "A fluorescence sensor for quantifying pH in the range from 6.5 to
8.5." Analytical Chimica Acta 160: 47-55)と共に、HPTSを生理学的及びバイオプロセスpH測定のための適切なプローブにする。
、染料及び消光剤は、分析物透過性ヒドロゲル又は他の高分子マトリックス内に一緒に閉じ込められ得る。適切な波長の光により励起される場合、蛍光染料は光を放出する(例えば蛍光発光する)。光の強度は、結合している分析物の量に伴って変わる消光の程度に応じて決まる。他の実施形態では、蛍光染料及び消光剤は、互いの代わりに、ヒドロゲル又は他の高分子マトリックスと共有結合され得る。
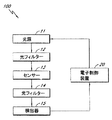
域に沿って配置され、指示薬系は励起光に応答して検出可能な放出シグナルを発生するよう設計される。センサーの好ましい実施形態は、放出シグナルを検出器に送るための光学手段をさらに包含する。このような光学手段は当該技術分野でよく知られており、そして例えば光を戻すための鏡、フィルター、レンズ、ビームスプリッター、及び光ファイバー束及び分割形状を包含し得る。
蛍光染料、例えばHPTS及びその誘導体を含む指示薬系は、分析物検出に用いられてきた。例えば米国特許第6,653,141号、同第6,627,177号、同第5,512,246号、同第5,137,833号、同第6,800,451号、同第6,794,195号、同第6,804,544号、同第6,002,954号、同第6,319,540号、同第6,766,183号、同第5,503,770号、及び同第5,763,238号;並びに同時係属中の米国特許出願第11/296,898号及び同第60/833,081号(これらの記載内容の全体は各々、参照により本明細書中で援用される)参照。特にいくつかの好ましい蛍光染料、消光剤/分析物結合部分、並びにポリヒドロキシル化合物濃度を光学的に決定するための方法に関連した詳述は、米国特許第6,653,141号及び第6,627,177号、並びに米国特許出願第11/296,898号及び第60/833,081号に開示されている。
一実施形態では、方法及びセンサーは、in vitroで媒質のpH並びに分析物の濃度をモニタリングする。別の実施形態では、方法及びセンサーは、in vivoでpH及び分析物濃度をモニタリングする。別の実施形態では、測定pH値は、in vitro又はin vivoでグルコース濃度をより正確に決定するためにも用いられ得る。
特定的には、pH値及びグルコース濃度の同時測定は、グルコース応答のシグナルの実時間補正を可能にする。しかしながら、いくつかの実施形態によるデバイスはpH又は分析物を決定するためにだけ用いられ得るセンサーを包含すると理解される(pHに関するその補正は、慣用的な2つのセンサー技術により、又はin vitroで血中pHを試験することにより実行され得る)。
一実施形態は、蛍光染料を用いてpH及びポリヒドロキシル化合物濃度を決定するための方法であって、消光剤と操作可能的に結合される蛍光染料を含むセンサーを提供するステップと、上記センサーを試料と接触させるステップと、第一の励起波長で上記センサーを照射するステップと、放出波長で上記センサーの第一の蛍光放出を検出するステップと
、第二の励起波長で上記センサーを照射するステップと、上記放出波長で上記センサーの第二の蛍光放出を測定するステップと、第一の放出及び第二の放出の比をpH較正曲線と比較して試料のpHを決定するステップと、放出消光を既知のpHで標準曲線と相関させて上記試料中のポリヒドロキシル化合物濃度を決定するステップとを包含する方法を提供する。もちろん、他のアルゴリズムがレシオメトリックpH感知に関して知られており、そして本発明の実施形態に従って用いられ得る。制御装置、例えばコンピューター又は専用デバイスは、いくつかの実施形態では、励起光の適用、検出器シグナルのモニタリング、比の決定、比を較正曲線と相関させること、グルコースシグナルを標準曲線と相関させること、pH変化に関して補正すること、ルーチンセンサー較正操作を実行すること、オペレーター動作を促すこと、正確性を保持するためにプログラムされたようにユーザーデータ入力を組み込むこと(例えばフィンガースティック・グルコース測定)等を含めた操作を制御するために用いられ得る。
先ず、種々のpHでセンサーの吸光度スペクトルを得て、等吸収点並びに酸形態及び塩基形態に関する吸収最大が生じる波長を決定し、次に少なくとも1つの既知のpH及びグルコース濃度でこれらの波長のうちの少なくとも2つから放出シグナルを獲得することにより実行され得る。
)」)(本明細書と同一日に提出)(この記載内容の全体は参照により本明細書中で援用される)に詳細に開示されている。
図3は、蛍光染料(この場合はHPTS)の励起/吸収スペクトルの一例を示す。異なるpHで得られた蛍光染料の吸収スペクトルから、λ酸、λ塩基及びλisoが決定され得る。より低いpH(例えばより酸性の条件)では、約405nmでのピークは約460nmでのピークより高く、したがって酸性形態の蛍光染料に関する吸収最大である。より高いpH(例えばより塩基性の条件)では、約460nmでのピークは約405nmでのピークより高く、したがって塩基性形態の蛍光染料に関する吸収最大である。λisoは、吸収がpHと無関係である波長であり、そしてそれは、例えばHPTSに関しては約422nmである。
図4は、I(塩基)/I(iso)比を用いるHPTS/MABP4を用いたレシオメトリックpH感知がグルコース濃度と無関係であることを示す。MABP4の構造を以下に示す:
図6は、溶液中の異なるpHでのSNARF−1の吸収スペクトルを示す。SNARFは、Molecular Probes, Inc.からの市販染料の一クラスに関する商標名である。SNARF−1を用いて、これらの実験を実行した。図7及び図8は、514nm励起/587nm放出(図7)又は514nm励起/625nm放出(図8)で決定された異なるpHでの溶液中のSNARF−1/3,3’−oBBVに関するグルコース応答曲線を示す。図9は、514nmの単一励起波長並びに587nm及び625nmの放出波長で決定されたI(塩基)/I(酸)比を用いた溶液中のSNARF−1/3,3’−oBBVに関する異なるグルコース濃度でのpHのレシオメトリック感知を示す。したがって、消光剤3,3’−oBBV(溶液中)と操作可能的に結合された二重−二重染料SNARF−1を単一エキサイター−二重エミッター・フルオロフォアとして用いて、pH(レシオメトリック)及びグルコースを共に決定し得る。
図10は、異なるpHでのHPTS−トリLysMA/3,3’−oBBV/DMAA指示薬系のグルコース応答を示す。図11は、I(塩基)/I(酸)比を用いたHPTS−トリLysMA/3,3’−oBBV/DMAAに関する異なるグルコース濃度でのpHのレシオメトリック感知を示す。この指示薬系は、生理学的pH範囲に亘って線形pH曲線を示すことが分かる。
図12は、I(塩基)/I(酸)比を用いたHPTS−トリCysMA/3,3’−oBBV/DMMA指示薬系に関する異なるグルコース濃度でのpHのレシオメトリック感知を示す。この指示薬系は、生理学的pH範囲に亘って線形pH曲線を提供することが分かる。この実施例に関しては、光ファイバーの末端に埋め込まれたヒドロゲル中に、指示薬系を固定した。手で持てる大きさの検出器を用いて、酸及び塩基放出シグナルを測定した。
Claims (21)
- 2つ又はそれより多くの分析物濃度の決定に用いるための光学センサーであって、
光路を規定し、血管内配置のための大きさに作られた光ファイバーと、該光ファイバーに会合され、少なくとも部分的に光路内に配置された指示薬系を含み、 前記指示薬系は、
第一分析物の濃度に応じて少なくとも第一及び第二の異なる形態で存在するフルオロフォアであって、前記異なる形態がそれらのそれぞれの第一の放出及び第二の放出に基づいて区別され得るフルオロフォアと 第二分析物を結合する結合部分であって、該結合部分が前記フルオロフォアと操作可能的に結合され、そして前記結合部分による前記第二分析物の結合が前記第二分析物の濃度に関連づけられる前記フルオロフォアの見掛けの濃度における光学的変化を引き起こす結合部分とを含み、
前記第一の放出及び前記第二の放出の比は前記第二分析物の濃度とは無関係である、光学センサー。 - 前記フルオロフォアが蛍光染料である請求項1記載の光学センサー。
- 前記蛍光染料が独立した化合物である請求項2記載の光学センサー。
- 前記蛍光染料がHPTS、SNARF−1、SNAFL−1、テトラキス(4−スルホフェニル)ポルフィン及びその誘導体から選択される請求項3記載の光学センサー。
- 前記蛍光染料が、HPTS−CysMA、HPTS−LysMA及びそれで構成されるポリマーから成る群から選択される請求項2記載の光学センサー。
- 前記結合部分が消光剤、及び第二分析物を可逆的に結合するための1つ又は複数の結合部位を含む請求項1〜5のいずれか1項記載の光学センサー。
- 前記消光剤がビオロゲンである請求項6記載の光学センサー。
- 前記1つ又は複数の結合部位がフェニルボロン酸基を含む請求項6記載の光学センサー。
- 前記結合部分がビオロゲン−ボロン酸付加物である請求項1〜5のいずれか1項記載の光学センサー。
- 前記結合部分が3,3'−oBBV又はその誘導体である請求項1〜5のいずれか1項
記載の光学センサー。 - 前記光学センサーが生理学的適合性物質を含む請求項1〜10のいずれか1項記載の光学センサー。
- 前記第一分析物がH+(pH)である請求項1〜11のいずれか1項記載の光学センサ
ー。 - 前記第二分析物がポリヒドロキシル化合物である請求項12記載の光学センサー。
- 前記ポリヒドロキシル化合物がグルコースである請求項13記載の光学センサー。
- 前記指示薬系が前記フルオロフォア及び前記結合部分を固定するための手段をさらに包含する請求項1〜14のいずれか1項記載の光学センサー。
- 前記固定するための手段がヒドロゲルを包含する請求項15記載の光学センサー。
- 前記指示薬系の前記フルオロフォア及び結合部分が単一分子を含む請求項1〜16のいずれか1項記載の光学センサー。
- 請求項1〜17のいずれか1項記載の光学センサーと励起光源と放出光検出器とを包含する、2つ又はそれより多くの分析物濃度を決定するためのデバイス。
- 制御装置をさらに包含する請求項18記載のデバイス。
- 血中pH及びグルコース濃度の決定に用いるためのセンサーであって、
血管内配置のための大きさに作られる光ファイバーを含み、
水不溶性ポリマーマトリックスであって、該ポリマーマトリックスはグルコースに対して透過性である水不溶性ポリマーマトリックス;
前記ポリマーマトリックスと会合される蛍光染料であって、該蛍光染料はpHに応じて少なくとも第一及び第二の異なる形態を示し、該異なる形態はそれらのそれぞれの第一の放出及び第二の放出に基づいて区別され得る蛍光染料;
血中グルコース濃度に関連づけられる量のグルコースを可逆的に結合するようになっている芳香族ボロン酸置換ビオロゲンを含む消光剤であって、該消光剤は前記ポリマーマトリックスと会合されかつ蛍光染料と操作可能的に結合され、そして該消光剤は結合ポリヒドロキシル化合物の量に関連づけられる前記蛍光染料により放出される光を調整するよう設計される、消光剤、
をさらに含むセンサー。 - 請求項20項に記載のセンサーと少なくとも1つの励起光源と放出光検出器とを包含する、血中pH及びグルコース濃度を決定するためのデバイス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/671,880 US7751863B2 (en) | 2007-02-06 | 2007-02-06 | Optical determination of ph and glucose |
| US11/671,880 | 2007-02-06 | ||
| PCT/US2008/052204 WO2008097747A1 (en) | 2007-02-06 | 2008-01-28 | Optical determination of ph and glucose |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010518397A JP2010518397A (ja) | 2010-05-27 |
| JP2010518397A5 JP2010518397A5 (ja) | 2011-03-10 |
| JP5017377B2 true JP5017377B2 (ja) | 2012-09-05 |
Family
ID=39323951
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009549167A Expired - Fee Related JP5017377B2 (ja) | 2007-02-06 | 2008-01-28 | pH及びグルコースの光学的決定 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US7751863B2 (ja) |
| EP (1) | EP2122361B1 (ja) |
| JP (1) | JP5017377B2 (ja) |
| AU (1) | AU2008214099A1 (ja) |
| CA (1) | CA2674513A1 (ja) |
| DK (1) | DK2122361T3 (ja) |
| WO (1) | WO2008097747A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8467843B2 (en) | 2009-11-04 | 2013-06-18 | Glumetrics, Inc. | Optical sensor configuration for ratiometric correction of blood glucose measurement |
| US8738107B2 (en) | 2007-05-10 | 2014-05-27 | Medtronic Minimed, Inc. | Equilibrium non-consuming fluorescence sensor for real time intravascular glucose measurement |
| US8838195B2 (en) | 2007-02-06 | 2014-09-16 | Medtronic Minimed, Inc. | Optical systems and methods for ratiometric measurement of blood glucose concentration |
Families Citing this family (112)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9155496B2 (en) | 1997-03-04 | 2015-10-13 | Dexcom, Inc. | Low oxygen in vivo analyte sensor |
| US7899511B2 (en) | 2004-07-13 | 2011-03-01 | Dexcom, Inc. | Low oxygen in vivo analyte sensor |
| US7192450B2 (en) | 2003-05-21 | 2007-03-20 | Dexcom, Inc. | Porous membranes for use with implantable devices |
| US6001067A (en) | 1997-03-04 | 1999-12-14 | Shults; Mark C. | Device and method for determining analyte levels |
| US6862465B2 (en) | 1997-03-04 | 2005-03-01 | Dexcom, Inc. | Device and method for determining analyte levels |
| US8527026B2 (en) | 1997-03-04 | 2013-09-03 | Dexcom, Inc. | Device and method for determining analyte levels |
| US6175752B1 (en) | 1998-04-30 | 2001-01-16 | Therasense, Inc. | Analyte monitoring device and methods of use |
| US8346337B2 (en) | 1998-04-30 | 2013-01-01 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8974386B2 (en) | 1998-04-30 | 2015-03-10 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US6949816B2 (en) | 2003-04-21 | 2005-09-27 | Motorola, Inc. | Semiconductor component having first surface area for electrically coupling to a semiconductor chip and second surface area for electrically coupling to a substrate, and method of manufacturing same |
| US8465425B2 (en) | 1998-04-30 | 2013-06-18 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8480580B2 (en) | 1998-04-30 | 2013-07-09 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US8688188B2 (en) | 1998-04-30 | 2014-04-01 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US9066695B2 (en) | 1998-04-30 | 2015-06-30 | Abbott Diabetes Care Inc. | Analyte monitoring device and methods of use |
| US6560471B1 (en) | 2001-01-02 | 2003-05-06 | Therasense, Inc. | Analyte monitoring device and methods of use |
| US20030032874A1 (en) | 2001-07-27 | 2003-02-13 | Dexcom, Inc. | Sensor head for use with implantable devices |
| US6702857B2 (en) | 2001-07-27 | 2004-03-09 | Dexcom, Inc. | Membrane for use with implantable devices |
| US8260393B2 (en) | 2003-07-25 | 2012-09-04 | Dexcom, Inc. | Systems and methods for replacing signal data artifacts in a glucose sensor data stream |
| US9247901B2 (en) | 2003-08-22 | 2016-02-02 | Dexcom, Inc. | Systems and methods for replacing signal artifacts in a glucose sensor data stream |
| US10022078B2 (en) | 2004-07-13 | 2018-07-17 | Dexcom, Inc. | Analyte sensor |
| US8010174B2 (en) | 2003-08-22 | 2011-08-30 | Dexcom, Inc. | Systems and methods for replacing signal artifacts in a glucose sensor data stream |
| US9282925B2 (en) | 2002-02-12 | 2016-03-15 | Dexcom, Inc. | Systems and methods for replacing signal artifacts in a glucose sensor data stream |
| US7134999B2 (en) | 2003-04-04 | 2006-11-14 | Dexcom, Inc. | Optimized sensor geometry for an implantable glucose sensor |
| US8423113B2 (en) | 2003-07-25 | 2013-04-16 | Dexcom, Inc. | Systems and methods for processing sensor data |
| EP1648298A4 (en) | 2003-07-25 | 2010-01-13 | Dexcom Inc | OXYGEN-IMPROVED MEMBRANE SYSTEMS FOR IMPLANTABLE DEVICES |
| US6931327B2 (en) | 2003-08-01 | 2005-08-16 | Dexcom, Inc. | System and methods for processing analyte sensor data |
| US7774145B2 (en) | 2003-08-01 | 2010-08-10 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US20190357827A1 (en) | 2003-08-01 | 2019-11-28 | Dexcom, Inc. | Analyte sensor |
| US8761856B2 (en) | 2003-08-01 | 2014-06-24 | Dexcom, Inc. | System and methods for processing analyte sensor data |
| US7494465B2 (en) | 2004-07-13 | 2009-02-24 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US8886273B2 (en) | 2003-08-01 | 2014-11-11 | Dexcom, Inc. | Analyte sensor |
| US8369919B2 (en) | 2003-08-01 | 2013-02-05 | Dexcom, Inc. | Systems and methods for processing sensor data |
| US7591801B2 (en) | 2004-02-26 | 2009-09-22 | Dexcom, Inc. | Integrated delivery device for continuous glucose sensor |
| US8676287B2 (en) | 2003-08-01 | 2014-03-18 | Dexcom, Inc. | System and methods for processing analyte sensor data |
| US7920906B2 (en) | 2005-03-10 | 2011-04-05 | Dexcom, Inc. | System and methods for processing analyte sensor data for sensor calibration |
| US20140121989A1 (en) | 2003-08-22 | 2014-05-01 | Dexcom, Inc. | Systems and methods for processing analyte sensor data |
| WO2005051170A2 (en) | 2003-11-19 | 2005-06-09 | Dexcom, Inc. | Integrated receiver for continuous analyte sensor |
| US9247900B2 (en) | 2004-07-13 | 2016-02-02 | Dexcom, Inc. | Analyte sensor |
| US8287453B2 (en) | 2003-12-05 | 2012-10-16 | Dexcom, Inc. | Analyte sensor |
| US8423114B2 (en) | 2006-10-04 | 2013-04-16 | Dexcom, Inc. | Dual electrode system for a continuous analyte sensor |
| US11633133B2 (en) | 2003-12-05 | 2023-04-25 | Dexcom, Inc. | Dual electrode system for a continuous analyte sensor |
| US8364231B2 (en) | 2006-10-04 | 2013-01-29 | Dexcom, Inc. | Analyte sensor |
| US8532730B2 (en) | 2006-10-04 | 2013-09-10 | Dexcom, Inc. | Analyte sensor |
| DE602004029092D1 (de) | 2003-12-05 | 2010-10-21 | Dexcom Inc | Kalibrationsmethoden für einen kontinuierlich arbeitenden analytsensor |
| EP1711791B1 (en) | 2003-12-09 | 2014-10-15 | DexCom, Inc. | Signal processing for continuous analyte sensor |
| US8808228B2 (en) | 2004-02-26 | 2014-08-19 | Dexcom, Inc. | Integrated medicament delivery device for use with continuous analyte sensor |
| US8277713B2 (en) | 2004-05-03 | 2012-10-02 | Dexcom, Inc. | Implantable analyte sensor |
| US8792955B2 (en) | 2004-05-03 | 2014-07-29 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US7783333B2 (en) | 2004-07-13 | 2010-08-24 | Dexcom, Inc. | Transcutaneous medical device with variable stiffness |
| US8565848B2 (en) | 2004-07-13 | 2013-10-22 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US7654956B2 (en) | 2004-07-13 | 2010-02-02 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US7857760B2 (en) | 2004-07-13 | 2010-12-28 | Dexcom, Inc. | Analyte sensor |
| US7722537B2 (en) * | 2005-02-14 | 2010-05-25 | Optiscan Biomedical Corp. | Method and apparatus for detection of multiple analytes |
| US8133178B2 (en) | 2006-02-22 | 2012-03-13 | Dexcom, Inc. | Analyte sensor |
| US8744546B2 (en) | 2005-05-05 | 2014-06-03 | Dexcom, Inc. | Cellulosic-based resistance domain for an analyte sensor |
| US8060174B2 (en) * | 2005-04-15 | 2011-11-15 | Dexcom, Inc. | Analyte sensing biointerface |
| US9757061B2 (en) | 2006-01-17 | 2017-09-12 | Dexcom, Inc. | Low oxygen in vivo analyte sensor |
| EP3513708B1 (en) | 2006-03-09 | 2022-12-28 | Dexcom, Inc. | Systems and methods for processing analyte sensor data |
| WO2007120381A2 (en) | 2006-04-14 | 2007-10-25 | Dexcom, Inc. | Analyte sensor |
| US7831287B2 (en) | 2006-10-04 | 2010-11-09 | Dexcom, Inc. | Dual electrode system for a continuous analyte sensor |
| US7751863B2 (en) * | 2007-02-06 | 2010-07-06 | Glumetrics, Inc. | Optical determination of ph and glucose |
| WO2008141243A2 (en) * | 2007-05-10 | 2008-11-20 | Glumetrics, Inc. | Device and methods for calibrating analyte sensors |
| US8597190B2 (en) | 2007-05-18 | 2013-12-03 | Optiscan Biomedical Corporation | Monitoring systems and methods with fast initialization |
| CA2688184A1 (en) | 2007-06-08 | 2008-12-18 | Dexcom, Inc. | Integrated medicament delivery device for use with continuous analyte sensor |
| EP3078714A1 (en) * | 2007-08-06 | 2016-10-12 | Medtronic Minimed, Inc. | Hpts-mono and bis cys-ma polymerizable fluorescent dyes for use in analyte sensors |
| EP4159114B1 (en) | 2007-10-09 | 2024-04-10 | DexCom, Inc. | Integrated insulin delivery system with continuous glucose sensor |
| WO2009049038A1 (en) * | 2007-10-11 | 2009-04-16 | Tufts University | Systems, devices, and methods employing fiber optic shape tracking |
| US8417312B2 (en) | 2007-10-25 | 2013-04-09 | Dexcom, Inc. | Systems and methods for processing sensor data |
| EP2217316A4 (en) | 2007-11-21 | 2013-01-16 | Glumetrics Inc | USE OF AN INTRAVASCULAR EQUILIBRIUM SENSOR FOR CLOSE GLYCEMIC CONTROL |
| US8682408B2 (en) | 2008-03-28 | 2014-03-25 | Dexcom, Inc. | Polymer membranes for continuous analyte sensors |
| US8583204B2 (en) | 2008-03-28 | 2013-11-12 | Dexcom, Inc. | Polymer membranes for continuous analyte sensors |
| US11730407B2 (en) | 2008-03-28 | 2023-08-22 | Dexcom, Inc. | Polymer membranes for continuous analyte sensors |
| WO2009129186A2 (en) | 2008-04-17 | 2009-10-22 | Glumetrics, Inc. | Sensor for percutaneous intravascular deployment without an indwelling cannula |
| PT2291640T (pt) | 2008-05-20 | 2019-02-26 | Univ Health Network | Dispositivo e método para imagiologia e monitorização baseados em fluorescência |
| EP2326944B1 (en) | 2008-09-19 | 2020-08-19 | Dexcom, Inc. | Particle-containing membrane and particulate electrode for analyte sensors |
| US9149220B2 (en) | 2011-04-15 | 2015-10-06 | Dexcom, Inc. | Advanced analyte sensor calibration and error detection |
| US9446194B2 (en) | 2009-03-27 | 2016-09-20 | Dexcom, Inc. | Methods and systems for promoting glucose management |
| GB2470757B (en) * | 2009-06-04 | 2013-11-06 | Haemaflow Ltd | Non invasive gas analysis |
| EP2483679A4 (en) | 2009-09-30 | 2013-04-24 | Glumetrics Inc | SENSORS WITH THROMORETIC COATINGS |
| WO2011075711A1 (en) * | 2009-12-17 | 2011-06-23 | Glumetrics, Inc. | System and method for maintaining glycemic control based on glucose activity measurements |
| EP2534470B1 (en) | 2010-02-08 | 2016-08-10 | Medtronic Minimed, Inc. | Antioxidant protection of a chemical sensor |
| EP2545373B1 (en) * | 2010-03-11 | 2022-08-24 | Medtronic Minimed, Inc. | Measuring analyte concentration incorporating temperature and ph correction |
| EP2580589B1 (en) | 2010-06-09 | 2016-08-31 | Optiscan Biomedical Corporation | Measuring analytes in a fluid sample drawn from a patient |
| US20130197333A1 (en) * | 2010-06-30 | 2013-08-01 | Edwards Lifesciences Corporation | Analyte sensor |
| US9134238B2 (en) * | 2010-12-01 | 2015-09-15 | Nalco Company | Method for determination of system parameters for reducing crude unit corrosion |
| JP5797911B2 (ja) | 2011-02-18 | 2015-10-21 | 日本光電工業株式会社 | 溶液のpH計測方法及び溶液のpH計測装置 |
| JP5681548B2 (ja) * | 2011-03-31 | 2015-03-11 | 日本光電工業株式会社 | 培地溶液のpH計測方法及びpH計測装置 |
| US9051598B2 (en) * | 2011-05-02 | 2015-06-09 | The Hong Kong University Of Science And Technology | Specific detection of D-glucose by a tetraphenylethene-base fluorescent sensor |
| DE102011101207B3 (de) * | 2011-05-11 | 2012-05-10 | Sartorius Stedim Biotech Gmbh | Fluoreszenzfarbstoff für pH-Sensor |
| EP2769226B1 (en) | 2011-07-15 | 2017-05-24 | Medtronic Minimed, Inc. | Combinations of fluorphores and pyridinium boronic acid quenchers for use in analyte sensors |
| WO2013049068A1 (en) | 2011-09-27 | 2013-04-04 | Glumetrics, Inc. | Method for functionalizing a porous membrane covering of an optical sensor to facilitate coupling of an antithrom-bogenic agent |
| US8748192B2 (en) | 2011-10-25 | 2014-06-10 | Arizona Board Of Regents, A Body Corporate Of The State Of Arizona, Acting For And On Behalf Of Arizona State University | Optical fluorescence dual sensors and methods of preparing and using them |
| WO2013102162A1 (en) * | 2011-12-29 | 2013-07-04 | Wellsense, Inc. | Analyte sensor with extended range of detection |
| EP2916722A4 (en) * | 2012-11-07 | 2016-07-20 | Medtronic Minimed Inc | DRY APPLICATION AND ONE-TO-VIVO CALIBRATION OF AN OPTICAL ANALYTIC SENSOR |
| US20140275843A1 (en) * | 2013-03-15 | 2014-09-18 | James S. Piccirillo | Continuous optode fluorescent measurement system |
| GB201401878D0 (en) * | 2014-02-04 | 2014-03-19 | Lightship Medical Ltd | Calibration method |
| CA2955976A1 (en) | 2014-07-24 | 2016-01-28 | University Health Network | Collection and analysis of data for diagnostic purposes |
| CN106999118B (zh) * | 2014-10-13 | 2020-07-17 | 葡萄糖传感器公司 | 分析物感测装置 |
| CN104792755B (zh) * | 2015-04-10 | 2017-12-05 | 山西大学 | 一种检测连翘酯苷a的组合物及其制备方法 |
| US10845305B1 (en) | 2015-11-20 | 2020-11-24 | Verily Life Sciences Llc | Method for increasing sensor resolution by spectrally stacking responsive dyes |
| CN108700527B (zh) * | 2016-02-08 | 2021-05-18 | 普森斯精密传感有限公司 | 传感器装置 |
| US20170290535A1 (en) | 2016-04-08 | 2017-10-12 | Medtronic Minimed, Inc. | Analyte sensor with indicators |
| US10871487B2 (en) | 2016-04-20 | 2020-12-22 | Glusense Ltd. | FRET-based glucose-detection molecules |
| US10555693B2 (en) * | 2017-02-12 | 2020-02-11 | Hoon Kim | Portable apparatus for noninvasively measuring blood glucose level and operating method thereof |
| US11331022B2 (en) | 2017-10-24 | 2022-05-17 | Dexcom, Inc. | Pre-connected analyte sensors |
| US11943876B2 (en) | 2017-10-24 | 2024-03-26 | Dexcom, Inc. | Pre-connected analyte sensors |
| WO2019133812A1 (en) * | 2017-12-28 | 2019-07-04 | Profusa, Inc. | System and method for analyzing biochemical sensor data |
| US10605741B2 (en) * | 2018-06-28 | 2020-03-31 | International Business Machines Corporation | Accurate colorimetric based test strip reader system |
| CN110327056B (zh) * | 2019-05-24 | 2021-01-01 | 武汉大学 | 一种用于可视化血糖检测的智能水凝胶及其制备方法 |
| US20210285877A1 (en) * | 2020-03-10 | 2021-09-16 | SciLogica Corp. | Polymer matrix for sensing |
| DE102020129522A1 (de) * | 2020-11-10 | 2022-05-12 | Endress+Hauser Conducta Gmbh+Co. Kg | Indikator für die Bestimmung eines pH-Werts einer Lösung |
| CN114088670A (zh) * | 2021-11-01 | 2022-02-25 | 上海烁谱科技有限公司 | 一种自参比比率荧光pH传感器 |
Family Cites Families (135)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2018792A (en) | 1933-10-17 | 1935-10-29 | Soc Of Chemical Ind | Process for the manufacture of hydroxypyrene |
| US2094224A (en) | 1934-05-25 | 1937-09-28 | Gen Aniline Works Inc | Pyrene 3, 5, 8, 10-tetra-sulphonic acid and derivatives thereof |
| US3846353A (en) | 1970-06-08 | 1974-11-05 | Department Of Health Education | Nonthrombogenic plastic material and method for making the same |
| US3996345A (en) | 1974-08-12 | 1976-12-07 | Syva Company | Fluorescence quenching with immunological pairs in immunoassays |
| GB2005418B (en) | 1977-07-26 | 1982-04-21 | Searle & Co | Electrochemical sensor system |
| US4654327A (en) | 1982-04-21 | 1987-03-31 | Research Corp. | Quaternary ammonium complexes of heparin |
| US4682895A (en) | 1985-08-06 | 1987-07-28 | Texas A&M University | Fiber optic probe for quantification of colorimetric reactions |
| US4798738A (en) | 1986-10-10 | 1989-01-17 | Cardiovascular Devices, Inc. | Micro sensor |
| US4689308A (en) | 1986-05-01 | 1987-08-25 | International Biomedics, Inc. | Article for preparing a chemical sensor for use |
| AT385755B (de) | 1986-06-13 | 1988-05-10 | Koller Ernst | Verfahren zur herstellung von neuen pyrensulfonsaeurederivaten |
| US4927222A (en) | 1986-06-16 | 1990-05-22 | Shiley Incorporated | Dual optical fiber device |
| US4822127A (en) | 1986-06-16 | 1989-04-18 | Shiley Incorporated | Multi-channel optical transmission system |
| US4886338A (en) | 1986-10-10 | 1989-12-12 | Minnesota Mining And Manufacturing Company | Optical fiber event sensor |
| US5012809A (en) | 1986-10-10 | 1991-05-07 | Shulze John E | Fiber optic catheter system with fluorometric sensor and integral flexure compensation |
| US4833091A (en) | 1987-02-06 | 1989-05-23 | Shiley Incorporated | Sensor system |
| US5093266A (en) | 1987-02-06 | 1992-03-03 | Shiley Inc. | Sensor system |
| US4785814A (en) | 1987-08-11 | 1988-11-22 | Cordis Corporation | Optical probe for measuring pH and oxygen in blood and employing a composite membrane |
| US4851195A (en) | 1987-08-17 | 1989-07-25 | Pfizer Hospital Products Group, Inc. | Carbon dioxide sensor |
| US5047020A (en) | 1987-09-14 | 1991-09-10 | Baxter International Inc. | Ionic heparin coating |
| US5185263A (en) | 1987-10-23 | 1993-02-09 | Avl Medical Instruments Ag | Method for calibration of a measurement apparatus |
| US4906232A (en) | 1988-03-01 | 1990-03-06 | Abbott Laboratories | Intravascular delivery device |
| US5361758A (en) | 1988-06-09 | 1994-11-08 | Cme Telemetrix Inc. | Method and device for measuring concentration levels of blood constituents non-invasively |
| AT390517B (de) | 1988-08-04 | 1990-05-25 | Avl Verbrennungskraft Messtech | Optischer sensor und verfahren zu dessen herstellung |
| US5188803A (en) | 1988-12-01 | 1993-02-23 | Abbott Laboratories | Device for preparing a medical sensor for use |
| US4889407A (en) | 1988-12-02 | 1989-12-26 | Biomedical Sensors Limited | Optical waveguide sensor and method of making same |
| JPH04505638A (ja) * | 1989-03-06 | 1992-10-01 | シーメンス アクチエンゲゼルシヤフト | バルクハンドリング可能な物品の電解表面処理装置 |
| US5512246A (en) | 1989-09-21 | 1996-04-30 | Anthony P. Russell | Method and means for detecting polyhydroxyl compounds |
| US5137833A (en) | 1989-09-21 | 1992-08-11 | Russell Anthony P | Method for detecting polyhydroxyl compounds |
| US5132432A (en) | 1989-09-22 | 1992-07-21 | Molecular Probes, Inc. | Chemically reactive pyrenyloxy sulfonic acid dyes |
| US5279596A (en) | 1990-07-27 | 1994-01-18 | Cordis Corporation | Intravascular catheter with kink resistant tip |
| US5176882A (en) | 1990-12-06 | 1993-01-05 | Hewlett-Packard Company | Dual fiberoptic cell for multiple serum measurements |
| US5335305A (en) | 1991-12-19 | 1994-08-02 | Optex Biomedical, Inc. | Optical sensor for fluid parameters |
| US5168587A (en) | 1992-05-18 | 1992-12-08 | Shutes Robert S | Patient positioning device |
| US5354448A (en) | 1992-05-22 | 1994-10-11 | Biomedical Sensors Ltd. | Electrochemical sensor |
| US5246109A (en) | 1992-05-22 | 1993-09-21 | Biomedical Sensors, Ltd. | Package for an active medical device |
| US5262037A (en) | 1992-05-22 | 1993-11-16 | Biomedical Sensors, Ltd. | Electrochemical sensor |
| US5230031A (en) | 1992-05-22 | 1993-07-20 | Biomedical Sensors, Ltd. | Barrier for a connector |
| US5280130A (en) | 1992-05-22 | 1994-01-18 | Biomedical Sensors, Ltd. | Assembly of a tube and a part and apparatus and method of manufacture |
| JP2599994Y2 (ja) | 1992-07-30 | 1999-09-27 | 株式会社堀場製作所 | 実験室用イオン濃度計の自動校正装置 |
| JP3224869B2 (ja) * | 1992-08-27 | 2001-11-05 | ダイセル化学工業株式会社 | 近赤外線吸収透明樹脂組成物及びその成形体 |
| WO1994010553A1 (en) | 1992-10-23 | 1994-05-11 | Optex Biomedical, Inc. | Fibre-optic probe for the measurement of fluid parameters |
| US5280548A (en) * | 1993-03-11 | 1994-01-18 | Boc Health Care, Inc. | Emission based fiber optic sensors for pH and carbon dioxide analysis |
| US5607644A (en) | 1993-06-10 | 1997-03-04 | Optical Sensors Incorporated | Optical sensor for the measurement of pH in a fluid, and related sensing compositions and methods |
| AU6686794A (en) | 1993-06-30 | 1995-01-24 | Biomedical Sensors Limited | Biphasic material |
| GB2284809B (en) | 1993-11-07 | 1998-04-29 | Japan Res Dev Corp | A fluorescent phenylboronic acid suitable for use in the detection of saccharides |
| US5514710A (en) | 1994-01-11 | 1996-05-07 | Molecular Probes, Inc. | Photocleavable derivatives of hydroxyprenesulfonic acids |
| US5511547A (en) | 1994-02-16 | 1996-04-30 | Biomedical Sensors, Ltd. | Solid state sensors |
| US5389217A (en) | 1994-04-28 | 1995-02-14 | Biomedical Sensors Ltd. | Measurement of bladder oxygen |
| DE69507465T2 (de) | 1994-05-02 | 1999-06-24 | Novartis Ag | OPTISCHES SENSORSYSTEM ZUR BESTIMMUNG VON pH-WERTEN UND IONENSTÄRKEN |
| JP2799837B2 (ja) | 1995-03-03 | 1998-09-21 | 科学技術振興事業団 | ビナフチル基を有するボロン酸化合物 |
| US5622259A (en) | 1995-06-07 | 1997-04-22 | Church; Jonathan M. | Reduction of discoloration in plastic materials |
| JP3183390B2 (ja) | 1995-09-05 | 2001-07-09 | キヤノン株式会社 | 光電変換装置及びそれを用いた撮像装置 |
| EP0862648B1 (en) | 1995-11-22 | 2004-10-06 | Medtronic MiniMed, Inc. | Detection of biological molecules using chemical amplification and optical sensors |
| US6766183B2 (en) | 1995-11-22 | 2004-07-20 | Medtronic Minimed, Inc. | Long wave fluorophore sensor compounds and other fluorescent sensor compounds in polymers |
| US6002954A (en) | 1995-11-22 | 1999-12-14 | The Regents Of The University Of California | Detection of biological molecules using boronate-based chemical amplification and optical sensors |
| US5747666A (en) | 1997-03-26 | 1998-05-05 | Willis; John P. | Point-of-care analyzer module |
| DE19738942A1 (de) | 1997-09-05 | 1999-03-25 | Pulsion Verwaltungs Gmbh & Co | Verfahren und Vorrichtung zur Injektionszeitpunkt- und Injektionsdauerbestimmung bei Thermodilutionsmessungen |
| US6117290A (en) | 1997-09-26 | 2000-09-12 | Pepex Biomedical, Llc | System and method for measuring a bioanalyte such as lactate |
| US6119028A (en) | 1997-10-20 | 2000-09-12 | Alfred E. Mann Foundation | Implantable enzyme-based monitoring systems having improved longevity due to improved exterior surfaces |
| US6702972B1 (en) | 1998-06-09 | 2004-03-09 | Diametrics Medical Limited | Method of making a kink-resistant catheter |
| GB9814506D0 (en) | 1998-07-03 | 1998-09-02 | Stanley Christopher J | Optical sensor for insitu measurement of analytes |
| AU5394099A (en) | 1998-08-07 | 2000-02-28 | Infinite Biomedical Technologies, Incorporated | Implantable myocardial ischemia detection, indication and action technology |
| US6248127B1 (en) | 1998-08-21 | 2001-06-19 | Medtronic Ave, Inc. | Thromboresistant coated medical device |
| US6304766B1 (en) | 1998-08-26 | 2001-10-16 | Sensors For Medicine And Science | Optical-based sensing devices, especially for in-situ sensing in humans |
| PT1108207E (pt) * | 1998-08-26 | 2008-08-06 | Sensors For Med & Science Inc | Dispositivos de sensores ópticos |
| GB9821575D0 (en) | 1998-10-02 | 1998-11-25 | Diametrics Medical Limited | Cranial bolt |
| GB2342863B (en) | 1998-10-02 | 2003-02-19 | Diametrics Medical Ltd | Probe |
| US6464849B1 (en) | 1999-10-07 | 2002-10-15 | Pepex Biomedical, L.L.C. | Sensor for measuring a bioanalyte such as lactate |
| US6375627B1 (en) | 2000-03-02 | 2002-04-23 | Agilent Technologies, Inc. | Physiological fluid extraction with rapid analysis |
| US6442413B1 (en) | 2000-05-15 | 2002-08-27 | James H. Silver | Implantable sensor |
| US7769420B2 (en) | 2000-05-15 | 2010-08-03 | Silver James H | Sensors for detecting substances indicative of stroke, ischemia, or myocardial infarction |
| US7181261B2 (en) | 2000-05-15 | 2007-02-20 | Silver James H | Implantable, retrievable, thrombus minimizing sensors |
| DK1307464T3 (da) | 2000-08-04 | 2013-03-18 | Senseonics Inc | Detektion af analytter i vandige miljøer |
| US7470420B2 (en) | 2000-12-05 | 2008-12-30 | The Regents Of The University Of California | Optical determination of glucose utilizing boronic acid adducts |
| US6627177B2 (en) | 2000-12-05 | 2003-09-30 | The Regents Of The University Of California | Polyhydroxyl-substituted organic molecule sensing optical in vivo method utilizing a boronic acid adduct and the device thereof |
| US6653141B2 (en) | 2000-12-05 | 2003-11-25 | The Regents Of The University Of California | Polyhydroxyl-substituted organic molecule sensing method and device |
| US6800451B2 (en) | 2001-01-05 | 2004-10-05 | Sensors For Medicine And Science, Inc. | Detection of glucose in solutions also containing an alpha-hydroxy acid or a beta-diketone |
| US7682669B1 (en) | 2001-07-30 | 2010-03-23 | Advanced Cardiovascular Systems, Inc. | Methods for covalently immobilizing anti-thrombogenic material into a coating on a medical device |
| GB0125195D0 (en) | 2001-10-19 | 2001-12-12 | Optomed As | Optical sensing of measurands |
| DE60323943D1 (de) | 2002-02-21 | 2008-11-20 | Encelle Inc | Immobilisierte bioaktive hydrogel matrizen für oberflächenbeschichtungen |
| US7317111B2 (en) | 2002-09-23 | 2008-01-08 | Aries Associates, Inc. | Green and orange fluorescent labels and their uses |
| US7226414B2 (en) | 2002-10-09 | 2007-06-05 | Biotex, Inc. | Method and apparatus for analyte sensing |
| US7390462B2 (en) * | 2002-12-17 | 2008-06-24 | The University Of Maryland Baltimore County | Ratiometric fluorescent pH sensor for non-invasive monitoring |
| US7358094B2 (en) | 2003-05-01 | 2008-04-15 | Bell Michael L | Sensor system for saccharides |
| US20080009687A1 (en) | 2003-06-06 | 2008-01-10 | Smith Joseph T | Coiled circuit bio-sensor |
| US7353055B2 (en) | 2003-06-18 | 2008-04-01 | Hogan Josh N | Non-invasive analysis system |
| US6931327B2 (en) | 2003-08-01 | 2005-08-16 | Dexcom, Inc. | System and methods for processing analyte sensor data |
| US20050124896A1 (en) | 2003-08-25 | 2005-06-09 | Jacob Richter | Method for protecting implantable sensors and protected implantable sensors |
| US7559894B2 (en) | 2003-09-18 | 2009-07-14 | New Paradigm Concepts, LLC | Multiparameter whole blood monitor and method |
| US7181260B2 (en) | 2003-11-14 | 2007-02-20 | Guillermo Gutierrez | Apparatus and method for measuring myocardial oxygen consumption |
| US7787923B2 (en) | 2003-11-26 | 2010-08-31 | Becton, Dickinson And Company | Fiber optic device for sensing analytes and method of making same |
| US8287453B2 (en) | 2003-12-05 | 2012-10-16 | Dexcom, Inc. | Analyte sensor |
| US8532730B2 (en) | 2006-10-04 | 2013-09-10 | Dexcom, Inc. | Analyte sensor |
| WO2005064336A1 (en) | 2003-12-09 | 2005-07-14 | Molecular Probes, Inc. | Pyrenyloxysulfonic acid fluorescent agents |
| US8029765B2 (en) | 2003-12-24 | 2011-10-04 | Masimo Laboratories, Inc. | SMMR (small molecule metabolite reporters) for use as in vivo glucose biosensors |
| GB2410793B (en) | 2004-02-05 | 2006-05-17 | Elan Vital | Fluid analyser systems |
| US20050233465A1 (en) | 2004-04-14 | 2005-10-20 | Bioprocessors Corp. | Compositions of matter useful as pH indicators and related methods |
| US20050241959A1 (en) | 2004-04-30 | 2005-11-03 | Kenneth Ward | Chemical-sensing devices |
| US8696564B2 (en) | 2004-07-09 | 2014-04-15 | Cardiac Pacemakers, Inc. | Implantable sensor with biocompatible coating for controlling or inhibiting tissue growth |
| AU2005277258B2 (en) * | 2004-08-19 | 2012-03-29 | Blood Cell Storage, Inc | Fluorescent pH detector system and related methods |
| US20060088722A1 (en) | 2004-10-25 | 2006-04-27 | Aller Robert C | Optical pH sensor |
| US20060105174A1 (en) | 2004-10-25 | 2006-05-18 | The Research Foundation Of State University Of New York | Optical pH sensor |
| US7306621B1 (en) | 2004-11-19 | 2007-12-11 | National Semiconductor Corporation | Heat transfer control for a prosthetic retinal device |
| EP1827551A1 (en) | 2004-12-06 | 2007-09-05 | SurModics, Inc. | Multifunctional medical articles |
| WO2006078432A2 (en) | 2005-01-18 | 2006-07-27 | Cyberkinetics Neurotechnology Systems, Inc. | Biological interface system with automated configuration |
| US20060189926A1 (en) | 2005-02-14 | 2006-08-24 | Hall W D | Apparatus and methods for analyzing body fluid samples |
| CA2621993A1 (en) | 2005-09-16 | 2007-03-29 | Bg Implant, Inc. | Glaucoma treatment devices and methods |
| DE102005056310B4 (de) | 2005-11-25 | 2017-02-02 | Drägerwerk AG & Co. KGaA | Verfahren und Vorrichtung zur Überwachung von Infusionen |
| DE502006009203D1 (de) | 2006-01-30 | 2011-05-12 | Pulsion Medical Sys Ag | System zum Einrichten einer Dilutionsmessstelle |
| US20090105087A1 (en) | 2006-03-15 | 2009-04-23 | Koninklijke Philips Electronics N.V. | Microelectronic device with controllable reference substance supply |
| US20080154107A1 (en) | 2006-12-20 | 2008-06-26 | Jina Arvind N | Device, systems, methods and tools for continuous glucose monitoring |
| US7417164B2 (en) | 2006-07-25 | 2008-08-26 | Glumetrics Inc. | Fluorescent dyes for use in glucose sensing |
| US9725549B2 (en) | 2006-10-27 | 2017-08-08 | Basf Se | Radiation-curable mixture containing low-molecular, ethylenically unsaturated compounds having non-aromatic ring systems |
| US7855192B2 (en) | 2007-01-26 | 2010-12-21 | Kosan Biosciences, Inc. | Macrolactams by engineered biosynthesis |
| USD626143S1 (en) | 2007-02-06 | 2010-10-26 | Glumetrics, Inc. | Computer-generated icon for a blood glucose display |
| US7829341B2 (en) | 2007-07-11 | 2010-11-09 | Glumetrics, Inc. | Polyviologen boronic acid quenchers for use in analyte sensors |
| EP2120680A2 (en) | 2007-02-06 | 2009-11-25 | Glumetrics, Inc. | Optical systems and methods for rationmetric measurement of blood glucose concentration |
| EP2122334B1 (en) | 2007-02-06 | 2018-01-24 | Medtronic Minimed, Inc. | Method for polymerizing a monomer solution within a cavity to generate a smooth polymer surface |
| US7751863B2 (en) | 2007-02-06 | 2010-07-06 | Glumetrics, Inc. | Optical determination of ph and glucose |
| TW200848019A (en) | 2007-03-06 | 2008-12-16 | Wyeth Corp | Aryl sulfonamides useful for modulation of the progesterone receptor |
| DE602008006382D1 (de) | 2007-05-01 | 2011-06-01 | Glumetrics Inc | Pyridin-boronsäure-quencher zur verwendung in analytsensoren |
| WO2008141243A2 (en) | 2007-05-10 | 2008-11-20 | Glumetrics, Inc. | Device and methods for calibrating analyte sensors |
| JP5517919B2 (ja) | 2007-05-10 | 2014-06-11 | グルメトリクス、 インク. | 即時血管内グルコース測定のための平衡非消費蛍光センサー |
| US8027737B2 (en) | 2007-08-01 | 2011-09-27 | Intelect Medical, Inc. | Lead extension with input capabilities |
| EP3078714A1 (en) | 2007-08-06 | 2016-10-12 | Medtronic Minimed, Inc. | Hpts-mono and bis cys-ma polymerizable fluorescent dyes for use in analyte sensors |
| US8202731B2 (en) | 2007-08-06 | 2012-06-19 | Glumetrics, Inc. | HPTS-mono and bis Cys-MA polymerizable fluorescent dyes for use in analyte sensors |
| EP2217316A4 (en) | 2007-11-21 | 2013-01-16 | Glumetrics Inc | USE OF AN INTRAVASCULAR EQUILIBRIUM SENSOR FOR CLOSE GLYCEMIC CONTROL |
| WO2009129186A2 (en) | 2008-04-17 | 2009-10-22 | Glumetrics, Inc. | Sensor for percutaneous intravascular deployment without an indwelling cannula |
| JP5721703B2 (ja) | 2009-06-05 | 2015-05-20 | メドトロニック ミニメド インコーポレイテッド | グルコース濃度を求めるための方法および測定デバイス |
| EP2483679A4 (en) | 2009-09-30 | 2013-04-24 | Glumetrics Inc | SENSORS WITH THROMORETIC COATINGS |
| US8467843B2 (en) | 2009-11-04 | 2013-06-18 | Glumetrics, Inc. | Optical sensor configuration for ratiometric correction of blood glucose measurement |
| WO2011084713A1 (en) | 2009-12-17 | 2011-07-14 | Glumetrics, Inc. | Glucose sensor and controller with user selectable output |
| WO2011075710A1 (en) | 2009-12-17 | 2011-06-23 | Glumetrics, Inc. | Identification of aberrant measurements of in vivo glucose concentration using temperature |
| WO2011075711A1 (en) | 2009-12-17 | 2011-06-23 | Glumetrics, Inc. | System and method for maintaining glycemic control based on glucose activity measurements |
| WO2011137178A1 (en) | 2010-04-27 | 2011-11-03 | Glumetrics, Inc. | Deployment system and method for optical analyte sensor |
-
2007
- 2007-02-06 US US11/671,880 patent/US7751863B2/en not_active Expired - Fee Related
-
2008
- 2008-01-28 EP EP08728399.0A patent/EP2122361B1/en active Active
- 2008-01-28 WO PCT/US2008/052204 patent/WO2008097747A1/en active Application Filing
- 2008-01-28 CA CA002674513A patent/CA2674513A1/en not_active Abandoned
- 2008-01-28 JP JP2009549167A patent/JP5017377B2/ja not_active Expired - Fee Related
- 2008-01-28 DK DK08728399.0T patent/DK2122361T3/da active
- 2008-01-28 AU AU2008214099A patent/AU2008214099A1/en not_active Abandoned
-
2010
- 2010-07-02 US US12/830,231 patent/US8498682B2/en active Active
-
2013
- 2013-07-25 US US13/951,125 patent/US8983565B2/en active Active
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8838195B2 (en) | 2007-02-06 | 2014-09-16 | Medtronic Minimed, Inc. | Optical systems and methods for ratiometric measurement of blood glucose concentration |
| US9839378B2 (en) | 2007-02-06 | 2017-12-12 | Medtronic Minimed, Inc. | Optical systems and methods for ratiometric measurement of blood glucose concentration |
| US8738107B2 (en) | 2007-05-10 | 2014-05-27 | Medtronic Minimed, Inc. | Equilibrium non-consuming fluorescence sensor for real time intravascular glucose measurement |
| US8467843B2 (en) | 2009-11-04 | 2013-06-18 | Glumetrics, Inc. | Optical sensor configuration for ratiometric correction of blood glucose measurement |
| US8700115B2 (en) | 2009-11-04 | 2014-04-15 | Glumetrics, Inc. | Optical sensor configuration for ratiometric correction of glucose measurement |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2674513A1 (en) | 2008-08-14 |
| JP2010518397A (ja) | 2010-05-27 |
| US8498682B2 (en) | 2013-07-30 |
| EP2122361A1 (en) | 2009-11-25 |
| EP2122361B1 (en) | 2014-03-12 |
| AU2008214099A1 (en) | 2008-08-14 |
| WO2008097747A1 (en) | 2008-08-14 |
| US20100274110A1 (en) | 2010-10-28 |
| US7751863B2 (en) | 2010-07-06 |
| US20140058225A1 (en) | 2014-02-27 |
| US20080188722A1 (en) | 2008-08-07 |
| DK2122361T3 (da) | 2014-06-23 |
| US8983565B2 (en) | 2015-03-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5017377B2 (ja) | pH及びグルコースの光学的決定 | |
| JP5517919B2 (ja) | 即時血管内グルコース測定のための平衡非消費蛍光センサー | |
| DK2989975T3 (en) | OPTICAL SYSTEMS AND PROCEDURES FOR RATIOMETRIC MEASUREMENT OF BLOOD GLUCOSE CONCENTRATION | |
| EP2545373B1 (en) | Measuring analyte concentration incorporating temperature and ph correction | |
| US8535262B2 (en) | Use of an equilibrium intravascular sensor to achieve tight glycemic control | |
| JP6534616B2 (ja) | 光検体センサの乾燥挿入および1点invivo較正 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110118 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110118 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111124 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120229 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120515 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120611 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150615 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5017377 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |