JP4875366B2 - ポリアミノポリカルボン酸鉄アルカリ塩の製造法 - Google Patents
ポリアミノポリカルボン酸鉄アルカリ塩の製造法 Download PDFInfo
- Publication number
- JP4875366B2 JP4875366B2 JP2006010832A JP2006010832A JP4875366B2 JP 4875366 B2 JP4875366 B2 JP 4875366B2 JP 2006010832 A JP2006010832 A JP 2006010832A JP 2006010832 A JP2006010832 A JP 2006010832A JP 4875366 B2 JP4875366 B2 JP 4875366B2
- Authority
- JP
- Japan
- Prior art keywords
- acid
- polyaminopolycarboxylic acid
- alkali
- ferric
- salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
粉末を取得する手段としては鉄アルカリ塩を製造した後のアルカリ過剰の水溶液に硫酸などの鉱酸の塩を添加することにより鉄アルカリ塩の溶解度を下げて結晶化しやすくし、濃縮、分離、乾燥する方法が開示記載されている(特許文献3及び特許文献4)。これらの方法では、結晶に鉱酸の塩が含まれるため、洗浄工程が必要になり工程が煩雑になる上、ろ液に大量の鉱酸の塩が存在するため、ろ液のリサイクル使用が困難であり、収率の向上がはかれないという難点がある。
ポリアミノポリカルボン酸と鉄およびアルカリ塩の反応方法としては、公知のものが使用できる。たとえば、前述の特許文献1及び特許文献2に開示された方法などがあげられる。
ポリアミノポリカルボン酸の第二鉄アンモニウム塩の製造は、水、ポリアミノポリカルボン酸、アルカリ水溶液、酸化鉄を常温で仕込んで加熱することにより行なうことができる。ここで、ポリアミノポリカルボン酸とアルカリ水溶液の代わりに、ポリアミノポリカルボン酸とポリアミノポリカルボン酸の部分中和物の水溶液を混合して使用することもできる。
酸化工程の後、ポリアミノポリカルボン酸第二鉄アルカリ塩水溶液を濃縮して、この塩の結晶を析出させ、結晶を回収する。このときの、スラリー濃度は、ポリアミノポリカルボン酸第二鉄アルカリ塩の回収率の点から40質量%以上が好ましく、45質量%以上がより好ましく、50質量%以上が特に好ましい。結晶中に分解物などの不純物が付着することを避ける目的で、スラリー濃度は、65質量%以下が好ましく、60質量%以下がより好ましく、55質量%以下が特に好ましい。濃縮は公知の各種濃縮法で行えるが、減圧濃縮がより好ましく、そのときの温度は、濃縮効率の点から濃縮温度は、10℃以上が好ましく、20℃以上がより好ましい。分解反応を抑制する点から、濃縮温度は80℃以下が好ましく、60℃以下がより好ましい。
所定スラリー濃度まで濃縮した後、減圧ろ過、遠心分離等の方法で結晶を分離することにより、高純度のポリアミノポリカルボン酸第二鉄アルカリ塩を得ることができる。このポリアミノポリカルボン酸第二鉄アルカリ塩は、洗浄無しで十分に製品として使用可能であるが、より高純度なポリアミノポリカルボン酸第二鉄アルカリ塩を得たい場合は、少量の冷水で洗浄しても良い。
なお、収率は高速液体クロマトグラフの分析結果から算出し、第一鉄イオンの量は分光光度計の分析結果から算出した。
(1)測定試料の調整:反応液2gを100mlのメスフラスコに入れ、水を加えて溶解させる。20%水酸化ナトリウム水溶液を20ml加え、超音波洗浄器で20分間振とうした後、水を加えて、メスアップし、ろ過する。ろ液を10mlとり、100mlのメスフラスコに入れ、試料希釈液を80ml加える。85%リン酸を添加し、pH3前後にした後、試料希釈液でメスアップする。
(2)試料の分析:高速液体クロマトグラフを使用し、波長254nmで測定する
(3)測定条件:カラム・・・Inertsil‐C4 4.6×150mm (GLサイエンス社製)、キャリア液流速・・・1ml/min、カラム温度・・・40℃
(4)キャリアの組成:0.2%トリ−n−プロピルアミン−40ppm硫酸銅水溶液(リン酸でpH 3.0に調整)。
(5)試料希釈液の組成:0.2%トリ−n−プロピルアミン−0.2%硫酸銅水溶液(リン酸でpH 3.0に調整)
(1)試料溶液の調製:試料25gを75gの純水に溶解する。
(2)測定用検液の調製:試料溶液3gを精秤し、250 mlのメスフラスコに移し、純水でメスアップする。
(3)全鉄の測定:20ml蓋付きガラス瓶に発色液10mlと検液をマイクロシリンジで50μl取り、Lーアスコルビン酸0.01gを加える。蓋をして4〜5回強く振り60分間放置後、分光光度計で535 nmの吸光度を測定する。
(4)第一鉄イオンの測定:20ml蓋付きガラス瓶に発色液10mlと検液をマイクロシリンジで50μl取り、蓋をして4〜5回強く振り60分間放置後、分光光度計で535nmの吸光度を測定する。
(5)第一鉄イオン/全鉄比の計算下記の式を用いて第一鉄イオン/全鉄の比を計算する。
第一鉄イオン/全鉄(%)=D1/D2 ×100
D1・・・第一鉄イオンの吸光度測定からの定量値
D2・・・全鉄の測定の吸光度測定からの定量値
(6)発色液の調製:発色液は以下の組成で調整。
バソフェナントロリンジスルホン酸二ナトリウム(第一鉄イオン用)0.5 g
酢酸ナトリウム1.5 g
酢酸 1.0 g
以上を純水200 mlに溶解する。
攪拌機、温度計、コンデンサーを備えた1Lのセパラブルフラスコ中に、常温下、水150g、99.6%ジエチレントリアミン五酢酸(DTPA)150g(0.38mol)、15%アンモニア水42.3g(0.373mol)、鉄含量71%の四三酸化鉄27.94g(0.355mol)、鉄粉0.279g(0.005mol)仕込み、攪拌しながら昇温し、85〜90℃で2.5時間熟成した。この反応液を目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、ジエチレントリアミン五酢酸第二鉄アンモニウム塩(DTPA・Fe・NH3塩)とした。この水溶液を攪拌しながら50℃で減圧濃縮した後、10℃まで冷却して3時間かけて、結晶を析出させた。このときのスラリー濃度は51%であった。この結晶を遠心分離して、結晶を回収し、ろ液129.6gを褐色瓶に保管した(室温で一日)。結晶を120℃で2時間減圧乾燥し、純度98.7%のDTPA・Fe・NH3塩一水和物結晶140.4g(DTPAベースの収率77.1%)を得た。全鉄イオンに対する第一鉄イオンの量は0.08%であった。
15%アンモニア水を41.8g(0.369mol)に変えた以外は、参考例1と同様に仕込んで反応を行った。この反応液に参考例1で保管したろ液を少量の水と共に加え、目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、DTPA・Fe・NH3塩とした。以降、参考例1と同様に処理した。
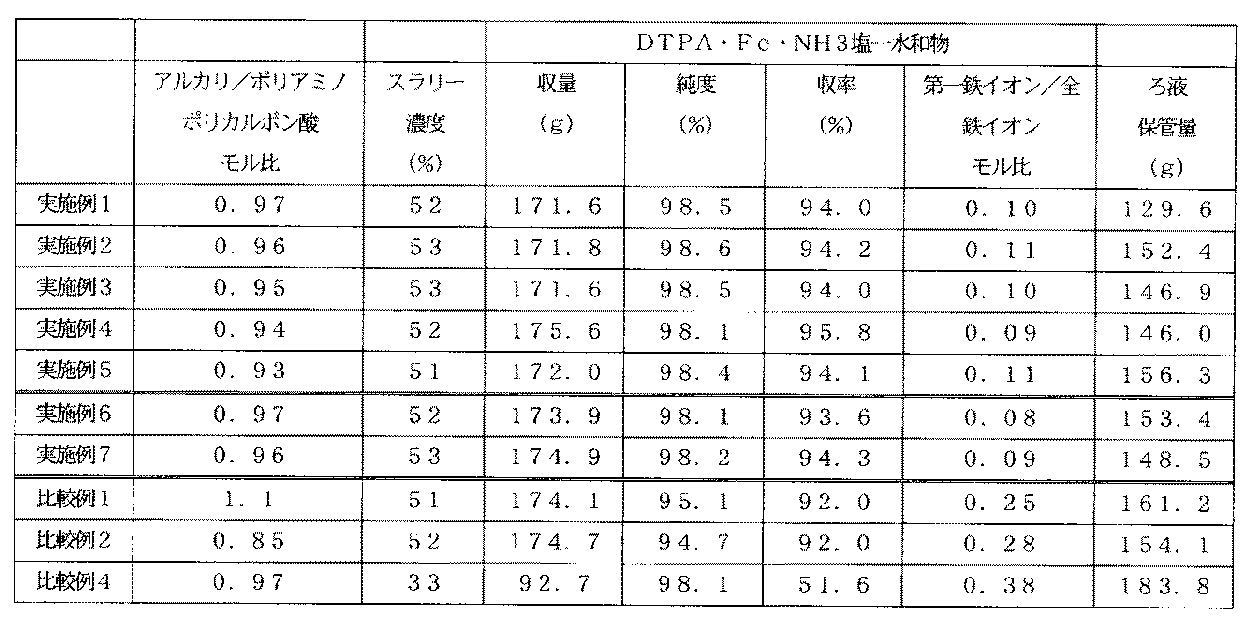
この結果を表1に示す。
15%アンモニア水を41.4g(0.365mol)に変えた以外は、実施例1と同様に仕込んで反応を行った。この反応液に実施例1で保管したろ液を少量の水と共に加え、実施例1と同様に処理した。
この結果を表1に示す。
15%アンモニア水の仕込み量を表1のように変えた以外は、実施例2と同様に反応、処理を行った。
この結果を表1に示す。
15%アンモニア水を30%水酸化ナトリウム水溶液49.73g(0.373mol)に変えた以外は、参考例1と同様に仕込んで反応、処理を行った。このときのスラリー濃度は51%、保管したろ液は131.0gであった。
その結果、純度98.4%のジエチレントリアミン五酢酸第二鉄ナトリウム塩(DTPA・Fe・Na塩)一水和物結晶141.0g(DTPAベースの収率76.2%)を得た。全鉄イオンに対する第一鉄イオンの量は0.06%であった。
30%水酸化ナトリウム水溶液を49.15g(0.369mol)に変えた以外は、参考例2と同様に仕込んで反応を行った。この反応液に参考例2で保管したろ液を少量の水と共に加え、目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、DTPA・Fe・NH3塩とした。以降、参考例2と同様に処理した。
この結果を表1に示す。
30%水酸化ナトリウム水溶液を48.64g(0.365mol)に変えた以外は、実施例6と同様に仕込んで反応を行った。この反応液に実施例6で保管したろ液を少量の水と共に加え、実施例6と同様に処理した。
この結果を表1に示す。
15%アンモニア水を47.4g(0.418mol)に変えた以外は、参考例1と同様に仕込んで反応、処理を行った。
その結果、純度96.5%のDTPA・Fe・NH3塩一水和物結晶144.2g(DTPAベースの収率77.4%)を得た。全鉄イオンに対する第一鉄イオンの量は0.10%であった。このときのスラリー濃度は51%、保管したろ液は132.5gであった。
参考例3と同様に仕込み、反応を行った。この反応液を目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、DTPA・Fe・NH3塩とした。この水溶液に、参考例3で保管したろ液を少量の水と共に加えて、攪拌しながら50℃で減圧濃縮した後、10℃まで冷却して3時間かけて、結晶を析出させた。以降は参考例1と同様に処理を行った。
この結果を表1に示す。
15%アンモニア水を36.6g(0.323mol)に変えた以外は、参考例1と同様に仕込んで反応、処理を行った。
その結果、純度95.1%のDTPA・Fe・NH3塩一水和物結晶147.1g(DTPAベースの収率77.7%)を得た。全鉄イオンに対する第一鉄イオンの量は0.10%であった。このときのスラリー濃度は51%、保管したろ液は135.7gであった。
参考例4と同様に仕込み、反応を行った。この反応液を目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、DTPA・Fe・NH3塩とした。この水溶液に、参考例4で保管したろ液を少量の水と共に加えて、攪拌しながら50℃で減圧濃縮した後、10℃まで冷却して3時間かけて、結晶を析出させた。以降は参考例1と同様に処理を行った。
この結果を表1に示す。
実施例1と同様の条件で反応を行い、この反応液に参考例1と同様の方法で取得し、保管したろ液を少量の水と共に加え、実施例1と同様に処理し、スラリー濃度68%になるようにこの水溶液を攪拌しながら50℃で減圧濃縮した。10℃まで冷却したところ、粘張性のスラッジとなりろ過できなかった。
実施例1と同様の条件で反応を行い、この反応液を目開き1μmのフィルターを使用し、ろ過して不溶物をろ別した。50〜55℃でボールフィルターを用いて空気を1.5L/分の流量で10時間吹き込むことにより、反応液中の錯体を酸化し、DTPA・Fe・NH3塩とした。この水溶液に、参考例1と同様の方法で取得し、保管したろ液を少量の水と共に加えて、攪拌しながら50℃で減圧濃縮した後、10℃まで冷却して3時間かけて、結晶を析出させた。このときのスラリー濃度は33%であった。以後、実施例1と同様に処理した。
この結果を表1に示す。
Claims (5)
- 水溶液中で、ポリアミノポリカルボン酸とアルカリおよび鉄化合物を反応させた後、分子状酸素で酸化処理を行って得たポリアミノポリカルボン酸第二鉄アルカリ塩水溶液を濃縮して、スラリー濃度が40〜65質量%になるようにこの塩の結晶を析出させ、次いで結晶と母液を分離回収するポリアミノポリカルボン酸第二鉄アルカリ塩の製造において、分離回収された母液の一部または全部を次回以後の製造にリサイクル使用することを特徴とするポリアミノポリカルボン酸第二鉄アルカリ塩の製造法。
- 分離回収された母液の一部または全部を次回以降の製造の、ポリアミノポリカルボン酸とアルカリおよび鉄化合物を反応させた後に添加して、分子状酸素で酸化処理を行った後、濃縮することを特徴とする請求項1記載のポリアミノポリカルボン酸第二鉄の製造法。
- ポリアミノポリカルボン酸が、分子構造中に窒素−水素結合を持たない化合物であることを特徴とする請求項1または2記載のポリアミノポリカルボン酸第二鉄アルカリ塩の製造法。
- ポリアミノポリカルボン酸とアルカリおよび鉄化合物を反応させる際の、アルカリ/ポリアミノポリカルボン酸モル比が0.9〜0.99であることを特徴とする請求項1〜3のいずれか一項記載のポリアミノポリカルボン酸第二鉄アルカリ塩の製造法。
- 母液のリサイクル使用を行う2回目以降の製造で、ポリアミノポリカルボン酸とアルカリおよび鉄化合物を反応させる際のアルカリ/ポリアミノポリカルボン酸モル比を、母液のリサイクル使用を行わない初回製造時のモル比よりも小さくすることを特徴とする請求項1〜4のいずれか一項記載のポリアミノポリカルボン酸第二鉄アルカリ塩の製造法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006010832A JP4875366B2 (ja) | 2006-01-19 | 2006-01-19 | ポリアミノポリカルボン酸鉄アルカリ塩の製造法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006010832A JP4875366B2 (ja) | 2006-01-19 | 2006-01-19 | ポリアミノポリカルボン酸鉄アルカリ塩の製造法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007191423A JP2007191423A (ja) | 2007-08-02 |
| JP4875366B2 true JP4875366B2 (ja) | 2012-02-15 |
Family
ID=38447403
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006010832A Expired - Fee Related JP4875366B2 (ja) | 2006-01-19 | 2006-01-19 | ポリアミノポリカルボン酸鉄アルカリ塩の製造法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4875366B2 (ja) |
-
2006
- 2006-01-19 JP JP2006010832A patent/JP4875366B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2007191423A (ja) | 2007-08-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5676206B2 (ja) | 四塩化ゲルマニウムの回収方法 | |
| BE886326A (fr) | Procede de fabrication de composes de titane au moyen d'un reducteur | |
| CN110438347A (zh) | 钠化清洁提钒方法 | |
| JP2001226344A (ja) | 2−ヒドロキシ−4−メチルチオブタン酸の製造方法 | |
| JP4875366B2 (ja) | ポリアミノポリカルボン酸鉄アルカリ塩の製造法 | |
| JP2015013858A (ja) | アゾ化合物類を合成するための方法 | |
| JP2000211906A (ja) | フリーヒドロキシルアミン水溶液の製造方法 | |
| US4275041A (en) | Process for manufacturing a stable titanyl sulfate solution | |
| JPH0696455B2 (ja) | 高純度硫酸コバルトの製造方法 | |
| JPH07224334A (ja) | 銅の分離回収方法 | |
| JP3503116B2 (ja) | 高濃度フリーヒドロキシルアミン水溶液の製造法 | |
| JP4441802B2 (ja) | 2,3−ピリジンジカルボン酸の製造方法 | |
| JP4322122B2 (ja) | 高純度ニオブ化合物及び/又はタンタル化合物の精製方法 | |
| JPS60231647A (ja) | パラフインのスルホ酸化で生じた反応混合物から残留硫酸を除く方法 | |
| JP4351912B2 (ja) | ニオブ化合物及び/又はタンタル化合物の精製方法 | |
| CN111732133A (zh) | 一种硫酸四氨钯的制备方法 | |
| US4599223A (en) | Separation of tungsten from rhenium | |
| JP3503115B2 (ja) | フリーヒドロキシルアミン水溶液の製造方法 | |
| RU2305066C2 (ru) | Способ получения йодата и йодида калия | |
| US6485700B1 (en) | Process for producing free hydroxylamine aqueous solution | |
| CN112830892A (zh) | 一种吡啶-3-磺酰氯的合成方法 | |
| CN111491916B (zh) | 甲硫氨酸的制造方法 | |
| FI70563B (fi) | Foerfarande foer framstaellning av titandioxid genom anvaendning av reduktionsmedel | |
| JP6983256B2 (ja) | 精製メチオニンの製造方法 | |
| JPH0288421A (ja) | アンモニウムミョウバンの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081226 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111109 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20111117 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20111125 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141202 Year of fee payment: 3 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 4875366 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141202 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141202 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141202 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141202 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |