JP4822654B2 - 血管疾患治療用hmgb1蛋白質インヒビタおよび/またはアンタゴニスト - Google Patents
血管疾患治療用hmgb1蛋白質インヒビタおよび/またはアンタゴニスト Download PDFInfo
- Publication number
- JP4822654B2 JP4822654B2 JP2002573044A JP2002573044A JP4822654B2 JP 4822654 B2 JP4822654 B2 JP 4822654B2 JP 2002573044 A JP2002573044 A JP 2002573044A JP 2002573044 A JP2002573044 A JP 2002573044A JP 4822654 B2 JP4822654 B2 JP 4822654B2
- Authority
- JP
- Japan
- Prior art keywords
- hmgb1
- hmg
- box domain
- cells
- amino acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Dermatology (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
さらに、HMGB1の阻害剤(すなわち、グリチルリジン(Glicyrrhizin))は抗炎症剤として利用可能であることは既に知られている(サカモト等、2001年、Biol.Pharm.Bull.,24(8)906−911;Yoh等、2002年、Dig.Dis.Sci.,47(8),1775−1781)。
したがって、HMGB1は、血管損傷の後のアテローム性動脈硬化症および再狭窄を促進可能な分子の顕著な特徴を全て有する。
結論として、HMGB1およびそのRAGEレセプタ間の相互作用を遮断できる各種の分子(すなわち、阻害剤クラスに属する全分子:抗体または抗体フラグメント、4方向DNA;およびHMGボックスアンタゴニストクラスに属する全分子:HMGボックスドメインを含むHMGB1フラグメント分子)は、血管形成のために血管上皮の損傷後、アテローム性動脈硬化症および再狭窄を回避するか、遅らせるか、または阻害するために、薬理的調薬の製造のために効果的に使用できる。
本発明の目的は、血管疾患治療用の治療薬の調薬のためにHMGB1およびRAGE間の相互作用を遮断できる分子を使用することである。
本発明のさらなる特徴および利点は、添付図面を参照して、以下の詳細な説明から容易に明らかになるであろう。
最初の段階で、HMGB1および誘導体の発現および精製が必要である。
全長HMGB1の発現はpT7−7rHMG1cmプラスミド(ケンブリッジ大学、J.O.Thomas教授から送られた)で形質転換したE.coliにおいて行われ、精製は以下の既知のプロトコル(Muller等、2001年、Biochemistry,40:10254−10261)で実施された。
イーストPichia Pastoriaの全長HMGB1の発現および精製を以下の既知のプロトコル(Mistry等、1997年、Biotechniques,22:718−729)で実施した。
走化性アッセイを周知のプロトコル(Degryse等、1999年、Blood,94:649−662)を使用して行った。変法ボイデンチャンバーを0.5μmポアサイズのフィルタ(Corning,Acton、MA)と共に使用し、フィブロネクチン(10μm/ml)のコラーゲンI(0.5Mの酢酸中100μg/ml)(Roche)で処理した。RSMC細胞(ミラン、バイヤーリサーチ研究所、Marco Bertulli博士により送られた)をDMEM血清フリー中で培養し、20.000−40.000細胞のサンプルをボイデンチャンバーの上部ウェルに添加した。試験されるべき分子を同じ血清フリー培地で培養し、下方ウェルに添加した。
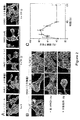
図1−A、1−B、1−C、1−Dに示すように、結果は、フィルタあたり10の高倍率フィールドでカウントされ、コントロールを超えたホールドとして発現された、細胞数の平均値±SDである。ランダム細胞移動(すなわち、化学誘引物質が無い状態の移動)は100%の任意の値を付与した。
統計的分析を、処理したペアでの比較のために、スチューデントのtテストを使用して、あるいは、試薬の高投与量を用いた処理の評価のために、ANOVAモデルを使用して実施した。
15.000−20.000のサンプルを、20−40%の密集度で、2cm2ウェルのガラスカバースリップにまき、DMEMプラス10%FCS中で24時間培養し、PBSで洗浄し、FCSの無いDMEM中でさらに24時間培養した。RSMCを、37℃で5〜120分の増加時間間隔で、HMGB1,100ng/mlを用いて刺激した。刺激後、RSMCを、3%のパラホルムアルデヒド、PBS中2%スクロース、pH7.5の溶液を用いて、室温で20分間固定し、PBS−BSA0.2%を用いて3回洗浄した。細胞を20mMヘペスpH7.4、300mMサッカロース、50mMNaCl,3mMMgCl2、0.5%(V/V)TritonX−100で4℃、3分間透過させ、再び、3回PBS−BSA0.2%で洗浄した。その後、RSMCをPBS−BSA2%で15分間37℃でインキュベートし、プライマリ抗体で37℃30分間インキュベートし、3回PBS−BSA0.2%で洗浄し、PBS−BSA2%で15分間インキュベートした。最後に、細胞をセカンダリ抗体および/または繊維性アクチンの可視化のためのロダミンと結合したファロイジンで染色し、場合によって、DAPI(4’,6−ジアミジノ−2−ヘニリンドロ、ロシュ)を使用して核をラベル化した。
−状態1:ここでは、細胞は、多数のストレス繊維および非分極細胞形により特徴付けられた未刺激細胞の典型的な外観を示す。
−状態2:ここでは、RSMCが低ストレス繊維含有量、膜波うち、アクチンセミリング、または延長形を示す。
2cm2ウェルのガラスカバースリップで成長した、RSMCの密集培養物をPBSで1回洗浄し、血清フリーDMEMで24時間FCS飢餓にした。その後、損傷を刺激するために、単層の中央領域にペプチドのチップで単線を形成した。このように処理した単層をPBSで1回洗浄し、HMGB1(100ng/ml)で補助したまたは補助しない血清フリー培地で48時間再生した。その後、細胞を固定し、TRITCファロイジンで染色した。移動の定量化を低倍率の写真にとり、細胞の無い空間に移動した細胞数を係数することにより行った。データは平均値±SDを表し、100%の値は刺激の無い状態で移動した細胞の数(基礎移動)に相当する。
図4に示すように、HMGB1刺激は5−2−倍だけ移動細胞の数を増加する。ボックスAおよびボックスB(10ng/ml)も試験して、両方共細胞移動を1.8−倍を刺激する。最終的に、bFGF(50ng/ml)との比較により、上記分子がより効果的であることを強調される。損傷の治癒が走化性および化学運動性の同じ信号伝達経路に基づくことを仮定可能である。
後で、信号伝達経路を検出した。移動信号として作用するために、HMGB1は応答細胞の膜に到達してリセプタに結合する必要がある。HMGB1がRSMCの表面に結合するかどうかを試験するために、百万の細胞をトリプシン処理し、20分間4℃で、ボックスA+Bペプチド800ngおよび5μgBSA含有PBS中でインキュベートした。ボックスA+ボックスBポリペプチドは内皮全長HMGB1より僅かに小さく、したがって、SDS−PAGEゲルで容易に区別できる。その後、細胞はペレット化され、上澄みは保存された。500μlの冷いPBSで2回洗浄した後、細胞をSDS−PAGEサンプルバッファー中に再懸濁し、100℃で5分間加熱し、12%のトリシン−SDSゲルに置いた(ラインP)。隣に20μlの上澄みを置いた(ラインS)。その後、ゲルをイモビロンフィルタにブロットし、インディアインクで染色した。
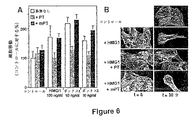
多くの化学誘導物質が、蛋白質(G蛋白質)に結合するヘテロ三量体のGTPに結合した膜レセプタを介して作用することを知るために、G蛋白質がHMGB1信号伝達に関連するかどうかを試験した。百日咳毒素が特異的サブクラスのG蛋白質すなわちGi/o蛋白質を阻害し、信号伝達経路における関与を明らかにするので、百日咳毒素(PT)を使用した(Baggiolini等、1994年、Adv.Immunol.,55:97−179;Haribabu等、1999年、.Biol.Chem.,274:37087−37092)。mPTつまりPTの不活性変異体をコントロールとして使用し、RSMCをPTまたはmPT(50ng/ml)で6時間前処理し、HMGB1(100ng/ml)、ボックスAまたはボックスB(10ng/ml)で30分間刺激した。走化性アッセイを前記のように行った。データは平均値±SDを表し、100%値は刺激剤の無い状態における基礎移動に相当する。図6−Aにおいて、HMGB1誘導走化性におけるPTの阻害効果を示す。これらのデータは、HMGB1により制御された信号伝達経路におけるGi/o蛋白質の関与を示唆する。図6−Bにおいて、細胞骨格再組織化を示す。アクチンフィラメントを前記にように可視化した。その後、HMGB1誘導信号伝達がMAPキナーゼ経路を含むかどうかを研究した。事実、これらの蛋白質はRAGEにより活性化され、細胞内運動性機構の調製に直接役割を果たすことが知られている。RSMCをPD98059(50mM)で1時間前処理するかまたは前処理せず、子牛胸腺(100ng/ml)からのHMGB1で30分間刺激し、リン酸化ERK1/2(ニューイングランドバイオラボズ、Beverly、MA)およびDAPIに対する特異的抗体で染色した。細胞の別のサンプルをTRITCファロイジンで染色し、細胞骨格の再組織化を可視化した。図7では、30分間で、いかにしてHMGB1刺激がRSMCにおいてERK1/2蛋白質の活性化を誘導するか、および核転移を誘導するか、逆に、リン酸化ERK蛋白質が殆ど検出されず、未刺激のRSMCの細胞質に位置するかを示す。さらに、PD98059,MEKの選択的阻害剤、ERKの上流レギュレータはHMGB1誘導ERKリン酸化および核転移ならびにRSMC移動および細胞骨格再組織化を阻害する。したがって、これらのデータはMAPキナーゼ経路がHMGB1誘導細胞移動において本質的な役割を果たしていることを示す。
技術状態を考慮して、ネクロシスを受ける損傷細胞が細胞外培地中にHMGB1を放出できるかどうかを検出した。
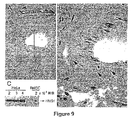
5μMのイオノマイシン(シグマ)および20μMのCCCP、またはmMデオキシグルコースおよび10mMアジ化ナトリウムで処理することにより、HeLa細胞およびHUVECを誘導してネクロシスさせた。37℃で16時間後、ネクロシスを受けた細胞の数を形態学的に記録し、50%に達したとき、上澄みを集めた。
免疫蛍光分析のため、細胞を4%PFAで固定し、抗HMGB1抗体でインキュベートし、セカンダリ抗体およびDAPIで染色した。細胞の透過化処理を、PBS中0.1%NP−40を使用して行った。
図8−Aにおいて、上澄み中の蛋白質および細胞ペレットのウェスタンブロット分析を表し、HMGB1をネクロシス細胞および損傷細胞の両方の上澄み中で回収した。図8−Bにおいて、シングルリビングおよびネクロシスHeLaにおいて実施された免疫蛍光アッセイを示す。HMGB1はネクロシス細胞の残物に結合しない。
結論として、上記の実験データつまり本発明の基礎は、核HMGB1蛋白質が、機構的損傷および/または炎症後に生じる血管再構築の強い媒介物であることおよび損傷またはネクロシス細胞により受動的に放出されうることを示す。
特に、これらのデータは以下のことを示唆する。
HMGB1は走化性アッセイおよび損傷アッセイにおけるbFGFまたはfMLPとして強力な化学誘導物質であり、プロ−ウロキナーゼでの観察に類似した細胞形および細胞骨格組織化の変化を促進する。これらの効果は特にHMGB1に起因し、潜在的な汚染物質に起因しない。さらに、HMGB1に対する抗体は、細胞移動における効果を阻害するが、非特異的コントロール抗体はそのようにはできない。
上記報告の実験は、RAGEがRSMCにおいて発現されること、および抗RAGE抗体がRSMCにおけるHMGB1の効果を阻害することを示す。
MAPキナーゼがRSMCのHMGB1誘導細胞移動に関与することが確認された。その理由は、ERK1/2がリン酸化されHMGB1刺激において細胞核に転位され、MEK阻害剤PD98059がHMGB1誘導細胞移動を遮断できるからである。さらに、データは、Gi/o蛋白質がHMGB1により活性化される工程に関与することも示す。その理由は、HMGB1誘導細胞移動はBordetella百日咳毒素により遮断され得るからである。G蛋白質は通常、7−膜貫通型−エリックスレセプタ(7TM)に結合するが、現時では、RAGEとG蛋白質の間の直接の関係は説明されていない。これまで、HMGB1がRAGEに加えて7TMレセプタ/G蛋白質レセプタに結合するために必要であるか、G蛋白質がRAGEの下流でまたはフィードバック機構で関与するかが知られている。
細胞が機械的に損傷を受けるかまたはネクロシスを受けるとき、HMGB1は非調整的な態様で放出される。これは、サイトカインまたはリポ多糖体で刺激した際を意味する。こうして、HMGB1はパラクリンの態様で近傍の細胞に個々の細胞の損傷または破壊を信号伝達することができる。細胞外HMGB1に応答する細胞はHMGB1を殆ど含まないことが明らかであり、核内には殆どない。RSMCはHeLa細胞または内皮細胞と比較してHMGB1を殆ど含まず、殆ど含まれないHMGB1は主には細胞質に存在する。移動性RSMCは細胞のリーディングエッジにおいて表面上にHMGB1を濃縮する傾向がある。移動性細胞のリーディングエッジにおけるHMGB1の濃縮により近傍細胞のHMGB1誘導応答を呼び起こす。つまり、インテグリン、ウロキナーゼレセプタまたはc−Src等の細胞移動に関与する分子の再配置は、運動性RSMCの特徴である。移動は細胞外プロテアーゼの活性化を伴い、HMGB1およびプラスミノーゲン活性化システム間の相互作用は細胞外マトリックス内で細胞移動を促進し得る。
HMGB1に対する平滑筋細胞の応答性、内皮細胞は多量のHMGB1を含むが、血管SMCは殆ど含まないという観察、および機械的損傷を受ける細胞からのHMGB1の放出、上記これらの全結果はアテローム性動脈硬化症および再狭窄において生じる組織再構築の間におけるHMGB1の潜在的な役割を示す。
本発明の目的である、HMGB1およびRAGEレセプタ間の相互作用を阻害できる分子の同定が可能な上記特別な実験結果は、分子の構造的なおよび機能的な特徴を考慮し、以下のとおりである。
1.HMGB1アンタゴニスト:HMGB1フラグメント、HMGボックス類似体、完全な全長分子よりもより効果的である、およびHMGボックスドメイン含有蛋白質、最後の2つは両方ともRAGEレセプタに結合可能である。
2.HMGB1阻害剤:分子、抗体または抗体フラグメントおよび4方向DNA、HMGボックスボメインに結合し、かつHMGB1がRAGEに結合するのを回避する。
これらの分子は、脈管形成後に生じる事象を含む、血管上皮損傷後のアテローム性動脈硬化症および/または再狭窄を防止するか、遅らせるか、または最小限にする薬理的調製用に有利に使用される。
本発明の付加的な目的は、繊維芽細胞移動を促進および/または誘導し、その結果積極的に結合組織再生成を調整する治療的薬剤の調製のために、HMGB1、HMGボックスに対応するHMGB1フラグメント、HMGボックスファミリーに属する他の蛋白質のHMGボックスドメイン、およびHMGボックスファミリーの他の蛋白質の使用である。
走化性アッセイは周知のプロトコルを使用して実施される(Degryse等、1999年、Blood、94:649−662)。0.5μmポアサイズ(Corning,Acton,MA)を有するフィルタを具えた変法ボイデンチャンバーを使用して、コラーゲンI(0.5Mの酢酸中の100μg/ml)およびフィブロネクチン(10μg/ml)(Roche)を処理した。マウス胎児繊維芽細胞を周知のプロトコルにしたがって培養した(Calogero等、1999年、Nat.Genet.,22:276−280)および24時間の血清飢餓の後、20.000−40.000細胞のサンプルをボイデンチャンバーの上方ウェルに添加した。E.coli発現組換えHMGB1を同じ血清フリー培地に希釈し、下方ウェルに添加した。
37℃で一晩中細胞移動をさせた。その後、フィルタの上方表面に残る細胞を書き取り、フィルタをメタノール中で固定し、20%メタノール中10%のクリスタルバイオレットの溶液中で染色した。全実験を少なくとも2回、三重に行った。
HMGB1への繊維芽細胞の応答性は、外傷または外科手術に起因する損傷の後生じる結合組織再構築の間、HMGB1の潜在的な役割を指摘する。さらに、抗RAGE抗体が前記応答を遮断する事実は細胞表面上のRAGEレセプタおよびHMGB1間の相互作用がHMGB1に対する繊維芽細胞感受性へ至る基本的な事象であることを示す。
−HMGB1および/またはHMGボックスに対応するHMGB1フラグメント、HMGボックスファミリーにおよびHMGボックスファミリーの他の蛋白質に属する他の蛋白質のHMGボックスドメインは、結合組織再生成を積極的に調節、すなわち促進および/または誘導する薬理的調製のために有利に使用される。
−アンタゴニストグループに属する、(RAGEレセプタに結合可能)、阻害剤グループに属する、(すなわち、RAGEレセプタにHMGボックスドメインブロッキングHMGB1結合を結合可能)HMGB1およびRAGE間の相互作用を阻害できる各種類の分子は、結合組織再生成を調製、すなわち遮断、遅延、または減少する薬理的調製のために有利に使用される。
Claims (6)
- 動脈の狭窄または再狭窄の処置のための治療上の薬剤の調製のための分子の使用であって、分子は、HMGB1に対する抗体、またはHMGB1に対する抗体のフラグメントであって、HMGB1タンパク質の活性をその受容体上でブロックするもの、またはHMGB1フラグメントであって、HMGB1と受容体結合において競合し、受容体活性を抑制するもので、HMGボックスドメインAのaa(アミノ酸)の1−90、HMGボックスドメインBのaaの91−180、およびHMGボックスドメインAまたはHMGボックスドメインBに対して15よりも多くの連続的なアミノ酸残基のための配列同一性を有する任意のポリペプチドを備えるHMGB1フラグメントからなる群より選ばれる、分子の使用。
- 動脈の狭窄または再狭窄は血管形成の後に起こる、請求項1記載の分子の使用。
- 分子はカテーテル、外科用器具およびステントからなる群より選ばれる器具から放出される、請求項1記載の分子の使用。
- 結合組織の再構築および創傷治癒を増進する治療上の薬剤の調製のための、次の、HMGB1および/またはHMGB1フラグメントであって、HMGB1と受容体結合において競合し、受容体活性を抑制するもので、HMGボックスドメインAのaa(アミノ酸)の1−90、HMGボックスドメインBのaaの91−180、およびHMGボックスドメインAまたはHMGボックスドメインBに対して15よりも多くの連続的なアミノ酸残基のための配列同一性を有する任意のポリペプチドを備えるHMGB1フラグメントの使用。
- 創傷および/または火傷および/または床ずれの治癒を含む結合組織の再構築を減らす治療上の薬剤の調製のための、次の、HMGB1に対する抗体、またはHMGB1に対する抗体のフラグメントであって、HMGB1タンパク質の活性をその受容体上でブロックするもの、またはHMGB1フラグメントであって、HMGB1と受容体結合において競合し、受容体活性を抑制するもので、HMGボックスドメインAのaa(アミノ酸)の1−90、HMGボックスドメインBのaaの91−180、およびHMGボックスドメインAまたはHMGボックスドメインBに対して15よりも多くの連続的なアミノ酸残基のための配列同一性を有する任意のポリペプチドを備えるHMGB1フラグメントの使用。
- 結合組織の再構築を増進する治療上の薬剤の調製のための、次の、HMGB1および/またはHMGB1フラグメントであって、HMGB1と受容体結合において競合し、受容体活性を抑制するもので、HMGボックスドメインAのaa(アミノ酸)の1−90、HMGボックスドメインBのaaの91−180、およびHMGボックスドメインAまたはHMGボックスドメインBに対して15よりも多くの連続的なアミノ酸残基のための配列同一性を有する任意のポリペプチドを備えるHMGB1フラグメントの使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IT2001MI000562A ITMI20010562A1 (it) | 2001-03-16 | 2001-03-16 | Inibitori o antagonisti della proteina hmg1 per il trattamento di disordini vascolari |
| ITMI2001A000562 | 2001-03-16 | ||
| PCT/IT2002/000153 WO2002074337A1 (en) | 2001-03-16 | 2002-03-12 | Hmgb1 protein inhibitors and/or antagonists for the treatment of vascular diseases |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2004523579A JP2004523579A (ja) | 2004-08-05 |
| JP2004523579A5 JP2004523579A5 (ja) | 2005-08-18 |
| JP4822654B2 true JP4822654B2 (ja) | 2011-11-24 |
Family
ID=11447291
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002573044A Expired - Fee Related JP4822654B2 (ja) | 2001-03-16 | 2002-03-12 | 血管疾患治療用hmgb1蛋白質インヒビタおよび/またはアンタゴニスト |
Country Status (15)
| Country | Link |
|---|---|
| US (4) | US7754217B2 (ja) |
| EP (1) | EP1368060B1 (ja) |
| JP (1) | JP4822654B2 (ja) |
| CN (2) | CN101773669A (ja) |
| AT (1) | ATE468137T1 (ja) |
| AU (1) | AU2002247977C1 (ja) |
| CA (1) | CA2439530C (ja) |
| DE (1) | DE60236413D1 (ja) |
| DK (1) | DK1368060T3 (ja) |
| ES (1) | ES2346408T3 (ja) |
| HK (1) | HK1069316A1 (ja) |
| IT (1) | ITMI20010562A1 (ja) |
| MX (1) | MXPA03008364A (ja) |
| PT (1) | PT1368060E (ja) |
| WO (1) | WO2002074337A1 (ja) |
Families Citing this family (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6303321B1 (en) | 1999-02-11 | 2001-10-16 | North Shore-Long Island Jewish Research Institute | Methods for diagnosing sepsis |
| US7151082B2 (en) | 1999-02-11 | 2006-12-19 | The Feinstein Institute For Medical Research | Antagonists of HMG1 for treating inflammatory conditions |
| ITMI20010562A1 (it) * | 2001-03-16 | 2002-09-16 | Marco E Bianchi | Inibitori o antagonisti della proteina hmg1 per il trattamento di disordini vascolari |
| US7220723B2 (en) | 2001-05-15 | 2007-05-22 | The Feinstein Institute For Medical Research | Inhibitors of the interaction between HMGB polypeptides and toll-like receptor 2 as anti-inflammatory agents |
| US7304034B2 (en) | 2001-05-15 | 2007-12-04 | The Feinstein Institute For Medical Research | Use of HMGB fragments as anti-inflammatory agents |
| BR0209689A (pt) * | 2001-05-15 | 2006-02-07 | Long Island Jewish Res Inst | Uso de fragmento de hmg como agente anti-inflamatório |
| KR20050054907A (ko) | 2002-07-03 | 2005-06-10 | 폰다지오네 센트로 산 라파엘 델 몬테 테이보 | 조직 손상의 치료 및/또는 조직 회복의 촉진에서hmgb1 단백질의 용도 |
| WO2004061456A2 (de) * | 2003-01-03 | 2004-07-22 | Alcedo Biotech Gmbh | Verwendungen von hmgb, hmgn, hmga proteinen |
| US7696169B2 (en) | 2003-06-06 | 2010-04-13 | The Feinstein Institute For Medical Research | Inhibitors of the interaction between HMGB polypeptides and toll-like receptor 2 as anti-inflammatory agents |
| CN1878793A (zh) | 2003-09-11 | 2006-12-13 | 鉴定医疗有限公司 | 拮抗hmgb1的单克隆抗体 |
| ITRM20040058A1 (it) * | 2004-02-03 | 2004-05-03 | Marco E Bianchi | Inibitori ed antagonisti di hmgb1 in grado di regolare la proliferazione delle cellule muscolari lisce ed endoteliali. |
| JP2008504335A (ja) * | 2004-07-02 | 2008-02-14 | クレアビリス・セラピューティクス・エスピーエー | Hmgb1に関連する病変の治療のための核酸 |
| US20090062187A1 (en) | 2004-07-20 | 2009-03-05 | Marco Bianchi | Use of Hmgb1 for Wound Healing |
| MX2007001155A (es) * | 2004-07-29 | 2007-08-14 | Creabilis Therapeutics Spa | Uso de inhibidores de k-252a y de quinasa para la prevencion o el tratamiento de patologias asociadas con hmgb1. |
| BRPI0514835A (pt) * | 2004-09-03 | 2008-06-24 | Creabilis Therapeutics Spa | variante de polipetìdeo de box de domìnio de ligação por alta afinidade de hmbg1 humano e/ou não humano ou de fragmento biologicamente ativo de box-a de hmgb1, molécula de ácido nucléico, uso, composição farmacêutica e dispositivo médico |
| US8129130B2 (en) | 2004-10-22 | 2012-03-06 | The Feinstein Institute For Medical Research | High affinity antibodies against HMGB1 and methods of use thereof |
| CN101132811B (zh) | 2004-10-22 | 2012-05-30 | 米迪缪尼有限公司 | 抗hmgb1的高亲和力抗体及其用法 |
| ITRM20050032A1 (it) * | 2005-01-21 | 2006-07-22 | Marco E Bianchi | Inibitori ed antagonisti di hmgb1 in grado di inibire la patogenesi e la progressione della malattia aterosclerotica. |
| WO2006114805A2 (en) * | 2005-04-28 | 2006-11-02 | Fondazione Centro San Raffaele Del Monte Tabor | Use of hmgb2 and hmgb3 proteins for medical applications |
| EP1909834A2 (en) | 2005-07-18 | 2008-04-16 | Critical Therapeutics, Inc. | Use of hmgb1 antagonists for the treatment of inflammatory skin conditions |
| MX2008002524A (es) | 2005-08-25 | 2008-03-14 | Creabilis Therapeutics Spa | Conjugados polimericos de k-252a y sus derivados. |
| WO2007031100A1 (en) * | 2005-09-14 | 2007-03-22 | Ostini, Marco | Active immunotherapy of life-threatening systemic inflammation |
| WO2007076200A2 (en) | 2005-11-28 | 2007-07-05 | Medimmune, Inc. | Antagonists of hmgb1 and/or rage and methods of use thereof |
| WO2007130725A2 (en) * | 2006-02-06 | 2007-11-15 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Use of hmgb1 for protection against ischemia reperfusion injury |
| US8546547B2 (en) | 2006-09-15 | 2013-10-01 | Creabilis Therapeutics S.P.A. | Polymer conjugates of Box-A of HMGB1 and Box-A variants of HMGB1 |
| WO2008099913A1 (ja) | 2007-02-15 | 2008-08-21 | Kumamoto University | ヒトhmgb-1に特異的に結合する抗体を有効成分として含有する治療剤 |
| RU2519714C2 (ru) | 2008-04-30 | 2014-06-20 | Дженомикс Ко., Лтд. | Средство для вовлечения происходящей из костного мозга плюрипотентной стволовой клетки в периферический кровоток |
| KR20160070169A (ko) | 2008-04-30 | 2016-06-17 | 가부시키가이샤 제노믹스 | 생체내 기능적 세포의 고효율 채취법 |
| WO2011007876A1 (ja) * | 2009-07-16 | 2011-01-20 | Necソフト株式会社 | Hmgb1結合核酸分子およびその用途 |
| JP5467313B2 (ja) | 2009-09-28 | 2014-04-09 | 国立大学法人 岡山大学 | アテローム動脈硬化抑制剤 |
| CA2778759A1 (en) | 2009-10-28 | 2011-05-05 | Genomix Co., Ltd. | Tissue-regeneration promoter using recruitment of bone marrow mesenchymal stem cells and/or pluripotent stem cells in blood |
| AU2011322482B2 (en) | 2010-10-30 | 2017-03-23 | Oxford University Innovation Limited | Treatment for Dupuytren's disease |
| CA2834255C (en) | 2011-04-26 | 2021-11-02 | Genomix Co., Ltd. | Peptide for inducing regeneration of tissue and use thereof |
| US9561274B2 (en) | 2011-06-07 | 2017-02-07 | University Of Hawaii | Treatment and prevention of cancer with HMGB1 antagonists |
| US9244074B2 (en) * | 2011-06-07 | 2016-01-26 | University Of Hawaii | Biomarker of asbestos exposure and mesothelioma |
| AU2013335684B2 (en) | 2012-10-25 | 2017-06-29 | Osaka University | Novel method for treating cardiac infarction using HMGB1 fragment |
| TR201807769T4 (tr) | 2012-10-25 | 2018-06-21 | Genomix Co Ltd | HMGB1 fragmanı kullanılarak spinal kord yaralanmasının tedavi edilmesine yönelik yeni yöntem. |
| AU2013375015A1 (en) | 2013-01-28 | 2015-08-13 | Evec Inc. | Humanized anti-HMGB1 antibody or antigen-binding fragment thereof |
| IL242807A0 (en) | 2015-11-26 | 2016-04-21 | Novamed Ltd | Test facility |
| JP7107839B2 (ja) | 2015-12-11 | 2022-07-27 | ルプレヒト-カールス-ウニベルジテート ハイデルベルク | Pkm2モジュレーター及びhmgb1の組合せ製剤 |
| TWI805565B (zh) | 2017-01-27 | 2023-06-21 | 日商斯德武利姆股份有限公司 | 心肌病、陳舊性心肌梗塞及慢性心臟衰竭的治療藥物 |
| EP3718561A4 (en) | 2017-12-01 | 2021-07-21 | Stemrim Inc. | Therapy for inflammatory bowel disease |
| CN115361966A (zh) * | 2020-04-22 | 2022-11-18 | 朱拉隆功大学 | 使dna恢复活力和防止dna损伤的组合物以及方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997039121A1 (en) * | 1996-04-16 | 1997-10-23 | Schering Aktiengesellschaft | Advanced glycosylation end-product receptor peptides and uses therefor |
| WO1998022138A1 (en) * | 1996-11-22 | 1998-05-28 | The Trustees Of Columbia University In The City Of New York | Method for treating symptoms of diabetes |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6054122A (en) * | 1990-11-27 | 2000-04-25 | The American National Red Cross | Supplemented and unsupplemented tissue sealants, methods of their production and use |
| US5470307A (en) * | 1994-03-16 | 1995-11-28 | Lindall; Arnold W. | Catheter system for controllably releasing a therapeutic agent at a remote tissue site |
| WO1997026913A1 (en) | 1996-01-26 | 1997-07-31 | The Trustees Of Columbia University In The City Of New York | A POLYPEPTIDE FROM LUNG EXTRACT WHICH BINDS AMYLOID-β PEPTIDE |
| US5864018A (en) * | 1996-04-16 | 1999-01-26 | Schering Aktiengesellschaft | Antibodies to advanced glycosylation end-product receptor polypeptides and uses therefor |
| US6303321B1 (en) * | 1999-02-11 | 2001-10-16 | North Shore-Long Island Jewish Research Institute | Methods for diagnosing sepsis |
| US6398808B1 (en) * | 1999-06-15 | 2002-06-04 | Scimed Life Systems, Inc. | Localized delivery of genetic information from biostable materials |
| ITMI20010562A1 (it) * | 2001-03-16 | 2002-09-16 | Marco E Bianchi | Inibitori o antagonisti della proteina hmg1 per il trattamento di disordini vascolari |
| BR0209689A (pt) * | 2001-05-15 | 2006-02-07 | Long Island Jewish Res Inst | Uso de fragmento de hmg como agente anti-inflamatório |
| ITRM20040058A1 (it) * | 2004-02-03 | 2004-05-03 | Marco E Bianchi | Inibitori ed antagonisti di hmgb1 in grado di regolare la proliferazione delle cellule muscolari lisce ed endoteliali. |
| US20090062187A1 (en) * | 2004-07-20 | 2009-03-05 | Marco Bianchi | Use of Hmgb1 for Wound Healing |
| WO2008137552A2 (en) * | 2007-05-02 | 2008-11-13 | Medimmune, Llc | Anti-rage antibodies and methods of use thereof |
-
2001
- 2001-03-16 IT IT2001MI000562A patent/ITMI20010562A1/it unknown
- 2001-03-16 US US10/471,641 patent/US7754217B2/en not_active Expired - Fee Related
-
2002
- 2002-03-12 DE DE60236413T patent/DE60236413D1/de not_active Expired - Lifetime
- 2002-03-12 EP EP02717057A patent/EP1368060B1/en not_active Expired - Lifetime
- 2002-03-12 AT AT02717057T patent/ATE468137T1/de active
- 2002-03-12 AU AU2002247977A patent/AU2002247977C1/en not_active Ceased
- 2002-03-12 DK DK02717057.0T patent/DK1368060T3/da active
- 2002-03-12 WO PCT/IT2002/000153 patent/WO2002074337A1/en active Application Filing
- 2002-03-12 MX MXPA03008364A patent/MXPA03008364A/es active IP Right Grant
- 2002-03-12 PT PT02717057T patent/PT1368060E/pt unknown
- 2002-03-12 CN CN200910252323A patent/CN101773669A/zh active Pending
- 2002-03-12 CA CA2439530A patent/CA2439530C/en not_active Expired - Fee Related
- 2002-03-12 JP JP2002573044A patent/JP4822654B2/ja not_active Expired - Fee Related
- 2002-03-12 ES ES02717057T patent/ES2346408T3/es not_active Expired - Lifetime
- 2002-03-12 CN CN028065670A patent/CN1537014B/zh not_active Expired - Fee Related
-
2005
- 2005-03-02 HK HK05101837.0A patent/HK1069316A1/xx not_active IP Right Cessation
-
2008
- 2008-01-02 US US11/968,506 patent/US8058239B2/en not_active Expired - Fee Related
-
2010
- 2010-02-17 US US12/707,264 patent/US20100297107A1/en not_active Abandoned
- 2010-02-17 US US12/707,222 patent/US20100172896A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997039121A1 (en) * | 1996-04-16 | 1997-10-23 | Schering Aktiengesellschaft | Advanced glycosylation end-product receptor peptides and uses therefor |
| WO1998022138A1 (en) * | 1996-11-22 | 1998-05-28 | The Trustees Of Columbia University In The City Of New York | Method for treating symptoms of diabetes |
Also Published As
| Publication number | Publication date |
|---|---|
| US8058239B2 (en) | 2011-11-15 |
| ITMI20010562A1 (it) | 2002-09-16 |
| ES2346408T3 (es) | 2010-10-15 |
| EP1368060A1 (en) | 2003-12-10 |
| CN1537014B (zh) | 2012-04-25 |
| JP2004523579A (ja) | 2004-08-05 |
| US20100297107A1 (en) | 2010-11-25 |
| WO2002074337A1 (en) | 2002-09-26 |
| AU2002247977B2 (en) | 2006-12-14 |
| US20100172896A1 (en) | 2010-07-08 |
| ATE468137T1 (de) | 2010-06-15 |
| US20040136979A1 (en) | 2004-07-15 |
| AU2002247977B8 (en) | 2007-03-15 |
| AU2002247977A2 (en) | 2004-02-26 |
| CN1537014A (zh) | 2004-10-13 |
| DE60236413D1 (de) | 2010-07-01 |
| WO2002074337A8 (en) | 2003-08-28 |
| US20080171052A1 (en) | 2008-07-17 |
| AU2002247977A1 (en) | 2002-10-03 |
| CN101773669A (zh) | 2010-07-14 |
| DK1368060T3 (da) | 2010-08-30 |
| MXPA03008364A (es) | 2004-11-12 |
| EP1368060B1 (en) | 2010-05-19 |
| AU2002247977C1 (en) | 2008-09-18 |
| HK1069316A1 (en) | 2005-05-20 |
| PT1368060E (pt) | 2010-08-24 |
| CA2439530A1 (en) | 2002-09-26 |
| CA2439530C (en) | 2016-11-08 |
| US7754217B2 (en) | 2010-07-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4822654B2 (ja) | 血管疾患治療用hmgb1蛋白質インヒビタおよび/またはアンタゴニスト | |
| Degryse et al. | The high mobility group (HMG) boxes of the nuclear protein HMG1 induce chemotaxis and cytoskeleton reorganization in rat smooth muscle cells | |
| JP4819364B2 (ja) | 線維細胞形成阻害の検出方法、ならびに線維細胞形成を増強する方法および化合物 | |
| Gowen et al. | Selective adhesion of macrophages to denatured forms of type I collagen is mediated by scavenger receptors | |
| US20090214549A1 (en) | Antigenic Epitopes Of Inteleukin-21, Related Antibodies And Their Use In Medical Field | |
| JPH06500555A (ja) | 病気の処置のためのペプチドの薬物 | |
| Chen et al. | Interleukin-17 induces angiogenesis in human choroidal endothelial cells in vitro | |
| JP2002539174A (ja) | 癌および血管新生関連の疾病の治療のためのldl様受容体リガンドを使用する組成物および方法 | |
| JP2008537877A (ja) | Rage/diaphanous相互作用および関連する組成物および方法 | |
| Ambort et al. | Specific processing of tenascin-C by the metalloprotease meprinβ neutralizes its inhibition of cell spreading | |
| US7824868B2 (en) | Formation of superfibronectin by BBK32 and uses therefor | |
| US10837007B2 (en) | Recombinant fusion proteins for preventing or treating adhesions of tissues or organs | |
| Das et al. | Evidence for binding of the ectodomain of amyloid precursor protein 695 and activated high molecular weight kininogen | |
| JPWO2005068504A1 (ja) | 炎症性サイトカイン抑制剤 | |
| ES2362655T3 (es) | Métodos y composiciones para suprimir la diferenciación de fibrocitos. | |
| Héry-Huynh et al. | Induction and regulation of murine emphysema by elastin peptides 2 | |
| TW200927162A (en) | Pharmaceutical compositions for treating diseases associated with angiogenesis and inflammation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050223 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080513 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080731 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080807 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081113 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20081114 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091124 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100223 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100302 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100323 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100423 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20100426 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20110125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110125 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110510 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110726 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110816 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110906 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140916 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |