JP4734498B2 - タンパク質−タンパク質相互作用を解析する方法 - Google Patents
タンパク質−タンパク質相互作用を解析する方法 Download PDFInfo
- Publication number
- JP4734498B2 JP4734498B2 JP2006518902A JP2006518902A JP4734498B2 JP 4734498 B2 JP4734498 B2 JP 4734498B2 JP 2006518902 A JP2006518902 A JP 2006518902A JP 2006518902 A JP2006518902 A JP 2006518902A JP 4734498 B2 JP4734498 B2 JP 4734498B2
- Authority
- JP
- Japan
- Prior art keywords
- protein
- protease
- sequence encoding
- nucleotide sequence
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6845—Methods of identifying protein-protein interactions in protein mixtures
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1055—Protein x Protein interaction, e.g. two hybrid selection
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/94—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving narcotics or drugs or pharmaceuticals, neurotransmitters or associated receptors
- G01N33/9406—Neurotransmitters
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/72—Assays involving receptors, cell surface antigens or cell surface determinants for hormones
- G01N2333/726—G protein coupled receptor, e.g. TSHR-thyrotropin-receptor, LH/hCG receptor, FSH
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Description
本発明は、対象分子間の相互作用を測定するための方法に関する。詳しくは、本発明は、細胞内におけるレポーター遺伝子の活性化を測定することによって、前記検定化合物と称される特定の物質が、二つ以上の特定の対象タンパク質間の相互作用を調節するか否かの測定に関し、ここで、前記調節又はその不在から、前記活性化、又はその欠如が起こる。前記測定は、トランスフォーム細胞又はトランスフェクション細胞を使用して行われ、これらのトランスフォーム細胞及びトランスフェクション細胞、更に、それらをトランスフォーム又はトランスフェクトするのに使用される薬剤も本発明の特徴を構成する。
レセプターのリガンドの同定によって例示される、タンパク質/タンパク質相互作用の研究が非常に注目されている。所与のレセプターに対する1つ又は複数のリガンドが既知であるとしても、より効果的な、又はより選択性の高いリガンドを同定することには利益がある。以下、このような方法で研究することが可能なクラスのタンパク質の非限定的具体例としてGPCRについてここでは説明する。
TM/LNB−7TMレセプター、アディポネクチンレセプター及びそれに関連のレセプター、及び、嗅覚、味覚、鋤鼻及びフェロモン関連レセプターを含む化学感受性レセプター、を含む。例として、ヒトのGPCRスーパーファミリーは、非限定的に、Vassilatisほか Proc. Natl. Acad. Sci. USA, 100:4903-4908(2002)、タケダ(Takeda)ほか, FEBS Letters, 520:97-101 (2002)、フレデリックソン(Fredricksson)ほか, Mol. Pharmacol., 63:1256-1272(2003); グルスマン(Glusman)ほか, Genome Res., 11:685-702
(2001); 及びゾズーリャ(Zozulya)ほか, Genome Biol., 2:0018.1-0018.12(2001)、を含み、これらの全てをここに参考文献として合体させる。
R、又、その他のシグナル伝達因子を発現する。その結果、測定される作動経路は、標的GPCRの他に、他の内在性分子によっても調節されるかもしれず、それによって誤った結果を導く可能性がある。
)、は、GPCRシグナルの終結をもたらすその他の活性を検討している。これらの終結プロセスは、過剰な細胞刺激を防止し、細胞外シグナルとそれに対応する細胞内経路との間の一時的な連鎖を強制する。
を測定するために、細胞の高解像度撮像に依存している。これが複雑な入れ込んだ手続きであることを当業者は認識するであろう。
れる本発明を教示、示唆するものではない。
従って、本発明によれば、検定化合物が対象の特定のタンパク質/タンパク質相互作用を調節するか否かを測定するための方法が提供され、この方法は、前記化合物を、(i)第1検定タンパク質をコードするヌクレオチド配列と、(ii)プロテアーゼ又はプロテアーゼの一部のための開裂部位をコードするヌクレオチド配列と、(iii)前記細胞内においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、とを含む核酸分子(a)と、(i)前記検定化合物の存在下における前記第1検定タンパク質に対するその相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列と、(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、とを含む核酸分子(b)とでトランスフォーム又はトランスフェクトされた細胞に接触させる工程と、前記レポーター遺伝子の活性を、前記化合物が前記タンパク質/タンパク質相互作用を調節するか否かの測定として、測定する工程とを含む。
の実施例及びその多数の具体的詳細を示すものではあるが、これは限定のためではなく例示のために提供されているものである、ということが理解されるべきである。本発明の本質から逸脱することなく、本発明の範囲内において、多くの置換、変更、追加および/又は再構成が可能であり、本発明は、そのような置換、変更、追加および/又は再構成を含むものである。
以下の図面は、本明細書の一部を形成するものであり、かつ、本発明のいくつかの態様を例示することを意図したものである。本発明は、これらの図面の1つ又は複数をここに提供される具体的実施例の詳細説明と共に参照することによってより良く理解されるであろう。
本発明は、対象物質が、レセプター、例えば、膜貫通レセプター等の膜結合タンパク質などの第1検定タンパク質と、アレスチンファミリーのメンバーなどの第2検定タンパク質との相互作用を調節するか否かを測定するための方法に関する。この方法は、真核細胞又は原核細胞とすることができる細胞を、二つの構造物によってコトランスフォーム又はコトランスフェクトすることを含む。前記第1構造物は、(i)膜貫通レセプターなどの前記第1検定タンパク質と(ii)プロテアーゼの開裂部位、をコードする配列、そして(iii)レポーター遺伝子を活性化するタンパク質をコードする配列とを含む。前記第2構造物は、(i)前記第1検定タンパク質とのその相互作用が測定される及び/決定される第2検定タンパク質をコードする配列、そして(ii)前記第1構造物の一部である
前記開裂部位に対して作用するのに十分な、プロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、を含む。特に好適な実施例において、これらの構造物は、細胞内に安定的に取り込まれる。
「ベクター」という用語は、そこでそれが複製することが可能な細胞への導入のために
その中に核酸配列を挿入することが可能なキャリア核酸分子を称するのに使用される。核酸配列は、「外来性」であることができ、これは、それが、その中にベクターが導入される前記細胞に対して異質であること、又は、前記配列が細胞内の配列に対しては同質であるが、宿主細胞核酸内の、その配列が通常は見られない位置にある、ということを意味する。ベクターは、プラスミド、コスミド、ウイルス(バクテリオファージ、動物ウイルス、及び植物ウイルス)、及び人工染色体(例えば、YAC)を含む。当業者は、標準組換え技術(例えば、マニアティス(Maniatis)ほか, Molecular Cloning, A Laboratory Manual(Cold Spring Harbor, 1990)及びオースベル(Ausubel)ほか, 1994, Current Protocols In Molecular Biology(John Wiley & Sons, 1996)ともにここに参考文献として合体させる)によって十分にベクターを構築することができるであろう。
々な適当な培地で成長させることができる。ある種のベクター中における前記組換えタンパク質の発現は、当業者によって理解されるように、宿主細胞を、ある種のプロモーターに対して特異的な物質に接触させることによって、例えば、IPTGを培地に添加することや、インキュベーションをより高い温度に切り替える、等、によって誘発させることができる。前記細菌を、更に追加時間、一般に、2時間から24時間、培養した後、前記細胞を、遠心分離によって収集し、残滓の培地を除去するために洗浄する。
文献として合体させる米国特許第5,871,986及び4,879,236号に記載され、例えば、INVITROGEN(登録商標)からMAXBAC(登録商標)2.0という名前で、そして、CLONTECH(登録商標)からBACKPACK(登録商標) BACULOVIRUS EXPRESSION SYSTEMという名前で購入することが可能な、昆虫細胞/バキュロウイルスシステムによって、異種核酸セグメントの高レベルのタンパク質発現を作り出すことが可能である。
能発現システムのもう1つの例は、INVITROGEN(登録商標)から入手可能であり、これは、T−REX(登録商標)(テトラサイクリン調節発現)システム、全長CMVプロモーターを使用する誘導可能哺乳動物発現システム、を坦持している。INVITROGEN(登録商標)は、更に、Pichia methanolica発現システムと呼ばれる酵母発現システムを提供しており、これは、メチロトローフ酵母、Pichia methanolica中での組換えタンパク質の高レベル産生用に構成されている。当業者は、核酸配列又は、その同族のポリペプチド、タンパク質、又はペプチド、を作り出すためにいかにして、発現構造物等のベクターを発現させるかを理解するであろう。
前記構造物は、プロモーター、ポリA配列、等の追加の5’および/又は3’要素を含むことができる。これらの要素は、宿主細胞由来、即ち、宿主細胞と同種のものとすることができ、或いは、それらは、別の源由来、即ち、異種のものとすることができる。
とが可能であろう。T3,T7又はSP6細胞質発現システムの使用がもう一つの可能な実施例である。真核細胞は、もしも、適切な細菌ポリメラーゼが、送達複合体の一部として、又は追加の遺伝子発現構造物として、提供されるのであれば、ある種の細菌プロモーターからの細胞質転写を支援することができる。
’メチル化Cap依存翻訳のリボソーム走査モデルを迂回して、内部部位で翻訳を開始することができる(ペルティエ(Pelletier)およびソーネンバーグ(Sonenberg), Nature, 334:320-325 (1988))。ピコルナウイルスファミリーの二つのメンバー(ポリオと
脳心筋炎)からのIRES要素が、哺乳動物メッセージからのIRES(マセジャック(Macejak)およびサーノウ(Sarnow), Nature, 353:90-94 (1991))1991)と共に、記
載されている((ペルティエ(Pelletier)およびソーネンバーグ(Sonenberg)、上述)。IRES要素は、異種オープンリーディングフレームに結合させることができる。それぞれがIRESによって分離された、複数のオープンリーディングフレームを同時に転写して、多シストロン性メッセージを作り出すことができる。IRES要素の性質により、各オープンリーディングフレームは、効率的な翻訳のためにリボソームにアクセス可能である。1つのメッセージを転写するために1つのプロモーター/エンハンサーを使用して、複数の遺伝子を効率的に発現させることができる(それぞれをここに参考文献として合体させる米国特許第5,925,565及び5,935,819号を参照)。
ベクターは、マルチクローニング部位(MCS)を含むことができ、これは、そのいずれもが、ベクターを消化するための標準組換え技術で連結可能な複数の制限酵素部位を含んでいる核酸領域である(例えば、ここに参考文献として合体させるカーボネッリ(Carbonelli)ほか, FEMS Microbiol. Lett. 172 (1): 75-82 (1999), レヴェンソン(Levenson)ほか, Hum. Gene Ther. 9(8): 1233-1236(1988)及びコセア(Cocea), Biotechniques, 23(5): 814-816(1997)を参照)。「制限酵素消化」とは、核酸分子内の特定の位置においてのみ作用する酵素による、核酸分子の触媒作用的な開裂をいう。これらの制限酵素の多くは、市販されている。そのような酵素の使用は当業者によって広く理解されている。多くの場合、ベクターは、外来性配列をベクターに結合させることを可能にするためにMCS内で切断する制限酵素を使用して、線形化(linearized)又は断片化される。「連結(ligation)」とは、互いに対して隣接、又は隣接しないものとすることが可能な、二つの核酸フラグメント間にリン酸ジエステル結合を形成するプロセスをいう。制限酵素と連結反応に関連する技術は、組換え技術の当業者にとって周知である。
最小化するように作用することができる。
本発明で使用される核酸送達のための適当な方法は、それによって、核酸分子(例えばDNA)を、ここに記載されているように、又は、当業者に知られているように、細胞に導入することが可能な実質的に全ての方法を含むものと考えられる。そのような方法は、非限定的に、生体外(ex vivo)トランスフェクション(ウィルソン(Wilson)ほか, Science, 244:1344-1346(1989), ナベル(Nabel)ほか, Science, 244:1342-1344(1989), 微量注入(ハーラン(Harlan)およびウェイントラウブ(Weintraub), J. Cell Biol,
101(3): 1094-1099 (1985); 米国特許第5,789,215号、ここに参考文献と
して合体させる)を含む、注入(ここにそのそれぞれを参考文献として合体させる、米国特許第5,994,624,5,981,274,5,945,100,5,780,448,5,736,524,5,702,932,5,656,610,5,589,466及びNo.5,580,859ッ号)、エレクトロポーレーション(米国特許第5,384,253号、ここに参考文献として合体させる; トゥル‐カパ(Tur-Kapa)ほか, Mol. Cell Biol., 6:716-718(1986); ポッター(Potter)ほか, Proc. Natl. Acad. Sci. USA, 81:7161-7165(1984)、リン酸カルシウム沈殿(グラハム(Gr aham)およびフ
ァン・デア・エブ(Van Der Eb); Virology, 52: 456-467(1973); Chen(チェン)及
びOkayama(オカヤマ), Mol. Cell Biol., 7(8): 2745-2752(1987); リッペ(Rippe)ほか, Mol. Cell Biol., 10:689-695(1990); DEAEデキストラン、その後にポリ
エチレングリコールの使用(ゴパル(Gopal), Mol. Cell Biol., 5:1188-190(1985)、直接音波装填(direct sonic loading)(フェッチハイマー(Fechheimer)ほか, Proc. Natl. Acad. Sci. USA, 89(17): 8463-8467(1987); リポソーム媒介トランスフェク
ション(ニコラウ(Nicolau)およびセネ(Sene), Biochem. & Biophys. Acta., 721:185-190 (1982); フラレー(Fraley)ほか, Proc. Natl. Acad. Sci, USA, 76:3348-3352
(1979); ニコラウ(Nicolau)ほか, Meth. Enzym., 149:157-176(1987); ワン(Wong)ほか, Gene, 10:879-894 (1980); カネダ(Kaneda)ほか, Science, 243:375-378 (1989); カトウ(Kato)ほか, J. Biol. Chem.,266: 3361-3364 (1991)及びレセプター媒介トランスフェクション(ウー(Wu)およびウー(Wu), J. Biol. Chem., 262: 4429-4432 (1987); ウー(Wu)およびウー(Wu), (1988); プロトプラストのPEG−
媒介トランスフォーメーション(オミラレー(Omirulleh)ほか, Plant Mol. Biol., 21
(3): 415-428(1987)、米国特許第4,684,611及び4,952,500号、そのそれぞれをここに参考文献として合体させる)、乾燥/抑制媒介DNA取り込み(desiccation/inhibition-mediated DNA uptake)(ポトリカス(Potrykus)ほかMol. Gen. Genet., 199(2): 169-177(1985)およびこれらの方法の任意の組み合わせ、のようなDNAの直接送達を含む。
ここに記載の方法と同様、本発明の特徴である生産物も好適実施例を有する。例えば、「三部構造物」即ち、検定タンパク質と、開裂部位と活性化タンパク質とをコードする配列を含む構造物、において、前記検定タンパク質は、好ましくは、GPCRファミリーのメンバーなどの膜貫通レセプターなどの膜結合タンパク質である。これらの配列は、それらがコードするタンパク質のC末端を、第2タンパク質に対するより良好で強力な相互作用を有するように改変することができる。そのような改変は、例えば、GPCRなどの前記検定タンパク質のC末端領域を、全てを前に定義した、AVPR2,AGTRLI,GRPR,F2PLI,CCR4、CXCR2/IL−8,CCR4又はGRPRのC末端コード領域で置換することを含む。
アレスチンファミリーのメンバーが好適であるが、特に前記第1タンパク質がGPCRでない場合には、他のタンパク質コード領域も使用可能である。これらの二部構造物の第2部分は前記プロテアーゼ又はプロテアーゼの一部をコードし、これは、前記第1構造物によってコードされた融合タンパク質から活性化分子を除去するように作用する。
ここでの使用において、「細胞」、「細胞ライン」、及び「細胞培養物」という用語は、相互交換可能に使用することができる。これらの用語は全て、更に、その任意又はすべての後続世代であるところの、それらの後代(progeny)も含む。尚、全ての後代は、意
図的又は不意の変異によって同じではないかもしれない、と理解される。前記宿主細胞は、一般に、前記第1検定タンパク質とともに、融合タンパク質の一部である転写因子によって活性化されるスクリーニング可能又は選択可能なマーカを発現するように操作(engineered)されたものとされるであろう。
腸内細菌、更に、SURE(登録商標)Competent Cells 及びSOLOPACKTM Gold Cells(STRATAGENE(登録商標),La Jolla)等の多数の市販されている細菌性宿主を含む。いくつか
の実施例において、E.coli LE392等の細菌細胞が、ファージウイルス用の宿主細胞として特に考えられる。
多くの宿主細胞が利用可能であり、当業者に知られている。同様に、ウイルス性ベクターを、真核又は原核宿主細胞、特に、そのベクターの複製又は発現を許容するもの、と使用することができる。
本発明は、その物理的相互作用が知られている、又は、推測される、任意の二つのタンパク質の使用を意図している。これらのタンパク質は、融合タンパク質として、すなわち、転写因子に融合された第1検定タンパク質と、この第1融合タンパク質中の開裂部位、前記転写因子を遊離する開裂の部位、を認識するプロテアーゼに融合された第2検定タンパク質、として存在する。これら検定タンパク質/融合物のに必要とされることは、(a)第1検定タンパク質が、開裂の前に核内に局所化できないこと、そして(b)プロテアーゼが、第2タンパク質への融合と、第1検定タンパク質の第2検定タンパク質への結合との両方の後でも活性状態に留まる必要があること、のみである。
)、 エストロゲンレセプター2(ESR2)等の必ずしも自然には膜結合ではないその
他のレセプター、を含む他のクラスの膜貫通レセプターの活性が含まれる。それぞれのケースにおいて、前記方法は、対象レセプターを含むキメラタンパク質の発現を指令する改変レセプター構造物によって細胞をトランスフェクションする工程を含み、前記構造物には、プロテアーゼ開裂部位と、それに後続の、転写因子をコードする核酸分子とが付着している。前記細胞は、前述の部位を認識し開裂する前記プロテアーゼに融合された相互作用タンパク質から成るキメラタンパク質の発現を指令する第2構造物と同時トランスフェクションされる。EGFR等のRTKの場合、この相互作用タンパク質は、ホスホリパーゼC(PLC)等のSH2(Srcホモロジードメイン2)含有タンパク質又はその一部、又は、Srcホモロジー2ドメイン含有トランスフォームタンパク質1(SHC1)から構成することができる。TGFβ、アクチビン、BMPレセプターなどのレセプターセリン/トレオニンキナーゼの場合、この相互作用タンパク質は、Smadタンパク質又はその一部とすることができる。インターフェロン−α/β又はインターフェロン−γガンマレセプターなどのサイトカインレセプターの場合、この相互作用タンパク質は、非限定的に、Stat1,Stat2等の転写(STAT)タンパク質、ヤヌスキナーゼ(JAK)タンパク質Jak1,Jak2又はTyk2、又はそれらの一部の、シグナルトランスデューサ及び活性化物質とすることができる。それぞれの場合において、前記トランスフェクト細胞は、前記レセプターに融合された前記転写因子によって調節されるレポーター遺伝子を含む。次に、前記トランスフェクト細胞を、特定の期間、検定化合物で処理し、この検定期間の最後に前記レポーター遺伝子の活性を測定する解析を行う。もしも、検定化合物が対象のレセプターを活性化すれば、前記対象レセプターと前記相互作用タンパク質との間の相互作用が刺激され、それによって前記プロテアーゼ部位が開裂し、融合された転写因子が遊離され、これを、レポーター遺伝子活性における増加として測定することが可能となる。
レポーター遺伝子を活性化する前記タンパク質は、検出可能なシグナルをもたらす、遺伝子、発現又は欠如に対する影響を与える任意のタンパク質とすることができる。典型的なタンパク質レポーターは、クロラムフェニコールアセチル基転移酵素(CAT)、β−グルクロニダーゼ(glucuronidase)(GUS)又はβ−ガラクトシダーゼ等の酵素を含
む。又、グリーン蛍光タンパク質、レッド蛍光タンパク質、シアン蛍光タンパク質ルシフェラーゼ、ベータラクタマーゼ、アルカリフォスファターゼ等の蛍光及び化学発光タンパク質も考えられる。
本発明に拠れば、操作された宿主細胞内でのレポーター遺伝子の発現を活性化するために転写因子が使用される。これら転写因子は、一般に、それらのDNA結合ドメインの構造に応じて分類され、それらは一般に、(a)ジンクフィンガー、(b)へリックス−ターン−へリックス(helix-turn-helix)、(c)ロイシンジッパー(leucine zipper)、
(d)へリックス−ループ−へリックス(helix-loop-helix)、又は(e)高移動性グループである。転写因子の活性化ドメインが、転写装置(RNAポリメラーゼ)の成分又は、その他の調節タンパク質と相互作用し、それによってDNA結合の効率に影響を与える。
転写因子ファミリーは、熱ショック/E2Fファミリー、POUファミリー及びATFファミリーを含む。tTAやGAL4等の特定の転写因子が本発明の使用に考えられる。
プロテアーゼは、特定の部位において他のタンパク質を開裂する十分に特徴付けられている酵素である。1つのファミリー、Ser/Thrプロテアーゼは、セリン及びトレオニン残基で開裂する。他のプロテアーゼは、システイン又はチオールプロテアーゼ、アスパラギン酸プロテアーゼ、メタロプロテイナーゼ、アミノペプチダーゼ、ジ及びトリペプチダーゼ、カルボキシペプチダーゼ、及びペプチジルペプチダーゼを含む。これらの選択は、当業者次第であり、勿論、ここに記載されている分子に限定される必要はない。酵素が触媒ドメインを有し、これらを全長プロテアーゼの代わりに使用することが可能であることはよく知られている。そのようなものも本発明に含まれる。1つの具体的実施例は、タバコエッチ病ウイルス核内封入Aプロテアーゼ又は、その活性部分である。当業者に明らかなように、その他のプロテアーゼの特定の開裂部位も使用可能である。
前記第1検定タンパク質は、この解析において前記相互作用タンパク質に対するその結合を増強するように改変することができる。例えば、ある種のGPCRは、リガンド刺激により、アレスチンにより安定的に、又はより高い親和性で結合し、この増強された相互作用は、別々のドメイン、例えば、C末端尾部におけるセリンとトレオニン残基のクラスター、によって媒介されることが知られている(オークレイ(Oakley)ほか, J.Biol.Chem. 274:32248-32257,1999及びオークレイ(Oakley)ほか, J.Biol.Chem. 276:19452-19460, 2001)。これを一例として使用して、レセプターなどの膜結合タンパク質の親和性を
増加するために、レセプターコード配列自身を、それが結合するタンパク質で改変できることが明らかである。そのような改変の具体例は、上述したもののような、レセプターなどの膜結合タンパク質のC末端領域の、それの、結合タンパク質に対してより高い親和性を有するがレセプター機能には影響しない別のレセプターの対応領域との置換を含む、改変である。例16及び20は、本発明のこの特徴の実施例を示すものである。
上述したように、本発明は、その一実施例において、二つの検定タンパク質の、同じ細胞内で発現された時の、相互作用を評価する簡単な方法を提供する。第1構造物は、上述したように、それ自身、レポーター遺伝子アクチベーターをコードする配列に連結されている、プロテアーゼ又はプロテアーゼ部分のための開裂部位をコードする配列に連結されている第1タンパク質をコードする配列を含む。ここで、「連結」とは、記載した配列が、融合して、全ての要素を含む1つのポリペプチドに翻訳可能な、1つの完全なオープンリーディングフレームを作り出すことを意味する。これらは、別のタンパク質又はペプチドをコードする又はコードしないものとすることができる追加のヌクレオチド配列によって分離されたものであっても、又は分離されないものであってもよい。前記組換え細胞に挿入される第2構造物も、上述した、即ち、それは、第2タンパク質と、前記プロテアー
ゼ又はプロテアーゼ部分をコードする配列との両方を含む。これらの要素は協働で、標的タンパク質相互作用に対するその作用が追求される候補物質と組み合わされて基本解析形態を構成する。
に関する。そのような解析は、様々な方法で実行可能であるが、いずれの場合でも、一対以上の検定タンパク質が同時に検定される。これは、例えば、そのそれぞれが、各相互作用タンパク質の対を検定するべく、トランスフォーム又はトランスフェクトされている複数の細胞のサンプルを提供することによって達成可能である。これらの異なるトランスフォーム細胞は、1つの容器内で同時に組み合わせ、検定することができ、或いは、各タイプの形質転換体を別々の容器に入れて、その後検定することも可能である。
ここに記載の組成物のいずれも、キットとして構成することができる。従って、このキットは、本発明の前記ベクター又は細胞のための適当な容器手段と、本発明に使用可能な追加の任意の試薬とを含むものとなる。
の追加構成部分を別々に入れることが可能な、第2、第3、又はその他追加の容器を含むものとされる。但し、種々の組み合わせの構成部分を1つのバイアル中に含ませることも可能である。本発明のキットは、更に、通常、市販のために、試薬容器を密に封じ込めるための手段を備える。そのような容器は、その中に所望のバイアルが保持される射出成形又は吹出し成形容器を含むことができる。
本発明を説明する具体的実施例は、下記の例から理解されるであろう。但し、本発明はこれらに限定されるものと解釈されてはならない。
標準命名法に 従って、以下“ADRB2”と称するヒトβ2アドレナリンレセプターをコードするDNAを使用して、融合構造物を形成した。そのヌクレオチド配列は、GenBankにおいて、受入番号NM_ 000024(配列識別番号1)で得られる。ここに参考文献とし
て合体させるゴッセン(Gossen)ほか, Proc. Natl. Acad. Sci. USA , 87: 5547-5551(1992)に記載されているテトラサイクリン調節性トランスアクチベーターtTAも使用された。ここに参考文献として合体させるパークス(Parks)ほか, Anal. Biochem., 216: 413-417 (1994)に記載されている、タバコエッチ病ウイルス核内封入Aプロテアーゼに対する認識及び開裂部位をコードする配列が、前記融合コード遺伝子のこれらの配列の間に挿入されている。前記CMVプロモーター領域を、ADRB2コード領域の上流側に配置し、ポリA配列を、前記tTA領域の下流側に配置した。
gattgaagat ctgccttctt gctggc(配列識別番号2)、及び、
gcagaacttg gaagacctgc ggagtcc(配列識別番号3)によって増幅した。
一方、前記コード領域の3’部分を、
ggactccgca ggtcttccaa gttctgc(配列識別番号4)、及び、
ttcggatcct agcagtgagt catttgt(配列識別番号5)によって増幅した。
tTAのコード領域を改変するのにもPCRが使用された。7アミノ酸配列ENLYFQS(配
列識別番号6)によって形成されている前記開裂部位は、ここに参考文献として合体させるパークス(Parks)ほか, Anal. Biochem., 216: 413-417(1994)によって教示されて
いる。7番目のアミノ酸は、P1’位置として知られており、これを他のアミノ酸と置換
することによって、TEV NIa−Proによる開裂の効率が減少することが知られている。カプスト(Kapust)ほか, Biochem. Bophys. Res. Commun., 294: 949-955(2002
)を参照。
ccggatcctc tagattagat aaaagtaaag tg(配列識別番号7)、及び
gactcgagct agcagtatcc tcgcgccccc taccc(配列識別番号8)、でのPCRによって、BamHI及びXbaI制限部位を5’末端に付加し、XhoI制限部位をtTAコード領域の3’末端に付加した。そして、TEV NIa−Pro開裂部位を、BamHIとXbaI部位の間で下記の配列、
gagaacctgt acttccag(配列識別番号9)に、オリゴヌクレオチドを連結することによ
って5’末端に付加した。
ENLYFQY(配列識別番号12)の場合は、
ggatccgaga acctgtactt ccagtacaga tta(配列識別番号10)、及び、
ctcgagagat cctcgcgccc cctacccacc(配列識別番号11)、そして
ENLYFQL(配列識別番号14)の場合は、
ggatccgaga acctgtactt ccagctaaga tta(配列識別番号13)、及び、
ctcgagagat cctcgcgccc cctacccacc(配列識別番号11)。
gcggccgcca ccatgaacgg taccgaaggc cca(配列識別番号15)、及び、
ctggtgggtg gcccggtacc a(配列識別番号16)を、使用したPCRによって、前記A
DRB2コード領域の開始コドンの5’にNotI制限部位が導入された。
第2の構造物も作成し、ここでは、以後“βアレスチン2又はARRB2”と称する(GenBank, NM_004313)(配列識別番号17)のコード配列を、TEVタンパク質のTEV
NIaプロテアーゼの触媒ドメイン(即ち、成熟NIaプロテアーゼのアミノ酸189−424、残基2040−2279)に連結した。これを行うために、ARRB2をコードするDNA配列を、BamHI制限部位をその5’末端に付加するように改変した。更に、この配列を、内在性の終止コドンをBamHI部位で置換するように改変した。下記のオリゴヌクレオチド、
caggatcctc tggaatggg gagaaaccg ggacc(配列識別番号18)、及び、
ggatccgcag agttgatcat catagtcgc(配列識別番号19)が使用された。得られたPC
R産物を、市販のベクターpGEM−T EASY(Promega)にクローニングした。前
記pGEM−T EASYベクターのマルチクローニング部位は、ARRBの開始コドンへのEcoRI部位5’を含む。
て、前記TEV NIa−Proコード領域を、前記内在性の開始コドンをBglII部位によって置換し、3’末端に、インフルエンザヘマグルチニンエピトープYPYDVPDYA(
配列識別番号20)をコードする配列を挿入し、その後、終止コドンとNotI制限部位とするように改変した。これは、
agatctagct tgtttaaggg accacgtg(配列識別番号21)、および、
gcggccgctc aagctaac tggaacatca tatgggtacg agtacaccaa ttcattcatg at(配列識別番号22)、を使用するPCRによって達成された。
ADRB2−TEV−NIa−Pro開裂部位t−TA及びARRB2−TEV−NIaプロテアーゼ融合タンパク質をコードするプラスミドを、HEK−293T細胞と、tTA依存プロモーターの制御下で、安定的にβ−ガラクトシダーゼ遺伝子を取り込んだ、HEK−293Tの誘導体である、「クローン41」とにトランスフェクトした。約5x104の細胞を、10%胎児ウシ血清、2mM L−グルタミン、100単位/mlペニシリ
ン、100μg/ml G418及び5μg/mlプリマイシン(purimycin)を添加した
DMEM培地中で、24ウェルプレートの各ウェルにプレーティングした。細胞を次の日、50%のコンフルエンシーにまで増殖させ、次に、0.4μgのプラスミドDNA、及び2μlのFugene(脂質とその他の物質を含有する専売のトランスフェクション試薬)を使用してトランスフェクトした。この混合物を、100μlのDMEM培地中で組み合わせ、細胞の添加の前に、室温で15分間インキュベートした。トランスフェクション細胞を、検定8〜20時間前に、レセプターのための公知のアゴニストである薬剤を添加することによってインキュベートし、その後、薬剤添加後、16−24時間インキュベートした。
前記細胞内のβ−ガラクトシダーゼのレベルを、先ず、ここに参考文献として合体させるマクグレガー(MacGregor)ほか, Somat. Cell Mol. Genet., 13: 253-265(1987)に
よって教示されているように、これらの細胞を、発色性物質、即ち、“X−gal”によって染色することによって測定した。培養後、細胞を、カルシウムとマグネシウムを含むD−PBS中で二回洗浄し、4%パラホルムアルデヒド中で5分間固定し、その後、追加の二回、それぞれ10分間、D−PBS、カルシウム及びマグネシウムによって洗浄した。固定された細胞を、予め、カルシウムとマグネシウムとを含むD−PBS中で、4%
X−Gal保存液の1:40希釈によって調製しておいた、5mMのフェリシアン化カリウム、5mMのフェロシアン化カリウム、2mMのMgCl2、0.1% X−Gal、とインキュベートした。
モヴィオール、0.1% 1.4−ジアザビシクロ[2.2.2]オクタン、24%グリセロール)で封入した。
細胞中におけるレポーター遺伝子活性のレベルをより正確に定量化し、分析におけるシグナル対バックグランド比を最大化するために一組の実験を行った。これは、β−ガラクトシダーゼ活性のための市販の化学発光解析を使用してレポーター遺伝子誘導のレベルを測定することによって達成された。クローン41細胞を、ADRB2−tTA融合構造物、前記高、中または低効率開裂部位のいずれかを含む、及び上述したARRB2−TEV−NIaプロテアーゼ発現プラスミド、でトランスフェクトした。細胞を、トランスフェクション後、1μMのイソプロテレノールで処理しないか、又は20時間処理し、薬剤添加の24時間後に発光解析を行った。簡単に説明すると、細胞培養後、培地を除去し、50μlの溶解緩衝液(100mMリン酸カリウム、pH7.8,0.2% Triton
X−100)を各ウェルに添加した。細胞を、緩やかに攪拌しながら、室温で5分間のインキュベーションによって溶解させた。溶解物を収集し、市販の製品によって分析した。
これらの実験は、レポーター遺伝子発現におけるアゴニスト刺激増加が、アゴニストによるレセプターの結合と活性化に依存することを証明するために構成された。
か, J. Biol. Chem. 266: 5-8 (1991)を参照。それぞれ異なる開裂部位をもつ三つの形態の変異体レセプター−tTA融合構造物が形成された。
これらの実験は、レポーター遺伝子発現のアゴニスト刺激増加が、TEV NIa−ProのARRB2への融合に依存するか否かを調べるために構成された。
これらの実験は、遺伝子発現が標的レセプターのアゴニストによって選択的に誘導されるか否か、或いは、それがその他の分子によって刺激することが可能であるか否か、を調べるために構成された。
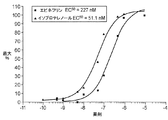
前記低効率開裂部位を含むADRB2−tTA融合構造物と上述のARRB2−TEV−NIaプロテアーゼ融合物とでコトランスフェクトされ、種々の量の、アドレナリンレセプターアゴニスト、イソプロテレノール及びエピネフリンのいずれか1つで処理されたクローン41細胞を使用して1セットの実験を行った。これらの解析は、上述した通りに行われた。図2aに示されているその結果は、これら二つのリガンドによるレポーター遺伝子発現の刺激の用量−反応曲線を示している。各ポイントは、三つの実験から得られた
平均値を表している。
Gタンパク質共役アルギニンバソプレッシンレセプター2(AVPR2)の分析を確立するために類似のセットの構造体を作成した。AVPR2コード領域(GenBank受入番号:
NM_000054)(配列識別番号23)を、プライマー、
gaattcatgc tcatggcgtc caccac(配列識別番号24)、及び、
ggatcccgat gaagtgtcct tggccag(配列識別番号25)でPCRを使用して、5’末端
にEcoRIを配置し、そして終止コドンをBamHI部位によって置換するように改変した。
ている。最大の反応によって、バックグランドレベルに対して、レポーター遺伝子発現の約40倍の誘導が得られた。
Gタンパク質共役セロトニンレセプター1a(HRT1A)の解析を確立するために、類似セットの実験を行った。前記HTR1Aコード領域(Genbank受入番号NM_000524)(配列識別番号26)を、プライマー、
gaattcatgg atgtgctcag ccctgg(配列識別番号27)、及び、
ggatccctgg cggcagaact tacac(配列識別番号28)、でのPCRを使用して、5’末
端にEcoRI部位を配置し、終止コドンをBamHI部位によって置換するべく改変した。
ター遺伝子発現の4.6倍の誘導が得られた。
Gタンパク質共役m2ムスカリンアセチルコリンレセプター(CHRM2)のための解析を確立するために類似の構造体を作成した。CHRM2コード領域(Genbank受入番号NM_000739)(配列識別番号29)を、プライマー、
gaattcatga ataactcaac aaactcc(配列識別番号30)、及び、
agatctcctt gtagcgccta tgttc(配列識別番号31)、でのPCRを使用して、5’末
端にEcoRI部位を配置し、終止コドンをBgIII部位によって置換するべく改変した。
したように解析を行った。カルバコールへの最大の反応によって、バックグランドレベルに対して、レポーター遺伝子発現の7.2倍の誘導が得られた。
Gタンパク質共役ケモカイン(C−Cモチーフ)レセプター5(CCR5)の解析を確立するためにα構造物も作成した。CCR5コード領域(Genbank受入番号NM_000579)(配列識別番号32)を、プライマー、
gcggccgcat ggattatcaa gtgtcaagtc c(配列識別番号33)、及び、
ggatccctgg cggcagaact tacac(配列識別番号34)、でのPCRを使用して、5’末
端にNotI部位を配置し、終止コドンをBamHI部位によって置換するべく改変した。
ggtctccaat tcatggatta tcaagtgtca agt(配列識別番号35)、及び、
gacgacagcc aggtacctat c(配列識別番号36)、を使用して、それが切断された時に
、EcoRI切断DNAと適合するヌクレオチド突出部分を残す、5’末端にBsaI部位を配置するようにも改変した。
て解析を行った。上述したように測定された、RANTESに対する最大反応によって、バックグランドに対するレポーター遺伝子発現の約40倍の誘導が得られた。
次に、Gタンパク質共役ドーパミン2レセプター(DRD2)の解析を確立するために一組の構造物を作成した。DRD2コード領域(Genbank受入番号NM_000795)(配列識別番号37)を、プライマー、
gaattcatgg atccactgaa tctgtcc(配列識別番号38)、及び、
agatctgcag tggaggatct tcagg(配列識別番号39)、を使用して、5’末端にEco
RI部位を配置し、終止コドンをBgIII部位によって置換するべく改変した。
これらの実験は、アゴニスト占有GPCRを安定的に結合するアレスチン変異体を使用した解析の増強を証明するように構成された。先ず、β−アレスチン−1(ARRB1)に対するTEV NIaプロテアーゼの融合物を構築した。ARRB1のコード領域(Genbank受入番号. NM_004041)(配列識別番号40)を、プライマー、
ggtaccatgg gcgacaaagg gacgcgagtg(配列識別番号41)、そして、
ggatcctctg ttgttgagct gtggagagcc tgtaccatcc tcctcttc(配列識別番号42)、での使用したPCRを使用して、5’末端にAsp718部位を配置し、終止コドンをBamHI部位で置換するべく改変した。
に、β−アレスチン−1のコード領域を、上述した配列識別番号41、及び、
ggatccattt gtgtcaagtt ctatgag(配列識別番号43)、でのPCRを使用して、5’
末端にAsp718部位を配置し、アミノ酸382のあとにBamHI部位を配置するべく、改変した。
る。これによって得られた改変ARRB1コード領域、“ARRB1(Δ383)”と称する、を、Asp718とEcoRI、そしてEcoRIとBamHIで切断し、他方、上述の前記改変TEV NIa−Proコード領域をBgIIIとNotIで切断した。これら三つのフラグメント全部を、市販のpcDNA3発現ベクターに連結し、Asp718とNotIで消化した。
ggtaccatgg gggagaaacc cgggacc(配列識別番号44)、及び、
ggatcctgtg gcatagttgg tatc(配列識別番号45)、でPCRを使用して、5’末端にAsp718部位を配置し、3’末端の81のヌクレオチドをBamHI部位で置換するように改変した。
この組の実験は、相互作用タンパク質に対する親和性を増大させるように構成されたレセプター改変体を使用した解析の増強を証明するために行われた。この例において、検定レセプターのC末端尾部ドメインが、高い親和性でアレスチンと結合することが知られているレセプターである、AVPR2からの対応の尾部ドメインによって置換された。これらの例において、前記融合結合部(junction)が、通常、レセプターC−末端の推定パルミトイル化部位の直後の位置に対応する、第7膜貫通螺旋の末端における保存NPXXYモチーフの後の15〜18のアミノ酸に作られた。
tgtgcgcgcg gacgcacccc acccagcctg ggt(配列識別番号46)、及び、
ctcgagagat cctcgcgccc cctacccacc(配列識別番号11)、によって、上述した低効率開裂部位を有するAVPR2−tTA構造物を増幅することによっ達成された。
gaattcatgg atccactgaa tctgtcc(配列識別番号47)、及び、
tgtgcgcgcg cagtggagga tcttcaggaa ggc(配列識別番号48)、でPCRを使用して行われた。
gcggccgcca ccatgaacgg taccgaaggc cca(配列識別番号49)、及び、
tgtgcgcgcg cacagaagct cctggaaggc(配列識別番号50)、でPCRを使用することによって行われた。
とBamHIで切断した。両フラグメントを、上述したAVPR2−低効率開裂部位−tTA構造物に連結し、EcoRIとBamHIで切断した。得られた構造物が“ADRB2−AVPR2尾部−tTA”である。(前述した米国特許公開出願2002/0106379、特に、配列識別番号3を参照)。
ggtctacttg atgaattcct ggcc(配列識別番号52)、及び、
gcgcgcacag aagtcccgga aacaccg(配列識別番号53)、でPCRを使用して行われた
。
で切断した。両フラグメントを、前記改変OPRKレセプター配列を含むプラスミドに連結し、予めEcoRIとXhoIによって消化しておいた、Asp718(5’)とXhoI(3’)でpcDNA3.1+にクローニングした。
この実験は、マルチプレックス形態を同時に使用して二つの検定レセプターの活性を測定する解析の使用を示すように構成された。
われた。24時間のインキュベーションの後、ADRB2−AVPR2尾部−tTAを発現するクローン41細胞とDRD2−AVPR2尾部−tTAを発現するクローン1H10細胞とを、トリプシン処理し、同量で混合し、96ウェルプレートの12のウェルに再プレーティングした。三つ組のウェルを、薬剤の添加無しでインキュベートするか、もしくは、1μMのイソプロテレノール、1μMのドーパミン、又は1μMの両アゴニストの混合物、のいずれかで即座に処理した。細胞を、リガンド添加後、約24時間で、レポーター遺伝子活性について解析した。培地を捨て、細胞を、40μlの溶解緩衝液[100mM リン酸カリウム pH7.8,0.2% Triton X−100]中に溶解し、細胞溶解物を、ベータ−ガラクトシダーゼ、及びルシフェラーゼ活性について、市販の発光検出用試薬を使用して解析した。
この実験は、マルチプレックス形態を同時に使用して二つの検定レセプターの活性を測定する解析の使用を説明するように構成された。
ウシ血清、2mM L−グルタミン、100単位/mlのペニシリン、500μg/mlのG418、及び3μg/mlのピューロマイシンを添加したDMEM中で24時間培養した。細胞を、100μlのDMEM、0.5μgのOPRK−AVPR2尾部−TEV
−NIa−Pro開裂(Leu)−tTA DNAと、2.5μlのFugene(「ク
ローン34.9細胞」)で、又は、100μlのDMEM、0.5μgのADRB2−A
VPR2尾部−TEV−NIa−Pro開裂(Leu)−tTA DNA,0.5μlの
ARRB2−TEV NIaプロテアーゼDNA及び5μgのFugene(「クローンHTL 5B8.1細胞」)で、一過性にトランスフェクトした。一過性にトランスフェクトされた細胞を、約24時間培養し、次に、トリプシン処理し、等量で混合し、96ウェルプレートのウェルに再プレーティングした。細胞を、10μM−U−69593、10μMのイソプロテレノール又はこれら両方のアゴニストの10μMの混合物、での処理の前に24時間インキュベートした。各実験条件において16のウェルを解析した。24時間後、細胞を溶解し、そしてベータ−ガラクトシダーゼ及びルシフェラーゼレポーター遺伝子の活性を上述のように解析した。その結果を図6に示す。U−69593での処理によって、ベータ−ガラクトシダーゼレポーター遺伝子活性の約15倍の誘導が起こったのに対して、ルシフェラーゼ活性は変化しないままであった。イソプロテレノールでの処理ではルシフェラーゼ活性の145倍の誘導が行ったのに対して、ベータ−ガラクトシダーゼ活性は変化しないままであった。U−69593とイソプロテレノールとの両方での処理ではベータ−ガラクトシダーゼとルシフェラーゼ活性の、それぞれ、9倍と136倍の誘導が起こった。
この例は、本発明の解析における異なる転写因子とプロモーターの使用を示すために行われた。
号55)のアミノ酸2−147をコードし、その後、リンカー、即ち、配列PELGSASAELTMVF(配列識別番号56)のリンカーが続き、その後、ネズミ核因子カツパ−B鎖p65タンパク質(GenBank受入番号A37932)(配列識別番号57)のアミノ酸368−549が
続くDNA配列にインフレーム融合された、融合構造物を作成した。前記CMVプロモーターを、AVPR2コード領域の上流側に配置し、ポリA配列を、GAL4−NFkB領域の下流側に配置した。この構造物を、AVPR2−TEV−NIa−Pro開裂(Leu)−GAL4と命名した。
トランスフェクトした。約2.5x104の細胞を、10%胎児ウシ血清、2mM L−グルタミン、100単位/mlのペニシリン、500μg/mlのG418及び3μg/mlのピューロマイシンを添加したDMEM培地中で96ウェルプレートの各ウェルにプレーティングした。細胞を、次の日、50%のコンフルエンシーに達するまで培養し、細胞への添加の前に室温で15分間インキュベートしておいた、85μlのDMEMと、0.1μgのAVPR2−TEV−Nia−Pro開裂(Leu)−GAL4DNAと、0.1μgのARRB2−TEV N1aプロテアーゼDNAと、1μlのFugeneからなる各ウェル当たり10μlの混合物で、トランスフェクトした。トランスフェクト細胞
を10μMのバソプレッシンでの処理の前に、約16時間培養した。6時間後、細胞を溶解し、ルシフェラーゼ活性を上述したように解析した。これらの条件下において、バソプレッシンでの処理によって、レポーター遺伝子活性の180倍の増加が行った。
このセットの実験は、相互作用タンパク質の親和性を増加させるように構成された他のレセプター改変体を使用した解析の増強を示すために行われた。この例において、検定レセプターのC末端尾部ドメインが、下記のレセプターの1つの対応の尾部ドメインと置換された。即ち、アペリン(apelin) Jレセプター−AGTRL1(受入番号NM_005161(配列識別番号58)、ガストリン遊離ペプチドレセプター−GRPR(受入番号NM_005314)(配列識別番号59)、プロテイナーゼ活性化レセプター2−F2RL1(受入番号NM_005242)(配列識別番号60)、CCR4(受入番号NM_005508)(配列識別番号61)、ケモカイン(C−X−Cモチーフ)レセプター4−CXCR4(受入番号NM_003467)(配列識別番号62)及びインターロイキン8レセプター、ベータ−CXCR2
/IL8b(受入番号NM_001557)(配列識別番号63)。
tgtgcgcgcg gccagagcag gtgcgca(配列識別番号64)、及び、
gaggatccgt caaccacaag ggtctc(配列識別番号65)、で増幅した。
前記GRPR C−末端フラグメントは、プライマー、
tgtgcgcgcg gcctgatcat ccggtct(配列識別番号66)、及び、
gaggatccga cataccgctc gtgaca(配列識別番号67)、で増幅した。
tgtgcgcgca gtgtccgcac tgtaaagc(配列識別番号68)、及び、
gaggatccat aggaggtctt aacagt(配列識別番号69)、で増幅した。
tgtgcgcgcg gcctttttgt gctctgc(配列識別番号70)、及び、
gaggatccca gagcatcatg aagatc(配列識別番号71)、で増幅した。
tgtgcgcgcg gcttgatcag caagggac(配列識別番号72)、及び、
gaggatccga gagtagtgga agtgtg(配列識別番号73)、で増幅した。
tgtgcgcgcg ggtccagcct caagate(配列識別番号74)、及び、
gaggatccgc tggagtgaaa acttga(配列識別番号75)、で増幅した。
アーゼ融合物のそれぞれで、コトランスフェクトした。1ウェル当り約2.5x104の細胞を、10%胎児ウシ血清、2mMのL−グルタミン、100単位/mlのペニシリン、500μg/mlのG418及び3μg/mlのピューロマイシンを添加したDMEM培地中で、96ウェルプレートにプレーティングした。細胞を、次の日50%のコンフルエンシーに達するまで増殖させ、細胞への添加の前に室温で15分間インキュベートしておいた、85μlのDMEM、0.25μgのAVPR2−TEV−NIa−Pro開裂(Leu)−GAL4 DNAと、0.25μgのARRB2−TEV NIaプロテアーゼDNA、及び2.5μlのFugene(脂質及びその他の物質を含む専売のトランス
フェクション試薬)とからなる、各ウェル当たり10μlの混合物でトランスフェクトした。トランスフェクト細胞を10μMのU−69593での処理の前に、約16時間培養した。6時間後、細胞を溶解し、ルシフェラーゼ活性を上述したように解析した。これらの条件下において、U−69593での処理によって、前記改変OPRKレセプターのそれぞれにおいて、レポーター遺伝子活性の下記の相対的増加が生じた。即ち、OPRK−AGTRL1 C−末端尾部−30倍、OPRK−GRPR C−末端尾部−312倍、
OPRK−F2RL1 C−末端尾部−69.5倍、OPRK−CCR4 C−末端尾部−3.5倍、OPRK−CXCR4 C−末端尾部−9.3倍、OPRK−IL8b C−末端尾部−113倍。
この実験は、上述したARRB2−TEV NIaプロテアーゼ融合タンパク質を安定的に発現する細胞ラインを作成するように構成された。
ク質を発現するとともに、チミジンキナーゼ(TK)プロモーターの制御下でハイグロマイシン耐性遺伝子を発現するプラスミドを作成した。
り10μlの混合物でトランスフェクトした。トランスフェクト細胞を10μMのイソプロテレノールでの処理の前に、約16時間培養した。6時間後、細胞を溶解し、ルシフェラーゼ活性を上述したように解析した。これらの条件下において、イソプロテレノールでの処理によって、前記三つの細胞ラインにおいて、レポーター遺伝子活性の、それぞれ、112倍(“HTLA 4C2.10”)、56倍(“HTLA 2C11.6”)及び180倍(“HTLA 5D4”)のそれぞれ増加が得られた。
この実験は、上述のARRB2−TEV NIaプロテアーゼと、ADRB2−AVPR2尾部−TEV−NIa−Pro開裂(Leu)−tTA融合タンパク質とを安定的に発現する細胞ラインを作成するように構成された。
この実験は、レセプターチロシンキナーゼ上皮増殖因子レセプター(EGFR)の活性を測定するための解析の使用を説明するために構成された。
列識別番号76)として入手可能な、ヒトEGFRをコードするDNAを含む第1融合構造物を作成した。これらの配列の間には、上述した、TEV NIa−Proのための低
効率開裂部位,ENLYFQL(配列識別番号14)を含むアミノ酸配列GGSGSENLYFQL(配列識別番号77)をコードするDNA配列が挿入されている。前記CMVプロモーターを、前記上皮増殖因子レセプターコード領域の上流側に配置し、ポリA配列を、tTA領域の下流側に配置した。この構造物を、EGFR−TEV−NIa−Pro開裂(Leu)−tTAと命名する。
インフレームで融合された、アミノ酸538〜759(GenBank受入番号NP_002651.2)(配列識別番号78)と、アミノ酸2040〜2279(GenBank受入番号AAA47910)(配
列識別番号79)とにそれぞれ対応する、ヒト ホスホリパーゼC ガンマ 1の二つの2H2ドメインをコードするDNAを含む、第2融合構造物を作成した。これらの配列の間には、アミノ酸NSSGGNSGS(配列識別番号80)をコードするリンカーDNA配列が挿入されている。前記CMVプロモーターを、前記PLC−ガンマ SH2ドメインのコード配列の上流側に配置し、ポリA配列を、TEV NIaプロテアーゼ配列の下流側に配置した。この構造物を、PLC ガンマ 1−TEVと命名する。
EV DNA、2μlのFugene(脂質及びその他の物質を含む専売のトランスフェ
クション試薬)とからなる、各ウェル当たり15μlの混合物でトランスフェクトした。トランスフェクト細胞を、特定のレセプターアゴニスト及びインヒビターでの処理の前に、約16時間培養した。6時間後、細胞を溶解し、ルシフェラーゼ活性を上述したように解析した。その結果を図7に示す。
この実験は、ヒトI型インターフェロンレセプターの活性を測定するための解析の使用を説明するように構成された。
列識別番号81)として入手可能な、ヒトインターフェロンレセプターI(IFNAR1)(557のアミノ酸)をコードするDNAを含む融合構造物を作成した。これらの配列の間には、上述したTEV NIa−Proに対する低効率開裂部位,ENLYFQL(配列識別番号14)を含むアミノ酸配列GSENLYFQL(配列識別番号82)コードするDNA配列が挿入されている。前記CMVプロモーターを、前記ヒトインターフェロンレセプターI(IFNAR1)コード領域の上流側に配置し、ポリA配列を、tTA領域の下流側に配置した。この構造物を、IFNAR1−TEV−NIa−Pro開裂(L)−tTAと命名する。
て入手可能な、ヒトインターフェロンレセプター2、スプライスバリアント2(IFNAR2.2)(515のアミノ酸)をコードするDNAを使用して第2融合構造物を作成した。これらの配列の間には、アミノ酸配列RS(Arg−Ser)をコードするDNA配列が挿入されている。前記CMVプロモーターを、ヒトインターフェロンレセプター2(IFNAR2.2)コード領域の上流側に配置し、ポリA配列を、TEV領域の下流側に配置した。この構造物を、IFNAR2.2−TEVと命名する。
R2.2−TEV、CMV−STAT1、及びCMV−STAT2 DNAのそれぞれ15ng又は、60ngの対照pcDNAプラスミドで、各ウェル当たり0.3μlのFugeneと共に、トランスフェクトした。トランスフェクト細胞を、5000U/mlのヒトインターフェロン−アルファ又は5000U/mlのヒトインターフェロン−ベータでの処理の前、8〜20時間培養した。インターフェロン添加時、培地を吸引し、2mM
L−グルタミン、100単位/mlのペニシリン、3μg/mlのピューロマイシン及び500μg/mlのG418を添加した293 SMF II培地で置換した。インターフェロン処理された細胞を、上述したようにルシフェラーゼレポーター遺伝子活性を解析する前に、更に18〜20時間培養した。結果を図8に示す。5000U/mlのIFN−αでの処理によってレポーター遺伝子活性が15倍増加したのに対して、5000U/mlのIFN−βでの処理によって10倍増加した。前記対照プラスミドpcDNA3とトランスフェクトされたHTL5B8.1細胞のインターフェロン処理ではレポーター遺伝子活性に効果は無かった。図9は、上述したIFNAR1(ENLYFQ(L)−tTa,IFNAR2.2−TEV,STAT1及びSTAT2発現構造物でトランスフェクトされたHTL5B8.1細胞におけるIFN−αに対して生成された用量−反応曲線を図示している。
この実験は、別の転写因子と別の細胞ラインを使用したヒトI型インターフェロンレセプターの活性を測定するための解析の使用を説明すべく構成された。
この組の実験は、前記相互作用タンパク質に対する検定レセプターの親和性を増加させるように構成されたレセプター改変体を使用する解析の更なる増強を説明すべく行われた。これらの例において、前記検定レセプターと、GRPR(Genbank受入番号NM_005314)(配列識別番号59)のC末端尾部ドメインとの間の融合接合部を、前記第7膜貫通螺旋の端部の保存NPXXYモチーフの後のアミノ酸17〜23として作成した。
tctagaggcctgatcatccggtctcac(配列識別番号88)、及び、
gaggatccgacataccgctcgtgaca(配列識別番号67)、でGRPRコード領域を含むプラスミドを増幅することによって達成された。
ggtctacttgatgaattcctggcc(配列識別番号52)、及び、
tctagatggaaaacagaagtcccggaaac(配列識別番号89)、でのPCRを使用して行われ
た。
ctcggatatctaaacagctgcatcaa(配列識別番号91)、及び、
tctagactttctgcagagacactggattc(配列識別番号92)、でPCRを使用して行われた
。
gaattcatggatccactgaatctgtcc(配列識別番号38)、及び、
tctagatcgaaggcagtggaggatcttcagg(配列識別番号93)、でPCRを使用して行われ
た。
末端尾部低効率開裂部位tTAを備えるOPRKレセプターを含むプラスミドに連結した。
この組の実験は、相互作用タンパク質に対する親和性を増大させるように構成された異なる組の検定レセプター改変を使用した解析の更なる増強を証明するために行われた。これらの例において、検定レセプターのC末端尾部ドメインが、GRPRの内在性のC末端尾部ドメインの一部と置換された。
tctagaggcctgatcatccggtctcac(配列識別番号94)、及び、
cggatccgttggtactcttgagg(配列識別番号95)、でGRPRコード領域を含むプラス
ミドを増幅することによって達成された。
この実験は、レセプター チロシンキナーゼ インスリン様増殖因子−1レセプター(IGF1R)の活性を測定、具体的には、細胞内シグナリングタンパク質SHC1(Srcホモロジー2ドメイン−含有トランスフォーミングタンパク質1)のリガンド誘導性の補充をモニタリングすることによって測定、するための解析の使用を示すように構成された。
番号97)、アミノ酸2040〜2279(GenBank受入番号AAA47910)(配列識別番号
79)に対応する、ヒトSHC1のPTBドメインをコードするDNAを含む、第2融合構造物を作成した。これらの配列の間には、アミノ酸NSGS(配列識別番号98)をコードするリンカーDNA配列が挿入されている。前記CMVプロモーターを、前記SHC1 PTBドメインコード配列の上流側に配置し、ポリA配列を、TEV NIaプロテアーゼ配列の下流側に配置した。この構造物を、SHC1−TEVと命名する。
この実験は、正常に膜結合しない二つの検定タンパク質の相互作用を測定する解析の使用を説明するように構成された。この例において、前記解析を使用して、核ステロイドホ
ルモンレセプター、ESR1(エストロゲンレセプター1またはERアルファ)、及びESR2(エストロゲンレセプター2又はERベータ)のリガンド誘導性の二量化を測定した。この例において、ESR1は、転写因子tTAに融合され、他方、TEV NIa−Proプロテアーゼの開裂部位を、ESR1とtTA配列の間に挿入する。このESR1−tTA融合物を、前記膜貫通タンパク質CD8の前記細胞内、C−末端への融合によって前記膜に係留させる。CD8は、本質的に、ESR1を細胞膜の細胞質側に係留する不活性足場(scaffold)として作用する。それに融合された転写因子は、ESR2とプロテアーゼとの相互作用までは、核に入ることができない。任意の膜貫通タンパク質を使用することが可能であろう。このCD8−ESR1−TEV NIa Pro開裂−tTA融合タンパク質は、tTA−依存性レポーター遺伝子を含有する細胞ラインにおいて、ESR2とTEV NIa−Proプロテアーゼとから成る第2融合タンパク質と共に、発現
される。ESR1とESR2とのエストロゲン誘導性の二量化は、それによって、膜結合融合物からのtTA転写因子の遊離を誘因し、これが、その後のレポーター遺伝子活性の誘導によって検出される。
番号NM_001768(配列識別番号99)として入手可能な、ヒトCD8遺伝子(235のア
ミノ酸)をコードするDNAを含む融合構造物を作成した。これらの配列の間には、前記アミノ酸配列GRA(Gly−Arg−Ala)をコードするDNA配列が挿入されている。次に、これによって得られた構造物を、上述したテトラサイクリン制御トランスアクチベーターtTAのアミノ酸3〜335をコードするDNA配列にインフレームで融合する。これらの配列の間には、上述したTEV NIa−Proの低効率開裂部位,ENL
FQL(配列識別番号14)を含む、アミノ酸配列GSENLYFQL(配列識別番号82)をコードするDNA配列が挿入されている。前記CMVプロモーターを前記ヒトCD8コード領域の上流側に配置し、ポリA配列を、tTA領域の下流側に配置した。この構造物を、CD8−ESR1−TEV−NIa−Pro開裂(L)−tTAと命名する。
応する、上述した、前記TEV NIaプロテアーゼの触媒ドメインをコードするDNA配列にインフレームで融合された、Genbank受入番号NM_001437(配列識別番号101)で入手可能な、ヒトエストロゲンレセプターベータ(ESR2)(530のアミノ酸)をコードするDNAを使用して第2融合構造物を作成した。これらの配列の間には、アミノ酸RS(Arg−Ser)をコードするDNA配列が挿入されている。前記CMVプロモーター領域を、前記ヒトエストロゲンレセプターベータ(ESR2)コード配列の上流側に配置し、ポリA配列を、TEV領域の下流側に配置した。この構造物を、ESR2−TEVと命名する。
時間培養した。50nMの17−β−エストラジオールでの処理によって、レポーター遺伝子活性の16倍の増加が得られた。
(1)検定化合物が対象の特定のタンパク質/タンパク質相互作用を調節するか否かを測定するための方法であって、以下でトランスフォーム又はトランスフェクトされた細胞に、前記化合物を接触させる工程、
(a)下記を含む核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、
(ii)プロテアーゼ又はプロテアーゼの一部に対する開裂部位をコードするヌクレオチド配列、及び
(iii)前記細胞内においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、そして、
(b)下記を含む核酸分子、
(i)前記検定化合物の存在下における、前記第1検定タンパク質との相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列、及び、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、
及び、前記化合物が前記タンパク質/タンパク質相互作用を調節するか否かの測定として、前記レポーター遺伝子の活性を測定する工程、とを含む、
検定化合物が対象の特定のタンパク質/タンパク質相互作用を調節するか否かを測定するための方法。
(2)前記第1検定タンパク質が、膜結合タンパク質である(1)に記載の方法。
(3)前記膜結合タンパク質が、膜貫通レセプターである(2)に記載の方法。
(4)前記膜貫通レセプターが、GPCRである(3)に記載の方法。
(5)前記プロテアーゼ又はプロテアーゼの一部が、タバコエッチ病ウイルス核内封入Aプロテアーゼである(1)に記載の方法。
(6)前記レポーター遺伝子を活性化する前記タンパク質が、転写因子である(1)に記載の方法。
(7)前記転写因子が、tTA又はGAL4である(6)に記載の方法。
(8)前記前記第2タンパク質が、抑制型タンパク質である(1)に記載の方法。
(9)前記抑制型タンパク質がアレスチンであり、前記第1タンパク質は膜貫通レセプターである(8)に記載の方法。
(10)前記細胞が、真核細胞である(1)に記載の方法。
(11)前記レポーター遺伝子が、外来性遺伝子である(1)に記載の方法。
(12)前記外来性遺伝子が、β−ガラクトシダーゼ又はルシフェラーゼをコードする(11)に記載の方法。
(13)前記第1検定タンパク質をコードする前記ヌクレオチド配列が、前記第2検定タンパク質との相互作用を増加させるように改変されている(1)に記載の方法。
(14)前記改変が、前記第1検定タンパク質のC末端領域のヌクレオチド配列の全部又は一部を、元の配列よりも前記第2検定タンパク質に対する親和性の高いアミノ酸配列をコードするヌクレオチド配列によって置換することを含む(13)に記載の方法。
(15)前記C末端領域の前記ヌクレオチド配列が、AVPR2,AGTRLI,GRPR,F2PL1,CXCR2/IL−8B,CCR4又はGRPRのC末端領域の全部又は一部をコードするヌクレオチド配列によって置換されている(14)に記載の方法。
(16)1つ以上の検定化合物を複数の細胞サンプルに接触させる工程を含み、前記サンプルのそれぞれは、前記単数又は複数の前記化合物によって接触され、ここで、前記細胞サンプルのそれぞれが、(a)及び(b)によってトランスフォーム又はトランスフェクトされており、前記化合物のいずれかが前記特定のタンパク質/タンパク質相互作用を調節するか否かを測定するべく前記複数のサンプル中におけるレポーター遺伝子の活性を測定する工程を含む(1)に記載の方法。
(17)前記膜結合タンパク質が、β2−アドレナリン作動性レセプター(ADRB2)、アルギニンバソプレッシンレセプター2(AVPR2)、セロトニンレセプター1a(HTR1A)、m2ムスカリン性アセチルコリンレセプター(CHRM2)、ケモカイン(C−Cモチーフ)レセプター5(CCR5)、ドーパミンD2レセプター(DRD2)、カッパーオピオイドレセプター(OPRK)、又はADRA1Aである(2)に記載の方法。
(18)そのそれぞれがその他すべてと異なる1つの検定化合物と、前記サンプルのそれぞれを接触させる工程を含む(16)に記載の方法。
(19)前記サンプルのそれぞれを前記検定化合物の混合物と接触させる工程を含む(16)に記載の方法。
(20)検定化合物が単数又は複数の対象のタンパク質相互作用を調節するか否かを測定する方法であって、前記検定化合物を複数の細胞サンプルに接触させる工程であって、前記細胞サンプルのそれぞれが、
(a)以下を含む第1核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、
(ii)プロテアーゼのための開裂部位をコードするヌクレオチド配列、及び、
(iii)前記細胞内においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、
(b)以下を含む第2核酸分子、
(i)前記対象検定化合物の存在下における前記第1検定タンパク質との相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼをコードするヌクレオチド配列、によってトランスフォーム又はトランスフェクトされており、ここで、前記第1検定タンパク質は前記複数のサンプルのそれぞれにおいて他の第1検定タンパク質と異なる、工程、及び、
前記複数のサンプルのうちの1つ又は複数における前記レポーター遺伝子の活性を、単数又は複数の対象タンパク質の相互作用の調節の測定として測定する工程、を含む、
検定化合物が単数又は複数の対象のタンパク質相互作用を調節するか否かを測定する方法。
(21)前記第2検定タンパク質が、各サンプルにおいて異なる(20)に記載の方法。
(22)前記第2検定タンパク質が、各サンプルにおいて同じである(20)に記載の方法。
(23)前記サンプルのすべてが共通の容器内で組み合わせられ、そして、各サンプルが異なる対の第1検定タンパク質と第2検定タンパク質を含む(20)に記載の方法。
(24)各サンプルが、異なる容器内で検定される(20)に記載の方法。
(25)あるサンプル内の前記レポーター遺伝子が、他のサンプル内のレポーター遺伝子と異なる(20)に記載の方法。
(26)前記化合物の混合物が、生体試料を含む(19)に記載の方法。
(27)前記生体試料が、脳脊髄液、尿、血液、血清、膿汁、腹水、滑液、組織抽出物、又は浸出物である(26)に記載の方法。
(28)(a)以下を有する核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、
(ii)プロテアーゼ又はプロテアーゼの一部の開裂部位をコードするヌクレオチド配列、及び、
(iii)細胞中においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、そして、
(b)以下を有する核酸分子、
(i)前記検定化合物の存在下におけるその前記第1検定タンパク質との相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列、及び、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、
によってトランスフォーム又はトランスフェクトされている組換え細胞。
(29)前記核酸分子の一方又は両方が、前記細胞のゲノムに安定的に組み込みまれている(28)に記載の組換え細胞。
(30)前記細胞が、前記レポーター遺伝子によってトランスフォーム又はトランスフェクトされている(28)に記載の組換え細胞。
(31)前記第1検定タンパク質が、膜結合タンパク質である(28)に記載の組換え細胞。
(32)前記膜結合タンパク質が、膜貫通レセプターである(31)に記載の組換え細胞。
(33)前記膜貫通レセプターが、GPCRである(32)に記載の組換え細胞。 (34)前記プロテアーゼ又はプロテアーゼの一部が、タバコエッチ病ウイルス核内封入Aプロテアーゼである(28)に記載の組換え細胞。
(35)前記レポーター遺伝子を活性化する前記タンパク質が、転写因子である(28)に記載の組換え細胞。
(36)前記膜結合タンパク質が、ADBR2、AVPR2、HTR1A、CHRM2、CCR5、DRD2、又はOPRKである(31)に記載の組換え細胞。
(37)前記転写因子が、tTA又はGAL4である(28)に記載の組換え細胞。
(38)前記前記第2タンパク質が、抑制型タンパク質である(28)に記載の組換え細胞。
(39)前記抑制型タンパク質がアレスチンであり、前記第1タンパク質が膜貫通レセプターである(38)に記載の組換え細胞。
(40)前記細胞が、真核細胞である(28)に記載の組換え細胞。
(41)前記細胞が、原核細胞である(28)に記載の組換え細胞。
(42)前記レポーター遺伝子が、外来性遺伝子である(28)に記載の組換え細胞。
(43)前記外来性遺伝子が、β−ガラクトシダーゼ又はルシフェラーゼをコードする(42)に記載の組換え細胞。
(44)前記第1検定タンパク質をコードする前記ヌクレオチド配列が、前記第2タンパク質との相互作用を増加させるように改変されている(28)に記載の組換え細胞。
(45)前記改変が、前記第1検定タンパク質のC末端領域のヌクレオチド配列の全部又は一部を、元の配列よりも前記第2検定タンパク質に対する親和性の高いアミノ酸配列をコードするヌクレオチド配列によって置換することを含む(44)に記載の組換え細胞。
(46)前記C末端領域の前記ヌクレオチド配列が、AVPR2,AGTRLI,GRPR,F2PL1,CXCR2/IL−8B又は CC4のC末端領域をコードするヌクレオチド
配列によって置換されている(44)に記載の組換え細胞。
(47)(i)検定タンパク質をコードするヌクレオチド配列、
(ii)プロテアーゼ又はプロテアーゼの一部の開裂部位をコードするヌクレオチド配列、及び、
(iii)細胞内でレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、
を5’から3’の順番で含む単離核酸分子。
(48)前記検定タンパク質が、膜結合タンパク質である(47)に記載の単離核酸分子。
(49)前記膜結合タンパク質が、膜貫通レセプターである(48)に記載の単離核酸分子。
(50)前記膜貫通レセプターが、GPCRである(49)に記載の単離核酸分子。
(51)前記プロテアーゼ又はプロテアーゼの一部が、タバコエッチ病ウイルス核内封入Aプロテアーゼである(47)に記載の単離核酸分子。
(52)前記レポーター遺伝子を活性化する前記タンパク質が、転写因子である(47)に記載の単離核酸分子。
(53)前記転写因子が、tTA又はGAL4である(52)に記載の単離核酸分子。
(54)前記膜結合タンパク質が、ADBR2、AVPR2、HTR1A、CHRM2、CCR5、DRD2、又はOPRKである(48)に記載の単離核酸分子。
(55)(47)に記載の単離核酸分子を含み、プロモーターに操作連結されている発現ベクター。
(56)(i)検定化合物の存在下において別の検定タンパク質とのその相互作用が測定される検定タンパク質をコードするヌクレオチド配列、及び、
(ii)開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、
を含む単離核酸分子。
(57)前記検定タンパク質が、抑制型タンパク質である(56)に記載の単離核酸分子。
(58)前記抑制型タンパク質が、アレスチンである(57)に記載の単離核酸分子。
(59)(56)に記載の単離核酸分子を含み、プロモーターに操作連結されている発現ベクター。
(60)(47)に記載の単離核酸分子の発現によって生成される融合タンパク質。
(61)(56)に記載の単離核酸分子の発現によって生成される融合タンパク質。
(62)検定化合物が対象の特定のタンパク質/タンパク質相互作用を調節するか否かを測定するのに有用な検定キットであって、
(a)以下を含む核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、
(ii)プロテアーゼ又はプロテアーゼの一部の開裂部位をコードするヌクレオチド配列、
(iii)細胞内でレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、
(b)以下を含む核酸分子、
(i)前記検定化合物の存在下における前記第1検定タンパク質とのその相互作用が測定される第2検定タンパク質をコードするするヌクレオチド配列、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、そして、
(c)前記(a)及び(b)のそれぞれを互いに対して分離して保持するための容器手段、
それぞれの別部分を含む、検定化合物が対象の特定のタンパク質/タンパク質相互作用を調節するか否かを測定するのに有用な検定キット。
(63)前記第1検定タンパク質が、膜結合タンパク質である(62)に記載の検定キット。
(64)前記膜結合タンパク質が、膜貫通レセプターである(63)に記載の検定キット。
(65)前記膜貫通レセプターが、GPCRである(64)に記載の検定キット。
(66)前記プロテアーゼ又はプロテアーゼの一部が、タバコエッチ病ウイルス核内封入Aプロテアーゼである(62)に記載の検定キット。
(67)前記レポーター遺伝子を活性化する前記タンパク質が、転写因子である(62)に記載の検定キット。
(68)前記転写因子が、tTA又はGAL4である(67)に記載の検定キット。
(69)前記第2タンパク質が、抑制型タンパク質である(62)に記載の検定キット。
(70)前記抑制型タンパク質がアレスチンであり、前記第1タンパク質が膜貫通レセプターである(69)に記載の検定キット。
(71)レポーター遺伝子をコードする単離核酸分子の別部分を含む(61)に記載の検定キット。
(72)前記レポーター遺伝子が、β−ガラクトシダーゼ又はルシフェラーゼをコードする(71)に記載の検定キット。
(73)前記第1検定タンパク質をコードする前記ヌクレオチド配列が、前記第2タンパク質との相互作用を増加させるように改変されている(62)に記載の検定キット。
(74)前記改変が、前記第1検定タンパク質のC末端領域のヌクレオチド配列の全部又は一部を、元の配列よりも前記第2検定タンパク質に対する親和性の高いアミノ酸配列をコードするヌクレオチド配列によって置換することを含む(73)に記載の検定キット。
(75)前記C末端領域の前記ヌクレオチド配列が、AVPR2,AGTRLI,GRPR,F2RL1,CXCR2/IL−8B,又はCCR4をコードするヌクレオチド配列によって置換されている(74)に記載の検定キット。
(76)前記膜結合タンパク質が、ADRB2、AVPR2、HTR1A、CHRM2、CCR5、DRD2、又はOPRKである(63)に記載の検定キット。
Claims (17)
- 検定化合物が対象の第1検定タンパク質と第2検体タンパク質間の特定相互作用を調節するか否かを測定するための方法であって、以下でトランスフォーム又はトランスフェクトされた細胞に、前記検定化合物を接触させる工程、
(a)下記を含む核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、ここで、前記第1検定タンパク質は膜貫通レセプターである、
(ii)前記細胞によって内因的に発現されるものではないプロテアーゼ又はプロテアーゼの一部に対する開裂部位をコードするヌクレオチド配列、及び
(iii)前記細胞内においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、
ここで、開裂部位をコードする前記ヌクレオチド配列は、膜貫通レセプターをコードする前記ヌクレオチド配列と細胞内でレポーター遺伝子を活性化するタンパク質をコードする前記ヌクレオチド配列の間に位置する、そして、
(b)下記を含む核酸分子、
(i)前記検定化合物の存在下における、前記第1検定タンパク質との相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列、及び、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、
及び、前記検定化合物が前記第1検定タンパク質と第2検体タンパク質間の特定相互作用を調節するか否かの測定として、前記レポーター遺伝子の活性を測定する工程、とを含む、検定化合物が対象の第1検定タンパク質と第2検体タンパク質間の特定相互作用を調節するか否かを測定するための方法。 - 前記膜貫通レセプターが、GPCRである請求項1に記載の方法。
- 前記プロテアーゼ又はプロテアーゼの一部が、タバコエッチ病ウイルス核内封入Aプロテアーゼである請求項1に記載の方法。
- 前記レポーター遺伝子を活性化する前記タンパク質が、転写因子である請求項1に記載の方法。
- 前記転写因子が、tTA又はGAL4である請求項4に記載の方法。
- 前記第2検定タンパク質が、抑制型タンパク質である請求項1に記載の方法。
- 前記抑制型タンパク質がアレスチンである請求項6に記載の方法。
- 前記細胞が、真核細胞である請求項1に記載の方法。
- 前記レポーター遺伝子が、外来性遺伝子である請求項1に記載の方法。
- 前記外来性遺伝子が、β−ガラクトシダーゼ又はルシフェラーゼをコードする請求項9に記載の方法。
- 前記検定化合物が、前記第1検定タンパク質のリガンドである請求項1に記載の方法。
- 前記検定化合物が、前記第1検定タンパク質のアゴニストである請求項1に記載の方法。
- 検定化合物が単数又は複数の対象のタンパク質相互作用を調節するか否かを測定する方法であって、前記検定化合物を複数の細胞サンプルに接触させる工程であって、前記細胞サンプルのそれぞれが、
(a)以下を含む第1核酸分子、
(i)第1検定タンパク質をコードするヌクレオチド配列、ここで、前記第1検定タンパク質は膜貫通レセプターである、
(ii)細胞によって内因的に発現するものではないプロテアーゼ又はプロテアーゼの一部に対する開裂部位をコードするヌクレオチド配列、及び、
(iii)前記細胞内においてレポーター遺伝子を活性化するタンパク質をコードするヌクレオチド配列、
ここで、開裂部位をコードする前記ヌクレオチド配列は、膜貫通レセプターをコードする前記ヌクレオチド配列と細胞内でレポーター遺伝子を活性化するタンパク質をコードする前記ヌクレオチド配列の間に位置する、そして、
(b)以下を含む第2核酸分子、
(i)前記対象検定化合物の存在下における前記第1検定タンパク質との相互作用が測定される第2検定タンパク質をコードするヌクレオチド配列、
(ii)前記開裂部位に対して特異的なプロテアーゼ又はプロテアーゼの一部をコードするヌクレオチド配列、によってトランスフォーム又はトランスフェクトされており、ここで、前記第1検定タンパク質は前記複数のサンプルのそれぞれにおいて他の第1検定タンパク質と異なる、工程、及び、
前記複数のサンプルのうちの1つ又は複数における前記レポーター遺伝子の活性を、単数又は複数の対象タンパク質の相互作用の調節の測定として測定する工程、を含む、検定化合物が単数又は複数の対象のタンパク質相互作用を調節するか否かを測定する方法。 - 前記第2検定タンパク質が、各サンプルにおいて異なる請求項13に記載の方法。
- 前記第2検定タンパク質が、各サンプルにおいて同じである請求項13に記載の方法。
- 前記サンプルのすべてが共通の容器内で組み合わせられ、そして、各サンプルが異なる対の第1検定タンパク質と第2検定タンパク質を含む請求項13に記載の方法。
- 前記各サンプルが、異なる容器内で検定される請求項13に記載の方法。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US48596803P | 2003-07-09 | 2003-07-09 | |
| US60/485,968 | 2003-07-09 | ||
| US51191803P | 2003-10-15 | 2003-10-15 | |
| US60/511,918 | 2003-10-15 | ||
| US56611304P | 2004-04-27 | 2004-04-27 | |
| US60/566,113 | 2004-04-27 | ||
| PCT/US2004/021887 WO2005007822A2 (en) | 2003-07-09 | 2004-07-09 | Method for assaying protein-protein interaction |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2007528713A JP2007528713A (ja) | 2007-10-18 |
| JP2007528713A5 JP2007528713A5 (ja) | 2007-12-13 |
| JP4734498B2 true JP4734498B2 (ja) | 2011-07-27 |
Family
ID=34084516
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006518902A Active JP4734498B2 (ja) | 2003-07-09 | 2004-07-09 | タンパク質−タンパク質相互作用を解析する方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US7049076B2 (ja) |
| EP (2) | EP1644734B1 (ja) |
| JP (1) | JP4734498B2 (ja) |
| CN (1) | CN1894581B (ja) |
| AT (1) | ATE534900T1 (ja) |
| AU (1) | AU2004257228B8 (ja) |
| CA (1) | CA2531698A1 (ja) |
| IL (1) | IL173023A0 (ja) |
| WO (1) | WO2005007822A2 (ja) |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070224615A1 (en) * | 2003-07-09 | 2007-09-27 | Invitrogen Corporation | Methods for assaying protein-protein interactions |
| CA2531698A1 (en) * | 2003-07-09 | 2005-01-27 | Sentigen Biosciences, Inc. | Method for assaying protein-protein interaction |
| EP1893627A4 (en) * | 2005-05-27 | 2009-11-11 | Sentigen Biosciences Inc | MULTIPLEXARRAY SUITABLE FOR THE INVESTIGATION OF PROTEIN-PROTEIN INTERACTIONS |
| DK1915617T3 (da) * | 2005-07-21 | 2011-11-21 | Aebi Ltd | Fremgangsmåder og sammensætninger til identifikation af et peptid, der har en intermolekylær interaktion med et interessemål |
| US20070218456A1 (en) * | 2006-02-08 | 2007-09-20 | Invitrogen Corporation | Cellular assays for signaling receptors |
| JP2009528545A (ja) * | 2006-03-02 | 2009-08-06 | ザ ユーエービー リサーチ ファウンデーション | マイコバクテリウム属の疾患検出、処置、および薬物開発 |
| ATE528647T1 (de) * | 2006-03-16 | 2011-10-15 | Life Technologies Corp | Verfahren zur untersuchung von protein-protein- interaktionen |
| WO2007149807A1 (en) * | 2006-06-20 | 2007-12-27 | Invitrogen Corporation | Methods for identifying modifiers of gpr1 activity |
| EP2078037A4 (en) | 2006-11-10 | 2010-01-27 | Dimerix Bioscience Pty Ltd | HETERODIMERS / OLIGOMERS OF THE RECEPTOR FOR THE THYROTROPIN RELEASING HORMONE OF THE OREXIN RECEPTOR |
| US9026409B2 (en) | 2007-08-06 | 2015-05-05 | Design Ready Controls, Inc. | Systems, methods, and software for automated design and manufacturing of HVAC control panels |
| CN102187225B (zh) * | 2007-09-04 | 2015-08-05 | 塞诺菲-安万特股份有限公司 | 使用蛋白酶活化的受体鉴别调节蛋白质-蛋白质相互作用的分子 |
| FR2934684B1 (fr) | 2008-07-31 | 2012-11-16 | Cis Bio Int | Methode de detection de l'internalisation de proteines membranaires. |
| EP2344676A1 (en) * | 2008-09-25 | 2011-07-20 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Combinatorial synthesis and use of libraries of short expressed nucleic acid sequences for the analysis of cellular events |
| JP5586285B2 (ja) * | 2009-03-18 | 2014-09-10 | オリンパス株式会社 | 受容体相互作用検出方法およびサイクリックampセンサータンパク質 |
| CA2821985C (en) | 2011-01-11 | 2019-07-09 | Dimerix Bioscience Pty Ltd | Combination therapy |
| GB201103453D0 (en) | 2011-03-01 | 2011-04-13 | Vib Vzw | Kinase substrate sensor |
| TW201302779A (zh) | 2011-04-13 | 2013-01-16 | Glaxosmithkline Biolog Sa | 融合蛋白質及組合疫苗 |
| US9804160B2 (en) | 2011-09-28 | 2017-10-31 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Protein-protein interaction as biomarkers |
| WO2014153044A1 (en) * | 2013-03-14 | 2014-09-25 | Temple University Of The Commonwealth System Of Higher Education | Treatment of patients with hyponatremia and cardiac disease |
| KR20150130283A (ko) * | 2013-03-15 | 2015-11-23 | 더 트러스티스 오브 더 유니버시티 오브 펜실바니아 | 생체분자 보조제를 갖는 백신 |
| GB201310008D0 (en) | 2013-06-05 | 2013-07-17 | Glaxosmithkline Biolog Sa | Immunogenic composition for use in therapy |
| KR101733609B1 (ko) * | 2014-02-07 | 2017-05-08 | 한국생명공학연구원 | 단백질 융합 디스플레이 기술을 이용한 물질 간 상호작용 고속분석 방법 |
| US10619155B2 (en) * | 2015-03-17 | 2020-04-14 | Brown University | Methods for labeling and manipulating a cellular circuit |
| CN104991072B (zh) * | 2015-06-16 | 2017-03-29 | 西北农林科技大学 | 一种昆虫体外蛋白质相互作用检测系统的制备方法及应用 |
| BR112018013663A2 (pt) | 2016-01-11 | 2019-01-22 | Univ Leland Stanford Junior | proteínas quiméricas e métodos de imunoterapia |
| MY196175A (en) * | 2016-01-11 | 2023-03-20 | Univ Leland Stanford Junior | Chimeric Proteins And Methods Of Regulating Gene Expression |
| GB201609604D0 (en) * | 2016-06-01 | 2016-07-13 | Ucl Business Plc | Cell |
| CN107976411B (zh) * | 2016-10-25 | 2020-10-23 | 中国科学院微生物研究所 | 包含别构转录因子调控系统的生物传感器、试剂盒及其在小分子检测中的用途 |
| WO2019062744A1 (zh) * | 2017-09-27 | 2019-04-04 | 北京大学 | 融合多肽 |
| CN108191979B (zh) * | 2017-12-08 | 2021-01-01 | 上海晶诺生物科技有限公司 | 一种荧光互补检测人趋化因子生物学活性的方法 |
| US20210310039A1 (en) * | 2018-07-31 | 2021-10-07 | The University Of Tokyo | Membrane protein activity measurement method |
| CN110853712B (zh) * | 2018-08-01 | 2022-06-07 | 清华大学 | 鉴定多对生物分子间相互作用调控因子的方法 |
| WO2020080891A1 (ko) * | 2018-10-19 | 2020-04-23 | 주식회사 프로티나 | 유방암 재발 예측 방법 |
| JP2022513606A (ja) * | 2018-12-10 | 2022-02-09 | イエール ユニバーシティ | 宿主の生理機能を形成する微生物叢代謝産物 |
| WO2022271264A1 (en) * | 2021-06-21 | 2022-12-29 | Massachusetts Institute Of Technology | Real-time g-protein coupled receptor (gpcr) linked bioluminescent sensing of biological targets and processes |
Family Cites Families (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3737901A (en) | 1971-05-03 | 1973-06-05 | Sierra Research Corp | Redundant aircraft clock synchronization |
| JPS57139012A (en) | 1981-02-23 | 1982-08-27 | Sankyo Co Ltd | Anthelmintic composition |
| NL8200523A (nl) | 1982-02-11 | 1983-09-01 | Univ Leiden | Werkwijze voor het in vitro transformeren van planteprotoplasten met plasmide-dna. |
| US4879236A (en) | 1984-05-16 | 1989-11-07 | The Texas A&M University System | Method for producing a recombinant baculovirus expression vector |
| US5168062A (en) | 1985-01-30 | 1992-12-01 | University Of Iowa Research Foundation | Transfer vectors and microorganisms containing human cytomegalovirus immediate-early promoter-regulatory DNA sequence |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US5168061A (en) * | 1986-05-15 | 1992-12-01 | Board Of Regents, The University Of Texas System | Human chorionic peptidase-1 |
| US4952500A (en) | 1988-02-01 | 1990-08-28 | University Of Georgia Research Foundation, Inc. | Cloning systems for Rhodococcus and related bacteria |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US5283173A (en) | 1990-01-24 | 1994-02-01 | The Research Foundation Of State University Of New York | System to detect protein-protein interactions |
| US5284746A (en) | 1990-02-08 | 1994-02-08 | Zymogenetics, Inc. | Methods of producing hybrid G protein-coupled receptors |
| US5384253A (en) | 1990-12-28 | 1995-01-24 | Dekalb Genetics Corporation | Genetic transformation of maize cells by electroporation of cells pretreated with pectin degrading enzymes |
| WO1993004169A1 (en) | 1991-08-20 | 1993-03-04 | Genpharm International, Inc. | Gene targeting in animal cells using isogenic dna constructs |
| US5439924A (en) | 1991-12-23 | 1995-08-08 | Virbac, Inc. | Systemic control of parasites |
| US5702932A (en) | 1992-07-20 | 1997-12-30 | University Of Florida | Microinjection methods to transform arthropods with exogenous DNA |
| DE4228457A1 (de) | 1992-08-27 | 1994-04-28 | Beiersdorf Ag | Herstellung von heterodimerem PDGF-AB mit Hilfe eines bicistronischen Vektorsystems in Säugerzellen |
| US5464758A (en) | 1993-06-14 | 1995-11-07 | Gossen; Manfred | Tight control of gene expression in eucaryotic cells by tetracycline-responsive promoters |
| US5814618A (en) | 1993-06-14 | 1998-09-29 | Basf Aktiengesellschaft | Methods for regulating gene expression |
| US5491084A (en) | 1993-09-10 | 1996-02-13 | The Trustees Of Columbia University In The City Of New York | Uses of green-fluorescent protein |
| US5656610A (en) | 1994-06-21 | 1997-08-12 | University Of Southern California | Producing a protein in a mammal by injection of a DNA-sequence into the tongue |
| FR2722208B1 (fr) | 1994-07-05 | 1996-10-04 | Inst Nat Sante Rech Med | Nouveau site interne d'entree des ribosomes, vecteur le contenant et utilisation therapeutique |
| US5871986A (en) | 1994-09-23 | 1999-02-16 | The General Hospital Corporation | Use of a baculovirus to express and exogenous gene in a mammalian cell |
| US5736524A (en) | 1994-11-14 | 1998-04-07 | Merck & Co.,. Inc. | Polynucleotide tuberculosis vaccine |
| NZ272574A (en) | 1995-07-14 | 1999-02-25 | Lilly Eli & Co Nz Ltd | Aqueous base suspension concentrate containing at least one ionophore antibiotic and wetting agent and/or a surfactant and xanthan gum optionally with a suspension agent, an antifreeze agent and an antifoaming agent; drench for veterinary treatment |
| US5780448A (en) | 1995-11-07 | 1998-07-14 | Ottawa Civic Hospital Loeb Research | DNA-based vaccination of fish |
| WO1997020931A1 (en) | 1995-12-08 | 1997-06-12 | The Government Of The United States Of America, Represented By The Secretary, Department Of Health And Human Services | Method and compositions for monitoring dna binding molecules in living cells |
| US5773422A (en) | 1996-01-29 | 1998-06-30 | Komer; Gene | Avermectin formulation |
| US5928906A (en) | 1996-05-09 | 1999-07-27 | Sequenom, Inc. | Process for direct sequencing during template amplification |
| EP0959891A1 (en) | 1996-07-30 | 1999-12-01 | Ashmont Holdings Limited | Anthelmintic formulations |
| US5945100A (en) | 1996-07-31 | 1999-08-31 | Fbp Corporation | Tumor delivery vehicles |
| US5981274A (en) | 1996-09-18 | 1999-11-09 | Tyrrell; D. Lorne J. | Recombinant hepatitis virus vectors |
| FR2753377B1 (fr) | 1996-09-19 | 1999-09-24 | Rhone Merieux | Nouvelle association parasiticide a base de 1-n-phenylpyra- zoles et de lactones macrocycliques endectocides |
| DE19654079A1 (de) | 1996-12-23 | 1998-06-25 | Bayer Ag | Endo-ekto-parasitizide Mittel |
| US5891646A (en) | 1997-06-05 | 1999-04-06 | Duke University | Methods of assaying receptor activity and constructs useful in such methods |
| US6528271B1 (en) | 1997-06-05 | 2003-03-04 | Duke University | Inhibition of βarrestin mediated effects prolongs and potentiates opioid receptor-mediated analgesia |
| US7128915B2 (en) | 1997-09-18 | 2006-10-31 | Research Development Foundation | Membrane virus host range mutations and their uses as vaccine substrates |
| US5994624A (en) | 1997-10-20 | 1999-11-30 | Cotton Incorporated | In planta method for the production of transgenic plants |
| TR200001313T2 (tr) | 1997-11-10 | 2002-06-21 | The General Hospital Corporation | Protein etkileşimlerini ve fonksiyonel ilişkileri kaydeden tarama sistemleri |
| US6884870B2 (en) | 1998-03-20 | 2005-04-26 | California Institute Of Technology | Fusion proteins for identifying proteases, protease target sites and regulators of protease activity in living cells |
| US6117639A (en) * | 1998-08-31 | 2000-09-12 | Vertex Pharmaceuticals Incorporated | Fusion proteins, DNA molecules, vectors, and host cells useful for measuring protease activity |
| US6893827B1 (en) * | 2000-02-07 | 2005-05-17 | Applera Corporation | Receptor function assay for G-protein coupled receptors and orphan receptors by reporter enzyme mutant complementation |
| US20030157553A1 (en) | 2000-03-03 | 2003-08-21 | Gabriel Berstein | Methods of assaying for G protein-coupled receptor ligands and modulators |
| US6333167B1 (en) | 2000-03-10 | 2001-12-25 | American Home Products Corp. | Methods and reagents for identifying inhibitors of proteolysis of membrane-associated proteins |
| US7018812B2 (en) | 2000-11-03 | 2006-03-28 | Duke University | Modified G-protein coupled receptors |
| EP1205191A1 (en) | 2000-11-13 | 2002-05-15 | Centre National De La Recherche Scientifique | Targeted modification of intracellular compounds |
| US6828112B2 (en) * | 2001-01-04 | 2004-12-07 | Myriad Genetics, Inc. | Method of detecting protein-protein interactions |
| US20030013137A1 (en) | 2001-03-13 | 2003-01-16 | Barak Larry S. | Automated methods of detecting receptor activity |
| EP1421210A4 (en) | 2001-07-31 | 2005-02-16 | Clontech Lab Inc | METHOD FOR DETECTING PROTEASE ACTIVITY IN ONE CELL |
| DE10211063A1 (de) * | 2002-03-13 | 2003-10-09 | Axaron Bioscience Ag | Neue Verfahren zur Detektion und Analyse von Protein-Interaktionen in vivo |
| CA2492008C (en) * | 2002-03-29 | 2012-06-26 | Xoma Technology Ltd. | Multigenic vectors plasmids and methods for increasing expression of recombinant polypeptides |
| EP1353182A3 (en) | 2002-04-12 | 2004-02-04 | Smithkline Beecham Corporation | Method of predicting cell-based assay results using binding profiles |
| US7001889B2 (en) | 2002-06-21 | 2006-02-21 | Merial Limited | Anthelmintic oral homogeneous veterinary pastes |
| KR100890579B1 (ko) * | 2002-08-19 | 2009-04-27 | 프로테온 주식회사 | Rna 결합 단백질의 유전자를 융합파트너로 이용한재조합 단백질의 제조방법 |
| DE60325640D1 (de) * | 2002-10-25 | 2009-02-12 | Mds Analytical Technologies Us | Verfahren zur identifizierung von transmembranrezeptoragonisten mit reduzierter internalisierung |
| CA2531698A1 (en) | 2003-07-09 | 2005-01-27 | Sentigen Biosciences, Inc. | Method for assaying protein-protein interaction |
-
2004
- 2004-07-09 CA CA002531698A patent/CA2531698A1/en not_active Abandoned
- 2004-07-09 WO PCT/US2004/021887 patent/WO2005007822A2/en active Application Filing
- 2004-07-09 AT AT04756784T patent/ATE534900T1/de active
- 2004-07-09 EP EP04756784A patent/EP1644734B1/en active Active
- 2004-07-09 JP JP2006518902A patent/JP4734498B2/ja active Active
- 2004-07-09 CN CN2004800248641A patent/CN1894581B/zh active Active
- 2004-07-09 AU AU2004257228A patent/AU2004257228B8/en active Active
- 2004-07-09 US US10/888,313 patent/US7049076B2/en active Active
- 2004-07-09 EP EP10186070A patent/EP2336768A1/en not_active Withdrawn
-
2006
- 2006-01-08 IL IL173023A patent/IL173023A0/en unknown
- 2006-02-02 US US11/346,759 patent/US8017398B2/en active Active
-
2011
- 2011-08-18 US US13/212,965 patent/US20120077706A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| IL173023A0 (en) | 2006-06-11 |
| CN1894581B (zh) | 2012-02-01 |
| CN1894581A (zh) | 2007-01-10 |
| EP2336768A1 (en) | 2011-06-22 |
| US7049076B2 (en) | 2006-05-23 |
| CA2531698A1 (en) | 2005-01-27 |
| EP1644734B1 (en) | 2011-11-23 |
| US8017398B2 (en) | 2011-09-13 |
| JP2007528713A (ja) | 2007-10-18 |
| US20050100934A1 (en) | 2005-05-12 |
| EP1644734A4 (en) | 2007-04-25 |
| AU2004257228A1 (en) | 2005-01-27 |
| ATE534900T1 (de) | 2011-12-15 |
| AU2004257228B2 (en) | 2008-12-18 |
| EP1644734A2 (en) | 2006-04-12 |
| EP2336768A9 (en) | 2011-08-10 |
| WO2005007822A2 (en) | 2005-01-27 |
| US20060147975A1 (en) | 2006-07-06 |
| AU2004257228B8 (en) | 2009-01-08 |
| WO2005007822A3 (en) | 2005-03-31 |
| US20120077706A1 (en) | 2012-03-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4734498B2 (ja) | タンパク質−タンパク質相互作用を解析する方法 | |
| JP5618829B2 (ja) | プロテアーゼ活性化レポーターを使用してのタンパク質−タンパク質相互作用を調節する分子の同定 | |
| WO2007149807A1 (en) | Methods for identifying modifiers of gpr1 activity | |
| US20070224615A1 (en) | Methods for assaying protein-protein interactions | |
| EP2002021B1 (en) | Methods for assaying protein-protein interaction | |
| WO2007032793A1 (en) | Multiplex array useful for assaying protein-protein interaction | |
| US8148110B2 (en) | Detection of molecular interactions by β-lactamase reporter fragment complementation | |
| AU2013229528A1 (en) | Membrane span-kinase fusion protein and the uses thereof | |
| WO2007002641A2 (en) | Method for identifying cart receptor and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071018 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100422 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100722 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100729 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100810 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100930 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101227 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110127 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20110228 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110228 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110316 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4734498 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140513 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |