JP4570870B2 - 心血管安全性アッセイ - Google Patents
心血管安全性アッセイ Download PDFInfo
- Publication number
- JP4570870B2 JP4570870B2 JP2003512705A JP2003512705A JP4570870B2 JP 4570870 B2 JP4570870 B2 JP 4570870B2 JP 2003512705 A JP2003512705 A JP 2003512705A JP 2003512705 A JP2003512705 A JP 2003512705A JP 4570870 B2 JP4570870 B2 JP 4570870B2
- Authority
- JP
- Japan
- Prior art keywords
- herg
- astemizole
- fragment
- channel
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000003556 assay Methods 0.000 title abstract description 49
- 230000002526 effect on cardiovascular system Effects 0.000 title description 7
- 150000001875 compounds Chemical class 0.000 claims abstract description 138
- 101001047090 Homo sapiens Potassium voltage-gated channel subfamily H member 2 Proteins 0.000 claims abstract description 130
- 102100022807 Potassium voltage-gated channel subfamily H member 2 Human genes 0.000 claims abstract description 70
- GXDALQBWZGODGZ-UHFFFAOYSA-N astemizole Chemical compound C1=CC(OC)=CC=C1CCN1CCC(NC=2N(C3=CC=CC=C3N=2)CC=2C=CC(F)=CC=2)CC1 GXDALQBWZGODGZ-UHFFFAOYSA-N 0.000 claims abstract description 46
- 229960004754 astemizole Drugs 0.000 claims abstract description 42
- 238000012216 screening Methods 0.000 claims abstract description 24
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 14
- 230000003993 interaction Effects 0.000 claims abstract description 11
- 239000012634 fragment Substances 0.000 claims description 48
- 238000000034 method Methods 0.000 claims description 37
- 239000012528 membrane Substances 0.000 claims description 31
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 30
- 238000002360 preparation method Methods 0.000 claims description 28
- 230000027455 binding Effects 0.000 claims description 27
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 23
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 22
- 108090000623 proteins and genes Proteins 0.000 claims description 22
- 102000004169 proteins and genes Human genes 0.000 claims description 21
- 229920001184 polypeptide Polymers 0.000 claims description 20
- 230000000694 effects Effects 0.000 claims description 14
- 238000011534 incubation Methods 0.000 claims description 11
- 206010003119 arrhythmia Diseases 0.000 claims description 10
- 239000000203 mixture Substances 0.000 claims description 9
- 239000007787 solid Substances 0.000 claims description 8
- 230000001939 inductive effect Effects 0.000 claims description 7
- 238000000926 separation method Methods 0.000 claims description 6
- 238000001914 filtration Methods 0.000 claims description 5
- 239000003153 chemical reaction reagent Substances 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- 238000006243 chemical reaction Methods 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 239000002904 solvent Substances 0.000 claims description 2
- 125000003275 alpha amino acid group Chemical group 0.000 claims 11
- 230000017858 demethylation Effects 0.000 claims 1
- 238000010520 demethylation reaction Methods 0.000 claims 1
- INQOMBQAUSQDDS-RLXJOQACSA-N iodo(tritritio)methane Chemical compound [3H]C([3H])([3H])I INQOMBQAUSQDDS-RLXJOQACSA-N 0.000 claims 1
- 238000012360 testing method Methods 0.000 abstract description 38
- 239000003814 drug Substances 0.000 abstract description 19
- 206010048610 Cardiotoxicity Diseases 0.000 abstract description 15
- 231100000259 cardiotoxicity Toxicity 0.000 abstract description 15
- 238000011161 development Methods 0.000 abstract description 6
- 210000004027 cell Anatomy 0.000 description 45
- 150000001413 amino acids Chemical group 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 239000000243 solution Substances 0.000 description 18
- 108091033319 polynucleotide Proteins 0.000 description 13
- 102000040430 polynucleotide Human genes 0.000 description 13
- 239000002157 polynucleotide Substances 0.000 description 13
- 238000000159 protein binding assay Methods 0.000 description 13
- 229940079593 drug Drugs 0.000 description 12
- 238000013537 high throughput screening Methods 0.000 description 12
- 238000002474 experimental method Methods 0.000 description 11
- 150000007523 nucleic acids Chemical class 0.000 description 8
- 238000001514 detection method Methods 0.000 description 7
- 102000039446 nucleic acids Human genes 0.000 description 7
- 108020004707 nucleic acids Proteins 0.000 description 7
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- 208000018452 Torsade de pointes Diseases 0.000 description 6
- 208000002363 Torsades de Pointes Diseases 0.000 description 6
- 229960002994 dofetilide Drugs 0.000 description 6
- 108091006146 Channels Proteins 0.000 description 5
- 229940024606 amino acid Drugs 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- LAGYWHSFHIMTPE-UHFFFAOYSA-N desmethylastemizole Chemical compound C1=CC(O)=CC=C1CCN1CCC(NC=2N(C3=CC=CC=C3N=2)CC=2C=CC(F)=CC=2)CC1 LAGYWHSFHIMTPE-UHFFFAOYSA-N 0.000 description 5
- BRZYSWJRSDMWLG-CAXSIQPQSA-N geneticin Chemical compound O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](C(C)O)O2)N)[C@@H](N)C[C@H]1N BRZYSWJRSDMWLG-CAXSIQPQSA-N 0.000 description 5
- 238000012188 high-throughput screening assay Methods 0.000 description 5
- 238000003345 scintillation counting Methods 0.000 description 5
- 238000002821 scintillation proximity assay Methods 0.000 description 5
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 210000000170 cell membrane Anatomy 0.000 description 4
- 239000002299 complementary DNA Substances 0.000 description 4
- IXTMWRCNAAVVAI-UHFFFAOYSA-N dofetilide Chemical group C=1C=C(NS(C)(=O)=O)C=CC=1CCN(C)CCOC1=CC=C(NS(C)(=O)=O)C=C1 IXTMWRCNAAVVAI-UHFFFAOYSA-N 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 3
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000011324 bead Substances 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 229960003276 erythromycin Drugs 0.000 description 3
- 239000008103 glucose Substances 0.000 description 3
- 230000009871 nonspecific binding Effects 0.000 description 3
- FYPMFJGVHOHGLL-UHFFFAOYSA-N probucol Chemical compound C=1C(C(C)(C)C)=C(O)C(C(C)(C)C)=CC=1SC(C)(C)SC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FYPMFJGVHOHGLL-UHFFFAOYSA-N 0.000 description 3
- 229960003912 probucol Drugs 0.000 description 3
- 230000002285 radioactive effect Effects 0.000 description 3
- 239000002287 radioligand Substances 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- GZKLJWGUPQBVJQ-UHFFFAOYSA-N sertindole Chemical compound C1=CC(F)=CC=C1N1C2=CC=C(Cl)C=C2C(C2CCN(CCN3C(NCC3)=O)CC2)=C1 GZKLJWGUPQBVJQ-UHFFFAOYSA-N 0.000 description 3
- 229960000652 sertindole Drugs 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 229960000351 terfenadine Drugs 0.000 description 3
- UISARWKNNNHPGI-UHFFFAOYSA-N terodiline Chemical compound C=1C=CC=CC=1C(CC(C)NC(C)(C)C)C1=CC=CC=C1 UISARWKNNNHPGI-UHFFFAOYSA-N 0.000 description 3
- 229960005383 terodiline Drugs 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 229920000858 Cyclodextrin Polymers 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 239000003416 antiarrhythmic agent Substances 0.000 description 2
- 230000003111 delayed effect Effects 0.000 description 2
- 230000002999 depolarising effect Effects 0.000 description 2
- 230000029087 digestion Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 238000002866 fluorescence resonance energy transfer Methods 0.000 description 2
- 238000012203 high throughput assay Methods 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 238000010369 molecular cloning Methods 0.000 description 2
- 230000010412 perfusion Effects 0.000 description 2
- 238000003752 polymerase chain reaction Methods 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 238000002953 preparative HPLC Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000002336 repolarization Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- DZZWHBIBMUVIIW-DTORHVGOSA-N sparfloxacin Chemical compound C1[C@@H](C)N[C@@H](C)CN1C1=C(F)C(N)=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1F DZZWHBIBMUVIIW-DTORHVGOSA-N 0.000 description 2
- 229960004954 sparfloxacin Drugs 0.000 description 2
- -1 sparfloxain Chemical compound 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- AWQSAIIDOMEEOD-UHFFFAOYSA-N 5,5-Dimethyl-4-(3-oxobutyl)dihydro-2(3H)-furanone Chemical compound CC(=O)CCC1CC(=O)OC1(C)C AWQSAIIDOMEEOD-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 241000700199 Cavia porcellus Species 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 102000013975 Delayed Rectifier Potassium Channels Human genes 0.000 description 1
- 108010050556 Delayed Rectifier Potassium Channels Proteins 0.000 description 1
- 206010013710 Drug interaction Diseases 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 102000004257 Potassium Channel Human genes 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 108010039491 Ricin Proteins 0.000 description 1
- 238000012300 Sequence Analysis Methods 0.000 description 1
- 238000003646 Spearman's rank correlation coefficient Methods 0.000 description 1
- 206010047281 Ventricular arrhythmia Diseases 0.000 description 1
- QUWIRVHHVVOBPE-UHFFFAOYSA-N acetonitrile;n-propan-2-ylpropan-2-amine;hydrate Chemical compound O.CC#N.CC(C)NC(C)C QUWIRVHHVVOBPE-UHFFFAOYSA-N 0.000 description 1
- 230000036982 action potential Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000001286 analytical centrifugation Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003288 anthiarrhythmic effect Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000005388 borosilicate glass Substances 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 210000002318 cardia Anatomy 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000012707 chemical precursor Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000012411 cloning technique Methods 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 125000000950 dibromo group Chemical group Br* 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 239000003596 drug target Substances 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000011067 equilibration Methods 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 238000012854 evaluation process Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 238000013213 extrapolation Methods 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 210000001320 hippocampus Anatomy 0.000 description 1
- 238000000265 homogenisation Methods 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000000670 ligand binding assay Methods 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000012402 patch clamp technique Methods 0.000 description 1
- 239000000816 peptidomimetic Substances 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 229920000729 poly(L-lysine) polymer Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 108020001213 potassium channel Proteins 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 210000001567 regular cardiac muscle cell of ventricle Anatomy 0.000 description 1
- 238000013391 scatchard analysis Methods 0.000 description 1
- 238000007423 screening assay Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000012085 test solution Substances 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 238000012036 ultra high throughput screening Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5014—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing toxicity
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/58—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances
- G01N33/60—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances involving radioactive labelled substances
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6887—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids from muscle, cartilage or connective tissue
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/32—Cardiovascular disorders
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Tropical Medicine & Parasitology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Plant Substances (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Plural Heterocyclic Compounds (AREA)
- Sampling And Sample Adjustment (AREA)
Description
数種の薬剤は、心臓の再分極(すなわち、表面心電図のQT間隔として「測定される」)を、特に過剰投与または薬物動態学的相互作用の場合に生命を脅かす可能性がある心室不整脈(ventricular arrhythmias)、例えばトルサード・ド・ポワント(TdP)が起こり得る程度まで延長し得るという証拠が得られた。
W.Haverkamp et al.(2000) Cardiovascular Research 47,219−233) Dall’Asta V.et al.(1997) Exp.Cell.Research 231,260−268) Dascal N.(1987) Crit.Rev.Biochem 22,341−356) Zhou Z.et al.(1998) Biophysical Journal 74,230−241 Chadwick C.et al.,(1993)Circulation Research,72,707−714)
本発明は、個体に心臓毒性を誘導する能力について試験化合物をスクリーニングするためのアッセイを提供し、該方法はHERGまたはその断片を含む供給源を、参照化合物および試験化合物と、参照化合物および試験化合物がHERGポリペプチドチャンネルに結合できる十分な時間インキューベーションし、そしてHERGに結合した参照化合物の量に及ぼす試験化合物の効果を測定することを含んでなる。
a)表面に配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物を、標識した参照化合物と、参照化合物のHERGポリペプチドチャンネルへの結合を可能とする十分な時間接触させ;
b)表面に配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物を、試験化合物と一緒に工程a)の標識した参照化合物と、参照化合物および試験化合物のHERGポリペプチドチャンネルへの結合を可能とする十分な時間接触させ;
c)工程a)でHERGチャンネルへ結合した標識した参照化合物の量を測定し;
d)工程b)でHERGチャンネルへ結合した標識した参照化合物の量を測定し;そしてe)工程a)で測定したHERGチャンネルへ結合した標識した参照化合物の量と、工程b)で測定したHERGポリペプチドチャンネルへ結合した標識した参照化合物の量とを比較することを含んでなる。
詳細な記述
本発明は心血管の安全性アッセイの分野に関し、そして個体に心臓毒性を誘導する能力について試験化合物をスクリーニングするためのアッセイおよびキットを提供する。該アッセイおよびキットは、アステミゾールとHERGカリウムチャンネルとの相互作用を、新規治療薬および他の作用物質の開発中に化合物の心臓毒性を予測すために活用することができるという知見に基づく。本発明は化学化合物ライブラリーの高処理量スクリーニングに特に有利な用途がある。
アッセイ
本発明のアッセイは、ポリペプチドチャンネルに結合する化合物をスクリーニングするために当該技術分野で一般的に知られている多くの形式で設計することができる。
i)近接検出アッセイに参加することができる第1標識で標識したHERG;
ii)近接検出アッセイに参加することができる第2標識で標識した参照化合物:
iii)工程i)のHERGおよび工程ii)の参照化合物を試験化合物と一緒に、参照化合物および試験化合物のHERGへの結合を可能とする十分な時間接触させ;そして
iv)工程i)のHERGと工程ii)の参照化合物との間の相互作用を、HERGおよび参照化合物が相互作用した時に第1標識と第2標識の近接により検出することを含んでなる。
a)HERGポリペプチドチャンネルとアステミゾールとの結合部位の構造にプローブを付け;
b)結合中にアステミゾールと相互作用するHERGポリペプチドチャンネルの結合部位の接触する原子を同定し;
c)(b)で同定した原子と相互作用する試験化合物を設計してHERG−アステミゾール相互作用に影響を及ぼし;そして
d)該設計した試験化合物を、HERGまたはその断片を含む供給源と接触させて、該化合物がHERGへ結合した標識したアステミゾールの量に影響を与える能力を測定する、ことにより、前述の結合に影響を及ぼす化合物の構造に基づく、または合理的な設計法に使用することもできると容易に考えるだろう。
キット
本発明は上記アッセイに使用することができるキットも提供する。1つの態様では、キットはa)HERGを含む供給源;b)参照化合物を含んでなる。
HERG cDNA(Genbank寄託番号:U04270(配列番号1))をpcDNA3ベクター(インビトロゲン(Invitrogen))のbamHI/EcoRI部位にサブクローン化した。このベクターはCMVプロモーターおよびSV40プロモーターを含み、これらはそれぞれ挿入されたcDNA(HERG)およびネオマイシン耐性遺伝子の発現を駆動する。HEK293細胞はこの構築物を用いてリン酸カルシウム沈殿法(ギブコ(Gibco))またはリポフェクタミン法(ギブコ)によりトランスフェクトした。800μg/mlジェネティシン(G418;ギブコ)で15〜20日間選択した後、単一コロニーをクローニングシリンダーで取り出し、そしてHERG電流について試験した。安定にトランスフェクトされた細胞は10%ウシ胎児血清および400μg/mlジェネティシンを補充した最少必須培地(MEM)で培養した。
膜は解凍し、そしてインキューベーションバッファー(Hepes 10nM pH7.4、40mM KCl、20mM KH2PO4、5mM MgCl2、0.5mM KHCO3、10mM グルコース、50mM グルタメート、20mM アスパルテート、14mM ヘプタン酸、1mM EGTA、0.1% BSA)で再度、均一化し、そして20〜100μgタンパク質を[3H]−アステミゾールと25℃で60分間、競合剤の存在下または不存在下でインキューベーションし、続いてFiltermate196回収器(パッカード、メリデン、コネチカット州)を使用してGF/Bフィルター上で迅速に濾過した。フィルターを氷冷したリンスバッファー(Tris−HCl 25mM pH7.4、130mM NaCl、5.5mM KCl、5mM グルコース、0.8mM MgCl2、50μM CaCl2、0.1% BSA)で徹底的にすすいだ。フィルターに結合した放射活性はTopcount(パッカード、メリデン、コネチカット州)でシンチレーションカウンティングにより測定し、そして結果を1分あたりのカウント(cpm)として表した。
溶液:浴溶液は(mMで)150NaCl、4KCl、5グルコース、10HEPES、1.8CaCl2および1MgCl2(NaOHでpH7.4にした)を含んだ。ピペット溶液は(mMで)120KCl、5EGTA、10HEPES、4MgATP、0.5CaCl2および2MgCl2(KOHでpH7.4にした)を含んだ。化合物はDMSOに溶解して10−2Mまたは10−1Mのストック溶液を得た。対照(=浴溶液+DMSO)および試験溶液(=浴溶液+DMSO+試験する化合物)は、0.3%、0.1%または0.03%DMSOを含んだ。試験および対照溶液はY−管系を使用して実験中の細胞に適用し、実験中の細胞に接近して溶液を迅速に交換した(0.5秒未満)。
電気生理学的測定:HERGを発現する付着したHEK293細胞を含むペトリ皿を、パッチクランプタワー(Patch Clamp Tower)の台に固定した。倒立顕微鏡を使用して細胞を観察した。ペトリ皿は室温で浴溶液を一定に潅流した。
測定のパラメーター分析:HERG電流は−80mVの保持電流から始めて+60mVに対して2秒間、脱分極した後、−40mVで最大の末尾電流として測定した。
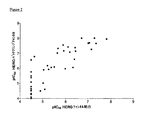
結合アッセイの薬物動態学的評価のために、322種の化合物をそれらが[3H]−アステミゾールのHERGチャンネルへの結合を阻害する能力について8種の濃度で試験し、そしてpIC50−値を非−線型回帰分析により算出した。pIC50値が利用できる場合、結合およびパッチクランプに関して効力の順位(スペルマン(Spearman))を比較した。
スコア1:10−6M以上でpIC50<6または遮断%<50%
スコア2:10−6から10−8Mの間で6から8の間のpIC50または遮断%<50%
スコア3:10−8以下でpIC50>8または遮断%>50%
42種の参照化合物がHERGチャンネルから[3H]−アステミゾール結合を置換する効力の順位は、遅延整流性K+電流の急激な活性化の機能的遮断について、電気生理学的データとよく相関する(rsp=0.87)(図2)。
Claims (21)
- HERGを含む供給源が:
i)配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドまたはその断片を形成する単離され、そして精製されたタンパク質;
ii)配列番号2のアミノ酸配列を含んでなるHERGポリペプチドまたはその断片を形成する単離され、そして精製されたタンパク質;
iii)表面にHERGポリペプチドチャンネルまたはその断片を発現する細胞;または
iv)表面にHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物、
からなる群から選択される請求項1に記載の方法。 - HERGを含む供給源が、表面に配列番号2からなるHERGポリペプチドチャンネルを発現する細胞の膜調製物である、請求項1に記載の方法。
- 個体に心不整脈を誘導し得る化合物をスクリーニングする方法であって;
a)表面に配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物を、請求項4に記載の放射能標識されたアステミゾールと、該アステミゾールのHERGポリペプチドチャンネルへの結合を可能とする十分な時間接触させ;
b)表面に配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物を、該方法により心不整脈誘導能が評価される化学的に定められた分子と一緒に工程a)の放射能標識されたアステミゾールと、該アステミゾールおよび該分子のHERGポリペプチドチャンネルへの結合を可能とする十分な時間接触させ;
c)工程a)でHERGチャンネルへ結合した放射能標識されたアステミゾールの量を測定し;
d)工程b)でHERGチャンネルへ結合した放射能標識されたアステミゾールの量を測定し;そして
e)工程a)で測定したHERGチャンネルへ結合した放射能標識されたアステミゾールの量と、工程b)で測定したHERGポリペプチドチャンネルへ結合した放射能標識されたアステミゾールの量とを比較する、
ことを含んでなる上記方法。 - 個体に心不整脈を誘導し得る化合物をスクリーニングする方法であって;
i)該方法に参加することができる第1の標識で標識されたHERGおよび請求項4に記載の放射標識されたアステミゾールと一緒に該方法により心不整脈誘導能が評価される化学的に定められた分子とを接触させ;
ii)該HERGと該アステミゾールとの間の相互作用を、該HERGと該アステミゾールが相互作用する時の第1の標識と第2の標識の近接性により検出する、
ことを含んでなる上記方法。 - a)HERGを含む供給源;
b)請求項4に記載の放射標識されたアステミゾール、
を含んでなる個体に心不整脈を誘導し得る化合物をスクリーニングするためのキット。 - HERGを含む供給源が;
i)配列番号2の配列に少なくとも80%同一であるアミノ酸配列を有するHERGポリペプチドまたはその断片を形成する単離され、そして精製されたタンパク質;
ii)配列番号2のアミノ酸配列含んでなるHERGポリペプチドまたはその断片を形成する単離され、そして精製されたタンパク質;
iii)表面にHERGポリペプチドチャンネルまたはその断片を発現する細胞;またはiv)表面にHERGポリペプチドチャンネルまたはその断片を発現する細胞の膜調製物、
から選択される請求項8に記載のキット。 - HERGを含む供給源が、固体支持体に結合した単離され、そして精製されたHERGポリペプチドチャンネルまたはその断片である、請求項8に記載のキット。
- 固体支持体が蛍光剤を含む固体支持体である請求項10に記載のキット。
- HERGを含む供給源が、配列番号2からなるアミノ酸配列を有するHERGポリペプチドチャンネルを表面に発現する細胞の膜調製物からなる、請求項8に記載のキット。
- 上記細胞がHEK293細胞である請求項12に記載のキット。
- 過剰な未結合の放射標識されたアステミゾールをインキューベーション混合物から除去する手段を場合により含んでなる、請求項13に記載のキット。
- 分離手段がGF/B濾過からなる請求項13に記載のキット。
- 請求項1に記載の方法における、配列番号2のアミノ酸配列を含んでなるHERGまたはその断片を形成する単離され、そして精製されたタンパク質の使用。
- 請求項1に記載の方法における、配列番号2のアミノ酸配列を含んでなるHERGポリペプチドチャンネルまたはその断片を表面に発現する細胞の使用。
- 請求項1に記載の方法における、配列番号2のアミノ酸配列を含んでなるHERGポリペプチドチャンネルまたはその断片を表面に発現する細胞の膜調製物の使用。
- 請求項1に記載の方法における、配列番号2からなるアミノ酸配列を有するHERGポリペプチドチャンネルを表面に発現する細胞の膜調製物の使用。
- 請求項1に記載の方法における、請求項4に記載の放射能標識されたアステミゾールの使用。
- 請求項12記載の方法における、標識されたアステミゾールの使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP01202689 | 2001-07-13 | ||
| PCT/EP2002/007364 WO2003006988A1 (en) | 2001-07-13 | 2002-07-02 | Cardiovascular safety assay |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005501037A JP2005501037A (ja) | 2005-01-13 |
| JP4570870B2 true JP4570870B2 (ja) | 2010-10-27 |
Family
ID=8180635
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003512705A Expired - Fee Related JP4570870B2 (ja) | 2001-07-13 | 2002-07-02 | 心血管安全性アッセイ |
Country Status (13)
| Country | Link |
|---|---|
| US (3) | US20040161805A1 (ja) |
| EP (1) | EP1410019B1 (ja) |
| JP (1) | JP4570870B2 (ja) |
| CN (1) | CN1276254C (ja) |
| AT (1) | ATE308046T1 (ja) |
| AU (1) | AU2002328312B8 (ja) |
| CA (1) | CA2450581C (ja) |
| DE (1) | DE60206923T2 (ja) |
| DK (1) | DK1410019T3 (ja) |
| ES (1) | ES2252505T3 (ja) |
| IL (2) | IL159819A0 (ja) |
| NZ (1) | NZ529496A (ja) |
| WO (1) | WO2003006988A1 (ja) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE0302775D0 (sv) * | 2003-10-20 | 2003-10-20 | Astrazeneca Ab | Chemical compound and assay |
| US7396524B2 (en) * | 2005-08-02 | 2008-07-08 | Main Line Health Heart Center | Methods for screening compounds for proarrhythmic risk and antiarrhythmic efficacy |
| US9820888B2 (en) | 2006-09-26 | 2017-11-21 | Smith & Nephew, Inc. | Wound dressing |
| GB0902368D0 (en) | 2009-02-13 | 2009-04-01 | Smith & Nephew | Wound packing |
| EP2670312B1 (en) | 2011-02-04 | 2020-11-18 | University of Massachusetts | Negative pressure wound closure device |
| US9421132B2 (en) | 2011-02-04 | 2016-08-23 | University Of Massachusetts | Negative pressure wound closure device |
| CN107280857A (zh) | 2012-05-22 | 2017-10-24 | 史密夫及内修公开有限公司 | 伤口愈合装置 |
| AU2013264938B2 (en) | 2012-05-22 | 2017-11-23 | Smith & Nephew Plc | Apparatuses and methods for wound therapy |
| MX2014014325A (es) | 2012-05-24 | 2015-08-06 | Smith & Nephew Inc | Dispositivos y metodos para tratar y cerrar heridas con presion negativa. |
| AU2013290346B2 (en) | 2012-07-16 | 2018-06-07 | Smith & Nephew, Inc. | Negative pressure wound closure device |
| CN105188622A (zh) | 2013-03-13 | 2015-12-23 | 史密夫和内修有限公司 | 负压伤口封闭装置以及用于以负压处理伤口的系统和方法 |
| RU2015142877A (ru) | 2013-03-14 | 2017-04-18 | СМИТ ЭНД НЕФЬЮ ПиЭлСи | Сжимаемые наполнители раны и системы и способы их применения в лечении ран с применением отрицательного давления |
| AU2014340232B2 (en) | 2013-10-21 | 2019-07-11 | Smith & Nephew Inc. | Negative pressure wound closure device |
| WO2016176513A1 (en) | 2015-04-29 | 2016-11-03 | Smith & Nephew Inc. | Negative pressure wound closure device |
| US10814049B2 (en) | 2015-12-15 | 2020-10-27 | University Of Massachusetts | Negative pressure wound closure devices and methods |
| US10575991B2 (en) | 2015-12-15 | 2020-03-03 | University Of Massachusetts | Negative pressure wound closure devices and methods |
| CA3089957C (en) * | 2017-02-04 | 2024-01-23 | AnaBios Corporation | System and methods for predicting drug-induced inotropic and pro-arrhythmia risk |
| EP3893825A1 (en) | 2018-12-13 | 2021-10-20 | University of Massachusetts | Negative pressure wound closure devices and methods |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4568649A (en) | 1983-02-22 | 1986-02-04 | Immunex Corporation | Immediate ligand detection assay |
| WO2000070079A1 (en) * | 1999-05-13 | 2000-11-23 | Ortho-Mcneil Pharmaceutical, Inc. | High throughput assay for modulators of nuclear receptors |
| AU2002241555A1 (en) * | 2000-10-30 | 2002-06-03 | Vanderbuilt University | Human kcr1 regulation of herg potassium channel block |
-
2002
- 2002-07-02 AT AT02762316T patent/ATE308046T1/de not_active IP Right Cessation
- 2002-07-02 DK DK02762316T patent/DK1410019T3/da active
- 2002-07-02 IL IL15981902A patent/IL159819A0/xx unknown
- 2002-07-02 NZ NZ529496A patent/NZ529496A/en not_active IP Right Cessation
- 2002-07-02 EP EP02762316A patent/EP1410019B1/en not_active Expired - Lifetime
- 2002-07-02 US US10/483,617 patent/US20040161805A1/en not_active Abandoned
- 2002-07-02 DE DE60206923T patent/DE60206923T2/de not_active Expired - Lifetime
- 2002-07-02 JP JP2003512705A patent/JP4570870B2/ja not_active Expired - Fee Related
- 2002-07-02 WO PCT/EP2002/007364 patent/WO2003006988A1/en not_active Ceased
- 2002-07-02 ES ES02762316T patent/ES2252505T3/es not_active Expired - Lifetime
- 2002-07-02 CA CA2450581A patent/CA2450581C/en not_active Expired - Lifetime
- 2002-07-02 AU AU2002328312A patent/AU2002328312B8/en not_active Ceased
- 2002-07-02 CN CNB02813995XA patent/CN1276254C/zh not_active Expired - Fee Related
-
2004
- 2004-01-12 IL IL159819A patent/IL159819A/en active IP Right Grant
-
2006
- 2006-11-06 US US11/593,399 patent/US7820453B2/en not_active Expired - Fee Related
-
2010
- 2010-08-20 US US12/860,387 patent/US20110076696A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| DK1410019T3 (da) | 2006-03-06 |
| CN1276254C (zh) | 2006-09-20 |
| DE60206923D1 (de) | 2005-12-01 |
| US20110076696A1 (en) | 2011-03-31 |
| HK1070693A1 (en) | 2005-06-24 |
| AU2002328312A1 (en) | 2003-01-29 |
| EP1410019A1 (en) | 2004-04-21 |
| WO2003006988A1 (en) | 2003-01-23 |
| CA2450581A1 (en) | 2003-01-23 |
| CN1541334A (zh) | 2004-10-27 |
| AU2002328312B2 (en) | 2006-12-14 |
| EP1410019B1 (en) | 2005-10-26 |
| CA2450581C (en) | 2010-11-02 |
| DE60206923T2 (de) | 2006-07-20 |
| ES2252505T3 (es) | 2006-05-16 |
| JP2005501037A (ja) | 2005-01-13 |
| US20080193924A1 (en) | 2008-08-14 |
| US7820453B2 (en) | 2010-10-26 |
| AU2002328312B8 (en) | 2007-02-15 |
| US20040161805A1 (en) | 2004-08-19 |
| IL159819A (en) | 2010-05-31 |
| ATE308046T1 (de) | 2005-11-15 |
| IL159819A0 (en) | 2004-06-20 |
| NZ529496A (en) | 2005-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20110076696A1 (en) | Cardiovascular safety assay | |
| Aggarwal et al. | Single‐molecule pull‐down (SiMPull) for new‐age biochemistry: Methodology and biochemical applications of single‐molecule pull‐down (SiMPull) for probing biomolecular interactions in crude cell extracts | |
| US20220088135A1 (en) | Methods of making and using soluble mhc molecules | |
| US7541476B2 (en) | Radiolabeled astemizole and method of making | |
| JP4566984B2 (ja) | 環状ヌクレオチドの細胞内濃度を決定する試験方法 | |
| Nibbs et al. | Structure–function dissection of D6, an atypical scavenger receptor | |
| EP1308726B1 (en) | Methods and compositions for screening modulators of integrins | |
| US7767409B2 (en) | Method for detection of substance bound to nuclear receptor | |
| JP2002335998A (ja) | Vegfの生物活性を定量するためのvegf応答性細胞をベースとしたアッセイ | |
| WO2008012941A1 (fr) | Méthode de diagnostic d'une insuffisance cardiaque | |
| van Doorn et al. | CHARACTERIZATION OF NITROIMIDAZOLE-PROTEIN ADDUCTS: TOWARDS A HYPOXIA-SPECIFIC TROPONIN ASSAY | |
| KR101119995B1 (ko) | 단백질 상호작용 억제제 선별방법 | |
| JP4527389B2 (ja) | リガンド結合阻害物質の生物活性を評価する方法 | |
| Chen et al. | Application of large-scale transient transfection to cell-based functional assays for ion channels and GPCRs | |
| US20060240483A1 (en) | Method and kit for monitoring recruitment of proteins to the intracellular domain of a receptor in intact cells | |
| Umezawa | Detecting mitochondrial RNA and other cellular events in living cells | |
| Fay et al. | Purification and Analysis of by Functional Site-Directed CB1 Fluorescence Labeling Methods | |
| KR20100067849A (ko) | 도파민 d1 수용체 발현 세포주 및 이를 이용한 신약 개발 방법 | |
| KR20210073547A (ko) | 류신 리치 α2 글리코 단백질 조성물 | |
| Bianchi et al. | APPLICATION of Large-SCALE TRANSIENT TRANSFECtion to CeLL-BASED |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050520 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20080202 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090203 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090501 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090602 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20090902 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20090909 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091202 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100105 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100405 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100412 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100702 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100803 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100811 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130820 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4570870 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |