JP4480098B2 - ポリマー電解質蓄電池用の再充電可能なリチウムアノード - Google Patents
ポリマー電解質蓄電池用の再充電可能なリチウムアノード Download PDFInfo
- Publication number
- JP4480098B2 JP4480098B2 JP32291697A JP32291697A JP4480098B2 JP 4480098 B2 JP4480098 B2 JP 4480098B2 JP 32291697 A JP32291697 A JP 32291697A JP 32291697 A JP32291697 A JP 32291697A JP 4480098 B2 JP4480098 B2 JP 4480098B2
- Authority
- JP
- Japan
- Prior art keywords
- anode
- lithium
- electrolyte
- rechargeable battery
- polymer electrolyte
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims description 135
- 229910052744 lithium Inorganic materials 0.000 title claims description 135
- 239000005518 polymer electrolyte Substances 0.000 title claims description 72
- 239000003792 electrolyte Substances 0.000 claims description 72
- 229910052783 alkali metal Inorganic materials 0.000 claims description 25
- 150000001340 alkali metals Chemical class 0.000 claims description 20
- 229910052751 metal Inorganic materials 0.000 claims description 18
- 239000002184 metal Substances 0.000 claims description 18
- 230000001351 cycling effect Effects 0.000 claims description 17
- 239000012535 impurity Substances 0.000 claims description 14
- 229910045601 alloy Inorganic materials 0.000 claims description 10
- 239000000956 alloy Substances 0.000 claims description 10
- 239000002131 composite material Substances 0.000 claims description 10
- -1 alkali metal cations Chemical class 0.000 claims description 8
- 238000006243 chemical reaction Methods 0.000 claims description 7
- 229910001416 lithium ion Inorganic materials 0.000 claims description 6
- 229910052759 nickel Inorganic materials 0.000 claims description 6
- 229910052802 copper Inorganic materials 0.000 claims description 5
- 230000008021 deposition Effects 0.000 claims description 5
- 239000000945 filler Substances 0.000 claims description 5
- 230000002441 reversible effect Effects 0.000 claims description 5
- 239000007784 solid electrolyte Substances 0.000 claims description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 4
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 4
- CPLXHLVBOLITMK-UHFFFAOYSA-N Magnesium oxide Chemical compound [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 claims description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 4
- 238000004090 dissolution Methods 0.000 claims description 4
- 239000002245 particle Substances 0.000 claims description 4
- 230000015572 biosynthetic process Effects 0.000 claims description 3
- 150000001768 cations Chemical class 0.000 claims description 3
- 238000005342 ion exchange Methods 0.000 claims description 3
- 229910000733 Li alloy Inorganic materials 0.000 claims description 2
- 239000004698 Polyethylene Substances 0.000 claims description 2
- 239000004743 Polypropylene Substances 0.000 claims description 2
- 239000000853 adhesive Substances 0.000 claims description 2
- 230000001070 adhesive effect Effects 0.000 claims description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 claims description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 2
- 239000004020 conductor Substances 0.000 claims description 2
- 125000005842 heteroatom Chemical group 0.000 claims description 2
- 229910052742 iron Inorganic materials 0.000 claims description 2
- 239000001989 lithium alloy Substances 0.000 claims description 2
- 239000000395 magnesium oxide Substances 0.000 claims description 2
- 229910052757 nitrogen Inorganic materials 0.000 claims description 2
- 239000001301 oxygen Substances 0.000 claims description 2
- 229910052760 oxygen Inorganic materials 0.000 claims description 2
- 229920000573 polyethylene Polymers 0.000 claims description 2
- 229920001155 polypropylene Polymers 0.000 claims description 2
- 239000000377 silicon dioxide Substances 0.000 claims description 2
- 239000012453 solvate Substances 0.000 claims description 2
- 229910000573 alkali metal alloy Inorganic materials 0.000 claims 3
- 238000010030 laminating Methods 0.000 claims 1
- 239000002985 plastic film Substances 0.000 claims 1
- 238000004804 winding Methods 0.000 claims 1
- 239000010408 film Substances 0.000 description 30
- 210000004027 cell Anatomy 0.000 description 22
- 229920000642 polymer Polymers 0.000 description 19
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 13
- 239000007787 solid Substances 0.000 description 12
- 230000000694 effects Effects 0.000 description 9
- XYYHNDVKALDFHQ-OXHZBIAZSA-N 1-octadecanoyl-2-(4Z,7Z,10Z,13Z,16Z,19Z-docosahexaenoyl)-sn-glycero-3-phosphoethanolamine zwitterion Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OCCN)OC(=O)CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CC XYYHNDVKALDFHQ-OXHZBIAZSA-N 0.000 description 7
- 230000035515 penetration Effects 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 6
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 239000011244 liquid electrolyte Substances 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 238000000034 method Methods 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- XHCLAFWTIXFWPH-UHFFFAOYSA-N [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] XHCLAFWTIXFWPH-UHFFFAOYSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 229910001935 vanadium oxide Inorganic materials 0.000 description 4
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- 229910052786 argon Inorganic materials 0.000 description 3
- 210000001787 dendrite Anatomy 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 239000005486 organic electrolyte Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000010406 cathode material Substances 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 230000005611 electricity Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229910001947 lithium oxide Inorganic materials 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-M methacrylate group Chemical group C(C(=C)C)(=O)[O-] CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 230000004660 morphological change Effects 0.000 description 2
- 229920005604 random copolymer Polymers 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 230000003746 surface roughness Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 229910000838 Al alloy Inorganic materials 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- 239000004971 Cross linker Substances 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- JFBZPFYRPYOZCQ-UHFFFAOYSA-N [Li].[Al] Chemical compound [Li].[Al] JFBZPFYRPYOZCQ-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M acrylate group Chemical group C(C=C)(=O)[O-] NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 238000001994 activation Methods 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000006388 chemical passivation reaction Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000011889 copper foil Substances 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 159000000011 group IA salts Chemical class 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 229910001234 light alloy Inorganic materials 0.000 description 1
- FUJCRWPEOMXPAD-UHFFFAOYSA-N lithium oxide Chemical compound [Li+].[Li+].[O-2] FUJCRWPEOMXPAD-UHFFFAOYSA-N 0.000 description 1
- 229910003002 lithium salt Inorganic materials 0.000 description 1
- 159000000002 lithium salts Chemical class 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 239000002923 metal particle Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000003586 protic polar solvent Substances 0.000 description 1
- 238000010298 pulverizing process Methods 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000007420 reactivation Effects 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000007725 thermal activation Methods 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/381—Alkaline or alkaline earth metals elements
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/381—Alkaline or alkaline earth metals elements
- H01M4/382—Lithium
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/40—Alloys based on alkali metals
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/40—Alloys based on alkali metals
- H01M4/405—Alloys based on lithium
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/40—Printed batteries, e.g. thin film batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Description
【発明の分野】
本発明は、ポリマー電解質蓄電池の再充電可能なリチウムアノードに関する。より特定的には本発明は、電気化学電池(generator)、例えば、元素形態または合金形態のリチウムまたは他のアルカリ金属から成るアノードとポリマー電解質とを含み、蓄電池の規格寿命中に得られるサイクル数を実質的に増加させることが可能であるという特徴をもつ電池に関する。
【0002】
【従来の技術】
有機電解質の存在下で再充電可能であるというリチウムの特性は、リチウムのようなアルカリ金属アノードの著しい形態変化を一般的に生じさせ、その結果として、アノードの有効性が失われ及び/または再充電中に樹枝状晶が出現する。この現象は金属リチウムを使用するすべての電池に極めて普遍的な現象である。参考文献としては、Industrial Chemistry Library,Volume 5,LITHIUM BATTERIES,New Materials,Developments and Perspectives,Chapter 1,J.R.Dahnら著、G.Pistoia編,Elsevier(1994)がある。この現象に関しては以下の理論に基づく説明が定説となっている。
【0003】
1−リチウムは有機電解質(溶媒+リチウム塩)の存在下で熱力学的に不安定であり、酸化層を形成する(酸化層は多少とも不動態化しており、ある種の条件下ではリチウムイオンの導体として維持される)。後者の場合、不動態化する層はSEI(固体電解質境界面(Solid Electrolyte Interface)と呼ばれる。
【0004】
2−継続的な放充電サイクル中にリチウムが溶解し、不均一に再付着し、最終的に電気絶縁性になるか及び/または有機電解質(溶媒+塩)との反応によって化学的に消費される。
【0005】
3−その結果として、アノードの活性が低下し、多少とも不動態化した分散リチウムからなる不整な多孔質アノードが形成される。
【0006】
一般には、リチウムアノード容量をカソード容量に比べて大きくすることによってこの現象を補償し、サイクル反復中の十分な充放電回数を確保している。アノード容量なる用語は、“クーロン”容量、即ち、アノード中に存在する電気量を意味する。1モルのリチウムは96,500クーロンに等価の電気量を含む。容量は通常は1cm2あたりのクーロン量であると定義され、例えば、10クーロン/cm2として表す。容量はまた、ミリアンペア時/cm2で表してもよく、双方の値は式:1mA時/cm2=3.6C/cm2によって換算できる。
【0007】
リチウムが100%の効率では再付着し難いこの普遍的挙動を、通常はF.O.M.(Figure of Merit品質係数)と呼ばれる概念を用いて表す。Second International Symposium on Polymer Electrolytes,Siena,Italy,June 14−16,1989,Belangerら。
【0008】
このような理由から、二次電池では通常、対応するカソードの3〜8倍の容量を有するリチウムアノードを使用する。この処置によって十分な回数の放充電サイクルを得ることはできるが、過剰量のリチウムを使用するので、その代償として電池のエネルギー密度は著しく低下する。更に、過剰量のリチウムは電池のコストもかなり上昇させる。また、Liの超過度が高いほど、再充電可能なLi蓄電池の取り扱いが危険になる。サイクル反復に伴ってリチウムの形態変化が大きくなり、リチウムの反応性が高くなるような場合にはいっそう危険である。
【0009】
リチウムアノードに関して使用される“形態”なる用語は、サイクル反復中に発達する表面の凹凸を意味する。いくつかの場合にはこの表面の凹凸がアノード自体の内部に伸長し、その場合にはサイクル反復中にアノードが多孔質になる。従って、表面の形態が発達するというとき、この形態という用語は、表面粗度の進行を意味する。表面粗度を±1ミクロンの精度で測定するために電極の表面を走査する多数の装置が公知である。
【0010】
ポリマー電解質の存在下でも、より低度にはなるがリチウムの形態の発達が生じることが観察された。この観察から、リチウムのアノードの形態の変化は反復条件下でアノードをサイクル使用するときに生じることが確認された。出願人は先に発表した論文にこの現象を記載した(Siena,Belangerら,前出)。試験中にF.O.M.>100という比較的高いF.O.M.値が観察されたが、この値の場合には、カソードの容量のほぼ3倍または3倍を上回る過剰量のリチウムを使用する必要がある。
【0011】
従って、商品化適性及び管理容易性の理由から、再充電可能な金属リチウム電池では一般に比較的厚いリチウムシートが使用されている。また、管理を容易にし電気接触を設けるために剛性電流コレクタをリチウムフィルムに貼合わせて使用することも可能である。
【0012】
最適設計及び最適性能のポリマー電解質電池を製造するため、及び、電気自動車用の十分なエネルギーを蓄積し得る電池を提供するために、出願人は、益々薄くなる膜厚のリチウムフィルムの製造方法を発明した。参考文献は、米国特許第4,517,265号、第4,652,506号、第4,794,060号及び第4,897,917号、並びに、米国特許出願第08/273,756号及び第08/273,759号である。出願人はまた、電池の製造コスト及びエネルギー密度を最適にするために剛性電流コレクタを削除した。
【0013】
例えば、出願人は実験室で、電流コレクタを備えない膜厚20〜40ミクロンのリチウムフィルムを使用して数mW時のデバイス及び10W時よりも大きい他のデバイスを作製した(J.Power Sources,54(1995)163)。
【0014】
すべての場合に、対応するカソードの容量の3倍及びときにはそれ以上の容量のアノードを用いることによってサイクル反復中に良好な性能が得られる。同様の条件下で、より薄くより低容量(カソード容量の3倍の容量)のリチウムフィルムを使用するときに、サイクル数の急激な減少が観察された。これらの電池では分解後に、リチウム薄フィルムの著しい形態変化が単なる肉眼によってまたは走査型電子顕微鏡によって観察された。このような極めて薄いシートの場合、形態変化がシート全体にわたって観察される。
【0015】
リチウムの形態変化は以下の条件下で特に速い。
【0016】
1−リチウムの超過度が小さいとき、
2−リチウムのフィルムが30ミクロンよりも薄いとき、及び、
3−リチウムが遊離しているとき、即ち剛性電流コレクタによって支持されていないとき。
【0017】
これらの観察は従来技術で観察された傾向を確認するものであり、金属リチウムアノードを有する電池の性能の最適化、即ち、最適の電力及びサイクル適性を追求するために、カソードの容量に対するリチウムの超過度を低下させたり、しばしば厚く高価な剛性電流コレクタの存在を削除したり、または、アノード/ポリマー電解質/カソード/コレクタのような電池を構成するフィルム群の膜厚を減少させたりする場合の重大な制約となる。。
【0018】
【発明が解決しようとする課題】
本発明の1つの目的は、金属リチウムのようなアルカリ金属アノードを使用し、十分な充放電サイクルの反復に耐えられる再充電可能なポリマー電解質電池を提供することである。
【0019】
本発明の別の目的は、リチウム容量の超過度が低いにもかかわらず多孔質アルカリ金属または電気絶縁アルカリ金属粒子を形成することなくアルカリ金属アノードの初期形態を維持することによってアノードの可逆性反応及びアノードの電流収集が維持される電池を提供することである。本発明のこの特徴は、本発明の条件下ではサイクル反復中にポリマー電解質によるリチウムの実質的消費が生じないことによって可能になったものである。
【0020】
本発明の別の目的は、50ミクロンを下回る程度の極めて薄いリチウムフィルムの使用を提案し、カソードに対する設置金属の超過度を低減及び/または削除し、しかも、良好なサイクル反復特性を維持することである。
【0021】
本発明の別の目的は、安全性、電気化学性能及びアノード容量の超過度に伴うコストの観点から、本発明の電池の要求するリチウムアノード容量の超過度を従来技術に比較して低減及び/または削除することである。
【0022】
【課題を解決するための手段】
本発明によれば、アルカリ金属アノードと、固体ポリマーとアルカリ金属塩とから成る電解質と、アルカリ金属イオンを可逆的にサイクル使用し得るカソードとを含み、アノードと電解質とが電池のサブアセンブリを形成している再充電可能な電池が提供される。サブアセンブリは以下の特性を有している。
【0023】
a.SEIフィルムの電気化学特性を実質的に完全に維持するように、固体ポリマー電解質は、アノードと反応でき最高で1,000Åに等価のリチウムを消費できる蓄積された可動性不純物を最大量で含む。
【0024】
b.ポリマー電解質は、均質で弾性であり、機械的圧力をアノードに伝達でき、また、その膜厚の35%未満の変形を利用してアノードの金属の樹枝状応力変形(dendritic stressまたはstrain)に抵抗し得る。
【0025】
より特定的には本発明は、展性の遊離アルカリ金属または合金から成るアノードと、アルカリ性カチオン伝導性でありセパレータとして作用する少なくとも1種のポリマー電解質と、アルカリ金属のカチオンに対して可逆性の少なくとも1つのカソードと、カソードの電流コレクタとから成る再充電可能な電池を提供する。本発明の電池の特徴は、
−アノードが、金属とポリマー電解質との反応を制限しかつ継続的な充放電サイクル中にリチウムイオンを交換し得るSEI不動態化フィルムを表面に備えた厚み100マイクロメータ未満の薄い金属シートから成り、
−ポリマー電解質は、機械的変形に抵抗性であり、アノードに圧力を伝達しその厚みの35%未満の割合の変形を生じることによってアノードの金属の樹枝状応力変形に抵抗し得る均一セパレータを構成し、
−セパレータのポリマー電解質及び任意に複合カソードを用いる場合のカソードのポリマー電解質は、アノード/ポリマー電解質の境界面のイオン交換品質を保持するために、リチウムに反応性でアノードの表面に蓄積される可動種が3000Å未満に等価のアルカリ金属の消費に対応する最大量で含んでおり、
−アルカリ金属アノードと電解質セパレータとカソードとコレクタとのアセンブリは、継続的な溶解/付着サイクル中にセパレータがアノードのシートを圧縮形態に維持して、SEIの化学的及び機械的結合性を維持できるように十分な機械的応力下に維持されていることである。
【0026】
本発明の好ましい実施態様によれば、アノードは厚み100ミクロン未満、例えば40ミクロン未満である。アノードは好ましくはリチウムまたはその合金から成る。電子伝導性及び側面電流収集を確保するために少し過剰に用いてもよい。また、両面をアノードとして使用できる非支持シートからアノードを製造してもよい。
【0027】
本発明の別の好ましい実施態様によれば、ポリマー電解質は通常は50ミクロン未満、例えば30ミクロン未満の厚みを有している。好ましいポリマー電解質は、アノードと同じアルカリ金属のアルカリ性塩のカチオンの溶媒和物を形成し得る酸素または窒素のようなヘテロ原子を含む。
【0028】
本発明の別の好ましい実施態様によれば、電解質は、蓄電池を短絡から保護することを続けながら約60℃で約200psiの応力に対して35%を上回る変形を生じることなく抵抗できる。
【0029】
本発明で使用される好ましいポリマー電解質は、60℃で約50psiの弾性率を有している。本発明のポリマー電解質においては好ましくは、ポリマーの鎖の架橋構造及び鎖の交絡部位が、変形率を初期厚みの35%未満、例えば25%未満に制限し、サイクル反復中のリチウムの変形に抵抗するために十分な密度で存在する。
【0030】
本発明によれば、このような変形特性は、好ましくは粒度1マイクロメータ未満の不活性充填剤を、変形率を上記のような範囲に制限するために十分な量で電解質に添加することによって得られる。好ましい充填剤は、粒度1ミクロン未満のアルミナ、シリカまたはマグネシアである。
【0031】
実質的に限定された量でポリマー電解質中に存在する不純物は例えば、ポリマー鎖の末端に位置する可動性の反応性官能基から成る。本発明によれば、不純物の使用量は、1000Åに等価のリチウムの消費に必要な量よりも少ない量でなければならない。この不純物レベルで、Li表面(SEI)の不動態化するフィルムの結合性を維持することが可能である。不純物はまた、水もしくは溶媒から構成されてもよく、または、Liを消費することによってLiに向かって拡散し得る少量のポリマーから構成されてもよい。不純物はまた、OHまたはNH末端基を有するプロトン性分子でもよい(後出の表1参照)。不純物レベルを最小に抑えることは本発明に不可欠である。何故なら、サイクル反復中のリチウムの表面形態の変化によってリチウム表面を回復することができないからである。
【0032】
本発明の特徴の1つを与えるために必要な機械的応力は、アノード、電解質及びカソードの各フィルムを一定の外側体積を超過しない大きさのコイルの形態に巻装するか、または、アノード、電解質及びカソードの各フィルムを圧縮性荷重、一般には5〜150psiの圧力下に維持することによって得られる。
【0033】
機械的応力を与える別の方法では、アノードと電解質とカソードとが一定の圧力または一定の体積に維持される角柱(prism)を構成する。角柱は例えば、アノード、電解質及びカソードの各フィルムから成るアセンブリからフラットコイルを形成するか、または、電池の構成素子の積層によって形成される。また、別の角柱型装置は電池の構成素子をジグザグに積層することによって得られる。別の方法で本発明の目的を果たす場合には、機械的手段によって電気化学デバイスを一定体積に圧縮する。
【0034】
別の実施態様によれば、アノードは、非支持アノードシートの結合性を維持しサイクル反復中の電流収集を確保するように硬化リチウムアノードから成る。アノードはまた、金属リチウムよりも展性が小さい高含量リチウム合金から成ってもよく、このようなアノードでは過剰量のリチウムが非変形性電流コレクタの機能を確保する。
【0035】
本発明の別の実施態様によれば、アノード容量は、可逆性カソード容量の約1.5〜3.5倍である。
【0036】
別の実施態様によれば、アノードは、リチウムのようなアルカリ金属またはその合金のシートから成り、シートに接着したコレクタに支持されている。コレクタは銅、鉄、ニッケルのような金属もしくは合金またはリチウムに対して安定な他の金属もしくは合金の導電性金属シートから構成され得る。また、同じくLiに対して安定なプラスチック材料、例えばポリプロピレンまたはポリエチレンのシートから製造されてもよい。
【0037】
別の実施態様によれば、アノードは、電解質と正極とから成る2つの半電池の間に装着されている。また、リチウムまたはその合金から成る2枚のアルカリ金属フィルムを薄い剛性中央支持体の両面に装着してもよい。
【0038】
別の実施態様によれば、電解質とアノードとの間、または、電解質とカソードとの間に接着性の薄い第二電解質を配備してもよく、この第二電解質は電池の種々の構成素子間に安定な境界面を形成する。
【0039】
本発明の特徴及び利点は添付図面に示す非限定例に関する以下の記載より明らかにされるであろう。
【0040】
【実施例】
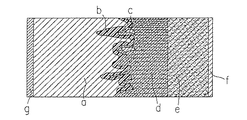
判り易くするためにSEIの厚みを実寸よりも拡大して図示していることを先ず理解されたい。図面、特に図1を参照すると、図示の電池は厚み約100ミクロンのLiOアノードaを有しており、このアノードは銅シートから成るアノードコレクタgに装着されている。電池は更に、当業者に公知の複合カソードeを有しており、この複合カソードはニッケルシートから成るカソードコレクタfに装着されている。カソードeとLioアノードaとの間に、、従来の多孔質セパレータに含浸された液体電解質dが存在している。符号bは、サイクル反復後のアノードの表面プロフィルをSEIフィルムと共に示す。符号cは、サイクル反復によって生じた電気絶縁電解質dに埋込まれた微粒子状Lioを示す。
【0041】
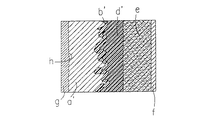
次に、従来技術のポリマー電解質を金属コレクタと共に使用した従来技術の電池(Siena,Belangero、前出)の多少進行したサイクル反復段階を示す図2を参照すると、この電池は、厚みが約20ミクロンである以外は図1の電池と同様のLio アノードa′を有しているが、銅シートから成るアノードコレクタgに装着されている。この電池は図1の電池と同様に、当業者に公知の複合カソードeを含み、カソードはニッケルシートから成るコレクタfに装着されている。カソードeとLio a′との間に、ポリマー電解質d′が配置されており、ポリマー電解質d′はSEIフィルムを伴うリチウムアノードのサイクル反復によって変形されている。符号hは、リチウムの析出/溶解のサイクルによって誘発されたLioシートa′の機械的変形を表す。符号b′は、SEIフィルムを伴うアノードのサイクル反復後の表面プロフィルを示す。
【0042】
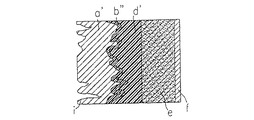
図3に示す電池は、電池がアノードのコレクタを有していない図2の電池の変形である。従って、この電池は非支持のLioアノードa′と、図2の電解質と同様のポリマー電解質dと複合カソードeとそのコレクタfとを含む。この場合、SEIフィルムを伴うアノードのサイクル反復後の表面プロフィルb″は図2に示す表面プロフィルよりも甚だしく損傷されている。参照符号iはコレクタのないLioシートの裏面のリチウムの付着/溶解サイクルによって誘発された機械的変形を示す。
【0043】
図2及び図3に示す2つの電池に関しては、電池が変形性ポリマー電解質を含む再充電可能なLio電池であり、Lio/SEI/ポリマー電解質の境界面に対する圧力を制御しないでサイクル反復試験した場合を扱っていることに注目されたい。
【0044】
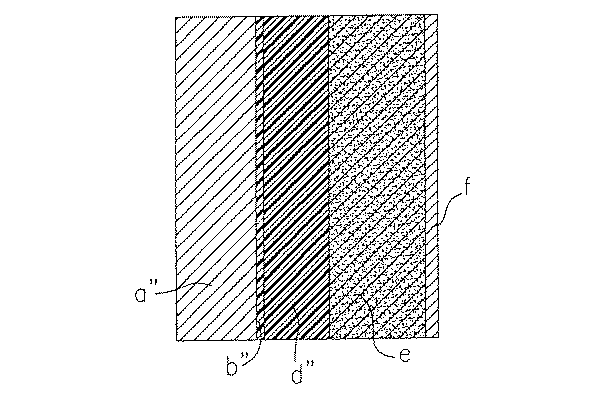
次に、図4を参照すると、本発明電池が、<30ミクロンの薄いフィルムの形態のリチウムアノードa″を含み、C/cm2で表されるアノードの容量が複合カソードeの容量の3倍未満であることが理解されよう。ニッケルから成るコレクタfを備えた複合カソードeとアノードa″との間に、Lioに反応性の不純物を低濃度で含みまた30ミクロン未満の厚みを有する微変形性ポリマー電解質(Slightly Deformable Polymer Electrolyte、SDPE)セパレータdが配置されている。Li+イオン伝導性のSEI(固体電解質境界面)は参照符号b″で示されている。本発明によれば、圧力iは、電池の体積応力また電気化学デバイスに対する外部圧力を介してLio/SEI/SDPE境界面に作用する。
【0045】
図5は、コレクタfに装着されたカソードe、固体ポリマー電解質d″、リチウムアノードa″及びそのコレクタgの極低温断面の顕微鏡写真である。
【0046】
図6に示す電池の構成素子は、図5に示す電池の対応する素子と同じであり、リチウムアノードa″、数百回のサイクル後のLio/SEI/SDPE境界面b″、固体ポリマー電解質d″、複合カソードe並びにそのコレクタfから成る。
【0047】
図1は、液体媒体中の多数回の充放電サイクル後に、リチウムの表面に樹枝状形態が発達し、粒子が表面から離脱してリチウムが電気的に絶縁されることを示す。
【0048】
他方、ポリマー媒体中の従来技術を示す図2及び図3を参照すると、サイクル反復後に、リチウムの形態は発達しているが、アノードの厚みが20ミクロンしかないので形態の発達は従来よりもはるかに少ない。圧力は全く作用させなかった。
【0049】
図4の場合、SDPE電解質は電池のアノードに圧力を伝達し、その結果としてリチウムの表面及び内部における形態の発達が阻止される。
【0050】
後述する本発明のいくつかの実施例においては、数百回のサイクル後にもリチウムの表面が極めて滑らかな状態を維持しており、表面の凹凸は1〜2ミクロン未満であることが証明される。
【0051】
これらの結果から、圧力とSDPE即ち微変形性電解質セパレータとの併用によって、薄いリチウムフィルムを高密度の均一な状態に維持できることが確認される。
【0052】
表1はポリエチレンオキシドのようなポリマーの鎖のOH末端基の濃度がポリマーの平均分子量に与える効果を示す。化学的に消費されたリチウムフィルムの厚みの概数値を得るために、リチウムと反応性種との反応を、1当量の反応に基づいて他の当量に関して計算する。
【0053】
表1は、ポリマー密度が1.1g/cc、電解質厚みが30ミクロン、OH末端基が鎖あたり2個、各OH基に1個のLi原子が反応すると想定したときの、種々の分子量の電解質と接触して反応したリチウムの量を示す。
【0054】
【表1】
【0055】
この表は、リチウムに到達し得る可動性の種だけを考察する。
【0056】
この基準は、リチウムフィルム(300〜500Å)の表面に存在する固体のSEIの性質及び電気化学特性を維持するために極めて重要であることが判明した。この基準は、プロトン性不純物、H2O、−OH、NH−などのようなLiを消費し得る他の不純物ソースにも応用できる。可動性の反応性液体の不純物によって設置リチウム(電池を組立てるときにリチウム電極に含まれていた量、クローン/cm2)の実質的な消費が生じると、不動態化しないかまたはLi+イオンの伝導をほとんど生じない極めて厚い酸化リチウムフィルムの形成が惹起される。
【0057】
サイクル反復中にLio/固体ポリマー電解質境界面の品質を維持するためには、ポリマー電解質は、必要な化学的純度に加えて、機械的セパレータとして機能できかつ放充電サイクル中にLio/固体ポリマー電解質境界面の幾何学形を維持し得る適正な機械的特性を有していなければならない。ポリマー電解質の巨視的及び微視的な機械的抵抗は、ポリマー電解質が放充電サイクル中のリチウムの機械的変形に抵抗できかつ予測される樹枝晶の出現に抵抗できる程度でなければならない。従って、局部的な機械的変形を生じ得るポリマー電解質を使用する方法は、液体電解質を用いる方法とは完全に異なる方法であり、後者の場合には概して、液体電解質を含浸させた一般には1ミクロンよりも小さい細孔を有する多孔質セパレータを用いることによって機械的分離が得られる。この場合樹枝晶の形成及びリチウムアノードの変形に抵抗する多孔質セパレータである。
【0058】
ポリマー電解質セパレータに必要な最低の機械的特性は、リチウムアノードに接触している電解質の面に対する標準侵入試験によって決定される。
【0059】
本発明の電池の好ましい製造方法では、リチウム表面とLio/固体ポリマー電解質境界面の幾何学形を、電池(円筒形)の内部境界及び/またはアセンブリに対する電池の圧力を制御することによって維持する。
【0060】
好ましくは、本発明の電池は200ミクロン未満の厚みを有しており、50ミクロン未満の厚みのリチウムアノードを含んでおり、該リチウムアノードの設定容量は対応するカソードの容量の4倍未満である。これらの電池では、リチウムアノードの甚だしい形態変化を生じることなく多数回の深いサイクルの反復が可能である。
【0061】
本発明の電池によれば、リチウムの微粉砕が不要であり、高度に分散したリチウムの反応性に伴う危険が除去されるので、安全性に関する懸念が劇的に軽減される。
【0062】
本発明を以下の非限定実施例によって説明する。
【0063】
実施例では、以下の3種類のポリマーを使用した。
【0064】
架橋性アリル官能基を有するエチレンオキシドベースのランダムコポリマー。これらのポリマーは、セパレータに機械的特性を与え、鎖の反応性末端基の数を制限するために、高い分子量(200,000以上)を有している(米国特許第4,578,326号及び第4,758,483号参照)。
【0065】
易架橋性メタクリレート官能基を有するエチレンオキシドベースのランダムコポリマー。これらのポリマーは、上記と同じ理由から高い分子量(200,000)を有している(カナダ特許出願第2,111,049号参照)。
【0066】
OH基を除去するように鎖末端に多官能アクリレート基を有する低分子量ポリマー(10,000のオーダ)。これらの易架橋性ポリマーは、高密度の架橋構造の存在に伴って低変形性という機械的特性を与える(1997年1月11日出願の米国特許出願第08/371,437号)。
【0067】
これらの種々のポリマーを架橋させる方法としては、例えば、フリーラジカル開始、化学的活性化、熱的活性化またはIrgacure 651の照射などがある。
【0068】
種々の実施例では、特性決定を行うために、以下の構成素子から成る4cm2の電池を組立てる。
【0069】
アノードは、任意にNi支持体を備えた約10〜35ミクロンの金属Liから成る。
【0070】
上記のポリマーとLiCF3SO2NとをO/Li=30/1で用いて膜厚10〜30ミクロンの電解質膜を作製する。
【0071】
活物質とカーボンブラックと電解質とをほぼ40:03:57の容量比で用いてカソードを作製し、通常はNiまたはAlから成る金属コレクタに担持させる。カソードは1〜2mA時/cm2の容量を有し、40〜80ミクロンの厚みを有する。アルゴン下のグローブボックス内で電池を組立てた。
【0072】
【実施例】
実施例1
双方共がリチウム/Niアノードと酸化バナジウムベースのカソードとを含む等しい2つの電池を組立てた。第一電池では、厚み50ミクロンの電解質膜を減圧下、80℃で24時間乾燥した(Karl Fischerの技術によってH2O<50ppm)。第二電池では、同じ膜を電池に使用する前に室内空気に30分間接触させた(水分>2000ppm)。2つの電池を60℃で20サイクル使用後、25℃で測定した電池のインピーダンスは、従来の方法で電解質を乾燥させた電池に比べて3倍以上(160オーム−cm2対50オーム−cm2)になっていた。
【0073】
第二の試験では、末端ヒドロキシル基を含む分子量Mw=2000のポリエチレンオキシドを20%の量で電解質に添加した。第一試験の場合と同様に、60℃でサイクル反復使用したリチウム/バナジウムオキシド電池は15サイクル未満以内に200オーム−cm2を上回るインピーダンスを生じたが、第一電池のインピーダンスは50オーム−cm2未満であった。
【0074】
主としてアノードに起因するインピーダンスの測定は、リチウムの表面に蓄積し得る可動な反応性不純物の効果に関する表1の結果を確認する。
【0075】
以後の実施例では、SEIの電気化学特性を維持するために、含水量または反応性不純物の含量を常に200ppm未満に維持する。
【0076】
実施例2
この実施例では、上記のポリマーのファミリーに属する4種類の膜を変形度に基づいて特性決定した。変形を特性決定するために、240gの錘で加重した7mmの突針を用い、40〜60ミクロンのオーダの膜厚のフィルムに対する針の侵入度を測定する装置を使用した。この試験は60℃で実施した。この温度は、電解質がアモルファスに維持される温度であり、また電池の動作温度に対応する温度である。
【0077】
結果を以下の表2に示す。変形性の特性決定後、これらの電解質を使用して実施例1の電池と同様の電池を組立てた。
【0078】
表2に示したようなセパレータの変形性の測定値が同じ条件下で測定した金属リチウムシートの測定値(2%のオーダ)に近いことは注目に値する。即ちこれらの値は、セパレータ電解質が非変形性であればサイクル反復中のLiの形態が制御される可能性があることを示唆する。
【0079】
【表2】
【0080】
侵入度は、通常は40〜60ミクロンの範囲の厚みに対するパーセンテージとして表される。この侵入試験はセパレータの変形性の半定量的な測定方法として使用されるであろう。
【0081】
本発明のセパレータとリチウムとの侵入度が実質的に等しい割合であることは、セパレータのヤング率がLiのヤング率即ち約80psiにほぼ等しいかもしくはこれを上回る値であるときは常に有利な効果が得られることを示唆する。
【0082】
実施例2a
“ソフト”であると考えられる電解質、典型的にはその厚みの66%の変形を生じることができ架橋剤非添加で乾燥した分子量200,000のVdB電解質を用いて電池を組立てた。これは図2の記載に対応する。分解後(100サイクル)、Cuがコレクタとして存在するのもかかわらず、電解質とリチウムとの間で極めて顕著な相互侵入が観察された。更に、50サイクル後には、クーロン効率の問題が観察された。Liの表面はまた、15ミクロンのオーダのかなりの凹凸を有していた。
【0083】
実施例3
アルゴン充填グローブボックスで、実施例2と同じ負荷条件下で30%の変形を生じる硬度を有し且つ2%過酸化ベンゾイルを含む架橋アニオン性電解質を用いて等しい3個の電池を組立てた。この電解質は半硬質電解質である。リチウムは35ミクロンの厚みを有し、厚み8ミクロンのNi電流コレクタで裏張りされ、使用したカソード物質、即ち1mA時/cm2の酸化バナジウム複合電極の約4倍の容量(クーロン)を有していた。これらの3個の電池を、各々0psi、50psi及び100psiの異なる圧縮性負荷(圧力)下に維持した以外は厳密に等しい電流及び電圧の条件下でサイクル反復使用した。100サイクル後、3個の電池を分解し、走査型電子顕微鏡(SEM)で観察した。0psiの圧力ではリチウムの形態がかなり発達していたが、50psiでは表面に若干の凹凸が生じており、100psiの負荷下の電池のリチウムは組立開始のときに使用したリチウムにほぼ等しい状態であった。これは、DEKTAK装置による表面プロフィル測定試験でも確認された。この場合の電解質の変形性はLiの変形性と同じ程度であった。圧力の影響は顕著であるが、長期間のサイクル反復中の形態的発達を完全に防ぐことはできない。
【0084】
実施例4
アルゴン充填グローブボックスで等しい2個の電池を組立てた。この実施例では、両面構造、即ち、容量1mA時/cm2の酸化バナジウムカソードと厚み35ミクロンの電解質フィルムとから成る2個の半電池間にサンドイッチされた非支持(遊離)リチウムを使用した。遊離リチウムは30ミクロンの厚みを有していた。電解質の硬度は35%であり、従ってこれは半硬質膜であると考えられる。構造は、正極/電解質/リチウム/電解質/正極に対応する。
【0085】
電池の全厚は200ミクロンの範囲である。この構造は、カソードの容量の2倍に等価の過剰のLiを含み、コレクタとして作用する。双方の電池を等しいサイクル反復条件、即ち、1.5〜3.3ボルトを電圧限度として6時間の放電モードと12時間の充電モードという条件で試験した。一方の電池には50psiの圧力を負荷し、他方に電池には圧力を負荷しないで50サイクル使用を実施した。双方の電池が優秀なサイクル反復特性、即ちほぼ100%のクローン効率及びカソード物質の高い利用率を示した。事後分析は、圧力を作用させずにサイクル使用した電池は±10ミクロンのピーク及びバレーを示す表面プロフィルを有していたが、第二の電池ではリチウムが極めて均一に維持されており、表面の凹凸は±1ミクロンを超えていなかった。
【0086】
実施例5
相対湿度1%未満の乾燥室で同様の2個の電池を組立てた。3.9cm2の寸法の2つの電池で同じ正極(5C/cm2の酸化バナジウム)及び30ミクロンの同じ厚みの電解質を使用した。一方の電池には厚み20ミクロンの遊離リチウムフィルムをアノードとして使用し、他方の電池には厚み9ミクロンのニッケル箔に厚み20ミクロンのリチウムを積層したアノードを使用した。
【0087】
100サイクル(C/6の放電及びC/12の充電)後に、双方の電池を分解して観察した。第一の電池では、非支持のリチウムが±5ミクロンのオーダの測定可能な表面形態を発達させており、その表面にカプセル化(不動態化)リチウムがある程度存在していた。これは継続的なサイクル中にリチウムと固体ポリマー電解質との間に生じた相互侵入の結果である(図3参照)。同じ期間中に第二の電池に発達した凹凸ははるかに少なかった。(水素の発生量を測定することによって)メタノールと反応したリチウムの化学的活性を測定すると、Liは、そのある程度の部分が電解質の大部分と電気接触していない場合であっても十分に活性であることが判明した。
【0088】
この実施例(電池#1)は、極めて薄い非支持Liの(Liの表面及び内部における)形態変化を示しており(図3参照)、無水ポリマー電解質の存在下で大半のリチウムが金属状態に維持されるので、サイクル反復によって電気接触が失われることを示す。しかしながら電池#2(図2)は、Liの薄いシートに接着する支持コレクタの使用によってこの形態変化が多少とも制御されることを示す。
【0089】
実施例6
サイクル反復の挙動を改善するために有利な要因の組合せを使用し得る。この実施例では、同様の2つの電池を等しいサイクル条件下でサイクル試験した。一方の電池を50psiの圧力下で使用し、他方の電池を0psiでサイクル試験した。第一電池は銅の電流コレクタに積層されたリチウムアノードを有していたが、第二電池では自立するリチウム箔を使用した。同じ半電池、即ち、厚み30ミクロンの電解質に積層された同じ複合カソードを使用して双方の電池を作製した。カソードの容量は7C/cm2であった。電解質は半硬質で約30%の侵入度を有していた。60℃では双方の電池の初期インピーダンスはほぼ等しい値であった。しかしながらサイクル反復中に、ピーク電流に対する第一電池の応答は第二電池に比べて改良されていた。また、第一電池は総合的にもより優れたサイクル反復挙動を示した。200サイクル後、双方の電池を分解し、リチウム表面の凹凸を分析すると、第一電池のほうが良好なリチウム形態を有していた。即ち、第二電池の凹凸±12ミクロンに比較して±3ミクロンであった。
【0090】
実施例7
実施例6と同様の電池において、電力特性及びサイクル反復特性を改善するために、電解質の硬度及びリチウム電流コレクタの使用という有利な2つの効果を組合せた。
【0091】
第一の電池では、膜厚30ミクロンのVdBメタクリレート膜を使用した(表2参照)。第二の電池の場合には、厚み35ミクロンのERM電解質をリチウムの電流コレクタと共に使用した。電解質は厚み20ミクロンであり、初期厚みの20%未満の変形に等価の硬度を有していた。前述の実施例2と同じ装置を使用した。各電池を圧力15psi下に維持した。300サイクル後であっても2つの電池のリチウム表面には実質的に凹凸がなく、凹凸は±1ミクロン未満であり、従って、SEIの幾何学的表面の撹乱が最小限に抑制されていた。電解質の表面も無傷に維持されていた(図6)。
【0092】
実施例8
別の4cm2の電池では、6C/cm2の正極に対して10ミクロンの銅箔に積層された極めて薄いリチウムアノード(10ミクロン)を使用した。これは、正極容量の約20%過剰に対応する。厚み25ミクロンの硬質電解質(侵入度20%)を使用し、電池を50psiの圧力下に維持した。120サイクルを過ぎてても、容量が十分に維持され、クーロン効率も優れていた(ほぼ100%)。
【0093】
この結果は、材料及びサイクル反復条件の適切な選択によって電池の挙動を顕著に改善し得ることを示す。金属リチウムを基材とする電池はいかなる所与の大きさの場合にも、リチウムの量を必要最小限まで減らすことが重要である。
【0094】
このようにして、特に異常な温度上昇が生じたとき、例えばLiの溶融温度を上回る温度上昇が生じたときの電池の安全性が大幅に改善される。
【0095】
実施例9
硬質セパレータとの組合せによって得られた利点はまた、正極/電解質/リチウム/電解質/正極に対応する両面構造によって確認された。。正極は有効容量5C/cm2を有し、電解質の厚みは20ミクロンであった。中央のリチウムアノードの厚みは0.5の過剰に対応する20ミクロンであった。電解質の硬度は前記の実施例7と同じであった。100サイクル(50psi)後、電池はサイクル反復中に良好な挙動を維持しており、リチウム表面の凹凸は±2ミクロン未満であった。リチウムは電流コレクタの役割を好適に果たす連続構造を維持していた。
【0096】
実施例10
この最後の実施例では、実施例8と同じ正極及び同じ電解質を使用した。アノードとしては、純粋な金属リチウムを使用する代わりに、1原子%のAlと99原子%のリチウムとを含むリチウムアルミニウム合金を使用した。この少量のアルミニウムはアノードの硬度に直接効果を与える。しかしながらこの合金は金属リチウムと同様の薄さで積層できる。
【0097】
このタイプの軽合金リチウムアノードは、アノードのサイクル反復挙動に対してもそのインピーダンスに対しても不利な影響を与えないことが観察された。リチウム表面の事後分析によれば、表面が純リチウムと同様に滑らかであることが確認される。
【0098】
先行実施例に示したように、純度、固体ポリマー電解質の低変形性、圧力の使用、Li電極に付着する金属支持体の使用、などの種々の要因の組合せによって、サイクル反復中のLi−ポリマー電解質境界面を最適にし、電池に組込むリチウムの超過度を低減することが可能である。
【0099】
ある種の無水“ポリマー電解質”とリチウムを化学的に消費しない金属リチウムアノードとを用いた電気化学電池の製造が可能になったため、リチウムアノードの形態の顕著な変化及びLio/ポリマー電解質境界面の顕著な変形を生じることなく、多数回の放充電サイクルを実行し得る最適化されたアノード/ポリマー電解質及び完全な電気化学電池を製造し得る実験条件及び配合組成が設計されるようになった。
【0100】
液体電解質が主流であった従来技術と対照的に、固体電解質を使用した場合のサイクル反復中のリチウムの形態の変化は、金属Lioの不動態化−化学的消費の結果でなく、薄いフィルムに対する機械的作用(放充電サイクルによって誘発される応力)の結果であることがここに確認された。本発明においては、固体系のこの特徴を利用し、サイクル反復中にリチウムアノードを圧縮形態に維持するために電解質と機械的圧力とを組合せる。
【0101】
本発明は、リチウムアノードのサイクル反復適性を確保するために必要なポリマー電解質の特性、例えば、変形性のような機械的特性、及び、化学的組成を規定している。例えば、プロトン性溶媒のようなLiに反応性の可動種が低含量であること、または、反応性末端基Liを含むポリマーが低分子量であること、などを規定している。本発明はまたLiのアノードに圧力を伝達するセパレータ電解質の機械的特性を利用している。
【0102】
従来技術と対照的に、最適化されたLio/ポリマー電解質アセンブリ、及び、カソード容量に対するリチウムの超過度が明らかに3未満、好ましくは1〜2、より好ましくは1未満であるような再充電可能な電池を提供することが可能になったことが立証された。
【図面の簡単な説明】
【図1】 多孔質セパレータに含浸させた液体電解質を用いる再充電可能リチウム電池の構造説明図である。
【図2】 従来技術によってポリマー電解質を使用し(Siena,Belangero、前出)金属アノードのコレクタを備えている電池をある程度進んだサイクル反復段階で示す説明図である。
【図3】 従来技術によってポリマー電解質を使用し(Siena,Belangero、前出)コレクタを備えていないので反対側に変形が生じている電池をある程度進んだサイクル反復段階で示す説明図である。
【図4】 分解後及びサイクル反復前の本発明の再充電可能なポリマー電解質電池の説明図であり、ポリマー電解質が微変形性であるときのポリマーリチウム境界面に対する機械的圧力の効果及びSEIのフィルムの維持を示す。
【図5】 本発明の蓄電池の種々の境界面を示す極低温断面の倍率1000倍の顕微鏡写真であり、数百回のサイクル後の高密度リチウムの薄いシートの維持、及び、境界面Lio/SEI/SDPE(Slightly Deformable Polymer Electrolyte微変形性ポリマー電解質)セパレータの維持を示す。
【図6】 数百回のサイクル後に分解したときの電解質SDPEの表面状態の維持を示す本発明の電池の極低温断面の概略図である。
Claims (27)
- アルカリ金属または展性アルカリ金属合金から成るアノードと、アルカリ性カチオンの導体でありセパレータとして作用する少なくとも1種のポリマー電解質と、アルカリ金属のカチオンに対して可逆性の少なくとも1つのカソードと、その電流コレクタと、から成り、
アノードが、前記金属と前記ポリマー電解質との反応を制限しかつ継続的な充放電サイクル中にリチウムイオンを交換し得る固体−電解質境界面の不動態化フィルムを表面に備えた厚み100マイクロメータ未満の薄い金属シートから成り、
ポリマー電解質は、機械的変形に抵抗性であり、アノードに圧力を伝達し、その厚みの35%未満の割合の変形を生じることによってアノードの金属の樹枝状応力に抵抗し得る均一セパレータを構成し、
セパレータのポリマー電解質及び任意に複合カソードを用いる場合のカソードのポリマー電解質は、アノード/ポリマー電解質の境界面のイオン交換品質を保持するために、リチウムに反応性でアノードの表面に蓄積できる可動種を3000Å未満に等価のアルカリ金属の消費に対応する最大量で含んでおり、
アルカリ金属アノードと電解質セパレータとカソードとコレクタとのアセンブリは、セパレータがアノードシートを所定位置に維持し、且つ、継続的な溶解/付着サイクル中にリチウム−ポリマー電解質境界面の結合性を維持し得るに十分な機械的応力下に維持されていることを特徴とする再充電可能な電池。 - 前記アノードが40マイクロメータ未満の厚みを有することを特徴とする請求項1に記載の再充電可能な電池。
- 電解質の変形率がその厚みの25%未満であることを特徴とする請求項1に記載の再充電可能な電池。
- 前記アノードがリチウムまたはその展性合金から成ることを特徴とする請求項1に記載の再充電可能な電池。
- 過剰の前記アノードが更にシートの電流コレクタとして使用されることを特徴とする請求項1に記載の再充電可能な電池。
- 前記アノードがその両面をアノードとして使用する非支持シートから成ることを特徴とする請求項1に記載の再充電可能な電池。
- ポリマー電解質が30ミクロン未満の厚みを有することを特徴とする請求項1に記載の再充電可能な電池。
- 前記ポリマー電解質が、アノードと同じアルカリ金属の塩のカチオンの溶媒和物を形成し得る酸素または窒素の供与体であるヘテロ原子を含むことを特徴とする請求項1に記載の再充電可能な電池。
- 前記ポリマー電解質が50psiのオーダのヤング率、即ち実質的に金属リチウムのヤング率を有することを特徴とする請求項1に記載の再充電可能な電池。
- 前記ポリマー電解質が、変形率を初期厚みの35%未満に制限するために十分な鎖の架橋密度または鎖の交絡密度を有しており、サイクル反復中のリチウムの変形に抵抗性であることを特徴とする請求項1に記載の再充電可能な電池。
- ポリマー電解質が前記硬度を与えるためにアルカリ金属に不活性の充填剤を含有し、前記充填剤は1マイクロメータ未満の粒度を有することを特徴とする請求項1に記載の再充電可能な電池。
- 前記充填剤がアルミナ、シリカまたはマグネシアであることを特徴とする請求項11に記載の再充電可能な電池。
- 電解質が、1000オングストロームのLi消費に等価の量よりも少ない量の不純物または可動反応性基を含むことを特徴とする請求項1に記載の再充電可能な電池。
- 機械的応力はセパレータが電池のアノードに作用させる圧力であり、5〜150psiの範囲であることを特徴とする請求項1に記載の再充電可能な電池。
- 前記機械的応力は、アノード、電解質及びカソードの各シートを一定の外側体積以内の大きさのコイルの形態に巻装することによって確保されることを特徴とする請求項1に記載の再充電可能な電池。
- アノードと電解質とカソードとが一定圧力または一定体積に維持される角柱の形態に形成されることを特徴とする請求項1に記載の再充電可能な電池。
- 角柱が、アノード、電解質及びカソードの各シートのフラット巻き取りシートを形成するか、または、ジグザグに積層することによって得られることを特徴とする請求項1に記載の再充電可能な電池。
- 前記アノードが、非支持アノードシートの結合性を維持しサイクル反復中の電流収集を確保する硬化リチウムアノードであることを特徴とする請求項1に記載の再充電可能な電池。
- リチウムアノードが、純Liよりも展性の小さい高リチウム含量のリチウム合金から成り、過剰のLiがアノードを非変形性の電流コレクタとして作用させ得ることを特徴とする請求項1に記載の再充電可能な電池。
- アノードの容量がカソードの可逆性容量の約1.5〜3.5倍であることを特徴とする請求項1に記載の再充電可能な電池。
- アノードがアルカリ金属またはアルカリ金属合金のシートから成り、前記シートに付着するコレクタによって支持されていることを特徴とする請求項1に記載の再充電可能な電池。
- プラスチックシート、典型的にはポリプロピレン、ポリエチレンのシートに支持されていることを特徴とする請求項1に記載の再充電可能な電池。
- 前記コレクタがCu、FeまたはNiの薄いシートから成ることを特徴とする請求項22に記載の再充電可能な電池。
- アノードが電解質と正極とから成る2個の半電池の間に装着されていることを特徴とする請求項1に記載の再充電可能な電池。
- アノードが薄い剛性の中央支持体の両面に装着されたアルカリ金属またはアルカリ金属合金の2枚のフィルムから成ることを特徴とする請求項1に記載の再充電可能な電池。
- 前記電解質と前記アノードとの間、または前記電解質と前記カソードとの間に、薄い粘着性の第二電解質が備えられており、前記第二電解質は、電池の種々の構成素子間の安定な境界面の形成を確保することを特徴とする請求項1に記載の再充電可能な電池。
- 再充電可能な電池に使用するための、展性アルカリ金属または合金から成るアノードと、アルカリ性カチオン伝導性でありセパレータとして作用する少なくとも1種のポリマー電解質との組合せであって、
アノードが、前記金属と前記ポリマー電解質との反応を制限しかつ継続的な充放電サイクル中にリチウムイオンを交換し得る固体−電解質境界面の不動態化フィルムを表面に備えた厚み100マイクロメータ未満の薄い金属シートから成り、
ポリマー電解質は、機械的変形に抵抗性であり、アノードに圧力を伝達しその厚みの35%未満の割合の変形を生じることによってアノードの金属の樹枝状応力に抵抗し得る均一セパレータを構成し、
セパレータのポリマー電解質の量は、リチウムに反応性でアノードの表面に蓄積できる種をアノード/ポリマー電解質境界面のイオン交換品質を保持するための最大量で含み、
アルカリ金属アノードと電解質セパレータとの組合せは、セパレータがアノードシートを所定位置に維持し、前記アノードとの組合せを含む電池の継続的な溶解/付着サイクル中にリチウム−ポリマー電解質境界面の結合性を維持するために十分な機械的応力下に維持されていることを特徴とする、前記アノードとポリマー電解質との組合せ。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2191019 | 1996-11-22 | ||
| CA002191019A CA2191019C (fr) | 1996-11-22 | 1996-11-22 | Anode de lithium rechargeable pour accumulateur a electrolyte polymere |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPH10214641A JPH10214641A (ja) | 1998-08-11 |
| JP4480098B2 true JP4480098B2 (ja) | 2010-06-16 |
Family
ID=4159296
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP32291697A Expired - Lifetime JP4480098B2 (ja) | 1996-11-22 | 1997-11-25 | ポリマー電解質蓄電池用の再充電可能なリチウムアノード |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US6007935A (ja) |
| JP (1) | JP4480098B2 (ja) |
| CA (1) | CA2191019C (ja) |
| DE (1) | DE19751289B4 (ja) |
| FR (1) | FR2756422B1 (ja) |
| GB (1) | GB2319654B (ja) |
| IT (1) | IT1296479B1 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6218048B1 (en) | 1998-04-07 | 2001-04-17 | Fmc Corporation | Method of preliminarily heat treating positive electrodes of secondary lithium and lithium-ion Batteries and resulting positive electrodes and batteries |
| US6664006B1 (en) | 1999-09-02 | 2003-12-16 | Lithium Power Technologies, Inc. | All-solid-state electrochemical device and method of manufacturing |
| US6645675B1 (en) | 1999-09-02 | 2003-11-11 | Lithium Power Technologies, Inc. | Solid polymer electrolytes |
| JP4959048B2 (ja) * | 2000-12-25 | 2012-06-20 | トータル ワイヤレス ソリューショオンズ リミテッド | シート状リチウム二次電池 |
| ITMI20020902A1 (it) * | 2002-04-26 | 2003-10-27 | Ausimont Spa | Processo per preparare membrane ionomeriche |
| KR100485091B1 (ko) * | 2002-10-25 | 2005-04-22 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 음극 및 이를 포함하는 리튬 이차 전지 |
| JP2004220819A (ja) * | 2003-01-09 | 2004-08-05 | Sony Corp | 電解質、負極および電池 |
| US7541715B2 (en) * | 2004-06-14 | 2009-06-02 | Massachusetts Institute Of Technology | Electrochemical methods, devices, and structures |
| US20050287441A1 (en) * | 2004-06-23 | 2005-12-29 | Stefano Passerini | Lithium polymer electrolyte batteries and methods of making |
| CN101522345B (zh) * | 2006-08-30 | 2012-08-29 | 尤米科尔股份公司及两合公司 | 包含金属或陶瓷核材料的核/壳型催化剂颗粒及它们的制备方法 |
| US8288308B2 (en) * | 2006-08-30 | 2012-10-16 | Umicore Ag & Co. Kg | Core/shell-type catalyst particles and methods for their preparation |
| RU2488196C1 (ru) * | 2012-06-04 | 2013-07-20 | федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Национальный исследовательский университет "МЭИ" (ФГБОУ ВПО "НИУ МЭИ") | Способ изготовления катода литиевого источника тока |
| US20170047586A1 (en) | 2014-04-16 | 2017-02-16 | Basf Se | Electrochemical cells exposed to hydrostatic pressure |
| DE102014108704B4 (de) * | 2014-06-20 | 2020-09-03 | Thyssenkrupp Ag | Metallionen-Akkumulator |
| DE102014222332A1 (de) | 2014-10-31 | 2016-05-04 | Robert Bosch Gmbh | Schichtaufbau für ein galvanisches Element |
| DE102017217042A1 (de) * | 2017-09-26 | 2019-03-28 | Robert Bosch Gmbh | Elektrochemische Zelle mit mäanderförmig ausgeführtem Stromableiter |
| KR102238829B1 (ko) * | 2018-02-07 | 2021-04-09 | 주식회사 엘지화학 | 리튬 금속 이차전지 및 이를 포함하는 전지모듈 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5114804A (en) * | 1981-08-13 | 1992-05-19 | Moli Energy Limited | Battery and method of making the battery |
| CA1173900A (fr) * | 1982-06-30 | 1984-09-04 | Hydro-Quebec | Anodes composites et souples de pile au lithium en milieu non-aqueux |
| CA1222543A (fr) * | 1984-04-11 | 1987-06-02 | Hydro-Quebec | Anodes denses d'alliages de lithium pour batteries tout solide |
| US4587182A (en) * | 1984-12-11 | 1986-05-06 | Moli Energy Limited | Constant volume lithium battery cell and process |
| FR2616971A1 (fr) * | 1987-06-18 | 1988-12-23 | Elf Aquitaine | Ensemble intermediaire pour la realisation sous la forme de films minces d'un accumulateur au lithium, procede de realisation de cet ensemble et procede de realisation de l'accumulateur |
| US5223353A (en) * | 1990-03-16 | 1993-06-29 | Ricoh Company, Ltd. | Solid electrolyte, electrochemical device including the same and method of fabricating the solid electrolyte |
| US5418091A (en) * | 1993-03-05 | 1995-05-23 | Bell Communications Research, Inc. | Polymeric electrolytic cell separator membrane |
| US5346788A (en) * | 1993-04-01 | 1994-09-13 | W. R. Grace & Co.-Conn. | Microporous polyurethane based battery separator |
| JPH06302314A (ja) * | 1993-04-01 | 1994-10-28 | Wr Grace & Co Connecticut | 電池隔離板 |
| US5354631A (en) * | 1993-06-08 | 1994-10-11 | Valence Technology, Inc. | Enhanced lithium surface |
| US5528920A (en) * | 1993-07-02 | 1996-06-25 | Hydro-Quebec | Process for laminating a thin film of lihium by controlled detachment |
| CA2111049A1 (fr) * | 1993-12-09 | 1995-06-10 | Paul-Etienne Harvey | Copolymere d'oxyde d'ethylene et/ou d'oxyde de propylene et d'au moins un oxiranne portant une fonction reticulable, un procede pour sa preparation et son utilisation pour l'elaboration de materiaux a conduction onique |
| JP3387188B2 (ja) * | 1993-12-29 | 2003-03-17 | ソニー株式会社 | コイン形リチウム電池 |
| US5648187A (en) * | 1994-02-16 | 1997-07-15 | Moltech Corporation | Stabilized anode for lithium-polymer batteries |
| WO1995029513A1 (en) * | 1994-04-20 | 1995-11-02 | Valence Technology, Inc. | Radiation curable frame for stacked cell construction and for edge sealing of electrochemical cells to retard dendritic short-circuits |
| US5434021A (en) * | 1994-08-12 | 1995-07-18 | Arthur D. Little, Inc. | Secondary electrolytic cell and electrolytic process |
-
1996
- 1996-11-22 CA CA002191019A patent/CA2191019C/fr not_active Expired - Lifetime
-
1997
- 1997-04-23 US US08/844,858 patent/US6007935A/en not_active Expired - Lifetime
- 1997-11-05 GB GB9723245A patent/GB2319654B/en not_active Expired - Lifetime
- 1997-11-19 DE DE19751289A patent/DE19751289B4/de not_active Expired - Lifetime
- 1997-11-20 IT IT97MI002586A patent/IT1296479B1/it active IP Right Grant
- 1997-11-21 FR FR9714872A patent/FR2756422B1/fr not_active Expired - Lifetime
- 1997-11-25 JP JP32291697A patent/JP4480098B2/ja not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| CA2191019A1 (fr) | 1998-05-22 |
| GB2319654B (en) | 2000-02-09 |
| FR2756422B1 (fr) | 2002-06-21 |
| GB9723245D0 (en) | 1998-01-07 |
| JPH10214641A (ja) | 1998-08-11 |
| FR2756422A1 (fr) | 1998-05-29 |
| GB2319654A (en) | 1998-05-27 |
| IT1296479B1 (it) | 1999-06-25 |
| CA2191019C (fr) | 2001-01-16 |
| DE19751289A1 (de) | 1998-05-28 |
| US6007935A (en) | 1999-12-28 |
| ITMI972586A1 (it) | 1999-05-20 |
| DE19751289B4 (de) | 2013-11-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4480098B2 (ja) | ポリマー電解質蓄電池用の再充電可能なリチウムアノード | |
| CN103718337B (zh) | 用于电极的电镀技术 | |
| US5800939A (en) | Battery and method for the manufacture of such a battery | |
| KR101389609B1 (ko) | 리튬 2차 전지와 그 이용 | |
| CN102144324B (zh) | 电化学电池中力的应用 | |
| TW529190B (en) | Polymer electrolyte battery and method of producing the same | |
| CN113422097B (zh) | 用于能量存储设备的纵向约束 | |
| CN100490218C (zh) | 隔片、凝胶电解质、非水电解质、电极和使用它们的电池 | |
| KR102339208B1 (ko) | 가압된 리튬 금속 중합체 배터리 | |
| KR20180101728A (ko) | 복합 고체 전해질을 갖는 리튬 배터리 | |
| CN113614951B (zh) | 制备用于二次电池的负极的方法 | |
| WO1997014188A1 (en) | Electrolytic cell and electrolytic process | |
| CN103493275B (zh) | 包括牺牲性锂电极和织物转化正极的锂离子电池前体 | |
| JP2002245998A (ja) | 電池パック及び電池 | |
| KR100462668B1 (ko) | 폴리머 전지 | |
| JPH11288738A (ja) | 固体電解質電池およびその製造方法 | |
| JP3500245B2 (ja) | ゲル状固体電解質二次電池 | |
| JP2003331838A (ja) | リチウム二次電池 | |
| JPH0950823A (ja) | 二次電池 | |
| JPH08222272A (ja) | 非水電解液二次電池と太陽電池との組み合わせ電池 | |
| JPH10261437A (ja) | ポリマ電解質およびそれを用いたリチウム・ポリマ電池 | |
| US11450845B2 (en) | Surface modification of silicon-containing electrodes using carbon dioxide | |
| JPH0695458B2 (ja) | 二次電池 | |
| JP2003317695A (ja) | 非水電解質リチウムイオン電池とそのためのセパレータ | |
| JPH10302841A (ja) | リチウム二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041102 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080724 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081022 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20090318 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091221 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100223 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20100301 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20100305 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100315 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130326 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140326 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |