JP4454249B2 - 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット - Google Patents
膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット Download PDFInfo
- Publication number
- JP4454249B2 JP4454249B2 JP2003114380A JP2003114380A JP4454249B2 JP 4454249 B2 JP4454249 B2 JP 4454249B2 JP 2003114380 A JP2003114380 A JP 2003114380A JP 2003114380 A JP2003114380 A JP 2003114380A JP 4454249 B2 JP4454249 B2 JP 4454249B2
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- acid probe
- fluorescent dye
- sequence
- probe
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 108020004711 Nucleic Acid Probes Proteins 0.000 title claims abstract description 32
- 239000002853 nucleic acid probe Substances 0.000 title claims abstract description 32
- 210000004153 islets of langerhan Anatomy 0.000 title claims abstract description 15
- 238000000034 method Methods 0.000 title claims description 38
- 102000009091 Amyloidogenic Proteins Human genes 0.000 title claims description 13
- 108010048112 Amyloidogenic Proteins Proteins 0.000 title claims description 13
- 108090000623 proteins and genes Proteins 0.000 title description 5
- 239000000523 sample Substances 0.000 claims abstract description 50
- 230000035772 mutation Effects 0.000 claims abstract description 38
- 239000007850 fluorescent dye Substances 0.000 claims abstract description 33
- 239000002773 nucleotide Substances 0.000 claims abstract description 25
- 125000003729 nucleotide group Chemical group 0.000 claims abstract description 25
- 108020004707 nucleic acids Proteins 0.000 claims abstract description 21
- 102000039446 nucleic acids Human genes 0.000 claims abstract description 21
- 150000007523 nucleic acids Chemical class 0.000 claims abstract description 21
- 238000011880 melting curve analysis Methods 0.000 claims abstract description 11
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims abstract description 9
- 230000000295 complement effect Effects 0.000 claims abstract description 9
- 239000004471 Glycine Substances 0.000 claims abstract description 7
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims abstract description 7
- 230000007423 decrease Effects 0.000 claims abstract description 7
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 claims abstract description 7
- 230000003321 amplification Effects 0.000 claims description 25
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 25
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 claims description 7
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 claims description 7
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 claims description 5
- 125000003275 alpha amino acid group Chemical group 0.000 claims 2
- 102000036770 Islet Amyloid Polypeptide Human genes 0.000 abstract description 21
- 108010041872 Islet Amyloid Polypeptide Proteins 0.000 abstract description 21
- 102220082839 rs149700042 Human genes 0.000 abstract description 19
- 150000001413 amino acids Chemical group 0.000 abstract description 5
- 238000009396 hybridization Methods 0.000 abstract description 2
- PLOPBXQQPZYQFA-AXPWDRQUSA-N amlintide Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H]1NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CCCCN)CSSC1)[C@@H](C)O)C(C)C)C1=CC=CC=C1 PLOPBXQQPZYQFA-AXPWDRQUSA-N 0.000 abstract 1
- 238000001514 detection method Methods 0.000 description 18
- 238000010791 quenching Methods 0.000 description 15
- 230000000171 quenching effect Effects 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 238000006243 chemical reaction Methods 0.000 description 13
- 239000013612 plasmid Substances 0.000 description 10
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 206010012601 diabetes mellitus Diseases 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 230000035945 sensitivity Effects 0.000 description 4
- 238000001962 electrophoresis Methods 0.000 description 3
- 108091008146 restriction endonucleases Proteins 0.000 description 3
- ABZLKHKQJHEPAX-UHFFFAOYSA-N tetramethylrhodamine Chemical compound C=12C=CC(N(C)C)=CC2=[O+]C2=CC(N(C)C)=CC=C2C=1C1=CC=CC=C1C([O-])=O ABZLKHKQJHEPAX-UHFFFAOYSA-N 0.000 description 3
- COCMHKNAGZHBDZ-UHFFFAOYSA-N 4-carboxy-3-[3-(dimethylamino)-6-dimethylazaniumylidenexanthen-9-yl]benzoate Chemical compound C=12C=CC(=[N+](C)C)C=C2OC2=CC(N(C)C)=CC=C2C=1C1=CC(C([O-])=O)=CC=C1C(O)=O COCMHKNAGZHBDZ-UHFFFAOYSA-N 0.000 description 2
- 238000000137 annealing Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000011109 contamination Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 238000007894 restriction fragment length polymorphism technique Methods 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 210000002237 B-cell of pancreatic islet Anatomy 0.000 description 1
- AHCYMLUZIRLXAA-SHYZEUOFSA-N Deoxyuridine 5'-triphosphate Chemical compound O1[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)C[C@@H]1N1C(=O)NC(=O)C=C1 AHCYMLUZIRLXAA-SHYZEUOFSA-N 0.000 description 1
- 101100286193 Homo sapiens IAPP gene Proteins 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 102000006943 Uracil-DNA Glycosidase Human genes 0.000 description 1
- 108010072685 Uracil-DNA Glycosidase Proteins 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- SUYVUBYJARFZHO-RRKCRQDMSA-N dATP Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-RRKCRQDMSA-N 0.000 description 1
- SUYVUBYJARFZHO-UHFFFAOYSA-N dATP Natural products C1=NC=2C(N)=NC=NC=2N1C1CC(O)C(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-UHFFFAOYSA-N 0.000 description 1
- RGWHQCVHVJXOKC-SHYZEUOFSA-J dCTP(4-) Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)C1 RGWHQCVHVJXOKC-SHYZEUOFSA-J 0.000 description 1
- HAAZLUGHYHWQIW-KVQBGUIXSA-N dGTP Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 HAAZLUGHYHWQIW-KVQBGUIXSA-N 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
Landscapes
- Health & Medical Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Optics & Photonics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
【発明の属する技術分野】
本発明は、膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキットに関する。
【0002】
【従来の技術】
膵ラ氏島アミロイドタンパク質(Islet Amyloid Polypeptide(IAPP))は2型糖尿病患者の膵ラ氏島に高頻度に沈着しているアミロイドの主要構成成分で、膵β細胞からインスリンと共に血中に分泌されている。IAPPのアミノ酸配列の20位のセリンがグリシンに置換するミスセンス変異(S20G変異)は日本人2型糖尿病患者の約2.6%、その中でも若年発症者の約10%に存在しており、この変異が存在することで糖尿病の発症リスクが高まるといわれている。
【0003】
IAPPにS20G変異をもたらす塩基の変異(以下、「IAPP S20G変異」ともいう)が存在するとその部分に制限酵素の認識部位が出現するため、PCRで変異部分を含むように増幅を行い、制限酵素で切断し、その後電気泳動で切断されたかどうかを検出するという方法(PCR-RFLP)で検出を行うことが知られている(非特許文献1)。
【0004】
PCRは数分子の鋳型から数10億倍もの分子を増幅するため、増幅産物がほんの少し混入した場合でも偽陽性、偽陰性の原因になり得る。PCR-RFLPはPCR反応後に増幅産物を取り出して制限酵素処理を行うという必要があるため、増幅産物が次の反応系に混入する恐れがある。よって、偽陽性、偽陰性の結果が得られてしまうことがある。さらに、PCR終了後、制限酵素で処理を行い、その後電気泳動を行うため、検出に必要な時間も非常に長くかかってしまう。また、操作が複雑なため、自動化が困難である。
【0005】
一方、一般に、変異を含む領域をPCRで増幅した後、蛍光色素で標識された核酸プローブを用いて融解曲線分析を行い、融解曲線分析の結果に基づいて変異を解析する方法が知られている(非特許文献2、特許文献1)。
【0006】
【非特許文献1】
日本糖尿病学会編、「糖尿病遺伝子診断ガイド」、文光堂、p.56−59
【非特許文献2】
クリニカルケミストリー(Clinical Chemistry)、2000年、第46巻、第5号、p.631−635
【特許文献1】
特開2002−119291号公報
【0007】
【発明が解決しようとする課題】
本発明の課題は、IAPP S20G変異を検出するのに有効な消光プローブを特定し、IAPP S20G変異を検出する方法及びそのためのキットを提供することを課題とする。
【0008】
【課題を解決するための手段】
上述のプローブを用いる方法に関する文献においては、プローブの設計に関し、末端部が蛍光色素により標識された消光プローブが標的核酸にハイブリダイゼーションしたとき、末端部分においてプローブ−核酸ハイブリッドの複数塩基対が少なくとも一つのGとCのペアを形成するように設計するという教示があるのみである。本発明者らは、IAPP S20G変異に関し、上記条件を満たす消光プローブを設計し、検出を試みたが、容易に検出を可能とする消光プローブは得られなかった。
【0009】
本発明者らは、IAPP S20G変異を含む特定の領域に基づいて消光プローブを設計することにより、消光プローブを用いる融解曲線分析によりIAPP S20G変異を検出できることを見出し、本発明を完成した。
本発明は、以下のものを提供する。
【0010】
(1)末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブであって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列を有し、5’末端が蛍光色素で標識されている前記核酸プローブ。
【0011】
(2)核酸プローブが、配列番号12または13を有する(1)の核酸プローブ。
【0012】
(3)一塩基多型の部位を有する核酸について、蛍光色素で標識された核酸プローブを用いて、蛍光色素の蛍光を測定することにより融解曲線分析を行い、融解曲線分析の結果に基づいて変異を検出する方法であって、一塩基多型は、膵ラ氏島アミロイドタンパク質をコードする核酸における、膵ラ氏島アミロイドタンパク質のアミノ酸配列の20位のセリンがグリシンに置換する変異をもたらす塩基配列の変異であり、核酸プローブは、(1)または(2)の核酸プローブである前記方法。
【0013】
(4)試料に含まれる核酸における一塩基多型の部位を含む領域を増幅して一塩基多型を有する核酸を得ることを含む(3)の方法。
【0014】
(5)増幅をDNAポリメラーゼを用いる方法により行う(4)の方法。
【0015】
(6)増幅を核酸プローブの存在下で行う(5)の方法。
【0016】
(7)末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブであって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列を有し、5’末端が蛍光色素で標識されている前記核酸プローブを含む、(3)の方法のためのキット。
【0017】
(8)核酸プローブが、配列番号12または13を有する(6)のキット。
【0018】
(9)膵ラ氏島アミロイドタンパク質をコードする核酸における、膵ラ氏島アミロイドタンパク質のアミノ酸配列の20位のセリンがグリシンに置換する変異をもたらす塩基配列の変異を含む領域を、DNAポリメラーゼを用いる方法で増幅するためのプライマーをさらに含む(7)または(8)のキット。
【0019】
【発明の実施の形態】
<1>本発明プローブ及び本発明検出方法
本発明プローブは、末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブであって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列を有し、5’末端が蛍光色素で標識されていることを特徴とする。
【0020】
本発明プローブは、配列番号1に示す塩基配列(IAPP S20G変異における変異型の塩基を有する配列)において塩基番号247で終わる13〜30塩基長の配列に相補的な配列を有する他は、特許文献1に記載された消光プローブと同様でよい。本発明に使用される消光プローブの塩基配列の例としては、配列番号12及び13が挙げられる。蛍光色素としては、特許文献1に記載されたものが使用できるが、具体例としては、FAM(商標)、TAMRA(商標)、BODIPY(商標) FL等が挙げられる。蛍光色素のオリゴヌクレオチドへの結合方法は、通常の方法、例えば特許文献1に記載の方法に従って行うことができる。
【0021】
本発明検出方法は、一塩基多型の部位を有する核酸について、蛍光色素で標識された核酸プローブを用いて、蛍光色素の蛍光を測定することにより融解曲線分析を行い、融解曲線分析の結果に基づいて変異を検出する方法であって、一塩基多型は、膵ラ氏島アミロイドタンパク質をコードする核酸における、膵ラ氏島アミロイドタンパク質のアミノ酸配列の20位のセリンがグリシンに置換する変異をもたらす塩基配列の変異であり、核酸プローブは本発明プローブであることを特徴とする。
【0022】
本発明検出方法は、IAPPをコードするDNAのIAPP S20G変異を含む領域を増幅すること、及び、本発明プローブを用いることの他は、通常の核酸増幅及び融解曲線分析(Tm解析)の方法に従って行うことができる。
【0023】
核酸増幅の方法としては、ポリメラーゼを用いる方法が好ましく、その例としては、PCR、ICAN、LAMP等が挙げられる。ポリメラーゼを用いる方法により増幅する場合は、本発明プローブの存在下で増幅を行うことが好ましい。用いるプローブに応じて、増幅の反応条件等を調整することは当業者であれば容易である。これにより、核酸の増幅後にプローブのTmを解析するだけなので、反応終了後増幅産物を取り扱う必要がない。よって、増幅産物による汚染の心配がない。また、増幅に必要な機器と同じ機器で検出することが可能なので、容器を移動する必要すらない。よって、自動化も容易である。
【0024】
以下、PCRを用いる場合を例として、さらに説明する。PCRに用いるプライマー対は、本発明プローブがハイブリダイゼーションできる領域が増幅されるようにする他は、通常のPCRにおけるプライマー対の設定方法と同様にして設定することができる。プライマーの長さ及びTmは、通常には、10mer〜40merで40〜70℃、好ましくは15mer〜25merで55〜60℃である。プライマー対の各プライマーの長さは同一でなくてもよいが、両プライマーのTmはほぼ同一(通常には、相違が2℃以内)であることが好ましい。なお、Tm値は最近接塩基対(Nearest Neighbor)法により算出した値である。プライマー対の例としては、配列番号2及び3に示す塩基配列を有するプライマーからなるものが挙げられる。
【0025】
PCRは、本発明で使用される本発明プローブの存在下で行うことが好ましい。これにより、増幅反応終了後に増幅産物を取り扱う操作を行うことなくTm解析を行うことができる。用いるプローブに応じて、プライマーのTmやPCRの反応条件を調整することは当業者であれば容易である。
【0026】
代表的なPCR反応液の組成を挙げれば、以下の通りである。
【0027】
【表1】
DNA断片 101〜108分子/反応
プライマー 200〜1000M
プローブ 100〜1000nM
ヌクレオチド 各20〜200μM
DNAポリメラーゼ 0.01〜0.03単位/μl
Tris-HCl(pH 8.4〜9.0) 5〜20mM
MgCl2 1.5〜3mM
KCl 10〜100mM
グリセロール 0〜20%
(最終液量:10〜100μl)
【0028】
また、代表的な温度サイクルを挙げれば、以下の通りであり、この温度サイクルを通常25〜40回繰り返す。
(1) 変性、90〜98℃、1〜60秒
(2) アニーリング、60〜70℃、10〜60秒
(3) 伸長、60〜75℃、10〜180秒
【0029】
アニーリング及び伸長を一ステップで行う場合には、60〜70℃、10〜180秒の条件が挙げられる。
【0030】
Tm解析は、本発明プローブの蛍光色素の蛍光を測定する他は通常の方法に従って行うことができる。蛍光の測定は、蛍光色素に応じた波長の励起光を用い発光波長の光を測定することに行うことができる。Tm解析における昇温速度は、通常には、0.1〜1℃/秒である。Tm解析を行うときの反応液の組成は、プローブとその塩基配列に相補的な配列を有する核酸とのハイブリダイゼーションが可能であれば特に制限されないが、通常には、一価の陽イオン濃度が1.5〜5 mM、pHが7〜9である。PCR等のDNAポリメラーゼを用いる増幅方法の反応液は、通常、この条件を満たすので、増幅後の反応液をそのままTm解析に用いることができる。
【0031】
Tm解析の結果に基づくIAPP S20G変異の検出は通常の方法に従って行うことができる。本発明における検出とは、変異の有無の検出の他、変異型DNAの定量、野生型DNAと変異型DNAの割合の測定も包含する。
【0032】
<2>本発明キット
本発明キットは、本発明の検出方法に用いるためのキットである。このキットは、末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブ(消光プローブ)であって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列を有し、5’末端が蛍光色素で標識されている前記核酸プローブを含むことを特徴とする。
【0033】
消光プローブについては、本発明プローブに関し、上記に説明した通りである。
【0034】
本発明検出キットは、消光プローブの他に、本発明の検出方法における核酸増幅を行うのに必要とされる試薬類、特にDNAポリメラーゼを用いる増幅のためのプライマーをさらに含んでいてもよい。
【0035】
本発明検出キットにおいて消光プローブ、プライマー及びその他の試薬類は、別個に収容されていてもよいし、それらの一部が混合物とされていてもよい。
【0036】
【実施例】
以下に、本発明を実施例により具体的に説明する。
【0037】
【実施例1】
ヒトIAPP遺伝子のS20G変異を含む塩基配列(配列番号1)に基づき、S20G変異を含む部分を増幅できるように表2に示すプライマーを設計した。表2中、位置は、配列番号1に示す塩基配列における塩基番号を示す。
【0038】
【表2】
プライマー
名称 配列(5'→3') mer 位置 配列番号
F cacatgtgcaacgcagcg 18 192-209 2
R ctcttgccatatgtattggatccc 24 296-273 3
【0039】
次に、表3に示す、末端部にCを有するプローブを設計した。表3中、位置は、配列番号1に示す塩基配列における塩基番号を示す。また、塩基配列中の大文字は、IAPP S20G変異の部位を示し、3'末端の(P)は、リン酸化されていることを示す。BODIPY(商標) FL及びTAMRA(商標)による標識は、常法に従って行った。
【0040】
【表3】
プローブ
名称 配列(5'→3') mer 位置 配列番号
5FL-mt-5-14 (BODIPY FL)-cattccGgcaacaa-(P) 14 229-242 4
5FL-mt-5-15 (BODIPY FL)-cattccGgcaacaac-(P) 15 229-243 5
5FL-wt-5-22 (BODIPY FL)-cattccAgcaacaactttggtg-(P) 22 229-250 6
5FL-mt-5-22 (BODIPY FL)-cattccGgcaacaactttggtg-(P) 22 229-250 7
3FL-wt-4-25 caccaaagttgttgcTggaatgaac-(BODIPY FL) 25 250-226 8
3FL-mt-3-22 gaatggcaccaaagttgttgcC-(BODIPY FL) 22 256-235 9
5FL-wt-2-24 (BODIPY FL)-cTggaatgaactaaaaaatttgcc-(P) 24 236-213 10
5FL-mt-2-24 (BODIPY FL)-cCggaatgaactaaaaaatttgcc-(P) 24 236-213 11
5FL-mt-1-21 (BODIPY FL)-caaagttgttgcCggaatgaa-(P) 21 247-227 12
5T-mt-1-21 (6-TAMRA)-caaagttgttgcCggaatgaa-(P) 21 247-227 12
5FL-mt-1-18 (BODIPY FL)-caaagttgttgcCggaat-(P) 18 247-230 13
5T-mt-1-18 (6-TAMRA)-caaagttgttgcCggaat-(P) 18 247-230 13
5FL-wt-1-18 (BODIPY FL)-caaagttgttgcTggaat-(P) 18 247-230 14
【0041】
IAPP S20G周辺領域約600bp(配列番号1)を組み込んだプラスミドをサンプルとして、Smart Cycler System(Cephied)を用い、以下の条件でPCR及びTm解析を行った。Tm解析における励起波長及び検出波長は、それぞれ450〜495nm及び505〜537 nm(BODIPY FL)、527〜555 nm及び565〜605 nm(TAMRA)であった。
【0042】
【表4】
反応液組成
H2O 15.95μL
10×Gene Taqバッファー 2.5μL
40% グリセロール 3.125μL
各10mM dATP,dUTP,dGTP,dCTP 0.5μL
2U/μL ウラシル-N-グリコシラーゼ 0.05μL
5μM プローブ 1μL
100mM MgCl2 0.375μL
100μM プライマーF 0.25μL
100μM プライマーR 0.125μL
5U/μL Gene Taq 0.125μL
サンプル(0〜2000コピー) 1μL
合計 25μL
【0043】
【表5】
【0044】
各プローブを用いてPCR及びTm解析を行った結果、プローブ5FL-mt-1-18、5T-mt-1-18、5FL-mt-1-21および5T-mt-1-21を用いたときのみ、Tm解析で解析の可能な蛍光強度の変化が認められた。なお、各プローブのIAPP S20G変異を含む塩基配列に対する配置を図1及び2に示す。図中、Wild配列(配列番号15)及びmutant配列(配列番号16)は、配列番号1の塩基配列の塩基番号213〜262に相当する。また、図中、Fは蛍光色素を示す。図1及び2に示す配置からみて、プローブがTm解析で使用できるかどうかは、蛍光色素を結合させたCの位置に依存すると考えられ、プローブの長さは、多型部位を含む限り、あまり重要でないと考えられる。
【0045】
以下、プローブ5FL-mt-1-21を用いて、ゲノムDNAの絶対量に関する感度、再現性、及び、変異型の割合に関する検出感度を検討した。
【0046】
上記プラスミドの代わりに、ゲノムDNA(野生型)をそれぞれ、0、20、200及び2000コピー含むサンプルを用いて、上記の方法を繰り返した。結果を図3に示す。図3から明らかなように、20コピーであっても検出可能であることが示された。
【0047】
次に、野生型の塩基配列(配列番号1の塩基配列において塩基番号285がAである他は上記プラスミドと同じ)を有するプラスミドを調製した。野生型プラスミドとこの変異型プラスミドとを混合したサンプル(wt/mt)を10個調製し、野生型プラスミドのみのサンプル(wt/wt)及び変異型プラスミドのみのサンプル(mt/mt)とともに、上記の方法を繰り返した。結果を図4に示す。図4から明らかなように、本方法は再現性に優れることが示された。
【0048】
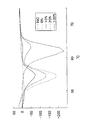
さらに、野生型プラスミドと変異型プラスミドとの比率を変えて、上記の方法を繰り返した。結果を図5に示す。比率に応じて、両ピークの高さが変化し、両ピークの高さの比に基づいて、比率を求めることが可能なことが示された。
【0049】
なお、図3〜5において縦軸は、蛍光強度の一次導関数の逆符号の値(-dF/dt)、横軸は温度(℃)である。
【0050】
【発明の効果】
本発明によれば、IAPP S20G変異を検出するのに有効な消光プローブが提供され、さらに、それを用いるIAPP S20G変異を検出する方法及びそのためのキットが提供される。Tm解析は数十秒で完了するため、検出に必要な時間も大幅に短略化出来る。プローブの存在下での核酸の増幅とTm解析を組み合わせる本発明の好ましい態様によれば、核酸の増幅後にプローブのTmを解析するだけなので、反応終了後増幅産物を取り扱う必要がない。よって、増幅産物による汚染の心配がない。また、増幅に必要な機器と同じ機器で検出することが可能なので、容器を移動する必要すらない。よって、自動化も容易である。
【0051】
【配列表】
【図面の簡単な説明】
【図1】 変異の識別不可能な消光プローブの位置を示す。
【図2】 変異の識別可能な消光プローブの位置を示す。
【図3】 実施例1の方法のゲノムDNAの絶対量に関する感度を示す。
【図4】 実施例1の方法の再現性を示す。
【図5】 実施例1の方法の変異型の割合に関する検出感度、定量性を示す。
Claims (9)
- 末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブであって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列からなり、5'末端が蛍光色素で標識されている前記核酸プローブ。
- 核酸プローブが、配列番号12または13からなる請求項1記載の核酸プローブ。
- 一塩基多型の部位を有する核酸について、蛍光色素で標識された核酸プローブを用いて、蛍光色素の蛍光を測定することにより融解曲線分析を行い、融解曲線分析の結果に基づいて変異を検出する方法であって、一塩基多型は、膵ラ氏島アミロイドタンパク質をコードする核酸における、膵ラ氏島アミロイドタンパク質のアミノ酸配列の20位のセリンがグリシンに置換する変異をもたらす塩基配列の変異であり、核酸プローブは、請求項1または2に記載の核酸プローブである前記方法。
- 試料に含まれる核酸における一塩基多型の部位を含む領域を増幅して一塩基多型を有する核酸を得ることを含む請求項3記載の方法。
- 増幅をDNAポリメラーゼを用いる方法により行う請求項4記載の方法。
- 増幅を核酸プローブの存在下で行う請求項5記載の方法。
- 末端が蛍光色素で標識され、ハイブリダイゼーションしたときに蛍光色素の蛍光が減少する核酸プローブであって、配列番号1に示す塩基配列において塩基番号247で終わる13〜30塩基長の配列に相補的な配列からなり、5'末端が蛍光色素で標識されている前記核酸プローブを含む、請求項3記載の方法のためのキット。
- 核酸プローブが、配列番号12または13からなる請求項7記載のキット。
- 膵ラ氏島アミロイドタンパク質をコードする核酸における、膵ラ氏島アミロイドタンパク質のアミノ酸配列の20位のセリンがグリシンに置換する変異をもたらす塩基配列の変異を含む領域を、DNAポリメラーゼを用いる方法で増幅するためのプライマーをさらに含む請求項7または8記載のキット。
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003114380A JP4454249B2 (ja) | 2003-04-18 | 2003-04-18 | 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット |
| PCT/JP2004/005509 WO2004092382A1 (ja) | 2003-04-18 | 2004-04-16 | 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット |
| AT04728056T ATE428782T1 (de) | 2003-04-18 | 2004-04-16 | Verfahren zum nachweis des gens einer mutante des pankreatischen insel-amyloidproteins sowie nukleinsäuresonde und kit dafür |
| US10/553,614 US7332306B2 (en) | 2003-04-18 | 2004-04-16 | Method of detecting pancreatic islet amyloid protein mutant gene and nucleic acid probe and kit therefor |
| EP04728056A EP1616952B1 (en) | 2003-04-18 | 2004-04-16 | Method of detecting pancryatic islet amyloid protein mutant gene and nucleic acid probe and kit therefor |
| DE602004020603T DE602004020603D1 (de) | 2003-04-18 | 2004-04-16 | Verfahren zum nachweis des gens einer mutante des pankreatischen insel-amyloidproteins sowie nukleinsäuresonde und kit dafür |
| CNB200480016499XA CN100404678C (zh) | 2003-04-18 | 2004-04-16 | 检测胰岛淀粉样蛋白突变基因的方法及其核酸探针和试剂盒 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003114380A JP4454249B2 (ja) | 2003-04-18 | 2003-04-18 | 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2004313119A JP2004313119A (ja) | 2004-11-11 |
| JP2004313119A5 JP2004313119A5 (ja) | 2006-04-27 |
| JP4454249B2 true JP4454249B2 (ja) | 2010-04-21 |
Family
ID=33296147
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003114380A Expired - Fee Related JP4454249B2 (ja) | 2003-04-18 | 2003-04-18 | 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US7332306B2 (ja) |
| EP (1) | EP1616952B1 (ja) |
| JP (1) | JP4454249B2 (ja) |
| CN (1) | CN100404678C (ja) |
| AT (1) | ATE428782T1 (ja) |
| DE (1) | DE602004020603D1 (ja) |
| WO (1) | WO2004092382A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101622363B (zh) * | 2007-07-13 | 2012-09-05 | 爱科来株式会社 | 用于检测jak2基因的突变的探针及其用途 |
| KR101536318B1 (ko) * | 2010-10-29 | 2015-07-13 | 아크레이 가부시키가이샤 | Egfr 유전자의 다형(多型) 검출용 프로브, 증폭용 프라이머 및 그 용도 |
| CN105717182B (zh) * | 2016-03-10 | 2018-05-11 | 中南大学 | 一种用于同步检测淀粉样多肽单体和聚集体的生物传感器及其构建方法和应用 |
| CN108489941B (zh) * | 2018-01-31 | 2021-07-27 | 吉林大学 | 溴酚蓝在作为检测牛胰岛素淀粉样纤维探针和作为牛胰岛素淀粉样纤维抑制剂方面的应用 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002008414A1 (fr) * | 2000-06-27 | 2002-01-31 | National Institute Of Advanced Industrial Science And Technology | Nouvelles sondes d'acides nucléiques et procédés d'essai d'acide nucléique par utilisation des mêmes |
| JP3963422B2 (ja) * | 2000-08-03 | 2007-08-22 | 日鉄環境エンジニアリング株式会社 | 核酸の測定方法 |
| ES2267803T3 (es) | 2000-08-11 | 2007-03-16 | University Of Utah Research Foundation | Sondas de oligonucleotidos marcados individuales. |
| CN1496412B (zh) * | 2001-03-14 | 2012-08-08 | 香港中文大学 | 用于评估中国血统的人种发展2型糖尿病危险性的方法和组合物 |
| CN1330775C (zh) * | 2002-05-08 | 2007-08-08 | 爱科来株式会社 | 靶核酸的检测方法 |
-
2003
- 2003-04-18 JP JP2003114380A patent/JP4454249B2/ja not_active Expired - Fee Related
-
2004
- 2004-04-16 CN CNB200480016499XA patent/CN100404678C/zh not_active Expired - Fee Related
- 2004-04-16 DE DE602004020603T patent/DE602004020603D1/de not_active Expired - Lifetime
- 2004-04-16 US US10/553,614 patent/US7332306B2/en not_active Expired - Fee Related
- 2004-04-16 AT AT04728056T patent/ATE428782T1/de not_active IP Right Cessation
- 2004-04-16 EP EP04728056A patent/EP1616952B1/en not_active Expired - Lifetime
- 2004-04-16 WO PCT/JP2004/005509 patent/WO2004092382A1/ja active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| CN100404678C (zh) | 2008-07-23 |
| EP1616952B1 (en) | 2009-04-15 |
| ATE428782T1 (de) | 2009-05-15 |
| EP1616952A1 (en) | 2006-01-18 |
| US20060275772A1 (en) | 2006-12-07 |
| CN1806046A (zh) | 2006-07-19 |
| JP2004313119A (ja) | 2004-11-11 |
| DE602004020603D1 (de) | 2009-05-28 |
| US7332306B2 (en) | 2008-02-19 |
| EP1616952A4 (en) | 2006-08-09 |
| WO2004092382A1 (ja) | 2004-10-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4454249B2 (ja) | 膵ラ氏島アミロイドタンパク質変異遺伝子の検出法ならびにそのための核酸プローブおよびキット | |
| JP4505838B2 (ja) | Nat2*6の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4336877B2 (ja) | β3アドレナリン受容体変異遺伝子の検出法ならびにそのための核酸プローブおよびキット | |
| JP4454366B2 (ja) | Mdr1遺伝子の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4437207B2 (ja) | Cyp2d6の変異の検出法ならびにそのための核酸プローブおよびキット | |
| EP1619258B1 (en) | Method of detecting or quantitatively determining mitochondrial dna 3243 variation, and kit therefor | |
| JP4505839B2 (ja) | Cyp2d6*4の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP5047448B2 (ja) | Cyp2c19の変異の検出法およびそのための核酸プローブ | |
| JP4437206B2 (ja) | Cyp2c9の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4276874B2 (ja) | ミトコンドリアdna3243変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4517175B2 (ja) | Nat2*7の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP5047450B2 (ja) | Cyp2c19*3アレルの検出法およびそのための核酸プローブ | |
| JP4517176B2 (ja) | Nat2*5の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4454365B2 (ja) | Cyp2d6*2の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP4454377B2 (ja) | チオプリンメチルトランスフェラーゼの変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP2004313073A (ja) | ミトコンドリアdna3243変異の検出法および定量法ならびにそのためのキット | |
| JP5860667B2 (ja) | Egfrエクソン21l858r遺伝子多型検出用プライマーセット及びその用途 | |
| JP2005192418A (ja) | 検出すべき特定配列の簡易検出方法 | |
| WO2014126398A1 (ko) | 아벨리노 각막 이상증 판별용 진단 키트 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060309 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090407 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090605 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091125 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100112 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100202 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130212 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130212 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130212 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140212 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |