JP2020176090A - ダサチニブ無水物を含有する固形製剤の製造方法 - Google Patents
ダサチニブ無水物を含有する固形製剤の製造方法 Download PDFInfo
- Publication number
- JP2020176090A JP2020176090A JP2019079741A JP2019079741A JP2020176090A JP 2020176090 A JP2020176090 A JP 2020176090A JP 2019079741 A JP2019079741 A JP 2019079741A JP 2019079741 A JP2019079741 A JP 2019079741A JP 2020176090 A JP2020176090 A JP 2020176090A
- Authority
- JP
- Japan
- Prior art keywords
- producing
- solid preparation
- preparation according
- dasatinib
- binder
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【課題】過酷条件下で保存した後であってもダサチニブ無水物の溶出性の遅延が抑制された製剤を提供すること。【解決手段】ダサチニブ無水物を含む粉末に対して、結合剤を有機溶媒を含む溶媒に溶解した造粒液を加えて湿式造粒する工程を介することを特徴とする、固形製剤の製造方法を提供する。ダサチニブ無水物は結晶形態であることが好ましく、また有機溶媒はアセトン、ジエチルエーテル、アルコール溶媒から選ばれることが好ましく、特にエタノールが好ましい。【選択図】図3
Description
本発明は原薬としてダサチニブ無水物を含有する固形製剤に関するものである。
ダサチニブは、慢性骨髄性白血病や再発又は難治性のフィラデルフィア染色体陽性急性リンパ性白血病の治療に用いられる化合物である。ダサチニブを含有する薬剤は、世界各国で広く発売されている。(非特許文献1等参考)。
ダサチニブは現在、錠剤の形状で医療現場に提供されている。ダサチニブを含有する固形製剤の処方や製造方法については、下記の特許文献1等の文献で紹介されてはいるが、参考となる公知の知見が乏しいのが現状である。
医薬品において薬物の溶出速度が一定なものになるようにすることは薬物の有効性を担保することの観点からみて重要である。そこで本発明者はダサチニブ無水物の溶出速度を安定に維持できる製剤を製造する方法を新たに開発することを目指した。
「スプリセル(登録商標)錠20mg、スプリセル(登録商標)錠50mg」医薬品インタビューフォーム 2018年1月改訂(第12版)
本発明は、過酷条件下で保存した後であってもダサチニブ無水物の溶出速度を安定に維持できる製剤を製造する有用な技術的手段を提供すること等を目的とするものである。
本発明者は、上記の課題を解決するために固形製剤の処方や製造方法を鋭意検討した結果、有機溶媒(エタノール)を用いて湿式造粒をする工程を介して得られた錠剤においてダサチニブ無水物の溶出性が安定に維持されていること等を見出した。本発明者は上記の知見に基づいて更に鋭意検討を重ねて、下記の発明を完成させるに至った。
本発明の好適な形態は以下(1)〜(9)において記述されるものである。
(1)ダサチニブ無水物を含む粉末に対して、結合剤を有機溶媒を含む溶媒に溶解した造粒液を加えて(滴下、噴霧等して)湿式造粒する工程を介することを特徴とする、固形製剤の製造方法。
(2)ダサチニブ無水物が結晶形態である、前記(1)に記載の固形製剤の製造方法。
(3)有機溶媒がアセトン、ジエチルエーテル、アルコール溶媒(メタノール、エタノール、ブタノール等)から選ばれる、前記(1)又は(2)に記載の固形製剤の製造方法。
(4)有機溶媒がエタノールである、前記(1)又は(2)に記載の固形製剤の製造方法。
(5)湿式造粒が流動層造粒であることを特徴とする、前記(1)〜(4)のいずれかに記載の固形製剤の製造方法。
(6)湿式造粒の際に用いる結合剤又はコーティング剤がヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、ポビドン、ポリビニルアルコール、アミノアルキルメタクリレートコポリマー、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー及びポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体から選ばれる、前記(1)〜(5)のいずれかに記載の固形製剤の製造方法。
(7)湿式造粒の際に用いる結合剤又はコーティング剤がアミノアルキルメタクリレートコポリマーEである、前記(1)〜(5)のいずれかに記載の固形製剤の製造方法。
(8)湿式造粒によって得られた顆粒を他の添加剤(滑沢剤等)と混合した後に打錠して素錠を製造する工程を含む、前記(1)〜(7)のいずれかに記載の固形製剤の製造方法。
(9)乳糖水和物及び結晶セルロースである賦形剤、クロスカルメロースナトリウムである崩壊剤及びステアリン酸マグネシウムである滑沢剤を用いる、前記(1)〜(8)のいずれかに記載の固形製剤の製造方法。
(1)ダサチニブ無水物を含む粉末に対して、結合剤を有機溶媒を含む溶媒に溶解した造粒液を加えて(滴下、噴霧等して)湿式造粒する工程を介することを特徴とする、固形製剤の製造方法。
(2)ダサチニブ無水物が結晶形態である、前記(1)に記載の固形製剤の製造方法。
(3)有機溶媒がアセトン、ジエチルエーテル、アルコール溶媒(メタノール、エタノール、ブタノール等)から選ばれる、前記(1)又は(2)に記載の固形製剤の製造方法。
(4)有機溶媒がエタノールである、前記(1)又は(2)に記載の固形製剤の製造方法。
(5)湿式造粒が流動層造粒であることを特徴とする、前記(1)〜(4)のいずれかに記載の固形製剤の製造方法。
(6)湿式造粒の際に用いる結合剤又はコーティング剤がヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、ポビドン、ポリビニルアルコール、アミノアルキルメタクリレートコポリマー、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー及びポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体から選ばれる、前記(1)〜(5)のいずれかに記載の固形製剤の製造方法。
(7)湿式造粒の際に用いる結合剤又はコーティング剤がアミノアルキルメタクリレートコポリマーEである、前記(1)〜(5)のいずれかに記載の固形製剤の製造方法。
(8)湿式造粒によって得られた顆粒を他の添加剤(滑沢剤等)と混合した後に打錠して素錠を製造する工程を含む、前記(1)〜(7)のいずれかに記載の固形製剤の製造方法。
(9)乳糖水和物及び結晶セルロースである賦形剤、クロスカルメロースナトリウムである崩壊剤及びステアリン酸マグネシウムである滑沢剤を用いる、前記(1)〜(8)のいずれかに記載の固形製剤の製造方法。
本発明は、過酷条件下で保存した後であってもダサチニブ無水物の溶出速度を安定に維持できる製剤等を製造することを可能とするものである。
以下で本発明の、ダサチニブ無水物を含有する固形製剤の処方及び製造方法、を詳細に説明する。但し以下の記載は本発明を説明するための例示であり、本発明をこの記載範囲にのみ特別限定する趣旨ではない。
<固形製剤の形態>
本発明に係る固形製剤の剤形として、顆粒並びに素錠(フィルムコーティング層や糖衣層等で覆われていない、打錠等により成形したままの錠剤を指す。以下同じ。)及びフィルムコーティング錠等の錠剤が挙げられるが、好ましくは素錠である。本発明に係る素錠はフィルムコーティング層を周囲に施してフィルムコーティング錠とすることが可能である。また本発明に係る顆粒は、素錠中に含有させることが可能である。本発明に係る錠剤の形状として、円形錠{円形平錠(隅角錠等含む)、円形R錠(隅角錠、2段R錠等含む)等}や異形錠等が挙げられる。
本発明に係る固形製剤の剤形として、顆粒並びに素錠(フィルムコーティング層や糖衣層等で覆われていない、打錠等により成形したままの錠剤を指す。以下同じ。)及びフィルムコーティング錠等の錠剤が挙げられるが、好ましくは素錠である。本発明に係る素錠はフィルムコーティング層を周囲に施してフィルムコーティング錠とすることが可能である。また本発明に係る顆粒は、素錠中に含有させることが可能である。本発明に係る錠剤の形状として、円形錠{円形平錠(隅角錠等含む)、円形R錠(隅角錠、2段R錠等含む)等}や異形錠等が挙げられる。
<原薬の物性>
本発明の固形製剤の製造に使用されるダサチニブは無水物であり、結晶形態のものが好ましい。ダサチニブ無水物のメディアン径(d50)は好ましくは10.0〜60.0μmである。ダサチニブ無水物は、必要に応じて適宜乾式又は湿式粉砕を行い、任意の粒子径に調整することも可能である。尚、上記粒子径はレーザー回析・散乱法によって測定(体積基準)することが可能である。ダサチニブは、素錠部分(望ましくは素錠に含有される顆粒内部)に含有され、素錠の全重量に対して好ましくは10.0〜50.0重量%、より好ましくは15.0〜30.0重量%の範囲で素錠中に含有される。ダサチニブは1錠中に20mg又は50mg含有されることが望ましい。
本発明の固形製剤の製造に使用されるダサチニブは無水物であり、結晶形態のものが好ましい。ダサチニブ無水物のメディアン径(d50)は好ましくは10.0〜60.0μmである。ダサチニブ無水物は、必要に応じて適宜乾式又は湿式粉砕を行い、任意の粒子径に調整することも可能である。尚、上記粒子径はレーザー回析・散乱法によって測定(体積基準)することが可能である。ダサチニブは、素錠部分(望ましくは素錠に含有される顆粒内部)に含有され、素錠の全重量に対して好ましくは10.0〜50.0重量%、より好ましくは15.0〜30.0重量%の範囲で素錠中に含有される。ダサチニブは1錠中に20mg又は50mg含有されることが望ましい。
<湿式造粒>
本発明の固形製剤の製造方法は、結晶形態のダサチニブ無水物を用いて湿式造粒する工程を含むことが望ましい。湿式造粒の方法として流動層造粒法や攪拌造粒法が挙げられ、特に好ましくは流動層造粒法である。攪拌造粒では、ダサチニブ無水物を含む粉末(攪拌中)に対して結合剤を含有する造粒液(水溶液等)を滴下することが行われる。流動層造粒では、結晶形態のダサチニブ無水物を含む粉末(流動化中)に対して結合剤を含有する造粒液(水溶液等)を噴霧することが行われる。
湿式造粒を行なう際の造粒液は、有機溶媒を含むものであり、結合剤を有機溶媒からなる溶液に加えたものであることが望ましい。有機溶媒として、例えばアセトン、ジエチルエーテル、アルコール溶媒(メタノール、エタノール、ブタノール等)等が挙げられ、好ましくはアセトン、アルコール溶媒であり、より好ましくはエタノールである。
本発明の固形製剤の製造方法は、結晶形態のダサチニブ無水物を用いて湿式造粒する工程を含むことが望ましい。湿式造粒の方法として流動層造粒法や攪拌造粒法が挙げられ、特に好ましくは流動層造粒法である。攪拌造粒では、ダサチニブ無水物を含む粉末(攪拌中)に対して結合剤を含有する造粒液(水溶液等)を滴下することが行われる。流動層造粒では、結晶形態のダサチニブ無水物を含む粉末(流動化中)に対して結合剤を含有する造粒液(水溶液等)を噴霧することが行われる。
湿式造粒を行なう際の造粒液は、有機溶媒を含むものであり、結合剤を有機溶媒からなる溶液に加えたものであることが望ましい。有機溶媒として、例えばアセトン、ジエチルエーテル、アルコール溶媒(メタノール、エタノール、ブタノール等)等が挙げられ、好ましくはアセトン、アルコール溶媒であり、より好ましくはエタノールである。
<素錠の製造に使用可能な医薬添加剤>
本発明の固形製剤に係る素錠の製造に用いられる、医薬的に許容可能な医薬添加剤としては、通常使用されている賦形剤、崩壊剤、結合剤、コーティング剤、可塑剤、滑沢剤、矯味剤、界面活性剤、着色剤等が使用できる。尚、本明細書において、各種添加剤(賦形剤、結合剤、崩壊剤、滑沢剤等)の語句の解釈は其々、製剤化において其の添加剤としての役割を発揮することが必須に期待されて使用されるもので結果的にも其の添加剤としての役割が発揮されたもの、と解することが好ましい。また当然であるが、本明細書における添加剤の語句の解釈において原薬が含まれることはない。
本発明の固形製剤に係る素錠の製造に用いられる、医薬的に許容可能な医薬添加剤としては、通常使用されている賦形剤、崩壊剤、結合剤、コーティング剤、可塑剤、滑沢剤、矯味剤、界面活性剤、着色剤等が使用できる。尚、本明細書において、各種添加剤(賦形剤、結合剤、崩壊剤、滑沢剤等)の語句の解釈は其々、製剤化において其の添加剤としての役割を発揮することが必須に期待されて使用されるもので結果的にも其の添加剤としての役割が発揮されたもの、と解することが好ましい。また当然であるが、本明細書における添加剤の語句の解釈において原薬が含まれることはない。
<賦形剤>
本発明に係る賦形剤として、例えば、乳糖(乳糖水和物、無水乳糖等)、マルトース、白糖、ショ糖、ブドウ糖、糖アルコール(D-マンニトール、エリスリトール、キシリトール、ソルビトール、イソマルト、マルチトール等)、デンプン(トウモロコシデンプン、バレイショデンプン、コメデンプン、コムギデンプン等)、結晶セルロース、ヒドロキシプロピルスターチ、アルファー化デンプン、部分アルファー化デンプン等が挙げられるが、好ましくは乳糖水和物又は結晶セルロースであり、より好ましくは乳糖水和物及び結晶セルロースである。賦形剤は素錠の全重量に対して好ましくは40.0〜90.0重量%、より好ましくは50.0〜75.0重量%の範囲で素錠中に含有される。
本発明に係る賦形剤として、例えば、乳糖(乳糖水和物、無水乳糖等)、マルトース、白糖、ショ糖、ブドウ糖、糖アルコール(D-マンニトール、エリスリトール、キシリトール、ソルビトール、イソマルト、マルチトール等)、デンプン(トウモロコシデンプン、バレイショデンプン、コメデンプン、コムギデンプン等)、結晶セルロース、ヒドロキシプロピルスターチ、アルファー化デンプン、部分アルファー化デンプン等が挙げられるが、好ましくは乳糖水和物又は結晶セルロースであり、より好ましくは乳糖水和物及び結晶セルロースである。賦形剤は素錠の全重量に対して好ましくは40.0〜90.0重量%、より好ましくは50.0〜75.0重量%の範囲で素錠中に含有される。
<崩壊剤>
本発明に係る崩壊剤は、例えば、カルメロース、カルメロースカルシウム、カルメロースカリウム、カルメロースナトリウム、クロスカルメロースナトリウム、カルボキシメチルスターチナトリウム、部分アルファー化デンプン、クロスポビドン及び低置換度ヒドロキシプロピルセルロース等から選ばれ、好ましくはクロスカルメロースナトリウムである。崩壊剤は素錠の全重量に対して好ましくは1.0〜20.0重量%、より好ましくは2.0〜10.0重量%の範囲で素錠中に含有される。
本発明に係る崩壊剤は、例えば、カルメロース、カルメロースカルシウム、カルメロースカリウム、カルメロースナトリウム、クロスカルメロースナトリウム、カルボキシメチルスターチナトリウム、部分アルファー化デンプン、クロスポビドン及び低置換度ヒドロキシプロピルセルロース等から選ばれ、好ましくはクロスカルメロースナトリウムである。崩壊剤は素錠の全重量に対して好ましくは1.0〜20.0重量%、より好ましくは2.0〜10.0重量%の範囲で素錠中に含有される。
<結合剤>
本発明に係る結合剤は、例えば、ヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、ポビドン、ポリビニルアルコール、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー、ポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体、アミノアルキルメタクリレートコポリマー(アミノアルキルメタクリレートコポリマーE、アミノアルキルメタクリレートコポリマーRSを含む。)等から選ばれ、好ましくはアミノアルキルメタクリレートコポリマー又はヒドロキシプロピルセルロースであり、最も好ましくはアミノアルキルメタクリレートコポリマーEである。尚、上記の結合剤は核粒子を被覆する目的でコーティング剤として使用することが可能である。結合剤及びコーティング剤は素錠の全重量に対して0.1〜20.0重量%、好ましくは2.0〜15.0重量%の範囲で素錠中に含有される。
本発明に係る結合剤は、例えば、ヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、ポビドン、ポリビニルアルコール、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー、ポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体、アミノアルキルメタクリレートコポリマー(アミノアルキルメタクリレートコポリマーE、アミノアルキルメタクリレートコポリマーRSを含む。)等から選ばれ、好ましくはアミノアルキルメタクリレートコポリマー又はヒドロキシプロピルセルロースであり、最も好ましくはアミノアルキルメタクリレートコポリマーEである。尚、上記の結合剤は核粒子を被覆する目的でコーティング剤として使用することが可能である。結合剤及びコーティング剤は素錠の全重量に対して0.1〜20.0重量%、好ましくは2.0〜15.0重量%の範囲で素錠中に含有される。
<流動化剤>
具体的な流動化剤としては、軽質無水ケイ酸、脂肪酸エステル、含水二酸化ケイ素、硬化油等を挙げる事ができ、好ましくは軽質無水ケイ酸である。流動化剤は、素錠の全重量に対して好ましくは0.1〜3.0重量%の範囲で素錠中に含有される。
具体的な流動化剤としては、軽質無水ケイ酸、脂肪酸エステル、含水二酸化ケイ素、硬化油等を挙げる事ができ、好ましくは軽質無水ケイ酸である。流動化剤は、素錠の全重量に対して好ましくは0.1〜3.0重量%の範囲で素錠中に含有される。
<滑沢剤>
本発明に係る滑沢剤は、例えば、ステアリン酸マグネシウム、ステアリン酸カルシウム、ステアリルフマル酸ナトリウム等から選ばれ、好ましくはステアリン酸マグネシウムである。滑沢剤は素錠の全重量に対して0.1〜3.0重量%の範囲で素錠中に含有されることが好ましい。
本発明に係る滑沢剤は、例えば、ステアリン酸マグネシウム、ステアリン酸カルシウム、ステアリルフマル酸ナトリウム等から選ばれ、好ましくはステアリン酸マグネシウムである。滑沢剤は素錠の全重量に対して0.1〜3.0重量%の範囲で素錠中に含有されることが好ましい。
<顆粒の構成及び製造方法>
本発明に係る顆粒は素錠の全重量に対して好ましくは15.0〜80.0重量%、より好ましくは25.0〜40.0重量%の範囲で素錠中に含有される。ダサチニブ無水物は造粒物100.0重量部に対して好ましくは50.0〜85.0重量部の範囲で前記造粒物中に含有される。結合剤及びコーティング剤は造粒物100.0重量部に対して好ましくは15.0〜50.0重量部の範囲で前記造粒物中に含有される。本発明に係る顆粒は、ダサチニブ無水物又は其れを含む顆粒に対して結合剤又はコーティング剤を含む造粒液を噴霧して流動層造粒法によって製造することが望ましい。
本発明に係る顆粒は素錠の全重量に対して好ましくは15.0〜80.0重量%、より好ましくは25.0〜40.0重量%の範囲で素錠中に含有される。ダサチニブ無水物は造粒物100.0重量部に対して好ましくは50.0〜85.0重量部の範囲で前記造粒物中に含有される。結合剤及びコーティング剤は造粒物100.0重量部に対して好ましくは15.0〜50.0重量部の範囲で前記造粒物中に含有される。本発明に係る顆粒は、ダサチニブ無水物又は其れを含む顆粒に対して結合剤又はコーティング剤を含む造粒液を噴霧して流動層造粒法によって製造することが望ましい。
<素錠の製造方法>
本発明に係る素錠は、一般的な製造方法によって作成することが可能であり、例えば以下の製造方法によって作成することが可能である。
まず、ダサチニブ、賦形剤及び崩壊剤等の粉末を流動層造粒機に投入して流動化させ、これに結合剤を溶解した溶液(造粒液)を噴霧することで造粒物を製造する。当該造粒物は乾燥及び整粒された後、滑沢剤等と混合した後に打錠機によって圧縮成形して錠剤(素錠)とする。錠剤を圧縮成形する際の打圧は400〜1500kgfであることが好ましい。
本発明に係る素錠は、一般的な製造方法によって作成することが可能であり、例えば以下の製造方法によって作成することが可能である。
まず、ダサチニブ、賦形剤及び崩壊剤等の粉末を流動層造粒機に投入して流動化させ、これに結合剤を溶解した溶液(造粒液)を噴霧することで造粒物を製造する。当該造粒物は乾燥及び整粒された後、滑沢剤等と混合した後に打錠機によって圧縮成形して錠剤(素錠)とする。錠剤を圧縮成形する際の打圧は400〜1500kgfであることが好ましい。
以下に実施例等により本発明を説明するが、本発明はこれらの実施例等に限定されるものではない。以下の実施例1並びに比較例1に記載の固形製剤の製造において用いられるダサチニブ無水物(N−6型)は事前に結晶形態であること並びに粒子径分布がd10=2.8、d50=24.0、d90=90.5であることが確認された。
ダサチニブ無水物600.0gを噴流流動層造粒機(MP−01/パウレック社製)に投入して流動化させ、アミノアルキルメタクリレートコポリマーE(オイドラギットEPO/エボニックジャパン社製)240.0gをエタノール960gに溶解した液を噴霧・乾燥して造粒物を得た。それを30メッシュの篩にて篩過して整粒された顆粒を得た。
得られた顆粒、乳糖水和物、結晶セルロース、クロスカルメロースナトリウム及びステアリン酸マグネシウムを混合して混合物を得た。そして当該混合末を打圧600kgfで打錠して1錠質量80.0mg、直径6.0mmの円形錠(素錠、ダサチニブ20mg含有)を得た。
尚、原薬並びに各添加剤は、当該錠剤が下記表1に示す処方(数値単位はmg)となるような量で上記製造に用いた。
得られた顆粒、乳糖水和物、結晶セルロース、クロスカルメロースナトリウム及びステアリン酸マグネシウムを混合して混合物を得た。そして当該混合末を打圧600kgfで打錠して1錠質量80.0mg、直径6.0mmの円形錠(素錠、ダサチニブ20mg含有)を得た。
尚、原薬並びに各添加剤は、当該錠剤が下記表1に示す処方(数値単位はmg)となるような量で上記製造に用いた。
[比較例1]
ダサチニブ無水物525.0gを噴流流動層造粒機(MP−01/パウレック社製)に投入して流動化させ、アミノアルキルメタクリレートコポリマーE(オイドラギットEPO/エボニックジャパン社製)210.0g、ラウリル硫酸ナトリウム(NIKKOL SLS/日光ケミカルズ社製)21.0g、ステアリン酸(Parteck LUB STA50/メルク社製)31.5gを精製水1210gに溶解した液を噴霧・乾燥して造粒物を得た。それを30メッシュの篩にて篩過して整粒された顆粒を得た。
得られた顆粒、乳糖水和物、結晶セルロース、クロスカルメロースナトリウム及びステアリン酸マグネシウムを混合して混合物を得た。そして当該混合末を、まず打圧600kgfで打錠して1錠質量80.0mg、直径6.0mmの円形錠(素錠、ダサチニブ20mg含有)を得た。
尚、原薬並びに各添加剤は、当該錠剤が下記表1に示す処方(数値単位はmg)となるような量で上記製造に用いた。
ダサチニブ無水物525.0gを噴流流動層造粒機(MP−01/パウレック社製)に投入して流動化させ、アミノアルキルメタクリレートコポリマーE(オイドラギットEPO/エボニックジャパン社製)210.0g、ラウリル硫酸ナトリウム(NIKKOL SLS/日光ケミカルズ社製)21.0g、ステアリン酸(Parteck LUB STA50/メルク社製)31.5gを精製水1210gに溶解した液を噴霧・乾燥して造粒物を得た。それを30メッシュの篩にて篩過して整粒された顆粒を得た。
得られた顆粒、乳糖水和物、結晶セルロース、クロスカルメロースナトリウム及びステアリン酸マグネシウムを混合して混合物を得た。そして当該混合末を、まず打圧600kgfで打錠して1錠質量80.0mg、直径6.0mmの円形錠(素錠、ダサチニブ20mg含有)を得た。
尚、原薬並びに各添加剤は、当該錠剤が下記表1に示す処方(数値単位はmg)となるような量で上記製造に用いた。
[試験例1]
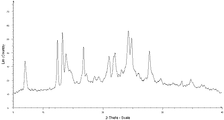
実施例1及び比較例1の其々で得られた錠剤について、製造直後及び温度60℃密閉条件下若しくは温度50℃相対湿度75%開放条件下のいずれかで2週間保存後に粉末X線回折測定法によって解析した。其の解析結果は図3に示される。
実施例1及び比較例1の其々で得られた錠剤について、製造直後及び温度60℃密閉条件下若しくは温度50℃相対湿度75%開放条件下のいずれかで2週間保存後に粉末X線回折測定法によって解析した。其の解析結果は図3に示される。
図3の結果から、実施例1及び比較例1の各錠剤からダサチニブ無水物の結晶形態に特徴的なピークがいくつか有意に確認されたため、保存前後に亘って結晶形態が安定に維持されていることが示唆される。
[試験例2]
実施例1及び比較例1で製造した各錠剤について、製造直後及び温度60℃密閉条件下若しくは温度50℃相対湿度75%開放条件下のいずれかで2週間保存後にダサチニブ無水物の溶出率(%)を測定した。溶出率の測定は、第17改正日本薬局方・一般試験法の溶出試験法(パドル法)に従って行ない、37℃の薄めたMcIlvaine緩衝液(pH4.0)900mL中に錠剤1錠を投入し、パドルを50rpm回転速度で回転させ、試験開始5、10、15及び30分後に測定した。尚、溶出したダサチニブ無水物の量はUV吸収法で測定した。其の溶出率の測定結果は下記の表2に示される。
実施例1及び比較例1で製造した各錠剤について、製造直後及び温度60℃密閉条件下若しくは温度50℃相対湿度75%開放条件下のいずれかで2週間保存後にダサチニブ無水物の溶出率(%)を測定した。溶出率の測定は、第17改正日本薬局方・一般試験法の溶出試験法(パドル法)に従って行ない、37℃の薄めたMcIlvaine緩衝液(pH4.0)900mL中に錠剤1錠を投入し、パドルを50rpm回転速度で回転させ、試験開始5、10、15及び30分後に測定した。尚、溶出したダサチニブ無水物の量はUV吸収法で測定した。其の溶出率の測定結果は下記の表2に示される。
表2の結果より、いずれの錠剤も製造直後はダサチニブ無水物が速やかに溶出するが、温度60℃密閉条件下で2週間又は温度50℃相対湿度75%開放条件下で2週間保存すると、実施例1の錠剤は溶出速度が大きく変化しないが、比較例1の錠剤は溶出速度が大きく遅延していた。よって本発明の錠剤はダサチニブ無水物の溶出速度の安定性(遅延防止等)に優れた錠剤であることが明らかになった。
本発明は、過酷条件下で保存した後であってもダサチニブ無水物の溶出性の遅延が抑制された製剤を工業的に製造し、医療現場に提供することに寄与するものである。
Claims (9)
- ダサチニブ無水物を含む粉末に対して、結合剤を有機溶媒を含む溶媒に溶解した造粒液を加えて湿式造粒する工程を介することを特徴とする、固形製剤の製造方法。
- ダサチニブ無水物が結晶形態である、請求項1に記載の固形製剤の製造方法。
- 有機溶媒がアセトン、ジエチルエーテル、アルコール溶媒から選ばれる、請求項1又は2に記載の固形製剤の製造方法。
- 有機溶媒がエタノールである、請求項1又は2に記載の固形製剤の製造方法。
- 湿式造粒が流動層造粒であることを特徴とする、請求項1〜4のいずれかに記載の固形製剤の製造方法。
- 湿式造粒の際に用いる結合剤又はコーティング剤がヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、ポビドン、ポリビニルアルコール、アミノアルキルメタクリレートコポリマー、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー及びポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体から選ばれる、請求項1〜5のいずれかに記載の固形製剤の製造方法。
- 湿式造粒の際に用いる結合剤又はコーティング剤がアミノアルキルメタクリレートコポリマーEである、請求項1〜5のいずれかに記載の固形製剤の製造方法。
- 湿式造粒によって得られた顆粒を他の添加剤(滑沢剤等)と混合した後に打錠して素錠を製造する工程を含む、請求項1〜7のいずれかに記載の固形製剤の製造方法。
- 乳糖水和物及び結晶セルロースである賦形剤、クロスカルメロースナトリウムである崩壊剤及びステアリン酸マグネシウムである滑沢剤を用いる、請求項1〜8のいずれかに記載の固形製剤の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019079741A JP2020176090A (ja) | 2019-04-19 | 2019-04-19 | ダサチニブ無水物を含有する固形製剤の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019079741A JP2020176090A (ja) | 2019-04-19 | 2019-04-19 | ダサチニブ無水物を含有する固形製剤の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2020176090A true JP2020176090A (ja) | 2020-10-29 |
Family
ID=72937667
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019079741A Pending JP2020176090A (ja) | 2019-04-19 | 2019-04-19 | ダサチニブ無水物を含有する固形製剤の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2020176090A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021050141A (ja) * | 2019-09-20 | 2021-04-01 | 日本化薬株式会社 | ダサチニブを有効成分とする医薬錠剤 |
-
2019
- 2019-04-19 JP JP2019079741A patent/JP2020176090A/ja active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021050141A (ja) * | 2019-09-20 | 2021-04-01 | 日本化薬株式会社 | ダサチニブを有効成分とする医薬錠剤 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11413295B2 (en) | Oral preparation of obeticholic acid | |
| JP6895779B2 (ja) | アジルサルタン含有固形医薬組成物 | |
| JP2019108324A (ja) | リバーロキサバン含有医薬組成物 | |
| JP2019535696A (ja) | ピリドン誘導体の医薬組成物およびその製造方法 | |
| JP2019147798A (ja) | ダサチニブ無水物の結晶形態が安定に維持された固形製剤の製造方法 | |
| JP2020176090A (ja) | ダサチニブ無水物を含有する固形製剤の製造方法 | |
| JP2015054851A (ja) | 被覆経口固形製剤 | |
| KR20180002977A (ko) | 방출특성 및 생체이용률이 개선된 소라페닙 토실레이트를 포함하는 경구투여용 약제학적 조성물 | |
| JP2007063217A (ja) | プランルカスト水和物含有錠及びその製造方法 | |
| JP2023036924A (ja) | レナリドミドを含む医薬組成物 | |
| WO2019116386A1 (en) | Oral pharmaceutical compositions of amorphous apremilast and process for preparing thereof | |
| WO2022153330A1 (en) | Pharmaceutical compositions comprising acalabrutinib | |
| JP6538321B2 (ja) | 経口組成物 | |
| JP7233852B2 (ja) | 変色が抑制された固形製剤 | |
| JP2019089758A (ja) | セレコキシブ含有錠剤における溶出性の改善方法 | |
| JP6199922B2 (ja) | 化学的な安定性が向上したイルベサルタン含有錠剤 | |
| JP2021024820A (ja) | 光安定性が向上した、ダサチニブ無水物フィルムコーティング錠剤 | |
| JP7547723B2 (ja) | アビラテロン酢酸エステル含有製剤 | |
| EP3761965A1 (en) | Ticagrelor-containing tablet formulation | |
| JP5204452B2 (ja) | ビカルタミド含有製剤 | |
| JP2017132724A (ja) | アムロジピン含有被覆造粒物を含む配合口腔内崩壊錠 | |
| JP6233911B2 (ja) | 化学的な安定性が向上したイルベサルタン含有錠剤 | |
| JP7407364B2 (ja) | ラメルテオン含有固形製剤 | |
| WO2022210829A1 (ja) | アビラテロン酢酸エステル含有錠剤 | |
| JP6858873B2 (ja) | セレコキシブを含む錠剤 |