JP2020009776A - 負極活物質、負極電極、リチウムイオン二次電池 - Google Patents
負極活物質、負極電極、リチウムイオン二次電池 Download PDFInfo
- Publication number
- JP2020009776A JP2020009776A JP2019167717A JP2019167717A JP2020009776A JP 2020009776 A JP2020009776 A JP 2020009776A JP 2019167717 A JP2019167717 A JP 2019167717A JP 2019167717 A JP2019167717 A JP 2019167717A JP 2020009776 A JP2020009776 A JP 2020009776A
- Authority
- JP
- Japan
- Prior art keywords
- negative electrode
- active material
- electrode active
- secondary battery
- ppm
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Cell Electrode Carriers And Collectors (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
【課題】二次電池の負極活物質として用いた際に、電池容量を増加させ、サイクル特性を向上させることが可能な負極活物質を提供する。【解決手段】負極活物質粒子を含む負極活物質であって、前記負極活物質粒子は、SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含有し、前記負極活物質粒子を含む負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行った状態において、前記充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有することを特徴とする負極活物質。【選択図】図1
Description
本発明は、負極活物質、負極電極、リチウムイオン二次電池、負極活物質の製造方法及びリチウムイオン二次電池の製造方法に関する。
近年、モバイル端末などに代表される小型の電子機器が広く普及しており、さらなる小型化、軽量化及び長寿命化が強く求められている。このような市場要求に対し、特に小型かつ軽量で高エネルギー密度を得ることが可能な二次電池の開発が進められている。この二次電池は、小型の電子機器に限らず、自動車などに代表される大型の電子機器、家屋などに代表される電力貯蔵システムへの適用も検討されている。
その中でも、リチウムイオン二次電池は小型かつ高容量化が行いやすく、また、鉛電池、ニッケルカドミウム電池よりも高いエネルギー密度が得られるため、大いに期待されている。
上記のリチウムイオン二次電池は、正極及び負極、セパレータと共に電解液を備えており、負極は充放電反応に関わる負極活物質を含んでいる。
この負極活物質としては、炭素系活物質が広く使用されている一方で、最近の市場要求から電池容量のさらなる向上が求められている。電池容量向上のために、負極活物質材としてケイ素を用いることが検討されている。なぜならば、ケイ素の理論容量(4199mAh/g)は黒鉛の理論容量(372mAh/g)よりも10倍以上大きいため、電池容量の大幅な向上を期待できるからである。負極活物質材としてのケイ素材の開発はケイ素単体だけではなく、合金、酸化物に代表される化合物などについても検討されている。また、活物質形状は、炭素系活物質では標準的な塗布型から、集電体に直接堆積する一体型まで検討されている。
しかしながら、負極活物質としてケイ素を主原料として用いると、充放電時に負極活物質が膨張収縮するため、主に負極活物質表層近傍で割れやすくなる。また、活物質内部にイオン性物質が生成し、負極活物質が割れやすい物質となる。負極活物質表層が割れると、それによって新表面が生じ、活物質の反応面積が増加する。この時、新表面において電解液の分解反応が生じるとともに、新表面に電解液の分解物である被膜が形成されるため電解液が消費される。このためサイクル特性が低下しやすくなる。
これまでに、電池初期効率やサイクル特性を向上させるために、ケイ素材を主材としたリチウムイオン二次電池用負極材料、電極構成についてさまざまな検討がなされている。
具体的には、良好なサイクル特性や高い安全性を得る目的で、気相法を用いケイ素及びアモルファス二酸化ケイ素を同時に堆積させている(例えば特許文献1参照)。また、高い電池容量や安全性を得るために、ケイ素酸化物粒子の表層に炭素材(電子伝導材)を設けている(例えば特許文献2参照)。さらに、サイクル特性を改善するとともに高入出力特性を得るために、ケイ素及び酸素を含有する活物質を作製し、かつ、集電体近傍での酸素比率が高い活物質層を形成している(例えば特許文献3参照)。また、サイクル特性を向上させるために、ケイ素活物質中に酸素を含有させ、平均酸素含有量が40at%以下であり、かつ集電体に近い場所で酸素含有量が多くなるように形成している(例えば特許文献4参照)。
また、初回充放電効率を改善するためにSi相、SiO2、MyO金属酸化物を含有するナノ複合体を用いている(例えば特許文献5参照)。また、サイクル特性改善のため、SiOx(0.8≦x≦1.5、粒径範囲=1μm〜50μm)と炭素材を混合して高温焼成している(例えば特許文献6参照)。また、サイクル特性改善のために、負極活物質中におけるケイ素に対する酸素のモル比を0.1〜1.2とし、活物質、集電体界面近傍におけるモル比の最大値、最小値との差が0.4以下となる範囲で活物質の制御を行っている(例えば特許文献7参照)。また、電池負荷特性を向上させるため、リチウムを含有した金属酸化物を用いている(例えば特許文献8参照)。また、サイクル特性を改善させるために、ケイ素材表層にシラン化合物などの疎水層を形成している(例えば特許文献9参照)。また、サイクル特性改善のため、酸化ケイ素を用い、その表層に黒鉛被膜を形成することで導電性を付与している(例えば特許文献10参照)。特許文献10において、黒鉛被膜に関するRAMANスペクトルから得られるシフト値に関して、1330cm−1及び1580cm−1にブロードなピークが現れるとともに、それらの強度比I1330/I1580が1.5<I1330/I1580<3となっている。また、高い電池容量、サイクル特性の改善のため、二酸化ケイ素中に分散されたケイ素微結晶相を有する粒子を用いている(例えば特許文献11参照)。また、過充電、過放電特性を向上させるために、ケイ素と酸素の原子数比を1:y(0<y<2)に制御したケイ素酸化物を用いている(例えば特許文献12参照)。
上述したように、近年、電子機器に代表される小型のモバイル機器は高性能化、多機能化がすすめられており、その主電源であるリチウムイオン二次電池は電池容量の増加が求められている。この問題を解決する1つの手法として、ケイ素材を主材として用いた負極からなるリチウムイオン二次電池の開発が望まれている。また、ケイ素材を用いたリチウムイオン二次電池は、炭素系活物質を用いたリチウムイオン二次電池と同等に近いサイクル特性が望まれている。しかしながら、炭素系活物質を用いたリチウムイオン二次電池と同等のサイクル安定性を示す負極活物質を提案するには至っていなかった。
本発明は、上記問題点に鑑みてなされたものであって、二次電池の負極活物質として用いた際に、電池容量を増加させ、サイクル特性を向上させることが可能な負極活物質、この負極活物質を含む負極活物質層を有する負極電極、及び、この負極電極を用いたリチウムイオン二次電池を提供することを目的とする。また、電池容量を増加させ、サイクル特性を向上させることが可能な負極活物質の製造方法を提供することを目的とする。また、そのような負極活物質を用いるリチウムイオン二次電池の製造方法を提供することを目的とする。
上記目的を達成するために、本発明は、負極活物質粒子を含む負極活物質であって、前記負極活物質粒子は、SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含有し、
前記負極活物質粒子を含む負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行った状態において、前記充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有することを特徴とする負極活物質を提供する。
前記負極活物質粒子を含む負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行った状態において、前記充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有することを特徴とする負極活物質を提供する。
このように、負極活物質が、ケイ素化合物(SiOx:0.5≦x≦1.6、以下、ケイ素酸化物とも称する)を含有する負極活物質粒子を含むものであり、かつ、上記の充電終止後において上記の2種類のピークを有するものであれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、高い電池容量を有するとともに、良好なサイクル特性が得られる。
また、前記25〜55ppmの範囲のピークは、前記Xが49回以内で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、当該二次電池が安定化するまでの時間(サイクル数)をより少なくすることができる。
また、前記0〜3ppmの範囲のピークは、前記Xが9回以内で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、負極活物質粒子の内部に安定したLi化合物が生成するまでの時間(サイクル数)をより少なくすることができる。
また、前記25〜55ppmの範囲のピーク及び前記0〜3ppmの範囲のピークは、前記Xが0回で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、当該二次電池が安定化するまでの時間及び負極活物質粒子の内部に安定したLi化合物が生成するまでの時間をさらに少なくすることができる。
また、前記25〜55ppmの範囲のピークは、前記0V定電流定電圧充電及び1.2V定電流放電のサイクルを49回以内繰り返す中で減少することが好ましい。
このような負極活物質であれば、Li挿入、脱離を繰り返すことによりケイ素酸化物のバルク状況がより安定化する。
また、前記負極活物質は、X線回折により得られるSi(111)結晶面に起因する回折ピークの半値幅(2θ)が1.2°以上であるとともに、その結晶面に対応する結晶子サイズは7.5nm以下であることが好ましい。
負極活物質が上記のSi結晶子の結晶性を有するケイ素酸化物を含有することで、このような負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、より良好なサイクル特性及び初期充放電特性が得られる。
また、前記負極活物質粒子のメジアン径は0.5μm以上20μm以下であることが好ましい。
負極活物質粒子のメジアン径が上記の範囲内にあることで、このような負極活物質粒子を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、より良好なサイクル特性及び初期充放電特性が得られる。
また、前記負極活物質粒子は、表層部に炭素材を含むことが好ましい。
このように、負極活物質粒子がその表層部に炭素材を含むことで、導電性の向上が得られるため、このような負極活物質粒子を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、電池特性を向上させることができる。
また、前記炭素材の平均厚さは1nm以上5000nm以下であることが好ましい。
被覆する炭素材の平均厚さが1nm以上であれば導電性向上が得られ、被覆する炭素材の平均厚さが5000nm以下であれば、このような負極活物質粒子を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、電池容量の低下を抑制することができる。
さらに本発明では、本発明の負極活物質を含むことを特徴とする負極電極を提供する。
このような負極電極であれば、この負極電極をリチウムイオン二次電池の負極電極として用いた際に、高い電池容量を有するとともに、良好なサイクル特性が得られる。
また、前記負極電極は、前記負極活物質を含む負極活物質層と、
負極集電体とを有し、
前記負極活物質層は前記負極集電体上に形成されており、
前記負極集電体は炭素及び硫黄を含むとともに、それらの含有量がいずれも100質量ppm以下であることが好ましい。
負極集電体とを有し、
前記負極活物質層は前記負極集電体上に形成されており、
前記負極集電体は炭素及び硫黄を含むとともに、それらの含有量がいずれも100質量ppm以下であることが好ましい。
このように、負極電極を構成する負極集電体が、炭素及び硫黄を上記のような含有量含むことで、充電時の負極電極の変形を抑制することができる。
さらに本発明では、負極電極として、上記本発明の負極電極を用いたものであることを特徴とするリチウムイオン二次電池を提供する。
このような負極電極を用いたリチウムイオン二次電池であれば、高容量であるとともに良好なサイクル特性が得られる。
さらに本発明では、負極活物質粒子を含む負極活物質の製造方法であって、
一般式SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含む負極活物質粒子を準備する工程と、
前記負極活物質粒子を含む負極活物質を含む負極と、金属リチウムからなる対極とを有する二次電池を作製する工程と、
前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行う工程と、
前記充電終止の状態において、前記負極活物質を7Li−MAS−NMRで測定する工程と、
前記7Li−MAS−NMRのスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有する負極活物質を選別する工程と
を有することを特徴とする負極活物質の製造方法を提供する。
一般式SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含む負極活物質粒子を準備する工程と、
前記負極活物質粒子を含む負極活物質を含む負極と、金属リチウムからなる対極とを有する二次電池を作製する工程と、
前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行う工程と、
前記充電終止の状態において、前記負極活物質を7Li−MAS−NMRで測定する工程と、
前記7Li−MAS−NMRのスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有する負極活物質を選別する工程と
を有することを特徴とする負極活物質の製造方法を提供する。
負極活物質をこのように選別して、負極活物質を製造することで、リチウムイオン二次電池の負極活物質として使用した際に、高容量であるとともに良好なサイクル特性を有する負極活物質を製造することができる。
さらに本発明では、上記本発明の負極活物質の製造方法によって製造した負極活物質を用いて負極を作製し、該作製した負極を用いてリチウムイオン二次電池を製造することを特徴とするリチウムイオン二次電池の製造方法を提供する。
この製造方法は、上記のように選別された負極活物質を用いることにより、高容量であるとともに良好なサイクル特性を有するリチウムイオン二次電池を製造することができる。
以上のように、本発明の負極活物質は、リチウムイオン二次電池の負極活物質として用いた際に、高容量で良好なサイクル特性が得られる。また、本発明の負極活物質の製造方法であれば、良好なサイクル特性を有するリチウムイオン二次電池用負極活物質を製造することができる。
以下、本発明について実施の形態を説明するが、本発明はこれに限定されるものではない。
前述のように、リチウムイオン二次電池の電池容量を増加させる1つの手法として、ケイ素材を主材として用いた負極をリチウムイオン二次電池の負極として用いることが検討されている。このケイ素材を用いたリチウムイオン二次電池は、炭素系活物質を用いたリチウムイオン二次電池と同等に近いサイクル特性が望まれているが、炭素系活物質を用いたリチウムイオン二次電池と同等のサイクル特性を示す負極活物質を提案するには至っていなかった。
そこで、本発明者らは、リチウムイオン二次電池の負極として用いた際に、良好なサイクル特性が得られる負極活物質について鋭意検討を重ねた。その結果、負極活物質粒子を含む負極活物質であって、この負極活物質粒子は、SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含有し、この負極活物質粒子を含む負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、この二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらにこの二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行った状態において、充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有することを特徴とする負極活物質を用いた際に、高い電池容量及び良好なサイクル特性が得られることを見出し、本発明をなすに至った。
<負極電極>
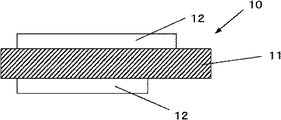
まず、負極電極(非水電解質二次電池用負極)について、説明する。図2は本発明の負極電極(以下、負極とも称する)の構成の一例を示す断面図である。
まず、負極電極(非水電解質二次電池用負極)について、説明する。図2は本発明の負極電極(以下、負極とも称する)の構成の一例を示す断面図である。
[負極の構成]
図2に示すように、負極10は、負極集電体11の上に負極活物質層12を有する構成になっている。また、負極活物質層12は負極集電体11の両面、又は、片面だけに設けられていても良い。さらに、本発明の負極活物質が用いられたものであれば、負極集電体11はなくてもよい。
図2に示すように、負極10は、負極集電体11の上に負極活物質層12を有する構成になっている。また、負極活物質層12は負極集電体11の両面、又は、片面だけに設けられていても良い。さらに、本発明の負極活物質が用いられたものであれば、負極集電体11はなくてもよい。
[負極集電体]
負極集電体11は、優れた導電性材料であり、かつ、機械的な強度に長けた物で構成される。負極集電体11に用いることができる導電性材料として、例えば銅(Cu)やニッケル(Ni)が挙げられる。また、この導電性材料は、リチウム(Li)と金属間化合物を形成しない材料であることが好ましい。
負極集電体11は、優れた導電性材料であり、かつ、機械的な強度に長けた物で構成される。負極集電体11に用いることができる導電性材料として、例えば銅(Cu)やニッケル(Ni)が挙げられる。また、この導電性材料は、リチウム(Li)と金属間化合物を形成しない材料であることが好ましい。
負極集電体11は、主元素以外に炭素(C)や硫黄(S)を含んでいることが好ましい。なぜならば、負極集電体11の物理的強度が向上するためである。特に、充電時に膨張する活物質層を負極が有する場合、集電体が上記の元素を含んでいれば、集電体を含む電極変形を抑制する効果がある。上記の含有元素のそれぞれの含有量は特に限定されないが、中でも100質量ppm以下であることが好ましい。なぜならば、より高い変形抑制効果が得られるためである。このような変形抑制効果によりサイクル特性をより向上できる。
また、負極集電体11の表面は粗化されていてもよいし、粗化されていなくてもよい。粗化されている負極集電体は、例えば、電解処理、エンボス処理、又は、化学エッチング処理された金属箔などである。粗化されていない負極集電体は、例えば、圧延金属箔などである。
[負極活物質層]
負極活物質層12は、リチウムイオンを吸蔵、放出可能な本発明の負極活物質を含んでおり、電池設計上の観点から、さらに、負極結着剤(バインダ)や導電助剤など他の材料を含んでいてもよい。
負極活物質層12は、リチウムイオンを吸蔵、放出可能な本発明の負極活物質を含んでおり、電池設計上の観点から、さらに、負極結着剤(バインダ)や導電助剤など他の材料を含んでいてもよい。
本発明の負極活物質は負極活物質粒子を含む。負極活物質粒子は、リチウムイオンを吸蔵、放出可能なコア部を有する。負極活物質粒子が、表層部に炭素材を含むものである場合は、さらに、導電性が得られる炭素被覆部を有する。
負極活物質粒子は、ケイ素化合物(SiOx:0.5≦x≦1.6)を含有するものであり、ケイ素化合物の組成としてはxが1に近い方が好ましい。なぜならば、安定した電池特性が得られるからである。なお、本発明におけるケイ素化合物の組成は必ずしも純度100%を意味しているわけではなく、微量の不純物元素を含んでいてもよい。
本発明の負極活物質は、該負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクル(以下、0V−1.2Vサイクルとも称する)をX回(X≧0)繰り返した後、さらに二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)(以下、60時間充電とも称する)を行った状態において、充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有することを特徴とする。なお、以下、0V−1.2Vサイクルから60時間充電までを合わせて、充電条件Aとも称する。
まず、充電条件Aの詳細について説明する。まず、0V定電流定電圧充電(0VCCCV)とは、リチウムを対極とした二次電池を作製した後、0Vまで定電流(電流密度:0.5mA/cm2)モードで充電し、0Vから定電圧モードになり、電流密度が0.1mA/cm2に達した後、充電終止することを意味する。次に、1.2V定電流放電とは、定電流(電流密度:0.5mA/cm2)モードで放電し、電位が1.2Vに達した後、放電終止することを意味する。次に、60時間充電とは、0Vまで定電流(電流密度:0.5mA/cm2)モードで充電し、0Vから定電圧モードになり、0Vになってから60時間経過後に充電終止することを意味する。
上記のように、本発明の負極活物質は、上記の充電条件Aで充電を行った場合に上記の2種類のピークが得られる活物質である。上記のように、負極活物質が、ケイ素化合物を含有する負極活物質粒子を含むものであり、かつ、上記の充電終止後において上記の2種類のピークを有するものであれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、高い電池容量を有するとともに、良好なサイクル特性が得られる。
ここで、25〜55ppmの範囲のピークは、Li−Si結合の存在を表しているものと推測される。このピークが得られる負極活物質は、Li挿入、脱離を繰り返すことによりケイ素酸化物のバルク状況が安定化しやすい。従って、このピークが得られる負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、安定した電池特性、特に、安定したサイクル特性を得ることができる。
一方、0〜3ppmの範囲のピークは、Liシリケート層(Li−O結合)の存在を表しているものと推測される。このピークが得られる負極活物質は、Li挿入、脱離を繰り返すことにより負極活物質粒子の内部に安定したLi化合物が生成しやすい。従って、このピークが得られる負極活物質は、ケイ素酸化物のバルク内において容易にLiが拡散するものとなる。従って、このピークが得られる負極活物質は、安定した電池材料となり、サイクル特性を向上させることができる。
0V−1.2VサイクルにおけるXの回数は特に限定されない。例えば、Xの上限は99とすることができる。すなわち、Xの範囲を0≦X≦99とすることができる。なお、Xの範囲はより好ましくは0≦X≦49、さらに好ましくは0≦X≦9、特に好ましくはX=0である。
Xの上限が99の場合は、0V−1.2Vサイクルを0回以上99回以下行った後、60時間充電を行った状態において、充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有するものであればよい。この場合、例えば、0V−1.2Vサイクルを19回行った後、20サイクル目の60時間充電時にこれらのピークが発現しても良いし、0V−1.2Vサイクルを49回行った後、50サイクル目の60時間充電時にこれらのピークが発現しても良い。
なお、本発明においては、先に0〜3ppmの範囲のピークが発現し、その後、このピークに加えて25〜55ppmの範囲のピークが発現してもよい。例えば、1サイクル目の60時間充電時(すなわち、X=0)に0〜3ppmの範囲のピークが発現し、10サイクル目の60時間充電時(すなわち、X=9)に0〜3ppmの範囲のピークと共に25〜55ppmの範囲のピークが発現してもよい。
本発明においては、特に、以下に示すような回数以内で2種類のピークが発現することが好ましい。
まず、25〜55ppmの範囲のピークは、Xが49回以内で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、当該二次電池が安定化するまでの時間(サイクル数)をより少なくすることができる。これにより、充放電サイクル初期のサイクル劣化率がより小さくなり、サイクル特性がより向上する。このような負極活物質を有する二次電池は、安定したサイクル特性を有する。
また、0〜3ppmの範囲のピークは、Xが9回以内で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、負極活物質粒子の内部に安定したLi化合物が生成するまでの時間(サイクル数)をより少なくすることができる。これにより、ケイ素酸化物のバルク内におけるLi拡散をより容易にすることができる。
また、25〜55ppmの範囲のピーク及び0〜3ppmの範囲のピークは、Xが0回で発現することが好ましい。
このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、当該二次電池が安定化するまでの時間及び負極活物質粒子の内部に安定したLi化合物が生成するまでの時間をさらに少なくすることができる。
また、25〜55ppmの範囲のピークは、0V定電流定電圧充電及び1.2V定電流放電のサイクルを49回以内繰り返す中で減少することが好ましい。すなわち、本発明の負極活物質は、0V−1.2Vサイクルを49回以内繰り返す中で、25〜55ppmの範囲のピークが発現及び減少することが好ましい。特に、25〜55ppmの範囲のピークが発現及び消失することが好ましい。この態様の具体例としては、1サイクル目の60時間充電時(すなわち、X=0)に25〜55ppmの範囲のピークが発現し、10サイクル目の60時間充電時(すなわち、X=9)に25〜55ppmの範囲のピークが減少する態様が挙げられる。
このような負極活物質であれば、Li挿入、脱離を繰り返すことによりケイ素酸化物のバルク状況がより安定化する。すなわち、Li挿入、脱離を繰り返すことにより活物質の状態が充放電に適した状態となる。
特に、本発明の負極活物質は、0V−1.2Vサイクルを繰り返す中で、25〜55ppmの範囲のピークが発現及び減少(特に消失)するだけでなく、このピークが0V−1.2Vサイクルを繰り返す中で0ppmに近い方向へ徐々にシフトすることが好ましい。このような負極活物質は、Li挿入、脱離を繰り返すことでより安定したバルク状況を作ることができる。
なお、上記のように25〜55ppmの範囲のピーク等が発現等する負極活物質がサイクル特性を向上させる理由は完全に解明はされていないが、少なくとも、上記の充電条件Aで充電を行った場合に上記の2種類のピークが得られる活物質がサイクル特性を向上させること自体は明らかである。
また、負極活物質は、X線回折により得られるSi(111)結晶面に起因する回折ピークの半値幅(2θ)が1.2°以上であるとともに、その結晶面に対応する結晶子サイズは7.5nm以下であることが好ましい。
ケイ素酸化物のケイ素結晶性は低いほどよく、ケイ素酸化物中のSi結晶子が上記の結晶性を有することで、このようなケイ素酸化物を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、より良好なサイクル特性及び初期充放電特性が得られる。
負極活物質粒子のメジアン径(D50:累積体積が50%となる時の粒子径)は特に限定されないが、0.5μm以上20μm以下であることが好ましい。メジアン径が上記の範囲であれば、充放電時においてリチウムイオンの吸蔵放出がされやすくなるとともに、粒子が割れにくくなるからである。メジアン径が0.5μm以上であれば、質量当たりの表面積を小さくでき、電池不可逆容量の増加を抑制することができる。一方で、メジアン径を20μm以下とすることで、粒子が割れ難くなるため新表面が出難くなる。
また、負極活物質粒子は、表層部に炭素材を含むことが好ましい。
このように、負極活物質粒子がその表層部に炭素材を含むことで、導電性の向上が得られるため、このような負極活物質粒子を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、電池特性を向上させることができる。
また、この炭素材の平均厚さは1nm以上5000nm以下であることが好ましい。
被覆する炭素材の平均厚さが1nm以上であれば導電性向上が得られ、被覆する炭素材の平均厚さが5000nm以下であれば、このような負極活物質粒子を含む負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、電池容量の低下を抑制することができる。
この炭素材の平均厚さは、例えば、以下の手順により算出できる。まず、TEM(透過型電子顕微鏡)により任意の倍率で負極活物質を観察する。この倍率は、厚さを測定できるように、目視で炭素材の厚さを確認できる倍率が好ましい。続いて、任意の15点において、炭素材の厚さを測定する。この場合、できるだけ特定の場所に集中せず、広くランダムに測定位置を設定することが好ましい。最後に、上記の15点の炭素材の厚さの平均値を算出する。
炭素材の被覆率は特に限定されないが、できるだけ高い方が望ましい。被覆率が30%以上であれば、電気伝導性がより向上するため好ましい。炭素材の被覆手法は特に限定されないが、糖炭化法、炭化水素ガスの熱分解法が好ましい。なぜならば、被覆率を向上させることができるからである。
また、負極活物質層12に含まれる負極結着剤として、例えば、高分子材料、合成ゴムなどのいずれか1種類以上を用いることができる。高分子材料は、例えば、ポリフッ化ビニリデン、ポリイミド、ポリアミドイミド、アラミド、ポリアクリル酸、ポリアクリル酸リチウム、カルボキシメチルセルロースなどである。合成ゴムは、例えば、スチレンブタジエン系ゴム、フッ素系ゴム、エチレンプロピレンジエンなどである。
負極導電助剤としては、例えば、カーボンブラック、アセチレンブラック、黒鉛、ケチェンブラック、カーボンナノチューブ、カーボンナノファイバーなどの炭素材料のいずれか1種以上を用いることができる。
負極活物質層12は、本発明の負極活物質(ケイ素系活物質)に加えて、炭素系活物質を含んでいてもよい。これにより、負極活物質層12の電気抵抗を低下するとともに、充電に伴う膨張応力を緩和することが可能となる。この炭素系活物質としては、例えば、熱分解炭素類、コークス類、ガラス状炭素繊維、有機高分子化合物焼成体、カーボンブラック類などを使用できる。
負極活物質層12は、例えば、塗布法で形成される。塗布法とは、ケイ素系活物質と上記の結着剤など、また、必要に応じて導電助剤、炭素系活物質を混合した後に、有機溶剤や水などに分散させ塗布する方法である。
[負極の製造方法]
負極10は、例えば、以下の手順により製造できる。まず、負極に使用する負極活物質の製造方法を説明する。最初に、一般式SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含む負極活物質粒子を準備する。次に、この負極活物質粒子を含む負極活物質を含む負極と、金属リチウムからなる対極とを有する二次電池を作製する。次に、このようにして作製された二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらにこの二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行う。次に、充電終止の状態において、負極活物質を7Li−MAS−NMRで測定する。次に、7Li−MAS−NMRのスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有する負極活物質を選別する。
負極10は、例えば、以下の手順により製造できる。まず、負極に使用する負極活物質の製造方法を説明する。最初に、一般式SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含む負極活物質粒子を準備する。次に、この負極活物質粒子を含む負極活物質を含む負極と、金属リチウムからなる対極とを有する二次電池を作製する。次に、このようにして作製された二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらにこの二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行う。次に、充電終止の状態において、負極活物質を7Li−MAS−NMRで測定する。次に、7Li−MAS−NMRのスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有する負極活物質を選別する。
ケイ素酸化物(SiOx:0.5≦x≦1.6)を含む負極活物質粒子は、例えば、以下のような手法により作製できる。まず、酸化珪素ガスを発生する原料を不活性ガスの存在下、減圧下で900℃〜1600℃の温度範囲で加熱し、酸化珪素ガスを発生させる。このとき、原料は金属珪素粉末と二酸化珪素粉末の混合物を用いることができる。金属珪素粉末の表面酸素及び反応炉中の微量酸素の存在を考慮すると、混合モル比が、0.8<金属珪素粉末/二酸化珪素粉末<1.3の範囲であることが望ましい。
次に、発生した酸化珪素ガスは吸着板(堆積板)上で固体化され堆積される。次に、反応炉内温度を100℃以下に下げた状態で酸化珪素の堆積物を取出し、ボールミル、ジェットミルなどを用いて粉砕、粉末化を行う。以上のようにして、負極活物質粒子を作製することができる。
なお、負極活物質粒子中のSi結晶子は、酸化珪素ガスを発生する原料の気化温度の変更、堆積板温度、酸化珪素ガスの蒸着流に対するガス(不活性ガス,還元ガス)の噴射量若しくは種類、負極活物質粒子生成後の熱処理又は後述する炭素材を堆積する際の温度若しくは時間で制御することができる。
なお、25〜55ppmの範囲のピーク及び0〜3ppmの範囲のピークが発現するサイクル数は、酸化珪素析出時の堆積板の温度、後述するCVDで炭素材を堆積する際の加熱温度若しくは時間又は酸化珪素の堆積物の粉砕条件で制御することができる。例えば、酸化珪素析出時の堆積板の温度を高くすると、これらのピーク(特に、25〜55ppmの範囲のピーク)が早く得られやすくなる。但し、この温度を高くしすぎると、これらのピークの発現が遅延することがある。
次に、準備した負極活物質粒子の表層部に炭素材を形成する。但し、この工程は必須ではない。炭素材の層を生成する方法としては、熱分解CVD法が望ましい。熱分解CVD法で炭素材の層を生成する方法の一例について以下に説明する。
まず、負極活物質粒子を炉内にセットする。次に、炉内に炭化水素ガスを導入し、炉内温度を昇温させる。分解温度は特に限定しないが、1200℃以下が望ましく、より望ましいのは950℃以下である。分解温度を1200℃以下にすることで、負極活物質粒子の意図しない不均化を抑制することができる。所定の温度まで炉内温度を昇温させた後に、負極活物質粒子の表層部に炭素材を生成する。また、炭素材の原料となる炭化水素ガスは特に限定しないが、CnHm組成においてn≦3であることが望ましい。n≦3であれば、製造コストを低くでき、また、分解生成物の物性を良好にすることができる。
このように、炭素材で負極活物質粒子を被覆することでバルク内部の化合物状態をより均一化にすることができ、活物質としての安定性が向上し、より高い効果を得ることができる。
次に、上記の負極活物質粒子を含む負極活物質を含む負極と、金属リチウムからなる対極とを有する二次電池を作製する。ここではこの試験用の二次電池の具体例として、2032型コイン電池を例に挙げる。
まず、2032型コイン電池に用いる負極を準備する。この負極は本発明の負極活物質を含むものであればよい。例えば、図2に示す負極が挙げられる。この負極の作製方法は、本発明の負極の製造方法と同様とすることができる。また、金属リチウムからなる対極を準備する。具体例としては、厚さ0.5mmの金属リチウム箔が挙げられる。次に、電解液及びセパレータを準備する。これらの具体例としては、後述する本発明の二次電池に用いるものと同様のものが挙げられる。
続いて、2032型コイン電池の底ブタ、リチウム箔、セパレータを重ねて、電解液を注液し、続けて負極、スペーサ(例えば、厚さ1.0mm)を重ねて、電解液を注液し、続けてスプリング、コイン電池の上ブタの順にくみ上げ、自動コインセルカシメ機でかしめることで、2032型コイン電池を作製できる。
次に、このようにして作製された二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらにこの二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行う。この充電条件Aの詳細は上述した通りである。Xの上限は、製造する負極活物質の品質に応じて適宜設定できる(例えば99)が、上述の通りできるだけ小さいことが好ましい。
次に、充電終止の状態において、負極活物質を7Li−MAS−NMRで測定する。負極活物質は、固体7Li−MAS−NMRにより測定される。この際、用いる装置は特に限定されないが、Bruker社製700NMR分光器が挙げられる。この際、プローブとして直径2.5mmロータを用い、試料回転速度は16kHz回転とし、測定環境温度は25℃とすることができる。
以下、1サイクル目の60時間充電時(すなわち、X=0)に0〜3ppmの範囲のピーク及び25〜55ppmの範囲のピークが発現した場合を例に、7Li−MAS−NMRの測定手順を説明する。
負極活物質のNMRを測定するためには、各サイクルに対して、通常、約20個のコイン電池が必要になる。これはNMRロータに詰める負極活物質を十分に確保するためである。従って、上記の例の場合は、20個のコイン電池を用意すればよい。まず、同一の製造条件で製造された負極活物質を含む負極を20個準備する。次に、この負極を有する2032型コイン電池を20個作製し、これらのコイン電池の充電を充電条件A(X=0)で行う。次に、充電終止の状態のコイン電池20個をグローブボックス中で解体し、負極から負極活物質を剥離させ、1つのNMRロータに詰め込む。次に、このようにしてNMRロータに詰め込まれた負極活物質のNMR測定を行う。この測定により、0〜3ppmの範囲のピーク及び25〜55ppmの範囲のピークが発現したことを確認し、試験を終了する。なお、2サイクル目に2種類のピークが発現する場合は、計40個のコイン電池を作製することになる。このような測定方法であれば、何サイクル目で2種類のピークが発現するかを確実に判別できる。
次に、7Li−MAS−NMRのスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有する負極活物質を選別する。例えば、ある製造条件で負極活物質を製造し、この負極活物質のNMR測定を行い、Xが9回以内で2種類のピークが得られることを確認した場合、同じ製造条件で製造した負極活物質は全て2種類のピークがXが9回以内で発現するものであるとみなして、負極活物質の選別を行うことができる。また、負極活物質を生成する条件又は炭素被覆の条件を変更させ、その都度7Li−MAS−NMRによる測定を行うことで、各製造条件において2種類のピークが得られるのにどれくらいの時間(サイクル数)がかかるのかを決定することもできる。
このような製造方法により製造された負極活物質は、Liとの反応時にケイ素酸化物のバルク内に存在する二酸化ケイ素成分が安定したLi化合物へ変化すると共に、ケイ素−リチウム結合状態が二次電池に適した状態へ誘導されるものとなる。
以上のようにして製造(選別)された負極活物質と、負極結着剤、導電助剤などの他の材料とを混合して、負極合剤とした後に、有機溶剤又は水などを加えてスラリーとする。次に、負極集電体11の表面に、上記の負極合剤スラリーを塗布し、乾燥させて、負極活物質層12を形成する。この時、必要に応じて加熱プレスなどを行ってもよい。以上のようにして、負極を作製できる。
<リチウムイオン二次電池>
次に、本発明のリチウムイオン二次電池について説明する。本発明のリチウムイオン二次電池は負極電極として、上記本発明の負極電極を用いたものである。ここでは具体例として、ラミネートフィルム型のリチウムイオン二次電池を例に挙げる。
次に、本発明のリチウムイオン二次電池について説明する。本発明のリチウムイオン二次電池は負極電極として、上記本発明の負極電極を用いたものである。ここでは具体例として、ラミネートフィルム型のリチウムイオン二次電池を例に挙げる。
[ラミネートフィルム型二次電池の構成]
図3に示すラミネートフィルム型のリチウムイオン二次電池30は、主にシート状の外装部材35の内部に巻回電極体31が収納されたものである。この巻回体は正極、負極間にセパレータを有し、巻回されたものである。また正極、負極間にセパレータを有し積層体を収納した場合も存在する。どちらの電極体においても、正極に正極リード32が取り付けられ、負極に負極リード33が取り付けられている。電極体の最外周部は保護テープにより保護されている。
図3に示すラミネートフィルム型のリチウムイオン二次電池30は、主にシート状の外装部材35の内部に巻回電極体31が収納されたものである。この巻回体は正極、負極間にセパレータを有し、巻回されたものである。また正極、負極間にセパレータを有し積層体を収納した場合も存在する。どちらの電極体においても、正極に正極リード32が取り付けられ、負極に負極リード33が取り付けられている。電極体の最外周部は保護テープにより保護されている。
正負極リードは、例えば、外装部材35の内部から外部に向かって一方向で導出されている。正極リード32は、例えば、アルミニウムなどの導電性材料により形成され、負極リード33は、例えば、ニッケル、銅などの導電性材料により形成される。
外装部材35は、例えば、融着層、金属層、表面保護層がこの順に積層されたラミネートフィルムであり、このラミネートフィルムは融着層が巻回電極体31と対向するように、2枚のフィルムの融着層における外周縁部同士が融着、又は、接着剤などで張り合わされている。融着部は、例えばポリエチレンやポリプロピレンなどのフィルムであり、金属部はアルミ箔などである。保護層は例えば、ナイロンなどである。
外装部材35と正負極リードとの間には、外気侵入防止のため密着フィルム34が挿入されている。この材料は、例えば、ポリエチレン、ポリプロピレン、ポリオレフィン樹脂である。
[正極]
正極は、例えば、図2の負極10と同様に、正極集電体の両面又は片面に正極活物質層を有している。
正極は、例えば、図2の負極10と同様に、正極集電体の両面又は片面に正極活物質層を有している。
正極集電体は、例えば、アルミニウムなどの導電性材により形成されている。
正極活物質層は、リチウムイオンの吸蔵放出可能な正極材のいずれか1種又は2種以上を含んでおり、設計に応じて結着剤、導電助剤、分散剤などの他の材料を含んでいてもよい。この場合、結着剤、導電助剤に関する詳細は、例えば、既に記述した負極結着剤、負極導電助剤と同様とすることができる。
正極材料としては、リチウム含有化合物が望ましい。このリチウム含有化合物は、例えば、リチウムと遷移金属元素からなる複合酸化物、又はリチウムと遷移金属元素を有するリン酸化合物が挙げられる。これらの正極材の中でも、ニッケル、鉄、マンガン、コバルトの少なくとも1種以上を有する化合物が好ましい。これらの正極材の化学式は、例えば、LixM1O2、又は、LiyM2PO4で表される。上記の化学式中、M1、M2は少なくとも1種以上の遷移金属元素を示しており、x、yの値は電池充放電状態によって異なる値を示すが、一般的に、0.05≦x≦1.10、0.05≦y≦1.10で示される。
リチウムと遷移金属元素とを有する複合酸化物としては、例えば、リチウムコバルト複合酸化物(LixCoO2)、リチウムニッケル複合酸化物(LixNiO2)などが挙げられ、リチウムと遷移金属元素とを有するリン酸化合物としては、例えば、リチウム鉄リン酸化合物(LiFePO4)、リチウム鉄マンガンリン酸化合物(LiFe1−uMnuPO4(0<u<1))などが挙げられる。上記の正極材を用いれば、高い電池容量が得られるともに、優れたサイクル特性も得られるからである。
[負極]
負極は、上記した図2の負極10と同様の構成を有し、例えば、集電体の両面に負極活物質層を有している。この負極は、正極活物質剤から得られる電気容量(電池としての充電容量)に対して、負極充電容量が大きくなることが好ましい。これにより、負極上でのリチウム金属の析出を抑制することができる。
負極は、上記した図2の負極10と同様の構成を有し、例えば、集電体の両面に負極活物質層を有している。この負極は、正極活物質剤から得られる電気容量(電池としての充電容量)に対して、負極充電容量が大きくなることが好ましい。これにより、負極上でのリチウム金属の析出を抑制することができる。
正極活物質層は、正極集電体の両面の一部に設けられており、負極活物質層も負極集電体の両面の一部に設けられている。この場合、例えば、負極集電体上に設けられた負極活物質層は対向する正極活物質層が存在しない領域が設けられている。これは、安定した電池設計を行うためである。
上記の負極活物質層と正極活物質層とが対向しない領域では、充放電の影響をほとんど受けることが無い。そのため、負極活物質層の状態が形成直後のまま維持され、これによって負極活物質の組成など、充放電の有無に依存せずに再現性良く組成などを正確に調べることができる。
[セパレータ]
セパレータは正極、負極を隔離し、両極接触に伴う電流短絡を防止しつつ、リチウムイオンを通過させるものである。このセパレータは、例えば、合成樹脂、あるいはセラミックからなる多孔質膜により形成されており、2種以上の多孔質膜が積層された積層構造を有しても良い。合成樹脂として、例えば、ポリテトラフルオロエチレン、ポリプロピレン、ポリエチレンなどが挙げられる。
セパレータは正極、負極を隔離し、両極接触に伴う電流短絡を防止しつつ、リチウムイオンを通過させるものである。このセパレータは、例えば、合成樹脂、あるいはセラミックからなる多孔質膜により形成されており、2種以上の多孔質膜が積層された積層構造を有しても良い。合成樹脂として、例えば、ポリテトラフルオロエチレン、ポリプロピレン、ポリエチレンなどが挙げられる。
[電解液]
活物質層の少なくとも一部、又は、セパレータには、液状の電解質(電解液)が含浸されている。この電解液は、溶媒中に電解質塩が溶解されており、添加剤など他の材料を含んでいても良い。
活物質層の少なくとも一部、又は、セパレータには、液状の電解質(電解液)が含浸されている。この電解液は、溶媒中に電解質塩が溶解されており、添加剤など他の材料を含んでいても良い。
溶媒は、例えば、非水溶媒を用いることができる。非水溶媒としては、例えば、炭酸エチレン、炭酸プロピレン、炭酸ブチレン、炭酸ジメチル、炭酸ジエチル、炭酸エチルメチル、炭酸メチルプロピル、1,2−ジメトキシエタン、テトラヒドロフランなどが挙げられる。この中でも、炭酸エチレン、炭酸プロピレン、炭酸ジメチル、炭酸ジエチル、炭酸エチルメチルのうちの少なくとも1種以上を用いることが望ましい。より良い特性が得られるからである。またこの場合、炭酸エチレン、炭酸プロピレンなどの高粘度溶媒と、炭酸ジメチル、炭酸エチルメチル、炭酸ジエチルなどの低粘度溶媒とを組み合わせて用いることで、電解質塩の解離性やイオン移動度を向上させることができる。
合金系負極を用いる場合、特に溶媒として、ハロゲン化鎖状炭酸エステル、又は、ハロゲン化環状炭酸エステルのうち少なくとも1種を含んでいることが望ましい。これにより、充放電時、特に充電時において、負極活物質表面に安定な被膜が形成される。ここで、ハロゲン化鎖状炭酸エステルとは、ハロゲンを構成元素として有する(少なくとも1つの水素がハロゲンにより置換された)鎖状炭酸エステルである。また、ハロゲン化環状炭酸エステルとは、ハロゲンを構成元素として有する(すなわち、少なくとも1つの水素がハロゲンにより置換された)環状炭酸エステルである。
ハロゲンの種類は特に限定されないが、フッ素が好ましい。これは、他のハロゲンよりも良質な被膜を形成するからである。また、ハロゲン数は多いほど望ましい。これは、得られる被膜がより安定的であり、電解液の分解反応が低減されるからである。
ハロゲン化鎖状炭酸エステルは、例えば、炭酸フルオロメチルメチル、炭酸ジフルオロメチルメチルなどが挙げられる。ハロゲン化環状炭酸エステルとしては、4−フルオロ−1,3−ジオキソラン−2−オン、4,5−ジフルオロ−1,3−ジオキソラン−2−オンなどが挙げられる。
溶媒添加物として、不飽和炭素結合環状炭酸エステルを含んでいることが好ましい。これは、充放電時に負極表面に安定な被膜が形成され、電解液の分解反応が抑制できるからである。不飽和炭素結合環状炭酸エステルとしては、例えば炭酸ビニレン、炭酸ビニルエチレンなどが挙げられる。
また、溶媒添加物として、スルトン(環状スルホン酸エステル)を含んでいることも好ましい。これは、電池の化学的安定性が向上するからである。スルトンとしては、例えば、プロパンスルトン、プロペンスルトンが挙げられる。
さらに、溶媒は、酸無水物を含んでいることが好ましい。これは、電解液の化学的安定性が向上するからである。酸無水物としては、例えば、プロパンジスルホン酸無水物が挙げられる。
電解質塩は、例えば、リチウム塩などの軽金属塩のいずれか1種類以上含むことができる。リチウム塩としては、例えば、六フッ化リン酸リチウム(LiPF6)、四フッ化ホウ酸リチウム(LiBF4)などが挙げられる。
電解質塩の含有量は、溶媒に対して0.5mol/kg以上2.5mol/kg以下であることが好ましい。これは、高いイオン伝導性が得られるからである。
[ラミネートフィルム型のリチウムイオン二次電池の製造方法]
最初に上記した正極材を用い正極電極を作製する。まず、正極活物質と、必要に応じて結着剤、導電助剤などを混合し正極合剤とした後に、有機溶剤に分散させ正極合剤スラリーとする。続いて、ナイフロール又はダイヘッドを有するダイコーターなどのコーティング装置で正極集電体に合剤スラリーを塗布し、熱風乾燥させて正極活物質層を得る。最後に、ロールプレス機などで正極活物質層を圧縮成型する。この時、加熱しても良く、また加熱又は圧縮を複数回繰り返しても良い。
最初に上記した正極材を用い正極電極を作製する。まず、正極活物質と、必要に応じて結着剤、導電助剤などを混合し正極合剤とした後に、有機溶剤に分散させ正極合剤スラリーとする。続いて、ナイフロール又はダイヘッドを有するダイコーターなどのコーティング装置で正極集電体に合剤スラリーを塗布し、熱風乾燥させて正極活物質層を得る。最後に、ロールプレス機などで正極活物質層を圧縮成型する。この時、加熱しても良く、また加熱又は圧縮を複数回繰り返しても良い。
次に、上記した負極10の作製と同様の作業手順を用い、負極集電体に負極活物質層を形成し負極を作製する。
正極及び負極を作製する際に、正極及び負極集電体の両面にそれぞれの活物質層を形成する。この時、どちらの電極においても両面部の活物質塗布長がずれていても良い(図2を参照)。
続いて、電解液を調製する。続いて、超音波溶接などにより、正極集電体に正極リード32を取り付けると共に、負極集電体に負極リード33を取り付ける。続いて、正極と負極とをセパレータを介して積層、又は巻回させて巻回電極体31を作製し、その最外周部に保護テープを接着させる。次に、扁平な形状となるように巻回体を成型する。続いて、折りたたんだフィルム状の外装部材の間に巻回電極体を挟み込んだ後、熱融着法により外装部材35の絶縁部同士を接着させ、一方向のみ解放状態にて、巻回電極体を封入する。正極リード、及び負極リードと外装部材の間に密着フィルムを挿入する。解放部から上記調製した電解液を所定量投入し、真空含浸を行う。含浸後、解放部を真空熱融着法により接着させる。以上のようにして、ラミネートフィルム型のリチウムイオン二次電池30を製造することができる。
以下、実施例及び比較例を示して本発明をより具体的に説明するが、本発明は下記の実施例に限定されるものではない。
(実施例1−1)
以下の手順により、図3に示したラミネートフィルム型のリチウムイオン二次電池30を作製した。
以下の手順により、図3に示したラミネートフィルム型のリチウムイオン二次電池30を作製した。
最初に正極を作製した。正極活物質はリチウムニッケルコバルト複合酸化物であるLiNi0.7Co0.25Al0.05O(リチウムニッケルコバルトアルミニウム複合酸化物:NCA)を95質量%と、正極導電助剤2.5質量%と、正極結着剤(ポリフッ化ビニリデン:PVDF)2.5質量%とを混合し、正極合剤とした。続いて正極合剤を有機溶剤(N−メチル−2−ピロリドン:NMP)に分散させてペースト状のスラリーとした。続いてダイヘッドを有するコーティング装置で正極集電体の両面にスラリーを塗布し、熱風式乾燥装置で乾燥した。この時正極集電体は厚み15μmのものを用いた。最後にロールプレスで圧縮成型を行った。
次に負極を作製した。負極活物質は金属ケイ素と二酸化ケイ素を混合した原料を反応炉に導入し、10Paの真空度の雰囲気中で気化させたものを吸着板上に堆積させ、十分に冷却した後、堆積物を取出しボールミルで粉砕した。粒径を調整した後、熱分解CVDを行うことで負極活物質粒子の表層部に炭素材を形成した。続いて、負極活物質粒子と負極結着剤の前駆体(ポリアミック酸)、導電助剤1(鱗片状黒鉛)と導電助剤2(アセチレンブラック)とを80:8:10:2の乾燥質量比で混合した後、NMPで希釈してペースト状の負極合剤スラリーとした。この場合には、ポリアミック酸の溶媒としてNMPを用いた。続いて、コーティング装置で負極集電体の両面に負極合剤スラリーを塗布してから乾燥させた。この負極集電体としては、電解銅箔(厚さ=15μm)を用いた。最後に、真空雰囲気中で400℃1時間焼成した。これにより、負極結着剤(ポリイミド)が形成された。また、これにより、負極集電体の両面に負極活物質層が形成された。このとき、負極集電体は炭素及び硫黄を含むとともに、それらの含有量がいずれも100質量ppm以下であった。
次に、溶媒(4−フルオロ−1,3−ジオキソラン−2−オン(FEC)、エチレンカーボネート(EC)及びジメチルカーボネート(DMC))を混合した後、電解質塩(六フッ化リン酸リチウム:LiPF6)を溶解させて電解液を調製した。この場合には、溶媒の組成を体積比でFEC:EC:DMC=10:20:70とし、電解質塩の含有量を溶媒に対して1.0mol/kgとした。
次に、以下のようにして二次電池を組み立てた。最初に、正極集電体の一端にアルミリードを超音波溶接し、負極集電体の一端にはニッケルリードを溶接した。続いて、正極、セパレータ、負極、セパレータをこの順に積層し、長手方向に巻回させ巻回電極体を得た。その捲き終わり部分をPET保護テープで固定した。セパレータは多孔性ポリプロピレンを主成分とするフィルムにより多孔性ポリエチレンを主成分とするフィルムに挟まれた積層フィルム(厚さ12μm)を用いた。続いて、外装部材間に電極体を挟んだ後、一辺を除く外周縁部同士を熱融着し、内部に電極体を収納した。外装部材はナイロンフィルム、アルミ箔及び、ポリプロピレンフィルムが積層されたアルミラミネートフィルムを用いた。続いて、開口部から調製した電解液を注入し、真空雰囲気下で含浸した後、熱融着し、封止した。
以上のようにして作製した二次電池のサイクル特性及び初回充放電特性を評価した。
サイクル特性については、以下のようにして調べた。最初に、電池安定化のため25℃の雰囲気下、2サイクル充放電を行い、2サイクル目の放電容量を測定した。続いて、総サイクル数が100サイクルとなるまで充放電を行い、その都度放電容量を測定した。最後に、100サイクル目の放電容量を2サイクル目の放電容量で割り、容量維持率を算出した。なお、サイクル条件として、4.2Vに達するまで定電流密度、2.5mA/cm2で充電し、電圧4.2Vに達した段階で4.2V定電圧で電流密度が0.25mA/cm2に達するまで充電した。また、放電時は2.5mA/cm2の定電流密度で電圧が2.5Vに達するまで放電した。
初回充放電特性については、初回効率(初期効率)(%)=(初回放電容量/初回充電容量)×100を算出した。なお、雰囲気及び温度はサイクル特性を調べた場合と同様にし、充放電条件はサイクル特性を調べた場合の0.2倍で行った。
次に、7Li−MAS−NMR測定試験用の二次電池として、2032型コイン電池を組み立てた。各サイクルに対して、同一の製造条件で製造された負極活物質を含む負極を有するコイン電池を20個用意した。
負極としては、上記の実施例1−1におけるラミネートフィルム型のリチウムイオン二次電池30の負極と同様の手順で作製したものを使用した。なお、この負極の片面における単位面積あたりの負極活物質層の堆積量(面積密度とも称する)は2.5mg/cm2であった。
電解液としては、上記の実施例1−1におけるラミネートフィルム型のリチウムイオン二次電池30の電解液と同様の手順で作製したものを使用した。
対極としては、厚さ0.5mmの金属リチウム箔を使用した。また、セパレータとして、厚さ20μmのポリエチレンを用いた。
続いて、2032型コイン電池の底ブタ、リチウム箔、セパレータを重ねて、電解液150mLを注液し、続けて負極、スペーサ(厚さ1.0mm)を重ねて、電解液150mLを注液し、続けてスプリング、コイン電池の上ブタの順にくみ上げ、自動コインセルカシメ機でかしめることで、2032型コイン電池を作製した。
7Li−MAS−NMRの測定条件は、上述の充電条件Aと同様の条件とした。すなわち、所定の回数0V−1.2Vサイクルを行い、その後60時間充電を行った。これにより、各サイクルにおけるNMRの測定結果を得た。なお、負極活物質のNMR測定は、負極活物質を含むコイン電池をグローブボックス中で解体し、負極から負極活物質を剥離させ、NMRロータに詰め込むことによって行った。また、本実施例における0V−1.2VサイクルのXの上限は99とした。例えば、100サイクル目の60時間充電時までに25〜55ppmの範囲のピークが発現しなかった負極活物質は、このピークが得られない負極活物質であるとみなし、表中の「25〜55ppm」に「無し」と記載した。
(実施例1−2〜実施例1−10、比較例1−1〜1−4)
ケイ素酸化物のバルク内酸素、X線回折により得られるSi(111)結晶面に起因する回折ピークの半価幅(半値幅)(これは、この半価幅から計算される結晶子サイズにも反映される)、25〜55ppmの範囲のピーク有無、0〜3ppmの範囲のピーク有無、「50回以内に発現及び減少」の有無(すなわち、0V−1.2Vサイクルを49回以内繰り返す中で25〜55ppmの範囲のピークが発現及び減少するか否か)並びに25〜55ppmの範囲のピーク発現時のサイクル数(Cyで示す)を変化させたことを除き、実施例1−1と同様に、二次電池の製造を行った。表1に実施例1−1〜実施例1−10及び比較例1−1〜1−4の結果を示す。
ケイ素酸化物のバルク内酸素、X線回折により得られるSi(111)結晶面に起因する回折ピークの半価幅(半値幅)(これは、この半価幅から計算される結晶子サイズにも反映される)、25〜55ppmの範囲のピーク有無、0〜3ppmの範囲のピーク有無、「50回以内に発現及び減少」の有無(すなわち、0V−1.2Vサイクルを49回以内繰り返す中で25〜55ppmの範囲のピークが発現及び減少するか否か)並びに25〜55ppmの範囲のピーク発現時のサイクル数(Cyで示す)を変化させたことを除き、実施例1−1と同様に、二次電池の製造を行った。表1に実施例1−1〜実施例1−10及び比較例1−1〜1−4の結果を示す。
なお、実施例1−1〜実施例1−10及び比較例1−1〜1−4の負極活物質は以下のような性質を有していた。負極活物質粒子のメジアン径は4μmであった。負極活物質粒子は、表層部に平均厚さ100nmの炭素材を含むものであった。特に、実施例1−1〜実施例1−10の負極活物質は全て、0〜3ppmの範囲のピークが1サイクル目の60時間充電時に発現し、一度発現した0〜3ppmの範囲のピークは0V−1.2Vサイクルを繰り返す中で減少することはなかった。なお、後述するように、充放電サイクル初期に25〜55ppmの範囲に出たピークが充放電サイクルを繰り返すことにより0ppmに近い方へシフトすることがある。この時、このシフトしたピークのピークシフト値は0〜3ppmの範囲のピークのピークシフト値より大きいため、0〜3ppmの範囲のピークが上記のシフトしたピークに埋もれてしまうことがある。
表1に示すように、SiOxで表されるケイ素酸化物において、xの値が、0.5≦x≦1.6の範囲外の場合、電池特性が悪化した。例えば、比較例1−1に示すように、酸素が十分にない場合(x=0.3)、25〜55ppmの範囲のピークが発現せず、また安定したLiシリケートピーク(0〜3ppmの範囲のピーク)も得ることができなかった。従って、二次電池の容量維持率が著しく悪化した。なお、二次電池の初期効率は高い値であったが、サイクル特性が大きく低下したことから、総合的に判断し、電池特性が悪いと結論付けた。一方、比較例1−3に示すように、酸素量が多くなると(x=1.8)、電子抵抗、イオン拡散抵抗が上昇し、電池評価が難しく、電池初期効率が大幅に低下した。そのため、サイクル特性の評価は中止した。また、比較例1−2は、SiOxのxが0.5であったが、2種類のピークが発現しなかったため、サイクル特性及び初期効率の結果は悪かった。
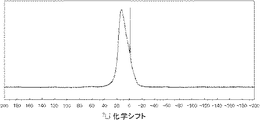
一方で、本発明の負極活物質を用いた二次電池(実施例1−1〜実施例1−10)は、良好なサイクル特性が得られた。図1は、本発明の実施例1−3において測定された7Li−MAS−NMRスペクトルである。図1中の25〜55ppmの範囲のピークは、Li−Si結合の存在を表しているものと推測される。
一方、図4は、負極活物質としてケイ素単体を含む一般的なケイ素単体負極を用いて測定された7Li−MAS−NMRスペクトルである。このスペクトルも実施例1−3と同様の条件で得られたものである。すなわち、このスペクトルは、実施例1−3と同様に2032型コイン電池を作製し、0V−1.2Vサイクルを行わずに、60時間充電のみを行い、60時間充電後の負極をNMRロータに詰めてNMR測定をし得られたものである。
図4に示すように、一般的なケイ素単体負極を用いたときの7Li−MAS−NMRから得られるピーク値は約10ppm近辺に発現する。一方、図1に示すように、ケイ素酸化物を含む負極を測定した場合は、ケイ素酸化物のバルク状況に応じて、ピーク値がプラス側に大きくシフトする。これはケイ素原子間距離が広いためだと推測している。このピーク値を得た後、このピークがLi挿入、脱離を繰り返す(0V−1.2Vサイクルを繰り返す)中で0ppmに近い方向へ徐々にシフトすることによって、安定したバルク状況を作ることができる。
図1に示す0〜3ppmの範囲のピークは、ケイ素酸化物の酸素側とLiとの反応を示しており、Liシリケート層の存在を表しているものと推測される。このピークが得られる負極活物質は、充放電により負極活物質粒子の内部に安定したLi化合物が生成しやすい。従って、このピークが得られる負極活物質は、ケイ素酸化物のバルク内において容易にLiが拡散するものとなる。従って、このピークが得られる負極活物質は、安定した電池材料となり、サイクル特性を向上させることができる。なお、図1における0ppm付近のシャープなピークはLiPF6の存在を表しているものであり、本質ではない。一方で、比較例1−4に示すように、0〜3ppmの範囲のピークが得られない負極活物質は、Li挿入、脱離を繰り返しても十分なシリケート層が得られないものである。このような負極活物質は、バルク内に肥大化したSiO2が存在し、Liを吸蔵し辛くなっていると考えられる。従って、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、サイクル特性が低下することとなる。
また、実施例1−1〜実施例1−6及び実施例1−8〜実施例1−10のように、25〜55ppmの範囲のピークは、Xが49回以内で発現することが好ましい。このような負極活物質であれば、この負極活物質をリチウムイオン二次電池の負極活物質として用いた際に、当該二次電池が安定化するまでの時間(サイクル数)をより少なくすることができる。これにより、充放電サイクル初期のサイクル劣化率がより小さくなり、サイクル特性がより向上する。このような負極活物質を有する二次電池は、安定したサイクル特性を有する。
また、上記の通り、Li−Si結合を示すと考えられるピークが大きくプラス側にシフトした状態に対して、充放電を繰り返し、このピークがより0に近づくことでケイ素酸化物のバルク内を安定化できるため、実施例1−1〜実施例1−6、実施例1−8及び実施例1−9のように、0V−1.2Vサイクルを49回以内繰り返す中で一度発現したLi−Si結合を示すピーク(25〜55ppmの範囲のピーク)は減少することが望ましい。特にこのピークは消失(消滅)することが好ましい。このように、「50回以内に発現及び減少」することで、ケイ素酸化物のバルクは、充放電サイクルのより初期に安定する。
例えば、このピークの発現サイクルが同じ(40サイクル目)である実施例1−5と実施例1−10を比較すると、このピークが50回以内に発現した後、50回より多くのサイクル(具体的には70回)で減少する実施例1−10よりも、「50回以内に発現及び減少」する実施例1−5の方が、サイクル初期における電池維持率低下が抑制され、サイクル特性がより向上する。従って、総合的に判断した場合、できるだけ早期サイクル時に上記ピークが発現及び減少する材料であることが望ましい。
(実施例2−1〜実施例2−6)
負極活物質粒子のメジアン径を変化させたこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表2に示す。なお、下記表2〜4には上記の実施例1−3の結果も併記してある。
負極活物質粒子のメジアン径を変化させたこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表2に示す。なお、下記表2〜4には上記の実施例1−3の結果も併記してある。
表2に示すように、負極活物質粒子の粒径が0.5μm以上であると、表面積の増加が抑制できるため、電池維持率、初期効率共により良い傾向にあった。また粒径が20μm以下であると充電時に負極活物質が膨張しにくくなり、負極活物質が割れにくくなるため、電池特性を向上させることができることが分かった。
(実施例3−1)
負極集電体に炭素及び硫黄を含有しなかったこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表3に示す。
負極集電体に炭素及び硫黄を含有しなかったこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表3に示す。
表3に示すように、負極集電体に炭素及び硫黄をそれぞれ100質量ppm以下含有させることで、充電時の負極電極の変形を抑制する可能となる。その結果、電池維持率が向上することが分かった。
(実施例4−1〜実施例4−7)
炭素材の厚さを変化させたこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表4に示す。
炭素材の厚さを変化させたこと以外、実施例1−3と同じ条件で二次電池を作製し、サイクル特性及び初回効率を評価した。結果を表4に示す。
炭素材の厚さを変化させ、電池特性を評価した結果、炭素材を堆積していない場合、電池初期効率、維持率共に低下した。炭素材は一部電解液の分解を抑制する効果があると推測される。炭素材の厚みを増すことで電池特性が安定するが、炭素材が厚くなると共に電池容量向上がし辛くなる。約5μm(5000nm)程度の厚みでも電池容量が向上しづらくなる。また炭素材の厚さを約7μm程度とした実験では容量がより発現しなくなった。これらの結果から総合的に判断し、炭素材の厚さは5μm以下が望ましいと考えられる。
なお、本発明は、上記実施形態に限定されるものではない。上記実施形態は、例示であり、本発明の特許請求の範囲に記載された技術的思想と実質的に同一な構成を有し、同様な作用効果を奏するものは、いかなるものであっても本発明の技術的範囲に包含される。
10…負極、 11…負極集電体、 12…負極活物質層、
30…ラミネートフィルム型のリチウムイオン二次電池、 31…巻回電極体、
32…正極リード、 33…負極リード、 34…密着フィルム、
35…外装部材。
30…ラミネートフィルム型のリチウムイオン二次電池、 31…巻回電極体、
32…正極リード、 33…負極リード、 34…密着フィルム、
35…外装部材。
Claims (9)
- 負極活物質粒子を含む負極活物質であって、前記負極活物質粒子は、SiOx(0.5≦x≦1.6)で表されるケイ素化合物を含有し、
前記負極活物質粒子を含む負極活物質を、対極として金属リチウムを有する二次電池の負極に用い、前記二次電池の0V定電流定電圧充電及び1.2V定電流放電のサイクルをX回(X≧0)繰り返した後、さらに前記二次電池の0V定電流定電圧充電(但し、0Vになってから60時間後に充電終止)を行った状態において、前記充電終止後の負極活物質が7Li−MAS−NMRスペクトルから得られる、ケミカルシフト値として25〜55ppmの範囲及び0〜3ppmの範囲にピークを有し、
前記25〜55ppmの範囲のピーク及び前記0〜3ppmの範囲のピークは、前記Xが0回で発現することを特徴とする負極活物質。 - 前記25〜55ppmの範囲のピークは、前記0V定電流定電圧充電及び1.2V定電流放電のサイクルを49回以内繰り返す中で減少することを特徴とする請求項1に記載の負極活物質。
- 前記負極活物質は、X線回折により得られるSi(111)結晶面に起因する回折ピークの半値幅(2θ)が1.2°以上であるとともに、その結晶面に対応する結晶子サイズは7.5nm以下であることを特徴とする請求項1又は請求項2に記載の負極活物質。
- 前記負極活物質粒子のメジアン径は0.5μm以上20μm以下であることを特徴とする請求項1から請求項3のいずれか1項に記載の負極活物質。
- 前記負極活物質粒子は、表層部に炭素材を含むことを特徴とする請求項1から請求項4のいずれか1項に記載の負極活物質。
- 前記炭素材の平均厚さは1nm以上5000nm以下であることを特徴とする請求項5に記載の負極活物質。
- 請求項1から請求項6のいずれか1項に記載の負極活物質を含むことを特徴とする負極電極。
- 前記負極電極は、前記負極活物質を含む負極活物質層と、
負極集電体とを有し、
前記負極活物質層は前記負極集電体上に形成されており、
前記負極集電体は炭素及び硫黄を含むとともに、それらの含有量がいずれも100質量ppm以下であることを特徴とする請求項7に記載の負極電極。 - 負極電極として、請求項7又は請求項8に記載の負極電極を用いたものであることを特徴とするリチウムイオン二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019167717A JP2020009776A (ja) | 2019-09-13 | 2019-09-13 | 負極活物質、負極電極、リチウムイオン二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019167717A JP2020009776A (ja) | 2019-09-13 | 2019-09-13 | 負極活物質、負極電極、リチウムイオン二次電池 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015252006A Division JP6680531B2 (ja) | 2015-12-24 | 2015-12-24 | 負極活物質の製造方法及びリチウムイオン二次電池の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2020009776A true JP2020009776A (ja) | 2020-01-16 |
Family
ID=69152295
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019167717A Pending JP2020009776A (ja) | 2019-09-13 | 2019-09-13 | 負極活物質、負極電極、リチウムイオン二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2020009776A (ja) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012093651A1 (ja) * | 2011-01-07 | 2012-07-12 | 株式会社大阪チタニウムテクノロジーズ | リチウムイオン二次電池負極材用粉末、これを用いたリチウムイオン二次電池負極およびリチウムイオン二次電池 |
| JP2015111547A (ja) * | 2013-10-29 | 2015-06-18 | 信越化学工業株式会社 | 負極活物質、負極活物質の製造方法、並びに、リチウムイオン二次電池 |
-
2019
- 2019-09-13 JP JP2019167717A patent/JP2020009776A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012093651A1 (ja) * | 2011-01-07 | 2012-07-12 | 株式会社大阪チタニウムテクノロジーズ | リチウムイオン二次電池負極材用粉末、これを用いたリチウムイオン二次電池負極およびリチウムイオン二次電池 |
| JP2015111547A (ja) * | 2013-10-29 | 2015-06-18 | 信越化学工業株式会社 | 負極活物質、負極活物質の製造方法、並びに、リチウムイオン二次電池 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6397262B2 (ja) | 非水電解質二次電池 | |
| US10629890B2 (en) | Negative electrode material for non-aqueous electrolyte secondary battery, negative electrode for non-aqueous electrolyte secondary battery, non-aqueous electrolyte secondary battery, and method of producing negative electrode active material particles | |
| JP6474548B2 (ja) | 非水電解質二次電池用負極材及び負極活物質粒子の製造方法 | |
| JP7265668B2 (ja) | リチウムイオン二次電池、モバイル端末、自動車及び電力貯蔵システム | |
| JP6181590B2 (ja) | 非水電解質二次電池用負極及び非水電解質二次電池 | |
| JP6268293B2 (ja) | 非水電解質二次電池用負極材及び負極活物質粒子の製造方法 | |
| TWI691115B (zh) | 非水電解質二次電池用負極活性物質及其製造方法、以及使用該負極活性物質的非水電解質二次電池及非水電解質二次電池用負極材料之製造方法 | |
| WO2016194288A1 (ja) | 非水電解質二次電池用負極活物質、非水電解質二次電池用負極、及び非水電解質二次電池、並びに負極活物質粒子の製造方法 | |
| WO2015118846A1 (ja) | 非水電解質二次電池用負極材、非水電解質二次電池用負極及びその製造方法並びに非水電解質二次電池 | |
| WO2015063979A1 (ja) | 負極活物質、負極活物質の製造方法、並びに、リチウムイオン二次電池 | |
| WO2015118830A1 (ja) | 非水電解質二次電池の負極材用の負極活物質、及び非水電解質二次電池用負極電極、並びに非水電解質二次電池 | |
| JP6719554B2 (ja) | リチウムイオン二次電池用負極活物質、リチウムイオン二次電池用混合負極活物質材料、及びリチウムイオン二次電池用負極活物質の製造方法 | |
| JP6445956B2 (ja) | 負極活物質、混合負極活物質材料、非水電解質二次電池用負極、リチウムイオン二次電池 | |
| JP6564740B2 (ja) | 負極活物質、負極、リチウムイオン二次電池、リチウムイオン二次電池の使用方法、負極活物質の製造方法及びリチウムイオン二次電池の製造方法 | |
| JP2017188319A (ja) | 負極活物質、混合負極活物質材料、及び負極活物質の製造方法 | |
| JP6215804B2 (ja) | 非水電解質二次電池用負極活物質、非水電解質二次電池用負極、及び非水電解質二次電池、並びに負極活物質粒子の製造方法 | |
| WO2017085907A1 (ja) | 負極活物質、負極電極、リチウムイオン二次電池、非水電解質二次電池用負極材の製造方法及びリチウムイオン二次電池の製造方法 | |
| JP2017147058A (ja) | 負極活物質、混合負極活物質材料、非水電解質二次電池用負極、リチウムイオン二次電池、及び負極活物質の製造方法 | |
| JP6680531B2 (ja) | 負極活物質の製造方法及びリチウムイオン二次電池の製造方法 | |
| JP6746526B2 (ja) | 負極活物質、混合負極活物質材料、及び負極活物質の製造方法 | |
| JP6634398B2 (ja) | 負極活物質、混合負極活物質材料、及び負極活物質の製造方法 | |
| JP2020009776A (ja) | 負極活物質、負極電極、リチウムイオン二次電池 | |
| JP6704327B2 (ja) | 負極活物質、負極、リチウムイオン二次電池、負極活物質の製造方法及びリチウムイオン二次電池の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190913 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200909 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201006 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210406 |