JP2017007964A - ロスバスタチンカルシウムの安定性が向上した錠剤 - Google Patents
ロスバスタチンカルシウムの安定性が向上した錠剤 Download PDFInfo
- Publication number
- JP2017007964A JP2017007964A JP2015122950A JP2015122950A JP2017007964A JP 2017007964 A JP2017007964 A JP 2017007964A JP 2015122950 A JP2015122950 A JP 2015122950A JP 2015122950 A JP2015122950 A JP 2015122950A JP 2017007964 A JP2017007964 A JP 2017007964A
- Authority
- JP
- Japan
- Prior art keywords
- tablet
- calcium
- rosuvastatin calcium
- organic acid
- acid salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【課題】
ロスバスタチンカルシウムを含有する錠剤において、カチオンが多価である無機塩の安定化剤を含まずとも、高温高湿度環境下での保存において、原薬が化学的に安定な錠剤を製造する。
【解決手段】
ロスバスタチンカルシウムと有機酸塩を含有する錠剤を、直打法によって製造する。有機酸塩は2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウムより選ばれることが好ましく、有機酸塩は水和物であることが好ましい。
【選択図】図1
ロスバスタチンカルシウムを含有する錠剤において、カチオンが多価である無機塩の安定化剤を含まずとも、高温高湿度環境下での保存において、原薬が化学的に安定な錠剤を製造する。
【解決手段】
ロスバスタチンカルシウムと有機酸塩を含有する錠剤を、直打法によって製造する。有機酸塩は2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウムより選ばれることが好ましく、有機酸塩は水和物であることが好ましい。
【選択図】図1
Description
本発明は、原薬として(E)−7−[4−(4−フルオロフェニル)−6−イソプロピル−2−[メチル(メチルスルホニル)アミノ]ピリミジン−5−イル]−(3R,5S)−3,5−ジヒドロキシヘプト−6−エン酸(一般名:ロスバスタチン)の医薬的に許容し得る塩(特にロスバスタチンカルシウム)を含有する錠剤であり、保存条件下での化学的な安定性が改善された錠剤の製造方法に関するものである。
ロスバスタチンカルシウムは、3−ヒドロキシ−3−メチルグルタリルCoA還元酵素(HMG−CoA還元酵素)の阻害剤として、高脂血症、家族性高コレステロール血症等の治療に用いられている化合物である(非特許文献1参考)。ロスバスタチンカルシウムと同じHMG−CoA還元酵素としては、プラバスタチンナトリウム、フルバスタチンナトリウム、アトルバスタチンカルシウム水和物、ピタバスタチンカルシウムなどがある。
原薬由来の分解物の増加については、ロスバスタチンカルシウムを含むHMG−CoA還元酵素を含有する錠剤について、塩基性化合物又はカチオンが多価である無機塩、金属塩などを含有する錠剤が幾つかの先行技術文献で示されている。特許文献1ではロスバスタチンと多価カチオン塩である第三リン酸カルシウムを含む錠剤が示され、特許文献2ではロスバスタチンカルシウムとアルカリ土類金属塩である塩化カルシウムや塩化マグネシウムを含む錠剤が示され、特許文献3ではHMG−CoA還元酵素であるプラバスタチンナトリウムと塩基性化合物である炭酸ナトリウムやリン酸水素二ナトリウムを含む錠剤が示される。先行技術では、ロスバスタチンカルシウム由来の分解物であるラクトン体(下記式(a))の発生を抑制するために、上記記載の塩基性化合物又はカチオンが多価である無機塩、金属塩を安定化剤として使用していることが述べられている。
医薬品を保存する上での、原薬由来分解物の生成抑制は、安定した品質の医薬品を患者に提供する上で達成すべき重要な課題である。そのため、ロスバスタチンカルシウムを含有する錠剤に含まれる医薬品添加物の処方を考案する上では、ラクトン体の発生を抑制するために、前記の安定化剤を使用することが第一に検討される。しかし、崩壊性の改善、着色防止、匂いの抑制などの課題を解決する上では先行技術の安定化剤を使用することが必ずしも好ましいとは限らない。そこで、本発明者らは、前記の安定化剤を含まずとも、ロスバスタチンカルシウム由来の分解物の発生が抑制された錠剤を製造することを目的として鋭意検討を重ねた。
「クレストール(登録商標)錠2.5mg、クレストール(登録商標)錠5mg」インタビューフォーム、2015年1月(改訂13版)
本発明の課題は、ロスバスタチンカルシウムを含有する錠剤において、カチオンが多価である無機塩の安定化剤を含まずとも、高温高湿度環境下での保存において、原薬の化学的に安定な錠剤を提供することである。
本発明者らは、ロスバスタチンカルシウムを含有する錠剤において、その分解物であるラクトン体の生成が抑制された錠剤を開発するため、汎用の添加剤を用いて製剤処方の検討を開始した。その結果、本発明者らは、意外にも、カチオンが多価である無機塩の安定化剤を使用せずとも、下記の特定の有機酸塩を使用することで、高温高湿度環境下での保存においてラクトン体の生成を有意に抑制させることが可能であることを見出した。さらに、製造方法等の検討も併せて行い、本発明を完成するに至った。
本発明の好ましい態様は、下記(1)〜(4)によって記述される。
(1)ロスバスタチンカルシウムと有機酸塩を含有し、直打法によって製造された錠剤であり、有機酸塩が2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウム二水和物より選ばれる錠剤。
(2)有機酸塩がクエン酸カルシウムである、前記(1)に記載の錠剤。
(3)有機酸塩が水和物である、前記(1)又は(2)に記載の錠剤。
(4)ロスバスタチンカルシウムが無晶形であり、錠剤がフィルムコーティング錠剤である、前記(1)〜(3)のいずれかに記載の錠剤。
(1)ロスバスタチンカルシウムと有機酸塩を含有し、直打法によって製造された錠剤であり、有機酸塩が2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウム二水和物より選ばれる錠剤。
(2)有機酸塩がクエン酸カルシウムである、前記(1)に記載の錠剤。
(3)有機酸塩が水和物である、前記(1)又は(2)に記載の錠剤。
(4)ロスバスタチンカルシウムが無晶形であり、錠剤がフィルムコーティング錠剤である、前記(1)〜(3)のいずれかに記載の錠剤。
本発明によれば、ロスバスタチンカルシウムを含有する錠剤に特定の有機酸塩を含ませる事で、高温高湿度環境下での保存において、原薬が化学的に安定な錠剤を医療現場に提供できる。
以下で本発明のロスバスタチンカルシウムを含有する錠剤の処方及び製造方法を詳細に説明する。但し、以下の記載は本発明を説明するための例示であり、本発明をこの記載範囲にのみ限定する趣旨ではない。
本発明において使用されるロスバスタチンカルシウムの平均粒子径(光散乱法による測定値)は10.0μm以下のものが好ましく、より好ましくは1.0〜5.0μmである。必要に応じて適宜乾式又は湿式粉砕を行い、任意の粒子径に調整することも可能である。ロスバスタチンカルシウムは、錠剤全重量に対して1.0〜5.0%の範囲で含有されていることが望ましい。また、ロスバスタチンカルシウムは無晶形であることが好ましい。
本発明の錠剤の製造に用いられる、医薬的に許容可能な添加剤としては、通常使用されている賦形剤、崩壊剤、滑択剤、流動化剤、遮光剤等が使用できる。なお、本発明における賦形剤、崩壊剤、滑沢剤、流動化剤、遮光剤とは「医薬品添加物辞典(日本医薬品添加剤協会編集、薬事日報社、2007年発行)」の「用途別索引」で当該名に分類されたものを指す。以下で本発明で用いられる具体的な添加物名称が列挙されるが、本発明で使用可能な医薬的に許容可能な添加剤はそれらに限定されない。
使用可能な賦形剤としては、トウモロコシ澱粉、バレイショ澱粉、D−マンニトール、エリスリトール、キシリトール、ソルビトール、イソマルト、マルチトール、白糖、ショ糖、ブドウ糖、アルファー化デンプン、ヒドロキシプロピルセルロース、ヒプロメロース、メチルセルロース、低置換度ヒドロキシプロピルセルロース、ポリビニルアルコール、ポビドン、エチルセルロース、乳糖水和物、結晶セルロース等を挙げる事ができる。錠剤全重量に対して賦形剤は、好ましくは60.0〜90.0%の範囲で含まれ、より好ましくは80.0〜90.0%の範囲で含まれる。
使用可能な崩壊剤としては、低置換度ヒドロキシプロピルセルロース、カルメロース、カルメロースカルシウム、カルメロースナトリウム、カルボキシメチルスターチナトリウム、クロスポビドン、カンテン末等を挙げる事ができ、好ましくはクロスポビドンである。錠剤全重量に対して崩壊剤は1.0〜10.0%の範囲で含まれることが好ましく、より好ましくは4.0〜6.0%である。
使用可能な滑択剤としては、軽質無水ケイ酸、ステアリン酸マグネシウム、ステアリン酸カルシウム、フマル酸ステアリルナトリウム、タルク、硬化油等を挙げる事ができ、好ましくはステアリン酸マグネシウム又はフマル酸ステアリルナトリウムであり、最も好ましくはステアリン酸マグネシウムである。錠剤全重量に対して滑択剤は0.5〜3.0%の範囲で含まれることが好ましい。
また本発明の錠剤は、光に対する安定性を向上させるなどの目的に応じて素錠表面にフィルム層を形成してフィルムコーティング錠剤とすることが可能である。フィルムコーティング層に含まれる遮光剤としては、酸化チタン、タルク、黄色三二酸化鉄、三二酸化鉄等を挙げる事ができる。
本発明の錠剤において含まれる、ロスバスタチンカルシウムの安定化剤としての有機酸塩には、2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウム二水和物等が挙げられ、好ましくはクエン酸カルシウムである。錠剤全重量に対して有機酸塩は好ましくは1.0〜30.0%の範囲で含まれ、より好ましくは5.0〜20.0%の範囲で含まれ、最も好ましくは5.0〜10.0%の範囲で含まれる。また、本発明に係る有機酸塩は水和物であることが好ましい。
本発明の錠剤の製造方法としては、湿製法、圧縮打錠法(直打法、セミ直打法、顆粒圧縮法)が挙げられるが、好ましくは直打法である。直打法では通常行われる操作、すなわち原薬と一部の製剤添加物を均一に混合後、さらに滑択剤などの製剤添加物を加えて均一に混合させた打錠用混合物を回転式打錠機に供給及び打錠して成形することによって、本発明の錠剤が製造される。本発明で得られる錠剤の形状は特に限定されず、円形錠、円形R錠、円形隅角錠、円形2段R錠や異形錠等のいずれの形状でもよいが、フィルムコーティングを施す場合は、R錠等が好ましい。
フィルムコーティングの方法については、特に限定されないが、商業的に製造する場合はフィルムコーティング機を用いたコーティング法が用いられる。得られた素錠をフィルムコーティング機に仕込み、フィルム成分を水に懸濁してこれをスプレーすれば、本発明のフィルムコーティング錠が得られる。
以下、実施例、比較例及び試験例を挙げて本発明を説明する。実施例、比較例で使用されるロスバスタチンカルシウムの形態は無晶形である。
<各有機酸塩とロスバスタチンカルシウムの混合物>
ロスバスタチンカルシウム1.0gを各有機酸塩(2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム一水和物、グルコン酸カルシウム四水和物、クエン酸カルシウム四水和物、安息香酸ナトリウム、クエン酸三ナトリウム二水和物のいずれか一つ)1.0gとポリエチレン製の袋に投入・混合して、各混合物2.0gを得た。
[成 分] [混合物中の重量(g)]
ロスバスタチンカルシウム 1.0
各有機酸塩 1.0
ロスバスタチンカルシウム1.0gを各有機酸塩(2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム一水和物、グルコン酸カルシウム四水和物、クエン酸カルシウム四水和物、安息香酸ナトリウム、クエン酸三ナトリウム二水和物のいずれか一つ)1.0gとポリエチレン製の袋に投入・混合して、各混合物2.0gを得た。
[成 分] [混合物中の重量(g)]
ロスバスタチンカルシウム 1.0
各有機酸塩 1.0
<有機酸塩含有ロスバスタチンカルシウム錠剤>
ロスバスタチンカルシウム2.6g、クロスポビドン3.75g、微結晶セルロース15.5g、クエン酸カルシウム四水和物5.66g、乳糖水和物46.5g、ステアリン酸マグネシウム0.94gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
さらに、その素錠をコーティング機(DRC−200、パウレック社製)に投入し、これに、予めヒプロメロース1.6g、トリアセチン0.2g、酸化チタン0.2gを精製水に加え、均一分散させた液を噴霧し、乾燥してフィルムコーティング錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.6
クエン酸カルシウム四水和物 5.66
乳糖水和物 46.5
微結晶セルロース 15.5
クロスポピドン 3.75
ステアリン酸マグネシウム 0.94
<フィルムコーティング層>
ヒプロメロース 1.6
トリアセチン 0.2
酸化チタン 0.2
ロスバスタチンカルシウム2.6g、クロスポビドン3.75g、微結晶セルロース15.5g、クエン酸カルシウム四水和物5.66g、乳糖水和物46.5g、ステアリン酸マグネシウム0.94gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
さらに、その素錠をコーティング機(DRC−200、パウレック社製)に投入し、これに、予めヒプロメロース1.6g、トリアセチン0.2g、酸化チタン0.2gを精製水に加え、均一分散させた液を噴霧し、乾燥してフィルムコーティング錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.6
クエン酸カルシウム四水和物 5.66
乳糖水和物 46.5
微結晶セルロース 15.5
クロスポピドン 3.75
ステアリン酸マグネシウム 0.94
<フィルムコーティング層>
ヒプロメロース 1.6
トリアセチン 0.2
酸化チタン 0.2
<直打法による製造方法>
ロスバスタチンカルシウム2.7g、各添加剤(三塩基性リン酸カルシウム、クエン酸カルシウム四水和物、乳糖水和物のいずれか一つ)5.7g、乳糖水和物46.3g、結晶セルロース15.5g、クロスポビドン3.8g、ステアリン酸マグネシウム1.0gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.7
各添加剤 5.7
乳糖水和物 46.3
結晶セルロース 15.5
クロスポピドン 3.8
ステアリン酸マグネシウム 1.0
ロスバスタチンカルシウム2.7g、各添加剤(三塩基性リン酸カルシウム、クエン酸カルシウム四水和物、乳糖水和物のいずれか一つ)5.7g、乳糖水和物46.3g、結晶セルロース15.5g、クロスポビドン3.8g、ステアリン酸マグネシウム1.0gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.7
各添加剤 5.7
乳糖水和物 46.3
結晶セルロース 15.5
クロスポピドン 3.8
ステアリン酸マグネシウム 1.0
<比較例1>
<各添加剤とロスバスタチンカルシウムの混合物>
ロスバスタチンカルシウム1.0gを各添加剤(リン酸水素カルシウム水和物、三塩基性リン酸カルシウム、三塩基性リン酸カルシウムβ型、アルギン酸ナトリウム、イソアスコルビン酸ナトリウム、メグルミン、L−アルギニンのいずれか一つ)1.0gとポリエチレン製の袋に投入・混合して、各混合物2.0gを得た。
[成 分] [混合物中の重量(g)]
ロスバスタチンカルシウム 1.0
各添加剤 1.0
<各添加剤とロスバスタチンカルシウムの混合物>
ロスバスタチンカルシウム1.0gを各添加剤(リン酸水素カルシウム水和物、三塩基性リン酸カルシウム、三塩基性リン酸カルシウムβ型、アルギン酸ナトリウム、イソアスコルビン酸ナトリウム、メグルミン、L−アルギニンのいずれか一つ)1.0gとポリエチレン製の袋に投入・混合して、各混合物2.0gを得た。
[成 分] [混合物中の重量(g)]
ロスバスタチンカルシウム 1.0
各添加剤 1.0
<比較例2>
<各添加剤含有ロスバスタチンカルシウム錠剤>
ロスバスタチンカルシウム2.6g、クロスポビドン3.75g、微結晶セルロース15.5g、各添加剤(三塩基性リン酸カルシウム、三塩基性リン酸カルシウムβ型、二塩基性リン酸カルシウム、L−アルギニン、乳糖水和物のいずれか一つ)5.66g、乳糖水和物46.5g、ステアリン酸マグネシウム0.94gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
さらに、その素錠をコーティング機(DRC−200、パウレック社製)に投入し、これに、予めヒプロメロース1.6g、トリアセチン0.2g、酸化チタン0.2gを精製水に加え、均一分散させた液を噴霧し、乾燥してフィルムコーティング錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.6
各添加剤 5.66
乳糖水和物 46.5
微結晶セルロース 15.5
クロスポピドン 3.75
ステアリン酸マグネシウム 0.94
<フィルムコーティング層>
ヒプロメロース 1.6
トリアセチン 0.2
酸化チタン 0.2
<各添加剤含有ロスバスタチンカルシウム錠剤>
ロスバスタチンカルシウム2.6g、クロスポビドン3.75g、微結晶セルロース15.5g、各添加剤(三塩基性リン酸カルシウム、三塩基性リン酸カルシウムβ型、二塩基性リン酸カルシウム、L−アルギニン、乳糖水和物のいずれか一つ)5.66g、乳糖水和物46.5g、ステアリン酸マグネシウム0.94gをポリエチレン製の袋に投入し、混合した。次いで、この混合物を、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
さらに、その素錠をコーティング機(DRC−200、パウレック社製)に投入し、これに、予めヒプロメロース1.6g、トリアセチン0.2g、酸化チタン0.2gを精製水に加え、均一分散させた液を噴霧し、乾燥してフィルムコーティング錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.6
各添加剤 5.66
乳糖水和物 46.5
微結晶セルロース 15.5
クロスポピドン 3.75
ステアリン酸マグネシウム 0.94
<フィルムコーティング層>
ヒプロメロース 1.6
トリアセチン 0.2
酸化チタン 0.2
<比較例3>
<攪拌造粒法による製造方法>
攪拌造粒機(VG−01型、パウレック社製)に、ロスバスタチンカルシウム2.7g、各添加剤(三塩基性リン酸カルシウム、クエン酸カルシウム四水和物、乳糖水和物のいずれか一つ)5.7g、乳糖水和物44.3g、結晶セルロース15.5g、クロスポビドン3.8gを投入し、これに、予めヒプロメロース2.0gを精製水に加え、均一分散させた液を加え、攪拌造粒した。得られた造粒物は流動層造粒機で乾燥させた後、ステアリン酸マグネシウム1.0gと混合して、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.7
各添加剤 5.7
乳糖水和物 44.3
ヒプロメロース 2.0
結晶セルロース 15.5
クロスポピドン 3.8
ステアリン酸マグネシウム 1.0
<攪拌造粒法による製造方法>
攪拌造粒機(VG−01型、パウレック社製)に、ロスバスタチンカルシウム2.7g、各添加剤(三塩基性リン酸カルシウム、クエン酸カルシウム四水和物、乳糖水和物のいずれか一つ)5.7g、乳糖水和物44.3g、結晶セルロース15.5g、クロスポビドン3.8gを投入し、これに、予めヒプロメロース2.0gを精製水に加え、均一分散させた液を加え、攪拌造粒した。得られた造粒物は流動層造粒機で乾燥させた後、ステアリン酸マグネシウム1.0gと混合して、ロータリー式打錠機(菊水製作所:VELA5−M型)を用いて圧縮成形し、下記組成の素錠を得た。
[成 分] [1錠当たりの重量(mg)]
<素錠>
ロスバスタチンカルシウム 2.7
各添加剤 5.7
乳糖水和物 44.3
ヒプロメロース 2.0
結晶セルロース 15.5
クロスポピドン 3.8
ステアリン酸マグネシウム 1.0
〔試験例1〕最適安定化剤の検討
実施例1並びに比較例1の各混合物2.0g、及び原薬1.0gについて、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した後にラクトン体及び5−ケト誘導体(ロスバスタチン由来分解生成物)の生成量をHPLC法で測定した結果を図1に示した。
図1の結果より、実施例1で使用された各有機酸塩は、ロスバスタチンカルシウム由来の分解生成物の発生を誘導する効果が十分に低いことから、ロスバスタチンカルシウムの安定化剤となり得ることが示唆された。
実施例1並びに比較例1の各混合物2.0g、及び原薬1.0gについて、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した後にラクトン体及び5−ケト誘導体(ロスバスタチン由来分解生成物)の生成量をHPLC法で測定した結果を図1に示した。
図1の結果より、実施例1で使用された各有機酸塩は、ロスバスタチンカルシウム由来の分解生成物の発生を誘導する効果が十分に低いことから、ロスバスタチンカルシウムの安定化剤となり得ることが示唆された。
〔試験例2〕有機酸塩の安定化作用
実施例2並びに比較例2の各錠剤について、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した前後にラクトン体の生成量をHPLC法で測定した結果を図2に示した。
図2の結果より、有機酸塩(クエン酸カルシウム四水和物)は安定化剤として機能することが示唆された。
実施例2並びに比較例2の各錠剤について、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した前後にラクトン体の生成量をHPLC法で測定した結果を図2に示した。
図2の結果より、有機酸塩(クエン酸カルシウム四水和物)は安定化剤として機能することが示唆された。
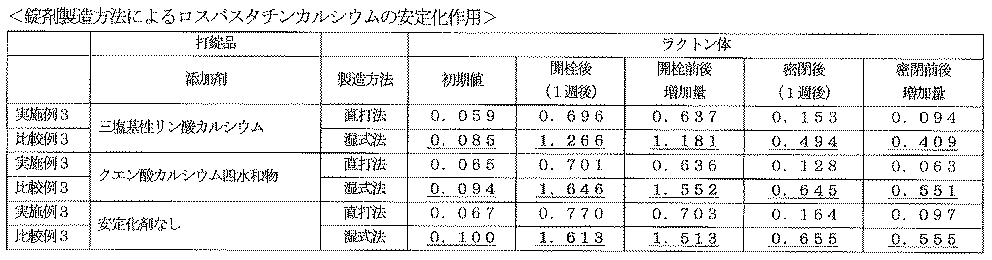
〔試験例3〕製造方法の安定化作用
実施例3並びに比較例3の錠剤について、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した前後にラクトン体の生成量をHPLC法で測定した結果を図3に示した。
図3の結果より、製造方法が直打法である方が、ロスバスタチンカルシウムの安定化に大きく寄与することが示唆された。
実施例3並びに比較例3の錠剤について、ガラス瓶に入れ、開栓及び密栓の状態で60度75%相対湿度条件下で1週間、保存した前後にラクトン体の生成量をHPLC法で測定した結果を図3に示した。
図3の結果より、製造方法が直打法である方が、ロスバスタチンカルシウムの安定化に大きく寄与することが示唆された。
以下に上記試験例1〜3で行った試験方法及び試験条件についての詳細な補足説明を記載する。
(補足1)分解生成物含量の測定方法
高湿度条件下での保存(ナガノサイエンス株式会社製:恒温恒湿槽LH21−11M、60℃75%RH、無包装状態にて1週間)前後、HPLCを用いて分解生成物の含量を測定した条件を以下に示す。
「HPLC測定条件」
検出器:フォトダイオードアレイ検出器
測定波長:242nm
カラム:CERi化学物質評価研究機構 L−column ODS(4.6×150、3μm)
カラム温度:50℃
移動相A:pH3.0の0.02mol/Lリン酸塩緩衝液/アセトニトリル混液(700:300)
移動相B:アセトニトリル/pH3.0の0.02mol/Lリン酸塩緩衝液混液(750:250)
グラジエント条件:以下の表1に示す通りに設定した。移動相組成は容量%で記載した。
分析時間:30分
流量:1.5mL/分
試料注入量:10μL
試料溶液の調整:ロスバスタチン2.5mg相当のロスバスタチンカルシウム錠を精製水・アセトニトリル混液(精製水75:アセトニトリル25)を用いて5mLとする。
本発明における加湿条件にて生成されるラクトン体は、上記手法による分解生成物の解析において、ロスバスタチンのピークの保持時間に対して、相対保持時間1.72に出現するピークである。なお、ラクトン体の含量はラクトン体のピーク面積をロスバスタチンのピーク面積で除して100をかけた数値とする。
高湿度条件下での保存(ナガノサイエンス株式会社製:恒温恒湿槽LH21−11M、60℃75%RH、無包装状態にて1週間)前後、HPLCを用いて分解生成物の含量を測定した条件を以下に示す。
「HPLC測定条件」
検出器:フォトダイオードアレイ検出器
測定波長:242nm
カラム:CERi化学物質評価研究機構 L−column ODS(4.6×150、3μm)
カラム温度:50℃
移動相A:pH3.0の0.02mol/Lリン酸塩緩衝液/アセトニトリル混液(700:300)
移動相B:アセトニトリル/pH3.0の0.02mol/Lリン酸塩緩衝液混液(750:250)
グラジエント条件:以下の表1に示す通りに設定した。移動相組成は容量%で記載した。
流量:1.5mL/分
試料注入量:10μL
試料溶液の調整:ロスバスタチン2.5mg相当のロスバスタチンカルシウム錠を精製水・アセトニトリル混液(精製水75:アセトニトリル25)を用いて5mLとする。
本発明における加湿条件にて生成されるラクトン体は、上記手法による分解生成物の解析において、ロスバスタチンのピークの保持時間に対して、相対保持時間1.72に出現するピークである。なお、ラクトン体の含量はラクトン体のピーク面積をロスバスタチンのピーク面積で除して100をかけた数値とする。
本発明によれば、ロスバスタチンカルシウムを含有する錠剤において、カチオンが多価である無機塩の安定化剤を含まずとも、高温高湿度環境下での保存において、原薬が化学的に安定な錠剤を医療現場に提供できる。
Claims (4)
- ロスバスタチンカルシウムと有機酸塩を含有し、直打法によって製造された錠剤であり、有機酸塩が2,4−ヘキサジエン酸カリウム、デヒドロ酢酸ナトリウム、グルコン酸カルシウム、クエン酸カルシウム、安息香酸ナトリウム、クエン酸三ナトリウムより選ばれる錠剤。
- 有機酸塩がクエン酸カルシウムである、請求項1に記載の錠剤。
- 有機酸塩が水和物である、請求項1又は2に記載の錠剤。
- ロスバスタチンカルシウムが無晶形であり、錠剤がフィルムコーティング錠剤である、請求項1〜3のいずれかに記載の錠剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015122950A JP2017007964A (ja) | 2015-06-18 | 2015-06-18 | ロスバスタチンカルシウムの安定性が向上した錠剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015122950A JP2017007964A (ja) | 2015-06-18 | 2015-06-18 | ロスバスタチンカルシウムの安定性が向上した錠剤 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017007964A true JP2017007964A (ja) | 2017-01-12 |
Family
ID=57761289
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015122950A Pending JP2017007964A (ja) | 2015-06-18 | 2015-06-18 | ロスバスタチンカルシウムの安定性が向上した錠剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017007964A (ja) |
-
2015
- 2015-06-18 JP JP2015122950A patent/JP2017007964A/ja active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2863018C (en) | A tablet comprising .alpha.,.alpha.,.alpha.-trifluorothymidine and 5-chloro-6-(2-iminopyrrolidine-1-yl)methyl-2,4(1h,3h)-pyrimidine dione hydrochloride | |
| US9399064B2 (en) | Pitavastatin-containing preparation and method for producing same | |
| WO2019146642A1 (ja) | γ-アミノ酪酸誘導体含有錠剤の化学的安定性を改善する方法 | |
| MX2014009833A (es) | Composicion farmaceutica de administracion oral. | |
| KR102517765B1 (ko) | 로수바스타틴 및 에제티미브를 포함하는 제약 조성물 및 그의 제조 방법 | |
| JP2015178482A (ja) | ロスバスタチン含有医薬製剤 | |
| JP2020059742A (ja) | ロスバスタチンカルシウムを含有する錠剤 | |
| JP6320260B2 (ja) | 医薬組成物 | |
| JP2010189443A (ja) | 揮散防止型固形製剤およびその製造方法 | |
| JP5248733B2 (ja) | 揮散防止型固形製剤およびその製造方法 | |
| JP2016155777A (ja) | モンテルカスト又はその塩を含む組成物 | |
| JP2015098467A (ja) | 安定性が改善された製剤 | |
| JP2017007964A (ja) | ロスバスタチンカルシウムの安定性が向上した錠剤 | |
| JP6433400B2 (ja) | HMG−CoAレダクターゼ阻害薬を含有する医薬製剤 | |
| JP2017014151A (ja) | 光安定性を向上した、シロドシンを含有する有核錠 | |
| JP6199922B2 (ja) | 化学的な安定性が向上したイルベサルタン含有錠剤 | |
| JP6095176B2 (ja) | ロスバスタチンカルシウムの光安定性が向上したフィルムコーティング錠剤 | |
| JP5065519B1 (ja) | 結晶性アトルバスタチンカルシウム含有錠剤の製造方法 | |
| RU2547574C2 (ru) | Лекарственная форма гиполипидемического действия и способ ее изготовления | |
| JP2021116283A (ja) | エゼチミブおよびアトルバスタチン含有錠剤 | |
| JP2013253026A (ja) | アンジオテンシンii受容体拮抗薬およびサイアザイド系利尿薬を含む医薬組成物 | |
| RO129060B1 (ro) | Compoziţie farmaceutică stabilă cu rosuvastatină calcică amorfă | |
| JP2016183150A (ja) | 医薬組成物 | |
| WO2009091346A2 (en) | Stable pharmaceutical formulation and preparation methods | |
| JP2018027987A (ja) | 医薬組成物 |