JP2016512201A - 急性腎障害の治療方法 - Google Patents
急性腎障害の治療方法 Download PDFInfo
- Publication number
- JP2016512201A JP2016512201A JP2015561753A JP2015561753A JP2016512201A JP 2016512201 A JP2016512201 A JP 2016512201A JP 2015561753 A JP2015561753 A JP 2015561753A JP 2015561753 A JP2015561753 A JP 2015561753A JP 2016512201 A JP2016512201 A JP 2016512201A
- Authority
- JP
- Japan
- Prior art keywords
- injury
- induced
- subject
- ischemia
- renal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/4025—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil not condensed and containing further heterocyclic rings, e.g. cromakalim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/34—Genitourinary disorders
- G01N2800/347—Renal failures; Glomerular diseases; Tubulointerstitial diseases, e.g. nephritic syndrome, glomerulonephritis; Renovascular diseases, e.g. renal artery occlusion, nephropathy
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/70—Mechanisms involved in disease identification
- G01N2800/7019—Ischaemia
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/70—Mechanisms involved in disease identification
- G01N2800/7038—Hypoxia
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Urology & Nephrology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pathology (AREA)
- Zoology (AREA)
- Hematology (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Wood Science & Technology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
被験者における急性腎障害、特に虚血誘発性腎障害及び/または低酸素誘発性腎障害を治療するための方法を提供する。この方法は、被験者に対してETA受容体アンタゴニスト、例えばアトラセンタンまたはその医薬として許容され得る塩を投与することを含む。腎障害を診断し、治療する方法も提供する。腎機能及び/または腎質量または容積の減少の抑制または予防方法、及び慢性腎臓病への進行を遅延させる方法をも提供する。
Description
本発明は急性腎障害の治療または予防方法に関する。
最近の研究は急性腎障害(AKI)に起因する入院の増加を報告している(Waiker SSら,Declining mortality in patients with acute renal failure,1988 to 2002,J.Am.Soc.Nephrol.,17:1143−1150,2006;Xue JLら,Incidence and mortality of acute renal failure in Medicare beneficiaries,1992 to 2001,J.Am.Soc.Nephrol.,1135−1142,2006)。これらの患者では罹患率及び死亡率が高く、有効な治療に対する緊急の要望がある。
急性腎障害は、腎臓の片方または両方が1つ以上の各種原因で傷つけられたときに起こり、血液からの老廃物の濾過のような腎機能が急速に低下する恐れがある。AKIの原因には、(1)腎毒性物質への露出、(2)外傷、火傷、膵炎、敗血症または感染に起因する全身炎症反応症候群、(3)末梢動脈閉塞性疾患、閉塞性動脈硬化症、低心拍出量、分布容積または変化した血管抵抗を含めた低血液量をもたらす生理的状態、(4)外傷性横紋筋融解症、(5)炎症性サイトカイン血症の持続または悪化、(6)尿路の閉塞、及び(7)急性腎障害の他の本質的な腎臓原因が含まれるが、これらに限定されない。被験者をAKIのリスクに曝す他の疾患及び状態には、腎臓移植術(ドナーまたはレシピエントとして)、両側動脈閉塞、両側急性腎静脈血栓症、急性尿酸腎症、血液量減少、心血管虚脱、急性両側上管閉塞、高カルシウム血性腎症、溶血性尿毒症症候群、急性尿閉、悪性腎硬化症、本態性混合型クリオ免疫グロブリン血症、オキサレート腎症、皮質壊死、出産後糸球体硬化症、過敏性腎症、強皮症、特発性急速進行性糸球体腎炎、グッドパスチャー症候群、非グッドパスチャー抗GBM疾患、急性細菌性心内膜炎または内臓敗血症、顕微鏡的結節性多発動脈炎、ウェゲナー肉芽腫症、アレルギー性肉芽腫症、急性放射線性腎炎、溶連菌感染後糸球体腎炎、非溶連菌感染後糸球体腎炎、びまん性増殖性ループス腎炎、膜増殖性糸球体腎炎、腎静脈血栓症、ワルデンストレームマクログロブリン血症、多発性骨髄腫、ベルジェ(IgA)腎症、ヘノッホ・シェーンライン紫斑病及び巣状糸球体硬化症が含まれる。AKIの結果は、最終的に代謝性アシドーシス、高カリウム血症、尿毒症、血液量減少、浮腫及び死を含めた多数の合併症を引き起こし得る老廃物が血流中に蓄積し始めることである。
AKIの病因は多様であるので、AKIの標準薬物治療は存在していない。AKIを患っている患者に直面したとき、医師は疾患を流体モジュレーションで管理し、腎臓損傷を最小限とすべく根底の原因を治療するように試みている。急性腎障害を治療するために無数の各種タイプの化合物が研究されたが、成功は限られている。提案されているAKIの治療には、利尿剤、カスパーゼ阻害剤、ミノサイクリン、グアノシン、ピフィスリン−α、PARP阻害剤、スフィンゴシン−1リン酸アナログ、アデノシン2Aアゴニスト、α−MSH、IL−10、フィブレート、PPAR−γアゴニスト、活性化Cタンパク質、iNOSインヒビター、インスリン、ピルビン酸エチル、組換えEPO、肝細胞増殖因子、一酸化炭素放出化合物、及びビリルビン、フェノルドパム及び心房性ナトリウム利尿ペプチドが含まれる。
幾つかの治療は前臨床的に有望であったが、臨床現場で研究したとき一部AKIの予防のための治療域が狭そうであり、遅れた治療は無効でありそうなので、失敗した(Jo SKら,Pharmacologic Treatment of Acute Kidney Injury:Why Drugs Haven’t Worked and What is on the Horizon,Clin.J.Am.Soc.Nephrol.,2:356−365,2007)。例えば、組換えヒトIGF−1(Miller SBら,Insulin−like growth factor I accelerates recovery from ischemic acute tubular necrosis in the rat,Proc.Natl.Acad.Sci.USA,89:11876−11880,1992)、及び心房性ナトリウム利尿ペプチド(Allgren RLら,Anaritide in acute tubular necrosis,Auriculin Anaritide Acute Renal Failure Study Group,N.Engl.J.Med.,336:828−834,1997;及びLewis Jら,Atrial natriuretic factor in oliguric acture renal failure,Auriculin Anaritide Acute Renal Failure Study Group,Am.J.Kidney Dis.,36:767−774,2000)はいずれもヒト治験で失敗した。
AKIは、幾つかの臨床検査パラメーター(例えば、血清クレアチニン(SCr)、糸球体濾過量(GFR)、血液尿素窒素(BUN)、炎症のマーカー)を調べることにより臨床的に診断され、評価され得る。AKIから生ずる腎障害は更に、腎障害分子1(KIM−1)、ヒト好中球ゼラチナーゼ関連リポカイン(NGAL)、インターロイキンn−18(IL−18)、シスタチンC、クルステリン、脂肪酸結合タンパク質及びオステオポンチンを含めた幾つかのバイオマーカーを用いて評価され得る(Cruz DNら,Neutrophil gelatinase−associated lipocalin as a biomarker of cardiovascular disease:a systematic review,Clin.Chem.Lab.Med.,50:1533−1545,2012)。
増大する数の臨床文献は、急性腎障害により慢性腎臓病が発症し始めるおそれがあることを示している(Ishani Aら,Acute kidney injury increases risk of ESRD among elderly,J.Am.Soc.Nephrol.,20:223−228,2009;Xue JLら,Incidence and mortality of acute renal failure in Medicare beneficiaries,1992 to 2001,J.Am.Soc.Nephrol.,17:1135−1142,2006;Waikar SSら,Declining mortality in patients with acute renal failure,1988 to 2002,J.Am.Soc.Nephrol.,17:1143−50,2006;Liangos Oら,,Epidemiology and outcomes of acute renal failure in hospitalized patients:a national survey,Clin.J.Am.Soc.Nephrol.,1:43−51,2006;Wald Rら,Chronic dialysis and death among survivors of acute kidney injury requiring dialysis JAMA,302:1179−85,2009;Goldberg Aら,The impact of transient and persistent acute kidney injury on long−term outcomes after acute myocardial infarction,Kidney Int.,76:900−910,2009)。例えば、最近の研究は、AKIのために透析を必要としている患者で慢性腎臓病(CKD)を発病するリスクが〜28倍高かったことを報告している(Lo LJら,Dialysis−requiring acute renal failure increases the risk of progressive chronic kidney disease,Kidney Int.,76:893−9,2009)。しかしながら、AKIがCKDの発症を開始するメカニズムは明確に確認されていない。
1つの卓越した理論によると、最初の虚血発作が尿細管周囲の微小血管損傷を引き起こし、これにより腎血流が少なくなり得る。これは、低酸素状態のために進行中の組織損傷を伴う持続的腎虚血になる可能性がある(Basile DPら,Impaired endothelial proliferation and mesenchymal transition contribute to vascular rarefaction following acute kidney injury,Am.J.Physiol.,300:F721−733,2011;Leonard ECら,VEGF−121 preserves renal microvessel structure and ameliorates secondary renal disease following acute kidney injury,Am.J.Physiol.,295:F1648−1657,2008)。十分な酸素化のために血流が不十分な場合には虚血が生じ、その結果最も重篤な形の低酸素症として組織低酸素症(少ない酸素)または無酸素症(酸素の不在)、最終的には組織壊死とそれ程ではないがアポトーシスが生じる。虚血により常に低酸素症が生じる。しかしながら、例えば貧血で生ずるように動脈血液の酸素含量が低下すると、低酸素症は虚血なしでも起こり得る。従って、虚血誘発性腎障害のモデルにおいて有効な治療は低酸素誘発性腎障害のモデルにおいても有効であろう。なぜならば、両モデルは必須栄養素を組織から奪うことにより、内皮機能不全、酸化ストレス及び炎症を引き起こすことにより組織損傷を引き起こすからである。
虚血から生ずる急性腎障害のメカニズムを規定する際の困難に寄与する因子の1つは、虚血性AKIの最も一般的に使用されているモデルの両側腎動脈閉塞(RAO)が進行性腎臓損傷を確実に生じないという事実である。むしろ、RAOが所謂“治癒欠陥”(例えば、持続性血管/微細血管損傷;塩感受性高血圧)を生ずるという事実があるにもかかわらず、GFRの持続性または進行性低下が生じなかった(例えば、Pechman KRら,Recovery from renal ischemia−reperfusion injury is associated with altered renal hemodynamics,blunted pressure natriuresis,and sodium−sensitive hypertension,Am.J.Physiol.,297:R1358−R1363,2009;Spurgeon−Pechman KRら,Recovery from acute renal failure predisposes hypertension and secondary renal disease in response to elevated sodium,Am.J.Physiol.,293:F269−F278,2007;Finn WFら,Recovery from postischemic acute renal failure in the rat,Kidney Int.,16:113−123,1979;Finn WFら,Attenuation of injury due to unilateral renal ischemia:delayed effects of contralateral nephrectomy,J.Lab.Clin.Med.,103:193−203,1984を参照されたい)。
最近、マウスの(両側ではなく)片側虚血性損傷の新しいモデルが進行中の尿細管壊死、間質性炎症、尿細管周囲の微小血管損傷、腎線維症、及び最終的に2〜3週間にわたる腎質量の40〜50%減少を生ずると報告された(Zager RAら,Acute unilateral ischemic renal injury induces progressive renal inflammation,lipid accumulation,histone modification,and “end−stage” kidney disease,Am.J.Physiol.,301:F1334−1345,2011)。モデル中の傷ついていない対側性腎の存在は尿毒症には起因する死亡率を改善し、研究者は急性腎障害をより詳しく調べることができる。片側虚血性腎障害のモデルは数週間のうちにほぼ「末期」の腎疾患を生ずる。この片側虚血モデルを使用することにより、進行性腎臓損傷に関与する幾つかの重要な病態生理学的事象が報告された。これらには、血清クレアチニンの段階的増加、BUN、炎症性サイトカイン生成、特定の抗炎症性防御(例えば、ヘムオキシゲナーゼ1及びIL−10)のダウンレギュレーション及び累積脂肪毒性が含まれる。これらは、進行性尿細管壊死、尿細管脱落、早期の線維形成、及び最終的には腎質量の顕著な減少となる(Zager RAら,Acute unilateral ischemic renal injury induces progressive renal inflammation,lipid accumulation,histone modification,and “end−stage” kidney disease,Am.J.Physiol.,301:F1334−1345,2011)。
従って、急性腎障害を治療するための有効で安全な治療法が要望されている。
J.Am.Soc.Nephrol.,17:1143−1150,2006
J.Am.Soc.Nephrol.,17:1135−1142,2006
Clin.J.Am.Soc.Nephrol.,2:356−365,2007
Proc.Natl.Acad.Sci.USA,89:11876−11880,1992
N.Engl.J.Med.,336:828−834,1997
Am.J.Kidney Dis.,36:767−774,2000
Clin.Chem.Lab.Med.,50:1533−1545,2012
J.Am.Soc.Nephrol.,20:223−228,2009
Clin.J.Am.Soc.Nephrol.,1:43−51,2006
JAMA,302:1179−85,2009
Kidney Int.,76:900−910,2009
Kidney Int.,76:893−9,2009
Am.J.Physiol.,300:F721−733,2011
Am.J.Physiol.,295:F1648−1657,2008
Am.J.Physiol.,297:R1358−R1363,2009
Am.J.Physiol.,293:F269−F278,2007
Kidney Int.,16:113−123,1979
J.Lab.Clin.Med.,103:193−203,1984
Am.J.Physiol.,301:F1334−1345,2011
本発明は、エンドセリン受容体アンタゴニスト、例えばアトラセンタンを用いる急性腎障害の治療方法に関する。本発明の1つの態様として、被験者における急性腎障害の治療方法を提供する。この方法は、被験者に対してETA受容体アンタゴニスト、例えばアトラセンタンまたはその医薬として許容され得る塩を投与することを含む。特に、この方法は、虚血誘発性腎障害または低酸素誘発性腎障害である腎障害を治療するのに適している。ETA受容体アンタゴニストを腎障害後に、例えば腎障害から少なくとも24時間後及び/または被験者が臨床的急性腎不全を発病後に投与し得る。幾つかの実施形態では、急性腎障害の発症及び/または診断前にETA受容体アンタゴニストを被験者に対して投与せず、幾つかの実施形態では、この方法はそのような投与を排除している。
本発明の別の態様として、被験者における虚血誘発性腎障害または低酸素誘発性腎障害の治療方法を提供する。本発明のさらに別の態様として、虚血誘発性腎障害または低酸素誘発性腎障害を有している被験者における慢性腎臓病への進行を遅らせる方法を提供する。本発明のさらなる別の態様として、被験者における虚血後または低酸素後の腎損傷を回復に向かわせる方法を提供する。これらの態様の各々において、方法は被験者に対してETA受容体アンタゴニストを投与することを含む。
本発明のさらに別の態様として、虚血誘発性腎障害または低酸素誘発性腎障害を有している被験者における腎質量の減少を抑制させる方法を提供する。この方法は、被験者を、急性腎障害を有すると診断し、AKI指標の第1回測定を実施し、被験者に対してETA受容体アンタゴニストを投与し、被験者にETA受容体アンタゴニストを一定期間投与した後にAKI指標の第2回測定を行うことを含む。AKI指標の第1回測定値と第2回測定値の差は有意でない。幾つかの実施形態では、AKI指標は腎質量、腎容積、糸球体濾過量、血清クレアチニン、血液尿素窒素または炎症のマーカーである。
本発明の別の態様として、被験者における急性腎障害の診断及び治療方法を提供する。この方法は、虚血誘発性腎障害または低酸素誘発性腎障害の指標のレベルを測定し、測定したレベルが虚血誘発性腎障害または低酸素誘発性腎障害を示すかを決定し、虚血誘発性腎障害または低酸素誘発性腎障害を患っている被験者に対してETA受容体アンタゴニストを投与することを含む。例えば、虚血誘発性腎障害または低酸素誘発性腎障害の指標には、尿細管障害残留物(すなわち、尿細管障害残留物(例えば、尿細管細胞円柱))を示す尿サンプル、腎臓で発現したET−1 mRNAのレベル、腎臓で発現したETA受容体mRNAのレベル、腎臓で発現したNGAL mRNAのレベル、ラクテートまたは炎症のマーカーが含まれる。具体的には、mRNA発現は腎臓の腎皮質内に局在化し得る。他の指標には、ET−1またはNGALのタンパク質のレベル、または細胞表面上のETA受容体発現または存在の他の測定値が含まれる。
先の方法において、ETA受容体アンタゴニストはアトラセンタンまたはその医薬として許容され得る塩であり得る。ETA受容体アンタゴニストを腎障害後、例えば腎障害から少なくとも24時間後に、または被験者が臨床的急性腎不全を発病した後に投与し得る。
本セクション及び本明細書中の全体の開示において使用されている見出しは限定的と意図されない。
本明細書中で使用されている単数形「a」、「an」及び「the」は、文脈上別段の意味であることが明白な場合を除き複数形を含む。本明細書中の数値範囲の記述について、その間に介在する数が同程度の精度で明白に考えられる。例えば、6〜9の範囲の場合には6及び9に加えて数7及び8が考えられ、6.0〜7.0の範囲の場合には数6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9及び7.0が明白に考えられる。
本明細書中で使用されている用語「約」は用語「おおよそ」と同義的に使用されている。例えば、用語「約」の使用は、示されている値を僅に外れる値、すなわち±10%を示す。こうした用量は、用語「約」及び「おおよそ」を用いて特許請求の範囲により包含される。
用語「投与する(administer)」、「投与する(administering)」、「投与した(administered)」または「投与(administration)」は、被験者または患者に対して薬物(例えば、アントラセンまたはその医薬として許容され得る塩)を与える方法を指す。投与ルートは、当業者に公知の手段によりなされ得る。その手段には、経口、口内、静脈内、皮下、筋肉内、経皮、吸入による等が含まれるが、これらに限定されない。
本明細書中で使用されている用語「活性物質」は、所望の生物学的効果を達成する物質またはその医薬として許容され得る塩を指す。用語「活性物質」及び「薬物」は本明細書中互換可能に使用される。本発明の剤形を製造する際に使用される活性物質の固体形態は重要でない、例えば、本発明の剤形を製造する際に使用される活性物質は非晶質でも結晶形でもよい。最終剤形は少なくとも検出可能な量の結晶性活性物質を含有している。活性物質の結晶性は粉末X線回折分析を用いて、示指走査熱量測定または当業界で公知の他の技術により検出され得る。
用語「アトラセンタン」、「atra」または「ABT−627」は、以下
用語BQ−788は、以下
活性物質の「有効量」または「治療有効量」は、非毒性であるが、所望の効果を与えるのに十分な活性物質の量を意味する。「有効な」活性物質の量は個人の年齢及び全身状態、具体的な活性物質等に応じて被験者毎に異なる。よって、正確な「有効量」を特定することは必ずしも可能でない。しかしながら、個人における適正な「有効量」はルーチンの実験を用いて決定され得る。
勿論、所望の結果を得るために他の投与レジメン、例えば1日2回以上の投与、長期間、徐放性または放出調節剤形等を利用できると理解されたい。ETA受容体アンタゴニストは腎虚血または低酸素の検出時に、またはその検出から24時間以内に投与し得ると考えられる。加えてまたは替えて、ETA受容体アンタゴニストは最長1週間、2週間、4週間、または8週間またはそれ以上投与し得る。或いは、ETA受容体アンタゴニストは急性腎障害が存在する限り、或いは障害が解消されるまで、または虚血または低酸素がもはや検出されなくなるまで投与し得る。
用語「エンドセリンサブタイプA受容体アンタゴニスト」、「ETA受容体アンタゴニスト」または「ETA受容体インヒビター」は、エンドセリンサブタイプA受容体を介するET−1シグナル化の効果を抑制する化合物を指す。ETA受容体アンタゴニストの例には、アンブリセンタン、アトラセンタン、アボセンタン、BMS 193884、BQ−123、CI−1020、クラゾセンタン、ダルセンタン、エドネンタン、S−0139、SB−209670、シタクスセンタン、TA−0201、タラセンタン、TBC 3711、テゾセンタン、YM−598、ZD−1611、ZD−4054、並びにその塩、エステル、プロドラッグ、代謝物、互変異性体、ラセミ体及びこれらのエナンチオマーが含まれるが、これらに限定されない。用語「エンドセリンアンタゴニスト」、または「ET−1アンタゴニスト」または「ET−1インヒビター」は、ET−1を抑制する化合物を指す。
用語「急性腎障害」または「急性腎不全」は、典型的には身体中に窒素性老廃物の蓄積をもたらすのに十分な腎機能の急速な悪化により確認される(例えば、Anderson and Schrier(1994),Harrison’s Principles of Internal Medicine,13版,Isselbacherら編,McGraw Hill Text,New Yorkを参照されたい)。急性腎不全では、少なくとも4〜8mmol/L/日(10〜20mg/dL/日)のBUNの増加率及び少なくとも40〜80μmol/L/日(0.5〜1.0mg/dL/日)の血清クレアチニンの増加率が典型的である。急性腎障害を患っている患者では、尿サンプルも尿細管障害残留物を含み得る。異化性(または、異化亢進性)である被験者では、BUNの増加率は100mg/dL/日を超えることがある。BUNまたは血清クレアチニンの増加率は一連の血液検査により測定され得、少なくとも2回の血液検査を好ましくは6〜72時間の間に、より好ましくは12〜24時間の間に実施する。「急性」腎不全(数日間にわたり悪化)と「急速進行性」腎不全(数週間にわたり悪化)はときどき区別される。しかしながら、本明細書中で使用されているフレーズ「急性腎障害」は両症候群を包含すると意図される。急性腎障害は上記したように臨床医により定期的に確認される。
本明細書中で使用されている用語「虚血誘発性腎障害」は、1回以上確認された腎虚血、または虚血/再潅流の発生に起因する腎障害を指す。用語「虚血性腎障害」は本明細書中互換可能に使用され得る。本明細書中で使用されている用語「低酸素誘発性腎障害」は、たとえ低酸素または無酸素が未知の原因または虚血以外の他の原因に起因していても、虚血、虚血再潅流、及び/または低酸素に起因する腎障害を指す。虚血誘発性腎障害は、例えば虚血性状態を認識することにより、または急性腎障害の幾つかの固有の腎原因を参照することにより臨床医により確認され得る。低酸素誘発性腎障害は、例えば低酸素状態を認識することにより、または急性腎障害の幾つかの固有の腎原因を参照することにより臨床医により確認され得る。腎障害の程度は、BUN及び血清クレアチニンの上昇を追跡することにより臨床評価される。
本明細書中で使用されている用語「炎症のマーカー」は、患者の身体の幾つかの様相が炎症状態にあるときにその身体から産生されるペブチドまたは化学物質を指す。炎症のマーカーの例には、トリグリセリド、非高密度リポタンパク質(HDL)、アポタンパク質B、フィブリノーゲン、可溶性腫瘍壊死因子受容体(sTNFR−2)、単球化学誘引性タンパク質−1、インターフェロンγ誘導タンパク質(IP−10)、マクロファージ炎症性タンパク質−1デルタ、血管細胞接着分子−1(VCAM)、血清アミロイドA、ヘムオキシゲナーゼ1、可溶性細胞間分子タイプ1(sICAM−1)、C−反応性タンパク質(CRP)、及びインターロイキンファミリーのメンバーが含まれる。これらのマーカーの幾つかが高レベルで存在することが発病に関係していることが判明している。例えば、CRPは全身性炎症のマーカーとして報告されている(Ridklerら,C−Reactive Protein and Other Markers of Inflammation in the Prediction of Cardiovascular Disease in Women,342(12):836−43,NEJM,2000)。炎症のマーカーは血液及び/または尿の採取により評価され得る。
本明細書中で使用されている用語「AKI指標」は、急性腎障害の存在を反映している臨床測定値を指す。考えられるAKI指標には、非限定的にGFR、血清シスタチンC、尿中アルブミン排泄、BUN、血清クレアチニン、尿中NGAL、尿中KIM−1、炎症のマーカーが含まれる幾つかの臨床検査パラメーター、及び非限定的に腎質量、及び腎臓尿細管細胞及び細胞残留物を示す尿サンプルが含まれる幾つかの形態的マーカーが含まれる。
本明細書中で使用されている用語「糸球体濾過量」または「GFR」は、実際または真の糸球体濾過量、及び糸球体濾過量の推算値を指す。糸球体濾過量の推算は、Modifiation of Diet in Renal Disease(MDRD)研究式、ベッドサイド・シュワルツ式、コッククロフト・ゴールトフォーミュラ、または他の臨床的に許容され得るフォーミュラまたは式を含めた幾つかの式を用いてなされ得る。
本明細書中で使用されている用語「臨床的急性腎不全」は、例えば一般開業医または腎臓専門医により臨床的に検出されるかまたは検出可能である腎機能の低下を指す。臨床的急性腎不全は低下した糸球体濾過量、尿生成物の減少または不在、血液中の増加した老廃物(特に、クレアチニンまたは尿素)、血尿(尿中の失血)、タンパク血尿(尿中のタンパク質損失)、または他の臨床指標により評価され得る。
本明細書中で使用されている用語「急性腎障害の固有の腎臓原因」には、
(1)血管系の異常、例えば血管収縮性疾患(例えば、悪性高血圧、強皮症、溶血性尿毒症、血栓性血小板減少性紫斑病)及び脈管炎(例えば、結節性多発動脈炎、過敏性血管炎、血清病、ウェゲナー肉芽腫症、巨細胞性動脈炎、混合性クリオグロブリン血症、ヘノッホ・シェーンライン紫斑病、全身性エリテマトーデス);
(2)糸球体の異常、例えば感染後異常(例えば、溶連菌、肺炎球菌、淋菌、ブドウ球菌、腸球菌、ウィルス[例えば、B型及びC型肝炎、おたふく風邪、はしか、エプスタイン・バール]、マラリア感染後、ブルセラ症、レジオネラ、リステリア、シャント腎炎、らい病、レプトスピラ症、または内臓膿腫に関連する)、並びに非感染性異常(例えば、急速進行性糸球体腎炎、膜性増殖性糸球体腎炎、グッドパスチャー症候群、全身性エリテマトーデス、ウェゲナー肉芽腫症);
(3)薬物関連の原因(例えば、ペニシリン、スルホンアミド、カルベニシリン、セファロスポリン、エリスロマイシン、ナフシリン、オキサシリン、非ステロイド系消炎剤、利尿剤(フロセミド、エタクリニック酸、チアジド、スピロノラクトン、マーキュリアル)、フェニトイン、フェノバルビタール、プロベネシド、アロプリノール、シメチジン)、感染関連原因(例えば、急性腎盂腎炎、連鎖球菌症、スタフィロコッカス症、レプトスピラ症、マラニア、サルモネラ症)、乳頭壊死(例えば、糖尿病、鎌状赤血球症、鎮痛薬乱用、アルコール中毒症に関連する)、及び他の各種原因(例えば、サルコイドーシス、白血病、リンパ腫)から生ずる急性間質性腎炎;
(4)結晶沈着(例えば、尿酸、オキサレート、メトトレキサート)、または多発性骨髄腫及びL鎖病からの管内閉塞;及び
(5)ネフロトキシン(例えば、アミノグリコシド、テトラサイクリン、アンホテリシン、ポリミキシン、セファロスポリンのような抗菌物質)、重金属(例えば、水銀、鉛、ヒ素、金塩、バリウム)及び他の各種化学物質(例えば、シスプラチン、ドキソルビシン、ストレプトゾシン、メトキシフラン、ハロタン、エチレングリコール、四塩化炭素)、または虚血(例えば、出血、低血圧、敗血症、火傷、腎梗塞、腎動脈解離、横紋筋融解症、外傷)、または他の各種原因(例えば、造影剤、輸血副作用、ミオグロビン血症、熱射病、ヘビにかまれた傷及び蜘蛛にかまれた傷)から生ずる急性尿細管壊死;
が含まれる。
(1)血管系の異常、例えば血管収縮性疾患(例えば、悪性高血圧、強皮症、溶血性尿毒症、血栓性血小板減少性紫斑病)及び脈管炎(例えば、結節性多発動脈炎、過敏性血管炎、血清病、ウェゲナー肉芽腫症、巨細胞性動脈炎、混合性クリオグロブリン血症、ヘノッホ・シェーンライン紫斑病、全身性エリテマトーデス);
(2)糸球体の異常、例えば感染後異常(例えば、溶連菌、肺炎球菌、淋菌、ブドウ球菌、腸球菌、ウィルス[例えば、B型及びC型肝炎、おたふく風邪、はしか、エプスタイン・バール]、マラリア感染後、ブルセラ症、レジオネラ、リステリア、シャント腎炎、らい病、レプトスピラ症、または内臓膿腫に関連する)、並びに非感染性異常(例えば、急速進行性糸球体腎炎、膜性増殖性糸球体腎炎、グッドパスチャー症候群、全身性エリテマトーデス、ウェゲナー肉芽腫症);
(3)薬物関連の原因(例えば、ペニシリン、スルホンアミド、カルベニシリン、セファロスポリン、エリスロマイシン、ナフシリン、オキサシリン、非ステロイド系消炎剤、利尿剤(フロセミド、エタクリニック酸、チアジド、スピロノラクトン、マーキュリアル)、フェニトイン、フェノバルビタール、プロベネシド、アロプリノール、シメチジン)、感染関連原因(例えば、急性腎盂腎炎、連鎖球菌症、スタフィロコッカス症、レプトスピラ症、マラニア、サルモネラ症)、乳頭壊死(例えば、糖尿病、鎌状赤血球症、鎮痛薬乱用、アルコール中毒症に関連する)、及び他の各種原因(例えば、サルコイドーシス、白血病、リンパ腫)から生ずる急性間質性腎炎;
(4)結晶沈着(例えば、尿酸、オキサレート、メトトレキサート)、または多発性骨髄腫及びL鎖病からの管内閉塞;及び
(5)ネフロトキシン(例えば、アミノグリコシド、テトラサイクリン、アンホテリシン、ポリミキシン、セファロスポリンのような抗菌物質)、重金属(例えば、水銀、鉛、ヒ素、金塩、バリウム)及び他の各種化学物質(例えば、シスプラチン、ドキソルビシン、ストレプトゾシン、メトキシフラン、ハロタン、エチレングリコール、四塩化炭素)、または虚血(例えば、出血、低血圧、敗血症、火傷、腎梗塞、腎動脈解離、横紋筋融解症、外傷)、または他の各種原因(例えば、造影剤、輸血副作用、ミオグロビン血症、熱射病、ヘビにかまれた傷及び蜘蛛にかまれた傷)から生ずる急性尿細管壊死;
が含まれる。
「医薬として許容され得る賦形剤」または「医薬として許容され得る添加剤」の記述中のような「医薬として許容され得る」は、生物学的または他の点で望ましくなくない材料を意味し、すなわちこれらの材料は望ましくない生物学的効果を引き起こすことなく患者に対して投与される医薬組成物に配合され得る。
用語「RAASインヒビター」は、レニン−アンジオテンシン−アルドステロン系(RAAS)の1つ以上のエレメントを抑制する化合物を指す。RAASインヒビターの例には、ACEインヒビター、ARB、レニンインヒビター、アルドステロンアンタゴニスト等が含まれる。
用語「被験者」は動物を指す。1つの態様では、動物はヒトまたは非ヒトを含めた哺乳動物、好ましくはヒト被験者である。用語「患者」及び「被験者」は本明細書中互換可能に使用され得る。
被験者が急性腎不全状態にあるか、または急性腎不全に陥るリスクにあるかの診断は他の要因の中で血清クレアチニン及び血液尿素窒素の循環レベルを測定する一連の血液検査に基づいて行うことが好ましい。「一連の」血液検査は急性腎不全の症状を呈している未診断の患者の入院時に直ちに数時間毎に行われ得る。しかしながら、より典型的には、連続する一連の血液検査は72時間を超えずに少なくとも6時間空け、12〜24時間空けることが好ましい。24または72時間以内の2回以上の血液検査に基づいて、血清クレアチニンまたはBUNの上昇率を計算することが可能である。加えてまたは替えて、尿サンプル中の尿細管障害残留物の存在を評価することにより診断がなされ得る。
他の腎臓を失った方法(例えば、肉体的外傷、外科的切除、先天異常)に関係なく、1つしか腎臓を有していない被験者は急性腎不全のリスクが高いと考えられ得る。これは特に、残りの腎臓を冒すおそれがある疾患または状態に起因して1つの腎臓を失っている被験者に当てはまる。同様に、既に腎臓移植のレシピエントであるか、長期透析(例えば、長期血液透析または継続して通院の腹膜透析)を受けている被験者は急性腎不全のリスクが高いと見なされ得る。急性腎障害を発病するリスクの高い他の群には、慢性腎臓病を有している被験者、糖尿病を有している被験者及び高齢者が含まれる。従って、これらの被験者の場合、上で検討した臨床指標をより注意深くモニターする必要があり、腎臓治療薬を用いる早期またはより攻撃的な介入が推奨され得る。
用語「治療する」及び「治療」は、症状の重症度及び/または頻度の低下、症状及び/またはその根本原因の解消、症状の発生及び/またはその根本原因の予防、及び損傷の改善または修復を指す。よって、例えば、患者を「治療する」は、感受性個人における特定の障害または悪い生理学的事象の予防、及び障害または疾患を抑制または後退させることにより臨床症状のある個人の治療を含む。
本発明の方法は、一部、急性腎障害を患っている被験者に対して例えば急性腎障害の発症または診断後にETA受容体アンタゴニストを治療上使用すると死亡率及び/または罹患率を低下させることができ、急性腎障害に関連する腎機能の永久的及び/または段階的低下を予防、抑制、遅延または軽減することができるという驚くべき知見に基づいている。腎障害は低酸素誘発性腎障害、またはより具体的には虚血誘発性腎障害であり得ると考えられる。
ETA受容体拮抗作用は、虚血誘発性及び/または低酸素誘発性腎障害に関連する肉体的腎臓喪失及び機能的腎臓喪失を予防または抑制させる。臨床現場では、腎臓喪失は、超音波技術または他の適当な視覚化技術を用いて腎質量または腎容積を測定することにより評価され得る。
実施形態では、開示されている方法からの腎臓保護効果は初期の虚血/再潅流障害相の前、その間及び/またはその後に起こり得る。実施形態では、ETA受容体アンタゴニストをAKI後の腎臓回復を促進させるために投与する。
実施形態では、開示されている方法からの腎臓保護効果により、炎症のマーカー及び腎臓ストレス及び機能不全を示す幾つかの臨床検査パラメーター(例えば、血清クレアチニン、GFR、BUN)が低下する。従って、本発明の幾つかの実施形態では、ETA受容体アンタゴニストを投与後いつかは、これらの炎症のマーカー及び/または幾つかの臨床検査パラメーターの測定値が経時的低下を示し、これは腎機能の改善に相関している。
ETA受容体拮抗作用により与えられる腎臓保護の正確なメカニズムは明確でない。しかしながら、特定の理論またはメカニズムに束縛されないが、腎臓保護性は以下、すなわち直接ETA拮抗作用、一酸化窒素シグナル化との相互作用、アンジオテンシンIIシステム及びTGFβ−媒介線維形成の1つ以上により生じ得ると考えられる。実際持続する組織虚血が上で示唆されているように進行的腎臓損傷のメディエーターであるとすると、ET−1媒介腎血管収縮は潜在的に重要な病的役割を果たし得る。ETA受容体拮抗作用で見られる幾つかの腎臓保護効果は腎微小血管拡張及び腎尿細管細胞の構造及び機能の保存に起因すると見られる。従って、本発明の方法の幾つかの実施形態では、ETA受容体アンタゴニストのみ、またはRAASインヒビター単独での治療に比して付加的腎臓保護を与えるためにETA受容体アンタゴニストとRAASインヒビターの組合せを投与し得る。
本明細書中に記載されている本発明の方法の他の適当な修飾及び改変は自明であり、本発明の範囲または本明細書中に開示されている実施形態を逸脱することなく適当な均等物を用いてなし得る。本発明を詳細に記載してきたが、例示のみで、本発明の範囲を限定すると意図しない目的で含まれる以下の実施例を参照することにより本発明はより明瞭に理解されるであろう。本明細書で言及されているすべての刊行物、米国特許及び公開明細書の開示内容は全体として参照により組み入れる。
実験はすべてCharles River Laboratories(マサチューセッツ州ウィルミントン)から得た30〜45グラムの雄CD−1マウスを用いて実施した。マウスは餌及び水を自由に摂取できるルーチンのビバリウム条件下で飼育した。手術を深ペントバルビタール麻酔(40〜50mg/Kg IP)下で実施した。手術終了時にブプレノルフィン(0.1mg/Kg IP)を用いて術後麻酔を施した。手順はすべてNIHガイドラインに従ってIACUC協会で認可されていた。
計算及び統計:値はすべて平均±1 SEMとして表す。統計比較は対応のないスチューデントt検定により実施した。mRNAのデータは競合RT−PCRにより作成し、所与のメッセージの結果をハウスキーピング遺伝子として使用した同時に測定したGAPDH産物に対する比として表示した。リアルタイムPCR(qPCR)を用いて作成したChIPデータはng/mg−全適用クロマチンとして表す。H及びE染色した腎切片を研究することにより調べた組織学的障害の重症度を、5匹のアトラセンタン治療(虚血後24時間及び虚血後2週間)マウス及び5匹のアトラセンタン治療していない虚血後対照由来の虚血後2週間の腎臓のスライドをブラインドスコアリングすることにより評価した。スコアは1+〜4+、すなわち(近位尿細管壊死の程度に基づいて)観察された最も軽い〜最も重い腎障害の半定量スケールで等級づけた。連続変動する結果をスチューデントt検定により比較した。組織学的データはウィルコクソン順位和検定により判断した。有意差は、<0.05のp値により判断した。
[実施例1]
本実施例では、虚血性腎障害後ET−1及びETA/ETB受容体発現を定量し、ET−1遺伝子クロマチンリモデリング及びRNAポリメラーゼII(Pol II)結合を評価した。10匹のマウスを正中開腹し、左腎茎を露出させ、非外傷性微小血管クランプを用いて×30分閉塞した。(低酸素を示す)全腎チアノーゼの発生により均一の虚血を確認した。体温を、腹部内体温計を用いてモニターし、外部熱源を用いて37℃に維持した。この虚血期間終了時に、血管クランプを外し、腎チアノーゼの低下により均一の再潅流を確認した。次いで、腹部切開部を、3−0クロム縫合糸を用いて二層で縫合した。次いで、マウスを麻酔から回復させた。10匹の追加のマウスに腎茎閉塞を除いて同じ外科手順を施し、偽手術対照として用いた。
本実施例では、虚血性腎障害後ET−1及びETA/ETB受容体発現を定量し、ET−1遺伝子クロマチンリモデリング及びRNAポリメラーゼII(Pol II)結合を評価した。10匹のマウスを正中開腹し、左腎茎を露出させ、非外傷性微小血管クランプを用いて×30分閉塞した。(低酸素を示す)全腎チアノーゼの発生により均一の虚血を確認した。体温を、腹部内体温計を用いてモニターし、外部熱源を用いて37℃に維持した。この虚血期間終了時に、血管クランプを外し、腎チアノーゼの低下により均一の再潅流を確認した。次いで、腹部切開部を、3−0クロム縫合糸を用いて二層で縫合した。次いで、マウスを麻酔から回復させた。10匹の追加のマウスに腎茎閉塞を除いて同じ外科手順を施し、偽手術対照として用いた。
手術から24時間または2週間目に、後片側虚血群の半数(N=5)または偽手術群の半数(N=5)のマウスに再び麻酔を施し、腹部切開部を開いた。血液サンプルを下大静脈から採取し、両腎臓を切除した。腎臓を氷冷し、腎皮質サンプルをカミソリの刃を用いて得、全RNA(RNeasy;Qiagen)及び全タンパク質のために抽出した。RNAサンプルを用いてET−1ならびに、ETA及びETB受容体についてはmRNAを決定した。腎皮質抽出物及び血漿中のET−1タンパク質濃度をELISAにより決定した。
腎虚血/再潅流がET−1遺伝子での遺伝子活性化ヒストン修飾を誘導して、(例えば、ET−1遺伝子クロマチンリモデリング及びRNAポリメラーゼII(Pol II)結合を介して)ET−1転写が潜在的に増加するかを調べるために、腎皮質クロマチン抽出物を以下の腎臓、すなわち3匹の偽手術したマウス(術後2週間)からの腎臓、3匹の虚血後2週間の腎臓、及び3匹の対応する対側性腎臓から作成した。クロマチン免疫沈降アッセイ(ChIP)を用いてPol II結合、ヒストンH3トリメチル化(H3K4m3)、ヒストンH3アセチル化(H3K9/K14)の程度、及びET−1遺伝子のエクソン1でのPol IIレベルを既に記載されているようにリアルタイムPCRにより評価した(27−30)。加えて、ET−1エクソン1でのヒストンH2A.Z変異体交換の程度も評価した(Naito Mら,Endotoxin mediates recruitment of RNA polymerase II to target genes in acute renal failure,J.Am.Soc.Nephrol.,19:1321−1330,2008;Naito M,ら,BRG1 increases transcription of proinflammatory genes in renal ischemia,J.Am.Soc.Nephrol.,20:1787−1796,2009;Naito Mら,Renal ischemia−induced cholesterol loading:transcription factor recruitment and chromatin remodeling along the HMG CoA reductase gene,Am.J.Pathol.,174:54−62,2008;Zager RAら,Progressive histone alterations and proinflammatory gene activation:consequences of heme protein/iron−mediated proximal tubule injury,Am.J.Physiol.Renal Physiol.,2010 Mar;298(3):F827−37,Epub 2009 Dec 23)。結果は、プローブしたクロマチンタンパク質1mgあたりのPol II、H3K4m3、H3K9−14 Ac、及びエクソン1でのH2A.Zの量として表示した。qPCRのために使用したプライマー対を表1に示す。
図1に示すように、片側虚血性障害の24時間以内に、偽手術対照由来の正常腎臓と比較してET−1 mRNAの4倍の増加(p<0.01)が観察された。虚血から2週間まで、ET−1 mRNAの著しい更なる増加が観察され、24時間時点で観察された値よりも10倍高い値に達した。対側性(非虚血)腎臓が正常なET−1 mRNAのレベルを維持しているとすると、これらの虚血後ET−1 mRNA増加は手術ストレスではなく、虚血から生じた。
腎皮質ET−1 mRNAの著しい増加は腎皮質ET−1タンパク質レベルのおおよそ8倍の増加(図2)に関連していた。対照的に、血漿または対側性腎臓ET−1レベルの有意な増加は観察されず、その値は正常なマウスまたは偽手術した対照で観察された値に近似していた。これは、虚血後2週間の腎臓中の高い腎皮質ET−1タンパク質のレベルは全身循環からの摂取ではなく、より多い腎ET−1産生の結果であったことを暗示している。
虚血性腎障害後のRNAポリメラーゼII(Pol II)結合及びET−1遺伝子でのヒストン修飾に関して、ヒストン修飾酵素系が活性化され、炎症性遺伝子でのクロマチンリモデリングを誘発する。これらの変化には、ヒストンH3トリメチル化、アセチル化及びヒストンH2A.Z交換が含まれる(Naito Mら,Endotoxin mediates recruitment of RNA polymerase II to target genes in acute renal failure,J.Am.Soc.Nephrol.,19:1321−1330,2008;Naito Mら,BRG1 increases transcription of proinflammatory genes in renal ischemia,J.Am.Soc.Nephrol.,20:1787−1796,2009;Naito Mら,Renal ischemia−induced cholesterol loading:transcription factor recruitment and chromatin remodeling along the HMG CoA reductase gene,Am.J.Pathol.,174:54−62,2008;Zager RAら,Progressive histone alterations and proinflammatory gene activation:consequences of heme protein/iron−mediated proximal tubule injury,Am.J.Physiol.Renal Physiol.,2010 Mar;298(3):F827−37,Epub 2009 Dec 23)。クロマチン構造を緩めることにより、影響を受けた遺伝子へのRNAポリメラーゼII(Pol II)補充を促進し、よって遺伝子転写率を向上させる。
前記変化が潜在的に虚血後のET−1遺伝子の段階的活性化に寄与し得るかを評価するために、虚血後2週間の腎臓サンプルにChIPアッセイを適用し、H3K4m3、H3K9/14アセチル化及びH2A.Zのレベルの有意な増加が観察された。これらの変化の機能的な有意差はPol II(転写を導く酵素)のET−1遺伝子への結合の平行増加により暗示された。これらのヒストン変化と遺伝子転写率間の関係に原因及び影響があることは完全に推定され得ないが、これらが各種生物学系における遺伝子活性化事象であることは公知であると言う事実から、これが本当であると示唆される。
図3に示すように、虚血後2週間目での腎皮質ET−1 mRNAの増加は、遺伝子転写の著しい増加を示すET−1遺伝子の出発エクソンへのPol II結合のおおよそ5倍の増加に関連していた。更に、3つの評価した「遺伝子活性化」ヒストンマーカー(H3K4m3、H3K9Ac、ヒストン変異体H2A.Z)の各々の高いレベルは上昇したPol IIレベルに相当した。よって、これらのChIPデータは、虚血誘発性急性腎障害により、多分上昇したPol II補充を介する高い遺伝子転写に寄与するET−1遺伝子での遺伝子活性化ヒストン修飾がもたらされることを示す。
腎皮質ETA及びETB受容体mRNA発現も虚血後評価した。図4に示すように、ETA受容体mRNAの3倍増加は虚血後24時間まで明らかであった。虚血後2週間まで、ETA受容体mRNAの更に8倍の増加が観察された。よって、基準値と比較して、ETA受容体mRNAのレベルは実験中〜25倍に増加した。かなり対照的に、ETB受容体mRNAの増加は虚血後24時間で観察されなかった。虚血後2週間まで、有意なETB受容体mRNA増加が観察されたが、ETA mRNA値と比較して定量的に取るに足らなかった(それぞれ、25×対2×)。
[実施例2]
本実施例は、虚血前及び虚血後の期間中のアトラセンタン治療が腎臓保護を与えるかを研究した。18匹のマウスに実施例1に記載されている片側虚血/再潅流(I/R)プロトコルを施した。9匹のマウスに高強力の特異的ETA受容体アンタゴニストであるアトラセンタンを投与した。アトラセンタンは飲料水(25μg/mL;〜5mg/Kg/日の用量と等しくなるように計画した)を用いて投与した。アトラセンタン投与は手術1日前に始め、残りの実験中続けた。新鮮なアトラセンタンを1週あたり〜2−3回2週間与えた。残りの9匹のマウスには餌及び水を自由に与え、対照として使用した。
本実施例は、虚血前及び虚血後の期間中のアトラセンタン治療が腎臓保護を与えるかを研究した。18匹のマウスに実施例1に記載されている片側虚血/再潅流(I/R)プロトコルを施した。9匹のマウスに高強力の特異的ETA受容体アンタゴニストであるアトラセンタンを投与した。アトラセンタンは飲料水(25μg/mL;〜5mg/Kg/日の用量と等しくなるように計画した)を用いて投与した。アトラセンタン投与は手術1日前に始め、残りの実験中続けた。新鮮なアトラセンタンを1週あたり〜2−3回2週間与えた。残りの9匹のマウスには餌及び水を自由に与え、対照として使用した。
虚血後2週間の回復期間が終了したら、マウスにペントバルビタールで再麻酔を施し、腹部切開部を再び開き、BUN及びET−1分析のために末梢血液サンプルを下大静脈から採取した後、左(虚血後)腎臓及び右(対側性)腎臓を取り出し、重量を測定した。虚血後の腎質量の減少の程度を偽手術したマウス、対照虚血後のマウス、及びアトラセンタン治療を受けた虚血後のマウスからの腎臓の重量を比較することにより評価した。最後に、虚血後の腎臓の前頭切片を5匹の対照マウス及び5匹のアトラセンタン治療マウスから採取し、10% 緩衝ホルマリンで固定し、その後の組織化学分析のために使用した。
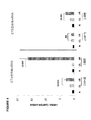
図5の左側パネルに示すように、片側I/R障害プロトコルは、偽手術したマウスから摘出した腎臓の重量と比較して腎質量(腎重量)のおおよそ45%の減少を引き起こした(p<0.0001)。偽手術は独立して正常なマウスから得た腎重量(示さず)と比較して腎重量に影響を与えなかった。アトラセンタンを腎虚血前から始めて、2週間の虚血後期間を通して継続的に投与すると、虚血後の腎臓の重量が正常な腎臓の重量と有意な差がなかったという事実から判断して著しい保護を与えた。この結果の写真を図6に示す。片側虚血/再潅流(I/R)腎臓(左端)のサイズ及び容積は正常腎臓(右端)と比較して著しく減少した。対照的に、虚血前及び虚血後にアトラセンタン治療を受けた腎臓はほぼ正常のサイズを示した。よって、腎虚血前及びその後にアトラセンタンを投与すると、腎容積又は質量の低下を抑制し得る。
[実施例3]
本実施例は、虚血後の期間中に限定したアトラセンタン治療が腎臓保護を与えるかを研究する。この実験は、アトラセンタンがその保護効果を誘導したときの問題の解決を助けるべく設計した。この目的のために、実施例2に記載されている同じプロトコルを繰り返したが、虚血性損傷を誘発させてから24時間後にアトラセンタンを投与した。2週間後、マウスに再び麻酔を施し、左及び右腎臓の重量を測定した。虚血後の腎臓重量減少の程度(上記した実験の主要エンドポイント)を調べた。値を片側虚血性腎臓±アトラセンタン治療(N=4、各群)及び正常なマウス由来の5つの腎臓で得た値と対比させた。
本実施例は、虚血後の期間中に限定したアトラセンタン治療が腎臓保護を与えるかを研究する。この実験は、アトラセンタンがその保護効果を誘導したときの問題の解決を助けるべく設計した。この目的のために、実施例2に記載されている同じプロトコルを繰り返したが、虚血性損傷を誘発させてから24時間後にアトラセンタンを投与した。2週間後、マウスに再び麻酔を施し、左及び右腎臓の重量を測定した。虚血後の腎臓重量減少の程度(上記した実験の主要エンドポイント)を調べた。値を片側虚血性腎臓±アトラセンタン治療(N=4、各群)及び正常なマウス由来の5つの腎臓で得た値と対比させた。
図5の右側パネルに示すように、薬物治療なしの虚血は腎重量を40%減少させた。虚血後のアトラセンタンはこの腎質量の低下を完全に阻止し、これにより前+後治療実験で見られる保護が再現される。このことは、アトラセンタンは即時の虚血/再潅流障害相(すなわち、虚血及び24時間再流の間)ではなく、遅れた(>24時間)虚血後の期間中にその保護効果を媒介したことを示す。このことから、虚血性腎障害を患っている被験者に対して該障害から24時間目またはその後にアトラセンタンを投与することは虚血及び低酸素の影響からの腎臓保護を与えるのに有効であることが示唆される。
[実施例4]
本実施例は、虚血性障害とは無関係の腎成長に対するアトラセンタンの可能性ある効果を研究する。アトラセンタン治療が腎虚血/虚血後の障害に対する影響とは無関係に腎成長またはサイズに影響を与えるかを確認するために、実施例2からの対側性(非虚血性)腎臓の重量を測定し、アトラセンタン治療を施したまたは施されていない虚血性腎臓と比較した。
本実施例は、虚血性障害とは無関係の腎成長に対するアトラセンタンの可能性ある効果を研究する。アトラセンタン治療が腎虚血/虚血後の障害に対する影響とは無関係に腎成長またはサイズに影響を与えるかを確認するために、実施例2からの対側性(非虚血性)腎臓の重量を測定し、アトラセンタン治療を施したまたは施されていない虚血性腎臓と比較した。
図7の左側パネルに示すように、対側性腎臓は正常腎臓と比較して腎サイズのおおよそ25%の増加を示した。このことは、既述されているように(Zager RAら,Acute unilateral ischemic renal injury induces progressive renal inflammation,lipid accumulation,histone modification,and “end−stage” kidney disease,Am.J.Physiol.,301:F1334−1345,2011)、虚血後の腎機能の低下に応答した腎肥大に一致している。アトラセンタンは、対側性腎臓重量が非薬物対薬物治療群で本質的に同一ならばこの腎肥大に対して影響を持たなかった。
[実施例5]
本実施例は、5匹の対照マウス及び実施例2からの5匹のアトラセンタン治療マウスの腎臓について腎組織を試験した。より具体的には、進行中の虚血後の障害に対するアトラセンタンの保護効果を確認するために、アトラセンタン治療を施した(前及び後)及びアトラセンタン治療を施されていない虚血後2週間目に得た腎臓において腎組織を調べた。4ミクロンの切片を切り、組織障害の重症度を全体的に評価するためにヘマトキシリンエオジンで染色した。加えて、腎尿細管細胞増殖をすべての活性細胞周期相(G1、S、G2、有糸分裂;Goなし)の核タンパク質マーカーであるKI−67について免疫組織化学的染色することにより評価した(Scholzen Tら,The Ki−67 protein:from the known and the unknown,J.Cell Physiol.,182:311−322,2000)。全腎臓切片に対するKI−67細胞の%を調べ、ScanScope AT(Aperio,カリフォルニア州ビスタ)で捕捉した後、核アルゴリズムスペクトルソフトウェア(パージョン11.1.1.764;Aperio)を用いて分析した。
本実施例は、5匹の対照マウス及び実施例2からの5匹のアトラセンタン治療マウスの腎臓について腎組織を試験した。より具体的には、進行中の虚血後の障害に対するアトラセンタンの保護効果を確認するために、アトラセンタン治療を施した(前及び後)及びアトラセンタン治療を施されていない虚血後2週間目に得た腎臓において腎組織を調べた。4ミクロンの切片を切り、組織障害の重症度を全体的に評価するためにヘマトキシリンエオジンで染色した。加えて、腎尿細管細胞増殖をすべての活性細胞周期相(G1、S、G2、有糸分裂;Goなし)の核タンパク質マーカーであるKI−67について免疫組織化学的染色することにより評価した(Scholzen Tら,The Ki−67 protein:from the known and the unknown,J.Cell Physiol.,182:311−322,2000)。全腎臓切片に対するKI−67細胞の%を調べ、ScanScope AT(Aperio,カリフォルニア州ビスタ)で捕捉した後、核アルゴリズムスペクトルソフトウェア(パージョン11.1.1.764;Aperio)を用いて分析した。
片側虚血プロトコルは、著しい近位尿細管脱落、広範囲の間質性炎症、進行中の近位尿細管壊死及び広範囲の管内円柱形成を引き起こした。これらの変化は腎皮質及び外線条全体で観察された。アトラセンタンはこれらの変化の各々を著しい低下させた。これらの変化の重症度の半定量スコア(1+〜4+;観察された最も軽い〜最も重い障害)を用いる盲検格付けは、アトラセンタン群における障害スコアの著しい低下(3.4±0.3対1.7±0.4;p<0.01)を示した。よって、組織学はアトラセンタン治療での保存された腎質量/腎重量と相関していた。
図7の右側パネルに示すように、KI−67免疫組織化学的染色は、正常な腎臓と比較して虚血後2週間の腎臓のすべてで腎尿細管細胞増殖の著しい増加を示した(p<0.001)。右側バネルは正常腎臓(A)、虚血後2週間(放置)の腎臓(B)、及び前後にアトラセンタン治療を施した虚血後2週間(放置)の左腎臓(C)を示す。虚血後の腎臓は、正常な腎臓で見られるものに比して核KI−67染色の著しい増加を示した。アトラセンタンは、KI−67核染色の頻度で示すこの増殖応答を変化させないようであった(KI−67核陽性の%:正常腎臓 2.4±0.6%;対照虚血 11.4±0.8%;虚血+アトラセンタン 10.8±1.2%)。
[実施例6]
本実施例は、アトラセンタン前治療が急性虚血性障害相を保護するかを研究する。より具体的には、アトラセンタンが急性障害相を鎮静し、よってその後腎質量を保持する可能性を、マウスに対して腎虚血を誘発させる前24時間及び誘発させた後24時間のアトラセンタン前治療の存在または非存在下で22.5分間または25分間の両側虚血性腎障害を施すことにより調べた。更にアトラセンタンが虚血性障害に対する保護を誘導する時間フレームを評価するために次の実験を行った。9匹のマウスをアトラセンタンを用いて24時間前治療した後、22.5分間(N=6)または25分間(N=3)の両側虚血性障害を施した。同数のマウスにアトラセンタン治療を施さないで同一の両側虚血プロトコルを施した。アトラセンタンは虚血後の期間中継続した。24時間後、マウスに再び麻酔を施し、腹部切開部を再度開き、血液サンプルを下大静脈から採取し、腎臓を再切開した。
本実施例は、アトラセンタン前治療が急性虚血性障害相を保護するかを研究する。より具体的には、アトラセンタンが急性障害相を鎮静し、よってその後腎質量を保持する可能性を、マウスに対して腎虚血を誘発させる前24時間及び誘発させた後24時間のアトラセンタン前治療の存在または非存在下で22.5分間または25分間の両側虚血性腎障害を施すことにより調べた。更にアトラセンタンが虚血性障害に対する保護を誘導する時間フレームを評価するために次の実験を行った。9匹のマウスをアトラセンタンを用いて24時間前治療した後、22.5分間(N=6)または25分間(N=3)の両側虚血性障害を施した。同数のマウスにアトラセンタン治療を施さないで同一の両側虚血プロトコルを施した。アトラセンタンは虚血後の期間中継続した。24時間後、マウスに再び麻酔を施し、腹部切開部を再度開き、血液サンプルを下大静脈から採取し、腎臓を再切開した。
障害の重症度を虚血後24時間目にBUN及び血漿クレアチニン濃度により評価した。アトラセンタンは虚血攻撃でのAKIの重症度を緩和するのに失敗した。図8に示すように、22.5分間または25分間の虚血攻撃(それぞれ、中程度または重症度の高窒素血症を誘発させる)で保護は観察されなかった。腎障害の第2マーカーとして、腎皮質NGAL mRNAのレベルも評価した。NGAL mRNAの測定値は図8で測定したBUN及び血漿クレアチニンよりも高感度の腎障害のマーカーに相当し、虚血性障害の誘発相に対するアトラセンタンの効果を調べるために測定した。図9に示すように、I/Rプロトコルの両方が著しいNGAL mRNA増加を誘発した。有意に高いNGAL mRNAのレベルが25分間対22.5分間の虚血で観察され、腎障害重症度の半定量的マーカーとして役立つ可能性が確認される。しかしながら、アトラセンタンがこれらのNGAL mRNA増加を低下させた例はなく、i)アトラセンタンは虚血性障害相を阻止できなかった;及びii)虚血後2週間目で観察されたその保護効果は遅れた虚血後/進行性腎障害相の間に生じたという結論が更に裏付けられる。
[実施例7]
アトラセンタンが近位尿細管細胞障害の早期相を阻止するかの別の評価として、既に詳細に記載されているように(Iwata Mら,Sphingosine:a mediator of acute renal tubular injury and subsequent cytoresistance,Proc.Natl.Acad.Sci,USA,9 2:8970−8974,1995;Iwata Mら,Protein synthesis inhibition induces cytoresistance in cultured human proximal tubular (HK−2) cells,Am.J.Physiol.,268:F1154−1163,1995)、正常なヒト腎臓由来の培養近位尿細管(HK−2)細胞をT24ウェルプレートにおいてケラチノサイト無血清培地中でインキュベートした。摂種からおおよそ18時間後、ウェルを(1)対照インキュベーション;(2)アトラセンタン単独(5μg/mL;予備実験により細胞形態または生存性(ラクテートデヒドロゲナーゼ(LDH)放出により測定)に対して単独作用を持たなかった最低のアトラセンタン用量であると判明した)でのインキュベーション;(3)7.5μM アンチマイシンA+10μM CaイオンフォアA23187+20mM 2−デオキシグルコース(“CAD”)を用いて誘導したATP枯渇/カルシウム過負荷障害;及び4)CAD+5μg アトラセンタン;の4群に分けた。18時間インキュベートした後、致死性細胞障害をLDH放出%により評価した。
アトラセンタンが近位尿細管細胞障害の早期相を阻止するかの別の評価として、既に詳細に記載されているように(Iwata Mら,Sphingosine:a mediator of acute renal tubular injury and subsequent cytoresistance,Proc.Natl.Acad.Sci,USA,9 2:8970−8974,1995;Iwata Mら,Protein synthesis inhibition induces cytoresistance in cultured human proximal tubular (HK−2) cells,Am.J.Physiol.,268:F1154−1163,1995)、正常なヒト腎臓由来の培養近位尿細管(HK−2)細胞をT24ウェルプレートにおいてケラチノサイト無血清培地中でインキュベートした。摂種からおおよそ18時間後、ウェルを(1)対照インキュベーション;(2)アトラセンタン単独(5μg/mL;予備実験により細胞形態または生存性(ラクテートデヒドロゲナーゼ(LDH)放出により測定)に対して単独作用を持たなかった最低のアトラセンタン用量であると判明した)でのインキュベーション;(3)7.5μM アンチマイシンA+10μM CaイオンフォアA23187+20mM 2−デオキシグルコース(“CAD”)を用いて誘導したATP枯渇/カルシウム過負荷障害;及び4)CAD+5μg アトラセンタン;の4群に分けた。18時間インキュベートした後、致死性細胞障害をLDH放出%により評価した。
HK−2細胞にATP枯渇(アンチマイシン/デオキシグルコース/Caイオンフォア;“CAD”)を添加すると中程度の尿細管細胞死が誘発され、LDH放出が8.6±0.1%の対照値から22.8±0.2%に上昇することが判明した。アトラセンタンは基準条件(9.0±0.1%)でも、ATP枯渇プロトコール(23.2±0.3%)でもLDH放出を変化させなかった。このことは再び、アトラセンタンが急性ATP枯渇障害相を阻止できなかったというインビボデータと一致している。
[実施例8]
本実施例はBQ−788の虚血後の腎障害に対する効果を研究する。8匹のマウスに片側虚血性障害プロトコルを施し、マウスの半分にETB特異的受容体アンタゴニストBQ−788を与えた。この物質を手術1日前から始めて3mmol/Kgの用量(ET−1/ETB結合アフィニティーのK1(100nM)を十分に超えるように選択した用量)で毎日皮下投与した(Khodorova Aら,Local injection of a selective endothelin−B antagonist inhibits endothelin−1−induced pain−like behavior and excitation of nociceptors in a naloxone−sensitive manner,J.Neurosci.,22:788−7796,2002;Webber KMら,Endothelin induces dopamine release from rat striatum via endothelin−B receptors,Neuroscience,86:1173−1180,1998)。対照片側虚血マウスには、等量のBQ−788ビヒクル(0.1ml 食塩液注射)を与えた。虚血から2週間後に腎臓を収集し、重量測定した。腎質量の虚血後の減少の程度を偽手術したマウス、対照の虚血後のマウス及びアトラセンタン治療を受けた虚血後のマウスからの腎臓と比較することにより評価した。
本実施例はBQ−788の虚血後の腎障害に対する効果を研究する。8匹のマウスに片側虚血性障害プロトコルを施し、マウスの半分にETB特異的受容体アンタゴニストBQ−788を与えた。この物質を手術1日前から始めて3mmol/Kgの用量(ET−1/ETB結合アフィニティーのK1(100nM)を十分に超えるように選択した用量)で毎日皮下投与した(Khodorova Aら,Local injection of a selective endothelin−B antagonist inhibits endothelin−1−induced pain−like behavior and excitation of nociceptors in a naloxone−sensitive manner,J.Neurosci.,22:788−7796,2002;Webber KMら,Endothelin induces dopamine release from rat striatum via endothelin−B receptors,Neuroscience,86:1173−1180,1998)。対照片側虚血マウスには、等量のBQ−788ビヒクル(0.1ml 食塩液注射)を与えた。虚血から2週間後に腎臓を収集し、重量測定した。腎質量の虚血後の減少の程度を偽手術したマウス、対照の虚血後のマウス及びアトラセンタン治療を受けた虚血後のマウスからの腎臓と比較することにより評価した。
2週間の時点で評価して、BQ−788は腎障害の低下を抑制しなかったことが判明した(対照虚血=0.23グラム;虚血+BQ−788=0.24グラム)。よって、これらの所見は、ETB受容体が血管拡張誘導において役割を発揮し、多分細胞保護効果を有するという示唆があるにもかかわらず、ETA受容体を介して媒介される虚血後の腎障害に対するET−1の効果を示している(Kawanabe Yら,Endothelin,Cell Molec.Life Sci.,68:195−203,2011;Motte Sら,Endothelin receptor antagonists,Pharmacol.Therapeutics,110:386−414,2006;Mino Nら,Protective effect of a selective endothelin receptor antagonist,BQ−123,in ischemic acute renal failure in rats,Eur.J.Pharmacol.,221:77−83,1992)。アトラセンタンにより発揮される腎臓保護効果は直接ETA受容体拮抗作用に起因せず、阻止されなかったETB受容体に対するET−1の利用可能性を高めることによるならば、ETB受容体拮抗作用は、ET−1/ETB受容体相互作用を介して媒介されると称されている細胞保護効果を阻止することにより、ETA受容体に結合するためにより多くのET−1を利用可能とすることにより、虚血事象後の腎障害を悪化させると予想されるだろう。しかしながら、BQ−788を虚血後及び虚血前に投与したときには腎臓損傷の増加は観察されなかった。実際、BQ−788は測定した腎パラメーターに対して影響を持たなかった。
このことから、急性腎障害、特に虚血誘発性腎障害及び低酸素誘発性腎障害の治療方法としてETA受容体の選択的拮抗作用はET−1阻害または非選択的ET受容体拮抗作用よりも望ましいことが示唆される。
本発明の先の記載は例示及び説明を与えるが、網羅しているとも、本発明を開示されている寸分違わないものに限定するとも意図されない。修飾及び改変が上記教示にてらして可能であり、また本発明の実施から獲得し得る。よって、本発明の範囲は特許請求の範囲及びその均等物により規定されると留意すべきである。
Claims (20)
- 被験者に対してETA受容体アンタゴニストを投与することを含む前記被験者における急性腎障害の治療方法。
- 前記急性腎障害が、虚血誘発性腎障害である請求項1に記載の方法。
- 前記急性腎障害が、低酸素誘発性腎障害である請求項1に記載の方法。
- 前記ETA受容体アンタゴニストがアトラセンタンまたはその医薬として許容され得る塩である、請求項1に記載の方法。
- 前記急性腎障害の発症または診断後に前記ETA受容体アンタゴニストを投与する、請求項1に記載の方法。
- 前記急性腎障害から少なくとも24時間後に前記ETA受容体アンタゴニストを投与する、請求項5に記載の方法。
- 前記被験者が臨床的急性腎不全を発病した後に前記ETA受容体アンタゴニストを投与する、請求項5に記載の方法。
- 被験者に対してETA受容体アンタゴニストを投与することを含む、前記被験者における虚血誘発性腎障害または低酸素誘発性腎障害の治療方法。
- 虚血誘発性腎障害または低酸素誘発性腎障害を有する被験者に対してETA受容体アンタゴニストを投与することを含む前記被験者における慢性腎臓病への進行を遅延させる方法。
- 被験者に対してETA受容体アンタゴニストを投与することを含む前記被験者における虚血後または低酸素後腎臓損傷を回復に向かわせる方法。
- 虚血誘発性腎障害または低酸素誘発性腎障害を有している被験者に対してETA受容体アンタゴニストを投与することを含む、前記被験者における腎質量または容積の減少の抑制方法。
- 被験者を、急性腎障害を有すると診断し;
急性腎障害指標の第1回測定を実施し;
前記被験者に対してETA受容体アンタゴニストを投与し;
前記被験者に対して前記ETA受容体アンタゴニストを一定期間投与した後、急性腎障害指標の第2回測定を実施する;
ことを含み、前記第1回測定値と第2回測定値の差が有意でない、前記被験者における急性腎障害の指標の低下方法。 - 前記急性腎障害が虚血誘発性または低酸素誘発性である、請求項12に記載の方法。
- 前記急性腎障害指標が腎質量、腎容積、糸球体濾過量、血清クレアチニン、血液尿素窒素または炎症のマーカーである、請求項12に記載の方法。
- 虚血誘発性腎障害または低酸素誘発性腎障害の指標のレベルを測定し;
測定したレベルが虚血誘発性腎障害または低酸素誘発性腎障害を示すかを決定し;
虚血誘発性腎障害または低酸素誘発性腎障害を患っている被験者に対してETA受容体アンタゴニストを投与する;
ことを含む前記被験者の急性腎障害を診断し、治療する方法。 - 虚血誘発性腎障害または低酸素誘発性腎障害の前記指標が尿細管障害残留物、腎臓中で発現したET−1 mRNA、ETA受容体mRNA、NGAL mRNAのレベル、ラクテートまたは炎症のマーカーである、請求項15に記載の方法。
- 前記ETA受容体アンタゴニストが、アトラセンタンまたはその医薬として許容され得る塩である、請求項8〜16のいずれか1項に記載の方法。
- 腎障害後、前記ETA受容体アンタゴニストを投与する、請求項8〜16のいずれか1項に記載の方法。
- 腎障害から少なくとも24時間後に前記ETA受容体アンタゴニストを投与する、請求項8〜16のいずれか1項に記載の方法。
- 前記被験者が臨床的急性腎不全を発病した後にETA受容体アンタゴニストを投与する、請求項8〜16のいずれか1項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361775174P | 2013-03-08 | 2013-03-08 | |
| US61/775,174 | 2013-03-08 | ||
| PCT/US2014/022688 WO2014138738A1 (en) | 2013-03-08 | 2014-03-10 | Methods of treating acute kidney injury |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016512201A true JP2016512201A (ja) | 2016-04-25 |
| JP2016512201A5 JP2016512201A5 (ja) | 2017-04-13 |
Family
ID=51492045
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015561753A Pending JP2016512201A (ja) | 2013-03-08 | 2014-03-10 | 急性腎障害の治療方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20160015701A1 (ja) |
| EP (1) | EP2964671A4 (ja) |
| JP (1) | JP2016512201A (ja) |
| CN (1) | CN105324395A (ja) |
| AU (1) | AU2014225320A1 (ja) |
| BR (1) | BR112015020788A2 (ja) |
| CA (1) | CA2901922A1 (ja) |
| HK (1) | HK1220209A1 (ja) |
| MX (1) | MX2015011730A (ja) |
| WO (1) | WO2014138738A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190097708A (ko) * | 2018-02-13 | 2019-08-21 | 서울대학교병원 | 체세포 복제 효율 증진용 조성물 |
| JP2019533660A (ja) * | 2016-10-05 | 2019-11-21 | ミトブリッジ,インコーポレーテッド | 急性腎障害を処置する方法 |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014179453A1 (en) | 2013-04-30 | 2014-11-06 | Abbvie, Inc. | Methods for improving lipid profiles using atrasentan |
| US20160128980A1 (en) * | 2014-11-07 | 2016-05-12 | Abbvie Inc. | Methods of treating ckd using predictors of fluid retention |
| EP3235496A1 (en) * | 2016-04-19 | 2017-10-25 | Noorik Biopharmaceuticals AG | Treatment of acute renal failure |
| WO2020006571A1 (en) * | 2018-06-29 | 2020-01-02 | pulseData Inc. | Machine learning systems and methods for predicting risk of renal function decline |
| US20220304979A1 (en) * | 2019-12-17 | 2022-09-29 | Chinook Therapeutics, Inc. | Methods of reducing disease flares |
| TW202130350A (zh) * | 2019-12-17 | 2021-08-16 | 美商奇努克治療美國公司 | 用阿曲生坦(ATRASENTAN)治療IgA腎病的方法 |
| EP4132509A4 (en) * | 2020-04-10 | 2024-04-03 | Chinook Therapeutics Inc | METHODS OF TREATING DIABETIC KIDNEY DISEASE |
| CN113209111A (zh) * | 2021-05-14 | 2021-08-06 | 上海海糖生物医药科技有限公司 | 一种褐藻寡糖的应用 |
| CN115005157B (zh) * | 2022-06-02 | 2023-12-26 | 上海交通大学医学院附属新华医院 | 一种低氧致急性肾损伤动物模型的构建方法 |
| CN116731117B (zh) * | 2023-06-19 | 2024-05-10 | 武汉大学 | Kim-1靶向性多肽及其在急性肾损伤中肾靶向性的应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08501778A (ja) * | 1992-09-22 | 1996-02-27 | ジェネンテク,インコーポレイテッド | 急性腎不全の予防方法 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060100743A1 (en) * | 2004-04-23 | 2006-05-11 | Renal Diagnostic Inc. | Automated non-invasive real-time acute renal failure detection system |
| US20060205733A1 (en) * | 2004-08-26 | 2006-09-14 | Encysive Pharmaceuticals | Endothelin a receptor antagonists in combination with phosphodiesterase 5 inhibitors and uses thereof |
| US9255931B2 (en) * | 2010-06-24 | 2016-02-09 | Morehouse School Of Medicine | Method and compositions for the treatment and detection of endothelin-1 related kidney diseases |
-
2014
- 2014-03-10 US US14/772,621 patent/US20160015701A1/en not_active Abandoned
- 2014-03-10 CA CA2901922A patent/CA2901922A1/en not_active Abandoned
- 2014-03-10 CN CN201480011012.2A patent/CN105324395A/zh active Pending
- 2014-03-10 BR BR112015020788A patent/BR112015020788A2/pt not_active IP Right Cessation
- 2014-03-10 JP JP2015561753A patent/JP2016512201A/ja active Pending
- 2014-03-10 WO PCT/US2014/022688 patent/WO2014138738A1/en active Application Filing
- 2014-03-10 EP EP14760019.1A patent/EP2964671A4/en not_active Withdrawn
- 2014-03-10 AU AU2014225320A patent/AU2014225320A1/en not_active Abandoned
- 2014-03-10 MX MX2015011730A patent/MX2015011730A/es unknown
-
2016
- 2016-07-13 HK HK16108216.3A patent/HK1220209A1/zh unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08501778A (ja) * | 1992-09-22 | 1996-02-27 | ジェネンテク,インコーポレイテッド | 急性腎不全の予防方法 |
Non-Patent Citations (2)
| Title |
|---|
| JPN. J. PHARMACOL., vol. Vol.82, JPN6017043735, 2000, pages 307 - 316 * |
| MOL. MED., vol. Vol.14(7-8), JPN6017043736, 2008, pages 502 - 516 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019533660A (ja) * | 2016-10-05 | 2019-11-21 | ミトブリッジ,インコーポレーテッド | 急性腎障害を処置する方法 |
| JP7065839B2 (ja) | 2016-10-05 | 2022-05-12 | ミトブリッジ,インコーポレーテッド | 急性腎障害を処置する方法 |
| KR20190097708A (ko) * | 2018-02-13 | 2019-08-21 | 서울대학교병원 | 체세포 복제 효율 증진용 조성물 |
| KR102177349B1 (ko) | 2018-02-13 | 2020-11-12 | 서울대학교병원 | 체세포 복제 효율 증진용 조성물 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN105324395A (zh) | 2016-02-10 |
| BR112015020788A2 (pt) | 2017-10-10 |
| EP2964671A1 (en) | 2016-01-13 |
| WO2014138738A8 (en) | 2015-12-30 |
| US20160015701A1 (en) | 2016-01-21 |
| EP2964671A4 (en) | 2016-08-31 |
| CA2901922A1 (en) | 2014-09-12 |
| HK1220209A1 (zh) | 2017-04-28 |
| WO2014138738A1 (en) | 2014-09-12 |
| MX2015011730A (es) | 2016-04-04 |
| AU2014225320A1 (en) | 2015-08-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2016512201A (ja) | 急性腎障害の治療方法 | |
| JP5392980B2 (ja) | 早発型の腎尿細管細胞障害を検出するための方法およびキット | |
| JP6822412B2 (ja) | 妊娠高血圧腎症のための診断アッセイ及び治療 | |
| Ataga et al. | The nephropathy of sickle cell trait and sickle cell disease | |
| Perazella et al. | The crystalline nephropathies | |
| JP2014503499A (ja) | 低酸素状態に基づく治療に適した被験体の事前選択 | |
| US9572787B2 (en) | Inhibition of renal fibrosis | |
| Frascà et al. | Renal cancer in kidney transplanted patients | |
| Gagnon et al. | Prospective study of urinalysis abnormalities in HIV-positive individuals treated with indinavir | |
| US20220143017A1 (en) | Pharmaceutical composition for preventing and treating diabetic nephropaphy including adenosine derivative | |
| Baines et al. | Antiviral inflammation during early pregnancy reduces placental and fetal growth trajectories | |
| Gustafsson et al. | Eosinophil activation in systemic sclerosis | |
| Ogura et al. | Potential amelioration of upregulated renal HIF-1alpha–endothelin-1 system by landiolol hydrochloride in a rat model of endotoxemia | |
| Kalimeris et al. | Mannitol and renal dysfunction after endovascular aortic aneurysm repair procedures: a randomized trial | |
| JP2019194173A (ja) | 腎障害の抑制におけるシラスタチンの利用 | |
| JP2015504088A (ja) | 肝疾患の治療 | |
| Pham et al. | Sickle cell disease | |
| Vijay et al. | Autosomal dominant polycystic kidney disease: a comprehensive review | |
| McDonald et al. | Effects of an endothelin receptor antagonist on a model of hypertensive retinopathy | |
| KR20230107866A (ko) | Btk 억제제를 사용한 전신성 홍반성 루푸스의 치료 방법 | |
| WO2021048162A1 (en) | Compound for inhibiting cell death | |
| TWI821836B (zh) | 一種用於緩解或預防慢性腎臟病進展的藥物組合物及其用途 | |
| Moriconi et al. | The Beneficial Effects of Bariatric-Surgery-Induced Weight Loss on Renal Function. Metabolites 2022, 12, 967 | |
| Srivastava et al. | Postoperative Renal Dysfunction in Recipient | |
| Joy et al. | Miscellaneous Etiologies of Acute Kidney Injury |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170309 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20171121 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180626 |