JP2016199486A - ジエポキシ化合物の製造方法 - Google Patents
ジエポキシ化合物の製造方法 Download PDFInfo
- Publication number
- JP2016199486A JP2016199486A JP2015079601A JP2015079601A JP2016199486A JP 2016199486 A JP2016199486 A JP 2016199486A JP 2015079601 A JP2015079601 A JP 2015079601A JP 2015079601 A JP2015079601 A JP 2015079601A JP 2016199486 A JP2016199486 A JP 2016199486A
- Authority
- JP
- Japan
- Prior art keywords
- group
- substituent
- saturated
- unsaturated
- hydrocarbon group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Epoxy Compounds (AREA)
- Catalysts (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
【課題】遷移金属やマグネシウム塩廃棄物の処理が必要なく、硬化することにより極めて優れた熱特性を有する硬化物を形成できる2つの脂環式エポキシ基を飽和炭化水素鎖で結合する化合物の簡便で効率的な製造方法の提供。【解決手段】式(1)で表される不飽和ジエポキシ化合物に含まれる炭素−炭素二重結合を、酸素を含む雰囲気下、ヒドラジンを用いて、飽和炭化水素鎖へ変換する飽和ジエポキシ化合物の製造方法。(R1〜R20は各々独立に、H、メチル基又はエチル基)【選択図】なし
Description
本発明は、重合することにより速やかに硬化して、優れた耐熱性を有する硬化物を形成することができるジエポキシ化合物の製造方法に関する。
エポキシ化合物は重合することにより、電気特性、耐湿性、耐熱性等に優れる硬化物を形成することが知られている。なかでも、ジエポキシ化合物は、コーティング剤、インク、接着剤、シーラント、封止剤、レジスト、複合材料、透明基材、透明フィルム又はシート、光学材料(例えば、光学レンズ等)、絶縁材料、光造形材料、電子材料(例えば、電子ペーパー、タッチパネル、太陽電池基板、光導波路、導光板、ホログラフィックメモリ等)などの用途を含む様々な方面で用いられている。
ジエポキシ化合物としては、現在、様々な種類のものが市販されており、例えば、3,4−エポキシシクロヘキシルメチル(3,4−エポキシ)シクロヘキサンカルボキシレート(特許文献1〜3参照)、3,4,3',4’−ジエポキシビシクロヘキシル(特許文献4参照)等が挙げられる。これらジエポキシ化合物は種々の硬化剤又は硬化触媒の下で重合することにより硬化物が得られる。
しかしながら、前記3,4−エポキシシクロヘキシルメチル(3,4−エポキシ)シクロヘキサンカルボキシレートはオキシラン酸素濃度が低く架橋点が少ないため得られる硬化物の強度が低く、耐熱性が低いことが問題であった。
また、3,4,3',4’−ジエポキシビシクロヘキシルは3,4−エポキシシクロヘキシルメチル(3,4−エポキシ)シクロヘキサンカルボキシレートに比べるとオキシラン酸素濃度が高いため、得られる硬化物はより優れた耐熱性を有するが、温度上昇に伴い機械特性(例えば、弾性率など)が大きく低下し熱安定性が低い点で、未だ十分満足できるものではなかった。さらに、3,4,3',4'−ジエポキシビシクロヘキシルは2つの脂環式エポキシ基(=脂環を構成する2つの炭素原子と1つの酸素原子とが互いに連結することにより形成される環式基である)が単結合で剛直に結合された構造を有するため、必ずしも2つの脂環式エポキシ基が架橋反応に適した位置に存在することができるわけでなく、架橋反応に関与できない脂環式エポキシ基が発生し、モノマーのオキシラン酸素濃度は高いにもかかわらず十分な耐熱性を有する硬化物が得られないという問題もあった。
一方、2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物は、常に架橋反応に適した位置に脂環式エポキシ基を存在させることが可能となり、架橋反応に関与できない脂環式エポキシ基を著しく低減することができること、それにより、極めて優れた熱特性を有する(具体的には、極めて高い耐熱性を有し、高温環境下に曝しても優れた機械特性を維持できる熱安定性を有する)硬化物を形成することができることが見いだされた(特許文献5参照)。
2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物の製造方法は、例えば、末端オレフィンと脂環式エポキシ基を有する化合物のメタセシス反応生成物である2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物の炭素−炭素二重結合のみを飽和炭化水素に変換する方法(特許文献5参照)や、特定のテトラヒドロベンジル化合物とGrignard試薬を反応させて得られる化合物をエポキシ化する方法(特許文献6参照)が知られている。
前者の方法において、炭素−炭素二重結合を飽和炭化水素へ変換する方法として、パラジウム触媒等の遷移金属触媒の存在下、水素ガスを用いて水素添加(接触水素添化)する方法が知られているが、エポキシ基の水素化が避けられず、エポキシ基がアルコールに変換された化合物が副生する。この場合、目的物と副生物は通常液状であり晶析による精製はできず、沸点も近いため蒸留での精製も難しく、カラム精製を行うとロスが大きく収率が低下するという問題があった。
そのため、パラジウム炭素触媒の活性を落としたとされるパラジウム炭素−エチレンジアミン複合錯体を用いて、2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物の炭素−炭素二重結合の水素添加反応を行っている。
そのため、パラジウム炭素触媒の活性を落としたとされるパラジウム炭素−エチレンジアミン複合錯体を用いて、2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物の炭素−炭素二重結合の水素添加反応を行っている。
しかし、パラジウムをはじめとする遷移金属触媒を使用するためコストが嵩む点、反応終了後の後処理において、反応に用いた遷移金属触媒のろ過だけでなく未反応原料やエポキシ基がアルコールに変換された化合物を除去するためシリカゲルカラムクロマトグラフィー精製を実施しており精製が煩雑である点、収率が中程度で効率性が悪い点、遷移金属廃棄物の処理が発生し廃棄物処理負荷が高いことが問題であった。
後者の方法においては、Grignard試薬由来のマグネシウム塩廃棄物が量論量発生し廃棄物処理負荷が高い点、鉄触媒を用いる場合は収率が低く効率性が悪い点、銅触媒を用いる場合は高価な配位子を必要として経済的に不利である点、不純物除去のためシリカゲルカラムクロマトグラフィー精製を実施しており精製が煩雑である点が問題であった。
SYNLETT,2014,25,671
したがって、本発明の目的は、遷移金属やマグネシウム塩廃棄物の処理が必要なく、硬化することにより極めて優れた熱特性を有する硬化物を形成することができる2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物の簡便で効率的な製造方法を提供することにある。
本発明者等は上記課題を解決するため鋭意検討したが、遷移金属触媒による水素化反応では、エポキシ基と炭素−炭素二重結合の選択性は官能基の反応性の違いによって決まり、炭素−炭素二重結合だけを水素化するのは困難で、不純物除去の精製のためにシリカゲルカラム精製が必須であることがわかった。また、特定のテトラヒドロベンジル化合物とGrignard試薬を反応させて得られる化合物をエポキシ化する方法では、量論量のマグネシウム塩廃棄物の発生は避けられないことがわかった。
炭素−炭素二重結合を水素化する方法として、酸素を含む雰囲気下、ヒドラジンを用いる水素化方法は公知(非特許文献1参照)であるが、エポキシ基が共存する化合物において炭素−炭素二重結合のみを飽和炭化水素鎖に変換する事例は示されていない。
また、酸素を含む雰囲気下、アロキサジンまたはイソアロキサジン化合物を触媒としてヒドラジンを用いる水素化方法において、末端オレフィンと末端エポキシ基を有する鎖状化合物である、1,2−エポキシ−9−デセンの末端オレフィンのみを水素化する例も公知(特許文献7参照)であるが、2つの脂環式エポキシ基をつなぐ炭素−炭素二重結合を含む不飽和炭化水素鎖の炭素−炭素二重結合の水素化の事例は示されていなかった。
また、酸素を含む雰囲気下、アロキサジンまたはイソアロキサジン化合物を触媒としてヒドラジンを用いる水素化方法において、末端オレフィンと末端エポキシ基を有する鎖状化合物である、1,2−エポキシ−9−デセンの末端オレフィンのみを水素化する例も公知(特許文献7参照)であるが、2つの脂環式エポキシ基をつなぐ炭素−炭素二重結合を含む不飽和炭化水素鎖の炭素−炭素二重結合の水素化の事例は示されていなかった。
そして、酸素を含む雰囲気下、ヒドラジンを用いて、2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物を水素化すると、遷移金属やマグネシウム塩廃棄物を発生することなく、簡便で効率的に2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物を得ることができることを見出した。本発明はこれらの知見に基づいて完成させたものである。
すなわち、本発明は、酸素を含む雰囲気下、ヒドラジンを用いて、下記式(1)
(式中、R1〜R20は、それぞれ独立して、水素原子、メチル基、又はエチル基を示す)
で表される不飽和ジエポキシ化合物に含まれる炭素−炭素二重結合を飽和炭化水素鎖へ変換することにより、下記式(2)
で表される不飽和ジエポキシ化合物に含まれる炭素−炭素二重結合を飽和炭化水素鎖へ変換することにより、下記式(2)
(式中、R1〜R20は前記に同じ)
で表される飽和ジエポキシ化合物を得る飽和ジエポキシ化合物の製造方法を提供する。
で表される飽和ジエポキシ化合物を得る飽和ジエポキシ化合物の製造方法を提供する。
前記炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応は、下記式(3)若しくは下記式(5)で表されるイソアロキサジン骨格を有する化合物、又は下記式(4)若しくは下記式(6)で表されるアロキサジン骨格を有する化合物を触媒として用いて行うことが好ましい。
(式中、R21は、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示し、
R22〜R25は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R26は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R21〜R26のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
R22〜R25は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R26は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R21〜R26のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
(式中、R31は、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示し、
R32〜R35は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R36は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R31〜R36のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
R32〜R35は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R36は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R31〜R36のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
(式中、R41は、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示し、
R42〜R45は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R46及びR47は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R41〜R47うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L1は一価の陰イオンを示す。)
R42〜R45は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R46及びR47は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R41〜R47うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L1は一価の陰イオンを示す。)
(式中、R51は、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示し、
R52〜R55は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R56及びR57は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R51〜R57うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L2は一価の陰イオンを示す。)
R52〜R55は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R56及びR57は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R51〜R57うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L2は一価の陰イオンを示す。)
前記炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応は、下記式(7)で表される(メタ)アクリロイルオキシ基を有する化合物と、下記式(8)で表される(メタ)アクリロイルオキシ基及びイソアロキサジン骨格を有する化合物との共重合体を触媒として用いて行うことも好ましい。
(式中、nは、1乃至6の整数を示し、
Aは、水素原子又はメチル基を示し、nが2以上の場合、n個のAは、それぞれ同一であっても異なっていてもよく、Xは、置換基を有していてもよい飽和または不飽和のn価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のn価の非環式炭化水素基、置換基を有していてもよいn価の芳香族炭化水素基、置換基を有していてもよいn価のヘテロ環基、(ポリ)アルキレンオキシ基、又はこれらの基の2以上が連結して形成されるn価の基を示す。)
Aは、水素原子又はメチル基を示し、nが2以上の場合、n個のAは、それぞれ同一であっても異なっていてもよく、Xは、置換基を有していてもよい飽和または不飽和のn価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のn価の非環式炭化水素基、置換基を有していてもよいn価の芳香族炭化水素基、置換基を有していてもよいn価のヘテロ環基、(ポリ)アルキレンオキシ基、又はこれらの基の2以上が連結して形成されるn価の基を示す。)
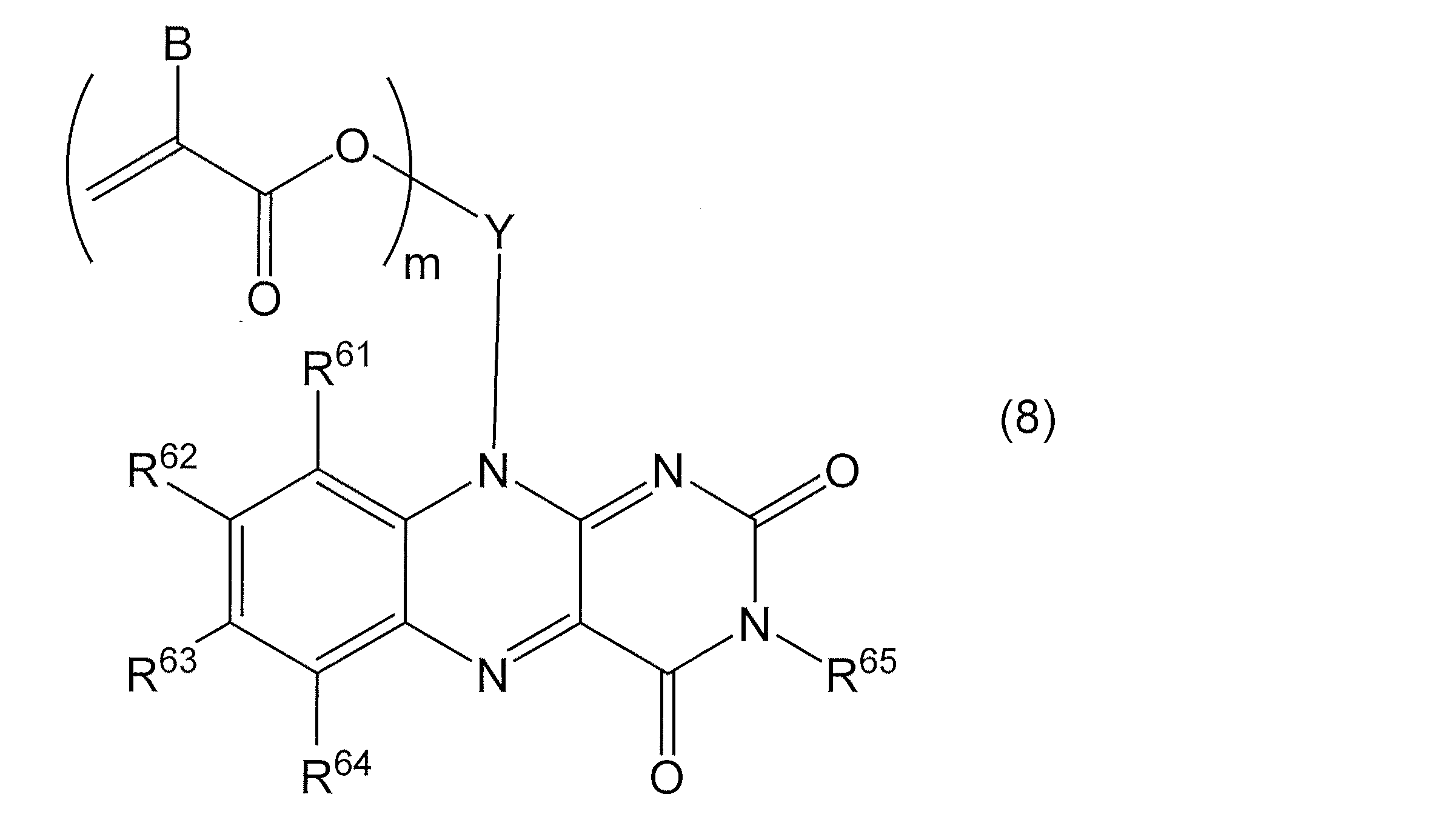
(式中、mは、1乃至6の整数を示し、
Bは、水素原子又はメチル基を示し、mが2以上の場合、m個のBは、それぞれ同一であっても異なっていてもよく、
Yは、置換基を有していてもよい飽和または不飽和のm+1価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のm+1価の非環式炭化水素基、置換基を有していてもよいm+1価の芳香族炭化水素基、又は置換基を有していてもよいm+1価のヘテロ環基を示し、
R61〜R64は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R65は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R61〜R65のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
Bは、水素原子又はメチル基を示し、mが2以上の場合、m個のBは、それぞれ同一であっても異なっていてもよく、
Yは、置換基を有していてもよい飽和または不飽和のm+1価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のm+1価の非環式炭化水素基、置換基を有していてもよいm+1価の芳香族炭化水素基、又は置換基を有していてもよいm+1価のヘテロ環基を示し、
R61〜R64は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R65は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R61〜R65のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
前記炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応は、前記式(5)で表されるイソアロキサジン骨格を有する化合物、又は前記式(6)で表されるアロキサジン骨格を有する化合物をカチオン交換型イオン交換樹脂とイオン交換して保持させたものを触媒として用いて行うことも好ましい。
前記炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応は、酸を触媒として用いて行うことも好ましい。
前記酸を触媒として用いて行う炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応において、酸が有機化合物であることが好ましい。
前記炭素−炭素二重結合を飽和炭化水素鎖へ変換する反応は、前記式(3)〜(6)の化合物、前記式(7)の化合物と前記式(8)の化合物の共重合体、及び前記式(5)の化合物若しくは前記式(6)の化合物が保持されたカチオン交換型イオン交換樹脂の少なくとも一つの触媒と、酸(好ましくは有機化合物である酸)との組み合わせを触媒として用いて行うことも好ましい。
本発明のジエポキシ化合物の製造方法によれば、酸素を含む雰囲気下、ヒドラジンを用いて、前記式(1)で表される2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物に含まれる炭素−炭素二重結合を飽和炭化水素鎖へ変換することで、金属を用いることなく反応を実施できるため金属廃棄物が発生せず、エポキシ基の開環物が生成しないため副生するアルコールの分離が不要となり、反応後、触媒を除去して濃縮するだけで高純度の2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物を得ることができる。そのため、硬化することにより極めて優れた熱特性を有する硬化物を形成することができる、2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物を、安価に且つ効率よく製造することができる。
本発明の下記式(2)で表される2つの脂環式エポキシ基を飽和炭化水素鎖で結合して得られる化合物(本明細書において、「飽和ジエポキシ化合物」と称することがある)の製造方法は、酸素を含む雰囲気下、ヒドラジンを用いて、下記式(1)で表される2つの脂環式エポキシ基を炭素−炭素二重結合を含む不飽和炭化水素で結合することで得られる化合物(本明細書において、「不飽和ジエポキシ化合物」と称することがある)に含まれる炭素−炭素二重結合を飽和炭化水素鎖へ変換すること(本明細書において、「水素化反応」と称することがある)で、式(2)で表される飽和ジエポキシ化合物を得ることを特徴とする。
(各式中、各記号は、前記と同義である。)
式(1)で表される不飽和ジエポキシ化合物に含まれる炭素−炭素二重結合の幾何異性は、E体又はZ体のいずれであってもよく、また、E体及びZ体の任意の割合の混合物も含まれる。式(1)で表される不飽和ジエポキシ化合物の幾何異性体としては、E体が好ましい。
式(1)及び(2)において、R1〜R20としては水素原子、メチル基、エチル基が好ましく、特に、水素原子が好ましい。
式(1)で表される不飽和ジエポキシ化合物に含まれる炭素−炭素二重結合の幾何異性は、E体又はZ体のいずれであってもよく、また、E体及びZ体の任意の割合の混合物も含まれる。式(1)で表される不飽和ジエポキシ化合物の幾何異性体としては、E体が好ましい。
式(1)及び(2)において、R1〜R20としては水素原子、メチル基、エチル基が好ましく、特に、水素原子が好ましい。
前記水素化反応においては、下記式(3)若しくは下記式(5)で表されるイソアロキサジン骨格を有する化合物(本明細書において、「イソアロキサジン化合物(3)」、「イソアロキサジン化合物(5)」とそれぞれ称することがある)、又は下記式(4)若しくは下記式(6)で表されるアロキサジン骨格を有する化合物(本明細書において、「アロキサジン化合物(4)」、「アロキサジン化合物(6)」とそれぞれ称することがある)を触媒として用いることが好ましい。
(各式中、各記号は、前記と同義である。)
イソアロキサジン化合物(3)、アロキサジン化合物(4)、イソアロキサジン化合物(5)及び/又はアロキサジン化合物(6)を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。
イソアロキサジン化合物(3)、アロキサジン化合物(4)、イソアロキサジン化合物(5)及び/又はアロキサジン化合物(6)を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。
あるいは、前記水素化反応においては、下記式(7)で表される(メタ)アクリロイルオキシ基を有する化合物(本明細書において、「(メタ)アクリロイルオキシ化合物(7)」と称することがある)と、下記式(8)で表される(メタ)アクリロイルオキシ基及びイソアロキサジン骨格を有する化合物(本明細書において、「(メタ)アクリロイルオキシイソアロキサジン化合物(8)」と称することがある)との共重合体を触媒として用いることも好ましい。
(各式中、各記号は、前記と同義である。)
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合体を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。さらに、当該触媒はイソアロキサジン骨格が共重合体に保持された状態で機能するため、回収、再利用が容易である。
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合体を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。さらに、当該触媒はイソアロキサジン骨格が共重合体に保持された状態で機能するため、回収、再利用が容易である。
また、前記水素化反応において、イソアロキサジン化合物(5)またはアロキサジン化合物(6)をカチオン交換型イオン交換樹脂に保持させたものを触媒として用いることも好ましい。
イソアロキサジン化合物(5)またはアロキサジン化合物(6)をカチオン交換型イオン交換樹脂に保持させたものを本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。また、当該触媒は樹脂に保持された状態で取り扱うことができるため、合成操作および精製が容易である。
イソアロキサジン化合物(5)またはアロキサジン化合物(6)をカチオン交換型イオン交換樹脂に保持させたものを本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。また、当該触媒は樹脂に保持された状態で取り扱うことができるため、合成操作および精製が容易である。
前記水素化反応においては、イソアロキサジン化合物(3)、アロキサジン化合物(4)、イソアロキサジン化合物(5)、アロキサジン化合物(6)、(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合体、カチオン交換型イオン交換樹脂に保持させたイソアロキサジン化合物(5)、及びカチオン交換型イオン交換樹脂に保持させたアロキサジン化合物(6)は、それぞれ単独で触媒として用いてもよく、2種以上を任意の割合で組み合わせて触媒として用いてもよい。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR65で示される「飽和または不飽和の脂環式炭化水素基」としては、例えば、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基などの3〜20員(好ましくは3〜15員、さらに好ましくは5〜8員)のシクロアルキル基;シクロペンテニル基、シクロへキセニル基などの3〜20員(好ましくは3〜15員、さらに好ましくは5〜8員)のシクロアルケニル基;パーヒドロナフタレン−1−イル基、ノルボルニル基、アダマンチル基、トリシクロ[5.2.1.02,6]デカン−8−イル、テトラシクロ[4.4.0.12,5.17,10]ドデカン−3−イル基などの橋かけ環式炭化水素基などが挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR65で示される「飽和または不飽和の非環式炭化水素基」としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、s−ブチル基、t−ブチル基、ペンチル基、ヘキシル基、デシル基、ドデシル基などの炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキル基;ビニル基、アリル基、1−ブテニル基などの炭素数2〜20(好ましくは2〜10、さらに好ましくは2〜3)のアルケニル基;エチニル基、プロピニル基などの炭素数2〜20(好ましくは2〜10、さらに好ましくは2〜3)のアルキニル基などが挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR65で示される「芳香族炭化水素基」としては、例えば、フェニル基、ナフチル基などの炭素数6〜20(好ましくは6〜14、さらに好ましくは6〜10)のアリール基などが挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR65で示される「ヘテロ環基」を構成する複素環には、芳香族性複素環及び非芳香族性複素環が含まれる。このような複素環としては、例えば、ヘテロ原子として酸素原子を含む3〜10員の複素環(例えば、オキシラン環などの3員環、オキセタン環などの4員環、フラン、テトラヒドロフラン、γ−ブチロラクトン環などの5員環、4−オキソ−4H−ピラン、テトラヒドロピランなどの6員環、ベンゾフラン、4−オキソ−4H−クロメン、クロマン環などの縮合環、3−オキサトリシクロ[4.3.1.14,8]ウンデカン−2−オン環、3−オキサトリシクロ[4.2.1.04,8]ノナン−2−オン環などの橋かけ環など)、ヘテロ原子として硫黄原子を含む4〜10員の複素環(例えば、チオフェン環などの5員環、4−オキソ−4H−チオピラン環などの6員環、ベンゾチオフェン環などの縮合環など)、ヘテロ原子として窒素原子を含む4〜10員の複素環(例えば、ピロール、ピロリジン、ピラゾール、イミダゾール、トリアゾール環などの5員環、ピリジン、ピリダジン、ピリミジン、ピラジン、ピペリジン、ピペラジン、トリアジン、ヘキサヒドロトリアジン環などの6員環、インドール、インドリン、キノリン、アクリジン、ナフチリジン、キナゾリン、プリン環などの縮合環など)、ヘテロ原子として酸素原子、硫黄原子、窒素原子等から選ばれる2種以上のヘテロ原子を含む4〜10員の複素環(例えば、例えば、オキサゾール、イソキサゾール、チアゾール、イソチアゾール、オキサジアゾール、チアジアゾール環などの5員環、モルホリン、チオモルホリン環などの6員環、ベンゾオキサゾール、ベンゾイソキサゾール、ベンゾチアゾール、ベンゾイソチアゾール、フェノキサジン環などの縮合環)などが挙げられる。
式(3)中のR22からR25、式(4)中のR32からR35、式(5)中のR42からR45、式(6)中のR52からR55、並びに式(8)中のR61からR64で示される「アミド基」としては、例えば、−NHC(=O)R(Rは、それぞれ前記で定義される脂環式炭化水素基、非環式炭化水素基、芳香族炭化水素基、又はヘテロ環基を示す。)で表される基などが挙げられる。
式(3)中のR22からR25、式(4)中のR32からR35、式(5)中のR42からR45、式(6)中のR52からR55、並びに式(8)中のR61からR64で示される「エステル基」としては、例えば、−COOR(Rは、それぞれ前記で定義される脂環式炭化水素基、非環式炭化水素基、芳香族炭化水素基、又はヘテロ環基を示す。)で表される基などが挙げられる。
式(3)中のR22からR25、式(4)中のR32からR35、式(5)中のR42からR45、式(6)中のR52からR55、並びに式(8)中のR61からR64で示される「アルコキシ基」としては、例えば、メトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、ブトキシ基、イソブチルオキシ基、s−ブチルオキシ基、t−ブチルオキシ基、ペンチルオキシ基、ヘキシルオキシ基、デシルオキシ基、ドデシルオキシ基などの炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルコキシ基などが挙げられる。
式(3)中のR22からR25、式(4)中のR32からR35、式(5)中のR42からR45、式(6)中のR52からR55、並びに式(8)中のR61からR64で示される「アルキルチオ基」としては、例えば、メチルチオ基、エチルチオ基、プロピルチオ基、イソプロピルチオ基、ブチルチオ基、イソブチルチオ基、s−ブチルチオ基、t−ブチルチオ基、ペンチルチオ基、ヘキシルチオ基、デシルチオ基、ドデシルチオ基などの炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキルチオ基などが挙げられる。
式(3)中のR22からR25、式(4)中のR32からR35、式(5)中のR42からR45、式(6)中のR52からR55、並びに式(8)中のR61からR64で示される「ハロゲン基」としては、例えば、フルオロ基、クロロ基、ブロモ基、ヨード基などが挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR64のうちの二つで形成される縮合炭化水素環としては、ベンゼン環、ナフタレン環などの炭素数6〜20(好ましくは6〜14、さらに好ましくは6〜10)の芳香族炭化水素環とイソアロキサジン骨格又はアロキサジン骨格との縮合環などが挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR64のうちの二つで形成される縮合複素環としては、上記で例示した「ヘテロ環基」を構成する複素環とイソアロキサジン骨格又はアロキサジン骨格との縮合環などが挙げられる。
式(7)中のXで示される「n価の脂環式炭化水素基」、「n価の非環式炭化水素基」、「n価の芳香族炭化水素基」及び「n価のヘテロ環基」としては、前記で定義、例示した「脂環式炭化水素基」、「非環式炭化水素基」、「芳香族炭化水素基」及び「ヘテロ環基」から、それぞれn−1個の水素原子を除外して形成される基が挙げられる。
式(7)中のXで示される「(ポリ)アルキレンオキシ基」としては、(ポリ)エチレンオキシ基、(ポリ)プロピレンオキシ基、(ポリ)イソプロピレンオキシ基、ブチレンオキシ、(ポリ)グリセリンなどが挙げられる。当該(ポリ)アルキレンオキシ基の重合度は特に制限されないが、1〜10が好ましく、1〜5がより好ましい。
式(7)中のXで示される「n価の脂環式炭化水素基」、「n価の非環式炭化水素基」、「n価の芳香族炭化水素基」、「n価のヘテロ環基」及び「(ポリ)アルキレンオキシ基」の2以上が連結して形成されるn価の基としては、特に制限はないが、例えば、下記式で表される基などが挙げられる。
(式中、m’及びn’は(ポリ)エチレンオキシ基の重合度を示し、それぞれ独立して、1〜10を示す。)
式(8)中のYで示される「m+1価の脂環式炭化水素基」、「m+1価の非環式炭化水素基」、「m+1価の芳香族炭化水素基」及び「m+1価のヘテロ環基」としては、前記で定義、例示した「脂環式炭化水素基」、「非環式炭化水素基」、「芳香族炭化水素基」及び「ヘテロ環基」から、それぞれm個の水素原子を除外して形成される基が挙げられる。
式(3)中のR21からR26、式(4)中のR31からR36、式(5)中のR41からR47、式(6)中のR51からR57、並びに式(8)中のR61からR65でそれぞれ示される「飽和または不飽和の脂環式炭化水素基」、「飽和または不飽和の非環式炭化水素基」、「芳香族炭化水素基」及び「ヘテロ環基」、式(7)中のXで示される「n価の脂環式炭化水素基」、「n価の非環式炭化水素基」、「n価の芳香族炭化水素基」及び「n価のヘテロ環基」、並びに式(8)中のYで示される「m+1価の脂環式炭化水素基」、「m+1価の非環式炭化水素基」、「m+1価の芳香族炭化水素基」及び「m+1価のヘテロ環基」がさらに有していてもよい置換基としては、それぞれ前記で定義される、飽和または不飽和の脂環式炭化水素基、飽和または不飽和の非環式炭化水素基、芳香族炭化水素基、ヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、ハロゲン基等が挙げられる。当該置換基の数は特に限定されず、任意に設定することができる。置換基が2以上存在する場合は、それらは、同一であっても異なっていてもよい。
なお、アロキサジンおよびイソアロキサジン骨格に直接置換する置換基の数は特に限定されないが、式(3)および式(4)においては1〜6個が好ましく、1〜4個がより好ましい。式(5)および式(6)においては1〜7個が好ましく、2〜5個がより好ましい。式(8)においては0〜5個が好ましく、1〜3個がより好ましい。置換基が2以上存在する場合は、それらは、同一であっても異なっていてもよい。
式(5)中のL1及び式(6)中のL2で示される「一価の陰イオン」としては、例えば、フッ化物イオン、塩化物イオン、臭化物イオン、ヨウ化物イオン等のハロゲン化物イオン、塩素酸イオン、臭素酸イオン、ヨウ素酸イオン等のハロゲン酸イオン、過塩素酸イオン、過臭素酸イオン、過ヨウ素酸イオン等の過ハロゲン酸イオン、ベンゼンスルホン酸イオン、パラトルエンスルホン酸イオン、メタンスルホン酸イオン、トリフルオロメタンスルホン酸イオン等のスルホン酸イオンなどが挙げられ、塩化物イオン、過塩素酸イオン、パラトルエンスルホン酸イオン、トリフルオロメンタンスルホン酸イオンなどが好ましい。
式(7)においてnが2以上の場合、n個のAは、それぞれ同一であっても異なっていてもよい。
式(8)においてmが2以上の場合、m個のBは、それぞれ同一であっても異なっていてもよい。
式(8)においてmが2以上の場合、m個のBは、それぞれ同一であっても異なっていてもよい。
式(1)で表される不飽和ジエポキシ化合物、式(2)で表される飽和ジエポキシ化合物、イソアロキサジン化合物(3)、アロキサジン化合物(4)、イソアロキサジン化合物(5)、アロキサジン化合物(6)、(メタ)アクリロイルオキシ化合物(7)及び(メタ)アクリロイルオキシイソアロキサジン化合物(8)が、分子内に不斉炭素原子を有する場合、当該不斉炭素原子に由来する各種立体異性体(エナンチオマー、ジアステレオマー等)並びにその任意の割合の混合物(ラセミ体、ジアステレオマー混合物等)も本願発明に含まれる。
前記式(3)中のR22からR26、式(4)中のR32からR36、式(5)中のR42からR45及びR47、式(6)中のR52からR55及びR57、及び式(8)中のR61からR65としては、水素原子、炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキル基、フェニル基等の炭素数6〜20(好ましくは6〜10)のアリール基、シクロヘキシル基等の炭素数3〜20(好ましくは3〜10)のシクロアルキル基、メチルオキシ基、エチルオキシ基等の炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキルオキシ基、シアノ基が好ましく、特に、水素原子、メチル基、フェニル基、シアノ基が好ましい。
前記式(3)中のR21、式(4)中のR31、式(5)中のR41、及び式(6)中のR51としては、置換基(例、ヒドロキシル基など)を有していてもよい炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキル基、置換基(例、C1-10アルキル基など)を有していてもよい炭素数6〜20(好ましくは6〜14、さらに好ましくは6〜10)のアリール基が好ましく、具体的には、メチル基、フェニル基、リビチル基、リビチル(2’,3’,4’,5’−テトラ−O−アセチル)基、リビチル(2’,3’,4’,5’−テトラ−O−ブチリル)基、またはリビチル(2’,4’:3’,5’−ジ−O−メチレン)基がより好ましい。
前記式(5)中のR46、及び式(6)中のR56としては、炭素数1〜20(好ましくは1〜10、さらに好ましくは1〜3)のアルキル基が好ましく、エチル基がより望ましい。
前記式(7)中のnとしては、1〜6の整数が好ましく、2〜4の整数がより好ましい。
前記式(8)中のmとしては、1〜8の整数が好ましく、2〜6の整数がより好ましい。
前記式(8)中のmとしては、1〜8の整数が好ましく、2〜6の整数がより好ましい。
イソアロキサジン化合物(3)の好適な具体例としては、下記式に示すような化合物が挙げられる。
アロキサジン化合物(4)の好適な具体例としては、下記式に示すような化合物が挙げられる。
イソアロキサジン化合物(5)の好適な具体例としては、下記式に示すような化合物が挙げられる
アロキサジン化合物(6)の好適な具体例としては、下記式に示す化合物が挙げられる。
(メタ)アクリロイルオキシ化合物(7)の好適な具体例としては、下記式に示すような化合物が挙げられる。
(式中、m’及びn’は、前記と同義である。)
(メタ)アクリロイルオキシイソアロキサジン化合物(8)の好適な具体例としては、下記式に示すような化合物が挙げられる。
(メタ)アクリロイルオキシイソアロキサジン化合物(8)の好適な具体例としては、下記式に示すような化合物が挙げられる。
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合は、溶媒中、例えば、2,2’−アゾビス(イソブチロニトリル)などのアゾ系重合開始剤や過酸化ベンゾイルなどの過酸化物系重合開始剤などのラジカル重合開始剤の存在下で行うことができる。好ましくは、溶媒はジグライム−ジメチルホルムアミド混合溶媒、重合開始剤は2,2’−アゾビス(イソブチロニトリル)である。
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の配合比は、特に限定されないが、(メタ)アクリロイルオキシ化合物(7)100重量部に対して(メタ)アクリロイルオキシイソアロキサジン化合物(8)を5重量部以上使用することが好ましく、10重量部以上使用することがより好ましい。(メタ)アクリロイルオキシイソアロキサジン化合物(8)の使用量がこの範囲より低いと、触媒活性が不十分となり、水素化反応の効率が低下する場合がある。また、(メタ)アクリロイルオキシイソアロキサジン化合物(8)の使用量の上限は、特に限定されないが、コスト競争力の観点から、(メタ)アクリロイルオキシ化合物(7)100重量部に対して50重量部以下が好ましく、30重量部以下がより好ましい。
ラジカル重合開始剤の使用量としては、特に限定されないが、(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の総重量100重量部に対して、0.01〜10重量部が好ましく、より好ましくは0.1〜5重量部である。
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合は、触媒活性に影響しない範囲で他のラジカル重合性モノマーを含んでいてもよい。
他のラジカル重合性モノマーとしては、N,N−ジメチルアクリルアミド、N,N−ジエチルアクリルアミド、N−t−ブチルアクリルアミド、N−n−ブトキシメチルアクリルアミド等の(メタ)アクリル酸アミド類、スチレン、ジビニルベンゼン、クロロスチレン等のビニルアリール類、塩化ビニル、酢酸ビニル、N−ビニルピロリドン等を使用することができる。
(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合は、触媒活性に影響しない範囲で他のラジカル重合性モノマーを含んでいてもよい。
他のラジカル重合性モノマーとしては、N,N−ジメチルアクリルアミド、N,N−ジエチルアクリルアミド、N−t−ブチルアクリルアミド、N−n−ブトキシメチルアクリルアミド等の(メタ)アクリル酸アミド類、スチレン、ジビニルベンゼン、クロロスチレン等のビニルアリール類、塩化ビニル、酢酸ビニル、N−ビニルピロリドン等を使用することができる。
イソアロキサジン化合物(5)又はアロキサジン化合物(6)を保持するカチオン交換型のイオン交換樹脂としては、市販のカチオン交換型イオン交換樹脂などを用いることができ、具体的には、例えば、アンバーライト IR124(H形)、アンバーリスト 15JWET、アンバーライト IRC176、アンバーリスト A21(オレガノ株式会社)、ダイヤイオン SK104H、ダイヤイオン PK212H、ダイヤイオン WK10、ダイヤイオン WK40L(三菱化学株式会社)、ナフィオン NR50(デュポン社)などが挙げられ、強酸性陽イオン交換型であるアンバーライト IR124(H形)、アンバーリスト 15JWET、ダイヤイオン SK104H、ダイヤイオン PK212H、ナフィオン NR50を用いることが好ましい。これらカチオン交換型イオン交換樹脂は、それぞれ単独で使用してもよく、2種以上を任意の割合で組み合わせて用いてもよい。
カチオン交換型イオン交換樹脂とイソアロキサジン化合物(5)またはアロキサジン化合物(6)とのイオン交換は、所定量のイオン交換樹脂とイソアロキサジン化合物(5)またはアロキサジン化合物(6)を含む溶液を混合して攪拌、振盪、静置した後、ろ過で回収してもよく、イオン交換樹脂にイソアロキサジン化合物(5)またはアロキサジン化合物(6)を含む溶液を連続して通過させてもよい。
一方で、本願発明の水素化反応においては、酸を触媒として用いることも好ましく、特に有機化合物である酸を触媒として用いることが特に好ましい。
酸を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。
酸を本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドが安定化されるため、ヒドラジンを式(1)で表される不飽和ジエポキシ化合物に対して大過剰に用いなくとも炭素−炭素二重結合の水素化を高収率で効率よく進行させることができる。
前記触媒として用いる酸は一般的に酸性を示す化合物であれば特に制限はなく、例えば、具体的には、硫酸、塩酸、燐酸などの無機酸、酢酸、蓚酸、p−トルエンスルホン酸、メタンスルホン酸、トリフルオロメタンスルホン酸、ビス(トリフルオロメタンスルホニル)イミド、ビス(ノナフルオロブタンスルホニル)イミドなどの有機酸が挙げられる。これら酸は、それぞれ単独で使用してもよく、2種以上を任意の割合で組み合わせて用いてもよい。これらの酸のうち、有機酸(有機化合物である酸)が好ましく、トリフルオロメタンスルホン酸、ビス(トリフルオロメタンスルホニル)イミド、ビス(ノナフルオロブタンスルホニル)イミドなどの超強酸、p−トルエンスルホン酸が特に好ましい。
さらには、本願発明の水素化反応においては、イソアロキサジン化合物(3)、アロキサジン化合物(4)、イソアロキサジン化合物(5)、アロキサジン化合物(6)、(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)との共重合体、イソアロキサジン化合物(5)若しくはアロキサジン化合物(6)を保持させたカチオン交換型イオン交換樹脂の少なくとも一つ(本明細書において、「(イソ)アロキサジン触媒」と称することがある)と、上記酸(好ましくは有機化合物である酸)とを組み合わせて触媒として用いることも好ましい。
(イソ)アロキサジン触媒と酸を組み合わせて本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドがさらに安定化され、反応の収率、効率が向上する。
上記(イソ)アロキサジン触媒と酸を組み合わせる場合の当量比は、特に限定されないが、(イソ)アロキサジン触媒に対して、酸を0.5〜6当量使用することが好ましく、1〜3当量使用することがより好ましい。
(イソ)アロキサジン触媒と酸を組み合わせて本発明の水素化反応の触媒として用いることにより、ヒドラジンと酸素から生成する還元剤であるジイミドがさらに安定化され、反応の収率、効率が向上する。
上記(イソ)アロキサジン触媒と酸を組み合わせる場合の当量比は、特に限定されないが、(イソ)アロキサジン触媒に対して、酸を0.5〜6当量使用することが好ましく、1〜3当量使用することがより好ましい。
前記水素化反応に用いるヒドラジンは、一水和物(抱水ヒドラジン)やその水溶液、硫酸塩や塩酸塩、無水ヒドラジン等を制限なく使用することができるが、取扱いが容易であることから一水和物(抱水ヒドラジン)やその水溶液が好ましい。
ヒドラジンの使用量は、式(1)で表される不飽和ジエポキシ化合物に対して、1当量以上、6当量以下の範囲内であることが好ましく、1当量以上、4当量以下の範囲内であることがより好ましい。ヒドラジン使用量が6当量を越えても構わないが、経済的に不利である。
前記水素化反応における「酸素を含む雰囲気」とは、少なくとも酸素が含まれる気体の環境下において水素化反応を行うことを意味する。酸素以外に含まれていてもよい気体としては、特に限定されないが、窒素、アルゴン、ヘリウムなどの不活性な気体が好ましい。「酸素を含む雰囲気」に含まれる酸素の濃度(体積%)は、特に限定されないが、1〜100体積%が好ましく、2〜100体積%が好ましい。「酸素を含む雰囲気」としては、分子状酸素、空気又は窒素で希釈した空気などを好適に使用することができる。
前記水素化反応における酸素を含む雰囲気を反応器内に形成する方法としては、一般的な手法を用いることができる。例えば、反応器の気相部に常圧の分子状酸素あるいは空気もしくは窒素で希釈した空気を連続的、または1回または数回にわたって間欠的に供給してもよく、また、反応液中へバブリングすることによって供給してもよい。供給する分子状酸素あるいは空気、窒素で希釈した空気は加圧してもよい。また、反応系の気相部には、酸素、窒素以外にも例えば、アルゴン、ヘリウムなどの不活性ガスが存在していてもよい。また、反応はバッチ式、セミバッチ式、連続式などの何れの方法で行うこともできる。
反応温度は、反応成分や触媒の種類などに応じて適宜選択でき、例えば、0℃から100℃、好ましくは5℃から80℃、より好ましくは10℃から60℃である。反応時間は例えば10分から80時間、好ましくは30分から60時間である。
また、前記水素化反応は、式(1)で表される不飽和ジエポキシ化合物が反応温度で液体であれば無溶媒で行うことができるが、必要に応じて溶媒を用いることもできる。前記水素化反応で使用する溶媒は特に制限がなく、一般的に反応溶媒として用いられている化合物を用いることができる。具体的には、たとえば、水、メタノール、エタノール、トリフルオロエチルアルコール等のフッ素を含んでいてもよいアルコール化合物、アセトニトリル等のニトリル化合物、酢酸エチル、プロピオン酸エチル等のエステル化合物、ジメチルホルムアミドやN−メチルピロリドンなどのアミド化合物、ジメチルスルホキシド等のスルホキシド、ジメチルエーテル、ジエチルエーテル、シクロペンチルメチルエーテル等の鎖状エーテル化合物、テトラヒドロフラン等の環状エーテル化合物、クロロホルム、ジクロロメタン、ジクロロエタン等のハロゲン化炭化水素、ベンゼン、トルエン、キシレン等の芳香族炭化水素化合物、ヘキサン、ヘプタン、シクロヘキサン等の炭化水素化合物が挙げられる。これら溶媒は、単独、またはこれらを組み合わせた混合溶媒として用いてもよい。これらの溶媒のうち、非プロトン性極性溶媒がより好ましく、アセトニトリルが特に好ましい。溶媒の使用量としては、例えば式(1)で表される不飽和ジエポキシ化合物100重量部に対して、例えば0〜20000重量部、好ましくは、100〜15000重量部、より好ましくは1000〜10000重量部である。
触媒の使用量((イソ)アロキサジン触媒と酸を組み合わせる場合はその総量)としては、式(1)で表される不飽和ジエポキシ化合物1モルに対して、例えば、0.0001〜0.2モル程度、好ましくは0.001〜0.1、より好ましくは0.01〜0.05モルである。
前記水素化反応は、反応器に、式(1)で表される不飽和ジエポキシ化合物、ヒドラジン、必要に応じて、(イソ)アロキサジン触媒、酸及び溶媒を、同時または順次投入又は滴下して、酸素を含む雰囲気下で、静置、振とう下あるいは攪拌下で行うことができるが、ヒドラジンの酸素による酸化を効率的に進行させるためには振とうまたは攪拌することが好ましい。
反応終了後、反応生成物である式(2)で表される飽和ジエポキシ化合物は、例えば、ろ過、濃縮、蒸留、抽出、晶析、再結晶、吸着、カラムクロマトグラフィーなどの分離精製手段やこれらを組み合わせた手段により分離精製できる。
また、(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合体を使用した場合は、反応終了後にろ過、洗浄することにより触媒を容易に回収、再利用することができる。
また、(メタ)アクリロイルオキシ化合物(7)と(メタ)アクリロイルオキシイソアロキサジン化合物(8)の共重合体を使用した場合は、反応終了後にろ過、洗浄することにより触媒を容易に回収、再利用することができる。
以下、実施例により本発明を具体的に説明するが、本発明はこれらに限定されるものではない。
(実施例1)
磁気攪拌子を入れた15mmφガラス製試験管(反応器)に、被還元基質としての1,2−ビス(3,4−エポキシシクロへキシル)エチレン0.25ミリモルと、酸素酸化触媒であるp−トルエンスルホン酸一水和物0.0125ミリモル(0.05当量)と、ヒドラジン一水和物1.0ミリモル(4当量)と、溶媒であるアセトニトリル2.0mLとを仕込んだ。
上記試験管に酸素ガスを満たしたガスバックを取り付け、35℃に温度調節した恒温槽に入れ、同温度で攪拌しながら反応させた。48時間後にガスクロマトグラフィー分析により、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの98%が消費され、水素化生成物である1,2−ビス(3,4−エポキシシクロへキシル)エタンのみが生成していることを確認した。
反応の終了を確認した後、反応液にクロロホルムを加え、水で洗浄した後に、クロロホルムを減圧留去した。その結果、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率96%で得られた。
ガスクロマトグラフィーの測定条件
装置:GC−2010Plus(島津製作所社製)
検出器:水素炎イオン化検出
分析カラム:DB−1(Agilent Technologies社製、内径0.25mm、長さ30m、膜厚0.25μm)
カラム温度:100℃から270℃まで10℃/分で昇温
キャリヤーガス:ヘリウム
磁気攪拌子を入れた15mmφガラス製試験管(反応器)に、被還元基質としての1,2−ビス(3,4−エポキシシクロへキシル)エチレン0.25ミリモルと、酸素酸化触媒であるp−トルエンスルホン酸一水和物0.0125ミリモル(0.05当量)と、ヒドラジン一水和物1.0ミリモル(4当量)と、溶媒であるアセトニトリル2.0mLとを仕込んだ。
上記試験管に酸素ガスを満たしたガスバックを取り付け、35℃に温度調節した恒温槽に入れ、同温度で攪拌しながら反応させた。48時間後にガスクロマトグラフィー分析により、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの98%が消費され、水素化生成物である1,2−ビス(3,4−エポキシシクロへキシル)エタンのみが生成していることを確認した。
反応の終了を確認した後、反応液にクロロホルムを加え、水で洗浄した後に、クロロホルムを減圧留去した。その結果、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率96%で得られた。
ガスクロマトグラフィーの測定条件
装置:GC−2010Plus(島津製作所社製)
検出器:水素炎イオン化検出
分析カラム:DB−1(Agilent Technologies社製、内径0.25mm、長さ30m、膜厚0.25μm)
カラム温度:100℃から270℃まで10℃/分で昇温
キャリヤーガス:ヘリウム
(実施例2)
実施例1において、酸素酸化触媒を添加しないこと、反応時間を72時間に変えた以外は実施例1と同様に反応、後処理を行ったところ、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率92%で得られた。
実施例1において、酸素酸化触媒を添加しないこと、反応時間を72時間に変えた以外は実施例1と同様に反応、後処理を行ったところ、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率92%で得られた。
(実施例3)
実施例1において、酸素酸化触媒をビス(トリフルオロメタンスルホン酸)イミド0.005ミリモル(0.02当量)に変えた以外は実施例1と同様に反応、後処理を行ったところ、1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率95%で得られた。
実施例1において、酸素酸化触媒をビス(トリフルオロメタンスルホン酸)イミド0.005ミリモル(0.02当量)に変えた以外は実施例1と同様に反応、後処理を行ったところ、1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率95%で得られた。
(実施例4)
15mmφガラス製試験管(反応器)に、被還元基質としての1,2−ビス(3,4−エポキシシクロへキシル)エチレン0.25ミリモルと、酸素酸化触媒である5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオン0.005ミリモル(0.02当量)を保持させたアンバーリスト 15JWETと、ヒドラジン一水和物1.0ミリモル(4当量)と、溶媒であるアセトニトリル2.0mLとを仕込んだ。
上記試験管に酸素ガスを満たしたガスバックを取り付け、35℃に温度調節した恒温槽に入れ、同温度で1000rpmで攪拌しながら反応させた。30時間後にガスクロマトグラフィー分析により、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが93%で生成していることを確認した。
反応の終了を確認した後、反応液にクロロホルムを加え、水で洗浄した後に、クロロホルムを減圧留去し、濃縮残渣から残留触媒をシリカゲルカラムクロマトグラフィーで除いた結果、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率82%で得られた。
15mmφガラス製試験管(反応器)に、被還元基質としての1,2−ビス(3,4−エポキシシクロへキシル)エチレン0.25ミリモルと、酸素酸化触媒である5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオン0.005ミリモル(0.02当量)を保持させたアンバーリスト 15JWETと、ヒドラジン一水和物1.0ミリモル(4当量)と、溶媒であるアセトニトリル2.0mLとを仕込んだ。
上記試験管に酸素ガスを満たしたガスバックを取り付け、35℃に温度調節した恒温槽に入れ、同温度で1000rpmで攪拌しながら反応させた。30時間後にガスクロマトグラフィー分析により、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの96%が消費され、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが93%で生成していることを確認した。
反応の終了を確認した後、反応液にクロロホルムを加え、水で洗浄した後に、クロロホルムを減圧留去し、濃縮残渣から残留触媒をシリカゲルカラムクロマトグラフィーで除いた結果、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率82%で得られた。
(実施例5)
実施例4において、p−トルエンスルホン酸1水和物0.0125ミリモル(0.05当量)を酸素酸化触媒として追加し、反応時間を48時間、ガスバック内のガスを空気とした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの93%が消費され、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率90%で生成していることを確認した。
実施例4において、p−トルエンスルホン酸1水和物0.0125ミリモル(0.05当量)を酸素酸化触媒として追加し、反応時間を48時間、ガスバック内のガスを空気とした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの93%が消費され、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率90%で生成していることを確認した。
(実施例6)
実施例4において、酸素酸化触媒を、リボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物0.005ミリモル(リボフラビンテトラメタクリレート基準、0.02当量)に変え、700rpmで振とうさせ、反応時間を50時間とした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの79%が消費されていることを確認し、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率76%で生成していることを確認した。
実施例4において、酸素酸化触媒を、リボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物0.005ミリモル(リボフラビンテトラメタクリレート基準、0.02当量)に変え、700rpmで振とうさせ、反応時間を50時間とした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの79%が消費されていることを確認し、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率76%で生成していることを確認した。
(実施例7)
実施例4において、酸素酸化触媒を5−エチル−3,7,8,10−テトラメチルルミフラビニウム過塩素酸塩に変え、反応時間を45時間にした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの94%が消費されていることを確認し、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率88%で生成していることを確認した。その後の後処理により、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率77%で得られた。
実施例4において、酸素酸化触媒を5−エチル−3,7,8,10−テトラメチルルミフラビニウム過塩素酸塩に変え、反応時間を45時間にした以外は実施例4と同様に反応、後処理を行った。その結果、被還元基質である1,2−ビス(3,4−エポキシシクロへキシル)エチレンの94%が消費されていることを確認し、目的物である1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率88%で生成していることを確認した。その後の後処理により、1,2−ビス(3,4−エポキシシクロへキシル)エタンが収率77%で得られた。
なお、実施例4で用いた5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオン0.005ミリモル(0.02当量)を保持させたアンバーリスト 15JWET、実施例6で用いたリボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物、及び実施例7で用いた5−エチル−3,7,8,10−テトラメチルルミフラビニウム過塩素酸塩は、それぞれ以下の合成例1、合成例2、及び合成例3によって製造した。
(合成例1)5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオンを保持させたアンバーリスト 15JWET
三方コックを取り付け、攪拌子を入れた50mLナス型フラスコ(反応器)に、3−メチルルミフラビン0.60mmolと、5%パラジウム炭素0.12mmolと、アセトアルデヒド24mmolと、エタノール12mLと、濃塩酸1mLと、水11mLを仕込んだ。
上記反応器に水素ガスを満たしたガスバックを取り付け、室温で24時間攪拌して反応させた。反応液をセライト545に通じて、触媒を取り除き、得られたろ液を1L三角フラスコに入れ、水で30倍に希釈し、攪拌子を入れて、空気下で3時間攪拌した。この溶液を一部取り出し紫外可視吸収スペクトルを測定したところ、5−エチル−3,7,8,10−テトラメチルルミフラビニウム塩が生成していることを確認した。
上記水溶液に、カチオン交換型イオン交換樹脂であるアンバーリスト15JWET1.63gを入れ、室温で6時間振とうさせた。ろ過によりイオン交換樹脂を取り出し、水20mL、メタノール20mL、水20mLで順次洗浄した後、凍結乾燥により、5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオンを保持させたアンバーリスト 15JWET0.851gを得た。元素分析値から、イオン交換樹脂中のフラビンの含有量を0.32mmol/gと決定した。
三方コックを取り付け、攪拌子を入れた50mLナス型フラスコ(反応器)に、3−メチルルミフラビン0.60mmolと、5%パラジウム炭素0.12mmolと、アセトアルデヒド24mmolと、エタノール12mLと、濃塩酸1mLと、水11mLを仕込んだ。
上記反応器に水素ガスを満たしたガスバックを取り付け、室温で24時間攪拌して反応させた。反応液をセライト545に通じて、触媒を取り除き、得られたろ液を1L三角フラスコに入れ、水で30倍に希釈し、攪拌子を入れて、空気下で3時間攪拌した。この溶液を一部取り出し紫外可視吸収スペクトルを測定したところ、5−エチル−3,7,8,10−テトラメチルルミフラビニウム塩が生成していることを確認した。
上記水溶液に、カチオン交換型イオン交換樹脂であるアンバーリスト15JWET1.63gを入れ、室温で6時間振とうさせた。ろ過によりイオン交換樹脂を取り出し、水20mL、メタノール20mL、水20mLで順次洗浄した後、凍結乾燥により、5−エチル−3,7,8,10−テトラメチルルミフラビニウムカチオンを保持させたアンバーリスト 15JWET0.851gを得た。元素分析値から、イオン交換樹脂中のフラビンの含有量を0.32mmol/gと決定した。
(合成例2)リボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物の合成
18mmφガラス製試験管(反応器)に、リボフラビンテトラメタクリレート0.25mmolと、エチレングリコールジメタクリレート4.54mmolと、溶媒であるジメチルホルムアミド3.25mLおよびジグライム2mLと、重合開始剤としての2,2’−アゾビス(イソブチロニトリル)0.08mmolを仕込んだ。
上記試験管を窒素ガスでバブリングした後、80℃に温度調節したオイルバス中で12時間加熱して反応させた。
生成した黄色い個体を粉砕し、25mmφ円筒ろ紙に入れ、ソックスレー抽出装置を用いて、テトラヒドロフラン100mLで2時間、メタノール100mLで2時間、ジエチルエーテル100mLで1時間、順次洗浄した後、減圧下、80℃で12時間乾燥させて、リボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物0.95gを得た。元素分析値より、共重合体中のフラビンの含有量を0.265mmol/gと決定した。
18mmφガラス製試験管(反応器)に、リボフラビンテトラメタクリレート0.25mmolと、エチレングリコールジメタクリレート4.54mmolと、溶媒であるジメチルホルムアミド3.25mLおよびジグライム2mLと、重合開始剤としての2,2’−アゾビス(イソブチロニトリル)0.08mmolを仕込んだ。
上記試験管を窒素ガスでバブリングした後、80℃に温度調節したオイルバス中で12時間加熱して反応させた。
生成した黄色い個体を粉砕し、25mmφ円筒ろ紙に入れ、ソックスレー抽出装置を用いて、テトラヒドロフラン100mLで2時間、メタノール100mLで2時間、ジエチルエーテル100mLで1時間、順次洗浄した後、減圧下、80℃で12時間乾燥させて、リボフラビンテトラメタクリレートとエチレングリコールジメタクリレートの共重合物0.95gを得た。元素分析値より、共重合体中のフラビンの含有量を0.265mmol/gと決定した。
(合成例3)5−エチル−3,7,8,10−テトラメチルルミフラビニウム過塩素酸塩の合成
Chemistry−An Asian Journal、Vol.1、No.1−2、pp.136−147、2006.に記載の方法に従い合成した。
Chemistry−An Asian Journal、Vol.1、No.1−2、pp.136−147、2006.に記載の方法に従い合成した。
Claims (7)
- 下記式(3)若しくは下記式(5)で表されるイソアロキサジン骨格を有する化合物、又は下記式(4)若しくは下記式(6)で表されるアロキサジン骨格を有する化合物を触媒として用いて行う、請求項1記載の飽和ジエポキシ化合物の製造方法。
R22〜R25は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R26は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R21〜R26のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
R32〜R35は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R36は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R31〜R36のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。)
R42〜R45は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R46及びR47は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R41〜R47うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L1は一価の陰イオンを示す。)
R52〜R55は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R56及びR57は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R51〜R57うちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。
L2は一価の陰イオンを示す。) - 下記式(7)で表される(メタ)アクリロイルオキシ基を有する化合物と、下記式(8)で表される(メタ)アクリロイルオキシ基及びイソアロキサジン骨格を有する化合物との共重合体を触媒として用いて行う、請求項1記載の飽和ジエポキシ化合物の製造方法。
Aは、水素原子又はメチル基を示し、nが2以上の場合、n個のAは、それぞれ同一であっても異なっていてもよく、
Xは、置換基を有していてもよい飽和または不飽和のn価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のn価の非環式炭化水素基、置換基を有していてもよいn価の芳香族炭化水素基、置換基を有していてもよいn価のヘテロ環基、(ポリ)アルキレンオキシ基、又はこれらの基の2以上が連結して形成されるn価の基を示す。)
Bは、水素原子又はメチル基を示し、mが2以上の場合、m個のBは、それぞれ同一であっても異なっていてもよく、
Yは、置換基を有していてもよい飽和または不飽和のm+1価の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和のm+1価の非環式炭化水素基、置換基を有していてもよいm+1価の芳香族炭化水素基、又は置換基を有していてもよいm+1価のヘテロ環基を示し、
R61〜R64は、それぞれ独立して、水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよいヘテロ環基、カルボキシル基、アミド基、エステル基、シアノ基、オキソ基、ホルミル基、スルホン酸基、リン酸基、ヒドロキシル基、メルカプト基、アミノ基、アルコキシ基、アルキルチオ基、又はハロゲン基を示し、
R65は水素原子、置換基を有していてもよい飽和または不飽和の脂環式炭化水素基、置換基を有していてもよい飽和または不飽和の非環式炭化水素基、置換基を有していてもよい芳香族炭化水素基、又は置換基を有していてもよいヘテロ環基を示す。
但し、R61〜R65のうちの二つで縮合炭化水素環若しくは縮合複素環を形成していてもよい。) - 前記式(5)で表されるイソアロキサジン骨格を有する化合物、又は前記式(6)で表されるアロキサジン骨格を有する化合物をカチオン交換型イオン交換樹脂とイオン交換して保持させたものを触媒として用いて行う、請求項1記載の飽和ジエポキシ化合物の製造方法。
- 酸を触媒として用いて行う、請求項1記載の飽和ジエポキシ化合物の製造方法。
- 酸が有機化合物である、請求項5記載の飽和ジエポキシ化合物の製造方法。
- 請求項2〜4の何れか1項に記載の触媒の少なくとも一つと、請求項5又は6に記載の酸との組み合わせを触媒として用いて行う、請求項1記載の飽和ジエポキシ化合物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015079601A JP2016199486A (ja) | 2015-04-08 | 2015-04-08 | ジエポキシ化合物の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015079601A JP2016199486A (ja) | 2015-04-08 | 2015-04-08 | ジエポキシ化合物の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2016199486A true JP2016199486A (ja) | 2016-12-01 |
Family
ID=57424178
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015079601A Pending JP2016199486A (ja) | 2015-04-08 | 2015-04-08 | ジエポキシ化合物の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2016199486A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018066557A1 (ja) | 2016-10-07 | 2018-04-12 | ミツミ電機株式会社 | センサチップ、起歪体、力覚センサ装置 |
-
2015
- 2015-04-08 JP JP2015079601A patent/JP2016199486A/ja active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018066557A1 (ja) | 2016-10-07 | 2018-04-12 | ミツミ電機株式会社 | センサチップ、起歪体、力覚センサ装置 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12065422B2 (en) | Reagents and process for direct C—H functionalization | |
| JP6020772B1 (ja) | 混合物及び重合性化合物の製造方法 | |
| EP2036899B1 (en) | Method for producing cyclic disulfonic acid ester | |
| JP2016199486A (ja) | ジエポキシ化合物の製造方法 | |
| JP5090107B2 (ja) | テトラキス(アリルオキシフェニル)炭化水素化合物の製造方法 | |
| JP6681007B2 (ja) | 過酸化水素の安定化剤を含有するエポキシ化合物の製造方法 | |
| JP2014205662A (ja) | (メタ)アクリル酸エステルの製造方法 | |
| JPWO2018025892A1 (ja) | 重合性トリプチセン誘導体化合物 | |
| CN114409714B (zh) | 一种合成1,3-二取代平面手性金属茂化合物的方法 | |
| JP5727830B2 (ja) | スルホニウム化合物 | |
| JP4905917B2 (ja) | ビニルエーテル化合物の製造法 | |
| JP5926130B2 (ja) | ジオレフィン化合物の製造方法、及びそれを含むジエポキシ化合物の製造方法 | |
| WO2014034628A1 (ja) | 脂環式エポキシ化合物及びその製造方法 | |
| JP2012201611A5 (ja) | ||
| JPWO2016063957A1 (ja) | デカリン誘導体及びその製造方法 | |
| JP5362208B2 (ja) | ビニルエーテル基を有するアダマンタン誘導体 | |
| JP2015017218A (ja) | 4−メチルテトラヒドロピランを溶媒とするカチオン重合方法 | |
| JP6679763B2 (ja) | 重合性組成物、及び、重合性組成物の製造方法 | |
| JP2019108319A (ja) | フルオロアルカンの製造方法 | |
| JP5178098B2 (ja) | 脂環式ビニルエーテル化合物 | |
| JP2018095591A (ja) | スルホニウム化合物ならびに熱重合開始剤 | |
| WO2025216186A1 (ja) | ヒドロキシビオチン誘導体及びビニルビオチン誘導体の製造方法 | |
| JP5499947B2 (ja) | ポリ(5−(メタ)アクリロイル−2−アザアダマンタン−n−オキシル)の製造方法 | |
| JP6845417B2 (ja) | ナフタレン型エポキシ化合物の製造方法及びナフタレン型エポキシ化合物 | |
| WO2023054429A1 (ja) | アルキルフランカルボン酸エステルの製造方法 |