JP2013536282A - ケイ酸塩発光材料及びその製造方法 - Google Patents
ケイ酸塩発光材料及びその製造方法 Download PDFInfo
- Publication number
- JP2013536282A JP2013536282A JP2013523453A JP2013523453A JP2013536282A JP 2013536282 A JP2013536282 A JP 2013536282A JP 2013523453 A JP2013523453 A JP 2013523453A JP 2013523453 A JP2013523453 A JP 2013523453A JP 2013536282 A JP2013536282 A JP 2013536282A
- Authority
- JP
- Japan
- Prior art keywords
- fluorescent powder
- source compound
- mol
- silicate
- silicate fluorescent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/08—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials
- C09K11/77—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing rare earth metals
- C09K11/7766—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing rare earth metals containing two or more rare earth metals
- C09K11/77742—Silicates
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/08—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials
- C09K11/87—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing platina group metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/70—Nanostructure
- Y10S977/773—Nanoparticle, i.e. structure having three dimensions of 100 nm or less
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Luminescent Compositions (AREA)
Abstract
【選択図】 図2
Description
M0金属ナノ粒子コロイドゾルを得る工程と、
化学式M2 aM3 bSicO[a+3(b+x)/2+2c]:xCe3+,yM0(式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc、又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd又はCuのナノ粒子から選ばれる1種である。)における対応元素の化学量論比により、M2源化合物、M3源化合物、Si源化合物、Ce源化合物及びM0金属ナノ粒子コロイドゾルを秤量する工程と、
Si源化合物のアルコール溶液にM0金属ナノ粒子コロイドゾルとM2源化合物、M3源化合物及びCe源化合物の溶液を加入して混合液を得る工程と、
混合液のpH値を、酸性を呈すまで調整し、水浴で加熱し反応させた後、乾燥して前駆体を得る工程と、
前駆体を仮焼する工程と、
仮焼された前駆体を、還元雰囲気の下で焙焼して、前記ケイ酸塩蛍光粉を得る工程と、
を備えることを特徴とする。
S1:M0金属ナノ粒子コロイドゾルを得る工程と、
S2:化学式M2 aM3 bSicOa+3(b+x)/2+2c:xCe3+,yM0(式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc、又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd又はCuのナノ粒子から選ばれる1種である。)における対応元素の化学量論比により、M2源化合物、M3源化合物、Si源化合物、Ce源化合物とM0の金属ナノ粒子コロイドゾルを秤量する工程と、
S3:Si源化合物のアルコール溶液にM0金属ナノ粒子コロイドゾルとM2源化合物、M3源化合物及びCe源化合物の溶液を加入して混合液を得る工程と、
S4:混合液のpH値を、酸性を呈すまで調整し、水浴で加熱し反応させた後、乾燥して前駆体を得る工程と、
S5:前駆体を仮焼する工程と、
S6:仮焼された前駆体を、還元雰囲気の下で焙焼して前記ケイ酸塩蛍光粉を得る工程と、
を備える。
1)M0源化合物を秤量して溶媒に溶解して、1×10−4mol/L〜1×10−2mol/Lの液体に調製・希釈し、前記溶媒は、水及び揮発性のアルコールであることが好ましく、その中で、揮発性のアルコールは、エタノールであることが好ましいが、これに限定されるものではない。
化学式がCa2.9Sc2Si3O12:0.1Ce3+,1×10−3Agであるケイ酸塩蛍光粉
硝酸銀3.4mgと、クエン酸ナトリウム35.28mgを秤量し、脱イオン水18.4mLに溶解させ、1.5分間撹拌した後、硼水素化ナトリウム3.8mgをエタノール10mLに溶解して得られた0.01mol/Lの硼水素化ナトリウムのアルコール溶液1.6mLをゆっくりと滴下した。攪拌を続けながら2分間反応させて、1×10−3mol/LのAgナノ粒子コロイドゾルを得た。ポリビニルピロリドン(PVP)0.01gを秤量して脱イオン水7mLに溶解させ、その後、Ag金属ナノ粒子2mLを加入し、12時間撹拌した。6×10−3molのテトラエチル・オルトシリケートを量り取って10mlのエタノールに溶解させ、その後、撹拌しながら、処理されたAg金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.9mL、1mol/Lの硝酸スカンジウム溶液4mL、0.05mol/Lの硝酸セリウム溶液4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で12時間乾燥して前駆体を得、得られた前駆体を研磨してマッフル炉に設置して900℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1300℃で5時間焼結して還元させ、室温まで冷却して、Ca2.9Sc2Si3O12:0.1Ce3+,1×10−3Agのケイ酸塩蛍光粉を得た。
化学式がCa2Sr0.8Sc1.8Si2.9O11.315:0.01Ce3+,1×10−4Auであるケイ酸塩蛍光粉
塩化金酸1.64mgを秤量してエタノール7.5mLに溶解し、完全に溶解した後、撹拌しながら、クエン酸ナトリウム5.6mg及び臭化ヘキサデシルトリメチルアンモニウム2.4mgのを加入した。硼水素化ナトリウム0.76mgを秤量してエタノール10mLに溶解させて、濃度0.002mol/Lの硼水素化ナトリウムのアルコール溶液10mLを得た。マグネチック撹拌をしながら、塩化金酸のアルコール溶液に硼水素化ナトリウムアルコール溶液2.5mLを加入し、30分間反応を続けて、Au含有量4×10−4mol/LのAuナノ粒子コロイドゾルを得、その後、ポリビニルピロリドン0.2gを秤量して脱イオン水5mLに溶解させ、溶解した後、4×10−4mol/LのAu金属ナノ粒子0.5mLを加入し、24時間撹拌した。5.8×10−3molのテトラエチル・オルトシリケートを量り取ってエタノール10mlに溶解し、その後、撹拌しながら、処理されたAu金属ナノ粒子、2mol/Lの塩化カルシウム溶液2mL、2mol/Lの硝酸ストロンチウム溶液0.8mL、1mol/Lの硝酸スカンジウム溶液3.6mL、0.05mol/Lの硝酸セリウム溶液0.4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を60℃の水浴に入れて5時間反応させ、120℃の焙炉で8時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して700℃で5時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1500℃で2時間焼結して還元させ、室温まで冷却して、Ca2Sr0.8Sc1.8Si2.9O11.315:0.01Ce3+,1×10−4Auのケイ酸塩蛍光粉を得た。
化学式がCa1.5Ba0.7Sr1.0Sc1.5Y0.6Si3.3O13.025:0.05Ce3+,2×10−3Ptであるケイ酸塩蛍光粉
塩化白金酸5.2mgを秤量してエタノール17mLに溶解させ、完全に溶解した後、撹拌しながら、クエン酸ナトリウム8mg及びドデシルスルホン酸ナトリウム1.2mgを加入し、その後、硼水素化ナトリウム0.4mgをエタノール10mLに溶解して得られた1×10−3mol/Lの硼水素化ナトリウムのアルコール溶液0.4mLをゆっくりと滴下し、5分間反応させ、さらに1×10−2mol/Lのヒドラジン水和物溶液2.6mLを加入して40分間反応させて、Pt含有量5×10−4mol/LであるPtナノ粒子コロイドゾルを得た。3−アミノプロピルトリメトキシシラン0.15gを秤量して脱イオン水6mLに溶解させ、5×10−4mol/LのPt金属ナノ粒子8mLを加入し、18時間撹拌した。6.6×10−3molのテトラエチル・オルトシリケートを量取ってエタノール10mlに溶解させ、その後、撹拌しながら、処理されたPt金属ナノ粒子、2mol/Lの硫酸ストロンチウム溶液1.5mL、2mol/Lの硝酸バリウム溶液0.7mL、2mol/Lの硝酸ストロンチウム溶液1mL、1mol/Lの塩化イットリウム溶液3mL、0.05mol/Lの硝酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を75℃の水浴に入れて4時間反応させ、110℃の焙炉で3時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して1000℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1250℃で12時間焼結して還元させ、室温まで冷却して、Ca1.5Ba0.7Sr1.0Sc1.5Y0.6Si3.3O13.025:0.05Ce3+,2×10−3Ptの蛍光粉を得た。6.6×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させ、その後、撹拌しながら処理されたAg金属ナノ粒子、2mol/Lの硝酸カルシウム溶液1.5mL、2mol/Lの硝酸バリウム溶液0.7mL、2mol/Lの硝酸ストロンチウム溶液1mL、1mol/Lの硝酸スカンジウム溶液2mL、0.05mol/Lの硝酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で3時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して1000℃で3時間熱処理を行い、さらに、チューブ炉でCOの弱い還元雰囲気の下、1250℃で12時間焼結して還元させ、室温まで冷却して、Ca1.5Ba0.7Sr1.0Sc1.5Y0.6Si3.3O13.025:0.05Ce3+,2×10−3Ptのケイ酸塩蛍光粉を得た。
化学式がCa2.74Mg0.06Sc2Si3.1O12.3:0.2Ce3+,1×10−2Pdであるケイ酸塩蛍光粉
塩化パラジウム0.43gを秤量して脱イオン水15mLに溶解させ、完全に溶解した後、撹拌しながら、クエン酸ナトリウム1.1g及びドデシル硫酸ナトリウム0.4gを加入し、その後、硼水素化ナトリウム0.038gをエタノール10mLに溶解して得られた0.1mol/Lの硼水素化ナトリウムのアルコール溶液5mLをゆっくりと滴下し、20分間反応させて、Pd含有量5×10−3mol/LであるPdナノ粒子コロイドゾルを得た。ポリビニルピロリドン0.3gを秤量して脱イオン水5mLに溶解させ、そして5×10−3mol/LのPd金属ナノ粒子4mLを加入し、3時間撹拌した。6.2×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させ、その後、撹拌しながら、処理されたPd金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.74mL、0.2mol/Lの硝酸マグネシウム溶液0.6mL、1mol/Lの硝酸スカンジウム溶液4mL、0.2mol/Lの硫酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を95℃の水浴に入れて3時間反応させ、80℃の焙炉で5時間乾燥して得られた前駆体を研磨した後、マッフル炉に設置して800℃で5時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1400℃で4時間焼結して還元させ、室温まで冷却して、Ca2.74Mg0.06Sc2Si3.1O12.3:0.2Ce3+,1×10−2Pdのケイ酸塩蛍光粉を得た。
化学式がCa1.0Sr1.0Mg0.9Sc1.9Si2.95O11.77:0.08Ce3+,8×10−4Cuであるケイ酸塩蛍光粉
硝酸銅1.6mgを秤量し、エタノール16mLに溶解させ、完全に溶解した後、撹拌しながらポリビニルピロリドン12mgを加入し、その後、硼水素化ナトリウム0.4mgをエタノール10mLに溶解して得られた1×10−3mol/Lの硼水素化ナトリウムのアルコール溶液4mLをゆっくりと滴下し、攪拌を続けてながら2分間反応させて、4×10−4mol/LのCuナノ粒子コロイドゾルを得た。5.9×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解した後、撹拌しながら、処理されたCu金属ナノ粒子、2mol/Lの硝酸カルシウム溶液1mL、2mol/Lの硝酸ストロンチウム溶液1mL、0.3mol/Lの硝酸マグネシウム溶液6mL、1mol/Lの硝酸スカンジウム溶液3.8mL、0.04mol/Lの硝酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて3時間反応させ、100℃の焙炉で8時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して750℃で5時間熱処理を行い、さらに、チューブ炉でH2の弱い還元雰囲気の下、1350℃で8時間焼結して還元させ、室温まで冷却して、Ca1.0Sr1.0Mg0.9Sc1.9Si2.95O11.77:0.08Ce3+,8×10−4Cuのケイ酸塩蛍光粉を得た。
化学式がCa2.88Sc1.94Y0.06Si3O12:0.12Ce3+,8×10−3Agであるケイ酸塩蛍光粉
硝酸銀6.8mgと、クエン酸ナトリウム70.56mgを秤量して、脱イオン水18.4mLに溶解させ、1.5分間撹拌した後、硼水素化ナトリウム7.6mgをエタノール10mLに溶解して得られた0.01mol/Lの硼水素化ナトリウムのアルコール溶液3.2mLをゆっくりと滴下した。攪拌を続けてながら2分間反応させて、2×10−3mol/LのAgナノ粒子コロイドゾルを得た。ポリビニルピロリドン0.01gを秤量して脱イオン水7mLに溶解させ、その後、Ag金属ナノ粒子8mLを加入し、6時間撹拌した。6×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させた後、撹拌しながら、処理されたAg金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.88mL、1mol/Lの硝酸スカンジウム溶液3.88mL、0.06mol/Lの硝酸イットリウム溶液2mL、0.2mol/Lの塩化セリウム溶液1.2mlのを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で6時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して800℃で6時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1450℃で5時間焼結して還元させ、室温まで冷却して、Ca2.88Sc1.94Y0.06Si3O12:0.12Ce3+,8×10−3Agのケイ酸塩蛍光粉を得た。
化学式がCa2.9Sc2Si3O12:0.1Ce3+であるケイ酸塩蛍光粉
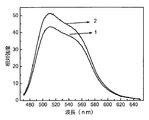
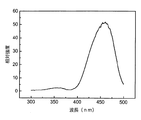
6×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させ、その後、撹拌しながら、2mol/Lの硝酸カルシウム溶液2.9mL、1mol/Lの硝酸スカンジウム溶液4mL、0.05mol/Lの硝酸セリウム溶液4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で12時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して900℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1300℃で5時間焼結して還元させ、室温まで冷却して、Ca2.9Sc2Si3O12:0.1Ce3+のケイ酸塩蛍光粉を得た。該ケイ酸塩蛍光粉の460nm青色光励起の下での発光スペクトルは、図2に示すグラフ2の通りである。発光スペクトルグラフから、本比較例のケイ酸塩蛍光粉の発光強度が、実施例1で製造したケイ酸塩蛍光粉の発光強度より弱いことが確認された。
M0金属ナノ粒子コロイドゾルを得る工程と、
化学式M2 aM3 bSicO[a+3(b+x)/2+2c]:xCe3+,yM0(式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc、又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd又はCuのナノ粒子から選ばれる1種である。)における対応元素の化学量論比により、M2源化合物、M3源化合物、Si源化合物、Ce源化合物及びM0金属ナノ粒子コロイドゾルを秤量する工程と、
Si源化合物のアルコール溶液にM0金属ナノ粒子コロイドゾルとM2源化合物、M3源化合物及びCe源化合物の溶液を加入して混合液を得る工程と、
混合液のpH値を、酸性を呈すまで調整し、水浴で加熱し反応させた後、乾燥して前駆体を得る工程と、
前駆体を仮焼する工程と、
仮焼された前駆体を、還元雰囲気の下で焙焼して、前記ケイ酸塩蛍光粉を得る工程と、
を備えることを特徴とする。
S1:M0金属ナノ粒子コロイドゾルを得る工程と、
S2:化学式M2 aM3 bSicOa+3(b+x)/2+2c:xCe3+,yM0(式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc、又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd又はCuのナノ粒子から選ばれる1種である。)における対応元素の化学量論比により、M2源化合物、M3源化合物、Si源化合物、Ce源化合物とM0の金属ナノ粒子コロイドゾルを秤量する工程と、
S3:Si源化合物のアルコール溶液にM0金属ナノ粒子コロイドゾルとM2源化合物、M3源化合物及びCe源化合物の溶液を加入して混合液を得る工程と、
S4:混合液のpH値を、酸性を呈すまで調整し、水浴で加熱し反応させた後、乾燥して前駆体を得る工程と、
S5:前駆体を仮焼する工程と、
S6:仮焼された前駆体を、還元雰囲気の下で焙焼して前記ケイ酸塩蛍光粉を得る工程と、
を備える。
1)M0源化合物を秤量して溶媒に溶解して、1×10−4mol/L〜1×10−2mol/Lの液体に調製・希釈し、前記溶媒は、水及び揮発性のアルコールであることが好ましく、その中で、揮発性のアルコールは、エタノールであることが好ましいが、これに限定されるものではない。
化学式がCa2.9Sc2Si3O12:0.1Ce3+,1×10−3Agであるケイ酸塩蛍光粉
硝酸銀3.4mgと、クエン酸ナトリウム35.28mgを秤量し、脱イオン水18.4mLに溶解させ、1.5分間撹拌した後、硼水素化ナトリウム3.8mgをエタノール10mLに溶解して得られた0.01mol/Lの硼水素化ナトリウムのアルコール溶液1.6mLをゆっくりと滴下した。攪拌を続けながら2分間反応させて、1×10−3mol/LのAgナノ粒子コロイドゾルを得た。ポリビニルピロリドン(PVP)0.01gを秤量して脱イオン水7mLに溶解させ、その後、Ag金属ナノ粒子2mLを加入し、12時間撹拌した。6×10−3molのテトラエチル・オルトシリケートを量り取って10mlのエタノールに溶解させ、その後、撹拌しながら、処理されたAg金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.9mL、1mol/Lの硝酸スカンジウム溶液4mL、0.05mol/Lの硝酸セリウム溶液4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で12時間乾燥して前駆体を得、得られた前駆体を研磨してマッフル炉に設置して900℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1300℃で5時間焼結して還元させ、室温まで冷却して、Ca2.9Sc2Si3O12:0.1Ce3+,1×10−3Agのケイ酸塩蛍光粉を得た。
化学式がCa2Sr0.8Sc1.8Si2.9O11.315:0.01Ce3+,1×10−4Auであるケイ酸塩蛍光粉
塩化金酸1.64mgを秤量してエタノール7.5mLに溶解し、完全に溶解した後、撹拌しながら、クエン酸ナトリウム5.6mg及び臭化ヘキサデシルトリメチルアンモニウム2.4mgのを加入した。硼水素化ナトリウム0.76mgを秤量してエタノール10mLに溶解させて、濃度0.002mol/Lの硼水素化ナトリウムのアルコール溶液10mLを得た。マグネチック撹拌をしながら、塩化金酸のアルコール溶液に硼水素化ナトリウムアルコール溶液2.5mLを加入し、30分間反応を続けて、Au含有量4×10−4mol/LのAuナノ粒子コロイドゾルを得、その後、ポリビニルピロリドン0.2gを秤量して脱イオン水5mLに溶解させ、溶解した後、4×10−4mol/LのAu金属ナノ粒子0.5mLを加入し、24時間撹拌した。5.8×10−3molのテトラエチル・オルトシリケートを量り取ってエタノール10mlに溶解し、その後、撹拌しながら、処理されたAu金属ナノ粒子、2mol/Lの塩化カルシウム溶液2mL、2mol/Lの硝酸ストロンチウム溶液0.8mL、1mol/Lの硝酸スカンジウム溶液3.6mL、0.05mol/Lの硝酸セリウム溶液0.4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を60℃の水浴に入れて5時間反応させ、120℃の焙炉で8時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して700℃で5時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1500℃で2時間焼結して還元させ、室温まで冷却して、Ca2Sr0.8Sc1.8Si2.9O11.315:0.01Ce3+,1×10−4Auのケイ酸塩蛍光粉を得た。
化学式がCa1.5Ba0.7Sr1.0Sc1.5Y0.6Si3.3O13.025:0.05Ce3+,2×10−3Ptであるケイ酸塩蛍光粉
塩化白金酸5.2mgを秤量してエタノール17mLに溶解させ、完全に溶解した後、撹拌しながら、クエン酸ナトリウム8mg及びドデシルスルホン酸ナトリウム1.2mgを加入し、その後、硼水素化ナトリウム0.4mgをエタノール10mLに溶解して得られた1×10−3mol/Lの硼水素化ナトリウムのアルコール溶液0.4mLをゆっくりと滴下し、5分間反応させ、さらに1×10−2mol/Lのヒドラジン水和物溶液2.6mLを加入して40分間反応させて、Pt含有量5×10−4mol/LであるPtナノ粒子コロイドゾルを得た。3−アミノプロピルトリメトキシシラン0.15gを秤量して脱イオン水6mLに溶解させ、5×10−4mol/LのPt金属ナノ粒子8mLを加入し、18時間撹拌した。6.6×10−3molのテトラエチル・オルトシリケートを量取ってエタノール10mlに溶解させ、その後、撹拌しながら、処理されたPt金属ナノ粒子、2mol/Lの硫酸ストロンチウム溶液1.5mL、2mol/Lの硝酸バリウム溶液0.7mL、2mol/Lの硝酸ストロンチウム溶液1mL、1mol/Lの塩化イットリウム溶液3mL、0.05mol/Lの硝酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を75℃の水浴に入れて4時間反応させ、110℃の焙炉で3時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して1000℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1250℃で12時間焼結して還元させ、室温まで冷却して、Ca1.5Ba0.7Sr1.0Sc1.5Y0.6Si3.3O13.025:0.05Ce3+,2×10−3Ptの蛍光粉を得た。
化学式がCa2.74Mg0.06Sc2Si3.1O12.3:0.2Ce3+,1×10−2Pdであるケイ酸塩蛍光粉
塩化パラジウム0.43gを秤量して脱イオン水15mLに溶解させ、完全に溶解した後、撹拌しながら、クエン酸ナトリウム1.1g及びドデシル硫酸ナトリウム0.4gを加入し、その後、硼水素化ナトリウム0.038gをエタノール10mLに溶解して得られた0.1mol/Lの硼水素化ナトリウムのアルコール溶液5mLをゆっくりと滴下し、20分間反応させて、Pd含有量5×10−3mol/LであるPdナノ粒子コロイドゾルを得た。ポリビニルピロリドン0.3gを秤量して脱イオン水5mLに溶解させ、そして5×10−3mol/LのPd金属ナノ粒子4mLを加入し、3時間撹拌した。6.2×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させ、その後、撹拌しながら、処理されたPd金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.74mL、0.2mol/Lの硝酸マグネシウム溶液0.6mL、1mol/Lの硝酸スカンジウム溶液4mL、0.2mol/Lの硫酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を95℃の水浴に入れて3時間反応させ、80℃の焙炉で5時間乾燥して得られた前駆体を研磨した後、マッフル炉に設置して800℃で5時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1400℃で4時間焼結して還元させ、室温まで冷却して、Ca2.74Mg0.06Sc2Si3.1O12.3:0.2Ce3+,1×10−2Pdのケイ酸塩蛍光粉を得た。
化学式がCa1.0Sr1.0Mg0.9Sc1.9Si2.95O11.77:0.08Ce3+,8×10−4Cuであるケイ酸塩蛍光粉
硝酸銅1.6mgを秤量し、エタノール16mLに溶解させ、完全に溶解した後、撹拌しながらポリビニルピロリドン12mgを加入し、その後、硼水素化ナトリウム0.4mgをエタノール10mLに溶解して得られた1×10−3mol/Lの硼水素化ナトリウムのアルコール溶液4mLをゆっくりと滴下し、攪拌を続けてながら2分間反応させて、4×10−4mol/LのCuナノ粒子コロイドゾルを得た。5.9×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解した後、撹拌しながら、処理されたCu金属ナノ粒子、2mol/Lの硝酸カルシウム溶液1mL、2mol/Lの硝酸ストロンチウム溶液1mL、0.3mol/Lの硝酸マグネシウム溶液6mL、1mol/Lの硝酸スカンジウム溶液3.8mL、0.04mol/Lの硝酸セリウム溶液2mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて3時間反応させ、100℃の焙炉で8時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して750℃で5時間熱処理を行い、さらに、チューブ炉でH2の弱い還元雰囲気の下、1350℃で8時間焼結して還元させ、室温まで冷却して、Ca1.0Sr1.0Mg0.9Sc1.9Si2.95O11.77:0.08Ce3+,8×10−4Cuのケイ酸塩蛍光粉を得た。
化学式がCa2.88Sc1.94Y0.06Si3O12:0.12Ce3+,8×10−3Agであるケイ酸塩蛍光粉
硝酸銀6.8mgと、クエン酸ナトリウム70.56mgを秤量して、脱イオン水18.4mLに溶解させ、1.5分間撹拌した後、硼水素化ナトリウム7.6mgをエタノール10mLに溶解して得られた0.01mol/Lの硼水素化ナトリウムのアルコール溶液3.2mLをゆっくりと滴下した。攪拌を続けてながら2分間反応させて、2×10−3mol/LのAgナノ粒子コロイドゾルを得た。ポリビニルピロリドン0.01gを秤量して脱イオン水7mLに溶解させ、その後、Ag金属ナノ粒子8mLを加入し、6時間撹拌した。6×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させた後、撹拌しながら、処理されたAg金属ナノ粒子、2mol/Lの硝酸カルシウム溶液2.88mL、1mol/Lの硝酸スカンジウム溶液3.88mL、0.06mol/Lの硝酸イットリウム溶液2mL、0.2mol/Lの塩化セリウム溶液1.2mlのを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で6時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して800℃で6時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1450℃で5時間焼結して還元させ、室温まで冷却して、Ca2.88Sc1.94Y0.06Si3O12:0.12Ce3+,8×10−3Agのケイ酸塩蛍光粉を得た。
化学式がCa2.9Sc2Si3O12:0.1Ce3+であるケイ酸塩蛍光粉
6×10−3molのテトラエチル・オルトシリケートを秤量してエタノール10mlに溶解させ、その後、撹拌しながら、2mol/Lの硝酸カルシウム溶液2.9mL、1mol/Lの硝酸スカンジウム溶液4mL、0.05mol/Lの硝酸セリウム溶液4mLを順次に加入し、その後、硝酸でpH値を3〜4に調整した後、該溶液を85℃の水浴に入れて4時間反応させ、100℃の焙炉で12時間乾燥して前駆体を得、得られた前駆体を研磨した後、マッフル炉に設置して900℃で3時間熱処理を行い、さらに、チューブ炉で95%N2+5%H2の弱い還元雰囲気の下、1300℃で5時間焼結して還元させ、室温まで冷却して、Ca2.9Sc2Si3O12:0.1Ce3+のケイ酸塩蛍光粉を得た。該ケイ酸塩蛍光粉の460nm青色光励起の下での発光スペクトルは、図2に示すグラフ2の通りである。発光スペクトルグラフから、本比較例のケイ酸塩蛍光粉の発光強度が、実施例1で製造したケイ酸塩蛍光粉の発光強度より弱いことが確認された。
Claims (10)
- 化学式が、M2 aM3 bSicO[a+3(b+x)/2+2c]:xCe3+,yM0である、ケイ酸塩蛍光粉。
式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc、又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd又はCuのナノ粒子から選ばれる1種である。 - M0金属ナノ粒子コロイドゾルを得る工程と、
化学式M2 aM3 bSicO[a+3(b+x)/2+2c]:xCe3+,yM0(式中、2.8≦a≦3.2、1.8≦b≦2.1、2.9≦c≦3.3、0.01≦x≦0.2、1×10−4≦y≦1×10−2であり、M2はSr、Ba、Mgから選ばれる少なくとも1種とCaとの組み合わせであり、M3はSc又はScとYとの組み合わせであり、M0は金属ナノ粒子を示し、Ag、Au、Pt、Pd、又はCuのナノ粒子から選ばれる1種である。)における対応元素の化学量論比により、M2源化合物、M3源化合物、Si源化合物、Ce源化合物とM0の金属ナノ粒子コロイドゾルを秤量する工程と、
Si源化合物のアルコール溶液にM0の金属ナノ粒子コロイドゾルとM2源化合物、M3源化合物及びCe源化合物の溶液を加入して混合液を得る工程と、
混合液のpH値を、酸性を呈すまで調整し、水浴で加熱し反応させた後、乾燥して前駆体を得る工程と、
前駆体を仮焼する工程と、
仮焼された前駆体を、還元雰囲の下で焙焼して前記ケイ酸塩蛍光粉を得る工程と、
を備える、ケイ酸塩蛍光粉の製造方法。 - 前記Si源化合物は、テトラエチル・オルトシリケートであり、
前記M2源化合物は、M2の硝酸塩、硫酸塩、塩化物から選ばれる少なくとも1種であり、
前記M3源化合物は、M3の硝酸塩、硫酸塩、塩化物から選ばれる少なくとも1種であり、
前記Ce源化合物は、Ceの硝酸塩、硫酸塩、塩化物から選ばれる少なくとも1種であることを特徴とする、請求項2に記載のケイ酸塩蛍光粉の製造方法。 - 前記M0金属ナノ粒子コロイドゾルを得る方法は、
M0源化合物を溶解させ、さらに助剤、還元剤を加入し、反応が終了した後、表面処理剤を加入して処理を行って、M0金属ナノ粒子コロイドゾルを得る工程を含み、
M0金属ナノ粒子コロイドゾルにおける前記助剤の含有量は1.5×10−4g/mL〜2.1×10−3g/mLであり、
前記還元剤の添加量とM0金属粒子とのモル比は、1.2:1〜4.8:1であり、
M0金属ナノ粒子コロイドゾルにおける前記表面処理剤の含有量は1.5×10−4g/mL〜2.1×10−3g/mLであることを特徴とする、請求項2に記載のケイ酸塩蛍光粉の製造方法。 - 前記M0金属ナノ粒子のコロイドゾルを得る工程において、
前記M0源化合物は、硝酸銀、塩化金酸、塩化白金酸、塩化パラジウム、硝酸銅から選ばれる少なくとも1種であり、
前記助剤は、ポリビニルピロリドン、クエン酸ナトリウム、臭化ヘキサデシルトリメチルアンモニウム、ドデシル硫酸ナトリウム、ドデシルスルホン酸ナトリウムから選ばれる少なくとも1種であり、
前記還元剤は、ヒドラジン水和物、アスコルビン酸、又は硼水素化ナトリウムから選ばれる少なくとも1種であり、
前記表面処理剤は、ポリビニルピロリドン、3−アミノプロピルトリメトキシシランから選ばれる少なくとも1種であることを特徴とする、請求項4に記載のケイ酸塩蛍光粉の製造方法。 - 前記混合液の調製工程において、Si源化合物のアルコール溶液におけるアルコールは、エタノールであることを特徴とする、請求項2に記載のケイ酸塩蛍光粉の製造方法。
- 前記前駆体を得る工程において、前記混合液のpH値は3〜6であり、前記水浴で加熱し反応させる際の温度は60〜95℃であり、前記乾燥温度は80〜120℃であることを特徴とする、請求項2に記載のケイ酸塩蛍光粉の製造方法。
- 前記前駆体を得る工程において、前記混合液のpH値を硝酸で調整することを特徴とする、請求項7に記載のケイ酸塩蛍光粉の製造方法。
- 前記前駆体の仮焼温度は700〜1000℃で、仮焼時間は3〜5時間であり、
前記前駆体の還元雰囲気の下での焙焼温度は1250〜1500℃で、焙焼時間が2〜12時間であることを特徴とする、請求項2に記載のケイ酸塩蛍光粉の製造方法。 - 前記還元雰囲気は、窒素と水素の混合ガス雰囲気、一酸化炭素還元雰囲気、水素還元雰囲気から選ばれる1種であることを特徴とする、請求項9に記載のケイ酸塩蛍光粉の製造方法。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/CN2010/075972 WO2012019359A1 (zh) | 2010-08-13 | 2010-08-13 | 硅酸盐发光材料及其制备方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013536282A true JP2013536282A (ja) | 2013-09-19 |
| JP5649730B2 JP5649730B2 (ja) | 2015-01-07 |
Family
ID=45567287
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013523453A Active JP5649730B2 (ja) | 2010-08-13 | 2010-08-13 | ケイ酸塩発光材料及びその製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9074136B2 (ja) |
| EP (1) | EP2604671A4 (ja) |
| JP (1) | JP5649730B2 (ja) |
| CN (1) | CN102933688B (ja) |
| WO (1) | WO2012019359A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015045260A1 (ja) * | 2013-09-30 | 2015-04-02 | パナソニックIpマネジメント株式会社 | 蛍光体及びこれを用いた発光装置、照明光源、照明装置 |
| JP2021533227A (ja) * | 2018-08-03 | 2021-12-02 | ボード オブ リージェンツ, ザ ユニバーシティ オブ テキサス システムBoard Of Regents, The University Of Texas System | ポリマー性マトリックスにおける蛍光体の分散を増進させるための方法及び組成物 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2832819A4 (en) * | 2012-03-29 | 2015-12-23 | Oceans King Lighting Science | METAL NANOPARTICLES DOTED SILICATE LIGHT MATERIALS AND METHOD FOR THE PRODUCTION THEREOF |
| US9416313B2 (en) * | 2013-08-22 | 2016-08-16 | Panasonic Intellectual Property Management Co., Ltd. | Yellow fluorescent substance, light-emitting device, illumination device, and vehicle |
| KR101900772B1 (ko) | 2017-04-27 | 2018-09-20 | 코오롱인더스트리 주식회사 | 이온 교환막, 이의 제조 방법 및 이를 포함하는 에너지 저장 장치 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040251809A1 (en) * | 2001-08-28 | 2004-12-16 | Mitsubishi Chemical Corporation | Phosphor, light emitting device using phosphor, and display and lighting system using light emitting device |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101677117B (zh) * | 2008-09-19 | 2012-03-21 | 展晶科技(深圳)有限公司 | 高演色性发光二极管的配置方法与系统 |
| CN101760195B (zh) * | 2010-01-22 | 2013-05-08 | 海洋王照明科技股份有限公司 | 硅酸盐蓝色发光材料及其制备方法 |
-
2010
- 2010-08-13 WO PCT/CN2010/075972 patent/WO2012019359A1/zh not_active Ceased
- 2010-08-13 EP EP20100855780 patent/EP2604671A4/en not_active Withdrawn
- 2010-08-13 CN CN201080067332.1A patent/CN102933688B/zh not_active Expired - Fee Related
- 2010-08-13 US US13/806,375 patent/US9074136B2/en not_active Expired - Fee Related
- 2010-08-13 JP JP2013523453A patent/JP5649730B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040251809A1 (en) * | 2001-08-28 | 2004-12-16 | Mitsubishi Chemical Corporation | Phosphor, light emitting device using phosphor, and display and lighting system using light emitting device |
Non-Patent Citations (5)
| Title |
|---|
| JPN6014024575; Beata Lipowska,Andrzej M Klonkowski: 'Energy Transfer and surface plasmon resonance in luminescent materials based on Tb(III) and Ag or Au' Journal of Non-Crystalline Solids 354, 2008, 4383-4387 * |
| JPN6014024577; Yuanhong Liu,Weidong Zhuang,Yunsheng Hu,Wengui Gao,Jianhua Hao: 'Synthesis and luminescence of sub-micron sized Ca3Sc2Si3O12:Ce green phosphors for white light-emitt' Journal of Alloys and Compounds 504, 2010, 488-492 * |
| JPN6014024578; Kadir Aslan,Meng Wu,Joseph R.Lakowicz,and Chris D.Geddes,: 'Fluorescent Core-Shell Ag@SiO2 Nanocomposites for Metal-Enhanced Fluorescence and Single Nanoparticl' J.AM.CHEM.SOC. 129, 2007, 1524-1525 * |
| JPN6014024579; Yu-Lin Min,Yong Wan,Shu-hong Yu: 'Au@Y2O3:Eu3+ rare earth oxide hollow sub-microspheres with encapsulated gold nanoparticles and their' Solid State Sciences 11, 2009, 96-101 * |
| JPN6014024580; Yuanhong Liu,Jianhua Hao,Weidong Zhuang,and Yunsheng Hu: 'Structural and luminescent properties of gel-combustion synthesized green-emitting Ca3Sc3Si3O12:Ce3+' Journal of Physics D:Applied Physics 42/24, 2009, 245102 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015045260A1 (ja) * | 2013-09-30 | 2015-04-02 | パナソニックIpマネジメント株式会社 | 蛍光体及びこれを用いた発光装置、照明光源、照明装置 |
| JPWO2015045260A1 (ja) * | 2013-09-30 | 2017-03-09 | パナソニックIpマネジメント株式会社 | 蛍光体及びこれを用いた発光装置、照明光源、照明装置 |
| US9840666B2 (en) | 2013-09-30 | 2017-12-12 | Panasonic Intellectual Property Management Co., Ltd. | Phosphor having inorganic oxide with cerium and terbium activators, light-emitting device illumination light source, and illumination device using same |
| JP2021533227A (ja) * | 2018-08-03 | 2021-12-02 | ボード オブ リージェンツ, ザ ユニバーシティ オブ テキサス システムBoard Of Regents, The University Of Texas System | ポリマー性マトリックスにおける蛍光体の分散を増進させるための方法及び組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2604671A1 (en) | 2013-06-19 |
| US9074136B2 (en) | 2015-07-07 |
| CN102933688B (zh) | 2014-03-19 |
| EP2604671A4 (en) | 2014-06-18 |
| WO2012019359A1 (zh) | 2012-02-16 |
| US20130092876A1 (en) | 2013-04-18 |
| CN102933688A (zh) | 2013-02-13 |
| JP5649730B2 (ja) | 2015-01-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Hussain et al. | Broad red-emission of Sr 3 Y 2 Ge 3 O 12: Eu 2+ garnet phosphors under blue excitation for warm WLED applications | |
| JP5649730B2 (ja) | ケイ酸塩発光材料及びその製造方法 | |
| JP5636098B2 (ja) | 金属ナノ粒子を有するハロゲン珪酸塩蛍光粉及びその調製方法 | |
| CN113403074A (zh) | 一种Mn4+激活的锑酸盐窄带红色荧光粉及其制备方法 | |
| Wang et al. | Ce: LuAG transparent ceramics for high-brightness solid-state lighting: Fabrication and effect of Ce concentration | |
| Hsu et al. | Microwave-hydrothermally synthesized (Sr 1− x− y Ce x Tb y) Si 2 O 2− δ N 2+ μ phosphors: efficient energy transfer, structural refinement and photoluminescence properties | |
| CN106753327B (zh) | 一种荧光粉的表面热处理修饰方法以及由其制成的cob光源 | |
| JP5688473B2 (ja) | インジウム・ガリウム酸化物発光材料、及びその製造方法 | |
| JP5913730B2 (ja) | 金属ナノ粒子含有の珪酸塩発光材料及びその調製方法 | |
| CN103122244B (zh) | 一种Eu2+激活的硅酸盐白光荧光粉及其制备方法 | |
| JP5570663B2 (ja) | 金属ナノ粒子をドープしたケイ酸塩発光材料及びその調製方法 | |
| CN109370580B (zh) | 一种铋离子激活的钛铝酸盐荧光粉及其制备方法与应用 | |
| Singh et al. | An insight into the luminescence properties of Ce3+ in garnet structured CaY2Al4SiO12: Ce3+ phosphors | |
| CN102492420B (zh) | 一种硅铝酸铯盐荧光粉及其制备方法 | |
| Ren et al. | Luminescence properties and energy transfer of color-tunable LaAl2. 03B4O10. 54: Tm3+, Dy3+ phosphors | |
| JP5707505B2 (ja) | ハロゲンケイ酸塩発光材料及びその調製方法 | |
| JP5612225B2 (ja) | ハロゲンホウ酸塩りん光体、及び、その作製方法 | |
| JP5599942B2 (ja) | 酸化イットリウム蛍光体およびその製造方法 | |
| CN104059653B (zh) | 钛酸钇发光材料及其制备方法 | |
| CN110373186B (zh) | 一种不含稀土的红色荧光粉及其制备方法 | |
| CN102174321A (zh) | 一种硅酸盐化合物发光材料及其制备方法 | |
| Tadge et al. | Mineral-Inspired Approach Mediated Design, Solution Synthesis, and Characterization and Luminescence Study of Blue Emitting Phosphor BaSc2Si3O10: Eu2+ | |
| JP2013535526A (ja) | 酸化物発光材料及びその調製方法 | |
| US20150267110A1 (en) | Silicate luminescent material and preparation method thereof | |
| TWI628262B (zh) | Method for preparing manganese activated zinc aluminum spinel oxynitride fluorescent powder |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140530 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140617 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140909 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141014 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20141111 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5649730 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |