JP2013501056A - ウイルス感染およびウイルス誘発腫瘍を治療する組成物および方法 - Google Patents
ウイルス感染およびウイルス誘発腫瘍を治療する組成物および方法 Download PDFInfo
- Publication number
- JP2013501056A JP2013501056A JP2012523680A JP2012523680A JP2013501056A JP 2013501056 A JP2013501056 A JP 2013501056A JP 2012523680 A JP2012523680 A JP 2012523680A JP 2012523680 A JP2012523680 A JP 2012523680A JP 2013501056 A JP2013501056 A JP 2013501056A
- Authority
- JP
- Japan
- Prior art keywords
- virus
- alkyl
- alkynyl
- alkenyl
- cmx001
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 CN(*)C(C=CN1C[C@@](CO)OCP(N=O)(O)=O)=NC1=O Chemical compound CN(*)C(C=CN1C[C@@](CO)OCP(N=O)(O)=O)=NC1=O 0.000 description 5
- JLVDVIXDYDGVLS-UHFFFAOYSA-N C(C1)C2COC1C2 Chemical compound C(C1)C2COC1C2 JLVDVIXDYDGVLS-UHFFFAOYSA-N 0.000 description 1
- SGOIRFVFHAKUTI-ZCFIWIBFSA-N C[C@H](C[n]1c2ncnc(N)c2nc1)OCP(O)(O)=O Chemical compound C[C@H](C[n]1c2ncnc(N)c2nc1)OCP(O)(O)=O SGOIRFVFHAKUTI-ZCFIWIBFSA-N 0.000 description 1
- VWFCHDSQECPREK-LURJTMIESA-N NC(C=CN1C[C@@H](CO)OCP(O)(O)=O)=NC1=O Chemical compound NC(C=CN1C[C@@H](CO)OCP(O)(O)=O)=NC1=O VWFCHDSQECPREK-LURJTMIESA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6571—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and oxygen atoms as the only ring hetero atoms
- C07F9/657163—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and oxygen atoms as the only ring hetero atoms the ring phosphorus atom being bound to at least one carbon atom
- C07F9/657181—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and oxygen atoms as the only ring hetero atoms the ring phosphorus atom being bound to at least one carbon atom the ring phosphorus atom and, at least, one ring oxygen atom being part of a (thio)phosphonic acid derivative
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/645—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having two nitrogen atoms as the only ring hetero atoms
- C07F9/6509—Six-membered rings
- C07F9/6512—Six-membered rings having the nitrogen atoms in positions 1 and 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6558—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system
- C07F9/65586—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system at least one of the hetero rings does not contain nitrogen as ring hetero atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6561—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings
- C07F9/65616—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings containing the ring system having three or more than three double bonds between ring members or between ring members and non-ring members, e.g. purine or analogs
Abstract
Description
本願は、2009年8月3日に出願された米国仮特許出願第61/230,931号の、35U.S.C.§119(e)に基づく利益を主張するものであり、その開示は、引用することにより本明細書の一部をなすものとする。
本発明は、概して、ウイルス感染およびウイルス誘発腫瘍を治療するための化合物、その類似体および方法に関する。
本発明のいくつかの態様によれば、様々な生物学的特性を持つ化合物が提供される。本明細書において記載されている化合物は、ウイルス誘発腫瘍の治療に関わる生物学的活性を有する。
R1、R1’、R2およびR2’は、独立に、−H、ハロゲン、−ORi、−SRi、−NHRi、−NRiRiiであり、かつ、RiおよびRiiは、独立に、水素または脂肪族であり、
R3は、薬学的に活性なホスホネート、ビスホスホネート、または薬理活性化合物のホスホネート誘導体であり、
Xは、存在する場合、
を有する。
を有するエタンジオールホスホネート種である。
Mは
ここで、R1、R1’、R2およびR2’は、独立に、−H、ハロゲン、−ORi、−SRi、−NHRi、−NRiRiiであり、かつ、RiおよびRiiは、独立に、水素または脂肪族であり、
Qは、存在する場合、
Bは、水素、F、CF3、CHF2、−CH3、−CH2CH3、−CH2OH、−CH2CH2OH、−CH(OH)CH3、−CH2F、−CH=CH2および−CH2N3からなる群から選択され、
Xは、セレン、硫黄または酸素(いくつかの実施形態において、酸素)であり、
R3は、ヒドロキシ、−OR2a、−BH3、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニルまたは−NR’Hであり(いくつかの実施形態において、R2はヒドロキシルである)、
R2aは、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニル、−P(=O)(OH)2または−P(=O)(OH)OP(=O)(OH)2であり、
R’は、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルキニル、C2〜8ヘテロアルケニル、C6〜10アリール、または置換もしくは非置換アミノ酸残基であり、
Zは、少なくとも1個のNを含む複素環式部分(いくつかの実施形態において、該複素環式部分はプリンまたはピリミジンから選択される)を含み、かつ
符号*は、式A、A’またはB中のメチレン部分とZとの結合点が、該複素環式部分の利用可能な窒素を介していることを指示する]
または薬学的に許容されるその塩を有する。
YはNまたはCXであり、
Xは、H、ハロ、C1〜6アルキル、C2〜6アルケニル、C2〜6アルキニル、CN、CF3、N3、NO2、C6〜10アリール、C6〜10ヘテロアリールおよびCORbからなる群から選択され、
Rbは、H、OH、SH、C1〜6アルキル、C1〜6アミノアルキル、C1〜6アルコキシおよびC1〜6チオアルキルからなる群から選択され、かつ
R11は、H、C1〜6アルキル、C2〜6アルケニル、C2〜6アルキニル、C3〜6シクロアルキル、C4〜12アルキルシクロアルキル、C6〜10アリール、およびC1〜6アルキル、C2〜6アルケニル、C2〜6アルキニルまたはC6〜10アリールで置換されているカルボニルからなる群から選択される]
の部分を含むがこれらに限定されない。
Yは−NRaRbまたは−ORaであり、
L2は、共有結合(すなわち、存在しない)、−N(−R15)−、N(−R15)C(=O)−、−O−、−S−、−S(=O)−または−S(=O)2−であり、
R13は、H、C1〜6アルキル、C1〜6ヘテロアルキル、C2〜6アルケニル、C6〜10アリール、C7〜16アリールアルキル、C3〜10カルボシクリル、C6〜10ヘテロシクリルまたはC7〜16ヘテロシクリルアルキルであり、
R14は、H、ハロ、ヒドロキシ、アルコキシ、−O(CH2)xOC(=O)OR15またはOC(=O)OR15であり、ここで、xは、2または3から10、15または20であり、
R15は、H、C1〜6アルキル、C1〜6ヘテロアルキル、C2〜6アルケニル、C6〜10アリール、C7〜16アリールアルキル、C3〜10シクロアルキル、C6〜10ヘテロシクリルまたはC7〜16ヘテロシクロアルキル(heterocyclalkyl)であり、かつ
Ra、Rbは、水素、C1〜6アルキルまたはC3〜6シクロアルキルおよびC3〜8ヘテロシクリルからなる群から独立に選択され、ここで、C3〜6シクロアルキルおよびC3〜8ヘテロシクリルは、1個または複数のC1〜5アルキルで場合により置換されていてよい]
の化合物を含むがこれらに限定されない。
の部分を含むがこれに限定されない。
nは0または1であり、mは0または1であり、pは0または1であり、
R1は、場合により置換されているアルキル、アルケニルまたはアルキニル、例えば、C1〜30アルキル、C2〜30アルケニルまたはC2〜30アルキニルであるか、あるいは一実施形態において、R1は、場合により置換されているC8〜30アルキル、C8〜30アルケニルまたはC8〜30アルキニルであるか、あるいはR1は、C8〜24アルキル、C8〜24アルケニルまたはC8〜24アルキニル(例えば、C17、C18、C19、C20、C21、C22、C23もしくはC24アルキル、アルケニルまたはアルキニル)であり、
R2およびR3は、それぞれ独立に、場合により置換されているC1〜25アルキル、C2〜25アルケニルまたはC2〜25アルキニルであり、
Dは、式V〜Xにおいて描写されている通りのメチレン基と直接連結しているシドフォビル、テノフォビル、環式シドフォビルまたはアデフォビルであってよい]を有する。例えば、Dがテノフォビルである場合、Dは、式:
W1、W2およびW3は、それぞれ独立に、−O−、−S−または−O(CO)−であり、
nは0または1であり、mは0または1であり、pは0または1であり、
R1は、場合により置換されているC12〜24アルキルまたはアルケニル(例えば、C12、C13、C14、C15、C16、C17、C18、C19、C20、C21、C22、C23もしくはC24アルキルまたはアルケニル)であり、
R2およびR3は、それぞれ独立に、場合により置換されているC1〜24アルキルもしくはC2〜24アルケニル、またはC2〜24アルキニルである。
Dは、式V〜Xにおいて描写されている通りのメチレン基と直接連結しているシドフォビル、テノフォビル、環式シドフォビルまたはアデフォビルである。
R1、R1’、R2およびR2’は、独立に、−H、ハロゲン、−NH2、−OHもしくは−SHまたは場合により置換されている−XRiであり、ここで、Xは、O、S、−NHまたは−NRiiであり、かつ、RiおよびRiiは、独立に、−(C1〜C24)アルキル、−(C1〜C24)アルケニル、−(C1〜C24)アルキニルまたは−(C1〜C24)アシルである]
を有する。
R3は、任意選択のリンカーL上の官能基と、またはCα上の利用可能な酸素原子と連結している、薬学的に活性なホスホネート、ビスホスホネート、または薬理活性化合物のホスホネート誘導体であり、
Xは、存在する場合、
Lは、原子価結合、または式−J−(CR2)t−G−[式中、tは1から24の整数であり、JおよびGは、独立に、−O−、−S−、−C(O)O−または−NH−であり、かつ、Rは、−H、置換もしくは非置換アルキル、またはアルケニルである]の二官能性連結分子であり、
mは0から6の整数であり、かつ
nは0または1である。
を有する。
を有する。
エチドロネート:1−ヒドロキシエチリデンビスホスホン酸(EDHP)、
クロドロネート:ジクロロメチレンビスホスホン酸(C12 MDP)、
チルドロネート(Tiludromate):クロロ−4−フェニルチオメチレンビスホスホン酸、
パミドロネート:3−アミノ−1−ヒドロキシプロピリデンビスホスホン酸(ADP)、
アレンドロネート:4−アミノ−1−ヒドロキシブチリデンビスホスホン酸、
オルパドロネート:3ジメチルアミノ−1−ヒドロキシプロピリデンビスホスホン酸(ジメチル−APD)、
イバンドロネート:3−メチルペンチルアミノ−1−ヒドロキシプロピリデンビスホスホン酸(BM21.0955)、
EB−1053:3−(1−ピロリジニル)−1−ヒドロキシプロピリデンビスホスホン酸、
リセドロネート(Risedmnate):2−(3−ピリジニル)−1−ヒドロキシ−エチリデンビスホスホン酸、
アミノ−オルパドロネート:3−(N,N−ジメチルアミノ−1−アミノプロピリデン)ビスホスホネート(IG9402)
等を含む。
本明細書において記載されている化合物の調製において利用される過程は、望ましい特定化合物によって決まる。特定置換基の選択および特定置換基の種々の可能な場所等の要因はいずれも、本発明の特定化合物の調製において辿られる経路において役割を果たす。それらの要因は、当業者には容易に認識される。
一実施形態において、本発明は、本明細書において記載されている化合物を含む医薬組成物である。別の実施形態において、医薬組成物は、薬学的に許容される担体をさらに含む。用語「薬学的に許容される担体」は、本明細書において使用される場合、対象への治療剤の送達のためのビヒクルとして使用される、それ自体は治療剤でない任意の物質を指す。薬学的に許容される担体、および種々の組成物の製造方法の例は、Remington’s Pharmaceutical Sciences、第18版、Mack Publishing Co.(1990)(米国特許出願第US2007/0072831号も参照)において記載されているものを含むがこれらに限定されない。
本発明の一態様は、対象(例えばヒト)における免疫抑制に関連するウイルス誘発性状態/疾患(例えば、ウイルス誘発腫瘍またはウイルス感染)を治療する方法であって、該対象に、治療有効量の本明細書において記載されている化合物を投与するステップを含む方法を提供する。一実施形態において、本明細書において記載されている化合物は、ウイルス複製および/またはウイルス感染/形質転換細胞を特異的に標的とする。例えば、CMX001は、BKウイルスおよびJCウイルス感染細胞等のポリオーマウイルス感染細胞に対する特異性を実証する(以下の実施例2参照)。一実施形態において、本明細書において記載されている化合物は、ウイルス感染および/または形質転換細胞に対し、正常(非感染細胞)と比較して高い細胞毒性を有する。
本明細書において記載されている化合物は、免疫抑制投薬法を必要としている対象のウイルス感染またはウイルス誘発腫瘍を治療するための追加の免疫抑制剤と組み合わせて使用され得る。当業者に公知である任意の免疫抑制剤を、本明細書において記載されている化合物と組み合わせて使用してよい。例示的な免疫抑制剤は、ダクリズマブ、バシリキシマブ、タクロリムス、シロリムス、ミコフェノレート(ナトリウムまたはモフェチルとして)、シクロスポリンA、グルココルチコイド、抗CD3モノクローナル抗体(OKT3)、抗胸腺細胞グロブリン(ATG)、抗CD52モノクローナル抗体(キャンパス1−H)、アザチオプリン、エベロリムス、ダクチノマイシン、シクロフォスファミド、白金、ニトロソ尿素、メトトレキサート、アザチオプリン、メルカプトプリン、ムロモナブ、IFNガンマ、インフリキシマブ、エタネルセプト、アダリムマブ、タイサブリ(ナタリズマブ)、フィンゴリモドおよびそれらの組合せを含むがこれらに限定されない。いくつかの実施形態において、医薬組成物は、CMX001およびタイサブリ(ナタリズマブ)を含む。
ここで、下記の例を参照して、本発明をさらに詳細に記述する。しかしながら、これらの例は例証を目的として与えられるものであり、本発明の範囲を限定するものとして解釈されるべきでない。
BKウイルスの複製を阻害するCMX001の活性を試験するために、BKウイルスのストックをHFF細胞中で調製し、ウイルスストックの希釈物を使用して、初代ヒト尿細管上皮細胞(RPTEC)を感染させた。次いで、感染細胞を含有するウェルにCMX001を添加し、プレートを5日間インキュベートした。全DNAを該プレートから調製し、ウイルスのDNAをqPCRによって定量化した。
JCウイルスを阻害するCMX001の能力を試験するために、COS−7細胞に、0.2の推定TCID50でJCV(Mad−4)を感染させた。37℃で2時間インキュベーション後、CMX001の量を増大させることなく、または増大させて、上清を新鮮培地に置き換え、5日間インキュベートした。DNA抽出後、JCウイルスをqPCRによって定量化した。
A.材料および方法
Bernhoffらによって記載されている通りの初代ヒト近位尿細管上皮細胞(RPTEC)、BKV(Dunlop)およびすべての方法(Bernhoffら、Cidofovir inhibits polyomavirus BK replication in human renal tubular cells downstream of viral early gene expression、Am J Transplant 8、1413〜1422(2008)を参照)。唯一の例外として、細胞内または細胞外BKV DNA負荷を定量化するための定量的PCR(qPCR)は、LTag遺伝子も標的とする異なるプライマー/プローブセットで実施した(Hirschら、J.Prospective study of polyomavirus type BK replication and nephropathy in renal−transplant recipients、N Engl J Med.、347、488〜496(2002)を参照)。各実験の前に、CMX001をメタノール/水/水酸化アンモニウム(50/50/2)中1mg/mlに新しく溶解した。それをRPTEC成長培地中でさらに希釈した。
(1)阻害濃度IC90の決定
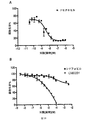
BKV後代に対するCMX001の効果を調査するために、感染2時間後に漸増濃度のCMX001を添加し、上清を感染72時間後に収穫した。CMX001が細胞外BKV負荷を濃度依存方式で低減させたことが観察された(図1a参照)。ウイルス流入を減じた場合、CMX001 0.31μMは、阻害濃度IC90を定義する平均90%だけBKV負荷を低減させた。BKV感染RPTECの感染72時間後における免疫蛍光染色は、CMX001濃度を増大させるにつれてBKV感染細胞の数が減少することを実証した(図1b)。CMX001 0.31uMで、BKVアグノタンパク質発現細胞におけるおよそ60%の減少が見られた。LTagを発現している細胞の数はあまり低減しなかったが、シグナル強度は未処理細胞におけるものよりも低かった。2.5uMのCMX001では、わずかな細胞のみがアグノタンパク質およびLTag発現について陽性であったが、ウェル中の細胞総数は低減しているように思われた。5uMのCMX001では、弱くLTag染色された細胞のみがわずかに観察されたがアグノタンパク質発現細胞は観察されず、総細胞数に対してはより顕著な効果があった。10uMのCMX001では、BKV感染細胞は観察されず、総細胞数はより一層低減した。結論として、CMX001は初期および後期BKVタンパク質の発現ならびに細胞外後代の産生を低減させたが、高濃度ではRPTECの増殖速度にも影響を及ぼすようであったということである。
位相差顕微鏡法によるRPTECの検査は、CMX001 0.31μMへの3日間の暴露中、生存能力低下の兆候を何ら明らかにしなかった。より感受性の高いアッセイを使用するために、非感染RPTECにおけるBrdU取り込みおよびWST−1アッセイを使用する、宿主細胞DNA複製および代謝活性を使用した。CMX001の添加は、非感染RPTECのDNA複製(図2a)および代謝活性(図2b)の両方を濃度依存方式で低減させた。未処理RPTECと比較して、0.08から10μMのCMX001は、DNA複製を15%から93%、および代謝活性を41%から88%、それぞれ減少させた。BKV複製の90%阻害を引き起こした0.31μMの濃度において、BrdU取り込みおよびWST−1活性におけるおよそ20%の低減が観察される。
BKVゲノム複製がCMX001の影響を受けたかを調査するために、感染24〜72時間後における細胞内BKV負荷をqPCRによって計測した。記載されている通りのアスパルトアシラーゼ(ACY)遺伝子を使用して、細胞内BKV負荷を細胞数に正規化した(Bernhoffら、2008;Randhawaら、Quantitation of DNA of polyomaviruses BK and JC in human kidneys.J Infect Dis.、192、504〜509(2005)を参照)。未処理RPTECと比較して、CMX001 0.31μMは、細胞内BKV負荷を、感染48時間後において94%、72時間後において63%低減させた(図3)。次いで、BKV生活環の第2ステップである細胞内BKVゲノム複製に対するCMX001の有意な阻害効果を同定することができる。このステップは、2つの機序によって:1.後期遺伝子転写のためのDNAテンプレートを増大させること、および2.後期プロモーターからの転写を活性化することによって、ウイルスの後期遺伝子発現も増大させる、LTag発現を必要とすることが公知である(Cole,C.N.、Polyomavirinae:The Viruses and Their Replication.In Fields Virology、第3版、1997〜2043頁、B.N.Fields、D.M.KnipeおよびP.H.Howley編、New York:Lippincott−Raven(1996))。
単一細胞レベルでのLTagの発現を調査するために、感染48および72時間後に免疫蛍光染色を実施した。感染48時間後において、BKV陽性細胞の数は、CMX001および未処理ウェルにおけるものとほぼ同じであった。感染72時間後において、CMX001処理細胞は、より少ないLTagプロ細胞を発現したようであった(図4a)。感染48および72時間後における後期タンパク質発現を免疫蛍光染色によって検査すると、CMX001処理RPTECにおいてアグノタンパク質(図4a)およびVP1(データは図示せず)の有意な低減が観察された。ウエスタンブロッティングにより、VP1の減少は感染48および72時間後においてそれぞれ86%および63%であることが分かり(図4b)、一方、LTag染色は感染48および72時間後においてそれぞれ33%および30%低減したことが分かった。興味深いことに、免疫蛍光法は、最大2.5μMのCMX001濃度を持つ未処理細胞にも匹敵するレベルでアグノタンパク質を発現するCMX001処理培養物において、いくつかの治療抵抗性細胞も明らかにした。CMX001は後期タンパク質発現を有意に低減させるだけでなく、感染の後期の時点において初期タンパク質発現も阻害すると結論付けられた。
BKV後代に対するCMX001の効果を経時的に検査するために、処理および未処理細胞の上清を指示された時点で収穫した。以前に記載された通り(Bernhoffら、2008)、未処理RPTEC中におけるBKV(Dunlop)の最初の生活環の完了には、48から72時間の間を要する。感染48時間後に、未処理細胞からの上清においてBKV負荷の増大が観察されたが、感染48時間後のCMX001処理細胞においては流入ウイルスのみが検出できた。72時間では、未処理およびCMX001処理細胞の両方においてウイルス負荷の増大が見られたが、CMX001処理細胞からの上清におけるBKV負荷は、未処理細胞におけるものよりも84%低かった(1.13×108Geq/ml)(図5)。CMX001処理RPTECにおける後代産生は、遅延し得ると結論付けられる。
ウイルス接種前における細胞の前処理によってBKV感染を阻害し得るか否かを調査するために、RPTECを4時間処理し、かつCMX001を感染20時間前に完全成長培地によって置き換えるか、または細胞を感染24時間前に23時間処理するがCMX001を感染1時間前に完全成長培地で置き換えるかのいずれかとした。感染20時間前に終了する4時間の処理は感染72時間後のBKV負荷にほとんど効果を及ぼさなかったが、感染1時間前までの23時間の処理は、ウイルス負荷を約50%低減させた(図6)。故に、CMX001前処理は、BKV複製を低減させるが予防しない。
CMX001の安定性を検査するために、ストック溶液1mg/mlを4または−20℃で1週間置き、次いで0.31uMに希釈し、感染3日後にBKV感染RPTECにおける細胞外BKV負荷を計測することにより、その抗ウイルス効果について試験した。新しく調製した薬物と比較して、4℃で保存した薬物は60%未満の活性を有し、一方、−20℃で保存した薬物はおよそ90%の活性を有していた(図7)。
BKV感染RPTECをCMX001で処理することによる暫定結果を、図1〜7および図1〜7に関連する上記の考察に示した。CMX001は、CDVよりも約400倍低い濃度におけるBKVゲノム複製のレベルでBKV感染を阻害する(CDV 40ug/ml=127uM対CMX001 0.31uM)。0.31uMの濃度のCMX001は、IC90を定義するおよそ90%、細胞外BKV負荷を低減させた。同じCMX001濃度は、非感染細胞における細胞DNA複製を22%、および代謝活性を20%減少させた。しかしながら、先の調査(Bernhoffら、2008)において、BKV感染は細胞DNA複製を約40%、および代謝活性を20%前後(round)増大させ、したがって、CMX001 0.31uMを使用してBKV−感染細胞を治療すると、DNA複製および代謝活性の両方が非感染細胞のレベルになるという仮説が成り立つことが示されているものがある。
A.材料および方法
(1)細胞培養物
COS−7細胞をDMEM−5%中で成長させた。前駆細胞に由来する星状膠細胞を、ゲンタマイシンを補充したMEM−E−10%中に維持した。感染COS−7細胞からのJCV Mad−4(ATCC VR−1583)上清に、1ml当たり104.5のTCID50を加えたものを、培養細胞の感染に使用した。
COS−7または星状膠細胞に、60〜70%の集密で、JCV(Mad−4)を0.2の推定TCID50で感染させた。37℃で2時間インキュベーション後、CMX001の濃度を増大させることなく、または増大させて、上清を新鮮培地に置き換えた。CMX001をメタノール/水/水酸化アンモニウム(50/50/2)中1mg/mlに新しく溶解し、次いで、それぞれの成長培地中でさらに希釈した。
リポフェクタミン2000(Invitrogen)を製造業者の取扱説明書に従って0.8:1のDNA:脂質比で使用することにより、再連結したJCV Mad−4 DNAを50%から70%集密的COS−7細胞にトランスフェクトした。
リン酸緩衝生理食塩水、pH6.8(PBS)中4%のp−ホルムアルデヒド(PFA)で、室温にて20分間細胞を固定し、PBS中0.2%のトリトンX−100で、室温にて10分間透過化した。室温にて5分間、PBSで2回洗浄した後、PFAをPBS中0.5MのNH4Clで室温にて7分間クエンチし、続いて、室温にて5分間、PBSで2回洗浄した。非特異的結合部位のブロッキングを、PBS中3%の乳で37℃にて15分間行った。一次抗体(3%乳PBS中ウサギ抗VP1 1:300)を、37℃で45〜60分間インキュベートした。細胞を、振とう器上室温にて5分間、PBSで2回洗浄した。二次抗体(ニワトリ抗ウサギCy3 1:2000)、およびDNAを染色するための5μg/mlのヘキスト33342色素を細胞に与え、次いで37℃で45〜60分間インキュベートした。細胞をPBSで2回、前述同様に洗浄した。カバーガラスをN没食子酸プロピル上に載置した。
100ulの細胞培養物上清、ならびにCorbett X−トラクタージーンおよびCorbett VX試薬(Qiagen、Hombrechtikon、Switzerland)からのDNA抽出後に、JCV負荷を定量化した。JCV DNA試料の検出のためのリアルタイムPCRプロトコールは、JCVラージTコード配列を標的としており、(5)の他の箇所に記載されている。
生存細胞におけるミトコンドリアデヒドロゲナーゼの比色WST−1アッセイ(Roche)によって、代謝活性をモニターした。COS−7細胞を96ウェルプレートに播種し、CMX001を指示された濃度で添加した。WST−1開裂生成物を、450nm(試料)および650nm(バックグラウンド)で計測した。WST−1プラス培地単独では、ブランクとして役立った。
「細胞増殖ELISA、BrdU」キット(Roche)を使用する、増殖性細胞におけるDNAへのBrdU取り込みの比色計測によって、DNA合成を定量化した。COS−7細胞を96ウェルプレートに播種し、CMX001を指示された濃度で添加した。450nm(試料)および650nm(バックグラウンド)における吸光度を、基質の添加2時間後に決定した。
(1)細胞培養物中におけるJCV Mad−4の複製
COS−7および星状膠細胞培養物中におけるJCV Mad−4の複製特徴を第一に調査した。感染7日後(d.p.i.)、JCV感染COS−7細胞を固定し、間接免疫蛍光法によって染色した。図8に示されている通り、JCV後期ウイルス性カプシドタンパク質VP1は、JCVがCOS−7細胞においてウイルスの生活環を完了していることを示唆する赤色シグナルとして検出可能である(図8、左パネル)。ヘキスト33342でのDNAの対比染色は、核を青色にマークした(図8、中央パネル)。両方の写真をマージしたもの(図8、右パネル)は、JCV Mad−4 VP1が感染COS−7細胞の核に存在することを指示していた。さらに高倍率では、VP1シグナルは核全体にわたって分散していたが、核小体は残してあった(図8、左パネル)。核において強度のVP1シグナルを示す細胞は、細胞質においても拡散染色パターンを有していた。JCV感染細胞は、同じ細胞培養物中に存在する非感染細胞(図8、右パネル)と比較して拡大した核(図8、中央パネル)を示した。データは、COS−7細胞がJCV Mad−4感染に感受性であること、および感染7日後に細胞の約30%がJCV生活環の後期に入ったことを実証している。
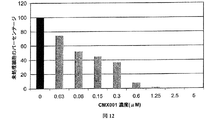
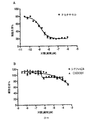
JCV後代に対するCMX001の効果を調査するために、感染2時間後に漸増濃度のCMX001を添加し、上清を感染5日後に収穫した。CMX001が細胞外JCV負荷を濃度依存方式で低減させたことが観察された(図12)。感染1日後と5日後との間で、未処理細胞におけるウイルス負荷は約2.5対数(1.24×107対5.09×109)増加した。対照的に、2.5μMのCMX001で処理した細胞においては、同じ期間中に2と2分の1倍(9.69×106対2.44×107)しか増大しないことが観察される。感染1日後のウイルス負荷として定義されるウイルス流入を減じると、CMX001は、0.15μMでJCVウイルス負荷を50%超低減させ、0.6μMでJCVを90%超低減させ、それぞれ感染5日後における阻害濃度IC−50およびIC−90を定義するものであった。
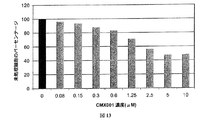
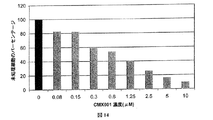
位相差顕微鏡法によるCOS−7の検査は、CMX001 0.6μMへの7日間の暴露中、生存能力低下の兆候を何ら明らかにしなかった。より感受性の高いアッセイを使用するために、非感染COS−7細胞におけるWST−1アッセイおよびBrdU取り込みを使用して、細胞代謝活性に対する効果を調査した。CMX001の添加は、非感染COS−7細胞の代謝活性(図13)およびDNA複製(図14)を濃度依存方式で低下させた。未処理COS−7細胞と比較して、CMX001濃度を0.08から10μMまで増大させることにより、代謝活性を3%から52%まで、およびDNA複製を83%から10%、それぞれ減少させた。0.6μMにおいて、COS−7細胞は、17%の代謝活性のささやかな損失、およそ50%低減したBrdU取り込みを示した。まとめると、CMX001は、高濃度では、宿主細胞代謝活性およびDNA複製を有意に低減させた。0.08から5μMのCMX001濃度の星状膠細胞でも同様の実験を行った。非感染星状膠細胞におけるDNA複製は、最高CMX001濃度において25%から92%減少した(データは図示せず)。両細胞型のDNA複製のCMX001関連阻害を比較すると、COS−7の感受性が若干低い(それぞれ83%対92%)ようであった。しかしながら、星状膠細胞について、該アッセイの2時間の基質インキュベーション期間は、光学密度がCOS−7の測定値と比較して低いため、最適ではないようであった。これは、星状膠細胞がCOS−7細胞と比較して緩徐な代謝を有していたとする本発明者らの観察と一致する。
JCV後代レベルに対するCMX001の効果を経時的に検査するために、処理および未処理細胞の上清を指示された時点で収穫した。感染1日後の上清を、流入ウイルスの目安として採取した。未処理細胞において、細胞外JCV負荷は、7日間の観察期間にわたって3を超える対数(1.24×107対5.67×1010geq/ml)だけ増大した。5μMのCMX001の存在下では、JCV負荷における1対数未満のささやかな変化のみが観察される(1.34×107対8.85×107geq/ml(図15)。JCウイルス負荷を、感染7日後のCMX001 5uM処理細胞について、感染3日後の未処理細胞におけるウイルス後代と比較すると、CMX001処理細胞におけるウイルス負荷は(9.72×107対8.85×107geq/ml)の91%にしか達していなかった。CMX001処理COS−7細胞における後代産生は遅延し得ると結論付けられた。
後期遺伝子発現に対するCMX001の効果を調査するために、JCV VP1について免疫蛍光染色を実施した。感染7日後に、未処理COS−7細胞のJCV VP1を比較として染色した(図16、上部パネル)。1.25μMのCMX001の添加は、JCV VP1シグナル(signaly)の有意な低減と関連していた(図16、中央パネル)。5μMの最高CMX001濃度では、本質的に免疫蛍光法によって観察され得るVP1陽性細胞はない(図16、下部パネル)。CMX001は、1.25μMから5μMの間のJCV後期タンパク質発現を有意に低減させると結論付けられた。
JCV後代レベルに対するCMX001の効果を経時的に検査するために、処理および未処理細胞の上清を指示された時点で収穫した。流入ウイルスを決定するために、感染1日後に試料を採取した。未処理細胞の感染経過において、細胞外JCV負荷は、7日間の観察期間にわたっておよそ1対数(3.22×107対2.30×108geq/ml)変化する。CMX001の存在下では、1対数未満のJCV負荷が見られた(1.34×107対8.85×107geq/ml(図17)。JCV複製は、COS−7よりも星状膠細胞において有意に緩徐であると結論付けられた。低濃度のCMX001の後代産生を阻害する傾向にもかかわらず、7日間の観察期間ではCMX001の阻害効果の計測が可能にならなかった。
暫定結果は、CMX001がCOS−7細胞におけるJCV複製を阻害することを示唆している。0.6μMのCMX001濃度は、細胞外JCV負荷をおよそ90%低減させた。この濃度は、CDV阻害について報告された濃度よりも2桁低いが、BKVについて観察されたものと同じ範囲内である。ここで、BKV複製のCMX001 IC−90を、初代尿細管上皮細胞において0.31μMと決定した(34)。CMX001は、宿主細胞代謝活性を17%、およびDNA複製を約50%減少させることが観察された。感染1から7日後に細胞外JCV負荷を計測すると、最高濃度のCMX001(5μM)で処理した細胞からのJCV負荷は、感染1日後における流入ウイルスよりも感染5日後において若干高いだけであり、4日以内に放出されるウイルスは極めて少ないまたは無いことを指示していた。感染7日後において、この濃度でJCV負荷におけるごくわずかな増大があり、後代ウイルスのレベルは、未処理細胞の感染3日後に計測されたウイルス負荷を下回っていた。星状膠細胞においては、低濃度のCMX001が後代ウイルスの蓄積を遅延させ得るという動向がある。しかしながら、感染7日後の未処理星状膠細胞における非効率的な後代ウイルス産生は、JCV複製周期が有意に緩徐であることを実証するものであった。
第一の患者は、鎌状赤血球貧血が発生したEBV関連頭蓋内移植後リンパ増殖性障害(PTLD)の病歴がある11歳の患者である。EBVは血漿中において陽性(2010年12月7日および12月14日)であり、脳生検はPTLDと一致していた。12月上旬に、患者は、持続性頭痛、悪心、嘔吐および下痢の3日間の病歴を提示した。患者は入院し、発作活動を伴う可能性がある激しい頭痛の急性エピソードを起こした。脳のCTは、右前頭葉におけるリング状増強塊を示し、脳生検はEBV関連PTLDと一致していた。患者はPICUに入れられた。高い頭蓋内圧力、無呼吸に関連する反復性発作は、挿管およびCMX001の緊急要求につながった。このEBV関連PTLD患者におけるCMX001の使用は、2009年12月26日から継続中である。患者はCMX001に十分耐性があったため、週に2回4mg/kgを受け続けている。該患者には、疾患の兆候および症状の臨床的改善、ならびに頭蓋内塊の低減とはいえないまでも安定化があった。血漿中におけるEBVは陰性のままである。
CMX001、シドフォビルおよび標準的な作用物質(細胞株の腫瘍型に応じて変動する)の細胞成長阻害活性を、多数の腫瘍型に由来する細胞株のパネルにおいて、MTSまたはSRBベースの細胞増殖アッセイを使用して評価した。
(1)細胞株:
試験において使用した細胞株を表3に収載する。細胞に新鮮培地を2〜3日ごとに供給し、それらの成長速度に応じて3〜5日ごとに継代させた。10〜15継代後、細胞を廃棄し、凍結ストックから新鮮培養物を確立した。細胞培養物をマイコプラスマおよび他の汚染物質について定期的に点検した。
滅菌ダルベッコリン酸緩衝生理食塩水(DPBS、pH7.4)中100mMのストックをCMX001およびシドフォビルについて作製し、−20℃で保存した。ドキソルビシン、ドセタキセル、オキサリプラチン、DTIC(ダカルバジン)およびシスプラチンは、Sigma−Aldrich(St.Louis、MO)から購入した。ゲムシタビンはEli Lilly and Companyによって製造され、Infusion Solutions Pharmacy(Tucson、AZ)から購入した。
インビトロ細胞増殖アッセイは、96ウェルプレートベースのMTSアッセイ(CellTiter96(C)アクオスワンソリューション細胞増殖アッセイ、Promega)またはSRB(スルホローダミンB)アッセイ(1〜3)を使用して実施した。手短に述べると、細胞を0日目に96ウェルマイクロタイタープレート(Falcon3072番)内において100μlの培地中で平板培養した。1日目、各化合物の10μlの連続希釈物(100μMの出発濃度での1:2希釈物9種;いくつかの事例において、400μM(CMX001またはシドフォビル)または1μM(いくつかの標準的な作用物質)の出発濃度)をプレートに3通り添加した。DMSOを溶媒として使用する標準的な作用物質については、0.5%の出発濃度でのDMSOの連続希釈物も、ビヒクル対照として含まれていた。
BioTek synergy(商標)HT多重検出マイクロプレートリーダーを使用して原データを獲得し、分析のためにMicrosoftエクセルにインポートした。各処理の平均シグナルは、ブランクシグナルを減じた後に3通りから算出した。生存パーセンテージ値は、下記の式:生存%=(薬物治療の平均シグナル/未処理対照の平均シグナル)×100を使用して算出した。データを最後にプリズム4ソフトウェア(GraphPad Software、San Diego、CA)にインポートして、非線形回帰曲線当てはめを使用して用量−活性曲線を生成し、IC50値を算出した。
各細胞株におけるCMX001、シドフォビルおよび標準的な作用物質の成長阻害プロファイルを、図18〜41に示す。IC50(50%成長を達成するために必要とされる濃度値を表4に収載する。
Claims (69)
- 対象において、ウイルス誘発腫瘍を治療するための方法であって、前記対象に、治療有効量の式Aもしくは式Bの化合物
Mは
Qは、存在する場合、
Bは、水素、−CH3、F、CF3、−CHF2、−CH2CH3、−CH2OH、−CH2CH2OH、−CH(OH)CH3、−CH2F、−CH=CH2および−CH2N3からなる群から選択され、
Xは、セレン、硫黄または酸素から選択され、
R3は、ヒドロキシ、−OR2a、−BH3、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニルまたは−NR’Hであり、
R2aは、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニル、−P(=O)(OH)2または−P(=O)(OH)OP(=O)(OH)2であり、
R’は、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルキニル、C2〜8ヘテロアルケニル、C6〜10アリール、または置換もしくは非置換アミノ酸残基であり、
Zは、少なくとも1個のNを含む複素環式部分を含み、かつ
符号*は、式(A)または(B)中のメチレンとZとの結合点が、前記複素環式部分の利用可能な窒素を介していることを指示する]、
または薬学的に許容されるその塩、立体異性体、ジアステレオマー、鏡像異性体もしくはラセミ体を投与するステップを含む方法。 - 式AまたはBの化合物が、ウイルス感染細胞および/またはウイルス複製を特異的に標的とする、請求項1に記載の方法。
- 前記対象がヒトである、請求項1に記載の方法。
- 前記腫瘍が、ポリオーマウイルス、パピローマウイルス、ヘルペスウイルス、アデノウイルス、エプスタイン・バーウイルス(EBV)、ヒトサイトメガロウイルス(HCMV)、B型肝炎ウイルス、C型肝炎ウイルスまたはそれらの組合せに関連する、請求項1から3のいずれかに記載の方法。
- 前記腫瘍が、ヒトパピローマウイルス、ワタオウサギパピローマウイルス、ウマパピローマウイルスおよびウシパピローマウイルスからなる群から選択されるパピローマウイルスに関連する、請求項4に記載の方法。
- 前記腫瘍が、ヒトパピローマウイルスに関連する子宮頸がんである、請求項4に記載の方法。
- 前記腫瘍が、エプスタイン・バーウイルス(EBV)に関連する移植後リンパ増殖性障害(PTLD)である、請求項4に記載の方法。
- 前記腫瘍が、サイトメガロウイルスに関連する膠芽細胞腫である、請求項4に記載の方法。
- 前記腫瘍が、BK、ジョン・カニンガムウイルス(JCV)、メルケル細胞ウイルス(MCV)、KIポリオーマウイルス(KIV)、WUポリオーマウイルス(WUV)、シミアンウイルス40(SV40)またはそれらの組合せに関連する、請求項4に記載の方法。
- 前記腫瘍が、BKウイルスまたはJCVに関連する、請求項4に記載の方法。
- 前記対象が免疫無防備状態である、請求項1から10のいずれかに記載の方法。
- 前記対象が、免疫抑制薬治療中の移植患者である、請求項11に記載の方法。
- 前記移植患者が、腎臓、骨髄、肝臓、肺、胃、骨、精巣、心臓、膵臓、腸およびそれらの組合せからなる群から選択される少なくとも1つの移植臓器を有する、請求項12に記載の方法。
- 前記対象がHIVに感染している、請求項11に記載の方法。
- 前記対象が、原発性または後天性免疫不全を有する、請求項11に記載の方法。
- 前記対象が、免疫抑制療法の結果として免疫無防備状態である、請求項11に記載の方法。
- 少なくとも1つの前記腫瘍が、脳がん、結腸直腸がん、上咽頭癌(NPC)、バーキットリンパ腫(BL)、リンパ腫(例えば、B細胞リンパ腫、ホジキンリンパ腫、ダンカン症候群)、メルケル細胞癌(MCC)、前立腺がん、肝細胞癌、子宮頸がん、肺がん、頭頸部扁平上皮がん、前立腺がん、乳がん、急性リンパ性白血病、成人急性骨髄性白血病、成人非ホジキンリンパ腫、脳腫瘍、小児がん、小児肉腫、慢性リンパ球性白血病、慢性骨髄性白血病、食道がん、有毛細胞白血病、腎臓がん、肝臓がん、多発性骨髄腫、神経芽細胞腫、口腔がん、膵臓がん、原発性中枢神経系リンパ腫、皮膚がんおよびそれらの組合せからなる群から選択される、請求項1から16のいずれかに記載の方法。
- Xが酸素である、請求項1から17のいずれかに記載の方法。
- R3がヒドロキシルである、請求項1から18のいずれかに記載の方法。
- Zが、グアニン−9−イル、アデニン−9−イル、2,6−ジアミノプリン−9−イル、2−アミノプリン−9−イルまたはその1−デアザ、3−デアザもしくは8−アザ化合物、あるいはシトシン−1−イルである、請求項1から19のいずれかに記載の方法。
- R1、R1’、R2またはR2’が、独立に、−O(C1〜C24)アルキル、−O(C2〜C24)アルケニル、−O(C2〜C24)アルキニル、−O(C1〜C24)アシル、−S(C1〜C24)アルキル、−S(C2〜C24)アルケニル、−S(C2〜C24)アルキニル、−S(C1〜C24)アシル、−NH(C1〜C24)アルキル、−NH(C2〜C24)アルケニル、−NH(C2〜C24)アルキニル、−NH(C1〜C24)アシル、−N((C1〜C24)アルキル)((C2〜C24)アルキル)、−N((C1〜C24)アルキル)((C2〜C24)アルケニル)、−N((C1〜C24)アルキル)((C2〜C24)アシル)、−N((C1〜C24)アルキル)((C2〜C24)アルキニル)、−N((C1〜C24)アルケイル))((C2〜C24)アルキニル)、−N((C1〜C24)アルケニル)((C2〜C24)アルケニル)、−N((C1〜C24)アルキニル)((C2〜C24)アルキニル)、−N((C1〜C24)アシル)((C2〜C24)アルキニル)または−N((C1〜C24)アシル)((C2〜C24)アルケニル)である、請求項1から21のいずれかに記載の方法。
- Mが、−O−(CH2)2−O−C1〜24アルキル、−O−(CH2)3−O−C1〜24アルキル、−O−CH2−CH(OH)−CH2−O−C1〜24アルキルおよび−O−CH2−CH(OH)−S−C1〜24アルキルからなる群から選択される、請求項1から22のいずれかに記載の方法。
- Mが−O−(CH2)a−O−(CH2)t−CH3[ここで、aは2から4であり、かつtは11から19である]である、請求項1から22のいずれかに記載の方法。
- Mが−O−(CH2)2−O−(CH2)15CH3、または−O−(CH2)2−O−(CH2)17CH3である、請求項1から22のいずれかに記載の方法。
- Mが−O−(CH2)3−O−(CH2)15CH3、または−O−(CH2)3−O−(CH2)17CH3である、請求項1から22のいずれかに記載の方法。
- Bが−CH3、または−CH2OHである、請求項1から26のいずれかに記載の方法。
- 前記対象が免疫抑制剤を必要としている、請求項1から28のいずれかに記載の方法。
- 前記対象に、少なくとも1種の免疫抑制剤を前記式AまたはBの化合物と組み合わせて投与するステップをさらに含む、請求項29に記載の方法。
- 前記免疫抑制剤が、前記対象に同時発生的にまたは順次に投与される、請求項30に記載の方法。
- 少なくとも1種の前記免疫抑制剤が、ダクリズマブ、バシリキシマブ、タクロリムス、シロリムス、ミコフェノレート(ナトリウムまたはモフェチルとして)、シクロスポリンA、グルココルチコイド、抗CD3モノクローナル抗体(OKT3)、抗胸腺細胞グロブリン(ATG)、抗CD52モノクローナル抗体(キャンパス1−H)、アザチオプリン、エベロリムス、ダクチノマイシン、シクロフォスファミド、白金、ニトロソ尿素、メトトレキサート、アザチオプリン、メルカプトプリン、ムロモナブ、IFNガンマ、インフリキシマブ、エタネルセプト、アダリムマブ、タイサブリ(ナタリズマブ)、フィンゴリモドおよびそれらの組合せからなる群から選択される、請求項30に記載の方法。
- 少なくとも1種の前記免疫抑制剤がタイサブリ(ナタリズマブ)である、請求項30に記載の方法。
- 免疫抑制剤を必要としている対象において、ウイルス感染を治療するための方法であって、前記対象に、治療有効量の式Aもしくは式Bの化合物
Mは
Qは、存在する場合、
Bは、水素、−CH3、F、CF3、−CHF2、−CH2CH3、−CH2OH、−CH2CH2OH、−CH(OH)CH3、−CH2F、−CH=CH2および−CH2N3からなる群から選択され、
Xは、セレン、硫黄または酸素から選択され、
R3は、ヒドロキシ、−OR2a、−BH3、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニルまたは−NR’Hであり、
R2aは、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニル、−P(=O)(OH)2または−P(=O)(OH)OP(=O)(OH)2であり、
R’は、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルキニル、C2〜8ヘテロアルケニル、C6〜10アリール、または置換もしくは非置換アミノ酸残基であり、
Zは、少なくとも1個のNを含む複素環式部分を含み、かつ
符号*は、式(A)または(B)中のメチレンとZとの結合点が、前記複素環式部分の利用可能な窒素を介していることを指示する]、
または薬学的に許容されるその塩、立体異性体、ジアステレオマー、鏡像異性体もしくはラセミ体を投与するステップを含む方法。 - 少なくとも1種の前記免疫抑制剤が、ダクリズマブ、バシリキシマブ、タクロリムス、シロリムス、ミコフェノレート(ナトリウムまたはモフェチルとして)、シクロスポリンA、グルココルチコイド、抗CD3モノクローナル抗体(OKT3)、抗胸腺細胞グロブリン(ATG)、抗CD52モノクローナル抗体(キャンパス1−H)、アザチオプリン、エベロリムス、ダクチノマイシン、シクロフォスファミド、白金、ニトロソ尿素、メトトレキサート、アザチオプリン、メルカプトプリン、ムロモナブ、IFNガンマ、インフリキシマブ、エタネルセプト、アダリムマブ、タイサブリ(ナタリズマブ)、フィンゴリモドおよびそれらの組合せからなる群から選択される、請求項35に記載の方法。
- 少なくとも1種の前記免疫抑制剤がタイサブリ(ナタリズマブ)である、請求項36に記載の方法。
- Xが酸素である、請求項35から37に記載の方法。
- R3がヒドロキシルである、請求項35から38のいずれかに記載の方法。
- Zが、グアニン−9−イル、アデニン−9−イル、2,6−ジアミノプリン−9−イル、2−アミノプリン−9−イルまたはその1−デアザ、3−デアザもしくは8−アザ化合物、あるいはシトシン−1−イルである、請求項35から39のいずれかに記載の方法。
- R1、R1’、R2、R2’が、独立に、−O(C1〜C24)アルキル、−O(C2〜C24)アルケニル、−O(C2〜C24)アルキニル、−O(C1〜C24)アシル、−S(C1〜C24)アルキル、−S(C2〜C24)アルケニル、−S(C2〜C24)アルキニル、−S(C1〜C24)アシル、−NH(C1〜C24)アルキル、−NH(C2〜C24)アルケニル、−NH(C2〜C24)アルキニル、−NH(C1〜C24)アシル、−N((C1〜C24)アルキル)((C2〜C24)アルキル)、−N((C1〜C24)アルキル)((C2〜C24)アルケニル)、−N((C1〜C24)アルキル)((C2〜C24)アシル)、−N((C1〜C24)アルキル)((C2〜C24)アルキニル)、−N((C1〜C24)アルケイル))((C2〜C24)アルキニル)、−N((C1〜C24)アルケニル)((C2〜C24)アルケニル)、−N((C1〜C24)アルキニル)((C2〜C24)アルキニル)、−N((C1〜C24)アシル)((C2〜C24)アルキニル)または−N((C1〜C24)アシル)((C2〜C24)アルケニル)である、請求項35から41のいずれかに記載の方法。
- Mが、−O−(CH2)2−O−C1〜24アルキ、−O−(CH2)3−O−C1〜24アルキル、−O−CH2−CH(OH)−CH2−O−C1〜24アルキルおよび−O−CH2−CH(OH)−S−C1〜24アルキルからなる群から選択される、請求項35から42のいずれかに記載の方法。
- Mが−O−(CH2)a−O−(CH2)t−CH3[ここで、aは2から4であり、かつtは11から19である]である、請求項35から42のいずれかに記載の方法。
- Mが−O−(CH2)2−O−(CH2)15CH3または−O−(CH2)2−O−(CH2)17CH3である、請求項35から42のいずれかに記載の方法。
- Mが−O−(CH2)3−O−(CH2)15CH3または−O−(CH2)3−O−(CH2)17CH3である、請求項35から42のいずれかに記載の方法。
- Bが−CH3または−CH2OHである、請求項35から46のいずれかに記載の方法。
- 少なくとも1種のウイルス感染が、ヒト免疫不全ウイルス(HIV)、インフルエンザ、単純ヘルペスウイルス−1(HSV−1)、単純ヘルペスウイルス−2(HSV−2)、ヒトヘルペスウイルス6(HHV−6)、水痘帯状疱疹ウイルス(VZV)、エプスタイン・バーウイルス(EBV)、リンホクリプトウイルス、サイトメガロウイルス(CMV)、オルトポックスウイルス、天然痘、牛痘、ラクダ痘、サル痘、B型肝炎、C型肝炎ウイルス、大痘瘡および小痘瘡ウイルス、ワクシニア、エボラウイルス、パピローマウイルス、アデノウイルス、ポリオーマウイルス、ならびにそれらの組合せからなる群から選択されるウイルスに関連する、請求項35から49のいずれかに記載の方法。
- 少なくとも1種の前記ウイルスが、ヒトサイトメガロウイルス、BKウイルス、ジョン・カニンガムウイルス、ヒトヘルペスウイルス6(HHV−6)、ヒト単純ヘルペスウイルス、アデノウイルス、エプスタイン・バーウイルスおよびそれらの組合せからなる群から選択される、請求項35から49に記載の方法。
- 少なくとも1種の前記ウイルスが、ヒトパピローマウイルス、ワタオウサギパピローマウイルス、ウマパピローマウイルス、ウシパピローマウイルスおよびそれらの組合せからなる群から選択される、請求項35から49に記載の方法。
- 少なくとも1種のウイルスが、ジョン・カニンガムウイルス(JCV)、BKウイルス、SV40、メルケル細胞ウイルス(MCV)、KIポリオーマウイルス(KIV)、WUポリオーマウイルス(WUV)、シミアンウイルス40(SV40)およびそれらの組合せからなる群から選択される、請求項50に記載の方法。
- 請求項1から53のいずれか一項に記載の治療方法を行うための、式AまたはBの化合物。
- 請求項1から53のいずれか一項に記載の方法を行うための薬剤を調製するための、式AまたはBの化合物の使用。
- (a)式Aもしくは式Bの化合物
Mは
Qは、存在する場合、
Bは、水素、−CH3、F、CF3、−CHF2、−CH2CH3、−CH2OH、−CH2CH2OH、−CH(OH)CH3、−CH2F、−CH=CH2および−CH2N3からなる群から選択され、
Xは、セレン、硫黄または酸素から選択され、
R3は、ヒドロキシ、−OR2a、−BH3、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニルまたは−NR’Hであり、
R2aは、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルケニル、C2〜8ヘテロアルキニル、−P(=O)(OH)2または−P(=O)(OH)OP(=O)(OH)2であり、
R’は、C1〜8アルキル、C2〜8アルケニル、C2〜8アルキニル、C1〜8ヘテロアルキル、C2〜8ヘテロアルキニル、C2〜8ヘテロアルケニル、C6〜10アリール、または置換もしくは非置換アミノ酸残基であり、
Zは、少なくとも1個のNを含む複素環式部分を含み、かつ
符号*は、式(A)または(B)中のメチレンとZとの結合点が、前記複素環式部分の利用可能な窒素を介していることを指示する]、
または薬学的に許容されるその塩、立体異性体、ジアステレオマー、鏡像異性体もしくはラセミ体と、
(b)少なくとも1種の免疫抑制剤と、
(c)薬学的に許容される担体と
を含む、医薬組成物。 - 少なくとも1種の前記免疫抑制剤が、ダクリズマブ、バシリキシマブ、タクロリムス、シロリムス、ミコフェノレート(ナトリウムまたはモフェチルとして)、シクロスポリンA、グルココルチコイド、抗CD3モノクローナル抗体(OKT3)、抗胸腺細胞グロブリン(ATG)、抗CD52モノクローナル抗体(キャンパス1−H)、アザチオプリン、エベロリムス、ダクチノマイシン、シクロフォスファミド、白金、ニトロソ尿素、メトトレキサート、アザチオプリン、メルカプトプリン、ムロモナブ、IFNガンマ、インフリキシマブ、エタネルセプト、アダリムマブ、タイサブリ(ナタリズマブ)、フィンゴリモドおよびそれらの組合せからなる群から選択される、請求項56に記載の組成物。
- 少なくとも1種の前記免疫抑制剤がタイサブリ(ナタリズマブ)である、請求項56に記載の組成物。
- Xが酸素である、請求項56から58のいずれかに記載の組成物。
- R2がヒドロキシルである、請求項56から59のいずれかに記載の組成物。
- Zが、グアニン−9−イル、アデニン−9−イル、2,6−ジアミノプリン−9−イル、2−アミノプリン−9−イルまたはその1−デアザ、3−デアザもしくは8−アザ化合物、あるいはシトシン−1−イルである、請求項56から60のいずれかに記載の組成物。
- Mが、−O−(CH2)2−O−C1〜24アルキル、−O−(CH2)3−O−C1〜24アルキル、−O−CH2−CH(OH)−CH2−O−C1〜24アルキル、および−O−CH2−CH(OH)−S−C1〜24アルキルからなる群から選択される、請求項56から62のいずれかに記載の組成物。
- Mが−O−(CH2)a−O−(CH2)t−CH3[ここで、aは2から4であり、かつtは11から19である]である、請求項56から62のいずれかに記載の組成物。
- Mが−O−(CH2)2−O−(CH2)15CH3または−O−(CH2)2−O−(CH2)17CH3である、請求項56から62のいずれかに記載の組成物。
- Mが−O−(CH2)3−O−(CH2)15CH3または−O−(CH2)3−O−(CH2)17CH3である、請求項56から62のいずれかに記載の組成物。
- Bが−CH3または−CH2OHである、請求項56から66のいずれかに記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US23093109P | 2009-08-03 | 2009-08-03 | |
| US61/230,931 | 2009-08-03 | ||
| PCT/US2010/044093 WO2011017253A1 (en) | 2009-08-03 | 2010-08-02 | Composition and methods of treating viral infections and viral induced tumors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013501056A true JP2013501056A (ja) | 2013-01-10 |
| JP2013501056A5 JP2013501056A5 (ja) | 2013-09-12 |
Family
ID=43544613
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012523680A Pending JP2013501056A (ja) | 2009-08-03 | 2010-08-02 | ウイルス感染およびウイルス誘発腫瘍を治療する組成物および方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20120164104A1 (ja) |
| EP (1) | EP2462152A4 (ja) |
| JP (1) | JP2013501056A (ja) |
| AU (1) | AU2010279678B2 (ja) |
| BR (1) | BR112012002551A2 (ja) |
| CA (1) | CA2770282A1 (ja) |
| WO (1) | WO2011017253A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016515128A (ja) * | 2013-03-15 | 2016-05-26 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 非環式ヌクレオシドホスホン酸ジエステル |
| JP2018522836A (ja) * | 2015-06-01 | 2018-08-16 | エクイガーミナル エスエー | 抗ウイルス組成物 |
| WO2024047811A1 (ja) * | 2022-08-31 | 2024-03-07 | シンバイオ製薬株式会社 | リンパ腫の治療用医薬組成物 |
| WO2024048657A1 (ja) * | 2022-08-31 | 2024-03-07 | シンバイオ製薬株式会社 | リンパ腫の治療用医薬組成物 |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006110655A2 (en) | 2005-04-08 | 2006-10-19 | Chimerix, Inc. | Compounds, compositions and methods for the treatment of poxvirus infections |
| US8524248B2 (en) | 2007-12-14 | 2013-09-03 | University of Pittsburgh—of the Commonwealth System of Higher Education | Methods to diagnose and immunize against the virus causing human Merkel cell carcinoma |
| EP3085377A1 (en) | 2008-01-25 | 2016-10-26 | Chimerix, Inc. | Methods of treating viral infections |
| US20120034266A1 (en) * | 2008-03-04 | 2012-02-09 | Nel Andre E | Methods and compositions for improving immune response by a nutraceutical antioxidant |
| WO2011011519A1 (en) | 2009-07-21 | 2011-01-27 | Chimerix, Inc. | Compounds, compositions and methods for treating ocular conditions |
| US20130072458A1 (en) * | 2009-10-30 | 2013-03-21 | Chimerix, Inc. | Methods of Treating Viral Associated Diseases |
| EP2534150B1 (en) | 2010-02-12 | 2017-04-05 | Chimerix, Inc. | Methods of treating viral infection |
| AU2011248620B2 (en) | 2010-04-26 | 2015-11-26 | Chimerix, Inc. | Methods of treating retroviral infections and related dosage regimes |
| EP2611818B1 (en) * | 2010-08-31 | 2016-08-24 | Chimerix, Inc. | Phosphonate ester derivatives and methods of synthesis thereof |
| US20140303092A1 (en) * | 2011-10-26 | 2014-10-09 | Chimerix, Inc | Hexadecyloxypropyl cidofovir for the treatment of double-stranded dna virus infection |
| EP2794624B1 (en) | 2011-12-22 | 2019-05-15 | Geron Corporation | Guanine analogs as telomerase substrates and telomere length affectors |
| CN103665043B (zh) | 2012-08-30 | 2017-11-10 | 江苏豪森药业集团有限公司 | 一种替诺福韦前药及其在医药上的应用 |
| WO2014146218A1 (zh) * | 2013-03-22 | 2014-09-25 | 当代绿能科技股份有限公司 | 马替麦考酚酯或其盐类用于制备抗流感病毒之药物的用途 |
| CN105899215A (zh) * | 2013-11-15 | 2016-08-24 | 奇默里克斯公司 | 十六烷氧基丙基膦酸酯的形态 |
| EP3194411B1 (en) | 2014-09-15 | 2022-05-04 | The Regents of the University of California | Nucleotide analogs |
| WO2016069630A1 (en) | 2014-10-27 | 2016-05-06 | Concert Pharmaceuticals, Inc. | Pyrimidine phosphonic acid esters bearing at least one deuterium atom |
| WO2017048956A1 (en) | 2015-09-15 | 2017-03-23 | The Regents Of The University Of California | Nucleotide analogs |
| CN113288896A (zh) * | 2021-05-28 | 2021-08-24 | 成都中医药大学 | 槐定碱在制备抗疱疹病毒的药物中的用途 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008133966A1 (en) * | 2007-04-27 | 2008-11-06 | Chimerix, Inc. | Methods of reducing nephrotoxicity in subjects administered with nucleoside |
Family Cites Families (44)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA777769A (en) | 1963-03-18 | 1968-02-06 | H. Roy Clarence | Substituted methylene diphosphonic acid compounds and detergent compositions |
| DE1248654B (de) | 1964-11-11 | 1967-08-31 | Albright & Wilson (Mf g) Limited, Oldbury, Warwickshire (Großbritannien) | Verfahren zur Herstellung von Phosphonsäuren und deren Salzen |
| DE2943498C2 (de) | 1979-10-27 | 1983-01-27 | Henkel KGaA, 4000 Düsseldorf | Verfahren zur Herstellung von 3-Amino-1-hydroxypropan-1,1-diphosphonsäure |
| US5047533A (en) | 1983-05-24 | 1991-09-10 | Sri International | Acyclic purine phosphonate nucleotide analogs |
| IT1196315B (it) | 1984-10-29 | 1988-11-16 | Gentili Ist Spa | Procedimento per la preparazione di acidi difosfonici |
| IL77243A (en) | 1984-12-21 | 1996-11-14 | Procter & Gamble | Pharmaceutical compositions containing geminal diphosphonic acid compounds and certain such novel compounds |
| GB8530603D0 (en) | 1985-12-12 | 1986-01-22 | Leo Pharm Prod Ltd | Chemical compounds |
| DE3623397A1 (de) | 1986-07-11 | 1988-01-14 | Boehringer Mannheim Gmbh | Neue diphosphonsaeurederivate, verfahren zu deren herstellung und diese verbindungen enthaltende arzneimittel |
| CS264222B1 (en) | 1986-07-18 | 1989-06-13 | Holy Antonin | N-phosphonylmethoxyalkylderivatives of bases of pytimidine and purine and method of use them |
| US5247085A (en) | 1987-11-30 | 1993-09-21 | Beecham Group P.L.C. | Antiviral purine compounds |
| SU1548182A1 (ru) | 1987-12-29 | 1990-03-07 | Институт молекулярной биологии АН СССР | 5 @ -Фосфонаты 3 @ -азидо-2 @ ,3 @ -дидезоксинуклеозидов, вл ющиес специфическими ингибиторами вируса СПИД в культуре лимфоцитов человека Н9/ШВ |
| US5196409A (en) | 1989-08-20 | 1993-03-23 | Yissum, Research Development Company Of The Hebrew University Of Jerusalem | Bisphosphonates, pharmaceutical compositions, and process for the treatment of irregularities in calcium metabolism |
| IL91362A0 (en) | 1989-08-20 | 1990-03-19 | Yissum Res Dev Co | Bisphosphonates,process for preparing them and pharmaceutical compositions containing them |
| IT1241674B (it) | 1989-10-12 | 1994-01-27 | Boehringer Biochemia Srl | Acidi gem-difosfonici, un processo per la loro preparazione e composizioni farmaceutiche che li contengono. |
| US5039819A (en) | 1990-09-18 | 1991-08-13 | Merck & Co., Inc. | Diphosphonate intermediate for preparing an antihypercalcemic agent |
| FI89365C (fi) | 1990-12-20 | 1993-09-27 | Leiras Oy | Foerfarande foer framstaellning av nya farmakologiskt anvaendbara metylenbisfosfonsyraderivat |
| US5183815A (en) | 1991-01-22 | 1993-02-02 | Merck & Co., Inc. | Bone acting agents |
| US5672697A (en) | 1991-02-08 | 1997-09-30 | Gilead Sciences, Inc. | Nucleoside 5'-methylene phosphonates |
| US5300687A (en) | 1991-07-18 | 1994-04-05 | Ortho Pharmaceutical Corporation | Trifluoromethylbenzylphosphonates useful in treating osteoporosis |
| US5270365A (en) | 1991-12-17 | 1993-12-14 | Merck & Co., Inc. | Prevention and treatment of periodontal disease with alendronate |
| JP3141053B2 (ja) | 1991-12-26 | 2001-03-05 | アベンティス ファーマ株式会社 | ビスホスホン酸誘導体 |
| SK144694A3 (en) | 1992-05-29 | 1995-06-07 | Procter & Gamble Pharma | Thio-substituted nitrogen containing heterocyclic phosphate compounds for treating calcium and phosphate metabolism |
| DK0600371T3 (da) | 1992-12-02 | 1999-09-20 | Hoechst Ag | Guanidinalkyl-1,1-bisphosphonsyrederivater, fremgangsmåde til deres fremstilling samt deres anvendelse |
| US5817647A (en) | 1993-04-01 | 1998-10-06 | Merrell Pharmaceuticals Inc. | Unsaturated acetylene phosphonate derivatives of purines |
| CA2171868A1 (en) | 1993-09-17 | 1995-03-23 | Petr Alexander | Method for dosing therapeutic compounds |
| US5798340A (en) | 1993-09-17 | 1998-08-25 | Gilead Sciences, Inc. | Nucleotide analogs |
| US5656745A (en) | 1993-09-17 | 1997-08-12 | Gilead Sciences, Inc. | Nucleotide analogs |
| US5441946A (en) | 1994-04-14 | 1995-08-15 | Rhone-Poulenc-Rorer Pharmaceuticals, Inc. | Phosphonate derivatives of lipophilic amines |
| EP0753523A1 (en) | 1995-07-10 | 1997-01-15 | Gador S.A. | Amino-substituted bisphosphonic acids |
| US5885973A (en) | 1995-12-27 | 1999-03-23 | Gador, S.A. | Bone mass anabolic composition comprising olpadronate |
| US5717095A (en) | 1995-12-29 | 1998-02-10 | Gilead Sciences, Inc. | Nucleotide analogs |
| TW369536B (en) | 1996-01-18 | 1999-09-11 | Mitsubishi Chem Corp | Phosphonate nucleotide compounds |
| US5877166A (en) | 1996-04-29 | 1999-03-02 | Sri International | Enantiomerically pure 2-aminopurine phosphonate nucleotide analogs as antiviral agents |
| US5922695A (en) | 1996-07-26 | 1999-07-13 | Gilead Sciences, Inc. | Antiviral phosphonomethyoxy nucleotide analogs having increased oral bioavarilability |
| US5760013A (en) | 1996-08-21 | 1998-06-02 | National Science Council | Thymidylate analogs and the use thereof |
| EP1012236A1 (en) * | 1997-08-15 | 2000-06-28 | Rubicon Laboratory Inc. | Retrovirus and viral vectors |
| EP1214074B1 (en) | 1999-09-24 | 2004-06-16 | Shire Biochem Inc. | Dioxolane nucleoside analogs for the treatment or prevention of viral infection |
| PT1914237E (pt) | 1999-12-03 | 2014-09-09 | Univ California | Compostos antivíricos de éster fosfonato |
| US20050187192A1 (en) * | 2004-02-20 | 2005-08-25 | Kucera Pharmaceutical Company | Phospholipids for the treatment of infection by togaviruses, herpes viruses and coronaviruses |
| TW200714289A (en) * | 2005-02-28 | 2007-04-16 | Genentech Inc | Treatment of bone disorders |
| WO2006110655A2 (en) | 2005-04-08 | 2006-10-19 | Chimerix, Inc. | Compounds, compositions and methods for the treatment of poxvirus infections |
| AR057023A1 (es) | 2005-05-16 | 2007-11-14 | Gilead Sciences Inc | Compuestos heterociclicos con propiedades inhibidoras de hiv-integrasa |
| ES2600792T3 (es) * | 2006-05-03 | 2017-02-10 | Chimerix, Inc. | Alcoxialquilésteres metabólicamente estables de fosfonatos, fosfonatos nucleosídicos y fosfatos nucleosídicos antivirales o antiproliferativos |
| US20090111774A1 (en) * | 2007-06-01 | 2009-04-30 | Luitpold Pharmaceuticals, Inc. | Pmea lipid conjugates |
-
2010
- 2010-08-02 EP EP10806986A patent/EP2462152A4/en not_active Withdrawn
- 2010-08-02 AU AU2010279678A patent/AU2010279678B2/en active Active
- 2010-08-02 JP JP2012523680A patent/JP2013501056A/ja active Pending
- 2010-08-02 CA CA2770282A patent/CA2770282A1/en not_active Abandoned
- 2010-08-02 US US13/388,771 patent/US20120164104A1/en not_active Abandoned
- 2010-08-02 WO PCT/US2010/044093 patent/WO2011017253A1/en active Application Filing
- 2010-08-02 BR BR112012002551A patent/BR112012002551A2/pt not_active IP Right Cessation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008133966A1 (en) * | 2007-04-27 | 2008-11-06 | Chimerix, Inc. | Methods of reducing nephrotoxicity in subjects administered with nucleoside |
Non-Patent Citations (2)
| Title |
|---|
| JPN6014034653; RANDHAWA, P. et al.: ANTIMICROBIOL AGENTS AND CHEMOTHERAPY Vol.50, No.4, 2006, p.1564-1566 * |
| JPN6015009099; Graft Vol.5, No.82, 2002, S82-87 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016515128A (ja) * | 2013-03-15 | 2016-05-26 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 非環式ヌクレオシドホスホン酸ジエステル |
| JP2019069984A (ja) * | 2013-03-15 | 2019-05-09 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 非環式ヌクレオシドホスホン酸ジエステル |
| JP2018522836A (ja) * | 2015-06-01 | 2018-08-16 | エクイガーミナル エスエー | 抗ウイルス組成物 |
| WO2024047811A1 (ja) * | 2022-08-31 | 2024-03-07 | シンバイオ製薬株式会社 | リンパ腫の治療用医薬組成物 |
| WO2024048657A1 (ja) * | 2022-08-31 | 2024-03-07 | シンバイオ製薬株式会社 | リンパ腫の治療用医薬組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2011017253A1 (en) | 2011-02-10 |
| BR112012002551A2 (pt) | 2017-06-13 |
| AU2010279678A1 (en) | 2012-03-01 |
| US20120164104A1 (en) | 2012-06-28 |
| AU2010279678B2 (en) | 2015-09-10 |
| EP2462152A4 (en) | 2013-02-13 |
| EP2462152A1 (en) | 2012-06-13 |
| CA2770282A1 (en) | 2011-02-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2013501056A (ja) | ウイルス感染およびウイルス誘発腫瘍を治療する組成物および方法 | |
| AU2010313273B2 (en) | Methods of treating viral associated diseases | |
| US20220296626A1 (en) | Nucleotide and nucleoside therapeutic compositions and uses related thereto | |
| ES2915381T3 (es) | Análogos de nucleótidos | |
| CN102939291B (zh) | 用于病毒感染治疗的具有降低的毒性的膦酸酯 | |
| TW201840563A (zh) | 治療b型肝炎病毒感染的化合物 | |
| WO2014124430A1 (en) | Nucleotide and nucleoside therapeutic compositions and uses related thereto | |
| AU2013356386B2 (en) | Nucleoside kinase bypass compositions and methods | |
| JP2023531524A (ja) | 1’-シアノヌクレオシド類似体及びその使用 | |
| EP2922859A1 (en) | Phosphonucleosides useful in the treatment of viral disorders | |
| US20170333459A1 (en) | Methods of treating orthopox virus infections and associated diseases | |
| KR20220142483A (ko) | 항바이러스 화합물 | |
| US20190085013A1 (en) | Nucleotide and nucleoside therapeutic compositions and uses related thereto | |
| AU2021330835A1 (en) | Phospholipid compounds and uses thereof | |
| US20230062181A1 (en) | Alkyne containing nucleotide and nucleoside therapeutic compositions and uses related thereto | |
| WO2017106710A1 (en) | Nucleotide and nucleoside therapeutic compositions and uses related thereto | |
| CA3193879A1 (en) | Phospholipid compounds and uses thereof | |
| WO2011011710A1 (en) | Methods of treating viral infections | |
| AU2015264949A1 (en) | Composition and methods of treating viral infections and viral induced tumors | |
| AU2015203573A1 (en) | Methods of treating viral associated diseases | |
| JP2021528465A (ja) | 代謝安定性プロドラッグ | |
| CN102665729A (zh) | 用于治疗病毒相关性疾病的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130802 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130802 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140815 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141113 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141120 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141215 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150306 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150706 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150707 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20151105 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20151204 |