JP2010528639A - 抗原提示細胞 - Google Patents
抗原提示細胞 Download PDFInfo
- Publication number
- JP2010528639A JP2010528639A JP2010510798A JP2010510798A JP2010528639A JP 2010528639 A JP2010528639 A JP 2010528639A JP 2010510798 A JP2010510798 A JP 2010510798A JP 2010510798 A JP2010510798 A JP 2010510798A JP 2010528639 A JP2010528639 A JP 2010528639A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- allergen
- phl
- vector
- der
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000000612 antigen-presenting cell Anatomy 0.000 title description 5
- 239000013566 allergen Substances 0.000 claims abstract description 185
- 238000000034 method Methods 0.000 claims abstract description 67
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 63
- 102000004196 processed proteins & peptides Human genes 0.000 claims abstract description 61
- 229920001184 polypeptide Polymers 0.000 claims abstract description 55
- 210000004027 cell Anatomy 0.000 claims description 103
- 239000013598 vector Substances 0.000 claims description 66
- 210000003958 hematopoietic stem cell Anatomy 0.000 claims description 57
- 108020004414 DNA Proteins 0.000 claims description 43
- 206010020751 Hypersensitivity Diseases 0.000 claims description 37
- 230000007815 allergy Effects 0.000 claims description 31
- 108010076504 Protein Sorting Signals Proteins 0.000 claims description 16
- 208000026935 allergic disease Diseases 0.000 claims description 16
- 239000012528 membrane Substances 0.000 claims description 16
- 238000011282 treatment Methods 0.000 claims description 16
- 241001430294 unidentified retrovirus Species 0.000 claims description 16
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 15
- 150000007523 nucleic acids Chemical class 0.000 claims description 14
- 230000002265 prevention Effects 0.000 claims description 14
- 230000001177 retroviral effect Effects 0.000 claims description 14
- 108020004707 nucleic acids Proteins 0.000 claims description 13
- 102000039446 nucleic acids Human genes 0.000 claims description 13
- 210000003651 basophil Anatomy 0.000 claims description 12
- 230000003248 secreting effect Effects 0.000 claims description 12
- 239000013603 viral vector Substances 0.000 claims description 12
- 230000000774 hypoallergenic effect Effects 0.000 claims description 11
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 10
- 210000004443 dendritic cell Anatomy 0.000 claims description 9
- 239000002245 particle Substances 0.000 claims description 8
- 102000053602 DNA Human genes 0.000 claims description 7
- 230000003612 virological effect Effects 0.000 claims description 7
- 241000713883 Myeloproliferative sarcoma virus Species 0.000 claims description 6
- 238000004519 manufacturing process Methods 0.000 claims description 6
- 108010061629 Dermatophagoides pteronyssinus antigen p 1 Proteins 0.000 claims description 5
- 108010061608 Dermatophagoides pteronyssinus antigen p 2 Proteins 0.000 claims description 5
- 108010061573 Dermatophagoides pteronyssinus antigen p 5 Proteins 0.000 claims description 5
- 108010061638 Dermatophagoides pteronyssinus antigen p 7 Proteins 0.000 claims description 5
- 208000032839 leukemia Diseases 0.000 claims description 5
- 210000001616 monocyte Anatomy 0.000 claims description 5
- 241000701022 Cytomegalovirus Species 0.000 claims description 4
- 241001529936 Murinae Species 0.000 claims description 4
- 210000000170 cell membrane Anatomy 0.000 claims description 4
- 239000003814 drug Substances 0.000 claims description 4
- 210000003979 eosinophil Anatomy 0.000 claims description 4
- 210000002540 macrophage Anatomy 0.000 claims description 4
- 210000000822 natural killer cell Anatomy 0.000 claims description 4
- 210000000440 neutrophil Anatomy 0.000 claims description 4
- 239000013600 plasmid vector Substances 0.000 claims description 4
- 241000829100 Macaca mulatta polyomavirus 1 Species 0.000 claims description 3
- 238000004520 electroporation Methods 0.000 claims description 3
- 239000003623 enhancer Substances 0.000 claims description 3
- 230000010076 replication Effects 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- 108010088751 Albumins Proteins 0.000 claims description 2
- 102000009027 Albumins Human genes 0.000 claims description 2
- 108010001857 Cell Surface Receptors Proteins 0.000 claims description 2
- 108010003533 Viral Envelope Proteins Proteins 0.000 claims description 2
- 125000002091 cationic group Chemical group 0.000 claims description 2
- 229920006317 cationic polymer Polymers 0.000 claims description 2
- 210000003917 human chromosome Anatomy 0.000 claims description 2
- 230000003993 interaction Effects 0.000 claims description 2
- 210000004779 membrane envelope Anatomy 0.000 claims description 2
- 102000006240 membrane receptors Human genes 0.000 claims description 2
- 238000000520 microinjection Methods 0.000 claims description 2
- 150000003904 phospholipids Chemical class 0.000 claims description 2
- 238000000053 physical method Methods 0.000 claims description 2
- 239000008194 pharmaceutical composition Substances 0.000 claims 1
- 230000003394 haemopoietic effect Effects 0.000 abstract description 6
- 230000006058 immune tolerance Effects 0.000 abstract description 3
- 241000699670 Mus sp. Species 0.000 description 65
- 239000000427 antigen Substances 0.000 description 41
- 229960004784 allergens Drugs 0.000 description 40
- 108091007433 antigens Proteins 0.000 description 40
- 102000036639 antigens Human genes 0.000 description 40
- 108090000623 proteins and genes Proteins 0.000 description 30
- 239000005090 green fluorescent protein Substances 0.000 description 29
- 210000002798 bone marrow cell Anatomy 0.000 description 27
- 239000012634 fragment Substances 0.000 description 22
- 230000014509 gene expression Effects 0.000 description 22
- 238000002054 transplantation Methods 0.000 description 20
- 235000018102 proteins Nutrition 0.000 description 19
- 102000004169 proteins and genes Human genes 0.000 description 19
- 238000002474 experimental method Methods 0.000 description 18
- 238000000684 flow cytometry Methods 0.000 description 18
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 15
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 15
- 210000000265 leukocyte Anatomy 0.000 description 15
- 241000700605 Viruses Species 0.000 description 14
- 210000002966 serum Anatomy 0.000 description 14
- 241000283725 Bos Species 0.000 description 12
- 239000002609 medium Substances 0.000 description 12
- 239000013612 plasmid Substances 0.000 description 12
- 230000027455 binding Effects 0.000 description 11
- 210000001185 bone marrow Anatomy 0.000 description 11
- 150000001413 amino acids Chemical group 0.000 description 10
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 9
- 238000000338 in vitro Methods 0.000 description 9
- 238000001727 in vivo Methods 0.000 description 9
- 238000010361 transduction Methods 0.000 description 9
- 230000026683 transduction Effects 0.000 description 9
- 206010068051 Chimerism Diseases 0.000 description 8
- 230000000694 effects Effects 0.000 description 8
- 230000028993 immune response Effects 0.000 description 8
- 238000009169 immunotherapy Methods 0.000 description 8
- 230000004044 response Effects 0.000 description 8
- 210000003491 skin Anatomy 0.000 description 8
- 241000699666 Mus <mouse, genus> Species 0.000 description 7
- 230000000172 allergic effect Effects 0.000 description 7
- 235000001014 amino acid Nutrition 0.000 description 7
- 210000000349 chromosome Anatomy 0.000 description 7
- 210000000987 immune system Anatomy 0.000 description 7
- 238000001890 transfection Methods 0.000 description 7
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 230000007774 longterm Effects 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 230000009257 reactivity Effects 0.000 description 6
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 5
- 239000012983 Dulbecco’s minimal essential medium Substances 0.000 description 5
- 108091028043 Nucleic acid sequence Proteins 0.000 description 5
- 206010070834 Sensitisation Diseases 0.000 description 5
- 102000007478 beta-N-Acetylhexosaminidases Human genes 0.000 description 5
- 108010085377 beta-N-Acetylhexosaminidases Proteins 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 238000010322 bone marrow transplantation Methods 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 238000010586 diagram Methods 0.000 description 5
- 239000012636 effector Substances 0.000 description 5
- 239000012894 fetal calf serum Substances 0.000 description 5
- 230000004927 fusion Effects 0.000 description 5
- 230000035755 proliferation Effects 0.000 description 5
- 230000008313 sensitization Effects 0.000 description 5
- 239000008279 sol Substances 0.000 description 5
- 230000000638 stimulation Effects 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- 210000003462 vein Anatomy 0.000 description 5
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 4
- 101100289995 Caenorhabditis elegans mac-1 gene Proteins 0.000 description 4
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 4
- 239000007995 HEPES buffer Substances 0.000 description 4
- 240000004760 Pimpinella anisum Species 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000002009 allergenic effect Effects 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 229960002949 fluorouracil Drugs 0.000 description 4
- 230000003053 immunization Effects 0.000 description 4
- 238000002649 immunization Methods 0.000 description 4
- 230000001939 inductive effect Effects 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 238000003780 insertion Methods 0.000 description 4
- 230000037431 insertion Effects 0.000 description 4
- 210000004698 lymphocyte Anatomy 0.000 description 4
- 230000035772 mutation Effects 0.000 description 4
- 210000005259 peripheral blood Anatomy 0.000 description 4
- 239000011886 peripheral blood Substances 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 230000003578 releasing effect Effects 0.000 description 4
- 238000012546 transfer Methods 0.000 description 4
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 3
- -1 Der f 3 Proteins 0.000 description 3
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 3
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 3
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 3
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 3
- 108700008625 Reporter Genes Proteins 0.000 description 3
- 108700019146 Transgenes Proteins 0.000 description 3
- 230000003187 abdominal effect Effects 0.000 description 3
- 230000000961 alloantigen Effects 0.000 description 3
- 125000000539 amino acid group Chemical group 0.000 description 3
- 230000001580 bacterial effect Effects 0.000 description 3
- 229910002091 carbon monoxide Inorganic materials 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000004700 fetal blood Anatomy 0.000 description 3
- 229960001340 histamine Drugs 0.000 description 3
- 210000003630 histaminocyte Anatomy 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 230000010354 integration Effects 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 231100000636 lethal dose Toxicity 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- 230000002093 peripheral effect Effects 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 238000010181 skin prick test Methods 0.000 description 3
- 210000004989 spleen cell Anatomy 0.000 description 3
- 210000000130 stem cell Anatomy 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 238000012384 transportation and delivery Methods 0.000 description 3
- 238000002255 vaccination Methods 0.000 description 3
- 108700001624 vesicular stomatitis virus G Proteins 0.000 description 3
- 208000023275 Autoimmune disease Diseases 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 108010062580 Concanavalin A Proteins 0.000 description 2
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 2
- 229930182566 Gentamicin Natural products 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 101100537948 Mus musculus Trir gene Proteins 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 238000012300 Sequence Analysis Methods 0.000 description 2
- 230000006052 T cell proliferation Effects 0.000 description 2
- 101710120037 Toxin CcdB Proteins 0.000 description 2
- 229920004890 Triton X-100 Polymers 0.000 description 2
- 239000013504 Triton X-100 Substances 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 229940074608 allergen extract Drugs 0.000 description 2
- 230000002052 anaphylactic effect Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000013575 birch pollen allergen Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000002759 chromosomal effect Effects 0.000 description 2
- 229920002055 compound 48/80 Polymers 0.000 description 2
- 230000000368 destabilizing effect Effects 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000013401 experimental design Methods 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 229960002518 gentamicin Drugs 0.000 description 2
- 210000003714 granulocyte Anatomy 0.000 description 2
- 230000009610 hypersensitivity Effects 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 239000012948 isocyanate Substances 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000003449 preventive effect Effects 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 230000003362 replicative effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 230000004043 responsiveness Effects 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 238000010254 subcutaneous injection Methods 0.000 description 2
- 239000007929 subcutaneous injection Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 238000013518 transcription Methods 0.000 description 2
- 230000035897 transcription Effects 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- 241001515965 unidentified phage Species 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- IQFYYKKMVGJFEH-OFKYTIFKSA-N 1-[(2r,4s,5r)-4-hydroxy-5-(tritiooxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound C1[C@H](O)[C@@H](CO[3H])O[C@H]1N1C(=O)NC(=O)C(C)=C1 IQFYYKKMVGJFEH-OFKYTIFKSA-N 0.000 description 1
- AZUYLZMQTIKGSC-UHFFFAOYSA-N 1-[6-[4-(5-chloro-6-methyl-1H-indazol-4-yl)-5-methyl-3-(1-methylindazol-5-yl)pyrazol-1-yl]-2-azaspiro[3.3]heptan-2-yl]prop-2-en-1-one Chemical compound ClC=1C(=C2C=NNC2=CC=1C)C=1C(=NN(C=1C)C1CC2(CN(C2)C(C=C)=O)C1)C=1C=C2C=NN(C2=CC=1)C AZUYLZMQTIKGSC-UHFFFAOYSA-N 0.000 description 1
- 206010002199 Anaphylactic shock Diseases 0.000 description 1
- 108010086828 Aspergillus niger Asp n 14 allergen Proteins 0.000 description 1
- 235000018185 Betula X alpestris Nutrition 0.000 description 1
- 235000018212 Betula X uliginosa Nutrition 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 241000701822 Bovine papillomavirus Species 0.000 description 1
- COXVTLYNGOIATD-HVMBLDELSA-N CC1=C(C=CC(=C1)C1=CC(C)=C(C=C1)\N=N\C1=C(O)C2=C(N)C(=CC(=C2C=C1)S(O)(=O)=O)S(O)(=O)=O)\N=N\C1=CC=C2C(=CC(=C(N)C2=C1O)S(O)(=O)=O)S(O)(=O)=O Chemical compound CC1=C(C=CC(=C1)C1=CC(C)=C(C=C1)\N=N\C1=C(O)C2=C(N)C(=CC(=C2C=C1)S(O)(=O)=O)S(O)(=O)=O)\N=N\C1=CC=C2C(=CC(=C(N)C2=C1O)S(O)(=O)=O)S(O)(=O)=O COXVTLYNGOIATD-HVMBLDELSA-N 0.000 description 1
- 101710132601 Capsid protein Proteins 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 101710094648 Coat protein Proteins 0.000 description 1
- 108020004635 Complementary DNA Proteins 0.000 description 1
- 206010010741 Conjunctivitis Diseases 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 241000252233 Cyprinus carpio Species 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 206010012434 Dermatitis allergic Diseases 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 108010055622 Dermatophagoides farinae antigen f 1 Proteins 0.000 description 1
- 108010082995 Dermatophagoides farinae antigen f 2 Proteins 0.000 description 1
- 108010082990 Dermatophagoides farinae antigen f 7 Proteins 0.000 description 1
- 108010061612 Dermatophagoides pteronyssinus antigen p 3 Proteins 0.000 description 1
- 108010061569 Dermatophagoides pteronyssinus antigen p 4 Proteins 0.000 description 1
- 108010061636 Dermatophagoides pteronyssinus antigen p 6 Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 241000283074 Equus asinus Species 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 102000004204 Fascin Human genes 0.000 description 1
- 108090000786 Fascin Proteins 0.000 description 1
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102100021181 Golgi phosphoprotein 3 Human genes 0.000 description 1
- 108010034983 Hev b 10 Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101001076408 Homo sapiens Interleukin-6 Proteins 0.000 description 1
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 1
- 238000012404 In vitro experiment Methods 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102000004889 Interleukin-6 Human genes 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 101710177504 Kit ligand Proteins 0.000 description 1
- 108010032926 Lep d I allergen Proteins 0.000 description 1
- 101710125418 Major capsid protein Proteins 0.000 description 1
- 101000932479 Mus musculus Fms-related tyrosine kinase 3 ligand Proteins 0.000 description 1
- 101000716728 Mus musculus Kit ligand Proteins 0.000 description 1
- 101000799460 Mus musculus Thrombopoietin Proteins 0.000 description 1
- 101710141454 Nucleoprotein Proteins 0.000 description 1
- 108010004729 Phycoerythrin Proteins 0.000 description 1
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 1
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 101710083689 Probable capsid protein Proteins 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 244000097202 Rathbunia alamosensis Species 0.000 description 1
- 235000009776 Rathbunia alamosensis Nutrition 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- HATRDXDCPOXQJX-UHFFFAOYSA-N Thapsigargin Natural products CCCCCCCC(=O)OC1C(OC(O)C(=C/C)C)C(=C2C3OC(=O)C(C)(O)C3(O)C(CC(C)(OC(=O)C)C12)OC(=O)CCC)C HATRDXDCPOXQJX-UHFFFAOYSA-N 0.000 description 1
- 102100034195 Thrombopoietin Human genes 0.000 description 1
- 108700009124 Transcription Initiation Site Proteins 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 210000000683 abdominal cavity Anatomy 0.000 description 1
- 108010032918 allergen Asp f 16 Proteins 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 208000003455 anaphylaxis Diseases 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 208000010216 atopic IgE responsiveness Diseases 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000007474 bm medium Substances 0.000 description 1
- 210000002449 bone cell Anatomy 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000013611 chromosomal DNA Substances 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 230000004186 co-expression Effects 0.000 description 1
- 238000012761 co-transfection Methods 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 210000000795 conjunctiva Anatomy 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000000139 costimulatory effect Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 238000004163 cytometry Methods 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000000779 depleting effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 229960003699 evans blue Drugs 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 229940116886 human interleukin-6 Drugs 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 229940042743 immune sera Drugs 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 230000005923 long-lasting effect Effects 0.000 description 1
- 230000002934 lysing effect Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 102000006392 myotrophin Human genes 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 210000004789 organ system Anatomy 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000007918 pathogenicity Effects 0.000 description 1
- 230000001991 pathophysiological effect Effects 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 210000003800 pharynx Anatomy 0.000 description 1
- 239000013573 pollen allergen Substances 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 102000037983 regulatory factors Human genes 0.000 description 1
- 108091008025 regulatory factors Proteins 0.000 description 1
- 108010056030 retronectin Proteins 0.000 description 1
- 239000006152 selective media Substances 0.000 description 1
- 231100000430 skin reaction Toxicity 0.000 description 1
- 230000036555 skin type Effects 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000005030 transcription termination Effects 0.000 description 1
- 230000010474 transient expression Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0647—Haematopoietic stem cells; Uncommitted or multipotent progenitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/35—Allergens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/462—Cellular immunotherapy characterized by the effect or the function of the cells
- A61K39/4621—Cellular immunotherapy characterized by the effect or the function of the cells immunosuppressive or immunotolerising
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/46433—Antigens related to auto-immune diseases; Preparations to induce self-tolerance
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/464839—Allergens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/16—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from plants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5156—Animal cells expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/53—DNA (RNA) vaccination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the dose, timing or administration schedule
Abstract
Description
本発明において、「少なくとも1つのアレルゲンに由来するポリペプチド」(「アレルゲン誘導体」)とは、アレルゲン又はその断片もしくは誘導体である少なくとも1つのポリペプチドを、DNAベクターのDNA領域がコードしていることを意味する。アレルゲン誘導体は、野生型アレルゲンの誘導体の中で、特にアレルギー誘発性が著しく低下した野生型アレルゲンの誘導体を含んでいる。アレルギー誘発性は、いくつかの手段によって低下させることができ、その手段の全てにおいて、分子内の二硫化ブリッジを分裂させることによってタンパク質の形態を不安定にし、それによって三次元構造を不安定化させることを目的としている。これらの誘導体はT細胞反応性を保持しながらもアレルギー誘発性を低下させることができ、野生型アレルゲンとの結合性においてIgEと競合するアレルゲン特異的IgGを特に誘発する免疫原を、高用量全身投与するのにより適している。したがって、低アレルギー性の誘導体は、療養及び予防目的に適している。
−1つ以上のアレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片を用意し、
−上記アレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片を、自家構造(造血細胞等)に提示するために、アレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片を、自家構造に直接取り付ける、又は自家構造に発現させることによって、アレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片を処理し、
−アレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片、を含む自家構造を個体へ移植し、そのアレルゲン/外来抗原、アレルゲン/外来抗原の誘導体、アレルゲン/外来抗原由来のエピトープ/断片に対する特異的な非応答性を誘引する。
a)膜アンカー型及び分泌型のPhl p 5及びGFPを運ぶ組換えレトロウイルスをコードする、レトロウイルスベクターの構築
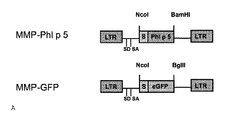
分泌型Phl p 5分子を有するレトロウイルスベクターを生成するために、オリジナルのPhl p 5シグナル配列を、ネズミ免疫グロブリン(pDisplay,インビトロジェン)のk短鎖のシグナル配列(S)に置き換え、重複PCR法(Ho et al. Gene 77:51-59, 1989)を用いて完全長Phl p 5及びeGFP(ベクター pEGFP−C1,クロンテック)に融合した(Vrtala et al. J Immunol 151(9):4773-4781,1993)(図1A)。膜アンカー型Phl p 5を生成するために、ヒト血小板由来成長因子(pDisplay,インビトロジェン)の膜貫通領域(TMD)を、シグナル配列及びPhl p 5又はeGFPにさらに融合した(図1B)。Phl p 5融合遺伝子の5’末端における制限部位NcoI及び3’末端における制限部位BamHIを、以下のプライマーによって挿入し、またeGFP融合遺伝子の5’末端における制限部位NcoI及び3’末端における制限部位BglII部位を、以下のプライマーによって挿入した(括弧内は配列番号を示す)。
リン酸カルシウム沈殿法(Pear et al., Proc. Natl. Acad. Sci. USA 90:8392-8396, 1993)により、293T細胞(John Iacomini、ボストンより提供)を、pMMP−Phl p 5 −TM(又はpMMP−eGFP−TM),pMD.G及びpMLVで、一過性トランスフェクトし、組換えレトロウイルスを生成した。MMPレトロウイルスベクターは、MFGの誘導体であり(Riviere et al. Proc Natl Acad Sci USA 92 (15):6733-6737,1995)、骨髄増殖性肉腫ウイルス(MPSV)末端反復配列プロモーター−エンハンサー因子を含んでいる。これらの転写因子は、造血細胞系統において発現を可能にすることが示されている(Bowtell et al. Mol Biol Med 4(4):229-50.,1987)。ベクターpMD.Gは、水疱性口内炎ウイルスG(VSV−G)外被タンパク質をコードし、VSV−G/レトロウイルス偽型を生成する(Ory et al.Proc Natl Acad Sci USA 93(21):11400-11406,1996)。トランスフェクトのために、10cmディッシュにおいて、10%ウシ胎児血清(FCS)を含むダルベッコ最少必須培地(DMEM)(GIBCO,インビトロジェン)で4.5×106の細胞を培養した。トランスフェクトの4時間前に、培地を、10%FCS及び25mM HEPES(MPバイオメディカルズ、エッシュウェーゲ、ドイツ)を含むイスコフ改変DMEM培地(GIBCO,インビトロジェン)に、入れ替えた。一つのディッシュを、それぞれpMMP−Phl p 5−TM(又はpMMP−eGFP−TM)(10μg)、pMD.G(5μg)及びpMLV(7.5μg)でトランスフェクトした。トランスフェクトから12〜16時間後、培地を、10%FCS及び10mM HEPESを含むDMEMに入れ替えた。トランスフェクトから72時間後にウイルス上清を回収し、超遠心分離機(製品名:Beckman ultracentrifuge)を用いてろ過及び濃縮した。ウイルス粒子の用量設定濃度を、NIH 3T3細胞の感染により測定し、フローサイトメトリーによって分析した。Epics XL−MCL フローサイトメトリー装置(製品名:Beckman Coulter、IL Alliance社、オーストリア)をデータ収集のために用い、Applied Cytometry Systems社製EXPO32 ADC Software(西シェフィールド、英国)を用いてフローサイトメトリーのデータを分析した。Phl p 5の表面発現を同定するために、完全長組換えPhl p 5に対するウサギポリクローナル抗血清(rPhl p 5)を、製造者の指示に従って、タンパク質Gカラム(Pierce)を用いて精製した。精製した抗体をビオチン化し、Phl p 5発現293T細胞で用量設定した。
a)実験計画
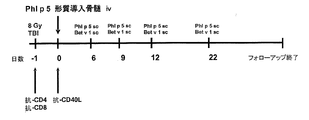
本実施例の目的は、遺伝的に組み換えた同質遺伝子的造血細胞の移植を通して、I型アレルギーの寛容誘引の方法を確立することである。BM単離の7日前に、ドナーのBalb/cマウスを、5−FUを用いて処置した(Bodine et al.Exp.Hematol 19:206-212,1991)。BMC(骨髄細胞)を以下に示すように単離して培養し、アレルゲン組み込みウイルス粒子で数回処理した。被提供者となるBalb/cマウスに、致死量の放射線を照射し(8 Gy)、抗CD4及び抗CD8モノクローナル抗体で処置した。骨髄移植(BMT)の直後、被提供者にMR1(抗CD40Lモノクローナル抗体)を与えた。マウスには、組換えPhl p 5及びBet v 1 を繰り返し注入し、免疫後BM移植を行った。一連の生体内及び生体外実験によって、免疫寛容を測定した。アレルゲン形質導入白血球(すなわち、分子キメラ化)の存在を確認する上で、マウスから何度か採血し、フローサイトメトリーでキメラ化を決定した(図4)。
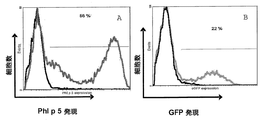
7日前に5−フルオロウラシル(5−FU;150mg/kg)で処理したマウスのBMCを採取し、単離したBMCを、製造者の指示にしたがって、RetroNectin(登録商標)(タカラバイオ株式会社、滋賀県、日本)でコートした細胞培養プレートで培養した。100ng/ml ヒトインターロイキン−6(製品名:IL−6;R&D Systems、米国)、100ng/ml 組換えマウス幹細胞因子(製品名:SCF;Biosource International社、米国)、50ng/ml 組換えマウストロンボポエチン(製品名:TPO;R&D Systems)、50ng/ml 組換えマウスFlt−3リガンド(R&D Systems)、及び0.1%ゲンタマイシン(MPバイオメディカルズ、ドイツ)の終濃度になるように15%FCS及びサイトカインを含む、DMEM(製品名:GIBCO、インビトロジェン)中でMNCを培養した。形質導入を、37℃で、5%CO2下において、96時間行った。BMCを1mlあたり4×106細胞の密度で培養し、感染多重度(MOI)1〜5でウイルス粒子に感染させた。24時間後、同じ数のウイルス粒子を用いて、細胞の形質導入を繰り返した。48時間後に、細胞をプレートから回収し、遠心分離機にかけ(Heraeus、1000rpm、RT、5分間)、BM培地、サイトカインカクテル中に再懸濁し、上記のようにウイルス粒子に感染させた。24時間後、細胞をプレートから回収し、小球型にして、M199培地(Sigma)、DNAse(Sigma)0.02U/ml、0.08%ゲンタマイシン(MPバイオメディカルズ社、エッシュウェーゲ、ドイツ)、及びHEPES(MPバイオメディカルズ社、ドイツ)10mMに再懸濁した。細胞を計数し、フローサイトメトリーによってPhl p 5又はGFPの表面発現を決定した(図3)。
形質導入の後、骨髄の機能を廃絶した(例えば、致死量の放射線が照射された)Balb/cマウスに、2〜4×106のBMCを静脈内に注入した。移植の1日前に、マウスの腹腔内に抗CD4抗体(GK1.5)及び抗CD8抗体(2.43)を0.5mg注入した。移植の直後、マウスに抗CD40L(MR1)(Bioexpress、西レバノン、NH、米国より抗体を購入)を0.5mg注入した。
形質導入したBMの被提供者細胞におけるのPhl p 5発現を、フローサイトメトリーを用いて調査した。実験された全ての白血球系統は、調査されている間(38週間)、常に高いレベルでPhl p 5を発現していた。キメラ化は約75%まで到達し、典型的な範囲は20〜40%であった(図4)。白血球を、CD4、CD8、B220、Mac−1に対するフルオレセインイソシアネート(FITC)結合抗体(Becton Dickinson、米国)及びフィコエリトリン−ストレプトアビジン(PEA、Becton Dickinson、米国)で発達させたビオチン化Phl p 5により染色した。Phl p 5を形質導入した宿主細胞を区別するために、二色フローサイトメトリーを用い(ヨウ化プロピジウム染色した死細胞を除く)、Tomitaらの文献に記載されている、Phl p 5ポジティブ細胞の比率として、キメラ化を算出した(Blood 83:939-948,1994)。
a)Phl p 5 分子キメラ化が、Phl p 5特異的抗体の発達を特異的に妨げる
BM移植マウスを2種類のアレルゲンに感作した6、9、12、及び22週間後、rPhl p 5及びrBet v 1(Biomay、オーストリア)の5μg/マウスを、Al(OH)3(Alu−Gel−S、Serva、ドイツ)に吸収させ、特異性をテストした。免疫化の1日前に、マウスから血液を採取し、血清を得た。血清を、分析されるまでの間、−20°Cで保管した。そして、抗原特異的IgG1及びIgE血清レベルを、ELISA(Vrtala et al., J Immunol 160 (12):6137-6144,1998)を用いて測定し(図5A及び図5B)、Phl p 5を形質導入したマウスが、Phl p 5に対して寛容であるか否かを分析した。組換えPhl p 5及びrBet v 1(5μg/ml)で、96ウェルプレート(Nunc、Maxisorp、デンマーク)をコートし、マウス血清をインキュベートした(IgG1用に1:500、IgE ELISA用に1:20)。IgG1結合又はIgE結合を、ラット抗マウスIgG1(1:1000)又はラット抗マウスIgE(1:1000)(Pharmingen、サンディエゴ、カルフォルニア)、及びHRP標識化したロバ抗ラット抗血清(1:2000)(アマシャム、バッキンガムシャー、英国)を用いて検出した。呈色反応を、ELISA−reader(Wlac、Perkin Elalmer、オーストリア)を用いて、405nmマイナス490nm波長において測定した。偽形質導入した(上述のように生成したウイルス上清と空のpMMPベクター)及び未処理の感作したBalb/cマウスの血清は、Phl p 5で形質導入したマウスと対照的に、高いPhl p 5特異的IgG1及びIgEレベルを示した。Phl p 5を形質導入したBMCを移植した全てのマウスにおいて、Phl p 5特異的IgG1及びIgEを検出可能レベルでは検出しなかったが、Bet v 1特異的IgG1及びIgEは高いレベルを示し、Phl p 5に対して特異的に寛容であることを示した。別の2つの実験においても、同様のデータが得られた。
ラット好塩基球白血病(RBL)実験を行い、因子レベルにおける寛容が得られたか否かを調査した。RBL−2H3細胞を96ウェル細胞培養プレート(4×104細胞/ウェル)に入れ、24時間、37℃及び5%CO2下で培養した。そして、細胞を、Phl p 5寛容マウス、偽形質導入したマウス、及び形質導入していない感作したBalb/cマウスのマウス血清(1:50希釈)で培養した。免疫前血清及び各アレルゲン注射後の血清を、RBL細胞で2時間、37°Cで培養した。上清を取り除き、細胞層を2×タイロード緩衝液(137mM NaCl、2.7mM KCl、0.5mMMgCl2、1.8mM CaCl2、0.4mM NaH2PO4、5.6mM D−グルコース、12mM NaHCO3、10mM HEPES、及び0.1%w/v BSA,pH 7.2)で洗浄した。予め荷重した細胞を、37°Cで30分間、rBet v 1のrPhl p 5(ウェル毎に0.03μg)を用いて刺激した。そして、ポジティブコントロールのために、細胞を、1%トリトン X−100を用いて溶解した。この上清を、クエン酸塩緩衝剤(0.1M、pH4.5)内で80μMの4−メチルウンベリフェリル−N−アセチル−β−D−グルコサミド(Sigma−Aldrich、オーストリア)と共に、37°Cで1時間インキュベートし、β−ヘキソサミニダーゼ活性を分析した。グリシン緩衝剤(0.2Mグリシン、0.2MNaCl、pH10.7)を100μl加えることで反応を停止し、蛍光性マイクロプレートリーダー(Wallac、Perkin Elmer、オーストリア)を用いて、λex:360/λem:465nmで蛍光性を測定した。分析結果を、蛍光性単位及び1%トリトン X−100で細胞を溶解した後に放出された合計β−ヘキソサミニダーゼの割合で求めた。
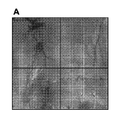
皮膚プリックテストを行い、皮膚I型過敏症反応の寛容を調べた。BM移植の30〜40週後、マウスの尾静脈に0.5% Evans blue(Sigma、米国)を100μl注射した。続いて、Phl p 5及びBet v 1(各0.5μg/ml、PBSで希釈)を30μl、毛の剃られた腹部皮膚の皮内に注射した。ポジティブコントロールとして、肥満細胞脱顆粒化合物48/80(20μg/ml、Sigma)を皮内に注射し、ポジティブコントロールとして、PBSを注射した。注射の20分後、マウスを処分し、転化した皮膚において、反応の青色強度を、個々のポジティブコントロールと比較した。図7において、上述したような、形質導入していない免疫化した、典型的なBalb/cマウスの転化腹部皮膚(A)は、Bet v 1及びPhl p 5の両方に対してポジティブ反応を示している。Phl p 5キメラマウスは、Bet v 1に対してはポジティブ反応を示すものの、Phl p 5に対してはポジティブ反応を示さなかった(B)。未処理のBalb/cマウスは、アレルゲンに対して全くポジティブ反応を示さなかった(C)。図7Dは、組換えアレルゲン及びコントロールの注射一覧表を示している。
B細胞寛容に加えてT細胞寛容をテストするべく、T細胞増殖実験を行った。マウスを処分したとき(BM移植後29又は40週目)に、年齢の一致した未処理Balb/cマウス(n=4)、Phl p 5を形質導入した(n=6)、及び形質導入していない(n=7)感作したマウスの脾臓を単離した。脾臓細胞を、1ウェルあたり2×105細胞の濃度で96丸底プレート(Nunc、デンマーク)に播種し、RPMI1640培地(Biochrome AG、ドイツ)において37°C及び5%CO2下で培養し、コンカナバリンA(Con A;0.5μg/ウェル、Sigma)、rPhl p 5(2μg/ウェル)、及びrBet v 1(2μg/ウェル)で刺激した。5日目の培地に、0.5μCi/ウェルのトリチウム化したチミジン(アマシャム)を用いて、16時間振動を与えて回収し、増殖反応をシンチレーションカウンターにより測定した。抗原(cpm)と培地コントロール値(cpm)との平均増殖の比率を求めた(刺激指数[SI])。形質導入していない、感作したBalb/cマウスと比較して、Phl p 5 キメラマウスではほとんど増殖が検出されなかった。Bet v 1で刺激したリンパ球の増殖は、形質導入していない、感作したマウスと比較して、Phl p 5キメラは同様であった(図8)。
a)膜アンカー型Bet v 1を運ぶ組換えレトロウイルスをコードするレトロウイルスベクターの構成
以下の実施例は、アレルゲンBet v 1を用いて行った。Bet v 1は主要なアレルゲンである、カンバの花粉である。Bet v 1は、病原性関連(PR)10タンパク質に属し、アレルゲンPhl p 5とは関連性を有さない。組換えレトロウイルスを生成するために、実施例1aに示すように、Bet v 1の全長cDNAを、シグナルペプチド及び膜貫通領域に融合した。そして、NcoI制限部位(3’末端)及びXhoI制限部位(5’末端)を、以下のプライマーを用いて挿入した(括弧内は配列番号を表す)。
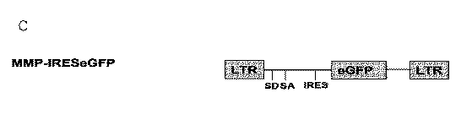
組換えレトロウイルスを、実施例1Bに記載のように生成した。293T細胞に、pMD.G、pMLV、及びコントロールとしての、プラスミドMMP−Bet v 1−TM−IRESeGFP又はMMP−IRESeGFPをコトランスフェクトし、VSV−Bet v 1−TM−GFP及びVSV−GFP(コントロールウイルス)を得た。ウイルス上清を濃縮し、NIH 3T3細胞を用いて用量設定した(実施例1Bに示すように)。Bet v 1をBet v 1に対するウサギポリクローナル抗血清(全長アレルゲン)を用いて検出し、血清をタンパク質Gカラムで精製し、抗体をビオチン化し、VSV−Bet v 1−TM−GFP感染NIH 3T3細胞によって用量設定した。Bet v 1及びGFP発現を、フローサイトメトリーで検出した。細胞表面におけるBet v 1発現を、ビオチン化Bet v 1抗体で検出し、ストレプトアビジン−PE−Cy5で対比染色した(図10B)。
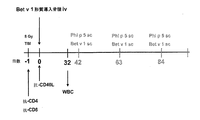
5−FU処置したBALB/cマウスの骨髄細胞を、実施例2Bに記載の方法にしたがって回収し、培養した。培養した骨髄細胞の形質導入を、VSV−Bet v 1−TM−GFP又はVSV−GFPを用いて、三度行った。Bet v 1−TMコンストラクトの発現を、フローサイトメトリーでレポーター遺伝子GFPを検出することによって測定し(図12A及びB)、細胞を計数して、2×106の形質導入した細胞を、致死量の放射線を照射した被提供者の尾静脈に注射した。実験計画は図11に示した。第−1日目に、マウスを抗CD4 mAb及び抗CD8 mAbで処理し、放射線照射した(8Gy)。第0日目には、骨髄を尾静脈に移植し、MR1を注射した。骨髄移植から6、9、15、及び22週間後に、形質導入した被提供者の骨髄を、rPhl p 5及びrBet v 1で感作した。観察期間を通して、Bet v 1のキメラ化を、フローサイトメトリーによって、白血球の異なる系統内において決定した。
被提供者におけるのキメラ化は、骨髄移植の32日後に検出された。1グループのBALB/cマウスを、VSV−Bet v 1−TM−GFPで形質導入したBMCで再構築し、コントロールグループのマウスを、VSV−GFPを形質導入したBMCで再構築した。フローサイトメトリーに基づく決定によれば、全てのマウスがキメラであった。B細胞及び骨髄系統のキメラ化を検出するために、白血球を、ビオチン化Mac1又はB220とともにインキュベートし、ストレプトアビジン−PE−Cy5で対比染色した。キメラ化を、レポーター遺伝子GFPの発現によって検出した。VSV−Bet v 1−TM−GFPを形質導入した被提供者の骨髄において、およそ2%〜5.5%のGFPポジティブ細胞が示された(図13)。VSV−GFPのが形質導入された被提供者においては、19%〜33.5%のキメラ化に到達した。
Claims (19)
- 少なくとも1つのアレルゲンに由来する少なくとも1つのポリペプチドをコードする核酸又はDNA分子を造血細胞に導入することによって、上記少なくとも1つのポリペプチドを細胞外に発現及び提示する造血細胞を生成する方法であって、
上記少なくとも1つのポリペプチドは、分泌シグナル配列、膜アンカー領域、及び/又は膜貫通領域に融合されている、方法。 - 上記造血細胞は、単球、マクロファージ、好中球、好塩基球、造血幹細胞、好酸球、T細胞、B細胞、NK細胞及び樹状細胞からなる群より選択されることを特徴とする請求項1に記載の方法。
- 上記少なくとも1つのポリペプチドをコードする上記DNA分子は、DNAベクターに含まれていることを特徴とする請求項1又は2に記載の方法。
- 上記DNAベクターは、ウイルスベクター、好ましくはレトロウイルスベクター、又はプラスミドベクターであることを特徴とする請求項3に記載の方法。
- 上記ベクターは、上記造血細胞に一過性に導入されていることを特徴とする請求項3又は4に記載の方法。
- 上記アレルゲンは、Phl p 1,Phl p 2,Phl p 5,Phl p 6,Der p 1,Der p 2,Der p 5,Der p 7,Der p 21,Fel d 1,Bet v 1,Ole e 1,Par j 2,Can f 1及びCan f 2からなる群より選択されることを特徴とする請求項1〜5のいずれかに記載の方法。
- 上記アレルゲンの誘導体が、低アレルギー性であることを特徴とする請求項1〜6のいずれかに1項に記載の方法。
- 上記DNA分子は、化学的方法、好ましくはカチオン性脂質及びカチオン性ポリマーを用いた方法、物理的方法、好ましくは粒子衝突、マイクロインジェクション若しくはエレクトロポレーションを用いた方法、細胞表面受容体若しくは多量のリン脂質とのウイルス外被の相互作用によるウイルス法によって、造血細胞に導入されることを特徴とする請求項1〜7のいずれか1項に記載の方法。
- アレルゲン由来のポリペプチドをコードする少なくとも1つの核酸分子を含み、
少なくとも1つの上記ポリペプチドは、分泌シグナル配列、膜アンカー領域、及び/又は膜貫通領域に融合されている、哺乳動物ウイルスベクターDNA。 - 上記アレルゲンは、Phl p 1,Phl p 2,Phl p 5,Phl p 6,Der p 1,Der p 2,Der p 5,Der p 7,Der p 21,Fel d 1,Bet v 1,Ole e 1,Par j 2,Can f 1及びCan f 2からなる群より選択されることを特徴とする請求項9に記載のベクター。
- 上記アレルゲンの誘導体は、低アレルギー性であることを特徴とする請求項9又は10に記載のベクター。
- モロニーマウス白血病レトロウイルスの末端反復配列(LTR)若しくは骨髄増殖性肉腫ウイルス(MPSV)の末端反復配列プロモーター−エンハンサーエレメント、プロモーター、好ましくはアルブミンプロモーター若しくはサイトメガロウイルス(CMV)プロモーター、複製起点、好ましくはEBV若しくはSV40の複製起点、又はヒト染色体S/MARを含んでいることを特徴とする請求項9〜11のいずれか1項に記載のベクター。
- 請求項1〜8のいずれか1項に記載の方法によって得られた、造血細胞。
- 上記少なくとも1つのポリペプチドが、膜アンカードメイン又は膜貫通ドメインに融合されていることを特徴とする請求項13に記載の細胞。
- 上記少なくとも1つのポリペプチドが、細胞膜の細胞外側に結合されていることを特徴とする請求項13又は14に記載の細胞。
- 請求項10〜14のいずれか1項に記載の哺乳類ウイルスベクターDNAを含んでいる、請求項13〜15のいずれか1項に記載の細胞。
- 上記造血細胞は、単球、マクロファージ、好中球、好塩基球、造血幹細胞、好酸球、T細胞、B細胞、NK細胞及び樹状細胞からなる群より選択されることを特徴とする請求項13〜16のいずれか1項に記載の細胞。
- アレルギーの治療又は予防のための医薬を製造するための、請求項9〜12のいずれか1項に記載のベクターDNAの使用、又は請求項13〜17のいずれか1項に記載の造血細胞の使用。
- 請求項9〜12のいずれか1項に記載のベクターDNA、又は請求項13〜17のいずれか1項に記載の造血細胞を含んでいる、薬剤組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US94241607P | 2007-06-06 | 2007-06-06 | |
| EP07450104A EP2000531A1 (en) | 2007-06-06 | 2007-06-06 | Antigen presenting cells |
| PCT/EP2008/056957 WO2008148831A2 (en) | 2007-06-06 | 2008-06-05 | Antigen presenting cells |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010528639A true JP2010528639A (ja) | 2010-08-26 |
Family
ID=38548713
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010510798A Pending JP2010528639A (ja) | 2007-06-06 | 2008-06-05 | 抗原提示細胞 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20100203640A1 (ja) |
| EP (2) | EP2000531A1 (ja) |
| JP (1) | JP2010528639A (ja) |
| AU (1) | AU2008258540A1 (ja) |
| CA (1) | CA2689317A1 (ja) |
| WO (1) | WO2008148831A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016530895A (ja) * | 2013-09-23 | 2016-10-06 | ウィルソン ウォルフ マニュファクチャリング コーポレイションWilson Wolf Manufacturing Corporation | 動物細胞を遺伝子改変する改良された方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL2438082T3 (pl) * | 2009-06-05 | 2014-11-28 | Phadia Ab | Alergeny wytwarzane drogą rekombinacji |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000066715A1 (de) * | 1999-05-04 | 2000-11-09 | Genethor Gmbh | Verfahren zur reduzierung von spezifischen immunreaktionen |
| JP2002507393A (ja) * | 1998-02-11 | 2002-03-12 | マキシジェン, インコーポレイテッド | 抗原ライブラリー免疫 |
| WO2004076481A2 (en) * | 2003-02-26 | 2004-09-10 | Glaxosmithkline Biologicals S.A. | Hypoallergenic der p 1 and der p 3 proteins from dermatographoides pteronyssinus |
| JP2006515984A (ja) * | 2002-09-27 | 2006-06-15 | バイオメイ プロダクションズ−アンド ハンデルス−アクティエンゲセルズシャフト | オオアワガエリ花粉アレルゲンPhlP7に基づく低アレルゲン性アレルギーワクチン |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1250430B1 (de) * | 2000-01-13 | 2005-05-11 | Angelika Reske-Kunz | Regulatorische sequenz zur spezifischen expression in dendritischen zellen und deren anwendungen |
-
2007
- 2007-06-06 EP EP07450104A patent/EP2000531A1/en not_active Withdrawn
-
2008
- 2008-06-05 US US12/663,239 patent/US20100203640A1/en not_active Abandoned
- 2008-06-05 WO PCT/EP2008/056957 patent/WO2008148831A2/en active Application Filing
- 2008-06-05 AU AU2008258540A patent/AU2008258540A1/en not_active Abandoned
- 2008-06-05 CA CA002689317A patent/CA2689317A1/en not_active Abandoned
- 2008-06-05 JP JP2010510798A patent/JP2010528639A/ja active Pending
- 2008-06-05 EP EP08760536A patent/EP2164950A2/en not_active Withdrawn
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002507393A (ja) * | 1998-02-11 | 2002-03-12 | マキシジェン, インコーポレイテッド | 抗原ライブラリー免疫 |
| WO2000066715A1 (de) * | 1999-05-04 | 2000-11-09 | Genethor Gmbh | Verfahren zur reduzierung von spezifischen immunreaktionen |
| JP2006515984A (ja) * | 2002-09-27 | 2006-06-15 | バイオメイ プロダクションズ−アンド ハンデルス−アクティエンゲセルズシャフト | オオアワガエリ花粉アレルゲンPhlP7に基づく低アレルゲン性アレルギーワクチン |
| WO2004076481A2 (en) * | 2003-02-26 | 2004-09-10 | Glaxosmithkline Biologicals S.A. | Hypoallergenic der p 1 and der p 3 proteins from dermatographoides pteronyssinus |
Non-Patent Citations (1)
| Title |
|---|
| JPN6012069060; Proc Natl Acad Sci USA(1995),Vol.92,No.15,p.6733-6737 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016530895A (ja) * | 2013-09-23 | 2016-10-06 | ウィルソン ウォルフ マニュファクチャリング コーポレイションWilson Wolf Manufacturing Corporation | 動物細胞を遺伝子改変する改良された方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008148831A3 (en) | 2009-03-05 |
| WO2008148831A2 (en) | 2008-12-11 |
| CA2689317A1 (en) | 2008-12-11 |
| EP2000531A1 (en) | 2008-12-10 |
| AU2008258540A1 (en) | 2008-12-11 |
| US20100203640A1 (en) | 2010-08-12 |
| EP2164950A2 (en) | 2010-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7399866B2 (ja) | CARTyrin組成物とその利用方法 | |
| AU2018393110B2 (en) | VCAR compositions and methods for use | |
| CA2590401C (en) | Adoptive immunotherapy with enhanced t lymphocyte survival | |
| JP2022087199A (ja) | 細胞の異なる亜型の活性を選択的にモジュレートするための方法 | |
| JP6422134B2 (ja) | キメラ抗原受容体 | |
| US8513208B2 (en) | Transient expression of immunomodulatory polypeptides for the prevention and treatment of autoimmune disease, allergy and transplant rejection | |
| CN110857319B (zh) | 一种分离的t细胞受体、其修饰的细胞、编码核酸及其应用 | |
| JP2008500812A (ja) | 免疫抑制サイトカイン | |
| US20120076808A1 (en) | Combined antigen and dna vaccine for preventing and treating autoimmune diseases | |
| US20150044244A1 (en) | Combined facilitator, antigen and dna vaccine for preventing and treating autoimmune diseases | |
| WO2020072390A1 (en) | Suicide module compositions and methods | |
| JP2015502135A (ja) | 多発性硬化症の治療のためのapc媒介寛容誘導 | |
| CN114127287A (zh) | 乙酰胆碱受体嵌合自身抗体受体细胞的组合物和方法 | |
| JP2018512154A (ja) | キメラタンパク質 | |
| Baranyi et al. | Persistent molecular microchimerism induces long‐term tolerance towards a clinically relevant respiratory allergen | |
| JP2010528639A (ja) | 抗原提示細胞 | |
| RU2769474C2 (ru) | Способы лечения рассеянного склероза с использованием аутологичных т-клеток | |
| US20230121433A1 (en) | Chimeric stimulatory receptors and methods of use in t cell activation and differentiation | |
| US20220273714A1 (en) | T-cell receptors and methods of use thereof | |
| JP2020508642A (ja) | 耐性を誘導するための操作された細胞 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110510 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130108 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130403 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130410 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130702 |