JP2010522154A - 結晶の製造方法 - Google Patents
結晶の製造方法 Download PDFInfo
- Publication number
- JP2010522154A JP2010522154A JP2009554087A JP2009554087A JP2010522154A JP 2010522154 A JP2010522154 A JP 2010522154A JP 2009554087 A JP2009554087 A JP 2009554087A JP 2009554087 A JP2009554087 A JP 2009554087A JP 2010522154 A JP2010522154 A JP 2010522154A
- Authority
- JP
- Japan
- Prior art keywords
- solvent
- flow rate
- active ingredient
- rate ratio
- ultrasonic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000013078 crystal Substances 0.000 title claims abstract description 22
- 238000004519 manufacturing process Methods 0.000 title description 2
- 238000000034 method Methods 0.000 claims abstract description 48
- 239000012296 anti-solvent Substances 0.000 claims abstract description 44
- 239000002904 solvent Substances 0.000 claims abstract description 42
- 239000004480 active ingredient Substances 0.000 claims abstract description 35
- 239000002245 particle Substances 0.000 claims abstract description 25
- 239000007788 liquid Substances 0.000 claims description 13
- 239000000203 mixture Substances 0.000 claims description 7
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical group CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 claims description 6
- 229960002052 salbutamol Drugs 0.000 claims description 6
- 239000002243 precursor Substances 0.000 claims description 4
- WMWTYOKRWGGJOA-CENSZEJFSA-N fluticasone propionate Chemical group C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O WMWTYOKRWGGJOA-CENSZEJFSA-N 0.000 claims description 3
- 229960000289 fluticasone propionate Drugs 0.000 claims description 3
- 238000002664 inhalation therapy Methods 0.000 claims description 2
- 239000012876 carrier material Substances 0.000 claims 1
- 210000004027 cell Anatomy 0.000 description 35
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 18
- -1 flunisonide Chemical compound 0.000 description 17
- 239000000523 sample Substances 0.000 description 16
- 238000002156 mixing Methods 0.000 description 11
- 239000003814 drug Substances 0.000 description 10
- 238000002604 ultrasonography Methods 0.000 description 10
- 229940079593 drug Drugs 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 238000010899 nucleation Methods 0.000 description 7
- 230000006911 nucleation Effects 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 6
- 239000002917 insecticide Substances 0.000 description 6
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 5
- 229960004436 budesonide Drugs 0.000 description 5
- XWTYSIMOBUGWOL-UHFFFAOYSA-N (+-)-Terbutaline Chemical compound CC(C)(C)NCC(O)C1=CC(O)=CC(O)=C1 XWTYSIMOBUGWOL-UHFFFAOYSA-N 0.000 description 4
- KWGRBVOPPLSCSI-WPRPVWTQSA-N (-)-ephedrine Chemical compound CN[C@@H](C)[C@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WPRPVWTQSA-N 0.000 description 4
- KUVIULQEHSCUHY-XYWKZLDCSA-N Beclometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)COC(=O)CC)(OC(=O)CC)[C@@]1(C)C[C@@H]2O KUVIULQEHSCUHY-XYWKZLDCSA-N 0.000 description 4
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 4
- 230000003750 conditioning effect Effects 0.000 description 4
- IMZMKUWMOSJXDT-UHFFFAOYSA-N cromoglycic acid Chemical compound O1C(C(O)=O)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=CC=CC2=C1C(=O)C=C(C(O)=O)O2 IMZMKUWMOSJXDT-UHFFFAOYSA-N 0.000 description 4
- 238000002425 crystallisation Methods 0.000 description 4
- 230000008025 crystallization Effects 0.000 description 4
- 239000012530 fluid Substances 0.000 description 4
- 229960002848 formoterol Drugs 0.000 description 4
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 4
- 239000000417 fungicide Substances 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 238000001471 micro-filtration Methods 0.000 description 4
- 108090000765 processed proteins & peptides Proteins 0.000 description 4
- 229960004017 salmeterol Drugs 0.000 description 4
- 238000001694 spray drying Methods 0.000 description 4
- 229960000195 terbutaline Drugs 0.000 description 4
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 4
- LSLYOANBFKQKPT-DIFFPNOSSA-N 5-[(1r)-1-hydroxy-2-[[(2r)-1-(4-hydroxyphenyl)propan-2-yl]amino]ethyl]benzene-1,3-diol Chemical compound C([C@@H](C)NC[C@H](O)C=1C=C(O)C=C(O)C=1)C1=CC=C(O)C=C1 LSLYOANBFKQKPT-DIFFPNOSSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102000004877 Insulin Human genes 0.000 description 3
- 108090001061 Insulin Proteins 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 229950000210 beclometasone dipropionate Drugs 0.000 description 3
- 229940124630 bronchodilator Drugs 0.000 description 3
- 239000000168 bronchodilator agent Substances 0.000 description 3
- 229940109248 cromoglycate Drugs 0.000 description 3
- 229960001022 fenoterol Drugs 0.000 description 3
- 230000000855 fungicidal effect Effects 0.000 description 3
- 239000004009 herbicide Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 229940125396 insulin Drugs 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000000361 pesticidal effect Effects 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 2
- 102000055006 Calcitonin Human genes 0.000 description 2
- 108060001064 Calcitonin Proteins 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 108010050904 Interferons Proteins 0.000 description 2
- HUYWAWARQUIQLE-UHFFFAOYSA-N Isoetharine Chemical compound CC(C)NC(CC)C(O)C1=CC=C(O)C(O)=C1 HUYWAWARQUIQLE-UHFFFAOYSA-N 0.000 description 2
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 description 2
- FZERHIULMFGESH-UHFFFAOYSA-N N-phenylacetamide Chemical compound CC(=O)NC1=CC=CC=C1 FZERHIULMFGESH-UHFFFAOYSA-N 0.000 description 2
- 239000005480 Olmesartan Substances 0.000 description 2
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- UCTWMZQNUQWSLP-UHFFFAOYSA-N adrenaline Chemical compound CNCC(O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-UHFFFAOYSA-N 0.000 description 2
- 239000003905 agrochemical Substances 0.000 description 2
- 239000000043 antiallergic agent Substances 0.000 description 2
- MXWJVTOOROXGIU-UHFFFAOYSA-N atrazine Chemical compound CCNC1=NC(Cl)=NC(NC(C)C)=N1 MXWJVTOOROXGIU-UHFFFAOYSA-N 0.000 description 2
- 239000003899 bactericide agent Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229960004015 calcitonin Drugs 0.000 description 2
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 239000000812 cholinergic antagonist Substances 0.000 description 2
- 239000003246 corticosteroid Substances 0.000 description 2
- 229960001334 corticosteroids Drugs 0.000 description 2
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- 229960002179 ephedrine Drugs 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- NYPJDWWKZLNGGM-UHFFFAOYSA-N fenvalerate Chemical compound C=1C=C(Cl)C=CC=1C(C(C)C)C(=O)OC(C#N)C(C=1)=CC=CC=1OC1=CC=CC=C1 NYPJDWWKZLNGGM-UHFFFAOYSA-N 0.000 description 2
- 229960002714 fluticasone Drugs 0.000 description 2
- MGNNYOODZCAHBA-GQKYHHCASA-N fluticasone Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(O)[C@@]2(C)C[C@@H]1O MGNNYOODZCAHBA-GQKYHHCASA-N 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 229940079322 interferon Drugs 0.000 description 2
- 229960001888 ipratropium Drugs 0.000 description 2
- OEXHQOGQTVQTAT-JRNQLAHRSA-N ipratropium Chemical compound O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 OEXHQOGQTVQTAT-JRNQLAHRSA-N 0.000 description 2
- 229960001268 isoetarine Drugs 0.000 description 2
- LMOINURANNBYCM-UHFFFAOYSA-N metaproterenol Chemical compound CC(C)NCC(O)C1=CC(O)=CC(O)=C1 LMOINURANNBYCM-UHFFFAOYSA-N 0.000 description 2
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 2
- 229960004398 nedocromil Drugs 0.000 description 2
- RQTOOFIXOKYGAN-UHFFFAOYSA-N nedocromil Chemical compound CCN1C(C(O)=O)=CC(=O)C2=C1C(CCC)=C1OC(C(O)=O)=CC(=O)C1=C2 RQTOOFIXOKYGAN-UHFFFAOYSA-N 0.000 description 2
- VTRAEEWXHOVJFV-UHFFFAOYSA-N olmesartan Chemical compound CCCC1=NC(C(C)(C)O)=C(C(O)=O)N1CC1=CC=C(C=2C(=CC=CC=2)C=2NN=NN=2)C=C1 VTRAEEWXHOVJFV-UHFFFAOYSA-N 0.000 description 2
- 229960005117 olmesartan Drugs 0.000 description 2
- 229960002657 orciprenaline Drugs 0.000 description 2
- 239000000575 pesticide Substances 0.000 description 2
- LCPDWSOZIOUXRV-UHFFFAOYSA-N phenoxyacetic acid Chemical compound OC(=O)COC1=CC=CC=C1 LCPDWSOZIOUXRV-UHFFFAOYSA-N 0.000 description 2
- SONNWYBIRXJNDC-VIFPVBQESA-N phenylephrine Chemical compound CNC[C@H](O)C1=CC=CC(O)=C1 SONNWYBIRXJNDC-VIFPVBQESA-N 0.000 description 2
- 229960001802 phenylephrine Drugs 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 229960002720 reproterol Drugs 0.000 description 2
- WVLAAKXASPCBGT-UHFFFAOYSA-N reproterol Chemical compound C1=2C(=O)N(C)C(=O)N(C)C=2N=CN1CCCNCC(O)C1=CC(O)=CC(O)=C1 WVLAAKXASPCBGT-UHFFFAOYSA-N 0.000 description 2
- 239000012047 saturated solution Substances 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 238000000527 sonication Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- XLNZEKHULJKQBA-UHFFFAOYSA-N terbufos Chemical compound CCOP(=S)(OCC)SCSC(C)(C)C XLNZEKHULJKQBA-UHFFFAOYSA-N 0.000 description 2
- 229960000278 theophylline Drugs 0.000 description 2
- 229960004295 valine Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- AKNNEGZIBPJZJG-MSOLQXFVSA-N (-)-noscapine Chemical compound CN1CCC2=CC=3OCOC=3C(OC)=C2[C@@H]1[C@@H]1C2=CC=C(OC)C(OC)=C2C(=O)O1 AKNNEGZIBPJZJG-MSOLQXFVSA-N 0.000 description 1
- LDVVMCZRFWMZSG-OLQVQODUSA-N (3ar,7as)-2-(trichloromethylsulfanyl)-3a,4,7,7a-tetrahydroisoindole-1,3-dione Chemical compound C1C=CC[C@H]2C(=O)N(SC(Cl)(Cl)Cl)C(=O)[C@H]21 LDVVMCZRFWMZSG-OLQVQODUSA-N 0.000 description 1
- WRRSFOZOETZUPG-FFHNEAJVSA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;hydrate Chemical compound O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC WRRSFOZOETZUPG-FFHNEAJVSA-N 0.000 description 1
- IAKOZHOLGAGEJT-UHFFFAOYSA-N 1,1,1-trichloro-2,2-bis(p-methoxyphenyl)-Ethane Chemical compound C1=CC(OC)=CC=C1C(C(Cl)(Cl)Cl)C1=CC=C(OC)C=C1 IAKOZHOLGAGEJT-UHFFFAOYSA-N 0.000 description 1
- NUBLQEKABJXICM-UHFFFAOYSA-N 1-(4-amino-3,5-dichlorophenyl)-2-[6-(2-pyridin-2-ylethoxy)hexylamino]ethanol Chemical compound C1=C(Cl)C(N)=C(Cl)C=C1C(O)CNCCCCCCOCCC1=CC=CC=N1 NUBLQEKABJXICM-UHFFFAOYSA-N 0.000 description 1
- PXMNMQRDXWABCY-UHFFFAOYSA-N 1-(4-chlorophenyl)-4,4-dimethyl-3-(1H-1,2,4-triazol-1-ylmethyl)pentan-3-ol Chemical compound C1=NC=NN1CC(O)(C(C)(C)C)CCC1=CC=C(Cl)C=C1 PXMNMQRDXWABCY-UHFFFAOYSA-N 0.000 description 1
- PDNHLCRMUIGNBV-UHFFFAOYSA-N 1-pyridin-2-ylethanamine Chemical compound CC(N)C1=CC=CC=N1 PDNHLCRMUIGNBV-UHFFFAOYSA-N 0.000 description 1
- FUFLCEKSBBHCMO-UHFFFAOYSA-N 11-dehydrocorticosterone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)C(=O)CO)C4C3CCC2=C1 FUFLCEKSBBHCMO-UHFFFAOYSA-N 0.000 description 1
- 239000005631 2,4-Dichlorophenoxyacetic acid Substances 0.000 description 1
- UFBJCMHMOXMLKC-UHFFFAOYSA-N 2,4-dinitrophenol Chemical compound OC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O UFBJCMHMOXMLKC-UHFFFAOYSA-N 0.000 description 1
- UFNOUKDBUJZYDE-UHFFFAOYSA-N 2-(4-chlorophenyl)-3-cyclopropyl-1-(1H-1,2,4-triazol-1-yl)butan-2-ol Chemical compound C1=NC=NN1CC(O)(C=1C=CC(Cl)=CC=1)C(C)C1CC1 UFNOUKDBUJZYDE-UHFFFAOYSA-N 0.000 description 1
- WVQBLGZPHOPPFO-UHFFFAOYSA-N 2-chloro-N-(2-ethyl-6-methylphenyl)-N-(1-methoxypropan-2-yl)acetamide Chemical compound CCC1=CC=CC(C)=C1N(C(C)COC)C(=O)CCl WVQBLGZPHOPPFO-UHFFFAOYSA-N 0.000 description 1
- ZRDUSMYWDRPZRM-UHFFFAOYSA-N 2-sec-butyl-4,6-dinitrophenyl 3-methylbut-2-enoate Chemical compound CCC(C)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1OC(=O)C=C(C)C ZRDUSMYWDRPZRM-UHFFFAOYSA-N 0.000 description 1
- XMTQQYYKAHVGBJ-UHFFFAOYSA-N 3-(3,4-DICHLOROPHENYL)-1,1-DIMETHYLUREA Chemical compound CN(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XMTQQYYKAHVGBJ-UHFFFAOYSA-N 0.000 description 1
- NKOHRVBBQISBSB-UHFFFAOYSA-N 5-[(4-hydroxyphenyl)methyl]-1,3-thiazolidine-2,4-dione Chemical compound C1=CC(O)=CC=C1CC1C(=O)NC(=O)S1 NKOHRVBBQISBSB-UHFFFAOYSA-N 0.000 description 1
- CTSLUCNDVMMDHG-UHFFFAOYSA-N 5-bromo-3-(butan-2-yl)-6-methylpyrimidine-2,4(1H,3H)-dione Chemical compound CCC(C)N1C(=O)NC(C)=C(Br)C1=O CTSLUCNDVMMDHG-UHFFFAOYSA-N 0.000 description 1
- XKJMBINCVNINCA-UHFFFAOYSA-N Alfalone Chemical compound CON(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XKJMBINCVNINCA-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 229930003347 Atropine Natural products 0.000 description 1
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 1
- HWSISDHAHRVNMT-UHFFFAOYSA-N Bismuth subnitrate Chemical compound O[NH+]([O-])O[Bi](O[N+]([O-])=O)O[N+]([O-])=O HWSISDHAHRVNMT-UHFFFAOYSA-N 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- QWOJMRHUQHTCJG-UHFFFAOYSA-N CC([CH2-])=O Chemical compound CC([CH2-])=O QWOJMRHUQHTCJG-UHFFFAOYSA-N 0.000 description 1
- 239000005745 Captan Substances 0.000 description 1
- TWFZGCMQGLPBSX-UHFFFAOYSA-N Carbendazim Natural products C1=CC=C2NC(NC(=O)OC)=NC2=C1 TWFZGCMQGLPBSX-UHFFFAOYSA-N 0.000 description 1
- 229930186147 Cephalosporin Natural products 0.000 description 1
- RAPBNVDSDCTNRC-UHFFFAOYSA-N Chlorobenzilate Chemical compound C=1C=C(Cl)C=CC=1C(O)(C(=O)OCC)C1=CC=C(Cl)C=C1 RAPBNVDSDCTNRC-UHFFFAOYSA-N 0.000 description 1
- JZUFKLXOESDKRF-UHFFFAOYSA-N Chlorothiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O JZUFKLXOESDKRF-UHFFFAOYSA-N 0.000 description 1
- 239000005944 Chlorpyrifos Substances 0.000 description 1
- MFYSYFVPBJMHGN-ZPOLXVRWSA-N Cortisone Chemical compound O=C1CC[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 MFYSYFVPBJMHGN-ZPOLXVRWSA-N 0.000 description 1
- MFYSYFVPBJMHGN-UHFFFAOYSA-N Cortisone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)(O)C(=O)CO)C4C3CCC2=C1 MFYSYFVPBJMHGN-UHFFFAOYSA-N 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- 239000005757 Cyproconazole Substances 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 108010000437 Deamino Arginine Vasopressin Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- IIUZTXTZRGLYTI-UHFFFAOYSA-N Dihydrogriseofulvin Natural products COC1CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 IIUZTXTZRGLYTI-UHFFFAOYSA-N 0.000 description 1
- IJVCSMSMFSCRME-KBQPJGBKSA-N Dihydromorphine Chemical compound O([C@H]1[C@H](CC[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O IJVCSMSMFSCRME-KBQPJGBKSA-N 0.000 description 1
- 239000005510 Diuron Substances 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- 102400000321 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- UXWOXTQWVMFRSE-UHFFFAOYSA-N Griseoviridin Natural products O=C1OC(C)CC=C(C(NCC=CC=CC(O)CC(O)C2)=O)SCC1NC(=O)C1=COC2=N1 UXWOXTQWVMFRSE-UHFFFAOYSA-N 0.000 description 1
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- RKUNBYITZUJHSG-UHFFFAOYSA-N Hyosciamin-hydrochlorid Natural products CN1C(C2)CCC1CC2OC(=O)C(CO)C1=CC=CC=C1 RKUNBYITZUJHSG-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 239000005867 Iprodione Substances 0.000 description 1
- ZCVMWBYGMWKGHF-UHFFFAOYSA-N Ketotifene Chemical compound C1CN(C)CCC1=C1C2=CC=CC=C2CC(=O)C2=C1C=CS2 ZCVMWBYGMWKGHF-UHFFFAOYSA-N 0.000 description 1
- 229930195714 L-glutamate Natural products 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108010000817 Leuprolide Proteins 0.000 description 1
- 239000005573 Linuron Substances 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 239000005802 Mancozeb Substances 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 239000005583 Metribuzin Substances 0.000 description 1
- 229940121948 Muscarinic receptor antagonist Drugs 0.000 description 1
- DDUHZTYCFQRHIY-UHFFFAOYSA-N Negwer: 6874 Natural products COC1=CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-UHFFFAOYSA-N 0.000 description 1
- 101710163270 Nuclease Proteins 0.000 description 1
- CHNUNORXWHYHNE-UHFFFAOYSA-N Oxadiazon Chemical compound C1=C(Cl)C(OC(C)C)=CC(N2C(OC(=N2)C(C)(C)C)=O)=C1Cl CHNUNORXWHYHNE-UHFFFAOYSA-N 0.000 description 1
- 239000005950 Oxamyl Substances 0.000 description 1
- 102000003982 Parathyroid hormone Human genes 0.000 description 1
- 108090000445 Parathyroid hormone Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 108010076181 Proinsulin Proteins 0.000 description 1
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 229940100389 Sulfonylurea Drugs 0.000 description 1
- 239000005839 Tebuconazole Substances 0.000 description 1
- NBQCNZYJJMBDKY-UHFFFAOYSA-N Terbacil Chemical compound CC=1NC(=O)N(C(C)(C)C)C(=O)C=1Cl NBQCNZYJJMBDKY-UHFFFAOYSA-N 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 239000005842 Thiophanate-methyl Substances 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- YEEZWCHGZNKEEK-UHFFFAOYSA-N Zafirlukast Chemical compound COC1=CC(C(=O)NS(=O)(=O)C=2C(=CC=CC=2)C)=CC=C1CC(C1=C2)=CN(C)C1=CC=C2NC(=O)OC1CCCC1 YEEZWCHGZNKEEK-UHFFFAOYSA-N 0.000 description 1
- 229960001413 acetanilide Drugs 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- NUFNQYOELLVIPL-UHFFFAOYSA-N acifluorfen Chemical compound C1=C([N+]([O-])=O)C(C(=O)O)=CC(OC=2C(=CC(=CC=2)C(F)(F)F)Cl)=C1 NUFNQYOELLVIPL-UHFFFAOYSA-N 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- XCSGPAVHZFQHGE-UHFFFAOYSA-N alachlor Chemical compound CCC1=CC=CC(CC)=C1N(COC)C(=O)CCl XCSGPAVHZFQHGE-UHFFFAOYSA-N 0.000 description 1
- QGLZXHRNAYXIBU-WEVVVXLNSA-N aldicarb Chemical compound CNC(=O)O\N=C\C(C)(C)SC QGLZXHRNAYXIBU-WEVVVXLNSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 1
- AKNNEGZIBPJZJG-UHFFFAOYSA-N alpha-noscapine Natural products CN1CCC2=CC=3OCOC=3C(OC)=C2C1C1C2=CC=C(OC)C(OC)=C2C(=O)O1 AKNNEGZIBPJZJG-UHFFFAOYSA-N 0.000 description 1
- XSDQTOBWRPYKKA-UHFFFAOYSA-N amiloride Chemical compound NC(=N)NC(=O)C1=NC(Cl)=C(N)N=C1N XSDQTOBWRPYKKA-UHFFFAOYSA-N 0.000 description 1
- 229960002576 amiloride Drugs 0.000 description 1
- 229960003556 aminophylline Drugs 0.000 description 1
- FQPFAHBPWDRTLU-UHFFFAOYSA-N aminophylline Chemical compound NCCN.O=C1N(C)C(=O)N(C)C2=C1NC=N2.O=C1N(C)C(=O)N(C)C2=C1NC=N2 FQPFAHBPWDRTLU-UHFFFAOYSA-N 0.000 description 1
- QXAITBQSYVNQDR-ZIOPAAQOSA-N amitraz Chemical compound C=1C=C(C)C=C(C)C=1/N=C/N(C)\C=N\C1=CC=C(C)C=C1C QXAITBQSYVNQDR-ZIOPAAQOSA-N 0.000 description 1
- 229960002587 amitraz Drugs 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 230000000954 anitussive effect Effects 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003092 anti-cytokine Effects 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000001679 anti-nematodal effect Effects 0.000 description 1
- 229940065524 anticholinergics inhalants for obstructive airway diseases Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229960005475 antiinfective agent Drugs 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000003434 antitussive agent Substances 0.000 description 1
- 229940124584 antitussives Drugs 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- RKUNBYITZUJHSG-SPUOUPEWSA-N atropine Chemical compound O([C@H]1C[C@H]2CC[C@@H](C1)N2C)C(=O)C(CO)C1=CC=CC=C1 RKUNBYITZUJHSG-SPUOUPEWSA-N 0.000 description 1
- 229960000396 atropine Drugs 0.000 description 1
- 229960003060 bambuterol Drugs 0.000 description 1
- ANZXOIAKUNOVQU-UHFFFAOYSA-N bambuterol Chemical compound CN(C)C(=O)OC1=CC(OC(=O)N(C)C)=CC(C(O)CNC(C)(C)C)=C1 ANZXOIAKUNOVQU-UHFFFAOYSA-N 0.000 description 1
- 229940092705 beclomethasone Drugs 0.000 description 1
- RIOXQFHNBCKOKP-UHFFFAOYSA-N benomyl Chemical compound C1=CC=C2N(C(=O)NCCCC)C(NC(=O)OC)=NC2=C1 RIOXQFHNBCKOKP-UHFFFAOYSA-N 0.000 description 1
- MITFXPHMIHQXPI-UHFFFAOYSA-N benzoxaprofen Natural products N=1C2=CC(C(C(O)=O)C)=CC=C2OC=1C1=CC=C(Cl)C=C1 MITFXPHMIHQXPI-UHFFFAOYSA-N 0.000 description 1
- 229960004217 benzyl alcohol Drugs 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- VEMKTZHHVJILDY-UXHICEINSA-N bioresmethrin Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)OCC1=COC(CC=2C=CC=CC=2)=C1 VEMKTZHHVJILDY-UXHICEINSA-N 0.000 description 1
- 229960001482 bismuth subnitrate Drugs 0.000 description 1
- JBRBWHCVRGURBA-UHFFFAOYSA-N broxaterol Chemical compound CC(C)(C)NCC(O)C1=CC(Br)=NO1 JBRBWHCVRGURBA-UHFFFAOYSA-N 0.000 description 1
- 229950008847 broxaterol Drugs 0.000 description 1
- VAIZTNZGPYBOGF-UHFFFAOYSA-N butyl 2-(4-{[5-(trifluoromethyl)pyridin-2-yl]oxy}phenoxy)propanoate Chemical group C1=CC(OC(C)C(=O)OCCCC)=CC=C1OC1=CC=C(C(F)(F)F)C=N1 VAIZTNZGPYBOGF-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 229960003563 calcium carbonate Drugs 0.000 description 1
- 229940117949 captan Drugs 0.000 description 1
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- DKVNPHBNOWQYFE-UHFFFAOYSA-N carbamodithioic acid Chemical compound NC(S)=S DKVNPHBNOWQYFE-UHFFFAOYSA-N 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 229960005286 carbaryl Drugs 0.000 description 1
- CVXBEEMKQHEXEN-UHFFFAOYSA-N carbaryl Chemical compound C1=CC=C2C(OC(=O)NC)=CC=CC2=C1 CVXBEEMKQHEXEN-UHFFFAOYSA-N 0.000 description 1
- 239000006013 carbendazim Substances 0.000 description 1
- JNPZQRQPIHJYNM-UHFFFAOYSA-N carbendazim Chemical compound C1=C[CH]C2=NC(NC(=O)OC)=NC2=C1 JNPZQRQPIHJYNM-UHFFFAOYSA-N 0.000 description 1
- DUEPRVBVGDRKAG-UHFFFAOYSA-N carbofuran Chemical compound CNC(=O)OC1=CC=CC2=C1OC(C)(C)C2 DUEPRVBVGDRKAG-UHFFFAOYSA-N 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 229940124587 cephalosporin Drugs 0.000 description 1
- 150000001780 cephalosporins Chemical class 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- QGTYWWGEWOBMAK-UHFFFAOYSA-N chlormephos Chemical compound CCOP(=S)(OCC)SCCl QGTYWWGEWOBMAK-UHFFFAOYSA-N 0.000 description 1
- SBPBAQFWLVIOKP-UHFFFAOYSA-N chlorpyrifos Chemical compound CCOP(=S)(OCC)OC1=NC(Cl)=C(Cl)C=C1Cl SBPBAQFWLVIOKP-UHFFFAOYSA-N 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 150000004777 chromones Chemical class 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 229960001117 clenbuterol Drugs 0.000 description 1
- STJMRWALKKWQGH-UHFFFAOYSA-N clenbuterol Chemical compound CC(C)(C)NCC(O)C1=CC(Cl)=C(N)C(Cl)=C1 STJMRWALKKWQGH-UHFFFAOYSA-N 0.000 description 1
- 229960004126 codeine Drugs 0.000 description 1
- OROGSEYTTFOCAN-DNJOTXNNSA-N codeine Natural products C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC OROGSEYTTFOCAN-DNJOTXNNSA-N 0.000 description 1
- 239000012809 cooling fluid Substances 0.000 description 1
- 239000000112 cooling gas Substances 0.000 description 1
- 229960004544 cortisone Drugs 0.000 description 1
- 229960000265 cromoglicic acid Drugs 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 102000003675 cytokine receptors Human genes 0.000 description 1
- 108010057085 cytokine receptors Proteins 0.000 description 1
- 229960004281 desmopressin Drugs 0.000 description 1
- NFLWUMRGJYTJIN-NXBWRCJVSA-N desmopressin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSCCC(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(N)=O)=O)CCC(=O)N)C1=CC=CC=C1 NFLWUMRGJYTJIN-NXBWRCJVSA-N 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- FSBVERYRVPGNGG-UHFFFAOYSA-N dimagnesium dioxido-bis[[oxido(oxo)silyl]oxy]silane hydrate Chemical compound O.[Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O FSBVERYRVPGNGG-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000012990 dithiocarbamate Substances 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- OFKDAAIKGIBASY-VFGNJEKYSA-N ergotamine Chemical compound C([C@H]1C(=O)N2CCC[C@H]2[C@]2(O)O[C@@](C(N21)=O)(C)NC(=O)[C@H]1CN([C@H]2C(C3=CC=CC4=NC=C([C]34)C2)=C1)C)C1=CC=CC=C1 OFKDAAIKGIBASY-VFGNJEKYSA-N 0.000 description 1
- 229960004943 ergotamine Drugs 0.000 description 1
- XCGSFFUVFURLIX-UHFFFAOYSA-N ergotaminine Natural products C1=C(C=2C=CC=C3NC=C(C=23)C2)C2N(C)CC1C(=O)NC(C(N12)=O)(C)OC1(O)C1CCCN1C(=O)C2CC1=CC=CC=C1 XCGSFFUVFURLIX-UHFFFAOYSA-N 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- PJMPHNIQZUBGLI-UHFFFAOYSA-N fentanyl Chemical compound C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 PJMPHNIQZUBGLI-UHFFFAOYSA-N 0.000 description 1
- 229960002428 fentanyl Drugs 0.000 description 1
- 229940125753 fibrate Drugs 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 229960000676 flunisolide Drugs 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- XDDAORKBJWWYJS-UHFFFAOYSA-N glyphosate Chemical class OC(=O)CNCP(O)(O)=O XDDAORKBJWWYJS-UHFFFAOYSA-N 0.000 description 1
- 229960002867 griseofulvin Drugs 0.000 description 1
- DDUHZTYCFQRHIY-RBHXEPJQSA-N griseofulvin Chemical compound COC1=CC(=O)C[C@@H](C)[C@@]11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-RBHXEPJQSA-N 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000000122 growth hormone Substances 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 230000002363 herbicidal effect Effects 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229960002003 hydrochlorothiazide Drugs 0.000 description 1
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- ONUFESLQCSAYKA-UHFFFAOYSA-N iprodione Chemical compound O=C1N(C(=O)NC(C)C)CC(=O)N1C1=CC(Cl)=CC(Cl)=C1 ONUFESLQCSAYKA-UHFFFAOYSA-N 0.000 description 1
- HOQADATXFBOEGG-UHFFFAOYSA-N isofenphos Chemical compound CCOP(=S)(NC(C)C)OC1=CC=CC=C1C(=O)OC(C)C HOQADATXFBOEGG-UHFFFAOYSA-N 0.000 description 1
- 229960004958 ketotifen Drugs 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001627 lamivudine Drugs 0.000 description 1
- JTEGQNOMFQHVDC-NKWVEPMBSA-N lamivudine Chemical compound O=C1N=C(N)C=CN1[C@H]1O[C@@H](CO)SC1 JTEGQNOMFQHVDC-NKWVEPMBSA-N 0.000 description 1
- 239000003199 leukotriene receptor blocking agent Substances 0.000 description 1
- 150000002617 leukotrienes Chemical class 0.000 description 1
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 1
- 229960004338 leuprorelin Drugs 0.000 description 1
- 229960003088 loratadine Drugs 0.000 description 1
- JCCNYMKQOSZNPW-UHFFFAOYSA-N loratadine Chemical compound C1CN(C(=O)OCC)CCC1=C1C2=NC=CC=C2CCC2=CC(Cl)=CC=C21 JCCNYMKQOSZNPW-UHFFFAOYSA-N 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- YKSNLCVSTHTHJA-UHFFFAOYSA-L maneb Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S YKSNLCVSTHTHJA-UHFFFAOYSA-L 0.000 description 1
- 229920000940 maneb Polymers 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- FOXFZRUHNHCZPX-UHFFFAOYSA-N metribuzin Chemical compound CSC1=NN=C(C(C)(C)C)C(=O)N1N FOXFZRUHNHCZPX-UHFFFAOYSA-N 0.000 description 1
- 238000003801 milling Methods 0.000 description 1
- 239000003750 molluscacide Substances 0.000 description 1
- 230000002013 molluscicidal effect Effects 0.000 description 1
- 229960002744 mometasone furoate Drugs 0.000 description 1
- WOFMFGQZHJDGCX-ZULDAHANSA-N mometasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(Cl)[C@@]4(C)C=CC(=O)C=C4CC[C@H]3[C@@H]2C[C@H]1C)C(=O)CCl)C(=O)C1=CC=CO1 WOFMFGQZHJDGCX-ZULDAHANSA-N 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 229960005181 morphine Drugs 0.000 description 1
- 230000004660 morphological change Effects 0.000 description 1
- DADSZOFTIIETSV-UHFFFAOYSA-N n,n-dichloroaniline Chemical compound ClN(Cl)C1=CC=CC=C1 DADSZOFTIIETSV-UHFFFAOYSA-N 0.000 description 1
- NQTXUKUXHJAGNR-UHFFFAOYSA-N n-diazenylethanimine Chemical compound CC=NN=N NQTXUKUXHJAGNR-UHFFFAOYSA-N 0.000 description 1
- LZGUHMNOBNWABZ-UHFFFAOYSA-N n-nitro-n-phenylnitramide Chemical compound [O-][N+](=O)N([N+]([O-])=O)C1=CC=CC=C1 LZGUHMNOBNWABZ-UHFFFAOYSA-N 0.000 description 1
- PLPRGLOFPNJOTN-UHFFFAOYSA-N narcotine Natural products COc1ccc2C(OC(=O)c2c1OC)C3Cc4c(CN3C)cc5OCOc5c4OC PLPRGLOFPNJOTN-UHFFFAOYSA-N 0.000 description 1
- 229960002259 nedocromil sodium Drugs 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- 150000002840 non-reducing disaccharides Chemical class 0.000 description 1
- 229960004708 noscapine Drugs 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- KZAUOCCYDRDERY-UHFFFAOYSA-N oxamyl Chemical compound CNC(=O)ON=C(SC)C(=O)N(C)C KZAUOCCYDRDERY-UHFFFAOYSA-N 0.000 description 1
- NVOYVOBDTVTBDX-PMEUIYRNSA-N oxitropium Chemical compound CC[N+]1(C)[C@H]2C[C@@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)[C@H](CO)C1=CC=CC=C1 NVOYVOBDTVTBDX-PMEUIYRNSA-N 0.000 description 1
- 229960000797 oxitropium Drugs 0.000 description 1
- 239000000199 parathyroid hormone Substances 0.000 description 1
- 229960001319 parathyroid hormone Drugs 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- XDRYMKDFEDOLFX-UHFFFAOYSA-N pentamidine Chemical compound C1=CC(C(=N)N)=CC=C1OCCCCCOC1=CC=C(C(N)=N)C=C1 XDRYMKDFEDOLFX-UHFFFAOYSA-N 0.000 description 1
- 229960004448 pentamidine Drugs 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 1
- 229960000395 phenylpropanolamine Drugs 0.000 description 1
- SIFMYPJMDXOSHN-UHFFFAOYSA-N phosphono 2-aminoacetate Chemical compound NCC(=O)OP(O)(O)=O SIFMYPJMDXOSHN-UHFFFAOYSA-N 0.000 description 1
- 239000005648 plant growth regulator Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- UAJUXJSXCLUTNU-UHFFFAOYSA-N pranlukast Chemical compound C=1C=C(OCCCCC=2C=CC=CC=2)C=CC=1C(=O)NC(C=1)=CC=C(C(C=2)=O)C=1OC=2C=1N=NNN=1 UAJUXJSXCLUTNU-UHFFFAOYSA-N 0.000 description 1
- 229960004583 pranlukast Drugs 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 229960002288 procaterol Drugs 0.000 description 1
- FKNXQNWAXFXVNW-BLLLJJGKSA-N procaterol Chemical compound N1C(=O)C=CC2=C1C(O)=CC=C2[C@@H](O)[C@@H](NC(C)C)CC FKNXQNWAXFXVNW-BLLLJJGKSA-N 0.000 description 1
- UMDTZVVSXXLZEE-UHFFFAOYSA-N prop-1-ynyl hydrogen sulfite Chemical compound CC#COS(O)=O UMDTZVVSXXLZEE-UHFFFAOYSA-N 0.000 description 1
- ZYHMJXZULPZUED-UHFFFAOYSA-N propargite Chemical compound C1=CC(C(C)(C)C)=CC=C1OC1C(OS(=O)OCC#C)CCCC1 ZYHMJXZULPZUED-UHFFFAOYSA-N 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- QNOWXBJDPNDAPH-UHFFFAOYSA-N pyridine;1h-pyrimidine-2,4-dione Chemical compound C1=CC=NC=C1.O=C1C=CNC(=O)N1 QNOWXBJDPNDAPH-UHFFFAOYSA-N 0.000 description 1
- MIXMJCQRHVAJIO-TZHJZOAOSA-N qk4dys664x Chemical compound O.C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]2(C)C[C@@H]1O.C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]2(C)C[C@@H]1O MIXMJCQRHVAJIO-TZHJZOAOSA-N 0.000 description 1
- 230000003134 recirculating effect Effects 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 239000003128 rodenticide Substances 0.000 description 1
- 229960004586 rosiglitazone Drugs 0.000 description 1
- 229940021597 salmeterol and fluticasone Drugs 0.000 description 1
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 1
- 229960002855 simvastatin Drugs 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- QAZLUNIWYYOJPC-UHFFFAOYSA-M sulfenamide Chemical compound [Cl-].COC1=C(C)C=[N+]2C3=NC4=CC=C(OC)C=C4N3SCC2=C1C QAZLUNIWYYOJPC-UHFFFAOYSA-M 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 229940065721 systemic for obstructive airway disease xanthines Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- QGHREAKMXXNCOA-UHFFFAOYSA-N thiophanate-methyl Chemical compound COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC QGHREAKMXXNCOA-UHFFFAOYSA-N 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- ZSDSQXJSNMTJDA-UHFFFAOYSA-N trifluralin Chemical compound CCCN(CCC)C1=C([N+]([O-])=O)C=C(C(F)(F)F)C=C1[N+]([O-])=O ZSDSQXJSNMTJDA-UHFFFAOYSA-N 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 238000004804 winding Methods 0.000 description 1
- 229950000339 xinafoate Drugs 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 229960004764 zafirlukast Drugs 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/08—Processes employing the direct application of electric or wave energy, or particle radiation; Apparatus therefor
- B01J19/10—Processes employing the direct application of electric or wave energy, or particle radiation; Apparatus therefor employing sonic or ultrasonic vibrations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/08—Bronchodilators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D9/00—Crystallisation
- B01D9/005—Selection of auxiliary, e.g. for control of crystallisation nuclei, of crystal growth, of adherence to walls; Arrangements for introduction thereof
- B01D9/0054—Use of anti-solvent
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D9/00—Crystallisation
- B01D9/0081—Use of vibrations, e.g. ultrasound
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D9/00—Crystallisation
- B01D9/02—Crystallisation from solutions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/18—Stationary reactors having moving elements inside
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2/00—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic
- B01J2/02—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic by dividing the liquid material into drops, e.g. by spraying, and solidifying the drops
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2/00—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic
- B01J2/18—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic using a vibrating apparatus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C227/00—Preparation of compounds containing amino and carboxyl groups bound to the same carbon skeleton
- C07C227/38—Separation; Purification; Stabilisation; Use of additives
- C07C227/40—Separation; Purification
- C07C227/42—Crystallisation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J31/00—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring
- C07J31/006—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring not covered by C07J31/003
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J75/00—Processes for the preparation of steroids in general
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00049—Controlling or regulating processes
- B01J2219/00051—Controlling the temperature
- B01J2219/00074—Controlling the temperature by indirect heating or cooling employing heat exchange fluids
- B01J2219/00105—Controlling the temperature by indirect heating or cooling employing heat exchange fluids part or all of the reactants being heated or cooled outside the reactor while recycling
- B01J2219/0011—Controlling the temperature by indirect heating or cooling employing heat exchange fluids part or all of the reactants being heated or cooled outside the reactor while recycling involving reactant liquids
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00049—Controlling or regulating processes
- B01J2219/00051—Controlling the temperature
- B01J2219/00074—Controlling the temperature by indirect heating or cooling employing heat exchange fluids
- B01J2219/00105—Controlling the temperature by indirect heating or cooling employing heat exchange fluids part or all of the reactants being heated or cooled outside the reactor while recycling
- B01J2219/00114—Controlling the temperature by indirect heating or cooling employing heat exchange fluids part or all of the reactants being heated or cooled outside the reactor while recycling involving reactant slurries
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Health & Medical Sciences (AREA)
- Crystallography & Structural Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Pulmonology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Toxicology (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Immunology (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Steroid Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
活性成分の結晶粒子を超音波照射の存在下で調製するための方法であって、第一の流れにおける少なくとも1種の溶質の溶媒溶液と第二の流れにおける反溶媒とを該反溶媒:溶媒の流速比を20:1より高く接触させてそれらを混合させる工程、及び生成した結晶を回収する工程を含む、方法。
【選択図】図1
【選択図】図1
Description
本発明は、小さな結晶を調製するための方法に関する。特に、本発明は、約10μm以下のサイズの小さな結晶を調製するための方法に関する。
結晶及び沈殿粒子サイズの制御は、いくつかの場合、特に関心のある活性成分の最終生成物形態が微細粉末の形態であるような医薬及び農薬産業で非常に重要である。活性成分が生物システムで挙動する場合は、特に粒子及び結晶形態のサイズなど多くの要因に依存する。小さな粒子はミリングなどの方法で製造されるが、そのような方法は材料特性に有害な効果を有し、所望の使用に不適当な有意な割合の粒子を製造することもあり、例えば小さ過ぎたり不適切な形状となったりする。そのような粒子は形態学的変化を受け、次々にアモルファス構造の形成を生じ得る望ましくない表面多形態学的変化となり得る。粒子は非常に帯電しており、流速を弱らせることもある。また、エアロゾルにおける使用のための粒子は非常に帯電している場合は諦めることもある。所望のサイズ範囲で結晶を溶液から直接結晶化させるのが望ましい。
長年、結晶化される活性成分を含有する溶媒を反溶媒と混合し、混合後に該溶液が過飽和して結晶化を起こすことによって結晶化を引き起こすことが知られている。混合は超音波照射や超音波照射が用いられない別の様式、例えば流体渦混合の存在下で行われ得る。"反溶媒"という用語は、関心のある活性成分(又は活性成分の前駆体)の溶媒からの沈殿を促進する流体を意味する。反溶媒は、冷却ガスや、化学反応で沈殿を促進するか又は溶媒における関心のある活性成分の溶解度を下げる流体を含み得る。それは異なる温度ではあるが溶媒と同じ液体であるか、又は溶媒と異なる液体であり得る。
長年、結晶化される活性成分を含有する溶媒を反溶媒と混合し、混合後に該溶液が過飽和して結晶化を起こすことによって結晶化を引き起こすことが知られている。混合は超音波照射や超音波照射が用いられない別の様式、例えば流体渦混合の存在下で行われ得る。"反溶媒"という用語は、関心のある活性成分(又は活性成分の前駆体)の溶媒からの沈殿を促進する流体を意味する。反溶媒は、冷却ガスや、化学反応で沈殿を促進するか又は溶媒における関心のある活性成分の溶解度を下げる流体を含み得る。それは異なる温度ではあるが溶媒と同じ液体であるか、又は溶媒と異なる液体であり得る。
欧州特許第1144065号明細書は、結晶化される活性成分を含む反溶媒と溶媒の混合を、10:1以下の反溶媒:溶媒の流速比を用いることによって超音波照射の存在下の連続的なフローセルで達成されるシステムを記載している。温かい溶媒を冷たい混和性の反溶媒と混合することを記載しているが、該冷たい反溶媒の正確な温度は開示されていない。
欧州特許第1469938号明細書は、結晶化される活性成分を含む反溶媒と溶媒の混合の流速が、10:1以下、典型的に2:1〜5:1の流速比で溶媒の流速を超えるシステムを記載している。混合は超音波照射の存在下で行われる。
先行技術の方法は、一般的に20:1未満(すなわち、10:1から低くても1:1の流速比)である反溶媒:溶媒の流速比で結晶の製造を可能にする。
欧州特許第1469938号明細書は、結晶化される活性成分を含む反溶媒と溶媒の混合の流速が、10:1以下、典型的に2:1〜5:1の流速比で溶媒の流速を超えるシステムを記載している。混合は超音波照射の存在下で行われる。
先行技術の方法は、一般的に20:1未満(すなわち、10:1から低くても1:1の流速比)である反溶媒:溶媒の流速比で結晶の製造を可能にする。
本発明では、超音波照射の存在下で物質の結晶質粒子を調製するための方法であって、第一の流れにおける溶媒中の少なくとも1種の溶質を第二の流れにおける反溶媒とを反溶媒:溶媒の流速比が20:1より高く接触させる工程、及び生成した結晶を回収する工程を含む方法が提供される。
反溶媒の流れは典型的に再循環され、例えば、連続的に再循環する流れ、すなわち、ここに記載される第二の流れとなる。典型的には、本発明の方法は、第二の流れは溶媒において加えられた溶質も含み得る連続的に循環する反溶媒の流れであり、該第二の流れ(すなわち反溶媒):溶媒の流速比が20:1より高い。
本発明に方法において反溶媒と溶媒の流速比を操作することにより、本発明はサイズが約10μm以下である所望のサイズの関心ある活性成分の結晶を提供する。本発明の方法によって達成される粒子の平均直径サイズは、500nm〜10μm、好ましくは約600nm〜約5μm及び最も好ましくは650nm〜約2μm、例えば700nm〜Lμmの範囲にある。
反溶媒の流れは典型的に再循環され、例えば、連続的に再循環する流れ、すなわち、ここに記載される第二の流れとなる。典型的には、本発明の方法は、第二の流れは溶媒において加えられた溶質も含み得る連続的に循環する反溶媒の流れであり、該第二の流れ(すなわち反溶媒):溶媒の流速比が20:1より高い。
本発明に方法において反溶媒と溶媒の流速比を操作することにより、本発明はサイズが約10μm以下である所望のサイズの関心ある活性成分の結晶を提供する。本発明の方法によって達成される粒子の平均直径サイズは、500nm〜10μm、好ましくは約600nm〜約5μm及び最も好ましくは650nm〜約2μm、例えば700nm〜Lμmの範囲にある。
溶質は活性成分又はその所望の前駆体にすることができ、例えば本発明の方法で結晶を形成することのできる関心のある薬剤又は農薬である。第一の流れに含まれる1種以上の溶質があり、例えば関心のある2種以上の溶質の混合物、例えば関心のある2種以上活性成分、例えば2種以上の薬剤又は2種以上の農薬が、前記溶質の意図される最終使用に依存して存在し得る。本発明の方法条件下で結晶化することのできる好適な溶質は、本発明の方法で結晶質粒子に形成され得る活性成分又は薬剤を含み、例えばコルチコステロイド、b2-作用剤、抗コリン剤、ロイコトリエン拮抗剤、吸入可能蛋白質又はペプチド、モメタゾンフロ酸エステル;ベクロメタゾンジプロピオネート;ブデソニド;フルチカゾン;デキサメタゾン;フルニソリド;トライアムシナロン;サルブタモール;アルブテロール;テルブタリン;サルメテロール;ビトルテロール;イプラトロピウムブロマイド;オキシトロピウムブロマイド;クロモグリク酸ナトリウム;ネドクロミルナトリウム;ザフィルルカスト;プランルカスト;ホルモテロール;エホルモテロール;バンブテロール;フェノテロール;クレンブテロール;プロカテロール;ブロキサテロール;(22R)-6a、9a-ジフルオロ-LLb、21-ジヒドロキシ-16a、17a-プロピルメチレンジオキシ-4-プレグネン-3、20-ジオン;TA-2005;チプレダン;インスリン;インターフェロン;カルシトニン;パラ甲状腺ホルモン;及び顆粒球コロニー刺激因子である。
本発明で製造され得る他の粒子は吸入によって有効に送達される任意の薬剤又は活性成分を含み、例えば、鎮痛剤、例えば、コデイン、ジヒドロモルヒネ、エルゴタミン、フェンタニル又はモルヒネ;狭心症製剤、例えば、ジルチアゼム;抗アレルギー剤、例えば、クロモグリケート、ケトチフェン又はネドクロミル;抗感染症剤、例えば、セファロスポリン、ペニシリン、ストレプトマイシン、スルホンアミド、テトラサイクリン又はペンタミジン;抗ヒスタミン剤、例えば、メタピリレン;抗炎症剤、例えばベクロメタゾン、フルニソニド、ブデソニド、チプレダン、トライアムシナロンアセトニド又はフルチカゾン鎮咳剤、例えば、ノスカピン;気管支拡張剤、例えば、エフェドリン、アドレナリン、フェノテロール、ホルモテロール、イソプレナリン、メタプロテレノール、フェニレフリン、フェニルプロパノールアミン、ピルブテロール、レプロテロール、リミテロール、サルブタモール、サルメテロール、テルブタリン;イソエタリン、トルブテロール、オルシプレナリン又は(-)-4-アミノ-3,5-ジクロロ-a[[[6-[2-(2-イリジニル)エトキシ]ヘキシル]アミノ]メチル]ベンゼンメタノール;利尿剤、例えば、アミロライド;抗コリン性剤、例えば、イプラトロピウム、アトロピン又はオキシトロピウム;ホルモン、例えば、コルチゾン、ヒドロコルチゾン又はプレドニゾロン;キサンチン、例えば、25アミノフィリン、コリンテオフィリネート、リシンテオフィリネート又はテオフィリン;及び、治療用蛋白質及びペプチド、例えば、インスリン又はグルカゴンである。当業者は、適切な場合には活性成分又は薬剤を含む医薬品を、塩(例えば、アルカリ金属又はアミン塩又は酸添加塩として)、エステル(例えば、低級アルキルエステル)、又は溶媒和物(例えば、水和物)の形態で用いられ、該医薬品の活性及び/又は安定性を最適化してよいことを理解する。
本発明の方法で得られた粒子による調製のために特に好適な薬剤は、吸入治療による喘息など呼吸器系障害の治療において使用する抗アレルギー性剤、気管支拡張剤及び抗炎症性ステロイドを含み、例えばクロモグリケート(例えば、ナトリウム塩として)、サルブタモール(例えば、遊離塩基又は硫酸塩の塩として)、サルメテロール(例えば、キシナホ酸塩)、テルブタリン(例えば、硫酸塩として)、レプロテロール(例えば、塩酸塩として)、二プロピオン酸ベクロメタゾン(例えば、一水和物として)、プロピオン酸フルチカゾン又は(-)-4-アミノ-3,5-ジクロロ-α-[[[6-[2-(2-ピリジニル)エトキシ]ヘキシル]アミノ]-メチル]ベンゼンメタノール及びその生理学的に許容される塩及び溶媒和物である。
当業者は、本発明の方法で製造される粒子が2種以上の活性成分の組み合わせを含有し得ることを理解する。活性成分は上記活性成分の好適な組み合わせから選択され得る。従って、気管支拡張剤の好適な組み合わせは、エフェドリン及びテオフィリン、フェノテロール及びイプラトロピウム、及びイソエタリン及びフェニレフリンを含む。
本発明の方法で製造される活性成分の粒子のさらなる好適な組み合わせは、コルチコステロイド、例えばブデソニド、二プロピオン酸ベクロメタゾン及びプロピオン酸フルチカゾンと、b2-作用剤、例えばサルブタモール、テルブタリン、サルメテロール及びフルチカゾン、サルメテロール及びホルモテロール及びその生理学的に許容される誘導体、特に硫酸塩を含む塩を含む。
本発明の方法で製造される活性成分の粒子のさらなる好適な組み合わせは、コルチコステロイド、例えばブデソニド、二プロピオン酸ベクロメタゾン及びプロピオン酸フルチカゾンと、b2-作用剤、例えばサルブタモール、テルブタリン、サルメテロール及びフルチカゾン、サルメテロール及びホルモテロール及びその生理学的に許容される誘導体、特に硫酸塩を含む塩を含む。
本発明の方法で得られる粒子の他の例は、クロモグリク酸ナトリウム又はネドクロミルでよいクロモンを含むか、又は炭水化物、例えばヘパリンを含み得る。本発明の方法で製造される粒子は吸入に好適な活性成分を含むか、全身性の使用のための薬理学的に活性な薬剤でよい。例えば、そのような活性粒子は、ペプチド又はポリペプチド又は蛋白質、例えばDase、ロイコトリエン又はインスリン(プロ-インスリンを含む)、シクロスポリン、インターロイキン、サイトカイン、抗サイトカイン及びサイトカイン受容体、ワクチン、成長ホルモン、ロイプロリド及び関連する類似物、インターフェロン、デスモプレシン、免疫グロブリン、エリスロポエチン及びカルシトニンを含み得る。
あるいは、本発明の方法で製造される活性成分は経口投与に好適となり得る。経口投与用の薬剤は上記全身性薬剤の1種でよい。活性成分は、消化管で低い溶解度を示す物質、例えば、トリケイ酸マグネシウム、炭酸カルシウム及び次硝酸ビスマスでよい。有機化合物は、例えば、コンビナトリアルケミストリーの全ての生成物、ロシグリタゾン及び他の関連するグリタゾン薬剤、ヒドロクロロチアジド、グリセオフルビン、ラミブジン及び他のヌクレアーゼ逆転者酵素阻害剤、シンバスタチン及び他のスタチン薬剤、ベンザフィブレート及び他のフィブレート薬剤及びロラチジン、及びその任意の他の生理学的に容認される塩及び誘導体を含み得る。
あるいは、本発明の方法で製造される活性成分は経口投与に好適となり得る。経口投与用の薬剤は上記全身性薬剤の1種でよい。活性成分は、消化管で低い溶解度を示す物質、例えば、トリケイ酸マグネシウム、炭酸カルシウム及び次硝酸ビスマスでよい。有機化合物は、例えば、コンビナトリアルケミストリーの全ての生成物、ロシグリタゾン及び他の関連するグリタゾン薬剤、ヒドロクロロチアジド、グリセオフルビン、ラミブジン及び他のヌクレアーゼ逆転者酵素阻害剤、シンバスタチン及び他のスタチン薬剤、ベンザフィブレート及び他のフィブレート薬剤及びロラチジン、及びその任意の他の生理学的に容認される塩及び誘導体を含み得る。
本発明の方法で製造された粒子に加えるのに好適な医薬賦形剤は、例えば炭水化物、特に単糖類、例えばフルクトース、グルコース及びガラクトース;非還元性二糖類、例えばスクロース、ラクトース及びトレハロース;非還元性オリゴ糖類、例えばラフィノース及びメレジトース;ポリサッカライド生成物由来の非還元性スターチ、例えばマルトデキストリン、デキストラン及びシクロデキストリン;及び非還元性アルジトール、例えばマンニトール及びキシリトールを含む。
本発明の方法で調製される活性成分の粒子が農薬活性の場合、活性成分は、例えば、植物成長調整剤、除草剤、及び/又は殺菌剤、例えば殺虫剤、防カビ剤、ダニ駆除剤、抗線虫剤、ダニ殺虫剤、殺鼠剤、殺バクテリア剤、軟体動物駆除剤又は鳥駆除剤でよい。
本発明の方法で調製される活性成分の粒子が農薬活性の場合、活性成分は、例えば、植物成長調整剤、除草剤、及び/又は殺菌剤、例えば殺虫剤、防カビ剤、ダニ駆除剤、抗線虫剤、ダニ殺虫剤、殺鼠剤、殺バクテリア剤、軟体動物駆除剤又は鳥駆除剤でよい。
本発明の方法で製造される有機不水溶性農薬活性成分の例は、例えばカルバメートからなる群から選択される殺虫剤、例えばメトミル、カルバリール、カルボフラン、又はアルジカルブ;有機チオリン酸塩、例えばEPN、イソフェンホス、イソキサチオン、クロルピリホス、又はクロルメホス;有機リン酸塩、例えばテルブホス、モノクロトホス、又はテラクロルビンホス;過塩素化有機物、例えばメトキシクロール;合成ピレスロイド、例えばフェンバレレート;線虫駆除剤カルバメート、例えばトリアジンからなる群から選択されるオキサミル除草剤、例えばメトリブジン、ヘキサキシノン、又はアトラジン;スルホニル尿素、例えば2-クロロ-N-[(4-メトキシ-6-メチル-L,3,5-トリアジン-2-イル)アミノカルボニル]-ベンゼンスルホンアミド;ウラシル(ピリミジン)、例えばレナシル、ブロマシル、又はテルバシル;尿素、例えばリヌロン、ジウロン、シデュロン、又はネブロン;アセトアニリド、例えばアラクロール、又はメトラクロール;チオカルバメート、例えばベンチオカルブ(SATURN)、トリアレート;オキサジアゾール-オン、例えばオキサジアゾン;フェノキシ酢酸、例えば2,4-D;ジフェニルエーテル、例えばフルアジホップ-ブチル、アシフルオルフェン、ビフェノックス、又はオキシフルオルフェン;ジニトロアニリン、例えばトリフルラリン;グリシンホスホネート、例えばグリホサート塩及びエステル;ジハロベンゾニトリル、例えばブロモキシニル、又はアイオキシニル;例えばニトリルオキシムからなる群から選択される殺菌剤、例えばシモキサニル(カーゼート);イミダゾール、例えばベノミル、カルベンダジム、又はチオファネート-メチル;トリアゾール、例えばトリアジメホン;スルフェンアミド、例えばカプタン;ジチオカルバメート、例えばマネブ、マンコゼブ、又はチラム;塩素化芳香族、例えばクロロネブ;ジクロロアニリン、例えばイプロジオン;例えばカルバメートからなる群から選択される殺虫剤、例えばピリミカルブ;例えば亜硫酸プロピニルからなる群から選択されるダニ殺虫剤、例えばプロパルギット;トリアザペンタジエン、例えばアミトラズ;塩素化芳香族、例えばクロロベンジレート、又はテトラジファン;及びジニトロフェノール、例えばビナパクリルを含む。
有機不水溶性農薬活性成分は、本発明で製造される粒子に数種の成分の混合物として含まれ得る。特に好ましい有機不水溶性農薬活性成分は、アトラジン、シモキサニル、クロロタラニル、シプロコナゾール、及びテブコナゾールである。
溶質を含む溶媒(すなわち、'溶液')の流れ及び反溶媒の流れは接触又は混合され、該2種の流れが単路又は軸に沿って同方向に、例えば、好適な送達手段の内腔内で、好適な容器又はチャンバー、例えば超音波連続的フローセル内に流れる。前記各流れは、予め決定されている流速で最初の供給源貯蔵器から送達手段にポンプされ得る。好適な送達手段は、直線又は曲線の導管などの管状手段、例えばパイプを含み、該2種の流れは同軸でそこで混合され得る。あるいは、該2種の流れは容器又はチャンバー、例えば超音波連続的フローセル内にポンピングによって分離送達手段、例えば2つの分離管状手段、例えば2つのパイプを介して導入され得る。
溶質を含む溶媒(すなわち、'溶液')の流れ及び反溶媒の流れは接触又は混合され、該2種の流れが単路又は軸に沿って同方向に、例えば、好適な送達手段の内腔内で、好適な容器又はチャンバー、例えば超音波連続的フローセル内に流れる。前記各流れは、予め決定されている流速で最初の供給源貯蔵器から送達手段にポンプされ得る。好適な送達手段は、直線又は曲線の導管などの管状手段、例えばパイプを含み、該2種の流れは同軸でそこで混合され得る。あるいは、該2種の流れは容器又はチャンバー、例えば超音波連続的フローセル内にポンピングによって分離送達手段、例えば2つの分離管状手段、例えば2つのパイプを介して導入され得る。
本発明の反溶媒:溶媒の流速比(以下では“流速比”)は20:1より高く、本発明の方法で得られた結晶のデザイン及び最終目的に依存していかなる流速比でもよい。本発明の方法で用いられる流速比は、関心のある物質、所定の目的に必要な結晶の所望のサイズ、及びどのようにして結晶が対象に、例えば哺乳類(例えば、ヒト;ウマ;ウシ;又はヒツジ)に好適な薬剤の形態で、又は植物に好適な農薬、例えば殺虫剤、除草剤、殺菌剤、殺細菌剤、又は殺ウイルス剤の形態で投与されるかを考慮して決定され得る。本発明の方法における使用に好適な流速比は、第二の流れ:第一の流れの任意の流速比、1000:1以下、例えば、900:1、800:1、700:1、600:1、500:1、400:1、300:1、200:1、100:1、50:1、40:1又は30:1、又はそれらの間の任意の流速比、例えば380:1、330:1、333:1、165:1、80:1などでよい。流速比は、所定の最終目的に必要な結晶のサイズ及び対象有機体に用いられる提案された送達媒体に支配される。
典型的には、結晶質粒子を本発明の方法で製造するのに好適な装置を通る反溶媒流の流速が、時間当たりのリットル(1/時間)[例えば、20L/時間]、あるいは時間当たりのミリリットル(mL/時間)の範囲であり、反溶媒の流速が溶媒システム(すなわち、溶媒中の溶質)よりも少なくとも20:1の値だけ高く、ここで定義されているより高い限りは当該最終目的に好適な任意の流速でよい。例えば、ベンチトップ装置では、本発明の第一の流れの流速は20L/時間でよく、第二の流れは60mL/時間でよい。該方法がより大きな装置、例えば、100リットル(100L)の容器で用いられる場合、第一の流れの処理流速は2400L/時間であり、第二の流れは120L/時間でよい。
当然に、当業者は前記各流れの流速は所望の任意の流速にできることを理解するが、該2種の流れの流速比は本発明に記載のものである。
当然に、当業者は前記各流れの流速は所望の任意の流速にできることを理解するが、該2種の流れの流速比は本発明に記載のものである。
小さなスケールの装置、例えば1リットル容量、5リットル容量又は10リットル容量を有するものにおける反溶媒の流速は、50L/時間以下、典型的には40L/時間、30L/時間、20L/時間、10L/時間又は5L/時間以下、又はその間の任意の値、例えば4L/時間、8L/時間、15L/時間などでよい。流速は、特定の最終目的のために関心のある部位に対して選択された管理ルートに必要な粒子のサイズに依存して当業者に決定され得る。従って、溶媒における溶質の加えられた溶液の流速は、接触して配置される反溶媒の少なくとも20倍である。本発明に用いられる流速比(333:1)の例は実施例で見出され、反溶媒は20L/時間で、溶媒中の溶質は60mL/時間で流れる。
反溶媒及び溶媒は、特定の活性成分又はその活性前駆体に好適となるように選択すべきであると理解される。反溶媒及び溶媒の対は互いに混和性でよい。混和性の対の例は、水及び2-プロパノール;及びエタノール及び水を含む。あるいは、反溶媒及び溶媒の対は、異なる温度ではあるが同一の液体でよい。典型的には、該液体の温度は-10℃〜+120℃にあるが、実質的な温度差は2℃内である。該温度は50℃以上の異なる温度で分離され、例えば、溶媒は温水(例えば、80℃)であり、反溶媒は冷水(例えば、10℃)である。適切な溶媒及び反溶媒の選択は、結晶化される物質に従わなければならない。
反溶媒及び溶媒は、特定の活性成分又はその活性前駆体に好適となるように選択すべきであると理解される。反溶媒及び溶媒の対は互いに混和性でよい。混和性の対の例は、水及び2-プロパノール;及びエタノール及び水を含む。あるいは、反溶媒及び溶媒の対は、異なる温度ではあるが同一の液体でよい。典型的には、該液体の温度は-10℃〜+120℃にあるが、実質的な温度差は2℃内である。該温度は50℃以上の異なる温度で分離され、例えば、溶媒は温水(例えば、80℃)であり、反溶媒は冷水(例えば、10℃)である。適切な溶媒及び反溶媒の選択は、結晶化される物質に従わなければならない。
貯蔵器、例えば連続的な超音波フローセル内で一度、反溶媒及び溶媒の混合流を超音波照射に付し、所望の平均サイズの結晶を形成する。超音波エネルギーは、反溶媒中の溶質の核生成及びそれに続く結晶化を、用いられていれば超音波プローブ、又はそのような配置が用いられていれば超音波エネルギー変換機、例えば巻き付き超音波エネルギー変換機の操作周辺で引き起こす。超音波エネルギーは連続的又は不連続的な様式、例えばパルス適用で適用され得る。任意の好適な供給源の超音波照射が用いられ得る。超音波プローブは例えば混合用容器、例えば連続的な超音波フローセルに挿入されるか、超音波照射体が混合容器に含有されるか、又は混合容器が超音波浴に収納されるか又は該混合用容器の外壁に固定されている超音波変換機を有し得る。超音波の振幅及び周波数は、核生成及び結晶成長の速度に影響する。超音波の周波数は、例えば20kHz〜1MHz、好ましくは10-500kHz、さらに好ましくは10-100kHz、例えば10、20、40、60、80、又は100kHz又はそれらの間の任意の周波数、例えば20kHz又は40kHzでよい。
超音波照射は、予め決められた用途に所望のサイズの結晶の形成に適切な振幅で用いられる。例えば80cm2の放射面を有する実験室プローブシステムでは、選択される振幅は約1-30μm、典型的に3-20μm、好ましくは5-10μm、例えば、5μmでよい。8cm2のプローブ面表面積及び5-80Wの電力要求を有するプローブが、2-15μmの振幅を用いて0.6-12.5W/cmの電力密度を提供する。該フローセルに接続されている変換機を含むより大きなシステム、例えば6リットルのフローセルでは、用いられる変換機の電力密度が150-600W/L、好ましくは250-600W/L、及びさらに好ましくは300-600W/L、例えば250W/L又は450W/Lでよい。
超音波照射は、予め決められた用途に所望のサイズの結晶の形成に適切な振幅で用いられる。例えば80cm2の放射面を有する実験室プローブシステムでは、選択される振幅は約1-30μm、典型的に3-20μm、好ましくは5-10μm、例えば、5μmでよい。8cm2のプローブ面表面積及び5-80Wの電力要求を有するプローブが、2-15μmの振幅を用いて0.6-12.5W/cmの電力密度を提供する。該フローセルに接続されている変換機を含むより大きなシステム、例えば6リットルのフローセルでは、用いられる変換機の電力密度が150-600W/L、好ましくは250-600W/L、及びさらに好ましくは300-600W/L、例えば250W/L又は450W/Lでよい。
超音波フローセルにおける混合成分の滞留時間は、10m秒〜約10秒でよい。再循環システムでは、滞留時間をデザインによって長くすることができる。当業者は、そこに配置される流体の各体積に対する超音波フローセル内の滞留時間は、デザインに依存して10m秒〜10秒のオーダーであると理解される。
該方法は、当技術分野で用いられている反応器、例えばバッチ供給反応器又は連続的フロー反応器でデザインに依存して用いられ得る。当業者は、そのような反応器タイプ及びそれらの操作に精通している。生成した結晶は、該バッチチャンバーから当技術分野で従来からある手段、例えばWO 03/092851に記載の方法で結晶を取り除くことによって収集又は収穫され得る。
本発明は添付される実施例及び図面を参照して記載される。実施例及び図面がいかなる様式でも本発明の範囲を限定するとは解釈しないと理解される。
本発明の方法は、従来の設備を用いて添付される図面に示されているように行われ得る。
該方法は、当技術分野で用いられている反応器、例えばバッチ供給反応器又は連続的フロー反応器でデザインに依存して用いられ得る。当業者は、そのような反応器タイプ及びそれらの操作に精通している。生成した結晶は、該バッチチャンバーから当技術分野で従来からある手段、例えばWO 03/092851に記載の方法で結晶を取り除くことによって収集又は収穫され得る。
本発明は添付される実施例及び図面を参照して記載される。実施例及び図面がいかなる様式でも本発明の範囲を限定するとは解釈しないと理解される。
本発明の方法は、従来の設備を用いて添付される図面に示されているように行われ得る。
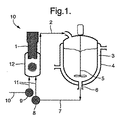
図1を参照すると、閉ループ結晶化装置10が第一のフィードチャンバー4(熱ジャケット3で囲まれている)にインペラー5を含み、軸方向出口6を有してそこから液体反溶媒が送達手段7に流れて第一の流速でポンプ8を介して超音波フローセルチャンバー12にポンプされる。同時に、溶媒中の液体溶質はポンプ9を介して反溶媒と異なる流速で、第二チャンバー(示さず)から送達手段10を介して送達手段11及び超音波フローセルチャンバー12へ通り、そこで該2種の液体が混合される。超音波プローブ1は該混合物を超音波エネルギーで照射し、該混合物は出口2を通って第一のフィードチャンバー4に流れ、連続的な閉フローループを完成する。フローサイクルは所望なサイズの結晶化粒子が達成されるまで繰り返す。装置10における使用では、飽和溶液が反溶媒と十分且つ迅速に混合され、チャンバー4の体積及び流速は超音波フローセルチャンバー12における滞留時間が例えば10秒となるようにする。プローブ1からの超音波エネルギーはチャンバー12の全体積に十分な強度で高周波の音波を与えて分散及び核生成を引き起こし、顕微鏡スケールで起こる局所的キャビテーションが核生成を引き起こす(及び安定な多形体の形成も促進する)流体温度及び圧力における変化を促進する。超音波の出力及びチャンバー12内の滞留時間を調整することにより、核生成の程度を制御することができる。超音波は、チャンバー12内の全ての結晶沈殿物を表面から除去する傾向にあるというさらなる利益を有する。
当業者は、図1の閉ループ結晶化装置10が、例えば送達手段11を単独の送達手段で置き換えることによって異なって配置され得ることを理解し、この場合、送達手段7及び10のための液体フィードが超音波フローセルチャンバー12に単独の入口を介して供給される前にそこに同軸で接触され得る。
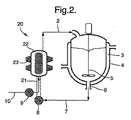
図2によれば、閉ループ結晶化装置20は図1と同じ配置であるが、チャンバー22がその外表面に配置された巻き付き超音波変換機23を有する。巻き付き変換機23はチャンバー22の全体積に十分な強度で高周波の音波を与えて核生成を引き起こし、超音波の出力及びチャンバー22内の滞留時間を調整することによって核生成の程度を制御することができる。超音波は、チャンバー22内の全ての結晶沈殿物を表面から除去する傾向にあるというさらなる利益を有する。
図2によれば、閉ループ結晶化装置20は図1と同じ配置であるが、チャンバー22がその外表面に配置された巻き付き超音波変換機23を有する。巻き付き変換機23はチャンバー22の全体積に十分な強度で高周波の音波を与えて核生成を引き起こし、超音波の出力及びチャンバー22内の滞留時間を調整することによって核生成の程度を制御することができる。超音波は、チャンバー22内の全ての結晶沈殿物を表面から除去する傾向にあるというさらなる利益を有する。
図2と図1の配置のさらなる違いは、送達手段7及び10からの2種の液体フィードが単一の送達手段21内にて同軸で接触され、単一の入口を介して超音波チャンバー22に供給されることである。
当業者は、超音波フローチャンバー22への送達手段も図1の装置の配置に従うことを理解する。
当業者は、熱ジャケットがデザインに依存して反溶媒の温度を所望の温度に保持するように設計されることを理解する。
当業者は、超音波フローチャンバー22への送達手段も図1の装置の配置に従うことを理解する。
当業者は、熱ジャケットがデザインに依存して反溶媒の温度を所望の温度に保持するように設計されることを理解する。
実施例1
2-プロパノール(0.7L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(200rpm)に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。L-バリン(1.5g)を水(35mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に60mL/時間の速度でポンプした。L-バリン溶液の添加終了後、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図3に示す。
2-プロパノール(0.7L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(200rpm)に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。L-バリン(1.5g)を水(35mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に60mL/時間の速度でポンプした。L-バリン溶液の添加終了後、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図3に示す。
実施例2
2-プロパノール(1L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。L-グルタミン酸(4.5g)を水(100mL)に溶解させて飽和溶液を形成し、超音波フローセルに第二の入口から該フローセルの底部に60mL/時間の速度でポンプした。L-グルタミン酸塩溶液を完全に添加し、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図4に示す。
2-プロパノール(1L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。L-グルタミン酸(4.5g)を水(100mL)に溶解させて飽和溶液を形成し、超音波フローセルに第二の入口から該フローセルの底部に60mL/時間の速度でポンプした。L-グルタミン酸塩溶液を完全に添加し、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図4に示す。
実施例3
ヘプタン(0.75L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(250rpm)に入れた。温度は5℃に調整した。ヘプタンを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは5℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。ブデソニド(1.5g)をメタノール(100mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に20mL/時間の速度でポンプした。ブデソニド溶液を完全に添加し、混合物を再循環にさらに30分間保持した。微結晶質生成物を超臨界二酸化炭素による乾燥(無極性溶媒を除去するため)、精密濾過又は噴霧乾燥のいずれかで単離した。
結果を図5に示す。
ヘプタン(0.75L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(250rpm)に入れた。温度は5℃に調整した。ヘプタンを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは5℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。ブデソニド(1.5g)をメタノール(100mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に20mL/時間の速度でポンプした。ブデソニド溶液を完全に添加し、混合物を再循環にさらに30分間保持した。微結晶質生成物を超臨界二酸化炭素による乾燥(無極性溶媒を除去するため)、精密濾過又は噴霧乾燥のいずれかで単離した。
結果を図5に示す。
実施例4
水(0.7L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(200rpm)に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。オルメサルタン(2.1g)をブタノン(70mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に20mL/時間の速度でポンプした。オルメサルタン溶液を完全に添加し、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図6に示す。
水(0.7L)を、熱調整ジャケットを備えた1Lの攪拌型結晶機(200rpm)に入れた。温度は16℃に調整した。2-プロパノールを、再循環ループの周りに隔膜ポンプ(20L/時間で操作する)及び30mmの直径の20kHz超音波プローブを備えた60mLの熱調整ガラス超音波フローセルを用いてポンプした。該プローブは該フローセルの最も高い位置に保持され、ゼロ振動の点(節点)で密閉/クランプした。フローセルは16℃に熱調整した。連続的な超音波を15W出力、5μmの振幅で適用した。オルメサルタン(2.1g)をブタノン(70mL)に溶解させ、超音波フローセルに第二の入口から該フローセルの底部に20mL/時間の速度でポンプした。オルメサルタン溶液を完全に添加し、微結晶質生成物を精密濾過又は噴霧乾燥で単離した。
結果を図6に示す。
Claims (16)
- 活性成分の結晶粒子を超音波照射の存在下で調製するための方法であって、第一の流れにおける少なくとも1種の溶質の溶媒溶液と第二の流れにおける反溶媒とを該反溶媒:溶媒の流速比を20:1より高く接触させてそれらを混合させる工程、及び生成した結晶を回収する工程を含む、方法。
- 前記溶質が少なくとも1種の活性成分又はその前駆体を含む、請求項1記載の方法。
- 前記溶質が少なくとも1種の活性成分を含む、請求項1又は2記載の方法。
- 前記溶質が2種の活性成分の混合物を含む、請求項1又は2記載の方法。
- 前記活性成分がプロピオン酸フルチカゾンである、請求項3記載の方法。
- 前記活性成分がサルブタモールである、請求項3記載の方法。
- 液体である前記反溶媒が液体である前記溶媒と混和性である、請求項1〜6のいずれか1項に記載の方法。
- 液体である前記反溶媒及び溶媒が同一のものであり、該反溶媒が該溶媒と異なる温度で保持される、請求項7記載の方法。
- 液体である前記反溶媒及び溶媒の温度が-10℃〜+120℃であり、該溶媒及び反溶媒の温度が少なくとも50℃の温度差で分けられる、請求項1〜8のいずれか1項に記載の方法。
- 前記溶質が吸入治療に好適な活性成分又はキャリア物質である、請求項1〜9のいずれか1項に記載の方法。
- 前記反溶媒:溶媒の流速比が1000:1以下である、請求項1〜10のいずれか1項に記載の方法。
- 前記流速比が20:1〜900:1である、請求項11記載の方法。
- 前記流速比が20:1〜500:1である、請求項12記載の方法。
- 前記流速比が20:1〜400:1である、請求項13記載の方法。
- 前記流速比が20:1〜380:1である、請求項14記載の方法。
- 前記流速比が約333:1である、請求項15記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0705159.2A GB0705159D0 (en) | 2007-03-19 | 2007-03-19 | Process for making crystals |
| PCT/GB2008/050191 WO2008114052A1 (en) | 2007-03-19 | 2008-03-18 | Process for making crystals |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014016565A Division JP5808830B2 (ja) | 2007-03-19 | 2014-01-31 | 結晶の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010522154A true JP2010522154A (ja) | 2010-07-01 |
Family
ID=38008612
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009554087A Pending JP2010522154A (ja) | 2007-03-19 | 2008-03-18 | 結晶の製造方法 |
| JP2014016565A Active JP5808830B2 (ja) | 2007-03-19 | 2014-01-31 | 結晶の製造方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014016565A Active JP5808830B2 (ja) | 2007-03-19 | 2014-01-31 | 結晶の製造方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US9162160B2 (ja) |
| EP (1) | EP2134457B1 (ja) |
| JP (2) | JP2010522154A (ja) |
| CN (1) | CN101636223B (ja) |
| BR (1) | BRPI0809275A2 (ja) |
| CA (1) | CA2680105C (ja) |
| ES (1) | ES2701728T3 (ja) |
| GB (2) | GB0705159D0 (ja) |
| IL (1) | IL200802A (ja) |
| RU (1) | RU2456066C2 (ja) |
| WO (1) | WO2008114052A1 (ja) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0705159D0 (en) * | 2007-03-19 | 2007-04-25 | Prosonix Ltd | Process for making crystals |
| EP2321023B1 (en) | 2008-07-18 | 2016-06-15 | Prosonix Limited | Process for improving crystallinity of fluticasone particles |
| GB0900080D0 (en) * | 2009-01-06 | 2009-02-11 | Prosonix Ltd | An apparatus and process for producing crystals |
| GB0918431D0 (en) | 2009-10-21 | 2009-12-09 | Prosonix Ltd | Process for improving crystallinity |
| EP2360147A1 (en) | 2010-02-22 | 2011-08-24 | CHIESI FARMACEUTICI S.p.A. | Process for preparing crystalline particles of a salt of 8-hydroxy-5-[(1R)-1-hydroxy-2-[[(1R)-2-(4-methoxyphenyl)-1-methylethyl]amino] ethyl]-2(1H)-quinolinone (carmoterol) |
| BR112012024059B1 (pt) | 2010-04-01 | 2021-06-01 | Chiesi Farmaceutici S.P.A. | Processo de preparo de um excipiente para composições farmacêuticas em pó para inalação, partículas carreadoras para uma formulação farmacêutica de pó seco, composição farmacêutica em forma de pó seco para inalação e inalador de pó seco |
| US9278867B2 (en) | 2010-12-30 | 2016-03-08 | Yava Technologies Inc. | Transition metal compound particles and methods of production |
| EP2500072A1 (en) | 2011-03-15 | 2012-09-19 | LEK Pharmaceuticals d.d. | A novel process of residual solvent removal |
| GB201113662D0 (en) | 2011-08-08 | 2011-09-21 | Prosonix Ltd | Pharmaceutical compositions |
| US9919816B2 (en) * | 2011-11-28 | 2018-03-20 | Nanomakers | Valve and sealed container for submicron particles, and method for using same |
| US8765725B2 (en) | 2012-05-08 | 2014-07-01 | Aciex Therapeutics, Inc. | Preparations of hydrophobic therapeutic agents, methods of manufacture and use thereof |
| PT3517541T (pt) | 2012-05-08 | 2020-08-28 | Nicox Ophthalmics Inc | Forma polimórfica de propionato de fluticasona |
| CN102872612B (zh) * | 2012-10-15 | 2013-11-27 | 中国工程物理研究院化工材料研究所 | 超声结晶器 |
| US9815865B2 (en) | 2013-01-07 | 2017-11-14 | Nicox Ophthalmics, Inc. | Preparations of hydrophobic therapeutic agents, methods of manufacture and use thereof |
| AU2014210942A1 (en) * | 2013-01-31 | 2015-08-20 | Prosonix Limited | Pharmaceutical compositions comprising multi-component crystalline particles suitable for use in inhalation therapy |
| GB201301721D0 (en) * | 2013-01-31 | 2013-03-20 | Prosonix Ltd | Pharmaceutical Preparations |
| CN103172476A (zh) * | 2013-04-08 | 2013-06-26 | 中国工程物理研究院化工材料研究所 | 一种亚微米颗粒1-氧-二氨基-3,5-二硝基吡嗪炸药的制备方法 |
| US9469548B2 (en) * | 2015-02-20 | 2016-10-18 | Hydro Dynamics, Inc. | Continuous hydrodynamic cavitation crystallization |
| CN105037253A (zh) * | 2015-05-27 | 2015-11-11 | 上海应用技术学院 | 一种超声逼晶法提纯化合物的方法 |
| CN105664816B (zh) * | 2016-03-17 | 2017-11-03 | 杭州成功超声设备有限公司 | 将基于振幅控制的超声波设备用于化工装置的三步式方法 |
| EP3369468A1 (en) * | 2017-02-23 | 2018-09-05 | Covaris, Inc. | Acoustic energy-based control of particle count in crystallization |
| US10583085B2 (en) | 2017-05-17 | 2020-03-10 | Chiesi Farmaceutici S.P.A. | Carrier particles for dry powder formulations for inhalation |
| BR112021001402A2 (pt) | 2018-07-27 | 2021-04-27 | Chiesi Farmaceutici S.P.A. | novas partículas carreadoras para formulações de pó seco para inalação |
| CN110330335A (zh) * | 2019-07-19 | 2019-10-15 | 中国工程物理研究院化工材料研究所 | 铋基卤化物陶瓷材料、制备方法及x射线探测器 |
| US11925907B2 (en) | 2019-07-22 | 2024-03-12 | Canopy Growth Corporation | Continuous crystallization of cannabinoids in a stirred-tank reactor |
| CN110773079B (zh) * | 2019-11-18 | 2022-03-01 | 江苏博迁新材料股份有限公司 | 一种超声喷雾法制备超细粉球的方法 |
| CN112972384B (zh) * | 2019-12-02 | 2022-03-18 | 长风药业股份有限公司 | 一种格隆溴铵和茚达特罗原料药微粉混合物的制备方法 |
| GB2599890A (en) | 2020-08-18 | 2022-04-20 | Ashe Robert | Improved loop reactor |
| CN114307840B (zh) * | 2022-01-08 | 2022-09-16 | 安徽省农业科学院棉花研究所 | 一种有机配方肥热返料设备 |
| CN115634635B (zh) * | 2022-10-20 | 2025-03-18 | 江苏瑞祥化工有限公司 | 一种高纯度粒状2,5-二氯苯胺的制备装置及制备方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002533205A (ja) * | 1998-12-24 | 2002-10-08 | グラクソ グループ リミテッド | 結晶粒子を調製するための装置および方法 |
| JP2003527323A (ja) * | 1999-08-19 | 2003-09-16 | アベンティス・フアーマ・リミテッド | 微細な医薬品材料の製造方法 |
| JP2004276334A (ja) * | 2003-03-13 | 2004-10-07 | Ricoh Co Ltd | 感熱記録材料 |
| JP2005525216A (ja) * | 2002-01-22 | 2005-08-25 | グラクソ グループ リミテッド | 結晶粒子を調製するための装置および方法 |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2033254C1 (ru) * | 1988-02-23 | 1995-04-20 | Александр Петрович Пляскин | Способ обработки материалов и устройство для его осуществления |
| GB9310030D0 (en) * | 1993-05-15 | 1993-06-30 | Scras | Dry processed particles and process for the preparation of the same |
| US5874029A (en) * | 1996-10-09 | 1999-02-23 | The University Of Kansas | Methods for particle micronization and nanonization by recrystallization from organic solutions sprayed into a compressed antisolvent |
| CA2299284C (en) * | 1997-08-05 | 2008-07-08 | Mfic Corporation | Multiple stream high pressure mixer/reactor |
| US6465015B1 (en) * | 1998-02-24 | 2002-10-15 | Arch Chemicals, Inc. | Sonic method of enhancing chemical reactions to provide uniform, non-agglomerated particles |
| AU755470B2 (en) * | 1999-01-29 | 2002-12-12 | Bristol-Myers Squibb Company | Sonic impinging jet crystallization apparatus and process |
| GB9925934D0 (en) | 1999-11-03 | 1999-12-29 | Glaxo Group Ltd | Novel apparatus and process |
| US6620351B2 (en) | 2000-05-24 | 2003-09-16 | Auburn University | Method of forming nanoparticles and microparticles of controllable size using supercritical fluids with enhanced mass transfer |
| GB0016040D0 (en) * | 2000-06-29 | 2000-08-23 | Glaxo Group Ltd | Novel process for preparing crystalline particles |
| GB0016002D0 (en) * | 2000-06-29 | 2000-08-23 | Glaxo Group Ltd | Novel process for preparing crystalline particles |
| GB0015981D0 (en) * | 2000-06-29 | 2000-08-23 | Glaxo Group Ltd | Novel process for preparing crystalline particles |
| US20040256749A1 (en) * | 2000-12-22 | 2004-12-23 | Mahesh Chaubal | Process for production of essentially solvent-free small particles |
| ATE322936T1 (de) * | 2001-05-05 | 2006-04-15 | Accentus Plc | Bildung kleiner krsitalle |
| EP1423096B1 (en) * | 2001-08-29 | 2006-08-16 | Dow Global Technologies Inc. | A process for preparing crystalline drug particles by means of precipitation |
| GB0125604D0 (en) | 2001-10-25 | 2001-12-19 | Glaxo Group Ltd | Novel process |
| GB0219815D0 (en) * | 2002-08-24 | 2002-10-02 | Accentus Plc | Preparation of small crystals |
| US20040197275A1 (en) * | 2002-10-17 | 2004-10-07 | Ecole Polytechnique Federale De Lausanne | Process for the manufacture of powders of inhalable medicaments |
| GB0300339D0 (en) * | 2003-01-08 | 2003-02-05 | Bradford Particle Design Ltd | Particle formation |
| US20070065372A1 (en) | 2003-02-21 | 2007-03-22 | Robert Price | Process for the production of particles |
| US7041144B2 (en) * | 2003-03-04 | 2006-05-09 | Five Star Technologies, Inc. | Hydrodynamic cavitation crystallization process |
| US20080194868A1 (en) * | 2003-03-04 | 2008-08-14 | Kozyuk Oleg V | Hydrodynamic cavitation crystallization device and process |
| NZ543772A (en) | 2003-04-29 | 2009-05-31 | Organon Nv | Antisolvent crystallisation process using membranes for the purification of inorganic or organic compositions |
| EP1620192A1 (en) * | 2003-04-29 | 2006-02-01 | Akzo Nobel N.V. | Processes involving the use of antisolvent crystallisation |
| GB0319797D0 (en) * | 2003-08-26 | 2003-09-24 | Leuven K U Res & Dev | Particle size reduction of poorly soluble drugs |
| US7208106B2 (en) * | 2003-10-24 | 2007-04-24 | Ferro Corporation | Method of forming particles |
| EP1688169A4 (en) * | 2003-11-28 | 2008-10-01 | Mitsubishi Chem Corp | PROCESS FOR PRODUCING FINE PARTICLES OF AN ORGANIC COMPOUND |
| JP2005177746A (ja) * | 2003-11-28 | 2005-07-07 | Mitsubishi Chemicals Corp | 有機化合物微粒子の製造方法 |
| GB0507165D0 (en) | 2005-04-08 | 2005-05-18 | Glaxo Group Ltd | Novel crystalline pharmaceutical product |
| TW200810789A (en) * | 2006-03-14 | 2008-03-01 | Merck & Co Inc | Processes and apparatuses for the production of crystalline organic microparticle compositions by micro-milling and crystallization on micro-seed and their use |
| US20080075777A1 (en) * | 2006-07-31 | 2008-03-27 | Kennedy Michael T | Apparatus and methods for preparing solid particles |
| GB0705159D0 (en) * | 2007-03-19 | 2007-04-25 | Prosonix Ltd | Process for making crystals |
| GB0711680D0 (en) * | 2007-06-18 | 2007-07-25 | Prosonix Ltd | Process |
| EP2360147A1 (en) * | 2010-02-22 | 2011-08-24 | CHIESI FARMACEUTICI S.p.A. | Process for preparing crystalline particles of a salt of 8-hydroxy-5-[(1R)-1-hydroxy-2-[[(1R)-2-(4-methoxyphenyl)-1-methylethyl]amino] ethyl]-2(1H)-quinolinone (carmoterol) |
-
2007
- 2007-03-19 GB GBGB0705159.2A patent/GB0705159D0/en not_active Ceased
-
2008
- 2008-03-18 BR BRPI0809275-3A2A patent/BRPI0809275A2/pt not_active Application Discontinuation
- 2008-03-18 CN CN200880008925.3A patent/CN101636223B/zh active Active
- 2008-03-18 EP EP08719036.9A patent/EP2134457B1/en active Active
- 2008-03-18 JP JP2009554087A patent/JP2010522154A/ja active Pending
- 2008-03-18 RU RU2009138325/05A patent/RU2456066C2/ru not_active IP Right Cessation
- 2008-03-18 US US12/531,322 patent/US9162160B2/en active Active
- 2008-03-18 GB GB0804995.9A patent/GB2447761B/en active Active
- 2008-03-18 WO PCT/GB2008/050191 patent/WO2008114052A1/en not_active Ceased
- 2008-03-18 CA CA2680105A patent/CA2680105C/en active Active
- 2008-03-18 ES ES08719036T patent/ES2701728T3/es active Active
-
2009
- 2009-09-08 IL IL200802A patent/IL200802A/en active IP Right Grant
-
2014
- 2014-01-31 JP JP2014016565A patent/JP5808830B2/ja active Active
-
2015
- 2015-09-15 US US14/854,750 patent/US10143991B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002533205A (ja) * | 1998-12-24 | 2002-10-08 | グラクソ グループ リミテッド | 結晶粒子を調製するための装置および方法 |
| JP2003527323A (ja) * | 1999-08-19 | 2003-09-16 | アベンティス・フアーマ・リミテッド | 微細な医薬品材料の製造方法 |
| JP2005525216A (ja) * | 2002-01-22 | 2005-08-25 | グラクソ グループ リミテッド | 結晶粒子を調製するための装置および方法 |
| JP2004276334A (ja) * | 2003-03-13 | 2004-10-07 | Ricoh Co Ltd | 感熱記録材料 |
Also Published As
| Publication number | Publication date |
|---|---|
| GB2447761B (en) | 2012-02-29 |
| IL200802A0 (en) | 2010-05-17 |
| GB0705159D0 (en) | 2007-04-25 |
| US10143991B2 (en) | 2018-12-04 |
| US20160001252A1 (en) | 2016-01-07 |
| BRPI0809275A2 (pt) | 2014-10-14 |
| CN101636223B (zh) | 2015-09-16 |
| ES2701728T3 (es) | 2019-02-25 |
| GB0804995D0 (en) | 2008-04-16 |
| CA2680105C (en) | 2016-05-17 |
| RU2009138325A (ru) | 2011-04-27 |
| WO2008114052A1 (en) | 2008-09-25 |
| CA2680105A1 (en) | 2008-09-25 |
| JP2014094965A (ja) | 2014-05-22 |
| US9162160B2 (en) | 2015-10-20 |
| IL200802A (en) | 2013-04-30 |
| EP2134457A1 (en) | 2009-12-23 |
| CN101636223A (zh) | 2010-01-27 |
| EP2134457B1 (en) | 2018-09-12 |
| RU2456066C2 (ru) | 2012-07-20 |
| GB2447761A (en) | 2008-09-24 |
| JP5808830B2 (ja) | 2015-11-10 |
| US20100018853A1 (en) | 2010-01-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5808830B2 (ja) | 結晶の製造方法 | |
| US9278323B2 (en) | Process for making crystals | |
| US20110288060A1 (en) | apparatus and process for producing crystals | |
| CA2729644C (en) | Process for improving crystallinity | |
| JP5154078B2 (ja) | 粒子の製造プロセス | |
| US20120309729A1 (en) | Barrier composition | |
| MXPA04007073A (es) | Aparato y proceso para preparar particulas cristalinas. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110317 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20121220 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130110 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130930 |