JP2010502574A - Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 - Google Patents
Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 Download PDFInfo
- Publication number
- JP2010502574A JP2010502574A JP2009525172A JP2009525172A JP2010502574A JP 2010502574 A JP2010502574 A JP 2010502574A JP 2009525172 A JP2009525172 A JP 2009525172A JP 2009525172 A JP2009525172 A JP 2009525172A JP 2010502574 A JP2010502574 A JP 2010502574A
- Authority
- JP
- Japan
- Prior art keywords
- conjugate
- rgd
- photosensitizer
- bacteriochlorophyll
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 C[*@](C(C=C1)=C(*)C(C=C2)=*(C3)C2=C(C2=CC=C4*2C)P)C1=C(*)C(C=C1)=*3C1=C4[Np] Chemical compound C[*@](C(C=C1)=C(*)C(C=C2)=*(C3)C2=C(C2=CC=C4*2C)P)C1=C(*)C(C=C1)=*3C1=C4[Np] 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/12—Cyclic peptides with only normal peptide bonds in the ring
- C07K5/123—Tripeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
- A61K41/0057—Photodynamic therapy with a photosensitizer, i.e. agent able to produce reactive oxygen species upon exposure to light or radiation, e.g. UV or visible light; photocleavage of nucleic acids with an agent
- A61K41/0071—PDT with porphyrins having exactly 20 ring atoms, i.e. based on the non-expanded tetrapyrrolic ring system, e.g. bacteriochlorin, chlorin-e6, or phthalocyanines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/08—Tripeptides
- C07K5/0815—Tripeptides with the first amino acid being basic
- C07K5/0817—Tripeptides with the first amino acid being basic the first amino acid being Arg
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/10—Tetrapeptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/12—Cyclic peptides with only normal peptide bonds in the ring
- C07K5/126—Tetrapeptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/64—Cyclic peptides containing only normal peptide links
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- Child & Adolescent Psychology (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Obesity (AREA)
- Cardiology (AREA)
- Diabetes (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Medicinal Preparation (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
Description
AMD:加齢黄斑変性症;Bchl a:バクテリオクロロフィルa:第5の同素環、中心Mg原子、173位にフィチル又はゲラニルゲラニル基、132位にCOOCH3基、132位にH原子、2、7、12、18位にメチル基、3位にアセチル基、及び8位にエチル基を有する、五環性7,8,17,18−テトラヒドロポルフィリンであり、本明細書中で化合物1と呼ぶ;Bphe:バクテリオフェオフィチンa(中心Mgが2つのH原子によって置き換えられているBchl);Bpheid:バクテリオフェオホルビドa(中心金属原子を有さないBpheに由来するC−172−遊離カルボン酸);Chl:クロロフィル;EC:内皮細胞;ECM:細胞外基質;NIR:近赤外線;Pd−Bpheid:Pd−バクテリオフェオホルビドa;PDT:光線力学的治療;RGD−4C:環状ノナペプチドCDCRGDCFC−NH2;ロドバクテリオクロリン(Rhodobacteriochlorin):17位に−CH2CH2COOH基、13位に−COOH、2、7、12、8位にメチル基、並びに3及び8位にエチル基を有する、四環性7,8,17,18−テトラヒドロポルフィリン;ROS:反応性酸素種;VTI:血管標的のイメージング;VTP:血管標的のPDT。
腫瘍細胞の成長及び発生は、連続的な酸素及び栄養素の供給に非常に依存するので、腫瘍細胞自体ではなく腫瘍血管構造を破壊するために光線力学的試薬を標的化することは、治療上の利点を提供し得る(Ruoslahti、2002)。そのような血管損傷には血栓の形成が含まれ、腫瘍血液灌流をさらに制限し得る(Huang他、1997)。さらに、腫瘍血管内皮細胞(EC)層の標的化により、治療用巨大分子による腫瘍間質の乏しい浸透が回避されると予測される(Huang他、1997;Burrows及びThorpe、1994)。腫瘍血管は腫瘍の微小環境に影響を受け、腫瘍関連の「シグネチャ」を獲得する可能性があるが、これらは悪性ではなく、薬物耐性を発生する可能性は低い。さらに、標的化した抗血管剤も腫瘍細胞に対して活性を有する場合は、有効性のさらなる増加を期待することができる。したがって、抗血管特性を抗腫瘍の細胞毒性活性と1つの薬物中で組み合わせることにより、その有効性は増加することが期待でき、したがって、必要な有効細胞毒性用量を低下させることができる。ECに加えて、一例では、腫瘍血管の管腔側モザイクの一部も腫瘍細胞を含むことが示されている(Ruoslahti、2002;Chang他、2000)。したがって、これらの腫瘍細胞は血液に直接曝されており、そうでなければ内皮障壁を越えることができない治療用巨大分子と自由に相互作用すると考えられている。
ECM構成成分のアルギニン−グリシン−アスパラギン酸Arg−Gly−Asp(RGD)モチーフは、フィブロネクチン(Pierschbacher及びRuoslahti、1984)並びにビトロネクチンと同様、インテグリンと結合する(Ruoslahti及びPierschbacher、1987;D’Souza SE他、1991;Joshi他、1993;Koivunen他、1994)。インテグリンに媒介される接着は、細胞の生存、増殖、及び遊走を調節する細胞内シグナル伝達事象をもたらす。25種程度のインテグリンが知られており、そのうち少なくとも8種が、RGDモチーフを一次認識配列としてそのリガンド中で結合する。
PDTにおける新規バクテリオクロロフィル(Bchl)誘導体の増感剤としての応用が、近年、本発明者らのグループによって、科学文献(Zilberstein他、2001;Schreiber他、2002;Gross他、1997;Zilberstein他、1997;Rosenbach−Belkin他、1996;Gross他、2003a;Koudinova他、2003;Preise他、2003;Gross他、2003b)及び特許公開の米国特許US5,726,169、US5,650,292、US5,955,585、US6,147,195、US6,740,637、US6,333,319、US6,569,846、US7,045,117、ドイツ特許DE41 21 876、欧州特許EP1 246 826、国際公開公報WO2004/045492、WO2005/120573中に報告されている。Bchl誘導体のスペクトル、光物理学、及び光化学により、これらは、PDTで現在使用されている他の増感剤を超える明白な利点を有する、最適な光収集分子となっている。これらのBchl誘導体は大部分が極性であり、非常に短い間循環中に留まり、他の組織への血管外遊走は実質的にない(Brandis他、2003)。したがって、これらの化合物は、光との短い(5〜10分間)側頭血管内遭遇及びPDTで生じた細胞毒性を有するROSに対する腫瘍血管のより高い感受性に依存する血管標的のPDTの良好な候補である。
H2N−C(=NH)NH−(CH2)5−CO−NH−CH(CH2)−(CH2)2−COOH
[式中、
Ar1、Ar2、Ar3、及びAr4は、同一又は異なり、それぞれ、炭素環アリール、ヘテロアリール及び混合カルボアリール−ヘテロアリール基から選択されるアリール基であり、アリール基のそれぞれは、未置換であるか、又は、ハロゲン原子、アリールがフェニルの場合はC2〜C8アルキル、アリールがヘテロアリール若しくは混合カルボアリール−ヘテロアリールの場合はC1〜C8アルキル、C1〜C8アルコキシ、カルボキシ、C1〜C8アルキルアミノ、アミノ−(C1〜C8)アルキルアミノ、トリ−(C1〜C8)アルキルアンモニウム、ヒドロキシ、及びCONH2から選択される1つ若しくは複数の置換基によって置換されており、Ar1、Ar2、Ar3、及びAr4のうちの少なくとも1つは、その置換基のうちの1つ又は架橋基を介して前記少なくとも1つのアリール基と連結したRGD含有ペプチド又はRGDペプチド模倣体によって置換されており;
nは、置換基が中性の場合は0であるか、又は、nは1〜4の整数であり;
Xは、アリール基が正荷電の場合は製薬上許容される陰イオンであるか、又は、アリール基が負荷電の場合は製薬上許容される陽イオンであり;
Mは、2Hであるか、又は、Mg、Pd、Pt、Co、Ni、Sn、Cu、Zn、Mn、In、Eu、Fe、Au、Al、Gd、Er、Yb、Lu、Ga、Y、Rh、Ru、Si、Ge、Cr、Mo、P、Re、Tl及びTc並びにその同位体からなる群から選択される原子である]。
[式中、
Mは、2H、又はMg、Pd、Pt、Co、Ni、Sn、Cu、Zn、Mn、In、Eu、Fe、Au、Al、Gd、Er、Yb、Lu、Ga、Y、Rh、Ru、Si、Ge、Cr、Mo、P、Re及びTc並びにその同位体からなる群から選択される原子を表し;
Xは、O又はN−R7であり;
R1、R’2及びR6は、それぞれ独立して、Y−R8、−NR9R’9若しくは−N+R9R’9R”9A−であるか、
又は、式II中のR1及びR6は、それらが付着している炭素原子と一緒になって、RGDペプチド若しくはRGDペプチド模倣体を含む環を形成し;
Yは、O又はSであり;
R2は、H、OH又はCOOR9であり;
R3は、H、OH、C1〜C12アルキル又はC1〜C12アルコキシであり;
R4は、−CH=CR9R’9、−CH=CR9Hal、−CH=CH−CH2−NR9R’9、−CH=CH−CH2−N+R9R’9R”9A−、−CHO、−CH=NR9、−CH=N+R9R’9A−、−CH2−OR9、−CH2−SR9、−CH2−Hal、−CH2−R9、−CH2−NR9R’9、−CH2−N+R9R’9R”9A−、−CH2−CH2R9、−CH2−CH2Hal、−CH2−CH2OR9、−CH2−CH2SR9、−CH2−CH2−NR9R’9、−CH2−CH2−N+R9R’9R”9A−、−COCH3、C(CH3)=CR9R’9、−C(CH3)=CR9Hal、−C(CH3)=NR9、−CH(CH3)=N+R9R’9A−、−CH(CH3)−Hal、−CH(CH3)−OR9、−CH(CH3)−SR9、−CH(CH3)−NR9R’9、−CH(CH3)−N+R9R’9 R’9A−、又は−C≡CR9であり;
R’4は、メチル又はホルミルであり;
R5は、=O、=S、=N−R9、=N+R9R’9A−、=CR9R’9、又は=CR9−Halであり;
R7、R8、R9、R’9及びR”9は、それぞれ独立して:
(a)H;
(b)C1〜C25ヒドロカルビル;
(c)ハロゲン、ニトロ、オキソ、OR、SR、エポキシ、エピチオ、−−NRR’、−CONRR’、−CONR−NRR’、−NHCONRR’、−NHCONRNRR’、−COR、COOR”、−OSO3R、−SO3R”、−SO2R、−NHSO2R、−SO2NRR’、=N−OR、−(CH2)n−CO−NRR’、−O−(CH2)n−OR、−O−(CH2)n−O−(CH2)n−R、−OPO3RR’、−PO2HR、及び−PO3R”R”からなる群から選択される1つ又は複数の官能基によって置換された、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、アルケニル又はアルキニル、より好ましくはC1〜C10又はC1〜C6アルキル(式中、R及びR’は、それぞれ独立して、H、ヒドロカルビル又はヘテロシクリルであり、R”はヒドロカルビル又はヘテロシクリルである);
(d)正荷電基、負荷電基、生理的条件下で正荷電基に変換される塩基性基、及び生理的条件下で負荷電基に変換される酸性基からなる群から選択される1つ又は複数の官能基によって置換された、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、より好ましくはC1〜C10又はC1〜C6アルキル;
(e)1つ若しくは複数のヘテロ原子及び/又は1つ若しくは複数の炭素環若しくはヘテロ環部分を含む、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、より好ましくはC1〜C10又はC1〜C6アルキル;
(f)1つ若しくは複数のヘテロ原子及び/又は1つ若しくは複数の炭素環若しくはヘテロ環部分を含み、上記(c)及び(d)で定義した1つ又は複数の官能基によって置換された、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、より好ましくはC1〜C10又はC1〜C6アルキル;
(g)アミノ酸残基、ペプチド、タンパク質、単糖、オリゴ糖、多糖、又は多座配位子及び金属とのそのキレート錯体によって置換された、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、より好ましくはC1〜C10、又はC1〜C6アルキル;或いは
(h)アミノ酸残基、ペプチド、タンパク質、単糖、オリゴ糖、多糖、又は多座配位子及び金属とのそのキレート錯体であり;
R7はさらに、−NRR’であってよく、R及びR’は、それぞれ、H、又は負荷電基、好ましくはSO3 −によって任意選択で置換された、C1〜C25ヒドロカルビル、好ましくはC1〜C25アルキル、より好ましくはC1〜C10若しくはC1〜C6アルキルであり;
R8はさらに、H+、又はR1、R’2及びR6は、それぞれ独立してY−R8である場合は陽イオンR+ 10であってよく;
R+ 10は、金属、アンモニウム基又は有機陽イオンであり;
A−は、生理的に許容される陰イオンであり;
mは0又は1であり;
7〜8位の点線は、任意選択の二重結合を表す]であるコンジュゲートに関し、前記式I、II又はIIIのクロロフィル又はバクテリオクロロフィルの誘導体は、少なくとも1つのRGD含有ペプチド残基を含む。
本明細書の実施例では、本発明の中間体及び化合物1〜10並びにコンジュゲート(11〜24)を、以下の化合物リスト及び付属書に従って、その対応する太字且つ下線を引いたアラビア番号によって提示する。すべての化合物及びコンジュゲートの式は、明細書の最後、参考文献の直前の付属書中に提示する。
1.バクテリオクロロフィルa(Bchl a)
2.132−OH−バクテリオクロロフィルa(132−OH−Bchl a)
3.バクテリオフェオホルビドa(Bpheid a)
4.132−OH−バクテリオフェオホルビドa(132−OH−Bpheid a)
4a.バクテリオプルプリン18(BPP18)
5.クロロフィルa(Chl a)
6.フェオホルビドa(Pheid a)
7.パラジウムバクテリオフェオホルビドa(Pd−Bpheid)
8.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミドカリウム塩
9.マンガン(III)132−OH−バクテリオフェオホルビドa(Mn(III)132−OH−Bpheid a)
10.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン−131−(2,3−ジヒドロキシプロピル)アミドカリウム塩
11.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(RGD−4C)アミドカリウム塩
12.マンガン(III)132−OH−バクテリオフェオホルビド−173−(環状RGDfK)アミド
13.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
14.マンガン(III)31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
15.銅(II)31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
16.31,32−ジデヒドロロドクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
17.マンガン(III)31,32−ジデヒドロロドクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
18.銅(II)31,32−ジデヒドロロドクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩
19.パラジウムバクテリオプルプリンN−(3−スルホプロピルアミノ)イミド−173−(環状RGDfK)アミドカリウム塩
20.メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシフェニル)ポルフィン
21.銅(II)メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシフェニル)ポルフィン
22.ガドリニウム(III)メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシフェニル)ポルフィン
23.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン−131−(2,3−ジヒドロキシプロピル)アミド−173−(環状RGDfK)アミド
24.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RGDfK)アミドカリウム塩。
25.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミドカリウム塩。
26.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(GRGDSP)アミドカリウム塩
27.バクテリオフェオホルビド−173−(環状RGDfK)アミド
28.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(3−[(3−アミノプロピル)アミノ]プロピル)アミド−173−(環状RGDfK)アミド
29.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2,3−ジヒドロキシプロピル)アミド−173−(環状RGDfK)アミド
30.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−モルホリノ−N−エチル)アミド−173−(環状RGDfK)アミド
31.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−{3−[4−(3−アミノプロピル)−ピペラジン−1−イル]−プロピル}アミド−173−(環状RGDfK)アミド
32.バクテリオフェオホルビド−173−(2−環状RGDK−アミド−N−エチル)アミド
33.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(GRGDSPK)アミドカリウム塩
34.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−[(GRGDSP)4K]アミドカリウム塩
35.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RGDf−N(Me)K)アミドカリウム塩
36.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)−173−N−[4−ヘプタン二酸ビス−(環状RGDyK−アミド)]アミドカリウム塩
37.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131,173−環状(2−RGD−アミド−N−エチル)ジアミド
38.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131,173−環状(2−RGD−アミド−N−エチル)ジアミド
39.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131,173−シクロ{3−[4−(3−アミノプロピル−DGR−アミド)−ピペラジン−1−イル]−プロピル}ジアミド
40.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−[4−(メチル−5−(6−グアニジノ−ヘキサノイルアミノ)−ペンタン酸)]アミドカリウム塩
41.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−[7−アミド−3−[[1−(4−グアニジノ−ブチリル)−ピペリジン−3−カルボニル]−アミノ]−ヘプタン酸]カリウム塩
42.パラジウム31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(2−スルホエチル)アミド−173−(環状RADfK)アミドカリウム塩
43.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(3−DTPA−アミド−N−プロピル)アミド−173−(環状RGDfK)アミド
44.31−オキソ−15−メトキシカルボニルメチル−ロドバクテリオクロリン131−(3−Gd−DTPA−アミド−N−プロピル)アミド−173−(環状RGDfK)アミド
(i)バクテリオクロロフィルa(Bchl a)、1を、Scherz及びParson、1984に記載のように得た。手順は、光合成細菌ロドブラム・サルフィドフィルム(Rhodovulum sulfidophilum)の乾燥(凍結乾燥)細胞から生体色素を抽出することから開始した。粗生体色素抽出物の精製は、DEAE−セファロースカラムクロマトグラフィーによって、Omata及びMurata、1983に従って実施した。手短に述べると、DEAE−セファロースを蒸留水で洗浄し、その後、1Mの酢酸ナトリウム緩衝液(pH=7)中に懸濁させることによって、酢酸形態に変換した。スラリーをアセトンで3回洗浄し、最後にメタノール−アセトン(1:3、v:v)に懸濁させて5℃で保管した。薄層クロマトグラフィー(TLC)によって純度を確認した。TLC条件の詳細な説明は、Fiedor他、1992に見つけることができる。
コンジュゲート11の合成
材料及び方法に記載のように得た化合物8を、以下のようにして、スキーム1に記載のように、環状ペプチドRGD−4Cと直接コンジュゲートさせた:化合物8(10mg)を、NHS(20mg)と、DMSO(3ml)中のEDC(20mg)の存在下で、終夜反応させた。得られた活性スクシンイミドエステル(Bauminger及びWilchek、1980)をCHCl3:MeOH(6:1、体積)を用いたシリカカラムで精製し、乾燥させ、さらに使用するまでアルゴン下で暗所に保った。RGD−4C(2mg、1.97μmol)を800μlのDMSOに溶かし、活性エステル(800μlのDMSO及び400μlのNaHCO3緩衝液、0.1M、pH8.5中に、4.8mg、5.13μmol)に加えた。反応混合物を室温で24時間インキュベーションし、アルゴン下で攪拌した。得られたコンジュゲート11を、HPLCを用いて精製し、質量分析によって同定した(1837m/z)(図1A〜1C)。収率:18%。
コンジュゲート12の合成
化合物9の合成から開始してコンジュゲート12を調製した。
材料及び方法に記載のように得た化合物4(20mg)を、事前にアルミナBカラム(1×5cm)に通し、アルゴン気泡を5〜10分間通したDMF(8ml)に溶かした。酢酸カドミウム(85mg、4に対して10当量)を加え、反応混合物を110℃まで加熱した。反応の進行をスペクトルで監視した(アセトン中)。メタル化が5分以内に起こった。MnCl2・2H20(55mg、10当量)を、反応が完了するまで攪拌しながら加えた(さらに5〜10分以内)。無機塩を除去するために、反応溶液を蒸発させた;固形物をアセトニトリルに再度溶かし、溶液を、ブフナー漏斗上のワットマン紙を通して濾過し、蒸発させた。最後に、水に再度溶かした粗生成物のHPLCを(LC−900装置、JASCO、日本;カラムS10P−μm ODS−A 250×20mm、YMC、日本)、50%のアセトニトリル水溶液を移動相として用い、8ml/分の流速で行い、純粋な生成物9が10.5〜13.5分で溶出され、生成物のクロリン混合物及び副産物からの完全分離がもたらされた。収率:88%。
化合物9(15mg)を、スルホ−NHS(30mg)及びDCC(24mg)と共にDMSOに溶かし、反応混合物を室温、アルゴン雰囲気下で終夜攪拌し、蒸発させ、5mMのリン酸緩衝液、pH8.0(1.5ml)に再度溶かし、濾過した。DMSO(2.5ml)中の環状RGDfK(30mg)を濾液に加え、混合物をアルゴン雰囲気下で6時間攪拌し、蒸発させ、水(2ml)に再度溶かし、調製用C18カラムのHPLCで、水中のアセトニトリルの勾配溶出、10〜40%、15分間の間、流速7ml/分を用いて精製した。精製したコンジュゲート12を減圧下で乾燥させ、施用まで−20℃、アルゴン雰囲気下で保管した。
コンジュゲート14の合成
以下のようにして、メタレート化されていないコンジュゲート13の合成から開始して表題化合物を調製した。
上記材料及び方法に記載のように調製したBpheid(化合物3)(40mg)を、クロロホルム(5ml)中のNHS(80mg)及びDCC(60mg)を用いて、攪拌下、室温で終夜、活性化させた。得られた活性エステルを、クロロホルムを溶出液として用いたシリカカラムで精製し、その後、DMSO(5ml)中の環状RGDfK(40mg)と、攪拌下、アルゴン雰囲気下で終夜反応させた。その後、1Mのリン酸水素二カリウム(1.5ml、pHを8.2に調節)に溶かしたタウリン(50mg)を反応に加え、混合物を蒸発させ、推定上の化合物13がもたらされた。生成物を、以前に記載されているように(Brandis他、2005)5mMのリン酸緩衝液、pH8.0、及びメタノールの勾配溶出を用いた逆相のHPLCによって精製した。収率:52%。
実施例2で用いた手順を使用して、マンガンを化合物13内に挿入した。生成物のコンジュゲート14を、以前に記載されているように(Brandis他、2005)、アセトニトリル及び水の勾配溶出を用いたHPLCによって精製した。
コンジュゲート15の合成
酢酸銅(2mg)の水溶液を、水中のコンジュゲート13(3mg)(実施例3(i)で調製)及びアスコルビン酸ナトリウム(2mg)の混合物に加えた。反応を分光光度法によってすぐに監視した。銅を大環状分子内に挿入した後、生成物を、RP−18カートリッジ(Lichrolut、Merck)で、最初に未反応の酢酸銅及びアスコルビン酸塩を洗い流すために水を用いて、その後、主化合物のコンジュゲート15を溶出させるためにメタノールを用いて精製し、これを回収し、蒸発させた。収率:86%。
コンジュゲート17の合成
メタレート化されていないコンジュゲート16の調製から開始して表題化合物を調製した。
Bpheidの代わりにPheid(化合物6)を出発物質として用いて、コムジュゲート16を実施例3(i)のように調製した。
実施例3(ii)に記載の手順に従って、上記で得られたコンジュゲート16を出発物質として用いて、コンジュゲート17を合成した。
コンジュゲート18の合成
上記実施例5の手順に従って、化合物16を出発物質として用いて、表題化合物を合成した。
コンジュゲート19の合成
コンジュゲート19の調製を、本明細書中以降、スキーム2に模式図で説明する。
コンジュゲート21の合成
以下のようにして、コンジュゲート20の合成から開始して表題化合物を調製した。
メソ−テトラ(4−カルボキシフェニル)ポルフィン(20mg、25μmol)を、DMSO(6ml)中のスルホ−NHS(4mg、36μmol)及びEDC(6mg、30μmol)と混合し、室温で24時間攪拌した。その後、環状RGDfK(20mg、33μmol)を加え、反応混合物をさらに24時間攪拌し、その後、蒸発乾固し、水に再度溶かし、調製用C18カラムのHPLCで、0.2%の酢酸中のアセトニトリルの勾配溶出、30〜50%、15分間の間、流速6ml/分を用いて精製した。精製したコンジュゲート20を減圧下で乾燥させ、−20℃で保管した。
コンジュゲート20(4mg)を50%のメタノール水溶液に溶かし、酢酸銅(2mg)及びアスコルビン酸ナトリウム(2mg)の水溶液を加えた。反応は2分間で完了した(分光光度法によって監視した)。生成物を、RP−18カートリッジ(Lichrolut、Merck)で、最初に未反応の酢酸銅及びアスコルビン酸塩を洗い流すために水を用いて、その後、主化合物を溶出させるためにメタノールを用いて精製し、コンジュゲート21、これを回収し、蒸発させた(UV−VISスペクトル:水中で418及び538nm)。
コンジュゲート22の合成
上記実施例8(i)で得られたコンジュゲート20(4mg)及びガドリニウムアセチルアセトネート(10mg)を、既に記載されているように(Horrocks他、1978)、イミダゾール(0.3g)中、210℃で加熱した。反応は50分間で完了した(分光光度法によって監視した)。イミダゾールの昇華後、実施例8(i)に記載のように生成物を水に再度溶かし、HPLCで精製した。
コンジュゲート23の合成
化合物10の合成から開始してコンジュゲート23を調製した。
Pd−Bpheid a(化合物7)(100mg)をN−メチルピロリドン(1ml)及び3−アミノ−2−プロパンジオール(405mg)に溶かし、溶液を3時間、室温、アルゴン雰囲気下で混合した。生成物10を、0.2%の酢酸/アセトニトリルを用いたYMC−C18調製用カラムを使用したHPLCで精製した。収率:86%。分析は、酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで行った。ESI−MS、陽性モード、805m/z。
化合物10(50mg)、NHS(80mg)及びDCC(216mg)を乾燥N,N−ジメチルホルムアミド(8ml)に溶かした。溶液を90分間、室温、アルゴン雰囲気下で攪拌した。形成された活性エステルを、0.2%の酢酸/アセトニトリルを用いたYMC−C18調製用カラムを使用したHPLCで精製し、酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析し、質量分析によって同定した:ESI−MS、陽性モード、902m/z。
コンジュゲート24の合成
化合物8(100mg)を、DMF(5ml)中のNHS(70mg)及びN−シクロヘキシルカルボジイミド−N’−メチルポリスチレン(120mg)で活性化させた。溶液を50℃で15時間攪拌し、焼結ガラスを通して濾過した。環状RGDfK(100mg)を、N−メチルモルホリン(100μl)を含むDMF(5ml)に溶かし、濾液に加えた。混合物をアルゴン雰囲気下、室温で24時間攪拌し、溶媒を真空下で蒸発させ、生成物24を、酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18調製用カラムを使用したHPLCで精製した。収率:23%。同じ条件下のYMC−C18分析用カラムを用いたLC−MSで分析を行った。UV−VISスペクトル(HPLC):332、386、516、及び750nm。ESI−MS、陽性モード、1425m/z。
コンジュゲート26の合成
Fmoc脱保護したGRGDSP樹脂(0.35mmol)に、6mlのDMF中の化合物25(530mg、0.7mmol)、HOBt、PyBOP(どちらも0.7mmol)及びDIEA(2.1mmol)の混合物を加え、反応を2時間、アルゴン雰囲気下で動揺させた。DMF(10×5ml)及びDCM(5×5ml)で洗浄した後、樹脂を真空下で少なくとも3時間乾燥させた。その後、ペプチドコンジュゲートを樹脂から切断し、85:5:5:5のTFA/チオアニソール/H2O/トリイソプロピルシラン(TIS)(10ml)のカクテル溶液を10分間、0℃で、その後、1時間、室温、Ar雰囲気下で使用することによって、脱保護した(Arg、Pbf;Asp、OtBu)。樹脂を濾過し、カクテル溶液(4ml)で洗浄し、合わせた濾液をN2流によってその体積の約半分まで蒸発させた。冷Et20(30ml)を加えた後、暗色沈殿物が現れた。Et2O層の遠心分離及び傾瀉、並びに冷Et2O(2×30ml)でさらに処理することにより、粗暗色固形物が得られ、これをRP−HPLCによってさらに精製した(264mg;58%)。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1306m/z。
コンジュゲート28〜31の合成
以下のようにして、メタレート化されていないBpheid−環状RGDfKコンジュゲート27の合成から開始して表題化合物を調製した。
Fmoc−Cα−アリル保護したアスパラギン酸を塩化2−クロロトリチル樹脂上に付着させた。次に、Fmoc化学によってグリシン、NG−Pbfアルギニン、Nε−Ddeリシン、及びフェニルアラニンを樹脂上に付着させて、fKRGDペプチジル樹脂を形成した。その後、2%−ピペリジン/DMFを用いてN末端のFmoc基を除去し、アスパラギン酸残基上のCα−アリル基を、DCM中のテトラキス(トリフェニルホスフィン)パラジウム及び1,3−ジメチルバルビツール酸(DMBA)を用いて除去した。HOBt/PyBOP及びDIEAの存在下でペプチドを環化させた。4%−ヒドラジン/DMFを用いてリシン残基のε−アミンを切断した。
PyBOP/HOBt(0.6mmol)をカップリング剤として用い、DIEA(1.8mmol)を基材として用いて、Bpheid(3、0.6mmol)をDMF中のfKRGDペプチジル樹脂(0.3mmol)上のε−NH2−Lysと結合させて、コンジュゲート27が得られた。
コンジュゲート27(0.1mmol)を樹脂上で、DMF中の表1中の適切なアミン(5〜6mmol)で、室温で2時間処理した。その後、過剰のアミンを洗い流し、生成物を樹脂から切断し、TFA含有カクテルで脱保護し、最後にRP−HPLCによって精製した。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った。結果を表1に示す。
コンジュゲート32の合成
コンジュゲート32は、ペプチジルアミン環状RGDK−NH2(材料及び方法に記載のように得た)及びBpheid a(3)を、DMF溶液中、DCCの存在下でカップリングさせ、次いでTFAを用いてPbf及びO−tBuの脱保護を行うことによって得た。生成物をRP−HPLCによって精製した。収率:53%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1135m/z。
コンジュゲート33の合成
コンジュゲート33は、実施例11のコンジュゲート24について記載した方法と同様に、化合物8を直鎖状ペプチドGRGDSPK(材料及び方法に記載のように得た)とコンジュゲートさせることによって得た。収率:55%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1537m/z。
コンジュゲート34の合成
コンジュゲート34は、実施例11のコンジュゲート24について記載した方法と同様に、化合物8を直鎖状ペプチド(GRGDSP)4K(材料及び方法に記載のように得た)とコンジュゲートさせることによって得た。収率:41%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った。MALDI−MS、陽性モード、3291(M+2Na)m/z。
コンジュゲート35の合成
コンジュゲート35は、実施例11のコンジュゲート24について記載した方法と同様に、化合物8を環状RGDf−N(Me)K(材料及び方法に記載のように得た)とコンジュゲートさせることによって得た。収率:58%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1439m/z。
コンジュゲート36の合成
コンジュゲート36は、実施例11のコンジュゲート24について記載した方法と同様に、化合物8を環状二量体ペプチド(環状RGDyK)2(材料及び方法に記載のように得た)とコンジュゲートさせることによって得た。収率:27%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った。MALDI−MS、陽性モード、2245(M+2Na)m/z。
コンジュゲート37の合成
コンジュゲート37は、Pd−Bpheid(化合物7)及びペプチドRGDから合成した。ペプチドは、Fmoc−Arg(Pbf)−Gly−OHと樹脂に結合したH−Asp−O−アリル残基とのカップリングによる固相手順によって調製した。
100mlの乾燥DCM中のFmoc−Gly−OH(4.162g;14mmol)及びDIEA(9.755g;56mmol)の溶液を、10gの塩化2−クロロトリチル樹脂(1.4mmol/g)と共に1時間、室温(rt)で攪拌した。DMF/DCM(1:1)中の5%のピペリジン、次いでDMF中の20%のピペリジンで処理することによってFmoc基を除去した。その後、DMF(130ml)中のFmoc−Arg(Pbf)−OH(18.17g;28mmol)を、HOBt(4.29g;28mmol)及びDIC(4.34ml;28mmol)を用いて15分間、室温で活性化させ、反応器に加えた。混合物を2時間、室温で攪拌した。ペプチジル樹脂を洗浄し、真空下で3時間乾燥させた。AcOH/2,2,2−トリフルオロエタノール(TFE)/DCM(1:1:3)のカクテル溶液と共に1時間、室温で攪拌することによって、保護したジペプチドを樹脂から切断した。冷Et2O(1l)で処理した後、油性残渣が固化した。冷Et2Oで濾過及び洗浄することにより、白色沈殿物(8.64g;87.5%)が約99%の均一性(HPLC)で得られた。
上記ステップ(i)で得られたジペプチドへの第3のアミノ酸の付着は、塩化2−クロロトリチル樹脂(0.5g;1.4mmol/g)を、DCM中のFmoc−Asp−O−アリル(138.4mg;0.35mmol)及びDIEA(244μl;1.4mmol)溶液と共に、1時間、室温で攪拌して、約0.7mmol/gの開始量を得ることによって開始した。その後、樹脂を洗浄し、上述のようにFmocを除去した。Fmoc−Arg(Pbf)−Gly−OH(371mg;0.525mmol)、HOBt(80.4mg;0.525mmol)及びDIC(81μl;0.525mmol)を2.5mlのDMFに溶かし、室温で20分間攪拌した。生じた溶液を洗浄したH−Asp−O−アリル樹脂に加え、混合物を2時間、室温で動揺させた。ペプチジル樹脂を洗浄し、Fmocを除去した。
3mlのDMF中の化合物7(268mg;0.375mmol)、HOBT(57.4mg;0.375mmol)及びDIC(58μl;0.375mmol)の混合物を30分間、室温で攪拌し、上記(ii)で得られたFmoc−脱保護したトリペプチジル樹脂のアリコート(約0.125mmol)に加えた。混合物を2時間、室温で動揺させ、7と直鎖状トリペプチドRGDとのコンジュゲートが得られた。この反応及び修飾ペプチジル樹脂を用いた続く操作のすべては、アルゴン雰囲気中、暗所で行った。洗浄後、樹脂をDMF中のエチレンジアミン(251μl;375mmol)を用いて1時間、室温で処理し、その後、洗浄した。アリル保護基を除去するために、樹脂をDCM中の[(C6H5)3P]4Pd0(87mg;0.075mmol)及びDMBA(137mg;0.875mmol)の溶液と共に2時間、室温で反応させた。
コンジュゲート38の合成
合成は0.175mmolのスケールで、実施例19に記載した手順と同じ手順を用いて実施したが、Pd−Bpheid7の代わりに化合物Bpheid3から開始した。粗生成物(160mg)をRP−HPLCによって精製して、17mgの純粋な(98%)環状RGDコンジュゲート38が得られた。ESI−MS982(M+H)m/z。
コンジュゲート39の合成
手順は実施例19と同様であるが、Bpheid残基とAsp残基との間の「橋」形成にはエチレンジアミンの代わりに1,4−ビス(3−アミノプロピル)−ピペラジンを用いた。粗生成物(158mg)をRP−HPLCによって精製して、12.5mgの純粋な(99%)環状RGDコンジュゲート39が得られた。ESI−MS1122(M+H)m/z。
コンジュゲート40の合成
コンジュゲート40は、コンジュゲート24について記載した方法と類似の方法によって得たが、直鎖状RGDペプチド模倣体5−(6−グアニジノ−ヘキサノイルアミノ)−ペンタン酸(RGD−PM1)を用いた。収率:42%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1123m/z。
コンジュゲート41の合成
コンジュゲート41は、コンジュゲート24について記載した方法と類似の方法によって得たが、直鎖状RGDペプチド模倣体1−(4−グアニジノ−ブチリル)−ピペリジン−3−カルボニル]−アミノ]−ヘプタン酸(RGD−PM2)を用いた。収率:66%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1220m/z。
コンジュゲート42の合成
コンジュゲート42は、実施例11のコンジュゲート24について記載した方法と類似の方法によって得たが、ペプチド環状RADfKを用いた。収率:30%。酢酸アンモニウム、pH4.5/アセトニトリルを用いたYMC−C18分析用カラムを使用したLC−MSで分析を行った:ESI−MS、陽性モード、1439m/z。
コンジュゲート43の合成
実施例13に記載のように、バクテリオフェオホルビド−173−(環状RGDfK)アミドコンジュゲート27の合成から開始して表題化合物を調製した。
コンジュゲート44の合成
酢酸ナトリウムで緩衝した水溶液(0.1N、pH5.5)中の塩化ガドリニウム(0.1mmol)を、2mLのDMF中のコンジュゲート43(6μmol)の溶液に加えた。混合物を周囲温度で終夜、攪拌しながら置いた。金属キレートの形成をLC−MSによって確認した(1799m/z)。反応混合物を蒸発させ、生成物を、RP−18カートリッジ(Lichrolut、Merck)で、最初に未反応のガドリニウム塩を洗い流すために水を用いて、その後、主化合物のコンジュゲート44を溶出させるためにメタノールを用いて精製し、これを回収し、蒸発させた(8mg、73%)。
材料及び方法
(i)Euで標識したRGD−4C。RGD−4C(10μlのDDW中に20nmol)を、イソチオシアナトフェニル−DTPA−Eu(150nmol、50μl)を含む100μlのK−リン酸緩衝液(0.1M、pH8.5)に加えた。混合物を終夜、室温で、常に攪拌しながらインキュベーションした。反応を停止させるために、1μlのトリス−Cl(1M、pH7.5)を加え、混合物を5分間攪拌し、その後、Sep−Pak C−18カートリッジに載せ、遊離Euを溶出させるためにDDWで洗浄した。その後、カラムを50%のエタノール水溶液で洗浄し、画分(250〜500μl)を回収し、その蛍光を測定した。
(ii)細胞培養。マウス胚性心臓内皮細胞(H5V)の単層を、25mMのHEPES、pH7.4、10%のウシ胎児血清(FCS)、2mMのグルタミン、0.06mg/mlのペニシリン及び0.1mg/mlのストレプトマイシンを含むダルベッコ変法イーグル培地(DMEM)/F12中、37℃、8%のCO2で培養した。ヒト臍静脈内皮細胞(HUVEC)を、10mMのHEPES、pH7.4、20%の熱失活FCS(56℃、30分間)、2mMのグルタミン、50mg/mlのゲンタマイシン、25μg/mlの内皮細胞成長因子(ECGF)、5IU/mlのヘパリンを含むM199培地(グルタミン及びアール塩を含む)中、37℃、5%のCO2で維持した。H5V細胞は、マリオネグリ薬理学研究所(Instituto Mario Negri)、Milan、イタリアのAnnunciata Vecci博士からご提供いただいた。HUVEC細胞は、ランバム病院(Rambam Medical Center)、Haifa、イスラエルから入手した。
(viii)動物:雄CD1ヌードマウス(8週齢、約30g)を飼育し、食糧及び水を自由に摂取させるように、ワイツマン科学研究所(Weizmann Institute of Science)、Rehovot、イスラエルの研究機関内の動物の管理及び使用に関する委員会(Institutional Animal Care and Use Committee)の指針(1996)に従った動物施設内で取り扱った。
環状ペプチドRGD−4Cの結合パラメータ及び生物活性の評価
環状ノナペプチドRGD−4Cの結合パラメータ及び生物活性を、それが血管感光剤の標的化に適切であるかどうかを試験するために特徴づけた。
(i)Euで標識したRGD−4Cの調製。Euで標識したRGD−4Cを用いた時間分解発光分光分析を使用して内皮細胞上に発現されるαvβ3インテグリン受容体の結合パラメータ特徴(親和性、特異性及び受容体/細胞の数)を決定した。この目的で、材料及び方法に記載のようにイソチオシアナトフェニル−DTPA−Euを直接コンジュゲートさせることによって、RGD−4CをEuで標識した。Eu−RGD−4Cの遊離イソチオシアナトフェニル−DTPA−Euからの分離は、Sep−Pak C−18を用いて実施した。材料及び方法に記載のように、カラムを50%のエタノール水溶液で洗浄し、画分を回収し、その蛍光を測定した。100%のエタノールでさらに洗浄することでは、どのような顕著な量のEu含有物質もカラムに保持されていたことが示されなかった。最終生成物のEu−RGD−4Cは、単一ピークとして定量的に溶出され(図3A)、これは質量スペクトル分析によって確認した(1499m/z)(図3B)。
RGD−4C結合の生物学的効果を、材料及び方法に記載の細胞円形化アッセイを用いて、H5V細胞及びヒト臍静脈内皮細胞(HUVEC)において特徴づけた。光学顕微鏡観察を用いて細胞の形態学的変化を記録した。図7Bに見られるように、100μMの濃度のRGD−4Cにより、皿から99%のH5V内皮細胞の剥離(n=200)が誘発され、一方で、RGD−4Cが存在しない場合には5%の円形化細胞しか観察されなかった(図7A参照)。新鮮な培地を用いて3時間、再度インキュベーションした後に細胞が回復したので、この効果は可逆的であった(以前にRGD−4Cが存在していた場合の皿中に8%の円形化細胞と、RGD−4Cが存在しない場合の6%)。
in vitroでのコンジュゲート24の結合、細胞の取り込み及び局在化
RGD−BChlコンジュゲートの結合パターンは、その作用機構を理解するために非常に重要である。コンジュゲート24は検出可能なNIR蛍光を提示し、蛍光顕微鏡観察を用いてその細胞結合及び局在化をin vitroで決定した。培養したH5V内皮細胞を、25μMの24と共に、10%のFCSを含むDMEM/F12培地中で、2時間37℃でインキュベーションした。その後、細胞培養物を洗浄し、PBS++を加えた。カスタム作製した蛍光顕微鏡を用いて、24を520nmで励起させ、放出された蛍光を780nmで検出した。
コンジュゲート24及び化合物8のin vivo体内分布
本発明のコンジュゲートは、潜在的な薬物担体である。したがって、そのin vivo体内分布は重要である。標的組織中のコンジュゲートのレベルを定量化するために、イオン結合プラズマ質量分析(ICP−MS)を用いて標的器官中の中心M原子(例えば、Pd、Cu)を追跡した。中心金属原子の安定結合は、標的器官中の化合物の時間依存性の濃度を監視及び正確に決定することを可能にする。コンジュゲート24及び化合物8の体内分布を、材料及び方法に記載のように、試料調製の方法(2)を用いて、ラットC6神経膠腫の腫瘍異種移植を有するCD1−ヌード雄マウスにおいて決定した。マウスCT26luc結腸癌の腫瘍移植片を保有するCD1−ヌード雄マウス及び4T1luc乳腺癌のマウスの腫瘍移植片を保有するCD1−ヌード雄マウスにおいても、24の体内分布を決定した。
コンジュゲート15のin vivo体内分布
Cu−コンジュゲート15の体内分布を、6〜8週齢の、20〜23gの重さ且つ6〜9mm3の乳房組織から得たヒト腺癌細胞(MDA−MB−231細胞)の腫瘍を保有する雌CD−1ヌードマウスで決定した。コンジュゲート(5%のDMSO/PBS中の30mg/ml)を尾部静脈に注射し、選択した時点で動物を屠殺した。Cu濃度は、材料及び方法に記載のようにICP−MSによって決定した。時間0を減算した後のICP−MSの結果を図13に示す。
コンジュゲート42のin vivo体内分布
RGD/インテグリンの認識の実際の役割を評価するために、ペプチド中のグリシンをアラニンで置き換えたコンジュゲート42の体内分布を測定し、コンジュゲート24の体内分布と比較した。1つのアミノ酸のみを置換することが、インテグリンの認識を妨害することは、他者によって実証されている(Pierschbacher及びRuoslahti、1987)。主に、RAD又はRGEペプチドをこの目的で使用した。体内分布アッセイは、上記実施例26に記載のように、マウスCT26luc結腸癌細胞の腫瘍移植片を有するCD1ヌード雄マウスを用いて行い、Pd濃度は、ICP−MSによって決定した。ICP−MSの結果を図14Aに示す。
コンジュゲート24又は化合物8を用いた処置後の、ラットC6神経膠腫異種移植を保有するマウスのin vivo蛍光イメージング
動的蛍光イメージを、ラットC6神経膠腫異種移植を保有するCD−1ヌード雄マウスから得た。蛍光イメージは、材料及び方法に記載のようにIVISシステムを用いて得た。注射した感光剤(化合物8又はコンジュゲート24)のクリアランスは、蛍光イメージングによってマウスで測定し、図15に実証した。右後肢の後側にラットC6神経膠腫異種移植を保有するマウスに、200nmol用量のコンジュゲート8(上の画像のマウス)又は200nmol用量の24(下の画像のマウス)を注射し、画像は注射後4、24、48及び72時間に撮影した。
コンジュゲート24を用いた処置後の、ルシフェラーゼで形質移入したマウスCT26luc結腸癌移植片を保有するマウスの動的蛍光イメージング
ルシフェラーゼで形質移入した細胞系は、生きている場合はルシフェリンの存在下で可視光を生じる。ルシフェリン発光により、生腫瘍細胞を監視することが可能となり、したがって、コンジュゲートの腫瘍部位でのホーミング、そのイメージング能力及びVTPの有効性を確証する手段が提供される。
コンジュゲート24を用いた処置後の、ルシフェラーゼで形質移入した4T1luc乳腺癌移植片を保有するマウスの動的蛍光イメージング
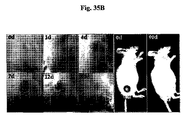
動的蛍光イメージを、ルシフェラーゼで形質移入したマウス4T1luc乳腺癌の移植片を保有するBALB/c雌マウスから、インテグリン受容体標的化コンジュゲート24を静脈内注射した後に得た。図17A〜17Cは、右後肢の後側にルシフェラーゼで形質移入した皮下のマウス4T1乳腺癌の移植片を保有する2匹の雌マウスの、200nmol用量のコンジュゲート24を注射した24時間後の蛍光及び発光イメージの写真を示す。蛍光及び発光イメージは、材料及び方法に記載のようにIVISシステムを用いて得た。
コンジュゲート26を用いた処置後の、子宮癌(MLS)を保有するマウスの動的蛍光
コンジュゲート26(8mg/kg)を、MLS子宮癌を保有する動物に静脈内注射した。8及び14時間後にIVISの画像を撮影した。図18に示すように、コンジュゲートは8時間後には蓄積を示さなかったが、14時間では高レベルの蛍光が腫瘍及び肝臓の領域中で観察された。
コンジュゲート24とαvβ3インテグリン受容体とのin vivo結合特異性の蛍光イメージングによる実証
特異的結合とは、コンジュゲートしていない増感剤によって阻害されるものと定義される。したがって、コンジュゲート24のin vivo結合特異性を実証するために、同じ結合部位の結合に対して遊離環状RGDfKと競合させることによって、その蓄積を遮断する試みを実施した。140nmolのコンジュゲート24を単独で投与した(図19、両パネルの左側のマウス、右後肢の後側に腫瘍を有する)、又はC6神経膠腫異種移植を保有するマウスに過剰の「遊離」(8.5μmol)環状RGDfKペプチドを注射した1時間後に140nmolのコンジュゲート24を投与した(図19、両パネルの右側のマウス、左後肢の後側に腫瘍を有する)24時間に蛍光イメージングを行った。同じ曝露時間の遮断した受容体異種移植の蛍光イメージを、図19に、定性的な比較を可能にするために同じ均等カラースケールで例示する。腫瘍に由来する蛍光強度は、コンジュゲート24を単独で投与した場合に、イメージング剤を投与する1時間前にペプチド環状RGDfKを投与した場合よりも高かった。正常組織では、取り込みは環状RGDfKを事前に投与することによって影響を受けなかった。
コンジュゲート42を用いた処置後の動的蛍光イメージング
RGD/インテグリンのin vivoの認識の実際の役割を評価するために、動的蛍光イメージを、後肢の後側にCT26luc移植片を保有するCD−1ヌード雄マウスから、コンジュゲート24(図20、それぞれのパネルの左側のマウス)又はペプチド中のグリシンをアラニンで置き換えたコンジュゲート42(環状RADfK);それぞれのパネルの右側のマウス)を投与した24時間後に得た。腫瘍組織におけるRGDコンジュゲートの蛍光シグナルは注射の3.5〜4時間後に最大に達するので、画像は注射の4時間後に撮影した。重要なことに、非特異的結合により、どちらのコンジュゲートも投与後に持続した基底レベルの蛍光を示した。しかし、腫瘍部位中のRGDコンジュゲートの蛍光強度はRADコンジュゲートよりも明らかに高かった。これらの結果は、腫瘍組織中にほぼ2倍のRGDコンジュゲートの蓄積を示すICP−MS測定によって、定量的に支持されている(上記実施例30及び図14A参照)。
肺転移の動的蛍光イメージング
肺の乳癌転移の4T1lucモデルの検出は、コンジュゲート24によって、BALB/c雌マウスに注射した注射の24時間後(15mg/kg)に可能となった(図22)。これらの結果は、肺の転移領域中の24の取り込みを、蛍光によって比較的高い精度で監視できることを示している。
リンパ節転移の動的蛍光イメージング
その左脚の後側にCT26luc原発腫瘍を保有し、近傍のリンパ節に転移を有するCD−1ヌード雄マウスの画像をとり、コンジュゲート24(15mg/kg)を静脈内注射した24時間後に写真撮影した。リンパ節中のCT26luc転移の検出は、コンジュゲート24の局在化によって可能となった。白黒写真、ルシフェルンとルシフェラーゼで形質移入した腫瘍細胞との反応に由来する生物発光シグナル、及びマウスの蛍光イメージを図24に示す。
化合物9を造影剤として用いた、ラットC6神経膠腫異種移植を保有するマウスのin vivo磁気共鳴画像法(MRI)
測定は、C6神経膠腫異種移植(直径10〜15mm;左脇、皮下)を保有するCD1ヌード雄マウス(平均重量約30g)で行った。7匹のマウスを、Mn−132−OH−Bpheid(化合物9)(15μmol/kg)で増強したMRIに使用した。
in vitroの標的化した光毒性
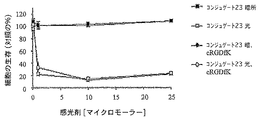
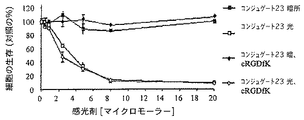
RGDペプチド−感光剤のコンジュゲート対コンジュゲートしていない感光剤の光線力学的力価を評価するために、コンジュゲート23及びコンジュゲートしていない感光剤10の光毒性を、培養したH5V内皮細胞のPDT後の生存を監視することによって決定した。
コンジュゲート24を用いたラットC6神経膠腫腫瘍のin vivoPDT
上記結果に基づいて、本発明者らは、コンジュゲート24を用いた固形腫瘍のPDTの新しい処置プロトコルを開発した。プロトコルのパラメータは、処置時間(薬物−光の間隔)−薬物を投与した3〜24時間後に照射;用量(mg/kg)−5〜24mg/kg;照射時間(分間)−5〜30分間;照射強度(mW/cm2)−100〜200mW/cm2;送達エネルギー(J/cm2)−30〜360J/cm2を含むべきである。
コンジュゲート24を用いたマウスCT26結腸腫瘍のin vivoPDT
ラットC6神経膠腫モデルを用いては、VTPの結果の即座の評価を得ることができず、これは、スクリーニングプロセスの過程の主要な不利点である。この問題に打ち勝つために、本発明者らは、ルシフェラーゼで形質移入した細胞からなるマウスCT26luc結腸癌モデルを用い、これは、治療効果の素早い評価を可能にする。
コンジュゲート13を用いた乳房腫瘍の腫瘍診断及びPDT処置
以下のようにして、ヒト乳癌MDA−MB−231細胞(ATCC)を赤色蛍光タンパク質(RFP)で形質移入した。
Claims (159)
- RGD含有ペプチド又はRGDペプチド模倣体とポルフィリン、クロロフィル又はバクテリオクロロフィルから選択される感光剤とのコンジュゲートであって、感光剤が、10、15、20位のそれぞれで4−メチルフェニル又はアセチル化グルコシルオキシフェニルによって、5位でスペーサーアームを介してポルフィリン大環状分子と連結した直鎖状RGD含有ペプチドの残基によって置換されている、メタレート化されていないポルフィリンであるコンジュゲートを除外したコンジュゲート。
- 感光剤が以下の式のテトラアリールポルフィリンである、請求項1に記載のコンジュゲート:
[式中、
Ar1、Ar2、Ar3、及びAr4は、同一又は異なり、それぞれ、炭素環アリール、ヘテロアリール及び混合カルボアリール−ヘテロアリール基から選択されるアリール基であり、アリール基のそれぞれは、未置換であるか、又は、ハロゲン原子、アリールがフェニルの場合はC2〜C8アルキル、アリールがヘテロアリール若しくは混合カルボアリール−ヘテロアリールの場合はC1〜C8アルキル、C1〜C8アルコキシ、カルボキシ、C1〜C8アルキルアミノ、アミノ−(C1〜C8)アルキルアミノ、トリ−(C1〜C8)アルキルアンモニウム、ヒドロキシ、及びCONH2から選択される1つ若しくは複数の置換基によって置換されており、Ar1、Ar2、Ar3、及びAr4のうちの少なくとも1つは、その置換基のうちの1つ又は架橋基を介して前記少なくとも1つのアリール基と連結したRGD含有ペプチド又はRGDペプチド模倣体によって置換されており;
nは、置換基が中性の場合は0であるか、又は、nは1〜4の整数であり;
Xは、アリール基が正荷電の場合は製薬上許容される陰イオンであるか、又は、アリール基が負荷電の場合は製薬上許容される陽イオンであり;
Mは、2Hであるか、又は、Mg、Pd、Pt、Co、Ni、Sn、Cu、Zn、Mn、In、Eu、Fe、Au、Al、Gd、Er、Yb、Lu、Ga、Y、Rh、Ru、Si、Ge、Cr、Mo、P、Re、Tl及びTc並びにその同位体からなる群から選択される原子である]。 - 炭素環アリール基が、それ自体で又は混合カルボアリール−ヘテロアリール基の一部として、置換された又は未置換の単環又は二環状芳香族基であり、前記ヘテロアリール基が、それ自体で又は混合カルボアリール−ヘテロアリール基の一部として、O、S及びNからなる群から選択される1〜3個のヘテロ原子を含む、置換された又は未置換の5〜6員の芳香環である、請求項2に記載のコンジュゲート。
- 前記炭素環アリール基が、フェニル、ビフェニル及びナフチルからなる群から選択され、前記ヘテロアリール基が、フリル、チエニル、ピロリル、イミダゾリル、チアゾリル、ピリジル、ピリミジル、及びトリアジニルからなる群から選択される、請求項3に記載のコンジュゲート。
- 炭素環アリール及び/又はヘテロアリール基のうちの1〜3個が、1つ又は複数のカルボキシ、C1〜C8アルキルアミノ、アミノ−(C1〜C8)アルキルアミノ、ヒドロキシ、又はCONH2基によって置換されている、請求項3又は4に記載のコンジュゲート。
- Mが、2Hであるか、又は、Pd、Cu、Mn及びGdから選択される金属である、請求項2に記載のコンジュゲート。
- RGD含有ペプチドがすべてL、すべてD又はL,Dの直鎖状又は環状ペプチドであり、アミノ酸が天然又は非天然のアミノ酸であり得る、請求項2に記載のコンジュゲート。
- RGD含有ペプチドが環状ペプチドである、請求項7に記載のコンジュゲート。
- 環状ペプチドが、−CO−NH−基を介してポルフィリン部分の少なくとも1つのアリール基と連結している、請求項8に記載のコンジュゲート。
- 前記環状ペプチドがペンタペプチドの環状RGDfK(配列番号1)である、請求項8又は9に記載のコンジュゲート。
- 前記環状ペプチドがノナペプチドRGD−4C(配列番号2)である、請求項8又は9に記載のコンジュゲート。
- (i)メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシフェニル)ポルフィン(20);(ii)銅(II)メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシ−フェニル)ポルフィン(21);及び(iii)ガドリニウム(III)メソ−5−(4−環状RGDfK−ベンズアミド)−10,15,20−トリス(4−カルボキシフェニル)ポルフィン(22)から選択される、請求項10に記載のコンジュゲート。
- 感光剤が、式I、II又はIIIのクロロフィル又はバクテリオクロロフィル、並びにその製薬上許容される塩及び光学異性体:
[式中、
Mは、2H、又はMg、Pd、Pt、Co、Ni、Sn、Cu、Zn、Mn、In、Eu、Fe、Au、Al、Gd、Er、Yb、Lu、Ga、Y、Rh、Ru、Si、Ge、Cr、Mo、P、Re及びTc、Tl並びにその同位体からなる群から選択される原子を表し;
Xは、O又はN−R7であり;
R1、R’2及びR6は、それぞれ独立して、Y−R8、−NR9R’9若しくは−N+R9R’9R”9A−であるか;又は、R1及びR6は、一緒になって、RGDペプチド又はRGDペプチド模倣体残基を含む環を形成し;
Yは、O又はSであり;
R2は、H、OH又はCOOR9であり;
R3は、H、OH、C1〜C12アルキル又はC1〜C12アルコキシであり;
R4は、−CH=CR9R’9、−CH=CR9Hal、−CH=CH−CH2−NR9R’9、−CH=CH−CH2−N+R9R’9R”9A−、−CHO、−CH=NR9、−CH=N+R9R’9A−、−CH2−OR9、−CH2−SR9、−CH2−Hal、−CH2−R9、−CH2−NR9R’9、−CH2−N+R9R’9R”9A−、−CH2−CH2R9、−CH2−CH2Hal、−CH2−CH2OR9、−CH2−CH2SR9、−CH2−CH2−NR9R’9、−CH2−CH2−N+R9R’9R”9A−、−COCH3、C(CH3)=CR9R’9、−C(CH3)=CR9Hal、−C(CH3)=NR9、−CH(CH3)=N+R9R’9A−、−CH(CH3)−Hal、−CH(CH3)−OR9、−CH(CH3)−SR9、−CH(CH3)−NR9R’9、−CH(CH3)−N+R9R’9 R’9A−、又は−C≡CR9であり;
R’4は、メチル又はホルミルであり;
R5は、=O、=S、=N−R9、=N+R9R’9A−、=CR9R’9、又は=CR9−Halであり;
R7、R8、R9、R’9及びR”9は、それぞれ独立して:
(a)H;
(b)C1〜C25ヒドロカルビル;
(c)ハロゲン、ニトロ、オキソ、OR、SR、エポキシ、エピチオ、−NRR’、−CONRR’、−CONR−NRR’、−NHCONRR’、−NHCONRNRR’、−COR、COOR”、−OSO3R、−SO3R”、−SO2R、−NHSO2R、−SO2NRR’、=N−OR、−(CH2)n−CO−NRR’、−O−(CH2)n−OR、−O−(CH2)n−O−(CH2)n−R、−OPO3RR’、−PO2HR、及び−PO3R”R”からなる群から選択される1つ又は複数の官能基によって置換されたC1〜C25ヒドロカルビル(式中、R及びR’は、それぞれ独立して、H、ヒドロカルビル若しくはヘテロシクリルであり、R’はさらに、RGDペプチド若しくはRGDペプチド模倣体の残基であってよいか、又は、R及びR’は、それらが付着しているN原子と一緒になって、O、S及びNから選択されるさらなるヘテロ原子を任意選択で含む5〜7員の飽和環を形成し、さらなるN原子は置換されていてもよく、R”は、H、陽イオン、ヒドロカルビル又はヘテロシクリルである);
(d)正荷電基、負荷電基、生理的条件下で正荷電基に変換される塩基性基、及び生理的条件下で負荷電基に変換される酸性基からなる群から選択される1つ又は複数の官能基によって置換されたC1〜C25ヒドロカルビル;
(e)1つ若しくは複数のヘテロ原子及び/又は1つ若しくは複数の炭素環若しくはヘテロ環部分を含むC1〜C25ヒドロカルビル;
(f)1つ若しくは複数のヘテロ原子及び/又は1つ若しくは複数の炭素環若しくはヘテロ環部分を含み、上記(c)及び(d)で定義した1つ又は複数の官能基によって置換されたC1〜C25ヒドロカルビル;
(g)アミノ酸残基、ペプチド、タンパク質、単糖、オリゴ糖、多糖、又は多座配位子及び金属とのそのキレート錯体によって置換されたC1〜C25ヒドロカルビル;或いは
(h)アミノ酸残基、ペプチド、タンパク質、単糖、オリゴ糖、多糖;又は多座配位子及び金属とのそのキレート錯体であり;
R7はさらに、−NRR’であってよく、R及びR’は、それぞれ、H、又は負荷電基、好ましくはSO3 −によって任意選択で置換されたC1〜C25ヒドロカルビルであり;
R8はさらに、H+、又はR1、R’2及びR6がそれぞれ独立してY−R8である場合は陽イオンR+ 10であってよく;
R+ 10は、金属、アンモニウム基又は有機陽イオンであり;
A−は、生理的に許容される陰イオンであり;
mが0又は1であり;
7〜8位の点線は、任意選択の二重結合を表す]であり、前記式I、II又はIIIのクロロフィル又はバクテリオクロロフィル誘導体が少なくとも1つのRGD含有ペプチド又はRGDペプチド模倣体の残基を含む、請求項1に記載のコンジュゲート。 - C1〜C25ヒドロカルビルのうちいずれかがC1〜C25アルキル、アルケニル又はアルキニルである、請求項13に記載のコンジュゲート。
- アルキルがC1〜C10アルキルである、請求項14に記載のコンジュゲート。
- アルキルがC2〜C3アルキルである、請求項15に記載のコンジュゲート。
- 7〜8位の点線が二重結合を表し、感光剤が式I、II又はIIIのクロロフィルである、請求項13に記載のコンジュゲート。
- 7〜8位の点線が存在せず、感光剤が式I、II又はIIIのバクテリオクロロフィルである、請求項13に記載のコンジュゲート。
- それぞれのR4が、独立して、アセチル、ビニル、エチル、若しくは1−ヒドロキシエチル基、又は前記1−ヒドロキシエチル基のエーテル若しくはエステルである、請求項12に記載のコンジュゲート。
- 感光剤が式I又はIIのバクテリオクロロフィルであり、3位のR4がアセチルであり、8位のR4がエチルであり、R’4がメチルであり、7〜8位が水素化されている、請求項13に記載のコンジュゲート。
- 感光剤が式I又はIIのクロロフィルであり、3位のR4がビニルであり、8位のR4がエチルであり、R’4がメチルであり、7〜8位に二重結合が存在する、請求項13に記載のコンジュゲート。
- 前記式I、II又はIIIのクロロフィル又はバクテリオクロロフィルが、COO−、COS−、SO3 −、若しくはPO3 2−から選択される少なくとも1つの負荷電基、又はCOOH、COSH、SO3H、若しくはPO3H2から選択される、生理的pHで負荷電基に変換される少なくとも1つの酸性基、又はその塩を含む、請求項13に記載のコンジュゲート。
- 前記クロロフィル又はバクテリオクロロフィルが式IIのものであり、R6が−NR9R’9であり、R9がHであり、R’9がSO3H又はそのアルカリ塩によって置換されたC1〜C10アルキルである、請求項22に記載のコンジュゲート。
- R6が−NH−(CH2)2−SO3K又は−NH−(CH2)3−SO3Kである、請求項23に記載のコンジュゲート。
- 前記式I、II又はIIIのクロロフィル又はバクテリオクロロフィルが少なくとも1つの正荷電基を含む、請求項13に記載のコンジュゲート。
- 前記正荷電基が、−N+(RR’R”)、−(R)N−N+(RR’R”)、O←N+(RR’)−、>C=N+(RR’)、−C(=NR)−N+RR’R”及び−(R)N−C(=NR)−N+RR’R”基から選択されるN含有基に由来する陽イオンであり、R、R’及びR”が、それぞれ独立して、H、ヒドロカルビル若しくはヘテロシクリルであるか、又は、R、R’及びR”のうちの2つが、それらが付着しているN原子と一緒になって、O、S若しくはNから選択される1つ若しくは複数のヘテロ原子を任意選択で含み、且つ追加のN原子でさらに任意選択で置換されている3〜7員の飽和環を形成する、請求項25に記載のコンジュゲート。
- 前記陽イオンが末端基又はアルキル鎖内に位置する基である、請求項26に記載のコンジュゲート。
- 前記陽イオンが式−N+(RR’R”)のアンモニウム基であり、R、R’及びR”のそれぞれが、独立して、H、ヒドロカルビル若しくはヘテロシクリルであるか、又は、R、R’及びR”のうちの2つが、N原子と一緒になって、O、S若しくはN原子を任意選択で含み、且つ追加のN原子でさらに任意選択で置換されている3〜7員の飽和環を形成する、請求項26に記載のコンジュゲート。
- 前記3〜7員の飽和環が、追加のN原子でハロ、ヒドロキシル若しくはアミノによって任意選択で置換されたC1〜C6アルキルによって任意選択で置換されたアジリジン、ピロリジン、ピペリジン、モルホリン、チオモルホリン、アゼピン又はピペラジンからなる群から選択される、請求項28に記載のコンジュゲート。
- 前記正荷電基が、1つ又は複数のN原子及び任意選択でO又はS原子を含む芳香族ヘテロ環化合物に由来する陽イオンである、請求項25に記載のコンジュゲート。
- 前記陽イオンが、ピラゾリウム、イミダゾリウム、オキサゾリウム、チアゾリウム、ピリジニウム、キノリニウム、イソキノリニウム、ピリミジニウム、1,2,4−トリアジニウム、1,3,5−トリアジニウム及びプリニウムから選択される、請求項30に記載のコンジュゲート。
- 前記少なくとも1つの正荷電基が、−O+(RR’)、−S+(RR’)、−Se+(RR’)、−Te+(RR’)、−P+(RR’R”)、−As+(RR’R”)、−Sb+(RR’R”)、及び−Bi+(RR’R”)からなる群から選択されるオニウム基であり、R、R’及びR”が、それぞれ独立して、H、ヒドロカルビル又はヘテロシクリルである、請求項25に記載のコンジュゲート。
- 生理的条件下で正荷電基に変換される少なくとも1つの塩基性基を含む、請求項13に記載のコンジュゲート。
- 前記塩基性基が末端基又はアルキル鎖内に位置する基である、請求項33に記載のコンジュゲート。
- 前記少なくとも1つの塩基性基が、−NRR’、−C(=NR)−NR’R”、−NR−NR’R”、−(R)N−C(=NR)−NR’R”、O←NR−、又は>C=NRであり、R、R’及びR”のそれぞれが、独立して、H、任意選択で置換されたヒドロカルビル若しくはヘテロシクリルであるか、又は、R、R’及びR”のうちの2つが、N原子と一緒になって、O、S若しくはN原子を任意選択で含み、且つ追加のN原子でさらに任意選択で置換されている3〜7員の飽和環を形成する、或いは、塩基性基がN含有芳香族ヘテロ環基である、請求項33に記載のコンジュゲート。
- 前記3〜7員の飽和環が、追加のN原子でハロ、ヒドロキシル若しくはアミノによって任意選択で置換されたC1〜C6アルキルによって任意選択で置換された、アジリジン、ピロリジン、ピペリジン、モルホリン、チオモルホリン、アゼピン又はピペラジンから選択され、前記N含有芳香族ヘテロ環基が、ピラゾリル、イミダゾリル、オキサゾリル、チアゾリル、ピリジル、キノリニル、イソキノリニル、ピリミジル、1,2,4−トリアジニル、1,3,5−トリアジニル又はプリニルである、請求項35に記載のコンジュゲート。
- 感光剤が式IIのクロロフィル又はバクテリオクロロフィルであり、R6が塩基性基−NR9R’9であり、R9がHであり、R’9が塩基性基−NH−(CH2)2〜6−NRR’によって置換されたC1〜C6アルキルであり、R及びR’のそれぞれが、独立して、H、NH2によって任意選択で置換されたC1〜C6アルキルであるか、又は、R及びR’が、N原子と一緒になってO若しくはN原子を任意選択で含み、且つ追加のN原子でさらに−(CH2)2〜6−NH2によって任意選択で置換されている、5〜6員の飽和環を形成する、請求項35に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、R6が−NH−(CH2)3−NH−(CH2)3−NH2、−NH−(CH2)2−1−モルホリノ、又は−NH−(CH2)3−ピペラジノ−(CH2)3−NH2である、請求項37に記載のコンジュゲート。
- 感光剤が式IIのクロロフィル又はバクテリオクロロフィルであり、R1及びR6が、一緒になって、RGDペプチド若しくはRGDペプチド模倣体を含む環を形成するである、請求項13に記載のコンジュゲート。
- 感光剤が式IIIのクロロフィル又はバクテリオクロロフィルであり、Xが−NR7であり、R7が−NRR’であり、RがHであり、R’が、SO3−によって置換されたC2〜6−アルキル又はそのアルカリ塩である、請求項13に記載のコンジュゲート。
- 感光剤が式IIIのバクテリオクロロフィルであり、Xが−NR7であり、R7が−NH−(CH2)3−SO3Kである、請求項40に記載のコンジュゲート。
- R7、R8、R9又はR’9が、それぞれ、1つ又は複数の−OH基によって置換されたC1〜6−アルキルである、請求項13に記載のコンジュゲート。
- 感光剤が式IIのクロロフィル又はバクテリオクロロフィルであり、R6が−NR9R’9であり、R9がHであり、R’9がHOCH2−CH(OH)−CH2−である、請求項42に記載のコンジュゲート。
- 感光剤が式IIのクロロフィル又はバクテリオクロロフィルであり、R6が−NR9R’9であり、R9がHであり、R’9が、多座配位子又は金属とのそのキレート錯体によって置換されたC1〜6−アルキルである、請求項13に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、前記多座配位子がEDTA、DTPA又はDOTAであり、R6が−NR9R’9であり、R9がHであり、R’9が、多座配位子又は金属とのそのキレート錯体によって置換されたC1〜6−アルキルである、請求項44に記載のコンジュゲート。
- R6が−NH−(CH2)3−NH−DTPAである、請求項45に記載のコンジュゲート。
- DTPAがGdとキレート化している、請求項46に記載のコンジュゲート。
- Mが、2Hであるか、又は、Pd、Mn、若しくはCuから選択される金属である、請求項13に記載のコンジュゲート。
- 感光剤が式I、II又はIIIのバクテリオクロロフィルである、請求項48に記載のコンジュゲート。
- 感光剤が式Iのバクテリオクロロフィルであり、MがPdである、請求項49に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdである、請求項49に記載のコンジュゲート。
- 感光剤が式IIIのバクテリオクロロフィルであり、MがPdである、請求項49に記載のコンジュゲート。
- 感光剤が式I、II又はIIIのクロロフィルである、請求項49に記載のコンジュゲート。
- 感光剤が式IIのクロロフィルであり、Mが2H、Cu又はMnである、請求項49に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPd、Mn、Cu又は2Hであり;mが0であり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3 −Me+であり、Me+がNa+又はK+である、請求項13に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPd又は2Hであり;mが0であり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−CH2−CH(OH)−CH2−OHである、請求項13に記載のコンジュゲート。
- 感光剤が式IIIのバクテリオクロロフィルであり、MがPdであり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;XがN−R7であり、R7が−NH−(CH2)3−SO3 −Me+であり、Me+がNa+又はK+である、請求項13に記載のコンジュゲート。
- 感光剤が式Iのバクテリオクロロフィルであり、MがMnであり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R2がOHであり;R3がCOOCH3であり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R5がOである、請求項13に記載のコンジュゲート。
- 感光剤が式IIのクロロフィルであり、MがMn、Cu又は2Hから選択され;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R4が、3位ではビニルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3 −Me+であり、Me+がNa+又はK+である、請求項13に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)3−NH−(CH2)3−NH2である、請求項13に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−モルホリノである、請求項13に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが、NH−に直接又はスペーサーを介して連結しているRGD含有ペプチド又はRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)3−ピペラジノ−(CH2)3−NH2である、請求項13に記載のコンジュゲート。
- RGD含有ペプチドがすべてL、すべてD又はL,Dの直鎖状又は環状ペプチドである、請求項13に記載のコンジュゲート。
- RGD含有ペプチドが4〜100、好ましくは5〜50、5〜30、5〜20、より好ましくは5〜10個のアミノ酸残基からなる、請求項63に記載のコンジュゲート。
- RGD含有ペプチドが4、5、6、7、9又は25個のアミノ酸残基からなる、請求項64に記載のコンジュゲート。
- RGD含有ペプチドが5個のアミノ酸残基からなる、請求項65に記載のコンジュゲート。
- アミノ酸が天然アミノ酸である、請求項63から66までのいずれか一項に記載のコンジュゲート。
- 天然アミノ酸がAla、Arg、Asp、Cys、Gln、Glu、Gly、Ile、Leu、Lys、Met、Phe、Pro、Ser、Thr、Tyr、及びValから選択される、67に記載のコンジュゲート。
- 天然アミノ酸が修飾されている、請求項67に記載のコンジュゲート。
- 修飾が、D−修飾、ペプチド結合のN−アルキル化、Lysのアミノ末端基又は遊離アミノ基のアシル化又はアルキル化、Asp又はGluのカルボキシ末端基又は遊離カルボキシ基のエステル化又はアミド化、及びSer又はTyrのヒドロキシル基のエステル化又はエーテル化を含む、請求項69に記載のコンジュゲート。
- 修飾がN−メチル化である、請求項70に記載のコンジュゲート。
- 修飾がD−修飾である、請求項70に記載のコンジュゲート。
- RGD含有ペプチドが非天然アミノ酸を含む、請求項63から66までのいずれか一項に記載のコンジュゲート。
- 非天然アミノ酸が、4−アミノ酪酸(Abu)、2−アミノアジピン酸、ジアミノプロピオン酸(Dap)、ヒドロキシリシン、ホモセリン、ホモバリン、ホモロイシン、ノルロイシン(Nle)、ノルバリン(Nva)、オルニチン(Orn)、及びナフチルアラニン(Nal)から選択される、請求項73に記載のコンジュゲート。
- RGD含有ペプチドが環状である、請求項63から65までのいずれか一項に記載のコンジュゲート。
- 前記環状ペプチドがペンタペプチドの環状RGDfK(配列番号1)であり、fがD−Pheを示す、請求項75に記載のコンジュゲート。
- 前記環状ペプチドが本明細書中でRGD−4C(配列番号2)と命名したノナペプチドである、請求項75に記載のコンジュゲート。
- 前記環状ペプチドがテトラペプチドの環状RGDK(配列番号4)である、請求項75に記載のコンジュゲート。
- 前記環状ペプチドがペンタペプチドの環状RGDf−n(Me)K(配列番号7)であり、fがD−Pheを示す、請求項75に記載のコンジュゲート。
- 前記環状ペプチドがペンタペプチドの環状RGDyK(配列番号8)であり、yがD−Tyrを示す、請求項75に記載のコンジュゲート。
- RGD含有ペプチドが直鎖状である、請求項63から66までのいずれか一項に記載のコンジュゲート。
- 前記直鎖状ペプチドがヘキサペプチドのGRGDSP(配列番号3)である、請求項81に記載のコンジュゲート。
- 前記直鎖状ペプチドがヘプタペプチドのGRGDSPK(配列番号5)である、請求項81に記載のコンジュゲート。
- 前記直鎖状ペプチドが配列(GRGDSP)4K(配列番号7)を有する、請求項81に記載のコンジュゲート。
- RGDペプチド模倣体を含む、請求項13に記載のコンジュゲート。
- 前記RGDペプチド模倣体が、11個の原子の鎖によって間隔が空いたグアニジン及びカルボキシル末端基を含む非ペプチド化合物であり、前記原子のうちの少なくとも5個が炭素原子であり、前記鎖が1つ又は複数のO、S又はN原子を含み、オキソ、チオキソ、ハロゲン、アミノ、C1〜C6アルキル、ヒドロキシル、若しくはカルボキシによって任意選択で置換され得るか、又は、前記鎖の1つ若しくは複数の原子が3〜6員の炭素環若しくはヘテロ環を形成し得る、請求項85に記載のコンジュゲート。
- 前記RGDペプチド模倣体が鎖中にN原子を含み、オキソ基によって置換されている、請求項86に記載のコンジュゲート。
- 前記RGDペプチド模倣体が以下の式を有する、請求項86に記載のコンジュゲート:
H2N−C(=NH)NH−(CH2)5−CO−NH−CH(CH2)−(CH2)2−COOH。 - 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、PがRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項88に記載のコンジュゲート(コンジュゲート40)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、PがRGDペプチド模倣体の残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項86に記載のコンジュゲート(コンジュゲート41)。
- R1及びR6が、一緒になって、−NH−RGD−CO−NH−(CH2)2−NH−又は−NH−RGD−CO−NH−(CH2)2−ピペラジノ−(CH2)2−NH−を含む環を形成する、請求項39に記載のコンジュゲート。
- 感光剤が式IIのバクテリオクロロフィルであり、mが0であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R1及びR6が、一緒になって、−NH−RGD−CO−NH−(CH2)2−NH−を含む環を形成し、且つMがPdであるか(コンジュゲート37)、若しくはMが2Hであり(コンジュゲート38)であるか、又は、R1及びR6が、一緒になって、−NH−RGD−CO−NH−(CH2)2−ピペラジノ−(CH2)2−NH−を含む環を形成し、且つMがPdである(コンジュゲート39)、請求項91に記載のコンジュゲート。
- 感光剤が式IIのクロロフィルであり、Mが2Hであり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R4が、3位ではビニルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項59に記載のコンジュゲート(コンジュゲート16)。
- 感光剤が式IIのクロロフィルであり、MがMnであり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R4が、3位ではビニルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項59に記載のコンジュゲート(コンジュゲート17)。
- 感光剤が式IIのクロロフィルであり、MがCuであり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R4が、3位ではビニルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項59に記載のコンジュゲート(コンジュゲート18)。
- 感光剤が式Iのバクテリオクロロフィルであり、MがMnであり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R2がOHであり;R3がCOOCH3であり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R5がOである、請求項58に記載のコンジュゲート(コンジュゲート12)。
- 感光剤が式Iのバクテリオクロロフィルであり、Mが2Hであり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R2がOHであり;R3がCOOCH3であり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R5がOである、請求項58に記載のコンジュゲート(コンジュゲート27)。
- 感光剤が式Iのバクテリオクロロフィルであり、Mが2Hであり;R1がNH−(CH2)2−NH−CO−Pであり、Pが配列番号4のRGD含有ペプチドの残基であり;R2がOHであり;R3がCOOCH3であり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R5がOである、請求項58に記載のコンジュゲート(コンジュゲート32)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号2のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート11)。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート13)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがMnであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート14)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがCuであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート15)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート24)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)3−SO3Kである、請求項57に記載のコンジュゲート(コンジュゲート19)。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが配列番号3のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート26)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号5のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート33)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号6のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート34)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号7のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート35)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−CH[(−(CH2)2−CO−NH−P]2であり、Pが配列番号8のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−(CH2)2−SO3Kである、請求項55に記載のコンジュゲート(コンジュゲート36)。
- 感光剤が式IIのバクテリオクロロフィルであり、MがPdであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−CH2−CH(OH)−CH2OHである、請求項56に記載のコンジュゲート(コンジュゲート23)。
- 感光剤が式IIのバクテリオクロロフィルであり、Mが2Hであり;mが0であり;R1がNH−Pであり、Pが配列番号1のRGD含有ペプチドの残基であり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が、−NH−(CH2)3−NH−CO−DTPA(コンジュゲート43)又はGdとのそのキレート錯体(コンジュゲート44)である、請求項13に記載のコンジュゲート。
- MがPdであり;R1がCOOHであり;R’2がメトキシであり;R4が、3位ではアセチルであり、8位ではエチルであり;R’4がメチルであり;R6が−NH−CH2−CH(OH)−CH2−OHである、請求項13に記載の式IIのバクテリオクロロフィル(化合物10)。
- 請求項1に記載の、RGD含有ペプチド又はRGDペプチド模倣体とポルフィリン、クロロフィル又はバクテリオクロロフィルから選択される感光剤のコンジュゲート及び製薬上許容される担体を含む薬剤組成物。
- 感光剤が請求項2から12までのいずれか一項に記載のポルフィリンである、請求項113に記載の薬剤組成物。
- 感光剤が、請求項13に記載の式I、II又はIIIのクロロフィル又はバクテリオクロロフィルである、請求項113に記載の薬剤組成物。
- 感光剤が式IIのクロロフィルである、請求項115に記載の薬剤組成物。
- クロロフィルコンジュゲートがコンジュゲート16、17及び18から選択される、請求項116に記載の薬剤組成物。
- 感光剤が式Iのバクテリオクロロフィルである、請求項115に記載の薬剤組成物。
- バクテリオクロロフィルIのコンジュゲートがコンジュゲート12、27及び32から選択される、請求項118に記載の薬剤組成物。
- 感光剤が式IIIのバクテリオクロロフィルである、請求項115に記載の薬剤組成物。
- バクテリオクロロフィルIIIのコンジュゲートがコンジュゲート19である、請求項120に記載の薬剤組成物。
- 感光剤が式IIのバクテリオクロロフィルである、請求項115に記載の薬剤組成物。
- バクテリオクロロフィルIIがRGDペプチドとコンジュゲートしている、請求項122に記載の薬剤組成物。
- バクテリオクロロフィルIIが配列番号1のRGDペプチドとコンジュゲートしている、請求項123に記載の薬剤組成物。
- バクテリオクロロフィルIIのコンジュゲートがコンジュゲート13、15、23、28、29、30、31、43、及び44から選択される、請求項124に記載の薬剤組成物。
- バクテリオクロロフィルIIコンジュゲートがコンジュゲート24である、請求項124に記載の薬剤組成物。
- バクテリオクロロフィルIIが配列番号2〜8のペプチドから選択されるRGDペプチドとコンジュゲートしている、請求項123に記載の薬剤組成物。
- バクテリオクロロフィルIIがコンジュゲート11、26、33、34、35、及び36から選択されるコンジュゲートである、請求項127に記載の薬剤組成物。
- バクテリオクロロフィルIIがRGDペプチド模倣体とコンジュゲートしている、請求項122に記載の薬剤組成物。
- バクテリオクロロフィルIIがコンジュゲート40及び41から選択される、請求項129に記載の薬剤組成物。
- 光線力学的治療(PDT)のための、請求項113から130までのいずれか一項に記載の薬剤組成物。
- 血管標的のPDT(VTP)のための、請求項131に記載の薬剤組成物。
- 腫瘍のVTPのための、請求項132に記載の薬剤組成物。
- 前記腫瘍が原発腫瘍又は黒色腫、結腸、乳房、肺、前立腺、脳若しくは頭頸部の癌からの転移である、請求項133に記載の薬剤組成物。
- 非新生物組織のVTPのための、請求項132に記載の薬剤組成物。
- 加齢黄斑変性症を処置するための、請求項135に記載の薬剤組成物。
- 脂肪組織への血管供給を制限することによって肥満症を処置するための、請求項135に記載の薬剤組成物。
- 診断目的での、請求項113から130までのいずれか一項に記載の薬剤組成物。
- 器官及び組織の可視化のための、請求項138に記載の薬剤組成物。
- 腫瘍の診断のための、請求項138に記載の薬剤組成物。
- 感光剤中のMが、2H又はCu、Pd Gd、Pt、Zn、Al、Eu、Er、Yb若しくはその同位体から選択される金属である、動的蛍光イメージングによる腫瘍診断のための、請求項140に記載の薬剤組成物。
- 感光剤中のMが、64Cu、67Cu、99mTc、67Ga、201Tl、195Pt、60Co、111In及び51Crから選択される放射性同位体である、放射線診断技術による腫瘍診断のための、請求項140に記載の薬剤組成物。
- 前記放射線診断技術が陽電子放射断層撮影(PET)であり、Mが64Cu又は67Cuである、請求項142に記載の薬剤組成物。
- 前記放射線診断技術が単一光子放射断層撮影(SPET)であり、Mが、99mTc、67Ga、195Pt、111In、51Cr及び60Coから選択される放射性同位体である、請求項142に記載の薬剤組成物。
- Mが、Mn3+、Cu2+、Fe3+、Eu3+、Gd3+及びDy3+から選択される常磁性金属であるか、又は、感光剤が多座配位子の金属キレート錯体によって置換され、金属が本明細書中で既に定義したとおりである、分子磁気共鳴画像法(MRI)による腫瘍診断のための、請求項140に記載の薬剤組成物。
- Mが、103Pd、195Pt、105Rh、106Rh、188Re、177Lu、164Er、117mSn、153Sm、90Y、67Cu及び32Pから選択される放射性同位体である、腫瘍の放射線療法のための、請求項113に記載の薬剤組成物。
- (a)腫瘍を有することが疑われる対象に、Mが、2Hであるか、又は、Cu、Pd Gd、Pt、Zn、Al、Eu、Er、Yb又はその同位体から選択される金属である、請求項1から112までのいずれか一項に記載のコンジュゲートを投与するステップと;
(b)標準の手順によって対象を照射し、疑われる領域の蛍光を測定するステップであって、より高い蛍光が腫瘍部位を示すステップと
を含む、動的蛍光イメージングによって腫瘍を診断する方法。 - (a)腫瘍を有することが疑われる対象に、Mが、64Cu、67Cu、99mTc、67Ga、201Tl、195Pt、60Co、111In又は51Crからなる群から選択される放射性同位体である、請求項1から112までのいずれか一項に記載のコンジュゲートを投与するステップと、
(b)対象をイメージングスキャナー内で走査し、疑われる領域の放射線レベルを測定するステップであって、増強した放射線が腫瘍部位を示すステップと
を含む、放射線診断技術によって腫瘍を診断する方法。 - 前記放射線診断技術が陽電子放射断層撮影(PET)であり、Mが64Cu又は67Cuである、請求項148に記載の方法。
- 前記放射線診断技術が単一光子放射断層撮影(SPET)であり、Mが99mTc、67Ga、195Pt、111In、51Cr及び60Coからなる群から選択される放射性同位体である、請求項148に記載の方法。
- (a)腫瘍を有することが疑われる対象に、Mが常磁性金属である、請求項1から112までのいずれか一項に記載のコンジュゲートを投与するステップと;
(b)前記投与の前に患者の体内の目的の標的領域の少なくとも1つのMR画像、その後に1つ又は複数のMR画像を作成することによって、患者を磁気共鳴画像法に供するステップと
を含む、腫瘍診断のための分子磁気共鳴画像法(MRI)方法。 - (a)腫瘍を有することが疑われる患者に、Mが、Mn3+、Cu2+、Fe3+、Eu3+、Gd3+及びDy3+から選択される常磁性金属である前記コンジュゲートを投与するステップと;
(b)0時点及びその後の2番目以降の時点でMR画像を作成するステップと;
(c)データを処理及び分析して腫瘍の存在の有無を診断するステップと
を含む、請求項151に記載のMRI方法。 - 感光剤−ペプチドのコンジュゲートを用いた蛍光イメージングによって腫瘍を診断する方法において、請求項1から112までのいずれか一項に記載のコンジュゲートを使用する改良方法。
- 感光剤−ペプチドのコンジュゲートを用いたPET又はSPET走査によって腫瘍を診断する方法において、請求項1から112までのいずれか一項に記載のコンジュゲートを使用する改良方法。
- 感光剤−ペプチドのコンジュゲートを用いたMRIによって腫瘍を診断する方法において、請求項1から112までのいずれか一項に記載のコンジュゲートを使用する改良方法。
- (a)必要としている個体に、請求項1から112までのいずれか一項に記載のコンジュゲートを投与するステップと;
(b)腫瘍の局所を照射するステップと
を含む、腫瘍の光線力学的治療の方法。 - 感光剤−ペプチドのコンジュゲートを用いた光線力学的治療の方法において、請求項1から112までのいずれか一項に記載のコンジュゲートを使用する改良方法。
- 必要としている個体に、請求項1から112までのいずれか一項に記載のコンジュゲートを投与するステップを含み、Mが、103Pd、195Pt、105Rh、106Rh、188Re、177Lu、164Er、117mSn、153Sm、90Y、67Cu及び32Pからなる群から選択される放射性同位体である、腫瘍の放射線療法の方法。
- 前記腫瘍が原発腫瘍又は黒色腫、結腸、乳房、肺、前立腺、脳若しくは頭頸部の癌からの転移である、請求項146から158までのいずれか一項に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US83940906P | 2006-08-23 | 2006-08-23 | |
| PCT/IL2007/001055 WO2008023378A1 (en) | 2006-08-23 | 2007-08-23 | Conjugates of rgd peptides and porphyrin or (bacterio)chlorophyll photosynthesizers and their uses |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013118542A Division JP6177013B2 (ja) | 2006-08-23 | 2013-06-05 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010502574A true JP2010502574A (ja) | 2010-01-28 |
| JP2010502574A5 JP2010502574A5 (ja) | 2010-10-07 |
Family
ID=38896083
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009525172A Pending JP2010502574A (ja) | 2006-08-23 | 2007-08-23 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
| JP2013118542A Expired - Fee Related JP6177013B2 (ja) | 2006-08-23 | 2013-06-05 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
| JP2016144093A Pending JP2017039700A (ja) | 2006-08-23 | 2016-07-22 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013118542A Expired - Fee Related JP6177013B2 (ja) | 2006-08-23 | 2013-06-05 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
| JP2016144093A Pending JP2017039700A (ja) | 2006-08-23 | 2016-07-22 | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20080138278A1 (ja) |
| EP (1) | EP2061512B1 (ja) |
| JP (3) | JP2010502574A (ja) |
| AU (1) | AU2007287205B8 (ja) |
| CA (1) | CA2661319C (ja) |
| DK (1) | DK2061512T3 (ja) |
| ES (1) | ES2763237T3 (ja) |
| HU (1) | HUE047789T2 (ja) |
| IL (1) | IL197195A (ja) |
| PT (1) | PT2061512T (ja) |
| RU (1) | RU2450018C2 (ja) |
| WO (1) | WO2008023378A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015030671A (ja) * | 2013-07-31 | 2015-02-16 | 国立大学法人 筑波大学 | 悪性腫瘍のpet診断用トレーサー |
| JP2019510807A (ja) * | 2016-04-10 | 2019-04-18 | イエダ リサーチ アンド ディベロップメント カンパニー リミテッド | バクテリオクロロフィル誘導体を含む、がんの治療のための併用療法 |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6850788B2 (en) | 2002-03-25 | 2005-02-01 | Masimo Corporation | Physiological measurement communications adapter |
| US9161696B2 (en) | 2006-09-22 | 2015-10-20 | Masimo Corporation | Modular patient monitor |
| US8840549B2 (en) | 2006-09-22 | 2014-09-23 | Masimo Corporation | Modular patient monitor |
| WO2009038660A1 (en) | 2007-09-14 | 2009-03-26 | Health Research, Inc. | Multimodality agents for tumor imaging and therapy |
| WO2009107139A1 (en) * | 2008-02-27 | 2009-09-03 | Yeda Research And Development Co. Ltd | Rgd-(bacterio)chlorophyll conjugates for photodynamic therapy and imaging of necrotic tumors |
| LT5567B (lt) | 2008-08-06 | 2009-04-27 | Vilniaus Universitetas | Maisto ir su maistu susietų paviršių nukenksminimo būdas |
| PT2358737T (pt) | 2008-10-23 | 2017-06-12 | Steba Biotech S A | Peptidomiméticos que contêm rgd e utilizações dos mesmos |
| US8263133B2 (en) * | 2009-02-18 | 2012-09-11 | The Regents Of The University Of California | Multivalent clustering targeting strategy for drug carriers |
| US9153112B1 (en) | 2009-12-21 | 2015-10-06 | Masimo Corporation | Modular patient monitor |
| PL219569B1 (pl) | 2010-02-19 | 2015-05-29 | Peptaderm Spółka Z Ograniczoną Odpowiedzialnością | Cykliczne tetrapeptydy i ich zastosowanie |
| JP2014522404A (ja) | 2011-05-31 | 2014-09-04 | ノース・キャロライナ・ステイト・ユニヴァーシティ | バクテリオクロリンイミド |
| CA2846011C (en) * | 2011-08-23 | 2019-10-15 | Yeda Research And Development Co.Ltd. | (bacterio)chlorophyll photosensitizers for treatment of eye diseases and disorders |
| EP2766834B1 (en) | 2011-10-13 | 2022-04-20 | Masimo Corporation | Medical monitoring hub |
| US9943269B2 (en) | 2011-10-13 | 2018-04-17 | Masimo Corporation | System for displaying medical monitoring data |
| US10149616B2 (en) | 2012-02-09 | 2018-12-11 | Masimo Corporation | Wireless patient monitoring device |
| US10307111B2 (en) | 2012-02-09 | 2019-06-04 | Masimo Corporation | Patient position detection system |
| KR101385196B1 (ko) | 2012-05-17 | 2014-04-14 | 주식회사 유니크메디케어 | 광 조사를 이용한 광감각제―펩타이드를 유효성분으로 포함하는 발모 개선 또는 촉진용 조성물 및 이를 이용한 방법 |
| CN105884905A (zh) * | 2012-09-05 | 2016-08-24 | 上海晟顺生物科技有限公司 | 同时具溶血栓、清除自由基和血栓靶向功能的新颖化合物及其制备方法和用途 |
| US9749232B2 (en) | 2012-09-20 | 2017-08-29 | Masimo Corporation | Intelligent medical network edge router |
| RU2548675C9 (ru) * | 2013-05-29 | 2015-11-10 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Московский государственный университет тонких химических технологий имени М.В. Ломоносова" (МИТХТ им. М.В. Ломоносова) | Аминоамиды в ряду бактериохлорофилла a, обладающие фотодинамической активностью, и способ их получения |
| US10832818B2 (en) | 2013-10-11 | 2020-11-10 | Masimo Corporation | Alarm notification system |
| US9522925B2 (en) * | 2014-11-09 | 2016-12-20 | Hong Kong Baptist University | Selective cancer tracking eradicator and the uses thereof |
| TN2017000554A1 (en) * | 2015-07-29 | 2019-04-12 | Novartis Ag | Novel combination for use in the treatment of cancer |
| SG10201506686WA (en) * | 2015-08-24 | 2017-03-30 | Agency Science Tech & Res | Conjugates |
| CN113367671A (zh) | 2015-08-31 | 2021-09-10 | 梅西莫股份有限公司 | 无线式病人监护系统和方法 |
| CN105837666A (zh) * | 2015-12-30 | 2016-08-10 | 田梗 | 一种用于诊断糖尿病性视网膜病的蛋白质 |
| US10617302B2 (en) | 2016-07-07 | 2020-04-14 | Masimo Corporation | Wearable pulse oximeter and respiration monitor |
| CN107759804B (zh) * | 2016-08-19 | 2019-12-03 | 四川大学 | 可定点结合含组氨酸标签蛋白的明胶衍生材料及其制备方法 |
| US11076777B2 (en) | 2016-10-13 | 2021-08-03 | Masimo Corporation | Systems and methods for monitoring orientation to reduce pressure ulcer formation |
| US10933134B2 (en) | 2017-03-16 | 2021-03-02 | Memorial Sloan Kettering Cancer Center | Combination therapies for treatment of cancer |
| WO2019204368A1 (en) | 2018-04-19 | 2019-10-24 | Masimo Corporation | Mobile patient alarm display |
| CN110215438B (zh) * | 2019-07-15 | 2021-06-29 | 中国医学科学院生物医学工程研究所 | 双载蒽环类药物及光敏剂介孔硅纳米粒的制备方法与应用 |
| US20210290184A1 (en) | 2020-03-20 | 2021-09-23 | Masimo Corporation | Remote patient management and monitoring systems and methods |
| USD980091S1 (en) | 2020-07-27 | 2023-03-07 | Masimo Corporation | Wearable temperature measurement device |
| USD974193S1 (en) | 2020-07-27 | 2023-01-03 | Masimo Corporation | Wearable temperature measurement device |
| USD1000975S1 (en) | 2021-09-22 | 2023-10-10 | Masimo Corporation | Wearable temperature measurement device |
| CN115960160A (zh) * | 2021-10-12 | 2023-04-14 | 南京大学 | 活细胞膜整合素αvβ3聚糖的原位糖链延长方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07503944A (ja) * | 1991-11-22 | 1995-04-27 | イエダ リサーチ アンド デベロツプメント カンパニー リミテツド | Arg−gly−asp配列の非ペプチド代替物およびそれらからなる医薬組成物 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL102645A (en) * | 1992-07-26 | 1998-02-22 | Yeda Res & Dev | Chlorophyll and bacteriochlorophyll derivatives, their preparation and pharmaceutical compositions comprising them |
| IL116126A0 (en) * | 1995-11-24 | 1996-01-31 | Yeda Res & Dev | Process for the preparation of bacteriochlorophyllis some novel compounds of this type and pharmaceutical compositions comprising them |
| US20030004334A1 (en) * | 2001-06-01 | 2003-01-02 | Ceramoptec Industries, Inc. | Water-soluble porphyrin derivatives and methods of their preparation |
-
2007
- 2007-08-23 CA CA2661319A patent/CA2661319C/en not_active Expired - Fee Related
- 2007-08-23 RU RU2009110226/04A patent/RU2450018C2/ru not_active IP Right Cessation
- 2007-08-23 EP EP07805515.9A patent/EP2061512B1/en active Active
- 2007-08-23 DK DK07805515.9T patent/DK2061512T3/da active
- 2007-08-23 AU AU2007287205A patent/AU2007287205B8/en not_active Ceased
- 2007-08-23 WO PCT/IL2007/001055 patent/WO2008023378A1/en active Application Filing
- 2007-08-23 US US11/843,996 patent/US20080138278A1/en not_active Abandoned
- 2007-08-23 JP JP2009525172A patent/JP2010502574A/ja active Pending
- 2007-08-23 ES ES07805515T patent/ES2763237T3/es active Active
- 2007-08-23 PT PT78055159T patent/PT2061512T/pt unknown
- 2007-08-23 HU HUE07805515A patent/HUE047789T2/hu unknown
-
2009
- 2009-02-23 IL IL197195A patent/IL197195A/en active IP Right Grant
-
2013
- 2013-06-05 JP JP2013118542A patent/JP6177013B2/ja not_active Expired - Fee Related
-
2016
- 2016-07-22 JP JP2016144093A patent/JP2017039700A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07503944A (ja) * | 1991-11-22 | 1995-04-27 | イエダ リサーチ アンド デベロツプメント カンパニー リミテツド | Arg−gly−asp配列の非ペプチド代替物およびそれらからなる医薬組成物 |
Non-Patent Citations (3)
| Title |
|---|
| JPN6012053054; Eur.J.Org.Chem.,Vol.8(2003)p.1486-1493 * |
| JPN6012053057; Tetrahedron Lett.,Vol.45(2004)p.5295-5299 * |
| JPN6012053061; Tetrahedron,Vol.54(1998)p.4151-4202 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015030671A (ja) * | 2013-07-31 | 2015-02-16 | 国立大学法人 筑波大学 | 悪性腫瘍のpet診断用トレーサー |
| JP2019510807A (ja) * | 2016-04-10 | 2019-04-18 | イエダ リサーチ アンド ディベロップメント カンパニー リミテッド | バクテリオクロロフィル誘導体を含む、がんの治療のための併用療法 |
| JP2022031823A (ja) * | 2016-04-10 | 2022-02-22 | イエダ リサーチ アンド ディベロップメント カンパニー リミテッド | バクテリオクロロフィル誘導体を含む、がんの治療のための併用療法 |
Also Published As
| Publication number | Publication date |
|---|---|
| HUE047789T2 (hu) | 2020-05-28 |
| WO2008023378A9 (en) | 2008-04-10 |
| ES2763237T3 (es) | 2020-05-27 |
| IL197195A (en) | 2015-10-29 |
| JP6177013B2 (ja) | 2017-08-09 |
| US20080138278A1 (en) | 2008-06-12 |
| AU2007287205A1 (en) | 2008-02-28 |
| RU2009110226A (ru) | 2010-09-27 |
| PT2061512T (pt) | 2020-01-14 |
| CA2661319C (en) | 2015-12-01 |
| IL197195A0 (en) | 2009-12-24 |
| RU2450018C2 (ru) | 2012-05-10 |
| JP2013231039A (ja) | 2013-11-14 |
| CA2661319A1 (en) | 2008-02-28 |
| DK2061512T3 (da) | 2020-01-20 |
| EP2061512B1 (en) | 2019-10-02 |
| AU2007287205B8 (en) | 2013-08-15 |
| WO2008023378A1 (en) | 2008-02-28 |
| AU2007287205B2 (en) | 2013-04-18 |
| EP2061512A1 (en) | 2009-05-27 |
| JP2017039700A (ja) | 2017-02-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6177013B2 (ja) | Rgdペプチドとポルフィリン又は(バクテリオ)クロロフィル光合成剤とのコンジュゲート及びその使用 | |
| US10689415B2 (en) | Conjugates of RGD peptides and (bacterio)chlorophyll photosensitizers | |
| RU2518296C2 (ru) | Конъюгаты rgd-(бактерио)хлорофилл для фотодинамической терапии и визуализации некротических опухолей | |
| Frochot et al. | Interest of RGD-containing linear or cyclic peptide targeted tetraphenylchlorin as novel photosensitizers for selective photodynamic activity | |
| RU2519736C2 (ru) | Rgd-содержащие пептидомиметики и их применение | |
| CA2569675C (en) | Cationic bacteriochlorophyll derivatives and uses thereof | |
| KR101659855B1 (ko) | 엽산을 포함하는 광역학 진단 또는 치료용 결합체 및 그를 포함하는 광역학 진단 또는 치료용 조성물 | |
| CN110023740A (zh) | 基于活性的探针化合物、组合物及其使用方法 | |
| WO2005000218A2 (en) | Macrocyclic cyanine and indocyanine bioconjugates provide improved biomedical applications | |
| KR101936559B1 (ko) | 분해가능 연결자를 포함하는 광증감제-펩타이드 결합체 및 그를 포함하는 광역학 진단 또는 치료용 조성물 | |
| Chu | Development of Cyclic Peptide-Conjugated Photosensitizers for Targeted Photodynamic Therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100823 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121012 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130115 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130205 |