JP2010143859A - ぶどう膜炎の予防及び/又は治療のための医薬 - Google Patents
ぶどう膜炎の予防及び/又は治療のための医薬 Download PDFInfo
- Publication number
- JP2010143859A JP2010143859A JP2008323057A JP2008323057A JP2010143859A JP 2010143859 A JP2010143859 A JP 2010143859A JP 2008323057 A JP2008323057 A JP 2008323057A JP 2008323057 A JP2008323057 A JP 2008323057A JP 2010143859 A JP2010143859 A JP 2010143859A
- Authority
- JP
- Japan
- Prior art keywords
- uveitis
- treatment
- prevention
- examples
- vitamin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 Cc1ncc(CO)c(*)c1O Chemical compound Cc1ncc(CO)c(*)c1O 0.000 description 1
Images
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Pyridine Compounds (AREA)
Abstract
Description
本発明はぶどう膜炎の予防及び/又は治療に有用な薬剤に関する。
ぶどう膜炎は先進国での成人中途失明原因の5−20%を占める難治性炎症性眼疾患の総称である。ぶどう膜炎は、脈絡膜、毛様体、又は虹彩に何らかの原因で炎症が起こる疾患であり、自己免疫が関与する内因性のものと感染症などによる外因性のものに分類できる。即ち、ベーチェット病、サルコイドーシス、原田病、HLA−B27関連ぶどう膜炎、間質性腎炎関連ぶどう膜炎、ヒトT細胞白血病ウイルス1(HTLV−1)ぶどう膜炎、若年性関節リウマチぶどう膜炎、眼トキソプラズマ症等、様々な要因によるぶどう膜炎があるが、原因が不明な場合も多い。
ぶどう膜炎については、これまでもっぱら免疫学的、微生物学的、分子生物学的側面から研究されてきた。糖尿病患者になぜかぶどう膜炎が起きることも昔から経験的に知られており、また、近年生活様式の変化に伴ってぶどう膜炎の原因も変化している。糖の非酵素的修飾(メイラード反応)は酸化ストレスの代表的反応であり、その結果、終末糖化産物(AGE)が産生される。中でもグリセルアルデヒド由来AGE(AGE−2)は活性・毒性が特に強く、毒性AGE(TAGE)とも呼ばれ、糖尿病腎症、糖尿病網膜症、アルツハイマー病、悪性腫瘍の重要な増悪因子であることが近年報告されている。しかし、これまで自己免疫疾患とTAGEの関連はほとんど検討されておらず、ぶどう膜炎と糖由来の酸化ストレスとの関係は極めて興味深い問題である。
実験的自己免疫性ぶどう膜網膜炎(EAU)は、臓器特異的なT細胞によって引き起こされる病態モデルであり、皮下に視細胞間レチノイド結合蛋白質(IRBP)やS抗原等の網膜関連抗原を免疫することで眼内に炎症が惹起されるため、眼サルコイドーシス、ベーチェット病、原田病等のヒト内因性ぶどう膜炎の動物モデルと考えられている。マウスではH−2r、H−2k、H−2bの3系統で誘導され、惹起アミノ酸配列も同定されている(非特許文献1)。
ぶどう膜炎の治療としてはステロイド剤の全身投与等が行われている。ステロイドの薬理学的な機序として、炎症局所への好中球やマクロファージの集積の抑制やサイトカイン発現の抑制、アポトーシスの誘導が報告されている。しかしながら、ステロイド剤の全身投与には副作用の問題がある。そこで持続性デポ型ステロイド製剤の経テノン嚢下球後投与やステロイド眼内インプラントの徐放製剤の開発・治験も行われているが、埋植することにより白内障や緑内障が高率に発症する。また、シクロスポリンも使われているが腎症、神経症状の増加が知られている。さらに、近年インフリキシマブがベーチェット病による難治性網膜ぶどう膜炎治療薬として適応が認可されたが、抗体製剤であること及びTNFαを阻害することによる副作用についての注意が必要である(非特許文献2)。このような状況から、安全性が高く、より有効な薬剤の開発が望まれている。
ぶどう膜炎の治療としてはステロイド剤の全身投与等が行われている。ステロイドの薬理学的な機序として、炎症局所への好中球やマクロファージの集積の抑制やサイトカイン発現の抑制、アポトーシスの誘導が報告されている。しかしながら、ステロイド剤の全身投与には副作用の問題がある。そこで持続性デポ型ステロイド製剤の経テノン嚢下球後投与やステロイド眼内インプラントの徐放製剤の開発・治験も行われているが、埋植することにより白内障や緑内障が高率に発症する。また、シクロスポリンも使われているが腎症、神経症状の増加が知られている。さらに、近年インフリキシマブがベーチェット病による難治性網膜ぶどう膜炎治療薬として適応が認可されたが、抗体製剤であること及びTNFαを阻害することによる副作用についての注意が必要である(非特許文献2)。このような状況から、安全性が高く、より有効な薬剤の開発が望まれている。
一方、ビタミンB6の1つであるピリドキサミンは、生体内でピリドキサール−5−リン酸に変換され、アミノ酸の代謝や神経伝達において補酵素として作用する。虚血再灌流損傷及び細胞機能障害治療剤としての用途が報告されている(特許文献1)。また、ピリドキサミンは、AGE産生阻害作用を有しており、糖尿病腎症(特許文献2)や糸球体疾患(特許文献3)の治療剤として有用であることが報告されている。さらに、ピリドキサール−5−リン酸がプリン受容体P2X7を介したIL−1β調節作用を有し、ぶどう膜炎にも有効である旨の記載があるが、実験的にぶどう膜炎に有効であることを裏付けるデータは開示されておらず、さらに、ビタミンB6(本発明のピリドキシン、ピリドキサール、ピリドキサミン)はP2X7を介したIL−1β調節作用を有していないと報告されている(特許文献4)。
本発明の目的は、ぶどう膜炎の予防及び/又は治療に有用な薬剤を提供することにある。
本発明者らは斯かる実情に鑑み、鋭意研究を重ねた結果、ビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物が、ぶどう膜炎の治療剤として有用であることを見出し、本発明を完成した。
即ち、本発明は、下記に関する。
[1] 下記一般式(1):
〔式中、Rはヒドロキシメチル基、ホルミル基、アミノメチル基から選択される〕
で表されるビタミンB6の少なくとも1種又は生理学的に許容されるその塩もしくはそれらの溶媒和物を有効成分として含有する、ぶどう膜炎の予防及び/又は治療のための医薬。
[2] Rがアミノメチル基である、上記[1]に記載のぶどう膜炎の予防及び/又は治療のための医薬。
[3] 式(1)の化合物が2塩酸塩である上記[1]又は[2]に記載の医薬。
[4] 上記[1]乃至[3]のいずれかに記載のビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物、及び医薬として許容される担体を含有する、ぶどう膜炎の予防及び/又は治療のための医薬組成物。
[5] ぶどう膜炎の予防及び/又は治療のための製剤を製造するための、上記[1]乃至[3]のいずれかに記載の医薬の使用。
[6] 治療が必要とされる患者に、上記[1]乃至[3]のいずれかに記載の医薬の有効量を投与することを特徴とする、ぶどう膜炎の予防及び/又は治療方法。
即ち、本発明は、下記に関する。
[1] 下記一般式(1):
で表されるビタミンB6の少なくとも1種又は生理学的に許容されるその塩もしくはそれらの溶媒和物を有効成分として含有する、ぶどう膜炎の予防及び/又は治療のための医薬。
[2] Rがアミノメチル基である、上記[1]に記載のぶどう膜炎の予防及び/又は治療のための医薬。
[3] 式(1)の化合物が2塩酸塩である上記[1]又は[2]に記載の医薬。
[4] 上記[1]乃至[3]のいずれかに記載のビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物、及び医薬として許容される担体を含有する、ぶどう膜炎の予防及び/又は治療のための医薬組成物。
[5] ぶどう膜炎の予防及び/又は治療のための製剤を製造するための、上記[1]乃至[3]のいずれかに記載の医薬の使用。
[6] 治療が必要とされる患者に、上記[1]乃至[3]のいずれかに記載の医薬の有効量を投与することを特徴とする、ぶどう膜炎の予防及び/又は治療方法。
本発明のぶどう膜炎の予防及び/又は治療に有用な薬剤は、ベーチェット病、サルコイドーシス、原田病、HLA−B27関連ぶどう膜炎、間質性腎炎関連ぶどう膜炎、ヒトT細胞白血病ウイルス1(HTLV−1)ぶどう膜炎、若年性関節リウマチぶどう膜炎、眼トキソプラズマ症等のぶどう膜炎の予防及び/又は治療に有用である。
本発明では、上記式(1)で表されるビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物が使用される。ビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物は1種でも2種以上の混合物でもよい。
塩としては、塩酸塩、硝酸塩、硫酸塩、リン酸塩、蓚酸塩、マレイン酸塩、コハク酸塩、メタンスルホン酸塩等の酸付加塩が挙げられ、リン酸塩、塩酸塩が好ましく、2塩酸塩が特に好ましい。また、ビタミンB6又は生理学的に許容されるその塩の溶媒和物としては、水和物や医薬品として許容される溶媒との溶媒和物が含まれる。
上記式(1)で表されるビタミンB6は、市販されているものを使用することができるほか、公知の製法、例えば、J. Am. Chem. Soc. 61, 1245-1247, 1939、J. Am. Chem. Soc. 61, 3307-3310, 1939、またはJ. Am. Chem. Soc. 66, 2088-2092, 1944に記載の製法に基づいて製造することができる。
塩としては、塩酸塩、硝酸塩、硫酸塩、リン酸塩、蓚酸塩、マレイン酸塩、コハク酸塩、メタンスルホン酸塩等の酸付加塩が挙げられ、リン酸塩、塩酸塩が好ましく、2塩酸塩が特に好ましい。また、ビタミンB6又は生理学的に許容されるその塩の溶媒和物としては、水和物や医薬品として許容される溶媒との溶媒和物が含まれる。
上記式(1)で表されるビタミンB6は、市販されているものを使用することができるほか、公知の製法、例えば、J. Am. Chem. Soc. 61, 1245-1247, 1939、J. Am. Chem. Soc. 61, 3307-3310, 1939、またはJ. Am. Chem. Soc. 66, 2088-2092, 1944に記載の製法に基づいて製造することができる。
本発明のぶどう膜炎の予防及び/又は治療に有用な薬剤は、用法に応じ種々の剤形の医薬品製剤とすることができる。斯かる剤形としては、例えば、散剤、顆粒剤、細粒剤、ドライシロップ剤、錠剤、カプセル剤、点眼剤、注射剤等を挙げることができる。
これらの製剤は、その剤形に応じて製剤学上使用される賦形剤、崩壊剤、結合剤、滑沢剤、希釈剤、緩衝剤、等張化剤、防腐剤、湿潤剤、乳化剤、分散剤、安定化剤、溶解補助剤等の担体(医薬品添加物ともいう)と適宜混合、希釈又は溶解し、常法に従い製造することができる。
これらの製剤は、その剤形に応じて製剤学上使用される賦形剤、崩壊剤、結合剤、滑沢剤、希釈剤、緩衝剤、等張化剤、防腐剤、湿潤剤、乳化剤、分散剤、安定化剤、溶解補助剤等の担体(医薬品添加物ともいう)と適宜混合、希釈又は溶解し、常法に従い製造することができる。
賦形剤としては、例えば、乳糖、白糖、塩化ナトリウム、ブドウ糖、デンプン、炭酸カルシウム、カオリン、微結晶セルロース、又は珪酸等が挙げられる。
崩壊剤としては、例えば、乾燥デンプン、アルギン酸ナトリウム、カンテン末、炭酸水素ナトリウム、炭酸カルシウム、ラウリル硫酸ナトリウム、ステアリン酸モノグリセリド、又は乳糖等が挙げられる。
結合剤としては、例えば、水、エタノール、プロパノール、単シロップ、ブドウ糖液、デンプン液、ゼラチン液、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルスターチ、メチルセルロース、エチルセルロース、シェラック、リン酸カルシウム、又はポリビニルピロリドン等が挙げられる。
滑沢剤としては、例えば、精製タルク、ステアリン酸塩、ホウ砂、ポリエチレングリコール等が挙げられる。
希釈剤としては、例えば、グリセリン、塩酸、酢酸、精製水、生理食塩液、エタノール、プロピレングリコール、ポリエチレングリコール、オリーブ油等の植物油、オレイン酸エチル等の有機酸エステル等が挙げられる。
緩衝剤としては、クエン酸、酢酸塩、リン酸塩、ホウ酸等が挙げられる。
等張化剤としては、例えば塩化ナトリウム又はブドウ糖等が挙げられる。
防腐剤としては、安息香酸、安息香酸ナトリウム、p−ヒドロキシ安息香酸メチル、p−ヒドロキシ安息香酸エチル、ベンジルアルコール、塩化ベンザルコニウム、ホウ酸等が挙げられる。
湿潤剤としては、例えば、塩化マグネシウム、オレイン酸ナトリウム、カロペプタイド、還元水アメ、グリセリン、水、プロピレングリコール、水アメ、メチルセルロース、ラウロマクロゴール、流動パラフィン等が挙げられる。
乳化剤としては、石鹸類、硫酸エステル塩、スルホン酸、界面活性剤、アルギン酸塩等が挙げられる。
分散剤としては、グリセリン、ソルビトール、アルギン酸ナトリウム、界面活性剤、クエン酸ナトリウム等が挙げられる。
安定化剤としては、例えばトラガント、アラビアゴム、ゼラチン、ピロ亜硫酸ナトリウム、EDTA、チオグリコール酸、又はチオ乳酸等が挙げられる。
溶解補助剤としては、クレゾール石鹸液、エタノール、グリセリン等が挙げられる。
崩壊剤としては、例えば、乾燥デンプン、アルギン酸ナトリウム、カンテン末、炭酸水素ナトリウム、炭酸カルシウム、ラウリル硫酸ナトリウム、ステアリン酸モノグリセリド、又は乳糖等が挙げられる。
結合剤としては、例えば、水、エタノール、プロパノール、単シロップ、ブドウ糖液、デンプン液、ゼラチン液、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルスターチ、メチルセルロース、エチルセルロース、シェラック、リン酸カルシウム、又はポリビニルピロリドン等が挙げられる。
滑沢剤としては、例えば、精製タルク、ステアリン酸塩、ホウ砂、ポリエチレングリコール等が挙げられる。
希釈剤としては、例えば、グリセリン、塩酸、酢酸、精製水、生理食塩液、エタノール、プロピレングリコール、ポリエチレングリコール、オリーブ油等の植物油、オレイン酸エチル等の有機酸エステル等が挙げられる。
緩衝剤としては、クエン酸、酢酸塩、リン酸塩、ホウ酸等が挙げられる。
等張化剤としては、例えば塩化ナトリウム又はブドウ糖等が挙げられる。
防腐剤としては、安息香酸、安息香酸ナトリウム、p−ヒドロキシ安息香酸メチル、p−ヒドロキシ安息香酸エチル、ベンジルアルコール、塩化ベンザルコニウム、ホウ酸等が挙げられる。
湿潤剤としては、例えば、塩化マグネシウム、オレイン酸ナトリウム、カロペプタイド、還元水アメ、グリセリン、水、プロピレングリコール、水アメ、メチルセルロース、ラウロマクロゴール、流動パラフィン等が挙げられる。
乳化剤としては、石鹸類、硫酸エステル塩、スルホン酸、界面活性剤、アルギン酸塩等が挙げられる。
分散剤としては、グリセリン、ソルビトール、アルギン酸ナトリウム、界面活性剤、クエン酸ナトリウム等が挙げられる。
安定化剤としては、例えばトラガント、アラビアゴム、ゼラチン、ピロ亜硫酸ナトリウム、EDTA、チオグリコール酸、又はチオ乳酸等が挙げられる。
溶解補助剤としては、クレゾール石鹸液、エタノール、グリセリン等が挙げられる。
例えば、散剤の場合は、必須成分のほかに、必要に応じて適当な賦形剤、滑沢剤等を加え、よく混合して調製すればよい。錠剤の場合は、必要に応じて適当な賦形剤、崩壊剤、結合剤、滑沢剤等を加え、常法に従い打錠して調製すればよい。また錠剤は必要に応じてコーティングを施し、フィルムコート錠、糖衣錠等にすることができる。
また、注射剤の場合は、液剤(無菌水又は非水溶液)、乳剤及び懸濁剤の形態とすることができる。これらに用いられる非水担体、希釈剤、溶媒又はビヒクルとしては、例えばプロピレングリコール、ポリエチレングリコール、オリーブ油等の植物油、オレイン酸エチル等の注射可能な有機酸エステルが挙げられる。また、該組成物には防腐剤、湿潤剤、乳化剤、分散剤等の補助剤を適宜配合することができる。
また、注射剤の場合は、液剤(無菌水又は非水溶液)、乳剤及び懸濁剤の形態とすることができる。これらに用いられる非水担体、希釈剤、溶媒又はビヒクルとしては、例えばプロピレングリコール、ポリエチレングリコール、オリーブ油等の植物油、オレイン酸エチル等の注射可能な有機酸エステルが挙げられる。また、該組成物には防腐剤、湿潤剤、乳化剤、分散剤等の補助剤を適宜配合することができる。
本発明の一般式(1)で表される化合物又は生理学的に許容されるその塩を含有する薬剤は経口的に投与することができる。投与量は、疾患の種類、患者の体重、年齢、性別、症状等により適宜決定される。好ましい投与量としては、通常50〜2,000mg/日/人である。経口投与は、1日に1回又は数回に分けて投与するのが好ましい。
本発明の化合物を含有する薬剤は局所投与も可能であり、局所投与する場合の剤形の好ましい例としては、点眼剤や注射剤が挙げられる。局所注射の方法の例としては、眼内注射、結膜下注射、テノン嚢下注射等が挙げられる。
本発明の化合物を含有する薬剤は局所投与も可能であり、局所投与する場合の剤形の好ましい例としては、点眼剤や注射剤が挙げられる。局所注射の方法の例としては、眼内注射、結膜下注射、テノン嚢下注射等が挙げられる。
以下に実施例を示して本発明をより詳細に説明するが、本発明はこれら実施例に限定されるものではない。
実施例1 実験的自己免疫性ぶどう膜網膜炎(EAU)に対する効果
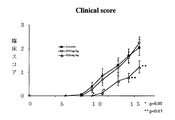
マウスEAUモデルによる評価は非特許文献1の方法に従った。すなわち、雌性B10.RBマウス(H−2k)(6〜8週令)を視細胞間レチノイド結合蛋白質(IRBP)由来K2ペプチド(ADKDVVVLSSRTGGV(配列番号1))と完全フロイントアジュバント(Difco)の混合エマルジョンで免疫し(皮下投与)、更に百日咳毒素(Sigma)を追加免疫として腹腔内投与した。3日おきに眼底を検査し、21日目に眼球摘出し、組織学的解析を行った。対照群(非薬剤投与群、蒸留水:N=19)、ピリドキサミン・2塩酸塩投与群(200mg/kg/日、1日1回経口投与:N=16)、ピリドキサミン・2塩酸塩投与群(400mg/kg/日、1日1回経口投与:N=22)の3群を設定した。投与は初回感作時から行った。臨床スコアは、Nambaらの報告(J. Immunol. 165, 2962-2969, 2000)と同様に眼内炎症の程度により0から4にスコア化した。
スコア0:変化なし
1:軽度血管炎(5限局病変未満、1線状病変以内)
2:多局所網脈絡膜病変 かつ/または 浸潤、重度血管炎(大型、壁肥厚、 浸潤)、5線状病変以内
3:線状型病変、広範な融合病変、網膜下新生血管、網膜出血、視神経乳頭浮腫
4:広範な網膜剥離、網膜萎縮
マウスEAUモデルによる評価は非特許文献1の方法に従った。すなわち、雌性B10.RBマウス(H−2k)(6〜8週令)を視細胞間レチノイド結合蛋白質(IRBP)由来K2ペプチド(ADKDVVVLSSRTGGV(配列番号1))と完全フロイントアジュバント(Difco)の混合エマルジョンで免疫し(皮下投与)、更に百日咳毒素(Sigma)を追加免疫として腹腔内投与した。3日おきに眼底を検査し、21日目に眼球摘出し、組織学的解析を行った。対照群(非薬剤投与群、蒸留水:N=19)、ピリドキサミン・2塩酸塩投与群(200mg/kg/日、1日1回経口投与:N=16)、ピリドキサミン・2塩酸塩投与群(400mg/kg/日、1日1回経口投与:N=22)の3群を設定した。投与は初回感作時から行った。臨床スコアは、Nambaらの報告(J. Immunol. 165, 2962-2969, 2000)と同様に眼内炎症の程度により0から4にスコア化した。
スコア0:変化なし
1:軽度血管炎(5限局病変未満、1線状病変以内)
2:多局所網脈絡膜病変 かつ/または 浸潤、重度血管炎(大型、壁肥厚、 浸潤)、5線状病変以内
3:線状型病変、広範な融合病変、網膜下新生血管、網膜出血、視神経乳頭浮腫
4:広範な網膜剥離、網膜萎縮
図1に臨床スコアに対するピリドキサミン・2塩酸塩投与による効果を示す。
ピリドキサミン・2塩酸塩200mg/kg/日投与群では対照群と差異は認められなかったが、400mg/kg/日投与群において、臨床重症度は常に軽度(p<0.01)であった。
また、組織学的スコアは、Caspiらの報告(J. Immunol. 140, 1490-1495, 1988)に従って、炎症組織像の重症度により0から4にスコア化した。
図2に組織学的スコアに対するピリドキサミン・2塩酸塩投与による効果を示す。対照群に比較し、ピリドキサミン・2塩酸塩400mg/kg/日投与群において、組織学的スコアが軽度(p=0.015)であった。
ピリドキサミン・2塩酸塩200mg/kg/日投与群では対照群と差異は認められなかったが、400mg/kg/日投与群において、臨床重症度は常に軽度(p<0.01)であった。
また、組織学的スコアは、Caspiらの報告(J. Immunol. 140, 1490-1495, 1988)に従って、炎症組織像の重症度により0から4にスコア化した。
図2に組織学的スコアに対するピリドキサミン・2塩酸塩投与による効果を示す。対照群に比較し、ピリドキサミン・2塩酸塩400mg/kg/日投与群において、組織学的スコアが軽度(p=0.015)であった。
Claims (6)
- Rがアミノメチル基である、請求項1に記載のぶどう膜炎の予防及び/又は治療のための医薬。
- 式(1)の化合物が2塩酸塩である請求項1又は2に記載の医薬。
- 請求項1乃至3のいずれかに記載のビタミンB6又は生理学的に許容されるその塩もしくはそれらの溶媒和物、及び医薬として許容される担体を含有する、ぶどう膜炎の予防及び/又は治療のための医薬組成物。
- ぶどう膜炎の予防及び/又は治療のための製剤を製造するための、請求項1乃至3のいずれかに記載の医薬の使用。
- 治療が必要とされる患者に、請求項1乃至3のいずれかに記載の医薬の有効量を投与することを特徴とする、ぶどう膜炎の予防及び/又は治療方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008323057A JP2010143859A (ja) | 2008-12-19 | 2008-12-19 | ぶどう膜炎の予防及び/又は治療のための医薬 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008323057A JP2010143859A (ja) | 2008-12-19 | 2008-12-19 | ぶどう膜炎の予防及び/又は治療のための医薬 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010143859A true JP2010143859A (ja) | 2010-07-01 |
Family
ID=42564664
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008323057A Pending JP2010143859A (ja) | 2008-12-19 | 2008-12-19 | ぶどう膜炎の予防及び/又は治療のための医薬 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2010143859A (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006136004A1 (en) * | 2005-05-05 | 2006-12-28 | Medicure International Inc. | Inhibition of atp-mediated, p2x7 dependent pathways by pyridoxal-5-phosphaste and vitamin b6 related compounds |
-
2008
- 2008-12-19 JP JP2008323057A patent/JP2010143859A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006136004A1 (en) * | 2005-05-05 | 2006-12-28 | Medicure International Inc. | Inhibition of atp-mediated, p2x7 dependent pathways by pyridoxal-5-phosphaste and vitamin b6 related compounds |
Non-Patent Citations (3)
| Title |
|---|
| JPN6013028863; M.R.Namazi: International Immunopharmacology Vol.4, 2004, p.349-353 * |
| JPN6013028865; P.Trittibach et al.: Gene Therapy Vol.15, No.22, 200811, p.1478-1488 * |
| JPN7013002222; MEDLINE(STN) AccessionNo.2002141477 , 2000 * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20190117675A1 (en) | Compositions And Methods To Treat And/Or Prevent Vision Disorders Of The Lens Of The Eye | |
| JP7082162B2 (ja) | マイボーム機能不全の治療剤 | |
| US20220023213A1 (en) | Nanocrystalline eye drop, preparation method and use thereof | |
| KR20100016270A (ko) | 비맥각계의 선택적 d2 수용체 작용제를 유효 성분으로서 함유하는 후안부 질환의 예방 또는 치료제 | |
| US11654140B2 (en) | Treatment of ocular inflammatory diseases using laquinimod | |
| KR20100016140A (ko) | 가령 황반 변성의 예방 또는 치료제 | |
| WO2011159632A1 (en) | Lysophosphatidic acid receptor antagonists for the treatment of conditions or diseases of the eye | |
| MX2012007941A (es) | Farmaceutico para impedir o tratar alteraciones acompañadas por angiogenesis ocular y/o permeabilidad vascular ocular elevada. | |
| EP2319539A1 (en) | Prophylactic or therapeutic agent for axial myopia | |
| JPWO2005079792A1 (ja) | 重症糖尿病網膜症の予防又は治療剤 | |
| JP4014053B2 (ja) | 糖尿病黄斑症の予防又は治療剤 | |
| WO2016068278A1 (ja) | 水晶体硬化抑制剤 | |
| US9579318B2 (en) | Histamine 4 receptor partial agonists, inverse agonists or antagonists for use in treating non-autoimmune uveitis | |
| JP2010143859A (ja) | ぶどう膜炎の予防及び/又は治療のための医薬 | |
| JP2020514347A (ja) | チオトロピウムを有効成分として含有する近視予防、近視治療および/または近視進行抑制剤 | |
| WO2016006621A1 (ja) | Pgd2拮抗剤を含有するアレルギー性疾患に伴う症状の治療用医薬 | |
| US10537563B2 (en) | Methods for treating ocular disease using inhibitors of CSF-1R | |
| KR20110084514A (ko) | 피리딘-3-카르발데히드 o-(피페리딘-1-일-프로필)-옥심 유도체를 유효 성분으로서 함유하는 망맥락막 변성 질환의 치료제 | |
| KR20150051493A (ko) | 이매티닙 또는 이의 약학적으로 허용되는 염을 유효성분으로 포함하는 혈관신생 관련 질환의 예방 또는 치료용 약학적 조성물 | |
| US11584709B2 (en) | Multitarget drug for treating diseases in mammals | |
| KR101869741B1 (ko) | 마시티닙 또는 이의 약학적으로 허용되는 염을 유효성분으로 포함하는 혈관 투과성 관련 질환의 예방 또는 치료용 약학적 조성물 | |
| WO2013180209A1 (ja) | ペプチド誘導体を含有する緑内障の治療剤 | |
| JP2024516003A (ja) | 糖尿病網膜症および関連する状態を治療するための方法および組成物 | |
| AU2022264438A1 (en) | Treatment of ocular diseases using endothelin receptor antagonists | |
| KR101674457B1 (ko) | 다사티닙 또는 이의 약학적으로 허용되는 염을 유효성분으로 포함하는 혈관 투과성 관련 질환의 예방 또는 치료용 약학적 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Effective date: 20111202 Free format text: JAPANESE INTERMEDIATE CODE: A621 |
|
| A521 | Written amendment |
Effective date: 20111202 Free format text: JAPANESE INTERMEDIATE CODE: A821 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140107 |