JP2010077133A - Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト - Google Patents
Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト Download PDFInfo
- Publication number
- JP2010077133A JP2010077133A JP2009244448A JP2009244448A JP2010077133A JP 2010077133 A JP2010077133 A JP 2010077133A JP 2009244448 A JP2009244448 A JP 2009244448A JP 2009244448 A JP2009244448 A JP 2009244448A JP 2010077133 A JP2010077133 A JP 2010077133A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- antibody
- human
- antibodies
- light chain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/40—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum bacterial
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/14—Prodigestives, e.g. acids, enzymes, appetite stimulants, antidyspeptics, tonics, antiflatulents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Immunology (AREA)
- Pulmonology (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Dermatology (AREA)
- Biochemistry (AREA)
- Otolaryngology (AREA)
- Nutrition Science (AREA)
- Neurology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Tropical Medicine & Parasitology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【解決手段】ヒト・インターロイキン5に特異的で、約3.5x10−11Mに等しいかまたはそれ未満の解離定数により特徴づけられる結合アフィニティーを有する齧歯類(例えば、ラットおよびマウス)の中和モノクローナル抗体。さらに齧歯類中和モノクローナル抗体のFc領域を欠失させることにより製造される、ヒト・インターロイキン−5に特異的な中和FabフラグメントまたはそのF(ab')2フラグメント。
【選択図】なし
Description
本願は、1994年12月23日出願のU.S.第08/363,131号の一部継続出願であるU.S.第08/470,110号および08/467,420号(ともに1995年6月6日出願)の一部継続出願である。
一般的には、本発明は、IL−5および過剰な好酸球産生により媒介される症状の治療および診断に有用な抗体および変化した抗体、そしてより詳細には、mAbs、Fab、キメラおよびヒト化抗体の分野に関する。
好酸球は、肺組織の過敏反応に関連したアレルギー性疾患を包含する広範囲の炎症性疾病状態の発生に関与している(非特許文献1)。注目すべき例は喘息であり、喘息は、非特異的気管支過敏症を引き起こす気道の可逆的閉塞により特徴づけられる。さらに喘息は、気管支粘膜のレベルの慢性的炎症反応ならびにマクロファージ、リンパ球および好酸球による特徴的な炎症の発生と因果関係がある。好酸球は、疾病の典型的な粘膜ダメージの開始において中心的役割を果たしているようである(非特許文献2)。数が増加した活性化された好酸球は、慢性喘息の患者の循環系、気管支分泌物および肺の実質において報告されており、種々の肺機能試験により測定される疾病の重さは血中好酸球数と相関関係がある(非特許文献3)。また、しばしば、脱顆粒反応の過程における増加した好酸球が、後期喘息反応中の患者気管支肺胞洗浄液(BAL)中に回収され、通常には、ステロイド療法の結果としての好酸球の減少は臨床的徴候の改善に関連している(非特許文献4)。
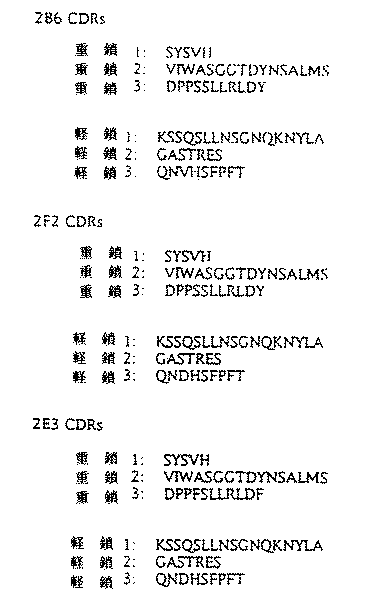
第1の態様において、本発明は、ヒト・インターロイキン5に特異的で、詳細な説明の欄において説明するように、約3.5x10−11Mに等しいかまたはそれ未満の解離定数により特徴づけられる結合アフィニティーを有する齧歯類(例えば、ラットおよびマウス)の中和モノクローナル抗体を提供する。かかるモノクローナル抗体の典型例はマウスのモノクローナル抗体2B6、2E6および2F2ならびに4A6のごときラットのモノクローナル抗体である。本発明のもう1つの態様は、SK119−2B6.206.75(1)、SK119−2E3.39.40.2、SK119−2F2.37.80.12、4A6(1)G1F7および5D3(1)F5D6のごときハイブリドーマである。
本発明は、マウス・モノクローナル抗体2B6のおいて例示されるヒト・IL−5特異性、中和活性、およびヒト・IL−5に対する高アフィニティーにより特徴づけられる種々の抗体、変化した抗体およびそれらのフラグメントを提供する。新規中和抗体を得るための慣用的なハイブリドーマ法、ファージディスプレイ組み合わせライブラリー、免疫グロブリンのチェイン・シャフリング、およびヒト化法により本発明抗体は製造された。これらの製造物は、例えば喘息のごときIL−5により媒介される疾病の治療のための治療および医薬組成物において有用である。また、これらの製造物は、ヒトにおける内在性IL−5レベルまたは活性化細胞からex vivoで放出されるIL−5レベルの測定(例えば、酵素結合免疫吸着アッセイ(ELISA))による、IL−5により媒介される症状の診断において有用である。
「変化した抗体」は、変化した免疫グロブリンコーディング領域によりコードされている蛋白をいい、選択された宿主細胞における発現により得ることができる。かかる変化した抗体は遺伝子組み換えによる抗体(例えば、キメラ抗体またはヒト化抗体)または免疫グロブリン不変領域の全部もしくは一部を欠く抗体フラグメント、例えば、Fv、Fab、またはF(ab')2等である。
本発明抗体、変化した抗体およびフラグメントの構築に使用するために、無傷のヒト・IL−5またはそれに由来するペプチドエピトープを与えることにより、非ヒト種(例えば、ウシ、ヒツジ、サル、ニワトリ、齧歯類(例えばマウスおよびラット)等)を用いて所望免疫グロブリンを得てもよい。慣用的なハイブリドーマ法を用いて、IL−5に対する非ヒト・mAbを分泌するハイブリドーマ細胞系を得る。次いで、実施例セクションに記載のごとくIL−5で被覆した96ウェルプレートを用いて、あるいは別法としてストレプトアビジンで被覆したプレートに結合したビオチン化IL−5を用いてかかるハイブリドーマを結合に関してスクリーニングする。
本発明は、ヒト・IL−5に指向されたmAb由来のFabフラグメントまたはF(ab')2フラグメントの使用も包含する。これらのフラグメントは、in vivoにおけるIL−5および好酸球により媒介される症状に対する防御剤として、あるいはin vitroでのIL−5診断薬の一部として有用である。Fabフラグメントは軽鎖全体および重鎖のアミノ末端部分を含んでおり;F(ab')2フラグメントはジスルフィド結合により結合している2個のFabフラグメントにより形成されるフラグメントである。mAbs 2B6、2E3および他の類似高アフィニティーIL−5結合抗体は、FabフラグメントおよびF(ab')2フラグメントのソースを提供するものであり、それらのフラグメントは慣用的手段、例えば、適当な蛋白分解酵素パパインおよび/またはペプシンでのmAbの開裂により、あるいは組み換え法により得ることができる。本明細書記載のごとく、これらのFabおよびF(ab')2フラグメントはそれら自体、治療、予防または診断薬、ならびに組み換え型抗体またはヒト化抗体の形成において有用な可変領域およびCDR配列を含む配列のドナーとして有用である。
上記mAb 2B6または他の抗体は、ドナー抗体の抗原結合特異性により特徴づけられる種々の変化した抗体の設計および取得に有用な配列、例えば、可変重鎖および/または軽鎖ペプチド配列、枠組み配列、CDR配列、機能的フラグメント、およびそれらのアナログ、およびそれらをコードしている核酸配列を提供する。
変化した免疫グロブリン分子は、キメラ抗体およびヒト化抗体のごとき組み換え法により抗体を包含する変化した抗体をコードしていてもよい。望ましい変化した免疫グロブリンコーディング領域はCDRをコードしている領域を含み、該領域は、IL−5抗体の抗原特異性、好ましくは本発明により提供されるような高アフィニティー抗体の抗原特異性を有するペプチドをコードしており、第1の免疫グロブリンパートナー(ヒト・枠組みまたはヒト・免疫グロブリン可変領域)中に挿入されている。
好ましくは、2B6または他の適当なドナーmAbs(例えば、2E3、2F2、4A6等)の可変軽鎖および/または重鎖配列およびCDRs、およびそれらをコードしている核酸配列を、変化した抗体、好ましくはヒト化抗体の構築に用いる。同一または類似の方法を用いて本発明の他の具体例を得てもよい。 選択されたドナーmAb、例えばマウス抗体2B6を産生するハイブリドーマを慣用的にクローンし、当業者に知られた方法、例えば、Sambrook et al., molecular Cloning (A Laboratory Manual),2nd Edition,Cold Spring Harbor Laboratory(1989)に記載の方法によりその重鎖および軽鎖可変領域のDNAを得る。ドナーmAb結合特異性を保持するのに必要な少なくともCDRをコードしている領域およびアクセプターmAb軽鎖および/または重鎖可変ドメイン枠組み領域含んでいる2B6の可変重鎖および軽鎖、ならびにヒト・免疫グロブリン由来の抗体鎖の残りの部分を、ポリヌクレオチドプライマーおよび逆転写酵素を用いて得る。既知データベースを用い、他の抗体と比較することによりCDRをコードしている領域を同定する。
適当な軽鎖可変枠組み領域を同様の方法で設計した。
また本発明は、有効量の本明細書記載の1種またはそれ以上の組み換え法による抗体または変化した抗体を包含する抗体、あるいはそれらのフラグメントを投与することを特徴とする、喘息のごとき好酸球増加症関連症候群にかかっているヒトの治療方法に関する。
ヒト・IL−5をDrosophila Schneider 2(S2)細胞において発現させ、均一に精製した。Spodoptera frugiperda 21(Sf21)細胞を用いてマウス・IL−5をバキュロウイルス中で発現させ、均一に精製した。モノクローナル抗体TRFK−5(中和ラット・抗−マウスIL−5抗体)をGenzyme Corp.(Cambridge,MA)から得た。
組み換えヒト・IL−5(IL−5)を、7匹のCAF1マウス(メス)(Charls River,Wilmington,MA)のパネルに対する免疫原として用いた。4カ月の期間にわたり、1:1の割合のTiterMAX(登録商標)(CytoRx Corp.,Norcross,GA)を用いて乳化したリン酸緩衝化食塩水(PBS)中のIL−5を動物に3回皮下注射した。最初の抗原量は50μgであり、追加免疫は25μgおよび10μgであった。追加免疫後、血清試料を集め、受容体結合阻害アッセイおよびB13増殖アッセイ(またはIL−5中和アッセイ(実施例2C))により、IL−5への結合および中和活性についてアッセイした。すべてのマウスは、IL−5に結合する血清試料を産生した。脾臓ドナーとして選択された動物を安楽死させる3日前に10μgの組み換えヒト・IL−5を静脈から追加免疫した。
Kohler et al.,Nature,256:495(1975)により初めて報告された融合法を変更して用いて、細胞単層(Kennet et al.,Eds.,"Hybridomas:A new dimension in biological analysis",pp.368-377,Plenum Press,New York)を用いる方法を行った。2匹のドナーマウスからの脾臓細胞をプールし、1千万個のSP2/0/Ag14骨髄腫細胞に対して5千万個の脾臓細胞の割合で融合を行った。融合が確認された細胞の上清を、IL−5に対する結合に関してELISAによりアッセイした。IL−5に対する抗体を産生する細胞を含むウェルを増殖させ、上清をIL−5受容体結合阻害アッセイおよびB13(中和)増殖アッセイにおいてスクリーニングした(下記)。
モノクローナル抗体2B6を産生するハイブリドーマ細胞系SK119−2B6.206.75(1)は、特許手続上の微生物の寄託に関するブダペスト条約に従って、American Type Culture Collection(ATCC),Rockville,MD,USAに受託番号HB 11783として寄託され、特許寄託物として受託された。
A. ELISA
MaxiSorb(登録商標)イムノプレート(Nunc,Naperville,IL)の個々のウェルを、0.05M炭酸バッファーpH9.6中0.2μgのIL−5で被覆した。4℃で一晩インキュベーション後、0.025% TweenR20含有PBSでプレートをすすぎ、0.025% TweenR20含有PBS中1% BSAにて室温で2時間ブロックした。未希釈ハイブリッド上清をIL−5被覆ウェルに添加し、室温で2時間インキュベーションした。プレートをすすいだ後、ヤギ・抗−マウスIgGおよびIgM標識ペルオキシダーゼ(Boehrionger Mannheim,Indianapolis,IN)を、1% BSAおよび0.025%TweenR20含有PBS中1/7500希釈して添加した。15分後、VMax(登録商標)マイクロプレートリーダー(Molecular Devices, Menlo Park,CA)により450nmにおいてプレートを読んだ。
ヒト・IL−5受容体(IL−5R)のα−鎖を発現するDrosophila S2細胞の膜抽出物を用いて受容体へのIL−5の結合に対する抗体の効果を測定した。膜を調製するために、109個の細胞を1000xg、4℃、10分間ペレット化した。細胞ペレットをドライアイス/エタノール浴で15分凍結した。ペレットを融解し、4℃の10mlのPBSに再懸濁し、1000xgで10分間ペレット化した。細胞ペレットをPBSで2回洗浄し、13.5mlの低張バッファー(10mM Tris pH7.5、3mM MgCl2、1mM ジチオスレイトール、1mM フェニルメチルスルホニルフルオリド、1μM ロイペプチン、1μM ペプスタチンA)に再懸濁し、氷上で5分間インキュベーションした。細胞懸濁液を15mlのDounceホモジナイザーでホモジナイズし、2.5M蔗糖溶液を用いて蔗糖最終濃度0.25Mとした。1000xgで15分の遠心分離により細胞残渣を除去した。細胞膜を100000xg、4℃で90分間ペレット化し、10mM Tris pH7.5、3mM MgCl2、250mM 蔗糖中に再懸濁し、−70℃で保存した。
親切にも、R.Palacios(Basel Institute of Immunology,Switzerland)からマウス・IL−5/IL−3依存性細胞系LyH7.B13(B13)を得た。L−グルタミン、非必須アミノ酸、ピルビン酸ナトリウム、ペニシリン−ストレプトマイシン(すべてGibcoBRL)ならびに2−メルカプトエタノール(5x10−5M,Sigma)、10% ウシ胎児血清(Globepharm,Surrey,UK)および1〜10ユニットのマウス・IL−5を補足したRPMI 1640培地(GibcoBRL, Renfrewshire,UK)中で1週間に2回細胞をサブクローンした。アッセイのために、96ウェル丸底プレート中、適当に希釈した試験試料の存在下、3系で48時間培養し、次いで、0.5μCiの3H−チミジン(Amersham,Bucks,UK)を添加して最後の4時間のインキュベーションを行った。それらを1205 Beteplate(LKB Wallac,Beds,UK)におけるシンチレーションカウンティングのために処理した。
固定化hIL−5と抗体に関する速度論的平衡結合特性を、BIAcore光学的バイオセンサー(Pharmacia Biosensor,Uppsala,Sweden)を用いて行った。以前に記載されているようにして(Karlsson et al.,J.Immunol.Meth.,145:229-240(1991)(その全体を参照により本明細書に記載されているものと見なす))速度論的データを評価した。
A. PCRおよび組み合わせライブラリーの構築
Huse et al.Science,246:1275(1989)およびKang,S.A.Methods:Comparison Methods Enzymol.,2:111(1991)(それら全体を参照により本明細書に記載されているものと見なす)により記載されたようにして、3匹のマウスの脾臓から精製したRNAを、cDNAキット(Boehringer Mannheim,Indianapolis,IN)により逆転写した(キット付属のプライマー(dT)15または3’Fd(IgG1、IgG2aおよびIgG3)およびカッパ軽鎖プライマーを用いる)。記載されたプライマーおよび温度サイクリング条件(上記Huseら)を用いてPCRにより免疫グロブリンcDNAを増幅した。AmpliWaxTMPCR Gem 100(Perkin Elmer Cetus,Norwalk,CT)ビーズおよび製造者のプロトコールを用いるホット・スタート(Hot Start)法をすべての反応に使用した。PCR生成物をゲル精製し、消化し、pMKFabGene3ベクター(Ames et al.,J.Immunol.,512:4572(1994))中に連結した。Fd cDNAを用いる連結後のライブラリー力価は5.1X107CFUであり、カッパcDNAを用いるライゲーション後の力価は1.5X106CFUであった。ファージミドライブラリーを用いて形質転換されたXL1-Blue細胞(Stratagene,La Jolla,CA)を、ヘルパーファージVCSM13(Stratagene)に感染させ、Barbas and Lerner,Methosa:Comparison Methods Enzymol.,2:119(1991)により記載されたようにしてファージを調製した。
4つのマイクロタイターウェル(Immulon II Removawell Strips,Dynatech Laboratories Inc.,Chantilly,VA)を、0.1M重炭酸,pH8.6中IL−5(1μg/ウェル)で4℃において被覆した。ウェルを水洗し、3% BSA含有PBSを用いて37℃で1時間ブロックした。ブロッキング溶液を除去し、ライブラリーをマイクロタイターウェルに添加し(50μl/ウェル)、37℃で2時間インキュベーションした。ウェルをTBS/TweenR(50mM Tris−HCl,pH7.5、150mM NaCl、0.5% TweenR20)で10回洗浄し、水で1回洗浄し、次いで、0.1M HCl(1mg/ml BSA含有グリシンでpH2.2に調節)で付着ファージを溶離した。
バイオパンニングの第3ラウンドおよび第4ラウンドから単離されたコロニーからのコロニー釣菌を記載されたようにして(Barbas and Lerner、上記)行った。0.5〜1.0μCiの125I−IL−5とともにフィルターを室温で1時間インキュベーションし、製造者の推奨手順に従ってBolton-Hunter試薬(NEN,Billerica,MA)を用いて1% BSA含有PBS中でヨウ素化し、PBS 0.25% Tweenで洗浄し、Kodak XARフィルムにさらした。IL−5反応性Fabsを発現しているコロニーをオートラジオグラフィーにより検出した。
ファージミドDNAをNheIおよびSpeIで消化して遺伝子IIIを除去し、自己連結させた。XL1−Blue細胞を形質転換し、単離されたコロニーを、1%グルコースおよび50μg/mlカルベニシリンを含有する5.0mlのスーパーブロス(SB)培地(30gトリプトン、20g酵母エキス、10gの3−[N−モルホリノ]プロパンスルホン酸(MOPS)、pHを7に調節)中で37℃で一晩増殖させた。この培養1mlからの細胞をBeckman GS-6R遠心分離機にて3500rpmで10分間ペレット化し、50μg/mlのカルベニシリンを含有する5mlのSBに植菌した。培養物を37℃で1時間振盪し、イソプロピル−b−D−チオガラクトピラノシド(IPTG;1mM)を添加し、培養物を28℃に移し、一晩おいた。30mM Tris pH8.0に懸濁した20%蔗糖中、4℃で20分間細胞を溶解し、次いで、微量遠心機で10分間遠心分離することによりペリプラスム抽出物から可溶性Fabを調製した。ウェルタンブロットにより、既知量のマウス・Fabを含有する試料と比較することによってFab濃度を評価した。別の細菌のペリプラスム抽出物は同様の濃度のFabを含んでおり、ウェスタンブロット分析による分析では1ないし20μg/mlの範囲であった。
重鎖のカルボキシ末端上にキレートするペプチドを加工作成して蛋白精製の助けとした。NheIおよびSpeIでの消化によるM13遺伝子IIIコーディング領域の除去後、6個のヒスチジン残基をコードしている1対の重複オリゴヌクレオチド:[配列番号:43]5’−CTAGCCACCACCACCACCACCACTAA−3’;[配列番号:44]3’−GGTGGTGGTGGTGGTGGTGATTGATC−5’をFab発現ベクター中にサブクローンした。上記のごとくFab発現の誘導を行った。28℃で一晩インキュベーションした後、20%蔗糖、30mM Tris pH8.0中4℃で30分インキュベーションすることにより細胞ペレットのペリプラスム溶解物を調製した。尿素およびBrij−35界面活性剤を清澄化した上清に添加して、最終濃度をそれぞれ、2Mおよび1%とした。室温で1時間撹拌後、処理され清澄化された上清を、5mlのニッケル−NTA金属キレーティングカラム(1.5x3cm)(バッファーA(100mM Na−リン酸、10mM Tris、0.3M NaCl、2M尿素,pH8.0)で平衡化されている)に、流速0.5ml/分で直接負荷した。4カラム体積分(20ml)の洗浄後、上と同じバッファー中pHを8から4にする6カラム体積分(30ml)の逆pHグラジエントで結合物質を溶離した。精製されたFabsは、pH5.5において対称形の鋭いピークとなってカラムから溶出した。精製Fabsは>90%の純度であり、DNA不含であった。
0.1M重炭酸バッファー,pH8.6に懸濁された(1mg/ml;ウェル1個あたり50ml)蛋白でImmulon IIプレート(Dynatech)を4℃で一晩被覆した。0.05% Tween(登録商標)20含有PBSにて希釈および洗浄を行った。プレートを洗浄し、1%BSA含有PBSにて室温で1時間ブロッキングした。可溶性Fabを含有する細菌懸濁液の種々の希釈物、または精製Fabsをプレートに添加した。1時間インキュベーション後、プレートを洗浄し、ビオチン化ヤギ・抗−マウスカッパ(Southern Biotechnology Associates,Inc.,Birmingham,AL)を添加(1:2000希釈;50μl/ウェル)して1時間おいた。プレートを洗浄し、ストレプトアビジン標識セイヨウワサビペルオキシダーゼを添加し(1:2000希釈;50μl/ウェル)1時間おいた。プレートを洗浄し、ABTSペルオキシダーゼ基質を添加し(100μl/ウェル;Kirkegaard & Perry Laboratories,Gaithersberg,MD)、405nmにおける光学密度をUVmax(登録商標)(Molecular Devices)マイクロプレートリーダーで読んだ。
IL−5で被覆したマイクロタイターウェルに対する複数ラウンドのバイオパンニングにより、IL−5に対するFabsを有するファージをライブラリーから選択した。4ラウンドの選択後、125I−IL−5を用いるコロニー釣菌アッセイによりIL−5反応性Fabsが同定された。第3ラウンドから34個のコロニーが、第4ラウンドから4個のコロニーが同定され、それらは標識IL−5に結合した。Fab−遺伝子III融合蛋白を発現している培養上清を用いる直接結合ELISAによりIL−5への結合を確認した。これらのコロニーからDNAを単離し、M13遺伝子IIIのコーディング領域を除去後、可溶性Fabの発現を誘導した。ペリプラスムフラクションを調製し、IL−5への結合についてELISAによりアッセイした。Fabは、別の蛋白rC5aへの結合を示すことなくIL−5に特異的に結合した。
FdおよびmAb(2B6)のκcDNAを、上記条件を用いるPCRにより単離した。ゲル精製したフラグメントをpMKFabGene3ベクター中にサブクローンし、これを修飾して遺伝子IIIのcDNAの3’末端にヘキサ−His配列を含むようにして、プラスミドpMKFabGene3Hを得た。2B6重鎖および軽鎖を有する機能的なIL−5結合Fabクローンをコロニー釣菌アッセイにより同定した。NheI/SpeI消化による遺伝子IIIの除去および自己連結を行って、重鎖をイン−フレームでヘキサ−Hisに融合させ、上記のごとく精製を可能にした。このFabは用量依存的に受容体結合を阻害し、IC50は約7.5μg/mlであり、親mAbであるマウス・2B6のIC50と同様であった。
中和mAb 2B6のFdをコードしているcDNAを、XhoI/SpeIフラグメントとしてpMKFabGene3H中にサブクローンして、軽鎖cDNAのかわりにSstI/XbaIフラグメントを含ませた。このファージミドをSstIおよびXbaIで消化し、IL−5免疫マウス由来(上記)のSstI/XbaI消化された軽鎖のPCR生成物と連結した。連結後のライブラリー力価は4x105CFUであった。バイオパンニングおよびコロニー釣菌アッセイを、組み合わせライブラリーに関して上で説明したように行った。
マウス・CDRsをヒト化抗体枠組み中に含むように1のヒト化抗体を設計した。下記操作を行うことにより、IL−5特異的マウス・抗体2B6のこのヒト化バージョンを調製した。
Boehringer Mannheim(Indianapolis,IN)から得たキットを用いて2B6、2F2および2E3ハイブリドーマ細胞系(実施例1)のそれぞれからmRNAを単離し、次いで、cDNAキット(Boehringer Mannheim)付属のプライマー(dT)15を用いて逆転写してcDNAを作成した。マウス・免疫グロブリンに特異的なPCRプライマーを用いて、重鎖可変領域のアミノ酸9(KABATナンバーリングシステム)からヒンジ領域まで伸長しているドメインならびに軽鎖可変領域のアミノ酸9(KABATナンバーリングシステム)から不変領域の末端まで伸長しているドメインをコードしているDNAを増幅した。独立別個のPCR反応により各抗体鎖の数個のクローンを得た。
マウス・軽鎖可変領域プライマーは[配列番号:26]:5’CCAGATGTGAGCTCGTGATGACCCAGACTCCA3’であった。
上記Aで得た重鎖および軽鎖マウスcDNAクローンを配列決定した。これらのクローンの可変領域の配列決定結果を配列番号:1〜6(図1〜6)に示す。各クローンは、マウス・重鎖可変領域または軽鎖可変領域間で保存されていることが知られているアミノ酸を含んでいた。CDRアミノ酸配列を以下に記載する。 2B6重鎖に関するCDR領域は配列番号:7、8および9である。図7参照。これらの配列は配列番号:1によりコードされている。軽鎖に関するCDR領域は配列番号:10、11および12である。図7参照。これらの配列は配列番号:2によりコードされている。
2B6のクローニング後、KABATおよびSWISS−PROT(Nuc. Acids Res.,20:2019-2022(1992))蛋白配列データベースにおいて可変領域重鎖および軽鎖のアミノ酸配列(図1および2)(それぞれ配列番号:15および16)を既知マウス・免疫グロブリン配列と比較してN末端残基に割り当てた。次いで、2B6重鎖および軽鎖可変領域の推定アミノ酸配列をヒト・免疫グロブリン蛋白配列データベースと比較して、マウス配列に最もぴったりと合致する重鎖および軽鎖両方のヒト・枠組みを同定した。さらに、CDR表現に影響しうるアミノ酸による潜在的矛盾を評価するためにFabドメインの構造的モデルから得られた位置のデータベースを用いて重鎖および軽鎖を評価した。矛盾位置における対応マウス・アミノ酸の置換により、ヒト化可変領域枠組みの合成中に矛盾は解決された。
2B6重鎖CDRs[図7および配列番号:1〜2]およびヒト・抗体の枠組み配列を得て、合成重鎖可変領域[配列番号:18]を作成した。結合した場合にアミノ酸21〜106(KABAT番号付け)をコードすることとなる4つの合成オリゴヌクレオチド[配列番号:27および28][配列番号:29および30]を用いてこれを作成した。次いで、COR枠組み(上記)に基づく別のヒト化重鎖由来の配列を含むpUC18をベースにしたプラスミドのHpaI−KpnI制限部位中にオリゴヌクレオチドを連結した。このプラスミドはシグナル配列[配列番号:17]および残りの可変領域配列を提供する。変異原性プライマーを用いるPCRまたは存在する制限部位中への合成リンカーの付加により、マッピングされた配列中のエラーを修正した。
IgG1イソタイプ由来のヒト化重鎖には配列番号:19に示す合成重鎖可変領域を用いる。2B6重鎖CDRsを含んでいるこの合成VHを上記のごとく設計し、合成した。
CHOにより発現されたキメラおよびヒト化2B6の精製を、慣用的なプロテインA(またはG)アフィニティークロマトグラフィー、次いで、イオン交換および分子ふるいクロマトグラフィーにより行うことができる。同様のプロセスをうまく用いて他のmAbs(例えば、呼吸器合胞体ウイルス、インターロイキン−4およびマラリアサーカムスポロゾイトに対するもの)の純度95%以上の精製が行われている。
プラスミドpCDIL5HZHC1.0[配列番号:49]を得てから、枠組み位置73のスレオニンをアスパラギンに置換した発現プラスミドpCDIL5HZHC1.1を作成した。EcoRVおよびXhoI末端[配列番号:51および配列番号:52]を有する合成リンカーを、同様にして消化されたpCDIL5HZHC1.0中に連結することにより、これを作成した。同様にして、発現プラスミドpCDIL5HZH1.2は、枠組み位置37においてバリンのかわりにイソロイシンを有する。HpaIおよびXbaI末端[配列番号:53および配列番号:54]を有する合成リンカーを、同様にして消化されたpCDIL5HZHC1.0中に連結することにより、これを作成した。さらに、HpaIおよびXbaI末端[配列番号:53および配列番号:54]を有する合成リンカーを、同様にして消化されたpCDIL5HZHC1.1中に連結することにより、pCDIL5HZHC1.3を作成した。
マウス・mAb 2B6重鎖可変領域のアミノ酸9〜104(KABAT番号付け)をコードしているDNAを、2B6ハイブリドーマ細胞系から得たcDNA(実施例4参照)のpGEM7Zf(+)をベースにしたPCRクローンpGEM7Zf(+)からAvaII−StyI制限フラグメントとして単離した。このフラグメントを4つの小型合成オリゴマーリンカー[配列番号:35および36][配列番号:37および38]とともにpUC18をベースにしたプラスミド(BstXI−HindIIIで消化)中で一緒にすることにより、隣接重鎖可変領域配列およびシグナル配列[配列番号:17]を提供した。密接に関連したマウス・重鎖から推定されたN末端アミノ酸のコンセンサスを、最初の8個のVH残基に関して帰属し、それらは配列番号:35および36中にコードされている。2B6重鎖の最初の15個のN末端アミノ酸を配列決定することにより重鎖の推定アミノ酸配列を確かめた。
40中にコードされている。2B6軽鎖の最初の15個のN末端アミノ酸を配列決定することにより軽鎖の推定アミノ酸配列を確かめた。次いで、この可変領域をEcoRV−NarIフラグメントとして単離し、すでにヒト・カッパ領域およびシグナル配列を含んでいる発現ベクターpCN中に連結した。
SEQ ID NO: 2: First base corresponds to Kabat position 25
SEQ ID NO: 3: First base corresponds to Kabat position 24
SEQ ID NO: 4: First base corresponds to Kabat 25
SEQ ID NO: 5: First base corresponds to Kabat position 24
SEQ ID NO: 6: First base corresponds to Kabat position 25
SEQ ID NO: 17: signal sequence
SEQ ID NO: 18: heavy chain variable region
SEQ ID NO: 19: heavy chain variable region
SEQ ID NO: 20: light chain variable region
SEQ ID NO: 21: light chain variable region
SEQ ID NO: 22: mouse gamma 1 hinge region primer
SEQ ID NO: 23: mouse gamma 2a hinge region primer
SEQ ID NO: 24: mouse heavy chain variable region primer
SEQ ID NO: 25: mouse kappa chain constant region primer
SEQ ID NO: 26: mouse light chain variable region primer
SEQ ID NO: 27: oligonucleotide encodes a part of heavy chain variable region
SEQ ID NO: 28: oligonucleotide encodes a part of heavy chain variable region
SEQ ID NO: 29: oligonucleotide encodes a part of heavy chain variable region
SEQ ID NO: 30: oligonucleotide encodes a part of heavy chain variable region
SEQ ID NO: 31: oligonucleotide encodes a part of light chain variable region
SEQ ID NO: 32: oligonucleotide encodes a part of light chain variable region
SEQ ID NO: 33: oligonucleotide encodes a part of light chain variable region
SEQ ID NO: 34: oligonucleotide encodes a part of light chain variable region
SEQ ID NO: 35: small synthetic oligomer linker
SEQ ID NO: 36: small synthetic oligomer linker
SEQ ID NO: 37: small synthetic oligomer linker
SEQ ID NO: 38: small synthetic oligomer linker
SEQ ID NO: 39: small synthetic oligomer linker
SEQ ID NO: 40: small synthetic oligomer linker
SEQ ID NO: 41: small synthetic oligomer linker
SEQ ID NO: 42: small synthetic oligomer linker
SEQ ID NO: 43: overlapping oligonucleotide
SEQ ID NO: 44: overlapping oligonucleotide
SEQ ID NO: 45: light chain
SEQ ID NO: 46: light chain
SEQ ID NO: 47: CDR3
SEQ ID NO: 48: CDR3
SEQ ID NO: 49: heavy chain
SEQ ID NO: 50: light chain
SEQ ID NO: 51: linker
SEQ ID NO: 52: linker
SEQ ID NO: 53: linker
SEQ ID NO: 54: linker
SEQ ID NO: 55: linker
SEQ ID NO: 56: linker
SEQ ID NO: 57: overlapping synthetic oligonucleotide
SEQ ID NO: 58: overlapping synthetic oligonucleotide
SEQ ID NO: 59: overlapping synthetic oligonucleotide
SEQ ID NO: 60: overlapping synthetic oligonucleotide
SEQ ID NO: 61: heavy chain variable region
SEQ ID NO: 62: heavy chain variable region
SEQ ID NO: 63: PCR primer
SEQ ID NO: 64: PCR primer
SEQ ID NO: 65: overlapping synthetic oligonucleotide
SEQ ID NO: 66: overlapping synthetic oligonucleotide
SEQ ID NO: 67: overlapping synthetic oligonucleotide
SEQ ID NO: 68: overlapping synthetic oligonucleotide
SEQ ID NO: 69: light chain variable region
SEQ ID NO: 70: light chain variable region
SEQ ID NO: 71: PCR primer
SEQ ID NO: 72: PCR primer
SEQ ID NO: 73: synthetic linker
SEQ ID NO: 74: synthetic linker
SEQ ID NO: 75: synthetic oligonucleotide linker
SEQ ID NO: 76: synthetic oligonucleotide linker
Claims (4)
- 重鎖および軽鎖を含んでなるヒト・インターロイキン−5に特異的なヒト化抗体であって、該重鎖および軽鎖の枠組み領域が少なくとも1の選択された抗体に由来するものであり、各鎖の相補性決定領域のアミノ酸配列がAmerican Type Culture Collection(ATCC)受託番号HB 11783、HB 11782、HB 11781、HB 11943、HB 11780またはHB 11942を有するハイブリドーマ細胞系の1つにより産生される、ヒト・インターロイキン−5に特異的な齧歯類の中和モノクローナル抗体に由来するものであるヒト化抗体。
- 請求項1のヒト化抗体および医薬上許容される担体を含んでなる、IL−5を中和するための組成物であって、過剰な好酸球産生、アレルギー性鼻炎、喘息、慢性好酸球性肺炎、アレルギー性気管支肺アスペルギルス症、セリアック病、好酸球性胃腸炎、Churg-Strauss症候群(結節性動脈周囲炎およびアトピー)、好酸球性筋肉痛症候群、過好酸球増加症候群、血管皮膚炎を包含する水腫性反応(ここで、好酸球は防御的役割をしている可能性がある)、ぜん虫感染、オンコセルカ皮膚炎、またはアトピー性皮膚炎からなる群より選択される症状の処置のための組成物。
- 配列番号:19の重鎖可変領域および配列番号:21の軽鎖可変領域を含む、ヒト化抗体。
- 請求項3のヒト化抗体および医薬上許容される担体を含んでなる、IL−5を中和するための組成物であって、過剰な好酸球産生、アレルギー性鼻炎、喘息、慢性好酸球性肺炎、アレルギー性気管支肺アスペルギルス症、セリアック病、好酸球性胃腸炎、Churg-Strauss症候群(結節性動脈周囲炎およびアトピー)、好酸球性筋肉痛症候群、過好酸球増加症候群、血管皮膚炎を包含する水腫性反応(ここで、好酸球は防御的役割をしている可能性がある)、ぜん虫感染、オンコセルカ皮膚炎、またはアトピー性皮膚炎からなる群より選択される症状の処置のための組成物。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US36313194A | 1994-12-23 | 1994-12-23 | |
| US08/363,131 | 1994-12-23 | ||
| US08/467,420 | 1995-06-06 | ||
| US08/470,110 | 1995-06-06 | ||
| US08/467,420 US5683892A (en) | 1994-12-23 | 1995-06-06 | DNA encoding recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders |
| US08/470,110 US5693323A (en) | 1994-12-23 | 1995-06-06 | Recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007269236A Division JP2008029355A (ja) | 1994-12-23 | 2007-10-16 | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012220614A Division JP2013091636A (ja) | 1994-12-23 | 2012-10-02 | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010077133A true JP2010077133A (ja) | 2010-04-08 |
| JP5177444B2 JP5177444B2 (ja) | 2013-04-03 |
Family
ID=23428947
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009244448A Expired - Lifetime JP5177444B2 (ja) | 1994-12-23 | 2009-10-23 | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト |
| JP2012220614A Pending JP2013091636A (ja) | 1994-12-23 | 2012-10-02 | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012220614A Pending JP2013091636A (ja) | 1994-12-23 | 2012-10-02 | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト |
Country Status (11)
| Country | Link |
|---|---|
| US (5) | US5683892A (ja) |
| EP (1) | EP1749840A3 (ja) |
| JP (2) | JP5177444B2 (ja) |
| KR (1) | KR100511544B1 (ja) |
| CN (1) | CN101353381A (ja) |
| CY (2) | CY2592B2 (ja) |
| FR (1) | FR15C0089I2 (ja) |
| HU (1) | HUS1500070I1 (ja) |
| NO (1) | NO2018035I1 (ja) |
| PT (1) | PT800536E (ja) |
| ZA (1) | ZA9510965B (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013157105A1 (ja) * | 2012-04-18 | 2013-10-24 | 公立大学法人大阪市立大学 | ムチンサブタイプ5ac特異的ヒト化抗体およびその利用 |
| WO2013157102A1 (ja) * | 2012-04-18 | 2013-10-24 | 公立大学法人大阪市立大学 | ムチンサブタイプ5ac特異的ヒト化抗体およびその利用 |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5683892A (en) * | 1994-12-23 | 1997-11-04 | Smithkline Beecham Corporation | DNA encoding recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders |
| US7399837B2 (en) * | 1995-12-22 | 2008-07-15 | Smithkline Beecham Corporation | Recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders |
| CA2208503C (en) * | 1994-12-23 | 2009-12-01 | Smithkline Beecham P.L.C. | Recombinant il-5 antagonists useful in treatment of il-5 mediated disorders |
| FR2783326B1 (fr) * | 1998-09-10 | 2000-12-01 | Immunotech Sa | Procede de detection ou de quantification des basophiles et des eosinophiles |
| WO2001025277A1 (en) * | 1999-10-07 | 2001-04-12 | Maxygen Aps | Single-chain antagonist polypeptides |
| PT1527100E (pt) * | 2002-03-29 | 2009-08-25 | Schering Corp | Anticorpos monoclonais humanos para interleucina-5 e métodos e composições compreendendo os mesmos |
| US7718076B1 (en) | 2006-02-14 | 2010-05-18 | Charles Lonnie Meurer | Methods of and common gantry drive for single-pass cleaning of multiple stages of a material separation and removal system |
| US7780015B1 (en) | 2006-08-24 | 2010-08-24 | Meurer Research, Inc. | Methods of and sludge collector with adjacent opposed oppositely-moving blades for moving sludge in a basin |
| ES2492943T3 (es) | 2007-04-30 | 2014-09-10 | Glaxosmithkline Llc | Procedimientos de administración de anticuerpos anti-IL5 |
| MX2010010667A (es) | 2008-03-28 | 2010-11-09 | Glaxosmithkline Llc | Metodos de tratamiento. |
| AU2011349049B2 (en) | 2010-12-22 | 2016-08-11 | Teva Pharmaceuticals Australia Pty Ltd | Modified antibody with improved half-life |
| US10870695B2 (en) | 2015-08-24 | 2020-12-22 | Glaxosmithkline Intellectual Property (No. 2) Limited | Biopharmaceutical compositions comprising interleukin-5 antibody |
| KR102651290B1 (ko) | 2016-12-23 | 2024-03-25 | 세파론 엘엘씨 | 항-il-5 항체 |
| US20190389958A1 (en) * | 2017-01-31 | 2019-12-26 | Msm Protein Technologies, Inc. | Anti-cxcr4 antibodies |
| AU2018219864A1 (en) * | 2017-02-10 | 2019-08-29 | Mayo Foundation For Medical Education And Research | Trailshort antibody and methods of use |
| MX2019014105A (es) * | 2017-05-26 | 2020-02-07 | Glaxosmithkline Ip Dev Ltd | Composiciones biofarmaceuticas y metodos relacionados. |
| US11390671B2 (en) | 2017-06-06 | 2022-07-19 | Glaxosmithkline Llc | Biopharmaceutical compositions and methods for pediatric patients |
| KR20200059239A (ko) * | 2017-09-29 | 2020-05-28 | 지앙수 헨그루이 메디슨 컴퍼니 리미티드 | Il-5 항체, 이의 항원 결합 단편 및 이의 의학적 적용 |
| CN109942706A (zh) * | 2017-12-21 | 2019-06-28 | 三生国健药业(上海)股份有限公司 | 结合人il-5的单克隆抗体、其制备方法和用途 |
| CN113769081A (zh) * | 2020-06-10 | 2021-12-10 | 三生国健药业(上海)股份有限公司 | 一种稳定的高浓度抗人il-5单克隆抗体液体制剂 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1993016184A1 (en) * | 1992-02-06 | 1993-08-19 | Schering Corporation | Design, cloning and expression of humanized monoclonal antibodies against human interleukin-5 |
| JPH06141885A (ja) * | 1992-11-05 | 1994-05-24 | Chemo Sero Therapeut Res Inst | モノクローナル抗体 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8800397D0 (en) | 1988-01-08 | 1988-02-10 | Sandoz Ltd | Improvements in/relating to organic compounds |
| IL92180A (en) * | 1988-11-03 | 1997-04-15 | Schering Corp | Pharmaceutical composition for preventing or reducing eosinophilia |
| US5096704A (en) * | 1988-11-03 | 1992-03-17 | Schering Corporation | Method of treating eosinophilia |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| IL162181A (en) * | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| ATE151113T1 (de) * | 1992-01-23 | 1997-04-15 | Merck Patent Gmbh | Fusionsproteine von monomeren und dimeren von antikörperfragmenten |
| AU1289795A (en) | 1993-11-19 | 1995-06-06 | Baylor College Of Medicine | Monoclonal antibodies specific for human interleukin-5 |
| GB9412230D0 (en) * | 1994-06-17 | 1994-08-10 | Celltech Ltd | Interleukin-5 specific recombiant antibodies |
| US5683892A (en) | 1994-12-23 | 1997-11-04 | Smithkline Beecham Corporation | DNA encoding recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders |
| US5783184A (en) | 1994-12-23 | 1998-07-21 | Smithkline Beecham Corporation | Method for treatment and diagnosis of IL-5 mediated disorders |
| CA2208503C (en) * | 1994-12-23 | 2009-12-01 | Smithkline Beecham P.L.C. | Recombinant il-5 antagonists useful in treatment of il-5 mediated disorders |
| WO2001012646A1 (en) | 1999-08-19 | 2001-02-22 | Smithkline Beecham Corporation | Sialoadhesin factor-1 agonist and antagonist antibodies |
-
1995
- 1995-06-06 US US08/467,420 patent/US5683892A/en not_active Expired - Lifetime
- 1995-06-06 US US08/470,110 patent/US5693323A/en not_active Expired - Lifetime
- 1995-12-22 KR KR10-2004-7015736A patent/KR100511544B1/ko not_active IP Right Cessation
- 1995-12-22 PT PT95944692T patent/PT800536E/pt unknown
- 1995-12-22 CN CNA200710186675XA patent/CN101353381A/zh active Pending
- 1995-12-22 EP EP06124848A patent/EP1749840A3/en not_active Ceased
- 1995-12-27 ZA ZA9510965A patent/ZA9510965B/xx unknown
-
1997
- 1997-09-30 US US08/940,371 patent/US5851525A/en not_active Expired - Lifetime
-
2002
- 2002-05-13 US US10/144,644 patent/US20030059429A1/en not_active Abandoned
-
2003
- 2003-11-04 US US10/700,740 patent/US6946130B2/en not_active Expired - Fee Related
-
2008
- 2008-05-16 CY CY0800009A patent/CY2592B2/xx unknown
-
2009
- 2009-10-23 JP JP2009244448A patent/JP5177444B2/ja not_active Expired - Lifetime
-
2012
- 2012-10-02 JP JP2012220614A patent/JP2013091636A/ja active Pending
-
2015
- 2015-12-16 FR FR15C0089C patent/FR15C0089I2/fr active Active
- 2015-12-17 HU HUS1500070C patent/HUS1500070I1/hu unknown
- 2015-12-18 CY CY2015056C patent/CY2015056I1/el unknown
-
2018
- 2018-10-04 NO NO2018035C patent/NO2018035I1/no unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1993016184A1 (en) * | 1992-02-06 | 1993-08-19 | Schering Corporation | Design, cloning and expression of humanized monoclonal antibodies against human interleukin-5 |
| JPH06141885A (ja) * | 1992-11-05 | 1994-05-24 | Chemo Sero Therapeut Res Inst | モノクローナル抗体 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013157105A1 (ja) * | 2012-04-18 | 2013-10-24 | 公立大学法人大阪市立大学 | ムチンサブタイプ5ac特異的ヒト化抗体およびその利用 |
| WO2013157102A1 (ja) * | 2012-04-18 | 2013-10-24 | 公立大学法人大阪市立大学 | ムチンサブタイプ5ac特異的ヒト化抗体およびその利用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2013091636A (ja) | 2013-05-16 |
| FR15C0089I1 (ja) | 2016-12-02 |
| US20030059429A1 (en) | 2003-03-27 |
| CY2592B2 (en) | 2009-11-04 |
| CN101353381A (zh) | 2009-01-28 |
| NO2018035I1 (no) | 2018-10-04 |
| FR15C0089I2 (fr) | 2016-07-01 |
| US5683892A (en) | 1997-11-04 |
| US5851525A (en) | 1998-12-22 |
| EP1749840A3 (en) | 2008-10-15 |
| CY2015056I2 (el) | 2016-06-22 |
| US5693323A (en) | 1997-12-02 |
| ZA9510965B (en) | 1996-09-16 |
| CY2015056I1 (el) | 2016-08-31 |
| KR100511544B1 (ko) | 2005-08-31 |
| EP1749840A2 (en) | 2007-02-07 |
| US6946130B2 (en) | 2005-09-20 |
| KR20040101388A (ko) | 2004-12-02 |
| US20040156850A1 (en) | 2004-08-12 |
| HUS1500070I1 (hu) | 2017-07-28 |
| JP5177444B2 (ja) | 2013-04-03 |
| PT800536E (pt) | 2007-02-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5177444B2 (ja) | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト | |
| US7399837B2 (en) | Recombinant IL-5 antagonists useful in treatment of IL-5 mediated disorders | |
| JP4954104B2 (ja) | Il−5介在障害を治療および診断するための改良方法 | |
| JP2008029355A (ja) | Il−5により媒介される疾病の治療に有用な組み換えil−5アンタゴニスト | |
| EP1163271B1 (en) | Recombinant il-18 antibodies and their use | |
| EP0730609B1 (en) | Recombinant il4 antibodies useful in treatment of il4 mediated disorders | |
| US7807793B2 (en) | Recombinant IL4 antibodies useful in treatment of IL4 mediated disorders | |
| WO1995001997A1 (en) | RECOMBINANT AND HUMANIZED IL-1β ANTIBODIES FOR TREATMENT OF IL-1 MEDIATED INFLAMMATORY DISORDERS IN MAN | |
| KR100509993B1 (ko) | Il-5 매개된 질환의 치료에 유용한 재조합 il-5 길항제 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111220 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20120309 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120319 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120807 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121002 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20121108 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121225 |
|
| EXPY | Cancellation because of completion of term |