6. 好ましい実施形態の説明
本発明は、変異型重鎖を含む分子、好ましくはポリペプチド、より好ましくは免疫グロブリン(例えば、抗体)に関し、前記変異型重鎖は、2種以上のIgGアイソタイプ由来のドメインまたは領域を含む。ある実施形態では、本発明は、IgG1のCH1およびヒンジドメインならびにIgG2、IgG3またはIgG4のFc領域を含む分子に関する。本発明はさらに、IgG2、IgG3またはIgG4由来のドメインまたは領域、および1つまたは複数の領域中の1種または複数のアミノ酸改変(例えば、置換、ならびに挿入または欠失を含む)を有する変異型重鎖を含む分子を包含し、この改変は、FcγRに対する前記変異型重鎖のFc領域の親和性を変更する、例えば、増大または低下させる。いくつかの実施形態では、本発明は、それだけに限らないが、米国特許出願公開第2005/0037000号、2003年1月9日出願の米国特許仮出願第60/439,498号、2003年3月19日出願の米国特許仮出願第60/456,041号、2003年10月23日出願の米国特許仮出願第60/514,549号、2004年7月12日出願の米国特許仮出願第60/587,251号、2004年12月13日出願の米国特許仮出願第60/636,056号、2004年11月10日出願の米国特許仮出願第60/626,510号および2005年8月10日出願の米国特許仮出願第60/707,419号に開示された改変のいずれも含む変異型重鎖のFc領域に対する改変を含む。上記出願のそれぞれは、その全体が参照により本明細書に組み込まれている。いくつかの実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を提供し、重鎖-抗体受容体相互作用、特にFc-FcγR相互作用を決定するための当業者に公知の方法および本明細書に開示の方法、例えば、ELISAアッセイまたは表面プラズモン共鳴アッセイにより決定した場合、この変異型重鎖のFc領域は、比較可能な分子、すなわち、IgG2、IgG3またはIgG4のFc領域を有する重鎖を含む前記分子と同一であるが1つまたは複数のアミノ酸改変を有していない分子と比べて高い親和性でFcγRIIIAに結合する。さらに他の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は、野生型Fc領域を含む比較可能な分子と比べて低下した親和性でFcγRIIIAに結合する。好ましい実施形態では、本発明の分子はさらに、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子がFcγRIIBに結合するよりも低い親和性で(Fc領域を介して)FcγRIIBに特異的に結合する。いくつかの実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて高い親和性でFcγRIIIAおよびFcγRIIBに結合する。他の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて高い親和性でFcγRIIBに結合する。別の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて低下した親和性でFcγRIIBに結合する。
本発明は、2種以上のIgGアイソタイプ由来のドメインまたは領域を含む重鎖の状況における本明細書で開示される、または当技術分野で知られているアミノ酸改変の使用を包含する。本明細書で開示される通り、Fc領域のアミノ酸改変は、免疫グロブリン結合および/またはエフェクター機能活性に大いに影響を及ぼすことができる。しかし、機能的特徴のこうした変化は、選択されたIgGアイソタイプの状況で実施するとさらに改良および/または操作することができる。同様に、アイソタイプの天然の特徴を1つまたは複数のアミノ酸改変によって操作することもできる。複数のIgGアイソタイプ(すなわち、IgG1、IgG2、IgG3およびIgG4)は、血清中半減期、補体結合、FcγR結合親和性およびエフェクター機能活性(例えば、ADCC、CDC)を含めた様々な物理学的および機能的特性を有する。好ましい実施形態では、アミノ酸改変およびIgG領域は、所望の特徴を有する変異型重鎖を操作するために、そのそれぞれの別個の結合および/またはエフェクター機能活性に基づいて独立に選択される。大部分の実施形態では、前記アミノ酸改変およびIgG領域は、IgG1状況で、本明細書に記載の通り、または当技術分野で知られている通り結合および/またはエフェクター機能活性について別々にアッセイされている。ある実施形態では、前記アミノ酸改変およびIgG領域は、野生型重鎖および/またはFc領域の状況でFcγR結合またはエフェクター機能について別々にアッセイすると類似の機能性、例えばFcγRIIAに対する親和性の増大を示す。次いで、前記アミノ酸改変と選択されたIgG領域の組合せが相加的に、またはより好ましくは相乗的に働いて、本発明の変異型重鎖の前記機能性を、同一のアイソタイプの対応する領域(複数可)を有する野生型重鎖と比べて改変する。他の実施形態では、前記アミノ酸改変およびIgG領域は、本明細書に記載の通り、または当技術分野で知られている通り野生型重鎖および/またはFc領域の状況でFcγR結合またはエフェクター機能について別々にアッセイすると、反対の機能性、例えば、それぞれFcγRIIAに対する親和性の増大および低下を示す。次いで、前記「反対の」アミノ酸改変と選択されたIgG領域の組合せが働いて、同一のアイソタイプの対応する領域(複数可)を有する野生型重鎖と比べて本発明の変異型重鎖の特定の機能性を選択的に強化するまたは低下させる。あるいは、本発明は、当技術分野で知られている、かつ/または本明細書に記載のアミノ酸改変と新規の特性を示す選択されたIgG領域との組合せを含む変異型重鎖を包含し、この特性は、本明細書に記載の通り前記改変および/または領域を独立にアッセイしても検出可能でなかった。
複数のIgGアイソタイプおよびそのドメインの機能的特徴は当技術分野で周知である。IgG1、IgG2、IgG3およびIgG4のアミノ酸配列は図Xに示す。本発明の変異型重鎖に使用するための、特定のIgGアイソタイプ由来の2種以上のドメインの選択および/または組合せは、FcγRに対する親和性を含めた、親アイソタイプの任意の既知のパラメーターに基づくことできる(表X、Flesch and Neppert, 1999, J. Clin. Lab. Anal. 14:141-156; Chappel et al., 1993, J. Biol. Chem. 33:25124-25131; Chappel et al., 1991, Proc. Natl. Acad. Sci. USA 88:9036-9040、そのそれぞれの全体が参照により本明細書に組み込まれている)。例えば、FcγRIIBに対して結合が制限された、または結合を示さないIgGアイソタイプ、例えば、IgG2またはIgG4由来の領域またはドメインの使用は、変異型重鎖が、活性化受容体に対する結合を最大化し、抑制性受容体に対する結合を最小化するように工学的に改変されることが望ましい場合に特に用いることができる。同様に、C1qまたはFcγRIIIAに優先的に結合することが知られているIgGアイソタイプ、例えば、IgG3(Bruggemann et al., 1987, J. Exp. Med 166:1351-1361)由来の領域またはドメインの使用は、当技術分野で知られているアミノ酸改変と組み合わせてADCCを増強して(表8参照)、エフェクター機能活性、例えば、補体活性化またはADCCが最大化されるように変異型重鎖を工学的に改変することができる。
本発明はまた、本発明の変異型重鎖の新規の状況で既知のIgG多型を導入するための、2種以上のIgGアイソタイプ由来のドメインまたは領域を含む重鎖の状況での本明細書で開示される、または当技術分野で知られているアミノ酸改変の使用を包含する。様々なIgGアイソタイプのFc領域に見られる多型は、特定のエフェクター機能活性を誘発する上でのその差の基礎となることが提案された(Kim et al., 2001, J. Mol. Evol. 53:1-9、その全体が参照により本明細書に組み込まれている)。したがって、本発明の変異型重鎖の状況での既知の多型の使用により、選択されたエフェクター細胞集団との特異的相互作用の調節を行うことができる。
いくつかの実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型Fc領域を含む比較可能な分子と比べて、どんなFcγRに対する検出可能な結合も示さない(例えば、例としてELISAアッセイにより決定した場合、FcγRIIA、FcγRIIBまたはFcγRIIIAに結合しない)。
特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は1種のFcγRのみに結合し、前記FcγRはFcγRIIIAである。別の特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は1種のFcγRのみに結合し、前記FcγRはFcγRIIAである。さらに別の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子を包含し、この変異型重鎖のFc領域は1種のFcγRのみに結合し、前記FcγRはFcγRIIBである。本発明は、特に、例えば、治療用抗体のエフェクター機能を増強する、例えば、ADCCを増強することにより、治療用抗体の有効性を増強するためのヒトまたはヒト化型治療用抗体(例えば、腫瘍特異的抗血管形成または抗炎症性モノクローナル抗体)の改変に関する。
本発明の分子のFcγRに対する親和性と結合特性は、Fc-FcγR相互作用、すなわち、Fc領域のFcγRへの特異的結合を決定するための当技術分野で公知の、ELISAアッセイ、表面プラズモン共鳴アッセイ、免疫沈降アッセイを含むがこれに限定されることはないin vitroアッセイ(生化学的または免疫学的ベースのアッセイ)を使って最初に決定される(セクション5.2参照)。好ましくは、本発明の分子の結合特性は、1つまたは複数のFcγ媒介物エフェクター細胞機能を決定するためのin vitro機能アッセイにより特徴付けもされる(セクション5.3参照)。最も好ましい実施形態では、本発明の分子は、in vitroベースのアッセイにおける結合特性と類似の結合特性を、(本明細書に記載し開示するモデルなどの)in vivoモデルにおいて有する。しかし、本発明は、in vitroベースのアッセイにおいて所望の表現型を示さないがin vivoでは所望の表現型を確かに示す本発明の分子を排除するものではない。
いくつかの実施形態では、変異型重鎖を含む本発明の分子は、アミノ酸342〜447から伸びていると定義される前記Fc領域のCH3ドメインに少なくとも1つのアミノ酸改変を含む。他の実施形態では、変異型重鎖を含む本発明の分子は、アミノ酸231〜341から伸びていると定義される前記Fc領域のCH2ドメインに少なくとも1つのアミノ酸改変を含む。他の実施形態では、変異型重鎖を含む本発明の分子は、アミノ酸118から215にわたるものと定義されるFc領域のCH1ドメイン中に少なくとも1つのアミノ酸改変を含む。いくつかの実施形態では、本発明の分子は、 少なくとも2つのアミノ酸改変を含み、それぞれの改変は変異型重鎖の別個の領域にある。例えば、1つの改変がCH3領域にあり、1つの改変がCH2領域にある、1つの改変がCH3領域にあり、1つの改変はCH1領域にある、または1つの改変がCH2領域にあり、1つの改変がCH1領域にある。本発明は、さらに、ヒンジ領域にアミノ酸改変を包含する。CH1、CH2および/またはCH3ドメインに1つまたは複数のアミノ酸改変のある本発明の分子は、本明細書に記載の、または当業者に公知の方法を使って決定される場合、FcγRに対する改変された親和性を有する。
特に好ましい実施形態では、本発明は、変異型重鎖を含み、前記変異体が、当業者に公知であり、および本明細書に例示された方法を使って測定された場合、FcγRIIA(CD32A)への増大した結合および/または増大したADCC活性を有する分子を包含する。本発明の方法に従って使用されるADCCアッセイは、NK依存性でもマクロファージ依存性でもよい。
本発明の重鎖変異体は、それだけに限らないが、エフェクター機能を変更する改変、およびFcγR結合親和性を変更する改変を含めた他の既知の重鎖改変、特にFc領域に対する改変と組み合わせてもよい。特定の実施形態では、CH1ドメイン、CH2ドメイン、CH3ドメインまたはヒンジ領域に第1のアミノ酸改変を含む本発明の重鎖変異体は、第1の改変が第2の改変に相加的な、相乗的な、または新規の特性を与えるように、第2の重鎖改変が第1の重鎖改変と同一ドメインに存在しないよう、第2の重鎖改変と組み合わせてもよい。いくつかの実施形態では、本発明の重鎖変異体は、CH1ドメインにはいかなるアミノ酸改変もない。他の実施形態では、本発明の重鎖変異体は、CH2ドメインにはいかなるアミノ酸改変もない。
本発明の重鎖変異体は、下の表3に開示する改変などの当技術分野における任意の改変と組み合わせてもよい。
他の実施形態では、本発明の重鎖変異体は、当技術分野における任意の既知の重鎖改変、例えば、以下の表4AおよびBで開示される改変と組み合わせることができる。
好ましい特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含む分子を包含し、前記分子がFcγRに対して改変された親和性を有するように、この変異型重鎖は、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を含み、ただし、前記変異型重鎖は、Sondermann et al., 2000 (Nature, 406: 267-273、この文献は参照によりその全体が本明細書に組み込まれているものとする)により開示された相互作用などのFc-FcγR相互作用の結晶解析および構造解析に基づいて、FcγRと直接接触している位置に置換がない。重鎖のFc領域内の、FcγRと直接接触している位置の例は、アミノ酸234〜239 (ヒンジ領域)、アミノ酸265〜269(B/Cループ)、アミノ酸297〜299(C'/Eループ)、およびアミノ酸327〜332 (F/Gループ)である。いくつかの実施形態では、変異型重鎖領域を含む本発明の分子は、構造解析および結晶解析に基づいて、FcγRと直接接触している少なくとも1つの残基の改変を含む。
前記FcγR相互作用ドメインは下位のヒンジ領域およびIgG重鎖のCH2およびCH3ドメイン内の選択部位に位置する。実際の接触位置に隣接するアミノ酸残基およびCH3ドメインのアミノ酸残基は、それぞれ突然変異誘発試験および小ペプチド阻害剤を使った試験により示されるように、IgG/FcγR相互作用に関与している(Sondermann et al., 2000 Nature、406: 267-273; Diesenhofer et al., 1981、Biochemistry、20: 2361-2370; Shields et al., 2001、J. Biol. Chem. 276: 6591-6604。これらの文献はそれぞれが参照によりその全体が本明細書に組み込まれているものとする)。本明細書で使用される直接接触とは、アミノ酸が互いの少なくとも1A、少なくとも2、もしくは、少なくとも3オングストローム以内に、または1Å、1.2Å、1.5Å、1.7Åもしくは2Åファンデルワールス半径内に存在することである。Fc相互作用タンパク質の結合をもたらすFc上の以前同定された部位の例となる一覧表は、下の表5に収載されている。いくつかの実施形態では、本発明は、下に収載した部位にはいかなる改変も有さない重鎖変異体を包含する。他の実施形態では、本発明は、改変が突然変異体の特性に相乗的または相加的効果を及ぼすように、本明細書に開示した他の改変と組み合わせて、下に収載した1つまたは複数の部位にアミノ酸改変を含む重鎖変異体を包含する。
表5は、前記重鎖Fc領域内の、Fc-FcR相互作用にとって重要であると以前同定されている部位を収載する。FcR-Fcとラベルされた列は、前記FcRが接触しているFc鎖を特定している。文字はデータを引用した参考文献を特定している。CはShields et al., 2001, J. Biol. Chem. 276: 6591-6604, DはJefferis et al., 1995、Immunol. Lett. 44: 111-7、EはHinton et al., 2004, J. Biol. Chem. 279(8): 6213-6, FはIdusogie et al., 2000, J. Immunol. 164: 4178-4184である。これらの文献は参照によりその全体を本明細書に組み込んでいるものとする。
別の好ましい実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む分子を包含し、前記分子が、野生型Fc領域を含む分子と比べて改変された親和性でFcγRに結合するように、この変異型重鎖は、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を含む。ある実施形態では、変異型重鎖を有するFcγRに対する親和性が改変された本発明の分子は、1つまたは複数のアミノ酸改変を有し、前記1つまたは複数のアミノ酸改変は、288位でのアスパラギンによる、330位でのセリンによる、および396位でのロイシンによる置換(MgFc10)(表6参照)、または334位でのグルタミン酸による、359位でのアスパラギンによる、および366位でのセリンによる置換(MgFc13)、または316位でのアスパラギン酸による、378位でのバリンによる、および399位でのグルタミン酸による置換(MgFc27)、または247位でのロイシンによる、および421位でのリシンによる置換(MgFc31)、または392位でのスレオニンによる、および396位でのロイシンによる置換(MgFc38)、または221位でのグルタミン酸による、270位でのグルタミン酸による、308位でのアラニンによる、311位でのヒスチジンによる、396位でのロイシンによる、および402位でのアスパラギン酸による置換(MgFc42)、または419位でのヒスチジンによる、および396位でのロイシンによる置換(MgFc51)、または240位でのアラニンによる、および396位でのロイシンによる置換(MgFc52)、または410位でのヒスチジンによる、および396位でのロイシンによる置換(MgFc53)、または243位でのロイシンによる、305位でのイソロイシンによる、378位でのアスパラギン酸による、404位でのセリンによる、および396位でのロイシンによる置換(MgFc54)、または255位でのイソロイシンによる、および396位でのロイシンによる置換(MgFc55)、または370位でのグルタミン酸による、および396位でのロイシンによる置換(MgFc59)、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、305位でのイソロイシンによる、および396位でのロイシンによる置換(MgFc88)、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、および396位でのロイシンによる置換(MgFc88A)、または243位でのロイシンによる、292位でのプロリンによる、および300位でのロイシンによる置換(MgFc155)、または435位でのヒスチジンによる、または270位でのグルタミン酸による置換、またはそれらの組合せである。特定の実施形態では、本発明は、変異型Fc領域を含み、前記変異型Fc領域が396位でのロイシンによる、270位でのグルタミン酸による、および243位でのロイシンによる置換を含む分子を包含する。別の特定の実施形態では、前記分子は、本明細書に開示する改変などの1つまたは複数のアミノ酸改変をさらに含む。
いくつかの実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、以下の119位、125位、132位、133位、141位、142位、147位、149位、162位、166位、185位、192位、202位、205位、210位、214位、215位、216位、217位、218位、219位、221位、222位、223位、224位、225位、227位、229位、231位、232位、233位、235位、240位、241位、242位、243位、244位、246位、247位、248位、250位、251位、252位、253位、254位、255位、256位、258位、261位、262位、263位、268位、269位、270位、272位、274位、275位、276位、279位、280位、281位、282位、284位、287位、288位、289位、290位、291位、292位、293位、295位、298位、301位、303位、304位、305位、306位、307位、308位、309位、310位、311位、312位、313位、315位、316位、317位、318位、319位、320位、323位、326位、327位、328位、330位、333位、334位、335位、337位、339位、340位、343位、344位、345位、347位、348位、352位、353位、354位、355位、358位、359位、360位、361位、362位、365位、366位、367位、369位、370位、371位、372位、375位、377位、378位、379位、380位、381位、382位、383位、384位、385位、386位、387位、388位、389位、390位、392位、393位、394位、395位、396位、397位、398位、399位、400位、401位、402位、404位、406位、407位、408位、409位、410位、411位、412位、414位、415位、416位、417位、419位、420位、421位、422位、423位、424位、427位、428位、431位、433位、435位、436位、438位、440位、441位、442位、443位、446位、447位のうちの1つまたは複数の位置にアミノ酸改変を有する変異型重鎖を含む分子を包含する。好ましくは、そのような突然変異体は、本明細書に開示され、例示された、かつ/または当業者に公知の方法を使って決定した場合、FcγRに対して改変された親和性を有しかつ/または改変されたエフェクター細胞媒介機能を有する分子をもたらす。
本発明は、IgG2、IgG3またはIgG4のFc領域を有し、下の表(表6)に収載する突然変異体のいずれからでも成り、またはいずれでも含む変異型重鎖を含む分子を包含する。
さらに他の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、2つを超えるアミノ酸改変を有する変異型重鎖を含む分子を包含する。このような変異体の非限定的な例は以下の表(表7)に記載する。本発明はまた、表6に記載の突然変異を含み、本明細書で開示される改変などの1つまたは複数のアミノ酸改変をさらに含む分子を包含する。
特定の実施形態では、変異型重鎖は、247位にロイシン、421位にリジンおよび270位にグルタミン酸(MgFc31/60);392位にスレオニン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc38/60/F243L);419位にヒスチジン、396位にロイシンおよび270位にグルタミン酸(MGFc51/60);419位にヒスチジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MGFc51/60/F243L);240位にアラニン、396位にロイシンおよび270位にグルタミン酸(MGFc52/60);255位にリジンおよび396位にロイシン(MgFc55);255位にリジン、396位にロイシンおよび270位にグルタミン酸(MGFc55/60);255位にリジン、396位にロイシン、270位にグルタミン酸および300位にリジン(MGFc55/60/Y300L);255位にリジン、396位にロイシン、270位にグルタミン酸および292位にグリシン(MGFc55/60/R292G);255位にリジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc55/60/F243L);370位にグルタミン酸、396位にロイシンおよび270位にグルタミン酸(MGFc59/60);270位にグルタミン酸、316位にアスパラギン酸および416位にグリシン(MgFc71);243位にロイシン、292位にプロリン、305位にイソロイシンおよび396位にロイシン(MGFc74/P396L);243位にロイシン、270位にグルタミン酸、392位にアスパラギンおよび396位にロイシン;または243位にロイシン、255位にロイシン、270位にグルタミン酸および396位にロイシン;297位にグルタミン酸、または個々の置換の任意の組合せを有する。
いくつかの実施形態では、本発明の分子、好ましくは免疫グロブリンは、1つまたは複数の炭水化物成分が前記分子に共有結合するように、1つまたは複数のグリコシル化部位をさらに含む。好ましくは、1つまたは複数のグリコシル化部位および/または重鎖に1つまたは複数の改変を有する本発明の抗体は、増強された抗体媒介エフェクター機能、例えば、親および/または野生型抗体と比べて増強されたADCC活性を有する。いくつかの実施形態では、本発明は、前記抗体の炭水化物成分と直接的にまたは間接的に相互作用することが知られている、241位、243位、244位、245位、245位、249位、256位、258位、260位、262位、264位、265位、296位、299位、および301位のアミノ酸を含むがこれらに限定されることはないアミノ酸の1つまたは複数の改変を含む抗体をさらに含む。抗体の炭水化物成分と直接的にまたは間接的に相互作用をするアミノ酸は、当技術分野で公知であり、例えば、Jefferis et al., 1995 Immunology Letters、44: 111-7を参照されたい。この文献は参照によりその全体が本明細書に組み込まれているものとする。
別の実施形態では、本発明は、好ましくは、抗体の機能、例えばFcγRへの結合活性を改変せずに、抗体の1つまたは複数の部位に1つまたは複数のグリコシル化部位を導入することにより改変された抗体を包含する。グリコシル化部位は、本発明の抗体の可変および/または定常領域に導入してもよい。本明細書で使用する「グリコシル化部位」は、オリゴ糖(すなわち、互いに連結している2個以上の単糖類を含有する炭水化物)が特異的におよび共有結合的に結合する抗体の特定のアミノ酸配列のすべてを含む。オリゴ糖側鎖は、典型的にはN-またはO-結合のいずれかを介して抗体の骨格に連結している。N-結合グリコシル化とは、オリゴ糖成分がアスパラギン残基の側鎖に結合することである。O-結合グリコシル化とは、オリゴ糖成分がヒドロキシアミノ酸、例えばセリン、スレオニンに結合することである。本発明の抗体は、N-結合およびO-結合グリコシル化部位を含む1つまたは複数のグリコシル化部位を含んでいてよい。当技術分野で公知のN-結合またはO-結合グリコシル化のためのグリコシル化部位はいずれも、本発明に従って使用してよい。本発明の方法に従って有用である典型的なN-結合グリコシル化部位は、アミノ酸配列、すなわち、Asn-X-Thr/Serであり、Xはいかなるアミノ酸でもよく、Thr/Serはスレオニンまたはセリンを示す。そのような部位または部位群は、本発明が属する技術分野で公知の方法を使って、本発明の抗体に導入してもよい。例えば、"In Vitro Mutagenesis," Recombinant DNA: A Short Course, J. D. Watson、et al. W.H. Freeman and Company, New York、1983, chapter 8, pp. 106-116を参照されたい。この文献は参照によりその全体が本明細書に組み込まれているものとする。グリコシル化部位を本発明の抗体に導入するための典型的な方法は、所望のAsn-X-Thr/Ser配列が得られるように、前記抗体のアミノ酸配列を改変するまたは変異導入することを含んでいてよい。
いくつかの実施形態では、本発明は、グリコシル化部位を付加するまたは欠失させることにより、本発明の抗体の炭水化物含有量を改変する方法を包含する。抗体の炭水化物含有量を改変するための方法は、当技術分野で公知であり、本発明内に包含される。例えば、米国特許第6,218,149号、欧州特許第0 359 096号、米国特許出願公開第2002/0028486号、国際公開第03/035835号、米国特許出願公開第2003/0115614号、米国特許第6,218,149号、米国特許第6,472,511号を参照されたい。これらの特許はすべてが、参照によりその全体が本明細書に組み込まれているものとする。他の実施形態では、本発明は、前記抗体の1つまたは複数の内在性の炭水化物成分を欠失させることにより、本発明の抗体の炭水化物含有量を改変する方法を包含する。特定の実施形態では、本発明は、297に隣接する位置を改変することにより、抗体のFc領域のグリコシル化部位を移動させることを包含する。特定の実施形態では、本発明は、296位がグリコシル化され、297位はグリコシル化されないように、296位を改変することを包含する。
6.1 変異型重鎖を有するポリペプチドおよび抗体
本発明は、2種以上のIgGアイソタイプ由来の重鎖ドメインまたは領域(例えば、CHドメイン、ヒンジ領域、Fc領域)を組み合わせること、および1つまたは複数の領域中の1つまたは複数のアミノ酸改変(例えば、置換、ならびに挿入または欠失を含む)の両方によるヒトIgG重鎖の機能性の改変に一部基づいており、この改変は、FcγRに対する前記変異型重鎖のFc領域の親和性を変更する、例えば、増大または低下させる。したがって、本発明は、2種以上のIgGアイソタイプ由来のドメインまたは領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(例えば、置換、しかし挿入または欠失も含む)を有する変異型重鎖を含む分子、好ましくはポリペプチド、より好ましくは免疫グロブリン(例えば、抗体)に関し、この改変は、FcRに対する変異型重鎖のFc領域の親和性を変更する。
アミノ酸置換は別として、本発明は、1つまたは複数の改変された特性、例えば改変されたエフェクター機能を有する重鎖変異体を作製するために、重鎖アミノ酸配列の他の改変を企図していることを当業者は理解するであろう。本発明は、FcγRへの結合を減少させるために重鎖の1つまたは複数のドメイン内の1つまたは複数のアミノ酸残基の欠失を企図している。好ましくは、本発明のこの実施形態によれば、わずか5個の、わずか10個の、わずか20個の、わずか30個の、わずか50個のFc領域残基が欠失していることになる。1つまたは複数のアミノ酸欠失を含む本明細書の変異型重鎖は、少なくとも約80%の、好ましくは少なくとも約90%の、最も好ましくは少なくとも約95%の野生型Fc領域をできれば保持していることになる。いくつかの実施形態では、例えば非免疫原性、FcγRIIIA結合、FcγRIIA結合、またはこれらの特性の組合せなどの、前記分子の1つまたは複数の特性が維持される。
別の実施形態では、本発明は、その変異体が改変されたエフェクター機能を含む、改変された特性を有する重鎖変異体を作製するためのアミノ酸の挿入を包含する。一特定の実施形態では、本発明は、少なくとも1つのアミノ酸残基、例えば、本明細書で同定した1つまたは複数の重鎖の位置に隣接して、1個または2個のアミノ酸残基、および好ましくはわずか10個のアミノ酸残基を導入することを包含する。別の実施形態では、本発明は、少なくとも1つのアミノ酸残基、例えば、FcγR相互作用および/または結合に影響することが当技術分野で公知の1つまたは複数の重鎖の位置に隣接して、1個または2個のアミノ酸残基、および好ましくはわずか10個のアミノ酸残基を導入することを包含する。
本発明は、本発明の重鎖変異体を作製するための非天然アミノ酸の組込みをさらに包含する。天然の生合成機構を使って非天然アミノ酸をタンパク質に組み込ませる方法など、そのような方法は当業者に公知であり、例えば、Wang et al., 2002 Chem. Comm. 1: 1-11; Wang et al., 2001, Science, 292: 498-500、van Hest et al., 2001. Chem. Comm. 19: 1897-1904を参照されたい。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。別の戦略は、アミノアシルtRNAの生合成を司る酵素に焦点を合わせており、例えば、Tang et al., 2001, J. Am. Chem. 123(44): 11089-11090, Kiick et al., 2001, FEBS Lett. 505(3): 465を参照されたい。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
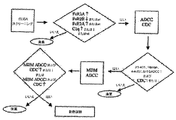
本発明の分子のFcγRに対する親和性および結合性は、重鎖-抗体受容体相互作用、特にFc-FcγR相互作用、すなわち、FcγRへのFc領域の特異的な結合を決定するための、ELISAアッセイ、表面プラズモン共鳴アッセイ、免疫沈降アッセイを含むがこれに限定されるものではない当技術分野では公知のin vitroアッセイ(生化学または免疫学ベースのアッセイ)を使って最初は決定される(セクション5.2参照)。好ましくは、本発明の分子の結合性は、1つまたは複数のFcγR媒介物エフェクター細胞機能を決定するためにも、in vitro機能アッセイにより特徴付けられる(セクション5.3参照)。最も好ましい実施形態では、本発明の分子は、in vitroベースのアッセイでの結合性に類似する結合性を、(本明細書に記載され開示されているモデルなどの)in vivoモデルで有する。しかし、本発明は、in vitroベースのアッセイでは所望の表現型を示さないが、in vivoでは所望の表現型を確かに示す本発明の分子を排除しない。本発明の分子のスクリーニングおよび特徴付けの代表的なフローチャートは図2で説明する。
本発明は、同一のアイソタイプのFc領域を有する野生型重鎖と比べて高い親和性で1つまたは複数のFcγRに結合する、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む分子を包含する。このような分子は、好ましくは、以下に述べる通りエフェクター機能をより効果的に媒介する。他の実施形態では、本発明は、同一のアイソタイプのFc領域を有する野生型重鎖と比べて低い親和性で1つまたは複数のFcγRに結合する、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む分子を包含する。エフェクター機能を低下させたりまたは除去するのは、ある種の場合、例えば、作用機序が標的抗原を担持する細胞に対し遮断または拮抗するが、死滅させることはない抗体の場合には好ましい。エフェクター機能を低下させたりまたは除去するのは、エフェクター細胞のFcγR活性化受容体を遮断すると考えられる自己免疫疾患の場合には好ましいであろう(この種の機能が宿主細胞に存在すると考えられる)。通常、増大したエフェクター機能は腫瘍および異質細胞に向けられると考えられる。
本発明の重鎖変異体は、エフェクター機能を変化させる改変を含むがこれに限定されることはない他の重鎖改変と組み合わせてもよい。本発明は、本発明の重鎖変異体を他の重鎖改変と組み合わせて、抗体またはFc融合物において相加的な、相乗的な、または新規の特性を提供することを包含する。好ましくは、本発明の重鎖変異体は、それが組み合わされる改変の表現型を増強する。例えば、本発明の重鎖変異体が、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子よりも高い親和性でFcγRIIIAに結合することが知られている突然変異体と組み合わされた場合、本発明の突然変異体との組合せにより、FcγRIIIA親和性が何倍にも増強される。
一実施形態では、本発明の重鎖変異体は、Duncan et al, 1988, Nature 332:563-564, Lund et al., 1991, J. Immunol 147:2657-2662, Lund et al, 1992, Mol Immunol 29:53-59, Alegre et al, 1994, Transplantation 57:1537-1543, Hutchins et al., 1995, Proc Natl. Acad Sci U S A 92:11980-11984, Jefferis et al, 1995, Immunol Lett. 44:111-117, Lund et al., 1995, Faseb J 9:115-119, Jefferis et al, 1996, Immunol Lett 54:101-104, Lund et al, 1996, J Immunol 157:4963-4969, Armour et aL, 1999, Eur J Immunol 29:2613-2624, Idusogie et al, 2000, J Immunol 164:4178-4184, Reddy et al, 2000, J Immunol 164:1925-1933, Xu et al., 2000, Cell Immunol 200:16-26, Idusogie et al, 2001, J Immunol 166:2571-2575, Shields et al., 2001, J Biol Chem 276:6591-6604, Jefferis et al, 2002, Immunol Lett 82:57-65, Presta et al., 2002, Biochem Soc Trans 30:487-490、米国特許第5,624,821号、米国特許第5,885,573号、米国特許第6,194,551号、PCT国際公開第00/42072号、PCT国際公開第99/58572号に開示されている重鎖変異体などの他の既知の重鎖変異体と組み合わせてもよい。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
いくつかの実施形態では、本発明の重鎖変異体は、1つまたは複数の工学的に改変されたグリコフォーム、すなわち、重鎖またはその領域を含む分子と共有結合している炭水化物組成物を含み、前記炭水化物組成物が重鎖またはその領域を含む親分子の炭水化物組成物とは化学的に異なる抗体またはFc融合物に組み込まれている。工学的に改変されたグリコフォームは、エフェクター機能を増強するまたは低下させることを含むがこれに限定されるものではない種々の目的に有用である可能性がある。工学的に改変されたグリコフォームは、例えば、工学的に改変されたまたは変異発現株を使うことにより、1つもしくは複数の酵素、例えば、DI N-アセチルグルコサミン転移酵素III(GnTI11)との同時発現により、種々の生物もしくは種々の生物由来の細胞系において重鎖またはその領域を含む分子を発現することにより、または、重鎖またはその領域を含む分子が発現された後に炭水化物(群)を改変することにより、当業者に公知のいかなる方法によって作製してもよい。工学的に改変されたグリコフォームを作製するための方法は、当技術分野では公知であり、Umana et al., 1999, Nat. Biotechnol 17:176-180, Davies et al., 20017 Biotechnol Bioeng 74:288-294, Shields et al、2002, J Biol Chem 277:26733-26740, Shinkawa et aL, 2003, J Biol Chem 278:3466-3473、米国特許第6,602,684号、米国特許出願第10/277,370号、米国特許出願第10/113,929号、PCT国際公開第00/61739A1号、PCT国際公開第01/292246A1号、PCT国際公開第02/311140A1号、PCT国際公開第02/30954A1号、Potillegent(商標) technology (Biowa, Inc. Princeton, NJ)、GlycoMAb(商標)glycosylation engineering technology (GLYCART biotechnology AG, Zurich, Switzerland)に記載された方法があるが、その方法に限定されるものではない。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。例えば、国際公開第00061739号、欧州特許出願公開第01229125号、米国特許出願公開第20030115614号、Okazaki et al., 2004、JMB、336: 1239-49を参照されたい。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
本発明の重鎖変異体は、種々の特性を最適化されていてもよい。最適化されてもよい特性には、FcγRに対して増強されたまたは低下した親和性、すなわち増強されたまたは低下したエフェクター機能があるが、これに限定されるものではない。好ましい実施形態では、本発明の重鎖変異体は、ヒト活性化FcγR、好ましくはFcγR、FcγRIIA、FcγRIIc、FcγRIIIA、およびFcγRIIIB、最も好ましくはFcγRIIIAに対して増強された親和性を有するように最適化されている。別の好ましい実施形態では、前記Fc変異体は、ヒト阻害性受容体FcγRIIBに対して低下した親和性を有するように最適化されている。これらの好ましい実施形態は、抗体およびFcの融合物に、ヒトにおける増強された治療上の特性、例えば、本明細書に記載し例証している増強されたエフェクター機能および比較的大きな抗癌効力を与えると期待される。これらの好ましい実施形態は、抗体およびFc融合物に、マウス異種移植腫瘍モデルにおいて増強された腫瘍除去を与えると期待される。
別の実施形態では、本発明の重鎖変異体は、FcγRI、FcγRIIA、FcγRIIB、FcγRIIc、FcγRIIIA、およびFcγRIIIBを含むが、これに限定されるものではないヒトFcγRに対する低下した親和性を有するように最適化されている。これらの実施形態は、抗体およびFcの融合物に、ヒトにおける増強された治療上の特性、例えば、低下したエフェクター機能および低下した毒性を与えると期待される。
別の実施形態では、本発明の重鎖変異体は、マウス、ラット、ウサギ、サルを含むがこれに限定されることはない非ヒト生物由来のFcγRに対する増強されたまたは低下した親和性を有する。非ヒトFcγRへの結合のために最適化される重鎖変異体は、実験での用途を見つけてもよい。例えば、所与の薬剤候補の有効性、毒性、および薬物動態などの特性を試験することができるマウスモデルは、種々の疾患に利用することができる。当技術分野では公知のように、癌細胞をマウスに移植しまたは注入してヒト癌を再現することができ、これは異種移植と呼ばれる方法である。1つまたは複数のマウスFcγRのために最適化されている重鎖変異体またはその部分を含む抗体またはFc融合物を試験すれば、前記抗体またはFc融合物の有効性、その作用機序などに関する貴重な情報が提供されるであろう。
FcγRへの結合を改変することは好ましいが、本発明はさらに、ネオナタル受容体(FcRn)への結合親和性が改変された重鎖変異体を企図している。特定の作用機序によって結合されることを目的にしてはいないが、FcRnに対する親和性が改良されている重鎖変異体は血中半減期が長くなると期待され、そのような分子は、例えば、慢性の疾患または障害の治療のために投与されたポリペプチドの長い半減期が望まれる場合には、哺乳動物の治療法に有用な用途を有するであろう。特定の作用機序によって結合されることを目的にしてはいないが、FcRn結合親和性が減少した重鎖変異体は、それに比べて、半減期が短くなると予想され、そのような分子は、例えば、短縮された循環時間が、例えば、in vivo画像診断法にまたは、長期間血流中を循環するままになると中毒性副作用があるポリペプチドに有利となる場合には、哺乳動物に投与してもよい。FcRn結合親和性が減少したFc領域変異体は、胎盤を通過する可能性は少ないと期待され、したがって、妊婦の疾患または障害の治療に利用してもよい。
他の実施形態では、これらの変異体は、国際公開第98/23289号、および国際公開第97/34631号、ならびに米国特許第6,277,375号に開示された改変などのFcRn親和性が変化した他の既知の重鎖改変と組み合わせてもよい。これらの特許文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
本発明は、例えば、IgG定常ドメインまたはそのFcRn結合断片(好ましくはFcまたはヒンジFcドメイン断片)に1つまたは複数のアミノ酸改変(すなわち、置換、挿入、もしくは欠失)を導入することにより、in vivoで半減期が増加した抗体を作製するための当技術分野で公知の他のあらゆる方法を包含する。例えば、国際公開第98/23289号、および国際公開第97/34631号ならびに米国特許第6,277,375号を参照されたい。これらの特許文献はそれぞれが、本発明の重鎖変異体と組み合わせて使用するために、参照によりその全体が本明細書に組み込まれているものとする。さらに、本発明の抗体は、前記抗体または抗体断片をin vivoにおいてさらに安定にする、またはin vivoで半減期を長くするためにアルブミンに結合させることができる。当技術分野で公知の技術は、例えば、国際公開第93/15199号、国際公開第93/15200号、および国際公開第01/77137号、ならびに欧州特許第413,622号を参照されたい。これらの特許文献はすべてが、参照によりその全体が本明細書に組み込まれているものとする。
本明細書に記載の変異体(群)は、多くの場合、前記変異体の使用目的によってさらに改変を受けてもよい。そのような改変には、前記アミノ酸配列の追加の改変(アミノ酸残基の置換、挿入および/または欠失)、異種ポリペプチド(群)への融合および/または共有結合改変を含んでいてもよい。そのような追加の改変は、Fc受容体結合および/またはADCC活性の改変などの改変された特性をもたらす本明細書に開示しているアミノ酸改変の前に、同時に、または、後で行ってもよい。
代案としてまたは追加として、本発明は本明細書に開示のアミノ酸改変と、in vitroおよび/またはin vivoにおいて決定される場合、前記重鎖のC1q結合および/または補体依存性細胞障害機能を改変する1つまたは複数の追加のアミノ酸改変を組み合わせることを包含する。好ましくは、本明細書で特に関心のある開始分子は、通常、C1qに結合し補体依存性細胞障害(CDC)を示す分子である。本明細書に記載の追加のアミノ酸置換は、一般的に、前記開始分子がC1qに結合しかつ/またはその補体依存性細胞障害機能を改変する、例えば、これらのエフェクター機能を低下させ、好ましくは無効にする能力を改変するのに役立つであろう。他の実施形態では、前記記載された位置の1つまたは複数の位置に置換を含み、C1q結合および/または補体依存性細胞障害(CDC)機能が改善された分子を本明細書では企図している。例えば、前記開始分子は、C1qに結合しかつ/またはCDCを媒介することができなくてもよく、これらの追加のエフェクター機能を獲得するように本明細書の教唆に従って改変されてもよい。さらに、既存のC1q結合活性を有し、随意にさらにCDCを媒介する能力を有する分子は、これらの活性のうちの一方または両方が改変される、例えば、増強されるように改変されてもよい。いくつかの実施形態では、本発明はCDC活性が改変され、C1q結合には全く改変がない、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を包含する。さらに別の実施形態では、本発明は、CDC活性が改変されC1q結合が改変された変異型Fc領域を包含する。
C1q結合および/または補体依存性細胞障害(CDC)機能が改変された重鎖を作製するために、改変されるアミノ酸の位置は、通常、270、322、326、327、329、331、333、および334の位置から選択され、IgG重鎖における前記残基の番号付けは、Kabat et al., Sequences of Proteins of Immunological Interest、5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1999)の場合のEUインデックスの番号付けである。これらのアミノ酸改変は、本明細書に開示されている1つまたは複数の重鎖改変と組み合わせて、C1q結合および/またはCDC活性への相乗的または相加的効果を提供してもよい。他の実施形態では、本発明は、C1q結合および/または補体依存性細胞障害(CDC)機能が改変され、396位でのロイシンによる、および255位でのロイシンによるアミノ酸置換、または396位でのロイシンによる、および419位でのヒスチジンによるアミノ酸置換、396位でのロイシンによる、および370位でのグルタミン酸によるアミノ酸置換、396位でのロイシンによる、および240位でのアラニンによるアミノ酸置換、396位でのロイシンによる、および392位でのスレオニンによるアミノ酸置換、247位でのロイシンによる、および421位でのリシンによるアミノ酸置換を含む重鎖変異体を包含する。本発明は、Idusogie et al., 2001, J. Immunol. 166(4) 2571-5, Idusogie et al., J. Immunol. 2000 164(8): 4178-4184に開示されている改変などの、C1q結合および/または補体依存性細胞障害(CDC)機能を改変する前記Fc領域のあらゆる既知の改変を包含する。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
上記で開示した通り、本発明は、エフェクター機能が変更された、例えば、C1q結合および/またはFcR結合が改変され、それによりCDC活性および/またはADCC活性が変更された重鎖領域を包含する。特定の実施形態では、本発明は、C1q結合の改良およびFcγRIII結合の改良を特徴とする、例えば、ADCC活性も改良されCDC活性も改良された、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を包含する。代替の実施形態では、本発明は、CDC活性の低下および/またはADCC活性の低下を特徴とする、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む分子を包含する。他の実施形態では、例えば、ADCC活性は改良されているが、CDC活性は低下している、またその逆の変異型重鎖を作製するために、これらの活性のうちの一方のみを増大させ、場合によってもう一方の活性を低下させてもよい。
A. FcγRIIIAおよび/またはFcγRIIAに対する親和性が増強され変更された突然変異体
本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変(例えば、置換)を有する変異型重鎖を含む分子を包含し、このような改変は、活性化FcγRに対する変異型Fc領域の親和性を変更する。いくつかの実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(例えば、置換)を有する変異型重鎖を含み、この改変は、FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも2倍増大させる。別の特定の実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(例えば、置換)を有する変異型重鎖を含み、この改変は、FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて2倍を超えて増大させる。本発明の他の実施形態では、1つまたは複数のアミノ酸改変は、FcγRIIIAおよび/またはFcγRIIAに対する変異型Fc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも3倍、4倍、5倍、6倍、8倍または10倍増大させる。本発明のさらに別の実施形態では、1つまたは複数のアミノ酸改変は、FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも3倍、4倍、5倍、6倍、8倍または10倍減少させる。そのような倍増は、好ましくはELISAまたは表面プラズモン共鳴アッセイにより決定される。特定の実施形態では、Fc領域がIgG2 Fc領域である場合、1つまたは複数のアミノ酸改変は、233位でのグルタミン酸による置換;234位でのロイシンによる置換;235位でのロイシンによる置換;237位でのグリシンによる置換または挿入を含まない、または単にそれではない。
別の特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含む分子を包含し、前記分子が、比較可能な分子、すなわち同一のアイソタイプのFc領域を有する野生型重鎖を含む分子がFcγRIIAに結合するよりも高い親和性でFcγRIIAに特異的に結合するように、この変異型重鎖は、同一のアイソタイプのFc領域を含む野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する。特定の実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(例えば、置換)を有する変異型重鎖を含み、この改変は、FcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも2倍増大させる。別の特定の実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(例えば、置換)を有する変異型重鎖を含み、この改変は、FcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて2倍を超えて増大させる。本発明の他の実施形態では、1つまたは複数のアミノ酸改変は、FcγRIIAに対する変異型重鎖の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも3倍、4倍、5倍、6倍、8倍または10倍増大させる。
特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数のアミノ酸改変(例えば、置換であるが、挿入または欠失も含む)を有する、変異型重鎖を含む分子、好ましくはポリペプチド、さらに好ましくは免疫グロブリン(例えば、抗体)を包含し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて少なくとも65%、少なくとも70%、少なくとも75%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも99%、少なくとも100%、少なくとも150%、および少なくとも200%増大させる。
特定の実施形態では、変異型重鎖のFc領域の親和性を増大させる1つまたは複数のアミノ酸改変は、347位でのヒスチジンによる、および339位でのバリンによる置換、または、425位でのイソロイシンによる、および215位でのフェニルアラニンによる置換、または408位でのイソロイシンによる、215位でのイソロイシンによる、および125位でのロイシンによる置換、または385位でのグルタミン酸による、および247位でのヒスチジンによる置換、または348位でのメチオニンによる、334位でのアスパラギンによる、275位でのイソロイシンによる、202位でのメチオニンによる、および147位でのスレオニンによる置換、または275位でのイソロイシンによる、334位でのアスパラギンによる、および348位でのメチオニンによる置換、または279位でのロイシンによる、および395位でのセリンによる置換、または246位でのスレオニンによる、および319位でのフェニルアラニンによる置換、または243位でのイソロイシンによる、および379位でのロイシンによる置換、または243位でのロイシンによる、255位でのロイシンによる、および318位でのリシンによる置換、または334位でのグルタミン酸による、359位でのアスパラギンによる、および366位でのセリンによる置換、または288位でのメチオニンによる、および334位でのグルタミン酸による置換、または334位でのグルタミン酸による、および380位でのアスパラギン酸による置換、または256位でのセリンによる、305位でのイソロイシンによる、334位でのグルタミン酸による、および390位でのセリンによる置換、または335位でのアスパラギンによる、370位でのグルタミン酸による、378位でのバリンによる、394位でのメチオニンによる、および424位でのロイシンによる置換、または233位でのアスパラギン酸による、および334位でのグルタミン酸による置換、または334位でのグルタミン酸による、359位でのアスパラギンによる、366位でのセリンによる、および386位でのアルギニンによる置換、または246位でのスレオニンによる、および396位でのヒスチジンによる置換、または268位でのアスパラギン酸による、および318位でのアスパラギン酸による置換、または288位でのアスパラギンによる、330位でのセリンによる、および396位でのロイシンによる置換、または244位でのヒスチジンによる、358位でのメチオニンによる、379位でのメチオニンによる、384位でのリシンによる、および397位でのメチオニンによる置換、または217位でのセリンによる、378位でのバリンによる、および408位でのアルギニンによる置換、または247位でのロイシンによる、253位でのアスパラギンによる、および334位でのアスパラギンによる置換、または246位でのイソロイシンによる、および334位でのアスパラギンによる置換、または320位でのグルタミン酸による、および326位でのグルタミン酸による置換、または375位でのシステインによる、および396位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、305位でのイソロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、および300位でのロイシンによる置換、または243位でのロイシンによる、270位でのグルタミン酸による、392位でのアスパラギンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、255位でのロイシンによる、270位でのグルタミン酸による、および396位でのロイシンによる置換を含む。In vitroにおいてFcγRIIIAに対する増強された親和性をもたらす他のアミノ酸置換の例は以下に開示し、表6に要約している。
特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む単離ポリペプチドを包含し、前記ポリペプチドが、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドと比べて高い親和性でFcγRIIIAに特異的に結合するように、前記変異型重鎖は、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変を含み、前記少なくとも1つのアミノ酸改変は、396位でのヒスチジンによる置換;または248位でのメチオニンによる置換;または396位でのロイシンによる置換;または379位でのメチオニンによる置換;または219位でのチロシンによる置換;または282位でのメチオニンによる置換;または401位でのバリンによる置換;または222位でのアスパラギンによる置換;または334位でのグルタミン酸による置換;または377位でのフェニルアラニンによる置換;または334位でのイソロイシンによる置換;または247位でのロイシンによる置換;または326位でのグルタミン酸による置換;または372位でのチロシンによる置換;または224位でのロイシンによる置換;または243位でのロイシンによる置換;または292位でのプロリンによる置換;または275位でのチロシンによる置換;または398位でのバリンによる置換;または334位でのアスパラギンによる置換;または400位でのプロリンによる置換;または407位でのイソロイシンによる置換;または372位でのチロシンによる置換を含む。
ある実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む単離ポリペプチドを包含し、前記ポリペプチドが、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドと比べて類似の親和性でFcγRIIIAに特異的に結合するように、前記変異型重鎖は、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変を含み、前記少なくとも1つのアミノ酸改変は、392位でのアルギニンによる置換;または315位でのイソロイシンによる置換;または132位でのイソロイシンによる置換;または162位でのバリンによる置換;または366位でのアスパラギンによる置換を含む。
ある実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む単離ポリペプチドを包含し、前記ポリペプチドが、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドと比べて低下した親和性でFcγRIIIAに特異的に結合するように、前記変異型重鎖は、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変を含み、前記少なくとも1つのアミノ酸改変は、414位でのアスパラギンによる置換;または225位でのセリンによる置換;または377位でのアスパラギンによる置換を含む。
いくつかの実施形態では、本発明の分子は、重鎖-抗体受容体相互作用、特にFc-FcγR相互作用、すなわちFc領域のFcγRへの特異的結合を決定するための当技術分野において公知の、ELISAアッセイ、表面プラズモン共鳴アッセイ、免疫沈降アッセイ(セクション5.2参照)を含むが、これに限定されることはないin vitroアッセイ(生化学または免疫学ベースのアッセイ)を使って決定される場合、FcγRIIIAおよび/またはFcγRIIAに対する改変された親和性を有する。好ましくは、活性化FcγR受容体に対する親和性が改変されたこれらの分子の結合特性は、1つまたは複数のFcγR媒介物エフェクター細胞機能(セクション5.3参照)を決定するためのin vitro機能アッセイにより決定されるその活性とも相関があり、例えば、FcγRIIIAに対する親和性が増強された変異型重鎖またはその領域のある分子は、増強されたADCC活性を有する。最も好ましい実施形態では、活性化Fc受容体、例えば、FcγRIIIAに対する改変された結合特性をin vitroアッセイにおいて有する本発明の分子は、(本明細書に記載され開示されたモデルなどの)in vivoモデルにおいても改変された結合特性を有する。しかし、本発明は、in vitroベースのアッセイにおいて改変されたFcγR結合を示さないが、in vivoにおいて所望の表現型を示す本発明の分子を排除するものではない。
B. FcγRIIIAに対する親和性は増強されFcγRIIBに対する親和性は低下しているまたは全くない突然変異体
特定の実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域中に1つまたは複数のアミノ酸改変(すなわち、置換)を有する変異型重鎖を含み、この1つまたは複数の改変は、FcγRIIIAおよびFcγRIIBに野生型の親和性で結合する、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて、FcγRIIIAに対する変異型重鎖のFc領域の親和性を増大させ、FcγRIIBに対する変異型重鎖のFc領域の親和性を減少させる。ある実施形態では、1つまたは複数のアミノ酸改変は、FcγRIIIAに対する変異型重鎖のFc領域の親和性を少なくとも65%、少なくとも70%、少なくとも75%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも99%、少なくとも100%、少なくとも200%、少なくとも300%、少なくとも400%増大させ、FcγRIIBに対する変異型重鎖のFc領域の親和性を少なくとも65%、少なくとも70%、少なくとも75%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも99%、少なくとも100%、少なくとも200%、少なくとも300%、少なくとも400%減少させる。
特定の実施形態では、IgG2、IgG3またはIgG4のFc領域を含み、変異型重鎖を含む本発明の分子は、ELISAアッセイおよび/またはch-4-4-20抗体を使ったADCCベースのアッセイ、もしくは変異型重鎖を坦持するキメラ4D5抗体を使った表面プラズモン共鳴アッセイに基づいて決定される場合、FcγRIIIAに対する親和性が増強され、FcγRIIBに対する親和性が低下しているまたは親和性が全くなく、275位でのイソロイシンによる、334位でのアスパラギンによる、および348位でのメチオニンによる置換、または279位でのロイシンによる、および395位でのセリンによる置換、または246位でのスレオニンによる、および319位でのフェニルアラニンによる置換、または243位でのロイシンによる、255位でのロイシンによる、および318位でのリシンによる置換、または334位でのグルタミン酸による、359位でのアスパラギンによる、および 366位でのセリンによる置換、または334位でのグルタミン酸による、および380位でのアスパラギン酸による置換、または256位でのセリンによる、305位でのイソロイシンによる、334位でのグルタミン酸による、および390位でのセリンによる置換、または335位でのアスパラギンによる、370位でのグルタミン酸による、378位でのバリンによる、394位でのメチオニンによる、および424位でのロイシンによる置換、または233位でのアスパラギン酸による、および334位でのグルタミン酸による置換、または334位でのグルタミン酸による、359位でのアスパラギンによる、366位でのセリンによる、および386位でのアルギニンによる置換、または312位でのグルタミン酸による、327位でのアスパラギンによる、および378位でのセリンによる置換、または288位でのアスパラギンによる、および326位でのアスパラギンによる置換、または247位でのロイシンによる、および421位でのリシンによる置換、または298位でのアスパラギンによる、および381位でのアルギニンによる置換、または280位でのグルタミン酸による、354位でのフェニルアラニンによる、431位でのアスパラギン酸による、および441位でのイソロイシンによる置換、または255位でのグルタミンによる、および326位でのグルタミン酸による置換、または218位でのアルギニンによる、281位でのアスパラギン酸による、および385位でのアルギニンによる置換、または247位でのロイシンによる、330位でのスレオニンによる、および440位でのグリシンによる置換、または284位でのアラニンによる、および372位でのロイシンによる置換、または335位でのアスパラギンによる、387位でのセリンによる、および435位でのグルタミンによる置換、または247位でのロイシンによる、431位でのバリンによる、および442位でのフェニルアラニンによる置換、または243位でのロイシンによる、292位でのプロリンによる、305位でのイソロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、および305位でのイソロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、および300位でのロイシンによる置換、または292位でのプロリンによる、305位でのイソロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、および292位でのプロリンによる置換、または292位でのプロリンによる置換を含む。
特定の実施形態では、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含む本発明の分子は、ELISAアッセイおよび/または変異型重鎖を坦持するch-4-4-20抗体を使ったADCCベースのアッセイに基づいて決定される場合、FcγRIIIAに対する親和性が増強され、FcγRIIBに対する親和性が低下しているまたは親和性が全くなく、379位でのメチオニンによる、219位でのチロシンによる、282位でのメチオニンによる、401位でのバリンによる、222位でのアスパラギンによる、334位でのイソロイシンによる、334位でのグルタミン酸による、275位でのチロシンによる、398位でのバリンによる置換を含む。さらに別の実施形態では、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含む本発明の分子は、ELISAアッセイおよび/またはch-4-4-20抗体を使ったADCCベースのアッセイ、もしくは変異型重鎖を坦持するキメラ4D5抗体を使った表面プラズモン共鳴アッセイに基づいて決定される場合、FcγRIIIAに対する親和性が増強され、FcγRIIBに対する親和性が低下しているまたは親和性が全くなく、243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる置換を含む。
C. FcγRIIIAおよびFcγRIIBへの親和性が増強された突然変異体
本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する変異型重鎖を含む分子を包含し、この改変は、FcγRIIIAおよびFcγIIBに対する変異型重鎖の親和性を少なくとも65%、少なくとも70%、少なくとも75%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも99%、少なくとも100%、少なくとも200%、少なくとも300%、少なくとも400%増大させ、FcγRIIBに対する変異型Fc領域の親和性を少なくとも65%、少なくとも70%、少なくとも75%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも99%、少なくとも100%、少なくとも200%、少なくとも300%、少なくとも400%減少させる。特定の実施形態では、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を含む野生型重鎖に比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む本発明の分子は、(ELISAアッセイおよび/またはch-4-4-20抗体を使ったADCCベースのアッセイ、もしくは、本明細書に記載の変異型重鎖を坦持するキメラ4D5抗体を使った表面プラズモン共鳴アッセイに基づいて決定される場合)、FcγRIIIAに対する親和性が増強され、FcγRIIBに対する親和性が増強され、415位でのイソロイシンによる、および251位でのフェニルアラニンによる置換、または399位でのグルタミン酸による、292位でのロイシンによる、および185位でのメチオニンによる置換、または408位でのイソロイシンによる、215位でのイソロイシンによる、および125位でのロイシンによる置換、または385位でのグルタミン酸による、および247位でのヒスチジンによる置換、または348位でのメチオニンによる、334位でのアスパラギンによる、275位でのイソロイシンによる、202位でのメチオニンによる、および147位でのスレオニンによる置換、または246位でのスレオニンによる、および396位でのヒスチジンによる置換、または268位でのアスパラギン酸による、および318位でのアスパラギン酸による置換、または288位でのアスパラギンによる、330位でのセリンによる、および396位でのロイシンによる置換、または244位でのヒスチジンによる、358位でのメチオニンによる、379位でのメチオニンによる、384位でのリシンによる、および397位でのメチオニンによる置換、または217位でのセリンによる、378位でのバリンによる、および408位でのアルギニンによる置換、または247位でのロイシンによる、253位でのアスパラギンによる、および334位でのアスパラギンによる置換、または246位でのイソロイシンによる、および334位でのアスパラギンによる置換、または320位でのグルタミン酸による、および326位でのグルタミン酸による置換、または375位でのシステインによる、および396位でのロイシンによる置換、または343位でのセリンによる、353位でのロイシンによる、375位でのイソロイシンによる、および383位でのアスパラギンによる置換、または394位でのメチオニンによる、および397位でのメチオニンによる置換、または216位でのアスパラギン酸による、345位でのリシンによる、および375位でのイソロイシンによる置換、または288位でのアスパラギンによる、330位でのセリンによる、および396位でのロイシンによる置換、または247位でのロイシンによる、および389位でのグリシンによる置換、または222位でのアスパラギンによる、335位でのアスパラギンによる、370位でのグルタミン酸による、378位でのバリンによる、および394位でのメチオニンによる置換、または316位でのアスパラギン酸による、378位でのバリンによる、および399位でのグルタミン酸による置換、または315位でのイソロイシンによる、379位でのメチオニンによる、および394位でのメチオニンによる置換、または290位でのスレオニンによる、および371位でのアスパラギン酸による置換、または247位でのロイシンによる、および398位でのグルタミンによる置換、または326位でのグルタミンによる、334位でのグルタミン酸による、359位でのアスパラギンによる、および366位でのセリンによる置換、または247位でのロイシンによる、および377位でのフェニルアラニンによる置換、または378位でのバリンによる、390位でのイソロイシンによる、および422位でのイソロイシンによる置換、または326位でのグルタミン酸による、および385位でのグルタミン酸による置換、または282位でのグルタミン酸による、369位でのイソロイシンによる、および406位でのフェニルアラニンによる置換、または397位でのメチオニンによる、411位でのアラニンによる、および415位でのアスパラギンによる置換、または223位でのイソロイシンによる、256位でのセリンによる、および406位でのフェニルアラニンによる置換、または298位でのアスパラギンによる、および407位でのアルギニンによる置換、または246位でのアルギニンによる、298位でのアスパラギンによる、および377位でのフェニルアラニンによる置換、または235位でのプロリンによる、382位でのメチオニンによる、304位でのグリシンによる、305位でのイソロイシンによる、および323位でのイソロイシンによる置換、または247位でのロイシンによる、313位でのアルギニンによる、および388位でのグリシンによる置換、または221位でのチロシンによる、252位でのイソロイシンによる、330位でのグリシンによる、339位でのスレオニンによる、359位でのアスパラギンによる、422位でのイソロイシンによる、および433位でのロイシンによる置換、または258位でのアスパラギン酸による、および384位でのリシンによる置換、または241位でのロイシンによる、および258位でのグリシンによる置換、または370位でのアスパラギンによる、および440位でのアスパラギンによる置換、または317位でのアスパラギンによる置換、および423位での欠失、または243位でのイソロイシンによる、379位でのロイシンによる、および420位でのバリンによる置換、または227位でのセリンによる、および290位でのグルタミン酸による置換、または231位でのバリンによる、386位でのヒスチジンによる、および412位でのメチオニンによる置換、または215位でのプロリンによる、274位でのアスパラギンによる、287位でのグリシンによる、334位でのアスパラギンによる、365位でのバリンによる、および396位でのロイシンによる置換、または293位でのバリンによる、295位でのグルタミン酸による、および327位でのスレオニンによる置換、または319位でのフェニルアラニンによる、352位でのロイシンによる、および396位でのロイシンによる置換、または392位でのスレオニンによる、および396位でのロイシンによる置換、または268位でのアスパラギンによる、および396位でのロイシンによる置換、または290位でのスレオニンによる、390位でのイソロイシンによる、および396位でのロイシンによる置換、または326位でのイソロイシンによる、および396位でのロイシンによる置換、または268位でのアスパラギン酸による、および396位でのロイシンによる置換、または210位でのメチオニンによる、および396位でのロイシンによる置換、または358位でのプロリンによる、および396位でのロイシンによる置換、または288位でのアルギニンによる、307位でのアラニンによる、344位でのグルタミン酸による、および396位でのロイシンによる置換、または273位でのイソロイシンによる、326位でのグルタミン酸による、328位でのイソロイシンによる、および396位でのロイシンによる置換、または326位でのイソロイシンによる、408位でのアスパラギンによる、および396位でのロイシンによる置換、または334位でのアスパラギンによる、および396位でのロイシンによる置換、または379位でのメチオニンによる、および396位でのロイシンによる置換、または227位でのセリンによる、および396位でのロイシンによる置換、または217位でのセリンによる、および396位でのロイシンによる置換、または261位でのアスパラギンによる、210位でのメチオニンによる、および396位でのロイシンによる置換、または419位でのヒスチジンによる、および396位でのロイシンによる置換、または370位でのグルタミン酸による、および396位でのロイシンによる置換、または242位でのフェニルアラニンによる、および396位でのロイシンによる置換、または255位でロイシンによる、および396位でのロイシンによる置換、または240位でのアラニンによる、および396位でのロイシンによる置換、または250位でのセリンによる、および396位でのロイシンによる置換、または247位でのセリンによる、および396位でのロイシンによる置換、または410位でのヒスチジンによる、および396位でのロイシンによる置換、または419位でのロイシンによる、および396位でのロイシンによる置換、または427位でのアラニンによる、および396位でのロイシンによる置換、または258位でのアスパラギン酸による、および396位でのロイシンによる置換、または384位でのリシンによる、および396位でのロイシンによる置換、または323位でのイソロイシンによる、および396位でのロイシンによる置換、または244位でのヒスチジンによる、および396位でのロイシンによる置換、または305位でのロイシンによる、および396位でのロイシンによる置換、または400位でのフェニルアラニンによる、および396位でのロイシンによる置換、または303位でのイソロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、305位でのイソロイシンによる、378位でのアスパラギン酸による、404位でのセリンによる、および396位でのロイシンによる置換、または290位でのグルタミン酸による、369位でのアラニンによる、393位でのアラニンによる、および396位でのロイシンによる置換、または210位でのアスパラギンによる、222位でのイソロイシンによる、320位でのメチオニンによる、および396位でのロイシンによる置換、または217位でのセリンによる、305位でのイソロイシンによる、309位でのロイシンによる、390位でのヒスチジンによる、および396位でのロイシンによる置換、または246位でのアスパラギンによる、419位でのアルギニンによる、および396位でのロイシンによる置換、または217位でのアラニンによる、359位でのアラニンによる、および396位でのロイシンによる置換、または215位でのイソロイシンによる、290位でのバリンによる、および396位でのロイシンによる置換、または275位でのロイシンによる、362位でのヒスチジンによる、384位でのリシンによる、および396位でのロイシンによる置換、または334位でのアスパラギンによる置換、または400位でのプロリンによる置換、または407位でのイソロイシンによる置換、または372位でのチロシンによる置換、または366位でのアスパラギンによる置換、または414位でのアスパラギンによる置換、または352位でのロイシンによる置換、または225位でのセリンによる置換、または377位でのアスパラギンによる置換、または248位でのメチオニンによる置換、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、305位でのイソロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、および300位でのロイシンによる置換、または243位でのロイシンによる、292位でのプロリンによる、300位でのロイシンによる、および396位でのロイシンによる置換、または243位でのロイシンによる、および396位でのロイシンによる置換、または292位でのプロリンによる、および305位でのイソロイシンによる置換を含む。
D. どのFcγRにも結合しない突然変異体
いくつかの実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、1つまたは複数の領域内に少なくとも1つのアミノ酸改変を含む変異型重鎖を含む分子を包含し、この分子は、当技術分野で公知のおよび本明細書で開示している標準的アッセイにより決定する場合、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べてどのFcγRにも結合しない。特定の実施形態では、すべてのFcγRへの結合を無効にする前記1つまたは複数のアミノ酸改変は、232位でのセリンによる、および304位でのグリシンによる置換、または269位でのリシンによる、290位でのアスパラギンによる、311位でのアルギニンによる、および433位でのチロシンによる置換、または252位でのロイシンによる置換、または216位でのアスパラギン酸による、334位でのアルギニンによる、および375位でのイソロイシンによる置換、または247位でのロイシンによる、および406位でのフェニルアラニンによる置換、または335位でのアスパラギンによる、387位でのセリンによる、および435位でのグルタミンによる置換、または334位でのグルタミン酸による、380位でのアスパラギン酸による、および446位でのバリンによる置換、または303位でのイソロイシンによる、369位でのフェニルアラニンによる、および428位でのロイシンによる置換、または251位でのフェニルアラニンによる、および372位でのロイシンによる置換、または246位でのグルタミン酸による、284位でのメチオニンによる、および308位でのアラニンによる置換、または399位でのグルタミン酸による、および402位でのアスパラギン酸による置換、または399位でのグルタミン酸による、および428位でのロイシンによる置換を含む。
D. FcγR媒介エフェクター機能が改変された突然変異体
本発明は、改変または追加されたエフェクター機能を示す、すなわち変異体が、同一のアイソタイプのFc領域を有する野生型重鎖を含む抗体では検出可能でない検出可能なレベルの1つまたは複数のエフェクター機能を示す、変異型重鎖(すなわち、IgG2、IgG3またはIgG4のFc領域、および同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する重鎖)を含む免疫グロブリンを包含する。いくつかの実施形態では、重鎖変異体を含む免疫グロブリンは、当技術分野で公知のおよび本明細書で例証されているアッセイ法を使って決定した場合、エフェクター細胞の存在の下ではエフェクター機能をより効果的に媒介する。他の実施形態では、重鎖変異体を含む免疫グロブリンは、当技術分野で公知のおよび本明細書で例証されているアッセイ法を使って決定した場合、エフェクター細胞の存在の下ではエフェクター機能をより非効果的に媒介する。特定の実施形態では、本発明の重鎖変異体は、組合せが相加的、相乗的効果を有するように、エフェクター機能を改変する他の既知の重鎖改変と組み合わせてもよい。本発明の重鎖変異体は、in vitroおよび/またはin vivoにおいてエフェクター機能を改変している。
特定の実施形態では、本発明の免疫グロブリンは、本明細書で開示したADCC活性アッセイを使って決定した場合、改変または増強されたFcγR媒介エフェクター機能を有する。本発明の分子により媒介することができるエフェクター機能の例には、C1q結合、補体依存性細胞傷害、抗体依存性細胞媒介性細胞傷害(ADCC)、貪食性などがあるが、これらの機能に限定されるものではない。本発明の分子のエフェクター機能は、当技術分野で公知の標準的方法を使って検定することができ、その例はセクション5.2に開示している。特定の実施形態では、変異型重鎖を含む本発明の免疫グロブリンは、ADCCを、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンよりも2倍効果的に媒介する。他の実施形態では、変異型重鎖を含む本発明の免疫グロブリンは、ADCCを、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンよりも、少なくとも4倍、少なくとも8倍、少なくとも10倍、少なくとも100倍、少なくとも1000倍、少なくとも104倍、少なくとも105倍効果的に媒介する。別の特定の実施形態では、本発明の免疫グロブリンは、C1q結合活性を改変した。いくつかの実施形態では、本発明の免疫グロブリンは、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンよりも、少なくとも2倍、少なくとも4倍、少なくとも8倍、少なくとも10倍、少なくとも100倍、少なくとも1000倍、少なくとも104倍、少なくとも105倍高いC1q結合活性を有する。さらに別の特定の実施形態では、本発明の免疫グロブリンは、補体依存性細胞傷害を改変した。さらに別の特定の実施形態では、本発明の免疫グロブリンは、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンよりも増強された補体依存性細胞傷害を有する。いくつかの実施形態では、本発明の免疫グロブリンは、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンよりも、少なくとも2倍、少なくとも4倍、少なくとも8倍、少なくとも10倍、少なくとも100倍、少なくとも1000倍、少なくとも104倍、少なくとも105倍高い補体依存性細胞傷害を有する。
他の実施形態では、本発明の免疫グロブリンは、当業者には既知のまたは本明細書で開示された標準的アッセイ法により決定される場合、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンと比べて貪食性活性を改変または増強した。いくつかの実施形態では、本発明の免疫グロブリンは、同一のアイソタイプのFc領域を有する野生型重鎖を含む免疫グロブリンと比べて、少なくとも2倍、少なくとも4倍、少なくとも8倍、少なくとも10倍高い貪食性活性を有する。
特定の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含む免疫グロブリンを包含し、免疫グロブリンが増強されたエフェクター機能、例えば、抗体依存性細胞媒介性細胞傷害または食作用を有するように、この変異型重鎖は、同一のアイソタイプのFc領域を含む野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する。特定の実施形態では、免疫グロブリンのADCC活性を増大させる1つまたは複数のアミノ酸改変は、379位でのメチオニンによる置換;または243位でのイソロイシンによる置換および379位でのロイシンによる置換;または288位でのアスパラギンによる置換、330位でのセリンによる置換および396位でのロイシンによる置換;または243位でのロイシンによる置換および255位でのロイシンによる置換;または334位でのグルタミン酸による置換、359位でのアスパラギンによる置換および366位でのセリンによる置換;または288位でのメチオニンによる置換および334位でのグルタミン酸による置換;または334位でのグルタミン酸による置換および292位でのロイシンによる置換;または316位でのアスパラギン酸による置換、378位でのバリンによる置換および399位でのグルタミン酸による置換;または315位でのイソロイシンによる置換、379位でのメチオニンによる置換および399位でのグルタミン酸による置換;または243位でのイソロイシンによる置換、379位でのロイシンによる置換および420位でのバリンによる置換;または247位でのロイシンによる置換および421位でのリシンによる置換;または248位でのメチオニンによる置換;または392位でのスレオニンによる置換および396位でのロイシンによる置換;または293位でのバリンによる置換、295位でのグルタミン酸による置換および327位でのスレオニンによる置換;または268位でのアスパラギンによる置換および396位でのロイシンによる置換;または319位でのフェニルアラニンによる置換、352位でのロイシンによる置換および396位でのロイシンによる置換;または243位でのロイシンによる置換、292位でのプロリンによる置換、300位でのロイシンによる置換、305位でのイソロイシンによる置換および396位でのロイシンによる置換;または243位でのロイシンによる置換、292位でのプロリンによる置換、300位でのロイシンによる置換および396位でのロイシンによる置換;または243位でのロイシンによる置換、292位でのプロリンによる置換および300位でのロイシンによる置換;または255位でのロイシンによる置換、396位でのロイシンによる置換、270位でのグルタミン酸による置換および300位でのロイシンによる置換;または240位でのアラニンによる置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または370位でのグルタミン酸による置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または392位でのスレオニンによる置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または370位でのグルタミン酸による置換および396位でのロイシンによる置換;または419位でのヒスチジンによる置換および396位でのロイシンによる置換;または255位でのロイシンによる置換、396位でのロイシンによる置換、270位でのグルタミン酸による置換および292位でのグリシンによる置換を含む。他の特定の実施形態では、本発明の変異型重鎖は、247位にロイシン、421位にリジンおよび270位にグルタミン酸(MgFc31/60);392位にスレオニン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc38/60/F243L);419位にヒスチジン、396位にロイシンおよび270位にグルタミン酸(MGFc51/60);419位にヒスチジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MGFc51/60/F243L);240位にアラニン、396位にロイシンおよび270位にグルタミン酸(MGFc52/60);255位にリジンおよび396位にロイシン(MgFc55);255位にリジン、396位にロイシンおよび270位にグルタミン酸(MGFc55/60);255位にリジン、396位にロイシン、270位にグルタミン酸および300位にリジン(MGFc55/60/Y300L);255位にリジン、396位にロイシン、270位にグルタミン酸および292位にグリシン(MgFc55/60/R292G);255位にリジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc55/60/F243L);370位にグルタミン酸、396位にロイシンおよび270位にグルタミン酸(MGFc59/60);270位にグルタミン酸、316位にアスパラギン酸および416位にグリシン(MgFc71);243位にロイシン、292位にプロリン、305位にイソロイシンおよび396位にロイシン(MGFc74/P396L);または243位にロイシン、270位にグルタミン酸、392位にアスパラギンおよび396位にロイシン;または243位にロイシン、255位にロイシン、270位にグルタミン酸および396位にロイシン;または297位にグルタミン酸を有する。
別の特定の実施形態では、免疫グロブリンのADCC活性を増大させる1つまたは複数のアミノ酸改変は、以下の表8に記載した突然変異のいずれかである。表8に記載した突然変異は、IgG1のFc領域の状況で元々同定された。
その代わりにまたはそれに加えて、本発明の分子を工学的に改変して、上記のアミノ酸改変または本明細書で開示された他の任意のアミノ酸改変を、この分子がC1q結合および/または補体依存性細胞傷害機能の変更または付与を示すように、変異型重鎖の非IgG1ドメインまたは領域の状況での1つまたは複数のさらなるアミノ酸改変と組み合わせることは有用であり得る。本明細書において特に対象となる開始分子は通常、C1qに結合し、補体依存性細胞傷害(CDC)を示す分子である。本明細書に記載のさらなるアミノ酸置換および/または重鎖改変、例えば、IgG2、IgG3またはIgG4のFc領域を有する天然のFc領域の置換は、一般に、C1qに結合しかつ/またはその補体依存性細胞傷害機能を改変する、例えば、これらのエフェクター機能を低下、好ましくは無効にする開始分子の能力を改変するのに役立つであろう。しかし、C1q結合および/または補体依存性細胞傷害(CDC)機能が付与または改良された、前記記載の位置のうちの1つまたは複数における置換を含む分子は、本明細書で企図されている。例えば、前記開始分子は、C1qに結合するかつ/またはCDCを媒介することができない場合があり、開始分子がこれらの追加のエフェクター機能を獲得するように、本明細書の教唆に従って改変してもよい。さらに、既存のC1q結合活性を有し、随意にさらにCDCを媒介する能力を有する分子は、これらの活性のうちの一方または両方が増強されるように、改変されてもよい。
上に開示する通り、C1q結合および/またはFcR結合を付与し、それによりCDC活性および/またはADCC活性を変化させるために、例えば、そのFc領域の置換および/またはアミノ酸改変によってエフェクター機能が変更された変異型重鎖を設計することができる。C1q結合の改良または付与およびFcγRIII結合の改良または付与を示し、例えば、ADCC活性が改良または付与され、CDC活性が改良または付与された、IgG2、IgG3またはIgG4のFc領域を有し、本明細書に記載の1つまたは複数のアミノ酸改変を有する変異型重鎖を作製することができる。あるいは、エフェクター機能を低下し、または取り除くことが望まれる場合、CDC活性の低下および/またはADCC活性の低下を示す、IgG2、IgG3またはIgG4のFc領域を含み、本明細書に記載の1つまたは複数のアミノ酸改変を有する変異型重鎖を工学的に改変してもよい。他の実施形態では、例えば、ADCC活性は改良されているが、CDC活性は低下している、またその逆の重鎖変異体を作製するために、これらの活性のうちの一方のみを増大させてよく、また場合によって他方の活性を低下させてもよい。
本発明は、本発明者ら同時出願であり、そのそれぞれの全体が参照により本明細書に組み込まれている国際公開第04/063351号および米国特許出願公開第2005/0037000号および第2005/0064514号に記載の通り酵母ライブラリーを使用して、IgG1重鎖、特にIgG1 Fc領域の状況ですでに同定されている重鎖、特にFc領域の特定のアミノ酸改変を包含する(表9)。前記IgG1突然変異体は、FcγRIIIAおよびFcγRIIBへの結合を判断するためにELISAアッセイを使って検定した。前記突然変異体は、本明細書に開示し例示している方法を使ってFc変異体をch-4-4-20抗体にクローン化することにより、ADCCアッセイでも試験した。太字の項目は、ADCCアッセイに先立って前記ch-4-4-20抗体を精製した実験を示している。使用した抗体濃度は、ADCCアッセイにおいて標準の0.5μg/mL〜1.0μg/mLの範囲であった。
ある実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する変異型重鎖を有する改変された免疫グロブリン分子(例えば、抗体)を提供し、この1つまたは複数のアミノ酸改変は、エフェクター機能を付与または変更し、かつ/またはFcγRに対する分子の親和性を増大または変更する。このような免疫グロブリンには、自然にFcγR結合領域(例えば、FcγRIIIAおよび/またはFcγRIIB結合領域)を含むIgG分子、自然にはFcγRに結合しない免疫グロブリン分子、またはFcγR結合領域(例えば、FcγRIIIAおよび/またはFcγRIIB結合領域)を含むように工学的に改変された免疫グロブリン誘導体が含まれる。本発明の改変された免疫グロブリンには、好ましくは、免疫特異的に、すなわち、特異的な抗原抗体結合を検定するための当技術分野で公知の免疫アッセイ法により決定される場合に非特異的結合と競合せずに、抗原に結合し、FcγR結合領域(例えば、FcγRIIIAおよび/またはFcγRIIB結合領域)を含有するあらゆる免疫グロブリン分子がある。そのような抗体には、ポリクローナル、モノクローナル、二重特異性、多重特異性、ヒト、ヒト化型、キメラ抗体、一本鎖抗体、Fab断片、F(ab')2断片、ジスルフィド連結Fv、および、VLもしくはVHドメインのいずれか、または、抗原に特異的に結合し、ある種の場合には、FcγR結合領域を含有するよう工学的に改変されるもしくはFcγR結合領域に融合される相補性決定領域(CDR)までも含有する断片があるがこれらに限定されない。
いくつかの実施形態では、本発明の分子は、重鎖の部分を含み、特にFc領域またはその部分を含む。本明細書で使用する用語「Fc領域の一部」とは、Fc領域の断片、好ましくはエフェクター活性および/またはFcγR結合活性のある部分(または、そのような活性を欠く突然変異体の比較可能な領域)のことである。Fc領域の断片は、大きさが5個のアミノ酸からアミノ酸を1個欠く全Fc領域までの範囲がある。Fc領域の部分は、N末端またはC末端から最大10個、最大20個、最大30個のアミノ酸が欠失している場合もある。
本発明のIgG分子は、好ましくはIgGのIgG1サブクラスであるが、それだけに限らないが、ラット、マウスおよび霊長類、例えば、チンパンジー、ヒヒおよびマカクを含めた所与の動物の任意の他のIgGサブクラスであってもよい。例えば、ヒトではIgGクラスにはIgG1、IgG2、IgG3およびIgG4が含まれ、マウスIgGにはIgG1、IgG2a、IgG2b、IgG2cおよびIgG3が含まれ、ラットには、IgG1、IgG2a、IgG2bおよびIgG2cが含まれる。
免疫グロブリン(および本明細書に使用の他のポリペプチド)は、鳥類および哺乳動物を含むいかなる動物起源由来でもよい。好ましくは、抗体はヒト、げっ歯類(例えば、マウスおよびラット)、ロバ、ヒツジ、ウサギ、ヤギ、モルモット、ラクダ、ウマ、またはニワトリである。本明細書で使用する「ヒト」抗体には、下に記載のおよび、例えば、Kucherlapatiらによる米国特許第5,939,598号に記載の、ヒト免疫グロブリンのアミノ酸配列を有する抗体があり、ヒト免疫グロブリンライブラリーから、または1つまたは複数のヒト免疫グロブリンのトランスジェニック動物、および内在性免疫グロブリンを発現しない動物から単離した抗体がある。
本発明の抗体は、単一特異性、二重特異性、三重特異性でも、さらに大きな多重特異性でもよい。多重特異性抗体は、ポリペプチドの異なるエピトープに特異的でもよいし、異種ポリペプチドまたは固体の支持物質などの異種エピトープに特異的でもよい。例えば、PCT国際公開国際公開第93/17715号、国際公開第92/08802号、国際公開第91/00360号、国際公開第92/05793号、Tutt, et al, J. Immunol., 147:60-69, 1991、米国特許第4,474,893号、米国特許第4,714,681号、米国特許第4,925,648号、米国特許第5,573,920号、米国特許第5,601,819号、Kostelny et al., J. Immunol., 148:1547-1553, 1992を参照されたい。
多重特異性抗体は、少なくとも2つの異なる抗原に対する結合特異性を有する。そのような分子は、通常は2つの抗原のみにしか結合しないが(すなわち、二重特異性抗体、BsAb)、三重特異性抗体などの追加の特異性のある抗体は本発明に包含される。BsAbの例には、無制限に、一方のアームは腫瘍細胞抗原に向けられもう一方のアームは細胞傷害分子に向けられた二重特異性抗体がある。
二重特異性抗体を作製する方法は当技術分野では公知である。全長二重特異性抗体の従来の作製は、2つの鎖が異なる特異性を有する2つの免疫グロブリン重鎖軽鎖対の共発現に基づいている(Millstein et al., Nature, 305:537-539 (1983)、本文献は参照によりその全体が本明細書に組み込まれているものとする)。免疫グロブリン重鎖および軽鎖の無秩序な組合せのせいで、これらのハイブリドーマ(クアドローマ)は10の異なる抗体分子の潜在的な混合物を産生し、そのうちの1つの抗体のみが正確な二重特異的構造を有する。通常、アフィニティークロマトグラフィー段階により行われる前記正確な分子の精製は、かなり厄介であり、生産収量は低い。類似の手法が国際公開第93/08829号、およびTraunecker et al., EMBO J., 10:3655-3659 (1991)に開示されている。
別の方法に従えば、所望の結合特異性を有する抗体可変ドメイン(抗体抗原結合部位)は、免疫グロブリン定常ドメイン配列に融合している。この融合物は好ましくは、IgG2、IgG3またはIgG4から独立に選択されるヒンジ領域、CH2領域およびCH3領域の少なくとも一部を含む免疫グロブリン重鎖定常ドメインを有する。軽鎖結合に必要な部位を含み、この融合物の少なくとも1つに存在する第1の重鎖定常領域(CH1)を有することが好ましい。いくつかの実施形態では、本発明の分子のCH1領域はIgG1由来である。前記免疫グロブリン重鎖融合物、および必要であれば免疫グロブリン軽鎖をコードするDNAを、別個の発現ベクターに挿入し、適切な宿主生物にコトランスフェクトする。構築に使用される不均等な割合の3つのポリペプチド鎖が最適収量を提供する場合、これは、実施形態中の前記3つのポリペプチド断片の相互の割合を調整するのに大きな柔軟性を提供する。しかし、均等な割合の少なくとも2つのポリペプチド鎖の発現が高収量をもたらす場合、または前記割合が特に重要ではない場合には、2つまたは3つすべてのポリペプチド鎖のコード配列を1つの発現ベクターに挿入することができる。
この方法の好ましい実施形態では、二重特異性抗体は、一方のアームの第1の結合特異性を備えているハイブリッド免疫グロブリン重鎖、およびもう一方のアームのハイブリッド免疫グロブリン重鎖軽鎖対(第2の結合特異性を与える)で構成されている。二重特異性分子の一方の半分だけに免疫グロブリン軽鎖が存在することが容易な分離法を提供するので、この非対称構造が、所望の二重特異性化合物の望まれない免疫グロブリン鎖の組合せからの分離を促進することが発見された。この方法は、国際公開第94/04690号に開示されている。さらに詳細な二重特異性抗体の作製は、例えば、Suresh et al., Methods in Enzymology、121:210 (1986)を参照されたい。国際公開第96/27011号に記載の別の方法に従えば、1対の抗体分子を、組換え細胞培養から回収されるヘテロ二量体の割合を最大にするよう工学的に改変することができる。好ましい接触面は、少なくとも抗体定常ドメインのCH3ドメインの一部を含む。この方法では、第1の抗体分子の接触面由来の1つまたは複数の小アミノ酸側鎖はさらに大きな側鎖(例えば、チロシンまたはトリプトファン)と置き換えられる。大きな側鎖(群)と同一のまたは類似の大きさの代償の「空洞」が、大きなアミノ酸側鎖をさらに小さなアミノ酸側鎖(例えば、アラニンまたはスレオニン)と置き換えることにより、第2の抗体分子の接触面に作られる。これは、ホモ二量体などの他の望まれない末端産物よりもヘテロ二量体の収量を増大させるための機序を提供する。
二重特異性抗体には、架橋または「ヘテロコンジュゲート」抗体がある。例えば、ヘテロコンジュゲートの抗体の一方はアビジンと結合し、もう一方はビオチンと結合することができる。そのような抗体は、例えば、免疫系細胞を望まれない細胞に標的するために(米国特許第4,676,980号)、およびHIV感染の治療のために(国際公開第91/00360号、国際公開第92/200373号、および欧州特許第03089号)提唱されてきた。ヘテロコンジュゲート抗体は、いかなる便利な架橋法を使って作製してもよい。適切な架橋剤は当技術分野では公知であり、米国特許第4,676,980号でいくつかの架橋技術とともに開示されている。
二価を超える抗体が企図されている。例えば、三重特異性抗体を調製することができる。例えば、Tutt et al., 1991, J. Immunol. 147: 60を参照されたい。この文献は参照により本明細書に組み込まれているものとする。
本発明の抗体には、他の方法で、すなわち、共有結合が、抗体が抗原に結合することおよび/または抗イディオタイプ応答を生じることを妨げないように、いかなる種類の分子でも抗体と共有結合させることにより改変される誘導体がある。例えば、抗体誘導体には、例えば、グリコシル化、アセチル化、ペグ化、リン酸化、アミド化、既知の保護/ブロッキング基による誘導体化、タンパク質切断、細胞リガンドまたは他のタンパク質への連鎖などにより改変された抗体があるが、これらの抗体に限定するつもりはない。数多くの化学修飾のうちいずれも、特定の化学的切断、アセチル化、ホルミル化、ツニカマイシンの代謝合成などを含むがこれらに限定されるものではない既知の技術により実施してもよい。そのうえ、前記誘導体は、1つまたは複数の非古典的なアミノ酸を含有していてもよい。
ヒトにおける抗体のin vivo使用およびin vitro検出アッセイを含むいくつかの使用のために、キメラ、ヒト化型、またはヒト抗体を使用するのが好ましいこともある。キメラ抗体は、マウスモノクローナル抗体由来の可変領域とヒト免疫グロブリン由来の定常領域を有する抗体など、抗体の異なる部分が異なる動物種由来である分子である。キメラ抗体を作製する方法は当技術分野で公知である。例えば、Morrison, Science, 229:1202, 1985, Oi et al., BioTechniques, 4:214 1986, Gillies et al., J. Immunol. Methods, 125:191-202, 1989、米国特許第5,807,715号、米国特許第4,816,567号、および米国特許第4,816,397号を参照されたい。これらの文献は、参照によりその全体が本明細書に組み込まれているものとする。ヒト化型抗体は、非ヒト種由来の1つまたは複数の相補性決定領域(CDR)、ならびにヒト免疫グロブリン分子由来のフレームワーク領域および定常ドメインを有し、所望の抗原に結合する非ヒト種由来の抗体分子である。多くの場合、ヒトフレームワーク領域のフレームワーク残基は、CDR供与体抗体由来の対応する残基で置換され、抗原結合を改変する、好ましくは改良するであろう。これらのフレームワーク置換は、当技術分野で公知の方法により、例えば、抗原結合にとり重要なフレームワーク残基を同定するためのCDRとフレームワーク残基の相互作用のモデル化、および特定の位置での珍しいフレームワーク残基を同定するための配列比較により、同定される。例えば、Queen et al.、米国特許第5,585,089号、およびRiechmann et al., Nature, 332:323, 1988を参照されたい。これらの文献は、参照によりその全体が本明細書に組み込まれているものとする。抗体は、例えば、CDRグラフティング(欧州特許第239,400号、PCT国際公開国際公開第91/09967号、米国特許第5,225,539号、米国特許第5,530,101号、および米国特許第5,585,089号)、ベニアリングまたはリサーフェシング(欧州特許第592,106号、欧州特許第519,596号、Padlan, Molecular Immunology, 28(4/5):489-498, 1991, Studnicka et al., Protein Engineering, 7(6):805-814, 1994, Roguska et al., Proc Natl. Acad. Sci. USA, 91:969-973, 1994)、および、チェインシャフリング(米国特許第5,565,332号)を含む当技術分野で公知の種々の技術を使ってヒト化することができる。これらの文献はすべて、参照によりその全体が本明細書に組み込まれているものとする。ヒト化型抗体は、米国特許第5,693,762号(Protein Design Labs)、米国特許第5,693,761号、(Protein Design Labs)、米国特許第5,585,089号(Protein Design Labs)、米国特許第6,180,370号(Protein Design Labs)、および米国特許公開第20040049014号、米国特許公開第200300229208号に開示された方法のいずれを使って製作してもよい。これらの特許文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
完全ヒト抗体は、ヒト患者の治療上の処置に特に好ましい。ヒト抗体は、ヒト免疫グロブリン配列由来の抗体ライブラリーを使った上記のファージディスプレイ法を含む、当技術分野で公知の種々の方法により作製することができる。米国特許第4,444,887号、および米国特許第4,716,111号、ならびにPCT国際公開国際公開第98/46645号、国際公開第98/50433号、国際公開第98/24893号、国際公開第98/16654号、国際公開第96/34096号、国際公開第96/33735号、および国際公開第91/10741号を参照されたい。これらの特許文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
ヒト抗体は、機能的内在性免疫グロブリンを発現することはできないが、ヒト免疫グロブリン遺伝子を発現することができるトランスジェニックマウスを使って作製することもできる。ヒト抗体を作製するためのこの技術の概観は、Lonberg and Huszar, Int. Rev. Immunol., 13:65-93、1995を参照されたい。ヒト抗体およびヒトモノクローナル抗体を作製するためのこの技術の詳細な議論、ならびにそのような抗体を作製するためのプロトコールは、PCT国際公開国際公開第98/24893号、国際公開第92/01047号、国際公開第96/34096号、国際公開第96/33735号、欧州特許第0 598 877号、米国特許第5,413,923号、米国特許第5,625,126号、米国特許第5,633,425号、米国特許第5,569,825号、米国特許第5,661,016号、米国特許第5,545,806号、米国特許第5,814,318号、米国特許第5,885,793号、米国特許第5,916,771号、および米国特許第5,939,598号を参照されたい。これらの特許文献は、参照によりその全体が本明細書に組み込まれているものとする。さらに、Abgenix, Inc. (Freemont、CA)、Medarex (NJ) and Genpharm (San Jose、CA)などの会社は、上記の技術に類似の技術を使って、選択された抗原に対して向けられたヒト抗体を提供することができる。
選択されたエピトープを認識する完全ヒト抗体は、「誘導選択」と呼ばれる技術を使って作製することができる。この方法では、選択された非ヒトモノクローナル抗体、例えばマウス抗体、を使って、同一エピトープを認識する完全ヒト抗体の選択を誘導する(Jespers et al., Bio/technology、12:899-903、1988参照)。
本発明は、天然の領域またはドメインを異種のアイソタイプの対応する領域またはドメインで置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、重鎖においてヒトまたはヒト化治療用抗体(例えば、腫瘍特異的モノクローナル抗体)を工学的に改変することを包含し、この改変は、同一のアイソタイプのFc領域を有する野生型重鎖を含む抗体と比べて当業者に知られている標準的アッセイによって決定される、FcγR、例えば、FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を変更または増大させる、かつ/またはエフェクター機能活性、例えば、ADCC活性、補体活性化、食作用活性などを付与または変更する。他の実施形態では、工学的に改変された治療用抗体は、変異型重鎖のFc領域によって媒介されるオリゴマー化活性を示し得る。別の実施形態では、本発明は、天然の領域またはドメインを異種のアイソタイプの対応する領域またはドメインで置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、重鎖においてヒトまたはヒト化治療用抗体(例えば、腫瘍特異的モノクローナル抗体)を工学的に改変することに関し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対するFc領域の親和性を増大させ、さらにFcγRIIBに対するFc領域の親和性を低下させる。
特定の実施形態では、本発明は、天然のFc領域をIgG2、IgG3またはIgG4のFc領域で置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、Her2/neu癌原遺伝子に特異的なヒト化型モノクローナル抗体(例えば、Carter et al., 1992, Proc. Natl. Acad. Sci. USA 89:4285-9に開示されたAb4D5ヒト化型抗体)を工学的に改変することを包含し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対するFc領域の親和性を増大させる。別の具体的な実施形態では、ヒト化Her2/neuモノクローナル抗体の改変はさらに、FcγRIIBに対する変異型重鎖のFc領域の親和性を低下させることもできる。さらに別の特定の実施形態では、本発明に従って工学的に改変されたHer2/neuに特異的なヒト化モノクローナル抗体はさらに、当技術分野で知られており、本明細書で開示および例示される標準的アッセイによって決定される増強されたエフェクター機能を有し得る。
別の実施形態では、本発明は、天然の領域またはドメインを異種のアイソタイプの対応する領域またはドメインで置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、マウスヒトキメラ抗CD20モノクローナル抗体2H7を工学的に改変することを包含し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対するFc領域の親和性を増大させる。別の特定の実施形態では、抗CD20モノクローナル抗体2H7の改変はさらに、FcγRIIBに対するFc領域の親和性を低下させることもできる。さらに別の特定の実施形態では、工学的に改変された抗CD20モノクローナル抗体2H7はさらに、当技術分野で知られており、本明細書で開示および例示される標準的アッセイによって決定される増強されたエフェクター機能を有し得る。
特定の実施形態では、本発明は、2B6または3H7のCDRを含むヒト化抗体を工学的に改変することを包含する。特に、配列番号1のアミノ酸配列を有する重鎖可変ドメインおよび配列番号2、配列番号3または配列番号4のアミノ酸配列を有する軽鎖可変ドメインを含む抗体。特定の実施形態では、本発明は、配列番号5のアミノ酸配列を有する重鎖可変ドメインおよび配列番号6のアミノ酸配列を有する軽鎖可変ドメインを含むヒト化抗体を工学的に改変することを包含する。
別の特定の実施形態では、本発明は、天然の領域またはドメインを異種のアイソタイプの対応する領域またはドメインで置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、それだけに限らないが、2002年8月12日出願の米国特許仮出願第60/403,266、2003年8月14日出願の米国特許出願第10/643,857号、2004年4月16日出願の米国特許仮出願第60/562,804号、2004年6月21日出願の米国特許仮出願第60/582,044号、2004年6月21日出願の米国特許仮出願第60/582,045号、2004年12月15日出願の米国特許仮出願第60/636,663号、および2005年2月11日出願の米国特許出願第10/524,134号に開示される任意の抗体を含めた抗FcγRIIB抗体を工学的に改変することを包含し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対するFc領域の親和性を増大させる。別の特定の実施形態では、本発明は、天然の領域またはドメインを異種のアイソタイプの対応する領域またはドメインで置換するまたは置き換えること、および少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)の両方により、それだけに限らないが、2004年5月10日出願の米国特許仮出願第60/569,882号、2004年6月21日出願の米国特許仮出願第60/582,043号、および2005年5月10日出願の米国特許出願第11/126,978号に開示される任意の抗体を含めたヒト化抗FcγRIIB抗体を工学的に改変することを包含し、この改変は、FcγRIIIAおよび/またはFcγRIIAに対するFc領域の親和性を増大させる。上記の出願はそれぞれ、その全体が参照により本明細書に組み込まれている。ヒト化してもしなくてもよい、本発明の方法に従って工学的に改変することができる抗FcγRIIB抗体の例は、ATCCアクセッション番号PTA-4591を有する2B6モノクローナル抗体およびATCCアクセッション番号PTA-4592を有する3H7、ATCCアクセッション番号PTA-5958を有する1D5モノクローナル抗体、ATCCアクセッション番号PTA-5959を有する1F2モノクローナル抗体、ATCCアクセッション番号PTA-5960を有する2D11モノクローナル抗体、ATCCアクセッション番号PTA-5961を有する2E1モノクローナル抗体およびATCCアクセッション番号PTA-5962を有する2H9モノクローナル抗体(すべて10801 University Boulevard, Manassas, VA02209-2011に寄託されている)であり、これらは参照により本明細書に組み込まれている。別の特定の実施形態では、抗FcγRIIB抗体の改変はさらに、FcγRIIBに対するFc領域の親和性を低下させてもよい。さらに別の特定の実施形態では、工学的に改変された抗FcγRIIB抗体はさらに、当技術分野で知られており、本明細書に開示および例示される標準的なアッセイによって決定される増強されたエフェクター機能を有し得る。特定の実施形態では、2B6モノクローナル抗体は、334位でのグルタミン酸による改変、359位でのアスパラギンによる改変および366位でのセリンによる改変(MgFc13);または316位でのアスパラギン酸による置換、378位でのバリンによる置換および399位でのグルタミン酸による置換(MgFc27);または243位でのイソロイシンによる置換、379位でのロイシンによる置換および420位でのバリンによる置換(MgFc29);または392位でのスレオニンによる置換および396位でのロイシンによる置換(MgFc38);または221位でのグルタミン酸による置換、270位でのグルタミン酸による置換、308位でのアラニンによる置換、311位でのヒスチジンによる置換、396位でのロイシンによる置換および402位でのアスパラギン酸による置換(MgFc42);または410位でのヒスチジンによる置換および396位でのロイシンによる置換(MgFc53);または243位でのロイシンによる置換、305位でのイソロイシンによる置換、378位でのアスパラギン酸による置換、404位でのセリンによる置換および396位でのロイシンによる置換(MgFc54);または255位でのイソロイシンによる置換および396位でのロイシンによる置換(MgFc55);または370位でのグルタミン酸による置換および396位でのロイシンによる置換(MgFc59);または243位でのロイシンによる置換、292位でのプロリンによる置換、300位でのロイシンによる置換、305位でのイソロイシンによる置換および396位でのロイシンによる置換(MgFc88);または243位でのロイシンによる置換、292位でのプロリンによる置換、300位でのロイシンによる置換および396位でのロイシンによる置換(MgFc88A);または243位でのロイシンによる置換、292位でのプロリンによる置換および300位でのロイシンによる置換(MgFc155)を含む(表6および7参照)。
特定の実施形態では、本発明は、255位でのロイシンによる置換、396位でのロイシンによる置換、270位でのグルタミン酸による置換および300位でのロイシンによる置換;または419位でのヒスチジンによる置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または240位でのアラニンによる置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または370位でのグルタミン酸による置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または392位でのスレオニンによる置換、396位でのロイシンによる置換および270位でのグルタミン酸による置換;または370位でのグルタミン酸による置換および396位でのロイシンによる置換;または419位でのヒスチジンによる置換および396位でのロイシンによる置換;または247位でのロイシンによる置換、421位でのリジンによる置換および270位でのグルタミン酸による置換;または255位でのロイシンによる置換、396位でのロイシンによる置換、270位でのグルタミン酸による置換および292位でのグリシンによる置換を有する重鎖を含む改変された分子を包含する。他の特定の実施形態では、変異型Fc領域は、247位にロイシン、421位にリジンおよび270位にグルタミン酸(MgFc31/60);392位にスレオニン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc38/60/F243L);419位にヒスチジン、396位にロイシンおよび270位にグルタミン酸(MGFc51/60);419位にヒスチジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MGFc51/60/F243L);240位にアラニン、396位にロイシンおよび270位にグルタミン酸(MGFc52/60);255位にリジンおよび396位にロイシン(MgFc55);255位にリジン、396位にロイシンおよび270位にグルタミン酸(MGFc55/60);255位にリジン、396位にロイシン、270位にグルタミン酸および300位にリジン(MGFc55/60/Y300L);255位にリジン、396位にロイシン、270位にグルタミン酸および292位にグリシン(MgFc55/60/R292G);255位にリジン、396位にロイシン、270位にグルタミン酸および243位にロイシン(MgFc55/60/F243L);370位にグルタミン酸、396位にロイシンおよび270位にグルタミン酸(MGFc59/60);270位にグルタミン酸、316位にアスパラギン酸および416位にグリシン(MgFc71);243位にロイシン、292位にプロリン、305位にイソロイシンおよび396位にロイシン(MGFc74/P396L);または243位にロイシン、270位にグルタミン酸、392位にアスパラギンおよび396位にロイシン;または243位にロイシン、255位にロイシン、270位にグルタミン酸および396位にロイシン;または297位にグルタミン酸を有する。
好ましい実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する変異型重鎖を含む分子を包含し、前記1つまたは複数のアミノ酸改変は、変異型重鎖、特にそのFc領域とFcリガンドの間の界面で改変を含まない、または単に含まない。Fcリガンドには、それだけに限らないが、FcγR、C1q、FcRn、C3、マンノース受容体、プロテインA、プロテインG、マンノース受容体および免疫グロブリン重鎖および、特にFc領域に結合する未発見の分子が含まれる。Fc領域とFcリガンドの間の界面にあるアミノ酸は、Fc領域または重鎖とリガンドの間で直接的および/または間接的に接触し、界面の立体構造を決定する上で構造的役割を果たし、またはエックス線結晶解析および分子モデリングなど構造解析によって決定すると、互いに少なくとも3オングストローム、好ましくは少なくとも2オングストローム以内にあるこれらのアミノ酸として定義される。Fc領域とFcリガンドの間の界面にあるアミノ酸には、Sondermannら(2000, Nature, 406: 267-273;その全体が参照により本明細書に組み込まれている)で開示されるものなど、Fc-FcγR相互作用の結晶および構造解析に基づき、FcγRと直接的に接触するこれらのアミノ酸が含まれる。FcγRと直接的に接触するFc領域内の位置の例は、アミノ酸234〜239(ヒンジ領域)、アミノ酸265〜269(B/Cループ)、アミノ酸297〜299(C'/Eループ)およびアミノ酸327〜332(F/G)ループである。いくつかの実施形態では、構造および結晶解析に基づき、変異型Fc領域を含む本発明の分子は、FcγRと直接的に接触しない、例えば、Fc-FcγR結合部位内にない少なくとも1つの残基の改変を含む。
好ましくは、本発明に包含される1つまたは複数のアミノ酸改変は、ヒンジ領域、例えばLeu234〜Pro238;Ala327、Pro329の近傍にあるFc領域のIgG1 CH2ドメイン内のアミノ酸に相当し、すべてのヒトFcγRに対するFc領域の結合に影響を及ぼす、Shieldsらによって同定される任意のアミノ酸を単に改変しない。
他の実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する重鎖変異体を包含し、重鎖変異体が、変異型重鎖のFc領域とFcリガンドの間の界面の位置にあるアミノ酸改変を有さない、または単に有さないように、この重鎖は、変更されたFcγR親和性および/または変更されたエフェクター機能を示す。好ましくは、Fc領域とFcリガンドの間の界面にある1つまたは複数の他のアミノ酸改変と組み合わせた本発明の重鎖変異体は、工学的に改変される特定の性質、例えば、変更されたFcγR親和性にさらなる影響を及ぼす。変異型重鎖のFc領域とFcリガンドの間の界面にあるアミノ酸を改変することは、当技術分野で知られている方法を使用して、例えば、Fc-リガンド複合体の構造解析に基づき行うことができる。例えば、限定されることはないが、結合界面に影響を及ぼす重鎖Fc内の位置のエネルギー的に好ましい置換を探ることにより、新たな界面立体構造を抽出する変異体を工学的に改変することができ、その一部がFcリガンドに対する結合を改善し得、その一部がFcリガンド結合を低下させ得、その一部が他の好ましい性質を有し得る。このような新たな界面立体構造は、例えば、界面を形成するFcリガンド残基との直接的相互作用、または側鎖または骨格立体構造の乱れなどの、アミノ酸改変によって引き起こされる間接的効果の結果であると思われる。
本発明は、Fc領域内にある297位の糖鎖の立体構造が変更された他の改変と組み合わせた本明細書で開示される任意のアミノ酸改変を含む重鎖変異体を含む分子を包含する。本発明は、所望の性質、例えば、FcγRに対する親和性の増大または低下をもたらすN297糖鎖における立体構造および組成の変化を包含する。このような改変はさらに、本発明の重鎖変異体の元のアミノ酸改変の表現型を増強することもできる。特定の作用機序によって縛られることを意図しないが、このような戦略は、糖鎖構造および立体構造がFc-FcγRおよびFc/Cl q結合に劇的に影響を及ぼすという知見によって裏付けられる(Umaha et aL, 1999, Nat Biotechnol 17:176-180、Davies et aL, 2001, Biotechnol Bioeng 74:288-294、Mimura et aL, 2001, J Biol Chem 276:45539、Radaev et aL, 2001, J Biol Chem 276:16478-16483、Shields et aL 2002, J Biol Chem 277:26733-26740、Shinkawa et aL, 2003, J Biol Chem 278:3466-3473)。
ある実施形態では、本発明は、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する変異型重鎖を含む分子を包含し、前記1つまたは複数の改変は、前記変異型重鎖のFc領域のグリコシル化への構造的かつ機能的依存性を解消する。この戦略は、N297糖鎖なしでの重鎖および/またはFcの構造、安定性、溶解性および機能(例えば、1つまたは複数のFcリガンドに対する変異型重鎖のFcの親和性)の最適化を含む。ある手法では、グリコシル化なしで溶媒に曝される位置は、それが安定であり、野生型Fc構造と構造的に一致し、凝集する傾向を有さないように改変される。Fc領域内でグリコシル化されていない、本発明に従って工学的に改変された重鎖を最適化するための手法は、それだけに限らないが、Cg2-Cg2二量体軸に対して内側に向く極性および/または荷電残基を組み込むことにより、およびグリコシル化されていないFc-FcγR界面またはグリコシル化されていないFcと一部の他のFcリガンドとの界面を直接的に増強するアミノ酸改変を設計することにより、グリコシル化されていないFc領域安定性および/または溶解性を増強するアミノ酸改変を設計することを含み得る。
本発明の重鎖変異体は、それだけに限らないが、エフェクター機能を変更する改変を含めた他の重鎖改変と組み合わせてもよい。本発明は、本発明の重鎖変異体を他の重鎖改変と組み合わせて、抗体またはFc融合物における相加的、相乗的、または新規の性質を提供することを包含する。このような改変は、CH1ドメイン、CH2ドメイン、ヒンジドメインもしくはCH3ドメインまたはその組合せ内であってもよい。好ましくは、本発明の重鎖変異体は、それと組み合わせる改変の性質を増強する。例えば、本発明の重鎖変異体を、同一のアイソタイプのFc領域を有する野生型Fc領域を含む比較可能な分子よりも高い親和性でFcγRIIIAに結合すること分かっている突然変異体と組み合わせた場合、本発明の突然変異体との組合せにより、FcγRIIIA親和性の増強の増大をもたらす。
一実施形態では、本発明の重鎖変異体、例えば、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変(例えば、置換)を含む重鎖を、そのそれぞれの全体が参照により本明細書に組み込まれているDuncan et al, 1988, Nature 332:563-564、Lund et al., 1991, J. Immunol 147:2657-2662、Lund et al, 1992, Mol Immunol 29:53-59、Alegre et al, 1994, Transplantation 57:1537-1543、Hutchins et al. , 1995, Proc Natl. Acad Sci U S A 92:11980-11984、Jefferis et al, 1995, Immunol Lett. 44:111-117、Lund et al., 1995, Faseb J 9:115-119、Jefferis et al, 1996, Immunol Lett 54:101-104、Lund et al, 1996, J Immunol 157:49634969、Armour et aL, 1999, Eur J Immunol 29:2613-2624、Idusogie et al, 2000, J Immunol 164:41784184、Reddy et al, 2000, J Immunol 164:1925-1933、Xu et al., 2000, Cell Immunol 200:16-26、Idusogie et al, 2001, J Immunol 166:2571-2575、Shields et al., 2001, J Biol Chem 276:6591-6604、Jefferis et al, 2002, Immunol Lett 82:57-65、Presta et al., 2002, Biochem Soc Trans 30:487-490)、US5,624,821、US5,885,573、US6,194,551、PCTWO00/42072、PCTWO99/58572に開示されるものなど、他の既知の重鎖変異体と組み合わせることもできる
。
6.1.1 ポリペプチドおよび抗体コンジュゲート
変異型重鎖を含む本発明の分子(すなわち、ポリペプチド、抗体)は、融合タンパク質を作製するために、異種ポリペプチド(すなわち、無関係なポリペプチド、またはその部分、好ましくは前記ポリペプチドの少なくとも10、少なくとも20、少なくとも30、少なくとも40、少なくとも50、少なくとも60、少なくとも70、少なくとも80、少なくとも90、または少なくとも100アミノ酸)に組換えで融合させても、または化学的にコンジュゲートさせ(共有結合的および非共有結合的コンジュゲーションの両方を含む)てもよい。前記融合は必ずしも直接的である必要はなく、リンカー配列を介して起きてもよい。
さらに、変異型重鎖を含む本発明の分子(すなわち、ポリペプチド、抗体)は、所与の生物学的応答を改変する治療薬または薬物成分にコンジュゲートしてもよい。治療薬または薬物成分は、古典的な化学的治療薬に制限されていると解釈すべきではない。例えば、前記薬物成分は、所望の生物活性を有するタンパク質でもポリペプチドでもよい。そのようなタンパク質は、例えば、アブリン、リシンA、シュードモナス外毒素(すなわち、PE-40)、もしくはジフテリア毒素、リシン、ゲロニン、およびヨウシュヤマゴボウ抗ウイルスタンパク質などの毒素、腫瘍壊死因子、αインターフェロン(IFN-α)、βインターフェロン(IFN-β)を含むがこれに限定されることはないインターフェロン、神経成長因子(NGF)、血小板由来成長因子(PDGF)、組織プラスミノーゲン活性化因子(TPA)、アポトーシス剤(例えば、PCT国際公開国際公開第97/33899号で開示されたTNF-α、TNF-β、AIM I)、AIM II(PCT国際公開国際公開第97/34911号参照)、Fasリガンド(Takahashi et al., J. Immunol.、6:1567-1574, 1994)、およびVEGI (PCT国際公開国際公開第99/23105号)などのタンパク質、血栓症薬もしくは抗血管新生薬(例えば、アンジオスタチンもしくはエンドスタチン)、または、例えば、リンホカイン(例えば、インターロイキン1(「IL-1」)、インターロイキン2(「IL-2」)、インターロイキン6(「IL-6」))、顆粒球マクロファージコロニー刺激因子(「GM-CSF」)、顆粒球コロニー刺激因子(「G-CSF」)、マクロファージコロニー刺激因子(「M-CSF」)、もしくは成長因子(例えば、成長ホルモン(「GH」))、プロテアーゼ、もしくはリボヌクレアーゼなどの生物学的応答調節物質がある。
本発明の分子(すなわち、ポリペプチド、抗体)は、精製を促進するためのペプチドなどのマーカー配列に融合させることができる。好ましい実施形態では、前記マーカーアミノ酸配列は、数ある中でもpQEベクター(QIAGEN, Inc.、9259 Eton Avenue、Chatsworth、CA、91311)に提供されているタグなどのヘキサヒスチジンペプチドであり、その多くが市販されている。例えば、Gentz et al., 1989, Proc. Natl. Acad. Sci. USA, 86:821-824に記載されているように、ヘキサヒスチジンは、融合タンパク質の便利な精製法を提供する。精製に有用な他のペプチドタグには、インフルエンザ赤血球凝集素タンパク質由来のエピトープに対応する赤血球凝集素「HA」タグ(Wilson et al., Cell、37:767 1984)、および「flag」タグ(Knappik et al., Biotechniques、17(4):754-761、1994)があるが、これらのタグに限定されるものではない。
追加の融合タンパク質は、遺伝子シャフリング、モチーフシャフリング、エキソンシャフリング、および/またはコドンシャフリング(合わせて「DNAシャフリング」と呼ぶ)の技術によって作製してもよい。DNAシャフリングを用いて、本発明の分子の活性を改変してもよい(例えば、より高い親和性とより低い解離速度を有する抗体)。一般に米国特許第5,605,793号、米国特許第5,811,238号、米国特許第5,830,721号、米国特許第5,834,252号、および米国特許第5,837,458号、ならびにPatten et al., 1997, Curr. Opinion Biotechnol. 8:724-33, Harayama, 1998、Trends Biotechnol. 16:76, Hansson、et al., 1999、J. Mol. Biol. 287:265、およびLorenzo and Blasco, 1998, BioTechniques 24:308を参照されたい(これらの特許文献および出版物はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする)。変異型Fc領域を含む本発明の分子、または本発明の分子をコードしている核酸は、変異性PCRによるランダム突然変異誘発、ランダムヌクレオチド挿入、または組換えに先立つ他の方法にかけることによりさらに改変してもよい。本発明の分子をコードしているポリヌクレオチドの1つまたは複数の部分は、1つまたは複数の異種分子の1つまたは複数の成分、モチーフ、セクション、部分、ドメイン、断片などと組み合わせてもよい。
本発明は、血清中半減時間を延ばすことを望まれている診断もしくは治療薬またはその他のあらゆる分子にコンジュゲートされ、かつ/または細胞の特定のサブセットに標的される、変異型重鎖を含む本発明の分子(すなわち、抗体、ポリペプチド)を包含する。本発明の分子を診断的に使って、例えば、臨床試験法の一部として、例えば、所与の治療計画の有効性を決定するために、疾患、障害、もしくは感染の発症または進行を監視することができる。本発明の分子と検出可能な物質を結合させることにより検出を促進することができる。検出可能な物質の例には、種々の酵素、補欠分子族、蛍光物質、発光物質、生物発光物質、放射性物質、陽電子放出物質、および非放射性常磁性金属イオンがある。前記検出可能な物質は、本発明の分子に直接結合させるもしくはコンジュゲートさせてもよいし、または当技術分野で公知の技術を使って媒介物(例えば、当技術分野で公知のリンカー)により間接的に結合させるもしくはコンジュゲートさせてもよい。例えば、本発明に従って診断薬として使用するため抗体にコンジュゲートすることができる金属イオンは、米国特許第4,741,900号を参照されたい。そのような診断および検出は、種々の酵素、西洋わさびペルオキシダーゼ、アルカリホスファターゼ、βガラクトシダーゼ、またはアセチルコリンエステラーゼを含むがこれらの酵素に限定されるものではない酵素; ストレプトアビジン/ビオチン、およびアビジン/ビオチンなどの、しかしこれらの物質に限定されることはない補欠分子族複合体; ウンベリフェロン、フルオレセイン、フルオレセインイソチオシアン酸、ローダミン、ジクロロトリアジニルアミンフルオレセイン、ダンシル塩化物、またはフィコエリトリンなどの、しかしこれらの物質に限定されるものではない蛍光物質; ルミノールなどのしかしこれに限定されるものではない発光物質; ルシフェラーゼ、ルシフェリン、およびエクオリンなどのしかしこれらの物質に限定されるものではない生物発光物質; ビスマス(213Bi)、炭素(14C)、クロム(51Cr)、コバルト(57Co)、フッ素(18F)、ガドリウム(153Gd、159Gd)、ガリウム(68Ga、67Ga)、ゲルマニウム(68Ge)、ホルミウム(166Ho)、インジウム(115In、113In、112In、111In)、ヨウ素(131I、125I、123I、121I)、ランタン(140La)、ルテチウム(177Lu)、マンガン(54Mn)、モリブデン(99Mo)、パラジウム(103Pd)、リン(32P)、プラセオジム(142Pr)、プロメチウム(149Pm)、レニウム(186Re、188Re)、ロジウム(105Rh)、ルテニウム(97Ru)、サマリウム(153Sm)、スカンジウム(47Sc)、セレン(75Se)、ストロンチウム(85Sr)、硫黄(35S)、テクネチウム(99Tc)、タリウム(201Ti)、スズ(113Sn、117Sn)、トリチウム(3H)、キセノン(133Xe)、イッテルビウム(169Yb、175Yb)、イットリウム(90Y)、亜鉛(65Zn)などの、しかしこれらの物質に限定されるものではない放射性物質; 種々の陽電子放出断層撮影を使った陽電子放出物質、および非放射性常磁性金属イオンを含む検出可能な物質に、本発明の分子を結合させることにより実現することができる。
変異型重鎖を含む本発明の分子(すなわち、抗体、ポリペプチド)は、細胞毒などの治療成分(例えば、細胞分裂阻害剤もしくは細胞破壊剤)、治療薬、または放射性元素(例えば、α放射体、γ放射体など)にコンジュゲートしてもよい。細胞毒または細胞傷害薬物には、細胞に有害なあらゆる薬剤がある。例には、パクリタキセル、サイトカラシンB、グラミシジンD、臭化エチジウム、エメチン、マイトマイシン、エトポシド、テノポシド、ビンクリスチン、ビンブラスチン、コルヒチン、ドキソルビシン、ダウノルビシン、ジヒドロキシアントラシンジオン、ミトキサントロン、ミトラマイシン、アクチノマイシンD、1-デヒドロテストステロン、グルココルチコイド、プロカイン、テトラカイン、リドカイン、プロプラノロール、ピューロマイシン、およびその類似体または相同体がある。治療薬には、代謝拮抗薬(例えば、メトトレキサート、6-メルカプトプリン、6-チオグアニン、シタラビン、5-フルオロウラシルダカルバジン)、アルキル化薬(例えば、メクロレタミン、チオエパクロラムブシル、メルファラン、カルムスチン(BSNU)、およびロムスチン(CCNU)、シクロトスファミド、ブスルファン、ジブロモマンニトール、ストレプトゾトシン、マイトマイシンC、およびシスジクロロジアミン白金(II)(DDP)シスプラチン))、アントラサイクリン(例えば、ダウノルビシン(以前はダウノマイシン)、およびドキソルビシン)、抗生物質(例えば、ダクチノマイシン(以前はアクチノマイシン)、ブレオマイシン、ミトラマイシン、およびアントラマイシン(AMC))、ならびに有糸分裂阻害剤(例えば、ビンクリスチン、およびビンブラスチン)があるが、これらの物質に限定されるものではない。
さらに、本発明の分子は、放射性物質などの治療成分または放射性金属イオンのコンジュゲートに有用な大環状キレート剤にコンジュゲートすることができる(放射性物質の上記の例を参照されたい)。ある実施形態では、大環状キレート剤は、リンカー分子を介して抗体に結合させることができる1,4,7,10-テトラアザ環式ドデカン-N,N',N'',N'''-四酢酸(DOTA)である。そのようなリンカー分子は当技術分野では公知であり、Denardo et al., 1998, Clin Cancer Res. 4:2483-90; Peterson et al., 1999, Bioconjug. Chem. 10:553; およびZimmerman et al., 1999, Nucl. Med. Biol. 26:943-50に記載されている。これらの文献はそれぞれが、参照によりその全体が本明細書に組み込まれているものとする。
そのような治療成分を抗体にコンジュゲートするための技術は公知である。Arnon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), 1985, pp. 243-56, Alan R. Liss, Inc.; Hellstrom et al., "Antibodies For Drug Delivery", Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), 1987, pp. 623-53, Marcel Dekker, Inc.; Thorpe、"Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", Monoclonal Antibodies '84: Biological And Clinical Applications, Pinchera et al. (eds.), 1985, pp. 475-506); "Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), 1985, pp. 303-16, Academic Press; およびThorpe et al., Immunol. Rev., 62:119-58, 1982を参照されたい。
本発明の分子が、変異型重鎖を含む抗体である1つの実施形態では、前記分子は、治療上の処置として使用するために、治療成分をその分子にコンジュゲートして、または治療成分をコンジュゲートせずに投与する、単独で投与する、または細胞傷害因子(群)および/またはサイトカイン(群)と組み合わせて投与することができる。代案として、本発明の抗体は、米国特許第4,676,980号でSegalにより記載されているように、第2の抗体にコンジュゲートさせ、抗体異種コンジュゲートを形成することができる。この特許文献は、参照によりその全体が本明細書に組み込まれているものとする。本発明の抗体は、標的抗原の免疫アッセイまたは精製に特に有用な固形支持体に結合させてもよい。そのような固形支持体には、ガラス、セルロース、ポリアクリルアミド、ナイロン、ポリスチレン、ポリ塩化ビニルまたはポリプロピレンがあるが、これらに限定されるものではない。
6.2 増強されたFcγRIII結合についての変異型重鎖を有する分子のスクリーニングおよびその特徴付け
FcγRに対する本発明の分子の親和性および結合特性はまず、それだけに限らないが、ELISAアッセイ、表面プラズモン共鳴アッセイ、免疫沈殿アッセイを含めた、重鎖-抗体受容体相互作用、特にFc-FcγR相互作用、すなわちFcγRに対するFc領域の特異的結合を決定するための、当技術分野で知られているin vitroアッセイ(生化学または免疫学に基づいたアッセイ)を使用して決定される。好ましくは、本発明の分子の結合特性は、1つまたは複数のFcγRメディエーターエフェクター細胞機能を決定するためのin vitro機能的アッセイによっても特徴付けられる。最も好ましい実施形態では、本発明の抗体は、in vitroベースのアッセイと類似のin vivoモデル(本明細書に記載および開示したものなど)における結合特性を有する。しかし、本発明は、in vitroベースのアッセイにおいて所望の表現型を示さないが、in vivoで所望の表現型を示す本発明の分子を除外しない。
いくつかの実施形態では、改変されたFcγR親和性(例えば、増強されたFcγRIIIA親和性)を有する変異型重鎖を含む分子のスクリーニングおよび同定は、好ましくは高処理能の形で、機能に基づくアッセイにおいて行われる。機能に基づくアッセイは、本明細書の第5.3節に記載のものなどの1つまたは複数のFcγR媒介性エフェクター細胞機能の特徴付けについて当技術分野で知られている任意のアッセイでよい。本発明の方法に従って使用することができるエフェクター細胞機能の非限定的な例には、それだけに限らないが、抗体依存性細胞媒介性細胞傷害(ADCC)、抗体依存性食作用、食作用、オプソニン化、オプソニン食作用、細胞結合、ロゼット形成、C1q結合、および補体依存性細胞媒介性細胞傷害がある。
Fc領域とFcγRの「特異的結合」という用語は、例えばELISAまたは表面プラズモン共鳴アッセイ(例えば、BIAcore(商標))を使用して決定される、単量体FcγRIIIAの場合で少なくとも約150nM、二量体FcγRIIBの場合で少なくとも約60nMの親和定数を有するFc領域と特定のFcγRの相互作用を指す。単量体FcγRIIIAについてのFc領域の親和定数は、150nM、200nMまたは300nMでよい。二量体FcγRIIBについてのFc領域の親和定数は、60nM、80nM、90nM、または100nMでよい。本発明の方法で使用する二量体FcγRIIBは、当業者に知られている方法を使用して生成することができる。通常、FcγRIIBの細胞外領域は、二量体化が可能である異種ポリペプチドと共有結合し、その結果、得られる融合タンパク質が二量体となる(例えば、参照によりその全体が本明細書に組み込まれている、2003年1月13日に出願された米国出願第60/439,709号(代理人整理番号11183-005-888)を参照されたい)。特異的相互作用は一般に、例えば、ヒトまたは他の脊椎動物あるいは無脊椎動物などの生存している個体中で起こる条件、ならびに哺乳動物細胞あるいは他の脊椎動物または無脊椎動物由来の細胞の維持および培養に使用する条件などの細胞培養中で起こる条件を含めた生理的条件下で安定である。
特定の実施形態では、変異型重鎖を含む本発明の分子とFcγR(1つまたは複数)の結合を特徴付けることは、Fc-FcγR相互作用を決定する生化学的アッセイ、好ましくはELISAに基づくアッセイを使用して実施される。1つまたは複数のFcγRとの相互作用について変異型重鎖を含む分子を特徴付け、少なくとも1つの生化学に基づくアッセイ、例えばELISAアッセイによってそれが1つまたは複数のFcγRについて変化した親和性を有することを決定した後、当技術分野で知られている標準的な組換えDNA技術の方法を使用してその分子を工学的に改変して完全な免疫グロブリンにし、さらなる生化学的特徴付けのために哺乳動物細胞中で変異型重鎖を含む免疫グロブリンを発現させることができる。(例えば免疫グロブリンのFc領域を置換して)その中に本発明の変異型重鎖を導入した免疫グロブリンは、それだけに限らないが、ポリクローナル抗体、モノクローナル抗体、二重特異性抗体、多重特異性抗体、ヒト化抗体、およびキメラ抗体を含めた任意の免疫グロブリンでよい。好ましい実施形態では、変異型重鎖を、細胞表面受容体、腫瘍抗原、または癌抗原に特異的な免疫グロブリン中に導入する。その中に本発明の変異型重鎖を導入した免疫グロブリンは、例えば、それだけに限らないが、KS1/4汎癌腫抗原(Perez and Walker, 1990, J. Immunol. 142: 3662-3667; Bumal, 1988, Hybridoma 7(4): 407-415)、卵巣癌抗原(CA125)(Yu et al., 1991, Cancer Res. 51(2): 468-475)、前立腺酸性リン酸塩(Tailor et al., 1990, Nucl. Acids Res. 18(16): 4928)、前立腺特異抗原(Henttu and Vihko, 1989, Biochem. Biophys. Res. Comm. 160(2): 903-910; Israeli et al., 1993, Cancer Res. 53: 227-230)、黒色腫関連抗原p97(Estin et al., 1989, J. Natl. Cancer Instit. 81(6): 445-446)、黒色腫抗原gp75(Vijayasardahl et al., 1990, J. Exp. Med. 171(4): 1375-1380)、高分子量黒色腫抗原(HMW-MAA)(Natali et al., 1987, Cancer 59: 55-63; Mittelman et al., 1990, J. Clin. Invest. 86: 2136-2144)、前立腺特異的膜抗原、癌胎児性抗原(CEA)(Foon et al., 1994, Proc. Am. Soc. Clin. Oncol. 13: 294)、多型上皮ムチン抗原、ヒト乳脂肪球抗原、CEA、TAG-72(Yokata et al., 1992, Cancer Res. 52: 3402-3408)、CO17-1A(Ragnhammar et al., 1993, Int. J. Cancer 53: 751-758)などの結腸直腸腫瘍関連抗原; GICA 19-9(Herlyn et al., 1982, J. Clin. Immunol. 2: 135)、CTA-1およびLEA、バーキットリンパ腫抗原38.13、CD19(Ghetie et al., 1994, Blood 83: 1329-1336)、ヒトBリンパ腫抗原CD20(Reff et al., 1994, Blood 83:435-445)、CD33(Sgouros et al., 1993, J. Nucl. Med. 34:422-430)、ガングリオシドGD2(Saleh et al., 1993, J. Immunol., 151, 3390-3398)、ガングリオシドGD3(Shitara et al., 1993, Cancer Immunol. Immunother. 36:373-380)、ガングリオシドGM2(Livingston et al., 1994, J. Clin. Oncol. 12: 1036-1044)、ガングリオシドGM3(Hoon et al., 1993, Cancer Res. 53: 5244-5250)などの黒色腫特異抗原、DNA腫瘍ウイルスのT抗原およびRNA腫瘍ウイルスのエンベロープ抗原を含めたウイルスによって誘導される腫瘍抗原などの細胞表面抗原の腫瘍特異的移植型(TSTA)、結腸のCEAなどの癌胎児性抗原α-フェトプロテイン、膀胱癌癌胎児性抗原(Hellstrom et al., 1985, Cancer. Res. 45:2210-2188)、ヒト肺癌抗原L6、L20などの分化抗原(Hellstrom et al., 1986, Cancer Res. 46: 3917-3923)、線維肉腫の抗原、ヒト白血病T細胞抗原Gp37(Bhattacharya-Chatterjee et al., 1988, J. of Immun. 141:1398-1403)、ネオ糖タンパク質、スフィンゴ脂質、EGFR(上皮成長因子受容体)などの乳癌抗原、HER2抗原(p185HER2)、多型上皮ムチン(PEM)(Hilkens et al., 1992, Trends in Bio. Chem. Sci. 17:359)、悪性ヒトリンパ球抗原APO-1(Bernhard et al., 1989, Science 245: 301-304)、胎児赤血球中に認められるI抗原、成体赤血球、着床前胚中に認められる初期内胚葉I抗原、胃腺癌中に認められるI(Ma)、乳房上皮中に認められるM18、M39、骨髄球中に認められるSSEA-1、結腸直腸癌中に認められるVEP8、VEP9、Myl、VIM-D5、D156-22、TRA-1-85(血液型H)、結腸腺癌中に認められるC14、肺腺癌中に認められるF3、胃癌中に認められるAH6、Yハプテン、胚性癌細胞中に認められるLey、TL5(血液型A)、A431細胞中に認められるEGF受容体、膵癌中に認められるE1シリーズ(血液型B)、胚性癌細胞中に認められるFC10.2、胃腺癌抗原、腺癌中に認められるCO-514(血液型Lea)、腺癌中に認められるNS-10、CO-43(血液型Leb)、A431細胞のEGF受容体中に認められるG49、結腸腺癌中に認められるMH2(血液型ALeb/Ley)、結腸癌中に認められる19.9、胃癌ムチン、骨髄球中に認められるT5A7、黒色腫中に認められるR24、4.2、GD3、D1.1、OFA-1、GM2、OFA-2、GD2、およびM1:22:25:8、ならびに4〜8細胞期胚中に認められるSSEA-3およびSSEA-4などの分化抗原(Feizi, 1985, Nature 314: 53-57)を含めた癌または腫瘍抗原に特異的に結合することができる。一実施形態では、抗原は、皮膚T細胞リンパ腫のT細胞受容体由来ペプチドである(Edelson, 1998, The Cancer Journal 4:62を参照されたい)。
いくつかの実施形態では、本発明の変異型重鎖を、抗フルオレセインモノクローナル抗体4-4-20 (参照によりその全体が本明細書に組み込まれている、Kranz et al., 1982 J. Biol. Chem. 257(12): 6987-6995)中に導入する。さらに他の実施形態では、本発明の変異型重鎖を、B細胞上のCD20細胞表面リン酸化タンパク質を認識するマウス-ヒトキメラ抗CD20モノクローナル抗体2H7 (参照によりその全体が本明細書に組み込まれている、Liu et al., 1987, Journal of Immunology, 139: 3521-6)中に導入する。さらに他の実施形態では、本発明の変異型重鎖を、Carter et al.により記載されている(参照によりその全体が本明細書に組み込まれている、1992, Proc. Natl. Acad. Sci. USA 89: 4285-9)ヒト上皮成長因子受容体2(p185 HER2)に対するヒト化抗体(Ab4D5)中に導入する。さらに他の実施形態では、本発明の変異型重鎖を、ヒト化抗TAG72抗体(CC49)(参照によりその全体が本明細書に組み込まれている、Sha et al., 1994 Cancer Biother. 9(4): 341-9)中に導入する。他の実施形態では、本発明の変異型重鎖を、リンパ腫の治療に使用するRituxan(ヒト化抗CD20抗体; リツキシマブ)(参照によりその全体が本明細書に組み込まれている、国際特許公開第02/096,948)中に導入する。
他の特定の実施形態では、本発明は、FcγRIIIAおよび/またはFcγRIIAについてFc領域の親和性を増大させる少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)による、それだけに限らないが、2002年8月12日に出願された米国仮出願第60/403,266号、2003年8月14日に出願された米国出願第10/643,857号、2004年4月16日に出願された米国仮出願第60/562,804号、2004年6月21日にそれぞれ出願された米国仮出願第60/582,044号、第60/582,045号、および第60/582,043号、2004年12月15日に出願された米国仮出願第60/636,663号、および2005年2月11日に出願された米国出願第10/524,134号で開示されている抗体のいずれかを含めた抗FcγRIIB抗体の工学的改変を包含する。他の特定の実施形態では、本発明は、FcγRIIIAおよび/またはFcγRIIAについてFc領域の親和性を増大させる少なくとも1つのアミノ酸残基の改変(例えば、置換、挿入、欠失)による、それだけに限らないが、2004年5月10日に出願された米国仮出願第60/569,882号および2005年5月10日に出願された米国出願第11/126,978号で開示されている抗体のいずれかを含めたヒト化抗FcγRIIB抗体の工学的改変を包含する。上記で述べた各出願は、参照によりその全体が本明細書に組み込まれている。本発明の方法に従って工学的に改変することができる、ヒト化してもよく、あるいはヒト化しなくてもよい抗FcγRIIB抗体の例は、ATCCアクセッション番号PTA-4591を有する2B6モノクローナル抗体およびATCCアクセッション番号PTA-4592を有する3H7、ATCCアクセッション番号PTA-5958を有する1D5モノクローナル抗体、ATCCアクセッション番号PTA-5959を有する1F2モノクローナル抗体、ATCCアクセッション番号PTA-5960を有する2D11モノクローナル抗体、ATCCアクセッション番号PTA-5961を有する2E1モノクローナル抗体およびATCCアクセッション番号PTA-5962を有する2H9モノクローナル抗体(すべて10801 University Boulevard, Manassas, VA 02209-2011に寄託)であり、これらは参照により本明細書に組み込まれている。他の特定の実施形態では、抗FcγRIIB抗体の改変はまた、FcγRIIBについてFc領域の親和性をさらに低下させることもできる。さらに他の実施形態では、工学的に改変された抗FcγRIIB抗体はさらに、当技術分野で知られ、本明細書で開示され例示されている標準的なアッセイによって決定される、増強されたエフェクター機能を有してもよい。いくつかの実施形態では、それだけに限らないが、Erbitux(商標)(IMC-C225としても知られる)(ImClone Systems Inc.)、EGFRに対するキメラモノクローナル抗体; 転移性乳癌患者治療用のヒト化抗HER2モノクローナル抗体であるHERCEPTIN(登録商標)(トラスツズマブ)(Genentech, CA); 血餅形成防止用の、血小板上の抗糖タンパク質IIb/IIIa受容体であるREOPRO(登録商標)(アブシキシマブ)(Centocor); 急性腎異種移植片拒絶防止用の免疫抑制性ヒト化CD25モノクローナル抗体であるZENAPAX(登録商標)(ダクリズマブ)(Roche Pharmaceuticals, Switzerland)を含めた癌抗原または細胞表面受容体に特異的な治療用モノクローナル抗体中にIgG2、IgG3またはIgG4のFc領域を有する本発明の変異型重鎖を導入する。他の例は、ヒト化抗CD18 F(ab')2(Genentech); ヒト化抗CD18 F(ab')2であるCDP860(Celltech, UK); CD4と融合した抗HIV gp120抗体であるPRO542(Progenics/Genzyme Transgenics); 抗CD14抗体であるC14(ICOS Pharm); ヒト化抗VEGF IgG1抗体(Genentech); マウス抗CA 125抗体であるOVAREX(商標)(Altarex); マウス抗17-IA細胞表面抗原IgG2a抗体であるPANOREX(商標)(Glaxo Wellcome/Centocor); キメラ抗EGFR IgG抗体であるIMC-C225(ImClone System); ヒト化αVβ3インテグリン抗体であるVITAXIN(商標)(Applied Molecular Evolution/MedImmune); ヒト化抗CD52 IgG1抗体であるCampath 1H/LDP-03(Leukosite); ヒト化抗CD33 IgG抗体であるSmart M195(Protein Design Lab/Kanebo); キメラ抗CD20 IgG1抗体であるRITUXAN(商標)(リツキシマブ)(IDEC Pharm/Genentech, Roche/Zettyaku); ヒト化抗CD22 IgG抗体であるLYMPHOCIDE(商標)(Immunomedics); ヒト化抗HLA抗体であるSmart ID10(Protein Design Lab); 放射標識マウス抗HLA DR抗体であるONCOLYM(商標)(Lym-1)(Techniclone); ヒト化IgG1抗体である抗CD11a(Genentech/Xoma); ヒト化抗ICAM3抗体であるICM3(ICOS Pharm); 霊長類化抗CD80抗体であるIDEC-114(IDEC Pharm/Mitsubishi); 放射標識マウス抗CD20抗体であるZEVALIN(商標)(IDEC/Schering AG); ヒト化抗CD40L抗体であるIDEC-131(IDEC/Eisai); 霊長類化抗CD4抗体であるIDEC-151(IDEC); 霊長類化抗CD23抗体であるIDEC-152(IDEC/Seikagaku); ヒト化抗CD3 IgGであるSMART抗CD3(Protein Design Lab); ヒト化抗補体因子5(C5)抗体である5G1.1(Alexion Pharm); 霊長類化抗CD4 IgG1抗体であるIDEC-151(IDEC Pharm/SmithKline Beecham); ヒト抗CD4 IgG抗体であるMDX-CD4(Medarex/Eisai/Genmab); ヒト化抗TNF-α IgG4抗体であるCDP571(Celltech); ヒト化抗α4β7抗体であるLDP-02(LeukoSite/Genentech); ヒト化抗CD4 IgG抗体であるOrthoClone OKT4A(Ortho Biotech); ヒト化抗CD40L IgG抗体であるANTOVA(商標)(Biogen); ヒト化抗VLA-4 IgG抗体であるANTEGREN(商標)(Elan); ヒト抗CD64(FcγR)抗体であるMDX-33(Medarex/Centeon);; ヒト化抗IgE IgG1抗体であるrhuMab-E25(Genentech/Norvartis/Tanox Biosystems); 霊長類化抗CD23抗体であるIDEC-152(IDEC Pharm); マウス抗CD-147 IgM抗体であるABX-CBL(Abgenix); ラット抗CD2 IgG抗体であるBTI-322(Medimmune/Bio Transplant); マウス抗CD3 IgG2a抗体であるOrthoclone/OKT3(Ortho Biotech); キメラ抗CD25 IgG1抗体であるSIMULECT(商標)(Novartis Pharm); ヒト化抗β2-インテグリンIgG抗体であるLDP-01(LeukoSite); マウス抗CD18F(ab')2であるAnti-LFA-1(Pasteur-Merieux/Immunotech); ヒト抗TGF-β2抗体であるCAT-152(Cambridge Ab Tech); およびキメラ抗第VII因子抗体であるCorsevin M(Centocor)である。
好ましくは免疫グロブリンとの関連で、本発明の変異型重鎖は、好ましくは高処理能の形で1つまたは複数の生化学アッセイおよび/あるいは1つまたは複数の機能アッセイを使用してさらに特徴付けることができる。いくつかの代替の実施形態では、本発明の変異型重鎖を免疫グロブリン中に導入せず、好ましくは高処理能の形で1つまたは複数の生化学に基づくアッセイおよび/あるいは1つまたは複数の機能アッセイを使用してそれをさらに特徴付ける。1つまたは複数の生化学アッセイは、Fc-FcγRまたは免疫グロブリン-抗原相互作用の動力学的パラメーターを決定するための、それだけには限定されないが、ELISAアッセイおよび表面プラズモン共鳴ベースのアッセイ、例えば、BIAcoreアッセイを含めた、免疫グロブリン-抗原、重鎖-抗体受容体またはFc-FcγR相互作用を同定するための、当技術分野で知られている任意のアッセイであってよい。標的抗原結合親和性の特徴付けまたは細胞表面に対する標的抗原密度の評価は、Scatchard分析などの当技術分野で周知の方法により、またはQuantum(商標)Simply Cellular(登録商標)(Bangs Laboratories, Inc., Fishers, IN)などの製造元の説明書の通りキットを使用することにより評価することもできる。1つまたは複数の機能アッセイは、当業者に知られまたは本明細書に記載した、1つまたは複数のFcγR媒介性エフェクター細胞機能を特徴付けるための、当技術分野で知られている任意のアッセイでよい。特定の実施形態では、変異型Fc領域を含む免疫グロブリンを、ELISAアッセイで、1つまたは複数のFcγR、例えば、FcγRIIIA、FcγRIIA、FcγRIIAとの結合についてアッセイし、その後1つまたは複数のADCCアッセイを行う。いくつかの実施形態では、変異型Fc領域を含む免疫グロブリンを、表面プラズモン共鳴に基づくアッセイ、例えば、BIAcoreを使用してさらにアッセイする。表面プラズモン共鳴に基づくアッセイは当技術分野で周知であり、第5.2節でさらに論じ、本明細書の、例えば、実施例6.1で例示する。
変異型重鎖を含む免疫グロブリンを特徴付ける例示的な高処理能アッセイは、例えば標準的な組換えDNA技術の方法によって、4-4-20抗体中に本発明の変異型重鎖を導入することと、変異型重鎖を含む4-4-20抗体とFcγR(例えば、FcγRIIIA、FcγRIIB)の特異的結合を特徴付けることと、(本明細書で開示されている方法を使用して)ADCCアッセイで変異型重鎖を含む4-4-20抗体を特徴付けることとを含んでよく、変異型重鎖を含む4-4-20抗体で標的細胞をオプソニン化し、次いで変異型重鎖を、ADCCアッセイで特徴付けられた第2の免疫グロブリン、例えば4D5、2H7中にクローン化することができ、変異型重鎖を含む第2の免疫グロブリンで標的細胞をオプソニン化する。次いで、ELISAに基づくアッセイを使用して変異型重鎖を含む第2の抗体をさらに分析して、FcγRとの特異的結合を確認する。
好ましくは、本発明の変異型重鎖は、ELISAアッセイで決定される、同一のアイソタイプのFc領域を有する野生型重鎖より高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合する。最も好ましくは、本発明の変異型重鎖は、ELISAアッセイで決定される、同一のアイソタイプのFc領域を有する野生型重鎖より高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合し、低い親和性でFcγRIIBに結合する。いくつかの実施形態では、変異型重鎖は、ELISAアッセイで決定される、同一のアイソタイプのFc領域を有する野生型重鎖がFcγRIIIAおよび/またはFcγRIIAに結合するより少なくとも2倍高い、少なくとも4倍高い、より好ましくは少なくとも6倍高い、最も好ましくは少なくとも8〜10倍高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合し、同一のアイソタイプのFc領域を有する野生型重鎖がFcγRIIBと結合する2分の1以下、4分の1以下、より好ましくは6分の1以下、最も好ましくは8〜10分の1以下の親和性でFcγRIIBと結合する。
本明細書で開示され、当業者に知られている方法を使用して、Fc-FcγR相互作用の動態パラメーターを決定する表面プラズモン共鳴に基づくアッセイ、例えば、BIAcoreを使用して任意の時点で本発明の変異型重鎖を含む免疫グロブリンを分析することができる。好ましくは、BIAcore分析によって決定される、単量体FcγRIIIAおよび/またはFcγRIIAとの結合についての本発明の分子のKdは約100nM、好ましくは約70nM、最も好ましくは約40nMであり、二量体FcγRIIBの結合についての本発明の分子のKdは約80nM、約100nM、より好ましくは約200nMである。
最も好ましい実施形態では、本発明の変異型重鎖(すなわち、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を有する野生型鎖と比べて少なくとも1つのアミノ酸改変を有する重鎖)を含む免疫グロブリンはさらに、動物モデルにおいてFcγRとの相互作用について特徴付けられる。本発明の方法での使用に好ましい動物モデルは、例えば、ヒトFcγRを発現するトランスジェニックマウス、例えば参照によりその全体が本明細書に組み込まれている米国特許第5,877,397号、および第6,676,927号に記載の任意のマウスモデルである。本発明の方法で使用するトランスジェニックマウスには、それだけに限らないが、ヒトFcγRIIIAを担持するヌードノックアウトFcγRIIIAマウス; ヒトFcγRIIAを担持するヌードノックアウトFcγRIIIAマウス; ヒトFcγRIIBおよびヒトFcγRIIIAを担持するヌードノックアウトFcγRIIIAマウス; ヒトFcγRIIBおよびヒトFcγRIIAを担持するヌードノックアウトFcγRIIIAマウス; ヒトFcγRIIIAおよびFcγRIIAを担持するヌードノックアウトFcγRIIIAおよびFcγRIIAマウス、ならびにヒトFcγRIIIA、FcγRIIAおよびFcγRIIBを担持するヌードノックアウトFcγRIIIA、FcγRIIAおよびFcγRIIBマウスがある。
6.2.1 FcγR-Fc結合アッセイ
本発明の分子とFcγRの結合を決定するためにFcγR-Fc結合アッセイを開発し、それによって、そのリガンドについての受容体の親和性が本質的に弱く、例えばFcγRIIBおよびFcγRIIIAについてはμM程度であるにもかかわらず、相互作用の検出および定量が可能となった。この方法は、国際公開第04/063351号ならびに米国特許出願公開第2005/0037000号および第2005/0064514号に詳細に記載されている。簡潔に述べると、この方法は、複合体化されていないFcγRと比べて変異型重鎖のFc領域の結合活性が改善されたFcγR複合体の形成を含む。本発明によれば、好ましい分子複合体は、(a)FcγRの可溶性領域(例えば、FcγRIIIA、FcγRIIAまたはFcγRIIBの可溶性領域); (b)FcγRの可溶性領域(例えば、FcγRIIIA、FcγRIIAまたはFcγRIIBの可溶性領域)のC末端に作動可能に連結したビオチン化15アミノ酸AVITAG配列(AVITAG); および(c)ストレプトアビジン-フィコエリスリン(SA-PE)を、四量体FcγR複合体を形成するモル比で(好ましくは5:1のモル比で)含む四量体免疫複合体である。本発明の好ましい実施形態によれば、例えば、15アミノ酸AVITAG配列中のリシン残基を特異的にビオチン化する大腸菌Bir A酵素というビオチンリガーゼを使用して融合タンパク質を酵素によりビオチン化する。本発明の特定の実施形態では、融合タンパク質の85%をビオチン化し、それは、ストレプトアビジンシフトアッセイを含むがそれだけに限らない、当業者に知られている標準的な方法によって決定される。本発明の好ましい実施形態によれば、ビオチン化可溶性FcγRタンパク質をSA-PEと1× SA-PE:5×ビオチン化可溶性FcγRのモル比で混合して四量体FcγR複合体を形成する。
本発明の好ましい実施形態では、Fc領域を含むポリペプチドは、単量体の非複合体化FcγRより少なくとも8倍高い親和性で、四量体FcγR複合体に結合する。Fc領域を含むポリペプチドと四量体FcγR複合体の結合は、例えば蛍光活性化細胞スクリーニング(FACS)、ラジオイムノアッセイ、ELISAアッセイなど、当業者に知られている標準的な技術を使用して決定することができる。
本発明は、細胞に基づくアッセイまたは無細胞アッセイでFc領域を含む分子の機能を決定するための、本発明の分子を含み、上記に記載の方法に従って形成された免疫複合体の使用を包含する。
便宜上、アッセイキット、すなわち、Fc領域を含む分子がFcγR四量体複合体に結合できるかどうかアッセイを行うための包装された組合せの試薬として試薬を提供することができる。Fc-FcγR相互作用を決定する際に使用する他の形態の分子複合体、例えば、参照によりその全体が本明細書に組み込まれている2003年1月13日に出願された米国仮出願第60/439,709号に記載のように形成された融合タンパク質も、本発明の方法での使用に企図される。
6.2.2 酵母ディスプレイライブラリーの使用
IgG重鎖のFc領域とFc受容体の分子相互作用は、構造的な技術と遺伝的な技術の両方によって以前から研究されている。これらの研究から、異なるFcγRとFcの機能的結合に決定的に重要なアミノ酸残基が同定された。これらの変化のうち、動物モデルにおいて治療用抗体のヒトFcγR媒介性効果を高めることが示されているものはない。これらの残基または他の潜在的に重要な残基での潜在的なアミノ酸変化すべての完全な分析は報告されていない。
本発明は、本発明の同時出願であり、そのそれぞれの全体が参照により本明細書に組み込まれている、国際公開第04/063351号ならびに米国特許出願公開第2005/0037000号および第2005/0064514号に開示される重鎖および/またはFc突然変異の使用を包含する。このアミノ酸改変(すなわち、突然変異)は、この出願に詳細に記載の無作為に変異を誘発されたIgG1 Fcのライブラリーおよびスクリーニングアッセイを使用して同定された。さらに、改変のための領域は、利用可能な情報、例えば、結晶構造データ、マウス/ヒトアイソタイプFcγR結合差、遺伝子データおよび変異誘発によって同定された追加の部位に基づいて選択することもできる。所望の結合特性を有する本発明の分子(例えば、野生型Fc領域を含む比較可能な分子と比べてFcγRIIIAについての変異型Fc領域の親和性を増強する少なくとも1つのアミノ酸改変を有する変異型Fc領域を有する分子)を同定した(第5.1節ならびに、例えば、表3および9を参照されたい)後、この節で記載したように、または当技術分野で知られている標準的な組換えDNA技術および任意の知られている突然変異生成技術を使用して他の分子(すなわち、治療用抗体)を工学的に改変して、同定された突然変異部位を担持する工学的改変分子を作製できることが当業者に理解されるであろう。
上記で参考文献として挙げた国際公開第04/063351号ならびに米国特許出願公開第2005/0037000号および第2005/0064514号から引用した以下の表は、Fc-FcγR相互作用、詳細にはIgG1とFcγRIIIAおよびFcγRIIBとのFc相互作用を変更することが判明したこれらの突然変異を要約する。表10および表11は、親和性を改善し、変異体IgG1のFc-FcγRIIIA相互作用のK
offを低下させた突然変異を要約し、この突然変異はそれぞれ、連続的平衡または動力学的FACSスクリーニングを使用して本発明者らによって同定された。表12および表13は、FcγRIIIAに対するIgG1 Fc結合を可能にしたが、IgG1 Fc-FcγRIIB結合を無くした突然変異を要約し、この突然変異は、連続的固相分離スクリーニングを使用して本発明者らによって同定された。
表14は、酵母ディスプレイに基づくアッセイおよびELISAの両方を使用して本発明者らによってすでに決定された突然変異およびそのFcγR結合特性を要約する。表14中の記号は、以下の通り表す:・は1倍の親和性の増大に相当し;+は50%の親和性の増大に相当し;-は1倍の親和性の低下に相当し;→は野生型Fc領域を含む比較可能な分子と比較して親和性の変化なしに相当する。
6.3 FACSアッセイ;固相アッセイおよび免疫学に基づくアッセイ
本発明のFcγR分子(例えば、抗体、融合タンパク質、コンジュゲート分子)は、様々な形で特徴付けることができる。具体的には、改変された重鎖を含む本発明の分子を、リガンド、例えばFcγRIIIA四量体複合体と免疫特異的に結合できるかどうかアッセイを行うことができる。そのようなアッセイは、溶液中で(例えば、Houghten, Bio/Techniques, 13:412-421, 1992)、ビーズ上で(Lam, Nature, 354:82-84, 1991)、チップ上で(Fodor, Nature, 364:555-556, 1993)、細菌上で(米国特許第5,223,409号)、胞子上で(米国特許第5,571,698号; 第5,403,484号; および第5,223,409号)、プラスミド上で(Cull et al., Proc. Natl. Acad. Sci. USA, 89:1865-1869, 1992)またはファージ上で(Scott and Smith, Science, 249:386-390, 1990; Devlin, Science, 249:404-406, 1990; Cwirla et al., Proc. Natl. Acad. Sci. USA, 87:6378-6382, 1990; およびFelici, J. Mol. Biol., 222:301-310, 1991)で行うことができる(これらの参照文献はそれぞれ、参照によりその全体が本明細書に組み込まれている)。次いで、リガンド、例えばFcγRIIIAと免疫特異的に結合することが明らかとなった分子を、リガンドに対するその特異性および親和性についてアッセイを行うことができる。
抗原(例えば、癌抗原)との免疫特異的結合および他の抗原(例えば、FcγR)との交差反応性について、当技術分野で知られている任意の方法により、改変された重鎖を含むように工学的に改変された本発明の分子(例えば、治療用抗体)のアッセイを行うことができる。免疫特異的結合および交差反応性の分析に使用することができるイムノアッセイには、それだけに限らないが、ほんの少数の例を挙げれば、ウェスタンブロット法、ラジオイムノアッセイ、ELISA(酵素結合免疫吸着アッセイ)、「サンドイッチ」イムノアッセイ、免疫沈降アッセイ、沈降素反応、ゲル拡散沈降素反応、免疫拡散アッセイ、凝集アッセイ、補体結合アッセイ、免疫放射測定アッセイ、蛍光イムノアッセイ、プロテインAイムノアッセイなどの技術を使用する競合的および非競合的アッセイ系がある。そのようなアッセイは日常的であり、当技術分野で周知である(例えば、参照によりその全体が本明細書に組み込まれている、Ausubel et al., eds, 1994, Current Protocols in Molecular Biology, Vol. 1, John Wiley & Sons, Inc., New Yorkを参照されたい)。
本発明の分子を特徴付けるための一例示的システムは、変異型重鎖を有する本発明の分子をコードする核酸がクローニングされている、抗フルオレセインモノクローナル抗体4-4-20の重鎖を含む哺乳動物発現ベクターを含む。得られた組換えクローンは、哺乳動物宿主細胞系(すなわち、ヒト腎細胞系293H)で発現させ、得られた組換え免疫グロブリンは、それだけに限らないが、ELISAおよびFACSを含めた当業者に知られている任意の標準的アッセイを使用して、FcγRに対する結合について分析する。
改変された重鎖を含む本発明の分子とリガンド、例えばFcγR四量体複合体の結合親和性および相互作用の解離速度は、競合的結合アッセイによって決定することができる。競合的結合アッセイの一例は、四量体FcγRなどの多量の非標識リガンドの存在下での、四量体FcγRなどの標識リガンド(例えば、3Hまたは125I)を、対象の分子(例えば、変異型重鎖(例えば、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を含む野生型重鎖と比べて1つまたは複数のアミノ酸改変を含む重鎖)を含む本発明の分子)とインキュベートすること、および標識リガンドに結合した分子を検出ことを含むラジオイムノアッセイである。リガンドについての本発明の分子の親和性および結合解離速度は、スキャッチャード分析によって飽和データから決定することができる。
好ましい実施形態では、BIAcore動力学分析を使用して、FcγRなどのリガンドと本発明の分子の結合速度および解離速度を決定する。BIAcore動力学分析は、表面上に分子(例えば、改変されたFc領域を含む分子)が固定化されたチップからのリガンドの結合および解離を検出することを含む。
FcγRに対する本発明の変異型重鎖を含む分子の結合の特徴付けは、それだけに限らないが、FcγRの多型変異体を含めた任意のFcγRを使用して行うこともできる。いくつかの実施形態では、Fc変異体の選択は、158位にフェニルアラニンを含むFcγRIIIAの多型変異体を使用して行う。他の実施形態では、特徴付けは、158位にバリンを含むFcγRIIIAの多型変異体を使用して行う。FcgRIIIA 158Vは、158Fよりも高いIgG1に対する親和性および増大したADCC活性を示し(例えば、両方の全体が参照により本明細書に組み込まれている、Koene et al., 1997, Blood, 90:1109-14、Wu et al., 1997, J. Clin. Invest. 100: 1059-70を参照されたい);この残基は実際、IgG1-FcγRIIIA共結晶化試験によって最近示されるIgG1のより低いヒンジ領域と直接的に相互作用し、例えば、その全体が参照により本明細書に組み込まれているSonderman et al., 2000, Nature, 100: 1059-70を参照されたい。試験により、場合によっては治療用抗体がFcγRIIIA-158Vホモ接合体患者において改善された効率を有することが示されている。例えば、ヒト化抗CD20モノクローナル抗体リツキシマブは、FcγRIIIA158Fホモ接合性患者と比較してFcγRIIIA158Vホモ接合性患者において治療上より有効であった(例えば、Cartron et al., 2002 Blood, 99(3): 754-8を参照されたい)。他の実施形態では、治療用抗体は、FcγRIIIA-158VおよびFcγRIIIA-158Fに対してヘテロ接合性の患者およびFcγRIIA-131Hの患者においてより有効であり得る。ある特定の作用機序によって縛られることを意図しないが、代替のアロタイプを有する本発明の分子の選択は、治療用抗体中で工学的に改変されると、前記アロタイプに対してホモ接合性の患者にとって臨床上より有効であろう変異体を提供し得る。
本発明は、セクション5.2および5.3に記載の方法に従って本発明の変異型重鎖を含む分子をスクリーニングすることを包含する。本発明の一態様は、所望の結合特性、詳細には、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドがFcγRIIIAおよび/またはFcγRIIAに結合するよりも高い親和性で、変異型重鎖またはその部分がFcγRIIIAおよび/またはFcγRIIAに結合できることを示す分子についてスクリーニングする方法を提供する。別の実施形態では、本発明は、所望の結合特性、詳細には、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドがFcγRIIIAおよび/またはFcγRIIAに結合するよりも高い親和性で、変異型重鎖またはその部分がFcγRIIIAおよび/またはFcγRIIAに結合できること、さらには同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドがFcγRIIBに結合するよりも低い親和性で、変異型重鎖またはその部分がFcγRIIBに結合できることを示すこうした変異型重鎖またはその部分を選択するための方法を提供する。本発明の方法を使用して、任意の所望の結合特性について本発明の重鎖における任意の突然変異をスクリーニングできることは当業者によって理解されよう。
好ましくは、当業者に知られている任意の技法を使用した蛍光活性化細胞選別(FACS)は、本発明の分子を特徴付けるために免疫学または機能に基づいたアッセイに使用される。フローソーターは、本発明の分子(例えば、1時間当たり1000万〜1億の細胞)に結合した、例えば、オプソニン化した大量の個々の細胞を迅速に調査することが可能である(Shapiro et al., Practical Flow Cytometry, 1995)。さらに、抗体挙動の最適化に使用される特定のパラメーターには、それだけに限らないが、リガンド濃度(すなわち、FcγRIIIA四量体複合体)、動力学的な競合時間、またはFACS厳密性が含まれ、これらはいずれも、特異的結合特性、例えば、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能なポリペプチドと比較してより高いFcγRIIIAに対する親和性を示す本発明の分子を含む抗体について選択するために変わり得る。生体細胞を選別および調査するためのフローサイトメーターは当技術分野で周知である。既知のフローサイトメーターは、例えば、米国特許第4,347,935号、第5,464,581号、第5,483,469号、第5,602,039号、第5,643,796号および第6,211,477号に記載されており、その全体の内容が参照により本明細書に組み込まれている。他の既知のフローサイトメーターは、Becton Dickinson and Company社製のFACS Vantage(商標)システムおよびUnion Biometrica社製のCOPAS(商標)システムである。
6.3.1 変異型重鎖を有する分子の機能アッセイ
本発明は、分子のエフェクター細胞機能を同定する、当技術分野で知られているアッセイを使用した、本発明の分子(例えば、IgG2、IgG3またはIgG4のFc領域を有し、上記に記載の酵母ディスプレイ技術/IgG1 Fc領域の分析によって同定された突然変異を含む変異型重鎖を含む抗体; または本発明の方法に従って工学的に改変された治療用モノクローナル抗体)の特徴付けを包含する。具体的には、本発明は、FcγR媒介性エフェクター細胞機能についての本発明の分子の特徴付けを包含する。本発明に従ってアッセイを行うことができるエフェクター細胞機能の例には、それだけに限らないが、抗体依存性細胞媒介性細胞傷害、食作用、オプソニン化、オプソニン食作用、C1q結合、および補体依存性細胞媒介性細胞傷害がある。エフェクター細胞機能活性を決定する、当業者に知られている任意の細胞に基づくアッセイまたは無細胞アッセイを使用することができる(エフェクター細胞アッセイについては、それぞれ参照によりその全体が本明細書に組み込まれている、Perussia et al., 2000, Methods Mol. Biol. 121: 179-92; Baggiolini et al., 1998 Experientia, 44(10): 841-8; Lehmann et al., 2000 J. Immunol. Methods, 243(1-2): 229-42; Brown EJ. 1994, Methods Cell Biol., 45: 147-64; Munn et al., 1990 J. Exp. Med., 172: 231-237, Abdul-Majid et al., 2002 Scand. J. Immunol. 55: 70-81; Ding et al., 1998, Immunity 8:403-411を参照されたい)。
一実施形態では、ヒト単球でのFcγR媒介性食作用について本発明の分子のアッセイを行うことができる。あるいは、本発明の分子のFcγR媒介性食作用は、他の食細胞、例えば、好中球(多形核白血球; PMN); ヒト末梢血単球、単球由来マクロファージでアッセイを行うこともでき、それらは、当業者に知られている標準的な手順を使用して得ることができる(例えば、Brown EJ. 1994, Methods Cell Biol., 45: 147-164を参照されたい)。一実施形態では、以前に記載されている方法(Tridandapani et al., 2000, J. Biol. Chem. 275: 20480-7)によりフルオレセイン化IgG-オプソニン化ヒツジ赤血球(SRBC)を貪食するTHP-1細胞の能力を測定することによって本発明の分子の機能を特徴付ける。例えば、FcγRIIIAについて増強された親和性を有する変異型重鎖を含む本発明の分子の食作用を測定する例示的なアッセイは、THP-1細胞を本発明の分子またはFcγRIIIAと結合しない対照抗体で処理すること、前記細胞の活性レベルを比較することからなり、細胞の活性(例えば、ロゼット形成活性(IgG被覆SRBCに結合しているTHP-1細胞の数)、接着活性(THP-1細胞に結合したSRBCの合計数)、および貪食速度)の相違から、本発明の分子の機能が示唆される。この例示的なアッセイを使用して、本発明の方法によって同定された分子のいずれかのアッセイを行うことができることを当業者なら理解することができる。
本発明の分子の食作用を決定する他の例示的なアッセイは、抗体依存性オプソニン食作用アッセイ(ADCP)であり、それは以下のことを含み得る: 大腸菌(Escherichia coli)標識FITC(Molecular Probes)や黄色ブドウ球菌(Staphylococcus aureus)-FITCなどの標的生体粒子を(i)FcγR依存性ADCPの対照抗体である、フルオレセインに対する抗体の野生型4-4-20抗体(参照によりその全体が本明細書に組み込まれているBedzyk et al., 1989, J. Biol. Chem, 264(3): 1565-1569を参照されたい); または(ii)FcγR依存性ADCPのバックグラウンド対照である、FcγRIIIとの結合を不能にするD265A突然変異を内部に有する4-4-20抗体(iii)本発明の方法によって同定され、実施例6.6で例示されているように作製された変異型Fc領域を担持する4-4-20抗体で被覆すること; およびオプソニン化粒子を形成すること; (i〜iii)に記載のオプソニン化粒子のいずれかをTHP-1エフェクター細胞(ATCCから入手可能な単球細胞系統)に1:1、10:1、30:1、60:1、75:1または100:1の比で添加して、FcγR媒介性食作用を起こさせること; 好ましくは、細胞および大腸菌-FITC/抗体を37℃で1.5時間インキュベートすること; インキュベーション後トリパンブルーを細胞に添加して(好ましくは室温で2〜3分置いて)、内部移行せずに細胞表面の外側に接着した細菌の蛍光を失活させること; 細胞をFACS緩衝液(例えば、PBS中0.1%BSA、0.1%アジ化ナトリウム)中に移すこと; FACS(例えば、BD FACS Calibur)を使用してTHP1細胞の蛍光を分析すること。好ましくは、アッセイで使用したTHP-1細胞を、細胞表面上のFcγRの発現についてFACSにより分析する。THP-1細胞は、CD32AとCD64をどちらも発現する。CD64は高親和性FcγRであり、本発明の方法に従ってADCPアッセイを行う際に遮断される。好ましくは、THP-1細胞を100μg/mLの可溶性IgG1または10%ヒト血清で遮断する。ADCPの程度を分析するために、好ましくはTHP-1細胞上にゲートを設定し、中央蛍光強度を測定する。個々の突然変異体のADCP活性を計算し、得られた野生型chMab 4-4-20に対して標準化した値としてそれを報告する。オプソニン化粒子とTHP-1細胞の比が30:1または60:1となるように、オプソニン化粒子をTHP-1細胞に添加する。最も好ましい実施形態では、培地中の大腸菌-FITC、大腸菌-FITCおよびTHP-1細胞(FcγR非依存性ADCP活性として働く)、大腸菌-FITC、THP-1細胞および野生型4-4-20抗体(FcγR依存性ADCP活性として働く)、大腸菌-FITC、THP-1細胞、4-4-20 D265A(FcγR依存性ADCP活性のバックグラウンド対照として働く)などの対照とともにADCPアッセイを行う。
他の実施形態では、当業者に知られている標準的な方法のいずれかを使用して(例えば、Perussia et al., 2000, Methods Mol. Biol. 121:179-92; Weng et al., 2003, J. Clin. Oncol. 21: 3940-3947; Ding et al., Immunity, 1998, 8:403-11を参照されたい)、エフェクター細胞、例えばナチュラルキラー細胞でのFcγR媒介性ADCC活性について本発明の分子のアッセイを行うことができる。本発明の分子のADCC活性を決定する例示的なアッセイは、標的細胞を[51Cr]Na2CrO4(この細胞膜透過性分子は、それが細胞質タンパク質に結合し、緩徐な動態で細胞から自発的に放出されるが、標的細胞の壊死後に大量に放出されるので、標識に一般に使用される)で標識すること; 標的細胞を、変異型重鎖を含む本発明の分子でオプソニン化すること; 標的細胞とエフェクター細胞の適当な比率で、マイクロタイタープレート中で、オプソニン化した放射標識標的細胞をエフェクター細胞と混合すること; 細胞の混合物を37℃で16〜18時間インキュベートすること; 上清を収集すること; および放射活性を分析することからなる51Cr放出アッセイに基づく。次いで、例えば下記の式: %溶解=(実験cpm-標的漏出cpm)/(界面活性剤溶解cpm-標的漏出cpm)×100%を使用して、本発明の分子の細胞傷害を決定することができる。あるいは、%溶解=(ADCC-AICC)/(最大放出-自発放出)。式: 特異的溶解=本発明の分子での%溶解-本発明の分子の不在下での%溶解を使用して、特異的溶解を計算することができる。標的:エフェクター細胞の比または抗体濃度を変化させることによって、グラフを作成することができる。
好ましくは、本発明のADCCアッセイで使用するエフェクター細胞は末梢血単核細胞(PBMC)であり、好ましくは、それは当業者に知られている標準的な方法を使用して、例えばFicoll-Paque密度勾配遠心分離を使用して正常ヒト血液から精製される。本発明の方法での使用に好ましいエフェクター細胞は、様々なFcγR活性化受容体を発現する。本発明は、重鎖抗体突然変異体が野生型IgG1抗体と比べてADCC活性および食作用の増大を示すかどうかを決定するための、FcγRI、FcγRIIAおよびFcγRIIBを発現するエフェクター細胞THP-1、ならびにFcγRIIAとFcγRIIBをどちらも発現する、ヒト全血に由来する単球由来初代マクロファージを包含する。
ヒト単球細胞系統THP-1は、高親和性受容体FcγRIおよび低親和性受容体FcγRIIAの発現を介して食作用を活性化する(Fleit et al., 1991, J. Leuk. Biol. 49: 556)。THP-1細胞は、FcγRIIAまたはFcγRIIBを構成的に発現しない。サイトカインでのこれらの細胞の刺激はFcR発現パターンに影響する(Pricop et al., 2000 J. Immunol. 166: 531-7)。サイトカインIL4の存在下でTHP-1細胞を増殖させると、FcγRIIB発現が誘導され、FcγRIIAおよびFcγRI発現の低下が起こる。FcγRIIB発現はまた、細胞密度の増大によっても増強される(Tridandapani et al., 2002, J. Biol Chem. 277: 5082-9)。その一方で、IFNγがFcγRIIIAの発現を引き起こすことができることが報告されている(Pearse et al., 1993 PNAS USA 90: 4314-8)。細胞表面上での受容体の存在の有無を、当業者に知られている一般的な方法を使用してFACSにより決定することができる。サイトカインによって誘導されるFcγRの発現から、FcγRIIBの存在下で活性化と阻害をどちらも試験する系が提供される。THP-1細胞がFcγRIIBを発現することができない場合、本発明はまた、他のヒト単球細胞系統U937をも包含する。これらの細胞は、IFNγおよびTNFの存在下で最後にマクロファージに分化することが示されている(Koren et al., 1979, Nature 279: 328-331)。
FcγR依存性腫瘍細胞死滅は、マウス腫瘍モデルにおいて、マクロファージおよびNK細胞によって媒介される(Clynes et al., 1998, PNAS USA 95: 652-656)。本発明は、食作用アッセイとADCCアッセイの両方でFc突然変異体が標的細胞の細胞性細胞傷害を誘発する効率を分析するエフェクター細胞としてのドナー由来水簸単球の使用を包含する。FcγRI、FcγRIIIA、およびFcγRIIBの発現パターンは、様々な増殖条件によって影響を受ける。凍結水簸単球、新鮮水簸単球、10%FBSで維持された単球、ならびにFBS+GM-CSFおよびまたはヒト血清で培養された単球からのFcγR発現は、当業者に知られている一般的な方法を使用して決定することができる。例えば、細胞をFcγR特異的抗体で染色し、それをFACSにより分析してFcRプロファイルを決定することができる。次いで、マクロファージのin vivoでのFcγR発現を最もよく模倣する条件を本発明の方法に使用する。
いくつかの実施形態では、本発明は、特に正しいFcγRプロファイルを有するヒト細胞を得ることができないときのマウス細胞の使用を包含する。いくつかの実施形態では、本発明は、マウスマクロファージ細胞系統RAW264.7(ATCC)を包含し、当技術分野で知られている方法を使用してそれにヒトFcγRIIIAをトランスフェクトし、安定したトランスフェクタントを単離することができる(例えば、Ralph et al., J. Immunol. 119: 950-4を参照されたい)。日常的な実験を使用したFACS分析により、FcγRIIIA発現についてトランスフェクタントを定量することができ、高発現体を本発明のADCCアッセイで使用することができる。他の実施形態では、本発明は、本明細書で開示されているものなどのノックアウトトランスジェニックマウスからの、ヒトFcγRを発現する脾臓腹腔マクロファージの単離を包含する。
リンパ球は、ドナーの末梢血(PBM)から、Ficoll-Paque勾配(Pharmacia)を使用して回収することができる。細胞の単離された単核集団内で、大部分のADCC活性が、その表面上にFcγRIIIAを含むがFcγRIIBを含まないナチュラルキラー細胞(NK)を介して生じる。これらの細胞を用いた結果から、NK細胞のADCCの誘発に対する突然変異体の効果が示唆され、水簸単球を用いて試験するための試薬が確立される。
本発明のADCCアッセイで使用する標的細胞には、それだけに限らないが、乳癌細胞系統、例えば、ATCCアクセッション番号HTB-30を有するSK-BR-3(例えば、Tremp et al., 1976, Cancer Res. 33-41を参照されたい); Bリンパ球; バーキットリンパ腫に由来する細胞、例えばATCCアクセッション番号CCL-86を有するRaji細胞(例えば、Epstein et al., 1965, J. Natl. Cancer Inst. 34: 231-240を参照されたい)、およびATCCアクセッション番号CCL-213を有するDaudi細胞(例えば、Klein et al., 1968, Cancer Res. 28: 1300-10を参照されたい)がある。標的細胞は、アッセイを行うべき免疫グロブリンの抗原結合部位によって認識されなければならない。
ADCCアッセイは、アポトーシス経路を介して細胞死を媒介するNK細胞の能力に基づく。NK細胞は、部分的にはFcγRIIIAが細胞表面上で抗原と結合したIgGを認識することによって細胞死を媒介する。本発明の方法に従って使用するADCCアッセイは、放射性に基づくアッセイでもよく、あるいは蛍光に基づくアッセイでもよい。変異型Fc領域を含む本発明の分子の特徴付けに使用するADCCアッセイは、標的細胞、例えばSK-BR-3、MCF-7、OVCAR3、Raji、Daudi細胞を標識すること、その抗原結合部位を介して標的細胞上の細胞表面受容体を認識する抗体で標的細胞をオプソニン化すること; 日常的な実験によって決定することができる適当な比率で、標識されたオプソニン化標的細胞とエフェクター細胞を混合すること; 細胞を回収すること; 使用した標識に基づく適当な検出スキームを使用して、溶解した標的細胞の上清中の標識を検出することを含む。当技術分野で知られている標準的な方法を使用して、放射性標識または蛍光標識で標的細胞を標識することができる。例えば、標識には、それだけに限らないが、[51Cr]Na2CrO4; および蛍光増強リガンドのアセトキシメチルエステルの2,2':6',2"-テルピリジン-6-6"-ジカルボキシレート(TDA)がある。
具体的な好ましい実施形態では、蛍光増強リガンドのアセトキシメチルエステルの2,2':6',2"-テルピリジン-6-6"-ジカルボキシレート(TDA)で標識されている標的細胞に対するADCC活性の測定に、時間分解蛍光定量アッセイを使用する。そのような蛍光定量アッセイは当技術分野で知られ、例えば、参照によりその全体が本明細書に組み込まれている、Blomberg et al., 1996, Journal of Immunological Methods, 193: 199-206を参照されたい。簡潔に述べると、標的細胞を膜透過性のTDAのアセトキシメチルジエステル(ビス(アセトキシメチル)2,2':6',2"-テルピリジン-6-6"-ジカルボキシレート、(BATDA))で標識し、それは生細胞の細胞膜全体に迅速に拡散する。細胞内エステラーゼはエステル基を分離し、再生した膜不透過性TDA分子が細胞内で捕捉される。エフェクター細胞および標的細胞を、例えば5%CO2下で37℃で少なくとも2時間、最大で3.5時間インキュベートした後、溶解された標的細胞から放出されたTDAをEu3+でキレート化し、形成したユーロピウム-TDAキレートを、時間分解蛍光測定器(例えば、Victor 1420、Perkin Elmer/Wallac)で定量する。
他の例示的な実施形態では、変異型重鎖を含む本発明の分子の特徴付けに使用するADCCアッセイは、下記のステップを含む: 好ましくは、4〜5×106個の標的細胞(例えば、SK-BR-3、MCF-7、OVCAR3、Raji細胞)を、ビス(アセトキシメチル)2,2':6',2"-テルピリジン-t-6"ジカルボキシレート(DELFIA BATDA Reagent、Perkin Elmer/Wallac)で標識する。最適な標識効率にするには、ADCCアッセイで使用する標的細胞の数は、好ましくは5×106を超えるべきでない。BATDA試薬を細胞に添加し、その混合物を37℃で、好ましくは5%CO2下で、少なくとも30分間インキュベートする。次いで、細胞を生理的緩衝液、例えば0.125mMのスルフィンピラゾールを有するPBS、および0.125mMのスルフィンピラゾールを含む培地で洗浄する。次いで、変異型重鎖を含む本発明の分子、すなわち、それだけに限らないが、ポリクローナル抗体、モノクローナル抗体、二重特異性抗体、多重特異性抗体、ヒト化抗体、およびキメラ抗体を含めた本発明の変異型重鎖を含む免疫グロブリンで、標識された標的細胞をオプソニン化(被覆)する。好ましい実施形態では、ADCCアッセイで使用する変異型重鎖を含む免疫グロブリンは、細胞表面受容体、腫瘍抗原、または癌抗原に特異的である。本発明の変異型重鎖が導入された免疫グロブリンは、第5.2節および第5.5.1節で列挙するものなどの任意の癌または腫瘍抗原に特異的に結合する。さらに、本発明の変異型Fc領域が導入された免疫グロブリンは、第5.5.1.2節で列挙するものなどの癌抗原に特異的な任意の治療用抗体でよい。いくつかの実施形態では、ADCCアッセイで使用する変異型Fc領域を含む免疫グロブリンは、抗フルオレセインモノクローナル抗体4-4-20(Kranz et al., 1982 J. Biol. Chem. 257(12): 6987-6995)、マウス-ヒトキメラ抗CD20モノクローナル抗体2H7 (Liu et al., 1987, Journal of Immunology, 139: 3521-6); またはヒト上皮成長因子2(p185 HER2)に対するヒト化抗体(Ab4D5)(Carter et al. (1992, Proc. Natl. Acad. Sci. USA 89: 4285-9)である。ADCCアッセイにおける標的細胞は、免疫グロブリンが標的細胞の細胞表面受容体に特異的に結合するように本発明の変異型重鎖が導入されている免疫グロブリンに従って選択される。好ましくは、本発明のADCCアッセイは、本発明の変異型重鎖を内部に有する複数の工学的改変抗体、例えば、抗Her2/neu、4-4-20、2B6、Rituxan、および2H7を使用して行う。
標的細胞をエフェクター細胞、例えばPBMCに添加して、エフェクター:標的の比を約1:1、10:1、30:1、50:1、75:1、または100:1にする。特定の実施形態では、変異型重鎖を含む免疫グロブリンが抗フルオレセイン抗体4-4-20の可変ドメインを有するとき (Kranz et. al., 1982, J. Biol. Chem., 257:6987-6995)、エフェクター:標的は75:1である。5%CO2下で、エフェクター細胞および標的細胞を37℃で少なくとも2時間、最大で3.5時間インキュベートする。細胞上清を回収し、酸性ユーロピウム溶液(例えば、DELFIA Europium Solution、Perkin Elmer/Wallac)に添加する。形成したユーロピウム-TDAキレートの蛍光を、時間分解蛍光測定器(例えば、Victor 1420、Perkin Elmer/Wallac)で定量する。最大放出(MR)および自発放出(SR)は、それぞれ1% TX-100および培地単独で標的細胞をインキュベートすることによって決定する。抗体非依存性細胞性細胞傷害(AICC)は、抗体の不在下で標的細胞およびエフェクター細胞をインキュベートすることによって測定する。好ましくは、各アッセイを三連で行う。特異的溶解の平均百分率は、実験放出(ADCC)-AICC)/(MR-SR)×100として計算する。
本発明は、NK依存性およびマクロファージ依存性ADCCアッセイの両方における本発明の重鎖変異体(すなわち、IgG2、IgG3またはIgG4のFc領域を有し、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変(例えば、置換)を含む重鎖)を含む分子の特徴付けを包含する。本発明の重鎖変異体は、NK依存性またはマクロファージ依存性アッセイにおいてアッセイした場合、変更されたエフェクター機能などの変更された表現型を有する。エフェクター機能を変更すると同定された重鎖変異体は、本出願、例えば表9と、本発明者らの同時出願であり、そのそれぞれの全体が参照により組み込まれている国際公開第04/063351号ならびに米国特許出願公開第2005/0037000号および第2005/0064514号の開示の両方で開示されている。例えば、表9に要約された5つのIgG1突然変異体は、野生型Fc領域と比べて増強されたADCC活性を有していた:MGFc-27(G316D、A378V、D399E);MGFc-31(P247L、N421K);MGFc-10(K288N、A330S、P396L);MGFc-28(N315I、V379M、T394M);MGFc-29(F243I、V379L、G420V)。野生型Fc領域と比べてADCC活性が変更された追加の突然変異体は国際公開第04/063351号に開示されている。国際公開第04/063351号では、突然変異体は、変異型Fc領域をヒト化抗体Ab4D5(ヒト上皮成長因子受容体(HER2/neu)に特異的)または抗CD-20モノクローナル抗体2H7中にクローニングすることによって同定された。野生型Fcを含む抗体と比べて、10のIgG1突然変異体が、4D5または2H7の状況で増強されたADCC活性を有し(MgFc42(G402D)、MgFc44(K344N、P396L)、MgFc45(H268D、E318D)、MgFc49(K261N、K210M、P396L)、MgFc51(Q419H、P396L)、MgFc52(V240A、P396L)、MgFc53(L410H、P396L)、MgFc54(F243L、V305I、A378D、F404S、P396L)、MgFc55(R255I、P396L)およびMgFc59(K370E、P396L))、4つのIgG1突然変異体が、4D5の状況で増大したADCC活性を有するが、2H7の状況で同等にすぎない、または低下したADCC活性を有していた(MgFc46(P217S、P396L)、MgFc47(K210M、P396L)、MgFc48(V379M、P396L)およびMgFc50(P247S、P396L))。MgFc38(K392T、P396L)およびMgFc43b(K288R、T307A、K344E、P396L)のみを4D5の状況で試験し、野生型Fcを含む4D5と比べてADCC活性の増大を示した。MgFc27(G316D、A378V、D399E)、MgFc29(F243I、V379L、G420V)およびMgFc57(L242F、P396L)のみ2H7の状況で試験し、野生型Fcを含む2H7と比べて不明瞭な(MgFc27)または増大した(MgFc29およびMgFc57)ADCC活性を示した。本発明者らによって同定され、4-4-20(IgG1)の状況で分析したさらなる突然変異体は、米国特許出願公開第2005/0037000号から引用した表15に要約される。表14において、変異体IgG1 Fcを含む抗体のADCC活性を野生型抗体(Wt)の活性と比べて示す。
本発明は、本発明の分子によるC1qの結合および補体依存性細胞傷害(CDC)の媒介を特徴付けるための、当技術分野で知られており、本明細書に例示したアッセイを包含する。C1q結合を決定するために、C1q結合ELISAを実施してもよい。例示的アッセイは以下を含むことができる。すなわち、アッセイプレートを被覆用緩衝液中の本発明の分子を含むポリペプチドまたは開始ポリペプチド(対照)で被覆して4℃で終夜置くことができる。次いで、プレートを洗浄しブロッキング処理することができる。洗浄後、ヒトC1qのアリコートを各穴に添加し、室温で2時間インキュベートすることができる。さらなる洗浄の後、ヒツジ抗補体C1qペルオキシダーゼコンジュゲート抗体100uLを各穴に添加し、室温で1時間インキュベートすることができる。洗浄緩衝液でプレートを再度洗浄することができ、OPD(O-フェニレンジアミン二塩酸塩(Sigma))を含む基質緩衝液100uLを各穴に添加することができる。黄色の出現によって観察される酸化反応を30分間進行させ、4.5 NH2 SO4を100uL添加することによってそれを停止することができる。次いで吸光度を(492〜405)nmで読み取ることができる。
本発明による好ましい分子は、このアッセイまたは類似のアッセイにおいて検出および測定した場合、C1q結合の著しい低下を示す分子である。好ましくは、変異型重鎖を含む分子は、同一のアイソタイプのFc領域を有する変異型重鎖を含む対照抗体と比較して、C1q結合の約50分の1の低下、約60分の1、約80分の1または約90分の1の低下を示す。最も好ましい実施形態では、Fc変異体を含む分子はC1qに結合せず、すなわち変異体は、対照抗体と比較してC1q結合の約100分の1以下の低下を示す。
本発明の別の例示的な分子は、比較可能な対照分子(例えば、同一のアイソタイプのFc領域を有する野生型重鎖を含む分子)よりも高いヒトC1qに対する結合親和性を含む分子である。このような分子は、同一のアイソタイプのFc領域を有する野生型重鎖を含む親分子と比較してヒトC1q結合において例えば、約2倍以上、好ましくは約5倍以上の改善を示し得る。例えば、ヒトC1q結合は、野生型Fc領域を含む分子と比較して約2倍〜約500倍、好ましくは約2倍または約5倍〜約1000倍向上し得る。
補体活性化を評価するため、例えば、参照によりその全体が本明細書に組み込まれている、Gazzano-Santoro et al., J. Immunol. Methods 202:163 (1996)に記載のように、補体依存性細胞傷害(CDC)アッセイを行うことができる。簡潔に述べると、様々な濃度の、変異型重鎖を含む分子およびヒト補体を緩衝液で希釈することができる。変異型重鎖を含む分子が結合する抗原を発現する細胞を希釈して、1ml当たり細胞約1×106個の密度にすることができる。変異型重鎖を含む分子、希釈したヒト補体、および抗原を発現する細胞の混合物を平底組織培養96穴プレートに添加し、それを37℃および5% CO2で2時間インキュベートして補体媒介性細胞溶解を促進することができる。次いで、アラマーブルー(alamar blue)(Accumed International)50μLを各穴に添加し、37℃で1晩インキュベートすることができる。96穴用蛍光測定器を使用して、530nmで励起し590nmで放出させて吸光度を測定する。その結果は、相対的蛍光単位(RFU)で表すことができる。標準曲線から試料濃度を算出することができ、非変異型分子、すなわち野生型重鎖を含む分子と比較したパーセント活性を、対象とする変異体について報告する。
いくつかの実施形態では、本発明の重鎖変異体は補体を活性化しない。好ましくは、変異体は上記のCDCアッセイでCDC活性を有さないように見える。本発明はまた、対照分子(野生型重鎖を含む分子)と比較して増強されたCDCを有する、例えば、(例えば、比較される各分子のIC50値において)in vitroまたはin vivoでCDC活性の約2倍〜約100倍の向上を示す変異体にも関する。補体アッセイは、モルモット、ウサギまたはヒト血清を用いて行うことができる。標的細胞の補体溶解は、それぞれ参照によりその全体が本明細書に組み込まれている、Korzeniewski et al., 1983 Immunol. Methods 64(3): 313-20; およびDecker et al., 1988 J. Immunol Methods 115(1): 61-9に記載のように、乳酸脱水素酵素(LDH)などの細胞内酵素の放出; または、本明細書に記載のように標的細胞を標識したユーロピウム、クロム51やインジウム111などの細胞内標識の放出をモニターすることによって検出することができる。
6.3.2 他のアッセイ
当技術分野で知られている、表面プラズモン共鳴に基づく任意のアッセイを使用して変異型Fc領域を含む本発明の分子のアッセイを行って、Fc-FcγR相互作用の結合の動態パラメーターを特徴付けることもできる。それだけに限らないが、Biacore AB (Uppsala, Sweden)から入手可能なBIAcore機器; Affinity Sensors (Franklin, MA.)から入手可能なIAsys機器; Windsor Scientific Limited (Berks, UK)から入手可能なIBISシステム、Nippon Laser and Electronics Lab (Hokkaido, Japan)から入手可能なSPR-CELLIAシステム、およびTexas Instruments (Dallas, TX)から入手可能なSPR Detector Spreetaを含めた市販されている任意のSPR機器を本発明で使用することができる。SPRに基づく技術の総説については、すべて参照によりその全体が本明細書に組み込まれている、Mullet et al., 2000, Methods 22: 77-91; Dong et al., 2002, Review in Mol. Biotech., 82: 303-23; Fivash et al., 1998, Current Opinion in Biotechnology 9: 97-101; Rich et al., 2000, Current Opinion in Biotechnology 11: 54-61を参照されたい。さらに、すべて参照によりその全体が本明細書に組み込まれている、米国特許第6,373,577号; 第6,289,286号; 第5,322,798号; 第5,341,215号; 第6,268,125号に記載のタンパク質とタンパク質の相互作用を測定するSPR機器およびSPRに基づく方法のいずれかが本発明の方法で企図される。
簡潔に述べると、SPRに基づくアッセイでは、結合対の構成要素を表面上に固定化し、溶液中で結合対の他の構成要素とその相互作用を実時間でモニターする。SPRは、複合体の形成または解離の後に起こる、表面の近くにある溶媒の屈折率の変化を測定することに基づく。固定化を行う表面はセンサーチップであり、それはSPR技術の心臓部である; それは、金の薄層で被覆されたガラス表面からなり、分子と表面の結合を最適化するように設計された一連の特殊化表面の基礎となる。様々なセンサーチップが、特に上記で列挙した会社から市販され、それらはすべて、本発明の方法で使用することができる。センサーチップの例には、BIAcore AB, Inc.から入手可能なもの、例えば、Sensor Chip CM5、SA、NTA、およびHPAがある。それだけに限らないが、アミン基を介する直接共有結合、スルフヒドリル基を介する直接共有結合、アビジン被覆表面とのビオチン結合、炭水化物基とのアルデヒド結合、およびNTAチップとのヒスチジンタグを介した結合を含めた当技術分野で知られている固定化の方法および化学反応のいずれかを使用して、本発明の分子をセンサーチップの表面上に固定化することができる。
いくつかの実施形態では、変異型重鎖を含む本発明の分子、例えばFc領域を含む免疫グロブリンとFcγRの結合の動態パラメーターは、BIAcore機器(例えば、BIAcore機器1000、BIAcore Inc., Piscataway, NJ)を使用して決定することができる。任意のFcγRを使用して、変異型Fc領域を含む本発明の分子との相互作用を評価することができる。特定の実施形態では、FcγRはFcγRIIIA、好ましくは可溶性単量体FcγRIIIAである。例えば、一実施形態では、可溶性単量体FcγRIIIAは、リンカー-AVITAG配列と連結したFcγRIIIAの細胞外領域である(参照によりその全体が本明細書に組み込まれている、2003年1月9日に出願された米国仮出願第60/439,498号(代理人整理番号11183-004-888)および2003年3月19日に出願された米国仮出願第60/456,041号を参照されたい)。他の特定の実施形態では、FcγRはFcγRIIB、好ましくは可溶性二量体FcγRIIBである。例えば、一実施形態では、可溶性二量体FcγRIIBタンパク質は、参照によりその全体が本明細書に組み込まれている、2003年1月13日に出願された米国仮出願第60/439,709号に記載の方法に従って調製する。
BIAcore機器を使用して、FcγRに対する、4-4-20抗体である、特にFc領域を含む変異型重鎖を含む分子の動態パラメーターを決定する例示的なアッセイは、以下のことを含む: BSA-FITCを、センサーチップ表面の4つのフローセルの1つに、好ましくはアミン結合化学反応により固定化し、その結果、BSA-FITCの約5000反応単位(RU)が表面上に固定化される。適切な表面を調製した後、本発明の重鎖変異体を担持する4-4-20抗体を表面に、好ましくは流速5μL/mLで20μg/mLの溶液を1分間注入することによって通過させる。表面に結合した4-4-20抗体のレベルは400〜700RUである。次に、HBS-P緩衝液(20mM HEPES、150 mM NaCl、3mM EDTA、pH7.5)中の受容体(FcγRIIAおよびFcγRIIB-Fc融合タンパク質)の希釈系列を表面上に100μL/分で注入する。異なる受容体希釈物間の抗体再生は、好ましくは、100mM NaHCO3 pH9.4; 3M NaClの5秒間の単回注入によって実施する。当技術分野で知られている任意の再生技術が本発明の方法で企図される。
データの組全体を収集した後、SPR機器製造業者、例えばBIAcore, Inc. (Piscataway, NJ)によって供給されるコンピュータアルゴリズムを使用して、得られた結合曲線を全体的に適合させる。このアルゴリズムはKonとKoffをどちらも計算するものであり、それから、みかけの平衡結合定数Kdが、2つの速度定数の比(すなわち、Koff/Kon)として推定される。個々の速度定数を導き出す方法のより詳細な処理は、BIAevaluaion Software Handbook (BIAcore, Inc., Piscataway, NJ)中に認めることができる。当技術分野で知られている任意の方法を使用して、得られたデータの分析を行うことができる。得られた動態データの解釈の様々な方法の総説については、すべて参照によりその全体が本明細書に組み込まれている、Myszka, 1997, Current Opinion in Biotechnology 8: 50-7; Fisher et al., 1994, Current Opinion in Biotechnology 5: 389-95; O'Shannessy, 1994, Current Opinion in Biotechnology, 5:65-71; Chaiken et al., 1992, Analytical Biochemistry, 201: 197-210; Morton et al., 1995, Analytical Biochemistry 227: 176-85; O'Shannessy et al., 1996, Analytical Biochemistry 236: 275-83を参照されたい。
好ましい実施形態では、SPR分析、例えばBIAcoreを使用して決定される動態パラメーターを、どのように本発明の分子が機能アッセイ、例えばADCCで機能するかの予測測定値として使用することができる。SPR分析から得られた動態パラメーターに基づいて本発明の物質の効果を予測する例示的な方法は、下記のことを含んでよい: 本発明の分子とFcγRIIIAおよびFcγRIIBの結合のKoff値を決定すること; ADCCデータに対して(1)FcγRIIIAのKoff(野生型)/Koff(突然変異型); (2)FcγRIIBのKoff(突然変異型)/Koff(野生型)をプロットすること。1より高い数は、野生型に比べて低いFcγRIIIAの解離速度および高いFcγRIIBの解離速度を示し、増強されたADCC機能を有する。
本発明は、本明細書に記載の通り、または本発明者らの同時出願であり、そのそれぞれの全体が参照により組み込まれている国際公開第04/063351号ならびに米国特許出願公開第2005/0037000号および第2005/0064514号に開示の通り、BIAcore動力学的分析を使用して同定された重鎖の特定の変異体を有する抗体を包含する。表26〜22は、本明細書に開示の通り、また前記出願に記載の通りBIAcore分析を使用してIgG1の状況で特徴付けられた種々の突然変異体を要約する。表16〜18に記載のこうした突然変異体はまた、FcγRIIIAおよびFcγRIIBに対する結合を決定するためのELISAアッセイおよびADCCアッセイを使用して試験された。使用される抗体濃度は、ADCCアッセイにおいて標準的な0.5μg/ml〜1.0μg/mlの範囲にある。表20〜22に記載のこうした突然変異体は、複数のアロタイプのFcγRIIIAおよびFcγRIIAに対する結合についてのBIAcore分析を使用してIgG1の状況で特徴付けた。表21に記載の突然変異体は、C1qに対する結合についてのBIAcore分析を使用して特徴付けた。BIAcoreまたはADCCアッセイのいずれかについて、Fc突然変異を示す通りch4-4-20、2B6または4D5抗体(それぞれIgG1)中にクローニングした。
6.4 本発明の分子の組換えによる産生方法
6.4.1 本発明の分子をコードするポリヌクレオチド
本発明はまた、本発明のポリペプチドおよび抗体を含めた本発明の分子をコードするポリヌクレオチドをも含む。当技術分野で知られている任意の方法によって、本発明の分子をコードするポリヌクレオチドを得、そのポリヌクレオチドのヌクレオチド配列を決定することができる。
本発明の方法によって同定された分子(例えば、抗体)のヌクレオチド配列を決定した後、当技術分野で周知の方法、例えば組換えDNA技術、部位特異的突然変異生成、PCRなど(例えば、どちらも参照によりその全体が本明細書に組み込まれている、Sambrook et al., 2001, Molecular Cloning, A Laboratory Manual, 3rd Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, NY; およびAusubel et al., eds., 1998, Current Protocols in Molecular Biology, John Wiley & Sons, NYに記載の技術を参照されたい)を使用してヌクレオチド配列を操作して、例えば、例えばアミノ酸置換、欠失、および/または挿入を生じさせることによって異なるアミノ酸配列を有する抗体を生成することができる。
特定の実施形態では、核酸が抗体をコードするとき、日常的な組換えDNA技術を使用して、1つまたは複数のCDRをフレームワーク領域内に挿入する。フレームワーク領域は、天然に存在するフレームワーク領域または共通フレームワーク領域、好ましくはヒトフレームワーク領域でよい(例えば、ヒトフレームワーク領域の一覧については、Chothia et al., 1998, J. Mol. Biol. 278: 457-479を参照されたい)。
他の実施形態では、当技術分野で利用可能なヒトライブラリーまたは任意の他のライブラリーを当技術分野で知られている標準的な技術によりスクリーニングして、本発明の分子をコードする核酸をクローン化することができる。
6.4.2 本発明の分子の組換え発現
本発明の分子(すなわち、抗体)をコードする核酸配列を得た後、分子を産生するベクターを、当技術分野で周知の技術を使用して、組換えDNA技術によって作製することができる。当業者に周知である方法を使用して、本発明の分子のコード配列ならびに適当な転写および翻訳調節シグナルを含む発現ベクターを構築することができる。これらの方法には、例えば、in vitro組換えDNA技術、合成技術、および in vivo遺伝子組換えがある(例えば、Sambrook et al., 1990, Molecular Cloning, A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, NYおよびAusubel et al. eds., 1998, Current Protocols in Molecular Biology, John Wiley & Sons, NYに記載の技術を参照されたい)。
本発明の方法によって同定された分子(すなわち、抗体)のヌクレオチド配列を含む発現ベクターを、従来の技術(例えば、エレクトロポレーション、リポソームトランスフェクション、リン酸カルシウム沈殿)によって宿主細胞に移入することができ、次いで、トランスフェクトされた細胞を従来の技術により培養して本発明の分子を産生する。特定の実施形態では、本発明の分子の発現は、構成的、誘導性または組織特異的プロモーターによって制御される。
本発明の方法によって同定された分子の発現に使用する宿主細胞は、大腸菌などの細菌細胞でもよく、あるいは、好ましくは、特に組換え免疫グロブリン分子全体を発現させるための真核細胞でもよい。具体的には、ヒトサイトメガロウイルスの主要中間初期遺伝子プロモーターエレメントなどのベクターと併せた、チャイニーズハムスター卵巣(CHO)などの哺乳動物細胞は、免疫グロブリンに有効な発現系である(Foecking et al., 1998, Gene 45:101; Cockett et al., 1990, Bio/Technology 8:2)。
様々な宿主発現ベクター系を利用して、本発明の方法によって同定された分子を発現させることができる。そのような宿主発現系は、本発明の分子のコード配列を作製しその後精製することができる媒体を表すが、適当なヌクレオチドコード配列で形質転換されまたはそれをトランスフェクトされたときにin situで本発明の分子を発現する細胞も表す。これらには、それだけに限らないが、本発明の方法によって同定された分子のコード配列を含む組換えバクテリオファージDNA、プラスミドDNAまたはコスミドDNA発現ベクターで形質転換された細菌(例えば、大腸菌および枯草菌(B. subtilis))などの微生物; 本発明の方法によって同定された分子をコードする配列を含む組換え酵母発現ベクターで形質転換された酵母(例えば、サッカロマイセスピチア(Saccharomyces Pichia)); 本発明の方法によって同定された分子をコードする配列を含む組換えウイルス発現ベクター(例えば、バキュロウイルス)に感染した昆虫細胞系; 本発明の方法によって同定された分子をコードする配列を含む、組換えウイルス発現ベクター(例えば、カリフラワーモザイクウイルス(CaMV)およびタバコモザイクウイルス(TMV))に感染し、または組換えプラスミド発現ベクター(例えば、Tiプラスミド)で形質転換された植物細胞系; あるいは哺乳動物細胞のゲノムに由来するプロモーター(例えば、メタロチオネインプロモーター)または哺乳動物ウイルスに由来するプロモーター(例えば、アデノウイルス後期プロモーター; ワクシニアウイルス7.5Kプロモーター)を含む組換え発現構築物を内部に有する哺乳動物細胞系(例えば、COS、CHO、BHK、293、293T、3T3細胞、リンパ球系細胞(米国特許第5,807,715号を参照)、Per C.6細胞(Crucellによって開発されたヒト網膜細胞))がある。
細菌の系では、有利には、発現させる分子に意図される使用に応じていくつかの発現ベクターを選択することができる。例えば、抗体の医薬組成物を生成するために大量のそのようなタンパク質を産生するとき、精製が容易である融合タンパク質産物の高レベルの発現を誘導するベクターが望ましい可能性がある。そのようなベクターには、それだけに限らないが、融合タンパク質が産生されるようにlacZコード領域とインフレームで抗体コード配列をベクター中に個々に連結することができる大腸菌発現ベクターpUR278(Ruther et al., 1983, EMBO J. 2:1791); pINベクター(Inouye & Inouye, 1985, Nucleic Acids Res. 13:3101-3109; Van Heeke & Schuster, 1989, J. Biol. Chem. 24:5503-5509)などがある。pGEXベクターを使用して、グルタチオンS-転移酵素(GST)との融合タンパク質として外来ポリペプチドを発現させることもできる。一般に、そのような融合タンパク質は可溶性であり、マトリックスグルタチオン-アガロースビーズとの吸着および結合、その後の遊離グルタチオン存在下での溶出によって、溶解した細胞から容易に精製することができる。pGEXベクターは、トロンビンまたは第Xa因子プロテアーゼ切断部位を含むように設計され、その結果、クローン化標的遺伝子産物を、GST部分から放出させることができる。
昆虫の系では、オートグラファカリフォルニカ(Autographa californica)核多核体病ウイルス(AcNPV)を、外来遺伝子を発現するベクターとして使用する。そのウイルスは、スポドプテラフルギペルダ(Spodoptera frugiperda)細胞中で増殖する。抗体コード配列をウイルスの非必須領域(例えば、ポリへドリン遺伝子)中に個々にクローン化し、AcNPVプロモーター(例えば、ポリへドリンプロモーター)の調節下に置くことができる。
哺乳動物宿主細胞では、ウイルスに基づくいくつかの発現系を利用することができる。アデノウイルスを発現ベクターとして使用する場合では、対象とする抗体コード配列を、アデノウイルス転写/翻訳調節複合体、例えば、後期プロモーターおよびトリパータイトリーダー配列と連結することができる。次いで、このキメラ遺伝子を、in vitroまたはin vivo組換えによってアデノウイルスゲノム中に挿入することができる。ウイルスゲノムの非必須領域(例えば、E1またはE3領域)中に挿入すると、生存可能であり、感染した宿主中で免疫グロブリン分子を発現することができる組換えウイルスが生じる(例えば、Logan & Shenk, 1984, Proc. Natl. Acad. Sci. USA 81:355-359を参照されたい)。特定の開始シグナルが、挿入された抗体コード配列の効率のよい翻訳に必要となる可能性もある。これらのシグナルは、ATG開始コドンおよび隣接する配列を含む。さらに、開始コドンは、挿入物全体が確実に翻訳されるために、所望のコード配列の読み枠を有する相になければならない。これらの外因性翻訳調節シグナルおよび開始コドンは、天然でも合成でも様々な由来のものでよい。発現の効率は、適当な転写エンハンサーエレメント、転写終結因子などを含めることによって高めることができる(Bittner et al., 1987, Methods in Enzymol. 153:51-544を参照されたい)。
さらに、挿入された配列の発現を調節し、または所望される特定の形で遺伝子産物を修飾およびプロセシングする宿主細胞株を選択することができる。タンパク質産物のそのような修飾(例えば、グリコシル化)およびプロセシング(例えば、切断)は、タンパク質の機能に重要である可能性がある。異なる宿主細胞は、タンパク質および遺伝子産物の翻訳後プロセシングおよび修飾について特徴および特定の機構を有する。発現される外来タンパク質の正しい修飾およびプロセシングが確実に行われるように、適当な細胞系統または宿主系を選択することができる。この目的のために、一次転写物の適切なプロセシング、グリコシル化、および遺伝子産物のリン酸化の細胞機構を有する真核宿主細胞を使用することができる。そのような哺乳動物宿主細胞には、それだけに限らないが、CHO、VERY、BHK、Hela、COS、MDCK、293、293T、3T3、WI38、BT483、Hs578T、HTB2、BT20およびT47D、CRL7030およびHs578Bstがある。
組換えタンパク質の長期にわたる高収量の産生のために、安定した発現が好ましい。例えば、本発明の抗体を安定して発現する細胞系統を工学的に改変することができる。ウイルスの複製起点を含む発現ベクターを使用するのではなく、適当な発現調節エレメント(例えば、プロモーター、エンハンサー、配列、転写終結因子、ポリアデニル化部位など)によって調節されたDNA、および選択マーカーで宿主細胞を形質転換することができる。外来DNAの導入後、工学的改変細胞を濃縮培地中で1〜2日間増殖させることができ、次いで選択培地に切り換える。組換えプラスミド中の選択マーカーは、選択に対する耐性を付与し、細胞がその染色体中にプラスミドを組み込み、それを増殖させてフォーカスを形成することを可能にし、そのフォーカスをクローン化し細胞系統中で増殖させることができる。有利には、この方法を使用して、本発明の抗体を発現する細胞系統を工学的に改変することができる。そのような工学的改変細胞系統は、本発明の抗体と直接的にまたは間接的に相互作用する化合物のスクリーニングおよび評価で特に有用である可能性がある。
それだけに限らないが、単純ヘルペスウイルスチミジンキナーゼ(Wigler et al., 1977, Cell 11: 223)、ヒポキサンチン-グアニンホスホリボシル転移酵素(Szybalska & Szybalski, 1992, Proc. Natl. Acad. Sci. USA 48: 202)、およびアデニンホスホリボシル転移酵素(Lowy et al., 1980, Cell 22: 817)遺伝子を含めたいくつかの選択系を使用することができ、これらの遺伝子はtk-、hgprt-またはaprt-細胞でそれぞれ使用することができる。また、代謝拮抗物質耐性を下記の遺伝子の選択の基礎として使用することもできる: メトトレキセートに対する耐性を付与するdhfr(Wigler et al., 1980, Proc. Natl. Acad. Sci. USA 77:357; O'Hare et al., 1981, Proc. Natl. Acad. Sci. USA 78: 1527); ミコフェノール酸に対する耐性を付与するgpt(Mulligan & Berg, 1981, Proc. Natl. Acad. Sci. USA 78: 2072); アミノグリコシドG-418に対する耐性を付与するneo(Clinical Pharmacy 12: 488-505; Wu and Wu, 1991, 3:87-95; Tolstoshev, 1993, Ann. Rev. Pharmacol. Toxicol. 32:573-596; Mulligan, 1993, Science 260:926-932; およびMorgan and Anderson, 1993, Ann. Rev. Biochem. 62:191-217; May, 1993, TIB TECH 11(5):155-215); およびハイグロマイシンに対する耐性を付与するhygro(Santerre et al., 1984, Gene 30:147)。使用することができる、組換えDNA技術の分野で一般に知られている方法は、Ausubel et al. (eds.), 1993, Current Protocols in Molecular Biology, John Wiley & Sons, NY; Kriegler, 1990, Gene Transfer and Expression, A Laboratory Manual, Stockton Press, NY; およびChapters 12 and 13, Dracopoli et al. (eds), 1994, Current Protocols in Human Genetics, John Wiley & Sons, NY.; Colberre-Garapin et al., 1981, J. Mol. Biol. 150:1に記載されている。
ベクター増幅によって、本発明の抗体の発現レベルを増大することができる(総説については、Bebbington and Hentschel, The use of vectors based on gene amplification for the expression of cloned genes in mammalian cells in DNA cloning, Vol. 3 (Academic Press, New York, 1987)を参照されたい)。抗体を発現するベクター系中のマーカーが増幅可能であるとき、宿主細胞の培養物中に存在する阻害剤のレベルを増大すると、マーカー遺伝子のコピー数が増大する。増幅した領域が抗体のヌクレオチド配列を伴うので、抗体の産生も増大する(Crouse et al., 1983, Mol. Cell. Biol. 3:257)。
宿主細胞に、第1のベクターが重鎖由来ポリペプチドをコードし、第2のベクターが軽鎖由来ポリペプチドをコードする本発明の2つの発現ベクターを同時にトランスフェクトすることができる。2つのベクターは、重鎖および軽鎖ポリペプチドの同等の発現を可能にする同一の選択マーカーを含んでよい。あるいは、重鎖と軽鎖のどちらのポリペプチドもコードする単一のベクターを使用することもできる。そのような状況では、軽鎖を重鎖の前に置いて、過剰な毒性遊離重鎖を回避すべきである(Proudfoot, 1986, Nature 322:52; Kohler, 1980, Proc. Natl. Acad. Sci. USA 77:2197)。重鎖および軽鎖のコード配列は、cDNAを含んでもよく、あるいはゲノムDNAを含んでもよい。
本発明の分子(すなわち、抗体)を組換えによって発現させた後、ポリペプチドまたは抗体の精製について当技術分野で知られている任意の方法によって、例えば、クロマトグラフィー(例えば、イオン交換クロマトグラフィー、アフィニティークロマトグラフィー、具体的にはプロテインAの後の特定の抗原についての親和性によるクロマトグラフィー、およびサイジングカラムクロマトグラフィー)、遠心分離、示差的溶解性(differential solubility)によって、あるいはポリペプチドまたは抗体の精製についての任意の他の標準的な技術によってそれを精製することができる。
6.5 予防方法および治療方法
エフェクター機能活性が付与および/または改変された本発明の分子は、FcγRによって媒介されるエフェクター細胞機能(例えば、ADCC)の効率の増強が望ましい(例えば、癌、感染症)、疾患、障害または感染を治療および/または予防するため、またその効果がエフェクター機能活性、例えばADCCによって媒介される治療用抗体の治療効果を増強する上で特に有用である。
本発明は、対象の癌を治療、予防または管理するための方法および組成物を包含し、この方法および組成物は、対象に、本発明に従って工学的に改変された変異型重鎖を含む治療上有効量の1つまたは複数の分子を投与することを含み、この分子は癌抗原にさらに結合する。変異型重鎖を含む本発明の分子は、原発腫瘍の増殖または退行、癌細胞の転移および感染症の予防、抑制、低減に特に有用である。ある特定の作用機序によって縛られることを意図しないが、本発明の分子は、腫瘍排除の割合の増強または腫瘍減少の割合の増強またはその組合せをもたらす抗体媒介性エフェクター機能を増強することにより癌治療の有効性を増強する。代替の実施形態では、本発明の改変された抗体は、オリゴマー化活性を本発明の変異型重鎖のFc領域に付与して細胞表面抗原および/または受容体の架橋および増強されたアポトーシスまたは負の増殖調節性シグナル伝達をもたらすことにより、癌治療の有効性を増強する。
本発明の態様によれば、本発明による重鎖を改変して免疫治療薬の抗体エフェクター機能活性、例えば、ADCC、CDC、食作用、オプソニン作用などの効力を付与または増大させることにより免疫治療薬を増強してもよい。特定の実施形態では、腫瘍細胞または感染細胞の抗体依存性細胞毒性および/または食作用は、免疫治療薬を本発明の変異型重鎖で改変することによって増強される。本発明の分子は、少なくとも1つの抗体媒介性エフェクター機能活性を増強することにより、免疫療法処置の有効性を増強することもできる。特定の一実施形態では、免疫療法処置の有効性は、補体依存性カスケードを増強することにより増強される。本発明の別の実施形態では、免疫療法処置の有効性は、標的とされる細胞、例えば腫瘍細胞の食作用および/またはオプソニン作用を増強することにより増強される。本発明の別の実施形態では、この処置の有効性は、標的とされる細胞、例えば腫瘍細胞の破壊において抗体依存性細胞性細胞傷害(「ADCC」)を増強することにより増強される。本発明の分子は、患者において治療効果を有さない、または患者の亜集団において治療効果を有する抗体を作製することもできる。
ある特定の作用機序によって縛られることを意図しないが、本発明に従って工学的に改変された治療用抗体は、一部は、変異型重鎖のFc部分が、特定のFcγRを低下したレベルで発現する標的細胞に結合できることにより、例えば、FcγR相互作用に対する改善された解離速度により、抗体がより長く標的細胞上にとどまることができることに基づいて、増強された治療効力を有する。
FcγRに対する親和性および結合活性が増強された本発明の抗体は、対象の癌または別の疾患もしくは障害の治療、予防または管理に特に有用であり、FcγRは、標的細胞集団において低レベルで発現される。本明細書では、細胞中でのFcγR発現は、当業者に知られている一般的な方法を使用して測定される、細胞当たりのこのような分子の密度に関して定義される。変異型重鎖を含む本発明の分子はまた、好ましくは、30,000から20,000分子/細胞の密度で、20,000から10,000分子/細胞の密度で、10,000分子/細胞以下の密度で、5000分子/細胞以下の密度で、または1000分子/細胞以下の密度で標的抗原、例えば癌抗原を発現する細胞において付与または増強された結合活性および親和性および/またはエフェクター機能を有する。本発明の分子は、亜集団の癌などの疾患または障害の治療、予防または管理において特定の有用性を有し、標的抗原は、標的細胞集団内で低レベルで発現される。
本発明の分子はまた、癌、自己免疫疾患、炎症性障害、感染性疾患などの疾患の治療または予防のために、当技術分野で知られている他の治療剤と組み合わせて有利に利用することができる。特定の実施形態では、本発明の分子は、例えば、分子と相互作用するエフェクター細胞の数または活性を増大させる役割を果たし、免疫応答を増大させる、モノクローナル抗体またはキメラ抗体、リンホカイン、または造血成長因子(例えば、IL-2、IL-3およびIL-7など)と組み合わせて用いることができる。本発明の分子はまた、例えば、以下の節5.4.1.2および5.4.2.1に詳述されている、例えば抗癌剤、抗炎症剤または抗ウイルス剤などの、疾患、障害または感染を治療するために用いられる、1種または複数の薬物と組み合わせて有利に利用することができる。
6.5.1 癌
本発明は、治療上有効量の、変異型Fc領域を含む1種または複数の分子を対象に投与することを含む、対象における癌の治療または予防のための方法および組成物を包含する。いくつかの実施形態では、本発明は、FγRIIIA-158VまたはFcγRIIIA-158F対立遺伝子にとってホモ接合性であるものなどのFcγR多型を有する対象における、癌の治療または予防のための方法および組成物を包含する。いくつかの実施形態では、本発明は、治療用抗体、例えば、腫瘍特異的モノクローナル抗体を、工学的に改変された抗体が、FcγRIIIA(158F)の低親和性対立遺伝子にとってホモ接合性である患者において増強された効力を有するように、本発明の方法によって工学的に改変することを包含する。他の実施形態では、本発明は、治療用抗体、例えば、腫瘍特異的モノクローナル抗体を、工学的に改変された抗体が、FcγRIIIA(158V)の高親和性対立遺伝子にとってホモ接合性である患者において増強された効力を有するように、本発明の方法によって工学的に改変することを包含する。
モノクローナル抗体の効力は、対象のFcγR多型に依存し得る(ともに、その全体が参照により本明細書に組み込まれている、Carton et al., 2002 Blood, 99: 754-8; Weng et al., 2003 J Clin Oncol.21(21):3940-7)。これらの受容体は、エフェクター細胞の表面上で発現され、ADCCを媒介する。低親和性活性化受容体の、高親和性対立遺伝子は、エフェクター細胞の、ADCCを媒介する能力を改善する。本発明の方法は、Fc突然変異を有する分子を工学的に改変させることによって、その改変されたFcドメインを介してエフェクター細胞上のFcγRに対する親和性を増強する。本発明の工学的に改変された抗体により、患者のFcγR多型に関わらず、患者にとってより良好な免疫療法用試薬が提供される。
本発明に従って工学的に改変された変異型重鎖を有する分子は、培養細胞系または患者由来PMBC細胞のいずれかを使用してADCCによって試験して、Fc突然変異がADCCを増強できることを決定する。本明細書に開示した方法を用いて、標準的なADCCを行う。リンパ球を、Ficoll-Paque勾配(Pharmacia)を用いて末梢血から採取する。標的細胞、すなわち培養細胞系または親由来細胞に、ユーロピウム(PerkinElmer)を添加し、エフェクターとともに37℃で4時間インキュベートする。放出されたユーロピウムを、蛍光プレートリーダー(Wallac)を用いて検出する。得られるADCCデータは、NK細胞媒介性細胞傷害を誘発する、Fc変異体の効力を示し、どのFc変異体を、患者試料および水簸した単球の両方で試験することができるかを明らかにする。次いで、分子の効力を増強する最大の潜在性を示すFc変異体を、患者からのPBMCを用いるADCCアッセイで試験する。健康なドナーからのPBMCは、エフェクター細胞として用いる。
本発明の態様によれば、変異型重鎖を含む本発明の分子は、抗体エフェクター機能、例えば、ADCC、CDC、食作用、オプソニン作用などの潜在性を付与する、または、野生型Fc領域を含有する分子と比べて増大させることによって、免疫療法の効力を増強する。特定の実施形態では、抗体依存性細胞毒性および/または腫瘍細胞の食作用は、変異型重鎖を有する本発明の分子を用いて付与または増強される。本発明の分子は、少なくとも1つの抗体媒介性エフェクター機能を付与または増強することによって、免疫療法の癌治療の効力を増強することができる。特定の一実施形態では、変異型重鎖を含む本発明の分子は、補体依存性カスケードを増強することによって、免疫療法治療の効力を付与または増強する。本発明の別の実施形態では、変異型重鎖を含む本発明の分子は、標的腫瘍細胞の食作用および/またはオプソニン作用を付与または増強することによって、免疫療法治療の効力を増強する。本発明の別の実施形態では、変異型重鎖を含む本発明の分子は、標的腫瘍細胞の破壊における抗体依存性細胞媒介性細胞傷害(「ADCC」)を増強することによって、治療の効力を付与または増強する。
本発明はさらに、例えば、治療用抗体のエフェクター機能(例えば、ADCC)を増強すること、またはエフェクター機能(in vitroまたはin vivoアッセイにおいて少なくとも検出可能)を有さない治療用抗体にエフェクター機能を付与することにより、治療用抗体の治療効力を増強するために、治療用抗体(例えば、腫瘍特異的モノクローナル抗体)を工学的に改変することを企図する。治療用抗体は、細胞傷害抗体および/またはオプソニン化抗体であることが好ましい。所望の結合特性を有する本発明の分子(例えば、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む分子であって、この改変は、比較可能な分子と比べて(すなわち、同一のアイソタイプのFc領域を有する野生型重鎖と比べて)FcγRIIIAおよび/またはFcγRIIAに対する変異型重鎖のFc領域の親和性を増強する分子)が、本発明の方法に従って同定されると(セクション5.2および表9参照)、治療用抗体は、セクション5.1に記載の通り、標準的な組換えDNA技術および任意の既知の変異誘発技術を用いて工学的に改変して、所望の結合特性を伴う同定された突然変異点を有する、工学的に改変された治療剤を製造できることが当業者によって理解されよう。癌治療における治療有用性を実証した、表23に記載の任意の治療用抗体は、本発明の方法に従って、例えば、同一のアイソタイプのFc領域を含む野生型重鎖を有する治療用抗体と比較して、エフェクター機能を付与する、またはFcγRIIIAおよび/またはFcγRIIAに対する増強された親和性を有するように変異型重鎖のドメインまたは領域を改変することによって工学的に改変することができ、癌抗原によって特徴付けられる癌の治療およびまたは予防に用いることができる。他の治療用抗体には、肺炎連鎖球菌血清型6Bに対するものなどの、病原性因子に対するものが含まれ、例えば、Sun et al., 1999, Infection and Immunity, 67(3): 1172-9を参照されたい。
本発明の重鎖変異体は、本明細書に開示したもの、または他のポリペプチドの臨床候補、すなわち臨床試験において承認された重鎖またはその部分(例えば、Fc領域)を含む分子、または本発明の重鎖変異体、およびそのヒト化型、親和性成熟型、改変型もしくは工学改変型から恩恵を受けることのできる任意の他の分子などの治療用抗体中に組み込むことができる。
本発明はまた、それだけに限らないが、ENBRELを含めた、治療有用性を有する重鎖またはその領域を含む任意の他のポリペプチドを、そのようなポリペプチドの治療効力を増強するために、本発明の方法に従って、例えば、エフェクター機能を誘発するのに必要な重鎖またはその領域(例えば、Fc領域)を含むポリペプチドのエフェクター機能を増強することによって工学的に改変することを包含する。
したがって、本発明は、癌抗原に結合し、細胞傷害であり、親治療用抗体よりも高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合し、かつ/または親抗体によって検出不可能に媒介される、または親抗体よりも効果的に1つまたは複数のエフェクター機能(例えば、ADCC、食作用)を媒介するように、本発明によって、Fc領域の1つまたは複数の部位で改変された治療用抗体を用いて、癌抗原を特徴とする癌を予防または治療する方法を提供する。別の実施形態では、本発明は、癌抗原に結合し、細胞傷害であり、親治療用抗体よりも高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合し、低い親和性でFcγRIIBに結合し、かつ/または親抗体により検出可能に媒介されない、または親抗体よりも有効に1つまたは複数のエフェクター機能(例えば、ADCC、食作用)を媒介するように、本発明によって工学的に改変された治療用抗体を用いて、癌抗原を特徴とする癌を予防または治療する方法を提供する。本発明によって工学的に改変された治療用抗体は、増強された細胞傷害活性(例えば、腫瘍細胞死滅の増強および/もしくは増強された、例えばADCC活性またはCDC活性)を有するので、癌の予防または治療に有用である。
癌抗原に関係する癌は、癌抗原に結合し、細胞傷害であり、例えば、増強されたエフェクター機能を有するように、本発明の方法によって工学的に改変された治療用抗体の投与によって治療または予防することができる。特定の一実施形態では、本発明の方法によって工学的に改変された治療用抗体は、特定の癌抗原に向けられた抗体の、抗体媒介性細胞傷害効果を増強する。例えば、限定の目的ではなく、以下の癌抗原に関係する癌は、本発明の方法および組成物によって、治療または予防することができる:KS1/4全癌腫抗原(Perez and Walker, 1990, J. Immunol. 142:32-37; Bumal, 1988, Hybridoma 7(4):407-415)、卵巣癌抗原(CA125)(Yu et al., 1991, Cancer Res. 51(2):48-475)、前立腺酸性ホスフェート(Tailor et al., 1990, Nucl. Acids Res. 18(1):4928)、前立腺特異抗原(Henttu and Vihko, 1989, Biochem. Biophys. Res. Comm. 10(2):903-910; Israeli et al., 1993, Cancer Res. 53:227-230)、黒色腫関連抗原p97(Estin et al., 1989, J. Natl. Cancer Instit. 81(6):445-44)、黒色腫抗原gp75(Vijayasardahl et al., 1990, J. Exp. Med. 171(4):1375-1380)、高分子量黒色腫抗原(HMW-MAA)(Natali et al., 1987, Cancer 59:55-3; Mittelman et al., 1990, J. Clin. Invest. 86:2136-2144))、前立腺特異膜抗原、癌胎児抗原(CEA)(Foon et al., 1994, Proc. Am. Soc. Clin. Oncol. 13:294)、多形性上皮ムチン抗原、ヒト乳脂肪小球抗原、直腸結腸腫瘍関連抗原、例えば:CEA、TAG-72 (Yokata et al., 1992, Cancer Res. 52:3402-3408)、CO17-1A (Ragnhammar et al., 1993, Int. J. Cancer 53:751-758); GICA 19-9(Herlyn et al., 1982, J. Clin. Immunol. 2:135)、CTA-1およびLEAなど、バーキットリンパ腫抗原-38.13、CD19(Ghetie et al., 1994, Blood 83:1329-1336)、ヒトB-リンパ腫抗原-CD20(Reff et al., 1994, Blood 83:435-445)、CD33(Sgouros et al., 1993, J. Nucl. Med. 34:422-430)、黒色腫特異抗原、例えば、ガングリオシドGD2(Saleh et al., 1993, J.Immunol., 151, 3390-3398)、ガングリオシドGD3(Shitara et al., 1993, Cancer Immunol. Immunother. 36:373-380)、ガングリオシドGM2(Livingston et al., 1994, J. Clin. Oncol. 12:1036-1044)、ガングリオシドGM3(Hoon et al., 1993, Cancer Res. 53:5244-5250)など、腫瘍特異移植型の細胞表面抗原(TSTA)、例えば、T-抗原DNA腫瘍ウイルスおよびRNA腫瘍ウイルスのエンベロープ抗原を含めたウイルス誘導腫瘍抗原など、癌胎児性抗原-α-フェトプロテイン、例えば、大腸のCEA、膀胱腫瘍癌の胎児性抗原(Hellstrom et al., 1985, Cancer. Res. 45:2210-2188)など、分化抗原、例えば、ヒト肺癌抗原L6、L20(Hellstrom et al., 1986, Cancer Res. 46:3917-3923)など、線維肉腫の抗原、ヒト白血病T細胞抗原-Gp37(Bhattacharya-Chatterjee et al., 1988, J. of Immun. 141:1398-1403)、ネオグリコプロテイン、スフィンゴ脂質、乳癌抗原、例えば、EGFR(上皮成長因子受容体)、HER2抗原(p185HER2)、多形性上皮ムチン(PEM)(Hilkens et al., 1992, Trends in Bio. Chem. Sci. 17:359)など、悪性ヒトリンパ球抗原-APO-1(Bernhard et al., 1989, Science 245:301-304)、分化抗原(Feizi, 1985, Nature 314:53-57)、例えば、致死的エルトロサイト(erthrocyte)および初期内胚葉において発見されたI抗原、胃のアデンカルシノーマ(adencarcinoma)において発見されたI(Ma)、乳房上皮において発見されたM18およびM39、骨髄細胞中に発見されたSSEA-1、直腸結腸癌において発見されたVEP8、VEP9、Myl、VIM-D5、およびD156-22、結腸腺癌において発見されたTRA-1-85(血液型H)、C14、肺腺癌において発見されたF3、胃癌において発見されたAH6、胚性癌細胞中に発見されたYハプテン、Ley、A431細胞中に発見されたTL5(血液型A)、EGF受容体、膵癌において発見されたE1系(血液型B)、胚性癌細胞、胃腺癌において発見されたFC10.2、腺癌において発見されたCO-514(血液型Lea)、腺癌において発見されたNS-10、結腸腺癌において発見されたCO-43(血液型Leb)、G49、EGF受容体、(血液型ALeb/Ley)、大腸癌、胃癌のムチンにおいて発見された19.9、骨髄細胞中に発見されたT5A7、黒色腫において発見されたR24、胚性癌細胞中に発見された4.2、GD3、D1.1、OFA-1、GM2、OFA-2、GD2、M1:22:25:8、ならびに4〜8細胞期の胚において発見されたSSEA-3、SSEA-4など。別の実施形態では、抗原は、皮膚T細胞リンパ腫からのT細胞受容体誘導ペプチドである(Edelson, 1998, The Cancer Journal 4:62を参照)。
本発明の方法および組成物によって治療または予防することのできる癌および関連した障害として、それだけに限らないが、以下のものが挙げられる:それだけに限らないが、急性白血病、急性リンパ球性白血病、急性骨髄球性白血病、例えば、骨髄芽球性白血病、前骨髄球性白血病、骨髄単球性白血病、単球性白血病、赤白血病および骨髄異形成症候群など、慢性白血病、例えば、それだけに限らないが、慢性骨髄球性(顆粒球性)白血病、慢性リンパ球性白血病など、ヘアリーセル白血病を含めた白血病;真性多血症;リンパ腫、例えばそれだけに限らないが、ホジキン疾患、非ホジキン疾患など;多発性骨髄腫、例えばそれだけに限らないが、くすぶり型多発性骨髄腫、非分泌性骨髄腫、骨硬化性骨髄腫、形質細胞性白血病、孤立性形質細胞腫および髄外性形質細胞腫など;ワルデンシュトレームマクログロブリン血症;意味未確定の単クローン性高ガンマグロブリン血症;良性単クローン性高ガンマグロブリン血症;重鎖病;骨および結合組織の肉腫、例えばそれだけに限らないが、骨肉腫(bone sarcoma)、骨肉腫(osteosarcoma)、軟骨肉腫、ユーイング肉腫、悪性巨細胞腫、骨の線維肉腫、脊索腫、骨膜肉腫、軟部組織肉腫、血管肉腫(angiosarcoma)(血管肉腫(hemangiosarcoma))、線維肉腫、カポジ肉腫、平滑筋肉腫、脂肪肉腫、リンパ管肉腫、神経鞘腫、横紋筋肉腫、滑膜肉腫など;それだけに限らないが、神経膠腫、星細胞腫、脳幹神経膠腫、上衣細胞腫、乏突起細胞腫、非グリア腫瘍、聴神経鞘腫、頭蓋咽頭腫、髄芽腫、髄膜腫、松果体細胞腫、松果体芽細胞腫、原発性脳リンパ腫を含めた脳腫瘍;それだけに限らないが、腺癌、小葉(小細胞)癌、乳管癌、乳房の髄様癌、乳房の粘液癌、管状乳癌、乳頭乳癌、パジェット病、および炎症性乳癌を含めた乳癌;それだけに限らないが、フェオクロモシトム(pheochromocytom)および副腎皮質癌を含めた副腎癌;甲状腺癌、例えばそれだけに限らないが、乳頭様または濾胞性甲状腺癌、髄様甲状腺癌および未分化甲状腺癌など;それだけに限らないが、膵島細胞腺腫、ガストリン産生腫瘍、グルカゴン産生腫瘍、VIP産生腫瘍、ソマトスタチン分泌腫瘍、およびカルチノイド腫瘍または膵島細胞腫瘍を含めた膵癌;それだけに限らないが、クッシング病、プロラクチン分泌腫瘍、先端巨大症、および尿崩症を含めた下垂体癌;それだけに限らないが、眼の黒色腫、例えば、虹彩黒色腫、脈絡膜黒色腫、および毛様体黒色腫など、ならびに網膜芽細胞腫を含めた眼癌;それだけに限らないが、扁平上皮癌、腺癌、および黒色腫を含めた膣癌;それだけに限らないが、扁平上皮癌、黒色腫、腺癌、基底細胞癌、肉腫、およびパジェット病を含めた外陰癌;それだけに限らないが、扁平上皮癌、および腺癌を含めた子宮頸癌;それだけに限らないが、子宮内膜癌および子宮肉腫を含めた子宮癌;それだけに限らないが、上皮性卵巣癌、境界型腫瘍、胚細胞腫瘍、および間質腫瘍を含めた卵巣癌;それだけに限らないが、扁平上皮癌、腺癌、腺様シクティック(cyctic)癌, 粘表皮癌, 腺扁平上皮癌、肉腫、黒色腫、形質細胞腫、疣状癌、および燕麦細胞(小細胞)癌を含めた食道癌;それだけに限らないが、腺癌、菌状(ポリープ状)、潰瘍性、表層拡大型、びまん性拡大型、悪性リンパ腫、脂肪肉腫、線維肉腫、および癌肉腫を含めた胃癌;大腸癌;直腸癌;それだけに限らないが、肝細胞癌および肝芽腫を含めた肝癌;それだけに限らないが、腺癌を含めた胆嚢癌;それだけに限らないが、パピラリー(pappillary)、小結節性、およびびまん性を含めた胆管癌;それだけに限らないが、非小細胞肺癌、扁平上皮癌(類表皮癌)、腺癌、大細胞癌および小細胞肺癌を含めた肺癌;それだけに限らないが、胚腫瘍、精上皮腫、未分化、古典的(典型的)、精母細胞、非セミノーム性、胎児性癌、奇形腫癌、絨毛癌(卵黄嚢腫瘍)を含めた精巣癌、それだけに限らないが、腺癌、平滑筋肉腫、および横紋筋肉腫を含めた前立腺癌;ペナル(penal)癌;それだけに限らないが、扁平上皮癌を含めた口腔癌;基底癌;それだけに限らないが、腺癌、粘表皮癌、および腺様嚢胞癌を含めた唾液腺癌;それだけに限らないが、扁平上皮癌、および疣状を含めた咽頭癌;それだけに限らないが、基底細胞癌、扁平上皮癌および黒色腫、表層拡大型黒色腫、小結節性黒色腫、悪性黒子黒色腫、肢端黒子型黒色腫を含めた皮膚癌;それだけに限らないが、腎細胞癌、腺癌、副腎腫、線維肉腫、移行上皮癌(腎盂および/またはウテレル(uterer))を含めた腎癌;ウィルムス腫瘍;それだけに限らないが、移行上皮癌、扁平上皮癌、腺癌、癌肉腫を含めた膀胱癌。さらに、癌には、粘液肉腫、骨原性肉腫、内皮肉腫、リンパ管内皮肉腫、中皮腫、滑膜腫、血管芽腫、上皮癌、嚢胞腺癌、気管支原性癌、汗腺癌、脂腺癌、乳頭様癌および乳頭様腺癌が含まれる(このような障害の総説に関して、Fishman et al., 1985, Medicine, 2d Ed., J.B. Lippincott Co., Philadelphia and Murphy et al., 1997, Informed Decisions: The Complete Book of Cancer Diagnosis, Treatment, and Recovery, Viking Penguin, Penguin Books U.S.A., Inc., United States of Americaを参照されたい)。
したがって、本発明の方法および組成物は、以下のものを含めた(それだけに限らないが)様々な癌または他の異常増殖性疾患の治療または予防にも有用である: 膀胱、乳房、大腸、腎臓、肝臓、肺、卵巣、膵臓、胃、前立腺、頸部、甲状腺および皮膚の癌を含めた癌;扁平上皮癌を含めて;白血病、急性リンパ球性白血病、急性リンパ芽球性白血病、B細胞リンパ腫、T細胞リンパ腫、バーキットリンパ腫を含めたリンパ系統の造血系腫瘍;急性および慢性骨髄性白血病ならびに前骨髄球性白血病を含めた骨髄系統の造血系腫瘍; 線維肉腫およびラブドミオスカルコマ(rhabdomyoscarcoma)を含めた間葉系由来の腫瘍;黒色腫、精上皮腫、テトラトカルシノーマ(tetratocarcinoma)、神経芽細胞腫および神経膠腫を含めた他の腫瘍; 星細胞腫、神経芽細胞腫、神経膠腫、およびシュワン腫を含めた中枢および末梢神経系の腫瘍;線維肉腫、ラブドミオスカラマ(rhabdomyoscarama)、および骨肉腫を含めた間葉系由来の腫瘍;ならびに黒色腫、キセノデルマ ペグメントスム(xenoderma pegmentosum)、角化棘細胞腫、精上皮腫、濾胞性甲状腺癌および奇形癌を含めた他の腫瘍。アポトーシスにおける異常によって生じる癌も、本発明の方法および組成物によって治療されるだろうことも企図されている。そのような癌として、それだけに限らないが、濾胞性リンパ腫、p53突然変異を伴う癌、乳房、前立腺および卵巣のホルモン依存性腫瘍、ならびに家族性大腸腺腫症、および骨髄異形成症候群などの前癌病変を挙げることができる。特定の実施形態では、卵巣、膀胱、乳房、大腸、肺、皮膚、膵臓、または子宮における、悪性腫瘍または異常増殖変化(異形成および形成異常など)、または過剰増殖障害は、本発明の方法および組成物によって治療または予防される。他の特定の実施形態では、肉腫、黒色腫、または白血病は、本発明の方法および組成物によって治療または予防される。
特定の実施形態では、本発明の分子(例えば、変異型重鎖を含む抗体、または本発明の方法によって工学的に改変された治療モノクローナル抗体)は、癌細胞の増殖を、本発明の前記分子の不在下での癌細胞の増殖と比べて、少なくとも99%、少なくとも95%、少なくとも90%、少なくとも85%、少なくとも80%、少なくとも75%、少なくとも70%、少なくとも60%、少なくとも50%、少なくとも45%、少なくとも40%、少なくとも45%、少なくとも35%、少なくとも30%、少なくとも25%、少なくとも20%、または少なくとも10%抑制または低減する。
特定の実施形態では、本発明の分子(例えば、本発明の方法に従って工学的に改変された変異型重鎖を含む抗体、または治療用モノクローナル抗体)は、細胞を死滅させる、または親分子よりも少なくとも5%、少なくとも10%、少なくとも20%、少なくとも25%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも60%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%または少なくとも100%高く癌細胞の増殖を抑制または低下させる。
6.5.1.1 併用療法
本発明はさらに、それだけに限らないが、現在標準的で実験的な化学療法、ホルモン療法、生物療法、免疫療法、放射線療法、または外科手術を含めた、癌または感染症の治療または予防について当業者に知られている他の療法と組み合わせて、本発明の分子を投与することを包含する。いくつかの実施形態では、本発明の分子は、治療または予防的有効量の1種または複数の抗癌剤、治療用抗体、または癌の治療および/または予防について当業者に知られている他の薬剤(節5.5.1.2を参照)と組み合わせて投与することができる。
ある実施形態では、本発明の1種または複数の分子は、癌の治療に有用な1種または複数の治療剤と同時的に、哺乳動物、好ましくはヒトに投与される。「同時的に」という用語は、予防剤または治療剤を正確に同時に投与することに限定されるのではなく、むしろ本発明の分子および他の薬剤を、順にかつ本発明の分子が、他の薬剤とともに作用して、それらが別の方法で投与される場合よりも増大した利点を提供できるような時間間隔内で哺乳動物に投与されることを意味する。例えば、それぞれの予防剤または治療剤(例えば、化学療法、放射線療法、ホルモン療法または生物療法)は、同時に、または異なる時点で任意の順序で経時的に投与することができるが、同時に投与されない場合、それらは、所望の治療または予防効果をもたらすように十分に接近した時間に投与されるべきである。それぞれの治療剤は、別々に、任意の適切な形態で、および任意の適当な経路によって投与することができる。様々な実施形態では、予防剤または治療剤は、1時間未満ずらして、約1時間ずらして、約1時間から約2時間ずらして、約2時間から約3時間ずらして、約3時間から約4時間ずらして、約4時間から約5時間ずらして、約5時間から約6時間ずらして、約6時間から約7時間ずらして、約7時間から約8時間ずらして、約8時間から約9時間ずらして、約9時間から約10時間ずらして、約10時間から約11時間ずらして、約11時間から約12時間ずらして、24時間以内ずらして、または48時間以内ずらして投与される。好ましい実施形態では、同じ患者来診において2種以上の成分が投与される。
他の実施形態では、予防剤または治療剤は、約2から4日ずらして、約4から6日ずらして、約1週間ずらして、約1から2週間ずらして、または2週間を超えてずらして投与される。好ましい実施形態では、予防剤または治療剤は、両方の薬剤が依然として活性である期間中に投与される。当業者は、投与された薬剤の半減期を決定することによって、そのような期間を決定することができるだろう。
ある実施形態では、本発明の予防剤または治療剤は、対象に周期的に投与される。サイクリング療法は、一時期に第1の薬剤の投与、続いて一時期に第2の薬剤および/または第3の薬剤の投与、およびこの経時的投与を繰り返すことを伴う。サイクリング療法により、1つまたは複数の療法に対する耐性発現を低減し、療法の1つの副作用を回避または低減し、かつ/または治療の効力を改善することができる。
ある実施形態では、予防剤または治療剤は、約3週間未満のサイクル、2週間毎に約1回、10日毎に約1回または毎週約1回投与される。1つのサイクルは、サイクル毎に約90分、サイクル毎に約1時間、サイクル毎に約45分にわたる注入による、治療剤または予防剤の投与を含むことができる。それぞれのサイクルは、少なくとも1週間の休止、少なくとも2週間の休止、少なくとも3週間の休止を含むことができる。投与されるサイクルの数は、約1から約12サイクル、さらに典型的には約2から約10サイクル、さらに典型的には約2から約8サイクルである。
さらに他の実施形態では、本発明の治療剤および予防剤は、連続注入または長期の休止期間のない頻回投与のいずれかによって、規則正しい投与計画で投与される。このような規則正しい投与は、休止期間のない一定間隔での投与を含むことができる。典型的には、治療剤、特に細胞傷害剤は、低用量で用いられる。このような投与計画は、長期間の比較的低用量の長期連日投与を包含する。好ましい実施形態では、低用量の使用により、有毒副作用を最小限にし、休止期間を省くことができる。ある実施形態では、治療剤および予防剤は、約24時間から約2日まで、約1週間まで、約2週間まで、約3週間まで、約1ヵ月まで、約2ヵ月まで、約3ヵ月まで、約4ヵ月まで、約5ヵ月まで、約6ヵ月までの範囲の長期低用量または連続注入によって送達される。このような投与計画の計画作成は、熟練した腫瘍医によって最適化することができる。
他の実施形態では、治療の複数のコースが同時的に哺乳動物に投与され、すなわち個々の用量の治療剤は、別々だが、本発明の分子が、他の薬剤または複数の薬剤とともに作用することができるような時間間隔内で投与される。例えば、1つの成分は、2週間毎に1回または3週間毎に1回投与することのできる他の成分と組み合わせて1週間当たり1回投与することができる。言い換えれば、治療剤の投与計画は、治療剤が同時に投与されなくても同時的に、または同じ患者来診の間に行われる。
他の予防剤および/または治療剤と組み合わせて用いられる場合、本発明の分子および予防剤および/または治療剤は、相加的にまたはより好ましくは相乗的に作用することができる。一実施形態では、本発明の分子は、同じ医薬組成物中の1種または複数の治療剤と同時的に投与される。別の実施形態では、本発明の分子は、別々の医薬組成物における1種または複数の治療剤と同時的に投与される。さらに別の実施形態では、本発明の分子は、別の予防剤または治療剤の投与の前または後に投与される。本発明は、同じまたは異なる投与経路、例えば経口および非経口によって、他の予防剤または治療剤と組み合わせて本発明の分子を投与することを企図する。ある実施形態では、本発明の分子が、それだけに限らないが、毒性を含めた有害副作用を潜在的に生じる別の予防剤または治療剤と同時的に投与される場合、その予防剤または治療剤は、有害副作用が誘発される閾値より下に当たる用量で有利に投与することができる。
本明細書で提供される投与量および投与頻度は、治療上有効および予防上有効という用語によって包含される。投与量および頻度はさらに、投与される特定の治療剤または予防剤、癌の重症度および種類、投与経路、ならびに患者の年齢、体重、応答および過去の病歴に応じた、それぞれの患者にとって特定の要因によって一般に変動するだろう。適当な投与計画は、そのような要因を考慮することにより、および以下の例えば、文献に報告され、Physician's Desk Reference (56th ed., 2002)に勧告されている投与量により、当業者によって選択することができる。
6.5.1.2 他の治療剤/予防剤
特定の実施形態では、本発明の方法は、癌の治療および/または予防に用いられる1種または複数の治療剤とともに、1種または複数の本発明の分子を投与することを包含する。一実施形態では、血管新生阻害剤を本発明の分子と組み合わせて投与することができる。本発明の方法および組成物に用いることのできる血管新生阻害剤として、それだけに限らないが、アンジオスタチン(プラスミノーゲン断片);抗血管新生アンチトロンビンIII;アンギオザイム(angiozyme);ABT-627; Bay 12-9566;ベネフィン;ベバシズマブ;BMS-275291;軟骨由来阻害剤(CDI);CAI;CD59補体断片;CEP-7055;Col 3;コンブレタスタチンA-4;エンドスタチン(コラーゲンXVIII断片);フィブロネクチン断片;Gro-β;ハロフギノン;ヘパリナーゼ;ヘパリンヘキササッカリド断片;HMV833;ヒト絨毛性ゴナドトロピン(hCG);IM-862;インターフェロンα/β/γ;インターフェロン誘導性タンパク質(IP-10);インターロイキン-12;クリングル5(プラスミノーゲン断片);マリマスタット;メタロプロテイナーゼ阻害剤(TIMPs);2-メトキシエストラジオール;MMI 270(CGS 27023A);MoAb IMC-1C11;ネオバスタット;NM-3;パンゼム;PI-88;胎盤リボヌクレアーゼ阻害剤;プラスミノーゲン活性化因子阻害剤;血小板因子-4(PF4);プリノマスタット;プロラクチン16kD断片;プロリフェリン関連タンパク質(PRP);PTK 787/ZK 222594;レチノイド;ソリマスタット(solimastat);スクアラミン;SS 3304;SU 5416;SU6668;SU11248;テトラヒドロコルチゾール-S;テトラチオモリブデート;サリドマイド;トロンボスポンジン-1(TSP-1);TNP-470;トランスフォーミング増殖因子-β(TGF-b);バスクロスタチン(vasculostatin);バソスタチン(カルレティキュリン断片);ZD6126;ZD 6474;ファルネシルトランスフェラーゼ阻害剤(FTI);およびビスホスホネートが挙げられる。
本発明の医薬組成物および剤形およびキットを含めた、本発明の様々な実施形態において、本発明の分子と組み合わせて用いることのできる抗癌剤として、それだけに限らないが、アシビシン;アクラルビシン;塩酸アコダゾール;アクロニン;アドゼレシン;アルデスロイキン;アルトレタミン;アンボマイシン(ambomycin);酢酸アメタントロン;アミノグルテチミド;アムサクリン;アナストロゾール;アントラマイシン;アスパラギナーゼ;アスペルリン(asperlin);アザシチジン;アゼテパ(azetepa);アゾトマイシン(azotomycin);バチマスタット;ベンゾデパ;ビカルタミド;塩酸ビサントレン;ビスナフィドジメシラート;ビセレシン;硫酸ブレオマイシン;ブレキーナルナトリウム;ブロピリミン;ブスルファン;カクチノマイシン;カルステロン;カラセミド;カルベチマー;カルボプラチン;カルムスチン;塩酸カルビシン(carubicin hydrochloride);カルゼレシン;セデフィンゴール;クロランブシル;シロレマイシン(cirolemycin);シスプラチン;クラドリビン;クリスナトールメシレート;シクロホスファミド;シタラビン;ダカルバジン;ダクチノマイシン;塩酸ダウノルビシン;デシタビン;デキソルマプラチン;デザグアニン;デザグアニンメシレート;ジアジクォン;ドセタキセル;ドキソルビシン;塩酸ドキソルビシン;ドロロキシフェン;クエン酸ドロロキシフェン;プロピオン酸ドロモスタノロン;ズアゾマイシン(duazomycin);エダトレキサート;塩酸エフロールニチン;エルサミトルシン(elsamitrucin);エンロプラチン;エンプロメート(enpromate);エピプロピジン;塩酸エピルビシン;エルブロゾール(erbulozole);塩酸エソルビシン(esorubicin hydrochloride);エストラムスチン;リン酸エストラムスチンナトリウム;エタニダゾール; エトポシド;リン酸エトポシド;エトプリン(etoprine);塩酸ファドロゾール;ファザラビン;フェンレチニド;フロクスウリジン;リン酸フルダラビン;フルオロウラシル;フルロシタビン;ホスキドン;ホストリエシンナトリウム;ゲムシタビン;塩酸ゲムシタビン;ヒドロキシ尿素;塩酸イダルビシン;イホスファミド;イルモホシン;インターロイキンII(組換えインターロイキンII、すなわちrIL2を含めて)、インターフェロンα-2a;インターフェロンα-2b;インターフェロンα-n1;インターフェロンα-n3;インターフェロンβ-Ia;インターフェロンγ-Ib;イプロプラチン;塩酸イリノテカン;酢酸ランレオチド;レトロゾール;酢酸ロイプロリド;塩酸リアロゾール; ロメトレキソールナトリウム;ロムスチン;塩酸ロソキサントロン;マソプロコール;マイタンシン;塩酸メクロレタミン;酢酸メゲストロール;酢酸メレンゲストロール;メルファラン;メノガリル;メルカプトプリン;メトトレキセート;メトトレキセートナトリウム;メトプリン(metoprine);メツレデパ;ミチンドミド;ミトカルシン(mitocarcin);ミトクロミン;マイトジリン(mitogillin);ミトマルシン(mitomalcin);マイトマイシン;ミトスペル(mitosper);ミトタン;塩酸ミトキサントロン;ミコフェノール酸;ノコダゾール;ノガラマイシン;オルマプラチン;オキシスラン;パクリタキセル;ペガスパルガーゼ;ペリオマイシン(peliomycin);ペンタムスチン(pentamustine);硫酸ペプロマイシン;ペルホスフアミド(perfosfamide);ピポブロマン;ピポスルファン;塩酸ピロキサントロン;プリカマイシン;プロメスタン;ポルフィマーナトリウム;ポルフィロマイシン;プレドニムスチン(prednimustine);塩酸プロカルバジン;ピューロマイシン;塩酸ピューロマイシン;ピラゾフリン;リボプリン;ログレチミド;サフィンゴール;塩酸サフィンゴール;セムスチン;シムトラゼン;スパルフォセートナトリウム;スパルソマイシン;塩酸スピロゲルマニウム;スピロムスチン;スピロプラチン;ストレプトニグリン;ストレプトゾシン;スロフェヌル;タリソマイシン;テコガランナトリウム(tecogalan sodium);テガフール;塩酸テロキサントロン;テモポルフィン;テニポシド;テロキシロン;テストラクトン;チアミプリン;チオグアニン;チオテパ;チアゾフリン;チラパザミン;クエン酸トレミフェン;酢酸トレストロン(trestolone acetate);リン酸トリシリビン;トリメトレキセート;グルクロン酸トリメトレキセート;トリプトレリン;塩酸ツブロゾール;ウラシルマスタード;ウレデパ;バプレオチド;ベルテポルフィン;硫酸ビンブラスチン;硫酸ビンクリスチン;ビンデシン;硫酸ビンデシン;硫酸ビネピジン(vinepidine sulfate);硫酸ビングリシナート(vinglycinate sulfate); 硫酸ビンロイロシン(vinleurosine sulfate);酒石酸ビノレルビン;硫酸ビンロシジン(vinrosidine sulfate);硫酸ビンゾリジン(vinzolidine sulfate);ボロゾール;ゼニプラチン;ジノスタチン;塩酸ゾルビシンが挙げられる。他の抗癌薬として、それだけに限らないが、20-epi-1,25 ジヒドロキシビタミンD3;5-エチニルウラシル;アビラテロン;アクラルビシン;アシルフルベン;アデシペノール(adecypenol);アドゼレシン;アルデスロイキン;ALL-TKアンタゴニスト;アルトレタミン;アンバムスチン;アミドクス(amidox);アミホスチン;アミノレブリン酸;アムルビシン;アムサクリン;アナグレリド;アナストロゾール;アンドログラホリド;血管新生阻害剤;アンタゴニストD;アンタゴニストG;アンタレリクス(antarelix);抗背方化形態形成タンパク質-1;抗アンドロゲン、前立腺癌;抗エストロゲン剤;アンチネオプラストン;アンチセンスオリゴヌクレオチド;アフィディコリングリシナート;アポトーシス遺伝子モジュレーター;アポトーシスレギュレーター;アプリン酸;ara-CDP-DL-PTBA;アルギニンデアミナーゼ;アスラクリン(asulacrine);アタメスタン;アトリムスチン;アキシナスタチン(axinastatin)1;アキシナスタチン2;アキシナスタチン3;アザセトロン;アザトキシン(azatoxin);アザチロシン;バッカチンIII誘導体;バラノール;バチマスタット;BCR/ABLアンタゴニスト;ベンゾクロリン;ベンゾイルスタウロスポリン;βラクタム誘導体;β-アレチン(alethine);ベタクラマイシン(betaclamycin)B;ベツリン酸;bFGF阻害剤;ビカルタミド;ビサントレン;ビスアジリジニルスペルミン;ビスナフィド;ビストラテン(bistratene)A;ビセレシン;ブレフラート(breflate);ブロピリミン;ブドチタン;ブチオニンスルホキシイミン;カルシポトリオール;カルホスチンC;カンプトテシン誘導体;カナリア痘IL-2;カペシタビン;カルボキサミド-アミノ-トリアゾール;カルボキシアミドトリアゾール;CaRest M3;CARN 700;軟骨由来阻害剤;カルゼレシン;カゼインキナーゼ阻害剤(ICOS);カスタノスペルミン;セクロピンB;セトロレリクス;クロルルンス(chlorlns);クロロキノキサリンスルホンアミド;シカプロスト;シス-ポルフィリン;クラドリビン;クロミフェン類似体;クロトリマゾール;コリスマイシン(collismycin)A;コリスマイシンB;コンブレタスタチンA4;コンブレタスタチン類似体;コナゲニン;クランベスシジン(crambescidin)816;クリスナトール;クリプトフィシン8;クリプトフィシンA誘導体;キュラシンA;シクロペンタントラキノン;シクロプラタム(cycloplatam);シペマイシン(cypemycin);シタラビンオクホスフェート(ocfosfate);細胞溶解因子;サイトスタチン(cytostatin);ダクリキシマブ(dacliximab);デシタビン;デヒドロジデムニン(dehydrodidemnin)B;デスロレリン;デキサメタゾン;デキシホスファミド(dexifosfamide);デキスラゾキサン;デキスベラパミル(dexverapamil);ジアジクォン;ジデムニンB;ジドックス(didox);ジエチルノルスペルミン;ジヒドロ-5-アザシチジン;ジヒドロタキソール,9-;ジオキサマイシン(dioxamycin);ジフェニルスピロムスチン;ドセタキセル;ドコサノール;ドラセトロン;ドキシフルリジン;ドロロキシフェン;ドロナビノール;デュオカルマイシンSA;エブセレン;エコムスチン;エデルホシン; エドレコロマブ;エフロールニチン;エレメン;エミテフール;エピルビシン;エプリステリド;エストラムスチン類似体;エストロゲンアゴニスト;エストロゲンアンタゴニスト;エタニダゾール;リン酸エトポシド;エキセメスタン;ファドロゾール;ファザラビン;フェンレチニド;フィルグラスチム;フィナステリド;フラボピリドール;フレゼラスチン;フルアステロン(fluasterone);フルダラビン;塩酸フルオロダウノルニシン(fluorodaunorunicin hydrochloride);ホルフェニメクス;フォルメスタン;ホストリエシン;ホテムスチン;ガドリニウムテキサフィリン;硝酸ガリウム;ガロシタビン;ガニレリクス;ゼラチナーゼ阻害剤;ゲムシタビン;グルタチオン阻害剤;ヘプスルファム(hepsulfam);ヘレグリン;ヘキサメチレンビスアセトアミド;ヒペリシン;イバンドロン酸;イダルビシン;イドキシフェン;イドラマントン;イルモホシン;イロマスタット;イミダゾアクリドン(imidazoacridone);イミキモド;免疫賦活ペプチド;インスリン様成長因子-1受容体阻害剤;インターフェロンアゴニスト;インターフェロン;インターロイキン;イオベングアン;ヨードドキソルビシン;イポメアノール, 4-;イロプラクト(iroplact);イルソグラジン;イソベンガゾール(isobengazole);イソホモハリコンドリン(isohomohalicondrin)B;イタセトロン;ジャスプラキノリド;カハラリド(kahalalide)
F;ラメラリン-Nトリアセテート;ランレオチド;レイナマイシン;レノグラスチム;硫酸レンチナン;レプトルスタチン(leptolstatin);レトロゾール;白血病抑制因子;白血球αインターフェロン;ロイプロリド+エストロゲン+プロゲステロン;リュープロレリン;レバミソール;リアロゾール;直鎖ポリアミン類似体;親油性ジサッカライドペプチド;親油性白金化合物;リソクリンアミド(lissoclinamide)7;ロバプラチン;ロンブリシン(lombricine);ロメトレキソール;ロニダミン;ロソキサントロン;ロバスタチン;ロキソリビン;ルルトテカン(lurtotecan);ルテチウムテキサフィリン;リソフィリン(lysofylline);溶解ペプチド;マイタンシン;マンノスタチン(mannostatin)A;マリマスタット;マソプロコール;マスピン;マトリライシン阻害剤;基質メタロプロテイナーゼ阻害剤;メノガリル;メルバロン;メテレリン(meterelin);メチオニナーゼ;メトクロプラミド;MIF阻害剤;ミフェプリストーン;ミルテホシン;ミリモスチム;ミスマッチ二重鎖RNA;ミトグアゾン;ミトラクトール;マイトマイシン類似体;ミトナフィド(mitonafide);ミトトキシン(mitotoxin)線維芽細胞成長因子-サポリン;ミトキサントロン;モファロテン;モルグラモスチム;モノクローナル抗体、ヒト絨毛性ゴナドトロピン;モノホスホリル脂質A+ミオバクテリウム(myobacterium)細胞壁sk;モピダモール;多剤耐性遺伝子阻害剤;多発性腫瘍サプレッサー1をベースとする療法(multiple tumor suppressor 1-based therapy);マスタード抗癌剤;ミカペルオキシド(mycaperoxide)B;マイコバクテリア(mycobacterial)細胞壁抽出物;ミリアポロン(myriaporone); N-アセチルジナリン;N-置換ベンズアミド;ナファレリン;ナグレスチプ(nagrestip);ナロキソン+ペンタゾシン;ナパビン(napavin);ナフテルピン;ナルトグラスチム;ネダプラチン;ネモルビシン(nemorubicin);ネリドロン酸;中性エンドペプチダーゼ;ニルタミド;ニサマイシン(nisamycin);一酸化窒素モジュレーター;ニトロキシド抗酸化剤;ニトルリン(nitrullyn);O6-ベンジルグアニン;オクトレオチド;オキセノン(okicenone);オリゴヌクレオチド;オナプリストン;オンダンセトロン;オンダンセトロン;オラシン(oracin);経口サイトカイン誘導因子;オルマプラチン;オサテロン;オキサリプラチン;オキサウノマイシン(oxaunomycin);パクリタキセル;パクリタキセル類似体;パクリタキセル誘導体;パラウアミン(palauamine);パルミトイルリゾキシン(palmitoylrhizoxin);パミドロン酸;パナキシトリオール;パノミフェン;パラバクチン(parabactin);パゼリプチン;ペガスパルガーゼ;ペルデシン;ペントサン多硫酸ナトリウム;ペントスタチン;ペントロゾール(pentrozole);ペルフルブロン;ペルホスフアミド(perfosfamide);ペリリルアルコール;フェナジノマイシン;フェニル酢酸塩;ホスファターゼ阻害剤;ピシバニール;塩酸ピロカルピン;ピラルビシン;ピリトレキシム;プラセチン(placetin)A;プラセチンB;プラスミノーゲン活性化因子阻害剤;白金錯体;白金化合物;白金-トリアミン錯体;ポルフィマーナトリウム;ポルフィロマイシン;プレドニゾン;プロピルビス-アクリドン;プロスタグランジンJ2;プロテアソーム阻害剤;タンパク質Aをベースとする免疫モジュレーター;タンパク質キナーゼC阻害剤;タンパク質キナーゼC阻害剤類、微細藻類;タンパク質チロシンホスファターゼ阻害剤;プリンヌクレオシドホスホリラーゼ阻害剤;プルプリン;ピラゾロアクリジン(pyrazoloacridine);ピリドキシル化ヘモグロビンポリオキシエチレンコンジュゲート(pyridoxylated hemoglobin polyoxyethylene conjugate);rafアンタゴニスト;ラルチトレキセド;ラモセトロン;rasファルネシルタンパク質トランスフェラーゼ阻害剤;ras阻害剤;ras-GAP阻害剤;脱メチルレテリプチン;エチドロン酸レニウム Re 186;リゾキシン;リボザイム;RII レチナミド(retinamide);ログレチミド;ロヒツキン(rohitukine);ロムルチド;ロキニメックス(roquinimex);ルビギノン(rubiginone)B1;ルボキシル(ruboxyl);サフィンゴール;サイントピン(saintopin);SarCNU;サルコフィトール(sarcophytol)A;サルグラモスチム;Sdi 1模倣剤;セムスチン;老化由来阻害剤(senescence derived inhibitor)1;センスオリゴヌクレオチド;シグナル伝達阻害剤;シグナル伝達モジュレーター;単鎖抗原結合タンパク質;シゾフィラン;ソブゾキサン;ナトリウムボロカプテート(sodium borocaptate);フェニル酢酸ナトリウム;ソルベロール(solverol);ソマトメジン結合タンパク質;ソネルミン(sonermin);スパルホス酸;スピカマイシンD;スピロムスチン;スプレノペンチン(splenopentin);スポンジスタチン(spongistatin)1;スクアラミン;幹細胞阻害剤;幹細胞分裂阻害剤;スチピアミド(stipiamide);ストロメライシン阻害剤;スルフィノシン(sulfinosine);超活性型(superactive)血管作用性小腸ペプチドアンタゴニスト;スラジスタ(suradista);スラミン;スウェインソニン;合成グリコサミノグリカン;タリムスチン;タモキシフェンメチオジド;タウロムスチン;タザロテン;テコガランナトリウム(tecogalan sodium);テガフール;テルラピリリウム(tellurapyrylium);テロメラーゼ阻害剤;テモポルフィン;テモゾロミド;テニポシド;テトラクロロデカオキシド;テトラゾミン(tetrazomine);タリブラスチン(thaliblastine);チオコラリン(thiocoraline);トロンボポエチン;トロンボポエチン模倣剤;チマルファシン;サイモポエチン受容体アゴニスト;チモトリナン;甲状腺刺激ホルモン;スズエチルエチオプルプリン(tin ethyl etiopurpurin);チラパザミン;二塩化チタノセン;トプセンチン(topsentin);トレミフェン;全能性幹細胞因子;翻訳阻害剤;トレチノイン;トリアセチルウリジン;トリシリビン;トリメトレキセート;トリプトレリン;トロピセトロン;ツロステリド;チロシンキナーゼ阻害剤;チロホスチン;UBC阻害剤;ウベニメクス;尿生殖洞由来成長阻害因子;ウロキナーゼ受容体アンタゴニスト;バプレオチド;バリオリン(variolin)B;ベクター系、赤血球遺伝子療法;ベラレソール;ベラミン(veramine);ベルジン(verdin);ベルテポルフィン;ビノレルビン;ビンキサルチン(vinxaltine);バイタクシン(vitaxin);ボロゾール;ザノテロン(zanoterone);ゼニプラチン;ジラスコルブ;およびジノスタチンスチマラマーが挙げられる。好ましいさらなる抗癌薬は、5-フルオロウラシルおよびロイコボリンである。
本発明の方法に用いることのできる治療用抗体の例として、それだけに限らないが、免疫抑制剤、急性の腎臓同種移植拒絶反応を予防するためのヒト化抗CD25モノクローナル抗体である、ZENAPAX(登録商標)(ダクリズマブ)(Roche Pharmaceuticals、スイス);マウス抗17-IA細胞表面抗原IgG2a抗体である、PANOREX(商標)(Glaxo Wellcome/Centocor); マウス抗イディオタイプ(GD3エピトープ)IgG抗体である、BEC2(ImClone System);キメラ抗EGFR IgG 抗体である、IMC-C225(ImClone System);ヒト化抗αVβ3インテグリン抗体であるVITAXIN(商標)(Applied Molecular Evolution/MedImmune);ヒト化抗CD33 IgG抗体である、Smart M195(Protein Design Lab/Kanebo);ヒト化抗CD22 IgG抗体である、LYMPHOCIDE(商標)(Immunomedics);ヒト化抗ICAM3抗体である、ICM3(ICOS Pharm);霊長類化抗CD80抗体である、IDEC-114(IDEC Pharm/Mitsubishi);ヒト化抗CD40L抗体である、IDEC-131(IDEC/Eisai);霊長類化抗CD4抗体である、IDEC-151(IDEC);霊長類化抗CD23抗体である、IDEC-152(IDEC/Seikagaku);ヒト化抗CD3 IgGである、SMART抗CD3(Protein Design Lab);ヒト化抗補体因子5(C5)抗体である、5G1.1(Alexion Pharm);ヒト化抗TNF-α抗体である、D2E7(CAT/BASF);ヒト化抗TNF-αFab断片である、CDP870(Celltech);霊長類化抗CD4 IgG1抗体である、IDEC-151(IDEC Pharm/SmithKline Beecham);ヒト抗CD4 IgG抗体であるMDX-CD4(Medarex/Eisai/Genmab);ヒト化抗TNF-α IgG4抗体である、CDP571(Celltech);ヒト化抗α4β7抗体である、LDP-02(LeukoSite/Genentech);ヒト化抗CD4 IgG抗体である、オルソクローンOKT4A(Ortho Biotech);ヒト化抗CD40L IgG抗体である、ANTOVA(商標) (Biogen); ヒト化抗VLA-4 IgG抗体である、ANTEGREN(商標)(Elan);およびヒト抗TGF-β2抗体である、CAT-152(Cambridge Ab Tech)が挙げられる。本発明によって用いることのできる治療用抗体の他の例は、表10に示されている。
6.5.2 自己免疫疾患および炎症性疾患
いくつかの実施形態では、本発明の分子は、IgG2、IgG3またはIgG4のFc領域を含む変異型重鎖を含み、1つまたは複数の領域中に同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有し、この改変は、FcγRIIBに対する変異型Fc領域の親和性を増大させるが、FcγRIIIAおよび/またはFcγRIIAに対する変異型Fc領域の親和性を低下させる。このような結合特性を有する本発明の分子は、免疫応答を制御することにおいて、例えば、自己免疫疾患または炎症性疾患に関連する免疫応答を抑制することにおいて有用である。任意の作用機序によって制約されることを意図していないが、FcγRIIBに対する増強された親和性ならびにFcγRIIIAおよび/またはFcγRIIAに対する低減された親和性を有する本発明の分子は、FcγRへの活性化応答の減衰および細胞応答性の抑制をもたらすことができる。
いくつかの実施形態では、変異型重鎖を含む本発明の分子は、免疫グロブリンではなく、少なくとも1つのアミノ酸改変を含み、この改変は、同一のアイソタイプのFc領域を有する野生型重鎖を含む分子と比べてFcγRIIBに対する変異型重鎖の親和性を増大させる。他の実施形態では、前記分子は、1つまたは複数のアミノ酸改変をさらに含み、この改変は、活性化FcγRに対する分子の親和性を低下させる。いくつかの実施形態では、分子は、可溶性(すなわち、膜結合ではない)変異型重鎖またはその部分(例えば、Fc領域)である。本発明は、本明細書に記載の通り、当業者に知られているものを含めた、様々なFc受容体に対するその親和性を調節する、可溶性変異型重鎖またはその領域内の他のアミノ酸改変を企図する。他の実施形態では、分子(例えば、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を有する変異型重鎖)を、当業者に知られており、本明細書に記載された技法を用いて改変して分子のin vivo半減期を増大させる。このような分子は、自己免疫障害を治療および/または予防することにおいて治療有用性を有する。任意の作用機序によって制約されることを意図していないが、FcγRIIBに対する増強された親和性を有するこのような分子は、活性化受容体の減衰およびしたがって免疫応答の減衰をもたらし、自己免疫障害を治療および/または予防することに対して治療効力を有するだろう。
ある実施形態では、FcγRIIBに対する変異型重鎖のFc領域の親和性を増大させるが、FcγRIIIAに対する変異型重鎖のFc領域の親和性を減少させる、1つまたは複数のアミノ酸改変は、246位でのスレオニンおよび396位でのヒスチジンによる置換;または268位でのアスパラギン酸および318位でのアスパラギン酸による置換;または217位でのセリン、378位でのバリン、および408位でのアルギニンによる置換;または375位でのシステインおよび396位でのロイシンによる置換;または246位でのイソルクシン(isolcucine)および334位でのアスパラギンによる、または247位でのロイシンによる、または372位でのチロシンによる、または326位でのグルタミン酸による、または224位でのロイシンによる置換を含む。
同一のアイソタイプのFc領域を有する野性型重鎖を含む比較可能な分子と比べて、FcγRIIBに対する増強された親和性ならびにFcγRIIIAおよび/またはFcγRIIAに対する低減された親和性を有する本発明の変異型重鎖は、自己免疫疾患または炎症性疾患を治療または予防するために用いることができる。本発明は、対象における自己免疫障害または炎症性障害に関係する1つまたは複数の症状を予防、治療または管理する方法であって、前記対象に、治療上または予防上有効量の、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて、FcγRIIBに対する増強された親和性ならびにFcγRIIIAおよびまたはFcγRIIAに対する低減された親和性を有する変異型重鎖を有する、1種または複数の本発明の分子を投与することを含む方法を提供する。
本発明は、対象における炎症性障害に関係する1つまたは複数の症状を予防、治療または管理する方法であって、前記対象に、治療上または予防上有効量の1種または複数の抗炎症剤を投与することをさらに含む方法も提供する。本発明はまた、自己免疫疾患に関係する1つまたは複数の症状を予防、治療または管理する方法であって、前記対象に、治療上または予防上有効量の1種または複数の免疫調節剤を投与することをさらに含む方法を提供する。節5.4.2.1は、抗炎症剤および免疫調節剤の限定されない例を提供する。
本発明の分子を投与することによって治療することのできる自己免疫障害の例として、それだけに限定されないが、円形脱毛症、強直性脊椎炎、抗リン脂質抗体症候群、自己免疫性アジソン病、副腎の自己免疫疾患、自己免疫性溶血性貧血、自己免疫性肝炎、自己免疫性卵巣炎および睾丸炎、自己免疫性血小板減少症、ベーチェット病、類天疱瘡、心筋症、セリアックスプルー-皮膚炎、慢性疲労免疫機能障害症候群(CFIDS)、慢性炎症性脱髄性多発ニューロパチー、チャーグ-ストラウス症候群、瘢痕性類天疱瘡、CREST症候群、寒冷凝集素病、クローン病、円板状ループス、本態性混合型クリオグロブリン血症、線維筋痛症-線維筋炎、糸球体腎炎、グレーブス病、ギランバレー、橋本甲状腺炎、特発性肺線維症、特発性血小板減少紫斑病(ITP)、IgAニューロパチー、若年性関節炎、扁平苔癬、ループスエルテマトースス(lupus erthematosus)、メニエール病、混合性結合組織疾患、多発性硬化症、1型または免疫介在性真性糖尿病、重症筋無力症、尋常性天疱瘡、悪性貧血、結節性多発性動脈炎、ポリクロンドリチス(polychrondritis)、多腺症候群、リウマチ性多発筋痛症、多発性筋炎および皮膚筋炎、原発性無ガンマグロブリン血症、原発性胆汁性肝硬変、乾癬、乾癬性関節炎、レイノー現象、ライター症候群、関節リウマチ、サルコイドーシス、強皮症、シェーグレン症候群、全身硬直症候群、全身性紅斑性狼瘡、紅斑性狼瘡、高安動脈炎、一過性アルテリスチス(arteristis)/巨細胞性動脈炎、潰瘍性大腸炎、ぶどう膜炎、疱疹状皮膚炎脈管炎(dermatitis herpetiformis vasculitis)などの脈管炎、白斑症、およびウェジナー肉芽腫症が挙げられる。炎症性障害の例として、それだけに限らないが、喘息、エンセフィリチス(encephilitis)、炎症性腸疾患、慢性閉塞性肺疾患(COPD)、アレルギー性障害、敗血症性ショック、肺線維症、未分化脊椎関節症、未分化関節症、関節炎、炎症性骨溶解、および慢性ウイルス感染または慢性バクテリア感染から生じる慢性炎症が挙げられる。本明細書の節2.2.2で述べたように、いくつかの自己免疫障害は、炎症状態に関係する。したがって、自己免疫障害と考えられているものと炎症性障害と考えられているものの間に共通部分が存在する。したがって、いくつかの自己免疫障害は、炎症性障害としても特徴付けることができる。本発明の方法によって、予防、治療または管理することのできる炎症性障害の例は、それだけに限らないが、喘息、エンセフィリチス、炎症性腸疾患、慢性閉塞性肺疾患(COPD)、アレルギー性障害、敗血症性ショック、肺線維症、未分化脊椎関節症、未分化関節症、関節炎、炎症性骨溶解、および慢性ウイルス感染または慢性バクテリア感染から生じる慢性炎症が挙げられる。
同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて、FcγRIIBに対する増強された親和性およびFcγRIIIAに対する低減された親和性を有する変異型重鎖を有する本発明の分子は、炎症性障害を有する動物、特に哺乳動物が受ける炎症を低減するために用いることもできる。特定の実施形態では、本発明の分子は、動物における炎症を、前記分子を投与されない、または親分子が投与された動物における炎症と比べて、少なくとも99%、少なくとも95%、少なくとも90%、少なくとも85%、少なくとも80%、少なくとも75%、少なくとも70%、少なくとも60%、少なくとも50%、少なくとも45%、少なくとも40%、少なくとも45%、少なくとも35%、少なくとも30%、少なくとも25%、少なくとも20%、または少なくとも10%低減する。
同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて、FcγRIIBに対する増強された親和性およびFcγRIIIAに対する低減された親和性を有する変異型重鎖を有する本発明の分子は、移植片の拒絶反応を予防するために用いることもできる。
本発明はさらに、抗体が、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子と比べて付与されたエフェクター機能および/またはFcγRIIBに対する増強された親和性およびFcγRIIIAに対する低減された親和性を有すると同定された、同一のアイソタイプのFc領域を有する野生型重鎖と比べて1つまたは複数のアミノ酸改変を含む本発明の変異型重鎖を含むように、自己免疫疾患または炎症性疾患の治療および/または予防のために、当技術分野で知られている任意の抗体を工学的に改変することを企図する。本発明によって工学的に改変することのできる、炎症性障害の治療または予防に用いられる抗体の、限定されない例を表24Aに示し、自己免疫障害の治療または予防に用いられる抗体の、限定されない例を表24Bに示す。
6.5.2.1 免疫調節剤および抗炎症剤
本発明は、FcγRIIBに対する増強された親和性ならびにFcγRIIIAおよび/またはFcγRIIAに対する低減された親和性を有する変異型重鎖を有する分子を他の治療剤とともに投与することを含む、自己免疫疾患および炎症性疾患の治療方法を提供する。免疫調節剤の例として、それだけに限らないが、メトトレキセート、ENBREL、REMICADE(商標)、レフルノミド、シクロホスファミド、シクロスポリンA、およびマクロライド系抗生物質(例えば、FK506 (タクロリムス))、メチルプレドニゾロン(MP)、コルチコステロイド、ステリオド(steriod)、ミコフェノール酸モフェチル、ラパマイシン (シロリムス)、ミゾリビン、デオキシスペルグアリン(deoxyspergualin)、ブレキナル、マロノニトリロアミンド(malononitriloaminde)(例えば、レフルナミド(leflunamide))、T細胞受容体モジュレーター、およびサイトカイン受容体モジュレーターが挙げられる。
抗炎症剤は、炎症性障害および自己免疫障害の治療において成功を示してきており、現在ではこのような障害に対する一般的で標準的な治療である。当業者に周知の任意の抗炎症剤は、本発明の方法に用いることができる。抗炎症剤の限定されない例として、非ステロイド性抗炎症薬(NSAID)、ステロイド性抗炎症薬、β-アゴニスト、抗コリン剤、およびメチルキサンチンが挙げられる。NSAIDの例として、それだけに限らないが、アスピリン、イブプロフェン、セレコキシブ(CELEBREX(商標))、ジクロフェナク(VOLTAREN(商標))、エトドラク(LODINE(商標))、フェノプロフェン(NALFON(商標))、インドメタシン(INDOCIN(商標))、ケトロラック(TORADOL(商標))、オキサプロジン(DAYPRO(商標))、ナブメントン(nabumentone)(RELAFEN(商標))、スリンダク(CLINORIL(商標))、トルメチン(TOLECTIN(商標))、ロフェコキシブ(VIOXX(商標))、ナプロキセン(ALEVE(商標)、NAPROSYN(商標))、ケトプロフェン(ACTRON(商標))およびナブメトン(RELAFEN(商標))が挙げられる。このようなNSAIDは、シクロオキシゲナーゼ酵素(例えば、COX-1および/またはCOX-2)を阻害することによって機能する。ステロイド性抗炎症薬の例として、それだけに限らないが、糖質コルチコイド、デキサメタゾン(DECADRON(商標))、コルチゾン、ヒドロコルチゾン、プレドニゾン(DELTASONE(商標))、プレドニゾロン、トリアムシノロン、アズルフィジン(azulfidine)、およびプロスタグランジンなどのエイコサノイド、トロンボキサン、およびロイコトリエンが挙げられる。
6.5.3 感染性疾患
本発明は、治療上または予防上有効量の1種または複数の本発明の分子を投与することを含む、対象における感染性疾患を治療または予防する方法を包含する。本発明の分子によって治療または予防することのできる感染性疾患は、それだけに限らないが、ウイルス、バクテリア、菌類、プロトザエ(protozae)、およびウイルスを含めた病原体に起因する。
本発明の方法とともに本発明の分子を用いて治療または予防することのできるウイルス性疾患として、それだけに限らないが、A型肝炎、B型肝炎、C型肝炎、インフルエンザ、水痘、アデノウイルス、単純ヘルペスI型 (HSV-I)、単純ヘルペスII型(HSV-II)、牛疫、ライノウイルス、エコーウイルス、ロタウイルス、呼吸器合胞体ウイルス、パピローマウイルス、パポーバウイルス、サイトメガロウイルス、エキノウイルス、アルボウイルス、フンタウイルス(huntavirus)、コクサッキーウイルス、流行性耳下腺炎ウイルス、麻疹ウイルス、風疹ウイルス、ポリオウイルス、天然痘、エプスタイン-バーウイルス、ヒト免疫不全症ウイルスI型(HIV-I)、ヒト免疫不全症ウイルスII型(HIV-II)、およびウイルスミニンギチス(viral miningitis)、脳炎、デング熱または天然痘などのウイルス性疾患の因子に起因するものが挙げられる。
バクテリアに起因する、本発明の方法とともに本発明の分子を用いて治療または予防することのできるバクテリア性疾患として、それだけに限らないが、ミコバクテリアリケッチア(mycobacteria rickettsia)、マイコプラズマ、ナイセリア、S.肺炎、ライム病菌(Borrelia burgdorferi)(ライム病)、バシラスアントラシス(Bacillus antracis) (炭疽病)、破傷風、連鎖球菌、ブドウ球菌、ミコバクテリウム、破傷風、ペルチスス(pertissus)、コレラ、ペスト、ジフテリア、クラミジア、黄色ブドウ球菌(S. aureus)およびレジオネラが挙げられる。
原虫に起因する、本発明の方法とともに本発明の分子を用いて治療または予防することのできる原虫疾患として、それだけに限らないが、リーシュマニア(leishmania)、コクジジオア(kokzidioa)、トリパノソーマ(trypanosoma)またはマラリアが挙げられる。
寄生虫に起因する、本発明の方法とともに本発明の分子を用いて治療または予防することのできる寄生虫疾患として、それだけに限らないが、クラミジアおよびリケッチアが挙げられる。
本発明の一態様によれば、変異型重鎖を含む本発明の分子は、野生型Fc領域を含む比較可能な分子と比べて、病原体、例えば、病原性タンパク質に対して増強された抗体エフェクター機能を有する。病原体の例として、それだけに限らないが、バクテリア(例えば、大腸菌(Escherichia coli)、肺炎桿菌(Klebsiella pneumoniae)、黄色ブドウ球菌(Staphylococcus aureus)、エンテロコッカスファエシアルス(Enterococcus faecials)、カンジダアルビカンス(Candida albicans)、プロテウス-ブルガリス(Proteus vulgaris)、スタフィロコッカス-ビリダンス(Staphylococcus viridans)、および緑膿菌(Pseudomonas aeruginosa))、病原体(例えば、B-リンパ球向性パポーバウイルス(LPV);百日咳菌(Bordatella pertussis);ボルナ病ウイルス(BDV);ウシコロナウイルス;脈絡髄膜炎ウイルス;デング熱ウイルス(Dengue virus);ウイルス、大腸菌(E. coli);エボラ(Ebola);エコーウイルス1;エコーウイルス-11(EV);エンドトキシン(LPS);腸内細菌;エンテリックオーファンウイルス(Enteric Orphan virus);エンテロウイルス;ネコ白血病ウイルス;口蹄疫ウイルス;ギボンサル白血病ウイルス(GALV);グラム陰性菌;ピロリ菌(Heliobacter pylori);肝炎Bウイルス(HBV);単純ヘルペスウイルス;HIV-1;ヒトサイトメガロウイルス;ヒトコロノウイルス(coronovirus); インフルエンザA、B&C;レジオネラ;メキシコリーシュマニア(Leishmania mexicana);リステリア菌(Listeria monocytogenes);麻疹ウイルス(measles virus);髄膜炎菌(meningococcus);麻疹ウイルス(morbillivirus);マウス肝炎ウイルス;マウス白血病ウイルス;マウスガンマヘルペスウイルス;マウスレトロウイルス;マウスコロナウイルスマウス肝炎ウイルス;マイコバクテリウムアビウム-M(Mycobacterium avium-M);淋菌(Neisseria gonorrhoeae);ニューカッスル病ウイルス;パルボウイルスB19;熱帯熱マラリア原虫(Plasmodium falciparum);ポックスウイルス;シュードモナス(Pseudomonas);ロタウイルス;サモネラチフィウリウム(Samonella typhiurium);赤痢菌(Shigella);連鎖球菌(Streptococci);T細胞リンパ球向性ウイルス 1;ワクチニアウイルス)が挙げられる。
特定の実施形態では、本発明の分子は、感染性疾患を生じさせる病原体の食作用および/またはオプソニン作用を増強することによって、感染性疾患の治療効力を増強する。別の特定の実施形態では、本発明の分子は、感染性疾患を生じさせる感染細胞のADCCを増強することによって、感染性疾患の治療効力を増強する。
いくつかの実施形態では、本発明の分子は、感染性疾患の治療および/または予防のために、治療上または予防上有効量の当業者に知られている1つまたはさらなる治療剤と組み合わせて投与することができる。本発明は、感染性疾患の治療およびまたは予防のために、当業者に知られている抗生物質と組み合わせた、本発明の分子の使用を企図する。本発明の分子と組み合わせて用いることのできる抗生物質として、それだけに限らないが、マクロライド(例えば、トブラマイシン(Tobi(登録商標)))、セファロスポリン(例えば、セファレキシン(Keflex(登録商標))、セフラジン(Velosef(登録商標))、セフロキシム(Ceftin(登録商標))、セフプロジル(Cefzil(登録商標))、セファクロル(Ceclor(登録商標))、セフィキシム(Suprax(登録商標))またはセファドロキシル(Duricef(登録商標)))、クラリスロマイシン(例えば、クラリスロマイシン(Biaxin(登録商標)))、エリスロマイシン (例えば、エリスロマイシン(EMycin(登録商標)))、ペニシリン(例えば、ペニシリンV(V-Cillin K(登録商標)またはPen Vee K(登録商標)))またはキノロン(例えば、オフロキサシン(Floxin(登録商標))、シプロフロキサシン(Cipro(登録商標))またはノルフロキサシン(Noroxin(登録商標)))、アミノグリコシド系抗生物質(例えば、アプラマイシン、アルベカシン、バンベルマイシン(bambermycin)、ブチロシン、ジベカシン、ネオマイシン、ネオマイシン、ウンデシレン酸塩、ネチルマイシン、パロモマイシン、リボスタマイシン、シソマイシン、およびスペクチノマイシン)、アンフェニコール(amphenicol)抗生物質(例えば、アジダムフェニコール(azidamfenicol)、クロラムフェニコール、フロルフェニコール、およびチアンフェニコール)、アンサマイシン抗生物質(例えば、リファミド(rifamide)およびリファンピン)、カルバセフェム(例えば、ロラカルベフ)、カルバペネム(例えば、ビアペネムおよびイミペネム)、セファロスポリン(例えば、セファクロル、セファドロキシル、セファマンドール、セファトリジン、セファゼドン(cefazedone)、セフォゾプラン、セフピミゾール、セフピラミド、およびセフピロム)、セファマイシン(例えば、セフブペラゾン、セフメタゾール、およびセフミノクス)、モノバクタム(例えば、アズトレオナム、カルモナム、およびチゲモナム(tigemonam))、オキサセフェム(例えば、フロモキセフ、およびモキサラクタム)、ペニシリン(例えば、アムジノシリン、アムジノシリンピボキシル、アモキシシリン、バカンピシリン、ベンジルペニシリン酸、ベンジルペニシリンナトリウム、エピシリン、フェンベニシリン(fenbenicillin)、フロキサシリン、ペナムクシリン(penamccillin)、ペネタメートヨウ化水素酸塩(penethamate hydriodide)、ペニシリンo-ベネタミン、ペニシリン0、ペニシリンV、ペニシリンV ベンザチン、ペニシリンV ヒドラバミン、ペニメピサイクリン(penimepicycline)、およびフェンシヒシリンカリウム(phencihicillin potassium))、リンコサミド(例えば、クリンダマイシン、およびリンコマイシン)、アンホマイシン、バシトラシン、カプレオマイシン、コリスチン、エンデュラシジン(enduracidin)、エンビオマイシン、テトラサイクリン(例えば、アピサイクリン(apicycline)、クロルテトラサイクリン、クロモサイクリン(clomocycline)、およびデメクロサイクリン)、2,4-ジアミノピリミジン(例えば、ブロジモプリム)、ニトロフラン(例えば、フラルタドン、および塩化フラゾリウム)、キノロンおよびその類似体(例えば、シノキサシン、クリナフロキサシン、フルメキン、およびグレパグロキサシン(grepagloxacin))、スルホンアミド(例えば、アセチルスルファメトキシピラジン、ベンジルスルファミド、ノプリルスルファミド(noprylsulfamide)、フタリルスルファセタミド、スルファクリソイジン、およびスルファシチン(sulfacytine))、スルホン(例えば、ジアチモスルホン、グルコスルホンナトリウム、およびソラスルホン)、サイクロセリン、ムピロシンおよびツベリンが挙げられる。
ある実施形態では、本発明の分子は、治療上または予防上有効量の、1種または複数の抗真菌剤と組み合わせて投与することができる。本発明の分子と組み合わせて用いることのできる抗真菌剤として、それだけに限らないが、アムホテリシンB、イトラコナゾール、ケトコナゾール、フルコナゾール、イントラテカル(intrathecal)、フルシトシン、ミコナゾール、ブトコナゾール、クロトリマゾール、ナイスタチン、テルコナゾール、チオコナゾール、シクロピロックス、エコナゾール、ハロプログリン(haloprogrin)、ナフチフィン、テルビナフィン、ウンデシレン酸塩、およびグリセオフルジン(griseofuldin)が挙げられる。
いくつかの実施形態では、本発明の分子は、治療上または予防上有効量の1種または複数の抗ウイルス剤と組み合わせて投与することができる。本発明の分子と組み合わせて用いることのできる有用な抗ウイルス剤として、それだけに限らないが、プロテアーゼ阻害剤、ヌクレオシド系逆転写酵素阻害剤、非ヌクレオシド系逆転写酵素阻害剤およびヌクレオシド類似体が挙げられる。抗ウイルス剤の例として、それだけに限らないが、ジドブジン、アシクロビル、ガングシクロビル(gangcyclovir)、ビダラビン、イドクスウリジン、トリフルリジン、およびリバビリン、ならびにフォスカーネット、アマンタジン、リマンタジン、サキナビル、インジナビル、アンプレナビル、ロピナビル、リトナビル、α-インターフェロン;アデフォビル、クレバジン(clevadine)、エンテカビル、プレコナリルが挙げられる。
6.6 ワクチン療法
本発明はさらに、それだけに限らないが、癌抗原および感染性疾患抗原(この例は以下に開示される)を含めた抗原剤または免疫原剤に対する免疫応答を誘発するために、本発明の組成物を用いることを包含する。本発明のワクチン組成物は、免疫応答が望まれる1種または複数の抗原剤または免疫原剤を含み、この1種または複数の抗原剤または免疫原剤は、FcγRIIIAに対する増強された親和性を有する本発明の変異抗体で被覆されている。特定の作用機序によって制約されることを意図していないが、抗原剤または免疫原剤を、FcγRIIIAに対する増強された親和性を有する本発明の変異抗体で被覆することにより、体液応答および細胞媒介応答を誘発することによって、所望の抗原剤または免疫原剤に対する免疫応答が増強される。本発明のワクチン組成物は、免疫応答、好ましくは抗原剤または免疫原剤に対する防御免疫応答を誘発することにおいて特に有効である。
いくつかの実施形態では、本発明のワクチン組成物中の抗原剤または免疫原剤は、免疫応答が望まれるウイルスを含む。このウイルスは、組換え型またはキメラとすることができ、弱毒化されていることが好ましい。組換え、キメラ、および弱毒性ウイルスの生成は、当業者に知られている標準的な方法を用いて行うことができる。本発明は、本発明によって製剤される、組換えウイルス生ワクチンまたは組換えウイルス不活化ワクチンを包含する。宿主における増殖は、自然感染で起こるものと同じ種類および規模の持続した刺激をもたらし、したがって実質的な長期免疫を付与するので、生ワクチンが好ましい場合がある。このような組換えウイルス生ワクチン製剤の生成は、ニワトリ胚の細胞培養物または尿膜におけるウイルスの繁殖とそれに続く精製を伴う従来の方法を用いて達成することができる。
特定の実施形態では、組換えウイルスは、それが投与される対象に対して非病原性である。この関連で、ワクチン目的のために遺伝子的に工学的に改変されたウイルスの使用は、これらの系統における弱毒性の存在を必要とする場合がある。トランスフェクションに用いられるテンプレートへの適切な突然変異(例えば、欠失)の導入は、弱毒性を有する新規なウイルスを提供することができる。例えば、温度感受性または寒冷適応に関係する特定のミスセンス突然変異は、欠失突然変異にすることができる。これらの突然変異は、寒冷または温度感受性の突然変異体に関係する点突然変異よりも安定であるはずであり、復帰突然変異の頻度は、極端に低いはずである。組換えウイルスを工学的に改変するための組換えDNA技術は、当技術分野で知られており、本発明に包含される。例えば、マイナス鎖RNAウイルスを改変する技法は、当技術分野で知られており、例えば、その全体が参照により本明細書に組み込まれている、米国特許第5,166,057号を参照されたい。
あるいは、本発明の皮内ワクチン製剤において用いるために、「自殺」性を有するキメラウイルスを構築してもよい。このようなウイルスは、宿主内で1回または数回の複製を行うのみだろう。ワクチンとして用いられる場合、この組換えウイルスは、限定された複製サイクル(複数も)を行い、十分なレベルの免疫応答を誘発するが、ヒト宿主においてはさらに進まず、疾患を引き起こさないだろう。あるいは、不活化(死滅)ウイルスを、本発明によって製剤することができる。不活化ワクチン製剤は、キメラウイルスを「死滅させる」ための従来の技法を用いて調製することができる。不活化ワクチンは、その感染力が破壊されているという意味で「死んで」いる。理想的には、ウイルスの感染力は、その免疫原性に影響することなく破壊される。不活化ワクチンを調製するために、キメラウイルスをニワトリ胚の細胞培養物または尿膜において増殖させ、ゾーン超遠心分離によって精製し、ホルムアルデヒドまたはβ-プロピオラクトンによって不活化し、プールすることができる。
ある実施形態では、他のウイルス性または非ウイルス性病原体に由来する抗原を含めて、完全に外来性のエピトープは、本発明の皮内ワクチン製剤において用いるためのウイルスに工学的に改変することができる。例えば、HIV(gp160、gp120、gp41)寄生虫抗原(例えば、マラリア)、細菌抗原または真菌抗原、あるいは腫瘍抗原などの非関連ウイルスの抗原は、弱毒系統に工学的に改変することができる。
実質的に、任意の異種遺伝子配列は、皮内ワクチン製剤において用いるための、本発明のキメラウイルスを構築することができる。好ましくは、異種遺伝子配列は、生物学的応答修飾因子として作用する部分およびペプチドである。好ましくは、任意の様々な病原体、または中和抗体に結合する抗原に対して防御免疫応答を誘発するエピトープは、キメラウイルスによって、またはキメラウイルスの一部として発現することができる。例えば、本発明のキメラウイルスに構築され得る異種遺伝子配列として、それだけに限らないが、インフルエンザならびにパラインフルエンザ赤血球凝集素ノイラミニダーゼならびにヒトPIV3のHN遺伝子およびF遺伝子などの融合糖タンパク質が挙げられる。さらに別の実施形態では、キメラウイルスに工学的に改変することのできる異種遺伝子配列には、免疫調節活性を有するタンパク質をコードするものが含まれる。免疫調節タンパク質の例として、それだけに限らないが、サイトカイン、インターフェロンタイプ1、γインターフェロン、コロニー刺激因子、インターロイキン-1、-2、-4、-5、-6、-12およびこれらの因子のアンタゴニストが挙げられる。
さらに他の実施形態では、本発明は、その表面で変異抗体を発現する、病原体細胞またはウイルス、好ましくは弱毒性ウイルスを包含する。
代替の実施形態では、本発明のワクチン組成物は、抗原剤または免疫原剤が、FcγRIIIAに対する増強された親和性を有する本発明の変異抗体に作動可能に連結している、融合ポリペプチドを含む。本発明のワクチン組成物において用いるための融合ポリペプチドの工学的改変は、通常の組換えDNA技術方法を用いて行われ、一般の技術レベル内である。
本発明はさらに、本発明の組成物を投与することによって、対象における寛容性を誘発する方法を包含する。好ましくは、対象における寛容性を誘発するのに適した組成物は、本発明の変異抗体で被覆された抗原剤または免疫原剤を含み、この変異抗体は、FcγRIIBに対するより高い親和性を有する。特定の作用機序によって制約されることを意図していないが、このような組成物は、FcγRIIB媒介阻害経路を活性化することによって寛容性を誘発することにおいて有効である。
6.7 組成物および投与方法
本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む本発明の分子(すなわち、抗体、ポリペプチド)を含む方法および医薬組成物を提供する。本発明はまた、有効量の本発明の融合タンパク質またはコンジュゲート分子、あるいは本発明の融合タンパク質またはコンジュゲート分子を含む医薬組成物を対象へ投与することによって、疾患、障害または感染に関係する1つまたは複数の症状を治療、予防、および回復する方法を提供する。好ましい態様では、抗体、融合タンパク質、またはコンジュゲート分子は、実質的に精製されている(すなわち、その効果を制限するか、または望まれない副作用を生じる物質が、実質的に存在しない)。特定の実施形態では、対象は、動物、好ましくは、非霊長類(例えば、雌ウシ、ブタ、ウマ、ネコ、イヌ、ラットなど)および霊長類(例えば、カニクイザルなどのサルおよびヒト)などの哺乳動物である。好ましい実施形態では、対象はヒトである。さらに別の実施形態では、本発明の抗体は、対象と同じ種に由来する。
様々な送達系、例えばリポソームでの被包物、微小粒子、マイクロカプセル、抗体または融合タンパク質を発現することのできる組換え細胞、受容体媒介エンドサイトーシス(例えば、Wu and Wu, 1987, J. Biol. Chem. 262:4429-4432を参照)、レトロウイルスベクターまたは他のベクターの一部としての核酸構築物などが知られており、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む本発明の分子(すなわち、抗体、ポリペプチド)を含む組成物を投与するために用いることができる。本発明の分子を投与する方法として、それだけに限らないが、非経口投与(例えば、皮内、筋肉内、腹腔内、静脈内および皮下)、硬膜外、および粘膜(例えば、鼻腔内および経口経路)が挙げられる。特定の実施形態では、本発明の分子は、筋肉内、静脈内、または皮下に投与される。この組成物は、任意の好都合な経路によって、例えば、注入または大量注射によって、上皮または粘膜皮膚の内層(例えば、口腔粘膜、直腸および腸の粘膜など)を通じた吸収によって投与することができ、他の生物活性剤とともに投与してもよい。投与は、全身的または局所的とすることができる。さらに、経肺投与も、例えば、吸入器または噴霧器の使用、およびエアロゾル化剤(aerosolizing agent)を含む製剤によって用いることができる。例えば、それぞれその全体が参照により本明細書に組み込まれている、米国特許第6,019,968号;第5,985,320号;第5,985,309号;第5,934,272号;第5,874,064号;第5,855,913号;第5,290,540号;および第4,880,078号;ならびにPCT国際公開第92/19244号;第97/32572号;第97/44013号;第98/31346号;および第99/66903号を参照されたい。
本発明は、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む本発明の分子(すなわち、抗体、ポリペプチド)が、抗体の量を表示しているアンプルまたは小袋(sachette)などの密封容器中に梱包されていることも提供する。一実施形態では、本発明の分子は、密封容器中の乾燥滅菌凍結乾燥粉末または無水濃縮物として供給され、例えば水または生理食塩水を用いて、対象への投与に適切な濃度に戻すことができる。好ましくは、本発明の分子は、少なくとも5mg、より好ましくは、少なくとも10mg、少なくとも15mg、少なくとも25mg、少なくとも35mg、少なくとも45mg、少なくとも50mg、または少なくとも75mgの単位用量で、密封容器中の乾燥滅菌凍結乾燥粉末として供給される。本発明の凍結乾燥された分子は、その当初の容器中で2と8℃の間で貯蔵されるべきであり、この分子は、元に戻された後、12時間以内、好ましくは6時間以内、5時間以内、3時間以内、または1時間以内に投与されるべきである。代替の実施形態では、本発明の分子は、分子、融合タンパク質、またはコンジュゲート分子の量および濃度を表示している密封容器中の液体形態で供給される。好ましくは、液体形態の本発明の分子は、少なくとも1mg/ml、より好ましくは、少なくとも2.5mg/ml、少なくとも5mg/ml、少なくとも8mg/ml、少なくとも10mg/ml、少なくとも15mg/kg、少なくとも25mg/ml、少なくとも50mg/ml、少なくとも100mg/ml、少なくとも150mg/ml、少なくとも200mg/mlの分子の、密封容器で供給される。
障害に関係する1つまたは複数の症状の治療、予防または回復に有効となる、本発明の組成物の量は、標準的な臨床技法によって決定することができる。製剤に用いられる正確な用量は、投与経路、および状態の重症度にも依存することになり、開業医の判断およびそれぞれの患者の状況によって決定されるべきである。有効用量は、in vitroまたは動物モデル試験系から導かれた用量-応答曲線から推定してもよい。
本発明によって包含される抗体について、患者に投与される用量は、典型的には、患者の体重1kg当たり0.0001mgから100mgである。好ましくは、患者に投与される用量は、患者の体重1kg当たり、0.0001mgと20mg、0.0001mgと10mg、0.0001mgと5mg、0.0001と2mg、0.0001と1mg、0.0001mgと0.75mg、0.0001mgと0.5mg、0.0001mgから0.25mg、0.0001から0.15mg、0.0001から0.10mg、0.001から0.5mg、0.01から0.25mgまたは0.01から0.10mgの間である。一般に、ヒト抗体は、外来性ポリペプチドに対する免疫応答のために、他の種由来の抗体よりもヒトの体内において長い半減期を有する。したがって、より少ない容量のヒト抗体およびより少ない頻度の投与が、多くの場合可能である。さらに、本発明の抗体またはその断片の投与の用量および頻度は、例えば、脂質化などの修飾により、抗体の取込みおよび組織透過性を増強することによって低減することができる。
一実施形態では、患者に投与される本発明の分子の用量は、単剤療法として用いられる場合、0.01mgから1000mg/日である。別の実施形態では、本発明の分子は、他の治療組成物と組み合わせて用いられ、患者に投与される用量は、前記分子が単剤療法として用いられる場合よりも低い。
特定の実施形態では、本発明の医薬組成物を、治療の必要のある範囲に局所的に投与することが望ましい場合があり、これは、例えば、限定の目的ではなく、局所注入によって、注射によって、またはインプラントの手段によって達成することができ、前記インプラントは、シアラスティック(sialastic)膜などの膜、または繊維を含めた、多孔質、非多孔質、またはゼラチン質材料である。好ましくは、本発明の分子を投与する場合、分子が吸収しない材料を用いることに注意しなければならない。
別の実施形態では、組成物は、小胞で、特にリポソームで送達することができる(Langer, Science 249:1527-1533 (1990); Treat et al., in Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein and Fidler (eds.), Liss, New York, pp. 353-365 (1989); Lopez-Berestein, ibid., pp. 317-327を参照されたい;一般に同書を参照されたい)。
さらに別の実施形態では、組成物は、制御放出系または徐放系で送達することができる。1種または複数の本発明の分子を含む徐放製剤を生産するために、当業者に知られている任意の技法を用いることができる。例えば、それぞれその全体が参照により本明細書に組み込まれている、米国特許第4,526,938号;PCT国際公開第91/05548;PCT国際公開第96/20698; Ning et al., 1996, "Intratumoral Radioimmunotheraphy of a Human Colon Cancer Xenograft Using a Sustained-Release Gel," Radiotherapy & Oncology 39:179-189、Song et al., 1995, "Antibody Mediated Lung Targeting of Long-Circulating Emulsions," PDA Journal of Pharmaceutical Science & Technology 50:372-397; Cleek et al., 1997, "Biodegradable Polymeric Carriers for a bFGF Antibody for Cardiovascular Application," Pro. Int'l. Symp. Control. Rel. Bioact. Mater. 24:853-854;およびLam et al., 1997, "Microencapsulation of Recombinant Humanized Monoclonal Antibody for Local Delivery," Proc. Int'l. Symp. Control Rel. Bioact. Mater. 24:759-760を参照されたい。一実施形態では、制御放出系においてポンプを用いることができる(Langer, supra; Sefton, 1987, CRC Crit. Ref. Biomed. Eng. 14:20; Buchwald et al., 1980, Surgery 88:507; and Saudek et al., 1989, N. Engl. J. Med. 321:5
74を参照)。別の実施形態では、抗体の制御放出を達成するために、ポリマー材料を用いることができる(例えば、Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Florida (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger and Peppas, 1983, J., Macromol. Sci. Rev. Macromol. Chem. 23:61;を参照。また、Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al., 1989, J. Neurosurg. 7 1:105); 米国特許第5,679,377号;米国特許第5,916,597号;米国特許第5,912,015号;米国特許第5,989,463号;米国特許第5,128,326号; PCT国際公開第99/15154号;およびPCT国際公開第99/20253号を参照)。徐放製剤において用いられるポリマーの例として、それだけに限らないが、ポリ(2-ヒドロキシエチルメタクリレート)、ポリ(メタクリル酸メチル)、ポリ(アクリル酸)、ポリ(エチレン-コ-酢酸ビニル)、ポリ(メタクリル酸)、ポリグリコリド(polyglycolide)(PLG)、ポリアンヒドリド(polyanhydride)、ポリ(N-ビニルピロリドン)、ポリ(ビニルアルコール)、ポリアクリルアミド、ポリ(エチレングリコール)、ポリラクチド(PLA)、ポリ(ラクチド-コ-グリコリド)(PLGA)、およびポリオルトエステルが挙げられる。さらに別の実施形態では、制御放出系は、治療標的(例えば、肺)の近くに配置することができ、したがって全身的用量の何分の1かが必要であるにすぎない(例えば、Goodson, in Medical Applications of Controlled Release, supra, vol. 2, pp. 115-138 (1984)を参照)。別の実施形態では、制御放出インプラントとして有用なポリマー組成物は、Dunnら(米国5,945,155を参照)に従って用いられる。この特別な方法は、ポリマー系からの生理活性物質のin situ制御放出の治療効果に基づいている。植込みは、一般に、治療処置の必要な患者の身体のどこにでも行うことができる。別の実施形態では、非ポリマー持続性送達系が用いられ、それによって、対象の身体における非ポリマーインプラントが、薬物送達系として用いられる。身体に植え込むと、インプラントの有機溶媒が、組成物から周囲の組織液に散逸、分散、または浸出し、非ポリマー材料は、徐々に凝固または凝結して固体の微孔質の基質を形成するだろう(米国5,888,533参照)。
制御放出系は、Langer (1990, Science 249:1527-1533)による総説において考察されている。1種または複数の本発明の治療剤を含む徐放製剤を生産するために、当業者に知られている任意の技法を用いることができる。例えば、それぞれその全体が参照により本明細書に組み込まれている、米国特許第4,526,938号;国際公開第91/05548号および第96/20698号; Ning et al., 1996, Radiotherapy & Oncology 39:179-189; Song et al., 1995, PDA Journal of Pharmaceutical Science & Technology 50:372-397; Cleek et al., 1997, Pro. Int'l. Symp. Control. Rel. Bioact. Mater. 24:853-854; and Lam et al., 1997, Proc. Int'l. Symp. Control Rel. Bioact. Mater. 24:759-760を参照されたい。
本発明の組成物が抗体をコードする核酸である、特定の実施形態では、核酸は、それを適切な核酸発現ベクターの一部として構築し、例えば、レトロウイルスベクターの使用(米国特許第4,980,286号を参照)により、あるいは直接注射により、あるいは微粒子照射(例えば、遺伝子銃;Biolistic, Dupont)の使用、または脂質、もしくは細胞表面受容体、もしくはトランスフェクト剤での被覆により、あるいは核に入ることが知られているホメオボックス様ペプチドに連結させて核酸を投与すること(例えば、Joliot et al., 1991, Proc. Natl. Acad. Sci. USA 88:1864-1868を参照)などにより、その核酸が細胞内になるように投与することによって、そのコードされる抗体の発現を促進するためにin vivoで投与することができる。あるいは、核酸は、相同組換えによって細胞内に導入し、発現のために宿主細胞DNA内に取り込ませることができる。
抗体について、対象に投与される治療上または予防上有効用量は、典型的には、対象の体重1kg当たり0.1mgから200mgである。好ましくは、対象に投与される用量は、対象の体重1kg当たり0.1mgと20mgの間であり、より好ましくは、対象に投与される用量は、対象の体重1kg当たり1mgから10mgの間である。本発明の抗体の投与量および投与の頻度は、例えば、脂質化などの修飾により、抗体または融合タンパク質の取込みおよび組織透過性(例えば、肺中への)を増強することによって低減することができる。
治療上または予防上有効量の本発明の分子での対象の治療は、単一治療を含むことができ、または好ましくは、一連の治療を含むことができる。好ましい例では、対象は、約1から10週間、好ましくは2から8週間、より好ましくは約3から7週間、およびさらにより好ましくは約4、5、または6週間、1週間当たり1回、体重1kg当たり約0.1から30mgの間の範囲の本発明の分子で治療される。他の実施形態では、本発明の医薬組成物は、1日1回、1日2回、または1日3回投与される。他の実施形態では、医薬組成物は、1週間に1回、1週間に2回、2週間毎に1回、1ヵ月1回、6週間毎に1回、2ヵ月毎に1回、1年に2回または1年当たり1回投与される。治療に用いられる分子の有効用量は、特定の治療の間に増減できることも理解されよう。
6.7.1 医薬組成物
本発明の組成物は、医薬組成物の製造に有用な原体薬剤組成物(例えば、不純または非滅菌組成物)および単位剤形の調製に用いることのできる医薬組成物(すなわち、対象または患者への投与に適した組成物)を含む。このような組成物は、予防または治療上有効量の本明細書に開示した予防剤および/または治療剤あるいはこれらの薬剤の組合せ、ならびに薬学的に許容される担体を含む。好ましくは、本発明の組成物は、予防または治療上有効量の1種または複数の本発明の分子および薬学的に許容される担体を含む。
特定の一実施形態では、医薬組成物は、治療上有効量の、IgG2、IgG3またはIgG4のFc領域を有する変異型重鎖を含む本発明の1つまたは複数の分子であって、前記変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子がFcγRIIIAおよび/またはFcγRIIAに結合するよりも高い親和性でFcγRIIIAおよび/またはFcγRIIAに結合し、かつ/または前記変異型重鎖は、エフェクター機能を付与する、または同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子よりも少なくとも2倍有効にエフェクター機能を媒介する分子、および薬学的に許容される担体を含む。別の実施形態では、医薬組成物は、治療上有効量の、変異型重鎖を含む本発明の1種または複数の分子であって、前記変異型重鎖のFc領域は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子がFcγRIIIAに結合するよりも高い親和性でFcγRIIIAに結合し、前記変異型重鎖は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子がFcγRIIBに結合するよりも低い親和性でFcγRIIBに結合し、かつ/または前記変異型重鎖は、同一のアイソタイプのFc領域を有する野生型重鎖を含む比較可能な分子よりも少なくとも2倍有効にエフェクター機能を媒介する分子、および薬学的に許容される担体を含む。別の実施形態では、前記医薬組成物は、1種以上の抗癌剤をさらに含む。
本発明は、本発明の重鎖における1つまたは複数のアミノ酸改変を含む、特定の癌抗原に特異的な治療用抗体(例えば、腫瘍特異的モノクローナル抗体)、および薬学的に許容される担体を含む医薬組成物を包含する。
特定の実施形態では、「薬学的に許容される」という用語は、動物における、より具体的にはヒトにおける使用のために、連邦政府または州政府の管理機関によって認可された、または米国薬局方もしくは他の一般に認知された薬局方に列挙されたことを意味する。「担体」という用語は、それとともに治療剤が投与される、希釈剤、アジュバント(例えば、フロイントアジュバント(完全および不完全)、賦形剤、またはビヒクルを指す。このような医薬担体は、水、およびラッカセイ油、大豆油、鉱油、ゴマ油などの石油、動物、野菜または合成由来の油を含めた油などの滅菌液体とすることができる。医薬組成物が静脈内に投与される場合、水は好ましい担体である。生理食塩水溶液およびデキストロース水溶液およびグリセロール溶液も、特に注射用溶液に対して液体担体として用いることができる。適当な医薬賦形剤として、デンプン、グルコース、ラクトース、スクロース、ゼラチン、麦芽、米、小麦粉、チョーク、シリカゲル、ステアリン酸ナトリウム、グリセロールモノステアレート、タルク、塩化ナトリウム、乾燥スキムミルク、グリセロール、プロピレン、グリコール、水、エタノールなどが挙げられる。必要に応じて、組成物は、少量の湿潤剤または乳化剤、またはpH緩衝剤も含むことができる。これらの組成物は、溶液、懸濁液、エマルジョン、錠剤、ピル、カプセル、粉末、徐放製剤などの形態をとることができる。
一般に、本発明の組成物の成分は、例えば、活性剤の量を表示しているアンプルまたは小袋などの密封容器中の乾燥した凍結乾燥粉末または無水濃縮物として、単位剤形で別々に、または一緒に混合して供給される。組成物が注入によって投与される場合、滅菌医薬品グレード水または生理食塩水を含有する注入ビンで分配することができる。組成物が、注射によって投与される場合、成分を投与前に混合できるように、滅菌注射用水または生理食塩水のアンプルを提供することができる。
本発明の組成物は、中性形態または塩形態で製剤することができる。薬学的に許容される塩には、それだけに限らないが、塩酸、リン酸、酢酸、シュウ酸、酒石酸などに由来するものなどの陰イオンで形成された塩、およびナトリウム、カリウム、アンモニウム、カルシウム、水酸化第二鉄、イソプロピルアミン、トリエチルアミン、2-エチルアミノエタノール、ヒスチジン、プロカインなどに由来するものなどの陽イオンで形成された塩が含まれる。
6.7.2 遺伝子治療
特定の実施形態では、本発明の分子をコードする配列を含む核酸が、遺伝子治療によって、疾患、障害または感染に関係する1つまたは複数の症状を治療、予防または回復(改善)するために投与される。遺伝子治療は、対象への発現した核酸または発現できる核酸の投与によって行われる療法を指す。本発明のこの実施形態では、核酸は、治療または予防効果を媒介する、そのコードされた抗体または融合タンパク質を産生する。
当技術分野で利用可能な遺伝子治療のための任意の方法を、本発明によって用いることができる。例示的な方法を以下に述べる。
遺伝子治療方法の一般的な総説については、Goldspiel et al., 1993, Clinical Pharmacy 12:488-505; Wu and Wu, 1991, Biotherapy 3:87-95; Tolstoshev, 1993, Ann. Rev. Pharmacol. Toxicol. 32:573-596; Mulligan, Science 260:926-932 (1993);およびMorgan and Anderson, 1993, Ann. Rev. Biochem. 62:191-217; May, 1993, TIBTECH 11(5):155-215を参照されたい。用いることのできる、組換えDNA技術の分野で一般に知られている方法は、Ausubel et al. (eds.), Current Protocols in Molecular Biology, John Wiley & Sons, NY (1993);およびKriegler, Gene Transfer and Expression, A Laboratory Manual, Stockton Press, NY (1990)に記載されている。
好ましい態様では、本発明の組成物は、抗体をコードする核酸を含み、前記核酸は、適当な宿主において抗体を発現する、発現ベクターの一部である。特に、このような核酸は、抗体コード領域に作動可能に連結したプロモーター、好ましくは異種プロモーターを有し、前記プロモーターは、誘導性または構成性、および必要に応じて組織特異的である。別の特定の実施形態では、抗体のコード配列および任意の他の所望の配列が、ゲノム中の所望の部位で相同組換えを促進する領域に隣接している核酸分子が用いられ、したがって抗体コード核酸の染色体内発現を提供する(Koller and Smithies, 1989, Proc. Natl. Acad. Sci. USA 86:8932-8935;およびZijlstra et al., 1989, Nature 342:435-438)。
別の好ましい態様では、本発明の組成物は、融合タンパク質をコードする核酸を含み、前記核酸は、適当な宿主において融合タンパク質を発現する、発現ベクターの一部である。特に、このような核酸は、融合タンパク質のコード領域に作動可能に連結したプロモーター、好ましくは異種プロモーターを有し、前記プロモーターは、誘導性または構成性、および必要に応じて組織特異的である。別の特定の実施形態では、融合タンパク質のコード配列および任意の他の所望の配列が、ゲノム中の所望の部位で相同組換えを促進する領域に隣接している核酸分子が用いられ、したがって融合タンパク質の染色体内発現を提供する。
対象への核酸の送達は、直接的(この場合、対象は、核酸または核酸保有ベクターに直接曝される)か、または間接的(この場合、細胞は最初にin vitroで核酸で形質転換され、次いで対象に移植される)のいずれであってもよい。これらの2つの手法は、それぞれin vivoまたはex vivo遺伝子治療として知られている。
特定の実施形態では、核酸配列は、in vivoで直接投与され、それが発現されることによってコードされた産物を産生する。これは、当技術分野で知られた任意の多数の方法によって、例えば、核酸配列を適切な核酸発現ベクターの一部として構築し、例えば、欠陥もしくは弱毒レトロウイルスベクターもしくは他のウイルスベクターを用いる感染(米国特許第4,980,286号)により、あるいは裸DNAの直接注射により、あるいは微粒子照射(例えば、遺伝子銃;Biolistic, Dupont)の使用、または脂質、もしくは細胞表面受容体、もしくはトランスフェクト剤での被覆、リポソーム、微小粒子、もしくはマイクロカプセルでの被包により、あるいは核に入ることが知られているペプチドに連結させて核酸配列を投与することにより、受容体媒介エンドサイトーシスを受けるリガンドに連結させて核酸配列を投与すること(例えば、Wu and Wu, 1987, J. Biol. Chem. 262:4429-4432を参照)(これは、特異的に受容体を発現する標的細胞型に用いることができる)などにより、その核酸配列が細胞内になるように投与することによって達成することができる。別の実施形態では、リガンドが、エンドソームを破壊するための膜融合ウイルスペプチドを含み、核酸がリソソーム分解するのを回避させている、核酸-リガンド複合体を形成することができる。さらに別の実施形態では、核酸は、特異的受容体を標的とすることにより、細胞特異的取込みおよび発現のためにin vivoで標的となることができる(例えば、PCT国際公開第92/06180号;92/22635号;92/20316号;93/14188号;93/20221号を参照)。あるいは、核酸は、相同組換えによって細胞内に導入し、発現のために宿主細胞DNA内に取り込ませることができる(Koller and Smithies, 1989, Proc. Natl. Acad. Sci. USA 86:8932-8935;およびZijlstra et al., 1989, Nature 342:435-438)。
特定の実施形態では、本発明の分子(例えば、抗体または融合タンパク質)をコードする核酸配列を含有するウイルスベクターが用いられる。例えば、レトロウイルスベクターを用いることができる(Miller et al., 1993, Meth. Enzymol. 217:581-599を参照)。これらのレトロウイルスベクターは、ウイルスゲノムの正確なパッケージングおよび宿主細胞DNAへの組込みのために必要な構成要素を含む。遺伝子治療に用いられる抗体または融合タンパク質をコードする核酸配列は、1つまたは複数のベクター中にクローン化され、これはヌクレオチド配列の対象へ送達を促進する。レトロウイルスベクターについてのさらに詳細は、Boesenら、(1994, Biotherapy 6:291-302)に見出すことができ、これは、幹細胞を化学療法に対してより耐性にするために、mdr 1遺伝子を造血幹細胞に送達するためのレトロウイルスベクターの使用を記載している。遺伝子治療におけるレトロウイルスベクターの使用を説明している他の文献は、Clowes et al., 1994, J. Clin. Invest. 93:644-651; Klein et al., 1994, Blood 83:1467-1473; Salmons and Gunzberg, 1993, Human Gene Therapy 4:129-141;およびGrossman and Wilson, 1993, Curr. Opin. in Genetics and Devel. 3:110-114である。
アデノウイルスは、遺伝子治療に用いることのできる他のウイルスベクターである。アデノウイルスは、遺伝子を呼吸上皮に送達するのに特に魅力的なビヒクルである。アデノウイルスは、呼吸上皮に自然に感染し、そこで軽い疾患を生じさせる。アデノウイルスベース送達系についての他の標的は、肝臓、中枢神経系、内皮細胞、および筋肉である。アデノウイルスは、非分裂細胞に感染できるという利点を有する。KozarskyおよびWilson(Current Opinion in Genetics and Development 3:499-503, 1993は、アデノウイルスベースの遺伝子治療の総説を示している。Boutら、(Human Gene Therapy, 5:3-10, 1994)は、遺伝子をアカゲザルの呼吸上皮に移行するための、アデノウイルスベクターの使用を実証した。遺伝子治療におけるアデノウイルスの使用の他の例は、Rosenfeld et al., 1991, Science 252:431-434; Rosenfeld et al., 1992, Cell 68:143-155; Mastrangeli et al., 1993, J. Clin. Invest. 91:225-234; PCT国際公開W094/12649;およびWang et al., 1995, Gene Therapy 2:775-783に見出すことができる。好ましい実施形態では、アデノウイルスが用いられる。
アデノ随伴ウイルス(AAV)も、遺伝子治療における使用に関して提唱されてきた(例えば、Walsh et al., 1993, Proc. Soc. Exp. Biol. Med. 204:289-300および米国特許第5,436,146号を参照)。
遺伝子治療への別の手法は、電気穿孔、リポフェクション、リン酸カルシウム媒介トランスフェクション、またはウイルス感染のような方法によって、遺伝子を組織培養中の細胞に移行させることを伴う。通常、移行方法は、選択可能マーカーの細胞への移行を含む。次いでこの細胞は、移行された遺伝子を取り込み、発現している細胞を単離するための選択下に置かれる。次いでこれらの細胞は、対象に送達される。
この実施形態では、得られる組換え細胞のin vivo投与の前に、核酸が細胞中に導入される。このような導入は、それだけに限らないが、トランスフェクション、電気穿孔、マイクロインジェクション、核酸配列を含有するウイルスベクターまたはバクテリオファージベクターでの感染、細胞融合、染色体媒介遺伝子導入、微小核体媒介遺伝子導入、スフェロプラスト融合などを含めた、当技術分野で知られている任意の方法によって行うことができる。外来遺伝子の細胞中への導入について、多くの技法が当技術分野で知られており(例えば、Loeffler and Behr, 1993, Meth. Enzymol. 217:599-618, Cohen et al., 1993, Meth. Enzymol. 217:618-644;およびClin. Pharma. Ther. 29:69-92, 1985を参照)、レシピエント細胞の必要な発生的および生理的機能が破壊されていないという条件で、本発明によって用いることができる。この技法は、核酸が細胞によって発現可能であり、好ましくは遺伝的であってその細胞の子孫によって発現可能であるように、核酸の細胞への安定な移行を提供すべきである。
得られる組換え細胞は、当技術分野で知られている様々な方法によって対象に送達することができる。組換え血液細胞(例えば、造血幹細胞または前駆細胞)は、静脈内に投与されることが好ましい。使用のために想定される細胞量は、所望の効果、患者の状態などに依存し、当業者によって決定することができる。
遺伝子治療の目的で核酸を導入することのできる細胞は、任意の所望の利用可能な細胞型を包含し、それだけに限らないが、上皮細胞、内皮細胞、ケラチノサイト、線維芽細胞、筋肉細胞、肝細胞; Tリンパ球、Bリンパ球、単球、マクロファージ、好中球、好酸球、巨核球、顆粒球などの血液細胞;様々な幹細胞または前駆細胞、特に骨髄、臍帯血、末梢血、胎児肝臓などから得られる造血幹細胞または造血前駆細胞を含む。
好ましい実施形態では、遺伝子治療に用いられる細胞は、対象に対して自己由来である。
遺伝子治療において組換え細胞が用いられる実施形態では、抗体または融合タンパク質をコードする核酸配列は、それらが細胞またはその子孫によって発現可能であるように細胞中に導入され、次いでこの組換え細胞は、治療効果を得るためにin vivo投与される。特定の実施形態では、幹細胞または前駆細胞が用いられる。単離し、in vitroで維持できる任意の幹細胞および/または前駆細胞は、本発明のこの実施形態によって潜在的に用いることができる(例えば、PCT国際公開第94/08598号; Stemple and Anderson, 1992, Cell 7 1:973-985; Rheinwald, 1980, Meth. Cell Bio. 21A:229;およびPittelkow and Scott, 1986, Mayo Clinic Proc. 61:771を参照)。
特定の実施形態では、遺伝子治療の目的で導入される核酸は、核酸の発現が、転写の適切な誘導因子の存在または不在を制御することによって制御可能であるように、コード領域に作動可能に連結した誘導性プロモーターを含む。
6.7.3 キット
本発明は、本発明の分子(すなわち、IgG2、IgG3またはIgG4のFc領域を含み、同一のアイソタイプのFc領域を有する野生型重鎖と比べて少なくとも1つのアミノ酸改変を有する変異型重鎖を含む抗体、ポリペプチド)で満たされた1つまたは複数の容器を含む医薬パックまたはキットを提供する。さらに、疾患の治療に有用な1種または複数の他の予防剤または治療剤も、この医薬パックまたはキットに含めることができる。本発明はまた、本発明の医薬組成物の1種または複数の成分で満たされた1つまたは複数の容器を含む医薬パックまたはキットを提供する。必要に応じてこのような容器(複数も)に、医薬品または生物学的製品の製造、使用または販売を管理する政府機関によって定められた形式での注意書を加えることができ、この注意書は、機関によるヒト投与のための製造、使用または販売の認可を反映する。
本発明は、上記方法に用いることのできるキットを提供する。一実施形態では、キットは、本発明の1種または複数の分子を含む。別の実施形態では、キットは、1つまたは複数の容器中に、癌の治療に有用な1種または複数の他の予防剤または治療剤をさらに含む。別の実施形態では、キットは、癌に関係する1種または複数の癌抗原に結合する1種または複数の細胞傷害抗体をさらに含む。ある実施形態では、他の予防剤または治療剤は、化学療法剤である。他の実施形態では、予防剤または治療剤は、生物学的治療剤またはホルモン治療剤である。
6.8 治療有用性の特徴付けおよび実証
本発明の医薬組成物、予防剤または治療剤のいくつかの態様は、好ましくは、ヒトでの使用の前に所望の治療活性について、細胞培養系において、および齧歯動物モデル系などの動物モデル生体において、in vitroで試験される。例えば、特定の医薬組成物の投与が望ましいかどうかを判定するのに用いることのできるアッセイには、患者の組織試料を培養で成長させ、本発明の医薬組成物に曝すか、または別の方法で接触させ、組織試料に対するそのような組成物の効果を観察する、細胞培養アッセイが含まれる。組織試料は、患者から生検によって得ることができる。この試験は、それぞれ個々の患者に対する、治療上最も有効な予防用または治療用分子(複数も)の同定を可能にする。様々な特定の実施形態では、in vitroアッセイは、自己免疫障害または炎症性障害に関与する細胞型の代表的な細胞(例えば、T細胞)を用いて行うことができ、本発明の医薬組成物が、そのような細胞型に対して所望の効果を有するかどうかを判定する。
予防剤および/または治療剤の組合せは、ヒトでの使用の前に、適当な動物モデル系において試験することができる。このような動物モデル系として、それだけに限らないが、ラット、マウス、ニワトリ、雌ウシ、サル、ブタ、イヌ、ウサギなどが挙げられる。当技術分野で周知の任意の動物系を用いることができる。本発明の特定の実施形態では、予防剤および/または治療剤の組合せは、マウスモデル系において試験される。このようなモデル系は、広く用いられており、当業者に周知である。予防剤および/または治療剤は、繰り返して投与することができる。この手順のいくつかの態様は、変わり得る。前記態様には、予防剤および/または治療剤を投与する時間体制、ならびにこのような薬剤が別々にまたは混合物として投与されるかどうかが含まれる。
本発明の方法に用いるのに好ましい動物モデルは、例えば、マウスエフェクター細胞上でヒトFcγRsを発現するトランスジェニックマウスであり、例えば、米国5,877,396(その全体が参照により本明細書に組み込まれている)に記載されている任意のマウスモデルを、本発明において用いることができる。本発明の方法において用いるためのトランスジェニックマウスとして、それだけに限らないが、ヒトFcγRIIIA保有マウス;ヒトFcγRIIA保有マウス; ヒトFcγRIIBおよびヒトFcγRIIIA保有マウス;ヒトFcγRIIBおよびヒトFcγRIIA保有マウスが挙げられる。
好ましくは、上述した機能アッセイにおいて最高レベルの活性を示す突然変異は、ヒトでの使用の前に、動物モデル研究において使用のための試験が行われる。ch4D5およびch520C9、2種類の抗Erb-B2抗体、およびchCC49、抗TAG72抗体を含めた、本発明の方法を用いて同定され、ADCCアッセイで試験されたFc突然変異体を有する抗体は、それらが、異種移植マウスモデルにおいて以前に用いられてきた(Hudsiak et al., 1989, Mol. Cell Biol. 9: 1165-72; Lewis et al., 1993, Cancer Immunol. Immunother. 37: 255-63; Bergman et al., 2001 Clin. Cancer Res. 7: 2050-6; Johnson et al., 1995, Anticancer Res. 1387-93)ので、動物モデルにおいて用いるのに好ましい。上述した方法を用いて、例えば、本明細書に開示し、例証した哺乳動物発現系およびIgG精製法を用いて、動物モデルにおいて用いるために、十分な量の抗体を調製することができる。
マウス異種移植モデルは、抗体分子のCDR領域の親和性および特異性ならびに抗体のFc領域の、免疫応答を誘発する能力に基づいて、腫瘍特異的標的に対して生じるマウス抗体の効力を検査するために用いることができる(Wu et al., 2001, Trends Cell Biol. 11: S2-9)。マウスエフェクター細胞上にヒトFcγRsを発現するトランスジェニックマウスは、独特であり、ヒトFc-FcγR相互作用の効力を試験するための目的にかなった動物モデルである。以下の表25に列挙したものなどの、Jeffrey Ravetch博士の研究室で生成されたFcγRIIIA、FcγRIIIBおよびFcγRIIAトランスジェニックマウス株の組(Rockefeller大学およびSloan Kettering Cancerセンターとのライセンス契約を通じて)を用いることができる。
好ましくは、FcγRIIIAに対する増強された結合およびFcγRIIBに対する低減された結合の両方を示す本発明の分子は、ADCCアッセイおよび食作用アッセイにおける活性の増大が、動物モデル実験で試験される。この動物モデル実験では、自然抗体を投与された対照と比較した、FcγRIIIAトランスジェニック、ヌードmCD16Aノックアウトマウスにおける変異型重鎖を有する抗体の効力の増大が検査される。好ましくは、8〜10匹のマウスの群が、標準的なプロトコールを用いて検査される。代表的な動物モデル実験は、以下のステップを含むことができる:乳癌モデルでは、第1日に、約2×106個のSK-BR-3細胞を、Matrigel(Becton Dickinson)と混合した0.1mLのPBSとともに皮下に注射する。最初に、野生型キメラ抗体およびアイソタイプの対照を投与することによって、所定の治療用量、第1日に4μg/gの初期用量での4D5の静脈内注射とそれに続く2μg/gの週単位の注射に対する曲線を確立する。腫瘍体積を6〜8週間モニターすることによって疾患の進行を測定する。アイソタイプの対照を注射された動物においては、腫瘍体積は時間とともに直線的に増大するはずである。対照的に、4D5を注射された群では、ほんの少しの腫瘍増殖しか起こらないはずである。標準的な用量研究からの結果は、Fc突然変異体を試験する実験についての上限を設定するために用いられる。これらの研究は、Fc突然変異体を含む抗体の治療量以下の用量を用いて行われる。FcγRIIBノックアウトマウス(Clynes et al., 2000, Nat. Med. 6: 443-6参照)において行われた実験では、10分の1の用量が異種移植モデルに対して用いられ、結果として腫瘍細胞増殖を遮断した。本発明の突然変異体は、FcγRIIIA活性化の増大およびFcγRIIB結合の低減を示すことが好ましいので、突然変異体は、10分の1の治療用量で検査される。異なる間隔での腫瘍寸法の検査により、より低い用量での抗体の効力が示される。t試験を用いるデータの統計分析は、データが有意であるかを判定する方法を提供する。効力の増大を示すFc突然変異体を、漸進的により低い用量で試験することによって、その効力の基準として最も少量の可能な用量を決定する。
本発明の併用療法の抗炎症活性は、当技術分野で知られており、Crofford L.J. and Wilder R.L., "Arthritis and Autoimmunity in Animals", in Arthritis and Allied Conditions: A Textbook of Rheumatology, McCarty et al.(eds.), Chapter 30 (Lee and Febiger, 1993)に記載されている、炎症性関節炎の様々な実験的動物モデルを用いることによって判定することができる。炎症性関節炎および自己免疫性リウマチ性疾患の実験的および自発的動物モデルは、本発明の併用療法の抗炎症活性を評価することにも用いることができる。以下のものは、例としてかつ限定によってではなく提供されるいくつかのアッセイである。
当技術分野で知られており、広く用いられている、関節炎または炎症性疾患についての主要動物モデルとして、アジュバント誘導性関節炎ラットモデル、コラーゲン誘導性関節炎ラットおよびマウスモデルならびに抗原誘導性関節炎ラット、ウサギおよびハムスターモデルが挙げられ、すべては、その全体が参照により本明細書に組み込まれている、Crofford L.J. and Wilder R.L., "Arthritis and Autoimmunity in Animals", in Arthritis and Allied Conditions: A Textbook of Rheumatology, McCarty et al.(eds.), Chapter 30 (Lee and Febiger, 1993)に記載されている。
本発明の併用療法の抗炎症活性は、カラゲナン誘導性関節炎ラットモデルを用いて評価することができる。カラゲナン誘導性関節炎は、慢性関節炎または炎症の研究において、ウサギ、イヌおよびブタにも用いられてきた。定量的組織形態計測的評価が、治療効力を判定するために用いられる。このようなカラゲナン誘導性関節炎モデルを用いるための方法は、Hansra P. et al., "Carrageenan-Induced Arthritis in the Rat," Inflammation, 24(2): 141-155, (2000)に記載されている。当技術分野で知られており、記載されているザイモサン誘導性炎症動物モデルも一般に用いられる。
本発明の併用療法の抗炎症活性は、Winter C. A. et al., "Carrageenan-Induced Edema in Hind Paw of the Rat as an Assay for Anti-inflammatory Drugs" Proc. Soc. Exp. Biol Med. 111, 544-547, (1962)に記載されている方法の改変を用いて、ラットにおけるカラゲナン誘導性足浮腫の抑制を測定することによっても評価することができる。このアッセイは、ほとんどのNSAIDの抗炎症活性のin vivoでの一次スクリーニングとして用いられてきており、ヒトの効力の予測とみなされている。試験予防剤または試験治療剤の抗炎症活性は、ビヒクルを投与された対照群と比べた、試験群の後足重量の増大の抑制率として表される。
さらに、炎症性腸疾患の動物モデルも、本発明の併用療法の効力を評価するために用いることができる(Kim et al., 1992, Scand. J. Gastroentrol. 27:529-537; Strober, 1985, Dig. Dis. Sci. 30(12 Suppl):3S-10S)。潰瘍性コリチス(cholitis)およびクローン病は、動物において誘発することのできるヒト炎症性腸疾患である。それだけに限らないが、アミロペクチン、カラギーン(carrageen)、硫酸アミロペクチン、および硫酸デキストランを含めた硫酸化多糖体、またはそれだけに限らないが、トリニトロベンゼンスルホン酸(TNBS)および酢酸を含めた化学性刺激剤は、炎症性腸疾患を誘発するために経口的に動物に投与することができる。
自己免疫障害の動物モデルも、本発明の併用療法の効力を評価するために用いることができる。1型糖尿病、甲状腺自己免疫、シテミックループスエルテマトースス(sytemic lupus eruthematosus)、および糸球体腎炎などの自己免疫障害のための動物モデルが、開発されてきた(Flanders et al., 1999, Autoimmunity 29:235-246; Krogh et al., 1999, Biochimie 81:511-515; Foster, 1999, Semin. Nephrol. 19:12-24)。
さらに、当業者に知られている任意のアッセイは、自己免疫疾患および/または炎症性疾患について、本明細書に開示した組合せ療法の予防および/または治療有用性を評価するために用いることができる。
本発明の予防および/または治療プロトコールの毒性および効力は、例えば、LD50(母集団の50%に致命的な用量)およびED50(母集団の50%に治療上有効な用量)を決定するための、細胞培養または実験動物における標準的な薬学手順によって求めることができる。毒性効果と治療効果の間の用量比は、治療指数であり、これは、比LD50/ED50として表すことができる。大きな治療指数を示す予防剤および/または治療剤が好ましい。有毒副作用を示す予防剤および/または治療剤を用いることができるが、非感染細胞への潜在的な損傷を最小限にし、それによって副作用を低減するために、そのような薬剤を患部組織部位に対する標的にする送達系を設計することに注意を払うべきである。
細胞培養アッセイおよび動物研究から得られたデータは、ヒトに用いるための予防剤および/または治療剤の投与量の範囲を処方することに用いることができる。このような薬剤の投与量は、ほとんどまたは全く毒性を含まないED50を含む循環濃度の範囲内にあることが好ましい。投与量は、用いられる剤形および利用される投与経路に応じて、この範囲内で変動してよい。本発明の方法に用いられる任意の薬剤について、治療有効用量は、最初に細胞培養アッセイから見積もることができる。用量は、細胞培養で決定されたIC50(すなわち、症状抑制の最大の半分を達成する試験化合物濃度)を含む循環血漿濃度範囲を達成するために、動物モデルにおいて処方することができる。このような情報は、ヒトにおいて有用な用量を、より正確に決定するために用いることができる。血漿の濃度は、例えば、高速液体クロマトグラフィーによって測定することができる。
本発明によって用いられる療法の抗癌活性も、当技術分野で知られており、その全体が参照により本明細書に組み込まれている、Relevance of Tumor Models for Anticancer Drug Development (1999, eds. Fiebig and Burger); Contributions to Oncology (1999, Karger); The Nude Mouse in Oncology Research (1991, eds. Boven and Winograd);およびAnticancer Drug Development Guide (1997 ed. Teicher)に記載されている、SCIDマウスモデルまたはトランスジェニックマウスまたはヒト異種移植片を有するヌードマウス、ハムスター、ウサギなどの動物モデルなどの、癌の研究用の様々な実験動物モデルを用いることによって求めることができる。
本発明の分子の治療効力を求めるための好ましい動物モデルは、マウス異種移植モデルである。異種移植腫瘍の源として用いることのできる腫瘍細胞株として、それだけに限らないが、乳腺癌を有する患者に由来し得る、SKBR3細胞およびMCF7細胞が挙げられる。これらの細胞は、erbB2およびプロラクチン受容体の両方を有する。SKBR3細胞は、ADCCおよび異種移植モデルとして、当技術分野で日常的に用いられてきた。あるいは、ヒト卵巣腺癌に由来するOVCAR3細胞を、異種移植腫瘍の源として用いることができる。
本発明のプロトコールおよび組成物は、ヒトでの使用の前に、所望の治療または予防活性について、in vitroで、次いでin vivoで試験されることが好ましい。治療剤および方法は、腫瘍または悪性細胞株の細胞を用いてスクリーニングすることができる。当技術分野で標準的な多くのアッセイを、そのような生存および/または増殖を評価するために用いることができ、例えば、細胞増殖は、3H-チミジン取込みを測定することによって、直接細胞計数によって、プロトオンコジーン(例えば、fos、myc)または細胞周期マーカーなどの既知の遺伝子の転写活性の変化を検出することによってアッセイすることができ、細胞生存率は、トリパンブルー染色によって評価することができ、分化は、形態の変化、軟寒天中の増殖および/またはコロニー形成の減少、三次元基底膜での管状ネットワーク形成または細胞外基質生成などに基づいて視覚的に評価することができる。
治療に用いるための化合物は、ヒトにおいて試験する前に、それだけに限らないが、ラット、マウス、ニワトリ、雌ウシ、サル、ウサギ、ハムスターなどを含めた適当な動物モデル系、例えば上述した動物モデルにおいて試験することができる。次いでこの化合物は、適切な臨床試験に用いることができる。
さらに、当業者に知られている任意のアッセイを、癌、炎症性障害または自己免疫疾患の治療または予防のために、本明細書に開示した組合せ療法の予防および/または治療有用性を評価するために用いることができる。
6.9 診断アッセイ
本発明は、1つまたは複数のFcγRに対する親和性および結合活性が変更された分子、例えば抗体を包含する。1つまたは複数のFcγRに対する親和性および結合活性が増強された本発明の抗体は、FcγRが低レベルで発現される細胞内システム(例えば、研究または診断の目的)において特に有用である。ある特定の作用機序によって縛られることを意図しないが、ある特定のFcγRに対する親和性および結合活性が増強された本発明の分子は、発現が低レベルであるため通常検出不可能であるFcγRの検出の感受性を増強するにより、研究および診断用ツールとして貴重である。