JP2008501802A - 医薬組成物 - Google Patents
医薬組成物 Download PDFInfo
- Publication number
- JP2008501802A JP2008501802A JP2007527639A JP2007527639A JP2008501802A JP 2008501802 A JP2008501802 A JP 2008501802A JP 2007527639 A JP2007527639 A JP 2007527639A JP 2007527639 A JP2007527639 A JP 2007527639A JP 2008501802 A JP2008501802 A JP 2008501802A
- Authority
- JP
- Japan
- Prior art keywords
- solid dispersion
- polymer
- pharmaceutical composition
- amorphous
- surfactant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/07—Tetrapeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1635—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
Description
本願は、35 USC §119(e)の下、2004年6月8日出願の米国特許仮出願番号60/578,043の優先権を主張し、その全ての内容を、引用により本明細書に包含させる。
本発明は医薬組成物に関する。
本発明者らは、結晶性VX−950と比較して、改善されたバイオアベイラビリティを有する、VX−950の形態および製剤を発見した。これらの形態および製剤は、HCV感染処置に有用である。
ある態様において、本固体分散体は約40%未満(例えば、約35%未満、約30%未満、約20%未満、約10%未満、約5%未満、または約1%未満)の結晶性VX−950を含む。例えば、ある態様において、本固体分散体は、実質的に結晶性VX−950を含まない。
ある態様において、本VX−950は実質的に純粋なL異性体である。
ある態様において、本固体分散体は噴霧乾燥により得られる。
ある態様において、本界面活性剤はラウリル硫酸ナトリウムまたはビタミンE TPGSである。
ある態様において、本医薬組成物はまた界面活性剤を、溶液中にまたはVX−950粒子の成分としてまたはその両方で含む。本界面活性剤は、例えば、SLSまたはビタミンE TPGSであり得る。
a)VX−950、ポリマー、および溶媒を含む混合物を形成させ;そして
b)該混合物を噴霧乾燥してVX−950を含む固体分散体を形成させることを含む。
ある態様において、本ポリマーが固体分散体中約30%から約70重量%の量で存在する。
a)VX−950、ポリマー(例えば、結晶化を阻害するまたは安定化するポリマー)、および溶媒の溶液を形成させ;
b)該溶液から溶媒を急速に除去して、VX−950および結晶化を阻害するポリマーを含む固体無定形分散体を形成させることを含む、
VX−950の固体分散体の製造法を提供する。ある態様において、本溶媒は噴霧乾燥により除去する。
a)VX−950、ポリマー(例えば、支持するためのポリマー、結晶化を阻害するポリマー、または安定化するポリマー)、および溶媒の混合物を形成させ;そして
b)該混合物を噴霧乾燥して、VX−950を含む固体分散体を形成させることを含む、
VX−950の固体分散体の製造法を提供する。
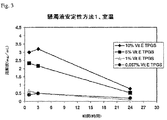
図1は、種々のVX−950組成物間の比較を記載する。
図2は、VX−950を含む種々の組成物間のラットpKの比較を記載する。
図3−6は、VX−950およびビタミンE TPGSを含む種々の懸濁液についての安定性データの比較を記載する。
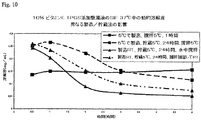
図7−10は、VX−950およびビタミンE TPGSを含む種々の懸濁液についての動的溶解度データの比較を記載する。
一般に、ラットにVX−950の微粉化した結晶性薬剤粉末を経口投与した後の絶対的バイオアベイラビリティは、0.5%未満であることが判明している。VX−950と慣用の医薬賦形剤の単純な混合物は、哺乳動物への経口投与により、類似の低いバイオアベイラビリティを示す。結晶形態のVX−950(すなわち、有意な割合のVX−950が結晶形態である)を含む組成物は、一般に、VX−950の十分な治療的有効性を提供する程度までの薬剤吸収を達成しない。ここに記載の組成物は、相対的に改善されたバイオアベイラビリティを提供する。従って、ある態様において、無定形VX−950の製剤を提供する。例えば、結晶性VX−950を含む不純物を実質的に含まない精製製剤が提供される。ある態様において、本発明は、VX−950を含む固体分散体の形の医薬組成物を含む。本発明の組成物は安定で、投与が容易であり、かつ投与によりVX−950の高いバイオアベイラビリティを与える。
無定形形態および固体分散体を得るための任意の方法が、本発明に関連して使用でき、例えば、US2003/0186952(その中で1092段落に引用の文献参照)およびUS2003/0185891に記載のものを含む。一般に、使用できる方法は、溶媒の混合物からの急速な除去または融解したサンプルの冷却を含む。このような方法は、回転蒸発、フリーズ−ドライ(すなわち、凍結乾燥)、真空乾燥、融解凝固、および融解押し出しを含むが、これらに限定されない。しかしながら、好ましい本発明の態様は、噴霧乾燥により得た無定形固体分散体を含む。従って、他の態様において、本発明は、溶媒を除去するために、得られた生成物の噴霧乾燥による乾燥を提供する。
VX−950およびポリマー(または固体状態担体)を含む固体分散体はここに包含される。
1. ポリマーのガラス遷移温度は、VX−950のガラス遷移温度より約10−15℃以上低い温度でなければならない。好ましくは、本ポリマーのガラス遷移温度は、VX−950のガラス遷移温度より高く、一般に薬剤生成物の望む貯蔵温度より少なくとも50℃高い。例えば、少なくとも約100℃、少なくとも約105℃、少なくとも約105℃、少なくとも約110℃、少なくとも約120℃、少なくとも約130℃、少なくとも約140℃、少なくとも約150℃、少なくとも約160℃、少なくとも約160℃、またはそれ以上である。
固体分散体または他の組成物は、界面活性剤を含み得る。界面活性剤または界面活性剤混合物は、一般に本固体分散体と水性媒体の間の界面張力を減少させる。適当な界面活性剤または界面活性剤混合物はまた、固体分散体からのVX−950の水溶性およびバイオアベイラビリティを高め得る。本発明と関連して使用するための界面活性剤は、ソルビタン脂肪酸エステル(例えば、Spans(登録商標))、ポリオキシエチレンソルビタン脂肪酸エステル(例えば、Tweens(登録商標))、ラウリル硫酸ナトリウム(SLS)、ドデシルベンゼンスルホン酸ナトリウム(SDBS)ジオクチルナトリウムスルホスクシネート(Docusate)、ジオキシコール酸ナトリウム塩(DOSS)、ソルビタンモノステアレート、ソルビタントリステアレート、ヘキサデシルトリメチルアンモニウムブロマイド(HTAB)、ナトリウムN−ラウロイルサルコシン、ナトリウムオレエート、ナトリウムミリステート、ナトリウムステアレート、ナトリウムパルミテート、Gelucire 44/14、エチレンジアミンテトラ酢酸(EDTA)、ビタミンE d−アルファトコフェリルポリエチレングリコール1000スクシネート(TPGS)、レシチン、MW 677−692、グルタミン酸一ナトリウム一水和物、Labrasol、PEG 8 カプリリック/カプリックグリセリド、Transcutol、ジエチレングリコールモノエチルエーテル、Solutol HS-15、ポリエチレングリコール/ヒドロキシステアレート、タウロコール酸、Pluronic F68、Pluronic F108、およびPluronic F127(または任意の他のポリオキシエチレン−ポリオキシプロピレン共ポリマー(Pluronics(登録商標))または飽和ポリグリコール化グリセリド(Gelucirs(登録商標)))を含むが、これらに限定されない。本発明と関連して使用できるこのような界面活性剤の具体例は、Span 65、Span 25、Tween 20、Capryol 90、Pluronic F108、ラウリル硫酸ナトリウム(SLS)、ビタミンE TPGS、Pluronicsおよびコポリマーを含むが、これらに限定されない。SLSおよびビタミンE TPGSが好ましい。
医薬組成物もここで提供される。本発明に従うVX−950および本固体分散体の形態は、患者に投与するための医薬組成物への製造のためにさらに加工できる。固体分散体は医薬組成物と見なし得るが、投与前にはさらなる加工が必要であるかもしれない(例えば、本固体分散体は錠剤または液体懸濁液にさらに製剤できる)。全てのこのような医薬組成物、投与形態、および医薬製剤(例えば、持続放出型または即時放出型製剤)は本発明の範囲内である。本製剤は、既知の方法に従い、既知成分を使用して製造できる(Handbook of Pharmaceutical Excipients参照)。認識される通り、経口製剤は、しばしば医薬投与に好ましい。
本発明の方法は、免疫調節剤;抗ウイルス剤;HCVプロテアーゼ阻害剤;HCVライフ・サイクルにおける他の標的の阻害剤;内部リボソーム侵入阻害剤、広域ウイルス阻害剤;他のチトクロームP−450阻害剤;またはこれらの組合せから選択される付加的薬剤を含む、他の成分の投与も含み得る。
下記成分を含む固体分散体を製造した(総重量のパーセンテージ):
下記成分を含む固体分散体を製造した(総重量のパーセンテージ):
下記成分を含む固体分散体を製造した(総重量のパーセンテージ):
経口投与製剤を下記の通り製造した。VX−950およびPVP K29/32を塩化メチレンに溶解し、次いでラウリル硫酸ナトリウムを添加し、溶液中で分散させて均質懸濁液を形成させた。この懸濁液を、90℃の入口温度および56℃の出口温度を使用して噴霧乾燥し、生成物をサイクロンから回収した。本噴霧乾燥分散体を、75℃で8時間流動床乾燥させた。
1回投与量ガラスバイアル中の1%HPMC媒体と混合した分散体を調薬した。バイアルに残った固体残渣は0.8%−4%であり、シリンジ中で水と混合して調薬したときの28%−56%と対照的であった(下記1月20日調薬)。分散体調薬は:VX950/PVPK−30/SLS(tox. lot、リフレッシュ)、VX950/HPMCAS/SLS/SDBS(5%PVPK−30含有結晶性DSから出発して、ISPで噴霧乾燥)、VX950/HPMC E15/10%Vit E TPGS、VX950/PVP−VA/10%Vit E TPGSであった。これらの試験の結果は下記に示す。
3製剤を、SD Micro噴霧乾燥機(100g)で製造した。最初の2製剤は同じ成分であるが、アセトン濃度が異なった。3番目の製剤は、HPCおよびHPMCフタレート(2:1)のポリマー混合物であった。全3製剤は1%SLSおよび1%SDBSならびに5%PVPK−30を有する薬剤物質を含んだ。
HPMCE 50/1%SLSを含む液体分散体を、下記の通りの室温または冷蔵条件下、数種の媒体中の懸濁液として、広範に調査した:
1. 1%HPMC媒体と、種々のレベルのVit E TPGS、3mg/mLのVX950濃度。
上記の全てについて、人工腸液(SIF)における37℃での動的溶解度を、製造1時間後、および上記の条件下貯蔵24時間後に評価した。
A. 1%HPMC媒体中のVit E TPGS濃度の懸濁液溶解度に対する影響を、異なる評価/貯蔵法について図3−6に証明する。
多くの本発明の態様を記載している。それにも係わらず、種々の修飾が本発明の精神および範囲から逸脱することなくなし得ることは、理解される。従って、他の態様は、添付の特許請求の範囲の範囲内である。
Claims (77)
- 無定形VX−950および第二成分を含む、組成物。
- 第二成分が界面活性剤、ポリマー、または不活性な薬学的に許容される物質である、請求項1記載の組成物。
- 該組成物が固体分散体、混合物または液体分散体を含む、請求項1記載の組成物。
- 該組成物が固体である、請求項1記載の組成物。
- 無定形VX−950を含む、固体分散体。
- 該固体分散体が約40%未満の結晶性VX−950を含む、請求項5記載の固体分散体。
- 該固体分散体が、実質的に結晶性VX−950を含まない、請求項5記載の固体分散体。
- 界面活性剤、ポリマー、または不活性な薬学的に許容される物質をさらに含む、請求項5記載の固体分散体。
- ポリマーを含み、該ポリマーが1個または1個以上の水溶性ポリマーまたは部分的に水溶性ポリマーである、請求項5記載の固体分散体。
- 該VX−950が、ポリマーの非存在下で、無定形VX−950と比較して改善された物理的または化学的安定性を有する、請求項5記載の固体分散体。
- 固体分散体がそのままの(neat)無定形VX−950のガラス遷移温度と比較して高いガラス遷移温度を有する、請求項5記載の固体分散体。
- 該VX−950が、そのままの無定形VX−950の緩和率と比較して低い緩和率を有する、請求項5記載の固体分散体。
- ポリマーを含み、該ポリマーが、固体分散体の投与後、ラットの血中のVX−950濃度が、ポリマーを含まないVX−950の投与で見られるよりも少なくとも約20%高くなるのに十分な量で存在する、請求項5記載の固体分散体。
- 対象ラットにおける血中のVX−950濃度が、ポリマーを含まないVX−950の投与で見られるよりも少なくとも約200%高い、請求項13記載の固体分散体。
- 対象ラットにおける血中のVX−950濃度が、ポリマーを含まないVX−950の投与で見られるよりも少なくとも約400%高い、請求項13記載の固体分散体。
- 該ポリマーがヒドロキシプロピルメチルセルロース(HPMC)である、請求項5記載の固体分散体。
- 該ポリマーが酢酸・コハク酸ヒドロキシプロピルメチルセルロース(HPMCAS)である、請求項5記載の固体分散体。
- 該ポリマーが約10重量%から約80重量%の量で存在する、請求項5記載の固体分散体。
- 該ポリマーが約70重量%の量で存在する、請求項18記載の固体分散体。
- 該ポリマーが約50重量%の量で存在する、請求項18記載の固体分散体。
- 該ポリマーが約49.5重量%の量で存在する、請求項18記載の固体分散体。
- 該VX−950が約10重量%から約80重量%の量で存在する、請求項5記載の固体分散体。
- 該VX−950が約70重量%の量で存在する、請求項22記載の固体分散体。
- 該VX−950が約50重量%の量で存在する、請求項22記載の固体分散体。
- 界面活性剤を含む、請求項5記載の固体分散体。
- 該界面活性剤がラウリル硫酸ナトリウムまたはビタミンE TPGSである、請求項25記載の固体分散体。
- 界面活性剤が約0.1から約15%の量で存在する、請求項25記載の固体分散体。
- 該界面活性剤が約1%から約5%の量で存在する、請求項27記載の固体分散体。
- 少なくとも約80重量%の該VX−950が無定形形態である、請求項5記載の固体分散体。
- 実質的に全ての該VX−950が無定形形態である、請求項29記載の固体分散体。
- 該VX−950がL異性体とD異性体の混合物である、請求項5記載の固体分散体。
- VX−950が実質的に純粋なL異性体である、請求項5記載の固体分散体。
- 該固体分散体が噴霧乾燥により得られる、請求項5記載の固体分散体。
- 無定形VX−950の医薬組成物。
- 該無定形VX−950が、実質的に結晶性VX−950を含まない、請求項34記載の組成物。
- 固体分散体としての無定形VX−950および1個以上の界面活性剤、ポリマー、不活性な薬学的に許容される物質、または薬学的に許容される担体を含む、医薬組成物。
- ポリマーを含み、該ポリマーが1個または1個以上の水溶性ポリマーまたは部分的に水溶性ポリマーである、請求項36記載の医薬組成物。
- 該VX−950が結晶性VX−950と比較して改善された物理的または化学的安定性を有する、請求項36記載の医薬組成物。
- 固体分散体が、そのままの無定形VX−950のガラス遷移温度よりも高いガラス遷移温度を有する、請求項36記載の医薬組成物。
- 該VX−950が、そのままの無定形VX−950の緩和率よりも低い緩和率を有する、請求項36記載の医薬組成物。
- ポリマーを含み、該ポリマーが、固体分散体の投与後、ラットの血中のVX−950濃度が、ポリマーを含まないVX−950の投与で見られるよりも少なくとも約20%高くなるのに十分な量で存在する、請求項36記載の医薬組成物。
- 対象ラットにおける血中のVX−950濃度が、少なくともポリマーを含まないVX−950の投与で見られるよりも約200%高い、請求項36記載の医薬組成物。
- 対象ラットにおける血中のVX−950濃度が、ポリマーを含まないVX−950の投与で見られるよりも少なくとも約400%高い、請求項36記載の医薬組成物。
- 該ポリマーがHPMCである、請求項36記載の医薬組成物。
- 該ポリマーがHPMCASである、請求項36記載の医薬組成物。
- VX−950の無定形固体分散体(ここで、該VX−950は、医薬組成物の約30−75%wt/wtを構成する)、
HPMCおよびHPMCASから成る群から選択される1個以上のポリマー(ここで、該ポリマーは、医薬組成物の約30−75%wt/wtを構成する)、および
界面活性剤(ここで、該界面活性剤は、医薬組成物の約0.5−2%wt/wtを構成する)
を含む、医薬組成物。 - 該ポリマーがHPMCである、請求項46記載の医薬組成物。
- 該ポリマーがHPMCASである、請求項46記載の医薬組成物。
- 該界面活性剤がラウリル硫酸ナトリウムまたはビタミンE TPGSである、請求項46記載の医薬組成物。
- 該VX−950が医薬組成物の約49.5%wt/wtを構成し、
該ポリマーがHPMCであって、医薬組成物の約49.5%wt/wtを構成し、そして
該界面活性剤がラウリル硫酸ナトリウムまたはビタミンE TPGSであって、医薬組成物の約1%wt/wtを構成する、
請求項46記載の医薬組成物。 - 該VX−950が医薬組成物の約49.5%wt/wtを構成し、
該ポリマーがHPMCASであって、医薬組成物の約49.5%wt/wtを構成し、そして
該界面活性剤がラウリル硫酸ナトリウムまたはビタミンE TPGSであって、医薬組成物の約1%wt/wtを構成する、
請求項46記載の医薬組成物。 - 医薬組成物の約70%wt/wtのVX−950、
HPMCおよびHPMCASから選択されるポリマー(これは、医薬組成物の約29%wt/wtを構成する)、および
ラウリル硫酸ナトリウムおよびビタミンE TPGSから選択される界面活性剤(これは、医薬組成物の約1%wt/wtを構成する)
を含む、医薬組成物。 - HPMCおよびHPMCASの群から選択される溶液中に無定形VX−950粒子およびポリマーを含む水性懸濁液を含む、医薬組成物。
- 該無定形VX−950が固体分散体の形である、請求項53記載の医薬組成物。
- 界面活性剤を溶液中に、もしくはVX−950粒子の成分としてまたはその両方でさらに含む、請求項53記載の医薬組成物。
- 該界面活性剤がSLSおよびビタミンE TPGSの群から選択される、請求項55記載の医薬組成物。
- 該ポリマーが溶液中にあるかもしくはVX−950粒子の成分としてであるか、またはその両方である、請求項53記載の医薬組成物。
- 該水性懸濁液が界面活性剤の約0.1%から約20重量%を構成する、請求項53記載の医薬組成物。
- 該水性懸濁液が、無定形VX−950を重量で約1mg/mlから約100mg/mlを含む、請求項53記載の医薬組成物。
- 該水性懸濁液が約0.1%から約2.0重量%のポリマーを含む、請求項53記載の医薬組成物。
- 水性懸濁液が約1重量%のポリマーを含む、請求項60記載の医薬組成物。
- VX−950の無定形形態を提供するためにVX−950の噴霧乾燥を含む、VX−950の無定形形態の製造法。
- VX−950と適当な溶媒を合わせて混合物を形成させ、次いで該混合物を噴霧乾燥してVX−950の無定形形態を得ることを含む、請求項62記載の方法。
- a)VX−950、ポリマー、および溶媒を含む混合物を形成させ;
b)該混合物を噴霧乾燥してVX−950を含む固体分散体を形成させることを含む、
請求項62記載の方法。 - 該ポリマーがHPMCおよびHPMCASから選択される、請求項64記載の方法。
- 該ポリマーが固体分散体中約30%から約70重量%の量で存在する、請求項64記載の方法。
- 該混合物が界面活性剤をさらに含む、請求項62記載の方法。
- 該界面活性剤がラウリル硫酸ナトリウム(SLS)またはビタミンE TPGSである、請求項67記載の方法。
- 該溶媒が塩化メチレンを含む、請求項64記載の方法。
- 該溶媒がアセトンを含む、請求項64記載の方法。
- 該溶媒が約0%から約30%アセトンおよび約70%から約100%塩化メチレンを含む、請求項64記載の方法。
- 該溶媒が約0%から約40%アセトンおよび約60%から約100%塩化メチレンを含む、請求項64記載の方法。
- 請求項64記載の方法に従い製造された、固体分散体。
- 請求項1に記載の無定形VX−950を投与することを含む、哺乳動物におけるC型肝炎ウイルス(HCV)感染の処置法。
- 請求項1に記載の固体分散体を投与することを含む、哺乳動物におけるHCV感染の処置法。
- 免疫調節剤;抗ウイルス剤;HCVNS3/4Aプロテアーゼの他の阻害剤;IMPDHの他の阻害剤;HCVライフ・サイクルにおけるNS3/4Aプロテアーゼ以外の標的の阻害剤;内部リボソーム侵入阻害剤、広域ウイルス阻害剤;チトクロームP−450阻害剤;またはこれらの組合せから選択される付加的薬剤の投与を含む、請求項75記載の方法。
- 請求項5記載の無定形VX−950を含む、医薬包装物またはキット。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US57804304P | 2004-06-08 | 2004-06-08 | |
| PCT/US2005/019929 WO2005123076A2 (en) | 2004-06-08 | 2005-06-08 | Pharmaceutical compositions |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012000814A Division JP5337262B2 (ja) | 2004-06-08 | 2012-01-05 | 医薬組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008501802A true JP2008501802A (ja) | 2008-01-24 |
| JP2008501802A5 JP2008501802A5 (ja) | 2008-07-24 |
Family
ID=35510250
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007527639A Pending JP2008501802A (ja) | 2004-06-08 | 2005-06-08 | 医薬組成物 |
| JP2012000814A Expired - Fee Related JP5337262B2 (ja) | 2004-06-08 | 2012-01-05 | 医薬組成物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012000814A Expired - Fee Related JP5337262B2 (ja) | 2004-06-08 | 2012-01-05 | 医薬組成物 |
Country Status (18)
| Country | Link |
|---|---|
| US (2) | US20060089385A1 (ja) |
| EP (1) | EP1765283A4 (ja) |
| JP (2) | JP2008501802A (ja) |
| KR (2) | KR101370580B1 (ja) |
| CN (2) | CN1988885A (ja) |
| AR (1) | AR049297A1 (ja) |
| AU (1) | AU2005253957B2 (ja) |
| BR (1) | BRPI0511900A (ja) |
| CA (1) | CA2569310A1 (ja) |
| IL (2) | IL179809A (ja) |
| MX (1) | MXPA06014253A (ja) |
| NO (1) | NO20070130L (ja) |
| NZ (1) | NZ588471A (ja) |
| RU (1) | RU2373923C2 (ja) |
| SG (1) | SG153800A1 (ja) |
| TW (1) | TWI389688B (ja) |
| WO (1) | WO2005123076A2 (ja) |
| ZA (2) | ZA200700030B (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012503669A (ja) * | 2008-09-24 | 2012-02-09 | バーテックス ファーマシューティカルズ インコーポレイテッド | 肝炎を治療するためのpeg−インターフェロン、リバビリンおよびvx−950を含む治療レジメ |
| JP2014507424A (ja) * | 2011-03-08 | 2014-03-27 | ザリカス ファーマスーティカルズ リミテッド | 固体分散物製剤およびその使用方法 |
| JP2015503560A (ja) * | 2011-12-29 | 2015-02-02 | アッヴィ・インコーポレイテッド | Hcv阻害剤を含む固体組成物 |
Families Citing this family (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HU227742B1 (en) * | 1996-10-18 | 2012-02-28 | Vertex Pharma | Inhibitors of serine proteases, particularly hepatitis c virus ns3 protease |
| SV2003000617A (es) | 2000-08-31 | 2003-01-13 | Lilly Co Eli | Inhibidores de la proteasa peptidomimetica ref. x-14912m |
| US20100074949A1 (en) | 2008-08-13 | 2010-03-25 | William Rowe | Pharmaceutical composition and administration thereof |
| MY169670A (en) | 2003-09-03 | 2019-05-08 | Tibotec Pharm Ltd | Combinations of a pyrimidine containing nnrti with rt inhibitors |
| AR045596A1 (es) * | 2003-09-05 | 2005-11-02 | Vertex Pharma | Inhibidores de proteasas de serina en particular proteasa ns3-ns4a del vhc |
| TW201424733A (zh) * | 2004-10-29 | 2014-07-01 | Vertex Pharma | 劑量型式 |
| WO2006130686A2 (en) * | 2005-06-02 | 2006-12-07 | Schering Corporation | Hcv protease inhibitors in combination with food |
| BRPI0610737A2 (pt) | 2005-06-02 | 2010-07-20 | Schering Corp | formulações farmacêuticas e métodos de tratamento usando as mesmas |
| EP2256113A1 (en) | 2005-08-02 | 2010-12-01 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases |
| US8399615B2 (en) | 2005-08-19 | 2013-03-19 | Vertex Pharmaceuticals Incorporated | Processes and intermediates |
| AR055395A1 (es) * | 2005-08-26 | 2007-08-22 | Vertex Pharma | Compuestos inhibidores de la actividad de la serina proteasa ns3-ns4a del virus de la hepatitis c |
| US7964624B1 (en) | 2005-08-26 | 2011-06-21 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases |
| CA2643688A1 (en) | 2006-02-27 | 2007-08-30 | Vertex Pharmaceuticals Incorporated | Co-crystals and pharmaceutical compositions comprising the same |
| CA2645684A1 (en) * | 2006-03-06 | 2007-09-13 | Abbott Laboratories | Compositions and methods of use of ritonavir for treating hcv |
| EP1993994A2 (en) | 2006-03-16 | 2008-11-26 | Vertex Pharmceuticals Incorporated | Deuterated hepatitis c protease inhibitors |
| EP2001498A4 (en) * | 2006-03-20 | 2013-01-23 | Vertex Pharma | PHARMACEUTICAL COMPOSITIONS |
| EA018811B1 (ru) * | 2006-03-20 | 2013-10-30 | Вертекс Фармасьютикалз Инкорпорейтед | Способы получения твердой дисперсии лекарственного средства и твердые дисперсии лекарственного средства, полученные этим способом |
| WO2007120595A2 (en) * | 2006-04-11 | 2007-10-25 | Novartis Ag | Amines for the treatment of hcv |
| RU2448976C2 (ru) | 2006-04-11 | 2012-04-27 | Новартис Аг | Ингибиторы hcv/вич и их применение |
| MX2009006806A (es) * | 2006-12-22 | 2009-08-27 | Vertex Pharma | Secado por rocio fluidizado. |
| WO2008074035A1 (en) | 2006-12-27 | 2008-06-19 | Abbott Laboratories | Hcv protease inhibitors and uses thereof |
| EP2124949A1 (en) * | 2007-02-23 | 2009-12-02 | Avera Pharmaceuticals, Inc. | Pharmaceutical formulation |
| GEP20125645B (en) * | 2007-02-27 | 2012-09-25 | Vertex Pharma | Co-crystals and pharmaceutical compositions comprising the same |
| MX2009009176A (es) * | 2007-02-27 | 2009-09-28 | Vertex Pharma | Inhibidores de serina-proteasas. |
| CL2008000746A1 (es) * | 2007-03-14 | 2008-09-22 | Tibotec Pharm Ltd | Composicion farmaceutica en solucion que comprende tmc278 y un polimero soluble en agua; proceso de preparacion de dicha composicion; y uso de un polvo que comprende tmc278 para tratar sida. |
| SI2305263T1 (sl) * | 2007-06-07 | 2012-10-30 | Novartis Ag | Stabilizirane amorfne oblike imatinib mezilata |
| JP5443360B2 (ja) * | 2007-08-30 | 2014-03-19 | バーテックス ファーマシューティカルズ インコーポレイテッド | 共結晶体およびそれを含む医薬組成物 |
| JP5149585B2 (ja) * | 2007-10-02 | 2013-02-20 | 浜松ホトニクス株式会社 | 微粒子分散液製造方法 |
| JP5161528B2 (ja) * | 2007-10-02 | 2013-03-13 | 浜松ホトニクス株式会社 | パクリタキセル微粒子、パクリタキセル微粒子分散液、および、これらの製造方法 |
| AR068756A1 (es) | 2007-10-10 | 2009-12-02 | Novartis Ag | Compuestos peptidicos, formulacion farmaceutica y sus usos como moduladores del virus de la hepatitis c |
| TW200922549A (en) * | 2007-10-19 | 2009-06-01 | Abbott Gmbh & Amp Co Kg | Solid dispersion product containing N-aryl urea-based compound |
| EP2214682A2 (en) * | 2007-11-05 | 2010-08-11 | Vertex Pharmaceuticals Incorporated | Hcv combination therapies comprising vx-950, peg-ifn and ribavirin |
| EP2396028A2 (en) | 2009-02-12 | 2011-12-21 | Vertex Pharmceuticals Incorporated | Hcv combination therapies comprising pegylated interferon, ribavirin and telaprevir |
| MX349923B (es) | 2009-04-03 | 2017-08-21 | Hoffmann La Roche | Composiciones del ácido propano-1-sulfónico {3-[5-(4-cloro-fenil)- 1h-pirrolo [2,3-b]-piridina-3-carbonil]-2,4-difluoro-fenil]-amida y el uso de las mismas. |
| US8512690B2 (en) | 2009-04-10 | 2013-08-20 | Novartis Ag | Derivatised proline containing peptide compounds as protease inhibitors |
| EP2459211A1 (en) | 2009-07-31 | 2012-06-06 | Medtronic, Inc. | Continuous subcutaneous administration of interferon- to hepatitis c infected patients |
| MX2012009926A (es) * | 2010-02-25 | 2012-10-05 | Vereniging Voor Christelijk Hoger Onderwijs Wetenschappelijk Onderzoek En Patientenzorg | Un proceso para la preparacion de peptidos prolil sustituidos y peptidomimeticos similares. |
| TW201208704A (en) | 2010-07-14 | 2012-03-01 | Vertex Pharma | Palatable pharmaceutical composition |
| WO2012109646A1 (en) | 2011-02-11 | 2012-08-16 | Vertex Pharmaceuticals Incorporated | Treatment of hcv in hiv infection patients |
| US8409560B2 (en) | 2011-03-08 | 2013-04-02 | Zalicus Pharmaceuticals Ltd. | Solid dispersion formulations and methods of use thereof |
| TW201600087A (zh) | 2011-10-21 | 2016-01-01 | 艾伯維有限公司 | 治療c型肝炎病毒(hcv)的方法 |
| US8466159B2 (en) | 2011-10-21 | 2013-06-18 | Abbvie Inc. | Methods for treating HCV |
| DK2583677T1 (da) | 2011-10-21 | 2015-01-19 | Abbvie Inc | Fremgangsmåder til behandling af HCV omfattende mindst to direktevirkende antivirale midler, ribavirin, men ikke inteferon |
| US8492386B2 (en) | 2011-10-21 | 2013-07-23 | Abbvie Inc. | Methods for treating HCV |
| US9034832B2 (en) | 2011-12-29 | 2015-05-19 | Abbvie Inc. | Solid compositions |
| WO2013116339A1 (en) | 2012-01-31 | 2013-08-08 | Vertex Pharmaceuticals Incorporated | High potency formulations of vx-950 |
| AU2013226076B2 (en) | 2012-02-27 | 2017-11-16 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition and administration thereof |
| ITMI20120608A1 (it) * | 2012-04-13 | 2013-10-14 | Dipharma Francis Srl | Procedimento per la preparazione di un inibitore delle proteasi virali in forma amorfa |
| WO2013178031A1 (en) * | 2012-06-01 | 2013-12-05 | Sunshine Lake Pharma Co., Ltd. | New forms of telaprevir and preparation methods thereof |
| CN104870439A (zh) * | 2012-12-21 | 2015-08-26 | 桑多斯股份公司 | 替拉瑞韦的新形式 |
| PE20151778A1 (es) | 2013-01-31 | 2015-12-16 | Gilead Pharmasset Llc | Formulacion combinada de dos compuestos antivirales |
| UA116237C2 (uk) | 2013-03-15 | 2018-02-26 | Бьорінгер Інгельхайм Інтернаціональ Гмбх | Тверда пероральна дозована композиція інгібітору нсv в аморфному стані |
| SI3038601T1 (sl) | 2013-08-27 | 2020-07-31 | Gilead Pharmasset Llc | Formulacija kombinacije dveh protivirusnih spojin |
| JP7129703B2 (ja) | 2016-04-28 | 2022-09-02 | エモリー ユニバーシティー | アルキン含有ヌクレオチド及びヌクレオシド治療組成物並びにそれらに関連した使用 |
| CN110193013B (zh) * | 2019-07-02 | 2022-02-08 | 力品药业(厦门)股份有限公司 | 一种去乙酰真菌环氧乙酯固体分散体及其制备方法 |
| WO2023225029A1 (en) * | 2022-05-16 | 2023-11-23 | Day One Biopharmaceuticals, Inc. | Oral liquid suspension of pan-raf kinase inhibitor |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997006781A1 (fr) * | 1995-08-11 | 1997-02-27 | Nissan Chemical Industries, Ltd. | Procedes permettant de rendre amorphes des medicaments peu solubles |
| JPH107558A (ja) * | 1996-06-19 | 1998-01-13 | Eisai Co Ltd | 溶解性改善製剤 |
| WO2002018369A2 (en) * | 2000-08-31 | 2002-03-07 | Eli Lilly And Company | Peptidomimetic protease inhibitors |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6054472A (en) * | 1996-04-23 | 2000-04-25 | Vertex Pharmaceuticals, Incorporated | Inhibitors of IMPDH enzyme |
| ES2287971T3 (es) * | 1997-08-11 | 2007-12-16 | Pfizer Products Inc. | Dispersiones farmaceuticas solidas con biodisponibilidad incrementada. |
| US20020017295A1 (en) * | 2000-07-07 | 2002-02-14 | Weers Jeffry G. | Phospholipid-based powders for inhalation |
| EP1027885B1 (en) * | 1999-02-09 | 2008-07-09 | Pfizer Products Inc. | Basic drug compositions with enhanced bioavailability |
| UY26615A1 (es) * | 2000-03-16 | 2001-10-25 | Pfizer Prod Inc | Inhibidor de la glucogeno fosforilasa. |
| US6777400B2 (en) * | 2000-08-05 | 2004-08-17 | Smithkline Beecham Corporation | Anti-inflammatory androstane derivative compositions |
| GB0102342D0 (en) * | 2001-01-30 | 2001-03-14 | Smithkline Beecham Plc | Pharmaceutical formulation |
| US6627760B1 (en) * | 2001-06-25 | 2003-09-30 | Astrazeneca Ab | Amorphous compound |
| JP2006504618A (ja) * | 2001-11-14 | 2006-02-09 | テバ ファーマシューティカル インダストリーズ リミティド | 非結晶性及び結晶性ロサルタン・カリウム、及びそれらの調製方法 |
| AR038375A1 (es) * | 2002-02-01 | 2005-01-12 | Pfizer Prod Inc | Composiciones farmaceuticas de inhibidores de la proteina de transferencia de esteres de colesterilo |
| US6828301B2 (en) * | 2002-02-07 | 2004-12-07 | Boehringer Ingelheim International Gmbh | Pharmaceutical compositions for hepatitis C viral protease inhibitors |
| ZA200603863B (en) * | 2003-10-27 | 2007-11-28 | Vertex Pharma | Combination for HCV treatment |
| TW201424733A (zh) * | 2004-10-29 | 2014-07-01 | Vertex Pharma | 劑量型式 |
-
2005
- 2005-06-08 SG SG200903859-7A patent/SG153800A1/en unknown
- 2005-06-08 EP EP05757623A patent/EP1765283A4/en not_active Withdrawn
- 2005-06-08 CA CA002569310A patent/CA2569310A1/en not_active Abandoned
- 2005-06-08 AR ARP050102345A patent/AR049297A1/es unknown
- 2005-06-08 WO PCT/US2005/019929 patent/WO2005123076A2/en active Application Filing
- 2005-06-08 KR KR1020077000437A patent/KR101370580B1/ko not_active IP Right Cessation
- 2005-06-08 NZ NZ588471A patent/NZ588471A/en not_active IP Right Cessation
- 2005-06-08 CN CNA200580024232XA patent/CN1988885A/zh active Pending
- 2005-06-08 JP JP2007527639A patent/JP2008501802A/ja active Pending
- 2005-06-08 AU AU2005253957A patent/AU2005253957B2/en not_active Ceased
- 2005-06-08 KR KR1020127008036A patent/KR20120039763A/ko not_active Application Discontinuation
- 2005-06-08 CN CN2011103013245A patent/CN102512372A/zh active Pending
- 2005-06-08 US US11/147,524 patent/US20060089385A1/en not_active Abandoned
- 2005-06-08 MX MXPA06014253A patent/MXPA06014253A/es not_active Application Discontinuation
- 2005-06-08 RU RU2006147247/15A patent/RU2373923C2/ru not_active IP Right Cessation
- 2005-06-08 ZA ZA200700030A patent/ZA200700030B/xx unknown
- 2005-06-08 TW TW094118847A patent/TWI389688B/zh not_active IP Right Cessation
- 2005-06-08 BR BRPI0511900-6A patent/BRPI0511900A/pt not_active IP Right Cessation
-
2006
- 2006-12-04 IL IL179809A patent/IL179809A/en not_active IP Right Cessation
-
2007
- 2007-01-08 NO NO20070130A patent/NO20070130L/no not_active Application Discontinuation
-
2008
- 2008-03-26 ZA ZA200802676A patent/ZA200802676B/en unknown
-
2012
- 2012-01-05 JP JP2012000814A patent/JP5337262B2/ja not_active Expired - Fee Related
- 2012-09-20 IL IL222003A patent/IL222003A0/en unknown
-
2013
- 2013-04-12 US US13/861,791 patent/US20130274180A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997006781A1 (fr) * | 1995-08-11 | 1997-02-27 | Nissan Chemical Industries, Ltd. | Procedes permettant de rendre amorphes des medicaments peu solubles |
| JPH107558A (ja) * | 1996-06-19 | 1998-01-13 | Eisai Co Ltd | 溶解性改善製剤 |
| WO2002018369A2 (en) * | 2000-08-31 | 2002-03-07 | Eli Lilly And Company | Peptidomimetic protease inhibitors |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012503669A (ja) * | 2008-09-24 | 2012-02-09 | バーテックス ファーマシューティカルズ インコーポレイテッド | 肝炎を治療するためのpeg−インターフェロン、リバビリンおよびvx−950を含む治療レジメ |
| JP2014507424A (ja) * | 2011-03-08 | 2014-03-27 | ザリカス ファーマスーティカルズ リミテッド | 固体分散物製剤およびその使用方法 |
| JP2015503560A (ja) * | 2011-12-29 | 2015-02-02 | アッヴィ・インコーポレイテッド | Hcv阻害剤を含む固体組成物 |
| JP2015227352A (ja) * | 2011-12-29 | 2015-12-17 | アッヴィ・アイルランド・アンリミテッド・カンパニー | Hcv阻害剤を含む固体組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR101370580B1 (ko) | 2014-03-06 |
| JP2012067138A (ja) | 2012-04-05 |
| CN102512372A (zh) | 2012-06-27 |
| WO2005123076A2 (en) | 2005-12-29 |
| TW200608975A (en) | 2006-03-16 |
| EP1765283A2 (en) | 2007-03-28 |
| AU2005253957B2 (en) | 2011-08-25 |
| ZA200802676B (en) | 2009-12-30 |
| BRPI0511900A (pt) | 2008-01-22 |
| RU2006147247A (ru) | 2008-07-20 |
| NO20070130L (no) | 2007-01-25 |
| AU2005253957A1 (en) | 2005-12-29 |
| NZ588471A (en) | 2012-02-24 |
| WO2005123076A3 (en) | 2006-06-15 |
| CN1988885A (zh) | 2007-06-27 |
| KR20070030270A (ko) | 2007-03-15 |
| AR049297A1 (es) | 2006-07-12 |
| SG153800A1 (en) | 2009-07-29 |
| IL179809A0 (en) | 2007-05-15 |
| TWI389688B (zh) | 2013-03-21 |
| MXPA06014253A (es) | 2007-07-13 |
| JP5337262B2 (ja) | 2013-11-06 |
| ZA200700030B (en) | 2009-06-24 |
| IL222003A0 (en) | 2012-12-02 |
| US20060089385A1 (en) | 2006-04-27 |
| CA2569310A1 (en) | 2005-12-29 |
| KR20120039763A (ko) | 2012-04-25 |
| RU2373923C2 (ru) | 2009-11-27 |
| US20130274180A1 (en) | 2013-10-17 |
| EP1765283A4 (en) | 2012-11-28 |
| IL179809A (en) | 2012-10-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5337262B2 (ja) | 医薬組成物 | |
| US20130079289A1 (en) | Pharmaceutical Compositions | |
| AU2007336516B2 (en) | Fluidized spray drying | |
| JP5890553B2 (ja) | 固体組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080602 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100316 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20100316 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110301 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110601 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110608 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110629 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110906 |