JP2005539031A - 野生型または変異型eNOSによる重症肢虚血の遺伝子療法 - Google Patents
野生型または変異型eNOSによる重症肢虚血の遺伝子療法 Download PDFInfo
- Publication number
- JP2005539031A JP2005539031A JP2004529471A JP2004529471A JP2005539031A JP 2005539031 A JP2005539031 A JP 2005539031A JP 2004529471 A JP2004529471 A JP 2004529471A JP 2004529471 A JP2004529471 A JP 2004529471A JP 2005539031 A JP2005539031 A JP 2005539031A
- Authority
- JP
- Japan
- Prior art keywords
- enos
- amino acid
- polypeptide
- mutation
- position corresponding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0071—Oxidoreductases (1.) acting on paired donors with incorporation of molecular oxygen (1.14)
- C12N9/0073—Oxidoreductases (1.) acting on paired donors with incorporation of molecular oxygen (1.14) with NADH or NADPH as one donor, and incorporation of one atom of oxygen 1.14.13
- C12N9/0075—Nitric-oxide synthase (1.14.13.39)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/022—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from an adenovirus
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- General Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Cardiology (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Heart & Thoracic Surgery (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Enzymes And Modification Thereof (AREA)
Abstract
本発明はeNOSポリペプチドまたは該eNOSポリペプチドをコードするポリヌクレオチドを使用して細胞内のeNOS活性を調節することによる重症肢虚血(CLI)の新規の予防、診断または治療方法を提供する。本発明の方法に使用するための、野生型および変異型eNOSポリペプチド、それに該ポリペプチドをコードするポリヌクレオチドが、提供される。本発明の変異型eNOSポリペプチドは、細胞内でリン酸化されている哺乳動物eNOSの機能性ドメイン内のある位置に対応する、少なくとも1つの変異を有する。
Description
本発明はeNOSポリペプチドおよびポリヌクレオチドを使用して細胞中のeNOS活性を調節することによる重症肢虚血(CLI)の予防、診断または治療方法に関する。本発明では該方法に使用するための野生型および変異型eNOSポリペプチド、ならびに該ポリペプチドをコードするポリヌクレオチドも提供される。
末梢動脈閉塞性疾患(PAOD)の罹患率は米国では約12%である。初期PAOD(跛行)は運動に伴う虚血性筋肉痛を特徴とする。PAODの進行による重症肢虚血(CLI)は安静時の低血流量・酸素供給量とそれに伴う安静時の筋肉痛および難治性皮膚潰瘍または壊疽を特徴とし[Rissanen et al., Eur. J. Clin. Invest. 31:651-666(2001); Dormandy and Rutherford, J. Vasc. Surg. 31:S1-S296 (2000)]、また年間1万人につき少なくとも5〜10人を見舞うと推定される。
POAD/跛行患者の治療には動脈硬化危険因子の管理、運動、さらにはCilastozolまたはPentoxyfyllineによる薬物療法などがある[Robeer et al., Eur. J. Vasc. Endovasc. Surg. 15:36-43 (1998)]。症状が持続するようなら、跛行、安静時痛および/または難治性虚血性潰瘍の治療に経皮経管的血管形成術(PTA)を行う場合もある。PTAは腸骨動脈および浅大腿動脈の短期狭窄または閉塞に最も適する。1年開存率は80〜90%である。さらにびまん性疾患の患者では外科的な血行再建術が推奨される。大動脈大腿動脈バイパス術および大腿膝窩動脈バイパス術の5年開存率はそれぞれ90%、70%である[前掲Dormandy and Rutherford, (2000)]。
しかし、外科的およびインターベンション的な血行再建術の進歩にもかかわらず、虚血性疼痛/潰瘍を主訴とする患者の20〜30%はびまん性遠位血管疾患のため外科的な血行再建術または血管形成術になじまないか、またはそうした療法が失敗に終わるし、また現行薬物療法は進行CLI患者の救肢にはほとんど無効である。
そうした患者の、大切断を回避した場合の1年後の生存率は50%未満である。さらに、切断を必要とする高齢患者はしばしば全身的な健康状態が不良であり、手術の危険が相対的に高く、また長期的な予後も不良である[前掲Dormandy and Rutherford, (2000)]。アンジオテンシン変換酵素阻害剤およびスタチンは虚血実験モデルでは血流を増進すると報告されているが、現在使用されている薬物で新血管形成を促進するものは一つもない[Fabre et al., Circulation 99:3043-3049 (1999); Kureishi et al., Nat Med 6:1004-1010 (2000)]。従って、改良型のCLI治療対策が求められている。
虚血性疾患に対する1つの新たしい治療対策では、血管形成を刺激する成長因子を使用して局所的な血管成長の増進をはかる[前掲Rissanen et al. (2001); Yla-Herttuala et al., Lancet 355: 213-222 (2000); Isner et al., J. Clin. Invest. 103-1231-1236 (1999); Rutanen et al., Curr. Cardiol. Report 3:29-36 (2001)]。血管成長は血管発生(vasculogenesis)、血管新生(angiogenesis)、動脈形成(arteriogenesis)に分けることができる。血管発生は血管芽細胞/内皮前駆細胞(EPCs)に由来する胎児期のin situ血管形成をいう。
血管新生は分化内皮細胞(ECs)の増殖と遊走の結果としての、既存毛細血管からの新血管の形成をいう[Risau et al., Nature 386: 671-674 (1997)]。動脈形成は既存細動脈の吻合に由来する筋性側副血管のin situ形成をいう[Schaper et al., Circ Res 79:911-919 (1996)]。しかし、内因性の血管新生および動脈形成ではCLIにおける血流量および酸素供給量の減少を十分に補えない。血管形成を刺激する成長因子のデリバリーはCLI治療のための治療対策の追加にはなるが、成長因子による血管新生の増進は加齢、動脈硬化およびその他の新血管危険因子による内皮機能障害のために限定されるおそれがあるとの証拠が強まっている。
内皮型一酸化窒素合成酵素(eNOS; 別名ecNOSまたはNOS 3)は重要な調節/仲介因子として血管新生に関与するとされてきた。ニトロプルシドなどのような一酸化窒素(NO)供与剤は内皮細胞の増殖と遊走を促進するが、NOS阻害剤はこれらの過程を抑制する[Ziche et al., J. Clin. Invest. 9:2036-2044 (1994); Morbidelli et al., Am. J. Physiol. 270:H411-H415 (1996)]。種々の研究からeNOS欠損マウス(eNOS-KO)では血管新生および創傷治癒に障害が及ぶことが判明した。Leeらは外植体の動脈を使用して内皮細胞の遊走、増殖および分化にはeNOSが必要であることをin vitroで立証した。
この研究成果は、eNOS-KOマウスの皮下注入マトリゲル(Matrigel)プラグ中への毛細血管形成の減少を立証することにより、in vivoで確認された。eNOS-KOマウスでは切除創治癒も著しく遅れたが、これは創傷修復に関連する血管新生過程における内皮NOの役割を際立たせるものである[Lee et al., Am. J. Physiol. 277:H1600-H1608 (1999)]。後肢虚血を外科的に誘発した後のeNOS-KOマウスでは著しい血管新生障害が明らかになった。後肢虚血を外科的に誘発したウサギにLアルギニン(NOSの基質)を投与すると血管新生が著しく改善したが、これは虚血によって引き起こされる血管新生で果たす内皮NOの役割を確認するものである[Murohara et al., J. Clin. Invest. 101: 2567-2578 (1998)]。
前述のように、虚血に呼応した血管新生は加齢や内皮機能障害により妨げられるおそれがあるとの証拠も強まっている。動物モデルでは内皮NO放出の減少や成長因子発現の減衰に起因する可能性の高い血管新生障害も観測された[Rivard et al., Circulation 99: 111-120(1996); Van Belle et al., Circulation 96:2667-2674 (1997)]。ラット後肢虚血モデルでは、ホモシステイン血症や高コレステロール血症などの危険因子は、おそらく内皮由来NOのバイオアベイラビリティーを低下させるためであろう、血管新生を弱めることが示された[Duan et al., Circulation 102:III 370-III 376 (2000)]。
従って、効果的なCLI治療法が求められている。虚血肢のNOバイオアベイラビリティーを高めるような、CLI治療のための遺伝子療法が開発されれば、損なわれていた血管新生の促進、既存微小血管機能障害の改善、既存血管の血管運動(拡張)活性の回復、および既存側副血管の再モデル化/成熟(動脈形成)への寄与など、多様な機序を通じて虚血を治すことも可能になるかもしれない。
本発明はeNOSポリペプチドまたは該eNOSポリペプチドをコードするポリヌクレオチドを使用した重症肢虚血(CLI)の予防、診断または治療方法に関する。本発明の方法を使用すれば、細胞中のeNOS活性を、eNOS活性に関連する疾患または障害を改善する方向へと、調節することができる。特に本発明の方法を使用すれば、虚血肢中の局所的なNO産生を増加させることによって、細胞中のeNOS活性を、虚血肢中のNO産生の低下に関連する疾患または障害を改善する方向へと、調節することができる。従って本発明は、治療を必要とする患者に、eNOSポリペプチドまたはその変異型もしくはそうしたポリペプチドをコードするポリヌクレオチドを投与することにより患部組織のNOレベルを上昇させるような遺伝子治療の方法を提供する。
本発明は一態様では、治療を必要とする患者に、哺乳動物eNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含むCLI治療方法を提供する。
本発明はさらに、CLIの症状たとえば微小血管の機能障害、潰瘍治癒および血管新生を治療する方法を提供する。本発明は一態様では、治療を必要とする患者に、eNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む血管新生の治療方法を提供するが、該eNOSポリペプチドは哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする。本発明は一実施態様では、治療を必要とする患者に、eNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む微小血管の機能障害を改善する方法を提供するが、該eNOSポリペプチドは哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする。
本発明は関連態様では、本発明の方法に使用するための、eNOSポリペプチドおよびeNOSポリペプチドをコードするポリヌクレオチドを提供する。本発明の方法に使用するための好適なポリヌクレオチドは、野生型または変異型eNOSポリペプチドまたはその変種をコードするポリペプチドなどである。コードされるeNOSポリペプチドは哺乳動物eNOSポリペプチドであるのが好ましく、またヒトeNOSポリペプチドであるのが最も好ましい。一態様では、該eNOSポリペプチドは配列番号:1によってコードされるヒトeNOSポリペプチドである。
別の態様では、本発明の方法に使用するための好適なポリヌクレオチドによりコードされるヒトeNOSポリペプチドは、配列番号:1のアミノ酸残基495に対応する位置に第1変異を、また配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、それぞれ有する。
別の態様では、本発明の方法に使用するための好適なポリヌクレオチドによりコードされるヒトeNOSポリペプチドは、配列番号:1のアミノ酸残基495に対応する位置に第1変異を、配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、また配列番号:1のアミノ酸残基2に対応する位置に第3変異を、それぞれ有する。
別の態様では、本発明の方法に使用するための好適なポリヌクレオチドによりコードされるヒトeNOSポリペプチドは、配列番号:1のアミノ酸残基495に対応する位置に第1変異を、配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、また配列番号:1のアミノ酸残基2に対応する位置に第3変異を、それぞれ有する。
好ましくは、配列番号:1のアミノ酸残基495に対応する位置の変異はAla、Gly、Val、Leu、Ile、Pro、Phe、Tyr、Trp、Met、Ser、Cys、Glu、Asn、Gln、Lys、ArgまたはHisへのアミノ酸置換であり、Ala、Val、LeuまたはIleへの置換であるのがなお好ましく、またAlaまたはValへの置換であるのが最も好ましい; 配列番号:1のアミノ酸残基1177に対応する位置の変異はAspへのアミノ酸置換である; また配列番号:1のアミノ酸残基2に対応する位置の変異はAlaへのアミノ酸置換である。
態様によっては、本発明の方法に使用するための好適なポリヌクレオチドによってコードされるヒトeNOSポリペプチドのリン酸化の度合いが基準ポリペプチドに比して加減されている。
態様によっては、本発明の方法に使用するための好適なポリヌクレオチドによってコードされるヒトeNOSポリペプチドのリン酸化の度合いが基準ポリペプチドに比して加減されている。
態様によっては、本発明の方法に使用するための好適なポリヌクレオチドによってコードされるヒトeNOSポリペプチドは基準eNOSポリペプチドに比して、より高いeNOS活性を有する。該ヒトeNOSポリペプチドは基準eNOSポリペプチドに比して、より高いNO産生、カルモジュリンに対する結合アフィニティーおよび/または還元酵素活性を有するのが好ましい。該ヒトeNOSポリペプチドは基準eNOSポリペプチドに比して、より高いNO産生を有するのが最も好ましい。
態様によっては、本発明の方法に使用するための好適なポリヌクレオチドによってコードされるヒトeNOSポリペプチドは基準eNOSポリペプチドに比して、より低いeNOS活性(たとえば該ポリペプチドのCa++-カルモジュリン仲介刺激における、基準eNOSポリペプチドに比して、より低いCa++依存性)を有する。
一態様では、本発明の方法に使用するための好適なポリヌクレオチドは、ヒトeNOSポリペプチドのアミノ酸と実質的に相同であるeNOSポリペプチドをコードする。
一態様では、本発明の方法に使用するための好適なポリヌクレオチドは、配列番号:1のアミノ酸配列と95〜99%の配列相同性を有するeNOSポリペプチドをコードする。
一態様では、本発明の方法に使用するための好適なポリヌクレオチドは、ヒトeNOSポリペプチドのアミノ酸と実質的に相同であるeNOSポリペプチドをコードする。
一態様では、本発明の方法に使用するための好適なポリヌクレオチドは、配列番号:1のアミノ酸配列と95〜99%の配列相同性を有するeNOSポリペプチドをコードする。
別の態様では、本発明の方法に使用するための好適なポリヌクレオチドは、eNOSポリペプチドをコードする核酸配列をコードする組換えベクターである。一態様では該核酸配列は、該eNOSが細胞中で発現するよう、少なくとも1つの調節配列へと作動可能に連結されている。好ましくは、少なくとも1つの調節配列はプロモーターたとえばCMVプロモーターである。一態様では、該組換えベクターはプラスミドベクターまたはアデノウイルスベクターである。
別の態様では、本発明の方法による治療は治療を必要とする患者の細胞中のeNOS活性の調節による。該細胞は内皮細胞であるのが好ましく、ヒト内皮細胞であるのがより好ましい。
別の態様では、本発明の方法による治療は治療を必要とする患者の細胞中のeNOS活性の調節による。該細胞は内皮細胞であるのが好ましく、ヒト内皮細胞であるのがより好ましい。
別の態様では本発明の方法は、ヒト野生型または変異型eNOSポリペプチドをコードするポリヌクレオチドの、治療を必要とする患者への投与前・中・後に、1つまたは複数の血管新生因子を投与するステップをさらに含む。本発明の方法に使用するための好適な血管新生因子はHFG、VEGF、FGF、内皮成長因子、上皮成長因子、血小板由来成長因子、TGF-アルファ、TGF-ベータ、PDGF、TNA-アルファまたはIGF、Del-1などが非限定的な例であるが、FGFであるのが好ましい。
一態様では、本発明の方法に使用するための好適なポリヌクレオチドは患者の細胞にex vivoで導入することにより投与する。別の態様では、本発明の方法に使用するための好適なポリヌクレオチドは患者の病変組織に、または周辺血管系に導入することにより投与する。本発明の方法に使用するための好適なポリヌクレオチドは患者の肢筋への筋内注射または動脈内注射により投与する。
本発明は別の態様では、治療を必要とする患者にeNOSポリペプチドを有効量投与するステップを含む重症肢虚血(CLI)の治療方法を提供するが、該eNOSポリペプチドは哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする。本発明の方法への使用に好適なeNOSポリペプチドは好ましくは、ヒトeNOSであり、また配列番号:1のアミノ酸残基495または1177に対応する位置に少なくとも1つの変異を有する。
一態様では、本発明の方法への使用に好適なeNOSポリペプチドは配列番号:1のアミノ酸残基495または1177に対応する位置に少なくとも1つの変異を有する。
一態様では、本発明の方法への使用に好適なeNOSポリペプチドは配列番号:1のアミノ酸残基495に対応する位置に第1変異を、また配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、それぞれ有する。
一態様では、本発明の方法への使用に好適なeNOSポリペプチドは配列番号:1のアミノ酸残基495に対応する位置に第1変異を、配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、また配列番号:1のアミノ酸残基2に対応する位置に第3変異を、それぞれ有する。
一態様では、本発明の方法への使用に好適なeNOSポリペプチドは配列番号:1のアミノ酸残基495に対応する位置に第1変異を、また配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、それぞれ有する。
一態様では、本発明の方法への使用に好適なeNOSポリペプチドは配列番号:1のアミノ酸残基495に対応する位置に第1変異を、配列番号:1のアミノ酸残基1177に対応する位置に第2変異を、また配列番号:1のアミノ酸残基2に対応する位置に第3変異を、それぞれ有する。
好ましくは、配列番号:1のアミノ酸残基495に対応する位置の変異はAla、Gly、Val、Leu、Ile、Pro、Phe、Tyr、Trp、Met、Ser、Cys、Glu、Asn、Gln、Lys、ArgまたはHisへのアミノ酸置換であり、Ala、Val、LeuまたはIleへの置換であるのがなお好ましく、またAlaまたはValへの置換であるのが最も好ましい; 配列番号:1のアミノ酸残基1177に対応する位置の変異はAspへのアミノ酸置換である; また配列番号:1のアミノ酸残基2に対応する位置の変異はAlaへのアミノ酸置換である。
本発明自体はもとより本発明の以上のような目的や他の目的、その様々な特徴については、添付の図面を参照しながら以下の説明を読めば、さらに理解が進むであろう。
本発明自体はもとより本発明の以上のような目的や他の目的、その様々な特徴については、添付の図面を参照しながら以下の説明を読めば、さらに理解が進むであろう。
本発明は重症肢虚血(CLI)治療のための新規対策を提供する。本発明は特に、eNOSポリペプチドまたはポリヌクレオチドを使用するCLI予防、診断および治療方法を提供する。本発明の方法を使用すれば、細胞中のeNOS活性を、eNOS活性に関連する疾患または障害を改善する方向へと、調節することができる。特に、本発明の方法を使用すれば、虚血肢中の局所的なNO産生を増加させることによって、細胞中のeNOS活性を、虚血肢中のNO産生の低下に関連する疾患または障害を改善する方向へと、調節することができる。
従って本発明の方法および組成物は様々な機序を通じて、たとえば1)血管新生の刺激、2)微小血管の機能障害の改善、3)既存血管の血管運動(血管拡張)活性の回復、および4)既存側副血管の再モデル化/成熟(動脈形成)などを通じて、病変組織のNOレベルを高め、もって根底にあるCLIの病態生理を標的にするための、新規治療対策を提供する。結果としてもたらされる皮膚、筋肉双方への血流量と酸素供給量の改善は、安静時痛の緩和や虚血性潰瘍の治癒につながると期待される。
さらに、本発明の変異型eNOSポリペプチドは野生型eNOSよりも効き目が強いという可能性もある。特異的な活性は変異型eNOS酵素のほうが著しく大きいためである。加えて、eNOSポリペプチドの活性はカルシウムによる厳密な調節が可能であり、抗oxLDL(酸化低密度リポタンパク質)性、抗加齢性である。従って、遺伝子療法に本発明のeNOS組成物を使用すれば、「過剰投与」に伴う毒性を成長因子とは対照的にごくわずかに抑えることができる。
本発明で引用する参考文献は参照によりその全体が本明細書に組み込まれる。
本発明で引用する参考文献は参照によりその全体が本明細書に組み込まれる。
用語の意味
本明細書で使用する専門用語、学術用語の意味は特に断らない限り当業者の常識の範囲内の意味とする。本明細書では技術上周知の様々な方法に言及する。本明細書で言及するそうした公知方法を開示している出版物等の資料は参照により本明細書にその全体が、あたかもその全文が開示されるかのように、組み込まれる。組換えDNA技術の一般原理を開示している標準参考著作には、Sambrook, J., et al. (1989) Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press, Planview, N.Y.; McPherson, M.J., Ed. (1991) Directed Mutagenesis: A Practical Approach, IRL Press, Oxford; Jones, J. (1992) Amino Acid and Peptide Synthesis, Oxford Science Publications, Oxford; Austen, B.M. and Westwood, O.M.R. (1991) Protein Targeting and Secretion, IRL Press, Oxfordなどがある。本発明の実施には技術上周知の任意好適の原料および/または方法が使用可能であるが、好ましい原料および/または方法を開示する。以下の説明と実施例で言及する原料、試薬等は特に断らない限り商業供給元から入手可能である。
本明細書で使用する専門用語、学術用語の意味は特に断らない限り当業者の常識の範囲内の意味とする。本明細書では技術上周知の様々な方法に言及する。本明細書で言及するそうした公知方法を開示している出版物等の資料は参照により本明細書にその全体が、あたかもその全文が開示されるかのように、組み込まれる。組換えDNA技術の一般原理を開示している標準参考著作には、Sambrook, J., et al. (1989) Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press, Planview, N.Y.; McPherson, M.J., Ed. (1991) Directed Mutagenesis: A Practical Approach, IRL Press, Oxford; Jones, J. (1992) Amino Acid and Peptide Synthesis, Oxford Science Publications, Oxford; Austen, B.M. and Westwood, O.M.R. (1991) Protein Targeting and Secretion, IRL Press, Oxfordなどがある。本発明の実施には技術上周知の任意好適の原料および/または方法が使用可能であるが、好ましい原料および/または方法を開示する。以下の説明と実施例で言及する原料、試薬等は特に断らない限り商業供給元から入手可能である。
「ポリペプチド」は本明細書では、全長タンパク質またはその断片、またはペプチドをいう。好ましい実施態様では、本発明のeNOS断片またはペプチドはeNOS活性たとえばNO産生能を保持する。しかし、eNOS活性のレベルは基準eNOSポリペプチドに比して(たとえば全長または野生型ポリペプチドに比して)加減してもよい。
ポリペプチドまたはポリヌクレオチドの「変種」は本明細書では、それぞれ基準ポリペプチドまたはポリヌクレオチド(たとえば野生型ポリペプチドまたはポリヌクレオチド)に比して一次、二次または三次構造が異なるポリペプチドまたはポリヌクレオチドをいう。たとえば基準アミノ酸または核酸配列とは異なる変異または修飾を含むようなアミノ酸または核酸配列である。実施態様によっては、eNOSの変種は異なるアイソフォームまたは多型でもよい。変種は、技術上周知の方法を用いて単離または生成した天然型、合成型、組換え型または化学修飾型のポリペプチドまたはポリヌクレオチドとすることができる。
ポリペプチドまたはポリヌクレオチドの「変異」は本明細書では、それぞれ基準ポリペプチドまたはポリヌクレオチド(たとえば野生型ポリペプチドまたはポリヌクレオチド)と比較した場合の一次、二次または三次構造の、天然型、合成型、組換え型または化学修飾型の変化または差異をいう。そうした変異を有するポリペプチドまたはポリヌクレオチドは技術上周知の方法を用いて単離または生成することができる。
「変異型eNOSポリペプチド」またはその文法的等価物(たとえばeNOS変異型、変異型eNOS、eNOS変異型ポリペプチド、eNOSポリペプチド変異型)は、哺乳動物eNOSの機能性ドメイン内のある位置に対応するアミノ酸残基中に少なくとも1つの変化または変異を有するeNOSポリペプチドまたはその断片または変種をいう。好ましい実施態様では、該変異はヒトeNOS(配列番号:1)のアミノ酸残基495に対応する位置のアミノ酸置換であり、該アミノ酸置換は好ましくはAlaまたはValへの置換である。別の好ましい実施態様では、変異型eNOSポリペプチドの活性を基準eNOSポリペプチドに比して加減している。
eNOSポリペプチドの「機能性ドメイン」は本明細書では、eNOS活性に関連する該ポリペプチド中の任意のアミノ酸残基、部位または領域をいい、その非限定的な例はタンパク質結合ドメイン(たとえばカルモジュリン結合ドメイン、キナーゼ結合ドメイン、またはリガンド結合ドメイン)、リン酸化部位、ミリストイル化部位、還元酵素ドメイン、または活性化部位などである。
「eNOS活性」は本明細書では、細胞内での該酵素に関連する任意の活性をいい、たとえばNO産生、カルモジュリン結合、血管新生の刺激、微小血管機能障害の改善、既存血管の血管運動(血管拡張)活性の回復、既存側副血管の再モデル化/成熟(動脈形成)などを非限定的に含む。eNOS活性はまた、該ポリペプチドに関連する任意の生物または細胞活性、特にeNOSポリペプチドの機能性ドメインに関連する任意のそうした活性でもよい。eNOS活性はまた、たとえば前記のまたは公知のeNOS活性のうち任意の活性の調節を非限定的に含む該酵素に関連する活性の調節でもよい。
eNOS活性の「調節」は本明細書では、そうした活性の増進、減退、誘発または抑制をいう。実施態様によっては、eNOS活性のそうした増進、減退、誘発または抑制は基準分子たとえば野生型または変異型eNOSポリペプチドに対して相対的である。
「疾患」、「病態」または「障害」は本明細書では、eNOS活性の調節によって改善することができる患者の細胞、組織または臓器内の望ましくない状態をいう。eNOSはたとえば血管新生、血管拡張、免疫調節、血小板凝集阻害、平滑筋の弛緩などを非限定的に含む多様な生理過程に関与している。従って、治療を必要とする患者の細胞、組織または臓器内のeNOS活性を調節すれば、本明細書で開示するように、疾患、病態または障害を改善することができる。
「患者」は本明細書では哺乳動物であり、またヒトであるのが好ましい。
「患者」は本明細書では哺乳動物であり、またヒトであるのが好ましい。
eNOSポリペプチドをコードするポリヌクレオチド
内皮型一酸化窒素合成酵素(eNOS; 別名ecNOSまたはNOS3)は3つの既知NO合成酵素アイソフォームのうちの1つである。eNOSはたとえば血管内皮細胞、心筋細胞、血小板、種々の平滑筋および免疫系細胞たとえばT細胞、好中球またはマクロファージなどで発見されている。本発明の方法に使用されるeNOSポリペプチドをコードするポリヌクレオチドは本明細書で開示する任意の細胞または組織に由来してよいが、内皮細胞に由来するのが好ましい。
内皮型一酸化窒素合成酵素(eNOS; 別名ecNOSまたはNOS3)は3つの既知NO合成酵素アイソフォームのうちの1つである。eNOSはたとえば血管内皮細胞、心筋細胞、血小板、種々の平滑筋および免疫系細胞たとえばT細胞、好中球またはマクロファージなどで発見されている。本発明の方法に使用されるeNOSポリペプチドをコードするポリヌクレオチドは本明細書で開示する任意の細胞または組織に由来してよいが、内皮細胞に由来するのが好ましい。
本発明の方法に使用されるeNOSポリペプチドをコードするポリヌクレオチドは任意の哺乳動物たとえばヒト、マウス、モルモット、イヌ、ウシ、ブタ、ラットまたはウサギに由来してよいが、ヒトに由来するのが好ましい。本明細書は一般にヒトeNOS(配列番号:1)およびその変異型の使用に関する。しかし、当業者には自明であろうが、本開示は前記のような他の種に由来するeNOSポリペプチドおよびポリヌクレオチド、ならびにその変異型にも、および/またはヒト以外の他の種を治療するためのeNOSポリペプチドをコードするポリヌクレオチドの使用にも、等しく当てはまる。
宿主細胞に(トランスフェクションまたはトランスダクションにより)導入しその中で発現させることができるeNOSポリペプチドをコードする任意の形態のポリヌクレオチドは本発明の方法への使用に好適である。
本発明のeNOSポリペプチドをコードするポリヌクレオチドの例は、eNOSポリペプチドをコードするcDNA、またはeNOSポリペプチドを間断なくコードするcDNAなどである。「間断なくコードする」ポリヌクレオチドは、イントロンまたは他の非コード配列を介在させているオープンリーディングフレーム(ORF)と対比して連続したORFをもつポリヌクレオチドをいう。
本発明のeNOSポリペプチドをコードするポリヌクレオチドの例は、eNOSポリペプチドをコードするcDNA、またはeNOSポリペプチドを間断なくコードするcDNAなどである。「間断なくコードする」ポリヌクレオチドは、イントロンまたは他の非コード配列を介在させているオープンリーディングフレーム(ORF)と対比して連続したORFをもつポリヌクレオチドをいう。
「遺伝子」は本明細書では、ポリペプチド鎖の産生に関与するDNA断片を意味し、コード領域の先行領域と後続領域(リーダーとトレーラー)、それに個別コード領域(エクソン)間の介在配列(イントロン)を含んでもよい。本発明は、本発明のeNOSをコードする単離遺伝子(たとえばゲノムクローン)を包含する。
本発明のポリヌクレオチドは組換えポリヌクレオチド、天然ポリヌクレオチド、合成または半合成ポリヌクレオチド、またはそれらの組合せでもよい。該ポリヌクレオチドはRNA、PNAまたはDNAたとえばcDNA、ゲノムDNA、および合成または半合成DNA、またはそれらの組合せでもよい。DNAは三本鎖、二本鎖または一本鎖のいずれでもよいし、ヘアピン等の立体構造を含んでもよい。RNAの例はmRNA、ポリアデニル化RNA、全RNA、一本鎖または二本鎖RNAなどである。本発明はDNA/RNA二本鎖も包摂する。
本発明の一実施態様では、eNOSをコードするポリヌクレオチドは天然ポリヌクレオチド配列を有し、たとえばヒト・ポリヌクレオチドである。eNOSをコードするポリヌクレオチドは多数の種で知られており、そうした種の例はヒト[Janssens et al. (1992) J. Biol. Chem. 267, 14:512-522]やウシ(米国特許第5,498,539号明細書)などである。本発明の天然ポリヌクレオチドはたとえば、野生型ポリヌクレオチド配列のアレル変異であるコード配列を有してもよい。アレル変異は周知のように1つまたは複数のヌクレオチドの置換、欠失または付加を含むような代替形のポリヌクレオチド配列であり、一般的にはコード化されるポリペプチドの機能を実質的に変化させない。天然型の一塩基多型(SNPs)を含むポリヌクレオチドを本発明の方法に使用してもよい。
別の実施態様では、本発明の方法に使用されるポリヌクレオチドは天然eNOSポリヌクレオチドの変種でもよい。ここでいうポリペプチドまたはポリヌクレオチドの「変種」は、該変種が野生型eNOSポリペプチドまたはそれをコードするポリヌクレオチドの1つのまたは複数の活性または特性を実質的に保持することを意味する。すなわち変種は、本発明の方法によってCLI患者の細胞、組織または臓器に導入すれば、CLIの1つまたは複数の症状を相当に改善しうるようなポリペプチドまたはポリヌクレオチドである。変種ポリヌクレオチドは野生型、変異型いずれのeNOSポリペプチドをコードしてもよい。
別の実施態様では、変種ポリヌクレオチドは野生型または変異型eNOSポリペプチドの変種(たとえば1つまたは複数の欠失、挿入、付加、置換、逆位または短縮、もしくはそれらの組合せを含むポリペプチド)をコードする。そうした変種ポリペプチドは、保存または非保存アミノ酸好ましくは保存アミノ酸との、1つまたは複数のアミノ酸置換を含んでもよい。被置換アミノ酸の全体の電荷、疎水性/親水性、側鎖部分および/または立体かさ高さを保つ保存的置換の例はGly/Ala、Val/Ile/Leu、Asp/Glu、Lys/Arg、Asn/Gln、Thr/SerおよびPhe/Trp/Tyrなどである。
本発明の方法に使用されるeNOSをコードする変種ポリヌクレオチドの例は、(i)1つまたは複数のヌクレオチドが別のヌクレオチドと置換している、または他の形で変異しているもの、(ii) 1つまたは複数のヌクレオチドが修飾されていて、たとえば置換基を含むもの、(iii)ポリヌクレオチドが他化合物たとえば該ポリヌクレオチドの半減期を延長するための化合物と融合しているもの、(iv)ポリヌクレオチドに追加のヌクレオチド(たとえばリーダー配列または分泌配列またはポリペプチド精製のために使用される配列をコードする追加ヌクレオチド)が共有結合しているもの、などである。該追加ヌクレオチドは異種起源でも、天然遺伝子に固有でもよい。
前記のタイプ(i)に属する変種ポリヌクレオチドの例は多型たとえば一塩基多型(SNPs)、アレル変異および変異型などである。変種ポリヌクレオチドはたとえば1つまたは複数の付加、挿入、欠失、置換、転位、転換、逆位、染色体転座、選択的スプライシングに由来する変種など、およびそれらの任意の組合せを含んでもよい。
前記のタイプ(ii)に属する変種ポリヌクレオチドの例は修飾たとえば検出可能マーカー(アビジン、ビオチン、放射性元素、蛍光標識および色素、エネルギー移動ラベル剤、エネルギー放出ラベル剤、結合パートナーなど)または発現、取り込み、カタログ化、標識、ハイブリダイゼーション、検出および/または安定性を改善する分子部分などの付加などである。
前記のタイプ(iii)に属する変種ポリヌクレオチドの例は種々の長さのpolyA+テール、5’キャップ構造、およびヌクレオチドアナログたとえばイノシン、チオヌクレオチドなどである。
前記のタイプ(iii)に属する変種ポリヌクレオチドの例は種々の長さのpolyA+テール、5’キャップ構造、およびヌクレオチドアナログたとえばイノシン、チオヌクレオチドなどである。
前記のタイプ(iv)に属する変種ポリヌクレオチドの例は多様なキメラ、ハイブリッドまたは融合ポリヌクレオチドである。たとえば本発明のポリヌクレオチドは、コード配列および同じリーディングフレーム内で融合された追加の非天然または異種コード配列(たとえばリーダー、シグナル、分泌、局在化、酵素、蛍光、抗生物質耐性および他のまたは診断用ペプチド)、またはコード配列および非コード配列たとえば5’末端か3’末端の非翻訳配列またはコード配列中に分散した非コード配列(イントロンなど)を含むことができる。
本発明の方法に使用される変種ポリヌクレオチドはまた、本発明のポリペプチドの特定および/または精製を可能にするマーカー配列にフレーム内で融合されたコード配列を有してもよい。該マーカー配列は、たとえば細菌宿主の場合にはマーカーに融合させた成熟ポリペプチドの精製に使用する(たとえばpQE-9ベクターによって供給される)ヘキサヒスチジン標識でもよいし、また哺乳動物宿主たとえばCOS-7細胞を使用する場合には、赤血球凝集素(HA)標識でもよい。該HA標識はインフルエンザ赤血球凝集素タンパク質に由来するエピトープに相当する[Wilson, I. et al. Cell, 37:767 (1984)]。
他タイプの変種ポリヌクレオチドは当業者には自明であろう。たとえばあるポリヌクレオチドの複数のヌクレオチドを、RNAse Hなどのようなヌクレアーゼに対する耐性、in vivo安定性の改善といった所期の目的に応じて種々のリンク手段たとえばエステル、スルファミン酸、スルファミド、ホスホロチオ酸、ホスホロアミド酸、メチルスルホン酸、カルバミン酸を介して結合することができる。たとえば米国特許第5,378,825号明細書を参照。任意所望のヌクレオチドまたはヌクレオチドアナログたとえば6-メルカプトグアニン、8-オキソグアニンなどを組み込むことができる。また、本発明のポリヌクレオチドはある生物の別の遺伝子座に由来するコード配列を、それが野生型eNOSと、または別の生物に由来するものと、実質的相同性を有する限りで、有してもよい(たとえばオーソログ)。
コード配列または調節配列の中に位置する他の変種配列は、本発明のeNOSポリペプチドの産生を、もしくは機能または活性を、増進するかもしれない。
他の変種ポリヌクレオチドは、野生型eNOSをコードする野生型ポリヌクレオチドと種々の度合いの配列相同性(同一性)を有し、または野生型eNOSと種々の度合いの配列相同性(同一性)を有する変種ポリペプチドをコードする。これはもちろん、該変種ポリヌクレオチドまたはポリペプチドが、本発明の方法においてCLI患者に導入されたときに、該疾患の1つまたは複数の症状を改善する能力を維持することが前提である。
他の変種ポリヌクレオチドは、野生型eNOSをコードする野生型ポリヌクレオチドと種々の度合いの配列相同性(同一性)を有し、または野生型eNOSと種々の度合いの配列相同性(同一性)を有する変種ポリペプチドをコードする。これはもちろん、該変種ポリヌクレオチドまたはポリペプチドが、本発明の方法においてCLI患者に導入されたときに、該疾患の1つまたは複数の症状を改善する能力を維持することが前提である。
少なくとも該ポリヌクレオチドまたはポリペプチドは野生型eNOSと実質的に相同であるか、または実質的な配列相同性(配列同一性)を示す。従って、本発明の範囲内のポリヌクレオチド、ポリペプチド、およびその断片は、野生型ポリヌクレオチドまたはポリペプチドとの配列相同性(同一性)が少なくとも約65〜70%、好ましくは約70〜75%、75〜80%、80〜85%または85〜90%、最も好ましくは約90〜95%または95〜99%であるようなポリヌクレオチドまたはアミノ酸配列を含んでもよい。本発明はまた、配列同一性の度合いはもっと低いものの、該eNOSが示す1つまたは複数の機能または活性を果たすに足る配列類似性を有するようなポリヌクレオチドまたはポリペプチドを包摂する。
ポリヌクレオチド配列について「実質的に相同(の)」とは、ヌクレオチド配列の同一性が少なくとも約90〜95%または95〜99%であることを意味する。
配列について「同一性%」または「%同一(の)」とは本明細書では、ある比較対象の配列(比較対象配列)を特許請求配列または開示配列(基準配列)と配列アラインメント後に比較して、次式に従って同一性%を求めたことを意味する:
配列について「同一性%」または「%同一(の)」とは本明細書では、ある比較対象の配列(比較対象配列)を特許請求配列または開示配列(基準配列)と配列アラインメント後に比較して、次式に従って同一性%を求めたことを意味する:
同一性% = 100[1-C/L)]
(式中、Cは基準配列と比較対象配列のアラインメント長にわたる基準配列と比較対象配列の間の差異の数であるが、差異を構成するものは、(i)アラインメント後の比較対象配列の中に対応する塩基またはアミノ酸を欠く基準配列中の各塩基またはアミノ酸、(ii)基準配列中の各ギャップ、および(iii)アラインメント後の比較対象配列中の塩基またはアミノ酸とは異なる基準配列中の各塩基またはアミノ酸である; またRは比較対象配列とのアラインメント長にわたる基準配列中の塩基またはアミノ酸の数であり、基準配列中のギャップはすべて塩基またはアミノ酸として計算する。)
(式中、Cは基準配列と比較対象配列のアラインメント長にわたる基準配列と比較対象配列の間の差異の数であるが、差異を構成するものは、(i)アラインメント後の比較対象配列の中に対応する塩基またはアミノ酸を欠く基準配列中の各塩基またはアミノ酸、(ii)基準配列中の各ギャップ、および(iii)アラインメント後の比較対象配列中の塩基またはアミノ酸とは異なる基準配列中の各塩基またはアミノ酸である; またRは比較対象配列とのアラインメント長にわたる基準配列中の塩基またはアミノ酸の数であり、基準配列中のギャップはすべて塩基またはアミノ酸として計算する。)
比較対象配列と基準配列の間に、前記の要領で計算した同一性%が規定の最低同一性%以上であるようなアラインメントが存在する場合には、前記の要領で計算した同一性%が規定の最低同一性%を下回る可能性のあるアラインメントがたとえ存在するとしても、該比較対象配列は基準配列に対して規定の最低同一性%を有することになる。
好ましい実施態様では、基準配列のうち比較目的のためにアラインメントをとる長さは、該基準配列の長さの30%以上、好ましくは40%以上、もっと好ましくは50%以上、さらになお好ましくは60%以上、さらになお好ましくは70%、80%または90%以上である。
同一性%または相同性%に関する本明細書の開示はヌクレオチドまたはアミノ酸配列に等しく適用されるものとする。
好ましい実施態様では、基準配列のうち比較目的のためにアラインメントをとる長さは、該基準配列の長さの30%以上、好ましくは40%以上、もっと好ましくは50%以上、さらになお好ましくは60%以上、さらになお好ましくは70%、80%または90%以上である。
同一性%または相同性%に関する本明細書の開示はヌクレオチドまたはアミノ酸配列に等しく適用されるものとする。
配列比較と両配列間の同一性または類似性%の決定は数理アルゴリズムを使用して行うことができる[Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part 1, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; and Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991]。
そうした数理アルゴリズムの好ましい非限定的な例はKarlin et al. (1993) Proc. Natl. Acad. Sci. USA 90:5873-5877で開示されている。そうしたアルゴリズムは、Altschul et al. (1997) Nucleic Acids Res. 25:3389-3402で開示のNBLASTおよびXBLASTプログラム(version 2.0)に組み込まれている。BLASTおよびGapped BLASTプログラムを使用するときは、各プログラム(たとえばNBLAST)のデフォルトパラメーターを使用することができる。一実施態様では、配列比較パラメーターをスコア=100、ワード長=12として設定することができるが、変更も可能である(たとえばW=5またはW=20)。
好ましい実施態様では、両アミノ酸配列間の同一性%がGCGソフトウェアパッケージ中のGAPプログラムに組み込まれているNeedleman et al. (1970)(J. Mol. Biol. 48:444-453)アルゴリズムにより、BLOSUM62マトリックスまたはPAM250マトリックス、およびギャップウェイト16、14、12、10、8、6または4、および長さウェイト1、2、3、4、5または6を使用して決定される。さらに別の実施態様では、両ヌクレオチド配列間の同一性%がGCGソフトウェアパッケージ中のGAPプログラムI [Devereux et al. (1984) Nucleic Acids Res. 12(1):387] により、NWSgapdna CMPマトリックス、ギャップウェイト40、50、60、70または80および長さウェイト1、2、3、4、5または6を使用して決定される。
配列比較に使用される数理アルゴリズムの別の好ましい非限定的な例はMyers and Miller, CABIOS (1989)のアルゴリズムである。そうしたアルゴリズムは、CGC配列アラインメントソフトウェアパッケージの一部であるALIGNプログラム(version 2.0)に組み込まれている。ALIGNプログラムをアミノ酸配列の比較に使用するときは、PAM120 weight residue table、ギャップ長ペナルティ12、およびギャップペナルティ4を使用することができる。追加の配列解析用アルゴリズムも公知であり、Torellis et al. (1994) Comput. Appl. Biosci. 10:3-5で開示されているADVANCEやADAM、それにPearson et al. (1988) PNAS 85:2444-8で開示されているFASTAなどがある。
タンパク質配列について「実質的に相同(の)」とは本明細書では、アミノ酸配列の同一性が約90〜95%または97〜99%以上であることを意味する。実質的に相同のアミノ酸配列は、本発明の変異型ポリペプチドをコードする核酸配列またはその一部と、高ストリンジェンシー条件下で、ハイブリダイズする核酸配列によってコードされうる。
「高ストリンジェンシー」条件は本明細書では、たとえばブロットを一晩(たとえば12時間以上)、長いポリヌクレオチドプローブと、たとえば約5×SSC、0.5% SDS、100μg/ml変性処理サケ精子DNAおよび50%ホルムアミドを含むハイブリダイゼーション液中、42℃でインキュベートすることを意味する。ブロットの洗浄は、たとえばミスマッチを5%bp未満とし、もって同一性95%超の配列の選択を可能にするような高ストリンジェンシー条件(たとえば0.1×SSC+0.1%SDS中、65℃での30分間の洗浄を2回)で行うことができる。
他の高ストリンジェンシー条件の非限定的な例は、30mM NaClおよび0.5%SDSを含む緩衝水溶液65℃での最終洗浄などである。別の高ストリンジェンシー条件の例は、7% SDS、0.5M NaPO4(pH 7.1)、7.1mM EDTA中、50℃での、たとえば一晩のハイブリダイゼーションと、それに続く1% SDS溶液、42℃での1回または複数回の洗浄である。高ストリンジェンシー洗浄は許容ミスマッチを5%未満とするが、低ストリンジェンシー条件では20%までのヌクレオチドミスマッチを許容する。こうした低ストリンジェンシー条件でのハイブリダイゼーションも可能であるが、その場合にはホルムアミド濃度、温度および/または塩濃度を低くし、インキュベーション時間を長くする。
本発明のポリヌクレオチド断片は、本発明と両立しうる限りで任意のサイズ(たとえばCLI患者に導入したときに治療効果を実現するうえで有効な任意所望のサイズ)でよい。たとえば本発明のポリヌクレオチド断片は全長遺伝子産物よりもやや短くてもよい。たとえば本発明のポリペプチドは少なくとも約10、25、50、100、200、300、400、500、600、800、1000または1200個のアミノ酸を含んでもよい。本発明のポリヌクレオチドはまた、たとえば融合ポリヌクレオチドまたはゲノム配列の一部であるポリヌクレオチドの場合には、全長cDNAより長くてもよい。
本発明のポリヌクレオチドは任意所望の方法で標識することができる。該ポリヌクレオチドはたとえば32P、35S、3Hまたは14Cなどの放射性トレーサーを使用して標識することができる。放射性標識は任意の方法で行うことができる。たとえば3’または5’末端の末端標識であるが、これには放射性ヌクレオチド、ポリヌクレオチドキナーゼ(ホスファターゼによる脱リン酸化を伴うまたは伴わない)またはリガーゼ(標識対象の末端次第)を用いることができる。非放射性標識の使用も可能であり、その場合は本発明のポリヌクレオチドに、免疫学的性質をもつ残基(抗原、ハプテン)、特定試薬に対し特異的なアフィニティーをもつ残基(リガンド)、検出可能な酵素反応を完了させる性質をもつ残基(酵素または補酵素、酵素基質、または酵素反応に関与する他の物質)、または特徴的な物理的性質(蛍光、所望波長での発光または吸光)をもつ残基などを結合させる。
eNOSポリペプチド
本発明はさらに、eNOSポリペプチドとその変異型に関する。
ヒトeNOS(たとえば配列番号:1がコードするヒトeNOS)の好適な変異の非限定的な例は:
(a) アミノ酸残基1177に対応するリン酸化部位の変異、すなわち該残基の他アミノ酸たとえばAspへの置換(S1177D)(国際公開WO 00/62605号明細書などを参照);
本発明はさらに、eNOSポリペプチドとその変異型に関する。
ヒトeNOS(たとえば配列番号:1がコードするヒトeNOS)の好適な変異の非限定的な例は:
(a) アミノ酸残基1177に対応するリン酸化部位の変異、すなわち該残基の他アミノ酸たとえばAspへの置換(S1177D)(国際公開WO 00/62605号明細書などを参照);
(b) アミノ酸残基2に対応するミリストイル化部位の変異、すなわち該残基の他アミノ酸たとえばAlaへの置換(G2A)(Sessa et al. (1993), Circulation Research 72, 921-924などを参照)。ミリストイル化部位変異型のeNOSポリペプチドは細胞膜よりもむしろ細胞質中に局在する可能性がある。そうした変異型は(野生型タンパク質に比して)eNOS/NO産生を抑制する病的刺激(oxLDLなど)に対して耐性である可能性がある。そうした性質は、変異型ポリペプチド(またはそれをコードするポリヌクレオチド)の、そうした病的外部刺激が存在するCLIの治療への使用に有利かもしれない);
(c) カルモジュリン結合部位(たとえば配列番号:1のアミノ酸478-522)内の変異、すなわち哺乳動物細胞ではリン酸化していると判明している該ドメイン内の一アミノ酸残基特にアミノ酸残基495に対応する変異。好ましい実施態様では、495に対応するアミノ酸残基の変異はAla、Gly、Val、Leu、Ile、Pro、Phe、Tyr、Trp、Met、Ser、Cys、Glu、Gln、Lys、ArgまたはHisへのアミノ酸置換であり、Ala、Val、LeuまたはIleへの置換であるのがなお好ましく、またAlaまたはValへの置換であるのが最も好ましい。そうした変異型はたとえば、本明細書にその全体が組み込まれる同時係属の米国出願第60/403,638号明細書で開示されている。
同時係属の米国出願第60/403,638号明細書はまた、eNOS活性を増進するような他の種々の変異をも開示している。そうした変異はeNOS分子の前記部位、前記機能性ドメイン内の他残基、または他の機能性ドメインのいずれに位置してもよい。
eNOSポリペプチドの、変異を導入しうる機能性ドメインは解析が十分に進んでおり(図1)、その例は(N末端からC末端へと順に)ミリストイル化コンセンサス配列部位、2つのパルミトイル化部位、酸化酵素ドメイン、(たとえば配列番号:1がコードするヒトeNOSのThr-495の)リン酸化コンセンサス配列部位を含むカルモジュリン結合部位(たとえば配列番号:1がコードするヒトeNOSのアミノ酸494-517)、および(たとえば配列番号:1がコードするヒトeNOSのSer-1177の)リン酸化コンセンサス配列を含む還元酵素ドメインなどである。
eNOSポリペプチドの、変異を導入しうる機能性ドメインは解析が十分に進んでおり(図1)、その例は(N末端からC末端へと順に)ミリストイル化コンセンサス配列部位、2つのパルミトイル化部位、酸化酵素ドメイン、(たとえば配列番号:1がコードするヒトeNOSのThr-495の)リン酸化コンセンサス配列部位を含むカルモジュリン結合部位(たとえば配列番号:1がコードするヒトeNOSのアミノ酸494-517)、および(たとえば配列番号:1がコードするヒトeNOSのSer-1177の)リン酸化コンセンサス配列を含む還元酵素ドメインなどである。
前記カルモジュリン結合部位、DPWKGS AAKGTGITRKKT FKEVANAVKISASL MGTVMAKRVKATI(たとえば配列番号:2、配列番号:1のアミノ酸残基478-522)には、Thr-495の置換以外のさらなる変異を導入することができる。他種の比較可能配列は特にリン酸化部位のN末端側残基がやや異なる可能性がある(図1の配列番号S:3-7を参照)。このモチーフ中の各アミノ酸は他の天然アミノ酸19種のうち任意のアミノ酸に、または非天然アミノ酸に、置換することができる。実施態様によっては、該変異は保存的変異(たとえばGly/Ala、Val/Ile/Leu、Asp/Glu、Lys/Arg、Asn/Gln、Thr/SerまたはPhe/Trp/Tyr)ではない。一実施態様では、配列番号:1のThr-495に対応するアミノ酸残基のすぐC末端側に位置する本発明のeNOSポリペプチドの1つまたは複数の残基たとえば残基496または498はArgまたはLysへと置換される。
本発明はまた、eNOSポリペプチドの他の機能性ドメイン内で1つまたは複数のアミノ酸が修飾されているeNOSポリペプチドを包含する。たとえば1つまたは複数の変異を、1つまたは複数の触媒ドメイン(たとえば酸化酵素または還元酵素ドメイン)または調節領域(たとえば自己阻害ループ)、あるいは本明細書で開示の、または公知の、他の任意の機能性ドメインに、導入することができる。該追加変異は本明細書で開示の任意のタイプの変異でよい。
本明細書で開示の任意の複数の変異の組合せを有する変異型ポリペプチドもまた本発明に使用可能である。好ましい実施例では、本発明の変異型eNOSポリペプチドは少なくとも2つの機能性ドメインに変異を有し、また出発または基準ポリペプチドよりも強いeNOS活性を示す。必要なら、1つのそうした追加変異を導入、解析した後に、同じ操作を、両機能性ドメインまたは別の機能性ドメインに第3変異を導入、解析するまで反復することができる、等々。
実施態様によっては、変異型eNOSポリペプチドの活性(たとえばNO産生の刺激)が各変異の追加ごとに増大し続ける。好ましい実施態様では、変異型ヒトeNOSポリペプチドは配列番号:1のThr-495およびSer-1177に対応する位置における(それぞれAla、Val、LeuまたはIle好ましくはAlaまたはValへの、および好ましくはAlaへの)アミノ酸置換およびミリストイル化部位のGlu-2における(好ましくはAlaへの)アミノ酸置換の組合せを含む。最も好ましい実施態様では、本発明のポリヌクレオチドはS1177D変異とG2A変異; S1177D変異とT495VまたはT495A変異; G2A変異とT495VまたはT495A変異; またはS1177D変異、G2A変異およびT495VまたはT495A変異をコードする。
本発明のeNOSがヒト以外の哺乳動物に由来するときは、該eNOS中の比較可能(相当)残基を変異させることができる。そうした生物の比較可能残基は技術上周知である。たとえばヒトeNOSの残基495はマウスでは残基494、モルモットでは残基498、イヌ、ウシ、ブタでは残基497、ラットでは残基22、ウサギでは残基40に対応する。
そうした変異型を生成させる方法は技術上慣用、周知であり、その例は相同組換え、部位指定変異法、カセット変異法、PCR系変異法などである[Sambrook et al., Molecular Cloning, CSH Press (1989)およびKunkel et al. (1985) PNAS 82, 488-492を参照]。そうした変異のための出発材料は任意の動物たとえばヒト、マウス、モルモット、イヌ、ウシ、ブタ、ウサギ、ラット、ヒツジ、ウマ、ヒト以外の霊長類等に由来するeNOS cDNAとすることができる。
前記のような変異型がeNOS活性の増進を示すかどうかは種々の標準試験により判定することができる。各種eNOS活性の試験が可能であり、あるいは本発明の遺伝子療法を使用してCLIの1つまたは複数の症状を緩和するという変異型eNOSポリヌクレオチドの能力を直接測定することもできる(実施例を参照)。
eNOSは数多くの生理反応において、L-Argを反応に関与する気体性の第2メッセンジャー分子に変換し、および/または調節機能を果たす。特定の機序にこだわるつもりはないが、eNOSをコードするポリヌクレオチドを病変細胞または組織に導入すると、eNOSが仲介する1つまたは複数の活性がCLI症状の緩和に寄与するとの考え方が提唱されている。
たとえばeNOSは次の作用を直接または間接に(たとえば産生するNOを通じて)仲介する: 血管新生の刺激; 微小血管機能障害の改善; 血管拡張の刺激; 側副血管形成の刺激; 四肢末梢血流の増進; 肢壊死の阻害; 皮膚潰瘍形成の阻害; 皮膚潰瘍治癒の増進; (血栓形成につながる)血小板接着および凝集の阻害または防止; 内皮細胞増殖および遊走の刺激; 白血球活性化および接着または平滑筋増殖の阻害; 免疫反応の調節; およびスーパーオキシドアニオンの消去。これらや他のeNOS活性の試験方法は技術上慣用周知である。たとえば側副血管依存性の虚血肢における毛細血管密度または血管運動反応性の向上によって裏付けられる肢壊死阻害を測定する方法などである[Murohara et al. (1998) J. Clin. Invest., 101, 2567-2568などを参照]。本明細書実施例をも参照。
eNOS活性試験用の動物モデルは技術上慣用周知である。たとえば前掲[Murohara et al. (1998); Couffinhal et al. (1998); Am J. Pathol 152, 1667-1669; Couffinhal et al. (1999) Circulation 99, 3188-3198; および本明細書実施例を参照。そうした試験の例はマウスおよびラットの外科的後肢虚血モデルであり、そこではたとえばeNOS欠損マウスに手術で虚血を起こさせる。前記参考文献では後肢血流および毛細血管密度の測定方法も開示されている。
変異型eNOSポリペプチドをコードする組換えベクター
本発明はまた本発明のポリヌクレオチドを含む組換えベクター、本発明の組換えベクターを含む宿主細胞、および本発明のポリペプチドの生産に関する。
本発明はまた本発明のポリヌクレオチドを含む組換えベクター、本発明の組換えベクターを含む宿主細胞、および本発明のポリペプチドの生産に関する。
本発明は、eNOSポリペプチドをコードするポリヌクレオチドを挿入した組換えベクターに関する。そうしたポリヌクレオチドは天然物から直接単離し、好適な発現ベクター中にクローニングしてもよいし、人為的に操作して天然型または変異型配列をもつようにしてもよい。DNAを変異させ、クローニングし、発現させる方法または本明細書で言及する他の分子生物学的方法は常法であり、種々の教科書や参考書で開示されている。たとえばSambrook, et al. Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor, N.Y., (1989); Wu et al. Methods in Gene Engineering (CRC Press, New York, NY, 1997); Recombinant Gene Expression Protocols, in Methods in Molecular Biology, Vol. 62 (Tuan, ed., Humana Press, Totowa, NJ, 1997); Current Protocols in Molecular Biology (Ausubel et al. Eds.) John Wiley & Sons, NY (1994-1999)を参照。
本発明は、前述のようなeNOSポリペプチドをコードするポリヌクレオチドを挿入して好適な発現調節配列(たとえばプロモーター及び/またはエンハンサー)と作動可能に連結させ、該eNOSポリペプチドが発現するようにした発現ベクター(たとえばプラスミドまたはウイルス発現ベクター)を含む組換えコンストラクトに関する。
そうしたコンストラクトは、本明細書で開示するようなin vivo遺伝子療法またはex vivo(細胞ベース)遺伝子療法のいずれかに使用することができる。
そうしたコンストラクトは、本明細書で開示するようなin vivo遺伝子療法またはex vivo(細胞ベース)遺伝子療法のいずれかに使用することができる。
哺乳動物細胞たとえばヒト細胞用に、好適な発現調節配列たとえば真核細胞またはそのウイルス中で遺伝子の発現を調節することが知られている構成的または調節性プロモーターまたは他の配列(エンハンサー)を選択することができる。種々のそうした発現調節配列が技術上周知である。内在性または異種性の発現調節配列が使用可能である。発現調節配列は組織特異的でもよい。一実施態様では、発現調節配列は高発現遺伝子に由来する。発現調節配列は任意所望の遺伝子から、たとえばCAT(クロラムフェニコールトランスフェラーゼ)ベクターまたは他の選択マーカー付きベクターを使用して選択することができる。そうした選択用の好適なベクターはpKK232-8とpCM7の2つである。
本発明の組換えベクターに使用することができる好適なプロモーターはたとえば真核生物プロモーター: CMV前初期、HSVチミジンキナーゼ、初期および後期SV40、アデノウイルス、レトロウイルス由来LTRs、およびマウスメタロチオネインIの各プロモーターなどである。好適なベクターおよびプロモーターの選択は十分に当業者のレベル内にある。
本発明のeNOSポリペプチドをコードするポリヌクレオチド配列の転写は、発現ベクターへのエンハンサー配列の挿入により増進することができる。エンハンサーは通常10〜300bpのシスエレメントであり、プロモーターに作用して転写を増進させる。代表例は複製起点の後期側のSV40エンハンサー100〜270bp、CMV前初期プロモーターエンハンサー、複製起点の後期側のポリオーマエンハンサー、およびアデノウイルスエンハンサーである。
本発明のeNOSポリペプチドをコードするポリヌクレオチド配列の転写は、発現ベクターへのエンハンサー配列の挿入により増進することができる。エンハンサーは通常10〜300bpのシスエレメントであり、プロモーターに作用して転写を増進させる。代表例は複製起点の後期側のSV40エンハンサー100〜270bp、CMV前初期プロモーターエンハンサー、複製起点の後期側のポリオーマエンハンサー、およびアデノウイルスエンハンサーである。
一般に、組換え発現ベクターもまた複製起点を含む。発現ベクターは翻訳開始のためのリポソーム結合部位、転写終結配列、ポリアデニル化部位、スプライス供与および受容部位、および/または5末端側の周辺または非転写配列を含んでもよい。所望の非転写遺伝要素の提供にはSV40スプライスおよびポリアデニル化部位に由来するDNA配列を使用してよい。該ベクターはまた、発現増幅用の好適な配列を含んでもよい。さらに発現ベクターは好ましくは、形質転換した宿主細胞を選択するための表現形質(たとえば真核細胞培養のためのジヒドロ葉酸還元酵素またはネオマイシン耐性)を与える1つまたは複数の選択マーカー遺伝子を含む。
多数の好適な組換え発現ベクターが技術上周知であり、市販品も多い。好適なベクターの例は染色体、非染色体および合成DNA配列たとえばSV40誘導体; バキュロウイルス; 酵母ベクター; プラスミドとウイルスDNAの組合せに由来するベクター; およびワクシニアウイルス、アデノウイルス、アデノ随伴ウイルス、TMV、鶏痘ウイルス、オーエスキー病ウイルスなどのようウイルスDNAなどである。しかし宿主中での複製能、生存能をもつ限り他の任意のベクターを使用してもよい。好適なクローニング/発現ベクターはたとえば前掲のSambrook et al.や他参考文献で開示されている。
遺伝子療法に特に有用な組換えベクターの例は、関心のある特定ポリヌクレオチドを運搬または発現するように構築した組換えレトロウイルスなどである。使用可能なレトロウイルスベクターの例は欧州特許第0415731号明細書; 国際公開第WO 90/07936号、WO 94/03622号、WO 93/25698号、WO 93/25234号の各明細書; 米国特許第5,219,740号明細書; 国際公開第WO 93/11230号およびWO 93/10218号の各明細書; Vile and Hart, Cancer Res. 53:3860-3864 (1993); Vile and Hart, Cancer Res. 53:962-967 (1993); Ram et al., Cancer Res. 53:83-88 (1993); Takamiya et al., J. Neurosci. Res. 33:493-503 (1992); Baba et al.,J. Neurosurg. 79:725-735 (1993); 米国特許第4,777,127号明細書; 英国特許第2,200,651号、欧州特許第0345242号および国際公開第WO 91/02805号の各明細書で開示されている。
前記レトロウイルスベクターコンストラクト用の好適なパッケージング細胞株は作製が容易であり(国際公開第WO 95/30763号明細書やWO 92/05266号明細書などを参照)、組換えベクター粒子産生用の産生系細胞株(別名ベクター細胞株)の作製への使用も容易である。本発明の好ましい実施態様では、パッケージング細胞株をヒト親細胞株(HT1080細胞など)またはミンク親細胞株から作製し、もってヒト血清中での不活性化に耐え切れるような組換えレトロウイルスの産生を可能にする。
本発明はまたアルファウイルス系ベクターを使用する。そうしたベクターは、たとえばシンドビスウイルス、セムリキ森林ウイルス(ATCC VR-67; ATCC VR-1247)、ロス河ウイルス(ATCC VR-373; ATCC VR-1246)、ベネズエラ馬脳炎ウイルス(ATCC VR-923; ATCC VR-1250; ATCC VR-1249; ATCC VR-532)などを含む多様なウイルスから構築することができる。そうしたベクター系の代表例は米国特許第5,091,309号、5,217,879号、5,185,440号の各明細書; および国際公開第WO 92/10578号、WO 94/21792号、WO 95/27069号、WO 95/27044号、WO 95/07994号の各明細書などで開示されている。
好適なベクターはアデノ随伴ウイルス(AAV)ベクターなどのようなパルボウイルスでもよい。代表例はSrivastava(WO 93/09239); Samulski et al., J. Vir. 63:3822-3828 (1989); Mendelson et al., Virol. 166:154-165 (1988); Flotte et al., PNAS 90:10613-10617 (1993)で開示されているAVVベクターなどである。
好ましい実施態様ではアデノウイルスベクターを使用する。種々の改良アデノウイルスベクター(たとえばAd5またはAd2由来)、特に非複製型ベクターおよび/または非ヘルパー依存型ウイルスが技術上周知である。アデノウイルスベクターの代表例はBerkner, Biotechniques 6:616; Rosenfeld et al., Science 252:431-434 (1991); WO 93/19191; Kolls et al., PNAS 215-219 (1994); Kass-Eisler et al., PNAS 90:11498-11502 (1993); Guzman et al., Circulation 88:2838-2848 (1993); Guzman et al., Cir. Res. 73: 1202-1207 (1993); Zabner et al., Cell 75:207-216 (1993); Li et al., Hum. Gene Ther. 4:403-409 (1993); Cailaud et al., Eur. J. Neurosci. 5: 1287-1291 (1993); Vincent et al., Nat. Genet. 5:130-134 (1993); Jaffe et al., Nat. Genet. 1:372-378 (1992); Levrero et al., Gene 101:195-202 (1992)で開示されている。
本発明への使用が可能な遺伝子療法用アデノウイルスベクターの例は国際公開第WO 94/12649号、WO 93/03769号、WO 93/19191号、WO 94/28938号、WO 95/11984号およびWO 95/00655号の各明細書で開示されている。Curiel, Hum. Gene Ther. 3:147-154 (1992)で開示されているアデノウイルス結合(たとえば標的化)DNAを使用してもよい。
好適なDNA配列をベクターに挿入するには多様な方法のうち任意のものを用いてよい。一般に、DNA配列は好適な制限酵素認識部位に、公知の方法で挿入することができる。そうしたあれこれの方法は当業者の範囲内にあるものとみなされる。本明細書で述べているあれこれの分子生物学的技術のための常法はすぐに閲覧できる文献たとえばSambrook et al., Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor, N.Y., (1989)などで開示されている。また、たとえばアデノウイルス遺伝子デリバリー担体の構築に有用なレスキュー組換え技術に関するGraham et al. (1988) Virology 63, 614-617を参照。本発明はまた、前記のようなコンストラクトを使用して種々の方法で遺伝子を導入した(またはウイルスを感染させた)宿主細胞および該細胞の子孫に関する[特にそうした細胞が、CLI治療を必要とする患者に移植(または再移植)しうる安定細胞株をもたらす場合]。
細胞ベース遺伝子療法のための好適な宿主の非限定的な例は骨格筋細胞、平滑筋細胞、骨髄由来幹細胞、血管内皮前駆細胞、線維芽細胞、樹状細胞、臍帯血由来細胞、および内皮細胞などである。宿主細胞へのコンストラクトのin vitro導入は任意好適の方法で行うことができる。たとえばリン酸カルシウム法、DEAEデキストラン法、リポフェクション法、遺伝子銃法、またはエレクトロポレーション法などである[Davis, L., Dibner, M., Battey, I., Basic Methods in Molecular Biology, (1986)]。
好適な宿主株の形質転換と該宿主株の適正細胞密度までの増殖に次いで、必要なら特定プロモーターを適正な手段(たとえば温度シフトまたは化学誘導)によって誘導し、細胞をさらなる期間にわたり培養することができる。遺伝子を導入した宿主細胞は、(必要ならば)プロモーターを活性化し、形質転換細胞を選択し、本発明遺伝子を増幅し、および/または細胞ベース遺伝子療法用に細胞を増殖させるように適宜改良した通常の栄養培地で培養することができる。温度やpHなどの細胞培養条件は、発現用に選択した宿主細胞に使用したものと同じであり、また当業者には自明であろう。
eNOSポリペプチドおよびポリヌクレオチドの使用によるCLI遺伝子療法
末梢動脈閉塞性疾患(PAOD)の進行による重症肢虚血(CLI)は、とりわけ進行性の微小循環系機能障害および血管新生障害を特徴とする。本発明は、野生型または変異型eNOSポリペプチドまたはそうしたポリペプチドをコードするポリヌクレオチドを使用してCLI患者(たとえばFontaine III 度またはIV度PAODの患者)を治療し、たとえば微小循環系機能障害または血管新生障害、白血球活性化、血小板凝集、毛細血管栓塞、内皮機能障害、一酸化窒素バイオアベイラビリティーの低下、内皮損傷、フリーラジカルの放出、組織損傷、壊死、安静時痛、足関節または足趾収縮期血圧の上昇および/または皮膚潰瘍などを非限定的に含むCLIの1つまたは複数の症状を改善するための遺伝子療法に関する。そうした療法の効果は損傷組織の内部または周辺における血管新生および/または血管拡張および/または創傷治癒の改善である。
末梢動脈閉塞性疾患(PAOD)の進行による重症肢虚血(CLI)は、とりわけ進行性の微小循環系機能障害および血管新生障害を特徴とする。本発明は、野生型または変異型eNOSポリペプチドまたはそうしたポリペプチドをコードするポリヌクレオチドを使用してCLI患者(たとえばFontaine III 度またはIV度PAODの患者)を治療し、たとえば微小循環系機能障害または血管新生障害、白血球活性化、血小板凝集、毛細血管栓塞、内皮機能障害、一酸化窒素バイオアベイラビリティーの低下、内皮損傷、フリーラジカルの放出、組織損傷、壊死、安静時痛、足関節または足趾収縮期血圧の上昇および/または皮膚潰瘍などを非限定的に含むCLIの1つまたは複数の症状を改善するための遺伝子療法に関する。そうした療法の効果は損傷組織の内部または周辺における血管新生および/または血管拡張および/または創傷治癒の改善である。
治療を必要とする患者への本発明のポリヌクレオチドまたはポリペプチドのデリバリーはin vivoで(たとえば該ポリヌクレオチドまたはポリペプチドを患者に直接投与して)、またはex vivoで(たとえば該ポリヌクレオチドまたはポリペプチドを細胞に、たとえば治療対象の患者から採取した細胞またはそれに由来する細胞株もしくは治療対象の患者に由来しない細胞または細胞株に導入し、このトランスフェクト細胞を患者に導入して)、行うことができる。
本発明の方法はeNOSをコードするポリヌクレオチドを有効量、遺伝子デリバリー担体ごとおよび/またはトランスフェクト細胞ごと、必要とする患者に投与するステップを含む。「有効量」は本明細書では、CLIの1つまたは複数の症状たとえば本明細書で開示の症状の測定可能または検出可能な減退または阻害を実現しうる量を意味する。
ex vivo(細胞ベース)遺伝子療法は常法である。発現可能なeNOS遺伝子を含む好適な細胞はすでに開示している。該細胞の患者への導入には、種々の好適な常法のうち任意の方法たとえば注入、移植(grafting、transplantation、implantation)、静脈内投与、担体包埋細胞のデリバリー、または本明細書で開示する種々のin vivo投与方法を用いることができる。他のデリバリー促進方法を使用してもよい。その非限定的な例はヒアルロニダーゼ注入法、エレクトロポレーション法、およびソノポレーション法である。
in vivo投与では、eNOSをコードするポリヌクレオチドを含む前記のようなコンストラクト(本明細書では「遺伝子デリバリー担体」ともいう)を、必要とする患者に、任意の常法により投与することができる。コンストラクトのデリバリーは局所的にも全身的にも可能である。好適なin vivoデリバリー経路は技術上周知であり、その非限定的な例は静脈内、筋内、腹腔内、皮内、動脈内および経口などの方法である。一般的な方法については、Jolly, Cancer Gene Therapy 1:51-64 (1994); Kimura, Human Gene Therapy 5:845-852 (1994); Connelly, Human Gene Therapy 1:185-193 (1995); およびKaplitt, Nature Genetics 6:148-153 (1994)などを参照。
遺伝子デリバリー担体は、通常の方法を用いて通常の製薬上許容しうる賦形剤または担体を含む製剤組成物へと調製することができる。薬剤の細胞膜貫通を増進する(浸透を促進する)ような、または分解しにくくするような製剤または賦形剤もまた技術上周知である。たとえば(ポリヌクレオチドなどのin vivoまたはex vivo導入用の)デリバリー担体は、SF-cholまたはDC-cholなどのコレステロール誘導体を含む陽イオンリポソームを使用するリポフェクション法; 合成DNA法(PINCなど); およびリポフェクタミンによるトランスフェクション法などを含む多様な常法のうち任意の方法により標的細胞に送達してもよい。一般的な方法は米国特許第5,656,565号明細書; Mannino et al. (1988) BioTechniques 6:682-690および所載の参考文献; およびGao et al. (1991) Biochem Biophys Res Comm 179:280-285などで開示されている。
一実施態様では、遺伝子デリバリー担体をCLI患者の病態発現部位に対し局所的に投与する。そうした局所的なデリバリーでは、たとえば非病変細胞または組織におけるNOの誘発に由来する無用の効果(たとえば副作用)を避けることができる。たとえば本発明のポリヌクレオチドは、片方または両方の大腿動脈の近位部分に挿入したカテーテルによって送達し、もって該大腿動脈からの血流を受け取る骨格筋細胞への導入を図ってもよい(米国特許第5,792,453号明細書などを参照)。末梢血管系または病変組織たとえば骨格筋への直接注入もまた、隔離組織灌流たとえば大腿動脈と大腿静脈の間に閉回路を設ける隔離肢灌流(ILP)と同様に、使用可能である(国際公開第WO 01/03728号明細書などを参照)。
別の実施態様では、常法により治療用ポリヌクレオチドを全身的に投与するが、該ポリヌクレオチドは関心のある細胞、組織または臓器に誘導されるよう改良してある。たとえばポリヌクレオチドは組織特異的な発現調節配列たとえばプロモーターまたはエンハンサーの制御下に置くことができる。
たとえば組織特異的な内皮転写調節配列をコンストラクト(たとえばアデノウイルスコンストラクト)内の導入遺伝子(たとえば本発明のeNOS遺伝子)へと融合すれば、導入遺伝子の発現を内皮細胞に限定することができる。内皮特異的プロモーターの例はTie-2プロモーター[Schlaeger et al. (1997) Proc Natl Acad Sci 1:94(7):3058-63]、内皮プロモーター[Lee et al. (1990) J. Biol. Chem. 265: 10446-10450]、およびeNOSプロモーター[Zhang et al. (1995) J. Biol. Chem. 270(25):15320-6]などである。Flt-1およびFlk-1プロモーターを使用してもよい[たとえばBu et al. (1997) J. Biol. Chem. 272:3216-32622を参照]。他のプロモーター候補は合成および天然の平滑筋特異的プロモーター[たとえばHauser et al. (2000) Mol. Therapy 2:16-24を参照]; Spc5-12合成プロモーター[Li et al. Nature (1999) 17:241-245]および国際公開第WO 99/02737号明細書などである。
他の遺伝子デリバリー担体および方法を使用してもよいが、その例は、アデノウイルスだけに結合または非結合した(たとえば標的化した)ポリカチオン性縮合DNA[たとえばCuriel, Hum. Gene Ther. 3:147-154 (1992)を参照]; リガンド結合DNA[たとえばWu, J. Biol. Chem. 264:16985-16987 (1989)を参照]; 真核細胞デリバリー担体細胞(たとえば1994年5月9日出願の米国出願第08/240,030号明細書、それに米国出願第08/404,796号明細書を参照); 光重合ヒドロゲル付着; 手持ち型遺伝子導入用パーティクルガン(たとえば米国特許第5,149,655号明細書を参照); 電離放射線(米国特許第5,206,152号明細書および国際公開第WO 92/11033号明細書を参照); 核電荷中和または細胞膜との融合などである。追加のアプローチはPhilip, Mol. Cell Biol. 14:2411-1418 (1994)およびWoffendin, Proc. Natl. Acad. Sci. 91:1582-1585 (1994)で開示されている。
裸DNAを使用してもよい。裸DNAの導入方法は国際公開第WO 90/11092号明細書および米国特許第5,580,859号明細書などで例示されている。生物分解性ラテックスビーズの使用により取込み効率を高めてもよい。DNAをコートしたラテックスビーズは、ビーズによるエンドサイトーシス開始後、細胞中に効率的に輸送される。この方法は、ビーズの処理によりその疎水性を高めて、エンドソーム破壊と細胞質中へのDNA放出を促すようにすることで、さらに改善を図ってもよい。遺伝子デリバリー担体として機能しうる好適なリポソームはたとえば米国特許第5,422,120号明細書、国際公開第WO 95/13796号、WO 94/23697号およびWO 91/14445号の各明細書、ならびに欧州特許第0524968号明細書で開示されている。
さらに、使用に好適な非ウイルス性デリバリー方法には機械的デリバリーシステムたとえばWoffendin, Proc. Natl. Acad. Sci. 91:11582-11585 (1994)で開示されているようなアプローチもある。また、コード配列や転写産物を光重合ヒドロゲル付着法で送達することもできる。コード配列のデリバリーに使用しうる他の慣用の遺伝子デリバリー方法には手持ち型遺伝子導入用パーティクルガン(たとえば米国特許第5,149,655号明細書を参照); および電離放射線の使用による導入遺伝子の活性化(米国特許第5,206,152号明細書および国際公開第WO 92/11033号明細書を参照)などがある。
プラスミドDNAとの複合体の形成による(i)急速なヌクレアーゼ消化からのプラスミドの保護、(ii)骨格筋などの標的組織へのインタクトプラスミドの分散保持および(iii)筋細胞によるプラスミド取込みの促進を目的に、ポリ(Nビニルピロリドン)やポリ(ビニルアルコール)などのようなPINC (“protective,interactive,noncondensing”)ポリマーがすでに開発されている(Mumper et al., 1996; Rolland and Mumper, 1998)。Mumper et al. (1998)は、該PINCポリマーが血清アルカリホスファターゼ(SEAP)、ヒト成長ホルモンおよびヒトIGF-1を含む種々の導入遺伝子をコードするプラスミドDNAのラットでの骨格筋へのトランスフェクション効率を(10〜15倍)増進し発現持続時間を延ばす(28日)ことを示した。
Abruzzese et al. (2000)は、該PINCポリマーがエレクトロポレーションと組み合せると、エリスロポエチンや血管内皮成長因子(FGG)などのような組換えタンパク質の、マウス骨格筋からの生成と分泌を100倍増進する結果となることを示した。Fewell et al. (2001)は、プラスミド-PINC複合体を免疫不全マウスの後肢筋に注入した後のヒト血液凝固因子IXの長期(120日)の持続的発現を立証した。
別の態様は前述のような方法であって、eNOSポリペプチドをコードするポリヌクレオチドに加えて、1つまたは複数の血管新生調節因子を、ポリペプチドとして、または該ポリペプチドをコードするポリヌクレオチドとして、該eNOS投与前・中・後に、投与するさらなるステップを含むことを特徴とする。多数のそうした血管新生調節因子が技術上周知であり、非限定的な例は成長因子、転写因子、血管活性物質、化学誘引分子などである。成長因子の例はHGF、VEGF(VEGF-2、VEGF-121、VEGF-145またはVEGF-165など)、FGF(FGF-1、-2、-4、-5など)、内皮成長因子、上皮成長因子、血小板由来内皮成長因子、TGF-α、TGF-β、PDGF、TNF-αまたはIGF、発育に伴う調節を受ける内皮細胞遺伝子座1(Del-1)などである。
潜在的な血管新生調節因子の非限定的な例は転写因子(EPAS、HIFなど)、血管活性物質[カリクレイン、C型心房性ナトリウム利尿ペプチド(CNP)、B1受容体作動薬など]、化学誘引因子(GM-CSF、MCP-1、IL-8など)および他ペプチド(PR-39など)である。そうした血管新生因子の、単独での(またはeNOSとの組合せによる)調製、投与および投与効果試験の各方法は常法である[たとえばPapapetropoulos et al., (1997) J Clin Invest 100, 3131-3139; Brock et al., (1991) Am J Pathol 138, 213-221; Ku et al., (1993) Am J Physiol. 265, H586-592; 国際公開第WO 01/03728号明細書および該明細書中の参考文献を参照]。
そうした成長因子は常法により、好適な発現ベクター(個別ベクターまたは本発明のeNOSポリヌクレオチドをも発現するベクター)中にクローニングすることができる[たとえばVEGFを使用する筋内遺伝子療法により血管新生を誘発する方法についてはRivard et al., (1999) Am J Pathol 154, 355-363を参照]。血管新生因子のクローンはもちろん、eNOSをコードするポリヌクレオチドに関して本明細書で述べているような任意の機能性変種または断片という形をとってもよいが、ただし保持される機能は野生型eNOS血管新生因子の血管新生機能でなければならない。
血管新生因子をコードする配列のインフレームまたは上流で、該ポリペプチドの宿主細胞からの分泌または細胞膜への付着を助長、促進する配列を融合すると有利な場合もある。そうした好適なリーダー配列は技術上周知である。
実施態様によっては、遺伝子デリバリーは骨格筋注入法である。虚血肢での新血管の形成を刺激する血管新生促進遺伝子の骨格筋注入は、便利で比較的非侵襲的な遺伝子デリバリー方法である。骨格筋は多核の、細胞分裂を終えた筋線維で構成されるため、導入遺伝子の効果的、長期的発現を助長する可能性がある。新血管形成には1〜2週間しか必要でないため、治療的な血管新生には一過性の遺伝子発現で十分である。新生血管が存続するにはもっと長期にわたる成長因子の発現を必要とする場合もありうるが、in vivoデータが示唆するところによれば、新生毛細血管/動脈を通じてひとたび血流が確立されると、治療用導入遺伝子の継続的な発現がなくてもこれらの新血管は開通状態を保つ(1)。
実施態様によっては、遺伝子デリバリーにアデノウイルスを使用する。血管新生遺伝子実験には量産が容易なアデノウイルスを使用した。該ウイルスは多様な起源(臓器および種)の分裂性および非分裂性細胞に感染し、また導入遺伝子の一過性発現を可能にする。アデノウイルスの遺伝子導入効率はコクサッキーウイルス/アデノウイルス受容体(CAR)およびαvインテグリンの有無に負う。また、成熟筋線維の筋膜および細胞外マトリックスは筋肉への効果的なウイルス性遺伝子デリバリーを妨げる物理的障害として機能することがある。
従って、消化酵素による筋膜と細胞外マトリックスの透過化処理でウイルス性遺伝子デリバリーを増進することができる。加えて、ヒアルロニダーゼによる前処理はウイルスまたはプラスミドを使用する導入遺伝子の発現を増進させる結果となりうる(米国特許第6,258,791号明細書)。加えて、CLI患者および実験動物の骨格筋で生じる炎症と虚血性損傷および筋線維の再生はウイルス性遺伝子デリバリーをさらに促進する可能性がある。
別の実施態様では、平滑筋への遺伝子デリバリーにプラスミドベクターを使用する。平滑筋への非ウイルス性遺伝子導入の効率を高めるためのアプローチがいくつか開発されている。たとえばエレクトロポレーション、PINCやPVPなどポリマーによるプラスミドとの複合体の形成、および裸DNAによる筋線維へのアクセスおよび浸透を増進するためのヒアルロニダーゼまたはコラゲナーゼなどの化合物による前処理などである。プラスミドDNAとポリマーとの複合体の形成は標的組織への取込みはもちろんin vivo安定性をも大幅に改善した。
ポリ(Nビニルピロリドン)やポリ(ビニルアルコール)などのようなPINC (“protective interactive noncondensing”)ポリマーが、プラスミドDNAとの複合体の形成による(i)急速なヌクレアーゼ消化からのプラスミドの保護、(ii)骨格筋などの標的組織へのインタクトプラスミドの分散保持、および(iii)筋細胞によるプラスミド取込みの促進を目的にすでに開発されている。最近、該PINCポリマーはいつくかの導入遺伝子のin vivo発現のレベルと持続時間を改善する効果のあることが示された。プラスミドの再投与が可能であることも立証された。
実施態様によっては、遺伝子デリバリーに局所的なカテーテル媒介VEGFアデノウイルス遺伝子療法を使用する。
以下の実施例は説明が目的であって、本発明を何ら限定するものではない。
実施態様によっては、遺伝子デリバリーに局所的なカテーテル媒介VEGFアデノウイルス遺伝子療法を使用する。
以下の実施例は説明が目的であって、本発明を何ら限定するものではない。
実施例1.変異型eNOSおよび組換えプラスミド/ウイルスベクター
単一変異型または二重変異型eNOSポリペプチドをコードするプラスミドベクターを、eNOS野生型およびポリペプチド変異型のin vitroおよびin vivo細胞内プラスミドベクターデリバリーおよび発現のために生成した。変異はKunkel部位指定変異誘発法によりeNOSポリヌクレオチド配列に直接生成させた(Kunkel, T.A. PNAS 1985; 82:488-492)。変異の確認を配列解析で行った。変異型コンストラクトのcDNAをプラスミドベクターpShuttle-CMV中にクローニングして、eNOSポリペプチドをコードするポリヌクレオチドがCMV発現カセット内に収まるようにした。従って、これらのコンストラクトでは該ポリヌクレオチドはCMVプロモーターに作動可能に連結され、該プロモーターによって変異型eNOSポリペプチドの発現が促進されることになった。
単一変異型または二重変異型eNOSポリペプチドをコードするプラスミドベクターを、eNOS野生型およびポリペプチド変異型のin vitroおよびin vivo細胞内プラスミドベクターデリバリーおよび発現のために生成した。変異はKunkel部位指定変異誘発法によりeNOSポリヌクレオチド配列に直接生成させた(Kunkel, T.A. PNAS 1985; 82:488-492)。変異の確認を配列解析で行った。変異型コンストラクトのcDNAをプラスミドベクターpShuttle-CMV中にクローニングして、eNOSポリペプチドをコードするポリヌクレオチドがCMV発現カセット内に収まるようにした。従って、これらのコンストラクトでは該ポリヌクレオチドはCMVプロモーターに作動可能に連結され、該プロモーターによって変異型eNOSポリペプチドの発現が促進されることになった。
単一変異型eNOSポリペプチドでは、ヒトeNOS(図1参照)のカルモジュリン結合部位内の位置495に対応するThrがAla、AspまたはValへと置換している(各変異をそれぞれT495A、T495D、T495Vと命名する)。二重変異型eNOSポリペプチドでは、位置1177に対応するSerがAspへと置換し、さらに位置495に対応するThrがAla、AspまたはValへと置換している(各変異をそれぞれT495A+S1177D、T495D+S1177D、T495V+S1177Dと命名する)。これらの変異は配列解析で確認し、またHEK293細胞中でのNO産生促進能を試験した(実施例2および図2)。
前記の単一変異型または二重変異型eNOSポリペプチドをコードするアデノウイルスベクターを、He et al.(1998) PNAS 95(5), 2509-2514で開示されている方法で生成し、eNOS野生型およびポリペプチド変異型のin vitroおよびin vivo細胞内ウイルスベクターデリバリーに使用した。(前記のような)変異型eNOSポリペプチドをコードするポリヌクレオチドを収めたpShuttleベクターを大腸菌 BJ5183に、E1およびE3欠失Ad5ゲノムを収めたプラスミドと共に、同時導入した。
該アデノウイルスベクターバックボーンは5型アデノウイルスに由来した。このベクターバックボーンは、アデノウイルス配列のヌクレオチド454および3333の間でE1領域を欠失し、また部分欠失E3領域(ヌクレオチド30004〜30750)が645bpの外来DNAに置き換わっている。E1欠失部位にはポリヌクレオチドを挿入して、CMVプロモーター(-632〜+7)とSV40ポリアデニル化シグナルを該ポリヌクレオチドと作動可能に連結させ、該ポリヌクレオチドによってコードされたポリペプチドを発現させるようにすることができる。
次に、結果として生成する、変異型eNOSポリペプチドをコードする組換えアデノウイルスプラスミドを制限酵素解析で選択し確認した。対応するウイルスは、該プラスミドから切り出した組換えアデノウイルスゲノムをもつ293細胞のトランスフェクションによりレスキューし、次いで293細胞中で増幅し、標準CsClグラジエント精製法により精製し、HAEC中でのNO産生試験に使用した(実施例3および図3)。
さらに、変異型eNOSポリペプチドNOS1177D (Sessa et al., Yale University)は配列番号:1の還元酵素ドメイン内のアミノ酸残基1177に対応する位置でAspへとアミノ酸置換している。この変異型eNOSポリペプチドの細胞内活性を試験するために、この変異型をコードするポリヌクレオチドを、前記のようなアデノウイルスバックボーンのE1欠失位置に挿入した。結果として生成する組換えベクターAd5NOS1177Dは変異型eNOSポリペプチドNOS1177Dをコードする。
該組換えベクターAd5NOS1177Dをパッケージング細胞に導入し、生成するウイルスをプラーク精製し、次いで2回の増幅にかけた。2回目の増幅に由来するウイルスを使用して3LバイオリアクターでHEK293細胞に大規模感染を起こした。生成したウイルスを次に2回のCsClグラジエント分離で精製し、10mM Tris pH 8.0、2mM MgCl2および4%ショ糖に対して透析した。アリコートの精製組換えウイルスもまたHAEC中でのNO産生試験に使用した(実施例3、5および7を参照)。
対照のAd5EGFPは緑色蛍光タンパク質(GFP)レポーター遺伝子をコードするアデノウイルスベクターであり、Collateral Therapeuticsが調製したものを、HEK293細胞中で増幅し、FPLCで精製した。次にこの精製ウイルスをPBS pH7.2および2%ショ糖に対して透析した。アリコートの精製対照ウイルスを-80℃で保存し、対照としての後続実験への使用に備えた(実施例5および7を参照)。
実施例2.HEK293細胞中での変異型eNOSポリペプチドの活性の検出と測定
HEK293細胞中での変異型eNOSポリペプチドの活性を試験し測定するために、変異型eNOSポリペプチドをコードするプラスミドベクター(実施例1を参照)を使用して、該変異型ポリペプチドをHEK293細胞に導入し発現させた。まず10% FBS (SeraCare)、2mM追加L-グルタミンおよび50μg/mlゲンタマイシンを含む増殖培地(Alpha MEM, Gibco 12561-056)を穴あたり2ml分注した6穴プレートにHEK293細胞を播いた。約75%コンフルエントになった時点で細胞に、T495A、Thr495DまたはT495V変異型eNOSポリペプチド(実施例1を参照)か野生型(WT)ヒトeNOS(配列番号:1)かまたは両方をコードするプラスミドシャトルベクターでトランスフェクトした。
HEK293細胞中での変異型eNOSポリペプチドの活性を試験し測定するために、変異型eNOSポリペプチドをコードするプラスミドベクター(実施例1を参照)を使用して、該変異型ポリペプチドをHEK293細胞に導入し発現させた。まず10% FBS (SeraCare)、2mM追加L-グルタミンおよび50μg/mlゲンタマイシンを含む増殖培地(Alpha MEM, Gibco 12561-056)を穴あたり2ml分注した6穴プレートにHEK293細胞を播いた。約75%コンフルエントになった時点で細胞に、T495A、Thr495DまたはT495V変異型eNOSポリペプチド(実施例1を参照)か野生型(WT)ヒトeNOS(配列番号:1)かまたは両方をコードするプラスミドシャトルベクターでトランスフェクトした。
このトランスフェクションは、WT eNOSまたは変異型eNOSをコードするプラスミドシャトルベクター8μg、リポフェクタミン2000(Invitrogen)60μlおよびOptiMEM (Gibco) 200 lを混合し、室温で30分間インキュベートした後に、該混合物111μl + OptiMEM 420μlを、HEK293細胞を含む各穴に分注して行った。37℃で2.5時間インキュベート後、各穴に2mlの増殖培地を加えた。
2日後(37℃、5%CO2での細胞インキベーション)、細胞のNO産生量をケミルミネセンス法で測定し、次いで細胞を溶解し、前述のようなELISA法で溶解液のeNOSタンパク質濃度を調べた。NO産生量はeNOSタンパク質の量で標準化し、異種プラスミド間のトランスフェクション効率の変動を補正するようにした。
2日後(37℃、5%CO2での細胞インキベーション)、細胞のNO産生量をケミルミネセンス法で測定し、次いで細胞を溶解し、前述のようなELISA法で溶解液のeNOSタンパク質濃度を調べた。NO産生量はeNOSタンパク質の量で標準化し、異種プラスミド間のトランスフェクション効率の変動を補正するようにした。
NO産生量の測定
培地を捨て、各穴を2mlのNO 分析用緩衝液 (5mM Na HEPES, 140mM NaCl, 5mM KCl, 1mM MgCl2, 10mgブドウ糖, 10mM CaCl2, 5mMアルギニン, pH 7.5)で2回洗浄した。次いでこの緩衝液を100U/mlスーパーオキシドジスムターゼ+40ng/ml VEGF添加NO 分析用緩衝液 1mlに取り替えた。穴をパラフィンでカバーし、37℃、30分間のインキュベーション後、前記緩衝液0.8mlでカバーし、細胞をSiemens NOA280ケミルミネセンス検出装置にかけてメーカーの説明書に従ってNOを測定した。本物のNOガスを標品として使用した。NO測定完了後、細胞上の残存緩衝液を捨て、細胞を0.6ml 細胞溶解緩衝液 [0.5% NP-40, 50mM Tris-HCl pH 7.5, 1μg/mlペプチスタチンA, 1μg/mlロイペプチン, 5μg/mlアプロチニン, 24μg/ml Pefabloc SC (Boehringer Mannheim)]に溶解し、マイナス20℃で保存した。
培地を捨て、各穴を2mlのNO 分析用緩衝液 (5mM Na HEPES, 140mM NaCl, 5mM KCl, 1mM MgCl2, 10mgブドウ糖, 10mM CaCl2, 5mMアルギニン, pH 7.5)で2回洗浄した。次いでこの緩衝液を100U/mlスーパーオキシドジスムターゼ+40ng/ml VEGF添加NO 分析用緩衝液 1mlに取り替えた。穴をパラフィンでカバーし、37℃、30分間のインキュベーション後、前記緩衝液0.8mlでカバーし、細胞をSiemens NOA280ケミルミネセンス検出装置にかけてメーカーの説明書に従ってNOを測定した。本物のNOガスを標品として使用した。NO測定完了後、細胞上の残存緩衝液を捨て、細胞を0.6ml 細胞溶解緩衝液 [0.5% NP-40, 50mM Tris-HCl pH 7.5, 1μg/mlペプチスタチンA, 1μg/mlロイペプチン, 5μg/mlアプロチニン, 24μg/ml Pefabloc SC (Boehringer Mannheim)]に溶解し、マイナス20℃で保存した。
eNOSタンパク質の測定
96穴ELISAプレート(Costar 3590)を100μl/穴のCoating Antibody(ウサギのポリクローナル抗eNOS抗体)、5μg/mlの50mM炭酸Na緩衝液(pH 9.5)でコートし、4℃で一晩インキュベートした。該ポリクローナル抗体(Babco)は、ヒトeNOSポリペプチドの残基599〜614に対応するペプチド+キーホールリンペットヘモシアニンで免疫したウサギから回収し、プロテインGセファロース (Amersham)を使用して精製した。プレートをPBS+0.01% Tween 20に溶解した0.5% I-Block(Tropix) 200μl/穴でブロックし、4℃で一晩インキュベートした。次にプレートを350μl/穴のPBS+0.5ml/L Tween 20で3回洗浄した。eNOSを含むHEK293細胞溶解液をプレートに加え、細胞溶解緩衝液で5〜10倍希釈して終容量を60μl/穴とし、室温で1.5〜2時間インキュベートした。次いでプレートを350μl/穴のPBS+0.5ml/L Tween 20で3回洗浄した。
96穴ELISAプレート(Costar 3590)を100μl/穴のCoating Antibody(ウサギのポリクローナル抗eNOS抗体)、5μg/mlの50mM炭酸Na緩衝液(pH 9.5)でコートし、4℃で一晩インキュベートした。該ポリクローナル抗体(Babco)は、ヒトeNOSポリペプチドの残基599〜614に対応するペプチド+キーホールリンペットヘモシアニンで免疫したウサギから回収し、プロテインGセファロース (Amersham)を使用して精製した。プレートをPBS+0.01% Tween 20に溶解した0.5% I-Block(Tropix) 200μl/穴でブロックし、4℃で一晩インキュベートした。次にプレートを350μl/穴のPBS+0.5ml/L Tween 20で3回洗浄した。eNOSを含むHEK293細胞溶解液をプレートに加え、細胞溶解緩衝液で5〜10倍希釈して終容量を60μl/穴とし、室温で1.5〜2時間インキュベートした。次いでプレートを350μl/穴のPBS+0.5ml/L Tween 20で3回洗浄した。
検出抗体として、Ref.2で開示の要領でユーロピウム標識したモノクローナル抗eNOS抗体(Transduction Labs N30020)を次のとおり加えた: 125ng/mlのユーロピウム標識抗体/Wallac 測定緩衝液 (Wallac/PerkinElmer 1244-111)、100μl/穴。プレートを室温で1.5時間インキュベートした。次にプレートを350μl/穴のPBS+0.5ml/L Tween 20で3回洗浄した。次いでWallac 増強緩衝液 (Wallac/PerkinElmer 1244-105) 100μl/穴を加えた。プレートをプレートシーラーで覆い、4℃で一晩保存し、次いで10分間の混合後、プレートをWallac 1420 VICTOR2マルチラベルカウンター(PerkinElmer Life Sciences)で、615nmでの時間分解蛍光をモニターしながら、読み取った[Aberle S. et al., Nitric Oxide 1, 226 (1997); Meurer J et al., Methods in Enzymology 359, 433-444(2002)]。
結果は、変異型eNOSポリペプチドがHEK293細胞中でNO産生を刺激すること、またT495AとT495Vの単一変異型、およびT495A+S1177DとT495V+S1177Dの二重変異型が野生型eNOSに比して高レベルのNO産生を刺激することを示唆する(図2)。
実施例3.HAE細胞中での変異型eNOSポリペプチド活性の検出と測定
10% FBS添加EGM増殖培地(Cambrex) 4mlを入れた6穴プレートにヒト動脈内皮細胞(HAEC) 350,000個/穴を播いた。細胞を37℃、5%CO2で培養した。翌日、野生型または変異型(Thr495Ala、Thr495Asp、Thr495ValまたはSer1177Asp)eNOSをコードするアデノウイルス(2×109個の総ウイルス粒子/穴、または約2×107個の感染粒子/穴)を各穴に加えた。ウイルスとの4時間のインキュベーション後、該培地を捨て、代わりに0.1%ゼラチン+30μMセピアプテリン(Sigma)添加のEBM増殖培地(Cambrex) 2mlを加えた。20時間後、ケミルミネセンス法で細胞によるNO産生を測定し、次いで細胞を溶解し、溶解液のeNOSタンパク質濃度をELISA法により後述の要領で測定した。NO産生量はeNOSタンパク質の量で標準化し、異なる変異型eNOSを収めた異なるアデノウイルスコンストラクトによるトランスフェクション効率の差の結果としての発現レベルの変動を補正するようにした。
10% FBS添加EGM増殖培地(Cambrex) 4mlを入れた6穴プレートにヒト動脈内皮細胞(HAEC) 350,000個/穴を播いた。細胞を37℃、5%CO2で培養した。翌日、野生型または変異型(Thr495Ala、Thr495Asp、Thr495ValまたはSer1177Asp)eNOSをコードするアデノウイルス(2×109個の総ウイルス粒子/穴、または約2×107個の感染粒子/穴)を各穴に加えた。ウイルスとの4時間のインキュベーション後、該培地を捨て、代わりに0.1%ゼラチン+30μMセピアプテリン(Sigma)添加のEBM増殖培地(Cambrex) 2mlを加えた。20時間後、ケミルミネセンス法で細胞によるNO産生を測定し、次いで細胞を溶解し、溶解液のeNOSタンパク質濃度をELISA法により後述の要領で測定した。NO産生量はeNOSタンパク質の量で標準化し、異なる変異型eNOSを収めた異なるアデノウイルスコンストラクトによるトランスフェクション効率の差の結果としての発現レベルの変動を補正するようにした。
結果は、変異型eNOSポリペプチドがHEK293細胞中でNO産生を刺激すること、T495AとT495Dの単一変異型が野生型eNOSに比して高レベルのNO産生を刺激することを示唆する(図3)。この研究結果は実施例2のそれとは異なる。NO放出を刺激するために細胞をVEGFで刺激したのに対して、実施例2の研究ではCaイオノフォアを使用しているからである。また、アデノウイルス注入ではプラスミドDNAによるインフェクションよりも細胞あたりeNOSタンパク質(およびNO)産生量が多かった。従って、この研究でのeNOSの過剰発現は変異型eNOSポリペプチドで観測されたNO活性レベルに寄与したかもしれない。
ヒト動脈内皮細胞は内在性の野生型eNOSを含むが、過剰発現した変異型eNOSからのNO産生量は該内在性eNOSのそれの約20倍である。実施例2および3で開示したデータでは、NO産生量をeNOSタンパク質の量で標準化し、種々の変異型eNOSポリペプチドが同じ範囲内の活性をもつようにしている。アデノウイルスベクターおよぴプラスミドベクターを使用して種々の変異型eNOSポリペプチドの間で検出されるNO産生レベルは、細胞内の他の制限因子、たとえばコファクターのアベイラビリティーなどに規定されるという可能性もある。
そこで、HAEC内の変異型eNOSポリペプチドをさらに試験して種々の細胞型におけるeNOS発現および活性の効果をさらに明らかにすることができる。
そこで、HAEC内の変異型eNOSポリペプチドをさらに試験して種々の細胞型におけるeNOS発現および活性の効果をさらに明らかにすることができる。
実施例4.eNOS-KOマウスCLIモデルの作成
CLI動物モデルを作成するために、3〜12月齢の野生型(WT)およびeNOS欠損(eNOS-KO)雄性マウスで片側大腿動脈の外科的切除を行った(後述の「材料と方法」を参照)。浅後肢血流の変化を、術前および術後1、4、7、10、14、21および28日目に、レーザードップラー灌流画像(LDPI)システムで測定した(図4)。該虚血肢に対し定量的血管造影法を術後1、5および10日目に行った。
CLI動物モデルを作成するために、3〜12月齢の野生型(WT)およびeNOS欠損(eNOS-KO)雄性マウスで片側大腿動脈の外科的切除を行った(後述の「材料と方法」を参照)。浅後肢血流の変化を、術前および術後1、4、7、10、14、21および28日目に、レーザードップラー灌流画像(LDPI)システムで測定した(図4)。該虚血肢に対し定量的血管造影法を術後1、5および10日目に行った。
WTマウスでは、血流は閉塞後第1週に著しく損なわれたが、28日目には虚血前ベースラインレベルの80%まで回復した。しかしeNOS-KOマウスでは後肢血流の回復は見られず(図4)、虚血肢が壊死した(図5)。術後10日目の大きな側副動脈の数は妥当性確認済みの血管造影スコア指数を使用して調べると、WT(C57BL/6)マウスではeNOS-KOマウスの2.6倍であった(図6)。術後28日目には、eNOS-KOマウスは壊死肢の自然脱落により虚血後肢の下部を喪失した。一方野生型マウスで、肢壊死のしるしを示したものはいなかった。
これらの結果は、虚血肢の血管新生と組織潅流における内皮由来NOの重要性を立証した。
これらの結果は、虚血肢の血管新生と組織潅流における内皮由来NOの重要性を立証した。
CLIモデルの精緻化
虚血性損傷の重症度は動脈切除の部位と長さに、また大腿静脈が無傷で残るか切除されるかの違いにも、左右されるように見受けられた。eNOS-KOマウスでは、大腿動脈および静脈全体の切除は重症虚血と短期的な全肢喪失を招いた。大腿動脈だけの切除(大腿静脈は無傷)はもっと段階的な虚血性壊死を招いた。大腿動脈だけの分節切除はヒトCLIに似た、それほど広範ではない虚血性壊死(足指または遠位肢の喪失)を招いた(図7)。
後でこのモデルを使用して、血流と救肢に対するインターベンションの効果を研究した。
虚血性損傷の重症度は動脈切除の部位と長さに、また大腿静脈が無傷で残るか切除されるかの違いにも、左右されるように見受けられた。eNOS-KOマウスでは、大腿動脈および静脈全体の切除は重症虚血と短期的な全肢喪失を招いた。大腿動脈だけの切除(大腿静脈は無傷)はもっと段階的な虚血性壊死を招いた。大腿動脈だけの分節切除はヒトCLIに似た、それほど広範ではない虚血性壊死(足指または遠位肢の喪失)を招いた(図7)。
後でこのモデルを使用して、血流と救肢に対するインターベンションの効果を研究した。
CLIに対する齢効果
前述のCLIモデルを使用して、血流の回復と虚血性損傷の度合いが動物の齢に大きく依存することを観測した。大腿動脈の分節切除を行うと、血流回復の障害と虚血性壊死の度合いはどちらも若いENOS-KOマウスよりも老いたマウスのほうがずっと重かった。3月齢のeNOS-KOマウスはWT対照と変わらなかった。14日目に血流の完全回復が肉眼的な病理変化を伴うことなく観測された。6月齢のマウスは血流回復が著しく遅れ、足指に栄養障害を呈し、結果的に足を喪失した例もある(図8)。11〜12月齢では、手術直後に足が変色し、術後1日目で急進行性の壊死を起こし、術後10日目で90%のマウスが肢を喪失する結果となった(図9)。
前述のCLIモデルを使用して、血流の回復と虚血性損傷の度合いが動物の齢に大きく依存することを観測した。大腿動脈の分節切除を行うと、血流回復の障害と虚血性壊死の度合いはどちらも若いENOS-KOマウスよりも老いたマウスのほうがずっと重かった。3月齢のeNOS-KOマウスはWT対照と変わらなかった。14日目に血流の完全回復が肉眼的な病理変化を伴うことなく観測された。6月齢のマウスは血流回復が著しく遅れ、足指に栄養障害を呈し、結果的に足を喪失した例もある(図8)。11〜12月齢では、手術直後に足が変色し、術後1日目で急進行性の壊死を起こし、術後10日目で90%のマウスが肢を喪失する結果となった(図9)。
肢喪失の結果として、いくつかの実験目標たとえばの定量的血管造影またはLDPI流量などは評価できなくなった実験群もある。その場合には、術後1、4、7、10、14、21および28日目のマウスの残存足指および脚を数えることにより、治療効果を判定した。
遺伝子デリバリーの最適化
研究によっては、細胞への遺伝子デリバリーにプラスミドDNA(pDNA)とエレクトロポレーションを併用した。そうした研究を行った目的は次の項目の最適化にあった: 1)DNA濃度、2)注入の容量、部位および回数、3)エレクトロポレーション条件、4)手術との関係でみた治療のタイミング、および5)ヒアルロニダーゼ前処理の適用(図10および11)。
遺伝子デリバリーはWTマウスにレポーター(ルシフェラーゼ)遺伝子を含むプラスミドpLucを使用して最適化し、注入後4日目に内転筋ホモジネート中のルシフェラーゼ活性から測定した。最良プロトコールもpNOS224(NOS1177D遺伝子を含むプラスミド)をeNOS-KOマウスに使用して試験した。これらの実験ではeNOSレベルはウェスタン法とeNOS特異的ELISA法で求めた(図12)。
研究によっては、細胞への遺伝子デリバリーにプラスミドDNA(pDNA)とエレクトロポレーションを併用した。そうした研究を行った目的は次の項目の最適化にあった: 1)DNA濃度、2)注入の容量、部位および回数、3)エレクトロポレーション条件、4)手術との関係でみた治療のタイミング、および5)ヒアルロニダーゼ前処理の適用(図10および11)。
遺伝子デリバリーはWTマウスにレポーター(ルシフェラーゼ)遺伝子を含むプラスミドpLucを使用して最適化し、注入後4日目に内転筋ホモジネート中のルシフェラーゼ活性から測定した。最良プロトコールもpNOS224(NOS1177D遺伝子を含むプラスミド)をeNOS-KOマウスに使用して試験した。これらの実験ではeNOSレベルはウェスタン法とeNOS特異的ELISA法で求めた(図12)。
実施例5.eNOS-KOマウスCLIモデルでのNOS1177D治療の効果
A. 6月齢eNOS-KOマウスでの壊死予防と血流増大
この研究には6月齢の雄性eNOS-KOマウスを使用した。マウスを大腿動脈分節切除後に2つの異なる治療群(各群n=8)へと無作為分配した。術後3日目、上脚の2部位(内転筋と大腿四頭筋)に一群には空ベクターを、他群には(NOS1177Dを含む)pNOS224を、それぞれエレクトロポレーション法で注入した。術後1、4、7、10、14、21および28日目に、上脚のLDPI流量測定値および画像をとった。研究終了時の虚血性壊死による脚喪失率は、空ベクター治療群(8/8)ではpNOS1177D治療群(4/8)に比して有意に高かった(p<0.05)。
28日目に動物を犠牲にし、肢を収集して治療効果の組織形態計測学的評価を行った。研究終了時の脚喪失率は空ベクター治療群(8/8)ではpNO224治療群(4/8)に比して有意に高かった(p<0.05)(図13)。さらに、pNOS治療群では潰瘍治癒効果も観測された(図14)。
A. 6月齢eNOS-KOマウスでの壊死予防と血流増大
この研究には6月齢の雄性eNOS-KOマウスを使用した。マウスを大腿動脈分節切除後に2つの異なる治療群(各群n=8)へと無作為分配した。術後3日目、上脚の2部位(内転筋と大腿四頭筋)に一群には空ベクターを、他群には(NOS1177Dを含む)pNOS224を、それぞれエレクトロポレーション法で注入した。術後1、4、7、10、14、21および28日目に、上脚のLDPI流量測定値および画像をとった。研究終了時の虚血性壊死による脚喪失率は、空ベクター治療群(8/8)ではpNOS1177D治療群(4/8)に比して有意に高かった(p<0.05)。
28日目に動物を犠牲にし、肢を収集して治療効果の組織形態計測学的評価を行った。研究終了時の脚喪失率は空ベクター治療群(8/8)ではpNO224治療群(4/8)に比して有意に高かった(p<0.05)(図13)。さらに、pNOS治療群では潰瘍治癒効果も観測された(図14)。
B. 11〜12月齢eNOS-KOマウスの救肢
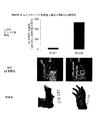
第2の研究には11〜12月齢eNOS-KOマウスを使用した。この月齢群では虚血性損傷の重症度と急進行のため、遺伝子デリバリープロトコールを修正した。プラスミドDNAの注入を手術と同じ日に、(内転筋、四頭筋、腓腹筋を含む)3部位に対して行い、またこれらの筋肉はベクター注入の20分前に遺伝子導入部位をヒアルロニダーゼで前処理した。空ベクター治療群では全頭が術後10日目までに重症型壊死と自然脱落のため虚血後肢を喪失した。一方、pNOS1177D治療群ではLDPI測定流量が著しく改善し、また虚血性壊死の重症度が著しく低下し全肢の救済が実現した(図15、16および18〜21)。
このプロトコール修正は遺伝子発現を著しく改善した(図17)。
第2の研究には11〜12月齢eNOS-KOマウスを使用した。この月齢群では虚血性損傷の重症度と急進行のため、遺伝子デリバリープロトコールを修正した。プラスミドDNAの注入を手術と同じ日に、(内転筋、四頭筋、腓腹筋を含む)3部位に対して行い、またこれらの筋肉はベクター注入の20分前に遺伝子導入部位をヒアルロニダーゼで前処理した。空ベクター治療群では全頭が術後10日目までに重症型壊死と自然脱落のため虚血後肢を喪失した。一方、pNOS1177D治療群ではLDPI測定流量が著しく改善し、また虚血性壊死の重症度が著しく低下し全肢の救済が実現した(図15、16および18〜21)。
このプロトコール修正は遺伝子発現を著しく改善した(図17)。
C. 結論
結論として、後肢虚血を外科的に引き起こしたeNOS-KOマウスのpNOS1177Dによる治療は血流を増大させ、虚血性壊死を緩和/予防し、結果的に救肢につながった。これらの結果は、内在性NOのアベイラビリティーが大きく損なわれるような病態にはNOS遺伝子デリバリーが治療効果をもたらすという証明である。
結論として、後肢虚血を外科的に引き起こしたeNOS-KOマウスのpNOS1177Dによる治療は血流を増大させ、虚血性壊死を緩和/予防し、結果的に救肢につながった。これらの結果は、内在性NOのアベイラビリティーが大きく損なわれるような病態にはNOS遺伝子デリバリーが治療効果をもたらすという証明である。
実施例6.非eNOS遺伝子欠失ラットでの新規CLIモデルの作成とeNOS遺伝子療法効果の試験
非eNOS欠失型の動物モデルでNOS1177Dの効果を評価するために、雄性成熟Sprague-Dawleyラットで上腿部に血液を供給する内側・外側大腿動脈および全側枝の結紮と除去により新規CLIモデルを作成した(図22)。図22および23は、術後1、4、10、17および28日目の該ラットCLIモデルの肉眼的な病理変化を示す。
非eNOS欠失型の動物モデルでNOS1177Dの効果を評価するために、雄性成熟Sprague-Dawleyラットで上腿部に血液を供給する内側・外側大腿動脈および全側枝の結紮と除去により新規CLIモデルを作成した(図22)。図22および23は、術後1、4、10、17および28日目の該ラットCLIモデルの肉眼的な病理変化を示す。
さらに、該ラットCLIモデルにおける血管新生のスコアリング方法を開発した。図23はラットCLIモデルの血管造影画像であり、正常肢(画像の左側)と虚血肢(画像の右側)を示す。また図24はラットCLIモデルの正常肢(画像の左側)と虚血肢(画像の右側)における動脈新生の血管造影スコアリング方法を示す。動脈新生を定量化するために、血管造影画像の大腿部の内側1/4、中間および外側1/4から始まる3本の直線を正常肢、虚血肢両方の内側大腿部に引き、治療内容(たとえばeNOS遺伝子療法の有無)を知らせていない2人の別個の研究者にこれらの線を越える動脈の総数を計算させた。変動を最小に抑えるために、この血管造影スコアは左後肢対右後肢の総動脈数比として表示した。
外科およびeNOS遺伝子療法プロトコール
ラットを2群に分け、手術の直後に各虚血後肢の(大内転筋、大腿四頭筋-内側広筋、および腓腹筋の)3部位にそれぞれ1×1011-ウイルス粒子/500 μl-PBS、都合3×1011-ウイルス粒子を、筋内注入した。9頭のラットには陰性対照としてAd5EGFP(実施例1)を注入し、また9頭には治療としてAd5NOS1177D(実施例1)を注入した。遺伝子導入後1、4、7、10、14および21日目に血流回復量をレーザードップラー潅流画像法(LDPI)により測定した。同時に、手術した後肢の写真を撮影して虚血性組織損傷を評価した。治療期間終了時には血管造影を実施した。
ラットを2群に分け、手術の直後に各虚血後肢の(大内転筋、大腿四頭筋-内側広筋、および腓腹筋の)3部位にそれぞれ1×1011-ウイルス粒子/500 μl-PBS、都合3×1011-ウイルス粒子を、筋内注入した。9頭のラットには陰性対照としてAd5EGFP(実施例1)を注入し、また9頭には治療としてAd5NOS1177D(実施例1)を注入した。遺伝子導入後1、4、7、10、14および21日目に血流回復量をレーザードップラー潅流画像法(LDPI)により測定した。同時に、手術した後肢の写真を撮影して虚血性組織損傷を評価した。治療期間終了時には血管造影を実施した。
NOS1177D投与ラットでは、血流の回復が術前レベルの31%(遺伝子療法後1日目)から57%(同10日目)まで進んだ。EGFP対照遺伝子を投与した対照ラットでは、後肢血流はわずかに回復したにすぎない(1日目30%、10日目37%)、10日目の両群間p=0.0226(図25)。
NOS治療群の壊死スコアは図26に示すような肉眼的病理段階I〜Vに基づいている。その結果は、NOS1177D遺伝子デリバリーがeNOS発現の増進傾向に伴い虚血性壊死の有意の防止につながることを示唆する(10日目のスコアはNOS治療群で1.89、対照群で2.89であり、p=0.014であった)(図27)。
NOS治療群の壊死スコアは図26に示すような肉眼的病理段階I〜Vに基づいている。その結果は、NOS1177D遺伝子デリバリーがeNOS発現の増進傾向に伴い虚血性壊死の有意の防止につながることを示唆する(10日目のスコアはNOS治療群で1.89、対照群で2.89であり、p=0.014であった)(図27)。
さらに、遺伝子導入後14日目に実施した後肢下部の動脈造影では、Ad5NOS1177D投与群の側副血管数がAd5EGFP投与群のそれを上回った(各血管造影スコアは1.21、0.88であり、p=0.0147であった)(図28)。
このように、ラットCLIモデルでのeNOS遺伝子療法は虚血性壊死を防止しうること、またこの治療効果は後肢での変異型eNOSポリペプチドのin vivo発現の増進と相関することを以上の結果は示している。
このように、ラットCLIモデルでのeNOS遺伝子療法は虚血性壊死を防止しうること、またこの治療効果は後肢での変異型eNOSポリペプチドのin vivo発現の増進と相関することを以上の結果は示している。
材料と方法
マウス後肢手術
どの実験にも3〜12月齢、体重20〜55gのeNOS-KO雄性成熟マウス(Jackson Laboratory, Bar Harbor, ME)を使用した。外科手術およびレーザードップラー灌流測定ではラットを1.5%イソフルランで麻酔した。マウスへの片側後肢虚血の創出には外科的処置を用いた。左後肢の上部、大腿動脈を覆う皮膚を切開した(2mm)。大腿動脈根部を分離し、すべての側肢を結紮した。最重度の虚血性損傷をもたらすときは大腿動脈および静脈の結紮と切除を行った。他の例では静脈抜きの大腿動脈の分離、切除を行うか、または動脈の分節切除だけを行った(図“1”を参照)。覆いの皮膚は外科用ステープルで縫合した。
マウス後肢手術
どの実験にも3〜12月齢、体重20〜55gのeNOS-KO雄性成熟マウス(Jackson Laboratory, Bar Harbor, ME)を使用した。外科手術およびレーザードップラー灌流測定ではラットを1.5%イソフルランで麻酔した。マウスへの片側後肢虚血の創出には外科的処置を用いた。左後肢の上部、大腿動脈を覆う皮膚を切開した(2mm)。大腿動脈根部を分離し、すべての側肢を結紮した。最重度の虚血性損傷をもたらすときは大腿動脈および静脈の結紮と切除を行った。他の例では静脈抜きの大腿動脈の分離、切除を行うか、または動脈の分節切除だけを行った(図“1”を参照)。覆いの皮膚は外科用ステープルで縫合した。
マウス後肢血流のレーザードップラー灌流画像(LDPI)解析
LDPI法で虚血(左)および正常(右)後肢の灌流を評価した。過剰な体毛を後肢から除去した。走査開始前に、マウスを37℃のヒーティングプレート上に置いて体温変動を最小限に抑えた。表示の各時点につきLDPIにより同じ脚部位を連続測定した。周囲光及び温度などの変数を極力少なくするために、灌流は左/右後肢潅流比として表示した。灌流解析は、麻酔手術前、手術直後、および手術後4、7、10、14、21および28日目に行った。
LDPI法で虚血(左)および正常(右)後肢の灌流を評価した。過剰な体毛を後肢から除去した。走査開始前に、マウスを37℃のヒーティングプレート上に置いて体温変動を最小限に抑えた。表示の各時点につきLDPIにより同じ脚部位を連続測定した。周囲光及び温度などの変数を極力少なくするために、灌流は左/右後肢潅流比として表示した。灌流解析は、麻酔手術前、手術直後、および手術後4、7、10、14、21および28日目に行った。
マウス骨格筋への遺伝子デリバリー
手術3日後、マウスを1.5%イソフルランで麻酔し、手術した後肢の内転筋と大腿四頭筋に、80μg/50μlの pNOS224または空プラスミド/PBSを、キャリパー電極(200V/cm, 20ms, 1Hz, 8 pulses)を使用するエレクトロポレーションの後に筋内注入した。
ヒアルロニダーゼ前処理では、ヒアルロニダーゼ20単位を50μlのPBSに溶解して内転筋、大腿四頭筋および腓腹筋に注入し、その2時間後に各筋肉に再び、80μg/50μlのpNOS224または空プラスミド/PBSを、キャリパー電極(200V/cm, 20ms, 1Hz, 8 pulses)を使用するエレクトロポレーションの後に注入した。
アデノウイルス注入では、1×1011 vp/50μl-注射液を大内転筋に注入した。
手術3日後、マウスを1.5%イソフルランで麻酔し、手術した後肢の内転筋と大腿四頭筋に、80μg/50μlの pNOS224または空プラスミド/PBSを、キャリパー電極(200V/cm, 20ms, 1Hz, 8 pulses)を使用するエレクトロポレーションの後に筋内注入した。
ヒアルロニダーゼ前処理では、ヒアルロニダーゼ20単位を50μlのPBSに溶解して内転筋、大腿四頭筋および腓腹筋に注入し、その2時間後に各筋肉に再び、80μg/50μlのpNOS224または空プラスミド/PBSを、キャリパー電極(200V/cm, 20ms, 1Hz, 8 pulses)を使用するエレクトロポレーションの後に注入した。
アデノウイルス注入では、1×1011 vp/50μl-注射液を大内転筋に注入した。
トランスフェクション効率研究のためのマウス骨格筋ホモジナイズ処理
筋肉片を切り出し、ウェスタン法、ELISA法または酵素活性法による解析のために処理するときまでマイナス80℃で保存した。組織をさいころに切り、25mM Tris pH 7.8、10%グリセロール、0.2% NP40、Roche Protease Inhibitorミニ錠剤(2mM EDTAとセリンおよびシステインプロテアーゼ阻害剤を含有)を含む溶解緩衝液を使用してKinematic Polytronホモジナイザーでホモジナイズ処理した。酵素活性用コファクターすなわち各4μMのFAD、FMN、BH4、3mM DTT、3mM CaCl2、0.125μMのカルモジュリンも加えた。ほとんどの内転筋は重量が25〜75mgであった。Eppendorf遠心機による最高速度での5〜10分間の遠心分離後、上清を確保し、ペレットは50〜75μl溶解緩衝液を使用してDuall Ground Glassホモジナイザーで再びホモジナイズ処理した。2回目の遠心分離後、2回分の上清を合わせた。3回目の遠心分離で筋肉ホモジネートの終濃度は100mg/ml、終容量は250〜750μlとなった。
筋肉片を切り出し、ウェスタン法、ELISA法または酵素活性法による解析のために処理するときまでマイナス80℃で保存した。組織をさいころに切り、25mM Tris pH 7.8、10%グリセロール、0.2% NP40、Roche Protease Inhibitorミニ錠剤(2mM EDTAとセリンおよびシステインプロテアーゼ阻害剤を含有)を含む溶解緩衝液を使用してKinematic Polytronホモジナイザーでホモジナイズ処理した。酵素活性用コファクターすなわち各4μMのFAD、FMN、BH4、3mM DTT、3mM CaCl2、0.125μMのカルモジュリンも加えた。ほとんどの内転筋は重量が25〜75mgであった。Eppendorf遠心機による最高速度での5〜10分間の遠心分離後、上清を確保し、ペレットは50〜75μl溶解緩衝液を使用してDuall Ground Glassホモジナイザーで再びホモジナイズ処理した。2回目の遠心分離後、2回分の上清を合わせた。3回目の遠心分離で筋肉ホモジネートの終濃度は100mg/ml、終容量は250〜750μlとなった。
eNOS特異的ELISA法
eNOSタンパク質の濃度はR&D Systemsの特異的ELISAキット(cat#DEN00)を使用して求めた。捕獲用抗体は試験用希釈液100μlを加えて活性化した。50〜100μlの筋肉ホモジネートまたはeNOS標品を各穴に分注した。プレートを室温で2時間穏やかに混合するか、またはマイナス4℃で一晩保存した。各穴を洗浄緩衝液(R&D Systems)で3回洗浄した。200μlの西洋ワサビペルオキシダーゼ結合抗体を加え、2時間反応させた。完全洗浄後、200μlの呈色試薬を加えた。30分後、0.5N硫酸で反応を停止させ、450nmで読み取った。eNOS濃度はeNOS標品由来の標準曲線を使用して計算した。
eNOSタンパク質の濃度はR&D Systemsの特異的ELISAキット(cat#DEN00)を使用して求めた。捕獲用抗体は試験用希釈液100μlを加えて活性化した。50〜100μlの筋肉ホモジネートまたはeNOS標品を各穴に分注した。プレートを室温で2時間穏やかに混合するか、またはマイナス4℃で一晩保存した。各穴を洗浄緩衝液(R&D Systems)で3回洗浄した。200μlの西洋ワサビペルオキシダーゼ結合抗体を加え、2時間反応させた。完全洗浄後、200μlの呈色試薬を加えた。30分後、0.5N硫酸で反応を停止させ、450nmで読み取った。eNOS濃度はeNOS標品由来の標準曲線を使用して計算した。
NOS活性試験
各筋肉ホモジネートまたは標品60μlを、NADPH、アルギニンおよび14Cアルギニンを含む反応ミックス20μlと、37℃で1時間反応させた。NADPHの終濃度は0.2mM、5μCの14Cアルギニンの終濃度は20μMであった。各2mMのEDTAとEGTAを添加した0.1M酢酸ナトリウムpH5.2緩衝液に懸濁させたAG 50W-樹脂で反応物をろ過して反応を停止させた。生成物の14Cシトルリンの放射能をWallac Micro Betaカウンターにより、Microscint-40を使用して測定した。
各筋肉ホモジネートまたは標品60μlを、NADPH、アルギニンおよび14Cアルギニンを含む反応ミックス20μlと、37℃で1時間反応させた。NADPHの終濃度は0.2mM、5μCの14Cアルギニンの終濃度は20μMであった。各2mMのEDTAとEGTAを添加した0.1M酢酸ナトリウムpH5.2緩衝液に懸濁させたAG 50W-樹脂で反応物をろ過して反応を停止させた。生成物の14Cシトルリンの放射能をWallac Micro Betaカウンターにより、Microscint-40を使用して測定した。
種々のNOSアイソマーを決定するためのマウス骨格筋溶解液のウェスタンブロット
SDS-PAGE:
各サンプルにつき筋肉ホモジネート30μlを、100mMジチオスレイトールを含む10μl 4xサンプル緩衝液(Invitrogen Cat. No. NP007)に加えた。100℃で7〜8分間加熱後、各サンプルを10% Tris-グリシンSDS-PAGEゲル(BMA PAGEr Cat.No.59102)に添加した。必要に応じて、組換えヒトeNOSを含むHEK細胞溶解液(40μl 1xサンプル緩衝液に溶解)1μlを陽性対照として加えた。ゲルの1レーンにはプレステインマーカー(Invitrogen LC5725) 10μlも添加した。1x Laemmli泳動緩衝液(Berlex Media Prep Department)を使用して130V(定電圧)で1.5時間ゲルを電気泳動した。
SDS-PAGE:
各サンプルにつき筋肉ホモジネート30μlを、100mMジチオスレイトールを含む10μl 4xサンプル緩衝液(Invitrogen Cat. No. NP007)に加えた。100℃で7〜8分間加熱後、各サンプルを10% Tris-グリシンSDS-PAGEゲル(BMA PAGEr Cat.No.59102)に添加した。必要に応じて、組換えヒトeNOSを含むHEK細胞溶解液(40μl 1xサンプル緩衝液に溶解)1μlを陽性対照として加えた。ゲルの1レーンにはプレステインマーカー(Invitrogen LC5725) 10μlも添加した。1x Laemmli泳動緩衝液(Berlex Media Prep Department)を使用して130V(定電圧)で1.5時間ゲルを電気泳動した。
ニトロセルロース膜へのブロッティング:
タンパク質をニトロセルロース膜に20V(定電圧)で2時間、転写した。転写には(転写緩衝液に予め浸漬した)Novex/Invitrogen装置を使用した [転写緩衝液= 100ml 10x転写緩衝液(Berlex Media Prep) + 200mlメタノール + 700ml H2O]。ブロッティング後、ニトロセルロース膜を20ml TBS + 5%脱脂粉乳に浸して4℃で一晩保存した(TBS=0.02M Tris-HCl, 0.12M NaCl, pH7.5)。
タンパク質をニトロセルロース膜に20V(定電圧)で2時間、転写した。転写には(転写緩衝液に予め浸漬した)Novex/Invitrogen装置を使用した [転写緩衝液= 100ml 10x転写緩衝液(Berlex Media Prep) + 200mlメタノール + 700ml H2O]。ブロッティング後、ニトロセルロース膜を20ml TBS + 5%脱脂粉乳に浸して4℃で一晩保存した(TBS=0.02M Tris-HCl, 0.12M NaCl, pH7.5)。
抗体によるタンパク質の検出(全ステップ室温で):
1時間15分にわたりブロットを1次抗体(TBS+0.1% Tween 20 + 5%脱脂粉乳で1:2000希釈した抗eNOSまたは抗bNOSマウスモノクローナルBD/Transduction Labs)中でインキュベートした。次いでブロットを次の要領で洗浄した: TBS+0.1% Tween 20で10分間1回、5分間2回。次いで1時間にわたりブロットを2次抗体[TBS+0.1% Tween 20 + 5%脱脂粉乳で1:3000希釈したペルオキシダーゼ結合ヤギ抗マウスIgG(Chemicon Intl. AP308PまたはRoche 1814168)]中でインキュベートした。前述と同様の洗浄と(Tween無添加の)TBSで5分間1回の洗浄後、ブロットを1分間、ECL試薬(Amersham Pharmacia RPN2106) 中でインキュベートした。次いでブロットをSaran Wrapで覆い、Amersham Pharmacia Hyperfilm ECL (RPN1674A)に1〜5分間転写し、フィルムを現像した。
1時間15分にわたりブロットを1次抗体(TBS+0.1% Tween 20 + 5%脱脂粉乳で1:2000希釈した抗eNOSまたは抗bNOSマウスモノクローナルBD/Transduction Labs)中でインキュベートした。次いでブロットを次の要領で洗浄した: TBS+0.1% Tween 20で10分間1回、5分間2回。次いで1時間にわたりブロットを2次抗体[TBS+0.1% Tween 20 + 5%脱脂粉乳で1:3000希釈したペルオキシダーゼ結合ヤギ抗マウスIgG(Chemicon Intl. AP308PまたはRoche 1814168)]中でインキュベートした。前述と同様の洗浄と(Tween無添加の)TBSで5分間1回の洗浄後、ブロットを1分間、ECL試薬(Amersham Pharmacia RPN2106) 中でインキュベートした。次いでブロットをSaran Wrapで覆い、Amersham Pharmacia Hyperfilm ECL (RPN1674A)に1〜5分間転写し、フィルムを現像した。
内皮NOの放出(NOアナライザー)
10% FBS添加Clonetics増殖培地(EGM) 4mlを入れた6穴プレートにヒト動脈内皮細胞(HAEC) 350,000個/穴を播いた。翌日、野生型または(Gly2および/またはSer1177)変異型eNOSをコードするアデノウイルス(2×109個の総ウイルス粒子/穴、または約2×107個の感染粒子/穴)を各穴に加えた。ウイルスとの4時間のインキュベーション後、該培地を捨て、代わりに0.1%ゼラチン+30μMセピアプテリン添加のClonetics基礎培地(EBM)2mlを加えた。翌朝、該培地を、100μg/ml酸化LDL(Intracel RP-047)添加または無添加の2ml新鮮EBM-ゼラチン-セピアプテリンに取り替えた。6時間後、該培地を捨て、各穴を2mlのNO 分析用緩衝液 (5mM Na HEPES, 140mM NaCl, 5mM KCl, 1mM MgCl2, 10mgブドウ糖, 10mM CaCl2, 5mMアルギニン, pH 7.5)で2回洗浄した。
10% FBS添加Clonetics増殖培地(EGM) 4mlを入れた6穴プレートにヒト動脈内皮細胞(HAEC) 350,000個/穴を播いた。翌日、野生型または(Gly2および/またはSer1177)変異型eNOSをコードするアデノウイルス(2×109個の総ウイルス粒子/穴、または約2×107個の感染粒子/穴)を各穴に加えた。ウイルスとの4時間のインキュベーション後、該培地を捨て、代わりに0.1%ゼラチン+30μMセピアプテリン添加のClonetics基礎培地(EBM)2mlを加えた。翌朝、該培地を、100μg/ml酸化LDL(Intracel RP-047)添加または無添加の2ml新鮮EBM-ゼラチン-セピアプテリンに取り替えた。6時間後、該培地を捨て、各穴を2mlのNO 分析用緩衝液 (5mM Na HEPES, 140mM NaCl, 5mM KCl, 1mM MgCl2, 10mgブドウ糖, 10mM CaCl2, 5mMアルギニン, pH 7.5)で2回洗浄した。
次いでこの緩衝液を100U/mlスーパーオキシドジスムターゼ+40ng/ml VEGF添加NO 分析用緩衝液 1mlに取り替えた。穴をパラフィンでカバーし、37℃、30分間のインキュベーション後、前記緩衝液0.8mlでカバーし、細胞をSiemens NOA280ケミルミネセンス検出装置にかけてメーカーの説明書に従ってNOを測定した。NO測定完了後、細胞上の残存緩衝液を捨て、細胞を0.3ml eNOS ELISA 細胞溶解緩衝液に溶解した。-20℃で一晩保存後、eNOS ELISA法で該溶解液(各5〜20μl)のeNOSタンパク質濃度を解析した。NO産生量はeNOSタンパク質の量で標準化し、異なる変異型eNOSを収めた異なるアデノウイルスコンストラクトによるトランスフェクション効率の差の結果としての発現レベルの変動を補正するようにした。
プラスミドコンストラクト
1. pGL3-Control。このプラスミドに収めた蛍ルシフェラーゼ遺伝子の発現はSV40プロモーター/エンハンサー(Promega)が促進する。プラスミドバックボーンはpGL3-Basicバックボーンである。
2. pcDNA3.1/eNOS224。eNOS224遺伝子はpcDNA3.1のCMVプロモーターにより発現を促進され、また変異型eNOSポリペプチドS1177Dをコードする。
3. pcDNA3.1/hygroはpcDNA3.1d(Promega)の対照プラスミドである。
1. pGL3-Control。このプラスミドに収めた蛍ルシフェラーゼ遺伝子の発現はSV40プロモーター/エンハンサー(Promega)が促進する。プラスミドバックボーンはpGL3-Basicバックボーンである。
2. pcDNA3.1/eNOS224。eNOS224遺伝子はpcDNA3.1のCMVプロモーターにより発現を促進され、また変異型eNOSポリペプチドS1177Dをコードする。
3. pcDNA3.1/hygroはpcDNA3.1d(Promega)の対照プラスミドである。
形態計測解析
左大腿動脈の結紮によりPAODに似た症状を発現させたeNOS-KOマウスを術後28日目に犠牲にした。後躯を皮剥ぎし、固定し、2日間脱灰液に浸した後、系統的無作為に樹脂ブロック化し、治療効果の形態計測的評価に使用した。要するに、後脚を股関節で離断し、4mm間隔で切断した。切断片はすべて単一カセットに収め、脱水し、各切断片の側面がブロックの切り出し面となるように包埋した。5μm厚の薄片を切り出し、ヘマトキシリンとエオシン(H&E)で染色し、C.A.S.T.ステレオロジーシステムによる形態計測評価に使用した。
左大腿動脈の結紮によりPAODに似た症状を発現させたeNOS-KOマウスを術後28日目に犠牲にした。後躯を皮剥ぎし、固定し、2日間脱灰液に浸した後、系統的無作為に樹脂ブロック化し、治療効果の形態計測的評価に使用した。要するに、後脚を股関節で離断し、4mm間隔で切断した。切断片はすべて単一カセットに収め、脱水し、各切断片の側面がブロックの切り出し面となるように包埋した。5μm厚の薄片を切り出し、ヘマトキシリンとエオシン(H&E)で染色し、C.A.S.T.ステレオロジーシステムによる形態計測評価に使用した。
治療脚、非治療脚のどちらも似たような病理変化を示した。最も一貫した変化は、筋体積の脂肪細胞による置換を伴う筋線維の喪失であった。この変化は大筋群に一貫して見られ、また通常、活動性筋変性の証拠を伴わなかった。しかし場合によっては、置換脂肪細胞の周辺や変性筋線維の周辺における急性および慢性の炎症性細胞浸潤の多さが裏付けるように、活動性組織破壊がなお進行中であった。正常に見える筋肉、脂肪置換組織、および炎症性細胞浸潤の各領域は顕微鏡で容易に識別された。これらの組織が占めるスライド上の面積を個別に定量した。スライド上の他の領域(骨、皮膚、結合組織など)はすべて一括し「その他」とした。これらの領域の大きさは個別に各脚の全体積のパーセンテージとして計算した。両群に関するこうしたステレオロジー研究の結果をANOVAで比較した(図21)。
次のパラメーターには統計的に有意の変化があった: eNOS治療肢の全体積は空ベクター治療肢のそれを有意に上回ったが、非手術(対照)肢との差はなかった。健康な筋肉の体積%もまた、空ベクター治療肢ではeNOSベクター治療肢と比較して有意に低下した。これに対して、置換脂肪量は空ベクター治療肢とeNOSベクター治療肢で差はなかった。炎症の大きさも空ベクター治療肢では増したが、有意差となるには至らなかった(P=0.0525)。
これらの変化は、筋線維は大腿動脈結紮の直後に失われたが、脂肪組織が喪失線維に取って代わったことを示す。しかし、一部の領域では脂肪組織さえも血流の支援を受けられず、活動性の炎症性細胞浸潤に裏付けられるような組織の壊死が続いた。eNOS治療はこれらの病理変化を改善した。
Claims (41)
- 治療を必要とする患者に、哺乳動物eNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む重症肢虚血(CLI)治療方法。
- eNOSポリペプチドがヒトeNOSポリペプチドである請求項1に記載の方法。
- ヒトeNOSポリペプチドのアミノ酸配列が配列番号:1である請求項2に記載の方法。
- eNOSポリペプチドが哺乳動物細胞内でリン酸化されているヒトeNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含む請求項3に記載の方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基495に対応する位置に変異を含む請求項4に記載の方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基1177に対応する位置に変異を含む請求項4に記載の方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基495に対応する位置に第1変異を、またアミノ酸残基1177に対応する位置に第2変異を、それぞれ含む請求項4に記載の方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基495に対応する位置に第1変異を、アミノ酸残基1177に対応する位置に第2変異を、またアミノ酸残基2に対応する位置に第3変異を、それぞれ含む請求項4に記載の方法。
- アミノ酸残基495に対応する位置の変異はAla、Val、LeuまたはIleへのアミノ酸置換である請求項6、7または8に記載の方法。
- アミノ酸残基1177に対応する位置の変異はAspへのアミノ酸置換である請求項6、7または8に記載の方法。
- アミノ酸残基2に対応する位置の変異はAlaへのアミノ酸置換である請求項8に記載の方法。
- eNOSポリペプチドのリン酸化の度合いが基準ポリペプチドに比して加減されている請求項4に記載の方法。
- eNOSポリペプチドが基準ポリペプチドに比してカルモジュリンに対する結合アフィニティーを高めている請求項4に記載の方法。
- eNOSポリペプチドのCa++-カルモジュリン仲介刺激でCa++依存性が基準eNOSポリペプチドに比して低下している請求項4に記載の方法。
- eNOSポリペプチドが基準eNOSポリペプチドに比して、より高いeNOS活性を有する請求項4に記載の方法。
- 活性がNOの生成である請求項15に記載の方法。
- 活性が還元酵素活性である請求項15に記載の方法。
- 基準ポリペプチドのアミノ酸配列がヒトeNOSのアミノ酸配列であるか、またはヒトeNOSのアミノ酸配列に由来する請求項12、13、14、15、16または17に記載の方法。
- 基準ポリペプチドのアミノ酸配列が配列番号:1であるか、または配列番号:1に由来する請求項18に記載の方法。
- eNOSポリペプチドのアミノ酸配列がヒトeNOSのアミノ酸配列と実質的に相同である請求項4に記載の方法。
- eNOSポリペプチドのアミノ酸配列が配列番号:1のアミノ酸配列と95〜99%の配列相同性を有する請求項20に記載の方法。
- ポリヌクレオチドはeNOSポリペプチドをコードする核酸配列を含む組換えベクターであり、該核酸配列は該eNOSが細胞中で発現するよう、少なくとも1つの調節配列へと作動可能に連結されている請求項1または4に記載の方法。
- 核酸配列がプロモーターへと作動可能に連結されている請求項22に記載の方法。
- 組換えベクターがウイルスベクターである請求項23に記載の方法。
- ウイルスベクターがアデノウイルスベクターである請求項24に記載の方法。
- 治療が患者細胞中のeNOS活性を調節するステップを含む請求項1または4に記載の方法。
- 細胞が内皮細胞である請求項26に記載の方法。
- 細胞が骨髄由来細胞である請求項26に記載の方法。
- 患者へのポリヌクレオチドの投与前・中・後に、1つまたは複数の血管新生因子を投与するステップをさらに含む請求項1または4に記載の方法。
- 血管新生因子がHGF、VEGF、FGF、内皮成長因子、上皮成長因子、血小板由来成長因子、TGF-アルファ、TGF-ベータ、PDGF、TNA-アルファまたはIGF、Del-1からなる血管新生因子群より選択される請求項29に記載の方法。
- 投与が患者細胞へのポリヌクレオチドのex vivo導入を含む請求項1または4に記載の方法。
- 投与が患者の病変組織へのポリヌクレオチドのデリバリーを含む請求項1または4に記載の方法。
- 投与が患者の末梢血管系へのポリヌクレオチドのデリバリーを含む請求項1または4に記載の方法。
- デリバリーは患者肢筋への筋内注射または動脈内注射による請求項33に記載の方法。
- 治療を必要とする患者にeNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む血管新生の治療方法であって、該eNOSポリペプチドが哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする方法。
- 治療を必要とする患者にeNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む微小血管機能障害の治療方法であって、該eNOSポリペプチドが哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする方法。
- 治療を必要とする患者にeNOSポリペプチドをコードするポリヌクレオチドを有効量投与するステップを含む重症肢虚血(CLI)の治療方法であって、該eNOSポリペプチドが哺乳動物細胞内でリン酸化されている哺乳動物eNOSの一アミノ酸残基に対応する位置に少なくとも1つの変異を含むことを特徴とする方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基495に対応する位置に変異を含み、また該変異はAla、Val、LeuまたはIleへのアミノ酸置換である請求項35、36または37に記載の方法。
- eNOSポリペプチドが配列番号:1のアミノ酸残基1177に対応する位置に変異を含み、また該変異はAspへのアミノ酸置換である請求項35、36または37に記載の方法。
- eNOSポリペプチドが
(i) アミノ酸残基495に対応する位置に、Ala、Val、LeuまたはIleへのアミノ酸置換である第1変異を、また
(ii) 配列番号:1のアミノ酸残基1177に対応する位置に、Aspへのアミノ酸置換である第2変異を、
それぞれ含む請求項1、35、36または37に記載の方法。 - eNOSポリペプチドが
(i) アミノ酸残基495に対応する位置に、Ala、Val、LeuまたはIleへのアミノ酸置換である第1変異を、
(ii) 配列番号:1のアミノ酸残基1177に対応する位置に、Aspへのアミノ酸置換である第2変異を、また
(iii) 配列番号:1のアミノ酸残基2に対応する位置に、Alaへのアミノ酸置換である第3変異を、
それぞれ含む請求項1、35、36または37に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US40363702P | 2002-08-16 | 2002-08-16 | |
| PCT/US2003/025626 WO2004016761A2 (en) | 2002-08-16 | 2003-08-15 | Gene therapy for critical limb ischemia with wild type or mutant enos |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005539031A true JP2005539031A (ja) | 2005-12-22 |
| JP2005539031A5 JP2005539031A5 (ja) | 2006-09-28 |
Family
ID=31888259
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004529471A Pending JP2005539031A (ja) | 2002-08-16 | 2003-08-15 | 野生型または変異型eNOSによる重症肢虚血の遺伝子療法 |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US20040120930A1 (ja) |
| EP (1) | EP1536689A4 (ja) |
| JP (1) | JP2005539031A (ja) |
| KR (1) | KR20050042162A (ja) |
| CN (2) | CN101391105A (ja) |
| AU (1) | AU2003263844A1 (ja) |
| BR (1) | BR0313515A (ja) |
| CA (1) | CA2494845A1 (ja) |
| IL (1) | IL166362A0 (ja) |
| MX (1) | MXPA05001763A (ja) |
| NO (1) | NO20051351L (ja) |
| PL (1) | PL375446A1 (ja) |
| RU (1) | RU2005107414A (ja) |
| WO (1) | WO2004016761A2 (ja) |
| ZA (1) | ZA200502181B (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2951306A4 (en) * | 2013-01-30 | 2016-07-27 | Univ Nebraska | COMPOSITIONS AND METHOD FOR TREATING COMPLICATIONS RELATED TO DIABETES |
| CN109415714A (zh) * | 2016-04-29 | 2019-03-01 | 艾诺奥医药品有限公司 | 体内使用软骨素酶和/或透明质酸酶以增强药剂的递送 |
| CN105944243A (zh) * | 2016-05-12 | 2016-09-21 | 段俊丽 | 一种eNOS表达与活化的调控装置及周围动脉疾病的治疗装置 |
| CN107802826B (zh) * | 2017-10-26 | 2020-02-18 | 首都医科大学宣武医院 | eNOS突变体在促进血管生成中的应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000062605A1 (en) * | 1999-04-16 | 2000-10-26 | Yale University | eNOS MUTATIONS USEFUL FOR GENE THERAPY AND THERAPEUTIC SCREENING |
| JP2002506008A (ja) * | 1998-03-09 | 2002-02-26 | セント エリザベス メディカル センター | 血管新生を調整するための組成物及び方法 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1016726A1 (en) * | 1998-12-30 | 2000-07-05 | Introgene B.V. | Gene therapy to promote angiogenesis |
-
2003
- 2003-08-15 JP JP2004529471A patent/JP2005539031A/ja active Pending
- 2003-08-15 WO PCT/US2003/025626 patent/WO2004016761A2/en active Search and Examination
- 2003-08-15 RU RU2005107414/13A patent/RU2005107414A/ru not_active Application Discontinuation
- 2003-08-15 MX MXPA05001763A patent/MXPA05001763A/es not_active Application Discontinuation
- 2003-08-15 CA CA002494845A patent/CA2494845A1/en not_active Abandoned
- 2003-08-15 PL PL03375446A patent/PL375446A1/xx not_active Application Discontinuation
- 2003-08-15 KR KR1020057002657A patent/KR20050042162A/ko not_active Application Discontinuation
- 2003-08-15 AU AU2003263844A patent/AU2003263844A1/en not_active Abandoned
- 2003-08-15 BR BR0313515-2A patent/BR0313515A/pt not_active IP Right Cessation
- 2003-08-15 US US10/642,255 patent/US20040120930A1/en not_active Abandoned
- 2003-08-15 EP EP03788540A patent/EP1536689A4/en not_active Withdrawn
- 2003-08-15 CN CNA2008101259592A patent/CN101391105A/zh active Pending
- 2003-08-15 CN CNB038194945A patent/CN100408101C/zh not_active Expired - Fee Related
-
2005
- 2005-01-18 IL IL16636205A patent/IL166362A0/xx unknown
- 2005-03-15 ZA ZA200502181A patent/ZA200502181B/en unknown
- 2005-03-15 NO NO20051351A patent/NO20051351L/no not_active Application Discontinuation
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002506008A (ja) * | 1998-03-09 | 2002-02-26 | セント エリザベス メディカル センター | 血管新生を調整するための組成物及び方法 |
| WO2000062605A1 (en) * | 1999-04-16 | 2000-10-26 | Yale University | eNOS MUTATIONS USEFUL FOR GENE THERAPY AND THERAPEUTIC SCREENING |
Non-Patent Citations (2)
| Title |
|---|
| FEBS LETTERS, vol. 443, JPN6009060777, 1999, pages 285 - 289, ISSN: 0001473917 * |
| JOURNAL OF CONTROLLED RELEASE, vol. 78, JPN6009060775, January 2002 (2002-01-01), pages 285 - 294, ISSN: 0001473916 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1688197A (zh) | 2005-10-26 |
| KR20050042162A (ko) | 2005-05-04 |
| NO20051351L (no) | 2005-04-28 |
| RU2005107414A (ru) | 2006-01-27 |
| AU2003263844A1 (en) | 2004-03-03 |
| CA2494845A1 (en) | 2004-02-26 |
| EP1536689A4 (en) | 2006-09-06 |
| CN100408101C (zh) | 2008-08-06 |
| CN101391105A (zh) | 2009-03-25 |
| ZA200502181B (en) | 2006-09-27 |
| US20040120930A1 (en) | 2004-06-24 |
| WO2004016761A2 (en) | 2004-02-26 |
| WO2004016761A3 (en) | 2005-03-17 |
| BR0313515A (pt) | 2005-10-18 |
| IL166362A0 (en) | 2006-01-16 |
| PL375446A1 (en) | 2005-11-28 |
| MXPA05001763A (es) | 2005-08-19 |
| EP1536689A2 (en) | 2005-06-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6479654B1 (en) | Forms of the angiogenic factor vascular endothelial cell growth factor: VEGF | |
| USRE37933E1 (en) | Viral vectors and their use for treating hyperproliferative disorders, in particular restenosis | |
| AU2021282480A1 (en) | Methods and pharmaceutical composition for the treatment and the prevention of cardiomyopathy due to energy failure | |
| US20090246183A1 (en) | eNOS mutations useful for gene therapy and therapeutic screening | |
| JP2001523103A (ja) | 腫瘍治療用血管形成アンタゴニストのアデノウイルスによる腫瘍内送達 | |
| JP2007195555A (ja) | 遺伝子発現を誘導するための組成物および方法 | |
| ZA200502183B (en) | Enos mutants useful for gene therapy | |
| CN103751211A (zh) | 用于愈合创伤的方法和药物组合物 | |
| Certelli et al. | Robust angiogenesis and arteriogenesis in the skin of diabetic mice by transient delivery of engineered VEGF and PDGF-BB proteins in fibrin hydrogels | |
| DE69737062T2 (de) | Gentherapie für kongestives herzversagen | |
| ZA200502181B (en) | Gene therapy for critical limb ischemia with wild type or mutant eNOS | |
| RU2491952C2 (ru) | Способы и фармакологические композиции для заживления ран | |
| CA2451311A1 (en) | Stimulation of vascularization with vegf-b | |
| RU2257911C2 (ru) | Способы и композиции, применимые для модуляции ангиогенеза с использованием протеинкиназы raf и ras | |
| JP2010239971A (ja) | 細胞におけるペルオキシソームカタラーゼ機能の促進 | |
| US9068174B2 (en) | Method for sensitizing tumor cells to chemotherapeutic prodrug CPT-11 | |
| US20100303790A1 (en) | Use of biliverdin reductase (bvr) and bvr peptide fragments to treat coronary disorders | |
| JP2006515168A5 (ja) | ||
| Ferraro | Intradermal delivery of plasmids encoding angiogenic growth factors by electroporation promotes wound healing and neovascularization |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060814 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060814 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091124 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100420 |