RU2491952C2 - Способы и фармакологические композиции для заживления ран - Google Patents
Способы и фармакологические композиции для заживления ран Download PDFInfo
- Publication number
- RU2491952C2 RU2491952C2 RU2010130763/15A RU2010130763A RU2491952C2 RU 2491952 C2 RU2491952 C2 RU 2491952C2 RU 2010130763/15 A RU2010130763/15 A RU 2010130763/15A RU 2010130763 A RU2010130763 A RU 2010130763A RU 2491952 C2 RU2491952 C2 RU 2491952C2
- Authority
- RU
- Russia
- Prior art keywords
- insulin
- cells
- wound
- skin
- pkc
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 106
- 230000029663 wound healing Effects 0.000 title description 67
- 239000008196 pharmacological composition Substances 0.000 title description 6
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims abstract description 533
- 108090001061 Insulin Proteins 0.000 claims abstract description 273
- 102000004877 Insulin Human genes 0.000 claims abstract description 265
- 229940125396 insulin Drugs 0.000 claims abstract description 265
- 206010072170 Skin wound Diseases 0.000 claims abstract description 81
- 239000003112 inhibitor Substances 0.000 claims abstract description 46
- 206010061218 Inflammation Diseases 0.000 claims abstract description 16
- 230000004054 inflammatory process Effects 0.000 claims abstract description 16
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 16
- 230000002829 reductive effect Effects 0.000 claims abstract description 8
- 230000004044 response Effects 0.000 claims abstract description 3
- 101150020891 PRKCA gene Proteins 0.000 claims description 25
- 208000027418 Wounds and injury Diseases 0.000 abstract description 287
- 230000000694 effects Effects 0.000 abstract description 98
- 102100024924 Protein kinase C alpha type Human genes 0.000 abstract description 82
- 101001051777 Homo sapiens Protein kinase C alpha type Proteins 0.000 abstract description 81
- 239000003814 drug Substances 0.000 abstract description 19
- 239000000126 substance Substances 0.000 abstract description 15
- 238000011161 development Methods 0.000 abstract description 10
- 230000009467 reduction Effects 0.000 abstract description 2
- 206010052428 Wound Diseases 0.000 description 281
- 108090000315 Protein Kinase C Proteins 0.000 description 247
- 102000003923 Protein Kinase C Human genes 0.000 description 243
- 210000004027 cell Anatomy 0.000 description 213
- 210000002510 keratinocyte Anatomy 0.000 description 182
- 230000014509 gene expression Effects 0.000 description 135
- 108010029485 Protein Isoforms Proteins 0.000 description 105
- 102000001708 Protein Isoforms Human genes 0.000 description 105
- 210000003491 skin Anatomy 0.000 description 100
- 230000004913 activation Effects 0.000 description 78
- 230000035876 healing Effects 0.000 description 69
- 230000035755 proliferation Effects 0.000 description 68
- 108090000623 proteins and genes Proteins 0.000 description 66
- 230000004069 differentiation Effects 0.000 description 54
- 238000011282 treatment Methods 0.000 description 54
- 239000008194 pharmaceutical composition Substances 0.000 description 48
- 239000004480 active ingredient Substances 0.000 description 47
- 230000001965 increasing effect Effects 0.000 description 47
- 208000015181 infectious disease Diseases 0.000 description 46
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 45
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 45
- 230000001939 inductive effect Effects 0.000 description 44
- 238000001727 in vivo Methods 0.000 description 43
- 230000005764 inhibitory process Effects 0.000 description 41
- 241000699670 Mus sp. Species 0.000 description 39
- 238000000338 in vitro Methods 0.000 description 39
- 230000002062 proliferating effect Effects 0.000 description 35
- 239000003102 growth factor Substances 0.000 description 34
- 239000000203 mixture Substances 0.000 description 34
- 241000701161 unidentified adenovirus Species 0.000 description 33
- 102000004169 proteins and genes Human genes 0.000 description 32
- 230000002500 effect on skin Effects 0.000 description 31
- 239000003795 chemical substances by application Substances 0.000 description 27
- 108090000385 Fibroblast growth factor 7 Proteins 0.000 description 26
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 26
- 102100028071 Fibroblast growth factor 7 Human genes 0.000 description 25
- 230000015572 biosynthetic process Effects 0.000 description 25
- 230000008569 process Effects 0.000 description 25
- 102100024040 Signal transducer and activator of transcription 3 Human genes 0.000 description 24
- 239000011575 calcium Substances 0.000 description 24
- 108010017324 STAT3 Transcription Factor Proteins 0.000 description 23
- 108020004459 Small interfering RNA Proteins 0.000 description 23
- 235000018102 proteins Nutrition 0.000 description 23
- 210000004927 skin cell Anatomy 0.000 description 23
- 239000013598 vector Substances 0.000 description 23
- 238000002474 experimental method Methods 0.000 description 22
- 239000012190 activator Substances 0.000 description 21
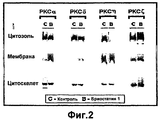
- 210000004379 membrane Anatomy 0.000 description 21
- 239000012528 membrane Substances 0.000 description 21
- 239000010410 layer Substances 0.000 description 19
- 230000002018 overexpression Effects 0.000 description 19
- 210000002950 fibroblast Anatomy 0.000 description 18
- 150000007523 nucleic acids Chemical class 0.000 description 18
- 230000000638 stimulation Effects 0.000 description 18
- 230000001131 transforming effect Effects 0.000 description 18
- 206010012601 diabetes mellitus Diseases 0.000 description 17
- 229940088597 hormone Drugs 0.000 description 17
- 102000039446 nucleic acids Human genes 0.000 description 17
- 108020004707 nucleic acids Proteins 0.000 description 17
- 206010040882 skin lesion Diseases 0.000 description 17
- 210000001519 tissue Anatomy 0.000 description 17
- 230000000699 topical effect Effects 0.000 description 17
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 17
- 101800003838 Epidermal growth factor Proteins 0.000 description 16
- 102400001368 Epidermal growth factor Human genes 0.000 description 16
- 239000003937 drug carrier Substances 0.000 description 16
- 229940116977 epidermal growth factor Drugs 0.000 description 16
- 239000005556 hormone Substances 0.000 description 16
- 230000002401 inhibitory effect Effects 0.000 description 16
- 210000002660 insulin-secreting cell Anatomy 0.000 description 16
- 231100000444 skin lesion Toxicity 0.000 description 16
- 229940104230 thymidine Drugs 0.000 description 16
- 230000006378 damage Effects 0.000 description 15
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 14
- 230000004663 cell proliferation Effects 0.000 description 14
- 210000001339 epidermal cell Anatomy 0.000 description 14
- 108020004999 messenger RNA Proteins 0.000 description 14
- 238000013518 transcription Methods 0.000 description 14
- 230000035897 transcription Effects 0.000 description 14
- 239000007788 liquid Substances 0.000 description 13
- 108010081589 Becaplermin Proteins 0.000 description 12
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 12
- 102000004889 Interleukin-6 Human genes 0.000 description 12
- 108090001005 Interleukin-6 Proteins 0.000 description 12
- 208000025865 Ulcer Diseases 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 12
- 230000024245 cell differentiation Effects 0.000 description 12
- 230000001684 chronic effect Effects 0.000 description 12
- 238000010348 incorporation Methods 0.000 description 12
- 230000006698 induction Effects 0.000 description 12
- 229940100601 interleukin-6 Drugs 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- 102000003706 Complement factor D Human genes 0.000 description 11
- 108090000059 Complement factor D Proteins 0.000 description 11
- 206010063560 Excessive granulation tissue Diseases 0.000 description 11
- 108010030506 Integrin alpha6beta4 Proteins 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 11
- 108091000080 Phosphotransferase Proteins 0.000 description 11
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 11
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 11
- 239000000499 gel Substances 0.000 description 11
- 210000001126 granulation tissue Anatomy 0.000 description 11
- -1 i.e. Proteins 0.000 description 11
- 230000001404 mediated effect Effects 0.000 description 11
- 102000020233 phosphotransferase Human genes 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 239000000725 suspension Substances 0.000 description 11
- 108090000994 Catalytic RNA Proteins 0.000 description 10
- 102000053642 Catalytic RNA Human genes 0.000 description 10
- 210000000270 basal cell Anatomy 0.000 description 10
- 230000002301 combined effect Effects 0.000 description 10
- 230000006870 function Effects 0.000 description 10
- 239000006210 lotion Substances 0.000 description 10
- 238000004519 manufacturing process Methods 0.000 description 10
- 238000012545 processing Methods 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- 210000001541 thymus gland Anatomy 0.000 description 10
- 238000011200 topical administration Methods 0.000 description 10
- 231100000397 ulcer Toxicity 0.000 description 10
- 239000013603 viral vector Substances 0.000 description 10
- 108010076365 Adiponectin Proteins 0.000 description 9
- 102000011690 Adiponectin Human genes 0.000 description 9
- 108091027757 Deoxyribozyme Proteins 0.000 description 9
- 101710103106 Guanine nucleotide-binding protein subunit beta-2-like 1 Proteins 0.000 description 9
- 241001529936 Murinae Species 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 9
- 230000001070 adhesive effect Effects 0.000 description 9
- 230000033115 angiogenesis Effects 0.000 description 9
- 239000000074 antisense oligonucleotide Substances 0.000 description 9
- 238000012230 antisense oligonucleotides Methods 0.000 description 9
- 108010005774 beta-Galactosidase Proteins 0.000 description 9
- 230000018109 developmental process Effects 0.000 description 9
- 238000001415 gene therapy Methods 0.000 description 9
- 208000014674 injury Diseases 0.000 description 9
- 239000002609 medium Substances 0.000 description 9
- 230000001105 regulatory effect Effects 0.000 description 9
- 108091092562 ribozyme Proteins 0.000 description 9
- 230000028327 secretion Effects 0.000 description 9
- 230000002195 synergetic effect Effects 0.000 description 9
- 230000003612 virological effect Effects 0.000 description 9
- 238000001262 western blot Methods 0.000 description 9
- 108020000948 Antisense Oligonucleotides Proteins 0.000 description 8
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 8
- 102100040445 Keratin, type I cytoskeletal 14 Human genes 0.000 description 8
- 101150009401 Prkcz gene Proteins 0.000 description 8
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 8
- 241000700605 Viruses Species 0.000 description 8
- 239000000853 adhesive Substances 0.000 description 8
- 239000006071 cream Substances 0.000 description 8
- 210000002615 epidermis Anatomy 0.000 description 8
- 230000012010 growth Effects 0.000 description 8
- 230000004807 localization Effects 0.000 description 8
- 239000003921 oil Substances 0.000 description 8
- 239000002674 ointment Substances 0.000 description 8
- 230000037361 pathway Effects 0.000 description 8
- 239000011241 protective layer Substances 0.000 description 8
- 102000005962 receptors Human genes 0.000 description 8
- 108020003175 receptors Proteins 0.000 description 8
- 238000011160 research Methods 0.000 description 8
- 230000009466 transformation Effects 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 108091062157 Cis-regulatory element Proteins 0.000 description 7
- 108090000386 Fibroblast Growth Factor 1 Proteins 0.000 description 7
- 102100031706 Fibroblast growth factor 1 Human genes 0.000 description 7
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 7
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 7
- 108091023040 Transcription factor Proteins 0.000 description 7
- 201000011510 cancer Diseases 0.000 description 7
- 239000000969 carrier Substances 0.000 description 7
- 230000001086 cytosolic effect Effects 0.000 description 7
- 230000007423 decrease Effects 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 239000013604 expression vector Substances 0.000 description 7
- 210000000301 hemidesmosome Anatomy 0.000 description 7
- 239000012133 immunoprecipitate Substances 0.000 description 7
- 108010044426 integrins Proteins 0.000 description 7
- 102000006495 integrins Human genes 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 7
- 230000004660 morphological change Effects 0.000 description 7
- 239000002773 nucleotide Substances 0.000 description 7
- 235000019198 oils Nutrition 0.000 description 7
- 239000002245 particle Substances 0.000 description 7
- 229920000642 polymer Polymers 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- 238000010186 staining Methods 0.000 description 7
- 230000001629 suppression Effects 0.000 description 7
- 230000001225 therapeutic effect Effects 0.000 description 7
- 102000014777 Adipokines Human genes 0.000 description 6
- 108010078606 Adipokines Proteins 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 108091034117 Oligonucleotide Proteins 0.000 description 6
- 102100024923 Protein kinase C beta type Human genes 0.000 description 6
- 239000000478 adipokine Substances 0.000 description 6
- 238000013459 approach Methods 0.000 description 6
- 210000002469 basement membrane Anatomy 0.000 description 6
- 230000033228 biological regulation Effects 0.000 description 6
- 238000004113 cell culture Methods 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 239000011521 glass Substances 0.000 description 6
- 230000001771 impaired effect Effects 0.000 description 6
- PBGKTOXHQIOBKM-FHFVDXKLSA-N insulin (human) Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3NC=NC=3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1=CN=CN1 PBGKTOXHQIOBKM-FHFVDXKLSA-N 0.000 description 6
- 238000013508 migration Methods 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 239000003883 ointment base Substances 0.000 description 6
- 239000012071 phase Substances 0.000 description 6
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- 238000012546 transfer Methods 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 5
- 108010072051 Glatiramer Acetate Proteins 0.000 description 5
- 101001051767 Homo sapiens Protein kinase C beta type Proteins 0.000 description 5
- 206010028980 Neoplasm Diseases 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 5
- 208000004210 Pressure Ulcer Diseases 0.000 description 5
- 239000012083 RIPA buffer Substances 0.000 description 5
- 239000013504 Triton X-100 Substances 0.000 description 5
- 229920004890 Triton X-100 Polymers 0.000 description 5
- 239000013543 active substance Substances 0.000 description 5
- 230000002411 adverse Effects 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- WQZGKKKJIJFFOK-FPRJBGLDSA-N beta-D-galactose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-FPRJBGLDSA-N 0.000 description 5
- 239000013592 cell lysate Substances 0.000 description 5
- 238000003776 cleavage reaction Methods 0.000 description 5
- 210000000805 cytoplasm Anatomy 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- 239000003623 enhancer Substances 0.000 description 5
- 238000010185 immunofluorescence analysis Methods 0.000 description 5
- 238000001114 immunoprecipitation Methods 0.000 description 5
- 230000005012 migration Effects 0.000 description 5
- 238000010369 molecular cloning Methods 0.000 description 5
- 230000000877 morphologic effect Effects 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 230000037390 scarring Effects 0.000 description 5
- 230000007017 scission Effects 0.000 description 5
- 230000019491 signal transduction Effects 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 4
- 108020003589 5' Untranslated Regions Proteins 0.000 description 4
- 108010039627 Aprotinin Proteins 0.000 description 4
- 102100026189 Beta-galactosidase Human genes 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- 239000004821 Contact adhesive Substances 0.000 description 4
- 206010056340 Diabetic ulcer Diseases 0.000 description 4
- 108060003393 Granulin Proteins 0.000 description 4
- 101000976075 Homo sapiens Insulin Proteins 0.000 description 4
- 102100022905 Keratin, type II cytoskeletal 1 Human genes 0.000 description 4
- 108010070514 Keratin-1 Proteins 0.000 description 4
- 108010066321 Keratin-14 Proteins 0.000 description 4
- 108010085895 Laminin Proteins 0.000 description 4
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 4
- 108700020796 Oncogene Proteins 0.000 description 4
- 102000000887 Transcription factor STAT Human genes 0.000 description 4
- 108050007918 Transcription factor STAT Proteins 0.000 description 4
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 4
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 4
- 108020000999 Viral RNA Proteins 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- 230000003321 amplification Effects 0.000 description 4
- 230000002547 anomalous effect Effects 0.000 description 4
- 230000000692 anti-sense effect Effects 0.000 description 4
- 229960004405 aprotinin Drugs 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 230000027455 binding Effects 0.000 description 4
- MJQUEDHRCUIRLF-TVIXENOKSA-N bryostatin 1 Chemical compound C([C@@H]1CC(/[C@@H]([C@@](C(C)(C)/C=C/2)(O)O1)OC(=O)/C=C/C=C/CCC)=C\C(=O)OC)[C@H]([C@@H](C)O)OC(=O)C[C@H](O)C[C@@H](O1)C[C@H](OC(C)=O)C(C)(C)[C@]1(O)C[C@@H]1C\C(=C\C(=O)OC)C[C@H]\2O1 MJQUEDHRCUIRLF-TVIXENOKSA-N 0.000 description 4
- 229960005539 bryostatin 1 Drugs 0.000 description 4
- 230000001413 cellular effect Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000008602 contraction Effects 0.000 description 4
- 230000001276 controlling effect Effects 0.000 description 4
- 210000004207 dermis Anatomy 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 239000012636 effector Substances 0.000 description 4
- 210000002919 epithelial cell Anatomy 0.000 description 4
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 4
- 230000006801 homologous recombination Effects 0.000 description 4
- 238000002744 homologous recombination Methods 0.000 description 4
- 238000010166 immunofluorescence Methods 0.000 description 4
- 238000011065 in-situ storage Methods 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 4
- 108010052968 leupeptin Proteins 0.000 description 4
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 4
- 239000006166 lysate Substances 0.000 description 4
- 238000001000 micrograph Methods 0.000 description 4
- 239000007758 minimum essential medium Substances 0.000 description 4
- 230000002297 mitogenic effect Effects 0.000 description 4
- 238000003199 nucleic acid amplification method Methods 0.000 description 4
- 239000006072 paste Substances 0.000 description 4
- 229950000964 pepstatin Drugs 0.000 description 4
- 108010091212 pepstatin Proteins 0.000 description 4
- FAXGPCHRFPCXOO-LXTPJMTPSA-N pepstatin A Chemical compound OC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@H](C(C)C)NC(=O)[C@H](C(C)C)NC(=O)CC(C)C FAXGPCHRFPCXOO-LXTPJMTPSA-N 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 230000023650 regulation of keratinocyte proliferation Effects 0.000 description 4
- 229960004586 rosiglitazone Drugs 0.000 description 4
- 230000011664 signaling Effects 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 108020005345 3' Untranslated Regions Proteins 0.000 description 3
- 208000010370 Adenoviridae Infections Diseases 0.000 description 3
- 206010060931 Adenovirus infection Diseases 0.000 description 3
- 206010009944 Colon cancer Diseases 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 3
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 3
- 244000062730 Melissa officinalis Species 0.000 description 3
- 235000010654 Melissa officinalis Nutrition 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- 102000043276 Oncogene Human genes 0.000 description 3
- 101000971435 Oryctolagus cuniculus Protein kinase C gamma type Proteins 0.000 description 3
- 229930040373 Paraformaldehyde Natural products 0.000 description 3
- 108010078137 Protein Kinase C-epsilon Proteins 0.000 description 3
- 101710183548 Pyridoxal 5'-phosphate synthase subunit PdxS Proteins 0.000 description 3
- 102100035459 Pyruvate dehydrogenase protein X component, mitochondrial Human genes 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 208000002847 Surgical Wound Diseases 0.000 description 3
- 108091023045 Untranslated Region Proteins 0.000 description 3
- 230000002159 abnormal effect Effects 0.000 description 3
- FHEAIOHRHQGZPC-KIWGSFCNSA-N acetic acid;(2s)-2-amino-3-(4-hydroxyphenyl)propanoic acid;(2s)-2-aminopentanedioic acid;(2s)-2-aminopropanoic acid;(2s)-2,6-diaminohexanoic acid Chemical compound CC(O)=O.C[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.OC(=O)[C@@H](N)CCC(O)=O.OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 FHEAIOHRHQGZPC-KIWGSFCNSA-N 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 208000011589 adenoviridae infectious disease Diseases 0.000 description 3
- 239000000443 aerosol Substances 0.000 description 3
- 150000001413 amino acids Chemical group 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 238000001574 biopsy Methods 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000004624 confocal microscopy Methods 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 230000002950 deficient Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 150000001982 diacylglycerols Chemical class 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 210000005175 epidermal keratinocyte Anatomy 0.000 description 3
- 210000000981 epithelium Anatomy 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 230000002068 genetic effect Effects 0.000 description 3
- 229960003776 glatiramer acetate Drugs 0.000 description 3
- 235000011187 glycerol Nutrition 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 3
- 238000000099 in vitro assay Methods 0.000 description 3
- 230000002458 infectious effect Effects 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 230000010354 integration Effects 0.000 description 3
- 229940043355 kinase inhibitor Drugs 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 239000000865 liniment Substances 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 210000003141 lower extremity Anatomy 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 210000002569 neuron Anatomy 0.000 description 3
- 230000005937 nuclear translocation Effects 0.000 description 3
- 238000011580 nude mouse model Methods 0.000 description 3
- 229920002866 paraformaldehyde Polymers 0.000 description 3
- 235000019271 petrolatum Nutrition 0.000 description 3
- 150000004633 phorbol derivatives Chemical class 0.000 description 3
- 239000002644 phorbol ester Substances 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 230000004962 physiological condition Effects 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 230000029279 positive regulation of transcription, DNA-dependent Effects 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 239000003909 protein kinase inhibitor Substances 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 238000012552 review Methods 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 210000001626 skin fibroblast Anatomy 0.000 description 3
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 230000005945 translocation Effects 0.000 description 3
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 235000015112 vegetable and seed oil Nutrition 0.000 description 3
- 239000008158 vegetable oil Substances 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 2
- TVEXGJYMHHTVKP-UHFFFAOYSA-N 6-oxabicyclo[3.2.1]oct-3-en-7-one Chemical compound C1C2C(=O)OC1C=CC2 TVEXGJYMHHTVKP-UHFFFAOYSA-N 0.000 description 2
- LPMXVESGRSUGHW-UHFFFAOYSA-N Acolongiflorosid K Natural products OC1C(O)C(O)C(C)OC1OC1CC2(O)CCC3C4(O)CCC(C=5COC(=O)C=5)C4(C)CC(O)C3C2(CO)C(O)C1 LPMXVESGRSUGHW-UHFFFAOYSA-N 0.000 description 2
- 108090000644 Angiozyme Proteins 0.000 description 2
- 101150111062 C gene Proteins 0.000 description 2
- 206010009900 Colitis ulcerative Diseases 0.000 description 2
- 108010035532 Collagen Proteins 0.000 description 2
- 102000008186 Collagen Human genes 0.000 description 2
- 208000011231 Crohn disease Diseases 0.000 description 2
- 108050006400 Cyclin Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 206010011985 Decubitus ulcer Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 2
- 102100021519 Hemoglobin subunit beta Human genes 0.000 description 2
- 108091005904 Hemoglobin subunit beta Proteins 0.000 description 2
- 208000032843 Hemorrhage Diseases 0.000 description 2
- 208000005176 Hepatitis C Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 102000013266 Human Regular Insulin Human genes 0.000 description 2
- 108010090613 Human Regular Insulin Proteins 0.000 description 2
- 108010044467 Isoenzymes Proteins 0.000 description 2
- 102100023970 Keratin, type I cytoskeletal 10 Human genes 0.000 description 2
- 102000011782 Keratins Human genes 0.000 description 2
- 108010076876 Keratins Proteins 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- 208000034693 Laceration Diseases 0.000 description 2
- 239000004166 Lanolin Substances 0.000 description 2
- 238000003231 Lowry assay Methods 0.000 description 2
- 238000009013 Lowry's assay Methods 0.000 description 2
- 206010028116 Mucosal inflammation Diseases 0.000 description 2
- 201000010927 Mucositis Diseases 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- LPMXVESGRSUGHW-GHYGWZAOSA-N Ouabain Natural products O([C@@H]1[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O1)[C@H]1C[C@@H](O)[C@@]2(CO)[C@@](O)(C1)CC[C@H]1[C@]3(O)[C@@](C)([C@H](C4=CC(=O)OC4)CC3)C[C@@H](O)[C@H]21 LPMXVESGRSUGHW-GHYGWZAOSA-N 0.000 description 2
- 101150111723 PDX1 gene Proteins 0.000 description 2
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 2
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 2
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 2
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 102100036691 Proliferating cell nuclear antigen Human genes 0.000 description 2
- 102000014458 Protein Kinase C-epsilon Human genes 0.000 description 2
- 108010015499 Protein Kinase C-theta Proteins 0.000 description 2
- 102000009516 Protein Serine-Threonine Kinases Human genes 0.000 description 2
- 108010009341 Protein Serine-Threonine Kinases Proteins 0.000 description 2
- 101710109947 Protein kinase C alpha type Proteins 0.000 description 2
- 208000017442 Retinal disease Diseases 0.000 description 2
- 206010038923 Retinopathy Diseases 0.000 description 2
- 102000006382 Ribonucleases Human genes 0.000 description 2
- 108010083644 Ribonucleases Proteins 0.000 description 2
- 241000283984 Rodentia Species 0.000 description 2
- LHHQTXPEHJNOCX-UHFFFAOYSA-N Rottlerin Natural products CC(=O)c1c(O)c(C)c(O)c(Oc2c(O)c3C=CC(C)(C)Cc3c(C(=O)C=Cc4ccccc4)c2O)c1O LHHQTXPEHJNOCX-UHFFFAOYSA-N 0.000 description 2
- 229920002684 Sepharose Polymers 0.000 description 2
- 206010040799 Skin atrophy Diseases 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 208000007107 Stomach Ulcer Diseases 0.000 description 2
- 244000166550 Strophanthus gratus Species 0.000 description 2
- 206010042496 Sunburn Diseases 0.000 description 2
- 108700012920 TNF Proteins 0.000 description 2
- 208000007536 Thrombosis Diseases 0.000 description 2
- 102000006601 Thymidine Kinase Human genes 0.000 description 2
- 108020004440 Thymidine kinase Proteins 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 201000006704 Ulcerative Colitis Diseases 0.000 description 2
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 2
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 2
- 208000000558 Varicose Ulcer Diseases 0.000 description 2
- 229930003316 Vitamin D Natural products 0.000 description 2
- QYSXJUFSXHHAJI-XFEUOLMDSA-N Vitamin D3 Natural products C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C/C=C1\C[C@@H](O)CCC1=C QYSXJUFSXHHAJI-XFEUOLMDSA-N 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 230000002730 additional effect Effects 0.000 description 2
- 229960003767 alanine Drugs 0.000 description 2
- 229940024606 amino acid Drugs 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 210000004102 animal cell Anatomy 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000000740 bleeding effect Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 230000012292 cell migration Effects 0.000 description 2
- 230000010307 cell transformation Effects 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 229960000541 cetyl alcohol Drugs 0.000 description 2
- 229920001436 collagen Polymers 0.000 description 2
- 210000002808 connective tissue Anatomy 0.000 description 2
- 229940038717 copaxone Drugs 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 210000004748 cultured cell Anatomy 0.000 description 2
- 230000003111 delayed effect Effects 0.000 description 2
- 239000005547 deoxyribonucleotide Substances 0.000 description 2
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 210000003890 endocrine cell Anatomy 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 238000007667 floating Methods 0.000 description 2
- 201000005917 gastric ulcer Diseases 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 208000024693 gingival disease Diseases 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 2
- 238000005469 granulation Methods 0.000 description 2
- 230000003179 granulation Effects 0.000 description 2
- 208000014617 hemorrhoid Diseases 0.000 description 2
- 229940103471 humulin Drugs 0.000 description 2
- 206010020718 hyperplasia Diseases 0.000 description 2
- 238000003119 immunoblot Methods 0.000 description 2
- 239000012678 infectious agent Substances 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 229940039717 lanolin Drugs 0.000 description 2
- 235000019388 lanolin Nutrition 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 238000000386 microscopy Methods 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 210000004877 mucosa Anatomy 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 210000003205 muscle Anatomy 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- LPMXVESGRSUGHW-HBYQJFLCSA-N ouabain Chemical compound O[C@@H]1[C@H](O)[C@@H](O)[C@H](C)O[C@H]1O[C@@H]1C[C@@]2(O)CC[C@H]3[C@@]4(O)CC[C@H](C=5COC(=O)C=5)[C@@]4(C)C[C@@H](O)[C@@H]3[C@@]2(CO)[C@H](O)C1 LPMXVESGRSUGHW-HBYQJFLCSA-N 0.000 description 2
- 229960003343 ouabain Drugs 0.000 description 2
- 238000004806 packaging method and process Methods 0.000 description 2
- 206010033675 panniculitis Diseases 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 239000012660 pharmacological inhibitor Substances 0.000 description 2
- DCWXELXMIBXGTH-UHFFFAOYSA-N phosphotyrosine Chemical compound OC(=O)C(N)CC1=CC=C(OP(O)(O)=O)C=C1 DCWXELXMIBXGTH-UHFFFAOYSA-N 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 230000002980 postoperative effect Effects 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 238000002731 protein assay Methods 0.000 description 2
- 108010027883 protein kinase C eta Proteins 0.000 description 2
- 108010008359 protein kinase C lambda Proteins 0.000 description 2
- ZCCUUQDIBDJBTK-UHFFFAOYSA-N psoralen Chemical compound C1=C2OC(=O)C=CC2=CC2=C1OC=C2 ZCCUUQDIBDJBTK-UHFFFAOYSA-N 0.000 description 2
- 230000001185 psoriatic effect Effects 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 238000005215 recombination Methods 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- 230000010076 replication Effects 0.000 description 2
- 230000003362 replicative effect Effects 0.000 description 2
- 230000001177 retroviral effect Effects 0.000 description 2
- DEZFNHCVIZBHBI-ZHACJKMWSA-N rottlerin Chemical compound CC(=O)C1=C(O)C(C)=C(O)C(CC=2C(=C(C(=O)\C=C\C=3C=CC=CC=3)C=3OC(C)(C)C=CC=3C=2O)O)=C1O DEZFNHCVIZBHBI-ZHACJKMWSA-N 0.000 description 2
- FGDZQCVHDSGLHJ-UHFFFAOYSA-M rubidium chloride Chemical compound [Cl-].[Rb+] FGDZQCVHDSGLHJ-UHFFFAOYSA-M 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 231100000241 scar Toxicity 0.000 description 2
- 230000036573 scar formation Effects 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 210000004739 secretory vesicle Anatomy 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 230000037380 skin damage Effects 0.000 description 2
- 230000007480 spreading Effects 0.000 description 2
- 238000003892 spreading Methods 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 210000004304 subcutaneous tissue Anatomy 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 239000006208 topical dosage form Substances 0.000 description 2
- 238000010361 transduction Methods 0.000 description 2
- 230000026683 transduction Effects 0.000 description 2
- 238000011426 transformation method Methods 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 230000001228 trophic effect Effects 0.000 description 2
- 230000036269 ulceration Effects 0.000 description 2
- 241001430294 unidentified retrovirus Species 0.000 description 2
- 229960005356 urokinase Drugs 0.000 description 2
- 230000000007 visual effect Effects 0.000 description 2
- 235000019166 vitamin D Nutrition 0.000 description 2
- 239000011710 vitamin D Substances 0.000 description 2
- 150000003710 vitamin D derivatives Chemical class 0.000 description 2
- 229940046008 vitamin d Drugs 0.000 description 2
- 230000010388 wound contraction Effects 0.000 description 2
- 230000037303 wrinkles Effects 0.000 description 2
- YIRMFCGQZJVDNO-FFXVZKRQSA-N (2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-1-[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-2-acetamidopropanoyl]amino]-3-carboxypropanoyl]amino]-6-aminohexanoyl]pyrrolidine-2-carbonyl]amino]-3-carboxypropanoyl]amino]-4-methylpentanoyl]amino]acetyl]amino]-4-carboxybutanoyl]amino]-3-methylpentanoyl]amino]-4-amino-4-oxobutanoyl]amino]-3-hydroxypropanoyl]amino]-3-phenylpropanoyl]amino]-3-carboxypropanoyl]amino]-6-aminohexanoyl]amino]propanoyl]amino]-6-aminohexanoyl]amino]-4-methylpentanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-3-hydroxybutanoyl]amino]-4-carboxybutanoyl]amino]-3-hydroxybutanoyl]amino]-5-amino-5-oxopentanoyl]amino]-4-carboxybutanoyl]amino]-6-aminohexanoyl]amino]-4-amino-4-oxobutanoyl]amino]-3-hydroxybutanoyl]amino]-4-methylpentanoyl]pyrrolidine-2-carbonyl]amino]-3-hydroxybutanoyl]amino]-6-aminohexanoyl]amino]-4-carboxybutanoyl]amino]-3-hydroxybutanoyl]amino]-3-methylpentanoyl]amino]-4-carboxybutanoyl]amino]-5-amino-5-oxopentanoyl]amino]-4-carboxybutanoyl]amino]-6-aminohexanoyl]amino]-5-amino-5-oxopentanoyl]amino]propanoyl]amino]-6-aminohexanoic acid Chemical compound CC[C@H](C)[C@H](NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCCN)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(C)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(O)=O YIRMFCGQZJVDNO-FFXVZKRQSA-N 0.000 description 1
- LIFNDDBLJFPEAN-BPSSIEEOSA-N (2s)-4-amino-2-[[(2s)-2-[[2-[[2-[[(2s)-5-amino-2-[[(2s)-2-[[(2s)-6-amino-2-[[(2s)-2-[[(2s)-5-oxopyrrolidine-2-carbonyl]amino]propanoyl]amino]hexanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]acetyl]amino]acetyl]amino]-3-hydroxypropanoyl]amino Chemical compound NC(=O)C[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)CNC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@@H]1CCC(=O)N1 LIFNDDBLJFPEAN-BPSSIEEOSA-N 0.000 description 1
- CBCKQZAAMUWICA-UHFFFAOYSA-N 1,4-phenylenediamine Chemical compound NC1=CC=C(N)C=C1 CBCKQZAAMUWICA-UHFFFAOYSA-N 0.000 description 1
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 1
- KISWVXRQTGLFGD-UHFFFAOYSA-N 2-[[2-[[6-amino-2-[[2-[[2-[[5-amino-2-[[2-[[1-[2-[[6-amino-2-[(2,5-diamino-5-oxopentanoyl)amino]hexanoyl]amino]-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-(diaminomethylideneamino)p Chemical compound C1CCN(C(=O)C(CCCN=C(N)N)NC(=O)C(CCCCN)NC(=O)C(N)CCC(N)=O)C1C(=O)NC(CO)C(=O)NC(CCC(N)=O)C(=O)NC(CCCN=C(N)N)C(=O)NC(CO)C(=O)NC(CCCCN)C(=O)NC(C(=O)NC(CC(C)C)C(O)=O)CC1=CC=C(O)C=C1 KISWVXRQTGLFGD-UHFFFAOYSA-N 0.000 description 1
- KIWODJBCHRADND-UHFFFAOYSA-N 3-anilino-4-[1-[3-(1-imidazolyl)propyl]-3-indolyl]pyrrole-2,5-dione Chemical compound O=C1NC(=O)C(C=2C3=CC=CC=C3N(CCCN3C=NC=C3)C=2)=C1NC1=CC=CC=C1 KIWODJBCHRADND-UHFFFAOYSA-N 0.000 description 1
- VXGRJERITKFWPL-UHFFFAOYSA-N 4',5'-Dihydropsoralen Natural products C1=C2OC(=O)C=CC2=CC2=C1OCC2 VXGRJERITKFWPL-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000002874 Acne Vulgaris Diseases 0.000 description 1
- 206010069754 Acquired gene mutation Diseases 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 108020004491 Antisense DNA Proteins 0.000 description 1
- 108020005544 Antisense RNA Proteins 0.000 description 1
- 102100021569 Apoptosis regulator Bcl-2 Human genes 0.000 description 1
- 241000239223 Arachnida Species 0.000 description 1
- 240000003291 Armoracia rusticana Species 0.000 description 1
- 235000011330 Armoracia rusticana Nutrition 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 210000003771 C cell Anatomy 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
- 108010003422 Circulating Thymic Factor Proteins 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 241001559589 Cullen Species 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- QNAYBMKLOCPYGJ-UHFFFAOYSA-N D-alpha-Ala Natural products CC([NH3+])C([O-])=O QNAYBMKLOCPYGJ-UHFFFAOYSA-N 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 101710187001 DNA terminal protein Proteins 0.000 description 1
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 1
- 108700020911 DNA-Binding Proteins Proteins 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 239000006145 Eagle's minimal essential medium Substances 0.000 description 1
- 208000002197 Ehlers-Danlos syndrome Diseases 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102100031780 Endonuclease Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 206010053177 Epidermolysis Diseases 0.000 description 1
- 206010014989 Epidermolysis bullosa Diseases 0.000 description 1
- 102000003972 Fibroblast growth factor 7 Human genes 0.000 description 1
- 102100037362 Fibronectin Human genes 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 102100028314 Filaggrin Human genes 0.000 description 1
- 101710088660 Filaggrin Proteins 0.000 description 1
- 101000834253 Gallus gallus Actin, cytoplasmic 1 Proteins 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 208000028782 Hereditary disease Diseases 0.000 description 1
- 108010033040 Histones Proteins 0.000 description 1
- 101100268553 Homo sapiens APP gene Proteins 0.000 description 1
- 101000971171 Homo sapiens Apoptosis regulator Bcl-2 Proteins 0.000 description 1
- 101001034652 Homo sapiens Insulin-like growth factor 1 receptor Proteins 0.000 description 1
- 101001090713 Homo sapiens L-lactate dehydrogenase A chain Proteins 0.000 description 1
- 101001059454 Homo sapiens Serine/threonine-protein kinase MARK2 Proteins 0.000 description 1
- 241001135569 Human adenovirus 5 Species 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 102000003746 Insulin Receptor Human genes 0.000 description 1
- 108010001127 Insulin Receptor Proteins 0.000 description 1
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 102100039688 Insulin-like growth factor 1 receptor Human genes 0.000 description 1
- 241000408495 Iton Species 0.000 description 1
- 241000721662 Juniperus Species 0.000 description 1
- 108010065038 Keratin-10 Proteins 0.000 description 1
- 208000001126 Keratosis Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-UWTATZPHSA-N L-Alanine Natural products C[C@@H](N)C(O)=O QNAYBMKLOCPYGJ-UWTATZPHSA-N 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- 125000000998 L-alanino group Chemical group [H]N([*])[C@](C([H])([H])[H])([H])C(=O)O[H] 0.000 description 1
- 102100024580 L-lactate dehydrogenase B chain Human genes 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 101710192606 Latent membrane protein 2 Proteins 0.000 description 1
- 102100031784 Loricrin Human genes 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 208000002720 Malnutrition Diseases 0.000 description 1
- NPPQSCRMBWNHMW-UHFFFAOYSA-N Meprobamate Chemical compound NC(=O)OCC(C)(CCC)COC(N)=O NPPQSCRMBWNHMW-UHFFFAOYSA-N 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 101100070645 Mus musculus Hint1 gene Proteins 0.000 description 1
- 102000015336 Nerve Growth Factor Human genes 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 101710163270 Nuclease Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 102000042846 PKC family Human genes 0.000 description 1
- 108091082203 PKC family Proteins 0.000 description 1
- 101150001670 PRKCG gene Proteins 0.000 description 1
- 102000003982 Parathyroid hormone Human genes 0.000 description 1
- 108090000445 Parathyroid hormone Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 241000255969 Pieris brassicae Species 0.000 description 1
- 229920002367 Polyisobutene Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102000001892 Protein Kinase C-theta Human genes 0.000 description 1
- 101710094033 Protein kinase C beta type Proteins 0.000 description 1
- 102100037314 Protein kinase C gamma type Human genes 0.000 description 1
- 101710144823 Protein kinase C gamma type Proteins 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 1
- 101000702488 Rattus norvegicus High affinity cationic amino acid transporter 1 Proteins 0.000 description 1
- 101000599054 Rattus norvegicus Interleukin-6 receptor subunit beta Proteins 0.000 description 1
- 108700005075 Regulator Genes Proteins 0.000 description 1
- 241001068295 Replication defective viruses Species 0.000 description 1
- 206010070834 Sensitisation Diseases 0.000 description 1
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 1
- 102000005157 Somatostatin Human genes 0.000 description 1
- 108010056088 Somatostatin Proteins 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 239000006180 TBST buffer Substances 0.000 description 1
- 206010043189 Telangiectasia Diseases 0.000 description 1
- 101710109576 Terminal protein Proteins 0.000 description 1
- 108010078233 Thymalfasin Proteins 0.000 description 1
- 108010046075 Thymosin Proteins 0.000 description 1
- 102000007501 Thymosin Human genes 0.000 description 1
- 101800001530 Thymosin alpha Proteins 0.000 description 1
- UGPMCIBIHRSCBV-XNBOLLIBSA-N Thymosin beta 4 Chemical compound N([C@@H](CC(O)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O)C(=O)[C@@H]1CCCN1C(=O)[C@H](CCCCN)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(C)=O UGPMCIBIHRSCBV-XNBOLLIBSA-N 0.000 description 1
- 102100034998 Thymosin beta-10 Human genes 0.000 description 1
- 101710091218 Thymosin beta-12 Proteins 0.000 description 1
- 102100035000 Thymosin beta-4 Human genes 0.000 description 1
- 102000009843 Thyroglobulin Human genes 0.000 description 1
- 108010034949 Thyroglobulin Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 102000014384 Type C Phospholipases Human genes 0.000 description 1
- 108010079194 Type C Phospholipases Proteins 0.000 description 1
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 102100039037 Vascular endothelial growth factor A Human genes 0.000 description 1
- 206010062910 Vascular infections Diseases 0.000 description 1
- 108020005202 Viral DNA Proteins 0.000 description 1
- 108010067390 Viral Proteins Proteins 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- FPIPGXGPPPQFEQ-BOOMUCAASA-N Vitamin A Natural products OC/C=C(/C)\C=C\C=C(\C)/C=C/C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-BOOMUCAASA-N 0.000 description 1
- 101000647994 Xenopus laevis Signal transducer and activator of transcription 3.1 Proteins 0.000 description 1
- ZKHQWZAMYRWXGA-KNYAHOBESA-N [[(2r,3s,4r,5r)-5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] dihydroxyphosphoryl hydrogen phosphate Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP(O)(=O)OP(O)(=O)O[32P](O)(O)=O)[C@@H](O)[C@H]1O ZKHQWZAMYRWXGA-KNYAHOBESA-N 0.000 description 1
- 206010000269 abscess Diseases 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 229940022663 acetate Drugs 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 206010000496 acne Diseases 0.000 description 1
- 208000037919 acquired disease Diseases 0.000 description 1
- 229930183665 actinomycin Natural products 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 1
- 239000002280 amphoteric surfactant Substances 0.000 description 1
- 238000002266 amputation Methods 0.000 description 1
- 229940031955 anhydrous lanolin Drugs 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- NUZWLKWWNNJHPT-UHFFFAOYSA-N anthralin Chemical compound C1C2=CC=CC(O)=C2C(=O)C2=C1C=CC=C2O NUZWLKWWNNJHPT-UHFFFAOYSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000002155 anti-virotic effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 239000003908 antipruritic agent Substances 0.000 description 1
- 239000003816 antisense DNA Substances 0.000 description 1
- 229960003093 antiseptics and disinfectants Drugs 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 210000001106 artificial yeast chromosome Anatomy 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000000376 autoradiography Methods 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- UDSAIICHUKSCKT-UHFFFAOYSA-N bromophenol blue Chemical compound C1=C(Br)C(O)=C(Br)C=C1C1(C=2C=C(Br)C(O)=C(Br)C=2)C2=CC=CC=C2S(=O)(=O)O1 UDSAIICHUKSCKT-UHFFFAOYSA-N 0.000 description 1
- 230000009172 bursting Effects 0.000 description 1
- 210000001736 capillary Anatomy 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 230000025084 cell cycle arrest Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000006727 cell loss Effects 0.000 description 1
- 230000011748 cell maturation Effects 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 230000030570 cellular localization Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 238000005352 clarification Methods 0.000 description 1
- 230000009668 clonal growth Effects 0.000 description 1
- 238000011278 co-treatment Methods 0.000 description 1
- 230000036569 collagen breakdown Effects 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 210000000172 cytosol Anatomy 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 229940124447 delivery agent Drugs 0.000 description 1
- 229940009976 deoxycholate Drugs 0.000 description 1
- KXGVEGMKQFWNSR-LLQZFEROSA-N deoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 KXGVEGMKQFWNSR-LLQZFEROSA-N 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 229960002311 dithranol Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 239000013013 elastic material Substances 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- HQMNCQVAMBCHCO-DJRRULDNSA-N etretinate Chemical compound CCOC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)C=C(OC)C(C)=C1C HQMNCQVAMBCHCO-DJRRULDNSA-N 0.000 description 1
- 229960002199 etretinate Drugs 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 230000030279 gene silencing Effects 0.000 description 1
- 230000009368 gene silencing by RNA Effects 0.000 description 1
- 238000012226 gene silencing method Methods 0.000 description 1
- 238000010363 gene targeting Methods 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 230000006377 glucose transport Effects 0.000 description 1
- 230000004190 glucose uptake Effects 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 229940075507 glyceryl monostearate Drugs 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 238000009499 grossing Methods 0.000 description 1
- 239000000122 growth hormone Substances 0.000 description 1
- 210000003780 hair follicle Anatomy 0.000 description 1
- 230000036074 healthy skin Effects 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 1
- 108010037536 heparanase Proteins 0.000 description 1
- 230000036732 histological change Effects 0.000 description 1
- 238000000265 homogenisation Methods 0.000 description 1
- 230000009215 host defense mechanism Effects 0.000 description 1
- 102000055848 human LDHA Human genes 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- 230000003463 hyperproliferative effect Effects 0.000 description 1
- 210000001822 immobilized cell Anatomy 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000007901 in situ hybridization Methods 0.000 description 1
- 238000005462 in vivo assay Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000004155 insulin signaling pathway Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 108010028309 kalinin Proteins 0.000 description 1
- 239000003410 keratolytic agent Substances 0.000 description 1
- 238000000021 kinase assay Methods 0.000 description 1
- 108010087599 lactate dehydrogenase 1 Proteins 0.000 description 1
- 239000002648 laminated material Substances 0.000 description 1
- 108010057670 laminin 1 Proteins 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 206010024217 lentigo Diseases 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 108010079309 loricrin Proteins 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 229960003646 lysine Drugs 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 230000001071 malnutrition Effects 0.000 description 1
- 235000000824 malnutrition Nutrition 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 210000004779 membrane envelope Anatomy 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- YDWPOGYTJVQQIL-UHFFFAOYSA-N methyl 2-(4-aminophenoxy)acetate Chemical compound COC(=O)COC1=CC=C(N)C=C1 YDWPOGYTJVQQIL-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000004530 micro-emulsion Substances 0.000 description 1
- 238000013048 microbiological method Methods 0.000 description 1
- 238000003801 milling Methods 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 230000008747 mitogenic response Effects 0.000 description 1
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 1
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 1
- 230000004899 motility Effects 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000003007 myelin sheath Anatomy 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- 210000000944 nerve tissue Anatomy 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000037311 normal skin Effects 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- 208000015380 nutritional deficiency disease Diseases 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 230000009965 odorless effect Effects 0.000 description 1
- 238000002515 oligonucleotide synthesis Methods 0.000 description 1
- 239000003605 opacifier Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- 125000000913 palmityl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 229960001319 parathyroid hormone Drugs 0.000 description 1
- 239000000199 parathyroid hormone Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000003209 petroleum derivative Substances 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- 150000004713 phosphodiesters Chemical class 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 239000003504 photosensitizing agent Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 230000035479 physiological effects, processes and functions Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000012514 protein characterization Methods 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 238000010298 pulverizing process Methods 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000007665 sagging Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 239000012723 sample buffer Substances 0.000 description 1
- 210000004761 scalp Anatomy 0.000 description 1
- 238000004621 scanning probe microscopy Methods 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 238000007790 scraping Methods 0.000 description 1
- 210000001732 sebaceous gland Anatomy 0.000 description 1
- 230000008313 sensitization Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000008054 signal transmission Effects 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 238000007390 skin biopsy Methods 0.000 description 1
- 230000008470 skin growth Effects 0.000 description 1
- 230000037204 skin physiology Effects 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000004055 small Interfering RNA Substances 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 230000037439 somatic mutation Effects 0.000 description 1
- 229960000553 somatostatin Drugs 0.000 description 1
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 description 1
- 210000004989 spleen cell Anatomy 0.000 description 1
- 238000003153 stable transfection Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229960004274 stearic acid Drugs 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000013517 stratification Methods 0.000 description 1
- 210000000434 stratum corneum Anatomy 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 210000000106 sweat gland Anatomy 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 208000009056 telangiectasis Diseases 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- NZVYCXVTEHPMHE-ZSUJOUNUSA-N thymalfasin Chemical compound CC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O NZVYCXVTEHPMHE-ZSUJOUNUSA-N 0.000 description 1
- 229960004231 thymalfasin Drugs 0.000 description 1
- LCJVIYPJPCBWKS-NXPQJCNCSA-N thymosin Chemical compound SC[C@@H](N)C(=O)N[C@H](CO)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CO)C(=O)N[C@H](CO)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@H]([C@H](C)O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@H](CCC(O)=O)C(O)=O LCJVIYPJPCBWKS-NXPQJCNCSA-N 0.000 description 1
- 108010044465 thymosin beta(10) Proteins 0.000 description 1
- 108010070478 thymosin beta(14) Proteins 0.000 description 1
- 108010079996 thymosin beta(4) Proteins 0.000 description 1
- 108010079161 thymosin beta(9) Proteins 0.000 description 1
- 239000000724 thymus hormone Substances 0.000 description 1
- 229960002175 thyroglobulin Drugs 0.000 description 1
- 230000003488 thyrotrophic effect Effects 0.000 description 1
- 239000003104 tissue culture media Substances 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 230000014621 translational initiation Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 229960004441 tyrosine Drugs 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 238000010200 validation analysis Methods 0.000 description 1
- LSGOVYNHVSXFFJ-UHFFFAOYSA-N vanadate(3-) Chemical compound [O-][V]([O-])([O-])=O LSGOVYNHVSXFFJ-UHFFFAOYSA-N 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
- 230000029812 viral genome replication Effects 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 210000002845 virion Anatomy 0.000 description 1
- 235000019155 vitamin A Nutrition 0.000 description 1
- 239000011719 vitamin A Substances 0.000 description 1
- 229940045997 vitamin a Drugs 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/74—Synthetic polymeric materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1858—Platelet-derived growth factor [PDGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/28—Insulins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/30—Insulin-like growth factors, i.e. somatomedins, e.g. IGF-1, IGF-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/45—Transferases (2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/022—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from an adenovirus
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Endocrinology (AREA)
- Diabetes (AREA)
- Molecular Biology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Изобретение относится к медицине и касается способа, при котором уменьшают воспаление, являющееся следствием ответа на рану кожи, путем введения достаточного количества ингибитора РКСα n-миристоилированного пептида и инсулина субъекту, нуждающемуся в этом. Изобретение обеспечивает существенное снижение частоты возникновения тяжелого воспаления раны. 27 пр. 43 ил., 5 табл.
Description
Область и предпосылки изобретения
Настоящее изобретение относится к способу и фармацевтической композиции для индукции и ускорения клеточной пролиферации и/или дифференцировки клеток и, таким образом, ускорения процесса заживления ран. Более подробно настоящее изобретение относится к применению модулируемой экспрессии и/или активации, т.е. инициированной посредством мембранной транслокации и активации серин-треониновых протеинкиназ, также известных как РКС, для индуцирования и/или ускорения пролиферации клеток и/или дифференцировки клеток, и/или миграции клеток, таким образом, ускоряя процесс заживления ран. Такую модулированную экспрессию можно выполнять в соответствии с указаниями по настоящему изобретению посредством (i) трансформации клеток ран экспрессирующей РКС конструкцией; (ii) трансформации клеток ран действующим в цис-положении элементом, интегрированным в участок, прилегающий к гену и расположенный перед геном эндогенной РКС в клетках раны; (iii) введения инсулина для индуцирования экспрессии и/или активации РКС в клетках ран; (iv) трансформации клеток ран экспрессирующей инсулин конструкцией, когда после экспрессии и секреции продуцируемый с нее инсулин служит в качестве активатора экспрессии и/или активации РКС; (v) трансформации клеток ран действующим в цис-положении элементом интегрированным в участок, прилегающий к гену и расположенный перед геном эндогенного инсулина в клетках ран, когда экспрессируемый и секретируемый инсулин служит активатором для экспрессии и/или активации РКС; (vi) имплантации секретирующих инсулин клеток в рану; (vii) трансформации клеток ран транс-действующим фактором, т.е., PDX1, для индукции продуцирования и секреции эндогенного инсулина, где инсулин служит активатором для экспрессии и/или активации РКС; и (viii) введения в рану модулятора РКС.
Настоящее изобретение, выполненное посредством любого из указанных выше способов, также можно применять ex vivo для получения кожных трансплантатов.
Выполнение закрытия раны представляет собой первичную задачу в обработке ран. Открытые кожные раны представляют главную категорию ран и включают ожоговые раны, неиротрофические язвы, пролежни, трофические язвы и диабетические язвы. Открытые кожные раны обычно заживают в результате процесса, включающего в себя шесть основных компонентов: (i) воспаление; (ii) пролиферация фибробластов; (iii) пролиферация кровеносных сосудов; (iv) синтез соединительной ткани; (v) эпителизация; и (vi) стягивание ран. Раневое заживление ухудшено, когда эти компоненты либо по отдельности или все вместе не функционируют должным образом. Ряд факторов могут влиять на заживление ран, включая недостаточное питание, инфицирование, фармакологические средства (т.е. актиномицин и стероиды), пожилой возраст и диабет [см. Hunt and Goodson in Current Surgical Diagnosis & Treatment (Way; Appleton & Lange), стр.86-98 (1988)].
В отношении диабета, сахарный диабет характеризуется нарушенной передачей сигнала инсулина, повышенным уровнем глюкозы в плазме и предрасположенностью к развитию хронических осложнений, вовлекающих несколько различных тканей. Нарушенное заживление ран, приводящее к изъязвлению нижних конечностей, находится среди наименее хорошо изученных в ряду всех хронических осложнений сахарного диабета. Кроме того, изъязвление кожи у диабетических пациентов требует огромных персональных усилий и финансовых затрат (29, 30). Кроме того, язвы нижних конечностей и последующая ампутация нижней конечности представляют собой наиболее частые причины госпитализации среди диабетических пациентов (30-33). При диабете процесс заживления ран нарушен, и зажившие раны характеризуются пониженной прочностью ран. Дефект в заживлении ткани связан с несколькими факторами, включая нейропатию, сосудистое заболевание и инфекцию. Тем не менее, другие механизмы, в результате которых диабетическое состояние, ассоциированное с анормальной передачей сигнала инсулина, нарушает заживление ран и меняет физиологию кожи, не выявлены.
Также существует общая проблема заживления ран после хирургических вмешательств в разных частях организма, где операция успешна, но раневой разрез не заживает.
Кожа представляет собой многослойный плоский эпителий, в котором клетки, претерпевающие рост и дифференцировку, строго пространственно разделены. В физиологическом состоянии пролиферация ограничена базальными клетками, прикрепленными к базальнои мембране. Дифференцировка представляет собой пространственный процесс, где базальные клетки теряют их адгезию к базальной мембране, прекращают синтез ДНК и претерпевают ряд морфологических и биохимических изменений. Конечным этапом созревания является образование ороговевшего слоя, формирующего защитный барьер кожи (1, 2). Самые ранние изменения, наблюдаемые, когда базальные клетки входят в дифференцировку, связаны со способностью базальных клеток отделяться и мигрировать от базальнои мембраны (3). Сходные изменения связаны с процессом заживления ран, когда повышены миграция в раневую область и пролиферативная способность клеток. Эти процессы обязательны для перестройки слоев кожи и индукции правильной дифференцировки эпидермальных слоев.
Анализ механизмов, регулирующих рост и дифференцировку эпидермальных клеток, был значительно упрощен благодаря развитию культуральных систем для мышиных и человеческих кератиноцитов (2, 4). Кератиноциты in vitro можно поддерживать в качестве базальных пролиферирующих клеток с высокой скоростью роста. Кроме того, дифференцировку можно индуцировать in vitro, следую последовательности созревания клеток in vivo.. Ранние события включают в себя потерю компонентов гемидесмосом (3, 5) и селективную потерю α6β4 интегрина, и прикрепление клеток к матриксным белкам. Это предполагает, что изменения в экспрессии интегринов являются ранними событиями в дифференцировке кератиноцитов. Ранняя потеря гемидесмосомного контакта приводит к супрабазальной миграции кератиноцитов и связана с индукцией кератина 1 (K1) в культивируемых кератиноцитах и в коже (1, 3, 6). Дальнейшая дифференцировка в фенотип гранулярного слоя связана со снижением экспрессии β1 и β4 интегринов, потерей адгезионного потенциала ко всем матриксным белкам с последующим формированием ороговевающей оболочки и смертью клеток.
Дифференцирующиеся клетки окончательно отшелушиваются от культуральной посуды как зрелые чешуйки (2, 7). Эта программа дифференцировки in vitro точно придерживается профиля зрелого эпидермиса in vivo.
Недавние исследования в биологии кератиноцитов подчеркивают участие путей протеинкиназы C, регулирующих пролиферацию и дифференцировку кожи. Семейство серин/треониновых киназ, семейство протеинкиназ С (РКС), играет важную регуляторную роль в ряде биологических явлений (8, 9). Семейство РКС состоит, по меньшей мере, из 12 отдельных изоформ, принадлежащих к 3 различным категориям: (i) обычные изоформы (α, β1, β2, γ), активируемые посредством Ca2+, форболовых эфиров и диацилглицерола, выделяемые внутриклеточно при помощи фосфолипазы C; (ii) необычные изоформы (δ, ε, η, θ), которые также активируются форболовыми эфирами и диацилглицеролом, но не посредством Сa2+; и (iii) нетипичные (ς, λ, τ) члены семейства, которые не активируются посредством Са2+, форболовыми эфирами или диацилглицеролом.
Предполагают, что при активации большинство, но не все изоформы, перемещаются в плазматическую мембрану из цитоплазмы. Тип изоформы и профиль распределения варьирует среди различных тканей и может меняться как функция фенотипа. В ряде исследований охарактеризованы структура и функция РКС вследствие ее важности в широком ряду конечных точек действия гормонов в клетках. В коже in vivo и в культуре идентифицировали пять изоформ РКС -α, δ, ε, η и ζ. В недавних исследованиях показано, что путь передачи сигнала РКС представляет собой важный внутриклеточный медиатор дифференцировочного ответа (10, 11). Кроме того, фармакологические активаторы РКС являются мощным индукторами дифференцировки кератиноцитов in vivo и in vitro (4, 12), и ингибиторы РКС препятствуют экспрессии маркеров дифференцировки (10).
При разработке настоящего изобретения предположили, что повышенная экспрессия и/или активация изоформ РКС могут быть полезными для ускорения процессов заживления ран. Вследствие сложности эффективного введения чужеродных генов в первичные клетки посредством традиционных способов исследование роли различных изоформ РКС в пролиферации и/или дифференцировке клеток кожи было затруднено. Короткое время жизни, дифференцировочный потенциал и невозможность выделения стабильных трансформантов делают невозможной эффективную передачу чужеродных генов в первичные клетки кожи.
Предыдущая часть описывает возможное применение инсулина в качестве терапевтического средства для заживления ран. Так, в патентах США №№5591709, 5461030 и 5145679 описано местное применение инсулина в ране для ускорения заживления ран. Однако в этих патентах описывают применение инсулина в сочетании с глюкозой, так как функцией инсулина является улучшение усвоения глюкозы и, таким образом, ускорение заживления ран.
В патентной заявке США №09/748466 и международной патентной заявке № РСТ/С 1398/21794 описаны композиции, содержащие инсулин для местного применения на коже с целью улучшения здорового состояния кожи или обработки неглубоких повреждений кожи. Однако ни в одной из этих патентных заявок не указано на применение инсулина для обработки хронических, II степени или глубоких ран.
В международной патентной заявке № PCT/US01/10245 описано применение цианоакрилового полимерного наполнителя в комбинации с инсулином или серебром для заживления ран. Однако применение инсулина в сочетании с другим биологически активным средством, способным модулировать экспрессию и/или активацию РКС, не указано и не предлагается в этой заявке.
В международной патентной заявке № PCT/US85/00695 описано местное применение инсулина для лечения диабета. Однако в этой патентной заявке нет указаний по применению инсулина с целью обработки не имеющих отношения к диабету ран.
В международной патентной заявке № PCT/US92/0308 6 описаны терапевтические микроэмульсионные композиции, которые могут содержать инсулин. Однако в этой заявке нет указаний по применению инсулина в композиции с целью заживления ран.
В патентах США №№4673649 и 4940660 описаны композиции для клонального роста кератиноцитов человека и эпидермальных клеток in vitro, включающие эпидермальный фактор роста и инсулин. В этих патентах описано применение инсулина для роста культивируемых клеток кожи, которые можно применять для трансплантации. Однако применение инсулина на ранах in vivo не указано в этих патентах.
Ни в одной из процитированных выше ссылок из уровня техники не указано и не предполагается применение инсулина для модулирования экспрессии и/или активации РКС для ускорения процесса заживления ран. Кроме того, в предшествующем уровне техники не указано или не предполагается использование конструкций нуклеиновых кислот или способов генетической трансформации для доставки инсулина в раны для ускорения процесса заживления ран.
Существует широко признанная необходимость, и было бы очень выгодно иметь новые подходы для ускорения процессов, связанных с заживлением ран. Кроме того, существует широко признанная необходимость, и было бы крайне полезно иметь эффективный способ вставки в клетки кожи рекомбинантных генов, которые будут ускорять процессы пролиферации и/или дифференцировки клеток и заживление ран.
Раскрытие изобретения
В практическом воплощении настоящего изобретения авторы изобретения обнаружили, что введение в раны только инсулина может служить причиной неблагоприятных побочных эффектов, таких как повышенный ангиогенез, воспаление, гиперплазия эпидермальных клеток и рубцевание (см. пример 23 в следующем ниже разделе "Примеры"). Также авторы настоящего изобретения обнаружили, что индуцированные инсулином побочные эффекты можно эффективно обойти посредством сочетания инсулина с одним или несколькими средствами, способными модулировать экспрессию и/или активацию РКС в колонизирующих раневую область клетках, значительно ускоряя процесс заживления ран.
Настоящее изобретение относится к новым способам и композициям для эффективного лечения ран без неблагоприятных побочных эффектов, посредством доставки в раневую область эффективного количества инсулина и/или других средств, способных модулировать экспрессию и/или активацию РКС в клетках, колонизирующих раневую область и обладающих синергическим действием с инсулином, для ускорения процесса заживления ран.
Таким образом, согласно одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию введения в поврежденную кожу или кожную рану терапевтически эффективного количества средства для модуляции продуцирования и/или активации РКС.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента терапевтически эффективное количество, по меньшей мере, одного средства для модуляции продуцирования и/или активности РКС; и фармацевтически приемлемый носитель.
Согласно следующему аспекту настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию введения в поврежденную кожу или кожную рану терапевтически эффективного количества инсулина и, по меньшей мере, одного дополнительного средства, обладающего синергическим действием с инсулином, для индукции или ускорения процесса заживления поврежденной кожи или кожной раны.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента терапевтически эффективное количество инсулина, по меньшей мере, одно дополнительное средство, обладающее синергическим действием с инсулином, и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно следующему аспекту настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию введения в поврежденную кожу или кожную рану однократной дозы терапевтически эффективного количества инсулина, таким образом, индуцируя или ускоряя процесс заживления поврежденной кожи или кожной раны.
Согласно следующему аспекту настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента подобранную однократную стандартную дозу инсулина, способную индуцировать или ускорять процесс заживления поврежденной кожи или кожной раны, и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно следующему аспекту настоящего изобретения, разработан способ индукции или ускорения процесса заживления застарелых кожных ран, где способ включает стадию введения в застарелые кожные раны однократной дозы терапевтически эффективного количества инсулина, таким образом, индуцируя или ускоряя процесс заживления застарелых кожных ран.
Согласно еще одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию имплантации в поврежденную кожу или кожную рану терапевтически эффективного количества клеток, секретирующих инсулин, с тем, чтобы индуцировать или ускорить процесс заживления поврежденной кожи или застарелой кожной раны.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента секретирующие инсулин клетки и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно еще одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию трансформации клеток поврежденной кожи или кожной раны для продукции и секреции инсулина с тем, чтобы индуцировать или ускорить процесс заживления поврежденной кожи или кожной раны.
Согласно следующему аспекту настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента конструкцию нуклеиновой кислоты, предназначенную для трансформации клеток поврежденной кожи или кожной раны для продукции и секреции инсулина, и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно еще одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию трансформации клеток поврежденной кожи или кожной раны для продукции протеинкиназы С с тем, чтобы индуцировать или ускорить процесс заживления поврежденной кожи или кожной раны.
Согласно следующему аспекту настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента конструкцию нуклеиновой кислоты, предназначенную для трансформации клеток поврежденной кожи или кожной раны для продукции протеинкиназы C, и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно еще одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию введения в поврежденную кожу или кожную рану терапевтически эффективного количества активатора РКС с тем, чтобы индуцировать или ускорить процесс заживления поврежденной кожи или кожной раны.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента терапевтически эффективное количество активатора РКС для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, и фармацевтически приемлемый носитель.
Согласно еще одному из аспектов настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает стадию введения в поврежденную кожу или кожную рану терапевтически эффективного количества сополимера-1.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента терапевтически эффективное количество сополимера-1 и фармацевтически приемлемый носитель, предназначенный для местного применения фармакологической композиции.
Согласно следующему аспекту настоящего изобретения, разработан способ индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где способ включает модулирование экспрессии и/или активации, по меньшей мере, одной изоформы РКС в дермальных клетках, колонизирующих поврежденную кожу или кожную рану; и введение в дермальные клетки терапевтически эффективного количества, по меньшей мере, одного дополнительного средства, выбранного из группы, состоящей из гормона, фактора роста, адипокина, РКСδ RACK и GW9662 с модулированием экспрессии и/или активности изоформы РКС с тем, чтобы индуцировать или ускорить процесс заживления поврежденной кожи или кожной раны.
Согласно еще одному из аспектов настоящего изобретения, предоставлена фармацевтическая композиция для индукции или ускорения процесса заживления поврежденной кожи или кожной раны, где фармацевтическая композиция содержит в качестве активного ингредиента терапевтически эффективное количество вещества для модулирования экспрессии или активации, по меньшей мере, одной изоформы РКС и, по меньшей мере, одно дополнительное средство, выбранное из группы, состоящей из гормона, фактора роста, адипокина, РКСβ RACK и GW9662, и фармацевтически приемлемый носитель.
В соответствии с описанными ниже дополнительными особенностями предпочтительных вариантов осуществления изобретения, рана выбрана из группы, состоящей из язвы, раны, связанной с диабетом, ожога, солнечного ожога, застарелой раны кожи, изъязвленной раны роговицы, раны при воспалительном заболевании желудочно-кишечного тракта, раны при воспалительном заболевании кишечника, раны при болезни Крона, язвенном колите, геморрое, раны при буллезном эпидермолизе, кожно-нарывной раны, псориатической раны, раны при дерматите, раны кожи животного, дибетической раны животного, раны при ретинопатии, раны полости рта (мукозит), раны вагинальной слизистой оболочки, раны при заболевании десны, рваной раны, раны хирургического разреза и послеоперационной спаечной раны.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, язва представляет собой диабетическую язву, пролежень, венозную язву, язву желудка и язву, связанную сВИЧ.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, инсулин является рекомбинантным.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, инсулин имеет природное происхождение.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, дополнительное средство представляет собой фактор роста тромбоцитов.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, дополнительное средство представляет собой ингибитор РКСα.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, введение выполняют посредством однократного применения.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, застарелой ране кожи по меньшей мере 2 суток.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, инсулин имеет инсулиновую концентрацию в интервале от 0,1 до 10 мкМ. В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, стандартная доза инсулина составляет от 0,001 до 5 нМ в 0,01-0,2 мл фармацевтической композиции.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, доза инсулина находится в интервале от 0,01 до 0,5 нМ в 0,01-0,2 мл фармацевтической композиции.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, фармацевтическая композиция выбрана из группы, состоящей из водного раствора, геля, крема, пасты, примочки, аэрозоля, суспензии, порошка, коллоидного раствора, бальзама и мази.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, фармацевтическая композиция включает твердую основу.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы для продукции и секреции инсулина.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы при помощи рекомбинантного гена PDX1, и поэтому клетки продуцируют и секретируют природный инсулин.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы при помощи последовательности действующего в цис-положении элемента, интегрированного перед геном эндогенного инсулина клеток, и поэтому клетки продуцируют и секретируют природный инсулин.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки способны к формированию секреторных гранул.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки представляют собой эндокринные клетки.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки являются человеческими.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки представляют собой гуманизированные по гистосовместимости клетки из животного источника.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки секретируют человеческий инсулин.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, секретирующие инсулин клетки представляют собой аутологичные клетки.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки выделены из группы, состоящей из фибробластов, эпителиальных клеток и кератиноцитов.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы для продукции активатора транскрипции протеинкиназы С, и поэтому клетки продуцируют природную протеинкиназу С.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы при помощи последовательности действующего в цис-положении элемента, интегрируемой перед геном эндогенной протеинкиназы С клеток, и поэтому клетки продуцируют природную протеинкиназу с.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, клетки трансформированы при помощи рекомбинантного гена протеинкиназы С, и поэтому клетки продуцируют рекомбинантную протеинкиназу С.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, протеинкиназа С выбрана из группы, состоящей из РКС-β1, РКС-β2, РКС-γ, РКС-θ, РКС-λ и РКС-τ.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, протеинкиназа С выбрана из группы, состоящей из РКС-α, РКС-δ, РКС-ε, РКС-η и РКС-ζ.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, сополимер-1 содержится в фармацевтической композиции, адаптированной для местного применения.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, изоформа РКС выбрана из группы, состоящей из РКСα, РКС-β, РКС-δ и РКС-ζ.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, гормон представляет собой инсулин.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, фактор роста выбран из группы, состоящей из IL-6, KFG и TNFα.
В соответствии с дополнительными особенностями в описанных предпочтительных вариантах осуществления, адипокин представляет собой адипсин или адипонектин.
Настоящее изобретение успешно преодолевает недостатки известных в настоящее время форм, предоставляя новые терапевтические средства для борьбы с повреждениями кожи или кожными ранами.
Краткое описание фигур
Изобретение далее описано только посредством примера со ссылкой на сопровождающие фигуры. С конкретной ссылкой на подробные описания фигур подчеркивают, что подробности показаны в виде примера и с целью иллюстративного обсуждения предпочтительных вариантов осуществления только настоящего изобретения, и представлены с целью предоставления того, что, как полагают, является наиболее пригодным и легко понятным описанием принципов и концептуальных аспектов изобретения. В этом отношении не проводили попыток показать структурные детали изобретения более подробно, чем это необходимо для принципиального понимания изобретения, описание, рассматриваемое во взаимосвязи с фигурами, делает очевидным для специалистов в этой области, как некоторые формы изобретения можно осуществлять на практике.
На фигурах:
На фиг.1 показано эффективное повышение экспрессии изоформ РКС с применением рекомбинантных аденовирусных векторов: левая панель:
четырехсуточные первичные кератиноциты инфицировали в течение 1 часа с применением β-gal аденовируса. Через 48 часов после инфекции клетки фиксировали, и активацию белка β-галактозидазы измеряли посредством индукции голубого цвета реакции по сравнению с неинфицированными кератиноцитами. Правая панель: четырехсуточные первичные кератиноциты инфицировали в течение 1 часа с применением рекомбинантных аденовирусов, с конкретной изоформой РКС. Через двадцать четыре часа белки инфицированных (Ad) и неинфицированных контрольных (С) культур выделяли для "вестерн-блот" анализа, образцы анализировали с применением антител к конкретной изоформе РКС, как описано ниже в разделе "Примеры".
На фиг.2 показано, что активация РКС посредством бриостатина 1 индуцирует транслокацию изоформ РКС с повышенной экспрессией. Четырехсуточные первичные кератиноциты инфицировали в течение 1 часа рекомбинантными аденовирусами с конкретной изоформой РКС.Через двадцать четыре часа после инфицирования, клетки либо не обрабатывали (С), либо стимулировали бриостатином 1 (В) в течение 30 минут, и фракционировали. Образцы белков подвергали "вестерн-блоттингу" и анализировали с применением антител к конкретной изоформе РКС.
На фиг.3 показано, что изоформы РКС с повышенной экспрессией активны в своей нативной форме. Четырехсуточные первичные кератиноциты инфицировали в течение 1 часа аденовирусами с рекомбинантной конкретной изоформой РКС. Через восемнадцать часов после инфекции клеточные лизаты изнеинфицированных контрольных клеток (C) и клеток с повышенной экспрессией изоформ РКС (OЕ) иммунопреципитировали с применением антител к конкретной изоформе РКС. Иммунопреципитаты подвергали исследованию активности РКС как описано ниже в разделе "Примеры".
На фиг.4 показано, что повышенная экспрессия конкретных изоформ РКС индуцирует различные морфологические изменения в первичных кератиноцитах. Первичные кератиноциты оставляли необработанными (C) или инфицировали аденовирусами с рекомбинантными РКСα, β, η или ζ. Через двадцать четыре часа культуры наблюдали посредством микроскопии в светлом поле и фотографировали (x20).
На фиг.5 показана различная локализация изоформ РКС с повышенной экспрессией в инфицированных первичных кератиноцитах. Первичные кератиноциты наносили на покрытые ламинином 5 предметные стекла. Культуры либо не обрабатывали или инфицировали аденовирусами с различными рекомбинантными РКС. Через двадцать четыре часа после инфекции клетки фиксировали, отмывали и высушивали на воздухе. Культуры анализировали посредством иммунофлуоресценции с применением антител к конкретным изоформам РКС, затем посредством конъюгированных с FITC вторых антител. Клетки сканировали посредством конфокальной микроскопии и фотографировали характерные поля зрения.
На фиг.6 показано, что изоформы РКС специфически регулируют а6р4 интегриновую экспрессию. Пятисуточные первичные кератиноциты мышиной кожи не обрабатывали или инфицировали рекомбинантными аденовирусами с РКСα, РКСδ, РКСη или РКСζ. Через сорок восемь часов после инфекции мембранные клеточные фракции подвергали SDS-PAGE электрофорезу, переносили на нитроцеллюлозные фильтры, выполняли иммуноблоттинг с антителами к α6 и β4 и анализировали с помощью ECL.
На фиг.7 показано, что повышенная экспрессия РКСη и РКСδ индуцирует пролиферацию кератиноцитов. Пятисуточные первичные кератиноциты мышиной кожи не обрабатывали или инфицировали рекомбинантными аденовирусами с РКСδ, РКСα, РКСη или РКСζ. Через сорок восемь часов после инфекции анализировали пролиферацию клеток при помощи включения 3H-тимидина в течение 1 часа, как описано в экспериментальных процедурах. Результаты представлены как имп./мин. на кювету, по сравнению с инфицированными β-галактозидазой кератиноцитами. Величины представлены в виде среднее ± стандартное отклонение повторенных три раза определений в 3 независимых экспериментах.
На фиг.8 показано, что повышенная экспрессия изоформ РКС действует на гемидесмосомальную локализацию α6β4 интегрина. Первичные кератиноциты помещали на покрытые ламинином 5 предметные стекла, и культуры кератиноцитов содержали в MEM с низким содержанием Ca2+ в течение 48 часов. После этого культуры оставляли необработанными (А) или инфицировали рекомбинантными аденовирусами с РКСα, РКСδ, РКСη или РКСζ (B-E соответственно). Через двадцать четыре часа после инфекции кератиноциты фиксировали в 4% параформальдегиде с последующей мягкой экстракцией в 0,2% Triton-X-100, отмывали в PBS и высушивали на воздухе, как описано в экспериментальных процедурах. Культуры подвергали иммунофлуоресцентному анализу с применением антител к конкретной изоформе α6, затем посредством конъюгированных с FITC вторых антител, как описано в экспериментальных процедурах.
На фиг.9A-B показано, что повышенная экспрессия РКСδ и РКСζ индуцирует in vitro открепление кератиноцитов. (A) - Первичные кератиноциты оставляли либо необработанными (C) или инфицировали аденовирусами с рекомбинантными РКСα, δ, η, или ζ. Прикрепление клеток анализировали через 24 и 48 часов после инфекции, снимая клетки и повторно нанося их на покрытые матриксом кюветы. Количество клеток представлено как концентрация белка (мг/кювету) прикрепленных клеток. (B) - Первичные кератиноциты не обрабатывали (C) или инфицировали аденовирусами с рекомбинантными РКСα, δ, η, или ζ. Открепление клеток анализировали через 24 часа после инфекции, собирая в культуральной среде открепленные плавающие клетки. Количество клеток представлено в виде концентрации белка (мг/кювету) открепленных клеток.
На фиг.10 показано, что РКСη, экспрессирована в активно пролиферирующих кератиноцитах. Первичные кератиноциты помещали на покрытые ламинином 5 предметные стекла. Через сорок восемь часов после этого кератиноциты инкубировали с раствором BrdU в течение 1 часа с последующим иммунофлуоресцентным анализом с применением антител к РКСη (красные) и BrdU (зеленые) как описано ниже в разделе "Примеры". Клетки сканировали посредством конфокальной микроскопии и фотографировали характерные поля зрения.
На фиг.11 показано, что РКСη индуцирует, в то время как мутант по РКСη снижает пролиферацию кератиноцитов. Первичные кератиноциты кожи инфицировали в течение 1 часа аденовирусами с рекомбинантной РКСη или доминантно негативным мутантом по РКСη. (DNРКСη или РКС DNη). Через сорок восемь часов после инфекции анализировали пролиферацию клеток посредством 1-часового включения 3Н-тимидина, как описано ниже в разделе "Примеры". Результаты представлены как имп/мин на кювету. Контролем являются неинфицированные клетки.
На фиг.12A-B показано, что повышенная экспрессия РКСη и DNРКСη специфически регулируют локализацию РКС и клеточную морфологию. Первичные кератиноциты кожи инфицировали в течение 1 часа аденовирусами с рекомбинантной РКСη или доминантно негативным мутантом по РКСη (РКС DNη). Через сорок восемь часов после инфекции кератиноциты фиксировали и подвергали (А) фотографированию в светлом поле (×20) и (В) иммунофлуоресцентному анализу с применением специфичных к РКСη антител, затем посредством конъюгированных с FITC вторых антител, как описано в экспериментальных процедурах. Контролем являются неинфицированные клетки.
На фиг.13A-B показано, что ингибирование экспрессии РКСη индуцирует дифференцировку кератиноцитов в пролиферирующих кератиноцитах. Первичные кератиноциты кожи поддерживали пролиферирующими в среде с низким содержанием Ca2+, или клетки дифференцировались в течение 24 часов в среде с 0,12 мМ Ca2+. После этого кератиноциты инфицировали в течение 1 часа аденовирусами с рекомбинантной РКСη или доминантно негативным мутантом по РКСη (РКС DNη). Через двадцать четыре часа после инфекции кератиноциты содержали в среде с низким содержанием Cа2+ или переносили в содержащую 0,12 мМ Ca2+ среду для дифференцировки дополнительно еще на 24 часа. Через сорок восемь часов после инфекции кератиноциты выделяли и подвергали 505-PAGE. Экспрессию РКСη (A) и кератина 1 (B) анализировали посредством "вестерн-блоттинга".
На фиг.14 показано, что местная экспрессия РКСη in vivo улучшает формирование грануляционной ткани и ускоряет заживление ран в мышиных резаных ранах. На спине голых мышей делали полнослойный разрез кожи длиной 7 мм. На 1 и 4 сутки после нанесения раны местно применяли аденовирусную суспензию с контрольной β-gal, РКСη и РКСα. Раны фиксировали в 4% параформальдегиде, и разрезы кожи гистологически анализировали с помощью окрашивания H&E и микроскопии в светлом поле. E - эпидермис, D - дерма.
На фиг.15 показано, что инсулин, но не IGF1 специфически индуцирует транслокацию РКСδ в пролиферирующих кератиноцитах. Выделяли первичные кератиноциты и помещали в планшеты, как описано ниже в разделе "Примеры". Пролиферирующие кератиноциты содержали в течение 5 суток в среде с низким содержанием Ca2+ (0,05 мМ) до тех пор, пока они достигали 80% конфлуэнтности. Клетки стимулировали 10-7 М инсулина (Ins) или 10-8 М IGF1 (IGF) в течение 15 минут. Клетки лизировали как описано, и 20 мкг мембранных или цитозольных экстрактов стимулированных или контрольных не стимулированных (Cont) клеток подвергали SDS-PACE и переносу. Блоты исследовали при помощи специфических поликлональных антител к каждой изоформе РКС.
На фиг.16 показано, что инсулин, но не IGF1 индуцирует активность РКСδ, культуры пятисуточных кератиноцитов стимулировали 10-7 М инсулина (Ins) или 10-8 М IGF1 (IGF) в течение указанного времени (1, 15 или 30 минут). РКС5 иммунопреципитирована из мембранных (голубые столбики, тет) и цитозольных (пурпурные столбики, cyto) фракций с применением специфических к РКСδ антител. Иммунопреципитаты РКСδ анализировали на активность РКС с применением киназного исследования in vitro как описано в экспериментальных процедурах. Каждая полоса представляет собой среднее ± CO повторенных три раза определений в 3 независимых экспериментах. Величины выражены как пМ АТФ/кювету/минуту.
На фиг.17А-В показано, что инсулин и IGF1 обладают аддитивным эффектом на пролиферацию кератиноцитов. Пролиферирующие кератиноциты поддерживали в течение пяти суток в среде с низким содержанием Ca2+ (0,05 мМ) до тех пор, пока они достигали 80% конфлуэнтности. (А) Культуры пятисуточных кератиноцитов стимулировали в течение 24 часов инсулином или IGF1 в указанных концентрациях. (B) Параллельно кератиноциты стимулировали 10-7 М инсулина (Ins) и возрастающими дозами IGF1 (IGF). При каждой концентрации правая колонка (полосатый столбик) представляет пролиферацию, наблюдаемую при одновременном добавлении обоих гормонов. Левая линия демонстрирует отдельное действие 10-7 М инсулина (красные столбики) и возрастающих концентраций IGF1 (серые столбики). Включение тимидина измеряли, как описано в экспериментальных процедурах. Показанные результаты представляют собой характерные результаты 6 экспериментов. Каждая линия представляет собой среднее ± CO повторенных три раза определений, выраженных как процент, превышающий контрольные нестимулированные кератиноциты.
На фиг.18A-B показана повышенная экспрессия рекобинантных РКС аденовирусных конструкций. Культуры кератиноцитов инфицировали с применением рекомбинантных аденовирусных конструкций, содержащих дикий тип РКСδ (WTРКСδ), дикий тип РКС5 (WTРКСα) или доминантно негативный мутант по РКСδ (DNРКСδ). (A) После инфицированил клетки культивировали в течение 24 часов, собирали, и 20 мкг белковых экстрактов анализировали посредством "вестерн-блоттинга" с применением специфических антител к РКСα или РКСδ. Представленные блоты являются типичными из 5 независимых экспериментов. (B) Через двадцать четыре часа после инфицирования клетки собирали, и иммунопреципитаты РКСα или РКСδ оценивали in vitro посредством киназного анализа.
На фиг.19 показано действие повышенной экспрессии РКС на индуцированную инсулином или IGF1 пролиферацию. Неинфицированные клетки (светло-голубые столбики) или клетки с повышенной экспрессией WTРКСδ (темно-голубые столбики), или DNРКСδ (косые голубые столбики) обрабатывали в течение 24 часов 10-7 М инсулина (Ins), 10-8 М IGF1 (IGF) или тем и другим вместе (Ins + IGF). Включение тимидина измеряли, как описано в экспериментальных процедурах. Каждая линия представляет собой среднее ± СО повторенных три раза определений, сделанных на отдельных культурах. Значения представлены как процент от контроля нестимулированных клеток из той же культуры в каждом эксперименте.
На фиг.20 показано, что ингибирование активности РКСδ специфически отменяет индуцированную инсулином пролиферацию кератиноцитов. Первичные кератиноциты культивировали, как описано ниже в разделе "Примеры". Неинфицированные клетки или инфицированные DNРКСδ кератиноциты стимулировали в течение 24 часов следующими концентрациями фактора роста: 10-7 М инсулина (Ins), 10-8 М IGF1 (IGF), 10 нг/мл EGF, 10 нг/мл PDGF, 1 нг/мл KGF или 5 нг/мл ECGF. Включение тимидина измеряли, как описано ниже в разделе "Примеры". Каждая линия представляет собой среднее ± CO повторенных три раза определений, сделанных на отдельных культурах.
Значения представлены как процент от контроля - нестимулированных клеток из той же культуры в каждом эксперименте.
На фиг.21 показано, что повышенная экспрессия РКСδ специфически опосредует индуцированную инсулином пролиферацию кератиноцитов. Первичные кератиноциты культивировали, как описано согласно фиг.1. Неинфицированные клетки или инфицированные кератиноциты с повышенной экспрессией WTРКСδ стимулировали в течение 24 часов следующими концентрациями фактора роста: 10-7 М инсулина (Ins), 10-8 M IGF1 (IGF), 10 нг/мл EGF, 10 нг/мл PDGF, 1 нг/мл KGF или 5 нг/мл ECGF. Включение тимидина измеряли, как описано ниже в разделе "Примеры". Каждая линия представляет собой среднее ± СО повторенных три раза определений, сделанных на отдельных культурах. Значения представлены как процент от контроля - нестимулированных клеток из той же культуры в каждом эксперименте.
На фиг.22А-В доказана значимость РКСδ и РКСζ в процессе заживления ран кожи in vivo. Применяя in vivo мышиную модель 29 вновь разработанных конкретных изоформ РКС у мышей, с отсутствием РКСα РКСδ и РКСζ, которых вместе с животными дикого типа одного с ними помета подвергали изучению заживления ран. Мышей анестезировали, и на спине мышей выполняли сквозную пункционную биопсию кожи диаметром 4 мм. Через неделю кожу мышей снимали, и заживление ран кожи оценивали, подвергая кожные трансплантаты испытанию на разрыв раны с применением способа разрывной камеры. Значения представлены в виде давления разрыва, представляющее собой измеренное камерой максимальное давление до совершения разрыва. Результаты представляют определения, полученные в разных группах из 12-20 мышей. Эксперименты повторяли, по меньшей мере, 3 раза.
На фиг.23 обозначено специфическое взаимодействие между STAT3 и РКСδ в первичных кератиноцитах кожи. Первичные кератиноциты не обрабатывали (верхняя панель) или инфицировали в течение 1 часа аденовирусами с рекомбинантной специфической изоформой РКС (нижняя панель). Клетки выделяли и иммунопреципитировали (IP) антителами к конкретной изоформе РКС. Иммунопреципитаты подвергали анализу "вестерн-блот" с применением антител к РКС или STAT3.
На фиг.24 продемонстрирована важность активации РКСδ для индуцированной инсулином транскрипционной активации STAT3. Первичные кератиноциты наносили на предметные стекла и содержали в течение 5 суток в среде с низким содержанием Ca2+ (0,05 мМ/л) до тех пор, пока они достигали 80% конфлуэнтности. Клетки не обрабатывали (Cont, верхняя панель) или предварительно обрабатывали 5 мкМ роттлерина в течение 7 минут (R, нижняя панель), затем 10-7 М инсулина в течение 5 минут (Ins). Клетки фиксировали метанолом, отмывали и высушивали на воздухе. Культуры анализировали посредством иммунофлуоресценции с применением антитела antiphospho-Tyr-705-STAT3, за которым следует конъюгированное с FITC антитело. Клетки сканировали посредством конфокальной микроскопии.
На фиг.25 показано, что повышенная экспрессия DN РКСδ ингибирует пролиферацию кератиноцитов, индуцированную посредством повышенной экспрессии РКСδ и STAT3. Первичные кератиноциты инфицировали в течение 1 часа рекомбинантными аденовирусными конструкциями, содержащими β-Gal (для контроля), РКСδ, WT STAT3, DN STAT3, или дважды инфицировали DN РКСδ, а затем STAT3. Через 24 часа после инфекции пролиферацию клеток анализировали посредством включения 3Н-тимидина в течение 1 часа. Результаты представлены как DPM/мг белка. Каждая линия представляет собой среднее из трех определений в планшете из той же культуры.
На фиг.26 продемонстрирована важность концентраций инсулина и частоты применений для заживления ран in vivo. На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и обрабатывали PBS (контроль) или применяли инсулин в различных концентрациях и с разной частотой (т.е. семь ежедневных повторных применений по сравнению с однократным применением). Через семь суток после ранения мышей умерщвляли и измеряли области обработанных ран. Результаты представлены как мм2 раневой области, и каждая линия представляет собой среднее из шести повторов ± стандартное отклонение (p<0,005).
На фиг.27 продемонстрированы гистологические эффекты концентраций и частоты применений инсулина на заживление ран in vivo. На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и обрабатывали различными концентрациями инсулина и с различной чатотой применений (т.е. семь ежедневных повторных применений по сравнению с однократным применением). Гистологические срезы ран выполняли через семь суток после ранения и анализировали эпидермальное и дермальное закрытие (раневое стягивание). Эпидермальное закрытие определяли посредством окрашивания антителами к кератину 14 (К14) (левая панель), и считали положительным, если рана положительно окрашивалась на протяжении всей щели. Дермальное закрытие считали положительным, если оба дермальных края раны можно было наблюдать в световом микроскопе в одном поле зрения при ×100 увеличении (правая панель). Результаты представлены как процент закрытия раны относительно контроля, и каждая линия представляет собой среднее шести повторений.
На фиг.28 продемонстрировано синергическое действие сочетания инсулина и выделенного из тромбоцитов фактора роста (PDGF-BB) на заживление ран in vivo. На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и обрабатывали однократным применением инсулина, PDGF-BB или комбинированными инсулином и PDGF-BB. Через семь суток после ранения обработанных мышей умерщвляли, и забирали биоптаты для гистологических анализов эпидермального и дермального закрытия (раневого стягивания). Эпидермальное закрытие определяли посредством окрашивания антителами к кератину 14 (К14) (левая панель), и считали положительным, если рана положительно окрашивалась на протяжении всей щели. Дермальное закрытие считали положительным, если оба дермальных края раны можно было наблюдать в световом микроскопе в одном поле зрения при ×100 увеличении (правая панель). Результаты представляли как суммарные, на гистограмме в виде процента закрытия раны относительно контроля, и каждая линия представляет собой среднее шести повторений.
Фиг.29A-D представляют собой фотографии, иллюстрирующие морфологический эффект комбинированных инсулина и ингибитора РКСα на заживление ран in vivo. На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и либо не обрабатывали (контроль), или обрабатывали инсулином (HO/01), комбинированным с ингибитором РКСα (HO/02). Через 7 суток после ранения забирали биопсии кожи для морфологических наблюдений. На фиг.29A-B показаны контрольные раны, тогда как на фиг.29C-D показаны обработанные раны.
Фиг.30 представляет собой гистологическую микрофотографию, иллюстрирующую комбинированное воздействие инсулина и ингибитора РКСα на дермальное закрытие (раневое стягивание). На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и либо не обрабатывали (контроль), или ежедневно обрабатывали инсулином (HO/01), комбинированным с ингибитором РКСα (HO/02). Через семь суток после ранения обработанных мышей умерщвляли. Выполняли гистологические срезы ран и наблюдали в световом микроскопе. Дермальное закрытие считали положительным, если оба дермальных края раны можно было наблюдать в световом микроскопе в одном поле зрения при ×100 увеличении. Область открытых ран в необработанном контрольном срезе (левая панель) была слишком большой, чтобы поместиться в одно поле зрения при ×100 увеличении, тогда как срез обработанной раны (правая панель) показывает положительное дермальное закрытие. Желтые пятнистые линии обозначают края дермы.
Фиг.31 представляет собой гистологическую микрофотографию, иллюстрирующую комбинированное воздействие инсулина и ингибитора РКСα на эпидермальное закрытие. На спине 8-10 недельных C57BL мышей выполняли раневые разрезы и либо не обрабатывали, или ежедневно обрабатывали инсулином (HO/01), комбинированным с ингибитором РКСα (HO/02). Через семь суток после ранения обработанных мышей умерщвляли. Выполняли гистологические срезы ран, окрашивали антителами к кератину 14 (указывающими на базальные кератиноциты) и наблюдали в световом микроскопе. Область открытых ран (обозначена стрелкой) в необработанном контрольном срезе (левая панель) была слишком большой, чтобы поместиться в одно поле зрения при x100 увеличении, тогда как срез обработанной раны (правая панель) показывает эпидермальное закрытие на всем протяжении раневой щели.
Фиг.32 представляет собой гистологическую микрофотографию, иллюстрирующую комбинированное воздействие инсулина и ингибитора РКСα на пространственную дифференцировку эпидермальных клеток. Раненных мышей (C57BL, 8-10 недель) ежедневно обрабатывали местными аппликациями инсулина (HO/01), комбинированного с ингибитором РКСα (HO/02). Через семь суток после ранения обработанных мышей умерщвляли. Выполняли гистологические срезы ран и окрашивали антителом к кератину 1 (К1), выделяющему начальную стадию пространственной дифференцировки клеток. Необработанный контрольный срез (левая панель) показывает крупную недифференцированную раневую область (обозначена стрелкой), тогда как в обработанном раневом срезе (правая панель) можно наблюдать массовое эпидермальное восстановление.
На фиг.33 продемонстрирован количественное действие инсулина, комбинированного с ингибитором РКСα на заживление ран in vivo. Раненных мышей (C57BL, 8-10 недель) ежедневно обрабатывали местными аппликациями инсулина (HO/01), комбинированного с ингибитором РКСα (HO/02). Через семь суток после ранения обработанных мышей умерщвляли. Выполняли гистологические срезы ран и анализировали дермальное сжатие, эпидермальное закрытие и пространственную дифференцировку, как описано выше в фиг.30-32. На гистограмме показана доля (процентная) от полностью заживших ран, что определяли посредством гистологического анализа в каждой обработанной группе.
Фиг.34A-G представляют собой фотографии, иллюстрирующие комбинированный эффект ингибирования экспрессии и/или активности РКСα и модулирования экспрессии и/или активности другой изоформы РКС в дермальных клетках, или введения гормона в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные фибробласты кожи инфицировали доминантно-негативной (DN) неактивной киназой РКСα. Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.34A), или инфицировали дикого типа (WT) РКСδ (фиг.34В), РКСη (фиг.34C), WT РКСζ (фиг.340) или WT РКСε (фиг.34Е). Наоборот РКСα- ингибированные культуры обрабатывали адипсином (2 мкг/мл; фиг.34F) или инсулином (6,7×10-7 М; фиг.34G). Через 24 часа после обработки получали фотографии.
Фиг.35А-Н представляют собой фотографии, иллюстрирующие комбинированный эффект ингибирования экспрессии и/или активности РКСα и модулирования экспрессии и/или активности другой изоформы РКС в дермальных клетках, или введения гормона в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные кератиноциты кожи инфицировали доминантно-негативной (DN) неактивной киназой РКСα. Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.35A), или инфицировали дикого типа (WT) РКСε (фиг.350), WT РКСζ (фиг.35E) или WT РКСη (фиг.35F). Наоборот РКСα-ингибированные культуры обрабатывали IL-6 (1 мкг на планшет; фиг.35B), KGF (1 мкг на планшет; фиг.35C), РКСδ RACK (10-7 М; фиг.35H) или TNFα (12 мкг/мл; фиг.35G). Через 24 часа после обработки получали фотографии.
Фиг.36A-B представляют собой фотографии, иллюстрирующие комбинированное воздействие ингибирования экспрессии и/или активности РКСζ, в дермальных клетках и введения фактора роста в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные фибробласты кожи инфицировали доминантно-негативной (DN) неактивной киназной формой РКСζ (DNζ). Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.36A) или KGF (1 мкг на планшет; фиг.36B). Через 24 часа после обработки получали фотографии.
Фиг.37A-D представляют собой фотографии, иллюстрирующие комбинированое воздействие ингибирования экспрессии и/или активности РКСζ в дермальных клетках и введения фактора роста или гормона в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные кератиноциты кожи инфицировали доминантно-негативной (DN) неактивной киназной формой РКСζ (DNζ). Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.37A) или IL-6 (1 мкг на планшет; фиг.37В), TNFα (12 мкг/мл; фиг.37C) или адипонектином (1 мкг на планшет; фиг.37D). Через 24 часа после обработки получали фотографии.
Фиг.38А-Е представляют собой фотографии, иллюстрирующие комбинированныое воздйствие ингибирования экспрессии и/или активности РКСβ в дермальных клетках и введения фактора роста, инсулина или GW9662 в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные фибробласты кожи инфицировали доминантно-негативной (DN) неактивной киназной формой РКСβ (DNβ). Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.38A), или обрабатывали KFG (1 мкг на планшет; фиг.38В), IL-6 (1 мкг на планшет; фиг.38С), инсулином (6,7×10-7 М; фиг.38D) или GW9662 (1 мкг на планшет; фиг.38Е). Через 24 часа после обработки получали фотографии.
Фиг.39A-E представляют собой фотографии, иллюстрирующие комбинированное воздействие стимуляции экспрессии и/или активации РКСδ и модулирования экспрессии и/или активности другой изоформы РКС в дермальных клетках, или введения гормона в дермальные клетки на закрытие ран кожи in vitro. Культивируемые первичные кератиноциты кожи инфицировали формой киназы РКСδ (DNδ) дикого типа (WT). Через двадцать четыре часа выполняли царапины, и культуры оставляли необработанными (фиг.39A) или инфицировали WT РКСζ (РКСζ; фиг.39В), WT РКСε (РКСε; фиг.39C) или DN РКСα (РКСα; фиг.39D). Наоборот, РКСδ-стимулированные культуры обрабатывали адипсином (2 мкг/мл; фиг.39Е). Через 48 часов после обработки получали фотографии.
Фиг.40А-F представляют собой фотографии, иллюстрирующие воздействие введения сополимера-1, инсулина, псевдосубстрата РКСа или их сочетаний, на закрытие ран кожи in vitro. Культивируемые первичные кератиноциты оставляли необработанными (фиг.40A) или обрабатывали только инсулином (6,7×107 М; фиг.40B), только сополимером-1 (55 мкг/планшет; фиг.40С), смесью инсулина и псевдосубстрата РКСα (6,7×10-7 М и 107 М, соответственно; фиг.40D), смесью сополимера-1 и инсулина (55 мкг/планшет и 6,7×10-7 М, соответственно; фиг.40D) или смесью сополимера-1, инсулина и псевдосубстрата РКСα (55 мкг/планшет, 6,7×10-7 М и 107 М, соответственно; фиг.40F). Через 48 часов после обработки получали Фотографии.
Фиг.41A-D представляют собой фотографии, иллюстрирующие воздействие сополимера-1, инсулина, псевдосубстрата РКСα или их комбинаций, на заживление ран in vivo. Раненных мышей оставляли необработанными (фиг.41A) или обрабатывали ежедневно в течение 4 суток местными аппликациями сополимера-1 (55 мкг/мл; фиг.41B), смесью сополимера-1 и инсулина (55 мкг/мл и 1 мкМ, соответственно; фиг.41C) или смесью сополимера-1, инсулина и псевдосубстрата РКСα (55 мкг/мл, 1 мкМ и 1 мкМ, соответственно; фиг.41D). Фотографии получали через 4 суток после ранения.
Фиг.42A-H представляют собой гистологические микрофотографии, иллюстрирующие воздействие близости тимуса к раневой щели на процесс заживления ран. На фиг.42A-B показан тимус нормального взрослого грызуна при ×200 увеличении. На фиг.42C показана увеличенная ×40 7-суточная застарелая рана, тимус наблюдали в непосредственной близости от раневой щели (в красном квадрате; увеличено при ×200, фиг.42D). Рана реэпителизирована, формируется грануляционная ткань и развивается дермальное стягивание. На фиг.42E-F показана 9-суточная застарелая рана мыши с STZ диабетом, увеличенная ×40 (фиг.42Е) и ×200 (фиг.42F), в непосредственной близости от раневой щели тимус не наблюдали, и не наблюдали реэпителизации, грануляционной ткани или дермального стягивания. На фиг.42G показана 9-суточная застарелая рана мыши с STZ диабетом, увеличенная ×40. Рану обрабатывали смесью инсулина и псевдосубстрата РКСα. Тимус наблюдали в непосредственной близости от раневой щели (в красном квадрате; увеличение ×20, фиг.42H). Рана реэпителизирована, формируется грануляционная ткань, и развивается дермальное стягивание.
Фиг.43 представляет собой фотографию, иллюстрирующую эффект инсулина, комбинированного с ингибитором РКСα, на заживление ран и поврежденной кожи. На спине Large Whites & Landrace домашних свиней выполняли продольные раневые разрезы и ежедневно обрабатывали в течение 15 суток PBS (контроль) или смесью из 1 мкМ инсулина и 1 мкМ псевдосубстрата РКСα (HO/03/03). Через 30 суток после ранения раны фотографировали. Обработанные HO/03/03 раны полностью зажили без образования рубца и демонстрируют значительно лучшую эстетику кожи по сравнению с буферным контролем.
Описание предпочтительных вариантов осуществления
Настоящее изобретение представляет собой способы и фармацевтические композиции, предназначенные для модулирования экспрессии и/или активации серин-треониновых протеинкиназ, также известных как РКС, для индукции и/или ускорения пролиферации клеток и/или дифференцировки клеток, и, таким образом, ускорения процесса заживления ран. Такую модулированную экспрессию можно выполнять в соответствии с указаниями по настоящему изобретению посредством (i) трансформации клеток ран экспрессирующей РКС конструкцией; (ii) трансформации клеток ран действующим в цис-положении элементом, вставляемым в участок, прилегающий и расположенный перед геном эндогенной РКС в клетках раны; (iii) введения инсулина и других средств, обладающих синергическим действием с инсулином для модулирования экспрессии и/или активации РКС в клетках ран; (iv) трансформации клеток ран экспрессирующей инсулин конструкцией, когда после экспрессии и секреции продуцируемый с нее инсулин служит в качестве активатора экспрессии и/или активации РКС; (v) трансформации клеток ран действующим в цис-положении элементом, вставляемым в участок, прилегающий и расположенный перед геном эндогенного инсулина в клетках раны, когда экспрессируемый и секретируемый инсулин служит активатором для экспрессии и/или активации РКС; (vi) имплантации секретирующих инсулин клеток в рану; (vii) трансформации клеток ран транс-действующим фактором, т.е., PDX1, для индукции продукции и секреции эндогенного инсулина, инсулин служит активатором для экспрессии и/или активации РКС; и (viii) введения в рану модулятора РКС. Принципы и действие способов и фармацевтических композиций по настоящему изобретению можно лучше понять со ссылкой на фигуры и сопровождающие описания.
До подробного объяснения, по меньшей мере, одного варианта осуществления изобретения необходимо понять, что изобретение не ограничено в его применении подробностями структуры и классификацией компонентов, указанных в следующем ниже описании, или проиллюстрированных примерами в разделе "Примеры". По изобретению возможны другие варианты осуществления или практического применения, или исполнение его различными путями. Также необходимо понять, что фразеология и терминология использована здесь с целью описания, и ее не следует рассматривать в качестве ограничения.
Взрослая кожа включает в себя два слоя: ороговевший многослойный эпидермис и подлежащий толстый слой богатой коллагеном дермальной соединительной ткани, обеспечивающей опору и питание. Кожа служит защитным барьером против внешнего мира. Следовательно, любое повреждение или разрушение в коже необходимо быстро и эффективно устранять. Как описано здесь выше в разделе "Предпосылки", первая стадия заживления достигается посредством образования тромба, закрывающего исходную рану. После этого воспалительные клетки, фибробласты и капилляры проникают в тромб, формируя грануляционную ткань. Следующие стадии включают в себя реэпителизацию раны, где базальные кератиноциты вынуждены утрачивать свои гемидесмосомные контакты, кератиноциты мигрируют на грануляционную ткань, покрывая рану. После миграции кератиноцитов, кератиноциты вступают в пролиферативный рост, позволяющий заменить клетки, потерянные при повреждении. После покрытия раны монослоем кератиноцитов, формируется новый многослойный эпидермис и вновь образовывается новая базальная мембрана (20-23). Показано, что в этом процессе принимают участие некоторые факторы роста, включающие ЕСГ семейство факторов роста, KGF, PDGF и TGFβ1 (22-24). Полагали, что среди этих факторов роста EGF и KGF тесно вовлечены в регуляцию пролиферации и миграции эпидермальных кератиноцитов (25, 26). Знание сигналов, запускающих миграцию клеток в раны, пролиферацию и формирование нового матрикса в раневой щели, является фундаментальным в понимании биологии заживления ран.
Чтобы облегчить понимание изобретения, далее в описании изобретения формулируют ряд терминов, определенных ниже.
Термин "рана" широко относится к повреждениям кожи и подкожной ткани, инициированным в любом одном из множества способов (т.е. пролежни при продолжительном постельном режиме, раны в результате травм, рубцы, язвы, ожоги и тому подобное), и с варьирующими характеристиками. Обычно раны относят к одной из четырех степеней, зависящих от глубины раны: (i) Степень 1: раны, ограниченные эпителием; (ii) Степень II: раны, распространяющиеся в дерму; (iii) Степень III: раны, распространяющиеся в подкожную ткань; и (iv) Степень IV (или полнослойные раны): раны с обнаженными костями (т.е. костная точка давления, такая как большой вертел или крестец).
Термин "рана с неполной глубиной" относится к ранам, охватывающим Степени I-III; примеры ран частичной толщины включают в себя ожоговые раны, пролежни, трофические язвы и диабетические язвы.
Термин "глубокая рана" включает в себя раны Степени III и Степени IV.
Термин "заживление" в отношении к ране относится к процессу восстановления раны при помощи образования рубца.
Фраза "индуцирующий или ускоряющий процесс заживления ран" относится либо к индукции формирования грануляционной ткани стягивания ран и/или индукции эпителизации (т.е. образование новых клеток эпителия). Заживление ран удобно измеряют по уменьшению раневой области.
В настоящем изобретении рассмотрена обработка всех типов ран, включая глубокие раны и хронические раны.
Термин "хроническая рана" относится к ране, не зажившей в течение тридцати суток.
Фраза "трансформируя клетки" относится к временному или постоянному изменению содержания нуклеиновой кислоты клетки посредством введения экзогенной нуклеиновой кислоты, которая либо интегрирует в геном клетки и генетически модифицирует клетку, или остается неинтегрированной.
Термин "действующий в цис-положении элемент" использован здесь для описания генетической области, служащей сайтом прикрепления для ДНК-связывающих белков (например, энхансеры, операторы и промоторы), влияя, таким образом, на активность одного или нескольких генов на той же хромосоме.
Фраза "транс-действующий фактор" применен здесь для описания фактора, связывающего действующий в цис-положении элемент, и посредством этого модулирует его активность по отношению к экспрессии гена. Так, PDX1 представляет собой трансдействующий фактор, связывающий промотор гена инсулина и модулирующий его активность.
Фраза "активатор транскрипции" применен здесь для описания фактора, повышающего экспрессию гена. Транс-действующий фактор представляет собой пример непосредственного активатора транскрипции.
Термин "активатор" применен здесь для описания повышающей активность молекулы.
Используемая здесь фраза "модулированная экспрессия и/или активация" относится к повышенной или ингибированной экспрессии и/или активации.
РКС представляет собой важный сигнальный путь, опосредующий пролиферацию и дифференцировку кератиноцитов. Изоформы РКС α, δ, ε, η и ζ экспрессированы в коже (4, 10). Во время разработки настоящего изобретения предполагали, что модулированная экспрессия и/или активация РКС может индуцировать пролиферацию и/или дифференцировку клеток и, таким образом, ускорять процесс заживления ран. Во время приведения настоящего изобретения к практическому применению эту теорию подтвердили рядом экспериментов, показывающих, что модулированная экспрессия и/или активация РКС действительно индуцирует пролиферацию клеток и клеточную дифференцировку, и ускоряет процесс заживления ран. Как указано здесь далее более подробно, предпринимали множество различных подходов к модулированию экспрессии и/или активации РКС, чтобы, таким образом, ускорить процесс заживления ран. Основываясь на экспериментальных данных, разработали другие подходы. Во время приведения настоящего изобретения к практическому применению открыли поразительный и новый феномен, что инсулин служит модулятором экспрессии и/или активации РКС. По существу, инсулин может служить терапевтическим средством для модулирования экспрессии и/или активации РКС для того, чтобы ускорять процесс заживления ран.
Большую важность для биологии заживления ран кожи представляют свойства различных изоформ РКС и их специфические эффекты на пролиферацию и/или дифференцировку клеток. Применение аденовирусных конструкций РКС дает возможность идентифицировать особые роли множества изоформ РКС в процессе заживления ран in vitro и in vivo. Все изоформы способны специфически затрагивать различные аспекты роста и дифференцировки кератиноцитов. Две изоформы РКСδ и РКСζ могут специфически регулировать интегриновую регуляцию (см. ниже пример 6), адгезию к базальной мембране (см. ниже пример 9) и формирование гемидесмосом (см. ниже пример 8). Обнаружили, что две изоформы РКСδ и РКСη регулируют потенциал пролиферации эпидермальных кератиноцитов (см. примеры 7 и 11). Дополнительно доминантно негативная изоформа РКСη (DNРКСη) способна специфически индуцировать дифференцировку в активно пролиферирующих кератиноцитах (см. ниже пример 12). В заключение, важность различных изоформ РКС в процессе заживления ран в коже также подтвердили в системе in vivo. Применение мышей, с отсутствием собственной РКС, где отсутствовала экспрессия различных изоформ РКС, показало, что РКСδ и РКСζ, которые, как было найдено, необходимы для процессов адгезии и подвижности в кератиноцитах кожи, также важны в процессе заживления ран in vivo в модели на животных (см. пример 19). Чрезкожные полнослойные биопсии в РКС "нулевой" коже позволили предположить что РКСδ и РКСζ, но не РКСα, необходимы для надлежащего заживления ран. Кроме того, ниже на примере 22 показано, что ингибитор РКСα эффективно способствует заживлению ран in vivo, показывая, таким образом, что изоформа РКСα может являться антагонистом заживления ран. РКСη обладает уникальным тканевым распределением. Она преимущественно экспрессирована в эпителиальных тканях (27, 28). Исследования гибридизации in situ, так же как и иммуногистохимические исследования демонстрировали, что РКСη. высоко экспрессирована в дифференцирующихся и дифференцированных слоях (27). Представленные здесь результаты предполагают роль РКСη, как функционального регулятора пролиферации и дифференцировки кожи, зависимого от клеточной физиологии. Когда кератиноциты поддерживали в пролиферативном состоянии в условиях с низким содержанием Ca2+, РКСη индуцировала коэффициент пролиферации в пять-семь раз выше по сравнению с контрольными кератиноцитами. Однако, когда индуцировали дифференцировку клеток, повышая концентрацию Са2+, дифференцировка повышалась с более быстрым и высоким коэффициентом по сравнению с контрольными клетками (см. пример 12). Это может объяснить способность РКСη резко индуцировать заживление ран и формирование грануляционной ткани так, что достигали пролиферативную способность и формирование слоев дифференцировки. Интересно, что результаты заживления ран in vivo и экспрессия РКСη в эмбриональной ткани, уровень экспрессии которой обычно невысок у взрослых, предполагают возможную роль РКСη в пролиферации и тканевой организации также и других тканей. Они включают в себя нервную ткань, так же как и кожу, и мышечную ткань, эффективно заживавшие в грануляционной ткани ран. Кроме того, способность специфически регулировать дифференцировку кератиноцитов и индуцировать нормальную дифференцировку в активно пролиферирующих клетках посредством применения доминантно негативного мутанта, позволяет специфически манипулировать дифференцировкой и контролировать гиперпролиферативные нарушения, вовлеченные в заживление ран.
Здесь приведен пример, показывающий, что заживляющая способность РКСη, проявленная in vivo, на раны, выполненные на спине голых мышей. Ниже на примере 14 показано, что введение экспрессирующих РКС конструкций в раны, приводило к формированию грануляционной ткани через четверо суток после местной инфекции.
Суммарно, представленные здесь результаты демонстрируют, что модулирование экспрессии и/или активации (активации мембран) различных изоформ РКС является эффективным средством борьбы с ранами. Таким образом, стимулировать заживление ран можно при помощи повышения экспрессии и/или активности изоформ РКСδ, РКСη и РКСζ, или ингибируя экспрессию и/или активность изоформы РКСα.
Таким образом, согласно одному аспекту настоящего изобретения, разработан способ индукции или ускорения процесса заживления повреждений или кожной раны, осуществляемый посредством введения в кожную рану терапевтически эффективного количества, по меньшей мере, одного средства для модулирования экспрессии и/или активации РКС. Следовательно, фармацевтическая композиция для осуществления способа согласно данному аспекту настоящего изобретения, содержит в качестве активного ингредиента терапевтически эффективное количество, по меньшей мере, одного средства для модулирования экспрессии и/или активации РКС; и фармацевтически приемлемый носитель.
Используемая здесь фраза "кожная рана" относится к любому типу ран эпителия, включающих в качестве не ограничивающих примеров язвы, такие как диабетическая язва, пролежень, венозная язва, язва желудка и язва, рана, связанная с ВИЧ, рана, связанная с диабетом, ожог, солнечный ожог, застарелая рана кожи, изъязвленная рана роговицы, рана при воспалительном заболевании желудочно-кишечного тракта, рана при воспалительном заболевании кишечника, рана при болезни Крона, рана при язвенном колите, геморрое, рана при буллезном эпидермолизе, кожно-нарывная рана, псориатическая рана, рана кожи животного, дибетическая рана животного, рана при ретинопатии, рана полости рта (мукозит), рана вагинальной слизистой оболочки, рана при заболевании десны, рваная рана, рана хирургического разреза и послеоперационная спаечная рана.
Используемая здесь фраза "повреждение кожи" относится к любому типу повреждений кожи или условий, таких как, например, морщины (например, индуцированные ультрафиолетовым излучением морщины), складки кожи, трещины, шишки, крупные поры (например, ассоциированные с придаточными структурами, такими как протоки потовых желез, сальных желез или волосяные фолликулы) или неровности или шероховатости, потеря эластичности кожи (потеря и/или инактивация функционального эластина кожи), провисание (включая отечность в области глаз и челюстей), потеря плотности кожи, потеря упругости кожи, потеря упругого возврата кожи после деформации, изменение цвета (включая круги под глазами), прыщи, желтизна, гиперпигментированные области кожи, такие как старческие пятна и лентиго, кератозы, ненормальная дифференцировка, гиперкератинизация, эластоз, распад коллагена и другие гистологические изменения в роговом слое, дерме, эпидермисе, сосудистой системе кожи (например, телеангиэктазия или паукообразные сосуды) и подлежащих тканях, особенно ближайших к коже.
Кожу не рассматривают как классическую ткань, отвечающую на инсулин. Поэтому эффекты инсулина в коже, по большей части, объясняют его способностью активировать близкородственный IGFR. Показали, что в кератиноцитах инсулин и IGF1 могут стимулировать оба рецептора и активировать сходные расположенные ниже эффекторы (34). Однако в настоящем изобретении демонстрируют, что, несмотря на то, что оба фактора роста индуцируют пролиферацию кератиноцитов в доза-зависимых условиях, каждый гормон осуществляет свои эффекты через различные сигнальные пути. Исходное свидетельство о различной регуляции пролиферации кератиноцитов посредством инсулина и IGF1 подтвердили данные, что эти гормоны оказывают аддитивное воздействие на пролиферацию кератиноцитов при добавлении их вместе в максимальной индуцирующей пролиферацию концентрации каждого гормона (см. пример 15). Чтобы идентифицировать точку расхождения сигнальных путей инсулина и IGF1 в регуляции пролиферации кератиноцитов, проверяли элементы, известные, как регулирующие пролиферацию кератиноцитов, и действующие, как находящиеся ниже эффекторы сигнального пути инсулина. Эти исследования показали, что передачу сигнала инсулина в пролиферации кератиноцитов специфически опосредует РКСδ (см. пример 17). РКСδ является единственной изоформой в семействе белков РКС, специфически вовлеченная в рост и созревание различных типов клеток (35). Однако показали, что тогда как РКСδ специфически регулируется при помощи нескольких факторов роста, включающих в себя EGF, фактор роста тромбоцитов и неиротрансмиттеры, показано, что ее физиологические эффекты принимают участие в ингибировании факторов роста клеточного роста, в том числе апоптоза, дифференцировки и задержки или остановки клеточного цикла (36-41). Недавно показали, что в течение 12-24 часов после повышения Ca2+ в культивируемых мышиных кератиноцитах селективная потеря интегринового комплекса α6β4 связана с индукцией K1 (6). Потеря экспрессии белка α6β4 является результатом транскрипционных и пост-транскрипционных событий, включающих в себя усиленный процессинг α6 и β4 цепей. В предварительных исследованиях установили связь между активацией РКС, процессингом и регуляцией интегрина α6β4. Эти результаты совпадают с предшествующими результатами о роли РКСδ, а также РКСζ, в потере экспрессии α6β4 и формировании гемидесмосом, индуцирующими открепление кератиноцитов. Однако в настоящем изобретении идентифицирована еще одна роль РКСδ, как мишени для индуцированной инсулином пролиферации кератиноцитов. Примеры ниже показывают, что только стимуляция инсулином, но не множеством факторов роста, включающих в себя в качестве не ограничивающих примеров EGF, KGF, PDGF, ECGF и IGF1, может транслоцировать и активировать РКСδ, но не любую другую из экспрессированных в коже изоформ РКС. Значимость РКСδ для стимуляции инсулином подтвердили позднее, когда митогенная стимуляция с помощью EGF, KGF, PDGF, ECGF и IGF1 не отменялась посредством доминантно-негативной РКСδ мутанта, и инсулин оказался основным активатором этой изоформы РКС в регуляции пролиферации кератиноцитов (см. пример 17). Однако, когда кератиноциты инфицировали WT РКСδ, митогенная стимуляция кератиноцитов посредством EGF и KGF повышалась. Это позволяет предположить, что активация РКСδ также необходима для пролиферативнои стимуляции других факторов роста посредством находящихся выше сигнальных путей. Кроме того, охарактеризовали находящиеся ниже элементы, опосредующие индуцированную инсулином активацию РКСδ, пролиферацию кератиноцитов и участие STAT3, активатора транскрипции в этом процессе. Белки STAT (сигнальные трансдукторы и активаторы транскрипции) представляют собой семейство транскрипционных факторов, привлекаемых множеством цитокинов и факторов роста. Среди семи известных членов STAT семейства STAT3 является уникальным. Прицельное разрушение STAT3, но не других членов семейства STAT, приводит к ранней эмбриональной летальности. Особенно, когда STAT3 условно удаляли в коже, восстановление кожи сильно нарушалось. При активации, белки STAT формируют гомо- или гетеродимеры, перемещаются в ядро и связываются с отвечающими элементами ДНК генов-мишеней для индукции транскрипции.
Обнаружили, что в кератиноцитах РКСδ, ноне другие изоформы РКС, экспрессированные в коже (РКСα, ζ, η и ε), конститутивно ассоциированы со STAT3 (см. пример 18). Кроме того, инсулин регулирует фосфорилирование, активацию и ядерную транслокацию STAT3 посредством специфической активации РКСδ. Ингибирование активности РКСδ посредством фармакологического ингибитора роттлерина или посредством повышенной экспрессии доминантно негативного РКСδ мутанта отменяло индуцированную инсулином активацию и ядерную транслокацию STAT3. Наконец, повышенная экспрессия доминантно негативного РКСδ мутанта ингибировала индуцированную посредством повышенной экспрессии STAT3 пролиферацию кератиноцитов (см. пример 18). Эти результаты говорят о роли индуцированной инсулином активности РКС5 в транскрипционной активации посредством STAT3 в пролиферации кератиноцитов кожи. Так как STAT3 важен для восстановления кожи и является находящимся ниже эффектором, привлекаемым множеством цитокинов и факторов роста, все эти результаты говорят об активации РКСδ как основного находящегося ниже элемента, опосредующего пролиферацию кератиноцитов посредством множества факторов роста кожи. Особенно, РКСδ может быть первостепенным кандидатом в патогенезе дефектного заживления ран, как это оказалось у больных диабетом. Связь между РКСδ и заживлением ран также можно подтвердить in vivo. Применяя вновь сконструированных РКСδ "нулевых" мышей, здесь показано, что отсутствие РКСδ задерживает заживление ран в коже мышей (см. пример 19). Связь между РКСδ и передачей сигнала установили в нескольких других системах. Например, недавно показано, что в культурах мышечных клеток РКСδ опосредует индуцированный инсулином транспорт глюкозы (42, 43). Сходно, в клетках с повышенной экспрессией рецептора инсулина, показано, что стимуляция инсулином ассоциирована с активацией РКСδ (44-46). Однако, тогда как в этих исследованиях опосредованная инсулином активация РКСδ связана с метаболическими эффектами инсулина, это первое сообщение, связывающее РКСδ с опосредованной инсулином пролиферации клеток. Идентифицировали двойственную роль РКСδ в регуляции пролиферации кератиноцитов и контроле ранних этапов дифференцировки, где показали, что клетки теряют свое прикрепление к подлежащей базальной мембране. Это может говорить об индуцированной инсулином РКСδ, как об основном кандидате регуляции физиологического баланса между пролиферацией и дифференцировкой в коже.
Таким образом, по указаниям настоящего изобретения модулирование экспрессии и/или активации является результатом влияния инсулина на клетки ран. Это можно осуществить посредством одного из множества альтернативных способов, как показано здесь ниже.
Одним способом является направленное введение инсулина в рану. Как описано в примерах 21 и 22 здесь ниже, местное применение инсулина в ранах в диапазоне концентраций от 0, до 10 мкМ эффективно активировало эпидермальное и дермальное закрытие и, следовательно, заживление ран. Кроме того, необычно и неожиданно, применение инсулина, комбинированного с фактором роста PDGF-BB или с ингибитором РКСα, приводило к значительному и синергическому улучшению процесса заживления ран по сравнению с одним инсулином.
Таким образом, согласно еще одному аспекту настоящего изобретения, предоставлен способ индукции или ускорения процесса заживления ран или повреждений кожи. Способ является результатом введения в раны кожи терапевтически эффективного количества инсулина и, по меньшей мере, одного дополнительного средства, обладающего синергическим действием с инсулином, для того чтобы индуцировать или ускорить процесс заживления ран или повреждений кожи. Предпочтительно средство представляет собой ингибитор РКСα. Более предпочтительно, средство представляет собой фактор роста, такой как PDGF, EGF, TGFβ, KGF, ECGF или IGF1, и, наиболее предпочтительно, средство представляет собой PDGF-BB.
Направленное введение инсулина, одного или комбинированного с еще одним средством, может быть результатом однократного или повторных применений. Во время приведения настоящего изобретения к практическому применению авторы неожиданно обнаружили, что обработка однократным применением инсулина в концентрации 1 мкМ существенно более эффективна в заживлении ран, чем семь повторных ежедневных применений инсулина подобной концентрации (см. пример 20 ниже).
Таким образом, согласно еще одному аспекту настоящего изобретения, предоставлен способ индукции или ускорения процесса заживления ран или повреждений кожи посредством введения в раны кожи однократной стандартной дозы терапевтически эффективного количества инсулина. Предпочтительно однократная стандартная доза содержит от 0,001 до 5 нМ, предпочтительно от 0,01 до 0,5 нМ инсулина, например, в водном растворе, геле, креме, пасте, примочке, аэрозоле, суспензии, порошке, коллоидном растворе, бальзаме или препарате мази в количестве, необходимом для того, чтобы закрыть участок ран кожи в 1 см, например, 0,01-0,2 мл.
Срок введения инсулина в раны может быть критичным, как проиллюстрировано в примере 20 в следующем ниже разделе "Примеры". Например, однократное применение инсулина в 4-суточные раны приводит к эффективному заживлению ран. Таким образом, согласно еще одному аспекту настоящего изобретения, предоставлен способ индукции или ускорения процесса заживления застарелых ран кожи посредством введения в раны однократной дозы терапевтически эффективного количества инсулина.
Используемая здесь фраза "застарелая рана кожи" относится к ране кожи, которой, по меньшей мере, одни сутки, двое суток, трое суток, предпочтительно, четверо суток.
Фармацевтическая композиция для индукции или ускорения процесса заживления ран или повреждений кожи, согласно еще одному аспекту настоящего изобретения, содержит в качестве активного ингредиента терапевтически эффективное количество инсулина, по меньшей мере, одно дополнительное средство, обладающее синергическим действием с инсулином, и фармацевтически приемлемый носитель, предназначенный для местного применения фармацевтической композиции.
Предпочтительно средство представляет собой ингибитор РКСα или фактор роста, такой как PDGF, EGF, TGFJ3, KGF, ECGF или IGF1, и наиболее предпочтительно средство представляет собой PDGF-BB. Фармацевтически приемлемый носитель может представлять собой в качестве не ограничивающих примеров гель, крем, пасту, примочку, аэрозоль, суспензию, порошок, коллоидный раствор, бальзам или мазь, как подробно указано ниже. Твердые основы также можно применять для пролонгированного высвобождения инсулина в раны. Следует понимать, что инсулин может быть природным или предпочтительно рекомбинантным, человеческим или из любого другого пригодного источника.
Согласно еще одному аспекту настоящего изобретения, фармацевтическая композиция для индукции или ускорения процесса заживления ран или повреждений кожи может содержать однократную стандартную дозу, способную индуцировать или ускорять процесс заживления повреждений или ран кожи, и фармацевтически приемлемый носитель, предназначенный для местного применения фармацевтической композиции. Предпочтительно однократная стандартная доза инсулина находится в диапазоне от 0,001 до 5 нМ, предпочтительно от 0,01 до 0,5 нМ, в 0,01-0,2 мл препарата стандартной дозы.
Согласно альтернативному варианту осуществления настоящего изобретения экспрессирующие и секретирующие инсулин клетки имплантируют в раны, чтобы индуцировать или ускорить процесс заживления ран или повреждений кожи. Такими инсулин-продуцирующими клетками могут быть естественно продуцирующие инсулин клетки, или альтернативно, такие клетки трансформируют, чтобы продуцировать и секретировать инсулин. Клетки можно трансформировать посредством, например, рекомбинантного гена PDX1 (см. инвентарные №№ GeneBank AH005712, Af035260, Af035259), представляющий собой транс-действующий фактор для продукции и секреции инсулина. Альтернативно, клетки можно трансформировать посредством последовательности действующего в цис-положении элемента, такого как активный и конститутивный или индуцибельный промотор, интегрируемый перед геном эндогенного инсулина клетки с целью нокаута/вставки с изменением функции гена, чтобы трансформировать клетки и повысить продукцию и секрецию естественного инсулина. Это можно получить, так как области, расположенные перед геном инсулина, клонированы (см. инвентарные №№E00011, NM000207). Альтернативно, клетки трансформируют рекомбинантным геном инсулина (например, инвентарные №J02547), и поэтому клетки продуцируют и секретируют рекомбинантный инсулин.
Фармацевтическая композиция для индукции или ускорения процесса заживления ран или повреждений кожи по этому аспекту настоящего изобретения, следовательно, содержит в качестве активного ингредиента секретирующие инсулин клетки и фармацевтически приемлемый носитель, предназначенный для местного применения фармацевтической композиции. Преимущественно вводимые в раны секретирующие инсулин клетки способны к формированию секреторных гранул, чтобы секретировать, таким образом, продуцированный инсулин. Секретирующими инсулин клетками могут быть эндокринные клетки. Они могут быть из человеческого источника или из гуманизированного по гистосовместимости животного источника. Наиболее предпочтительно секретирующие инсулин клетки, трансформированные или нет, принадлежат аутологичному источнику. Инсулин, секретированный посредством секретирующих инсулин клеток, предпочтительно является человеческим инсулином или имеет аминокислотную последовательность человеческого инсулина. Секретирующими инсулин клетками могут быть фибробласты, эпителиальные клетки или кератиноциты, при условии трансформации, как описано выше, применяемой с тем, чтобы сделать такие клетки способными к продукции и секреции инсулина.
По еще одному альтернативному варианту осуществления клетки ран кожи трансформируют для продукции и секреции инсулина, чтобы индуцировать или ускорить процесс заживления кожной раны.
Фармацевтическая композиция для индукции или ускорения процесса заживления ран кожи по этому аспекту настоящего изобретения, следовательно, содержит в качестве активного ингредиента конструкцию нуклеиновой кислоты, предназначенную для трансформации клеток кожной раны, чтобы продуцировать и секретировать инсулин, и фармацевтически приемлемый носитель, предназначенный для местного применения фармацевтической композиции.
Любой из описанных выше способов трансформации, например, трансформация кодирующей инсулин конструкцией, трансформация конструкцией, содержащей действующий в цис-положении элемент, для вставки ниже гена эндогенного инсулина посредством способа нокаут/вставки с изменением функции гена и трансформация конструкцией, кодирующей трансдействующий фактор, для активации продукции и секреции эндогенного инсулина можно применять в контексте этого варианта осуществления настоящего изобретения.
Предшествующие исследования об эффектах различных изоформ РКС в коже были затруднены из-за трудности эффективного введения чужеродных генов в первичные клетки посредством традиционных способов вследствие короткого времени жизни, потенциала дифференцировки и невозможности выделить стабильные трансформанты. Чтобы преодолеть эти препятствия, использовали вирусные векторы для введения интересующих генов. Вирусные векторы конструировали посредством модификации вирусного генома в форме вирусов с дефектом по репликации. Наиболее широко применяли вирусные векторы, представляющие собой ретровирусы и аденовирусы, применяемые как в экспериментальных, так и в целях генной терапии (13). Особенно, аденовирусная инфекция высокоэффективна в нереплицирующихся клетках, высокий титр вируса и высокая экспрессия трансдуцированного белка делает эту систему крайне выгодной для первичных культур, по сравнению с ретровирусными векторами. Так как аденовирусы не интегрируют в геном хозяина, и стабильные вирусные титры можно интерпретировать дефицитом репликации, эти вирусные конструкции связаны с минимальным риском злокачественных новообразований как у человека, так и на животных моделях (14). До настоящего времени в коже аденовирусные конструкции успешно применяли с высокой эффективностью инфекции в подходах ex vivo и in vivo (15, 16). В настоящем исследовании применяли аденовирусный вектор, сконструированный I. Satio и его коллегами (17). Длина космидной кассеты (pAxCAwt) составляет почти полную длину генома аденовируса-5, но у нее отсутствуют области E1A, Е1В и Е3, приводящие к дефектной репликации вируса. Она содержит составной промотор CAG, состоящий из непосредственно-раннего энхансер цитомегаловируса, куриного промотора β-актина и сигнала полиаденилирования β-глобина кролика, сильно индуцирующих экспрессию вставленных ДНК (13, 17). Представляющий интерес ген вставляли в космидную кассету, которую затем ко-трансфецировали в клетки эмбриональной селезенки человека 293 одновременно с концевым белковым комплексом (ТРС) на аденовирусной ДНК. В экспрессирующих области E1A и E1B клетках 293 происходит рекомбинация между космидной кассетой и аденовирусной DNA-TPC, производя желаемый рекомбинантный вирус эффективнее в сто раз, по сравнению с традиционными способами. Такой высокой эффективности достигают преимущественно благодаря применению аденовирусной DNA-TPC вместо протеинизированной ДНК. Кроме того, присутствие более длинных гомологичных областей повышает эффективность гомологичной рекомбинации. Восстановления репликации компетентных вирусов избегают благодаря присутствию множества сайтов EcoT221. В отношении этого следует заметить, что кератиноциты, инфицированные различными аденовирусными рекомбинантными РКС, через 24 часа демонстрировали эффективную повышенную экспрессию изоформ РКС (см. пример 1).
Таким образом, еще одним способом, посредством которого выполняли модулирование экспрессии и/или активации РКС, по настоящему изобретению, является индукция повышенной экспрессии РКС в клетках кожной раны. Этого можно достичь посредством трансформации клеток последовательностью действующего в цис-положении элемента, интегрированного посредством способа гомологичной рекомбинации, расположенного перед эндогенной протеинкиназой С клеток, и заставляя, таким образом, клетки продуцировать природную протеинкиназу C. Кроме того, альтернативно, этого можно достичь посредством трансформации клеток геном рекомбинантнои протеинкиназы С, такими как, но не ограниченных примерами, РКС-β1 ген (инвентарные №№X06318, NM02738), РКС-β2 ген (инвентарный №X07109), РКС-γ ген (инвентарный №L28035), РКС-θ ген (инвентарный №L07032), РКС-λ ген (инвентарный №D28577), РКС-τ ген (инвентарный №L8964), РКСα ген (инвентарный №Х52479), РКС-δ ген (инвентарные №№L07860, L07861), РКС-ε ген (инвентарный №Х72974), РКС-η ген (инвентарный №Z15108) и РКС-ζ ген (инвентарные №№Z15108, Х72973, NM002744) и, таким образом, заставляя клетки продуцировать рекомбинантную протеинкиназу C.
Следовательно, фармацевтическая композиция для индукции или ускорения процесса заживления кожной раны, по этому аспекту настоящего изобретения содержит в качестве активного ингредиента конструкцию нуклеиновой кислоты, предназначенную для трансформации клеток ран кожи с тем, чтобы продуцировать протеинкиназу C, и фармацевтически приемлемый носитель, предназначенный для местного применения фармацевтической композиции.
Кроме того, еще один способ, посредством которого выполняли модулирование экспрессии и/или активации РКС по настоящему изобретению представляет собой активатор РКС, такой как, но не ограниченный данными примерами Ca2+, инсулин или бриостатин-1 с тем, чтобы индуцировать или ускорить процесс заживления ран кожи.
Следовательно, фармацевтическая композиция для индукции или ускорения процесса заживления ран или повреждений кожи, согласно этому аспекту настоящего изобретения содержит в качестве активного ингредиента терапевтически эффективное количество активатора РКС с тем, чтобы индуцировать или ускорить процесс заживления ран или повреждений кожи, и фармацевтически приемлемый носитель.
Кроме того, еще одним способом, посредством которого выполняли модулирование экспрессии и/или активации РКС по настоящему изобретению, является способ со снижением экспрессии и/или активности изоформы РКС.
Снижение активности изоформ РКС можно выполнять посредством ингибитора изоформ псевдосубстрата РКС, такими как, например, РКСα, РКСζ или РКСη псевдосубстратными ингибиторами (CalbioChem, Калифорния, США), или еще одним ингибитором изоформ РКС, таким как, например, фармацевтический пептид LY379196 (Elly Lilly, США).
Альтернативно, снижение активности изоформ РКС можно выполнять посредством доминантно негативной (DN) РКС аденовирусной конструкцией, такой как описано здесь в разделе "Примеры" ниже.
Снижение экспрессии изоформ РКС можно выполнять посредством небольшой интерферирующей молекулы РНК (миРНК). Интерференция РНК представляет собой двустадийный процесс. На первой стадии, называемой стадией инициации, вводимые дцРНК, расщепляются на малые интерферирующие РНК (миРНК) длиной 21-23 нуклеотида (nt), возможно под действием Dicer, представителя семейства РНКаз III, семейства дцРНК-специфических рибонуклеаз, процессирующего дцРНК (введенные направленно или посредством трансгена или вируса) АТФ-зависимым образом. При успешном расщеплении РНК расщепляется на дуплексы длиной 19-21 п.о. (миРНК), каждый с двухнуклеотидными 3'-выступающими концами [Hutvagner and Zamore Curr. Opin. Genetics and Development 12: 225-232 (2002); and Bernstein Nature 409: 363-366 (2001)].
В эффекторной стадии, дуплексы миРНК связываются с нуклеазными комплексами, формируя индуцированный РНК молчащий комплекс (RISC). Для активации RISC необходимо АТФ-зависимое расплетание дуплекса миРНК. Затем активный RISC метит гомологичный транскрипт посредством взаимодействий пар оснований и расщепляет их РНК до 12-нуклеотидных фрагментов от 3' конца миРНК [Hutvagner and Zamore Curr. Opin. Genetics and Development 12: 225-232 (2002); Hammond et. al. (2001) Nat. Rev. Gen. 2: 110-119 (2001); and Sharp Genes. Dev 15: 485-90 (2001)]. Хотя механизм расщепления еще не определен окончательно, исследование показывает, что каждый RISC содержит одну миРНК и РНКазу [Hutvagner and Zamore Curr. Opin. Genetics and Development 12: 225-232 (2002)].
Из-за исключительной эффективности иРНК предложили стадию амплификации каскадом реакций иРНК. Амплификацию можно осуществлять посредством копирования введенных дцРНК, которые будут синтезировать большее количество миРНК, или посредством репликации образованных миРНК. Альтернативно или дополнительно, амплификацию можно выполнять посредством множества циклов RISC [Hammond et. al. Nat. Rev. Gen. 2: 110-119 (2001), Sharp Genes. Dev. 15: 485-90 (2001); Hutvagner and Zamore Curr. Opin. Genetics and Developme 12: 225-232 (2002)]. Более полную информацию о иРНК см. в следующих обзорах Tuschi ChemBiochem. 2: 239-245 (2001); Cullen Nat. Immunol. 3: 597-599 (2002); and Branti Biochem. Biophys. Act. 1575: 15-25 (2002).
Синтез молекул иРНК, пригодный для применения по настоящему изобретению, можно выполнять, как указано далее. Во-первых, изученная последовательность мРНК изоформ РКС расположена ниже старт-кодона для АА 2-нуклеотидных последовательностей. Появление каждых АА и 3'-прилегающих 19 нуклеотидов отмечают как потенциальные сайты-мишени миРНК. Предпочтительно, сайты-мишени миРНК выбирают из открытой рамки считывания, так как в сайтах связывания регуляторных белков нетранслируемых областей (UTRs) больше. UTR-связывающие белки и/или комплексы инициации трансляции могут интерферировать со связывающим эндонуклеазным комплексом миРНК [Tuschi ChemBiochem. 2: 239-245]. Однако следует понимать, что направленные в нетранслируемые области миРНК также могут быть эффективны, как продемонстрировано для GAPDH, где миРНК, направленная в 5'UTR, опосредовала около 90% снижения клеточной мРНК GAPDH, и полному отсутствию на уровне белка (www.ambion.com/techlib/tn/91/912.html).
Во-вторых, потенциальные сайты-мишени сравнивали с соответствующей геномной базой данных (например, человеческая, мышиная, крысиная и т.д.) с применением любого выравнивающего последовательности программного обеспечения, такое как программное обеспечение BLAST, доступное на сервере NCBI (www.ncbi.nlm.nih.gov/BLAST). Предполагаемые сайты-мишени, обнаружившие значительную гомологию с другими кодирующими последовательностями, отфильтровывали.
Определив последовательности-мишени, для синтеза миРНК выбрали матричную последовательность. Предпочтительные последовательности включают в себя низкое содержание G/C, так как доказали, что они более эффективны в опосредовании молчания генов по сравнению с теми, в которых содержание G/C выше, чем 55%. Для определения некоторые сайты-мишени предпочтительно выбирали вдоль по всей длине гена-мишени. Для лучшей оценки выбранных миРНК отрицательный контроль предпочтительно применяли в участках соединения. Предпочтительно отрицательный контроль миРНК включает в себя ту же нуклеотидную композицию, что и миРНК, но недостаточной гомологии с геномом. Таким образом, предпочтительно применяют кодируемую нуклеотидную последовательность миРНК, при условии, что она не обнаруживает какой-либо значительной гомологии с любым другим геном. По настоящему изобретению миРНК может быть удобной, например, способная ингибировать экспрессию РКСα миРНК, такая как любая из последовательностей нуклеиновых кислот, описанных в SEQ ID №№1-16.
Еще одним средством, способным понижать экспрессию изоформ РКС, является молекула ДНКзим, способная к специфическому расщеплению мРНК транскрипта или последовательности ДНК изоформ РКС. ДНКзимы представляют собой одноцепочечные полинуклеотиды, способные к расщеплению одно- и двухцепочечных последовательностей-мишеней (Breaker, R.R. and Joyce, G. Chemistry and Biology 1995; 2: 655; Santoro, S.W. & Joyce, G.F. Proc. Nati, Acad. Sci. USA 1997; 943: 4262). Для ДНКзимов предложили общую модель ("10-23" модель). "10-23" ДНКзимы имеют каталитический домен из 15 дезоксирибонуклеотидов, фланкированных посредством двух распознающих субстрат доменов, каждый от семи до девяти дезоксирибонуклеотидов. Этот тип ДНКзима может эффективно расщеплять свои субстраты РНК до соединений пурин: пиримидин (Santoro, S.W. & Joyce, G.F. Proc. Nati, Acad. Sci. USA 199; обзор ДНКзимов см. в LM [Curr Opin Mol Ther 4: 119-21 (2002)].
В патентной заявке США №6326174 Joyce et al. сообщали примеры конструкций и амплификации синтетических, сконструированных, распознающих сайты расщепления одно- и двухцепочечных мишеней ДНКзимов. Недавно наблюдали ингибирование экспрессии рецептора урокиназы ДНКзимами сходной конструкции, направленными против рецептора урокиназы человека, и удачное ингибирование in vivo метастазов раковых клеток толстой кишки (Iton et al 2002, Abstract 409, Ann Meeting Am Soc Gen Ther www.asgt.org). В еще одной заявке комплементарные к bcr-abi онкогенам ДНКзимы успешно ингибировали экспрессию онкогенов в лейкемических клетках, и снижали частоту рецидивов в случаях CML и ALL при трансплантации аутологичного костного мозга.
Снижение экспрессии изоформ РКС можно также выполнять посредством применения антисмыслового полинуклеотида, способного к специфической гибридизации с транскриптом мРНК, кодирующим изоформу РКС.
Конструирование антисмысловых молекул, которые можно применять для эффективного снижения экспрессии изоформ РКС, нужно выполнять с учетом двух аспектов, важных в подходе с применением антисмысловых молекул. Первый аспект представляет собой доставку олигонуклеотида в цитоплазму соответствующей клетки, тогда как вторым аспектом является конструирование олигонуклеотида, специфически связывающего указанную мРНК в клетках, в известной мере ингибируя их трансляцию.
В предшествующей области указаны ряд стратегий доставки, которые можно применять для эффективной доставки олионуклеотидов в широком диапазоне типов клеток [см., например, Luft J Mol Med 76: 75-6(1998); Kronenwett et al. 91: 852-62 (1998); Rajur et al. Bioconjug Chem 8: 935-40 (1997); Lavigne et al. Biochem Biophys Res Commun 237: 566-71 (1997) and Aoki et al. (1997) Biochem Biophys Res Commun 231: 540-5 (1997)].
Кроме того, также доступны алгоритмы для идентификации этих последовательностей с наивысшей рассчитанной аффинностью связывания для их мРНК-мишеней, основанные на термодинамическом цикле, принимающим в расчет энергетику структурных изменений мРНК-мишени и олигонуклеотида [см., например, Walton et al. Biotechnol Bioeng 65: 1-9 (1999)].
Такие алгоритмы успешно применяли для осуществления антисмыслового способа в клетках. Например, разработанный Walton et al. алгоритм, дал возможность ученым успешно сконструировать антисмысловые олигонуклеотиды для транскриптов бета-глобина кролика (RBG) и мышиного фактора некроза опухоли-альфа (TNF-альфа). Позднее, та же исследовательская группа сообщала, что доказано, что активность разумно выбранных антисмысловых олигонуклеотидов в модели с тремя мРНК-мишенями (лактатдегидрогеназы A и B человека и gp130 крысы) в культуре клеток, как определяли посредством способа кинетической ПЦР, эффективна почти во всех случаях, включая тесты к трем разным мишеням в двух типах клеток с применением олигонуклеотидов с фосфодиэфирными и фосфоротиоатными химическими связями.
Дополнительно, некоторые способы конструирования и прогнозирования эффективности специфических олигонуклеотидов с применением систем in vitro также публиковали (Matveeva etal., Nature Biotechnology 16: 1374-1375 (1998)].
В некоторых клинических исследованиях демонстрировали безопасность, целесообразность и активность антисмысловых олигонуклеотидов. Например, успешно применяли предназначенные для лечения рака антисмысловые олигонуклеотиды [Holmund et al., Curr Opin Mol Ther 1: 372-85 (1999)], тогда как в проведенных клинических исследованиях лечения злокачественных опухолей гематологического происхождения посредством антисмысловых олигонуклеотидов, направленных на гены c-myb, p53 и Bcl-2 показана толерантность к ним у пациентов [Gerwitz Curr Opin Mol Ther 1: 297-306 (1999)].
Позднее сообщали, что опосредованная антисмысловыми олигонуклеотидами супрессия экспрессии гена гепараназы человека ингибирует плевральную диссеминацию раковых клеток человека в мышиной модели [Uno et al., Cancer Res 61: 7855-60 (2001)].
Таким образом, существует общепринятое мнение, что современные разработки в области технологий с применением антисмысловых олигонуклеотидов, которые, как описано выше, приводят к образованию высоко точных алгоритмов конструирования антисмысловых олигонуклеотидов и широкому диапазону систем их доставки, как правило, дают возможность специалистам в данной области конструировать и выполнять соответствующие подходы с применением антисмысловых олигонуклеотидов для снижения экспрессии известных последовательностей без вынужденных обращений к неуместным исследованиям и ошибочным экспериментам.
Еще одно средство, способное снижать экспрессию изоформ РКС, представляет собой молекулу рибозима, способную специфически расщеплять кодирующий изоформу РКС транскрипт мРНК. Рибозимы все больше применяют для сиквенс-специфического ингибирования экспрессии генов посредством расщепления кодирующей интересующие белки мРНК [Welch et al. Curr Opin Biotechnol. 9: 486-96 (1998)]. Возможность конструирования рибозимов с тем, чтобы расщеплять любую специфическую мишень РНК делает их ценными инструментами в фундаментальных исследованиях и терапевтических применениях. В области клинической медицины рибозимы применяли для выявления вирусных РНК при инфекционных заболеваниях, основных онкогенов при раке и конкретных соматических мутаций при наследственных расстройствах [Welch et al., Clin Diagn Virol. 10: 163-71 (1998)]. Наиболее значительно то, что некоторые протоколы терапии с использованием рибозимных генов для пациентов с ВИЧ уже находятся на 1 стадии клинических испытаний. Позднее рибозимы применяли для исследований на трансгенных животных, для валидации генов-мишеней и выяснения каскадов реакций. Некоторые рибозимы находятся на разных стадиях клинических испытаний. ANGIOZYME является первым химически синтезированным исследованным в человеческих клинических испытаниях рибозимом. ANGIOZYME специфически ингибирует формирвание VEGE-r (рецептор фактора роста эндотелия сосудов), ключевого компонента в пути ангиогенеза. Ribozyme Pharmaceuticals, Inc., а также другие компании продемонстрировали важность подавляющих ангиогенез лекарственных средств в моделях на животных. HEPTAZYM представляет собой рибозим, сконструированный для селективного разрушения вирусной РНК гепатита С (HCV), в исследованиях на культурах клеток эффективно снижал вирусную РНК гепатита C (Ribozyme Pharmaceuticals, Incorporated - WEB home page).
Предпочтительно, фармацевтическая композиция для индукции или ускорения процесса заживления ран или повреждений кожи дополнительно содержит, по меньшей мере, дополнительное средство, выбранное из группы, состоящей из гормона, фактора роста, адипокина, РКСδ RACK и GW9662. Пригодным гормоном может быть, но не ограничен примерами, интерлейкин-6 (IL-6), фактор роста кератиноцитов (KFG) или фактор некроза опухоли альфа (TNFα). Пригодным адипокином может быть, но не ограничен примерами, адипсин или адипонектин.
Во время приведения настоящего изобретения к практическому применению, авторы настоящего изобретения необычно и неожиданно обнаружили, что сополимер-1 (глатирамера ацетат) способен к значительной активации заживления ран in vitro и in vivo (см. пример 26 ниже в разделе "Примеры"). Тогда как ранее сополимер-1 был известен как иммуномодулирующее средство, применяемое при лечении рассеянного склероза и расстройств центральной нервной системы (патенты США №№6620847, 6362161, 6342476, 6054430, 6046898, 5981589 и 5800808; патентные заявки США с регистрационными №№10/615865, 10/666857 и 10/014477), в предшествующем уровне техники не описывают и не предлагают применение сополимера-1 для ускорения процесса заживления ран.
Таким образом, согласно еще одному аспекту настоящего изобретения предоставлен способ индукции или ускорения процесса заживления ран или повреждений кожи, где способ выполняют посредством введения в раны или повреждения кожи терапевтически эффективного количества сополимера-1, предпочтительно в диапазоне концентраций от 1 до 500 мкг/мл. Следовательно, фармацевтическая композиция для осуществления способа согласно этому аспекту настоящего изобретения содержит, в качестве активного ингредиента терапевтически эффективное количество сополимера-1 и фармацевтически приемлемый носитель.
Терапевтически/фармацевтически активные ингредиенты по настоящему изобретению можно вводить в рану per se или в фармацевтической композиции, смешанной с пригодными носителями и/или наполнителями. Пригодные для применения фармацевтические композиции в контексте настоящего изобретения включают в себя те композиции, в которых активные ингредиенты содержатся в эффективном для достижения желаемого терапевтического эффекта количестве.
Используемые здесь "фармацевтические композиции" относятся к приготовлению одного или более описанных здесь активных ингредиентов, как белок, химические соединения, нуклеиновые кислоты или клетки, или физиологически приемлемые соли или их лекарственные формы, с другими химическими компонентами, такими как классические лекарственные средства, физиологически пригодные носители и наполнители. Целью фармацевтической композиции является облегчение введения композиции или клетки в организм. Фармацевтические композиции по настоящему изобретению можно получать посредством хорошо известных в данной области процессов, например, действием процессов обычного смешивания, растворения, гранулирования, изготовления драже, растирания в порошок, эмульгирования, инкапсулирования, включения или лиофилизации.
В дальнейшем фразы "физиологически пригодный носитель" и "фармацевтически приемлемый носитель" являются взаимозаменяемыми и относятся к носителю или растворителю, который не вызывает значительного раздражения в организме и не отменяет биологической активности и свойств вводимого конъюгата.
Здесь термин "наполнитель" относится к добавленному в фармакологическую композицию инертному веществу для дополнительного облегчения процессов и введения активных ингредиентов. Примеры наполнителей, без ограничения, включают в себя карбонат кальция, фосфат кальция, различные сахара и типы крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли.
Способы формулирования и введения активных ингредиентов можно найти в "Remington's Pharmaceutical Sciences", Mack Publishing Co., PA, последнее издание, введенное здесь в качестве ссылки.
Несмотря на то, что возможны различные, описанные ранее, пути введения активных ингредиентов, целью по настоящему изобретению предпочтительным является способ местного введения, и с помощью местного носителя. Местный носитель представляет собой носитель, который, как правило, пригоден для местного введения активных ингредиентов и включает в себя любой из таких известных в данной области материалов. Местный носитель выбран таким образом, чтобы дать композиции желаемую форму, например, как жидкий или нежидкий носитель, примочка, крем, паста, гель, порошок, мазь, раствор, жидкий растворитель, капли и нечто подобное, и может включать в себя материал, встречающийся в природе, или синтетического происхождения. Необходимо, очевидно, что выбранный носитель не оказывает неблагоприятного действия на активное средство или другие компоненты лекарственной формы для местного применения, и который стабилен по отношению ко всем компонентам лекарственной формы для местного применения. Примеры пригодных местных носителей для применения здесь включают в себя воду, спирты и другие нетоксичные органические растворители, глицерин, минеральное масло, силикон, вазелиновое масло, ланолин, жирные кислоты, растительные масла, парабены, воска, и что-либо подобное. Предпочтительными лекарственными формами здесь являются бесцветные мази без запаха, жидкости, примочки, крема и гели.
Мази представляют собой полутвердые препараты, основой которых обычно является вазелин или другие нефтепродукты. Специфической используемой основой мази, как следует понимать специалистам в данной области, является основа, обеспечивающая оптимальную доставку активных ингредиентов, и, предпочтительно, так же хорошо обеспечит другие желаемые характеристики, как, например, смягчение или что-либо подобное. Как и в случае с другими носителями или основами, основа мази должна быть инертной, стабильной, не вызывающей раздражения и сенсибилизации. Как объясняют у Remington: The Science and Practice of Pharmacy, 19th Ed. (Easton, Pa.: Mack PublishingCo., 1995), страницы 1399-1404, основы мазей можно сгруппировать в четыре класса: маслянистые основы, эмульгируемые основы, эмульсии и водорастворимые основы. Маслянистые основы мазей включают в себя, например, растительные масла, полученные из животных жиры и полученные из нефти полутвердые углеводороды. Эмульгируемые основы мазей, также известны, как абсорбирующие основы мазей, не содержат или содержат небольшое количество воды, например, сульфат гидроксистеарина, безводный ланолин и гидрофильный вазелин. Эмульсионные основы мазей представляют собой либо эмульсии вода в масле (W/O) или масло в воде (O/W), и включают в себя, например, цетиловый спирт, глицерилмоностеарат, ланолин и стеариновую кислоту. Предпочтительно водорастворимые основы мазей приготовлены из полиэтиленгликолей с разным молекулярным весом; можно вновь сделать ссылку на Remington: The Science and Practice of Pharmacy for further information.
Примочки представляют собой препараты, прикладываемые к поверхности кожи без растирания, и обычно являются жидкими или полутвердыми препаратами, в которых твердые частицы, включая активное средство, представлены на водной или спиртовой основе. Примочки обычно представляют собой суспензии из твердых частиц, и могут содержать жидкую маслянистую эмульсию типа "масло в воде". Здесь предпочтительно примочки представляют собой препараты для обработки больших областей тела из-за легкости применения более жидкой композиции. Как правило, необходимо, чтобы в примочке нерастворимое вещество было мелкоизмельченным. Обычно примочки содержат суспендирующие вещества для продукции более тонких дисперсий, а так же соединения, полезные для локализации и удержания активного средства в контакте с кожей, например, метилцеллюлоза, карбоксиметилцеллюлоза натрия, или что-либо подобное.
Кремы, содержащие выбранные активные ингредиенты, представляют собой, как известно в данной области, вязкую жидкость или полутвердые эмульсии, либо масло в воде, или вода в масле. Основы кремов смываются водой и содержат масляную фазу, эмульгатор и водную фазу. Масляную фазу также иногда называют "внутренней" фазой, как правило, состоящей из вазелина и жирного спирта, такого как цетиловый или стеариловый спирт; водная фаза обычно, хотя не обязательно, превышает масляную фазу по объему, и обычно содержит увлажнитель. Эмульгатор в препарате крема, как объясняют выше в Remington, обычно неионный, анионный, катионный или амфотерный сурфактант.
Препараты гелей предпочтительны для применения на коже головы. Как следует понимать специалистам в области формулирование местных активных ингредиентов, гели представляют собой полутвердые системы суспензионного типа. Однофазные гели содержат органические макромолекулы, распределенные, главным образом, равномерно по всему жидкому носителю, который обычно является водным, но также, предпочтительно, содержит спирт и, необязательно, масло.
Носители для нуклеиновых кислот включают в себя, но не ограничены примерами, липосомы, включающие в себя адресные липосомы, комплексообразующие средства нуклеиновых кислот, вирусные оболочки, и что-либо подобное. Однако также можно применять трансформацию незащищенными нуклеиновыми кислотами.
В лекарственные препараты изобретения для местного применения могут быть включены различные добавки, известные специалистам в данной области. Например, растворители можно применять для растворения некоторых активных ингредиентов веществ. Другие необязательные добавки включают в себя вещества, усиливающие проницаемость кожи, замутнители, антиоксиданты, гелеобразующие вещества, загустители, стабилизаторы и что-либо подобное.
Как уже упоминали выше, по настоящему изобретению средства местного применения для обработки ран могут содержать другие фармацевтически активные средства или ингредиенты, которые обычно применяют для обработки таких ран. Они включают в себя иммунодепрессанты, такие как циклоспорин, антиметаболиты, такие как метотрексат, кортикостероиды, витамин D и аналоги витамина D, витамин A или его аналоги, как этретинат, смола, деготь, противозудные средства и восстанавливающие роговицу средства, такие как можжевеловое масло, кератолитические средства, такие как салициловая кислота, смягчающие средства, умягчители, антисептики и дезинфицирующие вещества, такие как бактерицидный препарат детранол (также известный как антралин), фотосенсибилизаторы, такие как псорален и метоксален, и УФ-облучение. Также можно добавлять другие средства, такие как противомикробные средства, противогрибковые средства, антибиотики и противовоспалительные средства. Также можно совместно использовать обработку посредством оксигенации (высокого кислородного давления).
Топические композиции по настоящему изобретению также можно доставлять в кожу с применением обычных пластырей дермального типа или изделий, где композиция активных ингредиентов содержится в слоистой структуре, выполняющей функцию средства доставки лекарств, при прикреплении к коже. В такой структуре композиция активных ингредиентов содержится в слое, или "резервуаре", находящимся под верхним защитным слоем. Слоистая структура может содержать один резервуар, или она может содержать множество резервуаров. В одном варианте осуществления, резервуар включает в себя полимерный матрикс фармацевтически приемлемого контактного клейкого материала, служащего для прикрепления системы к коже при доставке активных ингредиентов. Примеры пригодных кожных контактных клейких материалов включают в себя, но не ограничены примерами, полиэтилены, полисилоксаны, полиизобутилены, полиакрилаты, полиуретаны, и что-либо подобное. Конкретный выбранный полимерный клей зависит от конкретных активных ингредиентов, носителя и т.д., т.е. клей должен быть сочетаемым со всеми компонентами композиции, содержащей активные ингредиенты. Альтернативно, резервуар, содержащий активные ингредиенты, и кожный контактный клей представлены в виде отдельных и обособленных слоев, где клей находится под резервуаром, который в этом случае может быть либо полимерным матриксом, как описано выше, или он может быть жидким или гидрогелевым резервуаром, или может иметь какую-нибудь другую форму.
Защитный слой в этих слоистых материалах, выполняющих функцию верхней поверхности средства, функционирует как основной структурный элемент слоистой структуры, и придает устройству значительную долю его эластичности. Выбираемый материал для защитного слоя нужно выбрать так, чтобы он являлся значительно герметичным, чтобы активировать ингредиенты и любые другие компоненты композиции, содержащей активные ингредиенты, таким образом, предотвращая потерю любых компонентов через верхнюю поверхность средства. Защитный слой может быть окклюзивным или неокклюзивным, в зависимости от того, желательно ли, чтобы кожа в течение доставки активных ингредиентов увлажнялась. Предпочтительно, защитный слой сделан из пленки или мембраны предпочтительно гибкого, эластичного материала. Примеры полимеров, пригодных для защитного слоя, включают в себя полиэтилен, полипропилен и полиэстеры.
Во время хранения и до применения слоистая структура включает в себя разделительный вкладыш. Непосредственно перед применением, этот вкладыш удаляют со средства, чтобы открыть его основную поверхность, либо резервуар активных ингредиентов, или отдельный слой контактного клея так, чтобы эту систему можно было прикрепить к коже. Этот разделительный вкладыш должен быть сделан из активных ингредиентов/непроницаемое для носителя вещество.
Такие средства можно производить с применением обычных способов, известных в данной области, например, посредством распределения жидкой смеси клея, активных ингредиентов и носителя на защитном слое, с последующим наслоением разделительного вкладыша. Аналогично, клейкую смесь можно распределять по разделительному вкладышу с последующим наслоением защитного слоя. Альтернативно, резервуар активных ингредиентов можно приготовить в отсутствие активных ингредиентов или инертного наполнителя, и затем заполнить посредством "пропитывания" активными ингредиентами/смесь носителя.
Как и в случае лекарственных средств для местного применения изобретения, композиция, содержащая активные ингредиенты с резервуарами активных ингредиентов этих слоистых систем, может содержать ряд компонентов. В некоторых случаях, активные ингредиенты можно выпускать "без примесей", т.е. в отсутствие дополнительных жидкостей. Однако в большинстве случаев, активные ингредиенты будут растворены, диспергированы или суспендированы в пригодном фармацевтически приемлемом носителе, обычно растворитель или гель. Другие компоненты, которые могут быть представлены, включают в себя консерванты, стабилизаторы, сурфактанты и что-либо подобное.
Описанные здесь фармацевтические композиции также могут включать в себя пригодные твердо- или гель-фазные носители или наполнители. Примеры таких носителей или наполнителей включают в себя, но не ограничены примерами, карбонат кальция, фосфат кальция, различные сахара, крахмалы, производные целлюлозы, желатин и полимеры, такие как полиэтиленгликоли.
Дозирование зависит от типа, тяжести и проявления повреждения, и от восприимчивости человека к активным ингредиентам, так же как от используемой лекарственной формы, активности конкретного конъюгата и используемого пути введения. Средние специалисты в данной области могут легко определить оптимальные дозировки, методологии дозирования и частоту повторений. Точную формулировку, путь введения и дозирование можно выбрать при помощи лечащего врача, исходя из состояния больного. (См., например, Fingi, et al., 1975, в "The Pharmacological Basis of Therapeutics", Ch.1 p.1).
Таким образом, в зависимости от тяжести и восприимчивости подлежащего лечению состояния, дозирование может представлять собой однократное или повторное введение, с курсом лечения длительностью от нескольких суток до нескольких недель, или до достижения выздоровления, или до достижения сокращения повреждения кожи.
В некоторых аспектах настоящего изобретения применяют способы (клеточной) генной терапии in vivo и ex vivo, включающие в себя трансформацию клеток и трансформацию гена по типу knock-in. Как применяют здесь, генная терапия относится к переносу интересующего генетического материала (например, ДНК или РНК) в хозяина для лечения или предотвращения генетического или приобретенного заболевания, или состояния, или фенотипа. Интересующий генетический материал кодирует продукт (например, белок, пептид, функциональную РНК, антисмысловую РНК), продукция которого желаема in vivo. H апример, интересующий генетический материал может кодировать гормон, рецептор, фермент, полипептид или пептид с терапевтическим действием. Для обзора см., обычно, текст "Gene Therapy" (Advanced in Pharmacology 40, Academic Press, 1997).
В генную терапию вовлечены два базовых способа (i) ex vivo; и (ii) in vivo генная терапия. При генной терапии ex VIVO клетки выделяют из пациента или получают из еще одного источника, и во время культивирования обрабатывают in vitro. Как правило, функциональная замена гена представляет собой введение в клетку посредством соответствующей системы доставки гена/способа (трансфекции, трансдукции, гомологичной рекомбинации и т.д.) и экспрессирующей системы по мере необходимости, и затем модифицированные клетки наращивают в культуре и возвращают хозяину/пациенту. Показали, что эти генетически реимплантированные клетки экспрессируют in situ трансфицированный генетический материал.
При генной терапии in vivo, клетки-мишени не выделяют из человека, скорее перенесенный генетический материал вводят в клетки организма реципиента in situ, которые находятся внутри реципиента. В альтернативном варианте осуществления, если ген хозяина является дефектным, ген восстанавливают in situ (Culver, 1998. (Abstract) Antisense DNA & RNA based therapeutics, February 1998, Coronado, CA). Показали, что эти генетически измененные клетки экспрессируют трансфицированный генетический материал in situ.
Экспрессирующий ген вектор способен доставлять/переносить гетерологическую нуклеиновую кислоту в клетку хозяина. Как известно в данной области, экспрессирующий вектор может включать в себя элементы для контроля позиционирования, экспрессии и транскрипции нуклеиновой кислоты в клетку селективным образом.
Следует заметить, что часто 5'UTR и/или 3'UTR гена можно замещать посредством 5'UTR и/или 3'UTR экспрессирующего вектора. Кроме того, как применяют здесь, экспрессирующий вектор может, по мере необходимости, не включать в себя 5'UTR и/или 3'UTR перенесенного действительного гена, а включать в себя только кодирующую специфические аминокислоты область.
Экспрессирующий вектор может включать в себя промотор для контроля транскрипции гетерологического материала, и может представлять собой конститутивный или индуцибельныи промотор, чтобы позволить избирательную транскрипцию. Необязательно сюда можно включать энхансеры, которые могут быть необходимы для получения необходимых уровней транскрипции. Как правило, энхансеры представляют собой любую нетранслируемую последовательность ДНК, работающую рядом с кодирующей последовательностью (in cis), чтобы изменить базальный уровень транскрипции, диктуемый промотором. Экспрессирующий вектор также может включать в себя ген отбора, как описано здесь ниже.
Векторы можно вводить в клетки или ткани посредством любого одного из множества известных в данной области способов. Описание таких способов можно обычно найти в Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Springs Harbor Laboratory, New York 1989, 1992), в Ausubel et al., Current Protocols in Molecular Biology, John Wiley and Sons, Baltimor, Maryland 1989), Chang et al. Somatic Gene Therapy, CRC Press, Ann Arbor, MI 1995), Vega et al., Gene Targeting, CRC Press, Ann Arbor, MI (995), Vectors: A Survey of Molecular Cloning Vectors and Their Uses, Butterworths, Boston MA 1988) и GilBoa et al. (Biotechniques 4 (6): 504-512, 1986), и включают в себя, например, стабильную или временную трансфекцию, липофекцию, электропорацию и инфекцию рекомбинантными вирусными векторами. Дополнительно, см. патент США 4866042 о векторах, вовлекающих центральную нервную систему, и также патенты США 5464764 и 5487992 о способах положительной-отрицательной селекции.
Введение нуклеиновых кислот посредством инфекции предлагает несколько преимуществ над другими перечисленными способами. Более высокую эффективность можно получить в результате их инфекционной природы. Кроме того, вирусы являются очень специализированными и типично инфицируют и размножаются в конкретных типах клеток. Таким образом, их природную специфичность можно применять для нацеливания векторов на конкретные типы клеток in vivo, или в пределах ткани, или смешанной культуры клеток. Также вирусные векторы можно модифицировать специфическими рецепторами или лигандами для изменения специфичности мишени через рецептор опосредованные события.
Конкретный пример введения вирусного ДНК-вектора и экспрессии рекомбинационных последовательностей представляет собой происходящий из аденовируса вектор Adenop53TK. Этот вектор экспрессирует ген тимидинкиназы (ТК) вируса герпеса для положительной или отрицательной селекции и экспрессирующую кассету для желаемых рекомбинантных последовательностей. Этот вектор можно применять для инфекции клеток, имеющих аденовирусный рецептор, включающий в себя большинство тканей эпителиального происхождения, так же как и другие. Этот вектор, так же как и другие, проявляющие сходные желаемые функции, можно применять для обработки смешанной популяции клеток, которые могут включать в себя, например, in vitro или ex VIVO культуру клеток, ткань или человека. Также могут быть включены признаки, ограничивающие экспрессию в отдельных типах клеток. Такие признаки включают в себя, например, промотор и регуляторные элементы, специфичные для желаемого типа клеток.
Дополнительно, рекомбинантные вирусные векторы полезны для экспрессии in vivo желаемой нуклеиновой кислоты, так как они предлагают преимущества, такие как латеральная инфекция и направленная специфичность. Латеральная инфекция присуща жизненному циклу, например, ретровирусов, и представляет собой процесс, посредством которого однажды инфицированные клетки продуцируют много вирионов-потомков, отпочковывающихся и инфицирующих соседние клетки. Результатом является то, что большая область быстро становится инфицированной, большая часть которой исходно не была инфицирована посредством исходных вирусных частиц. Существует отличие в типах вирусных инфекций, в которых инфекционный агент распространяется только через дочернее потомство. Также можно получать вирусные векторы, не способные распространяться латерально. Эта особенность может быть полезной, если желаемая цель представляет собой введение конкретного гена только в локализованном количестве намеченных клеток.
Как описано выше, вирусы представляют собой очень специализированные инфекционные агенты, которые разрабатывают во многих случаях для того, чтобы избежать механизмы защиты хозяина. Типично, вирусы инфицируют и размножаются в конкретных типах клеток. Направленная специфичность вирусных векторов использует его природную специфичность к специфически намеченным предопределенным типам клеток и, таким образом, вводит рекомбинантныи ген в инфицированную клетку. Применяемый вектор в способах и композициях изобретения зависит от желаемого намеченного типа клеток, и известен специалистам в данной области.
Ретровирусные векторы можно конструировать для функционирования либо в виде инфекционных частиц, или для прохождения одного начального цикла инфекции. В первом случае, геном вируса модифицировали так, чтобы он сохранял все необходимые гены, регуляторные последовательности и сигналы упаковки для синтеза новых вирусных белков и РНК. Когда эти молекулы синтезируются, клетка-хозяин упаковывает РНК в новые вирусные частицы, способные проходить дальнейшие циклы инфекции. Геном вектора также конструируют так, чтобы кодировать и экспрессировать желаемый рекомбинантныи ген. В случае неинфекционных вирусных векторов, геном вектора, как правило, подвергают мутированию для разрушения вирусного сигнала упаковки, необходимого для инкапсуляции РНК в вирусные частицы. Без такого сигнала любые сформированные частицы не содержат генома и, следовательно, не могут проходить через последующие циклы инфекции. Конкретный тип вектора будет зависеть от планируемого применения. Реально существующие векторы также известны и легко доступны в данной области или их может сконструировать специалист в данной области с применением хорошо известной методологии.
Рекомбинантныи вектор можно вводить несколькими способами. Например, если применяют вирусные векторы, в процедуре можно воспользоваться преимуществом их специфичности в отношении мишени и, следовательно, их не обязательно вводить локально в участок поражения. Однако местное введение может обеспечить более быстрое и более эффективное лечение.
Способы для трансформации клеток in vivo и ex vivo, включая сюда гомологичную рекомбинацию, применяемую в способах "knock-in", указаны, например, в патентах США 5487992, 5464764, 5387742, 5360735, 5347075, 5298422, 5288846, 5221778, 5175385, 5175384, 5175383, 4736866, а также у Burke and Olsen, Methods в Enzymology, 194:251-270 1991); Capecchi, Science 244: 1288-1292 (1989); Davies et al., Nucleic Acids Research, 20 (II): 2693-2698 (1992); Dickinson et al., Human Molecular Genetics, 2 (8):1299-1302 (1993); Duff and Lincoln, "Insertion of a pathogenic mutation into a yeast artificial chromosome containing the human APP gene and expression in ES cells". Research Advances in Alzheimer's Disease and Related Disorders, 1995; Huxley et al., Genomics, 9: 742-750 (1991); Jakobovits et al.. Nature, 362:255-261 (1993); Lamb et al., Nature Genetics, 5: 22-29 (1993); Pearson and Choi, Proc. Natl. Acad. Sci. USA (1993). 90: 10578-82; Rothstein, Methods in Enzymology, 194: 281-301 (1991); Schedl et al., Nature, 362: 258-261 (1993); Strauss et al. Science, 259: 1904-1907 (1993). Также дополнительная информация представлена в патентных заявках wO 94/23049, w0 93/14200, WO 94/06908, WO 94/28123.
Дополнительные объекты, преимущества и новые свойства настоящего изобретения будет понятны специалисту в данной области при изучении следующих далее примеров, которые не предназначены для ограничения. Кроме того, каждый из различных вариантов осуществления и аспектов настоящего изобретения, как указано выше и приведено в разделе формулы изобретения ниже, находит экспериментальную поддержку в следующих ниже примерах.
Примеры
Далее приведена ссылка на следующие ниже примеры, которые вместе с приведенными выше описаниями, иллюстрируют изобретение не лимитирующим образом.
Как правило, здесь применяют номенклатуру, и лабораторные процедуры, примененные в настоящем изобретении, включают в себя молекулярные, биохимические, микробиологические способы и способы рекомбинантных ДНК. Такие способы полностью описаны в литературе. Смотри, например, "Molecular Cloning: A Laboratory Manual "Sambrook et al., (1989); "Current Protocols in Molecular Biology" Volumes I-III Ausubel, R.M., ed. (1994); Ausubel et al., "Current Protocols in Molecular Biology", John Wiley and Sons, Baltimore, Matyland (1989); Perbal, "A Practical Guide to Molecular Cloning", John Wiley & Sons, New York (1988); Watson et al., "Recombinant DNA", Scientific American Books, New York; Birren et al. (eds) "Genome Analysis: A Laboratory Manual Series", Vols. 1-4, Cold Spring Harbor Laboratory Press, New York (1998); методологии, как излагают в патентах США №№4666828; 4683202; 4801531; 5192659 и 5272057; "Cell Biology: A Laboratoty Handbook", Volumes I-III Cellis" J.E., ed. (1994); "Culture of Animal Cells - A Manual of Basic Technique" by Freshney, Wiley-Liss, N.Y. (1994), Third Edition; "Current Protocols in Immunology" Volumes I-III Coligan J.E., ed. (1994); Stites et al. (eds), "Basic and Clinical Immunology" (8th Edition), Appleton & Lange, Norwalk, CT (1994); Mishell and Shiigi (eds), "Selected Methods in Cellular Immunology", w.H. Freeman and Co., New York (1980); доступные иммунологические исследования подробно описаны в патентной и научной литературе, смотри, например, патенты США №№3791932; 3839153; 3850752; 3850578; 3853987; 3867517; 3879262; 3901654; 3935074; 3984533; 3996345; 4034074; 4098876; 4879219; 5011771 и 5281521; "Oligonucleotide Synthesis" Gait, M.J., ed. (1984); "Nucleic acid Hybridization" Hames, B.D., and Haggins S.J., eds. (1985); "Transcription and Translation" Hames, B.D., и Haggins S.J., eds. (1984); "Animal Cell Culture" Freshney, R.I., ed. (1986); "Immobilized Cells and Enzymes" IRL Press, (1986); "A Practical Guide to Molecular Cloning" Perbal, В., (1984) и "Methods in Enzymology" Vol.1-317, Academic Press; "PCR Protocols: A Guide To Methods And Applications", Academic Press, San Diego, CA (1990); Marshak et al., "Strategies for Protein Purification and Characterization - A Laboratory Course Manual" CSHL Press (1996); которые все объединяют посредством ссылки, как будто полностью приведены здесь. Другие основные ссылки предоставлены по всему этому документу. Полагают, что процедуры, приведенные в данном описании, хорошо известны из уровня техники и представлены для удобства читателя. Вся содержащаяся здесь информация объединена посредством ссылки.
Материалы и экспериментальные способы
Материалы: Среда культуры ткани и сыворотка получены из Biological Industries (Beit HaEmek, Израиль). Повышенную химическую люминесценцию (ECL) выполняли с помощью коммерческого набора, полученного из BioRad (Израиль). Моноклональное антитело к p-tyr получали из Upstate Biotechnology Inc. (Lake Placid, NY, США). Поликлональные и моноклональные антитела к изоформам РКС получали из Santa Cruz (Калифорния, США) и Transduction Laboratories (Lexington, KY). Крысиные mAb (GoH3) к α6 мыши получали из Pharmingen (San Diego, CA). Антитело 6844 для α6А цитоплазматического домена получено в качестве подарка от Dr. V. Quaranta (Scripps Research Institute, La Jolla, CA). Крысиное mAb, направленное против внеклеточного домена мышиного β4 (346-11А) получено в качестве подарка от Dr. S.J. Kennel (Oak Ridge National Laboratory, Oak Ridge, TN). Крысиное mAb к фосфотирозину получали из Zymed (San Francisco, CA). IgG с пероксидазои хрена к кроличьим и мышиным антителам получали из Bio-Rad (Израиль). Леупептин, апротинин, PNSF, DTT, Na-ортованадат и пепстатин получали из Sigma Chemicals (St. Louis, МО). Инсулин (humulinR-рекомбинантный инсулин человека) получали из Eli Lilly France SA (Fergersheim, Франция). IGF1 получили в качестве подарка от Babco-Convance (Richmond, CA). BDGF-BB получали из R&D systems (Minneapolis) и миристоилированный псевдосубстрат РКСа получали из Calbinochem (San Diego, CA).
Выделение и культивирование мышиных кератиноцитов: Первичные кератиноциты выделяли из кожи новорожденных, как описано ранее (18). Кератиноциты культивировали в минимальной необходимой среде Игла (ЕМЕМ), содержащей 8% Chelex (Chelex-100, BioRad) обработанной эмбриональной телячьей сыворотки. Для поддержания пролиферативного базального клеточного фенотипа, конечную концентрацию Ca2+ установили до 0,05 мМ. Эксперименты выполняли через 5-7 суток культивирования.
Приготовление экстрактов клеток и анализ Вестерн-блот: Для получения грубых мембранных фракций готовили лизаты клеток посредством соскребания клеток в PBS, содержащий 10 мкг/мл апротинина, 10 мкг/мл леупептина, 2 мкг/мл пепстатина, 1 мМ PMSF, 10 мМ ЭДТА, 200 мкМ NaVO4 и 10 мМ NaF. После гомогенизации и 4 циклов замораживание/таяние, лизаты осаждали при 4°C в течение 20 минут в микроцентрифуге на максимальной скорости. Супернатант, содержащий растворимую цитозольную белковую фракцию переносили в другую пробирку. Осадок ресуспендировали в 2 50 мкл PBS, содержащего 1% Triton Х-100 с ингибиторами фосфатазы и протеазы, инкубировали в течение 30 минут при 4°C и осаждали в микроцентрифуге на максимальной скорости при 4°C. Супернатант содержит мембранную фракцию. Концентрации белка измеряли с применением модифицированного анализа Лоури (Bio-Rad DC Protein Assay Kit). Вестерн-блот анализ клеточных белковых фракций выполняли, как описано выше (б).
Приготовление клеточных лизатов для иммунопреципитации: Содержащие кератиноциты культуральные чашки отмывали в PBS без Са2+ и Mg2+. Клетки механически отделяли в буфере RIPA (50 мМ Трис-HCl рН 7,4; 150 мМ NaCl; 1 мМ ЭДТА; 10 мМ NaF; 1% Triton ×100; 0,1% 303, 1% дезоксихолата Na), содержащем смесь ингибиторов протеазы и фосфатазы (20 мкг/мл леупептина; 10 мкг/мл апротинина; 0,1 мМ PMSF; 1 мМ DTT; 200 мкМ ортованадата; 2 мкг/мл пепстатина). Препарат центрифугировали в микроцентрифуге на максимальной скорости в течение 20 минут при 4°C. Супернатант применяли для иммунопреципитации.
Иммунопреципитация: Лизат предварительно очищали посредством смешивания 300 мкг клеточного лизата с 25 мкл Protein A/G Sepharose (Santa Cruz, СА, USA), и суспензию непрерывно перемешивали в течение 30 минут при 4°C. Затем препарат центрифугировали на максимальной скорости при 4°C в течение 10 минут, и добавляли 30 мкл A/G Sepharose к супернатанту вместе со специфическими поликлональными или моноклональными антителами к отдельным антигенам (разведение 1:100). Образцы перемешивали всю ночь при 4°C. Затем суспензию центрифугировали на максимальной скорости в течение 10 минут при 4°C, и осадок отмывали в буфере RIPA. Суспензию снова центрифугировали при 15000 × g (4°С в течение 10 минут) и отмывали четыре раза в TBST. Добавляли буфер для образца (0,5 М Трис·HCl рН 6,8; 10% SDS; 10% глицерола; 4% 2-бета-меркаптоэтанола; 0,05% бромфенолового синего), и образцы кипятили в течение 5 минут, и затем подвергали SDS-PAGE.
Анализ прикрепления: 24-луночные чашки Петри (Greiner) покрывали (250 мкл/лунку) 20 мкг/мл матриксными белками в PBS в течение 1 часа при 37°C. После инкубации планшеты отмывали и инкубировали с 0,1% BSA в течение 30 минут при комнатной температуре для блокирования неспецифического связывания.
Культуры кератиноцитов коротко трипсинизировали 0,25% трипсином с последующим откреплением, клетки ресуспендировали и добавляли кератиноциты (1×106) на покрытые лунки и инкубировали в течение 1 часа при 37°С. Неадгезивные клетки удаляли, лунки промывали дважды с PBS, и оставшиеся клетки экстрагировали в 1 М NaOH. Количество клеток определяли посредством концентраций белков с применением модифицированного анализа Лоури (Bio-Rad Protein Assay Kit). Результаты рассчитывали посредством процентного отношения относительно необработанных контролей.
Иммунофлуоресценция: Первичные кератиноциты наносили на покрытые ламинином 5 предметные стекла. Двухсуточные кератиноциты инфицировали РКС аденовируса в течение одного часа, отмывали дважды в PBS и поддерживали в культуре с низким содержанием Са2+ MEM. Через двадцать четыре часа после инфекции клетки фиксировали в 4% параформальдегиде в течение 30 минут с последующим нарушением проницаемости клетки 0,2% Triton в течение 5 минут. Для анализа контрольные и инфицированные кератиноциты отмывали в PBS и инкубировали всю ночь при 4°c с антителами к РКС (Santa Cruz), растворенными в 1% BSA в PBS. После инкубации стекла дважды отмывали в течение 10 минут в PBS и инкубировали с биотинилированными вторыми антителами к кроличьим в течение 20 минут, дважды отмывали в PBS и инкубировали со стрептавидин-ПТС в течение 20 минут. Для анализа окрашивания α6β4, предметные стела обрабатывали 0,2% Triton X-100 в течение 5 минут на льду с последующей фиксацией в метаноле. Стекла инкубировали с антителами к α6 или β4 всю ночь с последующей инкубацией с биотинилированными вторыми антителами к кроличьим, соответственно, в течение 20 минут, дважды отмывали в PBS и инкубировали со стрептавидин-FITC в течение 20 минут. Затем отмывали два раза в PBS, стекла заключали в глицериновом буфере, содержащем 1% п-фенилендиамина (Sigma), и оценивали флуоресценцию посредством лазерной конфокальной сканирующей микроскопии (MRC1024, Bio-Rad, UK).
Аденовирусные конструкции: рекомбинантные аденовирусные векторы конструировали, как описано выше (19). Доминантно негативные мутанты мышиных РКС производили посредством замещения остатка лизина в АТФ-связывающем сайте на аланин. Мутантную кДНК вырезали из экспрессирующего вектора SRD с EcoR I и лигировали в космидную кассету pAxCAlw для конструирования вектора Ax. Доминантно негативная активность генов демонстрировали посредством его аутофосфорилирующей активности.
Трансакция кератиноцитов генами изоформ РКС: Культуральную среду удаляли, и культуры кератиноцитов инфицировали вирусным содержащим РКС рекомбинантные аденовирусы супернатантом в течение часа. Затем культуры дважды отмывали в MEM и снова вносили в питательную среду. Через десять часов после инфекции клетки переносили в MEM без сыворотки и с низким содержанием Ca2+ на 24 часа. Кератиноциты из контрольных и обработанных инсулином, или из обработанных IGF1 культур применяли для анализов пролиферации, захвата 86Rb, или экстрагировали и фракционировали в цитозольную и мембранную фракции для иммунопреципитации, иммунофлуоресценции и Вестерн-блоттинга, как описано.
Активность РКС: Специфическую активность РКС определяли в свежеприготовленных иммунопреципитатах из культур кератиноцитов последующими соответствующими обработками. Эти лизаты готовили в буфере RIPA без NaF. Активность измеряли с применением SignaTECT Protein Kinase C Assay System (Promega, Madison, WI, USA) в соответствии с инструкциями производителя. Псевдосубстрат РКСа применяли в этих исследованиях в качестве субстрата.
Пролиферация клеток: На 24-луночных планшетах измеряли пролиферацию клеток посредством включения [3H]тимидина. Клетки импульсно возбуждали [3H]тимидином (1 мкКи/мл) всю ночь. После инкубации клетки отмывали пять раз в PBS, и добавляли 5% TCA в каждую лунку на 30 минут. Раствор удаляли, и клетки растворяли в 1% Triton X-100. Меченный включенный в клетки тимидин считали в 3H-окне Tricarb жидкостного сцинтилляционного счетчика.
Активность Na+/K+ помпы: Активность Na+/K+ помпы определяли посредством измерений уабаин-чувствительного поглощения 86Rb целыми клетками в 1 мл PBS без K+ содержащем 2 мМ RbCl и 2,5 мкКи 86Rb. Поглощение Rb прерывали через 15 минут посредством удаления среды, после которого клетки быстро отмывали четыре раза в холодном 4°C PBS без K+, и растворяли в 1% Triton Х-100. Клетки из чашки добавляли к 3 мл H2O в сцинтилляционной виале. Образцы считали в 3H-окне Tricarb жидкостного сцинтилляционного счетчика. Поглощение Rb, специфически связанное с активностью Na+/K+ помпы определяли посредством вычитания накопленных имп/мин в присутствии 10-4 М уабаина из поглощения, определенного в отсутствие ингибитора.
Иммунокиназный анализ РКС: Очищенные и стандартизированные изозимы РКС были любезно предоставлены Dr. P. Blumberg (NCI, NIH, U.S.) и Dr. Marcello G. Kazanietz (University of Pennsylvania, School of Medicine). Первичные кератиноциты собирали в 500 мкл 1% Triton Lysis Buffer (1% Triton-X 100, 10 мкг/мл апротинина и леупептина, 2 г/мл пепстатина, 1 мМ PMSF, 1 мМ ЭДТА, 2 00 мкМ Na2V04, 10 мМ NaF в 1 × PBS). Лизаты инкубировали при 4°C в течение 30 минут и осаждали при 16000 × g в течение 30 минут при 4°C. Супернатанты переносили в новую пробирку. Иммунопреципитацию клеточных лизатов проводили всю ночь при 4°C с 5 мкг/образец анти-α6/GoH3 (Pharmingen) и 30 мкл/образец белка A/G-Plus agarose slurry (Santa Cruz). Бусы отмывали один раз буфером RIPA и дважды 50 мМ Трис/HCl рН 7,5. 35 мкл реакционного буфера (1 мМ CaCl2, 20 мМ MgCl2, 50 мМ Трис-HCl рН 7,5) добавляли к каждому анализу. Каждому анализу, 5,5 мкл/анализ суспензии фосфолипидных везикул, содержащих DMSO или 10 мМ ТРА, добавляли к взвеси вместе со стандартизированным количеством специфического изозима РКС. Реакцию инициировали посредством добавления 10 мкл/анализ 125 мМ АТФ (1,25 мкКи/анализ[γ-32P] АТФ, Amersham) и продолжали в течение 10 минут при 30°C. Затем бусы отмывали дважды в буфере RIPA. Добавляли 30 мкл/образец белок-нагрузочного красителя (3 × Laemmli, 5% SDS) и кипятили образцы в течение 5 минут на водной бане. Белки разделяли посредством SDS-PAGE на 8,5% геле, переносили на Protran мембраны (Schleicher & Schuell) и визуализировали посредством авторадиографии. В качестве контроля для активности РКС применяли фосфорилирование гистонов и фосфорилирование РКС субстратного пептида.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТОВ
ПРИМЕР 1
Эффективная сверхэкспрессия изоформ РКС с применением рекомбинантных аденовирусных векторов
Посредством применения аденовируса с рекомбинантной β-галактозидазой достигали высокой эффективности инфекции с более чем 90% популяции культивируемых кератиноцитов, экспрессирующих рекомбинантныи белок. Инфекция аденовирусом с рекомбинантной β-галактозидазой не влияет на жизнеспособность клеток или клеточный рост. Кроме того, экспрессия β-галактозидазы продолжалась вплоть до двух недель культивирования и ее применяли в качестве контроля инфекции в следующих далее экспериментах. Проверяли эффективность конструкций аденовируса с рекомбинантной РКС для индукции экспрессии белка и их способность правильно активироваться в культурах мышиных кератиноцитов. Как видно на "вестерн-блоте" на фиг.1, через 24 часа после 1 часа инфекции конструкциями аденовирусом с рекомбинантной РКС наблюдали существенное увеличение экспрессии конкретного белка РКС от 5 до 10 раз выше уровней эндогенной экспрессии конкретных изоформ. Рекомбинантныи белок можно выявлять в инфицированных культурах кератиноцитов уже через 6 часов после инфекции, а пик экспрессии получали через 24 часа. Экспрессия белка продолжалась на протяжении всего периода культивирования (до четырнадцати суток)
ПРИМЕР 2
Сверхэкспрессированные формы РКС активируются активаторами РКС
Рекомбинантные белки изоформ РКС, как правило, отвечали на активаторы РКС. Как видно на фиг.2, обработка бриостатином 1 индуцировала перемещение белков РКСα и η в мембранную фракцию, с меньшим эффектом на изоформы РКСη и ζ, сходно с результатами, полученными с эндогенными изоформами, и, как ожидали, исходя из требований их кофакторов.
ПРИМЕР 3
Сверхэкспрессированные формы РКС активируются в их нативной форме
Уже через 18 часов после инфекции, киназные анализы РКС выявили, что иммунопреципитаты отдельных изоформ РКС были ферментативно активными без дополнительной необходимости стимуляции активаторами РКС (фиг.3).
ПРИМЕР 4
Свврхэкспрессия конкретных форм РКС индуцирует в первичных кератиноцитах отчетливые морфологические изменения
Каждая из применяемых конструкций аденовирусов с РКС индуцировала в первичных кератиноцитах конкретное морфологическое изменение (фиг.4). Неинфицированные первичные культуры мышиных кератиноцитов и инфицированные β-галактозидазой клетки демонстрировали кубовидную морфологию, типичную для характеристик пролиферирующих базальных клеток в культуре. Вне зависимости от изоформной специфичности, все сверхэкспрессирующие РКС кератиноциты продемонстрировали морфологические изменения, типичные для активации РКС, включая сюда удлинение клеток и появление неироноподобных отростков. Однако, каждая из изоформ РКС обладала характерным эффектом на морфологию кератиноцитов. Инфекция РКСα индуцировала расслоение кератиноцитов с типичной плоской морфологией. Напротив, РКСη проявлялась в виде конденсированных клонов клеток, демонстрирующих морфологические характеристики базальных клеток, пролиферирующих с быстрой скоростью (фиг.4). Обнаружено, что две из изоформ оказывают воздействие на клеточный матрикс, а также на ассоциации клетка-клетка. Через 18-48 часов после инфекции РКСδ клетки выглядели удлиненными и увеличенными за счет неироноподобных выростов. За этим следовала постепенная потеря клеток в культуральной чашке, которая возрастала в течение периода культивирования. Кератиноциты, сверхэкспрессирующие РКСζ выглядели как шарообразные кластеры, свободно сидящие на культуральной чашке и постепенно разрушающиеся через несколько суток после инфекции.
ПРИМЕР 5
Различная локализация сверхэкспрессированных изоформ РКС в инфицированных первичных кератиноцитах
Различные морфологические изменения были ассоциированы с различной клеточной локализацией, как охарактеризовано посредством иммунофлюоресцентного анализа. В пролиферирующих кератиноцитах РКСα, РКСδ и РКСζ экспрессировались в цитоплазме, а также в плазматической мембране. Подобно экспрессии эндогенного белка, изоформа РКСη локализовалась в перинуклеарной области кератиноцитов (фиг.5). Динамическое изменение в распределении было связано с РКСδ и РКСζ, где следующая за откреплением клеток экспрессия изоформ РКС преимущественно локализовалась в клеточной мембране (фиг.5).
ПРИМЕР 6
Экспериментальные результаты регуляции экспрессии α6β4 изоформами РКС
Проверяли способность конкретных изоформ РКС регулировать белки, являющиеся характеристикой основного фенотипа пролиферирующего базального слоя. Так как супрессия интегрина α6β4 представляет собой одно из ранних событий, происходящих при дифференцировке кератиноцитов, оценивали способность различных изоформ РКС регулировать экспрессию интегрина α6β4, интегрина, который специфически локализуется в гемидесмосомах базального слоя. Как можно видеть на иммуноблоте, представленном на фиг.6, только изоформы РКСδ и РКСζ были способны супрессировать экспрессию α6β4 по сравнению с уровнями субъединиц интегрина α6β4 в контрольных каратиноцитах. В то же время уровни интегриновых субъединиц α3 или β1 не снижались. Напротив, соответственно, сверхэкспрессия изоформы РКСα приводила к увеличенному в размере от двух до трех раз выше уровня экспрессии в контроле уровню α6β4 (фиг.6). Сверхэкспрессия РКСη не влияла на уровень экспрессии белка α6β4. Некоторые характеристики ассоциированы с коммитированием клеток в направлении дифференцировки, и они после супрессии белка α6β4 включают в себя снижение скорости пролиферации, синтез нового кератина, открепление клеток и потерю присоединения к компонентам базальной мембраны. Изменений в экспрессии кератина при сверхэкспрессии различных изоформ РКС не наблюдали. Она включала в себя экспрессию К5 и К14, характерную для базальных пролиферирующих кератиноцитов, и К1 и К10, характерную для ранних стадий дифференцировки в шиповатые клетки. Кроме того, когда скорость пролиферации анализировали посредством включения 3H-тимидина корреляции между потерей экспрессии α6β4 и пролиферативным потенциалом не наблюдали.
ПРИМЕР 7
Сверхэкспрессированные РКСη и РКСδ индуцируют пролиферацию кератиноцитов in vitro
Сверхэкспрессия РКСη и РКСδ значимо индуцирует пролиферацию кератиноцитов в пять и в два раза выше, чем контрольные уровни, соответственно (фиг.7). РКСζ и РКСα не воздействуют на пролиферацию клеток.
ПРИМЕР 8
Сверхэкспрессированные РКСδ и ζ индуцируют открепление кератиноцитов in vitro
Исследовали адгезивные свойства сверхэкспрессирующих РКСδ и ζ кератиноцитов. По сравнению с контрольными кератиноцитами изменений в адгезивном потенциале к конкретным белкам матрикса, включающим в себя ламинин 1, ламинин 5, фибронектин и коллаген не наблюдали (данные не представлены). Однако в клетках, сверхэкспрессирующих изоформы РКСδ и РКСζ, потеря контакта клеток с культуральнои чашкой была ассоциирована с постепенным откреплением кератиноцита от культуральнои чашки (фиг.4).
ПРИМЕР 9
Эффекты сверхэкспрессии изоформ РКС на локализацию интегрина α6β4 в гемидесмосомах
Так как экспрессия α6β4 необходима для формирования гемидесмосомального адгезивного комплекса, исследовали связь супрессии α6β4 и клеточного открепления с локализацией α6β4 в гемидесмосомах. На фиг.8 представлен иммунофлуоресцентныи анализ ассоциации α6β4 с гемидесмосомальными комплексами. Как видно на фиг.8, по сравнению с контрольными инфицированными кератиноцитами, повышение экспрессии интегрина α6β4 в сверхэкспрессирующих РКСα кератиноцитах (фиг.6) ассоциировано с увеличенной интеграцией α6β4 с гемидесмосомальными комплексами. В сверхэкспрессирующих РКСη клетках также индуцирована ассоциация интегрина α6β4 с гемидесмосомальными комплексами, хотя и меньше, чем наблюдали в клетках, сверхэкспрессирующих РКСα. В соответствии с ожидаемым в сверхэкспрессирующих РКСδ и РКСζ кератиноциты выявили, что значительная супрессия интегрина α6β4 ассоциирована со сниженной интеграцией α6β4 с клеточными гемидесмосомальными комплексами (фиг.8). Данные результаты позволяют предположить, что интегрин α6β4 играет важную роль в ассоциации клеток с матриксом и прикреплении кератиноцитов к подлежащей базальной мембране. Кроме того, РКСδ и ζ, опосредовали супрессию α6β4, инициировали открепление клеток кератиноцитов отличным от процессов дифференцировки кератиноцитов путем. Наконец для установления связи опосредованной РКС супрессии α6β4, уменьшения интеграции α6β4 в гемидесмосомы и специфических морфологических изменений с откреплением кератиноцитов, исследовали изменения количества прикрепленных и открепленных клеток, сверхэкспрессирующих в течение периода культивирования различные изоформы РКС. На фиг.9 прикрепленные клетки считали в культурах через 24 и 48 часов после инфекцией аденовирусами с РКС. Как можно ясно заметить, индуцированные и РКСδ, и РКСζ клетки утрачиваются in vitro. Параллельно, потеря клеток в культуре коррелировала с увеличением клеток, плавающих в покрывающей среде. Данные результаты указывают на то, что РКСδ и РКСζ важны для контроля стадии открепления, связанной с ранними стадиями дифференцировки и миграции клеток.
ПРИМЕР 10
РКСη в физиологических условиях по-разному регулирует пролиферацию и дифференцировку кератиноцитов
Как ясно показано на фиг.7, сверхэкспрессирующие изоформу РКСη, клетки пролиферируют с повышенной скоростью, от пяти до семи раз превышающую скорость у контрольных неинфицированных клеток, и соответственно большую, чем в культурах кератиноцитов, сверхэкспрессирующих другие изоформы РКС. Однако индукция пролиферации зависела от стадии дифференцировки кератиноцитов, как определено посредством регуляции концентраций Ca2+ в среде. В пролиферирующих кератиноцитах, содержащихся при низких концентрациях Ca2+ (0,05 мМ), эндогенная РКСη локализовалась в перинуклеарной области большинства пролиферирующих клеток (фиг.10). В этих условиях сверхэкспрессия РКСη индуцировала существенное увеличение пролиферации кератиноцитов (фиг.11). Однако когда кератиноциты дифференцировались при повышающихся до 0,12 мМ концентрациях Са2+, сверхэкспрессия РКСη не стимулировала пролиферацию, но дополнительно стимулировала дифференцировку кератиноцитов. Данные результаты позволяют предположить, что сверхэкспрессированная РКСη только индуцирует пролиферацию в пролифирирующих в физиологических условиях клетках, но не препятствует клеточной дифференцировке. Несоответствие в регуляции экспрессии РКСη также наблюдали in vivo. В активно пролиферирующей коже, а также в нервных клетках эмбриона, идентифицировали экспрессию РКСη, тогда как в зрелом головном мозге взрослого не наблюдали РКСη, а в эпидермисе РКСη локализовался в гранулярном слое кожи.
ПРИМЕР 11
Сверхэкспрессия РКСη и DNРКСη специфически регулирует локализацию РКС и клеточную морфологию
Для дальнейшего подтверждения результатов, свидетельствующих о положительной роли РКСη в обеих стадиях пролиферации или дифференцировки у кератиноцитов, анализировали эффекты конструкции доминантно-негативного антивируса с неактивной киназой РКСη посредством изучения эффекта инфекции на пролиферирующие и дифференцирующиеся кератиноциты. Как видно на фиг.12 аденовирусная инфекция РКСη и DNРКСη была эффективна и на стадии пролиферации, и на стадии дифференцировки. Как и предсказано, в пролиферирующих кератиноцитах DNРКСη индуцировала дифференцировку кератиноцитов с существенным изменением клеточной морфологии, включающим в себя сглаживание клеток, потерю межклеточных связей подобно морфологическим изменениям, ассоциированным с индуцированной Ca2+ дифференцировкой (фиг.12A-B). Кроме того, данные изменения были ассоциированы с выключением пролиферации кератиноцитов (фиг.11) и существенной индукцией маркеров дифференцировки, включающих в себя кератин 1, кератин 10, лорикрин и филаггрин, повышенными до уровней, сходных с теми, которые присутствуют в нормальной коже in vivo (фиг.13A-B). В то же время при инициации программы дифференцировки, сверхэкспрессия DNРКСη не отменяла индукцированную Ca2+ дифференцировку. Эти результаты позволяют предположить, что РКСη и DNРКСη можно применять для различным образом регулируемой пролиферации и дифференцировки кератиноцитов в физиологических условиях.
ПРИМЕР 12
Эксперименты in vivo
Для тестирования способности РКСη различным образом регулировать клеточную пролиферацию и дифференцировку in vivo, оценивали способность РКСη индуцировать заживление полностью операционных ран, сделанных на спине голых мышей. Способность кератиноцитов экспрессировать экзогенный рекомбинантныи белок подтверждали применением контрольного аденовируса с β-gal. Как можно видеть на фиг.14, через две недели после инфекции экспрессия β-gal в кератиноцитах in vitro, а также в коже in vivo, сохранялась. Представляет интерес то, что когда сравнивали с контролем процесс заживления ран после локальной инфекции мышей аденовирусными конструкциями с РКСα и РКСη, только РКСη, индуцировала формирование грануляционной ткани уже через четверо суток после местной инфекции. Это также включало в себя организованное формирование мышечного, жирового и дермального слоев. В то же время в контрольной и инфицированной РКСα коже, не замечено конденсированной грануляционной ткани, и не наблюдали закрытия раны (фиг.14). Таким образом, РКСη можно рассматривать как первичного кандидата для регуляции пролиферации и дифференцировки кожи при индукции процессов заживления ран.
ПРИМЕР 13
Инсулин специфически индуцирует перемещение РКСδ в пролиферирующих кератиноцитах
Обнаружено, что на пролиферацию кератиноцитов влияют две изоформы РКС, продуцируемой в коже: РКСη и РКСδ. С целью испытания и идентифицирования эндогенных факторов, активирующих конкретные изоформы РКС, регулирующие пролиферацию в коже, оценивали способность некоторых факторов роста, известных как способствующие пролиферации кератиноцитов, включая сюда EGF, KGF, инсулин, PDGF и IGF1, активировать конкретные изоформы РКС, зависимым от роста образом. В коже экспрессируются изоформы РКС а, δ, ε, η и ζ. Так как активация изоформ РКС ассоциирована с их перемещением в мембранные фракции, исследовали воздействие этих факторов роста на перемещение различных изоформ РКС из цитозоля в мембрану. Как видно на фиг.15, уже через 5 минут после стимуляции, инсулин специфически индуцирует перемещение РКС5 из цитоплазмы в мембранные фракции. Экспрессия РКСδ на мембране сохранялась в течение нескольких часов после стимуляции инсулином. Напротив, IGF1 уменьшал экспрессию РКСδ на мембране и увеличивал ее относительный уровень экспрессии в цитоплазматической фракции. Другие факторы роста на перемещение и локализацию РКСδ значимо не влияли. Изменений в распределении других изоформ РКС после стимуляции любым из факторов роста, включающих в себя IGF1 и инсулин не наблюдали.
ПРИМЕР 14
Инсулин специфически индуцирует активацию РКСδ в пролиферирующих кератиноцитах
С целью определения того, достаточно ли перемещения РКСδ для активации, измеряли киназную активность РКС иммунопреципитатов из цитоплазмы и мембранных фракций обработанных инсулином и IGF1 кератиноцитов. Как показано на фиг.16, инсулин, но не IGF1, увеличивал активность РКСδ в мембранной фракции. Во фракции цитоплазмы повышения активности РКСα не наблюдали. Индуцируемая инсулином активация была специфична для РКСδ и после стимуляции инсулином, в течение периода до 30 минут, не наблюдали активации РКС α, ε, η или ζ. Все вместе эти результаты позволяют предположить, что селективную стимуляцию активации РКСδ инсулином, но не IGF1.
ПРИМЕР 15
Инсулин и IGF1 обладают аддитивным эффектом на пролиферацию кератиноцитов
С целью анализа того, играет ли специфическая активация РКСδ роль в специфическом индуцируемом инсулином митогенном пути в кератиноцитах митогенные эффекты инсулина и IGF1 анализировали посредством изучения их способности индуцировать пролиферацию кератиноцитов, измеряемую включением тимидиновой метки. Как показано на фиг.17A, и инсулин, и IGF1 стимулировали включение тимидина зависимым от доз образом с максимальной индукцией, достигаемой при 10-7 и 10-8 М, соответственно. При каждой концентрации максимальная стимуляция посредством IGF1 была больше, чем максимальная стимуляция инсулином. Представляет интерес то, что при всех концентрациях, когда оба гормона вводили совместно, мирогенные эффекты были аддитивными (фиг.17В). Данные результаты позволяют предположить, что инсулин регулирует пролиферацию кератиноцитов через определенный путь, не зависящий от индуцируемой IGF1 пролиферации кератиноцитов.
ПРИМЕР 16
Ассоциация между индуцированной инсулином активацией РКСδ и индуцированной инсулином пролиферацией кератиноцитов
С целью прямого изучения ассоциации между индуцированной инсулином активацией РКСδ и индуцированной инсулином пролиферацией кератиноцитов, для сверхэкспрессии РКСδ дикого типа (WTRKCδ), а также доминантно-негативного мутанта РКС с неактивной киназой, препятствующей активности эндогенной РКСδ (DNРКСδ), применяли конструкции аденовирусов с рекомбинантной РКС. Изучали эффекты сверхэкспрессии WTRKCδ и DNРКСδ на индуцированную инсулином пролиферацию кератиноцитов. Обе конструкции, а также конструкция РКСα, эффективно экспрессировались в кератиноцитах (фиг.18A). Кроме того, инфекция РКСδ и РКСα индуцировала специфичную для изоформы активность РКС в несколько раз выше контрольных уровней (фиг.18B). Как и ожидали, сверхэкспрессия DNРКСδ не индуцировала активность РКС. Как можно увидеть на фиг.19A, обработка нетрансфицированных клеток инсулином или сверхэкспрессия WTRKC6 без обработки инсулином увеличивали включение тимидина приблизительно до одинаковых уровней, от двух до трех раз больших, чем в необработанных клетках или клетках, трансдуцированных посредством РКСα. Кроме того, добавление инсулина к клеткам, уже сверхэкспрессирующим WTRKC5 не вызывало какого-либо дополнительного увеличения включения тимидина. IGF1 сходным образом увеличивал захват тимидина в неинфицированных клетках и в клетках, сверхэкспрессирующих WTRKCδ и РКСα (фиг.19A). Прямое участие РКСδ в индуцируемой инсулином пролиферации дополнительно проверяли посредством выключения активности РКСδ. Как видно на фиг.19B, базальное включение тимидина в клетки, сверхэкспрессирующие доминантно-негативную РКСδ было незначительным, но значимо меньшим, чем включение тимидина в неинфицированные клетки. Сверхэкспрессия DNРКСδ полностью уничтожала индуцированную инсулином пролиферацию, но не воздействовала на индуцируемую IGF1 пролиферацию. Кроме того, дополнительные эффекты инсулина и IGF1 были снижены по сравнению с дополнительными эффектами одного IGF1.
ПРИМЕР 17
Специфичность активации РКСδ для опосредуемого инсулином пути
Специфичность активации РКСδ для опосредуемого инсулином пути анализировали посредством исследования эффектов РКСδ и DNРКСδ на митогенный ответ на различные факторы роста, включающие в себя: IGF1, EGF, KGF, ECGF и PDGF. Как видно на фиг.20, сверхэкспрессия DNРКСδ селективно устраняла пролиферативные эффекты, индуцируемые инсулином, но не блокировала пролиферативные эффекты любых других тестируемых факторов роста. Однако сверхэкспрессия РКСδ имитировала индуцируемую инсулином пролиферацию и не воздействовала на индуцируемую IGF1 пролиферацию. Пролиферация, индуцируемая стимуляцией посредством EGF и KGF была увеличена (фиг.21). Эти данные указывают, что активация РКСδ инсулином опосредует пролиферацию кератиноцитов посредством пути, вовлекающего РКСδ и что данный путь расположен выше путей передачи сигнала EGF и KGF, двух основных факторов роста, из известных как регуляторы пролиферации кератиноцитов. В итоге, обнаружили, что инсулин представляет собой специфический регулятор активности РКСδ, который может быть конкретным кандидатом для регуляции пролиферации кератиноцитов, индуцируемой инсулином, EGF и KGF.
ПРИМЕР 18
Индуцируемая инсулином активность РКСδ и пролиферация кератиноцитов опосредованы транскрипционной активацией STAT3
Дополнительно охарактеризовывали роль РКСδ в передаче сигналов инсулином и обнаружили, что она вовлекает индукцию активации транскрипции, опосредуемой STAT3. Как видно на фиг.23, в первичных кератиноцитах показано, что РКСδ специфически ассоциируется с STAT3. После стимуляции инсулином РКСδ активируется и в свою очередь фосфорилирует и активирует STAT3 (фиг.24). Кроме того, ингибирование активности РКСδ фармакологическим ингибитором (ротлерин) также ингибирует активацию ядерной транслокации STAT3. Кроме того, как видно на фиг.25, сверхэкспрессия STAT3 индуцирует пролиферацию, сходную с пролиферацией, индуцируемой инсулином и сверхэкспрессией РКСδ, а ингибирование активности РКСδ сверхэкспрессией доминантно-негативного мутанта РКСδ ингибирует способность STAT3 индуцировать пролиферацию кератиноцитов. Суммарно данные результаты позволяют предположить, что инсулин и РКСδ играют роль в активации транскрипции, ассоциированной с пролиферацией кератиноцитов.
ПРИМЕР 19
РКСδ и РКСζ необходимы для процесса заживления ран in vivo
Важность изоформ РКС в процессе заживления ран in vivo устанавливали с применением нуль-мышей по конкретной изоформе РКС. Как видно на фиг.22A-B, когда делали глубокие раны на спине нуль-мышей по РКСδ, РКСζ, РКСα (нокаут, КО) и однопометных с ними животных дикого типа, замедленное заживление ран наблюдали у мышей, с отсутствием РКСδ и РКСζ, но не РКСα. Эти данные указывают на то, что даже в отсутствие диабетического фона, конкретные изоформы РКС необходимы для процесса заживления ран в коже.
ПРИМЕР 20
Однократное в сравнении с многократными применениями инсулина для заживления ран in vivo
На спине мышей C57BL в возрасте 8-10 недель посредством разреза делали раны и обрабатывали, как указано ниже: (i) ежедневно в течение 7 суток применяли 0,1 мкМ инсулина; (ii) ежедневно в течение 7 суток применяли 1 мкМ инсулина; (iii) ежедневно в течение 7 суток применяли 10 мкМ инсулина; (iv) 1 мкМ инсулина применяли однократно через 4 суток после нанесения ран; и (v) ежедневно в течение 7 суток применяли носитель (PBS) в качестве контроля. Всех мышей умерщвляли через семь суток после нанесения ран и измеряли их области открытых ран. Как видно на фиг.26, ежедневная обработка инсулином в концентрации 1 мкМ значимо более эффективна, чем ежедневные обработки инсулином в более низкой (0,1 мкМ) или более высокой (10 мкМ) концентрации. Неожиданно обработка одноразовым применением инсулина в концентрации 1 мкМ была значимо более эффективной, чем обработка семью ежедневными применениями инсулина в той же концентрации.
Так как наблюдаемые раны были покрыты рубцовой тканью, корректно оценить фактическое закрытие раны и формирование реконструированного эпидермиса было трудно. Поэтому эффекты инсулина на эпидермальное и дермальное закрытие раневой ткани определяли посредством гистологических параметров. Эпидермальное закрытие ран определяли окрашиванием раневых разрезов антителами к кератину 14 (К14, Babco-Convance, Richmond, CA, USA), выявлявших образование базальных клеток в раневой щели. Дермальное закрытие ран рассматривали положительным, если на обеих сторонах раны можно было наблюдать кожу в одном поле, наблюдаемом в световым микроскопе при увеличении х100.
Как видно на фиг.27, все обработки инсулином эффективно способствовали эпидермальному и дермальному закрытию. Подобно результатам, показанным на фиг.26, ежедневная обработка инсулином в концентрации 1 была значительно более эффективной, чем ежедневная обработка инсулином в концентрациях 0,1 мкМ или 10 мкМ. Кроме того, однократное применение инсулина при концентрации 1 мкМ было значительно более эффективным, чем применение семи повторов инсулина раз в сутки в той же концентрации.
Следовательно, данные результаты ясно обосновывает терапевтическую эффективность инсулина для заживления ран in vivo, как определено морфологическими, а также гистологическими параметрами. Данные результаты неожиданно показывают, что определение оптимального количество и/или частоты применений инсулина является важной стадией для правильного лечения ран.
ПРИМЕР 21
Сочетание инсулина и тромбоцит арного фактора роста (PDGF-BB) для заживления ран in vivo
На спине мышей C57BL в возрасте 8-10 недель посредством разреза делали раны и через 4 суток после нанесения ран обрабатывали, как указано ниже: (i) носитель (PBS) в качестве контроля; (ii) 1 мкМ инсулина; (iii) 10 мкМ PDGF-BB (R&D Systems, Minneapolis, USA); и (iv) 1 мкМ инсулин + 10 мкМ PDGF-BB. Через трое суток после обработки всех мышей умерщвляли и обработанные раны анализировали гистологически на эпидермальное и дермальное закрытие, как описано в примере 20 выше.
Как видно на фиг.28 обработка или только инсулином, или только PDGF-BB была частично эффективной на эпидермальное закрытие (увеличение на 30-4 0% по сравнению с контролем) и на дермальное закрытие (увеличение на 10-20% по сравнению с контролем). Однако обработка совместно инсулином и PDGF-ИИ приводила к значительно большему эпидермальному закрытию (приблизительно на 80% больше контроля), а также дермальному закрытию (приблизительно на 60%). Таким образом, результаты показывают, что сочетание инсулина и PDGF-BB воздействует на заживление раны синергичным образом. Результаты дополнительно указывают на потенциал сочетания инсулина с другими факторами роста или трансформирующим фактором, таким как EGF, TGFβ, KGF, для терапевтического лечения ран.
ПРИМЕР 22
Сочетание инсулина и ингибитора РКСα для лечения ран in vivo
На спине мышей C57BL в возрасте 8-10 недель посредством разреза делали раны и ежедневно в течение 7 суток обрабатывали или носителем (PBS) в качестве контроля или 0, 67 мкМ инсулином (НО/01; Humulin, Eli Lilly, USA) вместе с ингибитором РКСα (HO/02; миристоилированный псевдосубстрат РКСα; Calibiochem, San Diego, CA, USA). Через семь суток после нанесения ран всех мышей умерщвляли и обработанные раны анализировали на закрытие ран, эпидермальное закрытие, дермальное закрытие и пространственную дифференцировку эпидермальных клеток. Закрытие ран определяли измерением области открытой раны. Дермальное закрытие ран рассматривали положительным, если на обеих сторонах раны можно было наблюдать кожу в одном поле, наблюдаемом в световым микроскопе при увеличении ×100. Эпидермальное закрытие ран определяли окрашиванием раневых разрезов антителом к К14, выявлявшим формирование базальных клеток в раневой щели. Пространственную дифференцировку эпидермальных клеток определяли окрашиванием раневых разрезов антителом к К1, выявлявшим вновь сформированные эпителиальные клетки.
Как показано на фиг.28-32, совестное применение инсулина и (HO/01) и ингибитора РКСα (HO/02) значительно активизирует закрытие ран (фиг.29A-B), дермальное закрытие (фиг.30), эпидермальне закрытие (фиг.31) и пространственную дифференцировку эпидермальных клеток (фиг.32). Как можно видеть на фиг.33, обработка инсулином НО/01 совместно с ингибитором РКСα HO/02 увеличивала эпидермальное закрытие ран приблизительно от 15 до 70%, увеличивала пространственную дифференцировку эпидермальных клеток приблизительно от 15 до 50%, по сравнению с носителем в качестве контроля, соответственно.
Следовательно, результаты показывают, что терапевтическое лечение ран инсулином в сочетании с ингибитором РКСα эффективно активирует эпидермальное закрытие, дермальное закрытие, пространственную дифференцировку эпидермальных клеток, и последующее заживление ран.
ПРИМЕР 23
Сочетание инсулина и ингибитора РКСα преодолевает неблагоприятные побочные эффекты, вызываемые лечением только инсулином
На спине мышей C57BL в возрасте 8-10 недель посредством разреза делали раны и ежедневно в течение 7 суток обрабатывали или носителем (PBS) в качестве контроля или 1 мкМ инсулином (Humulin, Eli Lilly, USA) или смесью 1 мкМ инсулина вместе с 1 мкМ псевдосубстрата РКСα (Calibiochem, San Diego, CA, USA). Через семь суток после нанесения ран всех мышей умерщвляли и обработанные раны гистологически анализировали на пролиферативную способность эпидермиса (PCNA), ангиогенез, воспаление, эпидермальные клетки и процессы ремоделирования в раневой щели.
Как можно видеть в таблице 1 ниже, лечение только инсулином вызывало существенное увеличение частоты возникновения аномального ангиогенеза в ране по сравнению с контролем с буфером (60% и 25%, соответственно). Так как процесс заживления раны включает в себя быстро пролиферирующие зпидермальные клетки, такой усиленный ангиогенез может также увеличить риск запуска развития злокачественной опухоли. С другой стороны, когда инсулин объединяли с ингибитором РКСа, ангиогенеза в области обработанной раны не наблюдали.
| Таблица 1 | ||
| Действие одного инсулина и инсулина в сочетании с ингибитором. РКСα на интенсивность ангиогенеза в области раны | ||
| Обработка | Пролиферативная способность эпидермиса (слои базальных клеток, PCNA) | Ангиогенез |
| Контроль PBS (обработка PBS) n=4 |
5 | высокоаномальный |
| 7 | нормальный | |
| 8 | нормальный | |
| 6 | нормальный | |
| средняя 6,5 | ||
| Только инсулин n=5 |
8 | высокоаномальный |
| 8 | нормальный | |
| 6 | нормальный | |
| 5 | высокоаномальный | |
| 5 с | высокоаномальный | |
| средняя 6,4 | ||
| Инсулин + ингибитор РКСα n=5 |
6 | нормальный |
| 6 | нормальный | |
| 4 | нормальный | |
| 2 | нормальный | |
| 3 | нормальный | |
| средняя 4,2 | ||
Кроме того, обработка только инсулином приводила к увеличенному воспалению, гиперплазии эпидермальных клеток, замедленной дифференцировке шиповатого слоя эпидермальных клеток и усиленному рубцеванию. Ни одного из вредных побочных эффектов происходящих вследствие обработки только инсулином не наблюдали, когда с инсулином сочетали ингибитор РКСα.
ПРИМЕР 24
Ингибитор РКСα уменьшает воспаление ран
Поздний и тяжелый воспалительный ответ в ранах может подавлять процесс заживления, таким образом, предотвращая развитие такого воспаления, можно способствовать процессу заживления ран. Таким образом, в следующем ниже эксперименте тестировали действие ингибитора РКСα и инсулина на воспаление ран.
На спине мышей C57BL посредством разреза делали раны и ежедневно в течение 7 суток обрабатывали: (i) PBS, в качестве контроля; (ii) 1 мкМ ингибитора РКСα (миристоилированный псевдосубстрат; Calibiochem, USA); (iii) 1 мкМ инсулина (Eli Lilly, USA) или смесью 1 мкМ ингибитора РКСα и 1 мкМ инсулина. Через семь суток после нанесения ран всех мышей умерщвляли и обработанные раны обследовали на воспаление под микроскопом. Полученные в результате частоты возникновения тяжелого воспаления, наблюдаемые в области раны, обобщены в таблице 1а ниже.
| Таблица 1а | |
| Обработка | Частота возникновения тяжелого воспаления раны (%) |
| Контроль PBS | 60,0 |
| Ингибитор РКСα | 40,0 |
| Инсулин | 56,0 |
| Ингибитор РКСα + инсулин | 50,0 |
Результаты показывают, что введение в раны ингибитора РКСα вызывает существенное (33,3%) снижение частоты возникновения тяжелого воспаления раны по сравнению с контролем. Один инсулин не оказывал противовоспалительного эффекта в экспериментальных условиях.
Данные результаты указывают на то, что ингибитор РКСα можно применять в терапии для контроля тяжелого воспаления ран. Продемонстрированная способность ингибитора РКСα уменьшать воспаление, связанной с его способностью содействовать эпидермальному закрытию, дермальному закрытию и пространственной дифференцировке эпидермальных клеток (см. в примере 22 выше), делает его потенциально наиболее эффективным терапевтическим средством для заживления ран.
ПРИМЕР 25
Совместные эффекты модуляции экспрессии и/или активности конкретных изоформ РКС в дермальных клетках и введения в клетки различных средств на ускорение закрытия ран in vitro
Материалы и методы:
Реагенты: фактор D (адипсин) человека, Calbiochem, California USA; рекомбинантный мышиный TNFα, R&D Systems, Minneapolis USA; GW 9662, Cayman chemical, USA; псевдосубстратный ингибитор протеинкиназы Cα, Calbiochem, California USA; псевдосубстратный ингибитор протеинкиназы Cζ, Calbiochem, California USA; псевдосубстратный ингибитор протеинкиназы Cη, Calbiochem, California USA; PDGF-BB, Cytolab, Israel; IL-6, Cytolab, Israel; KGF/FGF-7, Cytolab, Israel; IGF-1, Cytolab, Israel; TGFβ2, Cytolab, Israel; эпидермальный фактор роста (EGF), мышь, cHEMICON INTERNATIONAL, California USA; РКСdelta RACK, AnaSpec, California USA; розиглитазон, Calbiochem. California USA; адипонектин, MBL, Massachusetts USA and Copaxone®, TEVA, Israel.
Анализ закрытия ран in vitro. Кератиноциты и фибробласты (дермальные клетки) культивировали в течение пяти суток в чашках Петри (вн. диам. 5 см), затем в каждой чашке с применением 200 мкл наконечника пипетки наносили перекрестные насечки. Культивируемые клетки инфицировали аденовирусными конструкциями, способными модулировать экспрессию и/или активность конкретных изоформ РКС. Таким образом, аденовирусные конструкции с РКС дикого типа (WT) применяли для активации конкретных РКС, тогда как аденовирусные конструкции с доминантно-негативной (DN) РКС применяли для ингибирования конкретных РКС. К культивируемым клеткам дополнительно добавляли одно из следующих веществ: инсулин (6,7×10-7 М), адипонектин (1 мкг на чашку), адипсин (2 мкг/мл), 1L-6 (1 мкг на чашку), GW9662 (1 мкг на чашку), KGF (1 мкг на чашку), TNFa (12 мкг/мл), TGFβ, розиглитазон, ингибиторы SRC, РКС6 RACK (10-7 М) и ингибирующий пептид псевдосусбстрата РКСα (10-7 М). Полученные в результате уровни закрытия ран определяли через 24-48 часов после обработки с применением значений индекса, находящихся в диапазоне от О (нет закрытия) до 10 (полное закрытие).
Результаты:
Эффекты совместных обработок на закрытие ран фибробластами in vitro обобщены в таблицах 2a-b и 3a-b ниже. Результаты показывают, что ингибирование экспрессии и/или активности РКСα в фибробластах в значительной степени способствуют закрытию ран при сочетании с введением в клетки адипсина или инсулина (значения индекса закрытия ран составляют 10 и 8, соответственно). Закрытие ран также ускорялось при ингибировании в клетках фибробластов РКСα совместно с ингибированием РКСη, ингибированием РКСε, активацией РКСδ или активацией РКСζ
(значения индекса закрытия ран составляют 9, 9, 9 и 7, соответственно; фиг.34A-E). Кроме того, закрытие ран ускоряло ингибирование в фибробластах РКСζ совместно с введением в клетки KGF (значения индекса закрытия ран составляют 7; фиг.36). Кроме того, дополнительно, закрытие ран ускорялось ингибированием в фибробластах РКСβ в сочетании с введением инсулина, 1L-6, KCGF или GW9662 (значения индекса закрытия ран составляют 8, 7, 9 и 8, соответственно; фиг.38A-E).
| Таблица 2а | ||||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||||
| Контроль | Адипсин | Инсулин | IL-6 | TGFβ | KGF | |
| Ингибирование РКСα | 4 | 10 | 8 | 3 | н.о. | 2 |
| Ингибирование РКСβ | 4 | н.о. | 8 | 7 | 1 | 9 |
| Ингибирование РКСζ | 2 | н.о. | 0 | 2 | н.о. | 7 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||||
| н.о. = не определяли | ||||||
| Таблица 2b | ||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||
| Адипонектин | Розиглитазон | GW9662 | Ингибиторы SRC | |
| Ингибирование РКСα | 3 | 5 | 2 | 3 |
| Ингибирование РКСβ | 3 | 3 | 8 | 2 |
| Ингибирование РКСζ | 2 | 2 | 1 | 1 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||
| Таблица 3а | ||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||
| Контроль | Активация РКСη | Ингибирование РКСη | Активация РКСε | |
| Ингибирование РКСα | 4 | 5 | 9 | 3 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||
| Таблица 3b | ||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||
| Ингибирование РКСε | Активация РКСδ | Активация РКСζ | Ингибирование РКСζ | |
| Ингибирование РКСα | 9 | 9 | 7 | 1 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||
Эффекты совместных обработок на закрытие ран кератиноцитами in vitro обобщены в таблицах 4a-b и 5a-b ниже. Результаты показывают, что Ингибирование экспрессии и/или активности РКСα в кератиноцитах в значительной степени способствуют закрытию ран при сочетании с введением в клетки KGF, IL-6, TNFα или пептида РКСδ RACK (значения индекса закрытия ран составляют 6, 8, 10 и 8, соответственно; фиг.35A-C и G). Закрытие ран также усиливалось при ингибировании в кератиноцитах РКСα совместно со стимуляцией в клетках РКСη, РКСε или РКСζ (значения индекса закрытия ран составляют 10, 9 и 6, соответственно; фиг.35А, D-F и Н). Кроме того, закрытию ран способствовало Ингибирование кератиноцитах РКСζ совместно с введением в клетки IL-6, TNFα или адипонектина (значения индекса закрытия ран составляют 9, 9 и 7, соответственно; фиг.37А-D). Кроме того, дополнительно, закрытие ран ускорялось стимуляцией активности и/или экспрессии в кератиноцитах РКСδ в сочетании с активацией РКСε, активацией РКСζ или ингибированием РКСα в клетках, или с введением в клетки адипсина (индекс закрытия ран составляет 7, 8, 8 и 8, соответственно; фиг.39A-E).
| Таблица 4а | ||||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||||
| Контроль | KGF | IL-6 | TNFa | Адипсин | Адипонектин | |
| Инсулин | н.о. | н.о. | н.о. | н.о. | н.о. | н.о. |
| Ингибирование РКСα | 3 | 6 | 8 | 10 | 4 | 2 |
| Активация РКСδ | н.о. | н.о. | н.о. | н.о. | 8 | н.о. |
| Ингибирование РКСζ | 0 | 0 | 9 | 9 | н.о. | 7 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||||
| н.о. = не определено. | ||||||
| Таблица 4b | |||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | |||||
| Розиглитазон | Ингибиторы SRC | РКСδ RACK | Псевдосубстрат РКСα | Псевдосубстрат РКСα+ | |
| Инсулин | н.о. | н.о. | 9 | 9 | н.о. |
| Ингибирование РКСα | 2 | 0 | 8 | н.о. | н.о. |
| Активация РКСδ | н.о. | н.о. | н.о. | н.о. | н.о. |
| Ингибирование РКСζ | 2 | 0 | 0 | н.о. | н.о. |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | |||||
| н.о. = не определено. | |||||
| Таблица 5а | ||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||
| Контроль | Активация РКСη, | Ингибирование РКСη | Активация РКСε | |
| Ингибирование РКСα | 3 | 10 | 5 | 9 |
| Ингибирование РКСδ | 3 | н.о. | н.о. | 7 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие) | ||||
| н.о. = не определено. | ||||
| Таблица 5b | ||||
| Эффект совместных обработок на закрытие фибробластами ран in vitro1 | ||||
| Ингибирование РКСε | Активация РКСζ | Ингибирование РКСζ | Ингибирование РКСα | |
| Ингибирование РКСα | 2 | 6 | 3 | - |
| Ингибирование РКСδ | 3 | 8 | 3 | 8 |
| 1шкала закрытия находилась в диапазоне от 0 (нет закрытия) до 10 (полное закрытие). | ||||
| н.о. = не определено. | ||||
Таким образом, результаты указывают, что закрытие ран можно существенно ускорить модуляцией в дермальных и эпидермальных клетках, колонизирующих область раны, экспрессии и/или активности конкретных изоформ РКС при сочетании с введением в клетки фактора роста, такого как IL-6, KGF, TNFα, гормона, такого как инсулин, адипокина, такого как адипсин или адипонектин, РКСδ RACK и/или GW9662.
ПРИМЕР 26
Введение сополимера-1 для заживления ран in vitro и in vivo
Материалы и методы:
Сополимер-1: сополимер-1 (глатирамера ацетат) представляет собой активный ингредиент лекарственного средства копаксон® (Сорахопе® (Теуа, Израиль)), который в клинике применяют для лечения рассеянного склероза. Сополимер-1 представляет собой синтетический полипептидный аналог основного белка миелина (МВР), являющегося природным компонентом миелиновой оболочки. Химически, сополимер-1 обозначает полимер L-глютаминовой кислоты с L-аланином, L-лизином и L-тирозином, ацетатом (соль). Его структурная формула представляет собой: (Glu, Ala, Lys, Tyr) х.Х CH3COOH (C5HNO4·C3H7NO2·C6H14N2O2·C9H11NO3) х·х C2H4O2. Средняя молекулярная масса глатирамера ацетата составляет 4700-11000 Дальтон. Его синтезируют посредством химической полимеризации четырех аминокислот, формируя продукты со средней молекулярной массой 23000 Дальтон (патент США №3849550).
Анализы in vitro: Анализы проводили по существу как описано в примере 24 выше. Сополимер-1 добавляли к культивируемым кератиноцитам в концентрации 55 мкг на чашку, или только его самого или в сочетании с псевдосубстратом РКСα (1 мкМ) и/или инсулином (1 мкМ). Полученные уровни закрытия ран определяли через 48 часов после обработки с применением значений индекса, находящихся в диапазоне от 0 (нет закрытия) до 10 (полное закрытие).
Анализы in vitro: На спине мышей C57BL посредством разреза делали раны (20 мм) и через 4 суток после нанесения ран обрабатывали, как указано ниже: (i) носитель (PBS) в качестве контроля; (ii) сополимер-1 (55 мкг/мл); (iii) смесь сополимера-1 (55 мкг/мл) и инсулина (1 мкМ); (iv) смесь ингибирующего пептида псевдосубстрата РКСα (1 мкМ) и инсулина (1 мкМ); и (v) смесь сополимера-1 (55 мкг/мл), ингибирующего пептида псевдосубстрата РКСа (1 мкМ) и инсулина (1 мкМ). Раны морфологически анализировали на (i) закрытие ран, (ii) формирование рубца и (iii) кровотечение/выделение из ран.
Результаты:
Анализы in vitro: Введение сополимера-1 в культивируемые кератиноциты обеспечивало закрытие ран in vitro до значения индекса 8 по шкале от 0 (нет закрытия) до 10 (полное закрытие). Сочетание сополимера-1 с ингибирующим пептидом псевдосубстрата РКСα или со смесью из ингибирующего пептида псевдосубстрата РКСα и инсулина, приводило к сходным эффектам (значения индекса закрытия ран составляют 8 и 9, соответственно; фиг.40A-F). Таким образом, результаты указывают, что сополимер-1 способен существенно ускорять закрытие ран in vitro самостоятельно.
Анализы in vivo: Введение в резаные раны сополимера-1, одного или в сочетании с инсулином и/или с псевдосубстратом РКСα, по сравнению с необработанным контролем, значительно уменьшало область раневой щели и ускоряло формирование рубца в ранах. Кроме того, все обработки с сополимером-1 эффективно предотвращали кровотечение и выделение в области раны.
Таким образом, результаты указывают, что введение в область раны эффективного количества сополимера-1, одного или в сочетании с инсулином и/или ингибирующим пептидом псевдосубстрата РКСα может значительно ускорить процесс заживления раны.
ПРИМЕР 27
Влияние секретируемых тимусом веществ на процесс заживления раны
Материалы и методы:
На верхней части спины (рядом с шеей) нормальных взрослых грызунов и мышей с 3Т2-диабетом проводили раневые разрезы. Животных умерщвляли через 7 или 9 суток после обработки, и раны гистологически анализировали на влияние присутствия тимуса рядом с раной и эпидермальное и дермальное закрытие ран с применением процедуры окрашивания, как описано в примере 20 выше.
Результаты:
Как можно видеть на фиг.42A-H, присутствие тимуса в непосредственной близости от раневой щели коррелировало с ускоренной эпителизацией, грануляцией ткани и Рубцовым сморщиванием кожи в ранах. Данные наблюдения указывают на то, что тимус секретировал вещества, которые могут эффективно содействовать процессу заживления ран. Таким образом, происходящие из тимуса вещества, такие как тимозин, бета-тимозины (например, тимозин бета 4, тимозин бета 10, тимозин бета 9; тимозин бета 12, тимозин бета 14), альфа-тимозины (например, тимозин альфа, 1/задаксин, протимозин альфа, паратимозин альфа), тимулин, IFGI, IFFII, NGF, соматостатин, тироглобулин, паратиреоидный гормон и/или тимические гормональные пептиды (ТНР) можно применять в лечении для ускорения процесса заживления ран.
Необходимо понимать, что определенные отличительные признаки изобретения, которые, для ясности, описаны в контексте отдельных вариантов осуществления изобретения, также можно определять в сочетании в одном из вариантов осуществления. Наоборот, различные отличительные признаки изобретения, которые, для ясности, описаны в контексте одного варианта изобретения, можно также определять отдельно или в любой пригодной субкомбинации.
Хотя изобретение описано в связи с его конкретными вариантами осуществления, понятно, что специалистам в данной области очевидны множество альтернатив, модификаций и вариаций. Таким образом, следует рассматривать все такие альтернативы, модификации и вариации, которые попадают в пределы сущности и основного объема приложенной формулы изобретения. Все указанные в данном описании публикации, патенты, патентные заявки полностью включены в данную заявку в качестве ссылки, до такой же степени, как если бы каждая отдельная публикация, каждый патент, каждая патентная заявка были конкретно и индивидуально указаны для включения сюда в качестве ссылки. Кроме того, цитирование или обозначение в данной заявке любой ссылки, не следует рассматривать как допущение того, что такая ссылка доступна как известный для данного изобретения уровень техники.
ЦИТИРУЕМЫЕ ССЫЛКИ ПО НОМЕРАМ
(Дополнительные ссылки процитированы в тексте)
1. Hennings, H., Michael, D., Cheng, С, Steinert, P., Holbrook, K., and Yuspa, S.H. Calcium regulation of growth and differentiation of mouse epidermal cells in culture. Cell, 19: 245-254, 1980.
2. Yuspa, S.H., Kilkenny, A.E., Steinert, P.M., and Roop, D.R. Expression of murine epidermal differentiation markers is tightly regulated by restricted extracellular calcium concentrations in vitro. J.Cell Biol., 109: 1207-1217, 1989.
3. Fuchs, E. Epidermal differentiation: the bare essentials. J.Cell Biol., 777:2807-2814,1990.
4. Yuspa, S.H. The pathogenesis of squamous cell cancer: lessons learned from studies of skin carcinogenesis-Thirty-third G.H.A. Clowes Memorial Award Lecture. Cancer Res., 54: 1178-1189, 1994.
5. Hennings, H. and Holbrook, K.A. Calcium regulation of cell-cell contact and differentiation of epidermal cells in culture. An ultrastructural study. Exp. Cell Res., 143: 127-142,1983.
6. Tennenbaum, Т., Li, L., Belanger, A.J., De Luca, L.M., and Yuspa, S.H. Selective changes in laminin adhesion and cc6p4 integrin regulation are associated with the initial steps in keratinocyte maturation. Cell Growth Differ., 7: 615-628, 1996.
7. Tennenbaum, Т., Belanger, A.J., Quaranta, V., and Yuspa, S.H. Differential regulation of integrins and extracellular matrix binding in epidermal differentiation and squamous tumor progression. J.Invest.Dermatol., 7; 157-161, 1996.
8. Nishizuka, Y. The molecular heterogeneity of РКС and its implications for cellular regulation. Nature, 334: 661-665, 1988.
9. Nishizuka, Y. The family of protein kinase С for signal transduction. JAMA, 262: 1826-1833, 1989.
10. Denning, M.F., Diugosz, A.A., Williams, E.K., Szallasi, Z., Blumberg, P.M., and Yuspa, S.H. Specific protein kinase С isozymes mediate the induction of keratinocyte differentiation markers by calcium. Cell Growth Differ., 6: 149-157, 1995.
11. Diugosz, A.A., Pettit, G.R., and Yuspa, S.H. Involvement of Protein kinase С in Ca +-mediated differentiation on cultured primary mouse keratinocytes. J.Invest.Dermatol., 94: 519-519, 1990.(Abstract)
12. Diugosz, A.A. and Yuspa, S.H. Coordinate changes in gene expression which mark the spinous to granular cell transition in epidermis are regulated by protein kinase C.J. Cell Biol, 120: 217-225, 1993.
13. Kuroki, Т., Kashiwagi, M., Ishino, К., Huh, N., and Ohba, M. Adenovirus-mediated gene transfer to keratinocytes-a review. J.Investig.Dermatol.Symp.Proc, 4: 153-157, 1999.
14. Rosenfeld, M.A., Siegfried, W., Yoshimura, K., Yoneyama, K., Fukayama, M., Stier, L.E., Paakko, P.K., Gi, P., Stratford-Perricaudet, M., Jallet, J., Pavirani, A., Lecocq, J.P., and Crystal, R.G. Adenovirus-mediated transfer of a recombinant al-antitrypsin gene to the lung epithelium in vivo. Science, 252; 431-434, 1991.
15. Setoguchi, Y., Jaffe, H.A., Danel, C, and Crystal, R.G. Ex Vivo and in vivo gene transfer to the skin using replication-deficient recombinant adenovirus vectors. J.Invest.Dermatol., 702; 415-421, 1994.
16. Greenhaigh, D.A., Rothnagel, J.A., and Roop, D.R. Epidermis: An attractive target tissue for gene therapy. J.Invest.Dermatol., 103: 63S-69S, 1994.
17. Miyake, S., Makimura, M., Kanegae, Y., Harada, S., Sato, Y., Takamori, K., Tokuda, C, and Saito, I. Efficient generation of recombinant adenoviruses using adenovirus DNA-terminal protein complex and a cosmid bearing the full-length virus genome. Proc. Natl. Acad. Sci. U.S.A, 93: 1320-1324, 1996.
18. Diugosz, A.A., Glick, A.B., Tennenbaum, Т., Weinberg, W.C., and Yuspa, S.H. Isolation and utilization of epidermal keratinocytes for oncogene research. In: P.K. Vogt and I.M. Verma (eds.). Methods in Enzymology, pp.3-20, New York: Academic Press. 1995.
19. Ohba, M., Ishino, K., Kashiwagi, M., Kawabe, S., Chida, K., Huh, N.H., and Kuroki, T. Induction of differentiation in normal human keratinocytes by adenovirus-mediated introduction of the eta and delta isoforms of protein kinase C. Mol. Cell Biol, 18: 5199-5207, 1998.
20. Weinstein, M.L. Update on wound healing: a review of the literature. Mil.Med., 163: 620-624, 1998.
21. Singer, A.J. and dark, R.A. Cutaneous wound healing. N. Engl. J. Med., 341: 738-746,1999.
22. Whitby, D.J. and Ferguson, M.W. Immunohistochemical localization of growth factors in fetal wound healing. Dev. BioL, 147: 207-215, 1991.
23. Kiritsy, C.P., Lynch,.В., and Lynch, S.E. Role of growth factors in cutaneous wound healing: a review. Crit.Rev.Oral Biol.Med., 4: 729-760, 1993.
24. Andresen, J.L., Ledet, Т., and Ehlers, N. Keratocyte migration and peptide growth factors: the effect ofPDGF, bFGF, EGF, IGF-I, aFGF and TGF-beta on human keratocyte migration in a collagen gel. Curr.Eye Res., 16: 605-613, 1997.
25. Wemer, S., Breeden, M., Hubner, G., Greenhaigh, D.G., and Longaker, M.T. Induction ofkeratinocyte growth factor expression is reduced and delayed during wound healing in the genetically diabetic mouse. J.Invest.Dermatol., 103: 469-473, 1994.
26. Threadgill, D.W., Diugosz, A.A., Hansen, L.A., Tennenbaum, Т., Lichti, U., Yee, D., LaMantia, C, Mourton, Т., Hen-up, K., Harris, R.C., Bamard, J.A., Yuspa, S.H., Coffey, R.J., and Magnuson, T. Targeted dismption of mouse EGF receptor: effect of genetic background on mutant phenotype. Science, 269: 230-234, 1995.
27. Osada, S., Mizuno, K., Theo, T.C., Akita, Y., Suzuki, K., Kuroki, Т., and Ohno, S. A phorbol ester receptor/protein kinase, nРКСn, a new member of the protein kinase С family predominantly expressed in lung and skin. J.Biol.Chem., 265: 22434-22440,1990.
28. Chida, K., Sagara, H., Suzuki, Y., Murakami, A., Osada, S., Ohno, S., Hirosawa, K., and Kuroki, T. The r] isoform of protein kinase С is localized on rough endoplasmic reticulum. Mol.Cell Biol., 14: 3782-3790, 1994.
29. Knighton, D.R. and Fiegel, V.D. Growth factors and comprehensive surgical care of diabetic wounds. Curr.Opin.Gen.Surg.,:32-9: 32-39, 1993.
30. Shaw, J.E. and Boulton, AJ. The pathogenesis of diabetic foot problems: an overview. Diabetes, 46 Suppi 2.S58-61: S5 8-S611997.
31. Coghlan, M.P., Pillay, T.S., Tavare, J.M., and Siddle, K. Site-specific anti-phosphopeptide antibodies: use in assessing insulin receptor serine/threonine phosphorylation state and identification ofserine-1327 as a novel site of phorbol ester-induced phosphorylation. Biochem. J., 503:893-899,1994.
32. Grunfeld, С. Diabetic foot ulcers: etiology, treatment, and prevention. Adv.Intem.Med., 37:103-32: 103-132, 1992.
33. Reiber, G.E., Lipsky, B.A., and Gibbons, G.W. The burden of diabetic foot ulcers. Am. J. Surg., 176: 5S-10S, 1998.
34. Wertheimer, E., Trebicz, M., Eldar, Т., Gartsbein, M., Nofeh-Mozes, S., and Tennenbaum, T. Differential Roles of Insulin Receptor and Insulin-Like Growth Factor-1 Receptor in Differentiation ofMurine Skin Keratinocytes. J.Invest.Dermatol., in press: 2000.
35. Gschwendt, M. Protein kinase С delta. Eur.J.Biochem., 259: 555-564, 1999.
36. Bajou, K., Noel, A., Gerard, R.D., Masson, V., Bmnner, N., Holst-Hansen, C., Skobe, M., Fusenig, N.E., Carmeliet, P., Collen, D., and Foidart, J.M. Absence of host plasminogen activator inhibitor 1 prevents cancer invasion and vascularization. Nat.Med., 4: 923-928, 1998.
37. Alessenko, A., Khan, W.A., Wetsel, W.C., and Hannun, Y.A. Selective changes in protein kinase С isoenzymes in rat liver nuclei during liver regeneration. Biochem.Biophys.Res.Commun., 182: 1333-1339, 1992.
38. Soltoff, S.P. and Toker, A. Carbachol, substance P, and phorbol ester promote the tyrosine phosphorylation of protein kinase С 5 in salivary gland epithelial cells. J.Biol.Chem, 270.- 13490-13495,1995.
39. Mischak, H., Pierce, J.H., Goodnight, J., Kazanietz, M.G., Blumberg, P.M., and Mushinski, J.F. Phorbol ester-induced myeloid differentiation is mediated by protein kinase C-a and -5 and not by protein kinase C-pTI, -s, -zeta and eta. J. Biol. Chem., 268: 20110-20115, 1993.
40. Sun, Q., Tsutsumi, К., Kelleher, M.B., Pater, A., and Pater, M.M. Squamous metaplasia of normal and carcinoma in situ of HPV 16-immortalized human endocervical cells. Cancer Res., 52: 4254-4260, 1992.
41. Mischak, H., Goodnight, J., Kolch, W., Martiny-Baron, G., Schaechtle, C., Kazanietz, M.G., Blumberg, P.M., Pierce, J.H., and Mushinski, J.F. over-expression of protein kinase C-5 and -s in NIH 3T3 cells induces opposite effects of growth, morphology, anchorage dependence, and tumorigenicity. J.Biol.Chem., 268: 6090-6096, 1993.
42. Braiman, L., Alt, A., Kuroki, Т., Ohba, M., Bak, A., Tennenbaum, Т., and Sampson, S.R. Protein kinase Cdelta mediates insulin-induced glucose transport in primary cultures of rat skeletal muscle. MoI.EndocrinoL, 13: 2002-2012,1999.
43. Braiman, L., Sheffi-Friedman, L., Bak, A., Tennenbaum, Т., and Sampson, S.R. Tyrosine phosphorylation of specific protein kinase С isoenzymes participates in insulin stimulation of glucose transport in primary cultures of rat skeletal muscle. Diabetes, 48: 1922-1929,1999.
44. Bandyopadhyay, G., Standaert, MX., Kikkawa, U., Ono, Y., Moscat, J., and Farese, R.V. Effects of transiently expressed atypical (zeta, lambda), conventional (alpha, beta) and novel (delta, epsilon) protein kinase С isoforms on insulin-stimulated translocation of epitope-tagged GLUT4 glucose transporters in rat adipocytes: specific interchangeable effects of protein kinases C-zeta and C-lambda. Biochem.J., 337: 461-470,1999.
45. Formisano, P., Oriente, F., Miele, C, Caruso, M., Auricchio, R., Vigliotta, G., Condorelli, G., and Beguinot, F. In NIH-3T3 fibroblasts, insulin receptor interaction with specific protein kinase С isoforms controls receptor intracellular routing. J.Biol.Chem, 273; 13197-13202, 1998.
46. Wang, Q.J., Bhattacharyya, D., Garfield, S., Nacro, K., Marquez, V.E., and Blumberg, P.M. Differential localization of protein kinase С delta by phorbol esters and related compounds using a fusion protein with green fluorescent protein. J. Biol. Chem., 274: 37233-37239, 1999.
Claims (1)
- Способ, при котором уменьшают воспаление, являющееся следствием ответа на рану кожи, путем введения достаточного количества ингибитора РКСα n-миристоилированного пептида и инсулина субъекту, нуждающемуся в этом.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US48690603P | 2003-07-15 | 2003-07-15 | |
| US60/486,906 | 2003-07-15 | ||
| US10/644,775 | 2003-08-21 | ||
| US10/644,775 US20040037828A1 (en) | 2002-07-09 | 2003-08-21 | Methods and pharmaceutical compositions for healing wounds |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2006104617/14A Division RU2359694C2 (ru) | 2003-07-15 | 2004-07-15 | Способы и фармакологические композиции для заживления ран |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010130763A RU2010130763A (ru) | 2012-01-27 |
| RU2491952C2 true RU2491952C2 (ru) | 2013-09-10 |
Family
ID=37134125
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010130763/15A RU2491952C2 (ru) | 2003-07-15 | 2004-07-15 | Способы и фармакологические композиции для заживления ран |
| RU2008138473/14A RU2404799C2 (ru) | 2003-07-15 | 2008-09-29 | Способы и фармакологические композиции для заживления ран |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2008138473/14A RU2404799C2 (ru) | 2003-07-15 | 2008-09-29 | Способы и фармакологические композиции для заживления ран |
Country Status (6)
| Country | Link |
|---|---|
| JP (4) | JP4790609B2 (ru) |
| CN (2) | CN101850108A (ru) |
| IL (1) | IL173148A (ru) |
| NZ (3) | NZ588743A (ru) |
| RU (2) | RU2491952C2 (ru) |
| ZA (1) | ZA200600235B (ru) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040037828A1 (en) * | 2002-07-09 | 2004-02-26 | Bar-Ilan University | Methods and pharmaceutical compositions for healing wounds |
| DK1651161T3 (da) * | 2003-08-07 | 2012-01-30 | Healor Ltd | Farmaceutiske præparater og fremgangsmåder til at fremme sårheling |
| US20100310542A1 (en) * | 2007-07-30 | 2010-12-09 | Healor Ltd. | Pharmaceutical Compositions for treating wouds and related methods |
| WO2012063237A2 (en) * | 2010-11-08 | 2012-05-18 | Healor Ltd. | Buffered ophthalmic compositions and methods of use thereof |
| AU2012286843A1 (en) * | 2011-07-28 | 2014-02-20 | Patricia J. Mclaughlin | Methods and compositions for treatment of epithelial wounds |
| CN103055304A (zh) * | 2013-01-19 | 2013-04-24 | 卓阳 | 一种治疗皮肤溃疡用复方温敏凝胶剂及其制备方法 |
| KR101523503B1 (ko) * | 2013-09-17 | 2015-05-29 | 강원대학교산학협력단 | 아디포넥틴으로부터 유래한 펩타이드 및 이를 포함하는 조성물 |
| CN106267163A (zh) * | 2015-06-09 | 2017-01-04 | 济南博创医药科技有限公司 | 一种治疗皮肤创伤的药物组合物及其药物制剂 |
| CN108514569A (zh) * | 2018-07-09 | 2018-09-11 | 广州中医药大学(广州中医药研究院) | 斜叶檀香提取物在制备皮肤创伤愈合药物中的应用 |
| CN112316148A (zh) * | 2019-08-01 | 2021-02-05 | 成都夸常奥普医疗科技有限公司 | 包含血浆的半流体的应用、包含该半流体和活性成分的药物组合物及其制备方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6537973B1 (en) * | 1992-03-16 | 2003-03-25 | Isis Pharmaceuticals, Inc. | Oligonucleotide inhibition of protein kinase C |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5948898A (en) * | 1992-03-16 | 1999-09-07 | Isis Pharmaceuticals, Inc. | Methoxyethoxy oligonucleotides for modulation of protein kinase C expression |
| GB2304047A (en) * | 1995-08-09 | 1997-03-12 | Univ Manchester | Pharmaceutical compositions containing cytokines |
| CA2244222A1 (en) * | 1996-01-23 | 1997-07-31 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for screening for transdominant effector peptides and rna molecules |
| BR0009772A (pt) * | 1999-04-14 | 2002-01-08 | Us Health | Composições contendo imunotoxinas e agentes que inibem a maturação de células dendrìticas para induzir tolerância imune a um enxerto |
| WO2002009639A2 (en) * | 2000-07-31 | 2002-02-07 | Bar Ilan University | Methods and pharmaceutical compositions for healing wounds |
| GB2369572A (en) * | 2000-11-29 | 2002-06-05 | Raft Trustees Ltd | Wound treatment composition comprising insulin |
-
2004
- 2004-07-15 NZ NZ588743A patent/NZ588743A/xx not_active IP Right Cessation
- 2004-07-15 NZ NZ545318A patent/NZ545318A/en not_active IP Right Cessation
- 2004-07-15 RU RU2010130763/15A patent/RU2491952C2/ru not_active IP Right Cessation
- 2004-07-15 CN CN200910217138A patent/CN101850108A/zh active Pending
- 2004-07-15 CN CN2004800265295A patent/CN1852722B/zh not_active Expired - Fee Related
- 2004-07-15 JP JP2006520104A patent/JP4790609B2/ja not_active Expired - Fee Related
- 2004-07-15 ZA ZA200600235A patent/ZA200600235B/xx unknown
- 2004-07-15 NZ NZ573737A patent/NZ573737A/en not_active IP Right Cessation
-
2006
- 2006-01-15 IL IL173148A patent/IL173148A/en not_active IP Right Cessation
-
2008
- 2008-09-29 RU RU2008138473/14A patent/RU2404799C2/ru not_active IP Right Cessation
-
2010
- 2010-12-22 JP JP2010285810A patent/JP2011057711A/ja active Pending
- 2010-12-22 JP JP2010285808A patent/JP2011057709A/ja not_active Ceased
- 2010-12-22 JP JP2010285809A patent/JP2011057710A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6537973B1 (en) * | 1992-03-16 | 2003-03-25 | Isis Pharmaceuticals, Inc. | Oligonucleotide inhibition of protein kinase C |
Non-Patent Citations (1)
Also Published As
| Publication number | Publication date |
|---|---|
| JP4790609B2 (ja) | 2011-10-12 |
| RU2008138473A (ru) | 2010-04-10 |
| IL173148A (en) | 2013-02-28 |
| JP2007530426A (ja) | 2007-11-01 |
| NZ588743A (en) | 2012-05-25 |
| JP2011057709A (ja) | 2011-03-24 |
| IL173148A0 (en) | 2006-06-11 |
| CN1852722B (zh) | 2011-06-08 |
| CN101850108A (zh) | 2010-10-06 |
| NZ545318A (en) | 2009-06-26 |
| CN1852722A (zh) | 2006-10-25 |
| JP2011057711A (ja) | 2011-03-24 |
| ZA200600235B (en) | 2007-04-25 |
| JP2011057710A (ja) | 2011-03-24 |
| RU2010130763A (ru) | 2012-01-27 |
| RU2404799C2 (ru) | 2010-11-27 |
| NZ573737A (en) | 2011-06-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2009225335B2 (en) | Methods and pharmaceutical compositions for healing wounds | |
| JP5385321B2 (ja) | 創傷治療のための方法および薬学的組成物 | |
| US20060258562A1 (en) | Methods and pharmaceutical compositions for healing wounds | |
| IL173148A (en) | Use of insulin for the preparation of pharmaceutical compositions for healing wounds | |
| AU2001284364A1 (en) | Methods and pharmaceutical compositions for healing wounds | |
| US20100129332A1 (en) | Methods and pharmaceutical compositions for healing wounds | |
| AU2011226776B2 (en) | Methods and pharmaceutical compositions for healing wounds | |
| US20030148924A1 (en) | Methods and pharmaceutical compositions of healing wounds | |
| IL154210A (en) | Pharmaceutical compositions and uses thereof for healing wounds |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20140716 |