JP2005531513A - 免疫応答を作製するための組成物および方法 - Google Patents
免疫応答を作製するための組成物および方法 Download PDFInfo
- Publication number
- JP2005531513A JP2005531513A JP2003574798A JP2003574798A JP2005531513A JP 2005531513 A JP2005531513 A JP 2005531513A JP 2003574798 A JP2003574798 A JP 2003574798A JP 2003574798 A JP2003574798 A JP 2003574798A JP 2005531513 A JP2005531513 A JP 2005531513A
- Authority
- JP
- Japan
- Prior art keywords
- hiv
- vector
- clade
- composition
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 230000028993 immune response Effects 0.000 title claims abstract description 73
- 239000000203 mixture Substances 0.000 title claims description 99
- 238000000034 method Methods 0.000 title claims description 37
- 239000013598 vector Substances 0.000 claims abstract description 241
- 108091007433 antigens Proteins 0.000 claims abstract description 140
- 102000036639 antigens Human genes 0.000 claims abstract description 140
- 239000000427 antigen Substances 0.000 claims abstract description 136
- 229960005486 vaccine Drugs 0.000 claims abstract description 124
- 230000001681 protective effect Effects 0.000 claims abstract description 6
- 230000035772 mutation Effects 0.000 claims description 146
- 241000725303 Human immunodeficiency virus Species 0.000 claims description 116
- 108090000623 proteins and genes Proteins 0.000 claims description 108
- 239000013612 plasmid Substances 0.000 claims description 97
- 102100034343 Integrase Human genes 0.000 claims description 54
- 241000700605 Viruses Species 0.000 claims description 54
- 241000713772 Human immunodeficiency virus 1 Species 0.000 claims description 51
- 102000004169 proteins and genes Human genes 0.000 claims description 44
- 150000007523 nucleic acids Chemical class 0.000 claims description 39
- 230000000694 effects Effects 0.000 claims description 37
- 108020004707 nucleic acids Proteins 0.000 claims description 35
- 102000039446 nucleic acids Human genes 0.000 claims description 35
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 claims description 27
- 108091005804 Peptidases Proteins 0.000 claims description 26
- 239000002671 adjuvant Substances 0.000 claims description 24
- 239000004365 Protease Substances 0.000 claims description 23
- 239000013600 plasmid vector Substances 0.000 claims description 23
- 241001183012 Modified Vaccinia Ankara virus Species 0.000 claims description 22
- 108010061833 Integrases Proteins 0.000 claims description 21
- 238000012217 deletion Methods 0.000 claims description 21
- 230000037430 deletion Effects 0.000 claims description 21
- 101710149951 Protein Tat Proteins 0.000 claims description 20
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 14
- 229910052725 zinc Inorganic materials 0.000 claims description 14
- 239000011701 zinc Substances 0.000 claims description 14
- 101710177291 Gag polyprotein Proteins 0.000 claims description 13
- 230000037452 priming Effects 0.000 claims description 13
- 108091032973 (ribonucleotides)n+m Proteins 0.000 claims description 11
- 108020000999 Viral RNA Proteins 0.000 claims description 10
- -1 rev Proteins 0.000 claims description 9
- 101710203526 Integrase Proteins 0.000 claims description 8
- 101710125418 Major capsid protein Proteins 0.000 claims description 8
- 108010089520 pol Gene Products Proteins 0.000 claims description 8
- 230000035892 strand transfer Effects 0.000 claims description 7
- 108091081024 Start codon Proteins 0.000 claims description 6
- 229940021995 DNA vaccine Drugs 0.000 claims description 5
- 102000004190 Enzymes Human genes 0.000 claims description 5
- 108090000790 Enzymes Proteins 0.000 claims description 5
- 108700004025 env Genes Proteins 0.000 claims description 5
- 108010041986 DNA Vaccines Proteins 0.000 claims description 4
- 230000002255 enzymatic effect Effects 0.000 claims description 4
- 108700004026 gag Genes Proteins 0.000 claims description 4
- 108700004029 pol Genes Proteins 0.000 claims description 4
- 230000002797 proteolythic effect Effects 0.000 claims description 4
- 230000006798 recombination Effects 0.000 claims description 4
- 238000005215 recombination Methods 0.000 claims description 4
- 108700026222 vpu Genes Proteins 0.000 claims description 4
- 230000001105 regulatory effect Effects 0.000 claims description 3
- 108700026220 vif Genes Proteins 0.000 claims description 3
- 239000003937 drug carrier Substances 0.000 claims description 2
- 108700004028 nef Genes Proteins 0.000 claims description 2
- 108700004030 rev Genes Proteins 0.000 claims description 2
- 108700004027 tat Genes Proteins 0.000 claims description 2
- 108700026215 vpr Genes Proteins 0.000 claims description 2
- 229940033330 HIV vaccine Drugs 0.000 claims 3
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 claims 3
- 206010027476 Metastases Diseases 0.000 claims 1
- 230000009401 metastasis Effects 0.000 claims 1
- 239000013603 viral vector Substances 0.000 abstract description 41
- 239000004615 ingredient Substances 0.000 abstract 1
- 108020004414 DNA Proteins 0.000 description 66
- 230000014509 gene expression Effects 0.000 description 44
- 210000004027 cell Anatomy 0.000 description 31
- 235000018102 proteins Nutrition 0.000 description 31
- 108020004705 Codon Proteins 0.000 description 28
- 239000013615 primer Substances 0.000 description 28
- 238000010367 cloning Methods 0.000 description 27
- 239000012634 fragment Substances 0.000 description 26
- 239000000047 product Substances 0.000 description 23
- 239000002773 nucleotide Substances 0.000 description 22
- 125000003729 nucleotide group Chemical group 0.000 description 22
- 102100038132 Endogenous retrovirus group K member 6 Pro protein Human genes 0.000 description 21
- 239000003795 chemical substances by application Substances 0.000 description 19
- 238000003752 polymerase chain reaction Methods 0.000 description 19
- 235000001014 amino acid Nutrition 0.000 description 18
- 229940024606 amino acid Drugs 0.000 description 18
- 150000001413 amino acids Chemical class 0.000 description 18
- 230000006870 function Effects 0.000 description 17
- 108010027225 gag-pol Fusion Proteins Proteins 0.000 description 14
- 208000015181 infectious disease Diseases 0.000 description 14
- 230000002163 immunogen Effects 0.000 description 13
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 description 12
- 230000001717 pathogenic effect Effects 0.000 description 12
- 230000004044 response Effects 0.000 description 12
- 230000002441 reversible effect Effects 0.000 description 12
- 241000701022 Cytomegalovirus Species 0.000 description 11
- 206010061598 Immunodeficiency Diseases 0.000 description 11
- 208000029462 Immunodeficiency disease Diseases 0.000 description 11
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 11
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 description 11
- 230000007813 immunodeficiency Effects 0.000 description 11
- 230000005847 immunogenicity Effects 0.000 description 11
- 229940065638 intron a Drugs 0.000 description 11
- 244000052769 pathogen Species 0.000 description 11
- 108091008146 restriction endonucleases Proteins 0.000 description 11
- 239000011780 sodium chloride Substances 0.000 description 11
- 229960000187 tissue plasminogen activator Drugs 0.000 description 11
- 238000013518 transcription Methods 0.000 description 11
- 230000035897 transcription Effects 0.000 description 11
- 108091028043 Nucleic acid sequence Proteins 0.000 description 10
- 241000700618 Vaccinia virus Species 0.000 description 10
- 206010046865 Vaccinia virus infection Diseases 0.000 description 10
- 241000700647 Variola virus Species 0.000 description 10
- 239000013604 expression vector Substances 0.000 description 10
- 239000003550 marker Substances 0.000 description 10
- 108020004999 messenger RNA Proteins 0.000 description 10
- 108090000765 processed proteins & peptides Proteins 0.000 description 10
- 238000002741 site-directed mutagenesis Methods 0.000 description 10
- 208000007089 vaccinia Diseases 0.000 description 10
- 230000003612 virological effect Effects 0.000 description 10
- 229930027917 kanamycin Natural products 0.000 description 9
- 229960000318 kanamycin Drugs 0.000 description 9
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 9
- 229930182823 kanamycin A Natural products 0.000 description 9
- 208000030507 AIDS Diseases 0.000 description 8
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 description 8
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 description 8
- 108700007698 Genetic Terminator Regions Proteins 0.000 description 8
- 125000000539 amino acid group Chemical group 0.000 description 8
- 230000008901 benefit Effects 0.000 description 8
- 238000009826 distribution Methods 0.000 description 8
- 230000008488 polyadenylation Effects 0.000 description 8
- 230000010076 replication Effects 0.000 description 8
- 241000282412 Homo Species 0.000 description 7
- 108091034117 Oligonucleotide Proteins 0.000 description 7
- 101000702488 Rattus norvegicus High affinity cationic amino acid transporter 1 Proteins 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 239000002245 particle Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 241000894006 Bacteria Species 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 230000005867 T cell response Effects 0.000 description 6
- 230000036039 immunity Effects 0.000 description 6
- 230000002779 inactivation Effects 0.000 description 6
- 238000011081 inoculation Methods 0.000 description 6
- 238000002703 mutagenesis Methods 0.000 description 6
- 231100000350 mutagenesis Toxicity 0.000 description 6
- 238000011144 upstream manufacturing Methods 0.000 description 6
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 5
- 241000287828 Gallus gallus Species 0.000 description 5
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 5
- 210000001744 T-lymphocyte Anatomy 0.000 description 5
- 230000001580 bacterial effect Effects 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 238000003776 cleavage reaction Methods 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 108010078428 env Gene Products Proteins 0.000 description 5
- 230000003053 immunization Effects 0.000 description 5
- 230000006698 induction Effects 0.000 description 5
- 230000002458 infectious effect Effects 0.000 description 5
- 238000007918 intramuscular administration Methods 0.000 description 5
- 239000002502 liposome Substances 0.000 description 5
- 230000007017 scission Effects 0.000 description 5
- 238000012163 sequencing technique Methods 0.000 description 5
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 4
- 108091026890 Coding region Proteins 0.000 description 4
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 4
- 241000030538 Thecla Species 0.000 description 4
- 101800001690 Transmembrane protein gp41 Proteins 0.000 description 4
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 4
- 235000009582 asparagine Nutrition 0.000 description 4
- 229960001230 asparagine Drugs 0.000 description 4
- 230000002238 attenuated effect Effects 0.000 description 4
- 239000011324 bead Substances 0.000 description 4
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 4
- 108010006025 bovine growth hormone Proteins 0.000 description 4
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 210000003527 eukaryotic cell Anatomy 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- 238000002649 immunization Methods 0.000 description 4
- 210000004877 mucosa Anatomy 0.000 description 4
- 238000004806 packaging method and process Methods 0.000 description 4
- 230000002028 premature Effects 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 238000002255 vaccination Methods 0.000 description 4
- 102000009410 Chemokine receptor Human genes 0.000 description 3
- 108050000299 Chemokine receptor Proteins 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 229940033332 HIV-1 vaccine Drugs 0.000 description 3
- 102100034349 Integrase Human genes 0.000 description 3
- 102000003812 Interleukin-15 Human genes 0.000 description 3
- 108090000172 Interleukin-15 Proteins 0.000 description 3
- 108010002350 Interleukin-2 Proteins 0.000 description 3
- 102000000588 Interleukin-2 Human genes 0.000 description 3
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 3
- 108090001074 Nucleocapsid Proteins Proteins 0.000 description 3
- 241000288906 Primates Species 0.000 description 3
- 101710150344 Protein Rev Proteins 0.000 description 3
- 108091027544 Subgenomic mRNA Proteins 0.000 description 3
- 230000000692 anti-sense effect Effects 0.000 description 3
- 230000003115 biocidal effect Effects 0.000 description 3
- 230000034303 cell budding Effects 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 210000002950 fibroblast Anatomy 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 3
- 229910052737 gold Inorganic materials 0.000 description 3
- 239000010931 gold Substances 0.000 description 3
- 230000003308 immunostimulating effect Effects 0.000 description 3
- 210000001161 mammalian embryo Anatomy 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 229920001184 polypeptide Polymers 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 230000001177 retroviral effect Effects 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 101150090490 vpu gene Proteins 0.000 description 3
- 108010076667 Caspases Proteins 0.000 description 2
- 101710170658 Endogenous retrovirus group K member 10 Gag polyprotein Proteins 0.000 description 2
- 101710186314 Endogenous retrovirus group K member 21 Gag polyprotein Proteins 0.000 description 2
- 101710162093 Endogenous retrovirus group K member 24 Gag polyprotein Proteins 0.000 description 2
- 101710094596 Endogenous retrovirus group K member 8 Gag polyprotein Proteins 0.000 description 2
- 101710177443 Endogenous retrovirus group K member 9 Gag polyprotein Proteins 0.000 description 2
- 101710091045 Envelope protein Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 2
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 2
- 208000031886 HIV Infections Diseases 0.000 description 2
- 108700010908 HIV-1 proteins Proteins 0.000 description 2
- 102100034347 Integrase Human genes 0.000 description 2
- 108091092195 Intron Proteins 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- 201000005505 Measles Diseases 0.000 description 2
- 108700026244 Open Reading Frames Proteins 0.000 description 2
- 238000012408 PCR amplification Methods 0.000 description 2
- 108010076504 Protein Sorting Signals Proteins 0.000 description 2
- 101710188315 Protein X Proteins 0.000 description 2
- 108020005067 RNA Splice Sites Proteins 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 102000006382 Ribonucleases Human genes 0.000 description 2
- 108010083644 Ribonucleases Proteins 0.000 description 2
- 241000607768 Shigella Species 0.000 description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 2
- 108020005202 Viral DNA Proteins 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000005875 antibody response Effects 0.000 description 2
- 210000000612 antigen-presenting cell Anatomy 0.000 description 2
- 230000000890 antigenic effect Effects 0.000 description 2
- 235000003704 aspartic acid Nutrition 0.000 description 2
- WXNRAKRZUCLRBP-UHFFFAOYSA-N avridine Chemical compound CCCCCCCCCCCCCCCCCCN(CCCN(CCO)CCO)CCCCCCCCCCCCCCCCCC WXNRAKRZUCLRBP-UHFFFAOYSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 230000029087 digestion Effects 0.000 description 2
- 235000013601 eggs Nutrition 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 description 2
- 238000002744 homologous recombination Methods 0.000 description 2
- 230000006801 homologous recombination Effects 0.000 description 2
- 238000012744 immunostaining Methods 0.000 description 2
- 230000000415 inactivating effect Effects 0.000 description 2
- 230000010468 interferon response Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 244000144972 livestock Species 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 2
- 239000004005 microsphere Substances 0.000 description 2
- 230000003472 neutralizing effect Effects 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000001566 pro-viral effect Effects 0.000 description 2
- 210000001236 prokaryotic cell Anatomy 0.000 description 2
- 230000006337 proteolytic cleavage Effects 0.000 description 2
- 238000010188 recombinant method Methods 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000010839 reverse transcription Methods 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000000638 solvent extraction Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 238000003146 transient transfection Methods 0.000 description 2
- 210000002845 virion Anatomy 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- BGKHCLZFGPIKKU-UHFFFAOYSA-N (13E,15S)-15-hydroxy-9-oxo-prosta-10,13-dienoic acid Natural products CCCCCC(O)C=CC1C=CC(=O)C1CCCCCCC(O)=O BGKHCLZFGPIKKU-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 1
- JXCKZXHCJOVIAV-UHFFFAOYSA-N 6-[(5-bromo-4-chloro-1h-indol-3-yl)oxy]-3,4,5-trihydroxyoxane-2-carboxylic acid;cyclohexanamine Chemical compound [NH3+]C1CCCCC1.O1C(C([O-])=O)C(O)C(O)C(O)C1OC1=CNC2=CC=C(Br)C(Cl)=C12 JXCKZXHCJOVIAV-UHFFFAOYSA-N 0.000 description 1
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical group N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 102100036465 Autoimmune regulator Human genes 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 101800001415 Bri23 peptide Proteins 0.000 description 1
- 101710117545 C protein Proteins 0.000 description 1
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 description 1
- 101710082513 C-X-C chemokine receptor type 4 Proteins 0.000 description 1
- 101800000655 C-terminal peptide Proteins 0.000 description 1
- 102400000107 C-terminal peptide Human genes 0.000 description 1
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 1
- 102000008203 CTLA-4 Antigen Human genes 0.000 description 1
- 229940045513 CTLA4 antagonist Drugs 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 108090000565 Capsid Proteins Proteins 0.000 description 1
- 206010057248 Cell death Diseases 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 102100023321 Ceruloplasmin Human genes 0.000 description 1
- 108091062157 Cis-regulatory element Proteins 0.000 description 1
- 108700010070 Codon Usage Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 108091035707 Consensus sequence Proteins 0.000 description 1
- 241000186216 Corynebacterium Species 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- 102000012410 DNA Ligases Human genes 0.000 description 1
- 108010061982 DNA Ligases Proteins 0.000 description 1
- 239000003155 DNA primer Substances 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 238000011510 Elispot assay Methods 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 101710121417 Envelope glycoprotein Proteins 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 241000700662 Fowlpox virus Species 0.000 description 1
- 229920002148 Gellan gum Polymers 0.000 description 1
- 229920001503 Glucan Polymers 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 108060003393 Granulin Proteins 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 102100021519 Hemoglobin subunit beta Human genes 0.000 description 1
- 108091005904 Hemoglobin subunit beta Proteins 0.000 description 1
- 108010088652 Histocompatibility Antigens Class I Proteins 0.000 description 1
- 102000008949 Histocompatibility Antigens Class I Human genes 0.000 description 1
- 108010027412 Histocompatibility Antigens Class II Proteins 0.000 description 1
- 102000018713 Histocompatibility Antigens Class II Human genes 0.000 description 1
- 101000928549 Homo sapiens Autoimmune regulator Proteins 0.000 description 1
- 102100034353 Integrase Human genes 0.000 description 1
- 102100037850 Interferon gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 108090000174 Interleukin-10 Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 108010092694 L-Selectin Proteins 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 102000016551 L-selectin Human genes 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 102000043129 MHC class I family Human genes 0.000 description 1
- 108091054437 MHC class I family Proteins 0.000 description 1
- 241000282553 Macaca Species 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- 208000005647 Mumps Diseases 0.000 description 1
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 239000005662 Paraffin oil Substances 0.000 description 1
- 208000002606 Paramyxoviridae Infections Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 201000005702 Pertussis Diseases 0.000 description 1
- 208000000474 Poliomyelitis Diseases 0.000 description 1
- 108010076039 Polyproteins Proteins 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 239000013616 RNA primer Substances 0.000 description 1
- 108700005075 Regulator Genes Proteins 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- 238000012300 Sequence Analysis Methods 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 206010043376 Tetanus Diseases 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 108700029229 Transcriptional Regulatory Elements Proteins 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 108010067390 Viral Proteins Proteins 0.000 description 1
- 239000000370 acceptor Substances 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 229960000723 ampicillin Drugs 0.000 description 1
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000036436 anti-hiv Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 229950010555 avridine Drugs 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 239000008366 buffered solution Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000007969 cellular immunity Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000007910 chewable tablet Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 108091036078 conserved sequence Proteins 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000002716 delivery method Methods 0.000 description 1
- 239000007933 dermal patch Substances 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 206010013023 diphtheria Diseases 0.000 description 1
- 241001493065 dsRNA viruses Species 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 101150030339 env gene Proteins 0.000 description 1
- 238000003114 enzyme-linked immunosorbent spot assay Methods 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 210000001723 extracellular space Anatomy 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 229960005191 ferric oxide Drugs 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 101150098622 gag gene Proteins 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 101150054900 gus gene Proteins 0.000 description 1
- 210000002443 helper t lymphocyte Anatomy 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 230000004727 humoral immunity Effects 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 230000005934 immune activation Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000001114 immunoprecipitation Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 208000010805 mumps infectious disease Diseases 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 101150023385 nef gene Proteins 0.000 description 1
- 231100000957 no side effect Toxicity 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 239000006179 pH buffering agent Substances 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 230000003071 parasitic effect Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 150000002972 pentoses Chemical class 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 101150088264 pol gene Proteins 0.000 description 1
- 229920001308 poly(aminoacid) Polymers 0.000 description 1
- 108091033319 polynucleotide Proteins 0.000 description 1
- 102000040430 polynucleotide Human genes 0.000 description 1
- 239000002157 polynucleotide Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- BGKHCLZFGPIKKU-LDDQNKHRSA-N prostaglandin A1 Chemical compound CCCCC[C@H](O)\C=C\[C@H]1C=CC(=O)[C@@H]1CCCCCCC(O)=O BGKHCLZFGPIKKU-LDDQNKHRSA-N 0.000 description 1
- 101150098213 rev gene Proteins 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 102200006478 rs786205837 Human genes 0.000 description 1
- 229930182490 saponin Natural products 0.000 description 1
- 150000007949 saponins Chemical class 0.000 description 1
- 235000017709 saponins Nutrition 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000037432 silent mutation Effects 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 101150098170 tat gene Proteins 0.000 description 1
- 229940124598 therapeutic candidate Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 238000011282 treatment Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 201000008827 tuberculosis Diseases 0.000 description 1
- 230000034512 ubiquitination Effects 0.000 description 1
- 238000010798 ubiquitination Methods 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 229940126580 vector vaccine Drugs 0.000 description 1
- 101150059019 vif gene Proteins 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000017613 viral reproduction Effects 0.000 description 1
- 101150024249 vpr gene Proteins 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/21—Retroviridae, e.g. equine infectious anemia virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/70—Vectors or expression systems specially adapted for E. coli
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5256—Virus expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/53—DNA (RNA) vaccination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/24011—Poxviridae
- C12N2710/24111—Orthopoxvirus, e.g. vaccinia virus, variola
- C12N2710/24141—Use of virus, viral particle or viral elements as a vector
- C12N2710/24143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16111—Human Immunodeficiency Virus, HIV concerning HIV env
- C12N2740/16122—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16111—Human Immunodeficiency Virus, HIV concerning HIV env
- C12N2740/16134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16211—Human Immunodeficiency Virus, HIV concerning HIV gagpol
- C12N2740/16222—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16211—Human Immunodeficiency Virus, HIV concerning HIV gagpol
- C12N2740/16234—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/15—Vector systems having a special element relevant for transcription chimeric enhancer/promoter combination
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/42—Vector systems having a special element relevant for transcription being an intron or intervening sequence for splicing and/or stability of RNA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/60—Vector systems having a special element relevant for transcription from viruses
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Virology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- General Chemical & Material Sciences (AREA)
- Communicable Diseases (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Hematology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Tropical Medicine & Parasitology (AREA)
- AIDS & HIV (AREA)
- Oncology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
本出願は2002年3月8日出願の米国特許出願第10/093,953号の一部継続出願であり、そして2001年3月2日出願の米国特許出願第09/798,675号の一部継続出願であり、そして4つの仮出願(2000年12月1日出願の米国特許出願第60/251,083号、2000年3月2日出願の米国特許出願第60/186,364号、2001年9月25日出願の米国特許出願第60/324,845号および2001年9月26日出願の米国特許出願第60/325,004号)の出願日の恩典および2001年12月6日に国際公開番号第WO01/92470号の下で英語で公開された2001年3月2日出願の国際出願PCT/US01/06795の出願日の恩典を請求する。これは、前記で列挙した先行の出願の内容はその全てを参照として本明細書に組み入れられる。
本発明は概して分子遺伝学および免疫学の分野を指向する。さらに詳細には、本発明は発現ベクターよびこれらのベクターを動物に投与する方法を特徴とする。
本明細書に記載する研究は少なくとも一部、国立衛生研究所からの助成金による支援を受けた(P01 AI43045、P01 AI49364、およびR21 AI44325)。従って米国政府はこの発明において一定の権利を有している。
ワクチンは世界保健に及ぼす絶大で、そして長期的な影響を有している。天然痘は撲滅され、ポリオはほぼ廃絶されており、そしてジフテリア、麻疹、流行性耳下腺炎、百日咳、および破傷風のような疾患が含まれる。それにもかかわらず、現在のワクチンはヒトおよび家畜が被る少数の感染しか対処していない。ワクチンがない一般の感染疾患に米国だけで年間約1200億ドルが費やされている(Robinsonら、American Academy of Microbiology、1996年5月31日から6月2日)。先進工業国では、免疫不全ウイルスのような感染が出現し、そして結核の薬物耐性型のような疾患が再出現しており、ワクチン開発に関する新たな脅威および挑戦をもたらしている。有効なワクチンがしばしば利用できないかまたは多大な経費がこのような第三世界諸国では、新しく、そして改善もされてもいるワクチンに関する必要性がさらに顕著である。
AIDSの蔓延の持続力は、しばしば変異し、そしていくつかの異なるクレード(またはサブタイプ)および組換え体で存在するヒト免疫不全ウイルス(HIV)に対する有効なワクチンに関する差し迫った必要性を明示している。天然にまたはヒトの介入の結果として生じ得るこれらのサブタイプおよび組換え体を、その核酸の配列における差異により区別することができる。1つのHIVクレード、サブタイプ、もしくはHIVの組換え体に対する、または複数のHIVクレード、サブタイプ、もしくはHIVの組換え体に対するワクチンとして単独で、または組み合わせで用いることができるDNAベクター、ウイルスベクターおよび組換えウイルス、例えば組換え改変ワクシニア・アンカラ(MVA)ウイルス(以下に詳細に記載する)を開発した(特記しない場合、「(複数の)クレード」なる用語はHIVのサブタイプまたは組換え体を包含することを意味する)。さらに、ベクターは、1つのクレードまたは2つもしくはそれ以上の異なるクレードから得られる種々の抗原をコードすることができ、そして選択された抗原および/またはベクターを処方する様式(例えば混合する)を操作して種々のクレード(例えば患者が暴露される可能性が最も高いクレード)に対する保護免疫応答を作製することができる。
本発明は幅広い種類のベクターおよびベクターの型(例えばプラスミドおよびウイルスベクター)を包含し、その各々は、必ずしも必要というわけではないが、その抗原が得られたまたは誘導された病原体に対して免疫応答を引き出す(例えば誘起または増強する)一つまたは複数の抗原をコードする一つまたは複数の核酸配列を含むことができる(免疫応答を引き出すタンパク質をコードする配列を本明細書では「ワクチンインサート」または単に「インサート」と称することがあり;変異が天然発生配列に導入される場合、得られた変異体は天然発生配列から「誘導される」)。「インサート」を含まないベクターは本発明の範囲内であり、そしてインサート自体もまた本発明の組成物であることを明らかにするために、ベクターは必ずしも抗原をコードする必要がないことが指摘される。
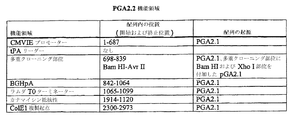
pGA1(図1および2参照)は(1)ColE1複製起点(複製起点(ori)を含有し、そしてRNAプライマーおよび2個の複製開始の負のレギュレーターをコードする672bp配列)、(2)カナマイシン抵抗性遺伝子(細菌におけるプラスミド選択のための抗生物質抵抗性遺伝子)、(3)ラムダT0ターミネーター、並びに(4)上流のイントロン(ここではCNVイントロンA)、CNV極初期(CMVIE)プロモーター、およびウシ成長ホルモンポリアデニル化配列由来の終止配列(BGHpA)を含む真核細胞発現カセットを含有する。組織プラスミノーゲンアクチベーター(tPA)リーダー配列の合成擬似物質もまた発現カセット内に含まれる。発現カセットは複数の制限部位を含むことができ、そしてこれらの部位はいずれかのHIVクレードに由来する抗原をコードする発現カセットの封入を促進することを、所望どおりに含めるかまたは排除することができる。pGA1のクローニング部位はtPAリーダーの上流にCla I部位、tPAリーダーのフレーム内にクローニングするためのNhe I部位、並びにBGHpAに先立ってクローニングするためのXmn I、Sma I、Rsr II、およびAvr II部位を含む。ColE1レプリケーターを含有する元来の構築されたプラスミドはpBR322であった(Bolivarら、Gene 2:95-113(1977);Sutcliffeら、Cold Spring Harbor Quant.Biol.43:77-90(1978))。
を含んだ。
pGA1.1(配列番号:2)は、多重クローニング部位がEcoRI部位を含むように変化していること以外はpGA1と同一である。これを以下のプライマー
(フォワード)
および
(リバース)(各々配列番号:17および18)を用いて部位特異的変異誘発により達成した。従って、pGA1.1ベクターは本発明の態様であり;pGAプラスミドの一つまたは複数の特徴または特性を有するその他のベクター(詳細な説明を参照)と同様であるが、多重クローニング部位の制限エンドヌクレアーゼ部位は異なっている(例えば本発明は、それ以外は実質的にpGA1に類似するが、その多重クローニング部位に多少異なる制限エンドヌクレアーゼ部位を有するプラスミドを包含する)。
pGA1.2(配列番号:3)は、多重クローニング部位がEcoRI部位の5'にBamHIおよびXhoI部位を含むように変化していること以外はpGA1.1と同一である。これをプライマー
およびリバースプライマー
を用いて部位特異的変異誘発により達成した。
pGA2を図5で図式的に説明し、そしてそのヌクレオチド配列を図6(配列番号:4)に示す。pGA2は、イントロンA配列がpGA2のCMVプロモーターから除去されていること以外はpGA1と同一である。CMVプロモーターのmRNAキャップ部位から8bp下流にCla I部位を導入することによりpGA1からpGA2を作製し;配列:
および
を有する相補的プライマーを用いたオリゴヌクレオチド部位特異的変異誘発を用いてCla I部位を導入した。新たなCla I部位を挿入した後、Cla IでpGA1を消化してpGA1から946bpのCla I断片を除去し、そして次にライゲートしてpGA2を生成させた。
pGA2.1(配列番号:5)は、多重クローニング部位がEcoRI部位を含むように変化していること以外はpGA2と同一である。これを以下のプライマー:フォワード
およびリバース
を用いて部位特異的変異誘発により達成した。従って、pGA2.1ベクターは本発明の態様であり;pGAプラスミドの一つまたは複数の特徴または特性を有するその他のベクター(詳細な説明を参照)と同様であるが、多重クローニング部位の制限エンドヌクレアーゼ部位は異なっている(例えば本発明は、それ以外は実質的にpGA1に類似するが、その多重クローニング部位に多少異なる制限エンドヌクレアーゼ部位を有するプラスミドを包含する)。
pGA2.2(配列番号:6)は、多重クローニング部位がEcoRI部位の5'にBamHIおよびXhoI部位を含むように変化していること以外はpGA1.1と同一である。これをフォワードプライマー
およびリバースプライマー
(各々配列番号:23および24)を用いて部位特異的変異誘発により達成した。
ベクターのpGA1およびpGA2シリーズのためのHIV-1ワクチンインサートを構築して、免疫欠損ウイルスにより用いられる同一のサブゲノムスプライシング機構を用いて単一のRNA転写体から複数のHIV-1タンパク質を発現した。これらの多タンパク質発現ベクターが感染性ウイルスを形成しなかったことを確認するために、欠失および点変異を導入してレトロウイルスライフサイクルの必須工程を不能化した。図9は正常なレトロウイルスゲノムおよび代表的なワクチンインサートの図式を示す。インサートで除去されている領域を点描する。Xは点変異を示す。欠失はプロウイルスDNAの逆転写、組み込みおよび発現のためのシス作動性エレメントをコードする長末端反復(LTR)の双方を含んだ。ウイルスRNAのキャプシド形成を促進する5'LTRに隣接する5'配列は除去されている。polコード化インテグラーゼの領域のコード化配列並びに補助遺伝子vifおよびvprは除去されている。そして、最終的にNef制御タンパク質をコードする遺伝子であるnefは除去されている。以下の実施例で記載する全てのインサートに共通する7つの点変異が図式に含まれる。これらは、ジンクフィンガーに媒介されるウイルスRNAのパッケージングを制限するヌクレオキャプシドタンパク質のジンクフィンガーにおける4つの変異、およびウイルスRNAの逆転写を防御する逆転写酵素における3つの変異を含む。gagおよび/またはpolを含むいずれかのワクチンインサートにおいて類似の変化を作製することができる。さらに、本明細書に記載するいずれかのプラスミドまたはベクター化された生ワクチンのいずれかに配置されるワクチンインサートにおいてこれらの変化(または類似の変化)を作製することができる(すなわちpGAベクターの一つまたは複数の特徴または特性を有するいずれかのプラスミド、pGAベクター自体、または単独でもしくはDNAプライムされた患者と組み合わせて(例えばブーストするために)用いることができるワクシニアベクター)。
pGA2/JS2の配列を図7a(配列番号:7)、その機能的領域およびこれらの領域の起源を図7bに、並びにその点変異の位置を図7cに示す。本明細書に記載するJS2インサートを米国、欧州および日本で蔓延しているHIV-1配列に対する免疫応答を引き出すように、クレードB HIV-1配列で設計した。前記したように、いずれかのクレードB単離体をその他のクレードB単離体の合理的な代表として使用することができる。HIV-1単離体はコレセプターとして異なるケモカインレセプターを使用し、そして伝染する大部分のウイルスはCCR-5コレセプターを使用するので(Berger、AIDS 11(補冊A):S3-16(1997))、設計したワクチンインサートはCCR-5使用Envであった。もちろん、いずれかその他のコレセプターを介して機能するか、または天然発生もしくは合成配列から免疫原性を高めるように構築されたEnvを同様に作製し、そして使用することができる。
およびアンチセンスプライマー
を用いて5'PCR産物を増幅した。
およびアンチセンスプライマー
を用いて3'PCR産物を増幅した。5'PCR産物をpGA1のCla IおよびNhe I部位でpGA1にクローン化し、そしてシークエンシングにより構築物の同一性を確認した。次いで3'PCR産物をEcoR IおよびNhe I部位で5'クローンに挿入してpBH10を生成させた。このプラスミドの構築によりLTR、インテグラーゼ、vif、vprおよびnef配列を欠くプロウイルス配列に至った(図9参照)。
pGA2/JS7の配列を図11a(配列番号:8)に、その機能的領域およびこれらの領域の起源を図11bに、そしてそのコドン変異の位置を図11cに示す。BH10のGag配列をJS7インサートではHIV-1-HXB-2のGag配列に置換する。これを以下のプライマー:
フォワード
およびリバース
を用いたHXB-2配列(p5'プラスミド、NIH AIDS Reserach and Reference Program、カタログ番号3119)のPCR増幅により達成した。フォワードプライマーはJS2インサートで見出されたのと同一の位置にCla I部位を導入し、そしてリバースプライマーはJS2インサートの同一部位に類似する独特なEcoR I部位を導入した。次いでこのPCR断片を変異誘発のためにpGA1.1に挿入した。次いでジンクフィンガー領域における安全性変異およびRT変異を、JS2インサートに関して前記したように導入した。JS7はまた、プロテアーゼの活性部位で不活性化コドン変異を有する点でJS2と異なっている。プライマー
および
を用いてこの変異を導入した。一度シークエンシングにより変異が確認されると、HXB-2 Gag-PolインサートをCla IおよびEcoR I部位を介してpGA2/JS2に導入した。ウイルスプロテアーゼによるpr55Gagポリタンパク質の時期尚早な切断のためにHIV-1タンパク質の凝集物を発現するJS2インサートと対照的に、JS7インサートはDNA発現細胞の原形質膜から出芽する未熟なウイルス様粒子(VLP)を形成する。
pGA2/JS7.1の配列を図12a(配列番号:9)に、その機能的領域およびこれらの領域の起源を図12bに、そしてそのコドン変異の位置を図12cに示す。pGA2/JS7.1は、vpuで開始コドンおよび直ぐ上流のATGが変異しているpGA2/JS7の誘導体である。これらの変異を導入してEnvの発現のレベルを上昇させた。部位特異的変異誘発キット(Stratagene)およびオリゴヌクレオチド:フォワード
およびリバース
を用いてVpuの開始コドンにおける変異を達成した。
pGA1/IS25の配列を図13a(配列番号:10)に、その機能的領域およびこれらの領域の起源を図13bに、そしてその点変異の位置を図13cに示す。本明細書に記載するIC25インサートを西アフリカで蔓延しているHIV-1配列に対する免疫応答を引き出すように、クレードAおよびG(AGと称する)の循環組換え体で設計した。前記したように、西アフリカからのいずれかのクレードAG単離体をその他のクレードAG単離体の合理的な代表として使用することができる。HIV-1単離体はコレセプターとして異なるケモカインレセプターを使用し、そして伝染する大部分のウイルスはCCR-5コレセプターを使用するので(Berger、AIDS 11(補冊A):S3-16(1997))、設計したAGワクチンインサートはCCR-5使用Envを有した。もちろん、いずれかその他のコレセプターを介して機能するか、または天然発生もしくは合成AG配列から免疫原性を高めるように構築されたEnvを同様に作製し、そして使用することができる。
およびリバースプライマー
を用いて5'Gag-RT PCR産物を増幅した。Env領域に関する3'PCR産物はvpu、tat、rev、およびenv配列並びにその各々のmRNAの適切なプロセシングおよび発現に必要なスプライスアクセプター部位を包含する。EcoR I部位をこの産物の5'末端に導入し、そしてNhe IおよびRsr II部位を3'末端に導入した。フォワードプライマー
およびリバースプライマー
を用いて3'PCR産物を増幅した。もちろん、患者928に由来するものはさらに発展させるのに特に好ましい(表2)。コドン変異ではなく欠失を伴う928配列をIC1と称した。
であった。
pGA1/IC2の配列を図14a(配列番号:11)に、その機能的領域およびこれらの領域の起源を図14bに、そしてその点変異の位置を図14cに示す。pGA1/IC2は、プロテアーゼに不活性化点変異を含有しないこと以外はpGA1/IC25と同一である。
pGA1/IC48の配列を図15a(配列番号:12)に、その機能的領域およびこれらの領域の起源を図15bに、そしてその点変異の位置を図15cに示す。pGA1/IC48は、プロテアーゼにおけるコドン変異が薬物抵抗性変異体に生じたものであること以外はpGA1/IC25と同一である(Jocabsenら、Virology 206:527-534(1995))。この変異はプロテアーゼ機能を部分的にのみ不活性化する。Stratageneキットおよび以下のオリゴヌクレオチド:
および
を用いて変異誘発を実施した。この変異はプロテアーゼ機能を部分的にのみ不活性化する。
pGA1/IC90の配列を図16a(配列番号:13)に、その機能的領域およびこれらの領域の起源を図16bに、そしてその点変異の位置を図16cに示す。pGA1/IC90は、プロテアーゼにおけるコドン変異が薬物抵抗性変異体に生じたものであること以外はpGA1/IC25と同一である(Jocabsenら、Virology 206:527-534(1995))。この変異はプロテアーゼ機能を部分的にのみ不活性化する。Stratageneキットおよび以下のオリゴヌクレオチド:
および
を用いて変異誘発を実施した。
pGA1/IN3の配列を図17a(配列番号:14)に、その機能的領域およびこれらの領域の起源を図17bに、そしてその点変異の位置を図17cに示す。本明細書に記載するIN3インサートを、インドでウイルスから回収されたクレードC配列から構築した。前記したように、いずれかのクレードC単離体をその他のクレードC単離体の合理的な代表として使用することができる。HIV-1単離体はコレセプターとして異なるケモカインレセプターを使用し、そして伝染する大部分のウイルスはCCR-5コレセプターを使用するので(Berger、AIDS 11(補冊A):S3-16(1997))、構築するために選択したCワクチンインサートはCCR-5使用Envを有した。もちろん、いずれかその他のコレセプターを介して機能するか、または天然発生もしくは合成C配列から免疫原性を高めるように構築されたEnvを同様に作製し、そして使用することができる。
、並びに断片の3'末端でXho I部位および2個の停止コドンを組み込んだリバースプライマー
を用いて作製した。Tat、Rev、Vpu、およびEnvをコードする3'断片をフォワードプライマー
およびリバースプライマー
を用いて作製した。Xho IおよびNhe I制限部位が3'断片の各々5'および3'末端で組み込まれるようにこれらを設計した。これらの断片を、定方向クローニングを用いてpGA1.2に導入しpGA1.2/IN1を作製した。
であった。
pGA1/IN2の配列を図18a(配列番号:5)に、その機能的領域およびこれらの領域の起源を図18bに、そしてその点変異の位置を図18cに示す。pGA1/IN2は、プロテアーゼにD25N不活性化点変異を有さない点でpGA1/IN3と異なっている。
JS、ICおよびINインサートの配列を用いて対合した組換え改変ワクシニア・アンカラ(rMVA)ベクターを調製した。これらの対合したベクターを種々DNAのブースター接種として使用することができる。また抗HIV免疫応答をプライミングおよびブースティングの双方を行うためにこれらを使用することもできる。ウイルスベクターを作製するために提供された配列は逆転写酵素に3つの不活性化点変異を含んだ。組換えMVAベクターを構築し、そして特徴づけした代表的な研究は以下のとおりである。
Claims (50)
- (a)ヒト免疫不全ウイルス(HIV)の第1サブタイプまたは組換え体に対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第1ベクター;および
(b)HIVの第2サブタイプまたは組換え体に対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第2ベクター;
を含む組成物。 - 薬学的に許容される担体またはアジュバントをさらに含む、請求項1記載の組成物。
- 第1ベクターのインサートまたは第2ベクターのインサートが、2つまたはそれ以上の、(a)gag、pol、env、tat、rev、nef、vif、vpr、もしくはvpu遺伝子または(b)その変異体および選択的に、(c)HIVゲノムの非コード化制御配列;の配列を含む、請求項1記載の組成物。
- 2つまたはそれ以上の配列の少なくとも1つが、ウイルスRNAのキャプシド形成を制限する変異を含む、請求項3記載の組成物。
- 2つまたはそれ以上の配列の少なくとも1つが、ジンクフィンガーをコードする一つまたは複数の配列に変異を有するgag配列を含む、請求項3記載の組成物。
- HIV-1の非コード化制御配列からシス作動性RNAのキャプシド形成配列の全てまたは一部が削除されている、請求項4記載の組成物。
- 2つまたはそれ以上の配列が、一つまたは複数のpolの酵素活性を阻害する変異を有するpol配列を含む、請求項3記載の組成物。
- 酵素活性がインテグラーゼ活性である、請求項7記載の組成物。
- 酵素活性が逆転写酵素活性である、請求項7記載の組成物。
- 酵素活性がプロテアーゼ活性である、請求項7記載の組成物。
- 酵素活性がpol配列の一部の削除またはpol配列への一つまたは複数の点変異の導入により阻害される、請求項8、9または10の組成物。
- 第1ベクターのインサートまたは第2ベクターのインサートが、一つまたは複数の欠失または点変異を有するtat、rev、nef、vif、vpr、またはvpuを含む、請求項3記載の組成物。
- 欠失または点変異がtat、rev、nef、vif、vpr、またはvpuの一つまたは複数の開始コドンを不活性化させる、請求項12記載の組成物。
- 第1ベクターまたは第2ベクターが、
(a)ジンクフィンガーが不活性化されているgagタンパク質;
(b)(i)pol配列のいくつかまたは全てを除去することによりインテグラーゼ活性が阻害されている、および(ii)pol配列内の一つまたは複数の点変異により逆転写酵素のポリメラーゼ、鎖転移および/またはRNアーゼH活性が阻害されているpolタンパク質;並びに
(c)変異を含まないenv、tat、rev、およびvpuをコードするプラスミドである、請求項3記載の組成物。 - コードされたタンパク質がサブタイプBもしくはD HIV-1から誘導されるかまたはサブタイプBもしくはD HIV-1の組換え体である、請求項14記載の組成物。
- 第1ベクターまたは第2ベクターがpGA2/JS2を含む、請求項14記載の組成物。
- コードされたタンパク質がサブタイプA HIV-1から誘導されるかまたはサブタイプA HIV-1の組換え体である、請求項14記載の組成物。
- 第1ベクターまたは第2ベクターがpGA1/IC2を含む、請求項17記載の組成物。
- コードされたタンパク質がサブタイプC HIV-1から誘導されるかまたはサブタイプC HIV-1の組換え体である、請求項14記載の組成物。
- 第1ベクターまたは第2ベクターがpGA1/IN2を含む、請求項19記載の組成物。
- コードされたタンパク質がHIV-1のサブタイプE、F、G、H、I、J、K、もしくはLサブタイプから誘導されるかまたはサブタイプE、F、G、H、I、J、K、もしくはL HIV-1の組換え体である、請求項14記載の組成物。
- 第1ベクターまたは第2ベクターが
(a)ジンクフィンガーが不活性化されているgagタンパク質;
(b)(i)pol配列のいくつかまたは全てを除去することによりインテグラーゼ活性が阻害されている、(ii)pol配列内の一つまたは複数の点変異により逆転写酵素のポリメラーゼ、鎖転移および/またはRNアーゼH活性が阻害されている、および(iii)プロテアーゼのタンパク質分解活性が一つまたは複数の点変異により阻害されているpolタンパク質;並びに
(c)変異を含まないenv、tat、rev、およびvpu;
をコードするプラスミドである、請求項3記載の組成物。 - コードされたタンパク質がサブタイプBもしくはD HIV-1から誘導されるかまたはサブタイプBもしくはD HIV-1の組換え体である、請求項22記載の組成物。
- 第1ベクターまたは第2ベクターがpGA2/JS7を含む、請求項23記載の組成物。
- コードされたタンパク質がサブタイプA HIV-1から誘導されるかまたはサブタイプA HIV-1の組換え体である、請求項22記載の組成物。
- 第1ベクターまたは第2ベクターがpGA1/IC25を含む、請求項25記載の組成物。
- コードされたタンパク質がサブタイプC HIV-1から誘導されるかまたはサブタイプC HIV-1の組換え体である、請求項22記載の組成物。
- 第1ベクターまたは第2ベクターがpGA1/IN3を含む、請求項27記載の組成物。
- コードされたタンパク質がHIV-1のサブタイプE、F、G、H、I、J、K、もしくはLサブタイプから誘導されるかまたはサブタイプE、F、G、H、I、J、K、もしくはL HIV-1の組換え体である、請求項22記載の組成物。
- 第1ベクターまたは第2ベクターが
(a)ジンクフィンガーが不活性化されているgagタンパク質;
(b)(i)インテグラーゼ活性が阻害されている、(ii)pol配列内の一つまたは複数の点変異により逆転写酵素のポリメラーゼ、鎖転移および/またはRNアーゼH活性が阻害されている、および(iii)pol配列内の一つまたは複数の点変異によりプロテアーゼのタンパク質分解活性が阻害されているpolタンパク質;
(c)変異体開始コドンを含むvpuタンパク質;並びに
(d)変異されていない形態のenv、tat、およびrev
をコードするプラスミドである、請求項3記載の組成物。 - コードされたタンパク質がサブタイプBもしくはD HIV-1から誘導されるかまたはサブタイプBもしくはD HIV-1の組換え体である、請求項30記載の組成物。
- 第1ベクターまたは第2ベクターがpGA2/JS7.1を含む、請求項31記載の組成物。
- コードされたタンパク質がHIV-1のサブタイプA、C、E、F、G、H、I、J、K、もしくはLサブタイプから誘導されるかまたはサブタイプA、C、E、F、G、H、I、J、K、もしくはL HIV-1の組換え体である、請求項30記載の組成物。
- ベクターがウイルスである、請求項1記載の組成物。
- ウイルスが組換えポックスウイルスである、請求項34記載の組成物。
- ウイルスが改変ワクシニア・アンカラウイルスである、請求項34記載の組成物。
- 改変ワクシニア・アンカラウイルスが、JS2またはJS7の配列に対合するクレードB配列をコードする組換え核酸を有する、請求項36記載の組成物。
- 改変ワクシニア・アンカラウイルスが、IC2またはIC25の配列に対合するクレードA配列をコードする組換え核酸を有する、請求項36記載の組成物。
- 改変ワクシニア・アンカラウイルスが、IN2またはIN3の配列に対合するクレードC配列をコードする組換え核酸を有する、請求項36記載の組成物。
- 改変ワクシニア・アンカラウイルスがサブタイプA、B、C、D、E、F、G、H、I、J、K、もしくはL HIV-1の組換え体であるかまたはDNAワクチンの配列に対合するサブタイプA、B、C、D、E、F、G、H、I、J、K、もしくはL HIV-1の組換え体である、請求項36記載の組成物。
- (a)HIVワクチンを必要とする対象を同定する段階;および
(b)ヒト免疫不全ウイルスに対する免疫応答を誘導または増強するワクチンインサートを含むベクターを含む治療上有効量の組成物を対象に投与する段階;
を含む、対象を処置する方法。 - (a)HIVワクチンを必要とする対象を同定する段階;および
(b)(i)ヒト免疫不全ウイルス(HIV)の第1サブタイプまたは組換えに対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第1ベクターおよび(ii)HIVの第2サブタイプまたは組換えに対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第2ベクターを含む治療上有効量の組成物を対象に投与する段階;
を含む、対象を処置する方法。 - (a)HIVワクチンを必要とする対象を同定する段階;並びに
(b)(i)ヒト免疫不全ウイルス(HIV)の第1サブタイプまたは組換え体に対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第1ベクター、(ii)HIVの第2サブタイプまたは組換え体に対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第2ベクター、および(iii)HIVの第3サブタイプまたは組換え体に対する免疫応答を引き出す一つまたは複数の抗原をコードするワクチンインサートを含む第3ベクターを含む治療上有効量の組成物を対象に投与する段階;
を含む、対象を処置する方法。 - 組成物を投与する段階が、保護免疫応答をプライムおよびブーストする目的で1回を超える頻度でプラスミドベクターを投与する段階を含む、請求項40、41、または42の方法。
- 組成物を投与する段階が、免疫応答をプライムする目的で1回または1回を超える頻度でプラスミドベクターを投与する段階、および免疫応答をブーストする目的で続けて1回または1回を超える頻度で改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項40、41、または42の方法。
- プラスミドベクターがJS2、JS7、もしくはJS7.1と称するインサート、および/またはIC2、IC25、IC48、もしくはIC90、と称するインサート、および/またはIN2もしくはIN3と称するインサートを含み、そしてここでブースティングは、プライミングのために用いられるプラスミドに対合したHIV配列を含有する改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項45記載の方法。
- プラスミドベクターがHIVクレードAおよび/またはクレードB、および/またはクレードC、および/またはクレードD、および/またはクレードE、および/またはクレードF、および/またはクレードG、および/またはクレードH、および/またはクレードJ、および/またはクレードK、および/またはクレードL、および/またはその組換えサブタイプを含み、そしてここでブースティングは、プライミングのために用いられるプラスミドに対合したHIV配列を含有する改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項45記載の方法。
- 組成物を投与する段階が、保護免疫応答をプライムおよびブーストする目的で1回を超える頻度で改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項40、41、または42の方法。
- プライミングが、クレードB組換えMVAウイルスおよび/またはクレードA組換えMVAウイルスおよび/またはクレードC組換えMVAウイルスおよび/またはいずれかのその組換えサブタイプを投与する段階を含み、そしてここでブースティングは、プライミングのために用いられる同一の改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項44記載の方法。
- プライミングが、改変ワクシニア・アンカラウイルスのクレードAおよび/またはクレードB、および/またはクレードC、および/またはクレードD、および/またはクレードE、および/またはクレードF、および/またはクレードG、および/またはクレードH、および/またはクレードJ、および/またはクレードK、および/またはクレードL、および/またはその組換えサブタイプを投与する段階を含み、そしてここでブースティングはプライミングのために用いられる同一の改変ワクシニア・アンカラウイルスを投与する段階を含む、請求項44記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/093,953 US20040105871A1 (en) | 2000-03-02 | 2002-03-08 | Compositions and methods for generating an immune response |
| US10/336,566 US8623379B2 (en) | 2000-03-02 | 2003-01-03 | Compositions and methods for generating an immune response |
| PCT/US2003/007177 WO2003076591A2 (en) | 2002-03-08 | 2003-03-10 | Compositions and methods for generating an immune response |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011113185A Division JP2011231112A (ja) | 2002-03-08 | 2011-05-20 | 免疫応答を作製するための組成物および方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005531513A true JP2005531513A (ja) | 2005-10-20 |
| JP2005531513A5 JP2005531513A5 (ja) | 2006-04-27 |
Family
ID=31996485
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003574798A Withdrawn JP2005531513A (ja) | 2002-03-08 | 2003-03-10 | 免疫応答を作製するための組成物および方法 |
| JP2011113185A Pending JP2011231112A (ja) | 2002-03-08 | 2011-05-20 | 免疫応答を作製するための組成物および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011113185A Pending JP2011231112A (ja) | 2002-03-08 | 2011-05-20 | 免疫応答を作製するための組成物および方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US8623379B2 (ja) |
| EP (2) | EP1483385A4 (ja) |
| JP (2) | JP2005531513A (ja) |
| CN (1) | CN1653176A (ja) |
| AU (1) | AU2008243079A1 (ja) |
| CA (1) | CA2478371C (ja) |
| WO (1) | WO2003076591A2 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8623379B2 (en) * | 2000-03-02 | 2014-01-07 | Emory University | Compositions and methods for generating an immune response |
| WO2005034992A2 (en) * | 2003-09-15 | 2005-04-21 | The Government Of The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Hiv vaccines based on env of multiple clades of hif |
| US7622125B2 (en) * | 2004-05-05 | 2009-11-24 | Novartis Vaccines And Diagnostics, Inc. | Polycistronic HIV vector constructs |
| JP4772045B2 (ja) * | 2004-07-16 | 2011-09-14 | アメリカ合衆国 | Cmv/r核酸コンストラクトを含むaidsに対するワクチン |
| WO2006026667A2 (en) * | 2004-08-27 | 2006-03-09 | The Government Of The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Recombinant mva viruses expressing glade a/g, clade b, and clade c modified hiv, gag and pol genes |
| EP1970441A1 (en) * | 2007-03-06 | 2008-09-17 | BioAlliance Pharma | Plasmid containing a sequence encoding a disintegrin domain of metargidin (RDD) |
| CN101569745A (zh) * | 2009-05-25 | 2009-11-04 | 苏州工业园区唯可达生物科技有限公司 | 抗多种艾滋病毒的组合疫苗及其组合方法 |
| CA2790426A1 (en) * | 2010-02-18 | 2011-08-25 | Emory University | Vectors expressing hiv antigens and gm-csf and related methods for generating an immune response |
| CN102258779B (zh) * | 2011-07-18 | 2013-07-24 | 曾毅 | 四种及四种以上hiv载体基因疫苗序贯及重复应用 |
| RU2709771C2 (ru) * | 2013-03-15 | 2019-12-19 | Симентис Лимитед | Иммунная модуляция |
| WO2016068919A1 (en) | 2014-10-29 | 2016-05-06 | Geovax, Inc. | Combination therapy for treating viral reservoirs |
| WO2016196471A1 (en) | 2015-06-02 | 2016-12-08 | Cooper Human Systems Llc | Methods and compositions for treatment of hiv infection |
| AU2017206102C1 (en) | 2016-01-08 | 2022-02-10 | Geovax Inc. | Compositions and methods for generating an immune response to a tumor associated antigen |
| US11098086B2 (en) | 2016-02-16 | 2021-08-24 | Geovax Inc. | Multivalent HIV vaccine boost compositions and methods of use |
| US11311612B2 (en) | 2017-09-19 | 2022-04-26 | Geovax, Inc. | Compositions and methods for generating an immune response to treat or prevent malaria |
| CN113164951B (zh) * | 2018-09-20 | 2023-09-08 | 塞弗德公司 | 使用半导体检测芯片的样品处理系统、装置及方法 |
| EP3894077A2 (en) | 2018-12-14 | 2021-10-20 | Cepheid | Diagnostic detection chip devices and methods of manufacture and assembly |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001092470A2 (en) * | 2000-03-02 | 2001-12-06 | Emory University | Dna expression vectors and methods of use |
| WO2003004657A1 (en) * | 2001-07-05 | 2003-01-16 | Chiron Corporation | Polynucleotides encoding antigenic hiv type b and/or type c polypeptides, polypeptides and uses thereof |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5169763A (en) | 1986-04-08 | 1992-12-08 | Transgene S.A., Institut Pasteur | Viral vector coding glycoprotein of HIV-1 |
| IL82104A0 (en) | 1986-04-08 | 1987-10-30 | Usa | Recombinant vaccinia virus expressing human retrovirus genes and method for producing htlb-iii envelope proteins |
| US5256767A (en) | 1987-06-10 | 1993-10-26 | The Immune Response Corporation | Retroviral antigens |
| CA1341245C (en) | 1988-01-12 | 2001-06-05 | F. Hoffmann-La Roche Ag | Recombinant vaccinia virus mva |
| IL89567A0 (en) | 1988-03-28 | 1989-09-10 | Univ Leland Stanford Junior | Mutated hiv envelope protein |
| DE3812605A1 (de) | 1988-04-15 | 1990-06-07 | Leskovar Peter Dipl Ing Dr Hab | Immunregulative stoffe und stoffgemische zur aktiven beeinflussung des krankheitsverlaufes |
| AU3775789A (en) | 1988-06-10 | 1990-01-05 | Applied Biotechnology, Inc. | A method of evaluating recombinant vaccines against immunodeficiency virus |
| US5747324A (en) | 1988-06-10 | 1998-05-05 | Therion Biologics Corporation | Self-assembled, defective, non-self-propagating lentivirus particles |
| US5614404A (en) | 1988-06-10 | 1997-03-25 | Theriod Biologics, Incorporated | Self-assembled, defective, non-self-propagating lentivirus particles |
| US6306625B1 (en) | 1988-12-30 | 2001-10-23 | Smithkline Beecham Biologicals, Sa | Method for obtaining expression of mixed polypeptide particles in yeast |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US6214804B1 (en) | 1989-03-21 | 2001-04-10 | Vical Incorporated | Induction of a protective immune response in a mammal by injecting a DNA sequence |
| GB8923123D0 (en) | 1989-10-13 | 1989-11-29 | Connaught Lab | A vaccine for human immunodeficiency virus |
| JPH05503629A (ja) | 1989-11-20 | 1993-06-17 | オンコーゲン リミテッド パートナーシップ | 抗ウィルス剤及び免疫原として使用される、非複製組換え製レトロウィルス粒子 |
| KR100242671B1 (ko) | 1991-03-07 | 2000-03-02 | 고돈 에릭 | 유전학적으로 처리한 백신 균주 |
| US5863542A (en) | 1991-03-07 | 1999-01-26 | Virogenetics Corporation | Recombinant attenuated ALVAC canaryopox virus containing heterologous HIV or SIV inserts |
| US5445953A (en) | 1991-08-26 | 1995-08-29 | Immuno Aktiengesellschaft | Direct molecular cloning of a modified poxvirus genome |
| DE69229390T2 (de) | 1991-08-26 | 1999-11-11 | Immuno Ag, Wien | Direkt molekuläre Klonierung eines modifizierten Genoms eines Chordopocken-Virus |
| EP0538496B1 (en) | 1991-08-26 | 2003-10-29 | Baxter Healthcare S.A. | Recombinant fowlpox virus with intact FPV-tk-gene |
| US5643578A (en) | 1992-03-23 | 1997-07-01 | University Of Massachusetts Medical Center | Immunization by inoculation of DNA transcription unit |
| US5593972A (en) | 1993-01-26 | 1997-01-14 | The Wistar Institute | Genetic immunization |
| US6171596B1 (en) | 1993-12-10 | 2001-01-09 | The United States Of America As Represented By The Department Of Health And Human Services | Oligomeric HIV-1 envelope glycoproteins |
| US5658785A (en) | 1994-06-06 | 1997-08-19 | Children's Hospital, Inc. | Adeno-associated virus materials and methods |
| US5955342A (en) | 1994-08-15 | 1999-09-21 | Connaught Laboratories Limited | Non-infectious, replication-defective, self-assembling HIV-1 viral particles containing antigenic markers in the gag coding region |
| US6291157B1 (en) | 1998-02-23 | 2001-09-18 | Connaught Laboratories Limited | Antigenically-marked non-infectious retrovirus-like particles |
| US6080408A (en) | 1994-08-22 | 2000-06-27 | Connaught Laboratories Limited | Human immunodeficiency virus type 1 nucleic acids devoid of long terminal repeats capable of encoding for non-infectious, immunogenic, retrovirus-like particles |
| US5676950A (en) | 1994-10-28 | 1997-10-14 | University Of Florida | Enterically administered recombinant poxvirus vaccines |
| DE69527089T2 (de) | 1995-04-19 | 2003-01-02 | Polymun Scientific Immunbiologische Forschung Gmbh, Wien | Monoklonale antikörper gegen hiv-1 und davon hergestellte impfstoffe |
| US5741492A (en) | 1996-01-23 | 1998-04-21 | St. Jude Children's Research Hospital | Preparation and use of viral vectors for mixed envelope protein vaccines against human immunodeficiency viruses |
| FR2747046B1 (fr) | 1996-04-05 | 1998-06-19 | Univ Paris Curie | Nouveaux vaccins issus de plasmovirus |
| US5846946A (en) | 1996-06-14 | 1998-12-08 | Pasteur Merieux Serums Et Vaccins | Compositions and methods for administering Borrelia DNA |
| US5747338A (en) | 1996-08-15 | 1998-05-05 | Chiron Corporation | Method and construct for screening for inhibitors of transcriptional activation |
| US6201663B1 (en) * | 1996-09-05 | 2001-03-13 | Kabushiki Kaisha Ohara | Magnetic head having a slider made of a glass-ceramic |
| US6204250B1 (en) | 1996-11-22 | 2001-03-20 | The Mount Sinai Medical Center Of The City Of New York | Immunization of infants |
| US6077662A (en) | 1996-11-27 | 2000-06-20 | Emory University | Virus-like particles, methods and immunogenic compositions |
| US6099847A (en) | 1997-05-15 | 2000-08-08 | The United States Of America As Represented By The Department Of Health And Human Services | Chimeric Gag pseudovirions |
| GB9711957D0 (en) * | 1997-06-09 | 1997-08-06 | Isis Innovation | Methods and reagents for vaccination |
| DE19726167B4 (de) | 1997-06-20 | 2008-01-24 | Sanofi-Aventis Deutschland Gmbh | Insulin, Verfahren zu seiner Herstellung und es enthaltende pharmazeutische Zubereitung |
| US6054312A (en) | 1997-08-29 | 2000-04-25 | Selective Genetics, Inc. | Receptor-mediated gene delivery using bacteriophage vectors |
| US6121021A (en) | 1997-12-16 | 2000-09-19 | Connaught Laboratories Limited | Constitutive expression of non-infectious HIV-like particles |
| US6156952A (en) | 1998-04-09 | 2000-12-05 | Constituent Institution Of The University Of Maryland System | HIV transgenic animals and uses therefor |
| AUPP349698A0 (en) | 1998-05-13 | 1998-06-04 | Altronic Distributors Pty Ltd | Mounting assembly |
| GB2337755B (en) | 1998-05-29 | 2003-10-29 | Secr Defence | Virus vaccine |
| AU5036899A (en) | 1998-06-26 | 2000-01-17 | Aventis Pasteur | Use of poxviruses as enhancer of specific immunity |
| US7935805B1 (en) * | 1998-12-31 | 2011-05-03 | Novartis Vaccines & Diagnostics, Inc | Polynucleotides encoding antigenic HIV Type C polypeptides, polypeptides and uses thereof |
| WO2001002607A1 (en) | 1999-07-06 | 2001-01-11 | Merck & Co., Inc. | Adenovirus carrying gag gene hiv vaccine |
| MXPA02006379A (es) | 1999-12-23 | 2004-06-21 | Medical Res Council | Mejoriasen o relacionadas con la respuesta inmune a vih. |
| AUPQ520800A0 (en) | 2000-01-21 | 2000-02-17 | Alfred Hospital | Prime-boost vaccination strategy |
| US8623379B2 (en) * | 2000-03-02 | 2014-01-07 | Emory University | Compositions and methods for generating an immune response |
| ES2282251T3 (es) | 2000-04-27 | 2007-10-16 | Sanofi Pasteur Limited | Vacunas contra la infeccion por vih. |
| KR100542336B1 (ko) | 2000-07-17 | 2006-01-11 | 산요덴키가부시키가이샤 | 반도체 레이저장치 |
| DK1372710T3 (da) | 2001-03-08 | 2010-01-18 | Us Gov Health & Human Serv | MVA der udtrykker modificeret HIV-kappe-, Gag- og Pol-gener |
| AU2003224644A1 (en) | 2002-02-27 | 2003-09-09 | The Government Of The United States Of America, Represented By The Secretary, Department Of Healtan | Conjugates of ligand, linker and cytotoxic agent and related compositions and methods of use |
-
2003
- 2003-01-03 US US10/336,566 patent/US8623379B2/en not_active Expired - Lifetime
- 2003-03-10 EP EP03716404A patent/EP1483385A4/en not_active Ceased
- 2003-03-10 WO PCT/US2003/007177 patent/WO2003076591A2/en active Application Filing
- 2003-03-10 EP EP10184784.6A patent/EP2368985B1/en not_active Expired - Lifetime
- 2003-03-10 JP JP2003574798A patent/JP2005531513A/ja not_active Withdrawn
- 2003-03-10 CA CA2478371A patent/CA2478371C/en not_active Expired - Lifetime
- 2003-03-10 CN CNA038104512A patent/CN1653176A/zh active Pending
-
2008
- 2008-10-31 AU AU2008243079A patent/AU2008243079A1/en not_active Abandoned
-
2011
- 2011-05-20 JP JP2011113185A patent/JP2011231112A/ja active Pending
-
2013
- 2013-12-20 US US14/137,095 patent/US9254319B2/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001092470A2 (en) * | 2000-03-02 | 2001-12-06 | Emory University | Dna expression vectors and methods of use |
| WO2003004657A1 (en) * | 2001-07-05 | 2003-01-16 | Chiron Corporation | Polynucleotides encoding antigenic hiv type b and/or type c polypeptides, polypeptides and uses thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| US20030175292A1 (en) | 2003-09-18 |
| WO2003076591A8 (en) | 2004-11-18 |
| EP1483385A4 (en) | 2005-08-24 |
| US20150004132A1 (en) | 2015-01-01 |
| CA2478371C (en) | 2013-12-31 |
| EP2368985B1 (en) | 2019-01-16 |
| CN1653176A (zh) | 2005-08-10 |
| WO2003076591A3 (en) | 2004-03-25 |
| EP2368985A2 (en) | 2011-09-28 |
| US9254319B2 (en) | 2016-02-09 |
| EP2368985A3 (en) | 2012-05-30 |
| CA2478371A1 (en) | 2003-09-18 |
| JP2011231112A (ja) | 2011-11-17 |
| US8623379B2 (en) | 2014-01-07 |
| AU2008243079A1 (en) | 2008-11-27 |
| EP1483385A2 (en) | 2004-12-08 |
| WO2003076591A2 (en) | 2003-09-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9254319B2 (en) | Compositions and methods for generating an immune response | |
| JP4554887B2 (ja) | 改変HIVエンベロープ、gag、およびpol遺伝子を発現するMVA | |
| US20200071724A1 (en) | Intergenic Sites Between Conserved Genes in the Genome of Modified Vaccinia Ankara (MVA) Vaccinia Virus | |
| US20130078276A1 (en) | Vectors expressing hiv antigens and gm-csf and related methods of generating an immune response | |
| JP5178196B2 (ja) | クレードA/G、クレードB、およびクレードC改変HIVenv、gag、およびpol遺伝子を発現する組換えMVAウイルス | |
| EP1610816B1 (en) | Mva virus expressing modified hiv envelope, gag, and pol genes | |
| JP5789263B2 (ja) | 再構築された挿入部位を含有する組換え改変ワクシニアアンカラ(mva)ワクシニアウイルス | |
| AU2002252199A1 (en) | MVA expressing modified HIV envelope, GAG, and POL genes | |
| Coupar et al. | Fowlpox virus vaccines for HIV and SHIV clinical and pre-clinical trials | |
| US20090227658A1 (en) | Methods and compositions for immunization against hiv | |
| US20090142373A1 (en) | Immunizing Against HIV Infection | |
| AU2003220111B2 (en) | Compositions and methods for generating an immune response | |
| Singh et al. | HIV vaccine development | |
| Part | Nonhuman Primates HIV/SIV Vaccine Trials Database | |
| Smith | Design and immunogenicity of a DNA vaccine against primate lentiviruses |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050907 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20050912 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20050907 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20050912 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060309 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060309 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20060310 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090602 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20090901 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20090908 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091202 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110104 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110120 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110520 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110601 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110701 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110801 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110817 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110913 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20111125 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130205 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130208 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20130430 |