JP2005515224A - テンプレート乳剤からの薬剤ナノ粒子 - Google Patents
テンプレート乳剤からの薬剤ナノ粒子 Download PDFInfo
- Publication number
- JP2005515224A JP2005515224A JP2003559482A JP2003559482A JP2005515224A JP 2005515224 A JP2005515224 A JP 2005515224A JP 2003559482 A JP2003559482 A JP 2003559482A JP 2003559482 A JP2003559482 A JP 2003559482A JP 2005515224 A JP2005515224 A JP 2005515224A
- Authority
- JP
- Japan
- Prior art keywords
- drug
- template
- solvent
- emulsion
- template emulsion
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003814 drug Substances 0.000 title claims abstract description 94
- 229940079593 drug Drugs 0.000 title claims abstract description 92
- 239000000839 emulsion Substances 0.000 title claims abstract description 80
- 239000002105 nanoparticle Substances 0.000 title 1
- 239000002245 particle Substances 0.000 claims abstract description 73
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 37
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 28
- 239000000203 mixture Substances 0.000 claims abstract description 28
- 238000000034 method Methods 0.000 claims abstract description 27
- 229940088679 drug related substance Drugs 0.000 claims abstract description 19
- 239000008186 active pharmaceutical agent Substances 0.000 claims abstract description 17
- 238000004519 manufacturing process Methods 0.000 claims abstract 2
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 36
- 239000002904 solvent Substances 0.000 claims description 31
- -1 glycol derivative ester Chemical class 0.000 claims description 20
- 239000003381 stabilizer Substances 0.000 claims description 19
- 239000004094 surface-active agent Substances 0.000 claims description 10
- 235000015112 vegetable and seed oil Nutrition 0.000 claims description 8
- 239000008158 vegetable oil Substances 0.000 claims description 8
- 235000012343 cottonseed oil Nutrition 0.000 claims description 7
- 239000002385 cottonseed oil Substances 0.000 claims description 7
- 229920000642 polymer Polymers 0.000 claims description 7
- 150000001335 aliphatic alkanes Chemical group 0.000 claims description 6
- 125000001931 aliphatic group Chemical class 0.000 claims description 5
- 235000014113 dietary fatty acids Nutrition 0.000 claims description 5
- 239000000194 fatty acid Substances 0.000 claims description 5
- 229930195729 fatty acid Natural products 0.000 claims description 5
- 150000004665 fatty acids Chemical class 0.000 claims description 5
- 229920001577 copolymer Polymers 0.000 claims description 4
- 229920001519 homopolymer Polymers 0.000 claims description 4
- 239000002480 mineral oil Chemical class 0.000 claims description 4
- 239000004006 olive oil Substances 0.000 claims description 4
- 235000008390 olive oil Nutrition 0.000 claims description 4
- 239000003549 soybean oil Substances 0.000 claims description 4
- 235000012424 soybean oil Nutrition 0.000 claims description 4
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 claims description 3
- 150000004996 alkyl benzenes Chemical group 0.000 claims description 3
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 3
- 150000008365 aromatic ketones Chemical class 0.000 claims description 3
- 150000008378 aryl ethers Chemical class 0.000 claims description 3
- 125000003118 aryl group Chemical class 0.000 claims description 3
- 150000002576 ketones Chemical class 0.000 claims description 3
- 235000010446 mineral oil Nutrition 0.000 claims description 3
- 238000004090 dissolution Methods 0.000 abstract description 12
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- POZRVZJJTULAOH-LHZXLZLDSA-N danazol Chemical compound C1[C@]2(C)[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=CC2=C1C=NO2 POZRVZJJTULAOH-LHZXLZLDSA-N 0.000 description 14
- 229960000766 danazol Drugs 0.000 description 14
- 239000012071 phase Substances 0.000 description 13
- 238000002156 mixing Methods 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 8
- 238000013019 agitation Methods 0.000 description 7
- 238000000149 argon plasma sintering Methods 0.000 description 7
- 238000001704 evaporation Methods 0.000 description 7
- 230000008020 evaporation Effects 0.000 description 7
- 239000008346 aqueous phase Substances 0.000 description 6
- 238000004108 freeze drying Methods 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 235000019198 oils Nutrition 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 238000009826 distribution Methods 0.000 description 5
- 239000003960 organic solvent Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 238000010521 absorption reaction Methods 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- GJRQTCIYDGXPES-UHFFFAOYSA-N iso-butyl acetate Natural products CC(C)COC(C)=O GJRQTCIYDGXPES-UHFFFAOYSA-N 0.000 description 4
- FGKJLKRYENPLQH-UHFFFAOYSA-M isocaproate Chemical compound CC(C)CCC([O-])=O FGKJLKRYENPLQH-UHFFFAOYSA-M 0.000 description 4
- OQAGVSWESNCJJT-UHFFFAOYSA-N isovaleric acid methyl ester Natural products COC(=O)CC(C)C OQAGVSWESNCJJT-UHFFFAOYSA-N 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 229920002451 polyvinyl alcohol Polymers 0.000 description 4
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 4
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 4
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 229930105110 Cyclosporin A Natural products 0.000 description 3
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 3
- 108010036949 Cyclosporine Proteins 0.000 description 3
- 239000004372 Polyvinyl alcohol Substances 0.000 description 3
- 230000036765 blood level Effects 0.000 description 3
- 229960001265 ciclosporin Drugs 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- QYDYPVFESGNLHU-UHFFFAOYSA-N elaidic acid methyl ester Natural products CCCCCCCCC=CCCCCCCCC(=O)OC QYDYPVFESGNLHU-UHFFFAOYSA-N 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- QYDYPVFESGNLHU-KHPPLWFESA-N methyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC QYDYPVFESGNLHU-KHPPLWFESA-N 0.000 description 3
- 229940073769 methyl oleate Drugs 0.000 description 3
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 3
- 239000008194 pharmaceutical composition Substances 0.000 description 3
- 239000000825 pharmaceutical preparation Substances 0.000 description 3
- 229940127557 pharmaceutical product Drugs 0.000 description 3
- 238000001238 wet grinding Methods 0.000 description 3
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 2
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 2
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 2
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 2
- 101000807541 Homo sapiens Ubiquitin carboxyl-terminal hydrolase 24 Proteins 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- 239000005642 Oleic acid Substances 0.000 description 2
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 102100037176 Ubiquitin carboxyl-terminal hydrolase 24 Human genes 0.000 description 2
- 238000002441 X-ray diffraction Methods 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- 238000004220 aggregation Methods 0.000 description 2
- 125000005907 alkyl ester group Chemical group 0.000 description 2
- 239000003945 anionic surfactant Substances 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 239000003093 cationic surfactant Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 239000008367 deionised water Substances 0.000 description 2
- 229910021641 deionized water Inorganic materials 0.000 description 2
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- DCAYPVUWAIABOU-UHFFFAOYSA-N hexadecane Chemical compound CCCCCCCCCCCCCCCC DCAYPVUWAIABOU-UHFFFAOYSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 2
- HJOVHMDZYOCNQW-UHFFFAOYSA-N isophorone Chemical compound CC1=CC(=O)CC(C)(C)C1 HJOVHMDZYOCNQW-UHFFFAOYSA-N 0.000 description 2
- 229960004125 ketoconazole Drugs 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- HYIMSNHJOBLJNT-UHFFFAOYSA-N nifedipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1[N+]([O-])=O HYIMSNHJOBLJNT-UHFFFAOYSA-N 0.000 description 2
- 229960001597 nifedipine Drugs 0.000 description 2
- 239000002736 nonionic surfactant Substances 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 2
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 2
- 238000003921 particle size analysis Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 238000000634 powder X-ray diffraction Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- ODLMAHJVESYWTB-UHFFFAOYSA-N propylbenzene Chemical compound CCCC1=CC=CC=C1 ODLMAHJVESYWTB-UHFFFAOYSA-N 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- UOCLXMDMGBRAIB-UHFFFAOYSA-N 1,1,1-trichloroethane Chemical compound CC(Cl)(Cl)Cl UOCLXMDMGBRAIB-UHFFFAOYSA-N 0.000 description 1
- XPZBNIUWMDJFPW-UHFFFAOYSA-N 2,2,3-trimethylcyclohexan-1-one Chemical compound CC1CCCC(=O)C1(C)C XPZBNIUWMDJFPW-UHFFFAOYSA-N 0.000 description 1
- LRFVTYWOQMYALW-UHFFFAOYSA-N 9H-xanthine Chemical class O=C1NC(=O)NC2=C1NC=N2 LRFVTYWOQMYALW-UHFFFAOYSA-N 0.000 description 1
- 102000055006 Calcitonin Human genes 0.000 description 1
- 108060001064 Calcitonin Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical class CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 244000043261 Hevea brasiliensis Species 0.000 description 1
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- NWGKJDSIEKMTRX-AAZCQSIUSA-N Sorbitan monooleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O NWGKJDSIEKMTRX-AAZCQSIUSA-N 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- ULUAUXLGCMPNKK-UHFFFAOYSA-N Sulfobutanedioic acid Chemical compound OC(=O)CC(C(O)=O)S(O)(=O)=O ULUAUXLGCMPNKK-UHFFFAOYSA-N 0.000 description 1
- BAECOWNUKCLBPZ-HIUWNOOHSA-N Triolein Natural products O([C@H](OCC(=O)CCCCCCC/C=C\CCCCCCCC)COC(=O)CCCCCCC/C=C\CCCCCCCC)C(=O)CCCCCCC/C=C\CCCCCCCC BAECOWNUKCLBPZ-HIUWNOOHSA-N 0.000 description 1
- PHYFQTYBJUILEZ-UHFFFAOYSA-N Trioleoylglycerol Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC(OC(=O)CCCCCCCC=CCCCCCCCC)COC(=O)CCCCCCCC=CCCCCCCCC PHYFQTYBJUILEZ-UHFFFAOYSA-N 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- ZCZSIDMEHXZRLG-UHFFFAOYSA-N acetic acid heptyl ester Natural products CCCCCCCOC(C)=O ZCZSIDMEHXZRLG-UHFFFAOYSA-N 0.000 description 1
- TUVYSBJZBYRDHP-UHFFFAOYSA-N acetic acid;methoxymethane Chemical compound COC.CC(O)=O TUVYSBJZBYRDHP-UHFFFAOYSA-N 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 239000002280 amphoteric surfactant Substances 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 230000000507 anthelmentic effect Effects 0.000 description 1
- 230000000049 anti-anxiety effect Effects 0.000 description 1
- 229940127003 anti-diabetic drug Drugs 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000000648 anti-parkinson Effects 0.000 description 1
- 230000003208 anti-thyroid effect Effects 0.000 description 1
- 239000000043 antiallergic agent Substances 0.000 description 1
- 239000003416 antiarrhythmic agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 239000001961 anticonvulsive agent Substances 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 229940030225 antihemorrhagics Drugs 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 239000000939 antiparkinson agent Substances 0.000 description 1
- 229940043671 antithyroid preparations Drugs 0.000 description 1
- 239000003434 antitussive agent Substances 0.000 description 1
- 229940124584 antitussives Drugs 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 239000002830 appetite depressant Substances 0.000 description 1
- 239000003212 astringent agent Substances 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000010836 blood and blood product Substances 0.000 description 1
- 229940125691 blood product Drugs 0.000 description 1
- 239000003633 blood substitute Substances 0.000 description 1
- GPPUEZVQNPTXQZ-UHFFFAOYSA-N butanoic acid;octanoic acid Chemical compound CCCC(O)=O.CCCCCCCC(O)=O GPPUEZVQNPTXQZ-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 description 1
- 229960004015 calcitonin Drugs 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- 239000007859 condensation product Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 239000002872 contrast media Substances 0.000 description 1
- 229940039231 contrast media Drugs 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000000032 diagnostic agent Substances 0.000 description 1
- 229940039227 diagnostic agent Drugs 0.000 description 1
- 238000002059 diagnostic imaging Methods 0.000 description 1
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 230000001882 diuretic effect Effects 0.000 description 1
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 1
- 229960003638 dopamine Drugs 0.000 description 1
- 239000013583 drug formulation Substances 0.000 description 1
- 239000003684 drug solvent Substances 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000003172 expectorant agent Substances 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 239000003163 gonadal steroid hormone Substances 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 230000000025 haemostatic effect Effects 0.000 description 1
- JPXGPRBLTIYFQG-UHFFFAOYSA-N heptan-4-yl acetate Chemical compound CCCC(CCC)OC(C)=O JPXGPRBLTIYFQG-UHFFFAOYSA-N 0.000 description 1
- AOGQPLXWSUTHQB-UHFFFAOYSA-N hexyl acetic acid ester Natural products CCCCCCOC(C)=O AOGQPLXWSUTHQB-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000000265 homogenisation Methods 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 239000003326 hypnotic agent Substances 0.000 description 1
- 230000000147 hypnotic effect Effects 0.000 description 1
- 239000012216 imaging agent Substances 0.000 description 1
- 239000000677 immunologic agent Substances 0.000 description 1
- 229940124541 immunological agent Drugs 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- JTEDVYBZBROSJT-UHFFFAOYSA-N indole-3-butyric acid Chemical compound C1=CC=C2C(CCCC(=O)O)=CNC2=C1 JTEDVYBZBROSJT-UHFFFAOYSA-N 0.000 description 1
- 229940070765 laurate Drugs 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- FJQXCDYVZAHXNS-UHFFFAOYSA-N methadone hydrochloride Chemical compound Cl.C=1C=CC=CC=1C(CC(C)N(C)C)(C(=O)CC)C1=CC=CC=C1 FJQXCDYVZAHXNS-UHFFFAOYSA-N 0.000 description 1
- 230000000510 mucolytic effect Effects 0.000 description 1
- 229940066491 mucolytics Drugs 0.000 description 1
- 239000003149 muscarinic antagonist Substances 0.000 description 1
- 239000003158 myorelaxant agent Substances 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229960002009 naproxen Drugs 0.000 description 1
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 1
- 229920003052 natural elastomer Polymers 0.000 description 1
- 229920001194 natural rubber Polymers 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 239000000734 parasympathomimetic agent Substances 0.000 description 1
- 238000010951 particle size reduction Methods 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 239000003090 pesticide formulation Substances 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000006069 physical mixture Substances 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229920001992 poloxamer 407 Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920001521 polyalkylene glycol ether Polymers 0.000 description 1
- 229920002857 polybutadiene Polymers 0.000 description 1
- 229920001083 polybutene Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000151 polyglycol Polymers 0.000 description 1
- 239000010695 polyglycol Substances 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 229920001289 polyvinyl ether Polymers 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 1
- 239000012217 radiopharmaceutical Substances 0.000 description 1
- 229940121896 radiopharmaceutical Drugs 0.000 description 1
- 230000002799 radiopharmaceutical effect Effects 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000005070 ripening Effects 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229940125723 sedative agent Drugs 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000007962 solid dispersion Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 230000002889 sympathetic effect Effects 0.000 description 1
- 229940065721 systemic for obstructive airway disease xanthines Drugs 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 229940043672 thyroid preparations Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- PHYFQTYBJUILEZ-IUPFWZBJSA-N triolein Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(OC(=O)CCCCCCC\C=C/CCCCCCCC)COC(=O)CCCCCCC\C=C/CCCCCCCC PHYFQTYBJUILEZ-IUPFWZBJSA-N 0.000 description 1
- 229940117972 triolein Drugs 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
Landscapes
- Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
水及びテンプレート剤を含むテンプレート乳剤を調製し;薬剤物質を含む薬剤含有混合物を調製し;次いでテンプレート乳剤を薬剤含有混合物と合わせて、薬剤粒子が配合されたテンプレート乳剤を形成することを含む、ミクロンサイズ又はサブミクロンサイズの薬剤の製造方法。本方法により調製した薬剤粒子も開示されている。得られた薬剤粒子は、非処理薬剤粒子及び他の方法を用いて調製した粒子と比較して、溶解速度がより速く、バイオアベイラビリティも高いことが実証された。
Description
本発明は、水性乳剤の調製、特に水溶性が低い医薬製品又は薬剤を含有する水性乳剤の調製に関する。
バイオアベイラビリティ(生物学的利用能)が高く、短時間で溶解することは、最終医薬製品の望ましい特性である。バイオアベイラビリティとは、医薬製品又は薬剤が、体に投与された後、ターゲット(標的)組織に利用されるようになる度合いを意味する用語である。バイオアベイラビリティが乏しいことは、医薬組成物、特に水溶性が低い活性成分を含有する医薬組成物の開発において、重大な課題である。例えば、口径投与では、低水溶性薬剤は、循環系に吸収される前に胃腸路から排除される傾向がある。
粒状薬剤の溶解速度は、表面積の増加、すなわち粒径(粒度)の減少につれ、増加することがあることが知られている。その結果、医薬組成物中の薬剤粒子のサイズ及びその範囲を制御するための努力が払われてきた。例えば、米国特許5,145,684号に記載されているように、湿式粉砕技法が用いられてきた。しかしながら、このような湿式粉砕技法には、粉砕媒体からの汚染に伴う課題がある。更に、薬剤を過度の機械的せん断力又は過度の高温に曝すことは、活性化合物が分解されるために、又は再結晶工程、すなわち、少なくとも一部が結晶状態から非結晶状態へと異なる結晶多形体もしくは変形体が形成されるために、薬剤が変化したり又はその活性を失う原因となりうる。このことは、Florence等のEffect of Particle Size Reduction on Digoxin Crystal Properties,Journal of Pharmaceutics and Pharmacology,Vol.26,No.6,479−480(1974年)及びR.Suryanarayanan及びA.G.MitchellのEvaluation of Two Concepts of Crystallinity Using Calcium Gluceptate as a Model Compound, International Journal of Pharmaceutics, Vol.24,1−17(1985年)に記載されている。加えて、湿式粉砕技法によれば、より大きい粒子が一部に常に存在する結果となり、粒子の完全溶解に要する時間に影響を与える。
米国特許第6,017,559号及び第6,074,986号は、農薬配合物の粒径を制御するためにテンプレート剤の使用を教示している。しかしながら、’559特許も’986特許も、薬剤物質のバイオアベイラビリティに関心を示していない。
ミクロン又はサブミクロン粒径範囲内の安定な医薬組成物であって、バイオアベイラビリティが向上し、しかも前記の従来技術に伴う課題を有しないものが提供されれば有利であろう。
第一態様において、本発明は、水及びテンプレート(鋳型)剤を含むテンプレート乳剤を調製し;薬剤物質を含む薬剤含有混合物を調製し;次いで前記テンプレート乳剤を前記薬剤含有混合物と合わせて、薬剤粒子が配合されたテンプレート乳剤を形成することを含む、ミクロンサイズ又はサブミクロンサイズの薬剤を製造する方法である。
この薬剤粒子配合テンプレート乳剤は、そのまま使用しても、又は薬剤物質の固体分散体が望ましい場合は溶剤をテンプレート乳剤から除去してもよい。
第二態様において、本発明は、水及びテンプレート剤を含むテンプレート乳剤を調製し;薬剤物質を含む薬剤含有混合物を調製し;次いでテンプレート乳剤を薬剤含有混合物と合わせて、テンプレート乳剤中に薬剤粒子を形成することを含む方法により製造された薬剤粒子である。
本発明は、いくつかの利点を有する。本発明は、小液滴を形成するために必要な高温及び機械的応力、すなわち、高いせん断力を、テンプレート乳剤のみに与え、薬剤含有混合物には与えないことにより、薬剤物質の生物活性を損う可能性を低減する。更に、テンプレート乳剤を形成するのに要するもの以外の更なる乳化剤を要しないので、最終薬剤配合物中に存在する賦形剤のレベルを低下させる。加えて、テンプレート剤を使用すると、得られる薬剤粒子の粒径及び粒径分布の制御が向上する。
本発明に使用するテンプレート乳剤とは、連続水相及び不連続相を含む安定な二相分散体であり、この不連続相は、非水性物質及び前記非水性物質の水相への移動を抑制することによりテンプレート乳剤の粒子成長を、例えば、オズワルト熟成により低減又は防止するのに十分な量の安定剤(この安定剤は不連続相には溶解するが、水相には溶解しない)を含むものであると定義する。
本発明のミクロンサイズ又はサブミクロンサイズの薬剤粒子を製造するために用いるテンプレート乳剤は、乳剤調製の技術分野で周知の技法を用いて調製し、テンプレート剤及び水を0.5〜50、好ましくは2〜20、最も好ましくは5〜10重量%含む。
テンプレート乳剤液滴が適切な大きさを有することが重要である。薬剤含有混合物をテンプレート乳剤と合わせる際、薬剤物質及び溶剤がテンプレート剤液滴中に移動し、液滴サイズを一定の予想可能な量増加させるであろう。このように、テンプレート乳剤中のテンプレート剤の液滴サイズが、得られる薬剤粒子の粒子成長の境界を設定することにより、得られる薬剤粒子のサイズを決定する。
本方法によれば、テンプレート乳剤中のテンプレート剤の液滴サイズ分布を適切に制御することにより、テンプレート乳剤中に得られる薬剤粒子のサイズ分布を制御できる。得られた水性乳剤の粒子サイズ分布曲線の形状は、使用したテンプレート剤の粒径分布曲線の形状を厳密に反映する。
テンプレート乳剤中のテンプレート剤にとって適切な液滴サイズを形成するために、ある種の攪拌を用いることが好ましい。使用する攪拌タイプは、限定的ではないが、テンプレート乳剤中のテンプレート剤にとって適切な液滴サイズが達成される限り、乳剤製造に用いる任意の従来タイプの攪拌を使用できる。適切な攪拌手段の例としては、攪拌、均質化及びマイクロ流動化装置、マイクロ混合機等の使用が挙げられる。
好ましくは、テンプレート剤は、水溶性が低い液体又はオイルである。テンプレート剤の好適例としては、アルキル置換ベンゼン、例えば、トルエン、キシレン又はプロピルベンゼン留分、及び混合ナフタレン及びアルキルナフタレン留分;鉱油;トリグリセリド油、例えば、綿実油、オリーブ油、大豆油及び植物油;水和植物油;脂肪酸のジアルキルアミド、特に脂肪酸のジメチルアミド;塩素化脂肪族及び芳香族炭化水素、例えば、1,1,1−トリクロロエタン及びクロロベンゼン;グリコール誘導体のエステル、例えば、ジエチレングリコールのn−ブチル、エチル、又はメチルエーテルのアセテート;ケトン、例えば、イソホロン及びトリメチルシクロヘキサノン;並びにアルキルアセテート、例えば、ヘキシル又はヘプチルアセテートが挙げられる。好ましいテンプレート剤は、安全と一般に見做されてFDAにより列挙されている(GRAS)か、又は標準操作により容易に除去可能なもの、すなわち、綿実油、オリーブ油、大豆油及び植物油;鉱油;アルキルアセテート;及びトルエンである。
好ましい態様において、テンプレート乳剤は、更に少なくとも1種の安定剤を含む。安定剤はいくつかの機能を有する。安定剤は、非水性物質の水相中の移動を抑制する乳化剤として作用することにより、テンプレート乳剤の液滴成長を低減又は防止することにより、テンプレート乳剤を安定化する。安定剤はまた、薬剤粒子の結晶成長、凝結及び凝集も抑制する。安定剤の好適例は、ポリマー、ホモポリマー又はコ−ポリマー、例えば、“Polymer Handbook”第3版、J.Brandrup及びE.H.Immergut編に記載のものである。好適なホモポリマー及びコ−ポリマーとしては、ポリオレフィン及び置換ポリオレフィン、例えば、ポリエチレン、ポリプロピレン、ポリブテン、ポリブタジエン、及びそれらの塩素化誘導体;ポリアクリレート及びポリメタクリレート;ポリ二置換エステル;ポリビニルエーテル、塩化物、アセテート、及びカルボキシレートエステル、例えば、ポリビニルブチレートカプリレート、ラウレート、ステアレート、ベンゾエート;ポリスチレン;天然ゴム及び塩化水素化ゴム;エチル、ブチル及びベンジルセルロース;セルロースエステル;並びにこれらのポリマーの組み合わせが挙げられる。他の適切なポリマーは、界面活性剤としても機能でき、しかも連続水相に不溶性であるポリマー、例えば、ノニオン性ポリアルキレングリコール/(ポリ)カルボン酸化合物;A−B−Aブロックタイプ界面活性剤;天然植物油の高分子量エステル、例えば、ステアリン酸及びオレイン酸のアルキルエステルである。ポリマーに加えて、極めて疎水性の小分子、すなわち、ヘキサデカンもまた同様に使用できる。好ましい安定剤は、GRAS−リストの一部、すなわち、ステアリン酸及びオレイン酸のアルキルエステルである。分子量又は架橋度に依存して、安定剤は液体もしくはオイルの物理的状態であることができるし、又は固体であることもできる。一般に、安定剤又は安定剤混合物の組成は、専ら分散相と相互反応するが、連続相とは相互反応しないというニーズに依存するであろう。安定剤は、分散相の0.1〜90、好ましくは0.5〜50重量%使用してよい。
一態様において、安定剤は界面活性剤である。本発明において有利に使用可能な界面活性剤は、当業者により容易に決定でき、各種のノニオン、アニオン、カチオン及び両性界面活性剤、又はこれら界面活性剤の配合物が挙げられる。好ましい界面活性剤は、不連続相のオイル液滴が凝集する傾向を有意に低減するものである。ノニオン界面活性剤の例としては、ポリアルキレングリコールエーテル及び脂肪族アルコール、脂肪族アミン又は脂肪酸とエチレンオキシド又はプロピレンオキシドとの縮合生成物;異なる分子量及び加水分解度のポリビニルアルコール;ポリビニルピロリドン;並びにBrij、Tween及びSpanシリーズの界面活性剤が挙げられる。アニオン界面活性剤としては、アルキルアリールスルホン酸の塩、硫酸化ポリグリコールエーテル、及びスルホコハク酸のエーテルが挙げられる。カチオン界面活性剤としては、第四アンモニウム化合物及び脂肪アミンが挙げられる。界面活性剤は一般に総組成物の0.1〜15、更に好ましくは2〜10、最も好ましくは約5重量%使用する。
テンプレート乳剤を、薬剤溶液又は粗薬剤乳剤であると本明細書で定義されている薬剤含有混合物と合わせる。薬剤溶液は、薬剤物質と水非混和性溶剤を含み、一方、粗薬剤乳剤は薬剤物質、水非混和性溶剤及び水を含む。
テンプレート乳剤と薬剤含有混合物の混合は、好ましくは周囲温度〜70℃、更に好ましくは、周囲温度〜50℃、最も好ましくは周囲温度で行う。適切な選択温度は、調製に使用された材料の溶融点及び薬剤の温度安定性に依存するであろう。テンプレート乳剤及び薬剤含有混合物は、液流混合の技術分野で知られている任意の技法を用いて合わせることができる。この工程は、薬剤物質のテンプレート液滴中への配合を成功させるのに攪拌を必須とはしないが、ある種の攪拌を適用すれば好ましい。使用されるタイプの攪拌は限定的ではなく、従来タイプの攪拌を用いることができる。薬剤物質は、一般に薬剤をテンプレート液滴に配合させるために用いた薬剤含有混合物の1〜50、更に好ましくは15〜30重量%用いる。適切な薬剤対溶剤の比率は、選択した溶剤への薬剤の溶解度に主に依存する。
好ましくは、薬剤物質は実質的に純粋形である。薬剤物質は、水への溶解性が低く、0.1〜10重量%の範囲の溶解度を有し、少なくとも1種の液体媒体中に分散可能であることが好ましい。好ましい薬剤物質としては、口径投与用の薬剤が挙げられ、例えば、鎮痛薬、抗炎症剤、駆虫薬、抗不整脈剤、抗生物質(ペニシリンを含む)、抗凝血薬、抗鬱剤、抗糖尿病薬、抗てんかん病薬、抗ヒスタミン剤、抗高血圧剤、抗ムスカリン剤、抗菌剤、抗腫瘍剤、免疫抑制剤、抗水腫薬(antithyroid)、抗ビールス剤、抗不安鎮静剤(催眠薬及び神経弛緩薬)、収れん薬、β−アドレナリン受容体ブロッキング剤、血液製剤及び代替品、噴門筋変力剤(cardiacinotropic agent)、対比媒体(contrast media)、コルチコステロイド、咳抑止剤(去痰薬及び粘液溶解薬)、診断薬、診断画像形成剤、利尿剤、ドーパミン薬(抗パーキンソン剤)、ハエモスタティックス(haemostatics)、免疫学剤(immuriological agent)、脂質調整剤、筋肉弛緩剤、副交感神経剤、甲状腺カルシトニン及びビホスホネート、プロスタグランジン、放射性薬品、性ホルモン(ステロイドを含む)、抗アレルギー剤、興奮薬及び食欲抑制剤、交感神経剤、甲状腺製剤、血管拡張剤(vasidilators)、及びキサンチンが挙げられる。これらの薬剤群についての記載及び各群内の種のリストは、Martindale、The Extra Pharmacopoeia、第29版、The Pharmaceutical Press、London、1989年に見出すことができ、これらの開示は引用することにより本明細書に取り入れる。
薬剤含有混合物には、少なくとも1種の溶剤を用いて、薬剤含有混合物とテンプレート乳剤を合わせた際、溶剤が薬剤をテンプレート剤中に移動させるように仕向ける。薬剤含有混合物に使用するのに好ましい溶剤は、低水溶性、好ましくは0.01〜2.0重量%の低水溶性、そして低蒸気圧、好ましくは0.5〜500mmHgの低蒸気圧を有しなければならない。好適な溶剤としては、アルカン及び塩素化アルカン、例えば、ジクロロメタン、脂肪族及び芳香族エーテル、脂肪族及び芳香族エステル、例えば、IBA,脂肪族及び芳香族ケトン、芳香族、例えば、トルエン、並びにこれらの組み合わせが挙げられる。
テンプレート乳剤と薬剤含有混合物を一旦合わせれば、薬剤物質はテンプレート剤液滴中に移動し、テンプレート乳剤中に薬剤粒子を形成するであろう。このような薬剤粒子のサイズは、光散乱法を用いて測定した場合、サブミクロンからミクロンの範囲内、0.2〜20、更に好ましくは0.5〜10、最も好ましくは0.5〜5ミクロンである。
好ましい態様において、本発明方法は、溶剤の除去工程を更に含む。標準の蒸発技法を用いて蒸発により大量の溶剤をテンプレート乳剤から除去して、薬剤物質を沈殿又は結晶化させることができる。こうして薬剤粒子のサイズは、テンプレート乳剤液滴のサイズにより制御される。
別の好ましい態様において、本発明方法は、追加の溶剤除去工程、特に水除去工程を含む。最終の溶剤除去は、乾燥の技術分野で知られている任意技法、すなわち、凍結乾燥、噴霧乾燥、定着又は流動化床乾燥、又はフラッシュ乾燥を用いて行うことができ;又は固体薬剤物質粒子を標準の分離技法により水相から単離することができる。
本発明組成物は、場合により賦形剤、例えば、標準の充填剤、バインダー、又は当業者に容易に明らかな崩壊剤を、総組成物の0〜15重量%含んでもよい。
得られた薬剤粒子は、再分散前の粒子と略同一の粒径で、水に再分散可能であることが望ましい。好ましくは、得られる再分散粒径が5ミクロン未満であるように、これらの粒子を水に再分散させる。
得られた薬剤粒子は、再分散前の粒子と略同一の粒径で、水に再分散可能であることが望ましい。好ましくは、得られる再分散粒径が5ミクロン未満であるように、これらの粒子を水に再分散させる。
本発明は、以下の実施例を考察することにより更に明らかになるであろう。但し、これらの実施例は単に本発明の例を示すためのものである。特に断わらない限り、すべての部及び%は重量部及び重量%である。
実施例1
綿実油(2.5g)、ポリビニルピロリドン55kD(7.5g)、メチルオリエート(1.1g)及び水(12.5g)を含むテンプレート乳剤を高せん断混合により調製した。このテンプレート乳剤の一部(4g)を、水(32g)で希釈して、平均直径0.19ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。テンプレート乳剤を、薬剤ダナゾール(danazol)(0.5g)及び溶剤ジクロロメタン(4.5g)を含む溶液と周囲温度で混合した。平均粒子直径は、最初2.4ミクロンまで増加し、そしてテンプレート剤による薬剤溶液の吸収後、次の20時間内に0.35ミクロンまで減少した。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色結晶固体を得た。この白色結晶を水に再分散したところ、最初に平均直径6.5ミクロンの粒子が得られたが、この粒子は2時間以内に分解して、平均直径0.3ミクロンの粒子となった。
綿実油(2.5g)、ポリビニルピロリドン55kD(7.5g)、メチルオリエート(1.1g)及び水(12.5g)を含むテンプレート乳剤を高せん断混合により調製した。このテンプレート乳剤の一部(4g)を、水(32g)で希釈して、平均直径0.19ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。テンプレート乳剤を、薬剤ダナゾール(danazol)(0.5g)及び溶剤ジクロロメタン(4.5g)を含む溶液と周囲温度で混合した。平均粒子直径は、最初2.4ミクロンまで増加し、そしてテンプレート剤による薬剤溶液の吸収後、次の20時間内に0.35ミクロンまで減少した。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色結晶固体を得た。この白色結晶を水に再分散したところ、最初に平均直径6.5ミクロンの粒子が得られたが、この粒子は2時間以内に分解して、平均直径0.3ミクロンの粒子となった。
ダナゾ−ル粒子の結晶度を、X線粉末回折(図1)により立証した。ダナゾール試料のピーク形状は、非処理ダナゾール対照物のピーク形状と実質的に同一であった。
ダナゾール粒子の試験管内溶解速度が高いことを、USP24モノグラフによる標準溶解プロトコルにより立証した(図2)。実質的にすべてのダナゾールが最初の10分間以内に溶解した。
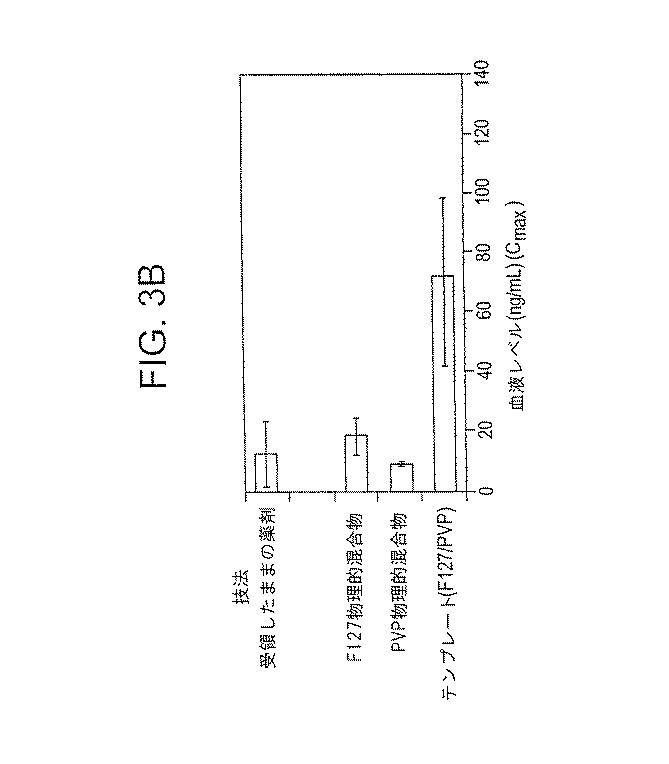
ダナゾール粒子のバイオアベイラビリティが向上したことを、カプセルの一回口径投与により17.0〜17.2mgのダナゾールを投与されたラットを用いて、生体内試験で立証した(図3A〜3C)。図3Aに示すように、ダナゾールテンプレート乳剤試料の曲線(AUC)の領域では、対照、すなわち、受領したままのダナゾール、並びに薬剤ダナゾールと安定剤PluronicF−127及びポリビニルピロリドン55kDの物理的混合物のAUCより明らかに高い。図3Bに示すように、ダナゾールテンプレート乳剤試料の最高血液レベル濃度(Cmax)は、対照について測定した最高血液レベル濃度より有意に高く、図3Cに示すように、この最高血液レベル濃度(Tmax)に達するのに要する時間は、対照についての時間に匹敵する。これらの結果は明らかに、ダナゾールテンプレート乳剤試料のバイオアベイラビリティが増進したことを実証するものである。
実施例2
トリオレイン(7.5g)、ポリビニルアルコール9−10kD(1.5g)、Span80(1.1g)及び水(7.5g)を含むテンプレート乳剤を高せん断混合により調製して、平均直径0.14ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤ダナゾール(0.5g)及び溶剤ジクロロメタン(4.5g)を含む溶液と周囲温度で混合した。平均粒子直径は、最初3.9ミクロンまで増加し、そしてテンプレート剤による薬剤溶液の吸収後、次の20時間以内に0.4ミクロンまで減少した。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色結晶固体を得た。この白色結晶を水に再分散したところ、最初に平均直径13.4ミクロンの粒子が得られたが、この粒子は12時間以内に分解して、平均直径0.8ミクロンの粒子となった。
トリオレイン(7.5g)、ポリビニルアルコール9−10kD(1.5g)、Span80(1.1g)及び水(7.5g)を含むテンプレート乳剤を高せん断混合により調製して、平均直径0.14ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤ダナゾール(0.5g)及び溶剤ジクロロメタン(4.5g)を含む溶液と周囲温度で混合した。平均粒子直径は、最初3.9ミクロンまで増加し、そしてテンプレート剤による薬剤溶液の吸収後、次の20時間以内に0.4ミクロンまで減少した。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色結晶固体を得た。この白色結晶を水に再分散したところ、最初に平均直径13.4ミクロンの粒子が得られたが、この粒子は12時間以内に分解して、平均直径0.8ミクロンの粒子となった。
実施例3
綿実油(7.5g)、ポリビニルアルコール9−10kD(7.5g)、及び10重量%のPluronicF−68を含む水(7.5g)を含むテンプレート乳剤を高せん断混合により調製して、平均直径0.3ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤シクロスポリン(cyclosporin)A(0.5g)及び溶剤トルエン(2.2g)を含む溶液と周囲温度で混合した。平均粒子直径は、テンプレート剤による薬剤溶液の吸収後、0.4ミクロンまで増加し、少なくとも24時間安定のままであった。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色粉末試料を得た。この白色粉末を水に再分散したところ、最初に平均直径14.5ミクロンの粒子が得られたが、この粒子は5時間以内に分解して、平均直径0.8ミクロンの粒子となった。
綿実油(7.5g)、ポリビニルアルコール9−10kD(7.5g)、及び10重量%のPluronicF−68を含む水(7.5g)を含むテンプレート乳剤を高せん断混合により調製して、平均直径0.3ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤シクロスポリン(cyclosporin)A(0.5g)及び溶剤トルエン(2.2g)を含む溶液と周囲温度で混合した。平均粒子直径は、テンプレート剤による薬剤溶液の吸収後、0.4ミクロンまで増加し、少なくとも24時間安定のままであった。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、白色粉末試料を得た。この白色粉末を水に再分散したところ、最初に平均直径14.5ミクロンの粒子が得られたが、この粒子は5時間以内に分解して、平均直径0.8ミクロンの粒子となった。
実施例4
安定剤Atlox4991及びメチルオリエート(12.5%)を含む水性テンプレート乳剤(水中に5%)を高せん断混合により調製した。このテンプレート乳剤を、薬剤シクロスポリンA(10%)、溶剤トルエン(40%)、安定剤Tween40(5%)及び水(45%)を含む粗薬剤乳剤と周囲温度で混合した。初期の平均粒子直径は、12.7ミクロン(光散乱により測定)であったが、15分後3.6ミクロン、25分後1.2ミクロン、20時間後0.64ミクロンとなり、その間、薬剤乳剤はテンプレート剤により吸収された。
安定剤Atlox4991及びメチルオリエート(12.5%)を含む水性テンプレート乳剤(水中に5%)を高せん断混合により調製した。このテンプレート乳剤を、薬剤シクロスポリンA(10%)、溶剤トルエン(40%)、安定剤Tween40(5%)及び水(45%)を含む粗薬剤乳剤と周囲温度で混合した。初期の平均粒子直径は、12.7ミクロン(光散乱により測定)であったが、15分後3.6ミクロン、25分後1.2ミクロン、20時間後0.64ミクロンとなり、その間、薬剤乳剤はテンプレート剤により吸収された。
実施例5及び6
綿実油(0.89%)、ポリビニルピロリドン55kD(2.68%)、メチルオリエート(0.39%)及び水(96.04%)を含むテンプレート乳剤(35g)を高せん断混合(20,000rpmで10分間)により周囲温度で調製し、体積平均直径0.28ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。テンプレート乳剤を、薬剤ニフェジピン(nifedipine)(1g)及び60:40混合比の溶剤トルエン/イソブチルアセテート(30g)を含む溶液と、薬剤ケトコナゾール(ketoconazole)(1g)及び溶剤ジクロロメタン(9g)を含む溶液と、周囲温度でそれぞれ混合した(表Aに示す)。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、乾燥粉末試料を得た。この粉末試料を脱イオン水に再分散した。薬剤溶液の添加後に測定したオイル液滴の体積平均直径、並びに乾燥及び水に再分散後の薬剤粒子の体積平均直径を表Aに示す。
綿実油(0.89%)、ポリビニルピロリドン55kD(2.68%)、メチルオリエート(0.39%)及び水(96.04%)を含むテンプレート乳剤(35g)を高せん断混合(20,000rpmで10分間)により周囲温度で調製し、体積平均直径0.28ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。テンプレート乳剤を、薬剤ニフェジピン(nifedipine)(1g)及び60:40混合比の溶剤トルエン/イソブチルアセテート(30g)を含む溶液と、薬剤ケトコナゾール(ketoconazole)(1g)及び溶剤ジクロロメタン(9g)を含む溶液と、周囲温度でそれぞれ混合した(表Aに示す)。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、乾燥粉末試料を得た。この粉末試料を脱イオン水に再分散した。薬剤溶液の添加後に測定したオイル液滴の体積平均直径、並びに乾燥及び水に再分散後の薬剤粒子の体積平均直径を表Aに示す。
粒径測定の分野の当業者に公知のX線回折を用いて、各例についての結晶度を測定したが、内部標準として酸化アルミニウムを用いた。次表Aは、使用物質及びそれらの結果を示す。表Aに用いるものとして、「PSA」とは粒径分析を意味する。「PSAredisp.」とは再分散粒子の粒径を意味する。
実施例7〜10
トルエン(5%)、ポリビニルアルコール9−10kD(5%)、Span60(0.37%)及び水(89.6%)を含むテンプレート乳剤(13g)を高せん断混合(20,000rpmで3分間)により周囲温度で調製し、体積平均直径0.40ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤ナプロキセン(naproxen)、シクロスポリンA、ニフェジピン又はケトコナゾール(0.5g)をそれぞれ含む溶液と、溶剤ジクロロメタン(4.5g)又は60:40のトルエン/イソブチルアセテートと、周囲温度でそれぞれ混合した(表Bに示す)。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、乾燥粉末試料を得た。この粉末試料を脱イオン水に再分散した。薬剤溶液の添加後に測定したオイル液滴の体積平均直径、並びに水に再分散後の薬剤粒子の体積平均直径を表Bに示す。
トルエン(5%)、ポリビニルアルコール9−10kD(5%)、Span60(0.37%)及び水(89.6%)を含むテンプレート乳剤(13g)を高せん断混合(20,000rpmで3分間)により周囲温度で調製し、体積平均直径0.40ミクロン(光散乱により測定)のテンプレート乳剤液滴を得た。このテンプレート乳剤を、薬剤ナプロキセン(naproxen)、シクロスポリンA、ニフェジピン又はケトコナゾール(0.5g)をそれぞれ含む溶液と、溶剤ジクロロメタン(4.5g)又は60:40のトルエン/イソブチルアセテートと、周囲温度でそれぞれ混合した(表Bに示す)。有機溶剤を乳剤から蒸発除去し、連続相を凍結乾燥により除去して、乾燥粉末試料を得た。この粉末試料を脱イオン水に再分散した。薬剤溶液の添加後に測定したオイル液滴の体積平均直径、並びに水に再分散後の薬剤粒子の体積平均直径を表Bに示す。
粒径測定の分野の当業者に公知のX線回折を用いて、各例についての結晶度を測定したが、内部標準として酸化アルミニウムを用いた。次表Bは、使用物質及びそれらの結果を示す。表Bに用いるものとして、「PSA」とは粒径分析を意味する。「PSAredisp.」とは再分散粒子の粒径を意味する。
「受領したままの薬剤」対照物と比較して、実施例7〜10で得られたテンプレート調製試料の試験管内溶解速度が改良されたことを、USP24モノグラフによる標準溶解プロトコルにより立証した。溶解の進行状態を、分析ツールとして高圧液体クロマトグラフィ(HPLC)又はUV/VIS検出を用いて、5分、10分、15分そして60分後に測定した。結果をテンプレート調製試料について、時間(分)対溶解試料%として表Cに示す。比較として、対照についての対応データを括弧内に示す。すべてのテンプレート調製物において、溶解速度が上昇するが、薬剤の迅速吸収が困難な最初の15分間において溶解速度が特に上昇した。
Claims (23)
- (a)水及びテンプレート剤を含むテンプレート乳剤を調製し;
(b)薬剤物質を含む薬剤含有混合物を調製し;次いで
(c)前記テンプレート乳剤を前記薬剤含有混合物と合わせて、テンプレート乳剤中に薬剤粒子を形成することを含む、ミクロンサイズ又はサブミクロンサイズの薬剤を製造する方法。 - 前記テンプレート乳剤が少なくとも1種の安定剤を更に含む請求項1記載の方法。
- 前記薬剤含有混合物が少なくとも1種の溶剤を更に含む請求項1記載の方法。
- 前記溶剤が低水溶性である請求項3記載の方法。
- 前記溶剤が低蒸気圧を有する請求項3記載の方法。
- 前記方法が溶剤除去工程を更に含む請求項3記載の方法。
- 前記方法が水除去工程を更に含む請求項6記載の方法。
- 前記テンプレート乳剤中の薬剤粒子の平均粒径が0.25ミクロン〜15ミクロンである請求項1記載の方法。
- 前記テンプレート剤が低水溶性である請求項1記載の方法。
- 前記テンプレート剤が、アルキル置換ベンゼン、綿実油、オリーブ油、大豆油、植物油、水和植物油、脂肪酸のジアルキルアミド、塩素化脂肪族炭化水素、塩素化芳香族炭化水素、グリコール誘導体のエステル、ケトン、鉱油、アルキルアセテート及びトルエンからなる群より選ばれる請求項9記載の方法。
- 前記安定剤が、ポリマー、ホモポリマー、コ−ポリマー、界面活性剤及びこれらの組み合わせからなる群より選ばれる請求項2記載の方法。
- 前記溶剤が、アルカン、塩素化アルカン、脂肪族エーテル、芳香族エーテル、脂肪族エステル、芳香族エステル、脂肪族ケトン、芳香族ケトン及びこれらの組み合わせから選ばれる請求項3記載の方法。
- (a)水及びテンプレート剤を含むテンプレート乳剤を調製し;
(b)薬剤物質を含む薬剤含有混合物を調製し;次いで
(c)前記テンプレート乳剤を前記薬剤含有混合物と合わせて、テンプレート乳剤中に薬剤粒子を形成することを含む方法により製造された薬剤粒子。 - 前記テンプレート乳剤が少なくとも1種の安定剤を更に含む請求項13記載の薬剤粒子。
- 前記薬剤含有混合物が少なくとも1種の溶剤を更に含む請求項13記載の薬剤粒子。
- 前記方法が溶剤除去工程を更に含む請求項15記載の薬剤粒子。
- 前記溶剤が低水溶性である請求項15記載の薬剤粒子。
- 前記溶剤が低蒸気圧を有する請求項15記載の薬剤粒子。
- 前記テンプレート乳剤中の薬剤の平均粒径が0.25ミクロン〜15ミクロンである請求項13記載の薬剤粒子。
- 前記テンプレート剤が低水溶性である請求項13記載の薬剤粒子。
- 前記テンプレート剤が、アルキル置換ベンゼン、綿実油、オリーブ油、大豆油、植物油、水和植物油、脂肪酸のジアルキルアミド、塩素化脂肪族炭化水素、塩素化芳香族炭化水素、グリコール誘導体のエステル、ケトン、鉱油、アルキルアセテート及びトルエンからなる群より選ばれる請求項20記載の薬剤粒子。
- 前記安定剤が、ポリマー、ホモポリマー、コ−ポリマー、界面活性剤及びこれらの組み合わせからなる群より選ばれる請求項14記載の薬剤粒子。
- 前記溶剤が、アルカン、塩素化アルカン、脂肪族エーテル、芳香族エーテル、脂肪族エステル、芳香族エステル、脂肪族ケトン、芳香族ケトン及びこれらの組み合わせから選ばれる請求項15記載の薬剤粒子。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US34895902P | 2002-01-14 | 2002-01-14 | |
| PCT/US2003/000726 WO2003059319A1 (en) | 2002-01-14 | 2003-01-10 | Drug nanoparticles from template emulsions |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005515224A true JP2005515224A (ja) | 2005-05-26 |
Family
ID=23370305
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003559482A Pending JP2005515224A (ja) | 2002-01-14 | 2003-01-10 | テンプレート乳剤からの薬剤ナノ粒子 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20030133987A1 (ja) |
| EP (1) | EP1467709A1 (ja) |
| JP (1) | JP2005515224A (ja) |
| AU (1) | AU2003235686A1 (ja) |
| CA (1) | CA2470533A1 (ja) |
| WO (1) | WO2003059319A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008053920A1 (en) * | 2006-10-31 | 2008-05-08 | Kaneka Corporation | Physiologically active substance-containing granular composition and method of producing the same |
| JP2009505976A (ja) * | 2005-08-12 | 2009-02-12 | アストラゼネカ・アクチエボラーグ | 方法 |
| JP2009519999A (ja) * | 2005-12-19 | 2009-05-21 | エテルナ ツェンタリス ゲゼルシャフト ミット ベシュレンクテル ハフツング | 低減された細胞毒性を有するアルキルリン脂質誘導体並びにそれらの使用 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2127736A1 (en) | 2003-04-10 | 2009-12-02 | The President and Fellows of Harvard College | Formation and control of fluidic species |
| DK1631261T3 (da) | 2003-05-22 | 2009-11-09 | Applied Nanosystems Bv | Fremstilling af små partikler |
| CN104069784B (zh) * | 2003-08-27 | 2017-01-11 | 哈佛大学 | 流体物种的电子控制 |
| WO2008002568A2 (en) * | 2006-06-26 | 2008-01-03 | Mutual Pharmaceutical Company, Inc. | Active agent formulations, methods of making, and methods of use |
| WO2008097165A1 (en) * | 2007-02-09 | 2008-08-14 | Astrazeneca Ab | Process for preparation of a stable dispersion of solid amorphous submicron particles in an aqueous medium |
| US20100159010A1 (en) * | 2008-12-24 | 2010-06-24 | Mutual Pharmaceutical Company, Inc. | Active Agent Formulations, Methods of Making, and Methods of Use |
| BR112012011336A2 (pt) | 2009-10-22 | 2018-10-16 | Api Genesis Llc | Composições compreendendo flavonoides, seu método de preparação, adesivo para aplicação de flavonoide, métodos de produção de flavonoide hidratado,métodos de preparação de formulação tópica, e uso de flavonoide |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IE58110B1 (en) * | 1984-10-30 | 1993-07-14 | Elan Corp Plc | Controlled release powder and process for its preparation |
| SE464743B (sv) * | 1989-06-21 | 1991-06-10 | Ytkemiska Inst | Foerfarande foer framstaellning av laekemedelspartiklar |
| US5145684A (en) * | 1991-01-25 | 1992-09-08 | Sterling Drug Inc. | Surface modified drug nanoparticles |
| GB9319129D0 (en) * | 1993-09-15 | 1993-11-03 | Dowelanco Ltd | Storage and dilution of stable aqueous dispersions |
| GB9414318D0 (en) * | 1994-07-15 | 1994-09-07 | Dowelanco Ltd | Preparation of aqueous emulsions |
-
2003
- 2003-01-10 CA CA002470533A patent/CA2470533A1/en not_active Abandoned
- 2003-01-10 WO PCT/US2003/000726 patent/WO2003059319A1/en not_active Ceased
- 2003-01-10 US US10/340,079 patent/US20030133987A1/en not_active Abandoned
- 2003-01-10 JP JP2003559482A patent/JP2005515224A/ja active Pending
- 2003-01-10 AU AU2003235686A patent/AU2003235686A1/en not_active Abandoned
- 2003-01-10 EP EP03729625A patent/EP1467709A1/en not_active Withdrawn
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009505976A (ja) * | 2005-08-12 | 2009-02-12 | アストラゼネカ・アクチエボラーグ | 方法 |
| JP2009519999A (ja) * | 2005-12-19 | 2009-05-21 | エテルナ ツェンタリス ゲゼルシャフト ミット ベシュレンクテル ハフツング | 低減された細胞毒性を有するアルキルリン脂質誘導体並びにそれらの使用 |
| WO2008053920A1 (en) * | 2006-10-31 | 2008-05-08 | Kaneka Corporation | Physiologically active substance-containing granular composition and method of producing the same |
| JP5256041B2 (ja) * | 2006-10-31 | 2013-08-07 | 株式会社カネカ | 生理活性物質含有粒子状組成物およびその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1467709A1 (en) | 2004-10-20 |
| WO2003059319A1 (en) | 2003-07-24 |
| US20030133987A1 (en) | 2003-07-17 |
| AU2003235686A1 (en) | 2003-07-30 |
| CA2470533A1 (en) | 2003-07-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6534979B2 (ja) | 低溶解性化合物の安定な複合体 | |
| DE69627835T2 (de) | Feste pharmazeutische zusammensetzung aus nanopartikeln | |
| US4826689A (en) | Method for making uniformly sized particles from water-insoluble organic compounds | |
| DE60211130T2 (de) | Neue formulierung mit modifizierter freisetzung | |
| AT391806B (de) | Verfahren zur herstellung einer festen dispersion eines pharmakologischen wirkstoffes in einer polymeren matrix | |
| AU2004295259B2 (en) | Method for preparing nano-scale or amorphous particle using solid fat as a solvent | |
| JP2005515224A (ja) | テンプレート乳剤からの薬剤ナノ粒子 | |
| DE602004006000T2 (de) | Verringerung der teilchengrösse von bioaktiven verbindungen | |
| Purohit et al. | Proof-of-concept in developing a 45% drug loaded amorphous nanoparticle formulation | |
| JP2025508347A (ja) | 医薬品有効成分の結晶化のための方法 | |
| Thakkar et al. | Excipients and their functionality for enabling technologies in oral dosage forms | |
| JP2016537332A (ja) | 非ヌクレオシド逆転写酵素阻害剤の組成物 | |
| FR2803748A1 (fr) | Composition d'itraconazole et procede de preparation | |
| Lagarón Cabello et al. | Pharmaceutical formulation with improved solubility and bioavailability | |
| CN101242809A (zh) | 方法 | |
| CN101605533B (zh) | 制备固体非晶亚微米颗粒在水性介质中的稳定分散体的方法 | |
| MXPA99008648A (en) | Stable compounds of low solub compounds | |
| KR20060006086A (ko) | 2가 산 코폴리머를 이용하여 크기를 안정화시킨 입자 | |
| Sorkhel et al. | RECENT SCENARIO OF GELUCIRES IN SOLID DISPERSION TECHNIQUES |