ES2948575T3 - Composición para su uso tópico a base de un complejo carnosina-magnesio - Google Patents
Composición para su uso tópico a base de un complejo carnosina-magnesio Download PDFInfo
- Publication number
- ES2948575T3 ES2948575T3 ES17706899T ES17706899T ES2948575T3 ES 2948575 T3 ES2948575 T3 ES 2948575T3 ES 17706899 T ES17706899 T ES 17706899T ES 17706899 T ES17706899 T ES 17706899T ES 2948575 T3 ES2948575 T3 ES 2948575T3
- Authority
- ES
- Spain
- Prior art keywords
- carnosine
- topical composition
- composition
- skin
- weight
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 136
- 230000000699 topical effect Effects 0.000 title claims abstract description 100
- 239000011777 magnesium Substances 0.000 title claims abstract description 58
- 229910052749 magnesium Inorganic materials 0.000 title claims abstract description 58
- CQOVPNPJLQNMDC-ZETCQYMHSA-N carnosine Chemical compound [NH3+]CCC(=O)N[C@H](C([O-])=O)CC1=CNC=N1 CQOVPNPJLQNMDC-ZETCQYMHSA-N 0.000 claims abstract description 98
- 108010087806 Carnosine Proteins 0.000 claims abstract description 97
- CQOVPNPJLQNMDC-UHFFFAOYSA-N N-beta-alanyl-L-histidine Natural products NCCC(=O)NC(C(O)=O)CC1=CN=CN1 CQOVPNPJLQNMDC-UHFFFAOYSA-N 0.000 claims abstract description 97
- QRYRORQUOLYVBU-VBKZILBWSA-N Carnosic acid Natural products CC([C@@H]1CC2)(C)CCC[C@]1(C(O)=O)C1=C2C=C(C(C)C)C(O)=C1O QRYRORQUOLYVBU-VBKZILBWSA-N 0.000 claims abstract description 94
- 229940044199 carnosine Drugs 0.000 claims abstract description 94
- 230000036314 physical performance Effects 0.000 claims abstract description 8
- 210000003491 skin Anatomy 0.000 claims description 50
- 210000001519 tissue Anatomy 0.000 claims description 26
- 239000000499 gel Substances 0.000 claims description 21
- 239000006071 cream Substances 0.000 claims description 14
- 238000010792 warming Methods 0.000 claims description 14
- 210000003205 muscle Anatomy 0.000 claims description 13
- 239000003795 chemical substances by application Substances 0.000 claims description 11
- 210000002615 epidermis Anatomy 0.000 claims description 11
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 claims description 8
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 claims description 8
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 claims description 8
- 210000002027 skeletal muscle Anatomy 0.000 claims description 8
- -1 propyl alcohols Chemical class 0.000 claims description 7
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 claims description 6
- 239000000314 lubricant Substances 0.000 claims description 6
- 239000003921 oil Substances 0.000 claims description 6
- 239000003755 preservative agent Substances 0.000 claims description 6
- 230000002335 preservative effect Effects 0.000 claims description 6
- 230000037384 skin absorption Effects 0.000 claims description 6
- 231100000274 skin absorption Toxicity 0.000 claims description 6
- 239000004094 surface-active agent Substances 0.000 claims description 6
- 239000002562 thickening agent Substances 0.000 claims description 6
- 239000003974 emollient agent Substances 0.000 claims description 5
- WCVRQHFDJLLWFE-UHFFFAOYSA-N pentane-1,2-diol Chemical compound CCCC(O)CO WCVRQHFDJLLWFE-UHFFFAOYSA-N 0.000 claims description 5
- 239000007921 spray Substances 0.000 claims description 5
- DSSYKIVIOFKYAU-XCBNKYQSSA-N (R)-camphor Chemical compound C1C[C@@]2(C)C(=O)C[C@@H]1C2(C)C DSSYKIVIOFKYAU-XCBNKYQSSA-N 0.000 claims description 4
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 claims description 4
- 240000004160 Capsicum annuum Species 0.000 claims description 4
- 235000002567 Capsicum annuum Nutrition 0.000 claims description 4
- XBLVHTDFJBKJLG-UHFFFAOYSA-N Ethyl nicotinate Chemical compound CCOC(=O)C1=CC=CN=C1 XBLVHTDFJBKJLG-UHFFFAOYSA-N 0.000 claims description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 4
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 claims description 4
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 claims description 4
- KVYGGMBOZFWZBQ-UHFFFAOYSA-N benzyl nicotinate Chemical compound C=1C=CN=CC=1C(=O)OCC1=CC=CC=C1 KVYGGMBOZFWZBQ-UHFFFAOYSA-N 0.000 claims description 4
- 239000001511 capsicum annuum Substances 0.000 claims description 4
- YNBADRVTZLEFNH-UHFFFAOYSA-N methyl nicotinate Chemical compound COC(=O)C1=CC=CN=C1 YNBADRVTZLEFNH-UHFFFAOYSA-N 0.000 claims description 4
- 229960001047 methyl salicylate Drugs 0.000 claims description 4
- 239000008601 oleoresin Substances 0.000 claims description 4
- 150000003839 salts Chemical class 0.000 claims description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 4
- 239000006260 foam Substances 0.000 claims description 3
- 229920002674 hyaluronan Polymers 0.000 claims description 3
- 239000006210 lotion Substances 0.000 claims description 3
- 239000002674 ointment Substances 0.000 claims description 3
- 238000011084 recovery Methods 0.000 claims description 3
- 239000000080 wetting agent Substances 0.000 claims description 3
- NKJOXAZJBOMXID-UHFFFAOYSA-N 1,1'-Oxybisoctane Chemical compound CCCCCCCCOCCCCCCCC NKJOXAZJBOMXID-UHFFFAOYSA-N 0.000 claims description 2
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 claims description 2
- NCZPCONIKBICGS-UHFFFAOYSA-N 3-(2-ethylhexoxy)propane-1,2-diol Chemical compound CCCCC(CC)COCC(O)CO NCZPCONIKBICGS-UHFFFAOYSA-N 0.000 claims description 2
- 229920001817 Agar Polymers 0.000 claims description 2
- 239000005711 Benzoic acid Substances 0.000 claims description 2
- 239000004287 Dehydroacetic acid Substances 0.000 claims description 2
- ZDQWESQEGGJUCH-UHFFFAOYSA-N Diisopropyl adipate Chemical compound CC(C)OC(=O)CCCCC(=O)OC(C)C ZDQWESQEGGJUCH-UHFFFAOYSA-N 0.000 claims description 2
- 241000206672 Gelidium Species 0.000 claims description 2
- 229920002907 Guar gum Polymers 0.000 claims description 2
- 239000004354 Hydroxyethyl cellulose Substances 0.000 claims description 2
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 claims description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 claims description 2
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 claims description 2
- 241001558929 Sclerotium <basidiomycota> Species 0.000 claims description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 claims description 2
- MSCCTZZBYHQMQJ-AZAGJHQNSA-N Tocopheryl nicotinate Chemical compound C([C@@](OC1=C(C)C=2C)(C)CCC[C@H](C)CCC[C@H](C)CCCC(C)C)CC1=C(C)C=2OC(=O)C1=CC=CN=C1 MSCCTZZBYHQMQJ-AZAGJHQNSA-N 0.000 claims description 2
- 235000010419 agar Nutrition 0.000 claims description 2
- 235000010233 benzoic acid Nutrition 0.000 claims description 2
- 229960004365 benzoic acid Drugs 0.000 claims description 2
- 229950004580 benzyl nicotinate Drugs 0.000 claims description 2
- MRUAUOIMASANKQ-UHFFFAOYSA-N cocamidopropyl betaine Chemical compound CCCCCCCCCCCC(=O)NCCC[N+](C)(C)CC([O-])=O MRUAUOIMASANKQ-UHFFFAOYSA-N 0.000 claims description 2
- 229940073507 cocamidopropyl betaine Drugs 0.000 claims description 2
- 229940071160 cocoate Drugs 0.000 claims description 2
- 229920001577 copolymer Polymers 0.000 claims description 2
- 235000019258 dehydroacetic acid Nutrition 0.000 claims description 2
- JEQRBTDTEKWZBW-UHFFFAOYSA-N dehydroacetic acid Chemical compound CC(=O)C1=C(O)OC(C)=CC1=O JEQRBTDTEKWZBW-UHFFFAOYSA-N 0.000 claims description 2
- 229940061632 dehydroacetic acid Drugs 0.000 claims description 2
- PGRHXDWITVMQBC-UHFFFAOYSA-N dehydroacetic acid Natural products CC(=O)C1C(=O)OC(C)=CC1=O PGRHXDWITVMQBC-UHFFFAOYSA-N 0.000 claims description 2
- PKPOVTYZGGYDIJ-UHFFFAOYSA-N dioctyl carbonate Chemical compound CCCCCCCCOC(=O)OCCCCCCCC PKPOVTYZGGYDIJ-UHFFFAOYSA-N 0.000 claims description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 230000002708 enhancing effect Effects 0.000 claims description 2
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 claims description 2
- 229940100524 ethylhexylglycerin Drugs 0.000 claims description 2
- 229940064982 ethylnicotinate Drugs 0.000 claims description 2
- 239000000665 guar gum Substances 0.000 claims description 2
- 235000010417 guar gum Nutrition 0.000 claims description 2
- 229960002154 guar gum Drugs 0.000 claims description 2
- 229920000591 gum Polymers 0.000 claims description 2
- RVYGVBZGSFLJKH-UHFFFAOYSA-N hexyl pyridine-3-carboxylate Chemical compound CCCCCCOC(=O)C1=CC=CN=C1 RVYGVBZGSFLJKH-UHFFFAOYSA-N 0.000 claims description 2
- 229940051295 hexylnicotinate Drugs 0.000 claims description 2
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 claims description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 claims description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 claims description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 claims description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 claims description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 claims description 2
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 claims description 2
- 229960001238 methylnicotinate Drugs 0.000 claims description 2
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 2
- 235000001968 nicotinic acid Nutrition 0.000 claims description 2
- 239000011664 nicotinic acid Substances 0.000 claims description 2
- 229960003921 octisalate Drugs 0.000 claims description 2
- WCJLCOAEJIHPCW-UHFFFAOYSA-N octyl 2-hydroxybenzoate Chemical compound CCCCCCCCOC(=O)C1=CC=CC=C1O WCJLCOAEJIHPCW-UHFFFAOYSA-N 0.000 claims description 2
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 2
- 235000010987 pectin Nutrition 0.000 claims description 2
- 239000001814 pectin Substances 0.000 claims description 2
- 229920001277 pectin Polymers 0.000 claims description 2
- 229960000292 pectin Drugs 0.000 claims description 2
- 229960005323 phenoxyethanol Drugs 0.000 claims description 2
- 150000003242 quaternary ammonium salts Chemical class 0.000 claims description 2
- 239000000377 silicon dioxide Substances 0.000 claims description 2
- 235000012239 silicon dioxide Nutrition 0.000 claims description 2
- 229920002545 silicone oil Polymers 0.000 claims description 2
- 235000019333 sodium laurylsulphate Nutrition 0.000 claims description 2
- 235000010199 sorbic acid Nutrition 0.000 claims description 2
- 239000004334 sorbic acid Substances 0.000 claims description 2
- 229940075582 sorbic acid Drugs 0.000 claims description 2
- WSWCOQWTEOXDQX-MQQKCMAXSA-N sorbic acid group Chemical group C(\C=C\C=C\C)(=O)O WSWCOQWTEOXDQX-MQQKCMAXSA-N 0.000 claims description 2
- 239000004408 titanium dioxide Substances 0.000 claims description 2
- 229950009883 tocopheryl nicotinate Drugs 0.000 claims description 2
- 239000000230 xanthan gum Substances 0.000 claims description 2
- 235000010493 xanthan gum Nutrition 0.000 claims description 2
- 229920001285 xanthan gum Polymers 0.000 claims description 2
- 229940082509 xanthan gum Drugs 0.000 claims description 2
- 239000011787 zinc oxide Substances 0.000 claims description 2
- 241000723346 Cinnamomum camphora Species 0.000 claims 2
- 235000019441 ethanol Nutrition 0.000 claims 2
- WHBKVWBGTBULQY-UHFFFAOYSA-N 2-propylheptyl octanoate Chemical compound CCCCCCCC(=O)OCC(CCC)CCCCC WHBKVWBGTBULQY-UHFFFAOYSA-N 0.000 claims 1
- CMBYOWLFQAFZCP-UHFFFAOYSA-N Hexyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCCCCC CMBYOWLFQAFZCP-UHFFFAOYSA-N 0.000 claims 1
- 125000005909 ethyl alcohol group Chemical group 0.000 claims 1
- 229940100463 hexyl laurate Drugs 0.000 claims 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims 1
- 229940074928 isopropyl myristate Drugs 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 15
- 238000011282 treatment Methods 0.000 abstract description 10
- 238000000034 method Methods 0.000 abstract description 7
- 229940091250 magnesium supplement Drugs 0.000 description 50
- 238000012360 testing method Methods 0.000 description 15
- 239000000872 buffer Substances 0.000 description 11
- 238000009472 formulation Methods 0.000 description 10
- 239000002609 medium Substances 0.000 description 10
- 239000004480 active ingredient Substances 0.000 description 8
- 159000000003 magnesium salts Chemical class 0.000 description 8
- 239000007864 aqueous solution Substances 0.000 description 7
- 238000012549 training Methods 0.000 description 7
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 6
- 239000000835 fiber Substances 0.000 description 6
- 230000001965 increasing effect Effects 0.000 description 6
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 230000009471 action Effects 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- JLVVSXFLKOJNIY-UHFFFAOYSA-N Magnesium ion Chemical compound [Mg+2] JLVVSXFLKOJNIY-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 230000003139 buffering effect Effects 0.000 description 4
- CVSVTCORWBXHQV-UHFFFAOYSA-N creatine Chemical compound NC(=[NH2+])N(C)CC([O-])=O CVSVTCORWBXHQV-UHFFFAOYSA-N 0.000 description 4
- 239000003623 enhancer Substances 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 230000003834 intracellular effect Effects 0.000 description 4
- 229910001425 magnesium ion Inorganic materials 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 235000019198 oils Nutrition 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- LDCYZAJDBXYCGN-UHFFFAOYSA-N 5-hydroxytryptophan Chemical compound C1=C(O)C=C2C(CC(N)C(O)=O)=CNC2=C1 LDCYZAJDBXYCGN-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 230000003078 antioxidant effect Effects 0.000 description 3
- 230000033228 biological regulation Effects 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 125000002883 imidazolyl group Chemical group 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 239000004310 lactic acid Substances 0.000 description 3
- 235000014655 lactic acid Nutrition 0.000 description 3
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 3
- 229960003390 magnesium sulfate Drugs 0.000 description 3
- 235000019341 magnesium sulphate Nutrition 0.000 description 3
- 210000001087 myotubule Anatomy 0.000 description 3
- 239000006174 pH buffer Substances 0.000 description 3
- 239000003642 reactive oxygen metabolite Substances 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 210000000434 stratum corneum Anatomy 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- PHIQHXFUZVPYII-ZCFIWIBFSA-N (R)-carnitine Chemical compound C[N+](C)(C)C[C@H](O)CC([O-])=O PHIQHXFUZVPYII-ZCFIWIBFSA-N 0.000 description 2
- POAOYUHQDCAZBD-UHFFFAOYSA-N 2-butoxyethanol Chemical compound CCCCOCCO POAOYUHQDCAZBD-UHFFFAOYSA-N 0.000 description 2
- LDCYZAJDBXYCGN-VIFPVBQESA-N 5-hydroxy-L-tryptophan Chemical compound C1=C(O)C=C2C(C[C@H](N)C(O)=O)=CNC2=C1 LDCYZAJDBXYCGN-VIFPVBQESA-N 0.000 description 2
- 229940000681 5-hydroxytryptophan Drugs 0.000 description 2
- 108010085443 Anserine Proteins 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 2
- 108010071840 Cytosol nonspecific dipeptidase Proteins 0.000 description 2
- 108010016626 Dipeptides Proteins 0.000 description 2
- 240000005636 Dryobalanops aromatica Species 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- SLRNWACWRVGMKD-UHFFFAOYSA-N L-anserine Natural products CN1C=NC(CC(NC(=O)CCN)C(O)=O)=C1 SLRNWACWRVGMKD-UHFFFAOYSA-N 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 101100010166 Mus musculus Dok3 gene Proteins 0.000 description 2
- BKAYIFDRRZZKNF-VIFPVBQESA-N N-acetylcarnosine Chemical compound CC(=O)NCCC(=O)N[C@H](C(O)=O)CC1=CN=CN1 BKAYIFDRRZZKNF-VIFPVBQESA-N 0.000 description 2
- 241000210053 Potentilla elegans Species 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- MYYIAHXIVFADCU-QMMMGPOBSA-N anserine Chemical compound CN1C=NC=C1C[C@H](NC(=O)CC[NH3+])C([O-])=O MYYIAHXIVFADCU-QMMMGPOBSA-N 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- UCMIRNVEIXFBKS-UHFFFAOYSA-N beta-alanine Chemical compound NCCC(O)=O UCMIRNVEIXFBKS-UHFFFAOYSA-N 0.000 description 2
- 229960004203 carnitine Drugs 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 229960003624 creatine Drugs 0.000 description 2
- 239000006046 creatine Substances 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229960002885 histidine Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 230000036542 oxidative stress Effects 0.000 description 2
- 239000006072 paste Substances 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 230000037081 physical activity Effects 0.000 description 2
- 230000035479 physiological effects, processes and functions Effects 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 210000001908 sarcoplasmic reticulum Anatomy 0.000 description 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 238000013334 tissue model Methods 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- RZALONVQKUWRRY-XOJLQXRJSA-N (2r,3r)-2,3-dihydroxybutanedioate;hydron;(3r)-3-hydroxy-4-(trimethylazaniumyl)butanoate Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.C[N+](C)(C)C[C@H](O)CC([O-])=O RZALONVQKUWRRY-XOJLQXRJSA-N 0.000 description 1
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- 229940043375 1,5-pentanediol Drugs 0.000 description 1
- WEZPLQKRXDBPEP-UHFFFAOYSA-N 1-(1-propoxypropan-2-yloxy)propan-2-ol Chemical compound CCCOCC(C)OCC(C)O WEZPLQKRXDBPEP-UHFFFAOYSA-N 0.000 description 1
- QWOZZTWBWQMEPD-UHFFFAOYSA-N 1-(2-ethoxypropoxy)propan-2-ol Chemical compound CCOC(C)COCC(C)O QWOZZTWBWQMEPD-UHFFFAOYSA-N 0.000 description 1
- DJCYDDALXPHSHR-UHFFFAOYSA-N 2-(2-propoxyethoxy)ethanol Chemical compound CCCOCCOCCO DJCYDDALXPHSHR-UHFFFAOYSA-N 0.000 description 1
- YUTGRHOAEOCWTD-UHFFFAOYSA-N 3-(3-propoxypropoxy)propan-1-ol Chemical compound CCCOCCCOCCCO YUTGRHOAEOCWTD-UHFFFAOYSA-N 0.000 description 1
- QQKKFVXSQXUHPI-NBVRZTHBSA-N Acidissiminol epoxide Chemical compound O1C(C)(C)C1CC(O)C(/C)=C/COC(C=C1)=CC=C1CCNC(=O)C1=CC=CC=C1 QQKKFVXSQXUHPI-NBVRZTHBSA-N 0.000 description 1
- 244000144927 Aloe barbadensis Species 0.000 description 1
- 235000002961 Aloe barbadensis Nutrition 0.000 description 1
- 244000144725 Amygdalus communis Species 0.000 description 1
- 235000011437 Amygdalus communis Nutrition 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 235000008534 Capsicum annuum var annuum Nutrition 0.000 description 1
- 240000008574 Capsicum frutescens Species 0.000 description 1
- XTJFFFGAUHQWII-UHFFFAOYSA-N Dibutyl adipate Chemical compound CCCCOC(=O)CCCCC(=O)OCCCC XTJFFFGAUHQWII-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- CCLQKVKJOGVQLU-QMMMGPOBSA-N L-homocarnosine Chemical compound NCCCC(=O)N[C@H](C(O)=O)CC1=CNC=N1 CCLQKVKJOGVQLU-QMMMGPOBSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 235000019687 Lamb Nutrition 0.000 description 1
- 206010049565 Muscle fatigue Diseases 0.000 description 1
- 208000029549 Muscle injury Diseases 0.000 description 1
- 102000003505 Myosin Human genes 0.000 description 1
- 108030001204 Myosin ATPases Proteins 0.000 description 1
- 108700016464 N-acetylcarnosine Proteins 0.000 description 1
- 108090000189 Neuropeptides Proteins 0.000 description 1
- 102000003797 Neuropeptides Human genes 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 235000002725 Olea europaea Nutrition 0.000 description 1
- 244000025272 Persea americana Species 0.000 description 1
- 235000011236 Persea americana var americana Nutrition 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000269435 Rana <genus> Species 0.000 description 1
- FCHAMFUEENBIDH-UHFFFAOYSA-N Severin Natural products CC1CCC2C(C)C3CCC4(O)C(CC5C4CC(O)C6CC(CCC56C)OC(=O)C)C3CN2C1 FCHAMFUEENBIDH-UHFFFAOYSA-N 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- 235000018936 Vitellaria paradoxa Nutrition 0.000 description 1
- 241001135917 Vitellaria paradoxa Species 0.000 description 1
- GELXFVQAWNTGPQ-UHFFFAOYSA-N [N].C1=CNC=N1 Chemical group [N].C1=CNC=N1 GELXFVQAWNTGPQ-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 230000037374 absorbed through the skin Effects 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000008168 almond oil Substances 0.000 description 1
- 235000011399 aloe vera Nutrition 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000002280 amphoteric surfactant Substances 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 239000010478 argan oil Substances 0.000 description 1
- 230000000386 athletic effect Effects 0.000 description 1
- 230000037147 athletic performance Effects 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 208000029560 autism spectrum disease Diseases 0.000 description 1
- 229940000635 beta-alanine Drugs 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 235000014121 butter Nutrition 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000012707 chemical precursor Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000008602 contraction Effects 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 231100000223 dermal penetration Toxicity 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 229940100539 dibutyl adipate Drugs 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 230000009189 diving Effects 0.000 description 1
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000002360 explosive Substances 0.000 description 1
- 210000001512 fast-twitch muscle fiber Anatomy 0.000 description 1
- 239000013020 final formulation Substances 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229960005150 glycerol Drugs 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 1
- 108700002498 homocarnosine Proteins 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 150000002433 hydrophilic molecules Chemical class 0.000 description 1
- 230000001146 hypoxic effect Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 210000002510 keratinocyte Anatomy 0.000 description 1
- 229940070765 laurate Drugs 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 229960002337 magnesium chloride Drugs 0.000 description 1
- 235000011147 magnesium chloride Nutrition 0.000 description 1
- 229960005336 magnesium citrate Drugs 0.000 description 1
- 235000002538 magnesium citrate Nutrition 0.000 description 1
- 239000004337 magnesium citrate Substances 0.000 description 1
- OVGXLJDWSLQDRT-UHFFFAOYSA-L magnesium lactate Chemical compound [Mg+2].CC(O)C([O-])=O.CC(O)C([O-])=O OVGXLJDWSLQDRT-UHFFFAOYSA-L 0.000 description 1
- 239000000626 magnesium lactate Substances 0.000 description 1
- 235000015229 magnesium lactate Nutrition 0.000 description 1
- 229960004658 magnesium lactate Drugs 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- 230000003020 moisturizing effect Effects 0.000 description 1
- 239000002858 neurotransmitter agent Substances 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229960003975 potassium Drugs 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011736 potassium bicarbonate Substances 0.000 description 1
- 235000015497 potassium bicarbonate Nutrition 0.000 description 1
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 1
- 239000001508 potassium citrate Substances 0.000 description 1
- 229960002635 potassium citrate Drugs 0.000 description 1
- QEEAPRPFLLJWCF-UHFFFAOYSA-K potassium citrate (anhydrous) Chemical compound [K+].[K+].[K+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O QEEAPRPFLLJWCF-UHFFFAOYSA-K 0.000 description 1
- 235000011082 potassium citrates Nutrition 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 210000003314 quadriceps muscle Anatomy 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000029058 respiratory gaseous exchange Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000009758 senescence Effects 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 210000002807 slow-twitch muscle fiber Anatomy 0.000 description 1
- 230000037078 sports performance Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 229940100611 topical cream Drugs 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 229940025703 topical product Drugs 0.000 description 1
- 230000007723 transport mechanism Effects 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 229940074410 trehalose Drugs 0.000 description 1
- PLSARIKBYIPYPF-UHFFFAOYSA-H trimagnesium dicitrate Chemical compound [Mg+2].[Mg+2].[Mg+2].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O.[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O PLSARIKBYIPYPF-UHFFFAOYSA-H 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/05—Dipeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/06—Aluminium, calcium or magnesium; Compounds thereof, e.g. clay
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/19—Cosmetics or similar toiletry preparations characterised by the composition containing inorganic ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/49—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Neurology (AREA)
- Diabetes (AREA)
- Birds (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Dermatology (AREA)
- Inorganic Chemistry (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Neurosurgery (AREA)
- Psychiatry (AREA)
- Gastroenterology & Hepatology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Emergency Medicine (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hospice & Palliative Care (AREA)
- Rheumatology (AREA)
- Endocrinology (AREA)
- Dispersion Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
La presente divulgación se refiere a una composición que comprende un complejo de carnosina-magnesio. La composición está diseñada para aplicarse sobre la piel y provoca un aumento de los niveles de carnosina en el cuerpo. La composición tópica que comprende un complejo de carnosina-magnesio tiene el efecto de mejorar el rendimiento físico de un atleta y puede ser eficaz para el tratamiento de una variedad de afecciones médicas. También se describe un método para preparar el complejo de carnosina-magnesio. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Composición para su uso tópico a base de un complejo carnosina-magnesio
Campo técnico
La presente divulgación se refiere a composiciones para su uso tópico, tales como productos de gel-crema, particularmente a una composición transdérmica tópica y a un método para suministrar nutrientes y/u otras sustancias a través de la piel.
Específicamente, la presente divulgación se refiere a un complejo carnosina-magnesio para su uso tópico. El complejo carnosina-magnesio puede absorberse a través de la piel y puede tener, entre otros, el efecto de mejorar el rendimiento físico de un atleta. Además, pueden mejorarse varias enfermedades en las que se produce una caída del pH o una oxidación patológica.
Antecedentes de la técnica
La carnosina (p-alanil-L-histidina) es un compuesto natural que contiene histidina que se encuentra en muchos tejidos animales, incluyendo el músculo esquelético, que es la fuente más abundante. La carnosina es un dipéptido multifuncional con un peso molecular de 226,23 Da. Es muy hidrófilo y tiene un coeficiente de partición (log P) de -2,972 ± 0,436 (SciFinder-Scholar: Advanced Chemistry Development (ACD/labs) Software v8.14 de Solaris, TM 2007).
La estructura molecular de la carnosina se muestra a continuación:
Es un ligando polidentado que tiene varios sitios de unión potenciales: dos átomos de nitrógeno de imidazol, un grupo ácido carboxílico y un grupo amino.
Es capaz de formar complejos metálicos con una diversidad de iones metálicos, por ejemplo, con Ni2+, Mn2+, Cd2+, Ca2+, Sr2+ y Mg2+.
Con el fin de formar un complejo con Mg2+, la carnosina se pone en solución acuosa donde se desprotona la función carboxílica de la carnosina (pK = 2,6) (E. J. Baran, Biochemistry, 2000, 65, 7, 789-797) para formar una especie aniónica con carga negativa:
En presencia de una sal de magnesio, la coordinación con el magnesio se produce a través de la interacción de la función carboxílica y el nitrógeno Ni del anillo de imidazol para formar un complejo catiónico carnosina-magnesio 1:1 con una constante de estabilidad del orden de 103 (E. J. Baran, Metal Complexes of Carnosine, Biochemistry, 2000, 65,7, 789-797; G. R. Lenz y A. E. Martell, Biochemistry, 1964, 3, 750-753):
La carnosina es un constituyente de varios tejidos y tiene numerosas funciones biológicas. Por ejemplo, la carnosina se usa en la regulación enzimática y en la regulación del calcio del retículo sarcoplásmico (G. Begum, et al., Journal of Sport Nutrition and Exercise Metabolism, 2005, 15, 493-514). También es capaz de actuar como tampón de pH y como antioxidante.
La carnosina se descompone en el cuerpo por la enzima carnosinasa que se encuentra en la mayoría de los tejidos excepto en el músculo esquelético. Esto explica parcialmente las concentraciones elevadas de carnosina que se encuentran en el músculo esquelético.
La concentración de carnosina en el músculo esquelético humano varía generalmente de 5 a 10 mM (peso húmedo) o de 15 a 40 mmol/kg (peso seco). Las concentraciones difieren de una especie animal a otra, en parte debido a las diferencias en la masa muscular. Por ejemplo, se ha publicado que los caballos tienen concentraciones de carnosina más altas que los perros galgos.
Los niveles de carnosina normalmente son más altos en las fibras musculares de contracción rápida en comparación con las fibras musculares de contracción lenta, lo que está en línea con la observación de que los animales que esprintan con frecuencia, tienen reacciones de vuelo explosivas o experimentan inmersiones hipóxicas prolongadas, tienen concentraciones iniciales de carnosina más altas. También se encontró que los atletas humanos implicados en deportes anaeróbicos, tales como los velocistas y los culturistas, tienen concentraciones intramusculares de carnosina más altas. Se publicó que el entrenamiento físico aumenta las concentraciones de carnosina muscular en este tipo de atletas según lo observado por Goebel et al. para seis sujetos masculinos que realizaron entrenamiento de velocidad dos veces por semana durante un total de 16 sesiones de entrenamiento. Se recogieron muestras musculares del vasto lateral una semana antes del entrenamiento y nuevamente dos días después del protocolo de entrenamiento. Los resultados revelaron que el contenido de carnosina muscular y el resultado de potencia media aumentaron significativamente después de las ocho semanas de entrenamiento (A. S. B. Goebel et al., Skin Pharmacology and Physiology, 2012, 25: 281-287). La carnosina se descubrió por primera vez como un tampón de pH intracelular en 1953 por Severin y sus colegas usando tejido muscular de rana (S. E. Severin, Effect of carnosine and anserine on action of isolated frog muscles - artículo en ruso - Dokl Akad Nauk SSSR 91: 691-694, 1953). A partir de entonces le siguieron estudios posteriores que examinaron esta relación en el tejido muscular humano. Cuando se implican músculos esqueléticos en ejercicio moderado a intenso, normalmente se genera ácido láctico. Este posteriormente se disocia en lactato y H+. La producción de protones puede alterar los niveles de pH y se sabe que la mayoría de los protones producidos en la sangre durante el ejercicio son tamponados por el sistema tamponante de bicarbonato. El pKa de este sistema es de 6,1, que es menor que el de la carnosina (pKa de 6,83) y, por lo tanto, se necesita un mayor cambio de pH para obtener beneficios de este sistema. Puesto que el pKa de la carnosina está más cerca del pH fisiológico, es probable que esta molécula actúe como un tamponante primario durante el ejercicio de alta intensidad. De hecho, el grupo imidazol del resto histidina de la carnosina lo hace especialmente eficaz como tamponante, teniendo un valor de pKa cercano al pH intracelular, ya que uno de los átomos de nitrógeno del anillo de imidazol puede utilizarse para aceptar un protón (A. A. Boldyrev et al., Physiol Rev 93, 1803-1845, 2013).
Un estudio realizado por Sewell y asociados (D. A. Sewell et al., Equine Exercise Physiol 3, 276-280, 1991) examinó específicamente la capacidad tamponante de la carnosina en diferentes tipos de fibras de caballo. Se encontró que la carnosina contribuía con aproximadamente el 20 % del tamponamiento en las fibras de tipo I y hasta el 46 % en las fibras de tipo IIb. Estos hallazgos son consistentes con la observación de que se acumula menos ácido láctico en las fibras de tipo I debido a la actividad muscular de menor intensidad asociada a este tipo de fibra.
Aparte de los efectos tamponantes, se ha encontrado que la carnosina tiene otras funciones fisiológicas. Por ejemplo, es capaz de actuar como un antioxidante eficaz contra el estrés oxidativo. Durante el ejercicio, pueden producirse especies reactivas de oxígeno (ERO) debido al aumento de la respiración (lo que provoca un aumento en el flujo de electrones en el sistema de transporte electrónico) o debido a una disminución del pH (conduciendo a que se libere oxígeno de la hemoglobina dando como resultado una pO2 aumentada en los tejidos). Algunos creen que la producción de ERO está relacionada con la fatiga muscular durante la actividad. La carnosina también está vinculada a la regulación enzimática relacionada con la activación de la miosina ATPasa, que se usa para ayudar a
mantener las reservas de ATP.
Por último, se ha descubierto que la carnosina desempeña una función en el acoplamiento de la contracción de electrones (C-E) en el músculo esquelético. Un estudio temprano de Lamont y Miller (C. Lamont et al., J Physiol 454, 421-434, 1992) mostró que la presencia de 15 mM de carnosina dio como resultado un aumento significativo en sensibilidad a Ca2+ en las fibras musculares de Rana Temporaria. Más recientemente, Dutka y Lamb (T. L. Dutka et al., J Muscle Res Cell Motil, 25, 203-213, 2004) examinó si la carnosina afecta al acoplamiento C-E en fibras funcionales en condiciones fisiológicas. Usaron fibras musculares extensoras largas de dedos de rata desolladas mecánicamente. Sus resultados mostraron que la carnosina no afectó a la liberación de Ca2+ del retículo sarcoplásmico; sin embargo, la carnosina fue capaz de aumentar la sensibilidad a Ca2+ de los componentes contráctiles de las fibras musculares. Se sugirió que un aumento en la sensibilidad a Ca2+ podría ayudar a mantener la producción de fuerza en las últimas fases de la fatiga una vez que la liberación de Ca2+ comienza a disminuir. Por lo tanto, niveles más altos de carnosina pueden ayudar a compensar la disminución de Ca2+ así como la acumulación de iones H+ durante el ejercicio de alta intensidad.
Teniendo en cuenta que la carnosina ayuda a controlar las concentraciones de Ca2+ y ácido láctico, actuando además como un antioxidante eficaz contra el estrés oxidativo, la formulación de un producto tópico que aumente la concentración de carnosina en el organismo sería de interés cosmético y farmacéutico notable.
Se entiende bien que con el fin de que un medicamento actúe, el principio activo contenido en el medicamento debe suministrarse al sitio de acción específico en una concentración eficaz y en el momento adecuado. Aunque estos requisitos se aplican a todos los tipos de principios activos, son particularmente importantes en la ciencia dermocosmética para principios activos que tienen funcionalidad tópica (J. W. Wiechers; Skin Delivery: What It Is and Why We Need It; Science and Applications of Skin Delivery Systems; 2008).
Un principio activo que se aplica por vía tópica a la piel debe ser capaz de penetrar la barrera superior de la piel, el estrato córneo (EC), antes de ser suministrado a su sitio de acción en las concentraciones necesarias. Sin embargo, aparte de los mecanismos de transporte específicos, en general, debido a las propiedades lipófilas del EC, las moléculas hidrófilas no son capaces de penetrar el estrato córneo eficazmente. Por lo tanto, obtener la biodisponibilidad cutánea de principios activos hidrófilos, como péptidos o sustancias similares a péptidos es un reto (A. S. B. Goebel et al. Skin Pharmacol Physiol 2012, 25, 281-287).
Moléculas potenciadoras tales como 1,2-pentilenglicol (PG) o etoxidiglicol (Transcutol) pueden aumentar la penetración dérmica de los péptidos mejorando su biodisponibilidad. De hecho, se publicó que la adición de PG a una preparación que contiene L-carnosina o N-acetil-L-carnosina dio como resultado un aumento significativo de la sustancia dentro del EC (A. S. B. Goebel et al., Skin Pharmacology and Physiology, 2012, 25: 281-287). Se detectaron concentraciones de dipéptido de aproximadamente 6 veces y más en el EC y en las capas viables de la piel en comparación con la formulación sin la molécula potenciadora.
El producto "Pulverización de protección y regeneración de la piel (Protection and Regeneration Spray for the Skin)" (registro Mintel ID 2426239) describe una pulverización de protección y regeneración para la piel que contiene carnosina y sulfato de magnesio.
El documento JP H04 178314 divulga un cosmético que contiene un derivado de L-carnosina, homocarnosina, su derivado o una de sus sales como componente activo.
El documento WO-A-2015/026954 se refiere a métodos de mantenimiento o mejora del rendimiento táctico y/o el rendimiento psicomotor, en donde se administra beta-alanina, o una sal o éster de la misma, a un individuo.
El documento WO-A-02/26940 divulga un método de alteración de la senescencia de las células que comprende aplicar a dichas células una cantidad eficaz de una composición en donde dicha composición incluye N-acetilcarnosina como principio activo.
A pesar de algunos avances, existe una necesidad en la técnica de una formulación tópica que sea capaz de aumentar la concentración de carnosina en el cuerpo.
Sumario de la invención
Los presentes inventores han encontrado inesperadamente que la presencia de iones de magnesio (Mg2+) coordinados con carnosina, produce un aumento significativo en el nivel de carnosina en la capa de piel inferior después de la aplicación en la piel. Adicionalmente, se encontró que una composición que contiene una cantidad fisiológicamente activa de un complejo carnosina-magnesio aplicada en la piel de los atletas, mejoró considerablemente el rendimiento físico de los atletas.
Un aspecto de la presente divulgación, por lo tanto, se refiere a una composición tópica que comprende una cantidad fisiológicamente activa de un complejo carnosina-magnesio, en donde la cantidad fisiológicamente activa
representa una cantidad de un complejo carnosina-magnesio del 0,5 al 5 % en peso de la composición tópica. La composición tópica puede estar en forma de un gel, una crema, una solución, una pomada, una pasta, una loción, un parche, una pulverización o una espuma. Preferentemente, la composición tópica está en forma de un gel. La composición tópica puede comprender aditivos seleccionados del grupo que comprende un lubricante, un portador, un agente espesante, un conservante, un tensioactivo, un humectante y un agente emoliente. También puede comprender un agente de calentamiento.
Además, el objeto de la presente divulgación es el uso de una composición tópica que comprende una cantidad fisiológicamente activa de un complejo carnosina-magnesio para mejorar el rendimiento físico de un atleta.
Descripción detallada de la invención
La presente divulgación se refiere a un producto de gel que contiene una cantidad fisiológicamente activa de un complejo carnosina-magnesio, que puede ser absorbido por el cuerpo a través de la aplicación en la piel y puede tener el efecto de mejorar el rendimiento físico de un atleta. En otras palabras, mediante la formación de un complejo con magnesio, puede suministrarse carnosina a través de la piel y puede llegar a su sitio de acción, tal como el tejido muscular esquelético.
Además, el complejo carnosina-magnesio puede actuar como agente tamponante, en particular, como tampón intracelular y/o intersticial, capaz de tamponar el pH y/o capaz de prevenir la acumulación de H+.
Específicamente, la presente divulgación se refiere a una composición tópica que comprende una cantidad fisiológicamente activa de un complejo carnosina-magnesio, en donde la cantidad fisiológicamente activa representa una cantidad de un complejo carnosina-magnesio del 0,5 al 5 % en peso de la composición tópica.
La composición tópica puede estar en forma de un gel, una crema, una solución, una pomada, una pasta, una loción, un parche, una pulverización o una espuma o en cualquier otra forma que sea adecuada para su aplicación en la piel. Preferentemente, la composición tópica está en forma de un gel.
La expresión "cantidad fisiológicamente activa", como se usa en el presente documento, puede indicar, en particular, una cantidad de un principio activo, tal como carnosina o un complejo carnosina-magnesio, que desencadenará la respuesta biológica o médica que busca el usuario.
El complejo carnosina-magnesio está presente en la composición tópica en una cantidad que varía del 0,5 al 5 % en peso de la composición tópica, lo que representa una cantidad fisiológicamente activa del complejo carnosinamagnesio. En particular, el complejo carnosina-magnesio puede estar presente en la composición tópica en una cantidad que varía del 0,6 al 4,5 % en peso, en particular, del 0,7 al 4 % en peso, en particular, del 0,75 al 3,5 % en peso, en particular, del 0,8 al 3 % en peso, tal como del 0,85 al 2,84 % en peso, de la composición tópica.
En una realización, la composición tópica puede comprender un componente potenciador de la absorción en la piel. El potenciador de la absorción en la piel también puede denominarse portador, en particular portador para el complejo carnosina-magnesio, lo que puede facilitar el transporte del complejo carnosina-magnesio a través de la piel.
El agente o portador de absorción en la piel puede comprender, en particular, un alcohol de éter, un alcohol alifático o éster o mezclas de los mismos, en particular, un alcohol de éter o una mezcla de alcoholes de éter. En particular, el portador puede comprender uno o más compuestos seleccionados del grupo que consiste en 2-(2-etoxietoxi)etanol, 3-(3-propoxipropoxi)-1-propanol, 2-(2-propoxietoxi)etanol, 1-(1-metil-2-propoxietoxi)propan-2-ol, 1-(2-etoxipropoxi)-2-propanol, 1,2-pentilenglicol, propilenglicol, alcoholes de cadena corta y larga tales como alcoholes y ésteres etílicos, propílicos, isopropílicos, miristílicos, laurílicos y octílicos, tales como salicilato de octilo y miristato de isopropilo. Preferentemente, el agente o portador de absorción en la piel puede comprender en particular 2-(2-etoxietoxi)etanol, también conocido como etoxidiglicol (Transcutol). El componente de absorción en la piel puede estar presente en la composición tópica en una cantidad que varía del 0,5 al 4 % en peso, en particular, del 0,75 al 3,5% en peso, tal como del 1,0 al 3% en peso, de la composición tópica. En una realización adicional, la composición tópica puede comprender uno o más componentes seleccionados del grupo que comprende un lubricante, un portador, un agente espesante, un conservante, un tensioactivo, agua, un agente humectante y un agente emoliente.
Los lubricantes pueden seleccionarse del grupo que comprende aceites de silicona, propil-eptil-caprilato, carbonato de dicaprililo, dicaprilil éter, cocoato de etilesilo, miristato de isopropilo, laurato de exilo, adipato de dibutilo y adipato de isopropilo, y mezclas de los mismos.
Un lubricante puede estar presente en la composición tópica en una cantidad que varía del 1 al 20 % en peso de la composición tópica.
Los portadores pueden seleccionarse del grupo que comprende dióxido de silicio, dióxido de titanio, óxido de cinc y
copolímeros de acrilato y mezclas de los mismos. Un portador puede estar presente en la composición tópica en una cantidad que varía del 0,2 al 6 % en peso de la composición tópica, preferentemente en una cantidad que varía del 0,4 al 0,2 % en peso de la composición tópica.
Un agente espesante puede seleccionarse del grupo que comprende goma de esclerocio, goma xantana, goma guar, pectina, agar agar, etoxietilcelulosa, hidroxietilcelulosa, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, ácidos hialurónicos y mezclas de los mismos.
Un agente espesante puede estar presente en la composición tópica en una cantidad que varía del 0,1 al 4% en peso de la composición tópica, preferentemente en una cantidad que varía del 0,2 al 2 % en peso de la composición tópica.
Un conservante puede seleccionarse del grupo que comprende fenoxietanol, etilhexilglicerina, ácido benzoico, sales benzoicas, ésteres benzoicos, ácido sórbico y sales sórbicas, ácido deshidroacético y sales deshidroacéticas, y mezclas de los mismos.
Un conservante puede estar presente en la composición tópica en una cantidad que varía del 0,1 al 1,5 % en peso de la composición tópica, preferentemente en una cantidad que varía del 0,4 al 0,8 % en peso de la composición tópica.
Un tensioactivo puede seleccionarse del grupo que comprende tensioactivos catiónicos tales como sales de amonio cuaternario, tensioactivos aniónicos tales como laurilsulfato de sodio, tensioactivos no iónicos tales como alquilpoliglucósido o tensioactivos anfóteros tales como cocamidopropilbetaína.
Un tensioactivo puede estar presente en la composición tópica en una cantidad que varía del 0,05 al 2 % en peso de la composición tópica, preferentemente en una cantidad que varía del 0,1 al 1 % en peso de la composición tópica. Un agente humectante puede seleccionarse del grupo que comprende glicerina, pentilenglicol, ácido hialurónico, trehalosa, linositol y mezclas de los mismos.
Un agente humectante puede estar presente en la composición tópica en una cantidad que varía del 0,5 al 5 % en peso de la composición tópica, preferentemente en una cantidad que varía del 1 al 3 % en peso de la composición tópica.
Un emoliente puede seleccionarse del grupo que comprende aceite de almendras dulces, aloe vera, mantequilla de Butyrospermum parkii, aceite de Olea europea, aceite de argán, aceite de Persea gratissima, aceite de coco y mezclas de los mismos.
Un emoliente puede estar presente en la composición tópica en una cantidad que varía del 1 al 10 % en peso de la composición tópica, preferentemente en una cantidad que varía del 2 al 4 % en peso de la composición tópica. Puede haber presente agua en la composición tópica en una cantidad que varía del 60 al 95 % en peso de la composición tópica, preferentemente en una cantidad que varía del 80 al 95 % en peso de la composición tópica. La composición tópica de la presente divulgación puede modificarse introduciendo un componente que tiene el efecto de calentar la piel durante la aplicación. Este componente se denomina agente de calentamiento.
Por lo tanto, la composición tópica de la presente divulgación puede comprender un agente de calentamiento. El agente de calentamiento puede elegirse de cualquier agente de calentamiento adecuado conocido en la técnica. Los ejemplos de agentes de calentamiento que pueden emplearse en la composición tópica de la presente divulgación incluyen agentes de calentamiento seleccionados del grupo que comprende nicotinato de metilo, nicotinato de etilo, nicotinato de hexilo, nicotinato de bencilo, nicotinato de tocoferilo, oleorresina de Capsicum annuum, aceite de corteza de Cinnamomum camphora, salicilato de metilo y mezclas de los mismos.
En una realización de la presente divulgación, puede haber presente un nicotinato en la composición tópica en una cantidad de entre el 0,05 - 0,1 % en peso de la composición tópica.
En otra realización de la presente divulgación, puede haber presente oleorresina de Capsicum annuum en la composición tópica en una cantidad de entre el 0,5-1 % en peso de la composición tópica.
En una realización adicional de la presente divulgación, el aceite de corteza de Cinnamomum camphora puede estar presente en la composición tópica en una cantidad del 1-10 % en peso de la composición tópica.
En otra realización, puede haber presente salicilato de metilo en la composición tópica en una cantidad del 1-10 % en peso de la composición tópica.
En una realización, la composición tópica puede comprender además creatina y/o carnitina, en particular, un complejo creatina-magnesio y/o un complejo carnitina-magnesio. En otras palabras, la composición tópica puede
comprender una combinación de un complejo carnosina-magnesio con un complejo creatina-magnesio y/o un complejo carnitina-magnesio, que puede proporcionar un efecto particular pronunciado, o incluso un efecto sinérgico, de mejora del rendimiento físico de un atleta. La creatina puede actuar como un tamponante extracelular, si se combina con carnosina, tiene un efecto sinérgico y mejora el rendimiento deportivo proporcionando tampones tanto intracelulares como extracelulares. La carnitina podría sinergizar con la carnosina a través de su papel en la producción de energía, así como en el tratamiento de los trastornos del espectro autista.
En una realización, la composición tópica puede comprender además bicarbonato de sodio, que puede tamponar el L-tartrato de L-carnitina altamente ácido y conferir un beneficio adicional como tamponante extracelular. En particular, el bicarbonato de sodio puede servir como un tamponante extracelular cuando se combina con la carnosina y mejoraría con la capacidad de la carnosina para mitigar el hidrógeno, este tampón extracelular no de bicarbonato mejoraría la eficacia del bicarbonato de sodio mitigando la liberación de iones H+ provenientes de la titulación por retroceso de los tampones no de bicarbonato.
En una realización, la composición tópica puede comprender además 5-hidroxitriptófano (5-HTP) también conocido como oxitriptán. El 5-HTP es un aminoácido de origen natural y un precursor químico, así como un intermediario metabólico en la biosíntesis de los neurotransmisores serotonina. Por lo tanto, la carnosina, un neuropéptido citoplasmático conocido, podría ayudar en el suministro por vía tópica de 5-HTP.
En una realización, la composición tópica puede comprender además potasio en formas que incluyen, pero sin limitación, citrato de potasio o bicarbonato de potasio. Una formulación de este tipo podría ayudar a retrasar la caída del pH intersticial durante el ejercicio de moderado a intenso. La mejora en el entorno de pH extracelular podría mejorar el equilibrio de K+ y evitar una caída en el flujo sanguíneo durante la aparición de la fatiga.
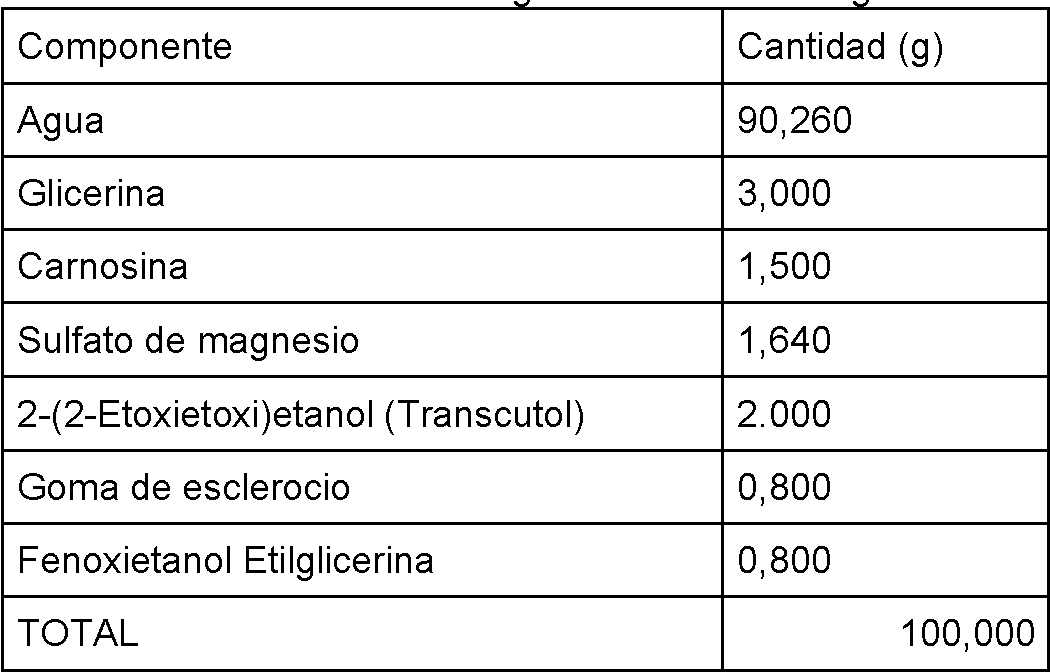
Una composición de ejemplo de la composición tópica proporcionada en forma de gel viene dada por los siguientes ingredientes (en porcentaje en peso):
, ,
La composición tópica que comprende un complejo carnosina-magnesio puede evitar la hidrólisis por carnosinasa y puede servir como tampón de pH.
El complejo carnosina-magnesio de la presente divulgación puede prepararse combinando una sal de magnesio, una solución acuosa y carnosina. Preferentemente, la sal de magnesio se añade a la solución acuosa que contiene carnosina. Preferentemente, se usa una cantidad estequiométrica de una sal de magnesio.
Las sales de magnesio adecuadas incluyen sulfato de magnesio o cloruro de magnesio o citrato de magnesio o lactato de magnesio. Preferentemente, la sal de magnesio es sulfato de magnesio. Preferentemente, la solución acuosa es agua.
La concentración de la sal de magnesio en la solución acuosa está en el intervalo entre el 1 y el 10 % en peso, preferentemente en el intervalo entre el 1 y el 5 % en peso.
La concentración de la carnosina en la solución acuosa está en el intervalo entre el 1 y el 10 % en peso, preferentemente en el intervalo entre el 1 y el 5 % en peso.
Una vez que la carnosina y la sal de magnesio están en contacto entre sí en una solución acuosa a temperatura ambiente, el complejo carnosina-magnesio se forma casi instantáneamente.
Una vez formado, el complejo carnosina-magnesio puede usarse para preparar una composición tópica. La composición tópica puede prepararse agitando los componentes diferentes.
El complejo carnosina-magnesio puede usarse para aumentar la concentración de carnosina en las capas inferiores de la piel. Dichas capas de la piel incluyen, por ejemplo, la epidermis.
El complejo carnosina-magnesio de la presente divulgación puede usarse para aumentar el rendimiento deportivo de un sujeto, tal como la duración del esfuerzo, la velocidad y la recuperación muscular. La presente divulgación puede mejorar muchas afecciones médicas, en particular, cuando se produce una caída del pH o una oxidación patológica.
Además, el objeto de la presente divulgación es el uso de una composición tópica que comprende un complejo carnosina-magnesio para aumentar la concentración de carnosina en las capas inferiores de la piel, tales como la epidermis.
La composición tópica de la presente divulgación también puede usarse para aumentar el rendimiento atlético (físico) de un sujeto.
La composición tópica de la presente divulgación es para su aplicación en la piel. Puede aplicarse en la piel de cualquier parte del cuerpo, pero es más adecuado para aplicarse a las piernas, brazos, torso.
Cuando la composición tópica que comprende un complejo carnosina-magnesio se aplica en la piel, después de 24 horas, entre el 0,0033 % y el 0,02 % de la carnosina aplicada en la piel puede atravesar la capa de piel de un modelo de epidermis humana reconstruida EpiDerm™ y puede encontrarse en el medio.
Cuando la composición tópica que comprende un complejo carnosina-magnesio se aplica en la piel, después de 48 horas, entre el 0.005 % y el 0,01 % de la carnosina aplicada en la piel puede atravesar la capa de piel de un modelo de epidermis humana reconstruida EpiDerm™ y puede encontrarse en el medio.
Cuando la composición tópica que comprende un complejo carnosina-magnesio se aplica en la piel, después de 24 horas entre el 0,033 % y el 0,01 % de la carnosina aplicada en la piel puede encontrarse en los homogeneizados del modelo de piel del modelo de epidermis humana reconstruida EpiDerm™. Cuando la composición tópica que comprende un complejo carnosina-magnesio se aplica en la piel, después de 48 horas, entre 0,05 % y 0,07 % de la carnosina aplicada en la piel puede encontrarse en los homogeneizados del modelo de piel del modelo de epidermis humana reconstruida EpiDerm™.
Las múltiples capas de la composición tópica pueden aplicarse en un área de la piel. Preferentemente, se aplican entre 1 y 5 capas de la composición tópica en un área de la piel, más preferentemente se aplican entre 1 y 3 capas de la composición tópica en un área de la piel.
La una o más capas de composición tópica pueden aplicarse en la piel de 1 a 5 veces al día, preferentemente de 1 a 3 veces al día. La composición tópica puede aplicarse en la piel en cualquier momento del día y antes, después o durante el ejercicio. Preferentemente, la composición tópica se aplica en la piel antes y después del ejercicio.
La composición tópica puede aplicarse en la piel en cualquier época del año y a cualquier temperatura ambiente. La composición tópica de la presente divulgación puede usarse según sea necesario durante el tiempo que se requiera.
La composición tópica de la presente divulgación puede ser utilizada por sujetos adultos de todos los sexos y etnias. Sección experimental
Materiales y métodos
En los experimentos se usaron las siguientes tres muestras:
Muestra A: Complejo carnosina-magnesio en la formulación de gel final (que tiene la formulación que se indica a continuación en la Tabla 1):
T l 1: F rm l i n l rn in -m n i
Muestra B: Carnosina libre, en la formulación de gel final como para la muestra A.
Muestra C: Formulación de gel final pero sin el principio activo carnosina Todas las muestras son formulaciones de gel.
Ejemplo 1
Evaluación de la penetración transepidérmica del complejo carnosina-magnesio en formulación de gel en modelos 3D de piel
El objetivo de los experimentos descritos es investigar el suministro de L-carnosina en la piel humana mediante la formulación de gel que contiene L-carnosina en asociación con magnesio, que forma un complejo monocatiónico (complejo carnosina-magnesio), con el objetivo de mejorar la biodisponibilidad. La investigación se realizó usando una preparación exenta de carnosina como producto de referencia (S. E. Severin et al. Effect of carnosine and anserine on action of isolated frog muscles (artículo en ruso). Dokl Akad Nauk SSSR 91: 691-694, 1953).
Modelo de epidermis humana reconstruida (EHR) EpiDerm™ y tratamientos
Se usó epidermis humana reconstruida (EHR) como modelo de tejido de piel humana. El modelo de tejido EpiDerm™ se adquirió en MatTek (MatTek In Vitro Life Science Laboratories, Bratislava, República Eslovaca). Tras la recepción, los tejidos se transfirieron a Medio de mantenimiento SkinEthic™ y se mantuvieron a 37 °C en una atmósfera de CO2 al 5 % humidificada.
El modelo de epidermis humana reconstruida (EHR) EpiDerm™ consiste en un tejido epidérmico tridimensional que crece en la interfaz aire-líquido a partir de queratinocitos humanos normales. El modelo es histológicamente similar a la epidermis humana, teniendo todas las capas celulares diferenciadas, y una barrera de permeabilidad funcional. Antes de realizar los tratamientos, el medio se retiró y se añadió medio nuevo. Para los tratamientos, se aplicaron 10 μl de las tres mezclas diferentes (A: complejo de carnosina; B: carnosina libre sin el potenciador; C: vehículo) cada una por vía tópica sobre tejidos de EHR separados, ya sea en una dosis única durante 24 h o en una aplicación repetida cada 24 h durante un total de 48 h. El tejido de control solo se expuso al medio. Puesto que no se observaron diferencias entre las dosis aplicadas a las 24 y 48 h para los tejidos control, las muestras se agruparon y se presentaron como el grupo de control. Todas las mezclas y muestras de control se analizaron por triplicado usando tres conjuntos de EHR para cada grupo.
Después de 24 o 48 h de tratamiento, se recogieron alícuotas de medio tisular y se centrifugaron durante 20 minutos para retirar las impurezas insolubles y los residuos de tejido a 1000xg a 4 °C. Los sobrenadantes transparentes se almacenaron a -20 °C hasta su análisis. Después de lavar con PBS y ultracongelar en nitrógeno líquido, los tejidos de EHR se homogeneizaron en un recipiente de vidrio con 150 μl de PBS en hielo. Después, los homogeneizados se centrifugaron durante 5 minutos a 5000xg para obtener los sobrenadantes que se almacenaron a -20 °C hasta su análisis.
ELISA para carnosina
Se determinaron los niveles de carnosina en los medios de cultivo de EHR y los homogeneizados se recogieron en diferentes puntos temporales (24 o 48 h), usando un kit ELISA (ensayo inmunoabsorbente ligado a enzimas) (Elabscience Biotechnology Co., Ltd). El procedimiento se realizó de acuerdo con las instrucciones del fabricante. La absorbancia óptica se midió con un lector de microplacas a 450 nm. Se obtuvo una curva de calibración usando carnosina como patrón. Todas las muestras se sometieron a ensayo por duplicado. El límite inferior de detección para carnosina fue de 8,438 ng/ml. Los resultados se expresan como ng/ml. Los cambios en los niveles de carnosina desde el nivel basal (EHR de control) se compararon sobre la base de un ensayo t de Student. Un valor P < 0,05 se consideró estadísticamente significativo.
Resultados
Los niveles de carnosina se midieron en medios y homogeneizados y los resultados para las tres muestras, A, B y C a las 24 horas (primer punto temporal) y 48 horas (segundo punto temporal) se publican a continuación.
Niveles de carnosina en medios
En el primer punto temporal, después de 24 horas desde el tratamiento, se detectó el nivel más alto de carnosina para la muestra A con un valor P de 0,028 en comparación con el nivel de carnosina en el tejido de control. Incluso si el nivel de carnosina para la muestra B fue más alto que para el tejido de control, estos datos tuvieron un valor P no significativo (p = 0,065).
La comparación entre muestras A y B muestra que el nivel de carnosina detectado en el medio de la muestra A fue significativamente más alto que el nivel de carnosina detectado en el medio de la muestra B (p = 0,043). El nivel de
carnosina detectado en el medio de la muestra C fue comparable a la concentración de carnosina registrada para el tejido de control.
En el segundo punto temporal, después de 48 horas desde el tratamiento, el nivel de carnosina en el medio de la muestra A fue más bajo que el nivel detectado en el primer punto temporal, aunque fue mayor que el nivel de carnosina detectado en el tejido de control.
Los niveles de carnosina en el medio de las muestras. B y C fueron similares a los niveles detectados en el primer punto temporal.
Tabla 2: valores de detección de carnosina en medios
T l : v l r rn in n m i
Niveles de carnosina en lisados de EHR
En el primer punto temporal, el tejido tratado con muestra A tenía un contenido de carnosina significativamente menor que el nivel detectado en el tejido de control (p = 0,019).
En el tejido tratado con la muestra B, el nivel de carnosina aumentó en comparación con el tejido de control, pero este dato no fue significativo (p = 0,708). El nivel de carnosina detectado en el tejido tratado con la muestra C fue similar al del control.
Después de 48 horas, en el segundo punto temporal, los niveles de carnosina detectados fueron equivalentes al control de tejido para todas las muestras.
T l 4: v l r i n rn in n h m n iz
T l : v l r rn in n h m n iz os
Conclusiones
De acuerdo con los datos recogidos, parece que en el primer punto temporal, 24 horas, la preparación A (complejo carnosina-magnesio en la formulación final) mostró un aumento significativo en el suministro de carnosina en la capa inferior de la piel. De hecho, un nivel más alto de carnosina pasó al medio con respecto a la preparación B. Como contraprueba, el contenido de carnosina fue más bajo en el tejido correspondiente.
En el segundo punto temporal, 48 horas, se observó un aumento no significativo en los niveles de carnosina en el medio. Esto puede deberse a las limitaciones del modelo de EHR in vitro, que después de 48 horas pierde sus propiedades iniciales y, por lo tanto, puede ser menos fiable.
Por último, se puede concluir que el complejo carnosina-magnesio fue eficaz para aumentar el suministro de carnosina a través de un modelo 3D de piel.
De hecho, la concentración de carnosina que quedaba en los tejidos fue casi la mitad de la de la muestra que contenía carnosina libre.
Ejemplo 2
Evaluación de los efectos del gel de carnosina-magnesio en futbolistas. Estudio piloto.
El objetivo del estudio piloto fue evaluar, los efectos del complejo carnosina-magnesio presente en una nueva formulación de gel para su uso tópico en los rendimientos de jugadores de fútbol.
o os
El estudio se dividió en dos partes correspondientes a los siguientes ejercicios:
1) un ensayo de recuperación intermitente yo-yo;
2) Ensayo de esprint de 1.000 m repetido 3 veces (1' 30 s entre series).
Se realizaron ensayos para cada atleta con y sin gel de carnosina-magnesio.
Preparación antes del rendimiento con una aplicación de crema de calentamiento
Se usó una crema de calentamiento que contenía guindilla para optimizar la preparación muscular antes de los ensayos. Este tipo de crema de calentamiento se usa habitualmente por los deportistas antes de cualquier actividad física para prevenir lesiones y traumatismos de carácter muscular que pueden producirse durante la actividad física. Diseño del estudio
Se evaluó el rendimiento de 11 atletas adultos entre 18 y 35 años (jugadores de fútbol). Durante la duración del período de ensayo, los atletas no tomaron ningún suplemento dietético, no se trataron con fármacos y se abstuvieron de entrenamientos o competencias adicionales.
Durante una fase previa al estudio, se evaluaron las diferencias entre el rendimiento de los atletas con y sin la crema de calentamiento con el fin de verificar si la crema de calentamiento provocaba algún efecto relevante.
En la fase de estudio, a la aplicación de la crema de calentamiento en las piernas le siguió un tratamiento tópico con gel de carnosina-magnesio usando la muestra A. Durante la fase de estudio, los atletas no realizaron ninguna otra actividad deportiva o competición. Para cada tipo de ejercicio, hubo un retraso de tres días entre el ensayo realizado con la aplicación solamente de la crema de calentamiento y el ensayo con la aplicación de la crema de calentamiento y el gel de carnosina-magnesio (muestra A).
Ensayo de recuperación intermitente yo-yo
En el ensayo yo-yo, el atleta corre entre delimitadores de velocidad colocados a 40 metros de distancia entre sí. La velocidad aumenta regularmente y el ensayo termina cuando el sujeto ya no puede mantener la velocidad. El resultado del ensayo se determina por la distancia recorrida durante el ensayo, y es un ensayo de resistencia.
Ensayo repetitivo de 1000 metros X 3 (1 minuto y 30 segundos de descanso entre cada ensayo)
Se registró el tiempo que tardó un atleta en correr 1000 m. El ensayo se repitió tres veces y se permitió que el atleta descansara durante 1 minuto y treinta segundos entre cada ensayo. El ensayo mide la resistencia.
RESULTADOS
Los resultados del rendimiento de cada atleta individual durante los diferentes ensayos realizados sin aplicación de ninguna crema tópica, después de la aplicación de la crema de calentamiento y después de la aplicación tanto de la crema de calentamiento como del gel de carnosina-magnesio (muestra A), se resumen en las Tablas 6 y 7.
Todos los atletas publicaron satisfacción y buenas sensaciones en las piernas durante y después del ejercicio. No se observaron efectos secundarios locales o sistémicos reconocidos.
Tabla 6: Resultados del ensa o Yo-Yo 40 m
continuación
Tabla 7: Resultados de ensa os re etitivos 1000 metros x 3 1 minuto 30 se undos entre ensa os
Conclusiones
La investigación in vitro mostró que con la aplicación del gel de carnosina-magnesio hubo un aumento significativo en el rendimiento de todos los atletas que participaron en el estudio.
Se observaron mejoras tanto en los ensayos tanto de duración de la velocidad como de resistencia.
Los atletas no publicaron ningún efecto secundario después del tratamiento con gel de carnosina-magnesio.
Claims (12)
1. Una composición tópica que comprende una cantidad fisiológicamente activa de un complejo carnosina-magnesio, en donde la cantidad fisiológicamente activa del complejo carnosina-magnesio representa una cantidad del complejo carnosina-magnesio del 0,5 al 5 % en peso de la composición tópica.
3. La composición tópica de acuerdo con la reivindicación 1 o 2, en donde la composición tópica está en forma de un gel, una crema, una solución, una pomada, una pasta, una loción, un parche, una pulverización o una espuma.
4. La composición tópica de una cualquiera de las reivindicaciones 1 a 3 que comprende además un componente potenciador de la absorción en la piel elegido del grupo que consiste en 1,2-pentilenglicol, etoxidiglicol (Transcutol), propilenglicol, alcoholes etílicos, propílicos, isopropílicos, miristílicos, laurílicos y octílicos, salicilato de octilo y miristato de isopropilo.
5. La composición tópica de una cualquiera de las reivindicaciones 1 a 3 que comprende además un lubricante, un portador, un agente espesante, un conservante, un tensioactivo, agua, un agente humectante y un agente emoliente.
6. La composición tópica de la reivindicación 5, en donde el lubricante se selecciona del grupo que comprende aceites de silicona, propil-heptil-caprilato, carbonato de dicaprililo, dicaprilil éter, cocoato de etilhexilo, miristato de isopropilo, laurato de hexilo, adipato de dibutilo y adipato de isopropilo, y mezclas de los mismos; el portador se selecciona del grupo que comprende dióxido de silicio, dióxido de titanio, óxido de cinc, copolímeros de acrilato y mezclas de los mismos; el agente espesante se selecciona del grupo que comprende goma de esclerocio, goma xantana, goma guar, pectina, agar agar, etoxietilcelulosa, hidroxietilcelulosa, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, ácidos hialurónicos y mezclas de los mismos; el conservante se selecciona del grupo que comprende fenoxietanol, etilhexilglicerina, ácido benzoico, sales benzoicas, ésteres benzoicos, ácido sórbico, sales sórbicas, ácido deshidroacético, sales deshidroacéticas y mezclas de los mismos; y el tensioactivo se selecciona del grupo que comprende sales de amonio cuaternario, laurilsulfato de sodio, alquilpoliglucósido y cocamidopropilbetaína.
7. La composición tópica de una cualquiera de las reivindicaciones 1 a 6 que comprende además un agente de calentamiento seleccionado del grupo que comprende nicotinato de metilo, nicotinato de etilo, nicotinato de hexilo, nicotinato de bencilo, nicotinato de tocoferilo, oleorresina de Capsicum annuum, aceite de corteza de Cinnamomum camphora, salicilato de metilo y mezclas de los mismos.
8. La composición tópica de la reivindicación 7, en donde si hay presente un nicotinato en la composición, está presente en el 0,05 - 0,1 % en peso de la composición; si hay presente oleorresina de Capsicum annuum en la composición, está presente en el 0,5 - 1 % en peso de la composición; si hay presente aceite de corteza de Cinnamomum camphora en la composición, está presente en el 1 - 10 % en peso de la composición; y si hay presente salicilato de metilo en la composición, está presente en el 1 -10 % en peso de la composición.
9. El uso de una composición tópica de acuerdo con una cualquiera de las reivindicaciones 1 a 8 para suministrar carnosina al tejido del músculo esquelético.
10. El uso de una composición tópica de acuerdo con una cualquiera de las reivindicaciones 1 a 8 para mejorar el rendimiento físico de un atleta, en donde el rendimiento físico del atleta es la duración del esfuerzo, la velocidad y la recuperación muscular.
11. El uso de una composición tópica de acuerdo con una cualquiera de las reivindicaciones 1 a 8 para suministrar carnosina a través de la piel.
12. El uso de una composición tópica de acuerdo con la reivindicación 11 para suministrar carnosina a través de la epidermis.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/IB2016/050927 WO2017144937A1 (en) | 2016-02-22 | 2016-02-22 | Compositions for topical use based on a carnosine-magnesium complex |
| US201662383528P | 2016-09-05 | 2016-09-05 | |
| PCT/IB2017/050907 WO2017145030A1 (en) | 2016-02-22 | 2017-02-17 | Composition for topical use based on a carnosine-magnesium complex |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2948575T3 true ES2948575T3 (es) | 2023-09-14 |
Family
ID=58108699
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17706899T Active ES2948575T3 (es) | 2016-02-22 | 2017-02-17 | Composición para su uso tópico a base de un complejo carnosina-magnesio |
Country Status (23)
| Country | Link |
|---|---|
| US (1) | US10973868B2 (es) |
| EP (1) | EP3419588B1 (es) |
| JP (1) | JP2019505556A (es) |
| KR (1) | KR20190019898A (es) |
| CN (1) | CN109379887B (es) |
| AU (1) | AU2017223147B2 (es) |
| BR (1) | BR112018017147B1 (es) |
| CA (1) | CA3015467A1 (es) |
| DK (1) | DK3419588T3 (es) |
| ES (1) | ES2948575T3 (es) |
| FI (1) | FI3419588T3 (es) |
| HR (1) | HRP20230641T1 (es) |
| HU (1) | HUE062574T2 (es) |
| IL (1) | IL261315A (es) |
| NZ (1) | NZ746026A (es) |
| PL (1) | PL3419588T3 (es) |
| PT (1) | PT3419588T (es) |
| RS (1) | RS64310B1 (es) |
| RU (1) | RU2018130087A (es) |
| SA (1) | SA518392244B1 (es) |
| SG (1) | SG11201806957RA (es) |
| SI (1) | SI3419588T1 (es) |
| WO (1) | WO2017145030A1 (es) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2572173B (en) * | 2018-03-21 | 2021-10-06 | Byrne Daniel | Personal cleansing composition |
| GB201900728D0 (en) * | 2019-01-18 | 2019-03-06 | Univ Birmingham | Drug delivery system |
| ZA202212072B (en) * | 2022-11-04 | 2023-08-30 | Daniel Byrne | Personal cleansing composition |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2968034B2 (ja) * | 1990-11-09 | 1999-10-25 | 協和醗酵工業株式会社 | 皮膚化粧料 |
| DE4307983A1 (de) * | 1993-03-13 | 1994-09-15 | Beiersdorf Ag | Wirkstoffe und kosmetische und dermatologische Zubereitungen |
| DE4328871A1 (de) * | 1993-08-27 | 1995-03-02 | Beiersdorf Ag | Mittel gegen empfindliche, hyperreaktive Hautzustände, atopische Dermatiden, Pruritus, Psoriasis Prurigo, Photodermatosen und Ichthyosis |
| RU2165749C1 (ru) * | 2000-07-06 | 2001-04-27 | Общество с ограниченной ответственностью "Научно-экспериментальное производство Микрохирургия глаза" | Способ восстановления эндотелия роговицы |
| AUPR038200A0 (en) * | 2000-09-26 | 2000-10-19 | Beta Peptide Foundation Pty Ltd, The | Compositions and methods for delaying, preventing, rejuvenating or reversing senescence |
| US20060141054A1 (en) * | 2004-10-25 | 2006-06-29 | Thomas Piccariello | Metal coordinated compositions |
| FR2885522B1 (fr) * | 2005-05-13 | 2020-01-10 | Sederma | Composition cosmetique ou dermopharmaceutique contenant de la teprenone |
| WO2012171106A1 (en) * | 2011-06-13 | 2012-12-20 | Levy Phillip | Skin cosmetic compositions comprising malus domestica extract and argania spinosa sprout extract for improving sktn appearance |
| CA2896646A1 (en) * | 2012-12-27 | 2014-07-03 | Hayashibara Co., Ltd. | Skin-exterior anti-ageing composition and production method therefor |
| JP2016532453A (ja) * | 2013-08-20 | 2016-10-20 | ナチュラル・オールタネイティブス・インターナショナル,インコーポレーテッド | 栄養補助を通して戦術パフォーマンスを維持または改善する方法 |
-
2017
- 2017-02-17 HU HUE17706899A patent/HUE062574T2/hu unknown
- 2017-02-17 PT PT177068996T patent/PT3419588T/pt unknown
- 2017-02-17 ES ES17706899T patent/ES2948575T3/es active Active
- 2017-02-17 BR BR112018017147-6A patent/BR112018017147B1/pt active IP Right Grant
- 2017-02-17 CN CN201780012582.7A patent/CN109379887B/zh active Active
- 2017-02-17 PL PL17706899.6T patent/PL3419588T3/pl unknown
- 2017-02-17 EP EP17706899.6A patent/EP3419588B1/en active Active
- 2017-02-17 US US16/077,794 patent/US10973868B2/en active Active
- 2017-02-17 KR KR1020187024172A patent/KR20190019898A/ko active Search and Examination
- 2017-02-17 HR HRP20230641TT patent/HRP20230641T1/hr unknown
- 2017-02-17 WO PCT/IB2017/050907 patent/WO2017145030A1/en active Application Filing
- 2017-02-17 SI SI201731370T patent/SI3419588T1/sl unknown
- 2017-02-17 NZ NZ746026A patent/NZ746026A/en unknown
- 2017-02-17 CA CA3015467A patent/CA3015467A1/en active Pending
- 2017-02-17 FI FIEP17706899.6T patent/FI3419588T3/fi active
- 2017-02-17 SG SG11201806957RA patent/SG11201806957RA/en unknown
- 2017-02-17 RS RS20230498A patent/RS64310B1/sr unknown
- 2017-02-17 DK DK17706899.6T patent/DK3419588T3/da active
- 2017-02-17 RU RU2018130087A patent/RU2018130087A/ru not_active Application Discontinuation
- 2017-02-17 JP JP2018544144A patent/JP2019505556A/ja active Pending
- 2017-02-17 AU AU2017223147A patent/AU2017223147B2/en active Active
-
2018
- 2018-08-19 SA SA518392244A patent/SA518392244B1/ar unknown
- 2018-08-22 IL IL261315A patent/IL261315A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| SA518392244B1 (ar) | 2021-08-02 |
| PL3419588T3 (pl) | 2023-09-18 |
| US10973868B2 (en) | 2021-04-13 |
| CN109379887B (zh) | 2021-12-21 |
| CA3015467A1 (en) | 2017-08-31 |
| PT3419588T (pt) | 2023-06-30 |
| EP3419588A1 (en) | 2019-01-02 |
| RU2018130087A (ru) | 2020-03-24 |
| EP3419588B1 (en) | 2023-04-05 |
| RU2018130087A3 (es) | 2020-03-24 |
| HRP20230641T1 (hr) | 2023-09-29 |
| SI3419588T1 (sl) | 2023-09-29 |
| FI3419588T3 (fi) | 2023-06-29 |
| IL261315A (en) | 2018-10-31 |
| JP2019505556A (ja) | 2019-02-28 |
| RS64310B1 (sr) | 2023-07-31 |
| AU2017223147B2 (en) | 2021-12-02 |
| BR112018017147B1 (pt) | 2022-05-31 |
| SG11201806957RA (en) | 2018-09-27 |
| CN109379887A (zh) | 2019-02-22 |
| KR20190019898A (ko) | 2019-02-27 |
| HUE062574T2 (hu) | 2023-11-28 |
| NZ746026A (en) | 2024-07-05 |
| BR112018017147A2 (pt) | 2019-01-02 |
| AU2017223147A1 (en) | 2018-09-27 |
| DK3419588T3 (da) | 2023-07-03 |
| US20190216880A1 (en) | 2019-07-18 |
| WO2017145030A1 (en) | 2017-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10004681B2 (en) | Seaweed-derived cosmetic compositions | |
| AU2017218138B2 (en) | Moisturizing compositions and uses thereof | |
| ES2703516T3 (es) | Composiciones de rejuvenecimiento dérmico | |
| ES2768323T5 (es) | Composiciones cosméticas que contienen al menos un hidrótropo y al menos un compuesto activo | |
| ES2948575T3 (es) | Composición para su uso tópico a base de un complejo carnosina-magnesio | |
| EP2763648A1 (en) | Hair care compositions and methods of use | |
| ES2903108T3 (es) | Composiciones y métodos de estimulación de células madre | |
| ES2794901T3 (es) | Composiciones y métodos para tratar afecciones de la piel con luz y ácidos policarboxílicos | |
| WO2020033450A1 (en) | Wrinkle reducing compositions and methods | |
| ES2932550T3 (es) | Composiciones estimulantes de células madre y métodos para tratar el melasma | |
| CN107375007B (zh) | 一种护肤品组合物、氨基酸皂及其制备方法 | |
| JP2019137695A (ja) | 皮膚有効成分の浸透方法 | |
| ES2606233T3 (es) | Composiciones para el tratamiento de la rosácea que comprende quitosano y una amida de ácido dicarboxílico | |
| ES2815849T3 (es) | Preparación externa líquida | |
| US20220401339A1 (en) | Seaweed-derived cosmetic compositions | |
| Liu et al. | Highly efficient conotoxin delivery enabled by a bio-derived ionic liquid | |
| KR101893970B1 (ko) | 레스베라트롤을 함유하는 화장료 조성물 | |
| WO2017144937A1 (en) | Compositions for topical use based on a carnosine-magnesium complex | |
| JP4246150B2 (ja) | 皮膚化粧料組成物 | |
| ES2237538T3 (es) | Composicion que comprende manganeso. | |
| JP2012097027A (ja) | 経皮吸収促進性皮膚外用剤 | |
| JP2009234957A (ja) | 皮膚用外用剤 | |
| BR102016030885B1 (pt) | Composição cosmética contendo leucina e ácido lático para o tônus muscular facial |