ES2880321T3 - Composiciones de inhibición de biopelícula que potencian el aumento de peso en el ganado - Google Patents
Composiciones de inhibición de biopelícula que potencian el aumento de peso en el ganado Download PDFInfo
- Publication number
- ES2880321T3 ES2880321T3 ES16754616T ES16754616T ES2880321T3 ES 2880321 T3 ES2880321 T3 ES 2880321T3 ES 16754616 T ES16754616 T ES 16754616T ES 16754616 T ES16754616 T ES 16754616T ES 2880321 T3 ES2880321 T3 ES 2880321T3
- Authority
- ES
- Spain
- Prior art keywords
- animal
- compounds
- acid
- feed
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 *[N+](*(CC(O)=O)CC(O)=O)[O-] Chemical compound *[N+](*(CC(O)=O)CC(O)=O)[O-] 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/02—Iron compounds
- C07F15/025—Iron compounds without a metal-carbon linkage
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/10—Aromatic or araliphatic carboxylic acids, or thio analogues thereof; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/36—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a singly bound oxygen or sulfur atom attached to the same carbon skeleton, this oxygen or sulfur atom not being a member of a carboxylic group or of a thio analogue, or of a derivative thereof, e.g. hydroxy-carboxylic acids
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/44—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a nitrogen atom attached to the same carbon skeleton by a single or double bond, this nitrogen atom not being a member of a derivative or of a thio analogue of a carboxylic group, e.g. amino-carboxylic acids
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N59/00—Biocides, pest repellants or attractants, or plant growth regulators containing elements or inorganic compounds
- A01N59/16—Heavy metals; Compounds thereof
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K20/00—Accessory food factors for animal feeding-stuffs
- A23K20/10—Organic substances
- A23K20/195—Antibiotics
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K20/00—Accessory food factors for animal feeding-stuffs
- A23K20/20—Inorganic substances, e.g. oligoelements
- A23K20/30—Oligoelements
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K50/00—Feeding-stuffs specially adapted for particular animals
- A23K50/10—Feeding-stuffs specially adapted for particular animals for ruminants
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K50/00—Feeding-stuffs specially adapted for particular animals
- A23K50/30—Feeding-stuffs specially adapted for particular animals for swines
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K50/00—Feeding-stuffs specially adapted for particular animals
- A23K50/60—Feeding-stuffs specially adapted for particular animals for weanlings
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K50/00—Feeding-stuffs specially adapted for particular animals
- A23K50/70—Feeding-stuffs specially adapted for particular animals for birds
- A23K50/75—Feeding-stuffs specially adapted for particular animals for birds for poultry
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/127—Antibiotics
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/16—Inorganic salts, minerals or trace elements
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/295—Iron group metal compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/7036—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin having at least one amino group directly attached to the carbocyclic ring, e.g. streptomycin, gentamycin, amikacin, validamycin, fortimicins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L12/00—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor
- A61L12/08—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor using chemical substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor
- A61L2/0005—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor for pharmaceuticals, biologicals or living parts
- A61L2/0082—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor for pharmaceuticals, biologicals or living parts using chemical substances
- A61L2/0088—Liquid substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor
- A61L2/16—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor using chemical substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor
- A61L2/16—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor using chemical substances
- A61L2/18—Liquid substances or solutions comprising solids or dissolved gases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor
- A61L2/16—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor using chemical substances
- A61L2/22—Phase substances, e.g. smokes, aerosols or sprayed or atomised substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D5/00—Coating compositions, e.g. paints, varnishes or lacquers, characterised by their physical nature or the effects produced; Filling pastes
- C09D5/14—Paints containing biocides, e.g. fungicides, insecticides or pesticides
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B1/00—Optical elements characterised by the material of which they are made; Optical coatings for optical elements
- G02B1/04—Optical elements characterised by the material of which they are made; Optical coatings for optical elements made of organic materials, e.g. plastics
- G02B1/041—Lenses
- G02B1/043—Contact lenses
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2202/00—Aspects relating to methods or apparatus for disinfecting or sterilising materials or objects
- A61L2202/20—Targets to be treated
- A61L2202/24—Medical instruments, e.g. endoscopes, catheters, sharps
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Polymers & Plastics (AREA)
- Zoology (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Food Science & Technology (AREA)
- General Chemical & Material Sciences (AREA)
- Animal Husbandry (AREA)
- Wood Science & Technology (AREA)
- Plant Pathology (AREA)
- Birds (AREA)
- Environmental Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Dentistry (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Mycology (AREA)
- Nutrition Science (AREA)
- Biomedical Technology (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Materials Engineering (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Fodder In General (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
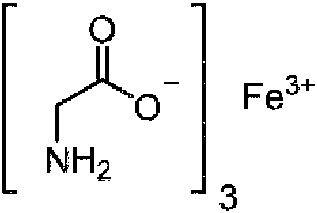
Un método no terapéutico de potenciación del crecimiento de un animal, comprendiendo el método provocar que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejos de Fe III de Fórmula I: Fe(III)x(ligando)y Fórmula I en donde x es un valor de número entero de 1-2, y es un valor de número entero de 1-3, y cada ligando presente es independientemente una base conjugada de un α-hidroxiácido seleccionado del grupo que consiste en ácido cítrico, ácido tartárico, ácido láctico, ácido glicólico, ácido isoleúcico, ácido málico y ácido mandélico; o cada ligando es una base conjugada de un aminoácido seleccionado independientemente del grupo que consiste en glicina, alanina, ácido aspártico, cisteína, ácido glutámico, isoleucina, leucina, metionina, fenilalanina, prolina, serina, treonina y valina; y sales y/o hidratos de los mismos, en donde el crecimiento del animal se potencia en comparación con un control sin tratar, en donde el crecimiento potenciado se basa en las mediciones de una o más características seleccionadas del grupo que consiste en peso corporal, peso corporal promedio (PCP), ingesta de pienso o ingesta de pienso promedio (IPP), aumento de peso o aumento de peso promedio (APP), e índice de conversión de pienso ajustado a la mortalidad (ICPM), y en donde el animal es un mamífero o un ave, y en donde, cuando el animal es un ave de corral, entonces: (a) se provoca que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejos de Fe III en forma de una composición que consiste esencialmente en el uno o más compuestos de complejos de Fe III y un pienso para aves de corral, o en forma de un agua potable para animales que consiste esencialmente en el uno o más compuestos de complejos de Fe III y agua; y/o (b) se provoca que el animal ingiera o absorba una cantidad eficaz del uno o más compuestos de complejos de Fe III en forma de una composición que no incluye un antibiótico como aditivo.
Description
DESCRIPCIÓN
Composiciones de inhibición de biopelícula que potencian el aumento de peso en el ganado
Campo de la invención
La presente invención se refiere en general a una clase de compuestos que tiene una amplia gama de actividades antimicrobianas de inhibición de biopelícula microbiana y otras actividades, así como muchos otros usos, especialmente como aditivos para piensos.
Antecedentes de la invención
El margen de beneficio de la producción de carne de vacuno, cerdo, pollo y otros tipos de carne, incluyendo la acuicultura, es muy pequeño. La rentabilidad frecuentemente depende de la eficiencia del pienso y del índice de aumento. El primer criterio se refiere a la cantidad de ingesta de pienso necesaria para producir una cantidad especificada de aumento de peso. El segundo criterio se refiere a la cantidad de aumento de peso diario (frecuentemente denominada aumento diario promedio o ADP) con un tipo y/o una cantidad especificados de pienso, si se trata de forraje, pastoreo y/o grano. Muchas variables afectan a estos criterios de rendimiento, incluyendo la especie, la edad, la genética, el clima, así como el tipo y la cantidad de pienso, forraje, hierba y suplementos.
Se han utilizado muchas composiciones diferentes para potenciar la eficiencia del pienso y el ADP. Algunas de estas, tales como la hormona del crecimiento, pueden usarse en exceso y dejar restos en la carne que después repercuten en el consumidor. Otras son relativamente caras para la cantidad de aumento. Otras requieren ensayos reglamentarios exhaustivos por ser suplementos farmacéuticos, y no meramente nutricionales.
Carroll et al., J. Agri. Res., 40(1): 921-926 (1930) se titula "Ferric Citrate as an Ingredient of Mineral Mixtures in Paired-Feeding Experiments with Growing Swine". Los autores no observaron ningún efecto y concluyeron que no había ninguna razón para creer que el suplemento de hierro confiriera ningún beneficio real a los cerdos tras recibirlo.
La Patente de los EE.UU. N.° 2.946.722 se concedió el 26 de julio de 1960 y se titula "Composition and Method for Treating Poultry". Ésta desvela y reivindica una composición para el tratamiento de aves de corral que consiste esencialmente en una sal atóxica de hidrosoluble de ácido propiónico y cantidades menores pero complementarias de metil rosanilina, citrato férrico de colina, bisulfito sódico de menadiona y compuestos de elementos traza.
Bremner et al., B. J. Nutr., 29(1): 229-243 (1973) se titula "Iron metabolism in the veal calf. The availability of different iron compounds" y analiza la evaluación del estado hematológico de terneros de raza Ayrshire criados con leche desnatada suplementada con grasa desde aproximadamente los 17 días de edad. Se compararon las disponibilidades relativas de hierro a partir de FeSO4, citrato férrico, etilendiaminotetraacetato férrico y fitato de hierro, como suplementos dietéticos, y los autores concluyeron que no había diferencias significativas entre los diferentes métodos de tratamiento. En una publicación suplementaria de los mismos autores, Bremner et al., B. J. Nutr., 30: 61-76 (1973), se realizaron estudios posteriores sobre la suplementación de hierro con FeSO4.
Miles y Maskell, J. Med. Microbiol., 20: 17-26 (1985) se titula "The antagonism of tetracycline and ferric iron in vivo" y publica que la disminución de la acción de la tetraciclina por un exceso moderado de Fe fácilmente disponible, ya sea endógeno o administrado, es un hecho poco probable, mientras que la disminución del efecto potenciador de la infección del hierro por la tetraciclina es mucho más probable.
El documento WO 98/09652 se publicó el 12 de marzo de 1998 y se titula "Composition, Antimicrobial Agent, Infection Preventive, and Food Against Helicobacter Pylori". Enseña productos farmacéuticos o adecuados para el tratamiento o la prevención de la gastritis, la úlcera gástrica y otras enfermedades provocadas por Helicobacter pylori.
Shiau y Su, J. Nutrition, 133: 483-388 (2003) se titula "Ferric citrate is half as effective as ferrous sulfate in meeting the iron requirement of juvenile tilapia, Oreochromis niloticus x O. aureus" y analiza experimentos de crecimiento realizados para estimar las necesidades mínimas de hierro en la dieta de alevines de tilapia híbrida, Oreochromis niloticus x O. aureus. Los autores concluyeron que el citrato férrico era aproximadamente un 50 % tan eficaz como el sulfato ferroso para satisfacer las necesidades de hierro.
El documento WO 03/040351 A1 se publicó el 15 de mayo de 2003. Se titula "A novel non-antibiotic strategy against OGIP infections based on an activated cereal product or ferric quinate" y describe una estrategia terapéutica no antibiótica para inhibir infecciones orogastrointestinales y patógenos, particularmente la adherencia y la colonización del Helicobacter pylori en el canal gastrointestinal y la prevención o el alivio de la enfermedad orogastrointestinal asociada.
Musk et al., Chem. Biol., 12(7): 789-796 (2005) se titula "Iron salts perturb biofilm formation and disrupt existing biofilms of Pseudomonas aeruginosa". Publica los resultados de un cribado de 4509 compuestos para seleccionar inhibidores de biopelículas no antibióticos en Pseudomonas aeruginosa PA14 realizado en placas de 384 pocillos y, entre esos
compuestos, el citrato férrico de amonio inhibió la formación de biopelículas de manera dependiente de la dosis; y otras sales de hierro actuaron de forma similar.
El documento US 2008/194679 se publicó el 14 de agosto de 2008 y se titula "Compositions andmethods forincreasing metabolic activity in animal tissue". Desvela métodos y composiciones que incluyen quelatos de aminoácidos metálicos con alto contenido en nitrógeno que pueden aumentar la actividad metabólica o la concentración de metales en animales. Se enseña que la composición de aminoácidos puede comprender un quelato de aminoácido con un primer metal y un primer ligando aminoacídico, donde el primer ligando aminoacídico está desprovisto de un enlace disulfuro y tiene al menos dos átomos de nitrógeno, y un complejo de aminoácido diferente del quelato de aminoácido que tiene un segundo metal y un segundo ligando aminoacídico.
El documento EP2286666 A1 se publicó el 23 de febrero de 2011. Se titula "Versatile Disinfectant" y describe un desinfectante versátil que contiene como componentes principales, un ion metálico con acción antimicrobiana, L-cisteína y ácido L-ascórbico, caracterizado por que contiene un tensioactivo que excluye un tensioactivo no iónico además de estos componentes principales. Se enseña en él que el desinfectante puede desinfectar un objeto que ha de tratarse para un entorno, un aparato, un cuerpo humano, un cuerpo animal, un cuerpo vegetal, una materia orgánica o similar poniendo el desinfectante en contacto con un objeto de este tipo que ha de tratarse.
El documento WO 2013/121214 A1 se publicó el 22 de agosto de 2013. Se titula "Iron complexes for the reduction of gastrointestinal tract colonisation by Campylobacter" y describe la administración de al menos un compuesto que se une a PMEP o FlaA de Campylobacter en una cantidad eficaz para reducir el número de Campylobacter presentes en el tracto gastrointestinal de animales.
Es un objetivo proporcionar composiciones, y métodos de uso de las mismas, para mejorar el rendimiento de crecimiento en ganado.
Es un objetivo adicional proporcionar composiciones y formulaciones que utilicen compuestos antibacterianos para tratar o prevenir la formación de biopelículas.
Sumario de la invención
La invención es como se define por las reivindicaciones adjuntas.
Se han desarrollado compuestos y composiciones que contienen los compuestos, y se describen adicionalmente en la presente solicitud, que son útiles como compuestos inhibidores de biopelículas selectivos, que también pueden utilizarse en formulaciones administradas a animales para aumentar la eficiencia del pienso y el aumento de peso, así como para disminuir la infección por organismos patógenos y su propagación.
Estos compuestos tienen la siguiente fórmula:
Fe(III)x(ligando)y Fórmula I
en donde
x es un valor de número entero de 1-2,
y es un valor de número entero de 1-3, y
cada ligando presente es independientemente una base conjugada de un a-hidroxiácido seleccionado de ácido cítrico, ácido tartárico, ácido láctico, ácido glicólico, ácido isoleúcico, ácido málico y ácido mandélico; o cada ligando es una base conjugada de un aminoácido seleccionado independientemente del grupo
que consiste en glicina, alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutámico, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptófano y valina; y sales y/o hidratos de los mismos. Sin embargo, cabe señalar que no todas las reivindicaciones adjuntas se refieren a todos los compuestos anteriores y que el alcance de protección está definido por las reivindicaciones adjuntas.
Los compuestos de ejemplo que se describen en el presente documento incluyen Lactato Férrico (Fe-Lac), Citrato Férrico (Fe-Cit), Tartrato Férrico (Fe-Tart), Glicinato Férrico (Fe-Gly), Malato Férrico, , y complejos férricos con L-fenilalanina (Fe-Phe) e hidratos, sales o derivados de los mismos. Las formas de lactato, citrato, glicinato, tartrato y malato tienen la ventaja de ser más hidrosolubles y, por tanto, pueden ser más fáciles de fabricar y utilizar en soluciones o piensos.
Los compuestos pueden administrarse a un animal o a un ser humano para la inhibición selectiva de la formación de biopelículas, en forma de un comprimido, cápsula, solución o suspensión oral, o pueden incorporarse en piensos o suplementos de piensos. Las composiciones son eficaces contra una amplia gama de especies microbianas, incluyendo S. epidermidis, E. faecalis, E. coli, S. aureus, Campylobacter spp. H. pylori y Pseudomonas. Los compuestos representan una nueva clase de inhibidores de biopelículas en comparación con la mayoría de los que
están en uso actualmente y son eficaces en el tratamiento y la prevención de infecciones microbianas.
Los compuestos también pueden administrarse junto con antibióticos para revertir la resistencia a antibióticos de las bacterias y pueden usarse para tratar las bacterias resistentes a antibióticos administrando los compuestos con antibióticos.
Los compuestos pueden aplicarse a un sustrato tal como un dispositivo médico, tubos, equipo de procesamiento o equipo en las industrias alimentaria, médica o informática en las que la formación de biopelículas y la contaminación bacteriana son un problema. Las composiciones pueden incorporarse en un recubrimiento que se pulveriza en forma de una solución o suspensión, puede incorporarse en un laminado, película o recubrimiento polimérico, o puede dispersarse en partículas o aerosoles para su administración. Los compuestos también pueden incorporarse en soluciones o suspensiones para su aplicación como desinfectante a una superficie infectada o a una superficie que tenga una biopelícula sobre la misma. También pueden usarse como desinfectantes para productos agrícolas tales como carne.
En una aplicación particularmente preferida, los compuestos se usan para mejorar el rendimiento de crecimiento de animales tales como ganado, incluyendo aves de corral, vacas, ovejas, cerdos y cabras, preferentemente en forma de suplementos para piensos y fórmulas, en lugar de, o en combinación con, compuestos bacteriostáticos o bactericidas existentes o que potencian el crecimiento. En una realización preferida, las composiciones pueden administrarse a animales, tales como ganado, para aumentar el rendimiento de crecimiento. Las composiciones también pueden usarse para disminuir los índices de conversión de pienso ajustados a la mortalidad (ICPM).
Existen ejemplos que demuestran la eficacia para potenciar el aumento de peso en ganado, incluyendo aves de corral (pollos) y cerdos.
Breve descripción de los dibujos
La Fig. 1 es un gráfico de barras del peso corporal promedio en el día 42 para pollos para todos los grupos de tratamiento de pollos que se describen en el Ejemplo Comparativo 1 y una comparación con un control comercial etiquetado como "Objetivo". El grupo de tratamiento 1 es el control negativo etiquetado como "CNC". El control positivo (etiquetado como "CC") se expuso a una cama sucia que contenía Campylobacter el día 20. Se trató a los pollos con Fe-Q o Fe-Tyr.
La Fig. 2 es un gráfico de barras del índice de conversión de pienso ajustado a la mortalidad (ICPM) en el día 42 para todos los grupos de tratamiento de pollos que se describen en el Ejemplo Comparativo 1 y una comparación con un control comercial etiquetado como "Objetivo".
La Fig. 3 es un gráfico de barras del número de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de excrementos de ave en el día 42 para los grupos de tratamiento 1-3 y 6-8 del Ejemplo Comparativo 1. La Fig. 4 es un gráfico de barras del número promedio de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de muestras de ciego en el día 42 para los grupos de tratamiento 1-3 y 5-8 del Ejemplo Comparativo 1.
La Fig. 5 es un gráfico de barras que muestra el índice de cobertura con biopelícula de Pseudomonas aeruginosa PAO1 sobre la superficie de un portaobjetos de vidrio, que compara Pseudomonas PAO1 sin Fe-Lac y Pseudomonas PAO1 + tratamiento con Fe-Lac 50, 100 y 300 pM, que se describe en el Ejemplo Comparativo 2. La Fig. 6 es un gráfico de barras que muestra el índice de cobertura con biopelícula de Pseudomonas aeruginosa PAO1 sobre la superficie de un portaobjetos de vidrio, que compara Pseudomonas PAO1 sin Fe-Cit y Pseudomonas PAO1 + tratamiento con Fe-Lac 100 y 300 pM, que se describe en el Ejemplo Comparativo 3. La Fig. 7 es un gráfico de barras que muestra el índice de cobertura con biopelícula de Pseudomonas aeruginosa PAO1 sobre la superficie de un portaobjetos de vidrio, que compara Pseudomonas PAO1 sin Fe-Tart y Pseudomonas PAO1 + tratamiento con Fe-Tart 100 y 300 pM, que se describe en el Ejemplo Comparativo 4. La Fig. 8 es un gráfico de barras que muestra el índice de cobertura con biopelícula de Pseudomonas aeruginosa PAO1 sobre la superficie de un portaobjetos de vidrio, que compara Pseudomonas PAO1 sin Fe-Gly y Pseudomonas PAO1 + tratamiento con Fe-Gly 100 y 300 pM, que se describe en el Ejemplo Comparativo 5. La Fig. 9 es un gráfico de barras que muestra el índice de cobertura con biopelícula de la cepa de Campylobacter jejuni NCTC11168 sobre la superficie de perlas, que compara el efecto del Fe-Tart a 50 pM, 100 pM y 300 pM, el efecto de FeQ (QPLEX) a 300 (comparativo) y el efecto de Fe-Cit a 50 pM, 100 pM, como se describe en el Ejemplo 6. Una muestra de control muestra la formación de biopelícula en ausencia de cualesquier aditivos.
La Fig. 10 es un gráfico de barras que muestra el número promedio de unidades formadoras de colonias por ml (ufc/ml) de Aislado Pulmonar de fQ N.° 11 de Cepas de Ee D frente a nada, 100 y 300 pg tratados con EDTA Férrico, Malato Férrico y Oxalato Férrico, que se describe en el Ejemplo Comparativo 8
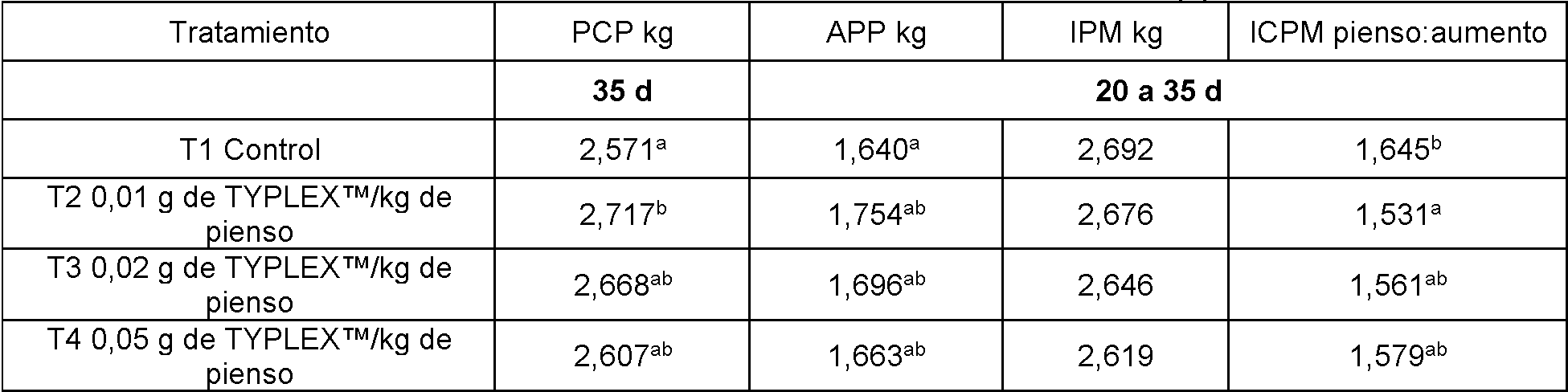
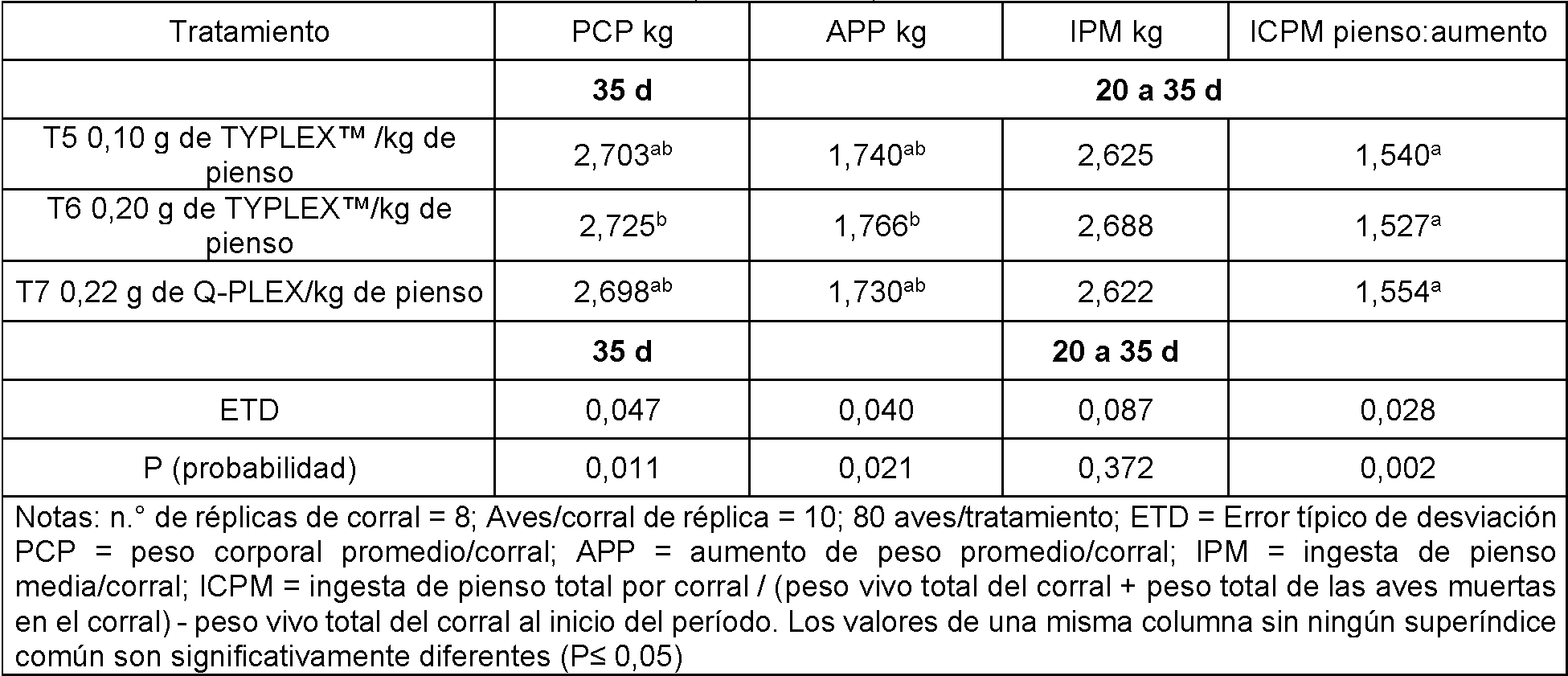
La Fig. 11 es un gráfico de barras que muestra el número promedio de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de muestras de ciego en el día 35 para grupos tratados con Lactato Férrico, FeQ (comparativo) y un control positivo, del Ejemplo 9.
La Fig. 12 es un gráfico de barras que muestra el peso corporal promedio en el día 42 para todos los grupos de tratamiento que se describen en el Ejemplo Comparativo 10.
La Fig. 13 es un gráfico que muestra el índice de conversión de pienso ajustado a la mortalidad (ICPM) en el día 42 para todos los grupos de tratamiento que se describen en el Ejemplo Comparativo 10.
La Fig. 14 es un gráfico que muestra el número de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento que se describen en el Ejemplo Comparativo 10. La Fig. 15 es un gráfico que muestra el número de unidades formadoras de colonias de Salmonella por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento del Ejemplo Comparativo 10.
La Fig. 16 es un gráfico que muestra el número de unidades formadoras de colonias de E. coli por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento que se describen en el Ejemplo Comparativo 10.
Descripción detallada de la invención
I. Definiciones
El término "alquilo" se refiere al radical de grupos alifáticos saturados (es decir, un alcano con un átomo de hidrógeno retirado), incluyendo grupos alquilo de cadena lineal, grupos alquilo de cadena ramificada, grupos cicloalquilo (alicíclicos), grupos cicloalquilo alquil-sustituidos y grupos alquilo cicloalquil-sustituidos.
En realizaciones preferidas, un alquilo de cadena lineal o de cadena ramificada tiene 30 o menos átomos de carbono en su cadena principal (por ejemplo, C1-C30 para las cadenas lineales y C3-C30 para las cadenas ramificadas), preferentemente 20 o menos, más preferentemente 15 o menos, mucho más preferentemente 10 o menos. Análogamente, los cicloalquilos preferidos tienen de 3-10 átomos de carbono en su estructura anular y más preferentemente tienen 5, 6 o 7 carbonos en la estructura anular. El término "alquilo" (o "alquilo inferior"), como se usa en toda la memoria descriptiva, los ejemplos y las reivindicaciones, tiene por objeto incluir tanto "alquilos sin sustituir" como "alquilos sustituidos", estos últimos se refieren a restos alquilo que tienen uno o más sustituyentes que reemplazan un hidrógeno en uno o más carbonos de la cadena principal hidrocarbonada. Dichos sustituyentes incluyen, pero sin limitación, halógeno, hidroxilo, carbonilo (tal como un carboxilo, alcoxicarbonilo, formilo o un acilo), tiocarbonilo (tal como un tioéster, un tioacetato o un tioformiato), alcoxilo, fosforilo, fosfato, fosfonato, fosfinato, amino, amido, amidina, imina, ciano, nitro, azido, sulfhidrilo, alquiltio, sulfato, sulfonato, sulfamoílo, sulfonamido, sulfonilo, heterociclilo, aralquilo o un resto aromático o heteroaromático.
A menos que el número de átomos de carbono se especifique de otra manera, "alquilo inferior", como se usa en el presente documento, significa un grupo alquilo, como se ha definido anteriormente, pero que tiene de uno a diez carbonos, más preferentemente de uno a seis átomos de carbono en su estructura de cadena principal. Análogamente, "alquenilo inferior" y "alquinilo inferior" tienen longitudes de cadena similares. En toda la solicitud, los grupos alquilo preferidos son alquilos inferiores. En realizaciones preferidas, un sustituyente designado en el presente documento como alquilo es un alquilo inferior.
Los expertos en la materia comprenderán que los restos sustituidos en la cadena de hidrocarburo pueden a su vez estar sustituidos, si es adecuado. Por ejemplo, los sustituyentes de un alquilo sustituido pueden incluir grupos halógeno, hidroxi, nitro, tioles, amino, azido, imino, amido, fosforilo (incluyendo fosfonato y fosfinato), sulfonilo (incluyendo sulfato, sulfonamido, sulfamoílo y sulfonato) y sililo, así como éteres, alquiltios, carbonilos (incluyendo cetonas, aldehídos, carboxilatos y ésteres) y -CF3, -CN. Los cicloalquilos pueden estar sustituidos de la misma manera.
El término "heteroalquilo", como se usa en el presente documento, se refiere a radicales que contienen carbono de cadena lineal o ramificada, o cíclicos, o combinaciones de los mismos, que contienen al menos un heteroátomo. Los heteroátomos adecuados incluyen, pero sin limitación, O, N, Si, P, Se, B y S, en donde los átomos de fósforo y azufre están opcionalmente oxidados y el heteroátomo de nitrógeno está opcionalmente cuaternizado. Los heteroalquilos pueden estar sustituidos como se ha definido anteriormente para los grupos alquilo.
Los términos "alquenilo" y "alquinilo", se refieren a grupos alifáticos insaturados análogos en longitud y posible sustitución a los alquilos descritos anteriormente, pero que contienen al menos un enlace doble o triple respectivamente.
Los términos "alcoxilo" o "alcoxi", como se usan en la presente memoria, se refieren a un grupo alquilo, como se ha definido anteriormente, que tiene un radical de oxígeno unido al mismo. Los grupos alcoxilo representativos incluyen metoxi, etoxi, propiloxi, terc-butoxi. Un "éter" es dos hidrocarburos unidos covalentemente por un oxígeno. En consecuencia, el sustituyente de un alquilo hace que ese alquilo y el éter sean o se parezcan a un alcoxilo, tal como puede representarse por uno de -O-alquilo, -O-alquenilo y -O-alquinilo. Los términos "aroxi" y "ariloxi", como se usan indistintamente en el presente documento, pueden representarse por -O-arilo u O-heteroarilo, en donde arilo y heteroarilo son como se definen a continuación. Los grupos alcoxi y aroxi pueden estar sustituidos como se ha descrito anteriormente para el alquilo.
"Arilo", como se usa en el presente documento, se refiere a sistemas de anillos biaromáticos o biheterocíclicos, heterocíclicos condensados, aromáticos condensados, heterocíclicos, aromáticos de C5-C10 miembros. Definido en términos generales, "arilo", como se usa en el presente documento, incluye grupos aromáticos de un solo anillo de 5, 6, 7, 8, 9 y 10 miembros que pueden incluir de cero a cuatro heteroátomos, por ejemplo, benceno, pirrol, furano, tiofeno, imidazol, oxazol, tiazol, triazol, pirazol, piridina, pirazina, piridazina, pirimidina. Aquellos grupos arilo que tienen
heteroátomos en la estructura del anillo también pueden denominarse "heterociclos de arilo" o "heteroaromáticos". El anillo aromático puede estar sustituido en una o más posiciones de anillo con uno o más sustituyentes incluyendo, pero sin limitación, halógeno, azida, alquilo, aralquilo, alquenilo, alquinilo, cicloalquilo, hidroxilo, alcoxilo, amino (o amino cuaternizado), nitro, sulfhidrilo, imino, amido, fosfonato, fosfinato, carbonilo, carboxilo, sililo, éter, alquiltio, sulfonilo, sulfonamido, cetona, aldehído, éster, heterociclilo, restos aromáticos o heteroaromáticos, -CF3, -CN y combinaciones de los mismos.
El término "arilo" también incluye sistemas de anillos policíclicos que tienen dos o más anillos cíclicos en los que dos o más átomos de carbono son comunes a dos anillos contiguos (es decir, "anillos condensados") en donde al menos uno de los anillos es aromático, por ejemplo, el otro o los otros anillos cíclicos pueden ser cicloalquilos, cicloalquenilos, cicloalquinilos, arilos y/o heterociclos. Los ejemplos de anillos heterocíclicos incluyen, pero sin limitación, bencimidazolilo, benzofuranilo, benzotiofuranilo, benzotiofenilo, benzoxazolilo, benzoxazolinilo, benzotiazolilo, benzotriazolilo, benzotetrazolilo, benzoisoxazolilo, benzoisotiazolilo, benzoimidazolinilo, carbazolilo, 4aH carbazolilo, carbolinilo, cromanilo, cromenilo, cinolinilo, decahidroquinolinilo, 2H,6H-1,5,2-ditiazinilo, dihidrofuro[2,3 b]tetrahidrofurano, furanilo, furazanilo, imidazolidinilo, imidazolinilo, imidazolilo, 1H-indazolilo, indolenilo, indolinilo, indolizinilo, indolilo, 3H-indolilo, isatinoílo, isobenzofuranilo, isocromanilo, isoindazolilo, isoindolinilo, isoindolilo, isoquinolinilo, isotiazolilo, isoxazolilo, metilendioxifenilo, morfolinilo, naftiridinilo, octahidroisoquinolinilo, oxadiazolilo, 1,2,3-oxadiazolilo, 1,2,4-oxadiazolilo, 1,2,5-oxadiazolilo, 1,3,4-oxadiazolilo, oxazolidinilo, oxazolilo, oxindolilo, pirimidinilo, fenantridinilo, fenantrolinilo, fenazinilo, fenotiazinilo, fenoxatinilo, fenoxazinilo, ftalazinilo, piperazinilo, piperidinilo, piperidonilo, 4-piperidonilo, piperonilo, pteridinilo, purinilo, piranilo, pirazinilo, pirazolidinilo, pirazolinilo, pirazolilo, piridazinilo, piridooxazol, piridoimidazol, piridotiazol, piridinilo, piridilo, pirimidinilo, pirrolidinilo, pirrolinilo, 2H-pirrolilo, pirrolilo, quinazolinilo, quinolinilo, 4H-quinolizinilo, quinoxalinilo, quinuclidinilo, tetrahidrofuranilo, tetrahidroisoquinolinilo, tetrahidroquinolinilo, tetrazolilo, 6H-1,2,5-tiadiazinilo, 1,2,3-tiadiazolilo, 1,2,4-tiadiazolilo, 1,2,5-tiadiazolilo, 1,3,4-tiadiazolilo, tiantrenilo, tiazolilo, tienilo, tienotiazolilo, tienooxazolilo, tienoimidazolilo, tiofenilo y xantenilo. Uno o más de los anillos pueden estar sustituidos como se ha definido anteriormente para "arilo".
El término "aralquilo", como se usa en el presente documento, se refiere a un grupo alquilo sustituido con un grupo arilo (por ejemplo, un grupo aromático o heteroaromático).
El término "aralquiloxi" puede estar representado por -O-aralquilo, en donde aralquilo es como se ha definido anteriormente.
"Biopelícula", como se usa en el presente documento, se refiere a cualquier grupo de microorganismos en el que las células se adhieren entre sí sobre una superficie.
"Formulación de limpieza", como se usa en el presente documento, significa una composición adecuada para su aplicación a una superficie para la eliminación de suciedad y aceites, para la desinfección o una combinación de las mismas. Las formulaciones de limpieza pueden ser antibacterianas, antimicrobianas o ambas. Las formulaciones de limpieza son adecuadas para su uso en la piel humana, cuando ninguno de los componentes de la composición esté presente en concentraciones que provoquen signos significativos de irritación cuando de aplican a la piel humana. Como se usa en el presente documento, los "signos significativos de irritación" incluyen eritema, enrojecimiento y/o hinchazón en el sitio de inyección o en el sitio de aplicación, necrosis en el lugar de aplicación, dermatitis exfoliativa en el sitio de aplicación y dolor intenso que impide la actividad diaria y/o requiera atención médica u hospitalización. Las formulaciones de limpieza pueden ser adecuadas para su uso en la cavidad bucal humana. Las formulaciones de limpieza pueden ser adecuadas para su uso con artículos que, posteriormente a la exposición y, opcionalmente, con niveles residuales de la composición de limpieza presentes sobre y/o en el artículo, después se pondrán en contacto con la piel humana u otra parte del cuerpo humano, tal como en donde el artículo (por ejemplo, una dentadura postiza) se pondrá en contacto con la cavidad bucal o se pondrá en contacto con el ojo (por ejemplo, una lente de contacto). Las formulaciones de limpieza pueden ser adecuadas para su uso con productos alimentarios y/o sus envases y, por ejemplo, pueden ser adecuadas para la limpieza de productos cárnicos y/o canales utilizadas en la producción de productos cárnicos. Las formulaciones de limpieza pueden ser adecuadas para la limpieza de equipos utilizados en la producción de alimentos. Las formulaciones de limpieza pueden ser adecuadas para su uso en la limpieza de dispositivos médicos, incluyendo dispositivos médicos implantables. La presente invención también puede proporcionar muchos otros tipos de formulaciones de limpieza, cuyos ejemplos adicionales se analizan en secciones adicionales de la presente solicitud.
El término "heteroátomo" como se usa en el presente documento significa un átomo de cualquier elemento distinto de carbono o hidrógeno. Son heteroátomos preferidos boro, nitrógeno, oxígeno, fósforo, azufre y selenio. Otros heteroátomos incluyen silicio y arsénico.
"Inhibir" o "inhibición" de la formación de biopelícula, como se usa en el presente documento, se refiere a una disminución de la formación y/o el crecimiento de microorganismos asociados a biopelículas.
Una "loción" es una formulación líquida de viscosidad baja a media.
El "índice de conversión de pienso ajustado a la mortalidad" (ICPM) es la ingesta de pienso total por corral dividida por
la suma del peso vivo total de un corral más el peso total de las aves muertas en un corral menos el peso vivo total del corral al inicio del período indicado.
Como se usa en el presente documento, el término "nitro" significa -NO2; el término "halógeno" designa -F, -Cl, -Br o -I; el término "sulfhidrilo" significa -SH; el término "hidroxilo" significa -OH; y el término "sulfonilo" significa -SO2-.
"Aceite", como se usa en el presente documento, se refiere a una composición que contiene al menos un 95 % en peso de una sustancia lipófila. Los ejemplos de sustancias lipófilas incluyen, pero sin limitación, aceites de origen natural y sintéticos, grasas, ácidos grasos, lecitinas, triglicéridos y combinaciones de los mismos.
Una "pomada" es una preparación semisólida que contiene una base de pomada y, opcionalmente, uno o más agentes activos.
"Administración parenteral", como se usa en el presente documento, significa la administración mediante cualquier método que no sea a través del tracto digestivo o por vías tópicas o regionales no invasivas.
"Paciente" o "sujeto" que ha de tratarse y/o usarse de acuerdo con cualquiera de los aspectos que se describen en el presente documento se refiere a un animal humano o no humano, tal como un primate, primate no humano, animal de laboratorio, animal de granja, ganado o una mascota doméstica. Los animales de ejemplo pueden incluir opcionalmente pollos, particularmente, un pollo de tipo cárnico, tal como un pollo de engorde, o una gallina ponedora, tal como una pollita o una gallina, o una gallina de cría. También se incluyen opcionalmente sin limitación otras aves de corral, tales como un pavo, gansos, codornices o patos, o ganado, tales como vacas, ovejas, cabras o cerdos, alpaca, banteng, bisonte, camello, gato, ciervo, perro, burro, gayal, cobaya, caballo, llama, mula, conejo, reno, búfalo acuático, yak, aunque el experto apreciará que otros animales, incluyendo animales de zoológico, animales cautivos, animales de caza, peces (incluyendo peces de agua dulce y salada, peces de piscifactoría y peces ornamentales), otros animales marinos y acuáticos, incluyendo mariscos tales como, pero sin limitación, ostras, mejillones, almejas, gambas, langostinos, langostas, cangrejos de río, cangrejos, sepia, pulpo y calamar, animales domésticos tales como perros y gatos, roedores (tales como ratones, ratas, cobayas, hámsters) y caballos, también se incluyen, así como cualquier otro animal doméstico, salvaje y de granja, incluyendo mamíferos, animales marinos, anfibios, aves, reptiles, insectos y otros invertebrados.
"Farmacéuticamente aceptable", como se usa en el presente documento, se refiere a aquellos compuestos, materiales, composiciones y/o formas farmacéuticas que son, dentro del alcance del buen criterio médico, adecuados para su uso en contacto con los tejidos de seres humanos y animales (tales como uno o más de los "pacientes" o "sujetos" animales como se ha analizado anteriormente) sin toxicidad excesiva, irritación, respuesta alérgica u otros problemas o complicaciones acordes con una relación beneficio/riesgo razonable.
"Sal farmacéuticamente aceptable", como se usa en el presente documento, se refiere a derivados de los compuestos que se definen en el presente documento, en donde el compuesto parental se modifica preparando sales de ácido o base del mismo.
"Terapéuticamente eficaz" o "cantidad eficaz", como se usa en el presente documento, significa que la cantidad de la composición utilizada es una cantidad suficiente para mejorar una o más causas o síntomas de una afección, colonización bacteriana, enfermedad o trastorno. Dicha mejora solo requiere una reducción o alteración, no necesariamente la eliminación. Como se usa en el presente documento, las expresiones "cantidad terapéuticamente eficaz", "cantidad terapéutica" y "cantidad farmacéuticamente eficaz" son sinónimos. Un experto en la materia puede determinar fácilmente la cantidad terapéutica adecuada.
El término "sustituido", como se usa en el presente documento, se refiere a todos los sustituyentes permitidos de los compuestos. En el sentido más amplio, los sustituyentes permisibles incluyen sustituyentes de compuestos orgánicos acíclicos y cíclicos, ramificados y no ramificados, carbocíclicos y heterocíclicos, aromáticos y no aromáticos. Los sustituyentes ilustrativos incluyen, pero sin limitación, halógenos, grupos hidroxilo o cualesquier otras agrupaciones orgánicas que contienen cualquier número de átomos de carbono, preferentemente 1-14 átomos de carbono y, opcionalmente, incluyen uno o más heteroátomos tales como oxígeno, azufre o nitrógeno, que se agrupan en formatos estructurales lineales, ramificados o cíclicos. Los sustituyentes representativos incluyen grupos alquilo, alquilo sustituido, alquenilo, alquenilo sustituido, alquinilo, alquinilo sustituido, fenilo, fenilo sustituido, arilo, arilo sustituido, heteroarilo, heteroarilo sustituido, halo, hidroxilo, alcoxi, alcoxi sustituido, fenoxi, fenoxi sustituido, aroxi, aroxi sustituido, alquiltio, alquiltio sustituido, feniltio, feniltio sustituido, ariltio, ariltio sustituido, ciano, isociano, isociano sustituido, carbonilo, carbonilo sustituido, carboxilo, carboxilo sustituido, amino, amino sustituido, amido, amido sustituido, sulfonilo, sulfonilo sustituido, ácido sulfónico, fosforilo, fosforilo sustituido, fosfonilo, fosfonilo sustituido, poliarilo, poliarilo sustituido, cíclico C3-C20, cíclico C3-C20 sustituido, heterocíclico, heterocíclico sustituido, aminoácido, péptido y polipéptido.
"Tratamiento", "tratar" o "aliviar", como se usan en relación con una enfermedad o infección, se refieren a una intervención realizada con la intención de alterar o inhibir la patología de un trastorno.
II. MÉTODOS DE FABRICACIÓN Y USO
La presente solicitud desvela que los complejos de hierro, preferentemente con un peso molecular del complejo inferior a 1.000 g/mol, son útiles para:
Potenciación del crecimiento de animales;
Potenciación del efecto de los antibióticos y otros agentes antimicrobianos y abordar la resistencia a antibióticos; Inhibición de la formación y el tratamiento de biopelículas preformadas; tratamiento de infecciones microbianas reduciendo la colonización microbiana; y desinfección de superficies.
Los compuestos preferidos que se describen en el presente documento incluyen los compuestos representados por la Fórmula I a continuación, particularmente, lactato férrico (también denominado en el presente documento Fe-Lac), citrato férrico (también denominado en el presente documento Fe-Cit), tartrato férrico (también denominado en el presente documento Fe-Tart) y glicinato férrico. Otros incluyen el EDTA férrico, malato férrico y oxalato férrico.
A. Potenciación del crecimiento de animales
En el presente documento se describe un método de potenciación del crecimiento de un animal, comprendiendo el método provocar que el animal ingiera y/o absorba una cantidad eficaz de uno o más compuestos de hierro. Sin embargo, ha de comprenderse que el alcance de la protección está definido por las reivindicaciones adjuntas, que se refieren, en particular en el contexto de la potenciación del crecimiento de un animal, a un método no terapéutico de potenciación del crecimiento de un animal, como se define adicionalmente por la reivindicación 1, y a un uso no terapéutico, como se define adicionalmente por la reivindicación 2, y las reivindicaciones dependientes de las mismas.
Normalmente, en una realización, uno o más de los compuestos se presentarán directamente al animal para su ingestión y/o absorción. Sin embargo, en una realización opcional alternativa, puede provocarse que el animal ingiera o absorba uno o más de los compuestos proporcionando al animal simultáneamente, por separado o secuencialmente componentes que provocan que el animal forme una cantidad eficaz del uno o más compuestos in situ. Por ejemplo, podría proporcionarse al animal una fuente de sulfato ferroso y simultáneamente, por separado o secuencialmente una fuente de otro a-hidroxiácido o sal del mismo, o podría proporcionársele una fuente de sulfato ferroso y simultáneamente, por separado o secuencialmente una fuente de un aminoácido natural o sintético, tal como L-fenilalanina.
En una realización, los uno o más compuestos son un complejo de un aminoácido con Fe III y un complejo de un ahidroxiácido con Fe III, como se define adicionalmente en las reivindicaciones adjuntas, o sales y/o hidratos de los mismos. Por ejemplo, uno o más compuestos pueden seleccionarse de entre uno o más del grupo que consiste en un complejo de L-fenilalanina con Fe III, lactato férrico (también denominado en el presente documento Fe-Lac), citrato férrico (también denominado en el presente documento Fe-Cit), tartrato férrico (también denominado en el presente documento Fe-Tart) y glicinato férrico (también denominado en el presente documento Fe-Gly). El uno o más compuestos de la invención, como se definen en las reivindicaciones adjuntas, no son un complejo de ácido quínico con Fe III.
Puede provocarse que el animal ingiera o absorba el uno o más de los compuestos, proporcionando el uno o más compuestos (o partes componentes de los mismos para formar el compuesto o compuestos in situ) por medios dietéticos, tales como en un pienso para animales o mezclado con él, como suplemento dietético y/o en el agua potable. Cabe señalar que, dependiendo de la solubilidad de los uno o más compuestos utilizados, puede ser beneficioso introducir un cosolvente para solubilizar para ayudar a la disolución en agua a una concentración eficaz.
1. Método de fabricación de piensos o suplementos de piensos enriquecidos para animales
En el presente documento se describen métodos para la producción de un producto de pienso para animales o suplemento de pienso para animales enriquecido con inhibidor de biopelículas. Un pienso para animales de ejemplo incluye pienso para un pollo (incluyendo un pollo de engorde y gallinas ponedoras). El método incluye las etapas de incorporar uno o más de los compuestos en el producto de pienso para animales o producto de suplemento de pienso para animales durante la preparación del pienso o suplemento. Un pienso para animales para su uso en los métodos que se describen en el presente documento puede incluir, uno o más compuestos de los compuestos en una cantidad de 0,001 a 20 g del uno o más compuestos por kg de pienso, tal como de 0,002 a 15 g/kg, o a un nivel de, hasta, o al menos, aproximadamente 0,002 g/kg, 0,005 g/kg, 0,01 g/kg, 0,02 g/kg, 0,03 g/kg, 0,04 g/kg, 0,05 g/kg, 0,1 g/kg, 0.
2 g/kg, 0,3 g/kg, 0,4 g/kg, 0,5 g/kg, 1 g/kg, 2 g/kg, 3 g/kg, 4 g/kg, 5 g/kg, 10 g/kg, 15 g/kg o 20 g/kg. Un suministro de agua potable para animales del primer aspecto, o para su uso en el mismo, puede comprender, o complementarse con, uno o más compuestos en una cantidad de 0,001 a 20 g del uno o más compuestos por L de agua, tal como de 0,002 a 15 g/l, o a un nivel de, hasta, o al menos, aproximadamente 0,002 g/l, 0,005 g/l, 0,01 g/l, 0,02 g/l, 0,03 g/l, 0,04 g/l, 0,05 g/l, 0,1 g/l, 0. 2 g/l, 0,3 g/l, 0,4 g/l, 0,5 g/l, 1 g/l, 2 g/l, 3 g/l, 4 g/l, 5 g/l, 10 g/l, 15 g/l o 20 g/l. Las mismas concentraciones pueden aplicarse al agua en la que viven animales acuáticos o de otro tipo.
Los uno o más compuestos pueden incorporarse en el producto en cualquier fase del proceso de producción, incluso
antes de una o más etapas de calentamiento, una o más etapas de calentamiento que incluyen exponer una composición que incluye el uno o más compuestos a una temperatura superior a 50 °C, superior a 60 °C, superior a 70 °C, superior a 80 °C, superior a 90 °C o superior a 100 °C, y preferentemente en donde la temperatura de exposición está en un intervalo seleccionado de 50-200 °C, 60-150 °C, 70-100 °C. En algunas realizaciones, un intervalo de temperatura para una etapa de calentamiento puede estar en el intervalo de 70-90 °C, tal como 75-88 °C, 80-87 °C, 81-86 °C u 82-85 °C.
Opcionalmente, un método adecuado para la producción de un pienso para animales, tal como un pienso para un pollo (incluyendo un pollo de engorde) puede incluir las etapas de:
(a) combinar componentes nutricionales y/u otros componentes dietéticos (tales como uno o más componentes seleccionados de trigo, soja, aceite de soja, minerales y otros aditivos) para formar una molienda u otra mezcla; (b) calentar la molienda u otra mezcla en una etapa de calentamiento como se ha descrito anteriormente, tal como con vapor a 85 °C durante un tiempo eficaz para matar cualquier patógeno, tal como Salmonella. Un período de 5 10 minutos, tal como 6-8 minutos, es un ejemplo de período eficaz a 85 °C, aunque el tiempo puede ajustarse dependiendo de la temperatura utilizada;
(c) enfriar la mezcla calentada. Preferentemente, el enfriamiento se realiza a una velocidad y en unas condiciones eficaces para evitar la formación de condensación, puesto que la condensación puede dar como resultado el crecimiento de patógenos incluyendo Salmonella.
(d) opcionalmente prensar la mezcla enfriada;
(e) formar gránulos de pienso a partir de la mezcla enfriada, por ejemplo, mediante granulación usando una extrusora que calienta el pienso a una temperatura adecuada, como se ha analizado anteriormente, por ejemplo, en el intervalo de 82-85 °C;
(f) adición de aditivos sensibles al calor, normalmente mediante pulverización. Los aditivos sensibles al calor pueden incluir enzimas, que (por ejemplo) pueden seleccionarse del grupo que consiste en fitasa, xilasa, betalactamasa.
De acuerdo con el método anterior para la producción de un producto de pienso para animales enriquecido con antibiótico, comprendiendo el método la etapa de incorporar uno o más de los compuestos en el producto de pienso para animales en una cualquiera o más fases de la producción, incluso durante la etapa (a), entre las etapas (a) y (b), durante la etapa (b), entre las etapas (b) y (c), durante la etapa (c), entre las etapas (c) y (d), durante la etapa (d), entre las etapas (d) y (e), durante la etapa (e), entre las etapas (e) y (f), durante la etapa (f) o después de la etapa (f).
El uno o más compuestos pueden incluirse en un pienso para animales o en un suplemento o premezcla de pienso para animales, para el pienso de aves comerciales tales como pollos, pavos, faisanes y patos. En una opción, los uno o más compuestos pueden incluirse, o usarse como suplemento, en un pienso para aves de corral, que puede ser un pienso "completo". Un pienso completo se diseña para que contenga todas las proteínas, la energía, las vitaminas, los minerales y otros nutrientes necesarios para un crecimiento adecuado, para la producción de huevos (si el ave es ponedora) y para la salud de las aves.
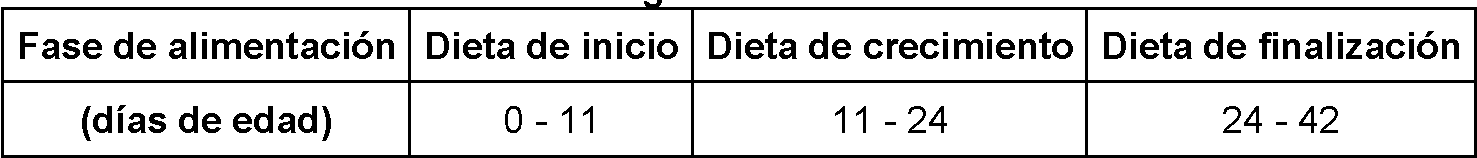
Normalmente se alimenta a los pollos utilizados en la producción comercial optimizada de pollos de engorde con diferentes dietas dependiendo de su edad. Por ejemplo, los pollos para la producción de pollos de engorde pueden criarse usando tres dietas. Estas dietas normalmente se denominan "de inicio", "de crecimiento" y "de finalización". También son posibles dietas de "preinicio". Por consiguiente, los compuestos que se desvelan en el presente documento pueden incluirse en una dieta de inicio solamente, una dieta de crecimiento solamente, una dieta de finalización solamente, una combinación de dos cualesquiera o una combinación de las tres.
Las dietas "de inicio", "de crecimiento" y "de finalización" se distinguen normalmente por el contenido de proteína en bruto, que con frecuencia se proporciona mediante ingredientes tales como la harina de soja (HDS). Por ejemplo, una dieta de inicio para un pollo de engorde puede contener opcionalmente contenidos de proteína en bruto de aproximadamente el 22-25 % en peso, tal como el 22 %, 23 %, 24 % o 25 %, prefiriéndose el 23 o 25 %. En un ejemplo adicional, una dieta de crecimiento para un pollo de engorde puede contener opcionalmente contenidos de proteína en bruto de aproximadamente el 21-23 % en peso, tal como el 21 %, 22 % o 23 %, prefiriéndose el 22 %. En un ejemplo adicional, una dieta de finalización para un pollo de engorde puede contener opcionalmente contenidos de proteína en bruto de aproximadamente el 19-23 % en peso, tal como el 19 %, 20 %, 21 %, 22 % o 23 %, prefiriéndose el 19 %, 20 % o 21 %.
Adicionalmente, o como alternativa, las dietas "de inicio", "de crecimiento" y "de finalización" pueden distinguirse por el contenido de energía metabolizable (EM), siendo normalmente el más bajo para la dieta de inicio y el más alto para la dieta de finalización, teniendo la dieta de crecimiento un nivel entre las dos. Por ejemplo, una dieta de inicio para un pollo de engorde puede tener una EM de aproximadamente 3000 o 3025 kcal/kg (± 50, 40, 30, 20, 10, 5 o menos kcal/kg). En un ejemplo adicional, una dieta de crecimiento para un pollo de engorde puede tener una EM de aproximadamente 3100 o 3150 kcal/kg (± 50, 40, 30, 20, 10, 5 o menos kcal/kg). En un ejemplo adicional, una dieta de crecimiento para un pollo de engorde puede tener una EM de aproximadamente 3200 kcal/kg (± 50, 40, 30, 20, 10, 5 o menos kcal/kg).
Un pienso para animales o suplemento de pienso para animales enriquecido como se describe en el presente documento puede ser un producto vegetariano o no vegetariano. Un producto vegetariano no contiene productos de carne o pescado. Una dieta no vegetariana puede contener cualquiera de los dos, o ambos, un producto de pescado (tal como harina de pescado) o un producto de carne (tal como derivados de carne, harina de huesos, etc.).
Pueden fabricarse composiciones de piensos similares para alimentar cerdos, otros tipos de aves de corral (patos, pavos, palomas), conejos, así como otros tipos de ganado, tales como ovejas, cabras y vacas.
Las composiciones de pienso son bien conocidas para otras especies de animales, incluyendo rumiantes tales como vacas, ovejas y cabras, cerdos, caballos, peces y crustáceos (gambas, cigalas, etc.). Muchas de éstas son específicas para la edad del animal, tal como durante la lactancia, en el destete, en el momento de aumento de peso máximo, durante la reproducción y para el mantenimiento. Puede añadirse una cantidad adecuada de compuesto para fines tales como maximizar el aumento de peso o mantener o restablecer el equilibrio gastrointestinal (especialmente durante los momentos de estrés, tales como después del tratamiento con antibióticos y en el destete).
2. Método de fabricación de agua potable enriquecida para animales
También se describen en el presente documento métodos para la producción de agua potable para animales enriquecida con inhibidores de biopelículas. Los métodos incluyen la adición de uno o más de los compuestos en un suministro de agua potable para animales. Las concentraciones adecuadas del uno o más compuestos en un suministro de agua potable son normalmente una concentración eficaz para producir el efecto del crecimiento potenciado en un animal en comparación con el crecimiento del animal con agua potable que no contiene los compuestos. La determinación de una concentración adecuada puede tener en cuenta la cantidad de agua potable consumida por el animal. Por ejemplo, un pollo de engorde en el Reino Unido (o a una temperatura equivalente a aquellas utilizadas en el Reino Unido) normalmente consume una cantidad diaria de agua potable que depende de su edad que puede calcularse por referencia a la edad del pollo en días multiplicada de aproximadamente 4-10 ml, tal como 5-9 ml, 6-8 ml, por ejemplo, aproximadamente 7,14 ml. Por lo tanto, por ejemplo, un pollo de engorde de 42 días puede tener un consumo de agua diario de 168 ml a 420 ml por día, más normalmente de aproximadamente 300 ml por día ± el 30%, 20%, 15%, 10%, 5%, 4% , 3%, 2% o 1 %. Los pollos de engorde criados a diferentes temperaturas pueden consumir más (por ejemplo, en el sur de los EE.UU., donde las temperaturas en verano serán altas y el consumo de agua podría ser mayor, particularmente en cobertizos en los que no se controla la temperatura) o menor.
El animal puede ingerir o absorber una cantidad eficaz de uno o más de los compuestos de forma regular y repetida. Por ejemplo, el animal puede ingerir o absorber una cantidad eficaz de uno o más compuestos semanalmente, cada dos días, todos los días o más de una vez al día durante la realización del método o uso. En una opción, los uno o más compuestos se incluyen en un pienso para animales, un suplemento de pienso para animales y/o en el agua potable y el animal ingiere el uno o más compuestos cuando come y/o bebe y, opcionalmente, cada vez que come y/o bebe. Esta ingestión o absorción de una cantidad eficaz de uno o más compuestos puede continuar durante un período de tiempo del crecimiento del animal que puede corresponder a un período de tiempo que es, es hasta, o es al menos, el 5 %, 10 %, 25 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o sustancialmente el 100 % de la vida del animal, desde el nacimiento hasta la muerte. La ingestión o absorción de una cantidad eficaz de uno o más compuestos puede comenzar el día del nacimiento del animal o a la edad de 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21,22, 23, 24, 25, 26, 2728, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41,42, 43, 44, 45, 46, 47 días o más. Después de que el animal comienza a ingerir o absorber el uno o más compuestos, el animal puede seguir haciéndolo de forma regular y repetida durante un período de tiempo que puede ser, o ser hasta, o al menos, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 2728, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47 días o más.
En el caso de los pollos, especialmente los pollos de engorde, los uno o más compuestos se ingieren preferentemente de forma repetida y regular en una dieta de inicio, en una dieta de crecimiento y/o en una dieta de finalización, como se describe en el presente documento.
Un suministro de agua potable para animales de, o para su uso en, los métodos que se desvelan en el presente documento, pueden incluir o suplementarse con, uno o más compuestos en una cantidad de 0,001 a 20 g del uno o más compuestos por L de agua, tal como de 0,002 a 15 g/l, o a un nivel de, hasta, o al menos, aproximadamente 0,002 g/l, 0,005 g/l, 0,01 g/l, 0,02 g/l, 0,03 g/l, 0,04 g/l, 0,05 g/l, 0,1 g/l, 0. 2 g/l, 0,3 g/l, 0,4 g/l, 0,5 g/l, 1 g/l, 2 g/l, 3 g/l, 4 g/l, 5 g/l, 10 g/l, 15 g/l o 20 g/l. Las mismas concentraciones pueden aplicarse al agua en la que viven animales acuáticos o de otro tipo.
3. Aditivos adicionales
Otros aditivos incluyen uno o más aditivos seleccionados de la lista que consiste en creatina, aminoácidos (por ejemplo, treonina) y sal y macrominerales, que incluyen aquellos seleccionados del grupo que consiste en calcio, fósforo, magnesio, sodio, potasio y cloruro.
Minerales traza, incluyendo cinc y/o selenio.
Vitaminas añadidas, que incluyen aquellas seleccionadas del grupo que consiste en vitamina A, ácido nicotínico, ácido pantoténico, piridoxina (B6) y biotina en piensos a base de maíz y trigo. Adicionalmente, los pollos de engorde tienen unas necesidades básicas de vitamina E de 10-15 mg/kg. La necesidad de suplementación adicional con vitamina E dependerá del nivel y el tipo de grasa de la dieta, del nivel de selenio y de la presencia de pro y antioxidantes. El tratamiento térmico de los piensos puede dar como resultado la destrucción de hasta el 20 % de la vitamina E. También puede proporcionarse colina en un pienso completo.
También pueden incluirse aditivos alimentarios no nutritivos. Se usan habitualmente enzimas en piensos para aves de corral para mejorar la digestibilidad de los ingredientes de los piensos. En general, hay disponibles enzimas de piensos que actúan sobre los hidratos de carbono, proteínas y minerales ligados a plantas. Las enzimas de polisacáridos no amiláceos (PNA) son económicamente beneficiosas en los piensos a base de trigo. Estas enzimas también permitirán una mayor flexibilidad en los niveles de cebada que han de incluirse en la ración. Pueden usarse enzimas fitasas para potenciar la utilización del fósforo del fitato. Pueden incluirse enzimas proteasas para que actúen sobre los productos vegetales. Pueden añadirse enzimas carbohidrasas, que pueden proporcionar respuestas beneficiosas cuando se usan en dietas de maíz-soja. Cuando se añaden enzimas antes del procesamiento térmico de los piensos para pollos de engorde, existe la posibilidad de una pérdida de actividad enzimática. Esto puede evitarse pulverizando enzimas sobre el pienso al final del procesamiento.
Pueden añadirse fármacos medicinales y profilácticos (distintos de los compuestos a continuación). Puede administrarse una amplia gama de medicamentos, por ejemplo, coccidiostáticos y antibióticos, a través del pienso. Pueden incluirse promotores de la digestión/promotores del crecimiento antibióticos y, por ejemplo, pueden proporcionar un modo de acción que implica la modificación de la microflora intestinal, con los consiguientes beneficios en la utilización de nutrientes.
Pueden añadirse prebióticos y se refieren a un grupo de sustancias que estimulan el crecimiento de microorganismos beneficiosos, a costa de los microorganismos perjudiciales. Los oligosacáridos forman el mayor grupo de estos productos en la actualidad.
Pueden añadirse probióticos para introducir microorganismos vivos en el tracto digestivo y ayudar a establecer una microflora estable y beneficiosa. El objetivo es proporcionar al intestino microorganismos positivos, no patógenos, que después impedirán la colonización con microorganismos patógenos por exclusión competitiva.
Pueden añadirse ácidos orgánicos. Pueden usarse productos ácidos orgánicos para reducir la contaminación bacteriana de los piensos (por ejemplo, después del tratamiento térmico) y también pueden favorecer el desarrollo de la microflora beneficiosa en el tracto digestivo del ave.
Se usan específicamente absorbentes para absorber micotoxinas. También pueden tener un efecto beneficioso sobre la absorción de nutrientes y la salud general de las aves. Existe una gama de productos disponibles para su uso como absorbentes, incluyendo diversas arcillas y carbón vegetal.
Los antioxidantes pueden proporcionar una protección importante contra la pérdida de nutrientes en piensos para pollos de engorde. Algunos ingredientes de los piensos, por ejemplo, la harina de pescado y las grasas, pueden protegerse. Las premezclas de vitaminas deben protegerse mediante un antioxidante, a menos que se proporcionen tiempos y condiciones óptimas de almacenamiento. Pueden añadirse antioxidantes adicionales al pienso final cuando sea inevitable un almacenamiento prolongado o unas condiciones de almacenamiento inadecuadas.
Pueden añadirse agentes antimoho. Por ejemplo, pueden añadirse inhibidores de moho a los ingredientes de los piensos, que se han contaminado, o a las raciones terminadas para reducir el crecimiento de hongos y la producción de micotoxinas.
Pueden añadirse agentes granuladores que se usan para mejorar la dureza de los gránulos. Algunos ejemplos de aglutinantes de gránulos son hemicelulosa, bentonita y goma guar.
Otros productos de posible uso en la producción de pollos de engorde incluyen aceites esenciales, nucleótidos, glucanos y extractos vegetales especializados. En las áreas del mundo donde su uso está permitido, puede usarse formaldehído para tratar/conservar los piensos.
Sin limitación, las dietas "de inicio", "de crecimiento" y "de finalización" de ejemplo incluyen aquellas que se muestran en los ejemplos.
4. Método de alimentación de los animales
Aunque lo siguiente es específico con respecto a los pollos, los expertos en la materia conocen las cantidades y el momento de alimentación adecuados y pueden determinarlos fácilmente, como demuestran los siguientes ejemplos.
Pueden alimentarse pollitos de engorde con la dieta de inicio durante aproximadamente los primeros 10-12 días (normalmente en el intervalo de los primeros 7-14 días de vida). Esta dieta de inicio puede ir seguida de la dieta de crecimiento, que se proporciona a los pollos de engorde durante casi 2 semanas (normalmente desde la edad de aproximadamente 11-24 días, aunque en cualquier caso, después del final del uso de la dieta de inicio). La dieta de finalización puede usarse durante el resto del período de producción (normalmente a partir de la edad de aproximadamente 24 o 25 días hasta la cosecha). Algunas naves de pollos de engorde usan más o menos dietas (por ejemplo, 4 dietas) y varían el momento de los cambios de dieta. Los pollos de engorde normalmente se cosechan entre 35 y 42 días, aunque este tiempo puede ser más largo o más corto. El mercado británico normalmente cosecha a los 30-35 días. Otros países, incluyendo algunos países europeos, cosechan a partir de los 25 días, aunque lo más normal es que sea a partir de los 30 días. Otros países, tales como los EE.UU., normalmente cosechan a los 42-47 días. Los pollos que no son de engorde, incluyendo los pollos criados libres, pueden ser cosechados a edades más avanzadas. Puede usarse cualquier edad de cosecha, aunque lo más típico (por ejemplo, en el contexto de los pollos de engorde) después del inicio de la dieta de finalización y, opcionalmente (y sin limitación), en cualquiera de los días 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70 o más, tal como hasta o aproximadamente 11 semanas, 12 semanas, 13 semanas, 14 semanas, 15 semanas, 16 semanas, 17 semanas, 18 semanas, 19 semanas, 20 semanas o más.
En algunas realizaciones, pueden realizarse métodos para la producción de pollos de engorde u otros animales en grupos que son de un solo sexo (es decir, grupos de animales únicamente hembras o únicamente machos) y/o pueden realizarse en grupos de animales de sexo mixto (es decir, machos y hembras mixtos). Por ejemplo, en el caso de la producción de pollos de engorde, puede ser adecuado seleccionar y criar un grupo de gallitos de un solo sexo juntos y puede ser adecuado cosechar los gallitos a una edad más temprana que los grupos de hembras o de sexo mixto. Por ejemplo, puede cosecharse un grupo de gallitos de un solo sexo de pollos de engorde a la edad de aproximadamente 30 días o, en otras opciones, a la edad de uno cualquiera o más de 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35 o más días. Por ejemplo, a la edad de 30 días, un grupo de gallitos sin tratar puede tener un peso objetivo promedio de aproximadamente 1,95 kg, mientras que en el caso del crecimiento potenciado resultante de los métodos que se desvelan en el presente documento, puede ser adecuado cosechar los gallitos en una fase más temprana al peso objetivo definido, o cosechar a la misma edad y un peso promedio mayor, o a la misma edad y peso objetivo con el uso de un consumo reducido de pienso para animales debido a una mayor eficiencia de conversión de pienso. En un ejemplo adicional, puede cosecharse un grupo de sexo mixto de pollos de engorde a la edad de aproximadamente 35 días o, en otras opciones, a la edad de uno o más de 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 o más días. Por ejemplo, a la edad de 35 días, un grupo de sexo mixto sin tratar puede tener un peso objetivo promedio de aproximadamente 2,1-2,2 kg, mientras que en el caso del crecimiento potenciado resultante de los métodos que se desvelan en el presente documento, puede ser adecuado cosechar el grupo de sexo mixto en una fase más temprana al peso objetivo definido, o cosechar a la misma edad y un peso promedio mayor, o a la misma edad y peso objetivo con el uso de un consumo reducido de pienso para animales debido a una mayor eficiencia de conversión de pienso.
En realizaciones en las que el animal que ha de criarse es una gallina ponedora, un proceso típico de cría de una gallina ponedora puede implicar el comienzo de la producción de huevos a alrededor de las 23 semanas de edad y el sacrificio a alrededor de las 60 semanas de edad. La gallina ponedora puede exponerse al uno o más compuestos antes de iniciar la puesta de huevos y/o durante la puesta de huevos y/o hasta el momento del sacrificio. El tratamiento puede durar, por ejemplo, aproximadamente 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55 o 60 semanas; el término "aproximadamente" en ese contexto puede incluir el significado de ± 4, 3, 2 o 1 semanas del valor indicado. Mientras que, normalmente, las gallinas ponedoras comienzan a poner huevos a las 23 semanas de edad, aprovechando los métodos que se desvelan en el presente documento para el crecimiento potenciado y/o la utilización de pienso potenciada, puede ser adecuado comenzar la producción de huevos a una edad más temprana, tal como a las 18, 19, 20, 21 o 22 semanas de edad. Además, aprovechando los métodos que se desvelan en el presente documento para el crecimiento potenciado y/o la utilización de pienso potenciada, la presente invención puede usarse para conseguir un efecto (en comparación con un grupo de control sin tratar que se cría en condiciones idénticas excepto por la aplicación de los compuestos) seleccionado de:
(a) la producción con huevos de calidad mejorada. La calidad mejorada, por ejemplo, puede seleccionarse del tamaño, la calidad de la cáscara, la célula de aire, la clara y la yema. La calidad de la cáscara se determina a partir de uno o más de entre el tamaño, los defectos visuales, el peso específico, el color, la resistencia a la rotura, el porcentaje de cáscara (peso de la cáscara x 100/peso del huevo), el espesor de la cáscara y la ultraestructura del huevo. La calidad mejorada puede reflejarse en una mayor proporción de huevos que se clasifican como grado de los EE.UU. A o AA;
(b) la producción de huevos de tamaño aumentado (tal como a un peso que es de hasta, o al menos, el 1 %, 2 %, 3 %, 4 %, 5 %, 6 %, 7 %, 8 %, 9 %, 10 %, 15 %, 20 % o más); y/o
(c) la producción de huevos en número aumentado (tal como en una cantidad promedio diaria, por grupo de al menos 100 animales y/o cuando se evalúa durante un período de al menos 10 días, que es una cantidad que es de hasta, o al menos, el 1 %, 2 %, 3 %, 4 %, 5 %, 6 %, 7 %, 8 %, 9 %, 10 %, 15 %, 20 % o más). El mismo enfoque puede adoptarse con otros animales ponedores. Los huevos producidos por gallinas ponedoras y otros animales
se etiquetan con información que indica la procedencia y la fecha o el origen.
En el presente documento también se proporcionan uno o más huevos, tal como una caja o un cartón de huevos, producidos por los animales (especialmente las gallinas ponedoras) que han sido tratados mediante uno o más de los métodos desvelados. Como se ha indicado anteriormente, dichos huevos normalmente llevarán una etiqueta que indica su procedencia y/o su fecha de origen. También se proporcionan productos derivados, especialmente productos alimenticios, producidos a partir de y/o que contienen huevos o partes de los mismos producidos por los animales (especialmente gallinas ponedoras) que han sido tratados mediante uno o más de los métodos desvelados.
En algunas realizaciones, los métodos y usos desvelados se realizan de manera que, durante el curso del tratamiento, el animal ingiere y/o absorbe una media diaria promedio de número total de moles del uno o más compuestos equivalente a una media diaria total promedio de FeQ de, hasta, o al menos, aproximadamente 1 |jg, 10 |jg, 100 |jg,
500 jg , 1 mg, 10 mg, 100 mg, 1 g, 2 g, 3 g, 4 g o 5 g.
En una opción adicional o alternativa, los métodos y usos desvelados se realizan de manera que, durante el curso del tratamiento, el animal ingiere y/o absorbe un número total de moles del uno o más compuestos equivalente a un total de FeQ de, hasta, o al menos, aproximadamente (a) 5 mg, 10 mg, 50 mg, 100 mg, 500 mg, 1 g, 5 g, 10 g, 50 g o 100 g por animal individual y/o (b) 1 mg, 2 mg, 3 mg, 4 mg, 5 mg, 10 mg, 50 mg, 100 mg, 200 mg, 300 mg, 400 mg, 500 mg,
600 mg, 700 mg, 800 mg, 900 mg, 1 g, 1,1 g, 1,2 g, 13 g, 1,4 g, 1,5 g, 1,6 g, 1,7 g, 1,8 g, 1,9 g, 2 g, 2,1 g, 2,2 g, 2,3 g,
2,4 g, 2,5 g, 2,6 g, 2,7 g, 2,8 g, 2,9 g, 3 g, 3,5 g, 4 g, 4,5 g, 5 g, 6 g, 7 g, 8 g, 9 g, 10 g, 20, g, 30 g, 40 g, 50 g, 60 g,
70 g, 80 g, 90 g o 100 g por kg de peso corporal promedio final, determinado el día de la administración final del uno o más compuestos.
El método de potenciación del crecimiento puede ponerse en práctica en múltiples animales, que opcionalmente pueden criarse juntos y, además, opcionalmente, en donde todos los animales criados juntos pueden emparejarse por edad con un mes, una semana o menos de diferencia, tal como, por ejemplo, con 6, 5, 4, 3, 2 o 1 días de diferencia.
Por ejemplo, el método puede ponerse en práctica en un grupo de hasta, aproximadamente, o al menos, 2, 3, 4, 5, 6,
7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 70, 80, 90, 100, 150, 200, 250, 300, 400, 500, 600, 700, 800, 900, 1x103, 2x103, 3x103, 4x103, 5x103, 6x103, 7x103, 8x103, 9x103, 1x104, 2x104, 3x104, 4x104, 5x104, 6x104, 9x104, 1x105, 2x105, 3x105, 4x105, 5x105, 6x105, 7x105, 8x105, 9x105, 1x106 o más, y todos los animales del grupo
pueden emparejarse opcionalmente por edad como se ha indicado anteriormente. El término "aproximadamente" en este contexto puede significar un margen del ±50 %, ±40 %, ±30 %, ±20 %, ±10 %, ±5 %, ±4 %, ±3 %, ±2 %, ±1 % o menos del valor indicado.
5. Animales que han de tratarse
Los animales tratados como se desvela en el presente documento pueden ser animales sanos, por ejemplo, animales que no están infectados o colonizados desventajosamente por bacterias u otros microorganismos. En otra realización, los animales pueden ser animales que no están sanos, infectados y/o colonizados desventajosamente por Campylobacter. El Campylobacter no es patógeno y no provoca enfermedad en el pollo por sí mismo (aunque, por supuesto, puede conducir a una intoxicación alimentaria si está presente en un producto cárnico derivado producido a partir del pollo), sin embargo, la colonización por Campylobacter puede considerarse desfavorable para el pollo ya que reduce su capacidad de crecimiento o de utilización eficiente del pienso. Como tal, en una realización, un animal que está colonizado desfavorablemente por bacterias u otros microorganismos es un animal que muestra un índice de crecimiento reducido, peso corporal reducido, aumento de peso reducido o un índice de conversión de pienso menos eficiente debido a la colonización, en comparación con un animal de control que difiere solo en que no tiene la colonización.
En algunas realizaciones, el animal puede ser un animal que ha estado expuesto a la cama (que incluye materia fecal) de uno o más de otros animales de la misma o diferente especie. Opcionalmente, la cama puede ser de animales que no están sanos que, por ejemplo, animales que están infectados y/o colonizados desfavorablemente por Campylobacter. En una realización, los animales tratados pueden ser pollos, tales como pollos de engorde, y pueden haberse expuesto a la cama de otros pollos, tal como una cama sucia como se describe en los presentes ejemplos y/o que porta Campylobacter y, opcionalmente, más patógenos, tales como Actinobacillus, Bordetalla, Clostridium, Corynebacterium, Escherichia coli, Globicatella, Listeria, Mycobacterium, Salmonella, Staphylococcus y Streptococcus. Como tales, los animales que han de tratarse pueden ser pollos (u otros animales) que están infectados y/o colonizados por uno o más de los patógenos anteriores.
En consecuencia, en algunas realizaciones, los métodos y usos desvelados pueden ser no terapéuticos, en el sentido de que el animal que ha de tratarse está sano y/o el método y el uso comprenden el sacrificio en última instancia del animal. En otras realizaciones, los métodos y usos desvelados pueden incluir beneficios terapéuticos para los animales que han de tratarse.
Los métodos y usos de potenciación del crecimiento de un animal, como se definen en las reivindicaciones adjuntas, incluyen potenciar una o más características seleccionadas del grupo que consiste en potenciar el peso corporal o (en
el caso de un grupo de animales) el peso corporal promedio (PCP), la ingesta de pienso o (en el caso de un grupo de animales) la ingesta de pienso promedio (IPP), el aumento de peso o (en el caso de un grupo de animales) el aumento promedio de peso (APP) y/o el índice de conversión de pienso ajustado a la mortalidad (iCPM).
En una realización (por ejemplo, en el contexto de un grupo de pollos criados en un corral), el ICPM durante un período dado puede calcularse de la siguiente manera:
ICPM = Ingesta de pienso total del período por corral / ((peso vivo total del corral peso total de las aves muertas en el corral) - peso vivo total del corral en el período anterior)
Por ejemplo, para el período de 0 a 20 días, el ICPM puede calcularse como:
ICPM día 0 a 20 = Ingesta de pienso total 0-20 días/((Peso corporal total el día 20 peso de mortalidad 0-20 días)-Peso corporal total día 0).
La potenciación del crecimiento del animal puede evaluarse en cualquier período conveniente durante el crecimiento del animal. Puede evaluarse, por ejemplo, desde el nacimiento hasta un punto temporal predeterminado, tal como hasta aproximadamente 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180 o más días. El término "aproximadamente" en este contexto puede significar ±5, ±4, ±3, ±2 o ± 1 días. Puede evaluarse, por ejemplo, desde el nacimiento hasta un punto temporal predeterminado, tal como hasta aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 % o 100 % de la vida del animal. Como alternativa, puede no medirse desde el nacimiento, sino medirse a lo largo de un período de la vida del animal que dure hasta aproximadamente 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180 o más días. De nuevo, el término "aproximadamente" en este contexto puede significar ±5, ±4, ±3, ±2 o ±1 días. Como alternativa, puede no medirse desde el nacimiento, sino medirse a lo largo de un período de la vida del animal representativo de aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 % o 99 % de la vida del animal.
En realizaciones para potenciar el crecimiento de pollos de engorde, que normalmente se sacrifican a una edad promedio de 35 días (en la UE) y 47 días (en los EE.UU.), el crecimiento potenciado puede medirse desde el nacimiento hasta la edad de sacrificio, o puede medirse hasta una edad más temprana, tal como de hasta 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 36, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46 o 47 días. Como alternativa, el crecimiento potenciado de pollos de engorde puede no medirse desde el nacimiento, sino durante otro período de la vida del pollo de engorde que dure, por ejemplo, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 36, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46 o 47 días.
El crecimiento potenciado, en algunas realizaciones, puede referirse a una potenciación en el crecimiento de un animal sujeto en comparación con un control que es de la misma raza de animal que el sujeto, o una potenciación en un grupo sujeto de animales en comparación con un grupo de control de un número equivalente de animales de la misma raza que el grupo sujeto, en donde el sujeto y el control tienen la misma edad o edad promedio (idealmente con un margen de error de menos de un día), en donde el crecimiento se mide durante el mismo período de tiempo (idealmente con un margen de error de menos de un día) y en donde el sujeto y el control se crían en las mismas condiciones, difiriendo solamente en que el sujeto recibe uno o más de los compuestos mientras que el control no.
En los métodos desvelados para potenciar el crecimiento de animales y, en particular, de aves de corral, tales como pollos y más preferentemente pollos de engorde, una potenciación del índice de crecimiento puede constituir una reducción del ICPM del sujeto en, hasta, o al menos, aproximadamente 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,10, 0,11, 0,12, 0,13, 0,14, 0,15, 0,16, 0,17, 0,18, 0,19 o 0,20. El término "aproximadamente" en este contexto puede incluir el significado de ± 5x10-3. La reducción del ICPM puede medirse, por ejemplo, entre los días 0 y 20, o entre los días 20 y 42 de la vida del animal o animales. En las condiciones económicas actuales, puede calcularse que una reducción del ICPM de 0,1 conducirá a un ahorro aproximado en el coste del pienso de aproximadamente 4 centavos de dólar de los EE.UU. por ave durante un período de crecimiento de 42 días y/o aproximadamente 10 libras esterlinas por tonelada de pienso para animales utilizado. Se apreciará que éstos son ahorros sustanciales en una industria en la que los costes normalmente se controlan a un nivel de aproximadamente 0,01 céntimos de dólar de los EE.UU. por ave.
En los métodos o el uso de los compuestos para potenciar el crecimiento de animales y, en particular, de aves de corral, tales como pollos y más preferentemente pollos de engorde, un aumento del índice de crecimiento puede constituir un aumento del PCP del sujeto en, hasta, o al menos, aproximadamente 10 g, 20 g, 30 g, 40 g, 50 g, 60 g, 70 g, 80 g, 90 g, 100 g, 110 g, 120 g, 130 g, 140 g, 150 g, 160 g, 170 g, 180 g, 190 g, 200 g, 210 g, 220 g, 230 g, 240 g, 250 g o más. El término "aproximadamente" en este contexto puede incluir el significado de ± 5 g, 4 g, 3 g, 2 g o 1 g. El aumento del PCP puede medirse, por ejemplo, entre los días 0 y 20, o entre los días 20 y 42, o durante la vida del animal o animales. El aumento del APP puede medirse, por ejemplo, entre los días 0 y 20, o entre los días 20 y 42 de la vida del animal o animales, o durante un período de tiempo seleccionado de 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 36, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45,
46 o 47 días. En el contexto de animales que normalmente (es decir, cuando no se tratan de acuerdo con los métodos desvelados) tienen un PCP más alto que el PCP normal de los pollos de engorde (es decir, cuando no se tratan de acuerdo con los métodos desvelados), entonces los valores anteriores pueden aumentar proporcionalmente. Es decir, por ejemplo, en el caso de un animal que tiene un PCP normal 10 veces superior al PCP normal de un pollo de engorde, entonces la potenciación del índice de crecimiento puede constituir un aumento del PCP del sujeto en, hasta, o al menos, aproximadamente 100 g, 200 g, 300 g, 400 g, 500 g, 600 g, 700 g, 800 g, 900 g, 1000 g, 1100 g, 1200 g, 1300 g, 1400 g, 1500 g, 1600 g, 1700 g, 1800 g, 1900 g, 2000 g, 2100 g, 2200 g, 2300 g, 2400 g, 2500 g o más, en donde el término "aproximadamente" en este contexto puede incluir el significado de ± 50 g, 40 g, 30 g, 20 g o 10 g.
Además, en el contexto de potenciar el crecimiento de animales y, en particular, de aves de corral, tales como pollos y más preferentemente pollos de engorde, una potenciación del índice de crecimiento puede constituir un aumento del aumento de peso promedio (APP) del sujeto en, hasta, o al menos, aproximadamente 10 g, 20 g, 30 g, 40 g, 50 g, 60 g, 70 g, 80 g, 90 g, 100 g, 110 g, 120 g, 130 g, 140 g, 150 g, 160 g, 170 g, 180 g, 190 g, 200 g, 210 g, 220 g, 230 g, 240 g, 250 g, 260 g, 270 g, 280 g, 290 g, 300 g o más durante un período de crecimiento, en comparación con un animal o grupo de animales de control. El término "aproximadamente" en este contexto puede incluir el significado de ± 5 g, 4 g, 3 g, 2 g o 1 g. El aumento del APP puede medirse, por ejemplo, entre los días 0 y 20, o entre los días 20 y 42 de la vida del animal o animales, o durante un período de tiempo seleccionado de 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 36, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46 o 47 días. En el contexto de animales que normalmente (es decir, cuando no se tratan de acuerdo con la presente invención) muestran un APP más alto que el APP normal de los pollos de engorde (es decir, cuando no se tratan de acuerdo con la presente invención), entonces los valores anteriores pueden aumentar proporcionalmente. Es decir, por ejemplo, en el caso de un animal que tiene un APP normal 10 veces superior al APP normal de un pollo de engorde durante un período de tiempo equivalente, entonces la potenciación del índice de crecimiento proporcionada por la presente invención puede constituir un aumento del APP del sujeto en, hasta, o al menos, aproximadamente 100 g, 200 g, 300 g, 400 g, 500 g, 600 g, 700 g, 800 g, 900 g, 1000 g, 1100 g, 1200 g, 1300 g, 1400 g, 1500 g, 1600 g, 1700 g, 1800 g, 1900 g, 2000 g, 2100 g, 2200 g, 2300 g, 2400 g, 2500 g, 2600 g, 2700 g, 2800 g, 2900 g, 3000 g o más, en donde el término "aproximadamente" en este contexto puede incluir el significado de ± 50 g, 40 g, 30 g, 20 g o 10 g.
En los Estados Unidos, la edad promedio de sacrificio de un pollo de engorde es de 47 días con un peso promedio de 2,6 kg; a la edad de 42 días, el peso promedio puede ser de aproximadamente 2,5 kg y en la UE, la edad promedio de sacrificio de un pollo de engorde es de 35 días con un peso promedio de 2,1-2,2 kg. Se apreciará que, como resultado del crecimiento potenciado proporcionado por los métodos y usos que se desvelan en el presente documento, será posible alcanzar el peso objetivo y cosechar el animal o los productos animales en una fase más temprana de la vida del animal de lo que sería posible con un control. Por ejemplo, en el contexto de un pollo de engorde, puede ser posible sacrificar al animal después de haber conseguido un peso corporal objetivo 1,2, 3, 4, 5, 6, 7, 8, 9, 10 o más días antes que un control. En ese contexto, el peso corporal objetivo de un pollo de engorde puede ser de, puede ser de hasta, o puede ser de al menos, aproximadamente 1000 g, 1100 g, 1200 g, 1300 g, 1400 g, 1500 g, 1600 g, 1700 g, 1800 g, 1900 g, 2000 g, 2100 g, 2200 g, 2300 g, 2400 g, 2500 g, 2600 g, 2700 g, 2800 g, 2900 g, 3000 g, 3100 g, 3200 g, 3300 g, 3400 g, 3500 g o más. El término "aproximadamente" en este contexto puede incluir ± 50 g, ± 40 g, ± 30 g, ± 20 g o ± 10 g del valor indicado. Dicho de otra manera, el pollo de engorde puede sacrificarse a, o antes de, la edad de 47, 46, 45, 44, 43, 42, 41,40, 39, 38, 37, 36, 35, 34, 33, 32, 31, 30, 29, 28, 27, 26 o 25 días, idealmente en donde ha alcanzado un peso corporal objetivo en el momento del sacrificio. Por lo tanto, por ejemplo, en una realización, el pollo de engorde se cría hasta un peso objetivo de aproximadamente 2,6 kg y el método o uso incluye la etapa de sacrificar al animal después de haber conseguido un peso corporal objetivo 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 o más días antes de la edad de 47 días. En otra realización ilustrativa, el pollo de engorde se cría hasta un peso objetivo de aproximadamente 2,5 kg y el método o uso incluye la etapa de sacrificar al animal después de haber conseguido un peso corporal objetivo 1,2, 3, 4, 5, 6, 7, 8, 9, 10 o más días antes de la edad de 42 días. En otra realización ilustrativa, el pollo de engorde se cría hasta un peso objetivo de aproximadamente 2,2 kg y el método o uso incluye la etapa de sacrificar al animal después de haber conseguido un peso corporal objetivo 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 o más días antes de la edad de 35 días.
En otra realización, el animal se cría durante la misma cantidad de tiempo que la norma de la industria, pero presenta un peso corporal mayor (tal como aproximadamente, al menos, o hasta, el 0,1 %. 0,5 %. 1 %. 2 %. 3 %, 4 %, 5 %, 10 %, 15 %, 20 %, 25 % o más) que la norma de la industria al final del proceso de cría. Por lo tanto, en el contexto de los pollos de engorde, el animal puede sacrificarse con un peso de aproximadamente 1000 g, 1100 g, 1200 g, 1300 g, 1400 g, 1500 g, 1600 g, 1700 g, 1800 g, 1900 g, 2000 g, 2100 g, 2200 g, 2300 g, 2400 g, 2500 g, 2600 g, 2700 g, 2800 g, 2900 g, 3000 g, 3100 g, 3200 g, 3300 g, 3400 g, 3500 g o más, en donde en el momento del sacrificio el peso corporal es aproximadamente, al menos, o hasta, el 0,1 %. 0,5 %. 1 %. 2 %. 3 %, 4 %, 5 %, 10 %, 15 %, 20 %, 25 % o más que el control. El término "aproximadamente" aplicado al peso en este contexto puede incluir ± 50 g, ± 40 g, ± 30 g, ± 20 g o ± 10 g del valor indicado.
En otra realización más, como resultado del efecto del crecimiento potenciado proporcionado por los métodos y usos desvelados, el animal es capaz de utilizar los piensos para animales con mayor eficiencia que un control. En consecuencia, en otra realización, los métodos y usos desvelados incluyen la opción de criar a un animal para que alcance un peso corporal objetivo usando menos pienso para animales que el necesario para que un control alcance
el peso objetivo. Por ejemplo, puede ser posible criar un animal para que alcance el peso objetivo usando una cantidad de pienso para animales enriquecido como se desvela en el presente documento que se reduce en peso en un 0,01 %, 0,05 %, 0,1 %, 0,2 %, 0,3 %, 0,4 %, 0,5 %, 1 %, 2 %, 3 %, 4 %, 5 %, 10 %, 15 %, 20 %, 25 % o más, en comparación con la cantidad del mismo pienso para animales que necesita un control para alcanzar el mismo peso objetivo. En ese contexto, el peso corporal objetivo de un pollo de engorde puede ser de, puede ser de hasta, o puede ser de al menos, aproximadamente 1000 g, 1100 g, 1200 g, 1300 g, 1400 g, 1500 g, 1600 g, 1700 g, 1800 g, 1900 g, 2000 g, 2100 g, 2200 g, 2300 g, 2400 g, 2500 g, 2600 g, 2700 g, 2800 g, 2900 g, 3000 g, 3100 g, 3200 g, 3300 g, 3400 g, 3500 g o más. El término "aproximadamente" en este contexto puede incluir ± 50 g, ± 40 g, ± 30 g, ± 20 g o ± 10 g del valor indicado.
Por ejemplo, en el contexto de la norma de la industria para criar un pollo de engorde durante 42 días, es normal proporcionar a cada pollo un total de 5,2 kg de pienso a lo largo de su vida (una media de 123,8 g de pienso por día de vida). En una situación de este tipo, una realización, implica alimentar a los pollos con una cantidad de pienso total reducida con respecto a 5,2 kg y/o reducida con respecto a un promedio medio de 123,8 g de pienso por día, en un 0. 01 %, 0,05 %, 0,1 %, 0,2 %, 0,3 %, 0,4 %, 0,5 %, 1 %, 2 %, 3 %, 4 %, 5 %, 10 %, 15 %, 20 %, 25 % o más, durante su crianza.
En consecuencia, los métodos y usos desvelados pueden comprender adicionalmente la etapa de criar al animal para permitir un crecimiento potenciado.
Otra realización descrita en el presente documento proporciona un método de prevención o reducción de la colonización del tracto gastrointestinal de un animal (tal como un animal descrito anteriormente) con Campylobacter y, opcionalmente, otras bacterias o microorganismos, provocando que el animal ingiera y/o absorba una cantidad eficaz de uno o más compuestos. Más específicamente, como se define en la reivindicación adjunta 9, la presente invención proporciona un producto dietético que comprende uno o más compuestos de complejo de Fe III de Fórmula 1, como se define adicionalmente por la reivindicación 9, para su uso en un método para el tratamiento o la profilaxis (incluyendo la reducción o la prevención) de la infección o colonización por Campylobacter en un animal no humano, en donde el producto dietético se administra al animal no humano solo en una cantidad eficaz para reducir la acumulación de biopelícula en el animal no humano. Por ejemplo, el uso puede ser para la reducción o la prevención de la colonización del tracto gastrointestinal de aves de corral u otros animales no humanos con Campylobacter.
La presente solicitud describe adicionalmente un método para la desinfección de un animal que comprende administrar al animal al menos uno o más compuestos que tienen la estructura de Fórmula I en una cantidad eficaz para reducir el número de Campylobacter y/u otras bacterias o microorganismos presentes en el tracto gastrointestinal del animal.
La presente solicitud describe adicionalmente un método para la desinfección de un animal que comprende administrar al animal al menos uno o más compuestos a continuación en una cantidad eficaz para prevenir que el Campylobacter y/u otras bacterias o microorganismos formen una biopelícula en el tracto gastrointestinal del animal o para reducir la cantidad de biopelícula formada por el Campylobacter y/u otras bacterias o microorganismos en el tracto intestinal del animal.
La presente solicitud describe adicionalmente un método para prevenir o reducir la transmisión de la infección por Campylobacter y/o la infección por otras bacterias o microorganismos, de un animal a otro, por ejemplo, prevenir o reducir la propagación del Campylobacter y/o la infección por otras bacterias o microorganismos, dentro de un rebaño o manada de animales, por ejemplo, prevenir la propagación de la infección por Campylobacter y/o la infección por otras bacterias o microorganismos, dentro de una bandada de pollos, incluyendo los pollos de engorde; el método comprende administrar a los animales, por ejemplo, la manada o el rebaño de animales, por ejemplo, la bandada de pollos, uno o más compuestos que tienen la estructura de Fórmula I en una cantidad eficaz para prevenir que el Campylobacter y/u otras bacterias o microorganismos, formen una biopelícula en el tracto gastrointestinal del animal o para reducir la cantidad de biopelícula formada por el Campylobacter y/u otras bacterias o microorganismos, en el tracto intestinal del animal.
Los métodos como se describen en el presente documento pueden permitir la desinfección, la prevención de la formación de biopelículas y la reducción de la transmisión del Campylobacter y/u otras bacterias o microorganismos, entre los animales impidiendo o reduciendo la adherencia del Campylobacter y/u otras bacterias o microorganismos, del tracto gastrointestinal de los animales. Esto es ventajoso porque cuanto menos Campylobacter y/u otras bacterias o microorganismos, haya en el tracto gastrointestinal de un animal en el momento del sacrificio, menor es el riesgo de contaminación de la carne del animal con Campylobacter y/u otras bacterias o microorganismos. Cuanto menos Campylobacter y/u otras bacterias o microorganismos haya en el tracto gastrointestinal de un animal, menor será la probabilidad de que el Campylobacter y/u otras bacterias o microorganismos, formen una biopelícula en el tracto gastrointestinal del animal. Cuanto menos Campylobacter y/u otras bacterias o microorganismos, haya en el tracto gastrointestinal de un animal, menor es la probabilidad de que el Campylobacter y/u otras bacterias o microorganismos, se propaguen de un animal a otro, por ejemplo, dentro de un rebaño o manada de animales.
Estos métodos que se describen en el presente documento también pueden usarse para reducir la cantidad de colonización del tracto gastrointestinal de cualquier animal con Campylobacter y/u otras bacterias o microorganismos.
Más específicamente, como se ha indicado anteriormente, el alcance de la reivindicación 9 adjunta se refiere a un producto dietético que comprende uno o más compuestos de complejo de Fe III de Fórmula I, como se define adicionalmente por la reivindicación 9, para su uso en un método para el tratamiento o la profilaxis de una infección o colonización por Campylobacter en un animal no humano. Puede ser particularmente ventajoso proporcionar el uno o más compuestos que tienen la estructura de Fórmula I a animales no humanos que serán sacrificados para el consumo humano. Las aves de corral incluyen las aves que se usan para el consumo humano, tales como pollos, gansos, pavos, faisanes y patos. Es particularmente ventajoso usar los compuestos para reducir o prevenir la colonización del tracto gastrointestinal de aves de corral, en particular pollos y, más particularmente, pollos de engorde, gallinas ponedoras y/o gallinas reproductoras, con Campylobacter porque los pollos son una de las principales fuentes de infección humana con Campylobacter.
El número de Campylobacter en el tracto gastrointestinal de los animales no humanos puede reducirse mediante los métodos definidos por la reivindicación 9. En una realización, el número de unidades formadoras de colonias (ufc) de Campylobacter en el tracto gastrointestinal de un animal no humano tratado con los compuestos puede reducirse en un 10 %, en un 20 %, en un 30 %, en un 40 %, en un 50 %, en un 60 %, en un 70 %, en un 80 %, en un 90 % o en un 100%. En una realización, el Campylobacter puede erradicarse sustancialmente del tracto gastrointestinal de un animal no humano tratado como se desvela en el presente documento.
10.000 ufc de Campylobacter son suficientes para la colonización exitosa de pollos. 1.000 ufc de Campylobacter son suficientes para infectar a un ser humano y provocar enfermedad en un ser humano. Por lo tanto, una cantidad eficaz de un compuesto desvelado es suficiente del compuesto para reducir el número de Campylobacter en el tracto gastrointestinal de un animal no humano, o sobre la superficie del ave, tal como la piel del cuello, a un número que es poco probable que provoque infección en seres humanos, tal como menos de 10.000 ufc, 5.000 ufc, 1.000 ufc, 500 ufc, 400 ufc, 300 ufc, 200 ufc, 100 ufc, 90 ufc, 80 ufc, 70 ufc, 60 ufc, 50 ufc o menos. El número de ufc de Campylobacter y/u otras bacterias o microorganismos que ingeriría un ser humano si comiera carne de un animal infectado puede estar relacionado con el número de Campylobacter y/u otras bacterias o microorganismos presentes en el tracto gastrointestinal del animal en el momento del sacrificio, pero también depende de otros factores tales como la cantidad de contaminación de la carne con el contenido del tracto gastrointestinal del animal en el momento del sacrificio.
Una cantidad eficaz del uno o más compuestos que tienen la estructura de Fórmula I, en este contexto, puede ser una cantidad suficiente del uno o más compuestos para prevenir la colonización del tracto gastrointestinal del animal no humano con Campylobacter.
En una realización, el uno o más compuestos que tienen la estructura de Fórmula I, pueden hacer que el Campylobacter sea menos virulento y menos capaz de infectar a los seres humanos incluso si el número total de Campylobacter y/u otras bacterias o microorganismos en el tracto gastrointestinal no disminuye. En la presente realización, la administración del compuesto a un animal no humano puede afectar al metabolismo del Campylobacter y hacerlo menos adaptable al entorno (por ejemplo, menos móvil), de manera que no pueda colonizar el tracto gastrointestinal y sea menos probable que se transmita a otros animales o a seres humanos.
Una cantidad eficaz de uno o más compuestos proporcionados a un animal no humano debe ser suficiente para proporcionar el grado necesario de reducción de la colonización por Campylobacter. Esto puede depender del tipo de compuesto y/o del tamaño del animal.
En una realización, el uno o más compuestos puede proporcionarse en un pienso para animales, bebida para animal u otras composiciones en una concentración dentro del intervalo de aproximadamente 1 pM a aproximadamente 1 M, preferentemente superior a 10 pM, 20 pM, 30 pM, 40 pM, 50 pM, 60 pM, 70 pM, 80 pM, 90 pM, 100 pM, 110 pM, 120 pM, 130 pM, 140 pM, 150 pM, 160 pM, 170 pM, 180 pM, 190 pM, 200 pM, 250 pM, 300 pM, 350 pM, 500 pM, 1 mM o más.
Por ejemplo, la concentración del uno o más compuestos puede ser:
(a) hasta 1 pM, 2 pM, 3 pM, 4 pM, 5 pM, 10 pM, 15 pM, 20 pM, 25 pM, 30 pM;
(b) dentro de un intervalo seleccionado del grupo que consiste en de 35 a 335 pM, de 40 a 300 pM, de 50 a 300 pM, de 50 a 250 pM, de 50 a 200 pM, de 60 a 300 pM, de 60 a 250 pM, de 60 a 200 pM, de 80 a 300 pM, de 80 a 250 pM, de 80 a 200 pM, de 100 a 300 pM, de 100 a 250 pM o de 100 a 200 pM; o
(c) al menos, o aproximadamente, 345 pM, 350 pM, 360 pM, 370 pM, 380 pM, 390 pM, 400 pM, 450 pM, 0,5 mM, 1 mM, 2 mM o más.
En otra realización, la concentración puede estar dentro de un intervalo seleccionado del grupo que consiste en de aproximadamente 1 pM a aproximadamente 1 mM, o de aproximadamente 30 pM a aproximadamente 0,5 mM, o de aproximadamente 60 pM a aproximadamente 0,3 mM.
En el caso de la bebida para animales (tal como el agua potable) u otros tipos de composición, opcionalmente, la concentración del uno o más compuestos en la composición puede estar dentro del intervalo de 0,002 a 15 g/l, o a un nivel de, hasta, o al menos, aproximadamente 0,002 g/l, 0,005 g/l, 0,01 g/l, 0,02 g/l, 0,03 g/l, 0,04 g/l, 0,05 g/l, 0,1 g/l,
0. 2 g/l, 0,3 g/l, 0,4 g/l, 0,5 g/l, 1 g/l, 2 g/l, 3 g/l, 4 g/l, 5 g/l, 10 g/l, 15 g/l o 20 g/l
En otra realización, el uno o más compuestos puede proporcionarse en un pienso para animales, bebida para animales u otra composición en una formulación de dosificación unitaria y/o a una concentración para entregar hasta, o al menos, aproximadamente 1 ng, 10 ng, 50 ng, 100 ng, 500 ng, 1 |jg, 10 |jg, 50 |jg, 100 jg , 500 jg , 1 mg, 10 mg, 100 mg, 500 mg, 1 g, 2 g, 3 g, 4 g o 5 g del uno o más compuestos.
Los métodos y usos desvelados pueden comprender adicionalmente la etapa de cosechar un producto del animal criado con un crecimiento potenciado.
El producto cosechado puede ser el cuerpo o una parte del cuerpo del animal. En ese caso, el proceso de cosecha incluye la etapa de sacrificio del animal y, opcionalmente, la preparación de una canal o parte de la misa como producto, tal como un producto cárnico. En consecuencia, el cuerpo cosechado o parte del cuerpo del animal puede ser un producto no alimenticio, un producto alimenticio o un precursor de un producto alimenticio. Las canales y las partes de las mismas pueden someterse a un proceso conocido como aprovechamiento de grasas para convertirlos en productos alimenticios humanos y no humanos, grasas y otros materiales que pueden comercializarse para fabricar productos comerciales tales como cosméticos, pintura, limpiadores, lacas, pegamento, jabón y tinta. Productos adicionales de este tipo que pueden ser productos alimenticios son, pero sin limitación, sangre, hueso, incluyendo el carbón de huesos, harina de huesos, etc., caldos creados con grasa animal, hueso y/o tejido conectivo, carmín también conocido como cochinilla (colorante alimentario), caseína (presente en la leche y el queso), aceite de civeta (aditivo aromatizante alimentario), gelatina, isinglass (que puede usarse, por ejemplo, en la clarificación de la cerveza y el vino), L-cisteína (que puede usarse, por ejemplo, en la producción de galletas y pan), manteca, carne (incluyendo pescado, aves de corral y caza) y cuajo (habitualmente utilizado en la producción de queso). La carne y los productos cárnicos pueden ser de interés particular.
En una realización particularmente preferida, el animal es un pollo, por ejemplo, un pollo de tipo cárnico, tal como un pollo de engorde, o una gallina ponedora, tal como una pollita o una gallina, y el producto se cosecha del animal criado. Mucho más preferentemente, el animal es un pollo de tipo cárnico, tal como un pollo de engorde, y el producto cosechado es una canal o parte de la canal del pollo. Después del sacrificio para producir la canal, puede o no procesarse adicionalmente, tal como para retirar uno o más elementos seleccionados del grupo que consiste en plumas, despojos, piel del cuello, cabeza, patas y otros elementos, y puede producir una canal entera faenada lista para la comercialización como producto cárnico, o lista para enviarla a un procesamiento adicional. En una realización, la canal procesada puede conservar el cuello o la piel del cuello, o al menos el 50 %, 60 %, 70 %, 80 %, 90 % o más de los mismos, como se determina por la longitud o el peso. El peso promedio del cuello o la piel del cuello puede estar en el intervalo de 15-25 g. El procesamiento adicional puede realizar una operación de despiece en donde la canal se corta en partes individuales y puede implicar el deshuesado (es decir, la retirada de los huesos de partes específicas) para producir artículos como filetes de pechuga u otros productos sin hueso.
En una realización de ejemplo, un proceso para el sacrificio y/o el procesamiento de un pollo puede incluir una cualquiera o más de los siguientes etapas metodológicas: (i) las aves llegan a la planta de procesamiento, normalmente en cajones de plástico; (ii) se usa luz azul para calmar a las aves; (iii) las aves se cuelgan; (iv) las aves entran en un tanque de aturdimiento; (v) las aves se sacrifican usando el sangrado del cuello, opcionalmente con una pausa de retardo para desangrar las aves; (vi) la piel y/o las plumas de las aves se calientan, por ejemplo, con agua, para aflojar los poros que sujetan las plumas; (vii) las plumas se retiran, por ejemplo, usando dedos de goma; (viii) se realiza una inspección para retirar las aves que no superen la evaluación de control de calidad; (ix) se usa un taladro u otro instrumento para crear un agujero en la canal y retirar el ano; (x) retirada de los intestinos y otros órganos internos, normalmente a través del agujero creado anteriormente; (xi) opcionalmente, la línea de producción se divide para la producción de pollos enteros y piezas de pollo; (xii) las piezas de pollo pueden cortarse usando un proceso automatizado y a través de un trabajo manual (trabajadores que cortan); incluyendo opcionalmente el hígado, el riñón y/o los corazones separados; (xiii) la canal de pollo entera y/o las piezas de pollo pueden etiquetarse directamente en el suelo de la planta de procesamiento, listas para la tienda de comestibles (incluyendo adicionalmente los precios opcionalmente) para que el producto pueda ir directamente al estante de la tienda.
Se apreciará que hay disponibles métodos alternativos para aturdir al ave y pueden sustituir al método indicado en el método anterior y/o utilizarse más generalmente de acuerdo con los métodos y usos que se desvelan en el presente documento. Los métodos de ejemplo alternativos de aturdimiento del ave incluyen, por ejemplo, aturdimiento en atmósfera controlada, matanza en atmósfera controlada, CO2 bifásico y descompresión lenta controlada.
Como alternativa, el ave puede no ser aturdida antes del sacrificio, por ejemplo, en el caso de la producción de un producto cárnico de acuerdo con leyes religiosas, tales como las leyes de sacrificio Halal, Qurrbani/Udhia y/o Shechita.
El procesamiento de la canal puede realizarse a temperaturas de refrigeración adecuadamente bajas, tales como aproximadamente 1, 2, 3, 4 o 5 °C.
En consecuencia, después del procesamiento de la canal del animal y/o la producción de piezas del mismo, la canal o parte de la misma puede procesarse adicionalmente para producir un producto de valor añadido y esto puede incluir
una o más etapas necesarias para preparar un producto listo para el consumidor, que pueden incluir la adición de uno cualquiera o más de condimentos, empanado, salsas y marinado, así como envases especiales para satisfacer la demanda del mercado de productos cómodos.
Adicionalmente, o como alternativa, el producto cosechado puede ser, por ejemplo, un subproducto del animal, tal como leche, huevos, lana, pelo, plumas o cama u otras materias fecales, y pueden recogerse del animal sin necesidad de sacrificar el animal. Dichos productos cosechados pueden procesarse adicionalmente y convertirse en otros productos. Por ejemplo, en el contexto de la leche, después pueden producirse productos lácteos adicionales (tales como mantequilla, queso, cuajada, yogur, suero de leche, leche en polvo, crema agria, salsas y otros alimentos lácteos cultivados, postres congelados tales como tartas heladas, otros postres congelados hechos con ingredientes lácteos). En el contexto de los huevos, después pueden producirse productos adicionales (en particular, productos alimenticios) que contienen o se producen con la totalidad o parte de los huevos recogidos. En el contexto de la lana, el pelo o las plumas, después puede ser posible, por ejemplo, producir fibras o tejidos, productos que contienen lana, pelo o plumas (tales como, pero sin limitación, productos rellenos), o los productos pueden ser resultado del procesamiento químico o enzimático de la lana, el pelo o las plumas. Por ejemplo, pueden producirse aminoácidos como producto de degradación de la lana, el pelo o las plumas. La cama de los pollos puede incluir una mezcla de heces, desperdicio de piensos, materiales de lecho y plumas que puede reciclarse o convertirse en abono y después esparcirse sobre las tierras de cultivo como fertilizante orgánico de bajo coste.
Todas y cada una de las etapas del proceso entero de cría de animales, cosecha de animales, sacrificio de animales, procesos de canales, producción de productos animales, producción de alimentos, envoltura, etiquetado, envío, almacenamiento y comercialización pueden beneficiarse de la aplicación de una desinfección o recubrimiento de la superficie, como se analiza adicionalmente a continuación. Por ejemplo, las zonas de cría de animales pueden contener una o más superficies desinfectadas conseguidas usando los métodos, usos y composiciones que se desvelan en el presente documento. Los recipientes para el transporte de animales, los aparatos utilizados en el sacrificio de animales, los aparatos utilizados en el procesamiento y/o el etiquetado de una canal de animal, o una parte de la misma, pueden contener una o más superficies desinfectadas conseguidas con los métodos, usos y composiciones que se desvelan en el presente documento. El producto animal, incluyendo una canal, un producto cárnico o cualquier otro producto de origen animal producido como se desvela en el presente documento, puede desinfectarse usando los métodos, usos y composiciones que se desvelan en el presente documento. El embalaje, los recipientes y/o los envoltorios para contener un producto animal, incluyendo una canal, un producto cárnico o cualquier otro producto animal pueden desinfectarse usando los métodos, usos y composiciones que se desvelan en el presente documento. Todas estas combinaciones de los enfoques forman realizaciones opcionales del primer aspecto.
La presente solicitud también desvela productos producidos por, y/o cosechados de, animales tratados como se desvela en el presente documento, incluyendo todos y cada uno de los productos analizados anteriormente, así como productos derivados que incluyen o se producen a partir de los mismos.
Por ejemplo, en el presente documento se describe una carne o un producto cárnico producidos de acuerdo con los métodos desvelados. Por ejemplo, una canal o parte de la misma que tenga un peso superior al de una canal o parte de la misma convencional, o que proceda de un animal que sea más joven que un control. Adicionalmente, o como alternativa, la canal o parte de la misma, o cualquier otro producto obtenido del animal, puede tener un nivel reducido de infección o colonización microbiana (tal como bacteriana, incluyendo Campylobacter) y/o una incidencia reducida de biopelículas en la misma, en comparación con un control.
B. Potenciación del efecto de los antibióticos y otros agentes antimicrobianos y abordamiento de la resistencia a antibióticos
Se ha descubierto que los compuestos que se describen en el presente documento son particularmente útiles en el tratamiento o la prevención de la infección por microorganismos resistentes a antibióticos. La presente solicitud desvela adicionalmente que pueden administrarse compuestos para provocar que los microorganismos pierdan su resistencia a antibióticos o para aumentar la sensibilidad del microorganismo a agentes antimicrobianos, para potenciar el efecto de los antibióticos y otros agentes antimicrobianos y abordar la resistencia a antimicrobianos y antibióticos.
De acuerdo con la divulgación de la presente solicitud, un producto que comprende el uno o más compuestos puede ser un producto dietético. El producto dietético puede o no incluir adicionalmente uno o más agentes antimicrobianos. Los productos dietéticos pueden incluir, por ejemplo, productos alimenticios, suplementos dietéticos, bebidas y cualquier otra composición tomada por vía oral, que incorporan el uno o más compuestos.
Como se describe en el presente documento, los uno o más compuestos se seleccionan del grupo que consiste en un complejo de un a-hidroxiácido con Fe III, o sales y/o hidratos del mismo. Más específicamente, en el contexto del producto dietético definido por la reivindicación 9, los uno o más compuestos se seleccionan de uno o más compuestos de complejo de Fe III de Fórmula I, como se define por la reivindicación 9.
Una divulgación adicional de la presente solicitud es un método para la preparación de un producto en sí, tal como un producto farmacéutico o veterinario, un dispositivo médico o un producto dietético, que es adecuado para su uso de acuerdo con los métodos y usos anteriores que se desvelan en el presente documento. El método puede incluir la etapa de mezclar, pulverizar, recubrir o combinar el uno o más compuestos con los materiales que forman la formulación o el dispositivo.
C. Inhibición de la formación y tratamiento de biopelículas preformadas
Un tercer aspecto de la presente divulgación se basa en el sorprendente hallazgo de que los compuestos tienen un amplio intervalo de acción en el tratamiento y la dispersión de biopelículas preexistentes y en la inhibición del desarrollo de biopelículas, creadas por una amplia gama de bacterias y otras fuentes microbianas, y que esta acción es eficaz en una gran diversidad de entornos.
En consecuencia, la presente solicitud describe un método de inhibición de la acumulación de biopelícula y/o alterar una biopelícula preexistente, en o sobre un tema o artículo que lo necesite, comprendiendo el método administrar al sujeto o al artículo una cantidad eficaz de uno o más compuestos que tienen la estructura de Fórmula I.
Más particularmente, la presente reivindicación 9 se refiere a un producto dietético, que comprende uno o más compuestos de complejo de Fe III de Fórmula I como se define por la reivindicación 9, para su uso en un método para el tratamiento o la profilaxis de una infección o colonización microbiana por Campylobacter en un animal no humano, mediante un método que comprende administrar por vía oral al animal no humano una cantidad eficaz del producto dietético, en donde el producto dietético se administra al animal no humano solo en una cantidad eficaz para reducir la acumulación de biopelícula en el animal no humano.
1. Organismos que ha de tratarse, inhibirse o destruirse
"Biopelícula", como se usa en el presente documento, se refiere a cualquier grupo de microorganismos en el que las células se adhieren a una superficie en una estructura compleja.
La formación de una biopelícula comienza con la unión de microorganismos que flotan libremente a una superficie. Estos primeros colonos se adhieren a la superficie inicialmente a través de una adhesión reversible y débil, a través de fuerzas de Van der Waals. Si los colonos no se separan inmediatamente de la superficie, pueden anclarse de forma más permanente usando estructuras de adhesión celular tales como los pili. Algunas especies no son capaces de adherirse a una superficie por sí mismas, pero en ocasiones son capaces de anclarse a la matriz o directamente a colonos anteriores. Es durante esta colonización que las células son capaces de comunicarse a través de la detección de quórum. Una vez que la colonización ha comenzado, la biopelícula crece a través de una combinación de división celular y reclutamiento. Las matrices de polisacáridos suelen encerrar biopelículas bacterianas. La fase final de la formación de biopelícula se conoce como dispersión y es la fase en la que la biopelícula se establece y solo puede cambiar de forma y tamaño.
En una realización, una biopelícula puede comprender, consistir esencialmente en, o consistir en, células microbianas que crecen en una biopelícula y que son fisiológicamente distintas de las células planctónicas del mismo organismo, que, por el contrario, son unicelulares. Opcionalmente, una biopelícula puede comprender, consistir esencialmente en, o consistir en, una especie o cepa de célula bacteriana.
En una opción alternativa, una biopelícula puede comprender, consistir esencialmente en, o consistir en, más de una especie o cepa de célula bacteriana, tal como hasta al menos 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40, 50, 6070, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900, 1000 o más especies o cepas diferentes de células bacterianas.
Las especies o cepas bacterianas de las biopelículas pueden incluir bacterias seleccionadas de una o más bacterias y/o arqueas gramnegativas, grampositivas, aeróbicas y anaeróbicas.
En consecuencia, en el presente documento se describen composiciones y métodos para inhibir, reducir o eliminar bacterias formadoras de biopelículas e infecciones bacterianas.
Las bacterias formadoras de biopelículas que han de ser inhibidas, reducidas, eliminadas o tratadas de acuerdo con la reivindicación 9 pueden ser Campylobacter seleccionado de Campylobacter jejuni.
Los ejemplos adicionales de biopelículas contemplados en el presente documento incluyen biopelículas que comprenden, consisten esencialmente en, o consisten en, clase de proteobacterias épsilon, tales como Campylobacter spp.
Campylobacter son bacterias gramnegativas, en forma de varilla espiral con un solo flagelo en uno o ambos polos. Pertenecen a la clase de las proteobacterias épsilon y están estrechamente relacionadas con Helicobacter y Wolinella. Se ha implicado al menos a una docena de especies de Campylobacter en enfermedades humanas, siendo C. jejuni
y C. coli las más comunes.
Campylobacter jejuni es la principal causa de gastroenteritis bacteriana humana (Pearson, et al., Appl Environ Microbiol., 59:987-996 (1993)). Las cuatro principales fuentes de infección son las carnes crudas (particularmente las de aves de corral), el agua no tratada, la leche cruda y los animales domésticos (Humphrey, et al., J Appl Bacteriol.
61:125-132. (1986) y Skirrow, Int J Food Microbiol., 12:9-16 (1991)). También se ha sugerido que, aunque no es universalmente el caso (Humphrey, et al., Public Health Lab Serv Microbiol Digest., 13:86-88. 91996), Jacobs-Reitsma, et al., Epidemiol Infect., 114:413-421 (1995) y Lindblom, et al., JHyg., 96:385-391 (1986)), la supervivencia en los sistemas de agua de instalaciones de cría de animales y de unidades de procesamiento de animales promueve la infección en animales y la contaminación cruzada de canales de animales (Humphrey, et al., Epidemiol Infect., 98:263-269 (1987), Kazwala, et al., Vet Rec. 1990;126:305-306. (1990) y, Pearson, et al., Appl Environ Microbiol., 59:987-996 (1993)). Por lo tanto, la supervivencia de C. jejuni en entornos acuáticos es importante tanto directa como indirectamente en la causa de enfermedades humanas.
Campylobacter spp. tienen proteínas de membrana externa (PME) (Buchanan, Curr. Opin. Struc. Biol., 9(40:455-461 (1999); Huyer, et al., FEMSMicrobiol. Lett., 37(3):247-250 (1986)]. Las proteínas de membrana externa principales (PMEP) tienen características estructurales únicas y actúan como porinas que son útiles para unir a las bacterias con su entorno. Campylobacter spp. poseen flagelos polares que proporcionan la motilidad necesaria para la colonización intestinal. El gen de la flagelina de Campylobacter tiene dos copias similares: flaA y flaB. La longitud de las regiones codificantes de las secuencias flaA y flaB son ambas de aproximadamente 1,7 kilobases y las secuencias flaA y flaB se ubican aproximadamente a 180 bases de distancia entre sí (Meinersmann, et al., Microbiology, 146(9):2283 (2000)).
Los métodos permiten la desinfección, la inhibición o la prevención de la formación de biopelículas sobre las superficies tratadas y la reducción de la transmisión de microorganismos formadores de biopelículas desde la superficie a otra superficie. El número de unidades formadoras de colonias bacterianas (ufc) sobre la superficie que se trata con los compuestos puede reducirse en un 50 %, en un 60 %, en un 70 %, en un 80 %, en un 90 % o en un 100 %, o, la acumulación de unidades formadoras de colonias bacterianas sobre la superficie tratada puede reducirse en un 50 %, en un 60 %, en un 70 %, en un 80 %, en un 90 % o en un 100 %.
La presente solicitud también desvela composiciones y artículos, incluyendo, pero sin limitación, composiciones farmacéuticas y veterinarias, composiciones de aditivos para alimentos o piensos y productos dentales, incluyendo masticables que pueden prepararse a partir del uno o más compuestos como se han definido anteriormente, y que se formulan y/o usan opcionalmente en combinación con uno o más antibióticos u otros agentes antimicrobianos. Como se describe en el presente documento, estas composiciones pueden usarse adicionalmente para el tratamiento o la profilaxis de una infección microbiana o de una biopelícula formada por bacterias u otros microorganismos, incluyendo uno o más de los siguientes: S. epidermidis, E. faecalis, E. coli, S. aureus, incluyendo Staphylococcus aureus resistente a la vancomicina (SARV) y Staphylococcus aureus resistente a la meticilina (SARM), Escherichia coli enteropatógena (ECEP), Escherichia coli uropatógena (ECUP), Pseudomonas, Streptococcus pneumoniae, Streptococcus anginosus, Neisseria gonorrhoeae, Salmonella (incluyendo la no tifoidea resistente a fármacos), Salmonella, incluyendo la Salmonella serotipo typhi resistente a fármacos, Salmonella Enteritidis, Salmonella Typhimurium, Mycoplasma, Eimeria, Enterococos, Shigella, Enterococcus resistente a la vancomicina (ERV), Streptococcus del grupo A resistente a la eritromicina, Streptococcus del grupo B resistente a la clindamicina, Enterobacterias resistentes a carbapenems (ERC), tuberculosis resistente a fármacos, Enterobacterias de espectro ampliado (ESBL), Acinetobacter resistente a múltiples fármacos (incluyendo MRAB), Clostridium difficile, E. coli enteropatógena (ECEP), Pseudomonas aeruginosa, Brachyspira, Propionibacterium acnes y Clostridium perfringens.
2. Métodos de administración
La Reivindicación 9 se refiere a la administración de un producto dietético, que comprende uno o más de los complejos de Fe III definidos. Los productos dietéticos pueden incluir, por ejemplo, productos alimenticios, suplementos dietéticos, bebidas y cualquier otra composición tomada por vía oral, que incorporan el uno o más compuestos.
Opcionalmente, los compuestos pueden añadirse al agua potable o a otros fluidos bebibles.
Por lo tanto, la administración puede incluir la administración enteral, incluyendo la administración en forma de formas farmacéuticas orales adecuadas, tales como comprimidos, cápsulas, soluciones, suspensiones, jarabes y pastillas para chupar. Opcionalmente, la administración enteral puede incluir la administración de formulaciones enterales de liberación controlada, incluyendo formas farmacéuticas orales, tales como cápsulas, comprimidos, soluciones y suspensiones, que se formulan para la liberación controlada, incluyendo la liberación prolongada y/o retardada.
3. Hospital y otros entornos
Los métodos y usos que se desvelan en el presente documento pueden ponerse en práctica en el hospital y también en otros entornos médicos y no médicos con el fin de abordar, inhibir, tratar, mejorar y/o alterar biopelículas.
4. Aplicaciones industriales, cosméticas y de consumo
La presente solicitud también desvela que las composiciones pueden usarse para desinfectar superficies industriales, impidiendo y/o retirando la acumulación de biopelícula sobre dichas superficies. En la presente divulgación, la formación de la biopelícula puede impedirse o inhibirse, o una biopelícula preformada puede retirarse mediante un método que comprende aplicar una composición que comprende el uno o más compuestos que tienen la estructura de Fórmula I, sobre una superficie que lo necesite, por ejemplo, en forma de una pulverización, espuma, gel, polvos; detergentes para platos o para la ropa (líquidos o sólidos), cera para superficies, limpiacristales, etc.
5. Aplicaciones médicas adicionales
La presente solicitud también desvela un uso adicional de los compuestos que tienen la estructura de Fórmula I y composiciones que comprenden uno o más del compuesto, para tratar cualquier afección médica asociada a la formación de biopelícula como resultado de microorganismos, incluyendo el Campylobacter.
Opcionalmente, el tratamiento de una infección microbiana en un sujeto que la necesite también puede incluir la administración adicional de uno o más agentes antimicrobianos, tales como uno o más antibióticos, al sujeto como se ha desvelado anteriormente.
III. COMPUESTOS Y COMPOSICIONES
Se desvela una clase de compuestos con una amplia gama de actividad, particularmente contra bacterias, y composiciones que incluyen estos compuestos. Los compuestos, que se encuentran más adelante en la presente solicitud, a continuación, y las composiciones que comprenden uno o más de los compuestos, se presentan en el presente documento como un cuarto aspecto de la presente divulgación.
Sin embargo, se apreciará que el alcance de la protección está definido por las reivindicaciones adjuntas, que se refieren, en particular, a un método no terapéutico de potenciación del crecimiento de un animal usando uno o más compuestos de complejo de Fe III de Fórmula I como se define adicionalmente por la reivindicación 1, a uso no terapéutico como se define adicionalmente por la reivindicación 2 de los compuestos de complejo de Fe III de la reivindicación 1 y a un producto dietético, que comprende uno o más compuestos de complejo de Fe III de Fórmula I como se define adicionalmente por la reivindicación 9 para su uso en un método para el tratamiento o la profilaxis de una infección o colonización por Campylobacter en un animal no humano como se define adicionalmente por la reivindicación 9.
De forma más general, sin embargo, como se desvela en el presente documento, los compuestos que se describen por la presente solicitud, y las composiciones que comprenden uno o más de estos compuestos, pueden usarse para inhibir o reducir la formación de biopelículas sobre una superficie, tratar o prevenir una infección y destruir algunos organismos resistentes a antibióticos. Por ejemplo, se desvelan compuestos y composiciones que comprenden uno o más de los compuestos, y métodos y usos que emplean uno o más de los compuestos y/o composiciones, para inhibir, reducir o impedir la formación o acumulación de biopelícula sobre una superficie o para eliminar, dispersar, reducir o erradicar la biopelícula sobre una superficie. También se desvelan compuestos y composiciones que comprenden uno o más de los compuestos, y métodos y usos que emplean uno o más de los compuestos y/o composiciones, para el tratamiento de, la inhibición del crecimiento de, y la inhibición de la colonización por, bacterias, tanto en entornos biológicos como no biológicos. También se desvelan compuestos y composiciones que comprenden uno o más de los compuestos, y métodos y usos que emplean uno o más de los compuestos y/o composiciones, para la desinfección de superficies, tanto en entornos biológicos como no biológicos, y productos que han sido recubiertos con, o tratados mediante, uno o más de los compuestos y/o composiciones. También se desvelan compuestos y composiciones que comprenden uno o más de los compuestos, y métodos y usos que emplean uno o más de los compuestos y/o composiciones, para potenciar los efectos de uno o más antibióticos, aumentar la sensibilidad de las bacterias (incluyendo las bacterias resistentes a antibióticos) a uno o más antibióticos y también para revertir la resistencia a antibióticos en bacterias. También se desvelan compuestos y composiciones que comprenden uno o más de los compuestos, y métodos y usos que emplean uno o más de los compuestos y/o composiciones, para potenciar el crecimiento de animales y su eficiencia en la utilización del pienso, en particular mediante la administración oral de composiciones de piensos y bebidas.
De acuerdo con la presente divulgación, todos los métodos y usos desvelados en la Sección II anterior pueden utilizar uno o más tipos de compuestos como se definen en esta sección III, incluyendo derivados, hidratos y sales como se definen en las subsecciones 1 y 2 s continuación, respectivamente.
A. Compuestos
Los siguientes compuestos como se describen en esta sección de la solicitud se desvelan por la presente.
También se desvelan composiciones que comprenden, que consisten esencialmente en, o que consisten en, uno o más de estos compuestos. Estas composiciones pueden usarse en todos los otros diversos aspectos, y métodos y usos desvelados anteriormente que emplean las composiciones, y pueden comprender, consistir esencialmente en, o
consistir en, uno o más tipos de compuestos como se definen en esta sección, incluyendo derivados y sales definidos en las subsecciones 1 y 2, respectivamente.
Los compuestos de interés particular para su uso de acuerdo con la presente invención incluyen complejos de Fe III que comprenden ligandos unidos al centro de hierro seleccionados de aminoácidos o a-hidroxiácidos, incluyendo, pero sin limitación, lactato férrico (también denominado en el presente documento Fe-Lac), citrato férrico (también denominado en el presente documento Fe-Cit), tartrato férrico (también denominado en el presente documento Fe-Tart), glicinato férrico (también denominado en el presente documento Fe-Gly) y el complejo de ion férrico con fenilalanina (también denominado en el presente documento Fe-Phe). Además, son de interés particular compuestos que son variantes, derivados y/o análogos estructurales y/o funcionales de los compuestos anteriores, como se describe adicionalmente a continuación en esta sección.
Los ligandos que pueden usarse en dichos complejos incluyen ligandos basados en aminoácidos o a-hidroxiácidos, como se define adicionalmente en las reivindicaciones adjuntas.
Sujeto al alcance de la definición de los compuestos de complejo de Fe III proporcionada en las reivindicaciones adjuntas, los aminoácidos de ejemplo pueden incluir, pero sin limitación, alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutámico, glicina, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptófano y valina, cada uno preferentemente en la isoforma L aunque, como se ha analizado anteriormente, en una realización alternativa uno o más (opcionalmente todos) pueden estar en la isoforma D. Las mezclas de isómeros ópticos de un mismo aminoácido pueden usarse, o no, en algunas realizaciones. El contexto para el que un aminoácido particular es relevante para la invención reivindicada en el presente documento se describe adicionalmente en las reivindicaciones.
Sujeto al alcance de la definición de los compuestos de complejo de Fe III proporcionada en las reivindicaciones adjuntas, los a-hidroxiácidos de ejemplo incluyen, pero sin limitación, ácido láctico, ácido glicólico, ácido cítrico, ácido tartárico, ácido málico y ácido mandélico.
De acuerdo con la presente invención, los compuestos son complejos de Fe III como se definen adicionalmente en las reivindicaciones adjuntas. En realizaciones preferidas, todos los ligandos son iguales. Los a-hidroxiácidos enumerados pueden contener más de un resto ácido carboxílico y la expresión base conjugada, como se usa en el presente documento, se refiere a ácidos que tienen al menos un grupo ácido en forma desprotonada. En algunas realizaciones, todos los grupos ácidos de un ligando derivado del a-hidroxiácido pueden estar desprotonados.
En otras realizaciones más de la presente invención, de los complejos de Fe de acuerdo con la Fórmula I, los uno o más ligandos presentes son independientemente una base conjugada de un aminoácido sustituido o no sustituido seleccionado del grupo de ligandos de aminoácidos definido por las reivindicaciones adjuntas, en donde x e y son como se han definido anteriormente; y sales y/o hidratos de los mismos.
En algunas realizaciones de la Fórmula I descrita anteriormente, la relación de x:y es de manera que la carga total de los complejos de Fe III es neutra. En determinadas realizaciones, los ligandos descritos anteriormente son ligandos bidentados o tridentados que forma complejos con el ion de Fe(III). En una realización alternativa, la carga total de los complejos de Fe III puede ser neutra debido a la presencia de un anión o un catión, tal como, pero sin limitación, ion hidróxido, cloruro, de sodio, de potasio o de litio. En otras realizaciones, los complejos de Fe pueden cristalizar incorporando una o más moléculas de base.
Los compuestos de ejemplo de complejos de Fe de acuerdo con la Fórmula I incluyen, pero sin limitación, los compuestos que se muestran a continuación:
1)
2 )
3)
4)
Glicinato férrico (indicado Fe-Gly)
En determinadas realizaciones, los compuestos que pueden unirse a PMEP o FlaA de Campylobacter, son complejos de Fe III que contienen cada uno tres ligandos bidentados, tal como se describe en el presente documento.
Se desvela que un compuesto de acuerdo con la Fórmula I, puede ser un compuesto que inhibe la formación de biopelículas por parte de bacterias medida en una perla de plástico, en donde la bacteria se cultiva en un medio que contiene el compuesto para formar una suspensión de crecimiento de la bacteria a 0,0001 DO/ml, la suspensión de crecimiento se deja crecer con perlas UV recubiertas de plástico (Lascells) y las perlas se someten a ensayo después de 24 horas para determinar la presencia de formación de biopelícula sobre las perlas (contando las bacterias después de su liberación de las perlas) y se comparan con un grupo de control en el que las bacterias no se cultivan en presencia del compuesto. Preferentemente, el compuesto inhibe la unión de las bacterias a las perlas recubiertas de plástico a un nivel de inhibición que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5%, incluso más preferentemente, o al menos, aproximadamente el 10%, 20%, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más del nivel de inhibición de la unión de las bacterias a las perlas UV recubiertas de plástico por un complejo de L-tirosina con Fe III o un complejo de ácido quínico con Fe III a la misma concentración molar. Se desvela que la bacteria puede ser Enterococcus faecalis, Staphylococcus epidermidis, Staphylococcus aureus, Campylobacter jejuni, Pseudomonas aeruginosa, Escherichia coli uropatógena y Escherichia coli enteropatógena.
También se desvela que un compuesto de acuerdo con la Fórmula I puede ser un compuesto que inhibe la unión de Helicobacter pylori al tejido gástrico humano (por ejemplo, como se determina mediante un método como se describe en el Ejemplo 5) a un nivel de inhibición que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5 %, incluso más preferentemente, o al menos, aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más del nivel de inhibición de la unión de las bacterias al tejido gástrico humano por un complejo de L-tirosina con Fe III o un complejo de ácido quínico con Fe III a la misma concentración molar, como se mide mediante el recuento del número promedio de bacterias unidas al tejido.
Se desvela adicionalmente que un compuesto de acuerdo con la Fórmula I, puede ser un compuesto que inhibe la formación de biopelículas de una bacteria, pero no inhibe el crecimiento planctónico de la bacteria, en donde la bacteria puede ser una o más de las siguientes: Enterococcus faecalis, Staphylococcus epidermidis, Staphylococcus aureus,
Campylobacter jejuni, Pseudomonas aeruginosa, Escherichia coli uropatógena y Escherichia coli enteropatógena. Preferentemente, los compuestos inhiben la formación de biopelículas (por ejemplo, como se mide mediante el índice de cobertura en el Ejemplo 7), a un nivel que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5 %, incluso más preferentemente, o al menos, aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más del nivel de inhibición de la biopelícula por un complejo de L-tirosina con Fe III o un complejo de ácido quínico con Fe III a la misma concentración molar.
Se desvela que un compuesto de acuerdo con la Fórmula I, puede ser un compuesto que impide la adhesión de las bacterias a una superficie y el impedimento de la adhesión de las bacterias a la superficie es a un nivel que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5 %, incluso más preferentemente, o al menos, aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más del nivel de unión de las bacterias por un complejo de L-tirosina con Fe III o un complejo de ácido quínico con Fe III a la misma concentración molar, como se mide mediante densidad óptica. Se desvela que la bacteria puede ser Enterococcus faecalis, Staphylococcus epidermidis, Staphylococcus aureus, Campylobacter jejuni, Pseudomonas aeruginosa, Escherichia coli uropatógena y Escherichia coli enteropatógena.
Se desvela que un compuesto de acuerdo con la Fórmula I, puede ser un compuesto que es capaz de hacer que una cepa de bacterias resistente a antibióticos sea sensible al antibiótico al que de otro modo es resistente (por ejemplo, cuando se determina mediante un método que comprende la inmersión de un parche en una solución del compuesto y un antibiótico, tal como la kanamicina, por ejemplo, a una concentración de 50 pg/ml como se describe en el Ejemplo 9, colocado en una placa con la cepa resistente al antibiótico (tal como una cepa resistente a la kanamicina de Escherichia coli enteropatógena o Campylobacter jejuni)) y provoca que la bacteria no crezca o reduce el índice de crecimiento de la cepa resistente a antibiótico en presencia del antibiótico en un nivel que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5 %, incluso más preferentemente, o al menos, aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más del nivel de reducción del índice de crecimiento provocado por un complejo de L-tirosina con Fe III o un complejo de ácido quínico con Fe III a la misma concentración molar.
Se desvela que un compuesto de acuerdo con la Fórmula I, puede ser un compuesto que provoca una disminución del índice de crecimiento a un nivel que es de, o al menos, aproximadamente el 1 %, 2 %, 3 %, 4 %, más preferentemente, o al menos, aproximadamente el 5 %, incluso más preferentemente, o al menos, aproximadamente el 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % o más de la disminución del índice de crecimiento medido mediante densidad óptica de una bacteria resistente a antibiótico cuando crece en presencia del compuesto y el antibiótico.
Se desvela que en lugar de la administración directa del uno o más compuestos, él o ellos o pueden formarse in vivo, mediante la administración de una sustancia adecuada que contenga hierro y uno o más ligandos adecuados capaces de formar los compuestos in vivo con el compuesto de hierro (véase: Campbell y Hasinoff, Ferrous sulfate reduces levodopa bioavailability: Chelation as a possible mechanism, Clin. Pharmacol. Ther. 45:220-5, 1989). Por ejemplo, puede administrarse sulfato ferroso y L-fenilalanina (como ligando) con el fin de formar Fe-Phe in vivo. En este ejemplo, el Fe2+ se oxida a Fe3+ in vivo y puede formar un complejo con la fenilalanina. Los compuestos también pueden formarse in vivo a partir de cualquier sustancia que pueda metabolizarse in vivo a los compuestos. Por ejemplo, podría administrarse fenilalanina con sulfato ferroso puesto que se metabolizará a tirosina in vivo y después podría formar un complejo con el hierro férrico (formado a partir de la oxidación de sulfato ferroso). Como alternativa, también podría administrarse cloruro férrico con, por ejemplo, fenilalanina.
Opcionalmente, uno o más compuestos para su uso en cualquiera de los métodos desvelados anteriormente, que son compuestos de acuerdo con la Fórmula I, pueden ser ligandos para las proteínas de la membrana externa principales (PMEP) o FlaA de Campylobacter y/o pueden ser capaces de regular negativamente la expresión de las proteínas FlaA y/o FlaB en una bacteria tal como Campylobacter, tal como hasta el punto de provocar una motilidad bacteriana reducida tal como cuando se determina mediante un método como se describe en el Ejemplo 21 de la presente solicitud. La unión de los compuestos a las PMEP o FlaA inhibe la unión, el enlace o la asociación de las PMEP o FlaA con otras proteínas, componentes de la biopelícula, superficies u otras bacterias.
Los compuestos que se desvelan en el presente documento que se unen a PMEP o FlaA de Campylobacter incluyen compuestos con estructuras descritas en esta sección, de acuerdo con las Fórmulas A o B, o compuestos adicionales como se describen a continuación. Se ha demostrado que estos compuestos inhiben tanto bacterias gramnegativas, tales como Pseudomonas aeruginosa, Campylobacter jejuni, Helicobacter pylori, Escherichia coli, Escherichia coli enteropatógena (ECEP), Escherichia coli uropatógena (ECUP) como bacterias grampositivas, tales como Staphylococcus epidermidis, Staphylococcus aureus y Enterococcus faecalis, que se cree que son predictivas de la eficacia con otras especies. Existe poca homología entre las PMEP de Campylobacter y otras bacterias. Se cree que los compuestos interactúan con varias proteínas bacterianas similares a las porinas de superficie que aún no se han identificado en otras bacterias.
En el caso de los compuestos que son complejos de Fe III que comprenden ligandos unidos al centro de hierro, en una opción no todos los ligandos serán iguales en las composiciones que comprenden los compuestos de complejo de Fe III. Por lo tanto, por ejemplo, en una composición que comprende un complejo de Fe III como se ha descrito anteriormente, puede ser que menos del 100 % de los ligandos de Fe III sean idénticos, aunque preferentemente al menos el 50 %, 60 %, 70 %, 80 %, 85 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 % o 99 % de los ligandos en la composición son idénticos. En ese contexto, en una realización el término "idéntico" discrimina entre las formas enantioméricas del ligando, es decir, los enantiómeros diferentes no son idénticos; mientras que, en otra realización, el término "idéntico" puede aplicarse a diferentes formas enantioméricas del ligando, es decir, las formas enantioméricas opcionalmente diferentes del mismo ligando se consideran idénticas.
1. Derivados
También se desvelan derivados de los compuestos en el presente documento. El término "derivado" no significa que el derivado se sintetice a partir del compuesto parental como material de partida o intermedio, aunque puede ser así. El término "derivado" puede incluir sales (por ejemplo, sales farmacéuticamente aceptables), profármacos o metabolitos del compuesto parental. Los derivados incluyen compuestos en los que los grupos amino libres del compuesto parental se han derivatizado para formar clorhidratos de amina, p-tolueno sulfoamidas, benzoxicarboamidas, t-butiloxicarboamidas, derivados de tipo tiouretano, trifluoroacetilamidas, cloroacetilamidas o formamidas. Los derivados incluyen compuestos que tienen uno o más sustituyentes amino o grupos hidrógeno reemplazados por grupos alquilo, aminoalquilo, arilo o heteroarilo sustituidos o sin sustituir que tienen de 1 a 30 átomos de carbono. En el contexto de la invención que se reivindica en el presente documento, un derivado es una sal y/o un hidrato de compuestos de complejo de Fe III de Fórmula I como se define en las reivindicaciones adjuntas.
2. Sales
Los compuestos de las Fórmulas que se describen en el presente documento, tales como los compuestos definidos anteriormente, puede estar en forma de sal, por ejemplo, una sal farmacéuticamente aceptable. Los ejemplos de sales farmacéuticamente aceptables incluyen, pero sin limitación, sales de ácidos minerales u orgánicos de restos básicos tales como aminas; y sales alcalinas u orgánicas de restos ácidos tales como ácidos carboxílicos. Las sales farmacéuticamente aceptables incluyen las sales no tóxicas convencionales o las sales de amonio cuaternario del compuesto parental formadas, por ejemplo, a partir de ácidos inorgánicos u orgánicos y bases inorgánicas u orgánicas no tóxicos. Dichas sales no tóxicas convencionales incluyen las derivadas de ácidos inorgánicos tales como los ácidos clorhídrico, bromhídrico, sulfúrico, sulfámico, fosfórico y nítrico; y las sales preparadas a partir de ácidos orgánicos, tales como las sales acética, propiónica, succínica, glicólica, esteárica, láctica, málica, tartárica, cítrica, ascórbica, pamoica, maleica, hidroximaleica, fenilacética, glutámica, benzoica, salicílica, sulfanílica, 2-acetoxibenzoica, fumárica, toluenosulfónica, naftalenosulfónica, metanosulfónica, etanodisulfónica, oxálica e isetiónica, y bases tales como hidróxido de litio, hidróxido de sodio, hidróxido de potasio e hidróxido de amonio.
Las sales farmacéuticamente aceptables de los compuestos pueden sintetizarse a partir del compuesto parental, que contiene un resto básico o ácido, mediante métodos químicos convencionales. Generalmente, dichas sales pueden prepararse haciendo reaccionar las formas de ácido o base libres de estos compuestos con una cantidad estequiométrica de la base o ácido adecuado en agua o en un disolvente orgánico, o en una mezcla de los dos; generalmente, medios no acuosos como éter, acetato de etilo, etanol, isopropanol o acetonitrilo. Se encuentran listas de sales adecuadas en Remington's Pharmaceutical Sciences, 20a ed., Lippincott Williams & Wilkins, Baltimore, MD, 2000, p. 704; y "Handbook of Pharmaceutical Salts: Properties, Selection, and Use", P. Heinrich Stahl y Camille G. Wermuth, Ed., Wiley-VCH, Weinheim, 2002.
B. Agentes antimicrobianos
Los agentes antimicrobianos que pueden usarse terapéuticamente y/o no terapéuticamente con los compuestos desvelados en el presente documento anteriormente, por ejemplo, para el tratamiento o la profilaxis de la infección microbiana en los métodos desvelados anteriormente ya sea por separado, simultánea o secuencialmente, incluyen, pero sin limitación: (i) Aminoglucósidos, incluyendo amikacina, gentamicina, kanamicina, neomicina, netilmicina, tobramicina, paromomicina, estreptomicina, espectinomicina; (ii) Ansaicinas, incluyendo geldanamicina, herbimicina, rifaximina, (iii) Carbacefema, incluyendo loracarbef, (iv) Carbapenemas, incluyendo ertapenem, doripenem, imipenem/cilastatina, meropenem, (v) Cefalosporinas, incluyendo cefadroxilo, cefazolina, cefalotina o cefalotina, cefalexina, cefaclor, cefamandol, cefoxitina, cefprozilo, cefuroxima, cefixima, cefdinir, cefditoreno, cefoperazona, cefotaxima, cefpodoxima, ceftazidima, ceftibuteno, ceftizoxima, ceftriaxona, cefepima, ceftarolina fosamilo, ceftobiprol, (vi) Glicopéptidos, incluyendo teicoplanina, vancomicina, telavancina, dalbavancina, oritavancina, (vii) Lincosamidas, incluyendo clindamicina, lincomicina, (viii) Lipopéptidos incluyendo daptomicina, (ix) Macrólidos incluyendo azitromicina, claritromicina, diritromicina, eritromicina, roxitromicina, troleandomicina, telitromicina, espiramicina, (x) Monobactamas, incluyendo aztreonam, (xi) Nitrofuranos, incluyendo furazolidona, nitrofurantoína, (xii) Oxazolidinonas, incluyendo linezolid, posizolida, radezolida, torezolida, (xiii) Penicilinas, incluyendo amoxicilina, ampicilina, azlocilina, carbenicilina, cloxacilina, dicloxacilina, flucloxacilina, mezlocilina, meticilina, nafcilina, oxacilina, penicilina G, penicilina V, piperacilina, temocilina, ticarcilina, amoxicilina/clavulanato, ampicilina/sulbactama, peperacilina/tazobactam, ticarcilina/clavulanato (xiv) Polipéptidos incluyendo bacitracina, colistina, polimixina B, (xv)
Quinolonas/Fluoroquinolona, incluyendo ciprofloxacino, enoxacino, gatifloxacino, gemifloxacino, levofloxacino, lomefloxacino, moxifloxacino, ácido nalidíxico, norfloxacino, ofloxacino, trovafloxacino, grepafloxacino, esparfloxacino, temafloxacino, (xvi) Sulfonamidas, incluyendo mafenida, sulfacetamida, sulfadiazina, sulfadiazina de plata, sulfadimetoxina, sulfametizol, sulfametoxazol, sulfanilamida, sulfasalazina, sulfisoxazol, trimetoprim-sulfametoxazol (cotrimoxazol), sulfonamidocrisoidina, (xvii) Tetraciclinas, incluyendo demeclociclina, doxiciclina, minociclina, oxitetraciclina, tetraciclina, (xviii) clofazimina, dapsona, capreomicina, cicloserina, etambutol, etionamida, isoniazid, pirazinamida, rifampicina (rifampina), rifabutina, rifapentina, estreptomicina, arsfenamina, cloranfenicol, fosfomicina, ácido fusídico, metronidazol, mupirocina, platensimicina, quinupristina/dalfopristina, tianfenicol, tigeciclina, tinidazol y trimetoprim; y combinaciones de los mismos. Los compuestos también pueden combinarse con triclosán y clorhexidina. Otros agentes antimicrobianos incluyen: aztreonam; cefotetan y su sal disódica; loracarbef; cefoxitina y su sal de sodio; cefazolina y su sal de sodio; cefaclor; ceftibuteno y su sal de sodio; ceftizoxima; sal de sodio de ceftizoxima; cefoperazona y su sal de sodio; cefuroxima y su sal de sodio; cefuroxima axetilo; cefprozilo; ceftazidima; cefotaxima y su sal de sodio; cefadroxilo; ceftazidima y su sal de sodio; cefalexina; nafato de cefamandol; cefepima y su clorhidrato, sulfato y sal de fosfato; cefdinir y su sal de sodio; ceftriaxona y su sal de sodio; cefixima y su sal de sodio; cefpodoxima proxetilo; meropenem y su sal de sodio; imipenem y su sal de sodio; cilastatina y su sal de sodio; azitromicina; claritromicina; diritromicina; eritromicina y sales clorhidrato, sulfato o fosfato, formas de etilsuccinato y estearato de la misma, clindamicina; sal clorhidrato, sulfato o fosfato de clindamicina; lincomicina y sal clorhidrato, sulfato o fosfato de la misma, tobramicina y su sal clorhidrato, sulfato o fosfato; estreptomicina y su sal clorhidrato, sulfato o fosfato; neomicina y su sal clorhidrato, sulfato o fosfato; acetil sulfisoxazol; colistimetato y su sal de sodio; quinupristina; dalfopristina; amoxicilina; ampicilina y su sal de sodio; ácido clavulánico y su sal de sodio o potasio; penicilina G; penicilina G benzatina, o sal de procaína; sal de sodio o potasio de penicilina G; carbenicilina y su sal disódica o indanilo disódica; piperacilina y su sal de sodio; ticarcilina y su sal disódica; sulbactam y su sal de sodio; moxifloxacino; ciprofloxacino; ofloxacino; levofloxacino; norfloxacino; gatifloxacino; mesilato de trovafloxacino; mesilato de alatrofloxacino; trimetoprim; sulfametoxazol; demeclociclina y su sal clorhidrato, sulfato o fosfato; doxiciclina y su sal clorhidrato, sulfato o fosfato; oxitetraciclina y su sal clorhidrato, sulfato o fosfato; clortetraciclina y su sal clorhidrato, sulfato o fosfato; metronidazol; dapsona; atovaquona; rifabutina; linezolida; polimixina B y su sal clorhidrato, sulfato o fosfato; sulfacetamida y su sal de sodio; claritromicina; y iones, sales y complejos de plata.
C. Excipientes y vehículos
Los compuestos anteriores pueden formularse para su uso como se describe en las reivindicaciones adjuntas.
Los compuestos anteriores pueden combinarse con uno o más vehículos y/o excipientes farmacéuticamente aceptables que se consideran seguros y eficaces y que pueden administrarse a un individuo sin provocar efectos secundarios biológicos indeseables o interacciones no deseadas.
El vehículo puede incluir todos los componentes presentes en la formulación farmacéutica distintos del principio o los principios activos. Los compuestos se incluyen en la formulación en una cantidad eficaz para conseguir el efecto deseado, por ejemplo, en una cantidad que sea eficaz para inhibir la formación de biopelículas o reducir su acumulación. Una cantidad eficaz de un compuesto proporcionado a un sujeto puede ser una cantidad suficiente para proporcionar el grado necesario de reducción de la colonización microbiana. Esto puede depender del tipo de compuesto y/o del tamaño del animal.
En una realización, una cantidad eficaz del compuesto puede ser una cantidad que es eficaz para entregar el compuesto al sitio en el que se requiere la acción en una concentración que varía de 1 pm a 1 M, preferentemente superior a 10 pM, 20 pM, 30 pM, 40 pM, 50 pM, 60 pM, 70 pM, 80 pM, 90 pM, 100 pM, 110 pM, 120 pM, 130 pM, 140 pM, 150 pM, 160 pM, 170 pM, 180 pM, 190 pM, 200 pM o más. Una concentración adecuada puede estar dentro del intervalo de aproximadamente 1 pm a aproximadamente 1 mM, o de aproximadamente 30 pm a aproximadamente 0. 5 mM, o de aproximadamente 60 pM a aproximadamente 0,3 mM. Estas concentraciones pueden aplicarse particularmente en el contexto de los aspectos segundo y/o tercero de la presente divulgación.
En otra realización, una cantidad eficaz del compuesto puede ser de 0,3 a 32 mg/día/kg de peso corporal del sujeto, tal como un pollo.
Los compuestos también pueden formularse para su uso como desinfectante, por ejemplo, en un entorno hospitalario o para la aplicación industrial.
1. Formulaciones parenterales
La presente solicitud desvela que los compuestos anteriores pueden formularse para la administración parenteral.
La administración parenteral puede incluir la administración a un paciente por vía intravenosa, por vía intradérmica, por vía intraarterial, por vía intraperitoneal, por vía intralesional, por vía intracraneal, por vía intraarticular, por vía intraprostática, por vía intrapleural, por vía intratraqueal, por vía intravítrea, por vía intratumoral, por vía intramuscular, por vía subcutánea, por vía subconjuntiva, por vía intravesicular, por vía intrapericárdica, por vía intraumbilical, por inyección y por infusión.
(a) Formulaciones de liberación controlada
Las formulaciones parenterales que se describen en el presente documento que comprenden uno o más compuestos anteriores pueden formularse para la liberación controlada, incluyendo la liberación inmediata, la liberación retardada, la liberación prolongada, la liberación pulsada y combinaciones de las mismas.
(b) Formulaciones inyectables/implantables
Los uno o más compuestos anteriores pueden incorporarse a implantes sólidos o semisólidos inyectables/implantables, tales como implantes poliméricos.
2. Formulaciones enterales
Los compuestos anteriores pueden formularse para la administración enteral.
Las formas farmacéuticas orales adecuadas incluyen comprimidos, cápsulas, soluciones, suspensiones, jarabes y pastillas para chupar. Los comprimidos pueden fabricarse usando técnicas de compresión o moldeo bien conocidas en la técnica. Las cápsulas de gelatina o no de gelatina pueden prepararse como cubiertas de cápsulas duras o blandas, que pueden encapsular materiales de relleno líquidos, sólidos y semisólidos, usando técnicas bien conocidas en la técnica.
Las formulaciones pueden prepararse usando un vehículo farmacéuticamente aceptable. Como se usa generalmente en el presente documento, "vehículo" incluye, pero sin limitación, diluyentes, conservantes, aglutinantes, lubricantes, disgregantes, agentes de hinchamiento, cargas, estabilizantes y combinaciones de los mismos.
El vehículo también incluye todos los componentes de la composición de recubrimiento, que puede incluir plastificantes, pigmentos, colorantes, agentes estabilizantes y sustancias de deslizamiento.
Los ejemplos de materiales de recubrimiento adecuados incluyen, pero sin limitación, polímeros de celulosa tales como ftalato de acetato de celulosa, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, ftalato de hidroxipropilmetilcelulosa y succinato de acetato de hidroxipropilmetilcelulosa; ftalato de acetato de polivinilo, polímeros y copolímeros de ácido acrílico y resinas metacrílicas que se comercializan con el nombre comercial EUDRAGIT® (Roth Pharma, Westerstadt, Alemania), zeína, goma laca y polisacáridos.
Adicionalmente, el material de recubrimiento puede contener vehículos convencionales tales como plastificantes, pigmentos, colorantes, sustancias de deslizamiento, agentes de estabilización, formadores de poros y tensioactivos.
Los "diluyentes", también denominados "cargas", normalmente son necesarios para aumentar el volumen de una forma farmacéutica sólida de manera que se proporcione un tamaño práctico para la compresión de comprimidos o la formación de perlas y gránulos. Los diluyentes adecuados incluyen, pero sin limitación, dihidrato de fosfato dicálcico, sulfato de calcio, lactosa, sacarosa, manitol, sorbitol, celulosa, celulosa microcristalina, caolín, cloruro de sodio, almidón seco, almidones hidrolizados, almidón pregelatinizado, dióxido de silicio, óxido de titanio, silicato de aluminio y magnesio y azúcar en polvo.
Los "aglutinantes" se usan para transmitir cualidades cohesivas a una formulación de dosificación sólida y, de este modo, garantizar que un comprimido o perla o gránulo permanezca intacto después de la formación de las formas farmacéuticas. Los materiales aglutinantes adecuados incluyen, pero sin limitación, almidón, almidón pregelatinizado, gelatina, azúcares (incluyendo sacarosa, glucosa, dextrosa, lactosa y sorbitol), polietilenglicol, ceras, gomas naturales y sintéticas tales como goma arábiga, tragacanto, alginato de sodio, celulosa, incluyendo hidroxipropilmetilcelulosa, hidroxipropilcelulosa, etilcelulosa y veegum, y polímeros sintéticos tales como copolímeros de ácido acrílico y ácido metacrílico, copolímeros de ácido metacrílico, copolímeros de metacrilato de metilo, copolímeros de metacrilato de aminoalquilo, ácido poliacrílico/ácido polimetacrílico y polivinilpirrolidona.
Los "lubricantes" se usan para facilitar la fabricación de comprimidos. Los ejemplos de lubricantes adecuados incluyen, pero sin limitación, estearato de magnesio, estearato de calcio, ácido esteárico, behenato de glicerina, polietilenglicol, talco y aceite mineral.
Los "disgregantes" se usan para facilitar la disgregación o "ruptura" de la forma farmacéutica después de su administración y generalmente incluyen, pero sin limitación, almidón, glicolato sódico de almidón, carboximetilalmidón sódico, carboximetilcelulosa sódica, hidroxipropilcelulosa, almidón pregelatinizado, arcillas, celulosa, alginina, gomas o polímeros reticulados, tales como PVP reticulado (POLYPLASDONE® XL de GAF Chemical Corp).
Los "estabilizantes" se usan para inhibir o retardar las reacciones de descomposición del fármaco, que incluyen, a modo de ejemplo, reacciones oxidativas. Los estabilizantes adecuados incluyen, pero sin limitación, antioxidantes, hidroxitolueno butilado (BHT); ácido ascórbico, sus sales y ésteres; vitamina E, tocoferol y sus sales; sulfitos tales
como metabisulfito de sodio; cisteína y sus derivados; ácido cítrico; galato de propilo y butilhidroxianisol (BHA).
(a) Formulaciones enterales de liberación controlada
Las formas farmacéuticas orales, tales como cápsulas, comprimidos, soluciones y suspensiones, pueden formularse para la liberación controlada, por ejemplo, para la liberación controlada del uno o más compuestos anteriores. Por ejemplo, los uno o más compuestos y uno o más agentes activos adicionales opcionales pueden formularse en nanopartículas, micropartículas y combinaciones de las mismas, y pueden encapsularse en una cápsula de gelatina blanda o dura o no de gelatina, o pueden dispersarse en un medio de dispersión para formar una suspensión oral o jarabe. Las partículas pueden estar formadas por el agente activo y un polímero o matriz de liberación controlada. Como alternativa, las partículas de agente activo pueden recubrirse con uno o más recubrimientos de liberación controlada antes de su incorporación en la forma farmacéutica acabada.
En otra realización, los uno o más compuestos y uno o más agentes activos adicionales opcionales se dispersan en un material de la matriz, que se gelifica o emulsiona tras el contacto con un medio acuoso, tal como los fluidos fisiológicos. En el caso de los geles, la matriz se hincha atrapando los agentes activos, que se liberan lentamente con el tiempo por difusión y/o degradación del material de la matriz. Dichas matrices pueden formularse en forma de comprimidos o en forma de materiales de relleno para cápsulas duras y blandas.
En otra realización más, los uno o más compuestos y uno o más agentes activos adicionales opcionales se formulan en una forma farmacéutica oral sólida, tal como un comprimido o una cápsula, y la forma farmacéutica sólida se recubre con uno o más recubrimientos de liberación controlada, tales como recubrimientos de liberación retardada o recubrimientos de liberación prolongada. El recubrimiento o los recubrimientos también pueden contener los compuestos y/o agentes activos adicionales.
(1) Formas farmacéuticas de liberación prolongada
Las formulaciones de liberación prolongada se preparan generalmente en forma de sistemas de difusión u osmóticos, que se conocen en la técnica. Un sistema de difusión normalmente consiste en dos tipos de dispositivos, un depósito y una matriz, y es bien conocido y se ha descrito en la técnica. Los dispositivos matriciales generalmente se preparan comprimiendo el fármaco con un vehículo polimérico de disolución lenta en forma de comprimido. Los tres principales tipos de materiales utilizados en la preparación de dispositivos matriciales son plásticos insolubles, polímeros hidrófilos y compuestos grasos. Las matrices de plástico incluyen, pero sin limitación, acrilato de metilo, metacrilato de metilo, cloruro de polivinilo y polietileno. Los polímeros hidrófilos incluyen, pero sin limitación, polímeros celulósicos tales como metil y etilcelulosa, hidroxialquilcelulosas tales como hidroxipropilcelulosa, hidroxipropilmetilcelulosa, carboximetilcelulosa de sodio y CARBOPOL® 934 (polímero de poliacrilato reticulado), óxidos de polietileno y mezclas de los mismos. Los compuestos grasos incluyen, pero sin limitación, diversas ceras, tales como cera de carnauba y triestearato de glicerilo y sustancias de tipo ceroso, incluyendo aceite de ricino hidrogenado o aceite vegetal hidrogenado, o mezclas de los mismos.
En determinadas realizaciones preferidas, el material plástico es un polímero acrílico farmacéuticamente aceptable, incluyendo, pero sin limitación, copolímeros de ácido acrílico y ácido metacrílico, metacrilato de metilo, copolímeros de metacrilato de metilo, metacrilatos de etoxietilo, metacrilato de cianoetilo, copolímero de metacrilato de aminoalquilo, poli(ácido acrílico), poli(ácido metacrílico), copolímero de ácido metacrílico y alquilamina, poli(metacrilato de metilo), poli(ácido metacrílico)(anhídrido), polimetacrilato, poliacrilamida, poli(anhídrido de ácido metacrílico) y copolímeros de metacrilato de glicidilo.
En determinadas realizaciones preferidas, el polímero acrílico se compone de uno o más copolímeros de metacrilato de amonio. Los copolímeros de metacrilato de amonio son bien conocidos en la técnica y se describen en el FN XVII como copolímeros totalmente polimerizados de ésteres de ácido acrílico y metacrílico con un contenido bajo de grupos amonio cuaternario.
En una realización preferida, el polímero acrílico es una laca de resina acrílica tal como la que está disponible en el mercado en Rohm Pharma con el nombre comercial EUDRAGIT®. En realizaciones preferidas adicionales, el polímero acrílico comprende una mezcla de dos lacas de resina acrílica disponibles en el mercado en Rohm Pharma con los nombres comerciales EUDRAGIT® RL30D y EUDRAGIT ® RS30D, respectivamente. EUDRAGIT® RL30D y EUDRAGIT ® RS30D son copolímeros de ésteres acrílicos y metacrílicos con un contenido bajo de grupos amonio cuaternario, la relación molar de los grupos amonio con respecto a los ésteres (met)acrílicos neutros restantes es de 1:20 en EUDRAGIT ® RL30D y de 1:40 en EUDRAGIT® RS30D. El peso molecular promedio es de aproximadamente 150.000. También se prefieren EUDRAGIT ® S-100 y EUDRAGIT ® L-100. Las designaciones de código RL (alta permeabilidad) y RS (baja permeabilidad) se refieren a las propiedades de permeabilidad de estos agentes. Las mezclas EUDRAGIT ® RL/RS son insolubles en agua y en fluidos digestivos. Sin embargo, los sistemas de partículas múltiples formados para incluir las mismas son hinchables y permeables en soluciones acuosas y fluidos digestivos.
Los polímeros descritos anteriormente, tales como EUDRAGIT ® RL/RS, pueden mezclarse entre sí en cualquier relación deseada con el fin de obtener en última instancia una formulación de liberación sostenida que tenga un perfil
de disolución deseable. Pueden obtenerse sistemas de partículas múltiples de liberación sostenida deseables, por ejemplo, a partir de EUDRAGIT® RL al 100 %, EUDRAGIT® RL al 50 % y EUDRAGIT ® RS al 50 %, y EUDRAGIT® RL al 10% y EUDRAGIT® RS al 90%. Un experto en la materia reconocerá que también pueden usarse otros polímeros acrílicos, tales como, por ejemplo, EUDRAGIT® L.
Como alternativa, pueden prepararse formulaciones de liberación prolongada usando sistemas osmóticos o aplicando un recubrimiento semipermeable a la forma farmacéutica. En este último caso, el perfil de liberación del fármaco deseado puede conseguirse combinando materiales de recubrimiento poco permeables y altamente permeables en una proporción adecuada.
Los dispositivos con diferentes mecanismos de liberación de fármacos descritos anteriormente pueden combinarse en una forma farmacéutica final que comprenda unidades individuales o múltiples. Los ejemplos de unidades múltiples incluyen, pero sin limitación, comprimidos de capas múltiples y cápsulas que contienen comprimidos, perlas o gránulos. Puede añadirse una porción de liberación inmediata al sistema de liberación prolongada ya sea por medio de la aplicación de una capa de liberación inmediata encima del núcleo de liberación prolongada usando un proceso de recubrimiento o compresión, o en un sistema de unidades múltiples, tal como una cápsula que contenga perlas de liberación prolongada e inmediata.
Los comprimidos de liberación prolongada que contienen polímeros hidrófilos se preparan mediante técnicas habitualmente conocidas en la técnica, tales como compresión directa, granulación en húmedo o granulación en seco. Sus formulaciones por lo general incorporan polímeros, diluyentes, aglutinantes y lubricantes, así como el principio activo farmacéutico. Los diluyentes habituales incluyen sustancias inertes en polvo, tales como almidones, celulosa en polvo, especialmente celulosa cristalina y microcristalina, azúcares tales como fructosa, manitol y sacarosa, harinas de grano y polvos comestibles similares. Los diluyentes típicos incluyen, por ejemplo, diversos tipos de almidón, lactosa, manitol, caolín, fosfato o sulfato de calcio, sales inorgánicas tales como cloruro de sodio y azúcar en polvo. También son útiles los derivados de celulosa en polvo. Los aglutinantes de comprimidos típicos incluyen sustancias tales como almidón, gelatina y azúcares tales como lactosa, fructosa y glucosa. También pueden usarse gomas naturales y sintéticas, incluyendo goma arábiga, alginatos, metilcelulosa y polivinilpirrolidona. También pueden servir como aglutinantes polietilenglicol, polímeros hidrófilos, etilcelulosa y ceras. Un lubricante es necesario en una formulación de comprimido para impedir que el comprimido y los punzones se peguen en la matriz. El lubricante se elige entre sólidos resbaladizos tales como talco, estearato de magnesio y de calcio, ácido esteárico y aceites vegetales hidrogenados.
Se preparan comprimidos de liberación prolongada que contienen materiales cerosos generalmente usando métodos conocidos en la técnica, tales como el método de mezcla directa, un método de congelación y un método de dispersión acuosa. En el método de congelación, el fármaco se mezcla con un material ceroso y se pulveriza o se congela y se tamiza y procesa.
(2) Formas farmacéuticas de liberación retardada
Pueden crearse formulaciones de liberación retardada recubriendo una forma farmacéutica sólida con una película polimérica, que es insoluble en el medio ácido del estómago y soluble en el medio neutro del intestino delgado.
Las unidades de dosificación de liberación retardada pueden prepararse, por ejemplo, mediante el recubrimiento de un agente activo o de una composición que contiene un agente activo con un material de recubrimiento seleccionado. La composición que contiene el agente activo puede ser, por ejemplo, un comprimido para su incorporación en una cápsula, un comprimido para su uso como núcleo interno en una forma farmacéutica de "núcleo recubierto", o una pluralidad de perlas partículas o gránulos que contienen agente activo, para su incorporación en un comprimido o cápsula. Los materiales de recubrimiento preferidos incluyen polímeros bioerosionables, hidrolizables gradualmente, hidrosolubles gradualmente y/o degradables enzimáticamente y pueden ser polímeros "entéricos" convencionales. Los polímeros entéricos, como apreciarán los expertos en la materia, se vuelven solubles en el entorno de pH mayor del tracto gastrointestinal inferior o se erosionan lentamente a medida que la forma farmacéutica pasa a través del tracto gastrointestinal, mientras que los polímeros degradables enzimáticamente son degradados por las enzimas bacterianas presentes en el tracto gastrointestinal inferior, particularmente, en el colon. Los materiales de recubrimiento adecuados para efectuar la liberación retardada incluyen, pero sin limitación, polímeros celulósicos tales como hidroxipropilcelulosa, hidroxietilcelulosa, hidroximetilcelulosa, hidroxipropilmetilcelulosa, succinato de acetato de hidroxipropilmetilcelulosa, ftalato de hidroxipropilmetilcelulosa, metilcelulosa, etilcelulosa, acetato de celulosa, ftalato de acetato de celulosa, trimelitato de acetato de celulosa y carboximetilcelulosa de sodio; polímeros y copolímeros de ácido acrílico, preferentemente formados a partir de ácido acrílico, ácido metacrílico, acrilato de metilo, acrilato de etilo, metacrilato de metilo y/o metacrilato de etilo, y otras resinas metacrílicas que están disponibles en el mercado con el nombre comercial EUDRAGIT® (Rohm Pharma; Westerstadt, Alemania), incluyendo EUDRAGIT® L30D-55 y L100-55 (soluble a pH 5,5 y superior), EUDRAGIT® L-100 (soluble a pH 6,0 y superior), EUDRAGIT® S (soluble a pH 7,0 y superior, como resultado de un mayor grado de esterificación) y EUDRAGITs® NE, RL y RS (polímeros insolubles en agua que tienen diferentes grados de permeabilidad y expansibilidad); polímeros y copolímeros de vinilo tales como polivinilpirrolidona, acetato de vinilo, ftalato de acetato de vinilo, copolímero de acetato de vinilo-ácido crotónico y copolímero de etileno-acetato de vinilo; polímeros degradables enzimáticamente tales como polímeros azoicos,
pectina, quitosano, amilosa y goma guar; zeína y goma laca. También pueden usarse combinaciones de diferentes materiales de recubrimiento. También pueden aplicarse recubrimientos multicapa usando polímeros diferentes.
Los pesos de recubrimiento preferidos para materiales de recubrimiento particulares pueden ser determinados fácilmente por los expertos en la materia mediante la evaluación de los perfiles de liberación individuales para comprimidos, perlas y gránulos preparados con diferentes cantidades de diversos materiales de recubrimiento. Es la combinación de materiales, método y forma de aplicación que produce las características de liberación deseadas, que solo pueden determinarse a partir de los estudios clínicos.
La composición de recubrimiento puede incluir aditivos convencionales, tales como plastificantes, pigmentos, colorantes, agentes estabilizantes, sustancias de deslizamiento, etc. Un plastificante está normalmente presente para reducir la fragilidad del recubrimiento y generalmente representará aproximadamente del 3 % en peso al 50 % en peso" o del 10 % en peso al 50 % en peso, con respecto al peso seco del polímero. Los ejemplos de plastificantes normales incluyen polietilenglicol, propilenglicol, triacetina, ftalato de dimetilo, ftalato de dietilo, ftalato de dibutilo, sebacato de dibutilo, citrato de trietilo, citrato de tributilo, citrato de trietil acetilo, aceite de ricino y monoglicéridos acetilados. Se usa preferentemente un agente estabilizante para estabilizar las partículas en la dispersión. Son agentes estabilizantes típicos los emulsionantes no iónicos, tales como los ésteres de sorbitano, polisorbatos y polivinilpirrolidona. Se recomiendan sustancias de deslizamiento para reducir los efectos de adherencia durante la formación y el secado de la película y generalmente representarán del 25 % en peso al 100 % en peso del peso del polímero en la solución de recubrimiento. Una sustancia de deslizamiento eficaz es el talco. También pueden usarse otras sustancias de deslizamiento tales como el estearato de magnesio y los monoestearatos de glicerol. También pueden usarse pigmentos tales como el dióxido de titanio. También pueden añadirse cantidades pequeñas de un agente antiespumante, tal como una silicona (por ejemplo, simeticona), a la composición de recubrimiento.
3. Formulaciones tópicas
La presente solicitud desvela que pueden formularse compuestos como se definen en la sección III para la administración tópica.
4. Formulaciones desinfectantes y limpiadoras
La presente solicitud desvela que pueden formularse compuestos anteriores en formulaciones de limpieza.
D. Conjugación de compuestos
El uno o más compuestos pueden presentarse como compuestos conjugados. Los compuestos pueden conjugarse con otros agentes con el fin de retener los compuestos sobre las superficies, por ejemplo, para impedir la formación de biopelículas sobre una superficie. En una realización, los compuestos pueden conjugarse con un agente que tenga afinidad por una superficie con el fin de conservar los compuestos sobre dicha superficie. Por ejemplo, los compuestos pueden conjugarse con un agente en donde el agente es un polímero u oligómero, y el polímero u oligómero tiene una afinidad alta por la superficie.
En otra realización, los compuestos pueden conjugarse con un agente en donde el agente comprende un resto reactivo adecuado para el anclaje a una superficie. El resto reactivo puede ser, por ejemplo, fotorreactivo, o capaz de acoplarse covalentemente a una superficie. El resto reactivo también puede incorporar espaciadores y enlazadores y otros grupos funcionales con el fin de colocar el compuesto en una ubicación deseada con respecto a la superficie. A continuación se muestran ejemplos de cómo el compuesto puede conjugarse con un agente que comprende un resto reactivo adecuado para el anclaje a una superficie.
En los ejemplos de referencia, se conjuga FeQ con un marco de calix[4] areno que comprende un resto reactivo. En un primer ejemplo, se conjuga FeQ a través de un enlazador con un marco de calix[4] areno que contiene un grupo funcional fotorreactivo. Un segundo ejemplo muestra que el resto reactivo puede colocarse en una ubicación diferente en el marco de calix[4] areno. Un tercer ejemplo muestra FeQ conjugado con un marco de calix[4] areno, en donde este último está funcionalizado con grupos tiol que son capaces de reaccionar con superficies. Debe comprenderse que pueden usarse diferentes enlazadores o ningún enlazador y que pueden usarse otros agentes en lugar del marco de calix[4] areno, incluyendo ciclodextrinas y otros polímeros y oligómeros.
En otra realización más, los compuestos pueden conjugarse con un agente que comprende una sustancia con una afinidad por una superficie. El agente puede incorporar espaciadores y enlazadores y otros grupos funcionales con el fin de colocar el compuesto en la ubicación deseada con respecto a la superficie. En una realización, el agente contiene hidroxiapatita.
A continuación se muestran ejemplos de cómo los compuestos pueden conjugarse a través de un enlazador con la hidroxiapatita. En el ejemplo de referencia, los enlazadores se unen en diferentes posiciones a uno de los ligandos de ácido quínico a través de un grupo funcional, Y', y en el otro extremo del enlazador se unen a la hidroxiapatita (HA) a través de un segundo grupo funcional, X'. En una realización alternativa, el grupo HA puede reemplazarse por un
grupo reactivo que puede unirse (o estar unido) a una superficie, tal como un compuesto fotorreactivo, isocianato, un grupo hidroxi, amina, trialcoxisilil éter, tal como un trietoxisilil éter o un éster de fosfato. Estos grupos pueden estar unidos directamente al polietilenglicol o puede haber un enlazador adicional insertado entre el grupo reactivo y el polietilenglicol.
E. Piensos y suplementos de piensos
Los compuestos pueden formularse en formulaciones que promueven el crecimiento, por ejemplo, en un pienso o fórmula para animales para mejorar el crecimiento del animal. Los uno o más compuestos pueden añadirse al agua potable para cualquiera de los animales para mejorar el crecimiento.
Además de los métodos y usos reivindicados como se definen por las reivindicaciones 1 y 2, la presente solicitud también desvela que los compuestos pueden ser útiles en el tratamiento de estanques, tanques u otros entornos acuáticos o marinos que contengan peces (incluye peces de agua dulce y salada, peces de piscifactoría y peces ornamentales), otros animales marinos y acuáticos, incluyendo mariscos o crustáceos tales como gambas, ostras, mejillones, almejas, langostinos, langostas, cangrejos de río, cangrejos, sepia, pulpo y cigalas.
El uno o más compuestos pueden usarse solos o en combinación con otros compuestos antimicrobianos, bactericidas o bacteriostáticos y/o agentes potenciadores del crecimiento.
Los compuestos pueden mejorar el rendimiento de crecimiento y pueden usarse para aumentar el peso corporal promedio durante el crecimiento. Los compuestos también pueden usarse para mejorar el índice de conversión de pienso. En particular, los compuestos pueden usarse para disminuir los índices de conversión de pienso ajustados a la mortalidad (ICPM). Los compuestos pueden usarse para producir animales con un peso corporal promedio mayor en un período de tiempo dado, o pueden usarse para alcanzar un peso corporal promedio objetivo en un período de tiempo más corto. Los compuestos pueden usarse para disminuir la cantidad de pienso necesaria para que un animal alcance un peso objetivo. Además, los compuestos pueden usarse en entornos de estrés para mejorar el crecimiento y el ICPM. Estos entornos incluyen, pero sin limitación, densidades altas de población de animales, cama de corral sucia, presencia de patógenos, presencia de Campylobacter y otras bacterias y entornos de temperaturas altas. Las composiciones son particularmente útiles en piensos para aves comerciales tales como pollos, pavos, faisanes y patos. Los piensos para aves de corral de ejemplo en los que pueden incluirse los compuestos, incluyen piensos para aves de corral que se denominan piensos "completos", porque están diseñados para contener toda la proteína, la energía, las vitaminas, los minerales y otros nutrientes necesarios para un crecimiento adecuado, para la producción de huevos y para la salud de las aves. La alimentación con cualquier otro ingrediente, mezclado con el pienso o proporcionado por separado, altera el equilibrio de nutrientes en el pienso "completo". No se recomienda alimentar con granos o suplementos adicionales con el pienso completo para aves de corral.
F. Tratamiento para promover el crecimiento
Como se ha analizado anteriormente con más detalle, se ha descubierto que el uno o más compuestos de la presente solicitud, anteriores, son particularmente útiles para promover el crecimiento.
Sin embargo, se apreciará que el alcance de la protección está definido por las reivindicaciones adjuntas. En el contexto de la promoción del crecimiento, esto se refiere, en particular, a un método no terapéutico de potenciación del crecimiento de un animal usando uno o más compuestos de complejo de Fe III de Fórmula I, como se define adicionalmente por la reivindicación 1, y a un uso no terapéutico, como se define adicionalmente por la reivindicación 2, de los compuestos de complejo de Fe III de la reivindicación 1 y las reivindicaciones dependientes de las mismas. Los compuestos pueden añadirse a piensos para animales o agua potable para animales con el fin de favorecer el crecimiento. La adición de los compuestos a piensos o a agua potable da como resultado un crecimiento mejorado. También se ha descubierto que los compuestos pueden añadirse a piensos o agua potable para animales con el fin de disminuir el índice de conversión de pienso ajustado a la mortalidad. Por lo tanto, es posible usar los compuestos para disminuir la cantidad de pienso necesaria para que un animal crezca. Los compuestos pueden administrarse adicionalmente con otros aditivos para animales y pueden administrarse en piensos comerciales. En una realización preferida, los compuestos se administran en piensos.
También se ha descubierto que los compuestos pueden administrarse a animales que están en un entorno de estrés con el fin de mejorar su rendimiento de crecimiento. En un entorno de estrés, los compuestos promueven el crecimiento que produce animales con pesos corporales promedio mayores. Los compuestos también disminuyen los índices de conversión de pienso ajustados a la mortalidad en entornos de estrés.
Ejemplos
Ejemplo Comparativo 1. Eficacia de FeQ y FeTyr para reducir el porte de Campylobacter y promover su crecimiento en pollos
Materiales y métodos
Se realizó un estudio para evaluar la promoción del crecimiento y la reducción del porte de Campylobacter usando FeQ y FeTyr en pollos de engorde Ross 308 machos con 7 grupos de tratamiento. Cada grupo de tratamiento comprendía cuatro réplicas de 10 aves por corral (40 aves/grupo de tratamiento y 4 corrales de 10 aves/grupo de tratamiento), con 2 grupos de control y 5 grupos de ensayo. Todos los grupos de ensayo y uno de los grupos de control se expusieron el día 20 del ensayo a una cama sucia, que dio positivo en Campylobacter. Este método se usó para proporcionar un método más natural para exponer a las aves a Campylobacter. Por lo tanto, había un control positivo en el que un grupo de tratamiento se expuso a Campylobacter y un grupo de control negativo en el que las aves no se expusieron, y cinco grupos de tratamiento que se expusieron todos a Campylobacter. El número total de aves utilizadas en los 7 grupos de tratamiento fue de 280. Los detalles de los tratamientos se proporcionan en la Tabla 1. El grupo de tratamiento 1 era un control negativo en el que las aves solo recibieron el pienso comercial y no se expusieron a una cama sucia que contenía Campylobacter. El grupo de tratamiento 2 era el control positivo en el que las aves recibieron el pienso comercial y se expusieron a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 3 recibió 0,22 g/l de FeQ en su agua potable y 0,22 g/kg de FeQ en su pienso durante todo el ensayo, y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 5 recibió 0,22 g/l de FeQ en su agua potable durante todo el ensayo, y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 6 recibió 0,22 g/kg de FeQ en su pienso durante todo el ensayo, y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 7 recibió 0,022 g/l de FeQ en su agua potable durante todo el ensayo, y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 8 recibió 0,02 g/l de FeTyr en su agua potable durante todo el ensayo, y se expuso a una cama sucia que contenía Campylobacter el día 20. El FeTyr se predisolvió en DMSO y se diluyó para proporcionar una solución de 0,02 g/l de FeTyr en agua. (Un grupo de tratamiento adicional 4 se retiró debido a problemas de solubilidad).
Tabla 1: Detalles del tratamiento
Se alimentó a las aves con un programa comercial de alimentación en tres fases, usando piensos de inicio, de crecimiento y de finalización con formulaciones que se muestran en la Tabla 2. Todas las dietas tenían coccidiostat (MAXIBAN® al 0,0625 % en dietas de fase de inicio y de finalización y MONTEBAN® al 0,06 % en la fase de finalización). A todas las dietas se les añadieron xilanasa (RONOZYMe® WX a 200 g por tonelada) y fitasa (RONOZy Me® P a 150 gramos por tonelada).
Tabla 2: Formulación basal del pienso para dietas de inicio, de crecimiento y de finalización Materia prima DIETA DE DIETA DE DIETA DE
INICIO % CRECIMIENTO % FINALIZACIÓN % Cebada 10,5 8,4 7,2
Trigo 50,0 55,0 60,0
Soja Ext Hipro 26,0 23,0 19,0
Soja de grasa entera Cherwell 5,0 5,0 5,0
HCl de L Lisina 0,40 0,30 0,30
DL-metionina 0,40 0,35 0,30
L-treonina 0,15 0,15 0,15
Aceite de soja 4,0 4,50 4,75
Piedra caliza 1,25 1,25 1,25
Fosfato MonoCal 1,50 1,25 1,25
Sal 0,25 0,25 0,25 Bicarbonato de sodio 0,15 0,15 0,15 Premezcla para pollos de engorde 0,40 0,40 0,40
(continuación)
Nutriente Análisis Análisis Análisis
Grasa (extracto de éter) 6,34 6,85 7,11
Proteína 21,85 20,64 19,14
Fibra 3,08 3,02 2,97
Ceniza 6,01 5,68 5,50
ME-P 12,78 13,04 13,22
Lisina total 1,45 1,28 1,17
Lisina disponible 1,35 1,19 1,09
Metionina 0,69 0,62 0,55
Metionina y cisteína totales 1,03 0,95 0,85
Treonina 0,91 0,86 0,79
Triptófano 0,25 0,23 0,21
Calcio 0,95 0,91 0,89
Fósforo 0,72 0,66 0,65
Fósforo disponible 0,48 0,42 0,42
Sal 0,30 0,30 0,30
Sodio 0,17 0,17 0,17
VitA 13,20 13,5 13,50
Vit D3 5,0 5,0 5,00
Vit E 100 100 100
El programa de alimentación se muestra en la Tabla 3. Las aves se criaron en corrales de suelo hasta el día 42 y se alimentaron con pienso de inicio, de crecimiento y de finalización los días 0 a 11, 11 a 24 y 24 a 42 días, respectivamente. Todas las aves se pesaron individualmente y se registraron las pesadas de pienso por corral los días 0, 11,21, 24 y 42.
Antes de exponer a los pollos con una cama sucia que contenía Campylobacter el día 20, cada corral se sometió a ensayo para Campylobacter usando hisopos cloacales. Todos los corrales dieron negativo para Campylobacter antes de la exposición. El día 20, la cama, que estaba naturalmente contaminada con Campylobacter, se sometió a ensayo para confirmar la presencia de Campylobacter y después se añadió (aproximadamente 2 kg/corral) a la cama en todos los corrales, excepto en los corrales para el grupo de tratamiento 1 (el control negativo). El día 28, se muestreó la cama del corral para confirmar la presencia o ausencia de Campylobacter. Los días 41 y 42, se tomaron muestras cecales de 3 aves por corral (12 aves por grupo de tratamiento) y se sometieron a ensayo para enumerar el Campylobacter. El día 42, se tomaron contenido digestivo, muestras fecales y contenido cecal de todas las aves y se agruparon por corral. También se tomaron dos aves por corral de los grupos de tratamiento 1-3, se sacrificaron y se tomaron muestras de sangre. Las muestras se analizaron para determinar la química sanguínea, incluyendo el análisis para determinar fosfatasa alcalina, aspartato aminotransferasa, alanina aminotransferasa, gamma-glutamil transferasa, lactato deshidrogenasa, proteína total, albúmina, globulina, amilasa y glucosa.
Con el fin de minimizar el riesgo de contaminación cruzada, se usaron medidas de bioseguridad convencionales de la industria, incluyendo: desinfección de botas, cambio de cubrecalzado y guantes entre corrales/tratamientos, entrar en los corrales negativos para Campylobacter antes de entrar en los corrales positivos para Campylobacter y dejar los corrales adyacentes vacíos. Se registraron la salud diaria, el sacrificio selectivo y la mortalidad. Todos los pesos de las aves se registraron a los 0, 11, 21, 24, 33 y 42 días. Se derivaron el aumento de peso, la ingesta de pienso y el índice de conversión de pienso (ICP) para cada período de alimentación.
Resultados
Las Tablas 4-13 muestran los efectos sobre los grupos de tratamiento en comparación con el grupo de control negativo (grupo de tratamiento 1) y el grupo de control positivo (grupo de tratamiento 2) para los períodos de 0-11 días, 11-20 días, 20-25 días, 11-25 días, 25-42 días, 20-42 días, 0-20 días y 0-42 días.
La Figura 1 muestra el peso corporal promedio en el día 42 para todos los grupos de tratamiento y una comparación con un control comercial etiquetado como "Objetivo". La figura muestra que el grupo de tratamiento 1 (el control negativo etiquetado como "CNC") alcanzó un peso corporal promedio (PCP) de 3,437 kg el día 42 (que era superior al del objetivo comercial de 2,979 kg). El control positivo (etiquetado como "CC"), que se expuso a una cama sucia que contenía Campylobacter el día 20, por el contrario, solo alcanzó un PCP de 3,186 kg el día 42, que era significativamente inferior al del control negativo (grupo de tratamiento 1). Este resultado demuestra que la exposición a una cama sucia contaminada con Campylobacter dio como resultado una reducción del crecimiento del pollo en un
promedio de 251 gramos. Sin embargo, cuando los pollos se expusieron a una cama sucia que contenía Campylobacter pero se trataron con FeQ o FeTyr en los grupos de tratamiento 3, 5, 6, 7 y 8, todos tratamiento obtuvieron mejores resultados que el control positivo, lo que demuestra que el tratamiento con FeQ y FeTyr tuvo un efecto positivo sobre el crecimiento. De hecho, la presencia de FeQ en el pienso a 0,22 g/kg (grupo de tratamiento 6) produjo pollos con un PCP de 3,464 kg, que era superior al del control negativo de 3,437 kg, a pesar de que el grupo de tratamiento 6 se había expuesto a cama sucia que contenía Campylobacter.
La Figura 2 muestra el índice de conversión de pienso ajustado a la mortalidad (ICPM) el día 42 para todos los grupos de tratamiento y una comparación con un control comercial etiquetado como "Objetivo". (Un número de ICPM inferior es un resultado mejor). La figura muestra que el grupo de tratamiento 1 (el control negativo etiquetado como "CNC") tuvo un ICPM de 1,563, que era inferior al del objetivo comercial de 1,703. El control positivo, etiquetado como "CC" que se expuso a la cama sucia que contenía Campylobacter el día 20 tuvo un ICPM de 1,679 significativamente superior al del control negativo. Por tanto, la exposición a una cama sucia infectada con Campylobacter dio como resultado un ICPM superior. Sin embargo, cuando los pollos se expusieron a una cama sucia infectada con Campylobacter pero se trataron con FeQ o FeTyr en los grupos de tratamiento 3, 5, 6, 7 y 8, todos tratamiento obtuvieron mejores resultados que el control positivo, lo que demuestra que el tratamiento con FeQ y FeTyr tuvo un efecto positivo sobre el ICPM (es decir, disminuyó el ICPM numérico). Los resultados muestran que los grupos de tratamiento 3, 5, 6, 7 y 8 tuvieron valores de ICPM de 1,595, 1,560, 1,563, 1,612 y 1,577, respectivamente. Además, los grupos de tratamiento 5 y 6 obtuvieron resultados tan buenos como los del control negativo incluso cuando se expusieron a cama sucia que contenía Campylobacter.
La Figura 3 muestra el número de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de excrementos de ave en el día 42 para los grupos de tratamiento 1-3 y 6-8. (Un número inferior es un mejor resultado).
Los resultados muestran que los grupos de tratamiento 3 y 6-8 obtuvieron mejores resultados que el control positivo (grupo de tratamiento 2), lo que demuestra que FeQ y FeTyr tuvieron un efecto positivo sobre la reducción de la infección por Campylobacter de las aves de corral. En concreto, los pollos tratados con FeTyr, FeQ en pienso y FeQ en pienso y agua tuvieron todos unidades formadoras de colonias de Campylobacter por gramo de excremento que eran similares o inferiores, a aquellas del grupo de control negativo (grupo de tratamiento 1). La detección de niveles bajos de Campylobacter en los controles negativos demuestra lo altamente contagiosa que es la bacteria y es probable que sea una indicación de que un número pequeño de aves en el grupo de control negativo se infectó a pesar de no haberse expuesto experimentalmente a cama sucia. Los resultados de la Fig. 3 para la concentración baja de FeQ en agua (0,022 g/l; grupo de tratamiento 7) parece mostrar menos efecto que los otros grupos de tratamiento, aunque se consideró más probable que esta diferencia se debiera a un error experimental, por ejemplo, después de la contaminación cruzada de las muestras.
Los resultados de la Fig. 4 confirman que el grupo de tratamiento 7 también tuvo un efecto altamente beneficioso. La Figura 4 muestra el número promedio de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de muestras de ciego en el día 42 para los grupos de tratamiento 1-3 y 5-8. Los resultados muestran que todos los grupos de tratamiento (3 y 5-8 obtuvieron mejores resultados que el control positivo (grupo de tratamiento 2), lo que demuestra que FeQ y FeTyr tuvieron un efecto positivo sobre la reducción de la infección por Campylobacter de las aves de corral.
El efecto de los tratamientos sobre la viabilidad global y el factor europeo de producción y eficiencia (FEPE) se muestra en la Tabla 12. (FEPE = [(Viabilidad x Peso vivo en kg al final del ensayo / Edad en días x ICP comercial) x 100].
El efecto del tratamiento con FeQ sobre el rendimiento de crecimiento en ausencia de exposición a Campylobacter durante la fase de inicio (0-11 días) y el período de 0-20 días se muestra en la Tabla 13. Puesto que los controles negativos y positivos (grupos de tratamiento 1 y 2) son idénticos antes de la exposición a la cama sucia el día 20, estos grupos pueden agruparse para compararlos con los grupos de tratamiento 3, 5, 6 y 7, con el fin de observar si FeQ tuvo un efecto sobre el crecimiento en ausencia de una exposición a cama sucia contaminada con Campylobacter durante los primeros 20 días de crecimiento. Los resultados demuestran que FeQ promueve el crecimiento de los pollos incluso en ausencia de exposición a una cama sucia contaminada con Campylobacter. El día 20, el peso corporal promedio (PCP) para los grupos de control (grupos de tratamiento 1 y 2) es de 0,927 kg frente a 0,963 kg para los grupos de tratamiento 3, 5, 6 y 7 que recibieron todos FeQ. Esta mejora en el peso corporal también se refleja en un ICPM significativamente mejor para las aves tratadas con FeQ. La Tabla 13 muestra que el ICPM para las aves tratadas en los grupos 3, 5, 6 y 7 es de 1,2996 frente a 1,3374 para los grupos de control (grupos de tratamiento 1 y
2). En concreto, el valor P es inferior a 0,05.
El mismo efecto positivo del tratamiento con FeTyr sobre el rendimiento de crecimiento en ausencia de exposición a Campylobacter es también evidente a partir de la Tabla 10. El APP durante los primeros 20 días de producción para pollos tratados con FeTyr (grupo de tratamiento 8) es de 0,895 kg en comparación con 0,884 y 0,889 kg para los grupos de tratamiento 1 y 2 (controles negativo y positivo). Además, el ICPM durante los primeros 20 días de producción para pollos tratados con FeTyr (grupo de tratamiento 8) es de 1,311 frente a 1,32 y 1,355 para los grupos de tratamiento 1 y 2, respectivamente. (Un valor de ICPM menor es una mejora).
Los resultados de este estudio demuestran que tanto FeQ como FeTyr promueven el crecimiento y disminuyen el
índice de conversión de pienso ajustado a la mortalidad (ICPM) en ausencia o presencia de cama sucia contaminada con Campylobacter.
Tabla 4. Efecto de los tratamientos sobre el rendimiento de crecimiento durante la fase de inicio (día 0-11) Tratamiento PCP IPP APP ICPM
Día 0 Día 11 Día 0-11
1 0,040 0,331 0,348 0,291 1,239b 2 0,040 0,337 0,359 0,297 1,228b 3 0,040 0,346 0,356 0,306 1,181ab 5 0,040 0,334 0,352 0,294 1,210ab 6 0,041 0,351 0,360 0,310 1,168a 7 0,040 0,325 0,348 0,285 1,236b 8 0,040 0,329 0,353 0,289 1,229b Valor P 0,136 0,418 0,979 0,463 0,005
ETD 0,000 0,013 0,016 0,013 0,018
Valor P para la
comparación
1 frente a 2 0,512 0,667 0,519 0,682 0,584
1 frente a 2 a 8 0,666 0,573 0,603 0,583 0,045 2 frente a 3567 0,632 0,844 0,723 0,834 0,054 5 frente a 6 0,099 0,213 0,627 0,233 0,033 5 frente a 7 0,141 0,466 0,804 0,494 0,170
2 frente a 8 0,645 0,538 0,709 0,549 0,982 a-b dentro de una columna refleja las diferencias entre tratamientos cuando P< 0,05; ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = índice de conversión de pienso ajustado a la mortalidad; ICP = Índice de conversión de pienso - comercial.________________________________________________________________
Tabla 5. Efecto de los tratamientos sobre el rendimiento de crecimiento global durante la fase de crecimiento ___________________________________________ (día 11-20)_____________________________________________ Tratamiento PCP IPP APP ICPM
Día 20 Día 11-20
1 0,924 0,799 0,593 1,362 2 0,929 0,838 0,592 1,421 3 0,972 0,857 0,625 1,375 5 0,943 0,821 0,609 1,348 6 0,991 0,841 0,640 1,343 7 0,947 0,829 0,622 1,333 8 0,935 0,809 0,606 1,351 Valor P 0,358 0,311 0,279 0,279
ETD 0,032 0,025 0,021 0,036
Valor P para la
comparación
1 frente a 2 0,875 0,133 0,977 0,115 1 frente a 2 a 8 0,248 0,094 0,175 0,987 2 frente a 3567 0,189 0,961 0,075 0,020 5 frente a 6 0,145 0,427 0,160 0,884 5 frente a 7 0,913 0,737 0,546 0,673 2 frente a 8 0,850 0,253 0,516 0,065
ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = ICP ajustado a la mortalidad; ICP = ICP comercial.
Tabla 6. Efecto de los tratamientos sobre el rendimiento de crecimiento durante el período de los días 20-25. Tratamiento PCP IPP APP ICPM
Día 25 Día 20-25
1 1,366 0,662 0,442 1,500
2 1,371 0,652 0,442 1,550
3 1,424 0,667 0,453 1,477
5 1,384 0,658 0,441 1,495
6 1,426 0,685 0,434 1,599
7 1,388 0,661 0,441 1,513
8 1,377 0,662 0,442 1,499
Valor P 0,723 0,916 0,999 0,882
ETD 0,044 0,026 0,030 0,096
Valor P para la
comparación
1 frente a 2 0,912 0,685 0,998 0,604
1 frente a 2 a 8 0,403 0,932 0,996 0,759
2 frente a 3567 0,339 0,444 0,990 0,707
5 frente a 6 0,361 0,311 0,826 0,294
5 frente a 7 0,930 0,902 0,988 0,854
2 frente a 8 0,892 0,693 0,999 0,604
ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = ICP ajustado a la mortalidad; ICP = ICP comercial.
Tabla 7. Efecto de los tratamientos sobre el rendimiento de crecimiento global durante la fase de crecimiento (día 11-25)
Tratamiento IPP APP ICPM
Día 11-25
1 1,462 1,035 1,421
2 1,490 1,034 1,457
3 1,524 1,078 1,417
5 1,479 1,050 1,409
6 1,526 1,075 1,440
7 1,490 1,064 1,406
8 1,471 1,048 1,414
Valor P 0,660 0,804 0,598
ETD 0,042 0,036 0,030
Valor P para la
comparación
1 frente a 2 0,516 0,984 0,241
1 frente a 2 a 8 0,293 0,406 0,891
2 frente a 3567 0,657 0,267 0,118
5 frente a 6 0,280 0,498 0,300
5 frente a 7 0,787 0,707 0,925
2 frente a 8 0,664 0,695 0,165
ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = ICP ajustado a la mortalidad.
Tabla 8. Efecto de los tratamientos sobre el rendimiento de crecimiento global durante la fase de finalización ___________________________________________ (día 25-42)___________________________________________ Tratamiento PCP IPP APP ICPM
Día 42 Día 25-42
1 3,437 3,479 2,070b 1,688
2 3,186 3,480 1,814a 1,889
3 3,342 3,387 1,918ab 1,773
5 3,407 3,357 2,023b 1,706
6 3,464 3,315 2,039b 1,704
7 3,304 3,362 1,916ab 1,793
8 3,341 3,434 1,964ab 1,716 Valor P 0,027 0,56 0,009 0,211
ETD 0,075 0,099 0,062 0,081
Valor P para la
comparación
1 frente a 2 0,004 0,997 <0,001 0,022
1 frente a 2 a 8 0,110 0,247 0,016 0,233
2 frente a 3567 0,004 0,129 0,004 0,035
5 frente a 6 0,455 0,680 0,800 0,988
5 frente a 7 0,187 0,960 0,101 0,294
2 frente a 8 0,053 0,649 0,027 0,046
a-b dentro de una columna refleja las diferencias entre tratamientos cuando P< 0,05; ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = ICP ajustado a la mortalidad; ICP = ICP comercial.
Tabla 9. Efecto de los tratamientos sobre el rendimiento de crecimiento durante el período experimental de ______________________ los días 20-42 (después de la exposición de las aves)________________________ Tratamiento IPP APP ICPM
Día 20-42
1 4,142 2,512b 1,653
2 4,131 2,256a 1,820
3 4,054 2,370ab 1,713
5 4,015 2,464ab 1,665
6 4,001 2,473ab 1,678
7 4,023 2,357ab 1,739
8 4,096 2,406ab 1,676 Valor P 0,767 0,025 0,344
ETD 0,110 0,068 0,075
Valor P para la
comparación
1 frente a 2 0,926 0,001 0,038 1 frente a 2 a 8 0,306 0,028 0,290
2 frente a 3567 0,229 0,008 0,055 5 frente a 6 0,898 0,894 0,856
5 frente a 7 0,941 0,138 0,331
2 frente a 8 0,752 0,042 0,070
a-b dentro de una columna refleja las diferencias entre tratamientos cuando P< 0,05; ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = Ajustado a la normalidad.
Tabla 10. Efecto global de los tratamientos sobre el rendimiento de crecimiento durante el período experimental de los días 0-20 (antes de la exposición de las aves).
Tratamiento IPP APP ICPM
Día 0-20
1 1,147 0,884 1,320
2 1,196 0,889 1,355
3 1,213 0,931 1,310
5 1,173 0,903 1,303
6 1,201 0,951 1,284
7 1,178 0,907 1,302
8 1,161 0,895 1,311
Valor P 0,623 0,368 0,225
ETD 0,038 0,032 0,025
Valor P para la comparación
1 frente a 2 0,215 0,881 0,181
1 frente a 2 a 8 0,191 0,251 0,627
2 frente a 3567 0,860 0,188 0,012
5 frente a 6 0,476 0,150 0,469
5 frente a 7 0,907 0,899 0,978
2 frente a 8 0,371 0,846 0,094 ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = Ajustado a la normalidad.
Tabla 11. Efecto global de los grupos de tratamiento sobre el rendimiento de crecimiento (días 0-42) Tratamiento IPP APP ICPM
Día 0-42
1 5,289 3,397b 1,563
2 5,328 3,145a 1,679
3 5,267 3,302ab 1,595
5 5,188 3,367ab 1,560
6 5,201 3,423b 1,563
7 5,201 3,265ab 1,612
8 5,258 3,301ab 1,577 Valor P 0,920 0,028 0,193
ETD 0,132 0,075 0,047
Valor P para la comparación
1 frente a 2 0,773 0,004 0,024 1 frente a 2 a 8 0,633 0,111 0,352
2 frente a 3567 0,29 0,004 0,018 5 frente a 6 0,920 0,461 0,954
5 frente a 7 0,924 0,190 0,284
2 frente a 8 0,601 0,053 0,043
a-b dentro de una columna refleja las diferencias entre tratamientos cuando P< 0,05; ETD = Errores típicos de la diferencia de las medias; PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = Ajustado a la normalidad.
Tabla 12. Efecto de los tratamientos sobre la viabilidad global y el factor europeo de producción y eficiencia
____________________________________________ (FEPE)____________________________________________
Tratamiento FEPE
Día 20 Día 42
1 318,3 282,8
2 334,7 250,7
3 350,4 262,9
5 352,0 278,3
6 364,8 265,0
7 354,5 276,2
8 336,4 296,0
Valor P 0,547 0,842
ETD 23,83 31,68
Valor P para la comparación
1 frente a 2 0,500 0,323
1 frente a 2 a 8 0,111 0,645
2 frente a 3567 0,285 0,437
5 frente a 6 0,599 0,680
5 frente a 7 0,919 0,949
2 frente a 8 0,945 0,170
Tabla 13. Efecto de los tratamientos sobre el rendimiento de crecimiento en ausencia de exposición a Campylobacter durante la fase de inicio (0-11 días) y el período de 0-20 días. Tratamiento PCP Día 11 PCP Día 20 IPP 0-20 días APP 0-20 días ICPM 0-20 Grupos 1 y 2 0,334 0,927 1,172 0,887 1,3374 FeQ (Grupos 3, 5, 6, 7) 0,339 0,963 1,191 0,923 1,2996 Valor P 0,584 0,079 0,432 0,078 0,029
ETD 0,009 0,020 0,024 0,020 0,016
PCP = peso corporal promedio (kg); IPP = ingesta de pienso promedio (kg); APP = aumento de peso promedio (kg); ICPM = índice de conversión de pienso ajustado a la mortalidad
Ejemplo de referencia 2 Fe-Lac Prevención de la formación de biopelícula por Pseudomonas aeruginosa.
Materiales y métodos
Se cultivó de forma rutinaria cepa PAO-1 de Pseudomonas aeruginosa en placas de agar LB (Luria-Bertani, Oxoid, Reino Unido) a 37 °C o en caldo a 37 °C con agitación a 200 rpm. Se incubaron portaobjetos de vidrio esterilizados por UV en 15 ml de medio definido RPMI-1640 (Sigma, Reino Unido) o en 15 ml de RPMI-1640 con Fe-Lac inoculado con bacterias diluidas (DO600 = 0,01) procedentes de cultivos de una noche a 37 °C con agitación a 60 rpm durante 72 horas. Los portaobjetos se retiraron del cultivo bacteriano y se lavaron con 15 ml de solución salina tamponada con fosfato a temperatura ambiente durante 5 minutos tres veces y después se aclararon con H2O destilada. Después del lavado, los portaobjetos se tiñeron con colorante SYTO17 20 pM (invitrogen, Reino Unido) a temperatura ambiente durante 30 minutos. Después de retirar el exceso de colorante y secar al aire, las muestras se examinaron con un microscopio de barrido láser Carl Zeiss LSM 700 con el software de formación de imágenes ZEN 2009 (Carl Zeiss, Alemania). El índice de cobertura de las bacterias sobre la superficie se analizó usando el software de código abierto Image J 1.44 (National Institute of Health, EE.UU.).
Resultados
La Figura 5A muestra el efecto de titulación sobre la formación de biopelícula en donde Fe-Lac a 50, 100 y 300 pM inhibe la formación de biopelícula por Pseudomonas aeruginosa. En ausencia de Fe-Lac (control), se midió un índice de cobertura mayor para Pseudomonas aeruginosa que en presencia de Fe-Lac.
La Figura 5B muestra el efecto de dispersión sobre la formación de biopelícula en donde Fe-Lac a 10, 50 y 100 pM inhibe la formación de biopelícula por Pseudomonas aeruginosa. En ausencia de Fe-Lac (control), se midió un índice de cobertura mayor para Pseudomonas aeruginosa que en presencia de Fe-Lac.
Ejemplo de referencia 3 Fe-Cit Prevención de la formación de biopelícula por Pseudomonas aeruginosa.
Materiales y métodos
Se cultivó de forma rutinaria cepa PAO-1 de Pseudomonas aeruginosa en placas de agar LB (Luria-Bertani, Oxoid, Reino Unido) a 37 °C o en caldo a 37 °C con agitación a 200 rpm. Se incubaron portaobjetos de vidrio esterilizados por UV en 15 ml de medio definido RPMI-1640 (Sigma, Reino Unido) o en 15 ml de RPMI-1640 con Fe-Cit inoculado con bacterias diluidas (DO600 = 0,01) procedentes de cultivos de una noche a 37 °C con agitación a 60 rpm durante 72 horas. Los portaobjetos se retiraron del cultivo bacteriano y se lavaron con 15 ml de solución salina tamponada con fosfato a temperatura ambiente durante 5 minutos tres veces y después se aclararon con H2O destilada. Después del lavado, los portaobjetos se tiñeron con colorante SYTO17 20 pM (invitrogen, Reino Unido) a temperatura ambiente durante 30 minutos. Después de retirar el exceso de colorante y secar al aire, las muestras se examinaron con un microscopio de barrido láser Carl Zeiss LSM 700 con el software de formación de imágenes ZEN 2009 (Carl Zeiss, Alemania). El índice de cobertura de las bacterias sobre la superficie se analizó usando el software de código abierto Image J 1.44 (National Institute of Health, EE.UU.).
Resultados
La Figura 6 muestra el efecto sobre la formación de biopelícula en donde Fe-Cit a 100 y 300 pM inhibe la formación de biopelícula por Pseudomonas aeruginosa. En ausencia de Fe-Cit (control), se midió un índice de cobertura mayor para Pseudomonas aeruginosa que en presencia de Fe-Cit.
Ejemplo de referencia 4 Fe-Tart Prevención de la formación de biopelícula por Pseudomonas aeruginosa.
Materiales y métodos
Se cultivó de forma rutinaria cepa PAO-1 de Pseudomonas aeruginosa en placas de agar LB (Luria-Bertani, Oxoid, Reino Unido) a 37 °C o en caldo a 37 °C con agitación a 200 rpm. Se incubaron portaobjetos de vidrio esterilizados por UV en 15 ml de medio definido RPMI-1640 (Sigma, Reino Unido) o en 15 ml de RPMI-1640 con Fe-Tart inoculado con bacterias diluidas (DO600 = 0,01) procedentes de cultivos de una noche a 37 °C con agitación a 60 rpm durante 72 horas. Los portaobjetos se retiraron del cultivo bacteriano y se lavaron con 15 ml de solución salina tamponada con fosfato a temperatura ambiente durante 5 minutos tres veces y después se aclararon con H2O destilada. Después del lavado, los portaobjetos se tiñeron con colorante SYTO17 20 pM (Invitrogen, Reino Unido) a temperatura ambiente durante 30 minutos. Después de retirar el exceso de colorante y secar al aire, las muestras se examinaron con un microscopio de barrido láser Carl Zeiss LSM 700 con el software de formación de imágenes ZEN 2009 (Carl Zeiss, Alemania). El índice de cobertura de las bacterias sobre la superficie se analizó usando el software de código abierto Image J 1.44 (National Institute of Health, EE.UU.).
Resultados
La Figura 7 muestra el efecto sobre la formación de biopelícula en donde Fe-Tart a 100 y 300 pM inhibe la formación de biopelícula por Pseudomonas aeruginosa. En ausencia de Fe-Tart (control), se midió un índice de cobertura mayor para Pseudomonas aeruginosa que en presencia de Fe-Tart.
Ejemplo de referencia 5 Fe-Gly Prevención de la formación de biopelícula por Pseudomonas aeruginosa.
Materiales y métodos
Se cultivó de forma rutinaria cepa PAO-1 de Pseudomonas aeruginosa en placas de agar LB (Luria-Bertani, Oxoid, Reino Unido) a 37 °C o en caldo a 37 °C con agitación a 200 rpm. Se incubaron portaobjetos de vidrio esterilizados por UV en 15 ml de medio definido RPMI-1640 (Sigma, Reino Unido) o en 15 ml de RPMI-1640 con Fe-Gly inoculado con bacterias diluidas (DO600 = 0,01) procedentes de cultivos de una noche a 37 °C con agitación a 60 rpm durante 72 horas. Los portaobjetos se retiraron del cultivo bacteriano y se lavaron con 15 ml de solución salina tamponada con fosfato a temperatura ambiente durante 5 minutos tres veces y después se aclararon con H2O destilada. Después del lavado, los portaobjetos se tiñeron con colorante SYTO17 20 pM (Invitrogen, Reino Unido) a temperatura ambiente durante 30 minutos. Después de retirar el exceso de colorante y secar al aire, las muestras se examinaron con un microscopio de barrido láser Carl Zeiss LSM 700 con el software de formación de imágenes ZEN 2009 (Carl Zeiss, Alemania). El índice de cobertura de las bacterias sobre la superficie se analizó usando el software de código abierto Image J 1.44 (National Institute of Health, EE.UU.).
Resultados
La Figura 8 muestra el efecto sobre la formación de biopelícula en donde Fe-Gly a 100 y 300 pM inhibe la formación de biopelícula por Pseudomonas aeruginosa. A 300 pM Fe-Gly fue capaz de inhibir la formación de biopelícula en comparación con la ausencia de Fe-Gly (control) cuando se midió una índice de cobertura mayor para Pseudomonas aeruginosa que en presencia de Fe-Gly.
Ejemplo 6: Inhibición de la formación de biopelícula sobre la superficie de perlas por Campylobacter jejuni NCTC 11168 usando Fe-Tart, FeQ (comparativo) y Fe-Cit
Materiales y métodos
El efecto de Fe-Tart, Fe-Cit y Fe-Q (QPLEX) sobre la formación de biopelículas por Campylobacter jejuni NCTC 1168 se sometió a ensayo como se describe en los materiales y métodos del Ejemplo 1 del documento PCT/US2015/044603 y los ejemplos anteriores.
Resultados
El efecto de Fe-Tart, FeQ (QPLEX) y Fe-Cit sobre la formación de biopelícula sobre la superficie de una perla por Campylobacter jejuni NCTC 11168 se sometió a ensayo como se describe en los materiales y métodos. Los datos de la Figura 9 muestran que Fe-Tart, FeQ (QPLEX) y Fe-Cit inhibieron la formación de biopelícula por C. jejuni en perlas UV recubiertas de plástico. Fe-Tart a 50, 100 y 300 j M, así como Fe-Cit a 50, 100 y 300 j M inhiben la formación de biopelícula por C. jejuni. Un control (sin adición de Fe-Tart, FeQ (QPLEX), o Fe-Cit) demostró un índice de cobertura significativamente superior de biopelícula de C. jejuni sobre la superficie de la perla.
Ejemplo 7: Potenciación del aumento de peso en cerdos destetados mediante la administración de complejos de Fe hidrosolubles
El objetivo de este estudio piloto es evaluar el efecto de tres complejos de Fe hidrosolubles (lactato férrico, citrato férrico y tartrato férrico) sobre el rendimiento de crecimiento y la microbiota colónica de cerdos destetados.
Materiales y métodos
Detalles de los animales
Número de tratamientos: 4 tratamientos
Número de réplicas: 4 corrales
Número de animales por corral: 4 cerdos (equilibrados por sexo en la medida de lo posible) Número de corrales en el estudio: 16 corrales
Especie y raza de los animales: cerdos recién destetados (Grandes Blancos x Landrace) Número total de animales: 64
Diseño experimental
Había cuatro (4) tratamientos, que tenía cada uno 4 corrales de réplica con 4 cerdos por corral de réplica, es decir, 16 cerdos por tratamiento o 64 cerdos en total. El Tratamiento 1 fueron dietas de control, mientras que los Tratamientos 2 a 4 fueron a través de proporcionar de agua que incluía diferentes complejos de Fe (Tabla 14).
Tabla 14. Tratamientos experimentales y estructura del tratamiento Tratamiento Aditivo Fe-tartrato (g/l) Fe-citrato (g/l) Fe-lactato (g/l) Corrales por trt 1 No - - - 4
2 Sí 0,2 4
3 Sí 0,2 4
2 Sí 0,2 4
Piensos
Los piensos utilizados fueron piensos comerciales convencionales, sin fármacos, adaptados para cerdos destetados. Los piensos se ofrecieron en forma de gránulos de 3 mm y a demanda. También había disponible agua a demanda.
Alojamiento
En este estudio se usó el edificio de Etología 3 de la Unidad de Cerdos Easter Howgate de la SRUC. Esta nave consiste en 6 salas, cada una con 4 corrales, por lo que tiene capacidad para 24 corrales de 4 m2 cada uno; para este estudio, se usaron 4 salas. La nave para animales, que es un edificio con control ambiental, se desinfectó antes de su uso y entre rondas. Los cerdos se colocaron en el destete sobre una capa gruesa de virutas de madera blanca fresca o paja en los corrales. Los corrales estaban equilibrados en la medida de lo posible en cuanto al origen y el sexo de la camada (2 machos intactos y 2 hembras). Los corrales se cubrieron con serrín o paja adicional según fuera necesario y se equiparon con un solo comedero y un bebedero de tetina. Los alimentos estuvieron disponibles a demanda durante todo el tiempo. El agua se suministró a través de botellas medidas por corral y también estaba
disponible. La temperatura ambiental se mantuvo en 26 °C durante los primeros 4 días después del destete y después se redujo 2 °C durante el resto del experimento. Las luces estuvieron encendidas desde las 08:00 hasta las 18:00 y las luces nocturnas se mantuvieron entre las 18:00 y las 08:00.
Parámetros medidos
La dieta se analizó para su análisis proximal (materia seca, proteína, grasa y fibra [Fibra Neutra Detergente]). Véase la Tabla 16.
Los cerdos se pesaron individualmente los días 0, 6 y 13. Se pesaron los cerdos retirados o encontrados muertos y se indicó la fecha.
El volumen de pienso ofrecido por corral se registró a diario desde el día 0 hasta el día 12, inclusive. Los rechazos de pienso se registraron a diario desde el día 1 hasta el día 13, inclusive.
El peso de los cerdos, el pienso ofrecido y los rechazos de pienso se usaron para determinar el aumento de peso promedio diario, la ingesta de pienso diaria y el índice de conversión de pienso, durante los días 0 a 6, 6 a 13, así como 0 a 13.
Desde el día 0 hasta el día 13, se registró el volumen de agua ofrecido por corral a diario y se registraron los niveles de agua de las botellas de agua antes de la alimentación matutina, antes del tupido.
Se tomaron a diario puntuaciones de heces, limpieza y salud (Apéndice). Las puntuaciones fecales son especialmente indicativas de la incidencia de diarrea y se usan en la industria como un indicador general de salud intestinal fácil de observar. Se tomaron muestras fecales de un cerdo macho seleccionado al azar los días 0 (destete), 4, 6 y 13. Las muestras fecales se almacenaron en condiciones que permitían su envío a Servicios Veterinarios SAC para la cuantificación de lactobacilos y coliformes, así como su relación (proporción L:C). Se usan como indicadores clave de la salud intestinal, siendo una relación L:C mayor indicativa de una salud intestinal mejor.
El mismo cerdo macho utilizado para el muestreo se sometió a autopsia el día 13, con énfasis en la evaluación de los tipos y las puntuaciones de las lesiones intestinales. Se llevaron registros diarios de la salud, el sacrificio selectivo y la mortalidad. Se registraron las causas de las muertes y los sacrificios y cualesquier muertes inexplicables o inesperadas o los cerdos en mal estado de salud se sometieron a autopsia por Servicios Veterinarios SAC. Se calculó el índice de conversión de pienso corregido por la mortalidad si ésta se produjo.
Tabla 15. Muestreo y análisis resumidos
Muestra N.° Análisis Laboratorio Notas
Pienso 1 Materia seca, proteína en bruto, DM Una sola muestra de pienso grasa, fibra (FND). Scientific
Heces 64 Lactobacilos y coliformes Servicios Los datos se expresaron en ufc/g y se veterinarios calculó su relación (relación L:C)
SAC
Autopsia 16 Autopsia general, con énfasis Servicios El mismo cerdo que se usó para el muestreo en las lesiones intestinales veterinarios fecal
SAC
Los datos recogidos se analizaron usando un análisis de la varianza (ANOVA), para someter a ensayo el efecto de la provisión de complejos de Fe en sí y del tipo de complejo de Fe. Los tratamientos se asignaron en bloques dentro de Etología 3, cada uno de los cuatro tratamientos propuestos en cada una de las cuatro salas utilizadas. Como tales, las salas se usaron como bloque en el modelo. Los efectos se consideraron significativos a P<0,05.
Apéndice. Puntuaciones de salud, heces y limpieza
Tipo Puntuación Descripción
Salud 1 Cerdos que están tumbados, sentados, de pie o caminando y responden activamente a la presencia humana; piel rosa, ojos brillantes, orejas erguidas 2 Cerdos que están tumbados/dormidos, que responden normalmente a la presencia humana tras una estimulación suave; piel rosa, ojos brillantes, orejas erguidas 3 Cerdos que están tumbados y ligeramente temblorosos, que no responden normalmente después de una estimulación suave, piel rosa-grisácea, ojos algo hundidos, orejas ligeramente caídas
4 Cerdos que muestran dolor, por ejemplo, patadas en el abdomen, tumbados retorcidos, con el lomo encorvado, piel gris, ojos hundidos, orejas caídas
________________(continuación)__________________________________________ Tipo______Puntuación Descripción___________________________________________________________ Heces 1 Forma firme de las heces (1,5 para heces blandas pero compactas, de tipo arcilla)
2 No hay heces formadas, poca diseminación ("diarrea normal")
3 No hay heces formadas, acuosas, se diseminan fácilmente ("diarrea acuosa") 4 No hay heces formadas, muy acuosas, motas de sangre, se diseminan rápidamente ("disentería")
Limpieza 1 Todos los cerdos están limpios
2 1 o 2 cerdos están un poco sucios
3 3 o 4 cerdos están un poco sucios
4 Todos los cerdos están muy sucios________________________________________ Acciones:
Si la puntuación de salud es 1 o 2, entonces no se requiere ninguna acción adicional.
Si la puntuación de salud o de heces es 3, poner en aviso al NACWO (oficial designado de cuidado y bienestar animal, por sus siglas en inglés)
Si la puntuación de salud es 4, o la puntuación de heces es 4, entonces buscar el consejo de un veterinario.
Resultados
Los resultados se muestran en las siguientes tablas.
Tabla 16. Peso corporal (kg/cerdo)
Tratamientos1 Días después del destete
0 4 7 14
Agua 9,77 10,88 11,92 15,61 Lactato férrico 9,74 10,35 10,94 15,05 Tartrato férrico 9,81 10,81 11,46 15,27 Citrato férrico 9,78 10,80 11,60 15,91
e.t.d. 0,11 0,29 0,20 0,38 Valores de P
Tratamiento 0,929 0,297 0,006 0,185 Comparaciones
Agua frente a todo 0,955 0,353 0,006 0,543 Agua frente a Fe-lactato 0,773 0,097 <0,001 0,175 Agua frente a Fe-tartrato 0,725 0,798 0,046 0,400 Agua frente a Fe-citrato 0,940 0,785 0,141 0,441 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras)
Tabla 17. Ingesta diaria de pienso promediada (g/día/cerdo)
Días después del destete
Tratamientos1 de 0 a 4 de 4 a 7 de 0 a 7 de 7 a 14 de 0 a 14 Agua 220 445 316 555 436 Lactato férrico 154 315 223 532 378 Tartrato férrico 190 410 284 516 400 Citrato férrico 202 428 299 590 445 e.t.d. 40 46 37 33 26 Valores de P
Tratamiento 0,455 0,075 0,134 0,204 0,100 Comparaciones
Agua frente a todo 0,280 0,139 0,149 0,750 0,221 Agua frente a Fe-lactato 0,137 0,019 0,033 0,510 0,055 Agua frente a Fe-tartrato 0,476 0,465 0,408 0,270 0,209 Agua frente a Fe-citrato 0,671 0,718 0,649 0,318 0,744 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras)
Tabla 18. Aumento de peso corporal promediado (g/día/cerdo)
Días después del destete Tratamientos1 de 0 a 4 de 4 a 7 de 0 a 7 de 7 a 14 de 0 a 14 Agua 278 345 307 527 417 Lactato férrico 153 197 172 587 380 Tartrato férrico 249 217 235 545 390 Citrato férrico 256 265 260 617 438
e.t.d. 78 91 30 45 27 Valores de P
Tratamiento 0,436 0,417 0,009 0,254 0,196 Comparaciones
Agua frente a todo 0,380 0,144 0,007 0,164 0,531 Agua frente a Fe-lactato 0,144 0,138 0,001 0,215 0,199 Agua frente a Fe-tartrato 0,717 0,193 0,039 0,699 0,346 Agua frente a Fe-citrato 0,781 0,401 0,146 0,079 0,452 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras)
Tabla 19. Índice de conversión de pienso (g/g)
Días después del destete Tratamientos1 de 0 a 4 de 4 a 7 de 0 a 7 de 7 a 14 de 0 a 14 Agua 0,80 1,56 1,07 1,08 1,05 Lactato férrico 0,54 -1,65 2,67 0,91 1,00 Tartrato férrico 0,79 2,98 1,23 0,95 1,03 Citrato férrico 0,79 1,81 1,17 0,98 1,03 e.t.d. 0,19 2,61 1,01 0,05 0,05 Valores de P
Tratamiento 0,463 0,378 0,388 0,067 0,806 Comparaciones
Agua frente a todo 0,542 0,815 0,469 0,017 0,500 Agua frente a Fe-lactato 0,191 0,249 0,147 0,013 0,359 Agua frente a Fe-tartrato 0,960 0,599 0,873 0,048 0,657 Agua frente a Fe-citrato 0,932 0,926 0,922 0,109 0,774 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras)
Tabla 20. Ingesta de agua diaria promediada (g/día/cerdo)
Días después del destete Tratamientos1 de 0 a 4 de 4 a 7 de 0 a 7 de 7 a 14 de 0 a 14 Agua 766 1120 921 1368 1148 Lactato férrico 641 885 746 1335 1040 Tartrato férrico 711 1115 884 1359 1122 Citrato férrico 664 1146 871 1451 1161 e.t.d. 102 105 92 97 90 Valores de P
Tratamiento 0,639 0,109 0,312 0,669 0,562 Comparaciones
Agua frente a todo 0,289 0,427 0,274 0,870 0,592 Agua frente a Fe-lactato 0,251 0,052 0,089 0,739 0,260 Agua frente a Fe-tartrato 0,605 0,961 0,698 0,929 0,773 Agua frente a Fe-citrato 0,345 0,809 0,598 0,418 0,894 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras)
Tabla 21. Recuentos de E. co li fecal (10log ufc/g)____________
Días después del destete Tratamientos1 0 4 7 14 Agua 8,26 7,12 6,30 5,15 Lactato férrico 8,40 7,80 6,37 5,98 Tartrato férrico 8,67 6,42 6,51 6,43 Citrato férrico 7,08 7,30 6,17 4,73 e.t.d. 0,40 1,34 1,20 0,55 Valores de P
Tratamiento 0,027 0,599 0,996 0,103 Comparaciones
Agua frente a todo 0,542 0,946 0,946 0,143 Agua frente a Fe-lactato 0,737 0,503 0,933 0,085 Agua frente a Fe-tartrato 0,332 0,526 0,829 0,028 Agua frente a Fe-citrato 0,024 0,908 0,925 0,512 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras); se muestreó un cerdo macho para este parámetro y se muestreó el mismo cerdo siempre
Tabla 22. Recuento de lactobacilos fecales (10log ufc/g)
Días después del destete Tratamientos1 0 4 7 14 Agua 8,81 7,33 8,44 8,79 Lactato férrico 8,68 8,76 8,97 8,77 Tartrato férrico 8,84 8,94 9,48 8,79 Citrato férrico 9,10 8,74 8,48 8,43 e.t.d. 0,28 0,83 0,55 0,55
Valores de P Tratamiento 0,531 0,256 0,275 0,906
Comparaciones Agua frente a todo 0,783 0,067 0,257 0,782 Agua frente a Fe-lactato 0,661 0,130 0,355 0,976 Agua frente a Fe-tartrato 0,918 0,092 0,098 0,995 Agua frente a Fe-citrato 0,330 0,155 0,944 0,552 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras); se muestreó un cerdo macho para este parámetro y se muestreó el mismo cerdo siempre
Tabla 23. Relación de lactobacilos con respecto a E. co li (L:C)
Días después del destete Tratamientos1
0 4 7 14 Agua 1,08 1,00 1,33 1,75 Lactato férrico 1,03 1,08 1,33 1,45 Tartrato férrico 1,02 1,27 1,45 1,28 Citrato férrico 1,27 1,57 1,65 1,91 e.t.d. 0,05 0,41 0,27 0,31 Valores de P
Tratamiento 0,010 0,498 0,615 0,263 Comparaciones
Agua frente a todo 0,477 0,223 0,332 0,261 Agua frente a Fe-lactato 0,449 0,788 0,962 0,193 Agua frente a Fe-tartrato 0,342 0,382 0,523 0,071 Agua frente a Fe-citrato 0,010 0,274 0,329 0,669 1cuatro corrales por tratamiento; cuatro cerdos por corral (dos machos y dos hembras); se muestreó un cerdo macho para este parámetro y se muestreó el mismo cerdo siempre
En resumen, los lechones tienden a estresarse mucho cuando son destetados y pueden infectarse fácilmente durante el período de dos semanas que sigue al destete. Esto da como resultado una disminución del rendimiento. Como demuestran los resultados, los lechones a los que se les administraron los complejos de hierro (III) hidrosolubles tuvieron índices de conversión de pienso mejorados (números más bajos) durante el período de 7 a 14 días en comparación con el grupo de control que solo recibió agua. Se cree que esto es resultado de la inhibición de la proliferación de la infección por E. coli que aparece en la segunda semana después del destete. Estos resultados son coherentes con los datos de las aves de corral del Ejemplo 1, en el que se miden niveles inferiores de E. coli tras el tratamiento con tirosinato y quinato férrico.
Ejemplo de referencia 8 Inhibición de biopelícula por compuestos de complejos de hierro - Resultados de titulaciones de EDTA férrico, malato férrico e hidroxilato de oxalato férrico en cepas clínicas de Aislado Pulmonar de FQ N.° 11 de Cepas de EED
Materiales y métodos
Compuestos de complejos de hierro: Se sometieron a ensayo EDTA férrico, malato férrico e hidroxilato de oxalato férrico usando cepas clínicas de Aislado Pulmonar de FQ N.° 11 de Cepas de EED.
Se colocaron perlas estériles en 3 ml de medio Eagle modificado de Dulbecco (DMEM), junto con la concentración deseada del complejo de hierro y se inocularon con EED n.° 11 PAO hasta una DO600 de 0,05. Después, las perlas se incubaron a 37 °C durante 24 horas.
Las perlas se lavaron suavemente tres veces en PBS, se colocaron en 1 ml de PBS y se sometieron a ultrasonidos en baño de agua durante 12 minutos. La biopelícula sobre cada cuenta se cuantificó contando las unidades formadoras de colonias. El PBS que contenía las células bacterianas de biopelícula se diluyó en serie y se colocaron 10 pl de cada dilución en agar LB. Estas placas se incubaron a 30 °C durante 24 horas y se contaron las colonias.
Los resultados se muestran en la Figura 10. Todos los compuestos de Fe sometidos a ensayo mostraron una inhibición estadísticamente significativa de las biopelículas formadas de aislados clínicos.
Ejemplo 9. Eficacia del lactato férrico y del FeQ (comparativo) para reducir
el porte de Campylobacter en pollos
Materiales y métodos
Se realizó un estudio para evaluar la reducción del porte de Campylobacter en pollos usando lactato férrico en un grupo de tratamiento y FeQ (Q-PLEX) en un segundo grupo de tratamiento. Un tercer grupo de tratamiento sirvió como control positivo. El lactato férrico y el FeQ se administraron a los grupos de tratamiento a una concentración de 340 pM en el agua potable. Cada grupo de tratamiento comprendía 12 aves por corral. Los tres grupos de tratamiento se expusieron por vía oral a 105 ufc de Campylobacter jejuni el día 14 del ensayo. El día 35 días, todas las aves se sacrificaron y se realizó una bacteriología cuantitativa en el contenido del ciego.
Resultados
Los resultados se muestran en la Figura 11. Las aves que fueron tratadas con lactato férrico y FeQ (Q-PLEX) en su agua potable tenían niveles inferiores de Campylobacter en los ciegos que las aves del grupo de control positivo, consiguiéndose los niveles inferiores usando lactato férrico.
Ejemplo Comparativo 10. Estudio de intervalo de dosis de FeTyr administrado en pienso para reducir el porte de Campylobacter en pollos y promover el crecimiento en pollos
Como se ha descrito anteriormente, puede usarse FeTyr para promover el crecimiento en pollos. Este estudio demuestra las dosis más eficaces en pollos para potenciar el aumento de peso.
Materiales y métodos
Se realizó un estudio para evaluar la promoción del crecimiento y la reducción del porte de Campylobacter usando FeTyr en pollos de engorde Ross 308 machos con 7 grupos de tratamiento. Cada grupo de tratamiento comprendía ocho réplicas de 10 aves por corral (80 aves/grupo de tratamiento), con 2 grupos de control y 6 grupos de ensayo. Todos los grupos de ensayo y ambos grupos de control se expusieron el día 20 del ensayo a una cama sucia, que dio positivo en Campylobacter. Este método se usó para proporcionar un método más natural para exponer a las aves a Campylobacter. Por lo tanto, había dos controles positivos en los que cada grupo de tratamiento se expuso a Campylobacter y cinco grupos de tratamiento que se expusieron todos a Campylobacter. El número total de aves utilizadas en los 7 grupos de tratamiento fue de 560.
Los detalles de los tratamientos se proporcionan en la Tabla 24. El grupo de tratamiento 1 era un control positivo en el que las aves solo recibieron el pienso comercial y se expusieron a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 2 recibió 0,01 g/kg de TYPLEX (FeTyr) en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 3 recibió 0,02 g/kg de TYPLEX (FeTyr) en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 4 recibió 0,05 g/kg de TYPLEX (FeTyr) en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 5 recibió 0,1 g/kg de TYPLEX (FeTyr) en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 6 recibió 0,2 g/kg de TYPLEX (FeTyr) en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. El grupo de tratamiento 7 era un segundo grupo de control y recibió 0,022 g/kg de FeQ en su pienso y se expuso a una cama sucia que contenía Campylobacter el día 20. Se alimentó a las aves con un programa comercial de alimentación en tres fases, usando piensos de inicio, de crecimiento y de finalización como se describe en el Ejemplo 1. Las aves se criaron en corrales de suelo hasta el día 42 y se alimentaron con pienso de inicio, de crecimiento y de finalización los días 0 a 11, 11 a 24 y 24 a 42 días, respectivamente. Todas las aves se pesaron individualmente y se registraron las pesadas de pienso por corral los días 0, 11,21, 24 y 42.
El día 20, la cama, que estaba naturalmente contaminada con Campylobacter, se sometió a ensayo para confirmar la presencia de Campylobacter y después se añadió (aproximadamente 2 kg/corral) a la cama en todos los corrales. El día 42, se tomaron muestras de ciego y se sometieron a ensayo para la enumeration de Campylobacter, E. coli y Salmonella.
Con el fin de minimizar el riesgo de contaminación cruzada, se usaron medidas de bioseguridad convencionales de la industria, incluyendo: desinfección de botas, cambio de cubrecalzado y guantes entre corrales/tratamientos, entrar en los corrales negativos para Campylobacter antes de entrar en los corrales positivos para Campylobacter y dejar los corrales adyacentes vacíos. Se registraron la salud diaria, el sacrificio selectivo y la mortalidad. Todos los pesos de las aves se registraron a los 0, 11, 21, 24, 33 y 42 días. Se derivaron el aumento de peso, la ingesta de pienso y el índice de conversión de pienso (ICP) para cada período de alimentación.
Resultados
Los resultados de crecimiento se resumen en las Tablas 24 a 34 y muestran los efectos sobre los grupos de tratamiento de FeTyr en cinco dosis diferentes (T2-T6) en pienso en comparación con el grupo de control (grupo de tratamiento 1, T1) y el grupo de control de FeQ (grupo de tratamiento 7, T7) para los períodos de 0-11 días, 11-20 días, 20-25 días, 25-35 días, 11-25 días, 25-42 días, 35-42 días, 0-25 días, 0-35 días y 0-42 días.
Tabla 24. Rendimiento zootécnico de 1 a 11 días de edad d
Tabla 25. Rendimiento zootécnico de 11 a 20 días de edad d
Tabla 26. Rendimiento zootécnico de 11 a 25 días de edad d
Tabla 27. Rendimiento zootécnico de 20-25 días de edad d
continuación
Tabla 28. Rendimiento zootécnico de 25-35 días de edad d
Tabla 29. Rendimiento zootécnico de 20-35 días de edad d
continuación
Tabla 30. Rendimiento zootécnico de 25-42 días de edad d
Tabla 31. Rendimiento zootécnico de 35-42 días de edad d
continuación
Tabla 32. Rendimiento zootécnico de 0-25 días de edad d
Tabla 33. Rendimiento zootécnico de 0-35 días de edad d
continuación
Tabla 34. Rendimiento zootécnico de 0-42 días de edad d
La Figura 12 muestra el peso corporal promedio en el día 42 para todos los grupos de tratamiento. La figura muestra que todos los grupos de tratamiento que recibieron FeTyr (TYPLEX) y FeQ (Q-PLEX) tuvieron un peso corporal promedio superior en el día 42 que el grupo de control.
La Figura 13 muestra el índice de conversión de pienso ajustado a la mortalidad (ICPM) en el día 42 para todos los grupos de tratamiento. (Un número de ICPM inferior es un resultado mejor). La figura muestra que todos los grupos de tratamiento que recibieron FeTyr (TYPLEX) y FeQ (Q-PLEX) tuvieron valores de ICPM mejorados en comparación con el grupo de control.
La Figura 14 muestra el número de unidades formadoras de colonias de Campylobacter por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento. (Un número inferior es un mejor resultado). Los resultados muestran que la alimentación con FeTyr (TYPLEX) o FeQ (Q-PLEX) en los piensos tuvo un efecto positivo sobre la reducción de la infección por Campylobacter de aves de corral.
La Figura 15 muestra el número de unidades formadoras de colonias de Salmonella por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento. (Un número inferior es un mejor resultado). Los resultados muestran que la alimentación con FeTyr (TYPLEX) o FeQ (Q-PLEX) en los piensos tuvo un efecto positivo sobre la reducción de la infección por Campylobacter de aves de corral.
La Figura 16 muestra el número de unidades formadoras de colonias de E. coli por gramo (ufc/g) de ciego en el día 42 para todos los grupos de tratamiento. (Un número inferior es un mejor resultado). Los resultados muestran que la alimentación con FeTyr (TYPLEX) o FeQ (Q-PLEX) en los piensos tuvo un efecto positivo sobre la reducción de la infección por Campylobacter de aves de corral.
Claims (11)
1. Un método no terapéutico de potenciación del crecimiento de un animal, comprendiendo el método provocar que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejos de Fe III de Fórmula I:
Fe(IN)x(ligando)y Fórmula I
en donde
x es un valor de número entero de 1-2,
y es un valor de número entero de 1-3, y
cada ligando presente es independientemente una base conjugada de un a-hidroxiácido seleccionado del grupo que consiste en ácido cítrico, ácido tartárico, ácido láctico, ácido glicólico, ácido isoleúcico, ácido málico y ácido mandélico; o cada ligando es una base conjugada de un aminoácido seleccionado independientemente del grupo que consiste en glicina, alanina, ácido aspártico, cisteína, ácido glutámico, isoleucina, leucina, metionina, fenilalanina, prolina, serina, treonina y valina;
y sales y/o hidratos de los mismos, en donde el crecimiento del animal se potencia en comparación con un control sin tratar, en donde el crecimiento potenciado se basa en las mediciones de una o más características seleccionadas del grupo que consiste en peso corporal, peso corporal promedio (PCP), ingesta de pienso o ingesta de pienso promedio (IPP), aumento de peso o aumento de peso promedio (APP), e índice de conversión de pienso ajustado a la mortalidad (ICPM), y en donde el animal es un mamífero o un ave, y
en donde, cuando el animal es un ave de corral, entonces:
(a) se provoca que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejos de Fe III en forma de una composición que consiste esencialmente en el uno o más compuestos de complejos de Fe III y un pienso para aves de corral, o en forma de un agua potable para animales que consiste esencialmente en el uno o más compuestos de complejos de Fe III y agua; y/o
(b) se provoca que el animal ingiera o absorba una cantidad eficaz del uno o más compuestos de complejos de Fe III en forma de una composición que no incluye un antibiótico como aditivo.
2. El uso no terapéutico de uno o más compuestos de complejos de Fe III de Fórmula I como se definen en la Reivindicación 1, o sales y/o hidratos de los mismos, en donde el crecimiento del animal se potencia en comparación con un control sin tratar,
para potenciar el crecimiento de un animal, provocando que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejo de Fe III,
en donde el crecimiento potenciado se basa en las mediciones de una o más características seleccionadas del grupo que consiste en peso corporal, peso corporal promedio (PCP), ingesta de pienso o ingesta de pienso promedio (IPP), aumento de peso o aumento de peso promedio (APP), e índice de conversión de pienso ajustado a la mortalidad (ICPM), y
en donde el animal es un mamífero o un ave, y
en donde, cuando el animal es un ave de corral, entonces:
(a) se provoca que el animal ingiera o absorba una cantidad eficaz de uno o más compuestos de complejos de Fe III en forma de una composición que consiste esencialmente en el uno o más compuestos de complejos de Fe III y un pienso para aves de corral, o en forma de un agua potable para animales que consiste esencialmente en el uno o más compuestos de complejos de Fe III y agua; y/o
(b) se provoca que el animal ingiera o absorba una cantidad eficaz del uno o más compuestos de complejos de Fe III en forma de una composición que no incluye un antibiótico como aditivo.
3. El método de la reivindicación 1, o el uso de la reivindicación 2, en donde el uno o más compuestos que tienen la estructura de Fórmula I se seleccionan del grupo que consiste en complejos de ion férrico con lactato, citrato, tartrato y glicinato.
4. El método de la reivindicación 1, o el uso de la reivindicación 2, en donde el uno o más compuestos son citrato férrico.
5. El método de las reivindicaciones 1, 3 o 4, o el uso de cualquiera de las reivindicaciones 2 a 4, en donde el uno o más compuestos se ofrecen al animal a través de una o más vías seleccionadas del grupo que consiste en un pienso para animales, un suplemento de pienso para animales y en agua potable.
6. El método de una cualquiera de las reivindicaciones 1 o 3 a 5, o el uso de cualquiera de las reivindicaciones 2 a 5, en donde:
(a) el animal es un adulto o una cría y se selecciona del grupo que consiste en aves de corral, cerdos, vacas, ovejas, camélidos, conejos, perro y gato;
(b) el animal se selecciona del grupo que consiste en pollos, pavos y patos;
(c) el animal es un pollo seleccionado del grupo que consiste en pollos de engorde y gallinas ponedoras;
(d) el animal es un cerdo y, opcionalmente, en donde la composición se administra al animal en el destete o después del mismo; o
(e) el animal es un rumiante y, opcionalmente, en donde la composición se administra al animal en el destete o después del mismo.
7. El método de una cualquiera de las reivindicaciones 1 o 3 a 6, o el uso de una cualquiera de las reivindicaciones 2 a 6, en donde el crecimiento potenciado se basa en las mediciones de una o más características seleccionadas del grupo que consiste en peso corporal, peso corporal promedio (PCP), aumento de peso o aumento de peso promedio (APP), e índice de conversión de pienso ajustado a la mortalidad (ICPM).
8. El método de una cualquiera de las reivindicaciones 1 o 3 a 7, o el uso de una cualquiera de las reivindicaciones 2 a 7, en donde
(a) el animal que ha de tratarse no está infectado con o colonizado desfavorablemente por bacterias u otros microorganismos y/o en cualquier caso está sano; y/o
(b) el animal es un animal no humano y el método o uso el comprenden el sacrificio en última instancia del animal no humano y, opcionalmente, la preparación de una canal del animal o de una pieza del mismo como producto, tal como un producto cárnico.
9. Un producto dietético, que comprende
uno o más compuestos de complejos de Fe III de Fórmula I:
Fe(III)x(ligando)y Fórmula I
en donde
x es un valor de número entero de 1-2,
y es un valor de número entero de 1-3 y
cada ligando presente es independientemente una base conjugada de un a-hidroxiácido seleccionado de ácido tartárico, ácido láctico, ácido glicólico, ácido isoleúcico, ácido málico y ácido mandélico; o cada ligando es una base conjugada de un aminoácido seleccionado independientemente del grupo que consiste en glicina, alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutámico, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptófano y valina; y sales y/o hidratos de los mismos;
para su uso en un método para el tratamiento o la profilaxis de una infección o colonización por Campylobacter en un animal no humano, mediante un método que comprende administrar por vía oral al animal no humano una cantidad eficaz del producto dietético,
en donde el producto dietético se administra al animal no humano solo en una cantidad eficaz para reducir la acumulación de biopelícula en el animal no humano.
10. El producto dietético para su uso de acuerdo con la reivindicación 9, en donde el producto se usa para el tratamiento o la profilaxis de un Campylobacter resistente a antibióticos.
11. El producto dietético para su uso de acuerdo con las reivindicaciones 9 o 10, en donde el animal no humano es:
(a) un adulto o una cría y se selecciona del grupo que consiste en aves de corral, cerdos, vacas, ovejas, camélidos, conejos y animales acuáticos;
(b) se selecciona del grupo que consiste en pollos, pavos y patos;
(c) un pollo seleccionado del grupo que consiste en pollos de engorde y gallinas ponedoras;
(d) cerdos; o
(e) un rumiante.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/US2015/044603 WO2016025448A2 (en) | 2014-08-13 | 2015-08-11 | Antimicrobial compounds and compositions, and uses thereof |
| US201662296386P | 2016-02-17 | 2016-02-17 | |
| US201662334746P | 2016-05-11 | 2016-05-11 | |
| PCT/US2016/046623 WO2017027742A1 (en) | 2015-08-11 | 2016-08-11 | Biofilm inhibiting compositions enhancing weight gain in livestock |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2880321T3 true ES2880321T3 (es) | 2021-11-24 |
Family
ID=57983707
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16754616T Active ES2880321T3 (es) | 2015-08-11 | 2016-08-11 | Composiciones de inhibición de biopelícula que potencian el aumento de peso en el ganado |
Country Status (9)
| Country | Link |
|---|---|
| US (8) | US9975914B2 (es) |
| EP (2) | EP3334440B1 (es) |
| CN (1) | CN108024563A (es) |
| BR (1) | BR112018002045B1 (es) |
| CA (1) | CA2995408C (es) |
| DK (1) | DK3334440T3 (es) |
| ES (1) | ES2880321T3 (es) |
| PL (1) | PL3334440T3 (es) |
| WO (2) | WO2017027742A1 (es) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10653658B2 (en) * | 2015-08-11 | 2020-05-19 | Akeso Biomedical, Inc. | Biofilm inhibiting compositions enhancing weight gain in livestock |
| EP3334440B1 (en) | 2015-08-11 | 2021-04-14 | Akeso Biomedical, Inc. | Biofilm inhibiting compositions enhancing weight gain in livestock |
| CN117959415A (zh) | 2016-09-13 | 2024-05-03 | 阿勒根公司 | 非蛋白质梭菌毒素组合物 |
| US20200188476A1 (en) * | 2017-04-18 | 2020-06-18 | The Regents Of The University Of California | Anti-microbial agent-polymer conjugates and methods of use thereof |
| WO2018204795A1 (en) * | 2017-05-04 | 2018-11-08 | Phoenix Dental, Inc. | Dental composition and method |
| AU2018367660C1 (en) * | 2017-11-19 | 2025-04-03 | Osartis Gmbh | Compositions and methods for treating intervertebral discs |
| BE1026147B1 (nl) * | 2018-03-29 | 2019-10-28 | Farm@Nutrition Besloten Vennootschap Met Beperkte Aansprakelijkheid | Samenstelling voor een voedingsadditief voor dieren en werkwijze om het additief toe te dienen. |
| RU2696388C1 (ru) * | 2018-08-17 | 2019-08-01 | ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ УЧРЕЖДЕНИЕ НАУКИ ИНСТИТУТ ПРОБЛЕМ ЭКОЛОГИИ И ЭВОЛЮЦИИ им. А.Н. СЕВЕРЦОВА РОССИЙСКОЙ АКАДЕМИИ НАУК (ИПЭЭ РАН) | Грибостойкая добавка для лакокрасочного материала |
| CN109122580B (zh) * | 2018-11-01 | 2023-10-20 | 杨凌泓雁换羽研究所 | 一种降低死淘提升产蛋率的病鸡换羽法 |
| CN109852557B (zh) * | 2018-11-30 | 2021-03-26 | 北京国环清华环境工程设计研究院有限公司 | 一种用于城镇存量垃圾稳定化处理的复合菌剂及其制备方法与应用 |
| CN109673856A (zh) * | 2018-12-29 | 2019-04-26 | 广西康佳龙农牧集团有限公司 | 一种防治仔猪黄白痢用的合生素饲料添加剂及应用 |
| CN109464472B (zh) * | 2019-01-17 | 2023-09-15 | 广西医科大学 | 一种铜绿假单胞菌家兔脓胸引流管生物膜模型建立方法 |
| CN109892581A (zh) * | 2019-04-15 | 2019-06-18 | 上海海洋大学 | 一种蟹香味的高钙鱼肉松及其制备方法 |
| CN112569225B (zh) * | 2019-09-27 | 2022-10-21 | 共生地球生物科技有限公司 | 非药物幽门杆菌杀菌组合物 |
| CN110583574A (zh) * | 2019-10-10 | 2019-12-20 | 安庆市立华牧业有限公司 | 产蛋鸡38~42周龄油苗注射后产蛋异常下降控制方法 |
| CN111773206A (zh) * | 2020-06-29 | 2020-10-16 | 广东利泰制药股份有限公司 | 谷氨酰胺在制备抑制大肠杆菌产生基因突变药物中的应用 |
| CN116491603B (zh) * | 2023-05-19 | 2025-08-12 | 徐州医科大学 | 一种防治小鼠艰难梭菌感染的高铁饲料及其应用 |
Family Cites Families (67)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA710277A (en) | 1965-05-25 | E. Barnhart Charles | Feedstuff for inhibiting anemia in swine | |
| US2946722A (en) | 1959-07-21 | 1960-07-26 | Walter H Hoffman | Composition and method for treating poultry |
| US3259500A (en) | 1961-10-11 | 1966-07-05 | Kentucky Res Foundation | Method for inhibiting anemia in young pigs by feeding the sow an iron agent |
| US3558778A (en) | 1966-10-27 | 1971-01-26 | Dow Chemical Co | Methods and compositions for use in animal husbandry |
| US3491187A (en) | 1967-02-27 | 1970-01-20 | Diamond Shamrock Corp | Iron salt-antibiotic compositions and use thereof |
| US4053592A (en) | 1973-03-16 | 1977-10-11 | Abbott Laboratories | Animal growth promotant |
| US4171379A (en) | 1978-04-05 | 1979-10-16 | Ralston Purina Company | Feed supplement for baby pigs |
| US4504471A (en) | 1982-09-27 | 1985-03-12 | Fujisawa Pharmaceutical Co., Ltd. | Animal growth promotant and method of use for animal growth |
| US4889645A (en) | 1985-02-08 | 1989-12-26 | Union Camp Corporation | Substituted-ammonium humate fluid loss control agents for oil-based drilling muds |
| CA2081884C (en) | 1990-05-02 | 2002-01-01 | Fred N. Teumac | Polymer compositions containing oxygen scavenging compounds |
| CN1069192A (zh) | 1992-07-14 | 1993-02-24 | 苏州市畜牧兽医站 | 乳猪用营养型生长促进剂 |
| US5516925A (en) | 1994-08-23 | 1996-05-14 | Albion International, Inc. | Amino acid chelates having improved palatability |
| US6024979A (en) | 1995-06-06 | 2000-02-15 | Solvay Animal Health, Inc. | Oral veterinary composition containing a fluoroquinolone antibacterial agent possessing superior absorption properties and an extended duration of therapeutic antimicrobial blood levels, and a method of treating a microbial infection in a ruminant |
| US6139879A (en) | 1997-06-25 | 2000-10-31 | Foliar Nutrients, Inc. | Fungicidal and bactericidal compositions for plants containing compounds in the form of heavy metal chelates |
| AU4134697A (en) | 1996-09-06 | 1998-03-26 | Otsuka Pharmaceutical Co., Ltd. | Composition, antimicrobial agent, infection preventive, and food against (helicobacter pylori) |
| US6086940A (en) | 1996-10-25 | 2000-07-11 | T.F.H. Publications, Inc. | High starch content dog chew |
| US5879697A (en) | 1997-04-30 | 1999-03-09 | Schneider Usa Inc | Drug-releasing coatings for medical devices |
| KR20010013377A (ko) | 1997-06-04 | 2001-02-26 | 데이비드 엠 모이어 | 마일드한 잔류성 항균 조성물 |
| US5891922A (en) | 1997-08-20 | 1999-04-06 | Preserve International, Preserve, Inc. | Cleaning and disinfectant biocide composition, and method for cleaning animal husbandry surfaces |
| US6773737B1 (en) | 1998-11-19 | 2004-08-10 | The Procter & Gamble Company | Microorganism reduction methods and compositions for food |
| US7143721B2 (en) | 1999-03-10 | 2006-12-05 | Ridley Block Operations, Inc. | Reducing ungulate pressure on post-burn areas in mosaic burns |
| RU2156080C1 (ru) | 1999-10-12 | 2000-09-20 | ЗАО "Белгородский завод лимонной кислоты" "Цитробел" | Премикс для сельскохозяйственных животных и птицы |
| CA2297002A1 (en) | 2000-01-26 | 2001-07-26 | Triosyn Corp. | Antimicrobial flash-dry disinfectant aerosol |
| US8512718B2 (en) | 2000-07-03 | 2013-08-20 | Foamix Ltd. | Pharmaceutical composition for topical application |
| US7431939B1 (en) | 2000-09-28 | 2008-10-07 | Mississippi State University | Inhibition of systemic infections in humans and vertebrates by dietary fibers |
| CA2442602A1 (en) | 2000-12-18 | 2002-08-01 | Probio Health, Llc | Probiotic compounds derived from lactobacillus casei strain ke01 |
| US7247338B2 (en) | 2001-05-16 | 2007-07-24 | Regents Of The University Of Minnesota | Coating medical devices |
| US6669980B2 (en) | 2001-09-18 | 2003-12-30 | Scimed Life Systems, Inc. | Method for spray-coating medical devices |
| SE0103695D0 (sv) | 2001-11-07 | 2001-11-07 | Thomas Boren | A novel non-antibiotic strategy against OGIP infections based on a cereal product |
| DE10228656A1 (de) | 2002-06-27 | 2004-01-22 | Ecolab Gmbh & Co. Ohg | Schaumdesinfektionsmittel |
| US7258875B2 (en) | 2003-12-04 | 2007-08-21 | Chiou Consulting, Inc. | Compositions and methods for topical treatment of skin infection |
| MXPA06006392A (es) | 2003-12-05 | 2007-03-15 | Childrens Hosp Medical Center | Composiciones de oligosacaridos y uso de estas en el tratamiento de infecciones. |
| JP2005325080A (ja) | 2004-05-17 | 2005-11-24 | Daiichi Fine Chemical Co Ltd | パントテン酸カルシウム及びビタミン類を含む組成物 |
| GB0422052D0 (en) | 2004-10-04 | 2004-11-03 | Dansico As | Enzymes |
| GB0423681D0 (en) | 2004-10-26 | 2004-11-24 | Sec Dep For Environment Food & | Vaccine and nucleic acids |
| US20060134227A1 (en) | 2004-12-22 | 2006-06-22 | Bortz Jonathan D | Compositions including iron |
| US20090035385A1 (en) | 2004-12-22 | 2009-02-05 | Drugtech Corporation | Compositions including iron |
| WO2006099153A2 (en) | 2005-03-11 | 2006-09-21 | Archer-Daniels-Midland Company | Compositions and methods providing rumen bypass protein in ruminant diets |
| CN101155516B (zh) | 2005-04-08 | 2012-10-03 | 雪印惠乳业株式会社 | 含乳蛋白的铁组合物 |
| JP2006321776A (ja) | 2005-05-18 | 2006-11-30 | Kyuuken:Kk | アミノ酸を配位して成る金属錯体である抗菌防カビ剤とその二次製品 |
| US20070269495A1 (en) * | 2006-05-18 | 2007-11-22 | Ashmead H Dewayne | Compositions and methods for enhancing mineral levels in animals with reduced environmental impact |
| KR101059408B1 (ko) | 2006-08-03 | 2011-08-29 | 아사히 가세이 일렉트로닉스 가부시끼가이샤 | 감광성 수지 조성물 및 적층체 |
| US20100249058A1 (en) | 2006-10-17 | 2010-09-30 | Idemitsu Kosan Co., Ltd. | Feed additive and feed |
| US20080194679A1 (en) | 2007-02-14 | 2008-08-14 | Ashmead H Dewayne | Compositions and methods for increasing metabolic activity in animal tissue |
| WO2008105983A1 (en) * | 2007-02-27 | 2008-09-04 | Albion International, Inc. | Mineral absorption from the stomach |
| US20090182044A1 (en) | 2008-01-11 | 2009-07-16 | Ashmed H Dewayne | Nitrate amino acid chelates |
| CA2723117C (en) | 2008-05-01 | 2015-06-16 | Anthrax Spores Killer Co., Limited | Versatile disinfectant |
| US8563017B2 (en) | 2008-05-15 | 2013-10-22 | Kimberly-Clark Worldwide, Inc. | Disinfectant wet wipe |
| US8399635B2 (en) | 2008-11-12 | 2013-03-19 | Synedgen, Inc. | Chitosan derivatives to treat animals or optimize animal health |
| US8273514B2 (en) | 2009-05-22 | 2012-09-25 | Xerox Corporation | Interfacial layer and coating solution for forming the same |
| BRPI1013053A2 (pt) | 2009-06-08 | 2016-04-05 | Idemitsu Kosan Co | agente de controle de coccidiose para um animal, aditivo para ração, método para a criação de um animal, e, líquido aquecido da castanha de caju e/ou cardanol |
| US8178709B2 (en) | 2009-07-21 | 2012-05-15 | Biolink Life Sciences, Inc. | Iron preparation suitable for pharmaceutical formulation and process for the preparation thereof |
| ES2654334T3 (es) | 2010-01-18 | 2018-02-13 | Concept Medical Research Private Limited | Método y sistema para el recubrimiento de dispositivos médicos insertables |
| WO2012034032A2 (en) | 2010-09-10 | 2012-03-15 | The Board Of Regents Of Unbiversity Of Texas System | Antimicrobial solutions |
| CA2820706C (en) | 2010-12-03 | 2018-05-22 | Ms Technologies, Llc | Optimized expression of glyphosate resistance encoding nucleic acid molecules in plant cells |
| WO2012097155A1 (en) | 2011-01-14 | 2012-07-19 | Chiasma Inc. | Improved pharmaceutical compositions for delivery of ferric iron compounds, and methods of use thereof |
| US8741375B2 (en) | 2011-06-07 | 2014-06-03 | Zinpro Corporation | Mixed amino acid metal salt complexes |
| ITMI20111033A1 (it) | 2011-06-08 | 2012-12-09 | Giuliano Leonardi | Procedimento per la preparazione di una composizione comprendente complessi metallici in matrice organica oleosa |
| WO2012167368A1 (en) | 2011-06-08 | 2012-12-13 | Chelation Partners Incorporated | Metal chelating compositions and methods for controlling the growth or activities of a living cell or organism |
| US20130022706A1 (en) | 2011-07-20 | 2013-01-24 | Inco Digestive, Llc | Animal Feed Additive |
| US9655912B2 (en) * | 2012-02-16 | 2017-05-23 | Akeso Biomedical, Inc. | Reduction of gastrointestinal tract colonisation by campylobacter |
| BR112015029468A8 (pt) * | 2013-06-06 | 2020-03-17 | Amip Llc | sistemas de dosagem oralmente administráveis, método para suplementar a nutrição de ferro em um indivíduo humano e métodos para mitigar um ou mais efeitos adversos gastrointestinais de ferro não absorvido |
| AU2014342114B2 (en) | 2013-11-01 | 2019-06-20 | Irobot Corporation | Scanning range finder |
| US9961886B2 (en) * | 2014-08-13 | 2018-05-08 | Akeso Biomedical, Inc. | Antimicrobial compounds and compositions, and uses thereof |
| EP3334440B1 (en) * | 2015-08-11 | 2021-04-14 | Akeso Biomedical, Inc. | Biofilm inhibiting compositions enhancing weight gain in livestock |
| US10653658B2 (en) * | 2015-08-11 | 2020-05-19 | Akeso Biomedical, Inc. | Biofilm inhibiting compositions enhancing weight gain in livestock |
| CN109689035A (zh) | 2016-03-22 | 2019-04-26 | 巴尔化学公司 | 包含胆碱的组合物 |
-
2016
- 2016-08-11 EP EP16754616.7A patent/EP3334440B1/en active Active
- 2016-08-11 PL PL16754616T patent/PL3334440T3/pl unknown
- 2016-08-11 EP EP16754382.6A patent/EP3334439B1/en not_active Not-in-force
- 2016-08-11 ES ES16754616T patent/ES2880321T3/es active Active
- 2016-08-11 WO PCT/US2016/046623 patent/WO2017027742A1/en not_active Ceased
- 2016-08-11 WO PCT/US2016/046618 patent/WO2017027738A1/en not_active Ceased
- 2016-08-11 BR BR112018002045-1A patent/BR112018002045B1/pt active IP Right Grant
- 2016-08-11 US US15/234,937 patent/US9975914B2/en active Active
- 2016-08-11 US US15/234,941 patent/US10555531B2/en active Active
- 2016-08-11 DK DK16754616.7T patent/DK3334440T3/da active
- 2016-08-11 CA CA2995408A patent/CA2995408C/en active Active
- 2016-08-11 CN CN201680046742.5A patent/CN108024563A/zh active Pending
-
2017
- 2017-11-17 US US15/816,405 patent/US10106567B2/en active Active
-
2018
- 2018-05-16 US US15/981,794 patent/US10647736B2/en not_active Expired - Fee Related
- 2018-08-03 US US16/054,713 patent/US10377785B2/en not_active Expired - Fee Related
- 2018-09-12 US US16/129,611 patent/US10301339B2/en active Active
-
2019
- 2019-04-18 US US16/387,671 patent/US10793587B2/en active Active
-
2020
- 2020-10-02 US US17/062,180 patent/US20210017208A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| US10793587B2 (en) | 2020-10-06 |
| US20180094011A1 (en) | 2018-04-05 |
| EP3334440A1 (en) | 2018-06-20 |
| EP3334439A1 (en) | 2018-06-20 |
| US20170042848A1 (en) | 2017-02-16 |
| US20190241594A1 (en) | 2019-08-08 |
| PL3334440T3 (pl) | 2021-11-02 |
| US10555531B2 (en) | 2020-02-11 |
| EP3334439B1 (en) | 2021-10-13 |
| US10301339B2 (en) | 2019-05-28 |
| BR112018002045B1 (pt) | 2022-06-14 |
| US20180340003A1 (en) | 2018-11-29 |
| WO2017027742A1 (en) | 2017-02-16 |
| US20190010180A1 (en) | 2019-01-10 |
| US20180258120A1 (en) | 2018-09-13 |
| DK3334440T3 (en) | 2021-07-26 |
| EP3334440B1 (en) | 2021-04-14 |
| US20210017208A1 (en) | 2021-01-21 |
| US10377785B2 (en) | 2019-08-13 |
| US20170044197A1 (en) | 2017-02-16 |
| US10647736B2 (en) | 2020-05-12 |
| US10106567B2 (en) | 2018-10-23 |
| CN108024563A (zh) | 2018-05-11 |
| BR112018002045A2 (pt) | 2018-09-18 |
| CA2995408A1 (en) | 2017-02-16 |
| CA2995408C (en) | 2021-01-05 |
| US9975914B2 (en) | 2018-05-22 |
| WO2017027738A1 (en) | 2017-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2880321T3 (es) | Composiciones de inhibición de biopelícula que potencian el aumento de peso en el ganado | |
| ES2966909T3 (es) | Compuestos y composiciones antimicrobianos, y usos de los mismos | |
| US11311511B2 (en) | Biofilm inhibiting compositions enhancing weight gain in livestock | |
| RU2484818C2 (ru) | Лактилаты для предупреждения и лечения инфекций, вызванных грамположительными бактериями у животных | |
| BG107626A (bg) | Приложение на бензофенантридиналкалоиди като добавка за фураж и като лечебно средство против чревновъзпаление | |
| JP2011182748A (ja) | 家畜又は家禽用飼料 | |
| US20200296998A1 (en) | Feed compositions enhancing zootechnical performance in livestock | |
| RU2831747C1 (ru) | Способ повышения многоплодия и крупноплодности свиней | |
| NL2022942B1 (en) | Use of iron chelate to reduce gastrointestinal tract colonisation by campylobacter | |
| EP3735128A1 (en) | Biofilm inhibiting compositions enhancing weight gain in livestock | |
| JPH03264526A (ja) | 魚類連鎖球菌感染症の予防または治療剤 | |
| UA118224U (uk) | Спосіб зменшення технологічних втрат при вирощуванні поросят в підсисний період |