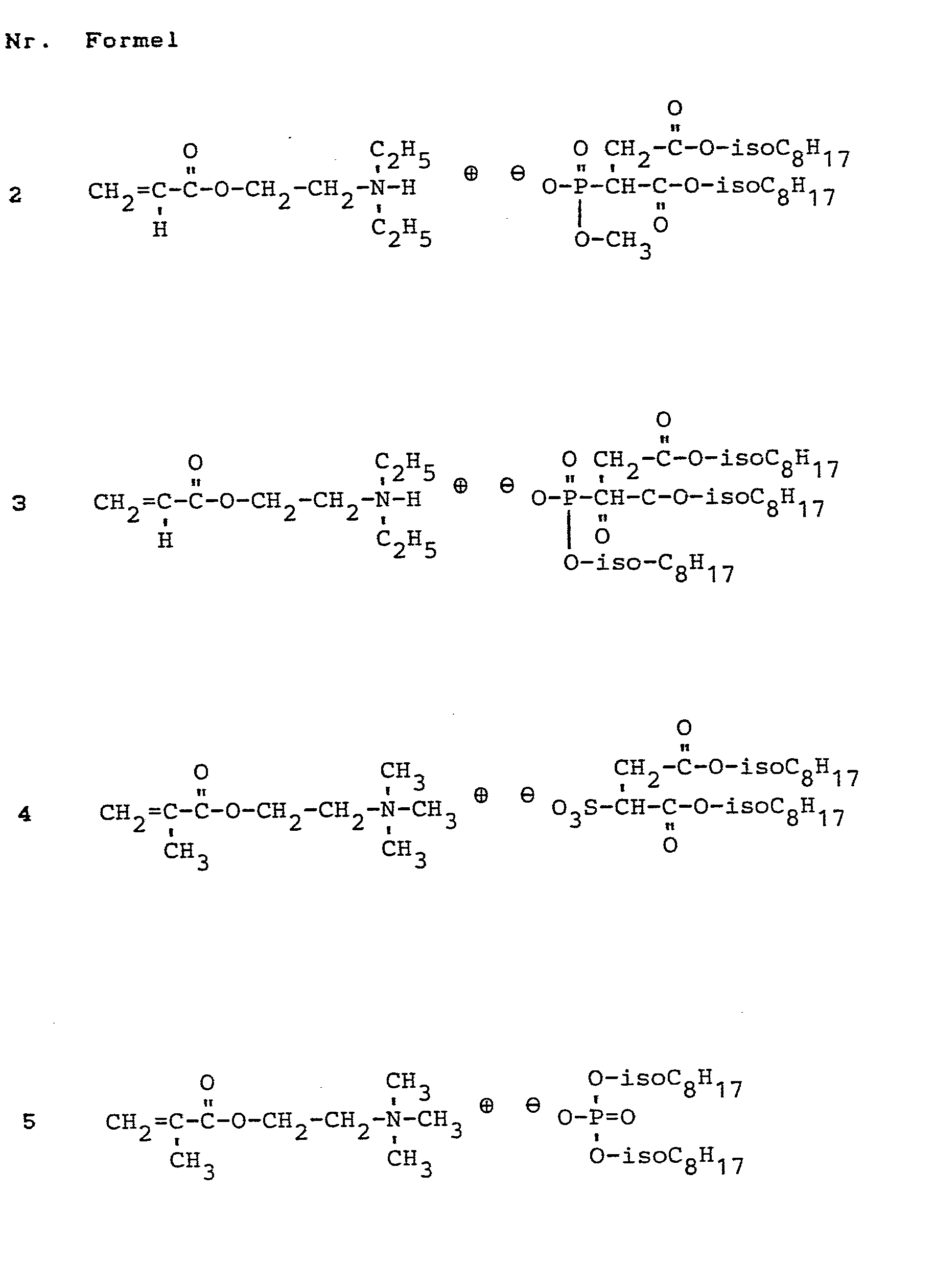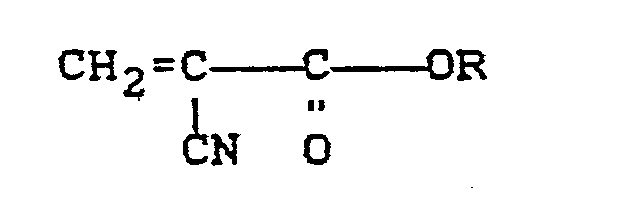EP0200067A2 - Elektrostatografischer Suspensionsentwickler und Verfahren zu dessen Herstellung - Google Patents
Elektrostatografischer Suspensionsentwickler und Verfahren zu dessen Herstellung Download PDFInfo
- Publication number
- EP0200067A2 EP0200067A2 EP86105087A EP86105087A EP0200067A2 EP 0200067 A2 EP0200067 A2 EP 0200067A2 EP 86105087 A EP86105087 A EP 86105087A EP 86105087 A EP86105087 A EP 86105087A EP 0200067 A2 EP0200067 A2 EP 0200067A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- pigment
- suspension developer
- cyanoacrylate
- developer according
- electrostatographic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03G—ELECTROGRAPHY; ELECTROPHOTOGRAPHY; MAGNETOGRAPHY
- G03G9/00—Developers
- G03G9/08—Developers with toner particles
- G03G9/12—Developers with toner particles in liquid developer mixtures
- G03G9/13—Developers with toner particles in liquid developer mixtures characterised by polymer components
- G03G9/131—Developers with toner particles in liquid developer mixtures characterised by polymer components obtained by reactions only involving carbon-to-carbon unsaturated bonds
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/29—Coated or structually defined flake, particle, cell, strand, strand portion, rod, filament, macroscopic fiber or mass thereof
- Y10T428/2982—Particulate matter [e.g., sphere, flake, etc.]
- Y10T428/2991—Coated
- Y10T428/2998—Coated including synthetic resin or polymer
Definitions
- the invention relates to an electrostatographic suspension developer, based on pigment particles coated with polycyanoacrylate, and to a method for producing the developer.
- Dry and wet development methods are known for developing electrostatic images on electrostatographic recording materials.
- the wet development processes are superior to the dry development processes with regard to edge sharpness and resolving power, especially in color copying processes.
- Suspension developers generally consist of a highly insulating carrier liquid, a pigment, a charge-determining substance (also called a control agent) and a polymer.
- the carrier liquid preferably has a volume resistance of at least 10 9 ohm.cm and a dielectric constant below 3.
- the pigments used are, for example, conventional azo dyes, xanthene dyes, Phthalocyanine dyes, as described, inter alia, in DE-A 29 44 021. Carbon black types are predominantly used as black pigments.
- the primary function of the polymer is to impart sufficient steric stabilization to the pigment dispersion and to ensure that the pigment particles adhere or are fixed to the image carrier.
- Numerous differently structured polymers can be used as components of electrostatographic suspension developers.
- the use of statistical copolymers which are composed of less polar monomers (for example C 6 -C 20 -alkyl (meth) acrylate) and more polar monomers (for example aminomethacrylates or vinylpyrrolidone) has been widely described (for example DE-A 19 27 592, DE-A 19 38 001, BE-A 784 367, JP-A 49 129 539 or JP-A 73 431 54).
- the use of styrene-butadiene copolymers is also possible (for example DE-A 23 37 419, DE-A 24 52 499 or JP-A 73 290 72).
- graft copolymers have also been used to build up suspension developers (for example DE-A 20 42 804, DE-A 21 03 045, DE-A 24 21 037, DE-A 25 32 281, DE-A 24 32 288, DE-A 29 35 287, GB-A 2 157 343, GB-A 2 029 049 or US-A 4033890.
- polymers contain ionic groups, these can play a role in the build-up of the toner charge generated by metal salts of organic acids with long aliphatic residues.
- carbon black pigments in liquid isoparaffin can be positively charged by organic phosphorus compounds (GB-A 1 151 141).
- a negative charge build-up is possible by adding basic metal alkyl sulfonates (GB-A 1 571 401).
- a disadvantage of the use of the known charge-determining substances in combination with conventional toner polymers is that the electrical properties of the liquid developers, such as conductivity and particle charge, are not stable when the concentration changes and are influenced to a large extent by water traces (e.g. atmospheric humidity). Furthermore, such liquid developers generally show a high electrical conductivity of the dispersion medium, which affects the electrophoretic deposition of the toner particles.
- the invention has for its object to provide an electrostatographic suspension developer with further improved positive toner charge, high charge stability and low conductivity of the dispersion medium.
- an electrostatographic suspension developer which contains a dispersed pigment in an electrically insulating carrier liquid with a volume resistance of at least 10 9 Ohm.cm and a dielectric constant below 3 and which is characterized in that the pigment is coated with polycyanoacrylate .
- Another object of the invention is a method for producing an electrostatographic suspension developer, which is characterized in that a dispersed basic or neutral pigment is coated in a non-polar carrier liquid with polycyanoacrylate by anionic polymerization.
- hydrocarbons As a carrier liquid with a volume resistance of min. least 10 9 Ohm.cm and a dielectric constant below 3 can hydrocarbons. Fluorocarbons or silicone oils are used; preference is given to hydrocarbon-based liquids, for example aromatic hydrocarbons such as benzene, toluene or xylenes or aliphatic C 6 -C 15 -hydrocarbons. like n-hexane. Cyclohexane. n-heptane, n-octane or decalin. Mixtures of different hydrocarbons can also be used. Branched aliphatic hydrocarbons such as isodecane and isododecane are particularly suitable.
- the black and color pigments usually used for suspension developers are suitable as pigments. if they have neutral or basic surfaces.
- the suitability of a pigment can be determined in a simple manner by measuring the pH with the aid of a glass electrode in a pigment-water suspension. This method is described in detail in DIN 53 200, for example.
- Suitable pigments have pH values of 6-12, preferably 7-11. It is possible in many cases. by a preferably alkaline pretreatment of the Pi g- mentes to affect the pH value, ie, to adjust the desired pH.
- the water content of the pigments is also important for their use according to the invention.
- pigments with a low water content preferably with a water content of less than 1, particularly preferably less than 0.10%, of water are used.
- Black pigments are primarily soot types. Carbon black with a primary particle size of 20-80 nm, a BET surface area of 20-150 m 2 / g and a pH value of 8-10 is preferred. Color pigments suitable without pretreatment are CI No. 74160, CI No. 45160 and CI No. 21100.
- Cyanoacrylates of the following general formula are preferably used to coat the pigments: in the R is alkyl, in particular having 1 to 10 carbon atoms, cycloalkyl, in particular cyclohexyl, alkenyl, in particular allyl, aryl, in particular phenyl and aralkyl, in particular benzyl.
- substituents mentioned can in turn be substituted with substituents customary in the field of polycyanoacrylates, e.g. Alkoxy groups, especially methoxy and ethoxy.
- substituents customary in the field of polycyanoacrylates e.g. Alkoxy groups, especially methoxy and ethoxy.
- Different cyanoacrylates can also be used at the same time to form appropriate copolymers.
- cyanoacrylates are ethyl, methyl, butyl, isobutyl, amyl and lauryl cyanoacrylate as well as methoxyethyl cyanoacrylate and ethoxyethyl cyanoacrylate, the isobutyl cyanoacrylate being particularly suitable.
- Special. Mixtures containing 5-50% by weight of allyl cyanoacrylate are particularly favorable.
- the amount of polycyanoacrylate is 2.5-350% by weight, preferably 10-250% by weight, based on the amount of pigment.
- the pigment is coated with an additional shell made from a copolymer of A) cationic monomers and B) free-radically polymerizable, olefinically unsaturated compounds.
- the copolymer generally acts as a charge-determining substance, i.e. it effects or increases the positive electrostatic charge of the coated pigment particles.
- the copolymer contains 0.1 to 80, preferably 0.5 to 50 and particularly preferably 2 to 20% by weight of polymerized cationic monomers (A).
- the cationic monomers contain onium groups, preferably ammonium, phosphonium or sulfonium groups; the negative counterions are derived from CH-acidic or sulfur or phosphorus-containing acidic compounds with at least one hydrocarbon radical having 6 to 24 carbon atoms.
- hydrocarbon radicals mentioned can be linear or branched alkyl, aryl, arylalkyl or alkylaryl radicals, which can optionally be substituted.
- the cationic monomers described above can be used directly to produce the additional copolymer shell. However, it is also possible first to prepare a copolymer with the basic monomers on which the cation part is based and then to introduce the positive charge by protonation or quaternization with, if appropriate, subsequent anion exchange.
- Suitable comonomers (B) are in principle all free-radically polymerizable, olefinically unsaturated compounds, in particular the known vinyl and vinylidene compounds.
- examples include: (meth) acrylic acid and its derivatives such as (meth) acrylic esters with C 1 to C 24 hydrocarbon radicals in the alcohol part, (meth) acrylic acid amide, (meth) acrylonitrile, vinyl esters such as vinyl acetate, vinyl propionate, vinyl aromatics such as Styrene or methyl styrene, also dienes such as butadiene and isoprene and halogen-containing monomers such as vinyl chloride and vinylidene chloride.
- Preferred comonomers are (meth) acrylic acid esters with at least one C 1 to G 24 hydrocarbon radical in the alcohol part and styrene. Mixtures of different monomers are also suitable. Good installation rates who which is achieved especially when at least some (meth) acrylic acid esters are used as comonomers. Copolymers which are not crosslinked or crosslinked by using polyfunctional monomers such as, for example, ethylene dimethacrylate or divinylbenzene can be built up.
- the copolymer not only charges the dispersed pigment coated with polycyanoacrylate, but also increases the dispersion stability of the pigment dispersion by steric shielding.
- Comonomers which improve the dispersant properties of the copolymer are, for example, vinyl or vinylidene monomers with a C 6 to C 24 hydrocarbon radical, in particular (meth) acrylic acid ester with C 6 to C 24 hydrocarbon radicals in the alcohol part, for example stearyl methacrylate, lauryl methacrylate or 2 -Ethylhexyl methacrylate, these comonomers preferably being used in amounts of 10 to 70% by weight (based on the copolymer). In this case it is advantageous to combine the comonomers mentioned here with those with C 1 to C 5 hydrocarbon radicals.
- the basic or neutral pigment is dispersed in a non-polar solvent.
- the solvents described above as the carrier liquid are particularly suitable as solvents.
- the solvents are dried well before use.
- the pigment concentration should preferably be 0.1 to 40% by weight. It is advisable to use a dispersing agent in the preparation of the dispersion.
- Soluble, high molecular weight compounds such as homopolymers or copolymers of (meth) acrylic acid esters, for example a 1: 1 copolymer of isobutyl methacrylate and lauryl methacrylate, can be used as dispersants.
- Particularly suitable dispersing aids are block copolymers, e.g. Styrene-stearyl methacrylate block copolymers or mercaptan-modified styrene-butadiene block copolymers (DE-A 34 12 085).
- the pigment is coated by adding the monomeric cyanoacrylates, preferably in the form of a feed process, for example over a period of 10 to 120 minutes.
- the anionic polymerization takes place under the catalytic action of the pigment and leads to high polymer conversions in short reaction times, generally from more than 70%, the polymer formed is formed in the form of a shell on the pigment surface.
- the polymerization temperature is not critical per se, the temperature range from 0 to 80 ° C. is preferred for practical reasons.
- the known control agents can be used to regulate the electrical charge of the pigment particles coated with polycyanoacrylate.
- These are e.g. Oil-soluble ionic compounds such as metal salts of long-chain organic acids.
- Mixtures of different control agents e.g. a mixture of different control agents with opposite charge effects can be used so that the strength of the charge on the toner or its polarity can be adjusted by changing the mixing ratio of the two control agents (GB-PS 1 411 287, 1 411 537 and 1 411 739).
- Particularly suitable, positive working control materials are described in GB-PS 1 151 141.
- These control substances are divalent or trivalent metal salts of an oxyacid derived from phosphorus and containing an organic radical.
- the positive charge of the pigment particles is generated or enhanced by applying an additional shell made of a copolymer of the cationic monomers A and comonomers B described above.
- This additional polymer shell is applied by a radical polymerization process in which the dispersion of the pigment coated with polycyanoacrylate with the monomer A or the basic monomer on which the cationic monomer A is based and comonomers B as well as a radical generator is added as starting component and the polymerization at a temperature of preferably 50 to 120 C is passed up to conversions of at least 70% *.
- the known per-compounds and preferably azo compounds can be used as radical formers.
- the monomers and radical formers are metered in, preferably by a feed process.
- the dispersion obtained by the present process can be diluted to the desired working concentration, for example to 0.01% to 1%, by adding further solvent as carrier liquid. On this occasion, if this should be desired, the solvent present can be replaced by another carrier liquid, for example by centrifugation and then redispersion.
- other polymeric additives can be used to prepare the suspension developer according to the invention, for example to increase the dispersion stability or to improve the adhesive and fixing properties of the dispersed pigment.
- the above-mentioned dispersing aids based on soluble high-molecular compounds are primarily suitable for increasing the dispersion stability.
- Resins which are compatible with the binder of the recording material are suitable as fixing substances. so that good adhesion of the generated image to the substrate is obtained after development.
- suitable resins are esters of hydrogenated rosin and long-oil oil, "rosin-modified phenol-formaldehyde resin, pentaerythritol esters of rosin, glycerol esters of hydrogenated rosin, ethyl cellulose, various alkyd resins, polyacrylic and polymethacrylic resin, polystyrene, poly (vinyl acetate).
- Specific examples of such resins can be found in the literature on electrostatographic suspension developers, e.g. in BE-PS 699 157 and in GB-A 1 151 141.
- the suspension developer showed very good storage stability.
- the particle size and conductivity were unchanged after 6 months of storage.
- Example 1 B 100 g of the pigment dispersion from Example 1 B are transferred to a stirred reactor with exclusion of moisture. With effective stirring, a solution of 36 g of isobutyl cyanoacrylate, 4 g of allyl cyanoacrylate and 50 g of isododecane is added dropwise within 30 minutes. Subsequently, the temperature to 80 * C is increased, and in 400 mg azobisisobutyronitrile was added. A solution of 10 g of N, N-dimethylaminoethyl methacrylate, 5 g of styrene, 5 g of butyl acrylate, 40 g of toluene and 40 g of isododecane is added while flushing with nitrogen.
- PTDCCP pentaisotridecyloxycarbonylcyclopentadiene
- Suspension developers A, B and C have a positive toner charge. They show excellent developer properties. Conductivity and particle size do not change during storage.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Liquid Developers In Electrophotography (AREA)
Abstract
Description
- Die Erfindung betrifft einen elektrostatografischen Suspensionsentwickler, auf der Basis von mit Polycyanacrylat umhüllten Pigmentteilchen, sowie ein Verfahren zur Herstellung des Entwicklers.
- Zum Entwickeln von elektrostatischen Bildern auf elektrostatografischen Aufzeichnungsmaterialien sind Trocken- und Naßentwicklungsverfahren bekannt. Dabei sind die Naßentwicklungsverfahren den Trockenentwicklungsverfahren hinsichtlich Randschärfe und Auflösungsvermögen, insbesondere bei Farbkopieverfahren, überlegen.
- Suspensionsentwickler bestehen im allgemeinen aus einer hochisolierenden Trägerflüssigkeit, einem Pigment, einer ladungsbestimmenden Substanz (auch Steuerstoff genannt) und einem Polymer. Die Trägerflüssigkeit besitzt vorzugsweise einen Volumenwiderstand von mindestens 109 Ohm.cm und eine Dielektrizitätskonstante unter 3. Als Pigmente werden z.B. übliche Azofarbstoffe, Xanthenfarbstoffe, Phthalocyaninfarbstoffe, wie sie u.a. in der DE-A 29 44 021 beschrieben werden. Als Schwarzpigmente werden überwiegend Rußtypen eingesetzt.
- Das Polymer hat in erster Linie die Aufgabe, der Pigmentdispersion eine ausreichende sterische Stabilisierung zu verleihen und eine Haftung bzw. Fixierung der Pigmentteil- chen am Bildträger zu gewährleisten.
- Zahlreiche unterschiedlich aufgebaute Polymere können als Komponente von elektrostatografischen Suspensionsentwicklern verwendet werden. So ist die Verwendung von statistischen Copolymerisaten, die aus weniger polaren Monomeren (z.B. C6-C20-Alkyl(meth)-acrylat) und stärker polaren Monomeren (z.B. Aminomethacrylate oder Vinylpyrrolidon) aufgebaut sind, vielfach beschrieben worden (z.B. DE-A 19 27 592, DE-A 19 38 001, BE-A 784 367, JP-A 49 129 539 oder JP-A 73 431 54). Die Anwendung von Styrol-Butadien-Copolymerisaten ist ebenso möglich (z.B. DE-A 23 37 419, DE-A 24 52 499 oder JP-A 73 290 72).
- Auch verschiedenartige Pfropfcopolymerisate sind zum Aufbau von Suspensionsentwicklern verwendet worden (z.B. DE-A 20 42 804, DE-A 21 03 045, DE-A 24 21 037, DE-A 25 32 281, DE-A 24 32 288, DE-A 29 35 287, GB-A 2 157 343, GB-A 2 029 049 oder US-A 4033890.
- Sofern die Polymeren ionische Gruppen enthalten, können diese eine Rolle beim Aufbau der Tonerladung spielen, In allgemeinen wird die Ladung der Tonerteilche, jedoch durch öllösliche ionogene Verbindungen (Steuerstoffd), z.B. durch Metallsalze von organischen Säuren mit langen aliphatischen Resten erzeugt. So können beispielsweise Ruß- pigmente in flüssigem Isoparaffin durch organische Phosphorverbindungen (GB-A 1 151 141) positiv geladen werden. Ein negativer Ladungsaufbau ist durch Zusatz von basischen Metallalkylsulfonaten möglich (GB-A 1 571 401).
- Nachteilig bei der Verwendung der bekannten ladungsbestimmenden Substanzen in Kombination mit üblichen Tonerpolymeren ist, daß die elektrischen Eigenschaften der Flüssigentwickler, wie Leitfähigkeit und Teilchenladung bei Konzentrationsänderungen nicht stabil sind und in hohem Maße von Wasserspuren (z.B. Luftfeuchtigkeit) beeinflußt werden. Weiterhin zeigen derartige Flüssigentwickler im allgemeinen eine hohe elektrische Leitfähigkeit des Dispersionsmediums, wodurch die elektrophoretische Abscheidung der Tonerteilchen beeinträchtigt wird.
- Aus der DE-OS 3 232 062 und der darin zitierten Literatur ist bekannt, die Pigmentteilchen eines Suspensionsentwicklers durch den Aufbau einer vernetzten PolymerhUlle mittels Fällungspolymerisation sterisch zu stabilisieren. Hierdurch wird schon eine erhebliche Verbesserung der Ladungsstabilität erhalten.
- Der Erfindung liegt die Aufgabe zugrunde, einen elektrostatografischen Suspensionsentwickler mit weiter verbesserter positiver Tonerladung, hoher Ladungsstabilität und geringer Leitfähigkeit des Dispersionsmediums bereitzustellen.
- Die Aufgabe wird erfindungsgemäß durch die Bereitstellung eines elektrostatografischen Suspensionsentwicklers gelöst, der in einer elektrisch isolierenden Trägerflüssigkeit mit einem Volumenwiderstand von mindestens 109 Ohm.cm und einer Dielektrizitätskonstante unter 3 ein dispergiertes Pigment enthält und der dadurch gekennzeichnet ist, daß das Pigment mit Polycyanacrylat beschichtet ist.
- In einer bevorzugten Ausführungsform enthält der Suspensionsentwickler ein Pigment mit einer inneren Hülle aus Polycyanacrylat und einer zusätzlichen Hülle aus einem Copolymerisat aus
- A. kationischen Monomeren, die Ammonium-, Phosphonium-oder Sulfoniumgruppen enthalten und deren Anionen sich von CH-aziden oder Schwefel oder Phosphor enthaltenden aziden Verbindungen mit mindestens einem Kohlenwasserstoffrest mit 6 bis 24 Kohlenstoffatomen ableiten, und
- B. radikalisch polymerisierbaren, olefinisch ungesättigten Verbindungen als Comonomere.
- Ein weiterer Gegenstand der Erfindung ist ein Verfahren zur Herstellung eines elektrostatografischen Suspensionsentwicklers, das dadurch gekennzeichnet ist, daß ein dispergiertes basisches oder neutrales Pigment in einer unpolaren Trägerflüssigkeit mit Polycyanacrylat durch anionische Polymerisation beschichtet wird.
- Als Trägerflüssigkeit mit einem Volumenwiderstand von min- . destens 109 Ohm.cm und einer Dielektrizitätskonstanten unter 3 können Kohlenwasserstoffe. Fluorkohlenwasserstoffe oder Silikonöle eingesetzt werden, bevorzugt werden Flüssigkeiten auf Kohlenwasserstoffbasis beispielsweise aromatische Kohlenwasserstoffe wie Benzol, Toluol oder Xylole oder aliphatische C6-C15-Kohlenwasserstoffe. wie n-Hexan. Cyclohexan. n-Heptan, n-Oktan oder Dekalin. Auch Mischungen unterschiedlicher Kohlenwasserstoffe können verwendet werden. Besonders geeignet sind verzweigte aliphatische Kohlenwasserstoffe wie Isodecan und Isododecan.
- Als Pigmente eignen sich die üblicherweise für Suspensionsentwickler eingesetzten Schwarz- und Farbpigmente. sofern sie neutrale oder basische Oberflächen aufweisen. Die Eignung eines Pigmentes läßt sich in einfacher Weise durch Messung des pH-Wertes mit Hilfe einer Glaselektrode in einer Pigment-Wasser-Suspension bestimmen. Diese Methode wird beispielsweise in der DIN 53 200 detailliert beschrieben. Geeignete Pigmente zeigen pH-Werte von 6 - 12, vorzugsweise 7 - 11. Es ist in vielen Fällen möglich. durch eine vorzugsweise alkalische Vorbehandlung des Pig- mentes den pH-Wert zu beeinflussen, d.h. den gewünschten pH-Wert einzustellen.
- Auch der Wassergehalt der Pigmente ist für ihren erfindungsgemäßen Einsatz von Bedeutung. Im allgemeinen werden Pigmente mit niedrigem Wassergehalt, vorzugsweise mit einem Wassergehalt von weniger als 1, besonders bevorzugt weniger als 0,10 % Wasser eingesetzt.
- Gut geeignete Schwarzpigmente sind in erster Linie basi- sche Rußtypen. Bevorzugt wird Ruß mit einer Primärteil- chengröße von 20 - 80 nm, einer BET-Oberfläche von 20 - 150 m2/g und einem pH-Wert von 8 - 10. Als Farbpigmente eignen sich ohne Vorbehandlung C.I. Nr. 74160, C.I. Nr. 45160 und C.I. Nr. 21100.
-
- Die genannten Substituenten können ihrerseits mit auf dem Gebiet der Polycyanacrylate üblichen Substituenten z.B. Alkoxygruppen, insbesondere Methoxy und Ethoxy substituiert sein. Es können gleichzeitig auch unterschiedliche Cyanacrylate unter Bildung entsprechender Copolymerer verwendet werden.
- Bevorzugte Beispiele für Cyanacrylate sind Ethyl-, Methyl-, Butyl-, Isobutyl-, Amyl- und Laurylcyanacrylat sowie Methoxyethylcyanacrylat und Ethoxyethylcyanacrylat, wobei das Isobutylcyanacrylat besonders geeignet ist. Gut geeignet ist auch Allylcyanacrylat, welches für sich allein oder in vorteilhafer Weise im Gemisch mit den obengenannten Alkylcyanacrylaten verwendet werden kann. Beson-. ders günstig sind Mischungen mit einem Gehalt an 5 - 50 Gew.-% Allylcyanacrylat. Die Menge an Polycyanacrylat beträgt 2,5 - 350 Gew.-%, vorzugsweise 10 - 250 Gew.-%, bezogen auf die Pigmentmenge.
- In einer besonderen Ausführungsform ist das Pigment mit einer zusätzlichen Hülle aus einem Copolymerisat aus A) kationischen Monomeren und B) radikalisch polymerisierbaren, olefinisch ungesättigten Verbindungen beschichtet. Das Copolymerisat wirkt dabei im allgemeinen als ladungsbestimmende Substanz, d.h. es bewirkt oder verstärkt die positive elektrostatische Aufladung der beschichteten Pigmentteilchen. Das Copolymerisat enthält 0,1 bis 80, vorzugsweise 0,5 bis 50 und besonders bevorzugt 2 bis 20 Gew.-% polymerisierte kationische Monomere (A).
- Die kationischen Monomeren enthalten Oniumgruppen, vorzugsweise Ammonium-, Phosphonium- oder Sulfoniumgruppen; die negativen Gegenionen leiten sich von CH-aziden oder Schwefel oder Phosphor enthaltenden aziden Verbindungen mit mindestens einem Kohlenwasserstoffrest mit 6 bis 24 Kohlenstoffatomen ab.
-
- R1 = ein Wasserstoffatom oder eine CH3-Gruppe,
- R2 = ein Kohlenwasserstoffrest mit 1 bis 18 Kohlenstoffatomen,
- R3 und R4 = gleich oder verschieden und ein Kohlenwasserstoffrest mit 1 bis 18 Kohlenstoffatomen, oder die Reste R3 und R4 bilden zusammen einen 5- oder 6-gliedrigen Ring,
- R5 = ein Wasserstoffatom oder ein Kohlenwasserstoffrest mit 1 bis 18 Kohlenstofftomen,
- X = eine der Gruppen
- Die genannten Kohlenwasserstoffreste können lineare oder verzweigte Alkyl-, Aryl-, Arylalkyl- oder Alkylarylreste sein, die gegebenenfalls substituiert sein können.
-
- R6 ein Kohlenwasserstoffrest mit 6 bis 24 Kohlenstoff- atomen und
- R7 ein Kohlenwasserstoffrest mit 1 bis 18 Kohlenwasserstoffatomen
-
- R8 für eine der Gruppen -COOR6 oder -SO2R6 steht, wobei R6 einen Kohlenwasserstoffrest mit 6 bis 24 C-Atomen bedeutet,
- R9 und R10 gleich oder verschieden sind und -CN, -NO2, Halogen, -COOR7 oder -SO2R7 bedeutet, und R7 ein Kohlenwasserstoffrest mit 1 bis 18 Kohlenstoffatomen ist.
- R11 für einen Kohlenwasserstoffrest mit 6 bis 24 Kohlenstoffatomen oder -COOR6.
- R12 für eine der Gruppen -CN oder -COOR7 steht und
- R13. R14. R15 gleich oder verschieden sind und ein Wasserstoffatom, die Gruppen -CN, -R7 oder -COOR7 bedeuten.
-
- Zur Herstellung der zusätzlichen Copolymerisathülle können die oben beschriebenen kationischen Monomere direkt verwendet werden. Es ist jedoch auch möglich, zunächst ein Copolymerisat mit den dem Kationenteil zugrundeliegenden basischen Monomeren herzustellen und anschließend die positive Ladung durch Protonierung oder Quarternierung mit gegebenenfalls anschließendem Anionenaustausch einzuführen.
- Als Comonomere (B) eignen sich prinzipiell alle radikalisch polymerisierbaren, olefinisch ungesättigten Verbindungen, insbesondere die bekannten Vinyl- und Vinylidenverbindungen. Beispielhaft seien aufgeführt: (Meth)acrylsäure und ihre Derivate wie z.B. (Meth)-acrylsäureester mit C1- bis C24-Kohlenwasserstoffresten im Alkoholteil, (Meth)-acrylsäureamid, (Meth)-Acrylnitril, Vinylester wie Vinylacetat, Vinylpropionat, Vinylaromaten wie Styrol oder «-Methylstyrol, ferner Diene wie Butadien und Isopren sowie halogenhaltige Monomere, wie Vinylchlorid und Vinylidenchlorid. Bevorzugte Comonomere sind (Meth)-acrylsäureester mit mindestens einem C1- bis G24-Kohlenwasserstoffrest im Alkoholteil und Styrol. Gut geeignet sind auch Mischungen verschiedener Monomere. Gute Einbauraten werden vor allem dann erzielt, wenn zumindest anteilmäßig (Meth)-acry1säureester als Comonomere verwendet werden. Es können sowohl unvernetzte als auch durch Verwendung von mehrfunktionellen Monomeren wie z.B. Ethylendimethacrylat oder Divinylbenzol vernetzte Copolymerisate aufgebaut werden.
- Es ist möglich, durch die Auswahl der Comonomeren (B) dem Copolymerisat verbesserte Dispergatoreigenschaften zu verleihen. In diesem Falle bewirkt das Copolymerisat nicht nur eine Aufladung des dispergierten, mit Polycyanacrylat beschichteten Pigmentes, sondern erhöht auch die Dispersionsstabilität der Pigmentdispersion durch sterische Abschirmung. Comonomere, die die Dispergatoreigenschaften des Copolymerisates verbessern, sind beispielsweise Vinyl-oder Vinylidenmonomere mit einem C6- bis C24-Kohlenwasserstoffrest, insbesondere (Meth)-acrylsäureester mit C6- bis C24-Kohlenwasserstoffresten im Alkoholteil, z.B. Stearylmethacrylat, Laurylmethacrylat oder 2-Ethylhexylmethacrylat, wobei diese Comonomere vorzugsweise in Mengen von 10 bis 70 Gew.-% (bezogen auf Copolymerisat) eingesetzt werden. Es ist in diesem Falle von Vorteil, die hier genannten Comonomeren mit solchen mit C1- bis C5-Kohlenwasserstoffresten zu kombinieren.
- Verbesserte Dispergatoreigenschaften des Comonomeren sind jedoch nicht kennzeichnend für die vorliegende Erfindung. Es ist durchaus möglich, die Dispersionsstabilität, wie weiter unten ausgeführt wird, durch weitere polymere Zusätze einzustellen.
- Zur Herstellung des erfindungsgemäßen Suspensionsentwicklers wird das basische oder neutrale Pigment in einem unpolaren Lösungsmittel dispergiert. Als Lösungsmittel eignen sich besonders gut die oben als Trägerflüssigkeit beschriebenen Substanzen. Die Lösungsmittel werden vor dem Einsatz gut getrocknet. Die Pigmentkonzentration soll vorzugsweise 0,1 bis 40 Gew.-% betragen. Es ist zweckmäßig bei der Zubereitung der Dispersion ein Dispergierhilfsmittel einzusetzen.
- Als Dispergierhilfsmittel können dabei lösliche, hochmolekulare Verbindungen, wie Homo- oder Mischpolymerisate aus (Meth)-acrylsäureestern, beispielsweise ein 1:1-Mischpolymerisat aus Isobutylmethacrylat und Laurylmethacrylat eingesetzt werden. Gut geeignet sind auch Mischpolymerisate mit einem Anteil von 0,1 - 15 Gew.-X an einpolymerisierten Monomeren mit OH-Gruppen, wie z.B. 2-Hydroxyethylmethacrylat.
- Besonders gut geeignete Dispergierhilfsmittel sind Blockcopolymerisate, wie z.B. Styrol-Stearylmethacrylat-Blockcopolymerisate oder mercaptanmodifizierte Styrol-Butadien-Blockcopolymere (DE-A 34 12 085).
- Die Beschichtung des Pigmentes erfolgt durch Zugabe der monomeren Cyanacrylate, vorzugsweise in Form eines Zulaufverfahrens, beispielsweise über einen Zeitraum von 10 bis 120 Min. Die anionische Polymerisation findet unter der katalytischen Wirkung des Pigmentes statt und führt in kurzen Reaktionszeiten zu hohen Polymerumsätzen, im allgemeinen von mehr als 70 %, wobei das gebildete Polymerisat in Form einer Hülle auf der Pigmentoberfläche gebildet wird. Die Polymerisationstemperatur ist an sich nicht kritisch, der Temperaturbereich von 0 - 80*C wird aus praktischen Gründen bevorzugt.
- Zur Regulierung der elektrischen Ladung der mit Polycyanacrylat umhüllten Pigmentteilchen, können die bekannten Steuerstoffe verwendet werden. Dies sind z.B. öllösliche ionogene Verbindungen wie etwa Metallsalze langkettiger organischer Säuren. Es können auch Gemische von verschiedenen Steuerstoffen, z.B. ein Gemisch von verschiedenen Steuerstoffen mit entgegengesetzten Ladungseffekten verwendet werden, so daß die Stärke der Ladung auf dem Toner oder deren Polarität durch Änderung des Mischungsverhältnisses der beiden Steuerstoffe eingestellt werden kann (GB-PS 1 411 287, 1 411 537 und 1 411 739). Besonders geeignete, positiv arbeitende Steuerstoffe werden in der GB-PS 1 151 141 beschrieben. Diese Steuerstoffe sind zwei-oder dreiwertige Metallsalze einer von Phosphor abgeleiteten, einen organischen Rest enthaltenden Oxysäure.
- In einer bevorzugten Ausführungsform der vorliegenden Erfindung wird die positive Aufladung der Pigmentteilchen durch das Aufbringen einer zusätzlichen Hülle aus einem Copolymerisat aus den oben beschriebenen kationischen Monomeren A und Comonomeren B erzeugt oder verstärkt. Das Aufbringen dieser zusätzlichen Polymerhülle erfolgt durch ein radikalisches Polymerisationsverfahren, bei dem die Dispersion des mit Polycyanacrylat umhüllten Pigmentes mit dem Monomeren A, bzw. dem basischen Monomeren, das dem kationischen Monomeren A zugrundeliegt, und Comonomeren B sowie einem Radikalbildner als Startkomponente versetzt wird und die Polymerisation bei einer Temperatur von vorzugsweise 50 - 120*C bis zu Umsätzen von mindestens 70 % geführt wird.
- Als Radikalbildner können die bekannten Perverbindungen und vorzugsweise Azoverbindungen angewendet werden. Die Dosierung der Monomeren und Radikalbildner erfolgt, vorzugsweise nach einem Zulaufverfahren.
- Die umhüllten Pigmentteilchen besitzen eine mittlere Teilchengröße von 0,1 bis 2 um. Die nach dem vorliegenden Verfahren erhaltene Dispersion kann durch Zugabe von weiterem Lösungsmittel als Trägerflüssigkeit auf die gewünschte Arbeitskonzentration, beispielsweise auf 0,01 % bis 1 % verdünnt werden. Bei dieser Gelegenheit kann, falls dies erwünscht sein sollte, vorliegendes Lösungsmittel beispielsweise durch Zentrifugieren und anschließendem Redispergieren durch eine andere Trägerflüssigkeit ausgetauscht werden. Neben Polycyanacrylat und dem beschriebenen Copolymerisat aus den Monomeren A und B können zur Herstellung des erfindungsgemäßen Suspensionsentwicklers weitere polymere Zusätze angewendet werden, beispielsweise um die Dispersionsstabilität zu erhöhen oder die Haft- und Fixiereigenschaften des dispergierten Pigmentes zu verbessern.
- Für die Erhöhung der Dispersionsstabilität eignen sich in erster Linie die weiter oben angeführten Dispergierhilfsmittel auf Basis löslicher hochmolekularer Verbindungen.
- Als fixierende Substanzen eignen sich Harze, die mit dem Bindemittel des Aufzeichnungsmaterials verträglich sind. damit nach der Entwicklung eine gute Haftung des erzeugten Bildes auf der Unterlage erhalten wird. Beispiele für geeignete Harze sind Ester von hydrogeniertem Kolophonium und fettem Öllack ("long-oil"), kolophoniummodifiziertes Phenol-Formaldehydharz, Pentaerythritolester von Kolophonium, Glycerinester von hydrogeniertem Kolophonium, Ethylcellulose, verschiedene Alkydharze, Polyacryl- und Polymethacrylharz, Polystyrol, Polyketonharz und Polyvinylacetat. Spezifische Beispiele solcher Harze sind in der Literatur über elektrostatografische Suspensionsentwickler zu finden, z.B. in der BE-PS 699 157 und in der GB-A 1 151 141.
- Mit den folgenden Beispielen wird die Herstellung erfindungsgemäßer Suspensionsentwickler im einzelnen erläutert:
- In einem 2-Liter Glasautoklaven werden unter Ausschluß von Wasser und Sauerstoff 1000 ml Cyclohexan, 5 ml Glykoldimethylether und 50 g Styrol vorgelegt. Die Mischung wird mit einer 1 molaren n-Butyllithiumlösung in n-Hexan vorsichtig bis zur schwachen Gelbfärbung titriert. Dann gibt man 3 ml der 1 molaren Butyllithiumlösung zu. Durch Außenkühlung wird die Polymerisationstemperatur bei 40°C gehalten. Nach einer Reaktionszeit von 60 Minuten gibt man 50 g Butadien zu und polymerisiert bei 50°C für 60 Minuten. Danach ist der Umsatz vollständig. Man gibt 48 ml n-Dodecylmercaptan und 0,5 g Azodiisobutyronitril zu und erwärmt 5 Stunden lang auf 80°C. Nach Abkühlen auf Raumtemperatur wird das Blockcopolymerisat mit 2000 ml Ethanol, dem 2 g 2,6-Ditertiär-butyl-p-methylphenol zugesetzt wurden, aus der Cyclohexanlösung ausgefällt und im Vakuum bis zu Gewichtskonstanz getrocknet. Man erhält 140 g eines farblosen Blockcopolymerisats. []= 0,272 dllg, Toluol, 25°C; 4,5 Gew.-% Schwefel im Polymerisat.
- 40 g Rußpigment mit einer Teilchengröße von 50 nm, einer BET-Oberfläche von 30 m2/g und einem pH-Wert nach DIN 53 200 von 8,5 werden unter Feuchtigkeitsausschluß zusammen mit 8 g Dispergierhilfsmittel aus A und 152 g getrocknetem Isododecan 16 Stunden lang in einer Stahlkugelmühle gemischt, wobei eine stabile Dispersion gebildet wird.
- Je 100 g der Dispersion aus B werden unter Feuchtigkeitsausschluß in einen Rührreaktor überführt. Unter Rühren werden bei Raumtemperatur 10, 20 und 40 g Isobutylcyanacrylat über einen Zeitraum von 30 Min. zugetropft. Nach beendeter Zugabe wird 2 Stdn. lang nachgerührt. Zu analytischen Zwecken wird umhülltes Pigment durch Zentrifugieren isoliert und durch Waschen mit Isododecan gereinigt. Der Umsetzungsgrad wird durch N-Analyse bestimmt.
- Nach dem Verdünnen der Dispersion aus 4 Gew.-% Feststoffgehalt wurden 5 mg Zink-mono-(2-butyl)-octylphosphat pro Gramm Feststoff zugegeben.
- Der Suspensionsentwickler zeigte eine sehr gute Lagerstabilität. Die Teilchengröße und die Leitfähigkeit waren nach 6-monatiger Lagerung unverändert.
- 100 g der Pigmentdispersion aus Beispiel 1 B werden unter Feuchtigkeitsausschluß in einen Rührreaktor überführt. Unter wirksamem Rühren wird bei Raumtemperatur eine Lösung aus 36 g Isobutylcyanacrylat, 4 g Allylcyanacrylat und 50 g Isododecan innerhalb von 30 Min. zugetropft. Anschließend wird die Temperatur auf 80*C erhöht und in 400 mg Azoisobuttersäuredinitril zugesetzt. Unter Stickstoffspülung wird eine Lösung aus 10 g N,N-Dimethylaminoethylmethacrylat, 5 g Styrol, 5 g Butylacrylat, 40 g Toluol und 40 g Isododecan zudosiert. Nach dem Zutropfen werden 2 Stunden bei 80°C und 2 weitere Stunden bei 90°C nachgerührt. Der Feststof wird durch Zentrifugieren (30 Min./2000 UpM) isoliert, mit Isododecan gewaschen und zur Herstellung einer 1 %igen Dispersion unter Anwendung von Ultraschall in reinem Isododecan dispergiert.
- Teilchengröße: 303 nm
-
- Die Suspensionsentwickler A, B und C weisen eine positive Tonerladung auf. Sie zeigen hervorragende Entwicklereigenschaften. Leitfähigkeit und Teilchengröße ändern sich bei Lagerung nicht.
bedeutet.
Claims (9)
beschichtet ist.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE3514867 | 1985-04-25 | ||
| DE19853514867 DE3514867A1 (de) | 1985-04-25 | 1985-04-25 | Elektrostatografischer suspensionsentwickler und verfahren zu dessen herstellung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0200067A2 true EP0200067A2 (de) | 1986-11-05 |
| EP0200067A3 EP0200067A3 (de) | 1988-07-20 |
Family
ID=6269037
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP86105087A Withdrawn EP0200067A3 (de) | 1985-04-25 | 1986-04-14 | Elektrostatografischer Suspensionsentwickler und Verfahren zu dessen Herstellung |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US4719164A (de) |
| EP (1) | EP0200067A3 (de) |
| JP (1) | JPS61249060A (de) |
| DE (1) | DE3514867A1 (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0670525A1 (de) * | 1994-02-24 | 1995-09-06 | Xerox Corporation | Flüssigentwicklerzusammensetzung |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5055370A (en) * | 1988-09-12 | 1991-10-08 | Fuji Photo Film Co., Ltd. | Image forming resin particles for liquid developer for printing plate |
| US5120632A (en) * | 1990-12-28 | 1992-06-09 | Xerox Corporation | Pigment passivation via polymer encapsulation |
| WO2005033352A2 (en) * | 2003-07-09 | 2005-04-14 | Fry's Metals, Inc. | Deposition and patterning process |
| KR20060069425A (ko) * | 2003-07-09 | 2006-06-21 | 프라이즈 메탈즈, 인크. | 코팅 금속 입자 |
| DE102004062437A1 (de) * | 2004-12-20 | 2006-06-22 | Basf Ag | Verfahren zum Kolorieren von zellulosehaltigen Substraten |
| US7413805B2 (en) * | 2005-02-25 | 2008-08-19 | Fry's Metals, Inc. | Preparation of metallic particles for electrokinetic or electrostatic deposition |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1772825A1 (de) * | 1967-07-10 | 1970-09-10 | Ricoh Kk | Fluessiger Entwickler fuer Elektrophotographie |
| GB1563240A (en) * | 1976-10-27 | 1980-03-19 | Hunt Chem Corp Philip A | Liquid electrostatorgraphic toners |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1484582A (en) * | 1974-02-26 | 1977-09-01 | Agfa Gevaert | Liquid developers for the development of electrostatic charge patterns |
| US4452861A (en) * | 1982-05-20 | 1984-06-05 | Rca Corporation | Solid particles encapsulated with cyanoacrylate polymer |
| DE3232062A1 (de) * | 1982-08-28 | 1984-03-01 | Agfa-Gevaert Ag, 5090 Leverkusen | Elektrostatographischer suspensionsentwickler und verfahren zu dessen herstellung |
-
1985
- 1985-04-25 DE DE19853514867 patent/DE3514867A1/de not_active Withdrawn
-
1986
- 1986-04-14 EP EP86105087A patent/EP0200067A3/de not_active Withdrawn
- 1986-04-14 US US06/851,489 patent/US4719164A/en not_active Expired - Fee Related
- 1986-04-23 JP JP61092454A patent/JPS61249060A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1772825A1 (de) * | 1967-07-10 | 1970-09-10 | Ricoh Kk | Fluessiger Entwickler fuer Elektrophotographie |
| GB1563240A (en) * | 1976-10-27 | 1980-03-19 | Hunt Chem Corp Philip A | Liquid electrostatorgraphic toners |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0670525A1 (de) * | 1994-02-24 | 1995-09-06 | Xerox Corporation | Flüssigentwicklerzusammensetzung |
Also Published As
| Publication number | Publication date |
|---|---|
| JPS61249060A (ja) | 1986-11-06 |
| US4719164A (en) | 1988-01-12 |
| DE3514867A1 (de) | 1986-11-06 |
| EP0200067A3 (de) | 1988-07-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0168748B1 (de) | Elektrostatographischer Suspensionsentwickler und Verfahren zu seiner Herstellung | |
| EP0009179B1 (de) | Verfahren zur Herstellung leicht dispergierbarer Titandioxidpigmente | |
| DE3138999C2 (de) | ||
| DE2512112C3 (de) | Elektrophotographischer Suspensionsentwickler | |
| EP0102025B1 (de) | Elektrostatographischer Suspensionsentwickler und Verfahren zu dessen Herstellung | |
| DE2333850C2 (de) | Elektrostatographischer Suspensionsentwickler | |
| EP0157269B1 (de) | Elektrostatographischer Suspensionsentwickler | |
| DE2657326C3 (de) | Elektrostatographischer Suspensionsentwickler | |
| DE2502933C2 (de) | Elektrostatographischer Suspensionsentwickler | |
| DE69008509T2 (de) | Farbelektrofotografie für hoch qualitative Halbtonbilder. | |
| EP0200067A2 (de) | Elektrostatografischer Suspensionsentwickler und Verfahren zu dessen Herstellung | |
| EP0168747B1 (de) | Elektrostatographischer Suspensionsentwickler und Verfahren zu seiner Herstellung | |
| DE3875105T2 (de) | Blockmischpolymerisat-dispergiermittel. | |
| DE3147177C2 (de) | Polymerbeschichtete Metallpigmente | |
| EP0213568B1 (de) | Elektrostatographischer Suspensionsentwickler | |
| DE3433086A1 (de) | Dispersionsstabilisator und seine verwendung | |
| DE3531132A1 (de) | Nicht-waessrige harzzusammensetzung und diese enthaltender elektrophotographischer entwickler | |
| EP0202467A2 (de) | Mit Polycyanacrylat umhülltes Pigment und ein Verfahren zur Umhüllung von Pigmenten | |
| DE2104310B2 (de) | Elektrophotographischer suspensionsentwickler | |
| DE4239135A1 (en) | Positively chargeable liq. electrophotographic developer - based on non-aq. resin dispersion stabilised with copolymer of macro:monomer and unsatd. monomer | |
| DE69029255T2 (de) | Entwickler für elektrostatische Elektrofotografie | |
| DE2657918C3 (de) | Verwendung von heterocyclischen Verbindungen bestimmter Struktur als photoelektrophoretische Teilchen oder Sensibilisatoren in elektrophoretophotographischen Verfahren | |
| DE2354360A1 (de) | Harzmasse und verfahren zu ihrer herstellung | |
| DE2421037A1 (de) | Fluessigentwickler fuer die elektrofotografie | |
| DD161025A1 (de) | Elektrofotografischer fluessigentwickler |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19860414 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): BE DE FR GB |
|
| RAP1 | Party data changed (applicant data changed or rights of an application transferred) |
Owner name: AGFA-GEVAERT AG |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): BE DE FR GB |
|
| 17Q | First examination report despatched |
Effective date: 19891128 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION HAS BEEN WITHDRAWN |
|
| 18W | Application withdrawn |
Withdrawal date: 19910208 |
|
| R18W | Application withdrawn (corrected) |
Effective date: 19910208 |
|
| RIN1 | Information on inventor provided before grant (corrected) |
Inventor name: GOOSSENS, JOHN, IR. Inventor name: WANICSZEK, HELMUT, DR. Inventor name: PODSZUN, WOLFGANG, DR. |