DE69918762T2 - Kombination aus Organothioverbindung und Zink-Mercaptoester als Hitzestabilisator bei PVC-Herstellung - Google Patents
Kombination aus Organothioverbindung und Zink-Mercaptoester als Hitzestabilisator bei PVC-Herstellung Download PDFInfo
- Publication number
- DE69918762T2 DE69918762T2 DE69918762T DE69918762T DE69918762T2 DE 69918762 T2 DE69918762 T2 DE 69918762T2 DE 69918762 T DE69918762 T DE 69918762T DE 69918762 T DE69918762 T DE 69918762T DE 69918762 T2 DE69918762 T2 DE 69918762T2
- Authority
- DE
- Germany
- Prior art keywords
- zinc
- composition according
- alkyl
- composition
- stabilizer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- -1 organothio compound Chemical class 0.000 title claims abstract description 40
- 229910052725 zinc Inorganic materials 0.000 title claims abstract description 31
- 239000011701 zinc Substances 0.000 title claims abstract description 31
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 title claims abstract description 22
- 239000012760 heat stabilizer Substances 0.000 title claims description 4
- 238000004519 manufacturing process Methods 0.000 title description 5
- 239000000203 mixture Substances 0.000 claims abstract description 76
- 229920000642 polymer Polymers 0.000 claims abstract description 39
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 18
- 150000002367 halogens Chemical class 0.000 claims abstract description 18
- KYNFOMQIXZUKRK-UHFFFAOYSA-N bishydroxyethyldisulfide Natural products OCCSSCCO KYNFOMQIXZUKRK-UHFFFAOYSA-N 0.000 claims abstract description 11
- 229920006324 polyoxymethylene Polymers 0.000 claims abstract description 5
- 239000003381 stabilizer Substances 0.000 claims description 36
- 125000000217 alkyl group Chemical group 0.000 claims description 20
- 150000002148 esters Chemical class 0.000 claims description 20
- 239000002253 acid Substances 0.000 claims description 17
- 125000004432 carbon atom Chemical group C* 0.000 claims description 12
- 150000001875 compounds Chemical class 0.000 claims description 9
- 239000003513 alkali Substances 0.000 claims description 6
- 150000001341 alkaline earth metal compounds Chemical class 0.000 claims description 5
- 125000003342 alkenyl group Chemical group 0.000 claims description 5
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 239000001257 hydrogen Substances 0.000 claims description 4
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 4
- 229910052783 alkali metal Inorganic materials 0.000 claims description 3
- 150000001340 alkali metals Chemical class 0.000 claims description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 3
- 239000004215 Carbon black (E152) Substances 0.000 claims description 2
- 229930195733 hydrocarbon Natural products 0.000 claims description 2
- 125000004925 dihydropyridyl group Chemical class N1(CC=CC=C1)* 0.000 claims 2
- 150000005840 aryl radicals Chemical class 0.000 claims 1
- 229940125773 compound 10 Drugs 0.000 claims 1
- 238000012545 processing Methods 0.000 abstract description 5
- 150000003568 thioethers Chemical class 0.000 abstract description 4
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 abstract description 2
- LSDPWZHWYPCBBB-UHFFFAOYSA-N Methanethiol Chemical compound SC LSDPWZHWYPCBBB-UHFFFAOYSA-N 0.000 abstract description 2
- DNJIEGIFACGWOD-UHFFFAOYSA-N ethyl mercaptane Natural products CCS DNJIEGIFACGWOD-UHFFFAOYSA-N 0.000 abstract 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 abstract 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 19
- 239000004800 polyvinyl chloride Substances 0.000 description 19
- YNGDWRXWKFWCJY-UHFFFAOYSA-N 1,4-Dihydropyridine Chemical class C1C=CNC=C1 YNGDWRXWKFWCJY-UHFFFAOYSA-N 0.000 description 11
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 8
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 8
- 239000000314 lubricant Substances 0.000 description 8
- 238000000034 method Methods 0.000 description 7
- 229920002554 vinyl polymer Polymers 0.000 description 7
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 6
- 239000004698 Polyethylene Substances 0.000 description 6
- 239000012188 paraffin wax Substances 0.000 description 6
- 229920000573 polyethylene Polymers 0.000 description 6
- 230000000052 comparative effect Effects 0.000 description 5
- 229920001577 copolymer Polymers 0.000 description 5
- 229920001519 homopolymer Polymers 0.000 description 5
- 125000003396 thiol group Chemical class [H]S* 0.000 description 5
- 150000003752 zinc compounds Chemical class 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- 229910000019 calcium carbonate Inorganic materials 0.000 description 4
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 4
- 239000008116 calcium stearate Substances 0.000 description 4
- 235000013539 calcium stearate Nutrition 0.000 description 4
- 230000015556 catabolic process Effects 0.000 description 4
- 238000009833 condensation Methods 0.000 description 4
- 230000005494 condensation Effects 0.000 description 4
- 238000006731 degradation reaction Methods 0.000 description 4
- 125000000611 organothio group Chemical group 0.000 description 4
- 229920002959 polymer blend Polymers 0.000 description 4
- 239000004408 titanium dioxide Substances 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 150000001339 alkali metal compounds Chemical class 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 229920000620 organic polymer Polymers 0.000 description 3
- 229920000098 polyolefin Polymers 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- PMNLUUOXGOOLSP-UHFFFAOYSA-N 2-mercaptopropanoic acid Chemical compound CC(S)C(O)=O PMNLUUOXGOOLSP-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- SOGAXMICEFXMKE-UHFFFAOYSA-N Butylmethacrylate Chemical compound CCCCOC(=O)C(C)=C SOGAXMICEFXMKE-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 2
- 239000000920 calcium hydroxide Substances 0.000 description 2
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- FJKIXWOMBXYWOQ-UHFFFAOYSA-N ethenoxyethane Chemical compound CCOC=C FJKIXWOMBXYWOQ-UHFFFAOYSA-N 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 238000010304 firing Methods 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 2
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 239000004611 light stabiliser Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 2
- 235000021317 phosphate Nutrition 0.000 description 2
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 239000004014 plasticizer Substances 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 239000000376 reactant Substances 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- HYHCSLBZRBJJCH-UHFFFAOYSA-M sodium hydrosulfide Chemical compound [Na+].[SH-] HYHCSLBZRBJJCH-UHFFFAOYSA-M 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 150000005846 sugar alcohols Polymers 0.000 description 2
- CWERGRDVMFNCDR-UHFFFAOYSA-N thioglycolic acid Chemical compound OC(=O)CS CWERGRDVMFNCDR-UHFFFAOYSA-N 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- AXCLYMZXSRACTQ-UHFFFAOYSA-L zinc;4-ethyl-2-sulfanyloctanoate Chemical compound [Zn+2].CCCCC(CC)CC(S)C([O-])=O.CCCCC(CC)CC(S)C([O-])=O AXCLYMZXSRACTQ-UHFFFAOYSA-L 0.000 description 2
- 229920002818 (Hydroxyethyl)methacrylate Polymers 0.000 description 1
- LKBMNSIEFNABEB-UHFFFAOYSA-N 1-[2-(2-dodecoxyethylsulfanyl)ethoxy]dodecane Chemical compound CCCCCCCCCCCCOCCSCCOCCCCCCCCCCCC LKBMNSIEFNABEB-UHFFFAOYSA-N 0.000 description 1
- FPBWSPZHCJXUBL-UHFFFAOYSA-N 1-chloro-1-fluoroethene Chemical group FC(Cl)=C FPBWSPZHCJXUBL-UHFFFAOYSA-N 0.000 description 1
- KUIZKZHDMPERHR-UHFFFAOYSA-N 1-phenylprop-2-en-1-one Chemical compound C=CC(=O)C1=CC=CC=C1 KUIZKZHDMPERHR-UHFFFAOYSA-N 0.000 description 1
- QVKXCBBIWLPDSM-UHFFFAOYSA-N 2,6-ditert-butyl-4-decoxyphenol Chemical compound CCCCCCCCCCOC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 QVKXCBBIWLPDSM-UHFFFAOYSA-N 0.000 description 1
- AWQKXJYKNFMHJP-UHFFFAOYSA-N 2-(2-hydroxyethoxy)ethyl decanoate Chemical compound CCCCCCCCCC(=O)OCCOCCO AWQKXJYKNFMHJP-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- FLPJVCMIKUWSDR-UHFFFAOYSA-N 2-(4-formylphenoxy)acetamide Chemical compound NC(=O)COC1=CC=C(C=O)C=C1 FLPJVCMIKUWSDR-UHFFFAOYSA-N 0.000 description 1
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical compound CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 1
- MXVMODFDROLTFD-UHFFFAOYSA-N 2-[2-[2-(2-butoxyethoxy)ethoxy]ethoxy]ethanol Chemical compound CCCCOCCOCCOCCOCCO MXVMODFDROLTFD-UHFFFAOYSA-N 0.000 description 1
- OYUNTGBISCIYPW-UHFFFAOYSA-N 2-chloroprop-2-enenitrile Chemical compound ClC(=C)C#N OYUNTGBISCIYPW-UHFFFAOYSA-N 0.000 description 1
- GAWAYYRQGQZKCR-UHFFFAOYSA-N 2-chloropropionic acid Chemical compound CC(Cl)C(O)=O GAWAYYRQGQZKCR-UHFFFAOYSA-N 0.000 description 1
- IGPIBLIHYRGADN-UHFFFAOYSA-N 2-hydroxyethyl decanoate Chemical compound CCCCCCCCCC(=O)OCCO IGPIBLIHYRGADN-UHFFFAOYSA-N 0.000 description 1
- VMCYRTNAPHJORO-UHFFFAOYSA-N 2-tert-butyl-4-octadecoxyphenol Chemical compound CCCCCCCCCCCCCCCCCCOC1=CC=C(O)C(C(C)(C)C)=C1 VMCYRTNAPHJORO-UHFFFAOYSA-N 0.000 description 1
- UHBAWOXYQROEIH-UHFFFAOYSA-N 3-chloro-4-(2-chlorobut-3-enoxy)but-1-ene Chemical compound C=CC(Cl)COCC(Cl)C=C UHBAWOXYQROEIH-UHFFFAOYSA-N 0.000 description 1
- DKIDEFUBRARXTE-UHFFFAOYSA-N 3-mercaptopropanoic acid Chemical compound OC(=O)CCS DKIDEFUBRARXTE-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- OSDWBNJEKMUWAV-UHFFFAOYSA-N Allyl chloride Chemical group ClCC=C OSDWBNJEKMUWAV-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- LKUNXBRZDFMZOK-GFCCVEGCSA-N Capric acid monoglyceride Natural products CCCCCCCCCC(=O)OC[C@H](O)CO LKUNXBRZDFMZOK-GFCCVEGCSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 239000004801 Chlorinated PVC Substances 0.000 description 1
- 239000004709 Chlorinated polyethylene Substances 0.000 description 1
- IEPRKVQEAMIZSS-UHFFFAOYSA-N Di-Et ester-Fumaric acid Natural products CCOC(=O)C=CC(=O)OCC IEPRKVQEAMIZSS-UHFFFAOYSA-N 0.000 description 1
- IEPRKVQEAMIZSS-WAYWQWQTSA-N Diethyl maleate Chemical compound CCOC(=O)\C=C/C(=O)OCC IEPRKVQEAMIZSS-WAYWQWQTSA-N 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- GWFGDXZQZYMSMJ-UHFFFAOYSA-N Octadecansaeure-heptadecylester Natural products CCCCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCCCC GWFGDXZQZYMSMJ-UHFFFAOYSA-N 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 239000004115 Sodium Silicate Substances 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- UWHCKJMYHZGTIT-UHFFFAOYSA-N Tetraethylene glycol, Natural products OCCOCCOCCOCCO UWHCKJMYHZGTIT-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical class C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- XECAHXYUAAWDEL-UHFFFAOYSA-N acrylonitrile butadiene styrene Chemical compound C=CC=C.C=CC#N.C=CC1=CC=CC=C1 XECAHXYUAAWDEL-UHFFFAOYSA-N 0.000 description 1
- 239000004676 acrylonitrile butadiene styrene Substances 0.000 description 1
- 229920000122 acrylonitrile butadiene styrene Polymers 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical class OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 125000005250 alkyl acrylate group Chemical group 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- VEZXCJBBBCKRPI-UHFFFAOYSA-N beta-propiolactone Chemical compound O=C1CCO1 VEZXCJBBBCKRPI-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- HDFRDWFLWVCOGP-UHFFFAOYSA-N carbonothioic O,S-acid Chemical class OC(S)=O HDFRDWFLWVCOGP-UHFFFAOYSA-N 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 229940074979 cetyl palmitate Drugs 0.000 description 1
- SZOPAPBTRRMGMD-UHFFFAOYSA-N chloroethene;1,1,2-trichloroethene Chemical group ClC=C.ClC=C(Cl)Cl SZOPAPBTRRMGMD-UHFFFAOYSA-N 0.000 description 1
- DHZSIQDUYCWNSB-UHFFFAOYSA-N chloroethene;1,1-dichloroethene Chemical compound ClC=C.ClC(Cl)=C DHZSIQDUYCWNSB-UHFFFAOYSA-N 0.000 description 1
- BMZQPXKCLRADET-UHFFFAOYSA-N chloroethene;2-ethylhexyl prop-2-enoate Chemical compound ClC=C.CCCCC(CC)COC(=O)C=C BMZQPXKCLRADET-UHFFFAOYSA-N 0.000 description 1
- HGAZMNJKRQFZKS-UHFFFAOYSA-N chloroethene;ethenyl acetate Chemical compound ClC=C.CC(=O)OC=C HGAZMNJKRQFZKS-UHFFFAOYSA-N 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000002485 combustion reaction Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- IEPRKVQEAMIZSS-AATRIKPKSA-N diethyl fumarate Chemical compound CCOC(=O)\C=C\C(=O)OCC IEPRKVQEAMIZSS-AATRIKPKSA-N 0.000 description 1
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 description 1
- 229940075557 diethylene glycol monoethyl ether Drugs 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229910001651 emery Inorganic materials 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- NHOGGUYTANYCGQ-UHFFFAOYSA-N ethenoxybenzene Chemical compound C=COC1=CC=CC=C1 NHOGGUYTANYCGQ-UHFFFAOYSA-N 0.000 description 1
- MEGHWIAOTJPCHQ-UHFFFAOYSA-N ethenyl butanoate Chemical compound CCCC(=O)OC=C MEGHWIAOTJPCHQ-UHFFFAOYSA-N 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- SUPCQIBBMFXVTL-UHFFFAOYSA-N ethyl 2-methylprop-2-enoate Chemical compound CCOC(=O)C(C)=C SUPCQIBBMFXVTL-UHFFFAOYSA-N 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- PBZROIMXDZTJDF-UHFFFAOYSA-N hepta-1,6-dien-4-one Chemical compound C=CCC(=O)CC=C PBZROIMXDZTJDF-UHFFFAOYSA-N 0.000 description 1
- PXDJXZJSCPSGGI-UHFFFAOYSA-N hexadecanoic acid hexadecyl ester Natural products CCCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCC PXDJXZJSCPSGGI-UHFFFAOYSA-N 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 150000002688 maleic acid derivatives Chemical class 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N methanesulfonic acid Substances CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- AWJZTPWDQYFQPQ-UHFFFAOYSA-N methyl 2-chloroprop-2-enoate Chemical compound COC(=O)C(Cl)=C AWJZTPWDQYFQPQ-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- RKISUIUJZGSLEV-UHFFFAOYSA-N n-[2-(octadecanoylamino)ethyl]octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(=O)NCCNC(=O)CCCCCCCCCCCCCCCCC RKISUIUJZGSLEV-UHFFFAOYSA-N 0.000 description 1
- NKBWPOSQERPBFI-UHFFFAOYSA-N octadecyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCCCC NKBWPOSQERPBFI-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 125000001741 organic sulfur group Chemical group 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 238000013021 overheating Methods 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- UCUUFSAXZMGPGH-UHFFFAOYSA-N penta-1,4-dien-3-one Chemical class C=CC(=O)C=C UCUUFSAXZMGPGH-UHFFFAOYSA-N 0.000 description 1
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 1
- 125000005498 phthalate group Chemical class 0.000 description 1
- DOIRQSBPFJWKBE-UHFFFAOYSA-N phthalic acid di-n-butyl ester Natural products CCCCOC(=O)C1=CC=CC=C1C(=O)OCCCC DOIRQSBPFJWKBE-UHFFFAOYSA-N 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920001490 poly(butyl methacrylate) polymer Polymers 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002620 polyvinyl fluoride Polymers 0.000 description 1
- 239000005033 polyvinylidene chloride Substances 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 229960000380 propiolactone Drugs 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- MWWATHDPGQKSAR-UHFFFAOYSA-N propyne Chemical group CC#C MWWATHDPGQKSAR-UHFFFAOYSA-N 0.000 description 1
- LKUNXBRZDFMZOK-UHFFFAOYSA-N rac-1-monodecanoylglycerol Chemical compound CCCCCCCCCC(=O)OCC(O)CO LKUNXBRZDFMZOK-UHFFFAOYSA-N 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical class OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- FDRCDNZGSXJAFP-UHFFFAOYSA-M sodium chloroacetate Chemical compound [Na+].[O-]C(=O)CCl FDRCDNZGSXJAFP-UHFFFAOYSA-M 0.000 description 1
- NTHWMYGWWRZVTN-UHFFFAOYSA-N sodium silicate Chemical compound [Na+].[Na+].[O-][Si]([O-])=O NTHWMYGWWRZVTN-UHFFFAOYSA-N 0.000 description 1
- 229910052911 sodium silicate Inorganic materials 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 1
- RVEZZJVBDQCTEF-UHFFFAOYSA-N sulfenic acid Chemical class SO RVEZZJVBDQCTEF-UHFFFAOYSA-N 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- QXJQHYBHAIHNGG-UHFFFAOYSA-N trimethylolethane Chemical compound OCC(C)(CO)CO QXJQHYBHAIHNGG-UHFFFAOYSA-N 0.000 description 1
- BSVBQGMMJUBVOD-UHFFFAOYSA-N trisodium borate Chemical compound [Na+].[Na+].[Na+].[O-]B([O-])[O-] BSVBQGMMJUBVOD-UHFFFAOYSA-N 0.000 description 1
- KOZCZZVUFDCZGG-UHFFFAOYSA-N vinyl benzoate Chemical compound C=COC(=O)C1=CC=CC=C1 KOZCZZVUFDCZGG-UHFFFAOYSA-N 0.000 description 1
- FUSUHKVFWTUUBE-UHFFFAOYSA-N vinyl methyl ketone Natural products CC(=O)C=C FUSUHKVFWTUUBE-UHFFFAOYSA-N 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
- GRLPGMSOIBAIPK-ATMONBRVSA-L zinc;(z)-4-(2-ethylhexoxy)-4-oxobut-2-enoate Chemical compound [Zn+2].CCCCC(CC)COC(=O)\C=C/C([O-])=O.CCCCC(CC)COC(=O)\C=C/C([O-])=O GRLPGMSOIBAIPK-ATMONBRVSA-L 0.000 description 1
- WCAACYUVCHFYHJ-UHFFFAOYSA-L zinc;2,2-bis(sulfanyl)propanoate Chemical compound [Zn+2].CC(S)(S)C([O-])=O.CC(S)(S)C([O-])=O WCAACYUVCHFYHJ-UHFFFAOYSA-L 0.000 description 1
- IPSHSWODJRJGAP-UHFFFAOYSA-L zinc;2-octadecylsulfanylpropanoate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCCSC(C)C([O-])=O.CCCCCCCCCCCCCCCCCCSC(C)C([O-])=O IPSHSWODJRJGAP-UHFFFAOYSA-L 0.000 description 1
- MZSZOQUECQHORO-UHFFFAOYSA-L zinc;2-octylsulfanylpropanoate Chemical compound [Zn+2].CCCCCCCCSC(C)C([O-])=O.CCCCCCCCSC(C)C([O-])=O MZSZOQUECQHORO-UHFFFAOYSA-L 0.000 description 1
- RBEYUVZBFYVXEX-UHFFFAOYSA-L zinc;2-sulfanylacetate Chemical compound [Zn+2].[O-]C(=O)CS.[O-]C(=O)CS RBEYUVZBFYVXEX-UHFFFAOYSA-L 0.000 description 1
- YCFZZALTCSESPA-UHFFFAOYSA-L zinc;2-sulfanylbutanedioate Chemical compound [Zn+2].[O-]C(=O)CC(S)C([O-])=O YCFZZALTCSESPA-UHFFFAOYSA-L 0.000 description 1
- CFTPOIAGZBUWDY-UHFFFAOYSA-L zinc;2-sulfanylbutanoate Chemical compound [Zn+2].CCC(S)C([O-])=O.CCC(S)C([O-])=O CFTPOIAGZBUWDY-UHFFFAOYSA-L 0.000 description 1
- QRHGLIRJVQVCJZ-UHFFFAOYSA-L zinc;2-sulfanyldecanoate Chemical compound [Zn+2].CCCCCCCCC(S)C([O-])=O.CCCCCCCCC(S)C([O-])=O QRHGLIRJVQVCJZ-UHFFFAOYSA-L 0.000 description 1
- URCVFQDXVRYNIJ-UHFFFAOYSA-L zinc;2-sulfanylicosanoate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCCC(S)C([O-])=O.CCCCCCCCCCCCCCCCCCC(S)C([O-])=O URCVFQDXVRYNIJ-UHFFFAOYSA-L 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/36—Sulfur-, selenium-, or tellurium-containing compounds
- C08K5/37—Thiols
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Materials For Medical Uses (AREA)
Description
- Halogenhaltige Polymere, besonders jene, die Chlor enthalten, werden in großem Umfang verwendet und haben große gewerbliche Signifikanz. Polyvinylchlorid (PVC) wird insbesondere in Verpackungen, Mauerbehängen, Rohren und vielen extrudierten Formlingen verwendet. Ein solch großer Umfang und unterschiedliche Verwendung der halogenhaltigen Polymere hängt von der Einarbeitung guter Hitze- und Lichtstabilisatoren darin ab. PVC hat beispielsweise bekanntermaßen eine Tendenz, bei längerem Erhitzen und Belichten während der Verarbeitung und Verwendung sich abzubauen. Verdunkelung oder andere Farbveränderung und der Verlust von Zugfestigkeit, Biegefestigkeit und Schlagfestigkeit sind die Ergebnisse eines solchen Abbaus. Wenn nicht gute billige Stabilisatoren für die Zugabe zu der Polymerzusammensetzung verfügbar sind, ist die Standzeit von Gegenständen aus der Zusammensetzung begrenzt und ihre Verwendung ernsthaft beschränkt, wie auch die Bedingungen zu ihrer Herstellung.
- Eine besonders lästige Form des Abbaus tritt auf, wenn die Polymerzusammensetzung in Gegenstände nach Methoden, die Wärme bis zum Schmelzen oder Erweichen des Polymers verwenden zu Gegenständen verarbeitet werden. Eine Farbveränderung kann während der ersten wenigen Minuten bei hohen Temperaturen (zum Beispiel von etwa 175 bis etwa 200°C) auftreten, und diese Farbe wird allgemein als frühe Farbe oder frühe Verfärbung bezeichnet. Das Vermeiden einer solch frühen Farbe ist bemerkenswert wichtig bei der Herstellung von Kunststoffröhren und Mauerbehängen. Es ist natürlich auch wichtig, die Färbung und Zersetzung des Polymers, während dieses bei längerer Dauer hohen Temperaturen ausgesetzt wird, zu verhindern oder zu verringern, was zu plötzlichem und katastrophalem Abbau zu einem pechartigen Schmirgelmaterial und zur Bildung korrosiver Materialien, wie HCl, im Inneren der Herstellungsanlage führen kann. Die inneren, hochpolierten Oberflächen der Anlagen können so im wesentlichen unbrauchbar gemacht werden. Ein besonders unangenehmer Fall eines solchen plötzlichen Abbaus tritt oftmals auf, wenn Zinkverbindungen als Stabilisatoren verwendet werden, dieses Phänomen ist als „Zinkbrand" in der PVC-Industrie bekannt.
- Ein Beispiel von Zinkbrand ist in der US-Patentschrift 4,515,916 erläutert, wo eine PVC-Zusammensetzung, die Zink-bis-(octylthioglycolat) und ein substituiertes Dihydropyridin als Co-Stabilisator enthielt, zeigte sich eine solche Verbrennung nach 3 Minuten auf einer Zweiwalzenmühle bei 193°C.
- In der US-Patentschrift 3,417,039 lehrt Penneck eine stabilisierende Zusammensetzung für chlorhaltige Polymere, die ein Zinksalz einer Carbonsäure umfaßt, welche Schwefelsubstituenten, einen mehrwertigen Alkohohl und eine organische schwefelhaltige Verbindung der Formel R1-S(1-2)-R2 hat, die beispielhalber Bis-(n-dodecyloxyethyl)-sulfid ist. Die geeigneten salzbildenden Säuren schließen Benzoesäure, Salizylsäure, Phthalsäure und Maleinsäure ein. Zink-2-ethylhexylmaleat ist ein bevorzugtes Salz. Wie nachfolgend gezeigt, überwindet die Stabilisierungszusammensetzung nach Penneck nicht das Zinkbrandproblem.
- Die GB-A-936770 beschreibt Stabilisatorzusammensetzungen für halogenhaltige Polymere, die eine Organothioverbindung und bis zu 500 ppm (0,05 phr) einer Zinkverbindung umfassen, welche ein Zinkmercaptoester sein kann. Diese Literaturstelle lehrt, daß der Gehalt der Zinkverbindung auf 50 ppm oder weniger gehalten werden sollte.
- Die EP-A-133 130 beschreibt zahlreiche Kombinationen von Organothioverbindungen und Organometallverbindungen, vorzugsweise Organozinkverbindungen, und hat ein Beispiel der Verwendung von 0,15% eines Zinkmercaptoesters und eines Pentaerythrit-Mercaptoesters.
- Wir haben nun festgestellt, daß man mit Organothioverbindungen hervorragende Co-Stabilisatoren in Verbindung mit dem Zink-bis-(mercaptosäureester) bekommt, wenn er während der Verarbeitung halogenhaltiger Polymere, wie PVC, bei hoher Temperatur vorhanden ist.
- Es ist ein Ziel dieser Erfindung, eine halogenhaltige Polymerzusammensetzung mit verbesserter Wärmebeständigkeit zu bekommen.
- Ein weiteres verwandtes Ziel dieser Erfindung ist es, Zinkbrand während der Verarbeitung von PVC-Zusammensetzungen bei erhöhten Temperaturen zu vermeiden.
- Die vorliegende Erfindung besteht aus einer Polymerzusammensetzung, die ein halogenhaltiges Polymer und eine Wärmestabilisatorzusammensetzung umfaßt, wobei diese Stabilisatorzusammensetzung
- (A) eine Organothioverbindung ausgewählt unter Dithiodiglycol, Polyformalen und Polyacetalen dieses Dithiodiglycols und von Mercaptoalkanolen der allgemeinen Formel worin R1 und R2 gleich oder verschieden sind und Wasserstoff oder C1 bis C18-Alkyl bedeuten und i 0 oder eine ganze Zahl von 1 bis 6 einschließlich bedeutet,
- (B) 0,2 bis 1,7 Gewichtsteile je 100 Teile Polymer wenigstens eines Zinkmercaptoesters, ausgewählt unter (B1), einem Zinkmercaptosäureester mit der Formel Zn-[S(CH2)x-C(=O)OR]2, worin R ein Kohlenwasserstoffrest mit 2 bis 22 Kohlenstoffatomen ist und x 1 oder 2 ist, (B2) einen Zinkmercaptosäureester der Formel Zn-[S(CHR)a(CH2)b-[C(=O)O]R']2, worin R' Methyl oder C(=O)OR'' ist, R'' [(CH2-[C-(R*)(R2*)]yCH2O)2R3*] ist, R* H, Alkyl oder Hydroxyalkyl ist, R2* OH, Hydroxy-substituiertes Alkyl oder O(O=)C-R4* ist, R3* H, (O=)C-R4* oder Alkyl ist, R4* Alkyl oder Alkenyl ist, a = 0 oder 1, b = 1 oder 2, y = 0 oder 1 und z = 1 bis 4 mit der Maßgabe, daß, wenn z größer als 1 ist, y = 0, und (B3) einen Zinkmercaptoalkylcarbonsäureester der Formel Zn-[SCH2(CH2)qO-C(=O)R5*]2, worin R5* eine Alkyl- oder Alkenylgruppe mit 1 bis 18 Kohlenstoffatomen oder ein Arylrest mit 6 bis 12 Kohlenstoffatomen ist und q aus 1 bis 6 Kohlenstoffatomen besteht,
- (C) 0 bis 20 Gew.-%, bezogen auf die Stabilisatorzusammensetzung, einer basischen Alkali- oder Erdalkaliverbindung und
- (D) 0 bis 10 Gew.-%, bezogen auf die Stabilisatorzusammensetzung, eines substituierten Dihydropyridins umfaßt.
- Die Organothioverbindungen, die für die Zwecke dieser Erfindung geeignet sind, sind bekannte Verbindungen und weiden unter Dithiodiglycol, Polyformalen und Polyacetalen dieses Dithiodiglycols und Mercaptoalkanolen der allgemeinen Formel ausgewählt, worin R1 und R2 gleich oder verschieden sind und Wasserstoff oder C1 bis C18-Alkyl sind und i 0 oder eine ganze Zahl von 1 bis 6 einschließlich ist.
- Beispiele der mercaptanhaltigen organischen Verbindungen, die durch diese Formel I beschrieben sind, sind beispielsweise, aber nicht ausschließlich die folgenden Verbindungen: Dithiodiglycol und Polyformale und Polyacetale desselben mit der Formel H-(OCH2CH2SSCH2 CH2OCR2)2-OH, worin R Wasserstoff oder Methyl ist und n = 3–12, sind die bevorzugten organischen Sulfide für die Zwecke dieser Erfindung. Die Bildung dieser Polymeren ist in der US-Patentschrift 4,184,890 und der US-Patentschrift 4,097,299 beschrieben.
- Die Zinkmercaptoester der Formel B' sind beispielsweise Zink-bis-(2-ethylhexylthioglycolat), Zink-bis-(octylmercaptopropionat), Zink-bis-(octadecylthioglycolat), Zink-bis-(octadecylmercaptopropionat) und Zink-bis-(ethylthioglycolat). Sie werden leicht hergestellt durch Umsetzung des entsprechenden Mercaptosäureesters mit Zinkchlorid in Gegenwart eines geeigneten Wasserstoffchlorid-Spülmittels, wie Ammoniak, Ammoniumhydroxid und Alkalimetallhydroxid oder einem Carbonat hiervon. Eine andere Methode ist die Kondensation des Mercaptosäureesters mit Zink in einem organischen Medium, wie einem hoch-siedenden Naphtha, Xylol, Paraffinwachs und dergleichen. Irgendein Verhältnis der Zinkverbindung und des Mercaptoesters wird ausreichen, solange die Reaktionsbedingungen derart sind, daß sie die Kondensation treiben, doch ist es bevorzugt, ein stöchiometrisches Verhältnis der Reaktionspartner zu verwenden. Atmosphärendruck ist geeignet, doch die Umsetzung wird zufriedenstellend bei etwa 50 bis etwa 80°C unter vermindertem Druck verlaufen. Die Maximaltemperatur ist etwa 140–150°C.
- Der Zink-bis-mercaptosäureester kann auch unter jenen ausgewählt werden, die in der US-Patentschrift 5,536,767 beschrieben sind. Solche Ester sind etwa Zink-bis-thioglycolat, Zink-bis-mercaptopropionat und Zink-mercaptosuccinat eines mehrwertigen Alkohols oder Esters, Carboxylat oder Ester-carboxylat hiervon mit wenigstens einer funktionellen Hydroxylgruppe, wie beispielhalber durch Ethylenglycol, Glycerin, Tetraethylenglycol, Trimethylolethan, Pentaerythritol, Glycolether, wie Tetraethylenglycolmonobutylether und Diethylenglycolmonoethylether, Glycolmonocarboxylate, wie Diethylenglycolmonocaprat und Ethylenglycolmonocaprat, und Glycerincarboxylate, wie Glycerinmonocaprat, die alle entweder im Handel erhältlich sind oder leicht nach herkömmlichen Methoden herstellbar sind. Die Mercaptosäureester können nach herkömmlichen Verfahren hergestellt werden, wobei die Mercaptosäure und die Verbindung mit der Hydroxylgruppe in Gegenwart eines geeigneten Katalysators, wie Methansulfonsäure oder p-Toluolsulfonsäure und eine azeotropen organischen Lösungsmittels, wie Toluol oder Heptan, erhitzt werden. Alternativ kann die Veresterung bei vermindertem Druck durchgeführt werden. Die Umsetzung wird fortgesetzt, bis die Säurezahl auf etwa 12 bis 15 reduziert ist.
- Die Säuren, aus welchen die Ester stammen, sind auch allgemein im Handel erhältlich, können aber auch gegebenenfalls durch Verfahren hergestellt werden, die in der chemischen Technik seit langem bekannt sind. Mercaptoessigsäure kann beispielsweise durch Umsetzung von Natriumhydrogensulfid mit Natriumchloracetat und anschließendes Ansäuern gewonnen werden. β-Mercaptopropionsäure erhält man in etwa 80% Ausbeute mit der Umsetzung von Natriumhydrogensulfid mit β-Propiolacton in Acetonitril und anschließende Ansäuerung. Mercaptobernsteinsäure kann durch Zugabe von Schwefelwasserstoff an der Doppelbindung von Maleinsäureanhydrid und anschließende Hydrolyse hergestellt werden. Auch geeignet für die Zwecke dieser Erfindung sind die Alkylester von α-Mercaptopropionsäure, die aus α-Chlorpropionsäure und Natriumthiosulfat nach dem in der US-Patentschrift 2,413,361 beschriebenen Verfahren, welches unter Bezugnahme hier einbezogen wird, hergestellt werden kann.
- Die Zinkmercaptoalkylcarbonsäureester von (B3) leiten sich von den bekannten „Umkehrestern" her, die so bezeichnet werden, da sie die Produkte der Umsetzung von Mercaptoalkoholen und Carbonsäuren statt von Mercaptocarbonsäuren und Alkoholen sind. Die Herstellung der Ester und ihre Verwendung als Stabilisatoren für Vinylchloridpolymere sind in der US-Patentschrift 2,870,182 beschrieben, die hier unter Bezugnahme eingeführt wird. Es ist bevorzugt, daß q 1 oder 2 ist und daß R5 bevorzugt eine Alkylgruppe mit 7 bis 17 Kohlenstoffatomen oder einer Phenylgruppe ist. Sie werden leicht durch Umsetzung des entsprechenden Mercaptoalkylesters mit Zinkchlorid in Gegenwart eines geeigneten Chlorwasserstoffspülmittels, wie Ammoniak, Ammoniumhydroxid und Alkalimetallhydroxid oder Carbonat hiervon hergestellt. Eine andere Methode ist die Kondensation des Mercaptoalkylesters mit Zinkoxid in einem organischen Medium, wie einem hoch-siedenden Naphtha, Xylol, Paraffinwachs und dergleichen. Irgendein Verhältnis der Zinkverbindung und des Mercaptoalkylesters wird genügen, solange die Reaktionsbedingungen derart sind, daß die Kondensation vorangetrieben wird, doch ist es bevorzugt, ein stöchiometrisches Verhältnis der Reaktionspartner zu benutzen. Atmosphärendruck ist geeignet, doch wird die Reaktion zufriedenstellen bei etwa 50 bis etwa 80°C unter vermindertem Druck ablaufen. Die maximale Temperatur ist etwa 140–150°C.
- Die halogenhaltigen Polymere, die durch die Stabilisatorzusammensetzungen dieser Erfindung stabilisiert werden und die in den Polymerzusammensetzungen dieser Erfindung brauchbar sind, schließen beispielsweise halogenierte Polyolefinhomopolymere, halogenierte Polyolefincopolymere, Polymergemische, die ein halogeniertes Polyolefinhomopolymer oder -copolymer enthalten, Vinylhalogenidhomopolymere, Vinylhalogenidcopolymere und Polymergemische, die Vinylhalogenidhomopolymere oder Vinylhalogenidcopolymere enthalten, welche in der Praxis dieser Erfindung brauchbar sind. Beispielsweise können (1) Polyvinylchlorid, Polyvinylidenchlorid, Polyvinylbromid, Polyvinylfluorid, Polyvinylidenfluorid, (2) Copolymere von Vinylchlorid mit einem copolymerisierbaren ethylenisch ungesättigten Monomer, wie Vinylidenchlorid, Vinylacetat, Vinylbutyrat, Vinylbenzoat, Diethylfumarat, Diethylmaleat, andere Alkylfumerate und Maleate, wie Vinylpropionat, Methylacrylat, 2-Ethylhexylacrylat, Butylacrylat, Ethylacrylat und andere Alkylacrylate, Methylmethacrylat, Ethyl methacrylat, Butylmethacrylat, Hydroxyethylmethacrylat und andere Alkylmethacrylate, Methyl-α-chloracrylat, Styrol, Vinylether, wie Vinylethylether, Vinylchlorethylether, Vinylphenylether, Vinylketone, wie Vinylmethylketon, Vinylphenylketon, 1-Fluor-1-chlorethylen, Acrylnitril, Chloracrylnitril, Allylidendiacetat, Chlorallylidendiacetat, Ethylen und Propylen und (3) Polymergemische, wie Gemische von Polyvinylchlorid und Polyethylen, Polyvinylchlorid und chloriertem Polyethylen, Polyvinylchlorid und Polymethylmethacrylat, Polyvinylchlorid und Polybutylmethacrylat, Polyvinylchlorid und Polystyrol, Polyvinylchlorid und Acrylnitril-Butadien-Styrolcopolymer sowie Polyvinylchlord und Polyethylen und Polymethylmethacrylat. Typische Vinylhalogenidcopolymerre, die bei dieser Erfindung brauchbar sind, schließen Vinylchlorid-Vinylacetat (87 : 13), Vinylchlorid-Vinylidenchlorid (95 : 5), Vinylchlorid-Trichlorethylen (95 : 5) und Vinylchlorid-2-Ethylhexylacrylat (80 : 20) ein. Die Polymergemische, die bei der Verwertung dieser Erfindung brauchbar sind, umfassen physikalische Gemische von wenigsten zwei bestimmten Polymerarten und enthalten 25 bis 95 Gew.-% Vinylhalogenidhomopolymer.
- Der Begriff basische Alkali- oder Erdalkalimetallverbindungen, wie hier verwendet, bedeutet Verbindungen, die aus der Gruppe der Oxide, Hydroxide, Sulfide, Silikate, Phosphate, Borate und Carbonate von Alkalimetallen und Erdalkalimetallen ausgewählt sind. Bevorzugt sind die Alkalimetalle Lithium, Natrium und Kalium und die Erdalkalimetalle Magnesium, Calcium, Strontium und Barium. Beispiele basischer Alkali- oder Erdalkalimetallverbindungen schließen, wenn auch nicht ausschließlich, Calciumhydroxid, Magnesiumhydroxid, Lithiumhydroxid, Natriumborat und Natriumsilikat ein.
- Die Menge einer jeden Komponente in den Stabilisatorzusammensetzungen dieser Erfindung kann über einen weiten Bereich variieren, doch umfassen sie allgemein in Gewichtsprozenten etwa 5 bis etwa 85%, vorzugsweise etwa 20 bis etwa 50%, bezogen auf das Zinkmercaptoester-Gewicht, und etwa 20 bis etwa 60%, vorzugsweise etwa 20 bis etwa 40%, bezogen auf das Gewicht der Organothioverbindung. Der Stabilisator kann auch 0 bis etwa 40%, vorzugsweise etwa 5 bis etwa 30% einer basischen Alkali- oder Erdalkaliverbindung enthalten. Obwohl festgestellt wurde, daß die Stabilisatorzusammensetzung nach dieser Erfindung besser als eine solche ist, in welcher die Organothioverbindung durch ein substituiertes Dihydropyridin ersetzt ist, ergibt eine Stabilisatorzusammensetzung nach dieser Erfindung, die eine Kombination der Organothioverbindung und des substituierten Dehydropyrins umfaßt, sowohl ausgezeichnete Früh- als auch Langzeitfarbenechtheit. So enthalten Stabilisatorzusammensetzungen nach dieser Erfindung 0 bis etwa 40% des substituierten Dihydropyridins der US-4,515,916. Wenn verwendet, liegt eine bevorzugte Menge des Dihydropyridins bei 5 bis etwa 30% des Gesamtgewichts der Stabilisatorzusammensetzung.
- Schmiermittel sind gegebenenfalls in der Stabilisatorzusammensetzung nach dieser Erfindung vorhanden wegen ihres wichtigen Effekts einer Reduzierung der Temperatur der Polymerzusammensetzungen während des Knetens und Extrudierens. Wenn verwendet, enthält die Stabilisatorzusammensetzung bis zu etwa 75 Gew.-%, vorzugsweise etwa 60 Gew.-% oder mehr eines Schmiermittels, wie eines Paraffinwachses, von Calciumstearat, Ethylen-bis-stearamid, Stearylstearat, Ce tylpalmitat und andere Esterwachse können verwendet werden. Von 0 bis etwa 15% eines teiloxidierten Polyethylens, wie Allied Chemical's AC629A-Produkt können als ein zusätzliches Schmiermittel in den Stabilisatorzusammensetzungen dieser Erfindung verwendet werden.
- Es wird leicht verständlich für einen Fachmann auf diesem technischen Gebiet sein, daß die genaue Menge an Stabilisatorzusammensetzung, die verwendet wird, von mehreren Faktoren abhängt, wie beispielsweise, doch nicht ausschließlich, dem verwendeten teilchenförmigen halogenhaltigen organischen Polymer, und die erforderliche Menge der Stabilisatorzusammensetzung wird um so größer sein, je länger die Zeit ist, die erforderlich ist, einem Abbau zu widerstehen. Im allgemeinen kann die wirksame Menge eines bevorzugten Stabilisators, d. h. eines solchen, der ein Schmiermittel und ein substituiertes Dihydropyridin enthält, so gering wie etwa 2,0 Gewichtsteile oder weniger je hundert Gewichtsteile des Polymers (phr) des halogenhaltigen Polymers sein. Ohne das Schmiermittel und das substituierte Dihydropyridin kann die Menge etwa 0,6 phr oder weniger sein. Obwohl es keine kritische Obergrenze für die Menge von Stabilisatorzusammensetzung gibt, führen Mengen oberhalb 3,5 phr des bevorzugten Stabilisators (2 phr Stabilisator ohne Schmiermittel oder substituiertem Dihydropyridin), bezogen auf das Gewicht des halogenhaltigen Polymers, keine verbesserte Steigerung der Effektivität. Stärker bevorzugt werden die Stabilisatorzusammensetzungen, die sowohl Schmiermittel als auch substituiertes Dihydropyridin enthalten, in Mengen verwendet, die im Bereich von etwa 2,0 bis etwa 3,0 Gewichts-phr des halogenhaltigen Polymers verwenden. Die bevorzugte Menge an Stabilisator ohne Schmiermittel und ohne substituiertes Dihydropyridin liegt bei etwa 0,6 bis etwa 1,0 phr.
- Die Organothioverbindungen und die Zinkmercaptoester werden vorzugsweise in den Polymerzusammensetzungen dieser Erfindung in der kleinsten Menge verwendet, die ausreicht, die erwünschte Widerstandsfähigkeit gegen Zersetzung in der Hitze den halogenhaltigen organischen Polymeren zu erteilen. Die halogenhaltigen organischen Polymerzusammensetzungen nach dieser Erfindung umfassen 0,1 bis etwa 1,2 phr, vorzugsweise etwa 0,2 bis etwa 0,4 phr der Organothioverbindung und etwa 0,2 phr bis etwa 1,7 phr, vorzugsweise von etwa 0,4 bis etwa 0,8 phr des Zinkmercaptoesters, bezogen auf das Gewicht der Polymerzusammensetzung. Vorzugsweise umfassen die Polymerzusammensetzungen etwa 0,1 bis etwa 0,8 phr einer basischen Alkali- oder Erdalkaliverbindung und etwa 0,1 bis etwa 0,8 Gew-phr des substituierten Dihydropyridins.
- Außer dem halogenhaltigen Polymer und der Stabilisatorzusammensetzung kann die Polymerzusammensetzung nach dieser Erfindung herkömmliche Zusatzstoffe enthalten, wie Füllstoffe, Pigmente, Weichmacher, Farbstoffe, Antioxidationsmittel und Ultraviolettlicht-Stabilisatoren. Materialien, wie kalzinierte Tone, Calciumcarbonat und Talkum, können als Füllstoffe verwendet werden. Geeignete Pigmente schließen Titandioxid, Ruß und Eisenoxid ein. Phthalate, Sebacate, Adipate, Phosphate und Fettsäureester mit 16 bis 150 Kohlenstoffatomen sind repräsentativ für wohlbekannte Weichmacher, die für die Zusammensetzungen dieser Erfindung geeignet sind. Geeignete Antioxi dationsmittel sind beispielsweise Tricresylphosphit, 2,6,-Di-t-butyl-4-methylphenol, 2,6,-Di-t-butyl-4-decyloxyphenol und 2-t-Butyl-4-octadecyloxyphenol.
- Die Polymerzusammensetzung dieser Erfindung kann nach Methoden, die dem Fachmann bekannt sind, und unter Verwendung herkömmlicher Gerätschaften hergestellt werden. Die Stabilisatorzusammensetzung kann zu dem halogenhaltigen Polymer unter kontinuierlichem Mischen in einem Mischer mit hoher Intensität, wie einem Henschel-Mischer, zugegeben werden. Die wesentliche Betrachtung ist jene, daß die Stabilisatorzusammensetzung und das halogenhaltige Polymer sorgfältig durchmischt werden.
- Die stabilisierten halogenhaltigen Polymerzusammensetzungen dieser Erfindung können verwendet werden, um Gegenstände, wie Röhren, zu fertigen. Verschiedene herkömmliche Formtechniken können benutzt werden, um die stabilisierten Zusammensetzungen in irgendeine erwünschte Form zu bringen. Die folgenden Beispiele erläutern die Erfindung.
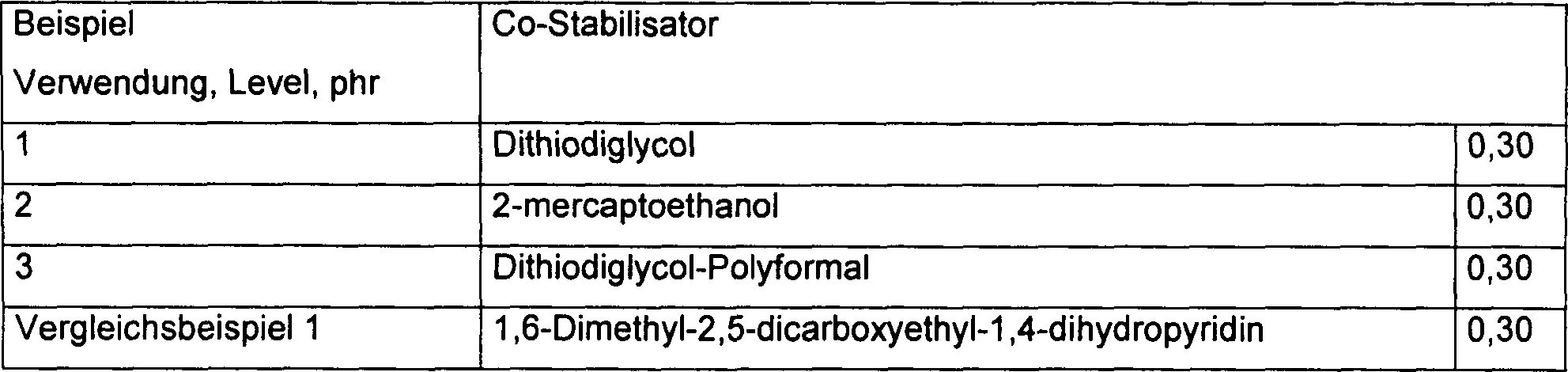
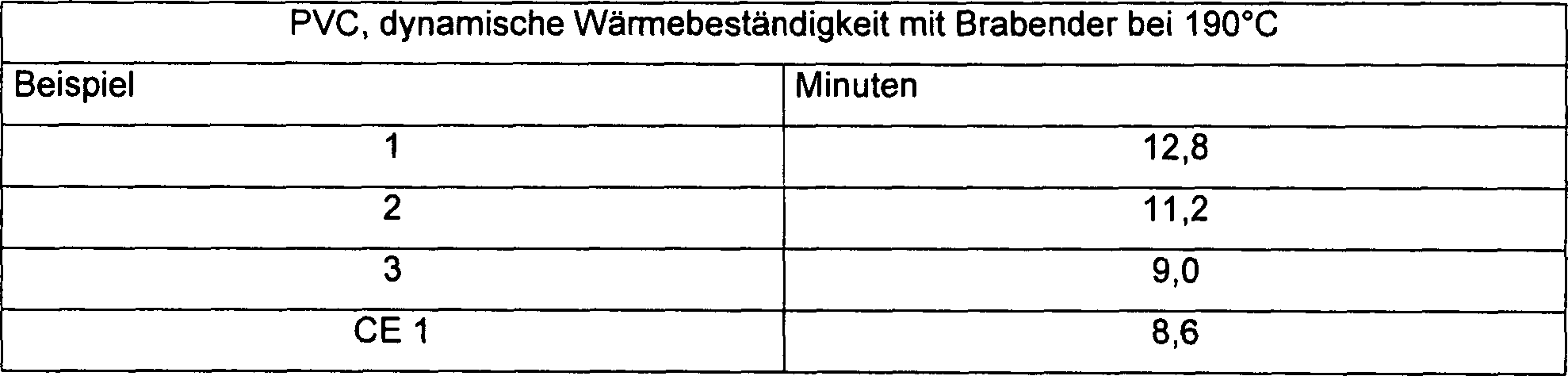
- Beispiele 1–3 und Vergleichsbeispiel 1
- Eine PVC-Röhrenzusammensetzung enthielt:
Bestandteil Menge PVC-Harz (k = 67) 100,0 Teile Calciumcarbonat 5,00 phr Titandioxid 1,0 phr Calciumstearat 0,45 phr Paraffinwachs 1,2 phr oxidiertes Polyethylen 0,15 phr Calciumhydroxid 0,3 phr Zink-bis-(2-ethylhexylthioglycolat) 0,4 phr - Beispiel 4 und Vergleichsbeispiel 2
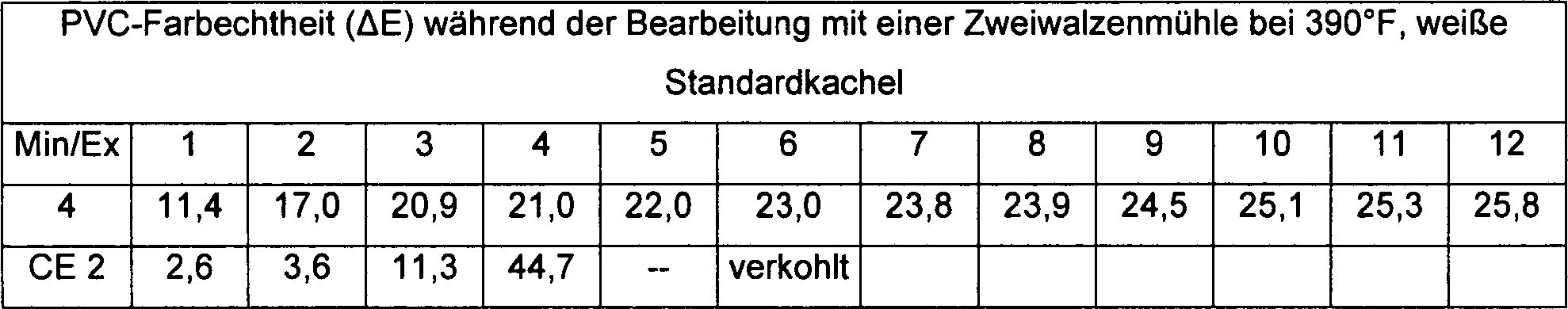
- Eine PVC-Röhrenzusammensetzung enthielt:
Bestandteil Menge PVC-Harz (k = 65) 100,0 Teile Calciumcarbonat 5,00 phr Titandioxid 1,0 phr Calciumstearat 0,60 phr Paraffinwachs 1,2 phr oxidiertes Polyethylen 0,15 phr - Die Zusammensetzung, wie in Tabelle IV gezeigt, modifiziert, und die resultierenden Zusammensetzungen wurden auf einer horizontalen Standard-Zweiwalzenmühle (Walzengeschwindigkeit 30F/40R) bei 390°F (199°C) verarbeitet, wobei Späne in Abständen von einer Minute abgenommen wurden. Die Farbeigenschaften der Späne wurden unter Verwendung eines Hunter Labs Kolorimeters (L, a, b) gemessen, und der Weißindex (WI) wurde als die Messung zum Vergleich in Tabelle V gewählt. Das DTS, gemessen wie oben beschrieben, aber bei 190°C und bei 60 Umdrehungen je Minute, ist in Tabelle VI gezeigt. Die Zusammensetzung in dem Vergleichsbeispiel 2 ist ähnlich jener der von Beispiel 13 in dem US-Patent Nr. 3,417,039 (Penneck).
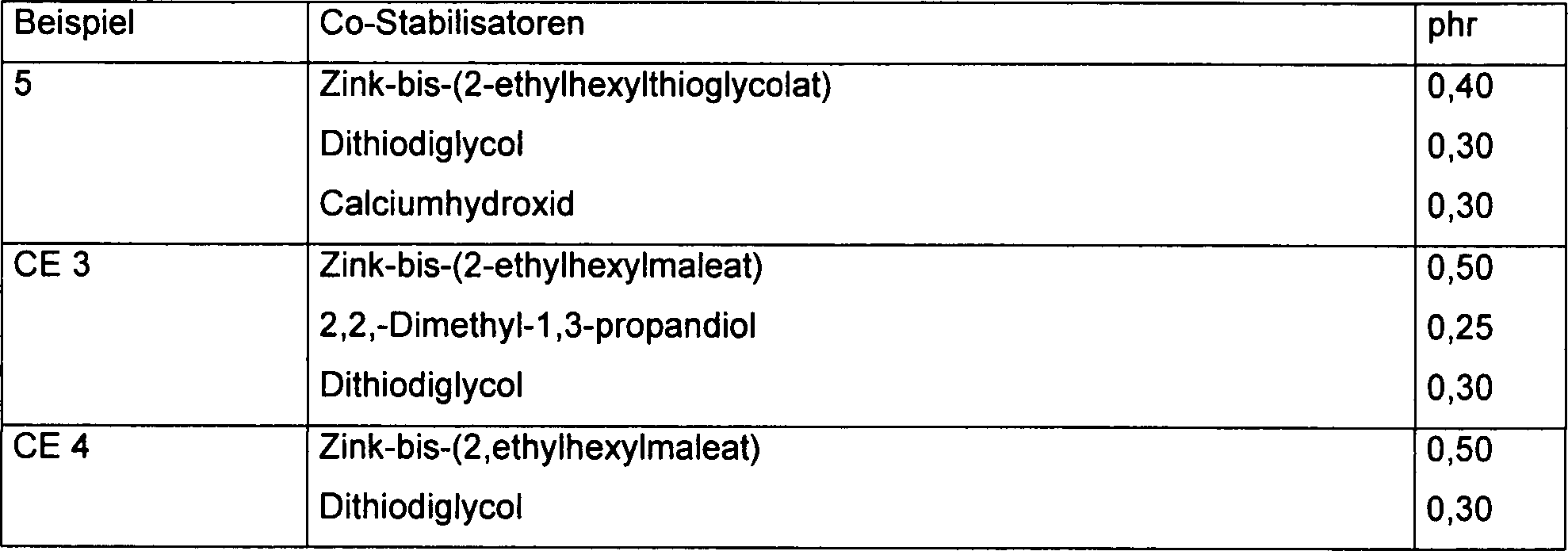
- Beispiel 5 und Vergleichsbeispiele 3 und 4
- Eine PVC-Röhrenzusammensetzung enthielt:
Bestandteil Menge PVC-Harz (k = 65) 100,0 Teile Calciumcarbonat 5,00 phr Titandioxid 1,0 phr Calciumstearat 0,60 phr Paraffinwachs 1,2 phr oxidiertes Polyethylen 0,15 phr - Es wurde, wie in Tabelle VII gezeigt, modifiziert und die resultierenden Zusammensetzungen wurden auf einer hoirzontalen Standard-Zweiwalzenmühle (Walzengeschwindigkeiten 30F/40R) bei 390°F (199°C) verarbeitet, wobei Späne in Abständen von einer Minute abgenommen wurden. Die Farbeigenschaften der Späne wurden unter Verwendung eines Hunter Labs Kolorimeters (L, a, b) gemessen, und die Gesamtenergie (ΔE) wurde als das Vergleichsmaß in Tabelle VIII gewählt.
Claims (16)
- Polymerzusammensetzung, die ein halogenhaltiges Polymer und eine Wärmestabilisatorzusammensetzung umfaßt, wobei diese Stabilisatorzusammensetzung: (A) eine Organothioverbindung ausgewählt unter Dithiodiglycol, Polyformalen und Polyacetalen dieses Dithiodiglycols und von Mercaptoalkanolen der allgemeinen Formel worin R1 und R2 gleich oder verschieden sind und Wasserstoff oder C1 bis C18-Alkyl bedeuten und i 0 oder eine ganze Zahl von 1 bis 6 einschließlich bedeutet, (B) 0,2 bis 1,7 Gewichtsteile je 100 Teile Polymer wenigstens eines Zinkmercaptoesters, ausgewählt unter (B1), einem Zinkmercaptosäureester mit der Formel Zn-[S(CH2)x-C(=O)OR]2, worin R ein Kohlenwasserstoffrest mit 2 bis 22 Kohlenstoffatomen ist und x 1 oder 2 ist, (B2) einen Zinkmercaptosäureester der Formel Zn-[S(CHR)a(CH2)b-[C(=O)O]R']2, worin R' Methyl oder C(=O)OR'' ist, R'' [(CH2-[C-(R*)(R2*)]yCH2O)2R3*] ist, R* H, Alkyl oder Hydroxyalkyl ist, R2* OH, Hydroxy-substituiertes Alkyl oder O(O=)C-R4* ist, R3* H, (O=)C-R4* oder Alkyl ist, R4* Alkyl oder Alkenyl ist, a = 0 oder 1, b = 1 oder 2, y = 0 oder 1 und z = 1 bis 4 mit der Maßgabe, daß, wenn z größer als 1 ist, y = 0, und (B3) einen Zinkmercaptoalkylcarbonsäureester der Formel Zn-[SCH2(CH2)qO-C(=O)R5*]2, worin R5* eine Alkyl- oder Alkenylgruppe mit 1 bis 18 Kohlenstoffatomen oder ein Arylrest mit 6 bis 12 Kohlenstoffatomen ist und q aus 1 bis 6 Kohlenstoffatomen besteht, (C) 0 bis 20 Gew.-%, bezogen auf die Stabilisatorzusammensetzung, einer basischen Alkali- oder Erdalkaliverbindung und (D) 0 bis 10 Gew.-%, bezogen auf die Stabilisatorzusammensetzung, eines substituierten Dihydropyridins umfaßt.
- Zusammensetzung nach Anspruch 1, worin die Organothioverbindung (A) ein Dithiodiglycol ist.
- Zusammensetzung nach Anspruch 1, worin die Organothioverbindung (A) ein Dithiodiglycolpolyformal ist.
- Zusammensetzung nach einem der vorausgehenden Ansprüche, bei der der Zinkmercaptoester der Zinkmercaptosäureester von B1 ist.
- Zusammensetzung nach Anspruch 4, in der x 1 ist und R 8 Kohlenstoffatome besitzt.
- Zusammensetzung nach einem der Ansprüche 1 bis 3, worin der Zinkmercaptoester der Zinkmercaptosäureester von B2 ist.
- Zusammensetzung nach Anspruch 6, worin r = 2 und R3 Alkyl ist.
- Zusammensetzung nach Anspruch 6, worin z = 1, y = 1 und R2 ist OH:
- Zusammensetzung nach Anspruch 6, worin z = 1, R3 (O=)C-R4 ist und R4 Alkyl ist.
- Zusammensetzung nach Anspruch 6, worin z = 1, y = 1, R1 Alkyl ist und R2 Hydroxyalkyl ist.
- Zusammensetzung nach einem der Ansprüche 1 bis 3, worin der Zinkmercaptoester das Zinkmercaptoalkyl von B3 ist.
- Zusammensetzung nach Anspruch 11, worin q 1 und R5* eine Alkylgruppe mit 1 bis 7 Kohlenstoffatomen ist.
- Zusammensetzung nach einem der vorausgehenden Ansprüche, worin ein substituiertes Dihydropyridin 5% bis 20% des Gesamtgewichtes der Stabilisatorzusammensetzung bildet.
- Zusammensetzung nach einem der vorausgehenden Ansprüche, worin eine basische Alkali- oder Erdalkalimetallverbindung 10% bis 15% des gesamten Gewichtes der Stabilisatorzusammensetzung bildet.
- Polymerzusammensetzung nach einem der vorausgehenden Ansprüche, worin die Menge der Stabilisatorzusammensetzung 0,4 bis 2,0% des Gesamtgewichtes ausmacht.
- Gegenstand aus einer Polymerzusammensetzung nach einem der vorausgehenden Ansprüche.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15390998A | 1998-09-16 | 1998-09-16 | |
| US153909 | 1998-09-16 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69918762D1 DE69918762D1 (de) | 2004-08-26 |
| DE69918762T2 true DE69918762T2 (de) | 2005-08-04 |
Family
ID=22549230
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69918762T Expired - Lifetime DE69918762T2 (de) | 1998-09-16 | 1999-09-14 | Kombination aus Organothioverbindung und Zink-Mercaptoester als Hitzestabilisator bei PVC-Herstellung |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US6462116B2 (de) |
| EP (1) | EP0987295B1 (de) |
| JP (1) | JP4334700B2 (de) |
| KR (1) | KR20000023159A (de) |
| CN (1) | CN1253144A (de) |
| AT (1) | ATE271581T1 (de) |
| AU (1) | AU732467B2 (de) |
| BR (1) | BR9904140A (de) |
| CA (1) | CA2280441A1 (de) |
| CO (1) | CO5211002A1 (de) |
| DE (1) | DE69918762T2 (de) |
| ID (1) | ID23636A (de) |
| SG (1) | SG81301A1 (de) |
| TW (1) | TW460524B (de) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MXPA02011789A (es) | 2001-12-06 | 2005-08-26 | Rohm & Haas | Composicion estabilizada de polimero, que contiene halogeno. |
| TW200303887A (en) * | 2002-03-07 | 2003-09-16 | Rohm & Haas | Organic based thermal stabilizers and heat stabilized polymer compositions |
| US20040063826A1 (en) * | 2002-09-30 | 2004-04-01 | Sobieski Robert T. | Halogen-containing vinyl polymer compounds |
| US20040061095A1 (en) * | 2002-09-30 | 2004-04-01 | Sobieski Robert T. | Halogen-containing vinyl polymer stabilizers |
| US7029759B2 (en) | 2002-09-30 | 2006-04-18 | Omnova Solutions Inc. | Halogen-containing vinyl polymer compositions |
| US7659331B2 (en) * | 2003-02-06 | 2010-02-09 | Honeywell International Inc | Shapeable resin compositions |
| US7087708B2 (en) * | 2003-04-17 | 2006-08-08 | Polymeright, Inc. | Poly ((polythioalkyl)esters), their applications and derivatives |
| US8158726B2 (en) | 2003-04-17 | 2012-04-17 | Polymeright, Inc. | Poly(thioesters), their applications and derivatives |
| JP2005113114A (ja) * | 2003-10-03 | 2005-04-28 | Rohm & Haas Co | ハロゲン含有ビニルポリマー用熱安定剤組成物 |
| US7488433B2 (en) * | 2004-07-30 | 2009-02-10 | Rohm And Haas Company | Thermal stabilizer compositions for halogen-containing vinyl polymers |
| CN1757669A (zh) * | 2004-10-08 | 2006-04-12 | 罗门哈斯公司 | 用于含卤素的烯类聚合物的热稳定剂组合物 |
| CN101440173B (zh) * | 2008-12-23 | 2011-08-31 | 南京工业大学 | 用于含氯聚合物热稳定体系的含硫锌皂组合物及其制备方法 |
| US8161246B2 (en) * | 2009-03-30 | 2012-04-17 | Via Technologies, Inc. | Prefetching of next physically sequential cache line after cache line that includes loaded page table entry |
| KR101415195B1 (ko) | 2012-08-22 | 2014-07-21 | 부산대학교 산학협력단 | Pvc 기반의 금속-고분자 나노복합체, 이를 포함하는 코팅 조성물 및 코팅막 |
| CN105694298B (zh) * | 2016-04-19 | 2017-08-25 | 南通鼎尚电子材料有限公司 | 耐热pvc |
| CN105713319B (zh) * | 2016-04-19 | 2017-07-21 | 汕头市升平塑胶制刷厂有限公司 | 一种耐热pvc |
| CN105801607B (zh) * | 2016-04-19 | 2018-05-22 | 广东共力建材有限公司 | 一种pvc热稳定剂及其制备方法 |
| CN105802074B (zh) * | 2016-04-19 | 2017-08-25 | 佛山市稳格家居用品有限公司 | 耐热pvc |
| CN105713320B (zh) * | 2016-04-19 | 2017-09-22 | 赖树兴 | Pvc用热稳定剂及其制备方法 |
| CN105885281B (zh) * | 2016-04-19 | 2017-10-17 | 赖树兴 | 一种pvc用热稳定剂及其制备方法 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2954362A (en) * | 1956-06-11 | 1960-09-27 | Union Carbide Corp | Stabilized vinyl chloride resin compositions |
| US3067166A (en) * | 1959-09-17 | 1962-12-04 | Ferro Corp | Stabilized halogen containing vinyl resins |
| NL270499A (de) * | 1960-10-24 | |||
| BE613012A (de) * | 1961-01-26 | |||
| GB1038723A (de) * | 1962-03-26 | |||
| NL292138A (de) * | 1962-05-01 | 1900-01-01 | ||
| GB1045245A (en) * | 1964-04-25 | 1966-10-12 | Bakelite Xylonite Ltd | Stabiliser compositions for chlorine-containing polymers |
| US3507827A (en) * | 1967-01-27 | 1970-04-21 | Argus Chem | Stabilizer composition for lessening early discoloration of polyvinyl chloride resins when heated |
| US3544510A (en) * | 1968-05-15 | 1970-12-01 | Cincinnati Milacron Chem | Mercaptal stabilized halogen-containing resins |
| US3647748A (en) * | 1969-02-19 | 1972-03-07 | Tenneco Chem | Stabilized vinyl halide resin compositions |
| US4111873A (en) * | 1976-06-07 | 1978-09-05 | American Cyanamid Company | Heat stabilized halogen-containing polymers |
| US4172207A (en) * | 1977-02-22 | 1979-10-23 | Mack Gerry P | Process for mercaptoalkanedicarboxylic acid esters |
| US4279806A (en) * | 1978-08-23 | 1981-07-21 | Associated Lead Inc. | Antimony mercaptides as processing stabilizers for vinyl halide resins |
| US4336168A (en) * | 1980-04-28 | 1982-06-22 | Tenneco Chemicals, Inc. | Stable liquid antimony stabilizer compositions and vinyl halide resins containing same |
| US4360619A (en) * | 1981-02-26 | 1982-11-23 | Carstab Corporation | Stabilizer compositions and polymers containing same |
| DE3274118D1 (en) * | 1981-06-02 | 1986-12-11 | Thiokol Morton Inc | Stabilising materials for halogen-containing polymers, polymer compositions containing the same and shaped articles formed therefrom |
| US4391757A (en) * | 1981-11-27 | 1983-07-05 | Carstab Corporation | Organic antimony containing stabilizer compositions for halogenated polymers |
| FR2524474A1 (fr) * | 1982-03-30 | 1983-10-07 | Rhone Poulenc Spec Chim | Procede de stabilisation de polymeres a base de chlorure de vinyle, compositions stabilisantes pour la mise en oeuvre du procede et polymeres ainsi stabilises |
| US4515916A (en) * | 1982-05-18 | 1985-05-07 | Morton Thiokol Inc. | Stabilizers for halogen containing polymers comprising zinc mercaptoesters, basic inorganic alkali or alkaline earth metal compounds and, substituted dihydropyridines |
| US4617334A (en) * | 1982-08-09 | 1986-10-14 | Morton Thiokol, Inc. | Stabilizer compositions for PVC |
| EP0133130B1 (de) * | 1983-08-02 | 1987-12-09 | Societe Nationale Elf Aquitaine | Verfahren zur Wärmestabilisierung von Polyvinylhalogeniden und die so stabilisierten Harze |
| DE3332003A1 (de) * | 1983-09-05 | 1985-03-21 | Henkel KGaA, 4000 Düsseldorf | Stabilisierte polyvinylchlorid-formmassen |
| DE3624079A1 (de) * | 1986-07-17 | 1988-01-21 | Huels Chemische Werke Ag | Stabilisierte polyvinylchlorid-harze |
| FR2617175B1 (fr) * | 1987-06-26 | 1989-10-27 | Kornbaum Simon | Procede de stabilisation des resines halogeno-vinyliques lors de leur transformation |
| US4810736A (en) * | 1987-12-07 | 1989-03-07 | Morton Thiokol, Inc. | Compositions for stabilizing halogen-containing organic polymers |
| US5278218A (en) * | 1990-12-10 | 1994-01-11 | Rhone-Poulenc Chimie | Zinc stannate/zinc hydroxystannate heat-stabilized chloropolymers |
| TW258744B (de) * | 1993-05-05 | 1995-10-01 | Morton Int Inc | |
| US5332772A (en) * | 1993-05-05 | 1994-07-26 | Morton International, Inc. | Combination heat stabilizer/lubricant for PVC processing and method for producing the same |
-
1999
- 1999-08-13 TW TW088113910A patent/TW460524B/zh not_active IP Right Cessation
- 1999-08-13 CA CA002280441A patent/CA2280441A1/en not_active Abandoned
- 1999-08-26 AU AU44712/99A patent/AU732467B2/en not_active Ceased
- 1999-09-06 ID IDP990843A patent/ID23636A/id unknown
- 1999-09-06 SG SG9904367A patent/SG81301A1/en unknown
- 1999-09-14 AT AT99307241T patent/ATE271581T1/de not_active IP Right Cessation
- 1999-09-14 EP EP99307241A patent/EP0987295B1/de not_active Expired - Lifetime
- 1999-09-14 BR BR9904140-5A patent/BR9904140A/pt not_active IP Right Cessation
- 1999-09-14 DE DE69918762T patent/DE69918762T2/de not_active Expired - Lifetime
- 1999-09-15 CO CO99058627A patent/CO5211002A1/es not_active Application Discontinuation
- 1999-09-15 KR KR1019990039470A patent/KR20000023159A/ko not_active Ceased
- 1999-09-16 JP JP26243699A patent/JP4334700B2/ja not_active Expired - Fee Related
- 1999-09-16 CN CN99120307A patent/CN1253144A/zh active Pending
-
2001
- 2001-05-30 US US09/870,080 patent/US6462116B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP0987295B1 (de) | 2004-07-21 |
| SG81301A1 (en) | 2001-06-19 |
| KR20000023159A (ko) | 2000-04-25 |
| AU4471299A (en) | 2000-04-06 |
| ATE271581T1 (de) | 2004-08-15 |
| TW460524B (en) | 2001-10-21 |
| JP2000095913A (ja) | 2000-04-04 |
| ID23636A (id) | 2000-05-04 |
| CO5211002A1 (es) | 2002-10-30 |
| DE69918762D1 (de) | 2004-08-26 |
| CN1253144A (zh) | 2000-05-17 |
| BR9904140A (pt) | 2000-10-10 |
| US20010036987A1 (en) | 2001-11-01 |
| CA2280441A1 (en) | 2000-03-16 |
| US6462116B2 (en) | 2002-10-08 |
| AU732467B2 (en) | 2001-04-26 |
| EP0987295A1 (de) | 2000-03-22 |
| JP4334700B2 (ja) | 2009-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69918762T2 (de) | Kombination aus Organothioverbindung und Zink-Mercaptoester als Hitzestabilisator bei PVC-Herstellung | |
| DE69120234T2 (de) | Stabilisierte, halogenhaltige Polymerzusammensetzung | |
| DE2822508C2 (de) | ||
| DE69516668T2 (de) | Polyolester-weichmacher für pvc | |
| DE2531308A1 (de) | Neue organozinnverbindungen und deren verwendung als stabilisator | |
| DE69918779T2 (de) | Latente Mercaptanstabilisatoren für verbesserte Witterungsbeständigkeit von klaren Halogenpolymerzusammensetzungen | |
| US4336168A (en) | Stable liquid antimony stabilizer compositions and vinyl halide resins containing same | |
| DE69912338T2 (de) | Ein latentes Merkaptan als Wärmestabilisator | |
| DE2802531C2 (de) | ||
| US4515916A (en) | Stabilizers for halogen containing polymers comprising zinc mercaptoesters, basic inorganic alkali or alkaline earth metal compounds and, substituted dihydropyridines | |
| DE69425089T2 (de) | Eine Kombination Wärmestabilisator/Gleitmittel für die PVC-Verarbeitung und Methode zur deren Herstellung | |
| DE68920139T2 (de) | Stabilisierungsmittel für halogenhaltige polymere. | |
| DE69419561T2 (de) | Polyolester von Zinkmercaptosäuren als Wärmestabilisatoren für die PVC Verarbeitung | |
| DE2559201B2 (de) | Organozinnverbindungen und ihre Verwendung als Stabilisatoren | |
| DE2719526A1 (de) | Organo-zinn-verbindungen und deren verwendung | |
| DE2703904A1 (de) | Stabilisatorzusammensetzung und sie enthaltende kunststoffzusammensetzung | |
| EP0070092B1 (de) | Stabilisatoren für halogenhaltige Polymere, diese enthaltende Polymerzusammensetzungen und daraus hergestellte geformte Gegenstände | |
| US4358555A (en) | Stabilizers for halogen containing polymers comprising alkyltin compounds, zinc mercaptoesters and basic alkali or alkaline earth metal compounds | |
| DE69913909T2 (de) | Ein wohlriechendes Verfahren zum Stabilisieren von Halogen-enthaltenden Polymeren | |
| DE60212307T2 (de) | Stabilisierte Halogenhaltige Polymerzusammensetzung | |
| DE2522510C2 (de) | Zusammensetzung zur Herstellung von zelligen Vinylchloridpolymeren | |
| DE2456278C3 (de) | Thermoplastische transparente und schlagfeste Masse auf der Grundlage von Vinylchlorid-Polymerisaten | |
| DE4300059C1 (de) | Verwendung von Monosalicylaten zweiwertiger Metalle zur Stabilisierung chlorhaltiger Polymere | |
| MXPA99007757A (en) | Combination of an organotio compound and a zinc ester market, as a thermoestabilizer in processing of |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8328 | Change in the person/name/address of the agent |
Representative=s name: MUELLER-BORE & PARTNER, PATENTANWAELTE, EUROPEAN PAT |
|
| 8327 | Change in the person/name/address of the patent owner |
Owner name: ROHM AND HAAS CHEMICALS LLC, PHILADELPHIA, PA., US |
|
| 8364 | No opposition during term of opposition |