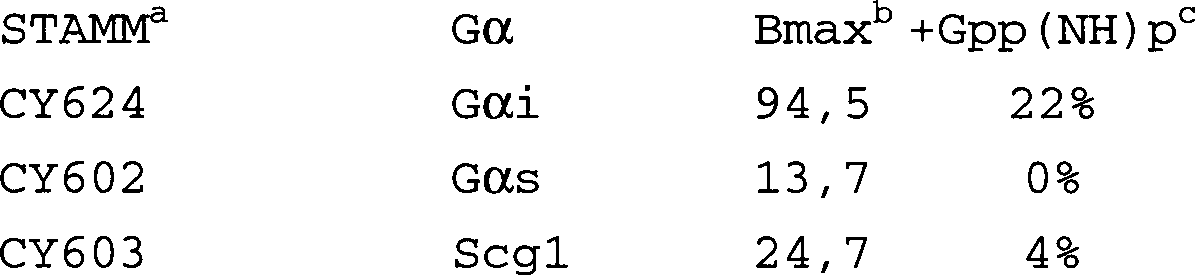-
Technisches
Gebiet der Erfindung
-
Die
vorliegende Erfindung betrifft Expressionskonstrukte für heterologe
G-Protein-gekoppelte Rezeptoren, derartige Rezeptoren exprimierende
Hefezellen, zur Herstellung solcher Zellen geeignete Vektoren sowie
Verfahren zur Herstellung und Verwendung davon.
-
Technischer
Hintergrund der Erfindung
-
Die
Wirkungen für
viele extrazelluläre
Signale, beispielsweise Neurotransmitter, Hormone, Duftstoffe und
Licht, werden von Rezeptoren mit sieben Transmembrandomänen (G-Protein-gekoppelten
Rezeptoren) sowie heterotrimären
guaninnukleotidbindenden regulatorischen Proteinen (G-Proteinen)
vermittelt. G-Proteine
umfassen drei Untereinheiten: eine guanylnukleotidbindende α-Untereinheit,
eine β-Untereinheit sowie
eine γ-Untereinheit
[für eine Übersicht,
siehe Conklin, B.R. und Bourne, H.R. (1993 Cell 73, 631-641]. Je
nachdem, ob GDP oder GTP an die α-Untereinheit
gebunden ist, zyklieren G-Proteine zwischen zwei Formen. Ist GDP gebunden,
so existiert das G-Protein als ein Heterotrimer in Form des Gαßγ-Komplexes. Ist GTP
gebunden, so dissoziiert die α-Untereinheit, wobei
ein Gβγ-Komplex
zurückbleibt.
Von Bedeutung ist dabei, daß,
wenn ein Gαβγ-Komplex
mit einem aktivierten G-Protein-gekoppelten Rezeptor in einer Zellmembran
operativ in Verbindung tritt, die Geschwindigkeit des Austauschs
von gebundenem GDP gegen GTP steigt und sich somit die Geschwindigkeit
der Dissoziation der gebundenen Gα-Untereinheit
vom Gβγ-Komplex erhöht. Die
freie Gα-Untereinheit
und der Gβγ-Komplex sind in der
Lage, ein Signal auf nachgeschaltete Elemente verschiedener Signaltransduktionswege
zu übertragen.
Dieses grundlegende Schema von Ereignissen bildet die Grundlage
für eine
Vielzahl unterschiedlicher Zellsignalisierungs phänomene. Für eine Übersicht, siehe H.G. Dohlman,
J. Thorner, M. Caron und R.J. Lefkowitz, Ann. Rev. Biochem, 60,
653-688 (1991). G-Protein-vermittelte Signalisierungssysteme sind
in so verschiedenen Organismen wie Hefe und Mensch vorhanden. Die
Hefe Saccharomyces cerevisiae wird als eukaryontischer Modellorganismus
genutzt. Aufgrund der Leichtigkeit, mit der sich die genetische
Konstitution der Hefe Saccharomyces cerevisiae manipulieren läßt, hat
sich unter den Forschern ein detailliertes Verständnis vieler komplexer biologischer
Wege herausgebildet. Dabei konnte bei zahlreichen Systemen demonstriert
werden, daß die
Proteinstruktur evolutionär
so konserviert ist, daß viele heterologe
Proteine ihre Hefeäquivalente
ersetzen können.
So können
beispielsweise Gα-Proteine aus Säugern heterotrimere
Komplexe mit Gβγ-Proteinen aus Hefe
bilden [Kang, Y.-S., Kane, J., Kurjan, J., Stadel, J.M. und Tipper,
D.J. (1990) Mol. Cell. Biol. 10, 2582-2590]. Ferner konnte von Murphy
et al. (J. Cell. Biochem. Bd. 18B, Seite 224, 1994) eine autokrine
Stimulierung der Hefe durch Austausch der Gα-Untereinheit der Hefe gegen ein modifiziertes
menschliches Gαi2 demonstriert werden. Dies repräsentiert
ein sehr spezifisches System, das auf der Expression des Angiotensin-II-Typ-Rezeptors
(der die menschliche G-Protein-α-Untereinheit (Gαi2) übernimmt)
und dem Angiotensin-II-Octapeptid als entsprechenden Liganden beruht.
Die G-Protein-gekoppelten Rezeptoren stellen wichtige Ziele für neue therapeutische
Arzneistoffe dar. Die Entdeckung solcher Arzneistoffe erfordert
notwendigerweise Screening-Tests mit hoher Spezifität und hohem
Durchsatz. So erfordert beispielsweise ein therapeutisches Eingreifen
in die Somatostatin-Wachstumshormon-Achse
neue chemische Wirkstoffe, die Somatostatinrezeptorsubtyp-selektiv
wirken. Bei dem Somatostatinrezeptor (SSTR) handelt es sich um einen
Prototyp der Klasse von Rezeptoren mit sieben Transmembrandomänen in Säugerzellen.
Das zyklische Tetradecapeptidsomatostatin wurde zuerst aus Hypothalamus isoliert,
und es konnte gezeigt werden, daß es sich dabei um einen starken
Inhibitor der Freisetzung von Wachstumshormon aus dem Hypophysenvorderlappen
handelt und daß es
breite modulatorische Wirkungen im ZNS und in peripheren Geweben
aufweist. Als Reaktion auf die Bindung von Somatostatin aktiviert
der SSTR ein heterotrimeres G-Protein, das wiederum die Aktivität verschiedener
Effektorproteine, einschließlich,
ohne darauf beschränkt
zu sein, Adenylatcyclasen, Ionenkanälen und Phospholipasen, modifiziert.
Die Somatostatineffekte werden über
die Wirkungsweise von in fünf
unterschiedlichen Rezeptorsubtypen codierten Genprodukten, die kürzlich kloniert werden
konnten, weitergeleitet [Strnad, J., Eppler, C.M., Corbett, M. und
Hadcock, J.R. (1993) BBRC 191, 968-976; Yamada, Y., Post, S.R.,
Wang, K., Tager, H.S., Bell, G.I. und Seino, S. (1992) Proc. Natl.
Acad. Sci. USA 89, 251-255; Meyerhof, W., Paust, H.-J., Schonrock,
C. und Richter, D. (1991); Kluxen, F.-W., Bruns, C. und Lubbert,
H. (1992) Proc. Natl. Acad. Sci. USA 89, 4618-4622; Li, X.-J., Forte,
M., North, R.A., Rose, C.A. und Snyder, S. (1992) J. Biol. Chem.
267, 21307-21312; Bruno, J.F., Xu, Y., Song, J. und Berelowitz,
M. (1992) Proc. Natl. Acad. Sci. USA 89, 11151-11154; O'Carrol, A.-M., Lolait,
S.J., Konig, M. und Mahan, L. (1992) Mol. Pharmacol. 42, 939-946].
Screening-Tests, bei denen zur Anpassung an die funktionelle Expression
der G-Protein-gekoppelten
Rezeptoren genetisch modifizierte Hefestämme eingesetzt werden, bieten
bei der Forschung an der Bindung von Liganden an den Somatostatinrezeptor
ebenso wie eine Reihe weiterer Rezeptoren, die mit verschiedenen
Krankheitszuständen
in Verbindung gebracht werden, signifikante Vorteile.
-
Kurze Beschreibung
der Erfindung
-
Ein
erster Aspekt der vorliegenden Erfindung richtet sich auf Expressionsvektoren
sowie damit transformierte Hefezellen, wobei die Vektoren eine erste,
für einen
G- Protein-gekoppelten
Rezeptor, beispielsweise den Somatostatinrezeptor, codierende heterologe
Nukleotidsequenz sowie eine zweite, für einen G-Protein-αßγ-Komplex in seiner
Gesamtheit oder einen Teil davon codierende Nukleotidsequenz enthalten.
In bestimmten Ausführungsformen
ist eine für
eine α-Untereinheit
eines heterologen G-Proteins codierende Nukleotidsequenz in ihrer
Gesamtheit oder teilweise an eine Nukleotidsequenz von der Hefe-G-Protein-α-Untereinheit
fusioniert. In bestimmten bevorzugten Ausführungsformen enthalten die
Expressionsvektoren und transformierten Zellen eine dritte heterologe
Nukleotidsequenz, die einen auf Pheromon reagierenden Promotor sowie
ein stromabwärts
von dem auf Pheromon reagierenden Promotor liegendes und damit operativ
assoziiertes Indikatorgen umfaßt.
Die Vektoren und Zellen können
ferner mehrere Mutationen enthalten. Dazu gehören 1) eine Mutation des SCG1/GPA1-Gens
aus Hefe, durch die das Hefe-Gα-Protein
inaktiviert wird, was die Wechselwirkung des heterologen Rezeptors
mit dem G-Protein erleichtert; 2) eine Mutation eines Hefegens, um
dessen Funktion zu inaktivieren und der Hefezelle zu ermöglichen,
trotz der Aktivierung des Signaltransduktionswegs der Reaktion auf
Pheromon weiterzuwachsen, wobei es sich hier bei bevorzugten Ausführungsformen
um Mutationen der Gene FAR1 und/oder FUS3 handelt, und 3) eine Mutation
eines Hefegens, deren Effekt in einem starken Anstieg der Empfindlichkeit
der Reaktion der Zelle auf die rezeptorabhängige Aktivierung des Signaltransduktionswegs
der Reaktion auf Pheromon besteht, wobei es sich bei bevorzugten
Genen diesbezüglich
um die Gene SST2, STE50, SGV1, STE2, STE3, PIK1, AFRI, MSG5 und
SIG1 handelt.
-
Bei
einem zweiten Aspekt der vorliegenden Erfindung handelt es sich
um ein chimärisches
Expressionskonstrukt sowie damit transformierte Hefezellen, wobei
das Konstrukt eine erste, für
einen Hefe-G-Protein-gekoppelten
Rezeptor codierende Nukleotidsequenz in operativer Assoziation mit
einer heterologen Nukleotidsequenz, die für einen heterologen G-Protein-gekoppelten Rezeptor
codiert, umfaßt.
Dabei können
die Konstrukte und Zellen eine zweite heterologe Nukleotidsequenz
enthalten, die einen auf Pheromon reagierenden Promotor sowie ein
stromabwärts
von dem auf Pheromon reagierenden Promotor liegendes und mit diesem
operativ assoziiertes Indikatorgen umfaßt. Die Konstrukte und Zellen
können
ferner mehrere Mutationen enthalten. Zu diesen gehören 1) eine
Mutation eines Hefegens, um dessen Funktion zu inaktivieren und
der Hefezelle zu ermöglichen,
trotz der Aktivierung des Signaltransduktionswegs der Reaktion auf
Pheromon weiterzuwachsen, wobei es sich hier bei bevorzugten Ausführungsformen
um Mutationen der Gene FAR1 und/oder FUS3 handelt, und 2) eine Mutation
eines Hefegens, deren Effekt in einem starken Anstieg der Empfindlichkeit
der Reaktion der Zelle auf die rezeptorabhängige Aktivierung des Signaltransduktionswegs
der Reaktion auf Pheromon besteht, wobei es sich bei bevorzugten
Genen diesbezüglich
um die Gene SST2, STE50, SGV1, STE2, STE3, PIK1, AFRI, MSG5 und
SIG1 handelt. Ein produktives Signal wird in einem Bioassay durch
Kopplung des heterologen Rezeptors an ein Hefeprotein nachgewiesen.
-
Bei
einem dritten Aspekt der vorliegenden Erfindung handelt es sich
um ein Verfahren zum Testen von Verbindungen zur Bestimmung der
Auswirkungen einer Ligandenbindung an die heterologen Rezeptoren durch
Messung der Auswirkungen auf das Zellwachstum. In bestimmten bevorzugten
Ausführungsformen
werden dabei Hefezellen der oben beschriebenen Art in zur Auslösung der
Expression heterologer Proteine geeignetem Wachstumsmedium kultiviert,
in Agar-Wachstumsmedium eingebettet und auf die Oberfläche der Agarplatten
ausgebrachten Verbindungen ausgesetzt. Dabei erwartet man Auswirkungen
auf das Wachstum der eingebetteten Zellen um Verbindungen herum,
die den heterologen Rezeptor aktivieren. Ein verstärktes Wachstum
könnte
bei Verbindungen, die als Agonisten wirken, beobachtet werden, während ein
reduziertes Wachstum bei solchen, die als Antagonisten wirken, beobachtet
werden könnte.
-
Kurze Beschreibung
der Zeichnungen
-
1.
Die angegebenen Gα-Expressionsplasmide
enthaltende Stämme
werden mit Paarungspheromon (α-Faktor) behandelt.
Ein Maß für die erhaltene
Signaltransduktion wird durch ein FUS1-lacZ tragendes Reporterplasmid
bereitgestellt. Die Daten sind als Prozent β-Galactosidaseaktivität, gemessen
in einem lediglich das Wildtyp-Gα-Protein
exprimierenden Stamm, dargestellt.
-
2.
Das angegebene CUP1p-Gα-Expressionsplasmid
enthaltende Stämme,
die in die angegebene Kupferkonzentration enthaltendem Medium angezogen
wurden, werden mit Paarungspheromon (α-Faktor) behandelt. Ein Maß für die erhaltene
Signaltransduktion wird durch ein FUS1-lacZ tragendes Reporterplasmid bereitgestellt.
Die Daten sind als Prozent β-Galactosidaseaktivität, gemessen
in einem kein exogenes Gα-Protein
exprimierenden Stamm, dargestellt.
-
3.
Sättigungsbindung
von 3H-Spiperon an aus einem den Serotoninrezeptor
5HT1a exprimierenden Stamm (CY382) präparierte Hefemembranfraktionen.
Bmax = 3,2 pmol/mg Protein; Kd – 115
nM.
-
4.
Aminoterminale chimärische
Ste2/5HT1a-Rezeptoren.
Der CHI11-Rezeptor enthält
die ersten 14 Aminosäuren
des Hefeproteins Ste2. Der CHI17-Rezeptor weist einen Austausch
des Aminoterminus des Rezeptors 5HT1a über die ersten beiden Transmembrandomänen gegen
den entsprechenden Bereich des Rezeptors Ste2 auf. Der CHI18-Rezeptor
weist die gleichen Ste2-Sequenzen auf, und zwar direkt an den Aminoterminus
des 5HT1a- Rezeptors
fusioniert, so daß ein
Rezeptor erzeugt wird, von dem vorhergesagt wird, daß er die
Zellmembran neunmal überspannt.
Die Bmax-Werte wurden durch Messen der maximalen Bindung des radioaktiv
markierten Liganden 3H-Spiperon bestimmt. Die Werte sind als pmol
gebundener radioaktiv markierter Ligand pro mg Gesamtprotein angegeben.
-
5.
Analyse der kompetitiven Bindung der Agonisten Isoproterenol oder
Epinephrin gegenüber 125I-Cyanopindolol mit von einem den β2-adrenergen
Rezeptor exprimierenden Wildtyp-Hefestamm präparierten Rohmembranextrakten.
Die Daten sind als Prozent Maximalbindung des radioaktiv markierten
Liganden dargestellt. IC50-Werte = 10 nM, Isoproterenol;
200 nM, Epinephrin.
-
6.
Analyse der kompetitiven Bindung der Agonisten Isoproterenol oder
Epinephrin gegenüber 125I-Cyanopindolol mit aus einem den β2-adrenergen
Rezeptor sowie Säuger-Gαs coexprimierenden
Hefestamm präparierten
Extrakten. Die Daten sind als Prozent Maximalbindung des radioaktiv
markierten Liganden dargestellt. IC50-Werte = 10 nM, Isoproterenol;
60 nM, Epinephrin.
-
7.
Sättigungsbindung
von [125I]tyr11S-14
an Membranen von den SSTR2-Subtyp sowie Scgl/Giα2 coexprimierenden
Hefezellen. Membranen von den SSTR2-Subtyp exprimierenden Hefezellen wurden
wie unter Experimentelle Vorgehensweisen beschrieben präpariert.
Die Sättigungsbindung
wurde mit 20-1600 pM [125I]tyr11S-14 durchgeführt. Die
nichtspezifische Bindung für
jeden Punkt in Form von gebundenen cpm in Gegenwart von 1 μM kaltem
S-14 reichte von 10 bis 40%. Dargestellt ist ein mit Doppelbestimmung
durchgeführtes
repräsentatives
Experiment.
-
8.
Immunoblot, der die Expression des Somatostatinrezeptors zeigt.
Membranfraktionen wurden aus den angegebenen Hefestämmen isoliert.
Teilmengen von 5 bis 30 μm
Protein werden mittels Polyacrylamidgelelektrophorese/Western-Blot-Analyse
untersucht. Die Molekulargewichtsmarker sind in Kilodalton angegeben.
Die Somatostatinrezeptor-Proteinbanden
sind mit Pfeilen gekennzeichnet. Mehrere Spezies dieses Rezeptors
sind zu sehen, und zwar Doppel- sowie Dreifachbanden zusätzlich zu
dem 43 kd großen
einfachen Rezeptor. Spuren 1+2: CY602 (siehe Tabelle 1); 3+4: CY603;
5+6: CY624; 7: keinen Rezeptor exprimierender kongener Stamm.
-
9.
Immunoblot, der die Expression des muskarinischen Acetylcholinrezeptors
(mAchR) zeigt. Membranfraktionen werden aus den angegebenen Hefestämmen isoliert.
Teilmengen von jeweils 30 μg
Protein werden mittels Polyacrylamidgelelektrophorese/Western-Blot-Analyse,
wie im Text beschrieben, untersucht. Die Molekulargewichtsmarker
sind in Kilodalton angegeben. mAchR-Proteinbanden sind mit Pfeilen gekennzeichnet.
-
10. Immunoblot, der die Expression von α2-AR zeigt.
Membranfraktionen werden aus den angegebenen Hefestämmen isoliert.
Teilmengen von jeweils 30 μg
Protein werden mittels Polyacrylamidgelelektrophorese/Western-Blot-Analyse
untersucht. Die Molekulargewichtsmarker sind in Kilodalton angegeben. α2-AR-Proteinbanden sind
mit Pfeilen gekennzeichnet.
-
11. Somatostatinrezeptor-Expressionsplasmid pJH1.
-
12. G-Protein-Expressionsplasmid pLP82.
-
13 (A&B).
Dosisabhängige
Reaktion des Wachstums von Hefezellen auf Somatostatin. Kulturen des
Hefestamms LY268 werden in Agar (obere Platte) eingebettet oder
gleichmäßig über die
Oberfläche
von Agarplatten ausgestrichen (untere Platte) und den angegebenen,
auf oben auf den Agar gelegte Papierscheibchen punktförmig aufgetragenen
Mengen an den genannten Verbindungen ausgesetzt. Die Platten werden
bei 30°C
inkubiert.
-
14 (A,B,C,&D). Die Reaktion des Wachstums von
Somatostatin ausgesetzten Hefezellen hängt von der Menge des exprimierten
chimärischen
G-Proteins ab. Kulturen von im Text beschriebenen Hefestämmen werden
in Agar eingebettet und den angegebenen, auf oben auf den Agar gelegte
Papierscheibchen punktförmig
aufgetragenen Mengen an den genannten Verbindungen ausgesetzt. Die
Platten werden bei 30°C inkubiert.
-
15 (A,B,C,&D). Die Reaktion des Wachstums von
Somatostatin ausgesetzten Hefezellen hängt von der Menge des exprimierten
Hefe-G-Proteins ab. Kulturen von im Text beschriebenen Hefestämmen werden
in Agar eingebettet und den angegebenen, auf oben auf den Agar gelegte
Papierscheibchen punktförmig aufgetragenen
Mengen an den genannten Verbindungen ausgesetzt. Die Platten werden
bei 30°C
inkubiert.
-
16 (A&B).
Hefezellen, die eine Mutation im sst2-Gen zeigen, zeigen eine erhöhte Resistenz
gegenüber
AT, wenn sie Paarungspheromon ausgesetzt werden. Kulturen von Hefestämmen werden
in Agar eingebettet und den angegebenen, auf oben auf den Agar gelegte
Papierscheibchen punktförmig
aufgetragenen Mengen an α-Paarungsfaktor ausgesetzt.
Die Platten werden bei 30°C
inkubiert.
-
17 (A,B,C,&D). Eine Mutation im sst2-Gen verbessert
das Wachstum der Somatostatin ausgesetzten Hefezellen. Kulturen
von im Text beschriebenen Hefestämmen
werden in Agar eingebettet und den angegebenen, auf oben auf den
Agar gelegte Papierscheibchen punktförmig aufgetragenen Mengen an
den genannten Verbindungen ausgesetzt. Die Platten werden bei 30°C inkubiert.
-
18. Ligandenbindung an den in Hefe exprimierten
CCKB-Rezeptor der Ratte. Aus Über-Nacht-Flüssigkulturen
von LY613-Zellen wurden Rohmembranfraktionen präpariert und danach wie in Methoden
und Material beschrieben Sättigungsagonistenbindungstests
durchgeführt.
Die Sättigungsbindung wurde
mit 4-60 nM[3H] CCK-8 (25 μg Protein/Röhrchen)
durchgeführt.
Die nichtspezifische Bindung für
jeden Punkt in Form von gebundenen cpm in Gegenwart von 1 μM kaltem
CCK-8 reichte von 20 bis 60%. Dargestellt ist ein mit Doppelbestimmung
durchgeführtes
repräsentatives
Experiment.
-
19 (A&B).
Wachstum von Hefe als Reaktion auf CCKB-Rezeptoragonisten.
Hefestämme,
die den CCKB-Rezeptor der Ratte funktionell
exprimieren (LY628, LLY631), wurden wie in Material und Methoden
beschrieben kultiviert und auf SC-Galactose (2%)-ura, trp, his-Agarmedium
ausplattiert (2 × 104 Zellen/ml). Sterile Filterscheibchen wurden
auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl DMSO, das jeweils eine Menge
von 10 μl
der angegebenen Verbindungen enthielt, gesättigt. Anschließend wurden
die Platten 3 Tage bei 30°C
inkubiert. (A) CCK-8, (B) CCK-4.
-
20. A2a-Adenosinrezeptor-Sättigungsbindungstest.
Radioligandenbindungstests wurden in 96-Loch-Mikroliterplatten unter Verwendung von
Bindungspuffern (50 nM HEPES, pH 7,4, 10 mM MgCl2, 0,25%
BSA) mit Proteaseinhibitoren (5 μg/ml
Leupeptin, 5 μg/ml
Aprotinin, 100 μg/ml
Bacitracin und 100 μg/ml Benzamidin)
durchgeführt.
Alle Komponenten wurden in Proteaseinhibitoren enthaltendem Bindungspuffer verdünnt und
in der folgenden Reihenfolge in die Löcher der Mikroliterplatte gegeben:
Bindungspuffer, kalter Kompetitor (NECA, Endkonzentration 1 μM), [3H]NECA (1-50 nM). Die Bindungsreaktionen
wurden durch Zugabe von 82 μg
Membranprotein in einem Volumen von 170 μl gestartet. Das endgültige Reaktionsvolumen betrug
200 μl/Loch.
Alle Inkubationen wurden über
einen Zeitraum von 2 Stunden bei Raumtemperatur durchgeführt. Freier
Radioligand wurde von gebundenem Liganden mittels schneller Filtration
durch ein Glasfaserfilter unter Verwendung eines Zellernters von
der Firma Inotech getrennt. Die Filterscheibchen wurden danach mehrere
Male mit kaltem (4°C)
Bindungspuffer ohne BSA vor dem Zählen gewaschen.
-
21. Wachstum von Hefe als Reaktion auf A2A-Adenonsinrezeptoragonisten.
Wie in Material und Methoden beschrieben kultivierte LY595-Zellen
wurden auf SC-Galactose (2%)-ura, trp, his-Agarmedium (2 × 104 Zellen/ml) ausplattiert. Sterile Filterscheibchen
wurden auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl DMSO, das die 10 μg der angegebenen
Verbindungen enthielt, gesättigt.
Anschließend
wurden die Platten 3 Tage bei 30°C
inkubiert. (A, B) CGS-21680, (B) NECA (C) DPMA.
-
22. Wachstum von SSTR5 enthaltenden Hefezellen
als Reaktion auf Somatostatinrezeptoragonisten. Wie in Material
und Methoden beschrieben kultivierte LY620-Zellen wurden auf SC-Galactose (2%)-ura,
trp, his-Agarmedium
(2 × 104 Zellen/ml) ausplattiert. Sterile Filterscheibchen
wurden auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl sterilem Wasser, das die angegebenen
Mengen der angegebenen Verbindungen enthielt, gesättigt. Anschließend wurden
die Platten 3 Tage bei 30°C
inkubiert. (A) 60 nmol S-14, (B) 30 nmol S-28.
-
23. Wachstum von Schweine-SSTR2 enthaltenden Hefezellen
als Reaktion auf Somatostatinrezeptoragonisten. LY474 (zwei unabhängige Isolate:
21,22) wurden wie in Material und Methoden beschrieben kultiviert
und auf SC-Galactose (2%)-ura, trp, his-Agarmedium (2 × 104 Zellen/ml)
ausplattiert. Sterile Filterscheibchen wurden auf die Oberfläche des verfestigten
Agars gelegt und mit 10 μl
sterilem Wasser, das die angegebenen Mengen der angegebenen Verbindungen
enthielt, gesättigt.
Anschließend
wurden die Platten 3 Tage bei 30°C
inkubiert. (1) 600 pmol, (2) 60 pmol.
-
24. Die Deletion von MSG5 erhöht die Empfindlichkeit des
Hefe-Biotests. Kulturen von Hefestämmen wurden zur Expression
des SSTR2 wie in Material und Methoden beschrieben induziert und
auf SC-Galactose
(2%)-ura, trp, his-Agarmedium (2 × 104 Zellen/ml)
ausplattiert. Sterile Filterscheibchen wurden auf die Oberfläche des
verfestigten Agars gelegt und mit 10 μl sterilem Wasser, das die angegebenen
Mengen an S-14 enthielt, gesättigt.
Anschließend
wurden die Platten 3 Tage bei 30°C
inkubiert. (A) MPY459 sst2ΔADE2 msg5ΔLEU2, (B)
MPY458 SST2 msg5ΔLEU2,
(C) LY288 SST2 MSG5, (D) LY268 sst2ΔADE2 MSG5.
-
25 (A&B).
Wachstum von Hefe als Reaktion auf GRF-rezeptoragonisten. Wie in Material und
Methoden beschrieben kultivierte CY990-Zellen wurden auf SC-Galactose (2%)-ura,
trp, his-Agarmedium (2 × 104 Zellen/ml) ausplattiert. Sterile Filterscheibchen
wurden auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl sterilem Wasser, das 20 nmol
der angegebenen Verbindungen enthielt, gesättigt. Anschließend wurden
die Platten 3 Tage bei 30°C
inkubiert. (A) hGRF(1-29)-NH2, (B) hGRF
(1-29), (D-arg2)-hGRF(1-29).
-
26 (A&B).
Auswirkung der Überexpression
von STE50 auf den SSTR2-Biotest. Das Testmedium sowie die Hefestämme wurden
wie in Material und Methoden beschrieben hergestellt. Platte A enthält den STE50-Überexpressionsstamm CY560;
Platte B enthält
den Kontrollstamm CY562. Auf jede Platte wurden mit Lösungen der
folgenden Peptide gesättigte
Filterscheibchen aufgebracht: 1 mM Hefe-α-Pheromon (links, Mitte), 1 μg/ml Somatostatin-14
(rechts, oben), 100 μg/ml
Somatostatin-14 (rechts, unten). Die Platten wurden 3 Tage bei 30°C inkubiert.
-
27 (A&B).
Biotest von Verbindungen mit Somatostatinrezeptor- und/oder Antagonisteneigenschaften.
LY364-Zellen wurden auf SC-Galactose (2%)-ura, trp, his-Agarmedium
(2 × 104 Zellen/ml) ausplattiert. Für den Antagonistentest
wurde Somatostatin (20 nM S-14)
vor dem Gießen
zu dem geschmolzenen Agar gegeben. Sterile Filterscheibchen wurden
auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl sterilem Wasser, das die Testverbindungen
enthielt, gesättigt.
Anschließend
wurden die Platten 3 Tage bei 30°C
inkubiert. (Links) Test für
Somatostatinagonisten. Somatostatin (S-14) wurde auf Positionen
in der unteren Reihe, linke Seite aufgetragen (6 nmol, 600 pmol,
60 pmol, 600 pmol), (Rechts) Test für Somatostatinantagonisten.
Somatostatin (S-14) wurde auf Positionen in der unteren Reihe, linke
Seite aufgetragen (6 nmol, 600 pmol, 60 pmol, 600 pmol).
-
28 (A&B)
Fusion von STE2-Sequenzen an den Aminoterminus von SSTR2 reduziert
die Signalisierungseffizienz als Reaktion auf Somatostatin. LY268-
und LY322-Zellen wurden auf SC-Galactose (2%)-ura, trp, his-Agarmedium
ausplattiert (2 × 104 Zellen/ml). Sterile Filterscheibchen wurden
auf die Oberfläche
des verfestigten Agars gelegt und mit 10 μl Somatostatin (S-14) gesättigt. Anschließend wurden
die Platten 3 Tage bei 30°C
inkubiert. (A) LY268. S-14 wurde im Uhrzeigersinn von oben auf Filterscheibchen
aufgetragen: Träger,
60 nmol, 6 nmol, 600 pmol, 60 pmol, 6 pmol. (B) LY322. S-14 wurde
im Uhrzeigersinn von oben auf Filterscheibchen aufgetragen: 0,6
pmol, Träger,
60 nmol, 6 nmol, 600 pmol, 60 pmol, 6 pmol.
-
Ausführliche
Beschreibung der Erfindung
-
Nukleotidbasen
werden im vorliegenden Text wie folgt abgekürzt:
| A-Adenin | G-Guanin |
| C-Cytosin | T-Thymin |
| U-Uracil
(hier
manchmal mit „ura" abgekürzt) | |
-
Aminosäurereste
werden im vorliegenden Text entweder auf drei Buchstaben oder einen
einzigen Buchstaben wie folgt abgekürzt:
| Ala;
A-Alanin | Leu;
L-Leucin |
| Arg;
R-Arginin | Lys;
K-Lysin |
| Asn;
N-Asparagin | Met;
M-Methionin |
| Asp;
D-Asparaginsäure | Phe;
F-Phenylalanin |
| Cys;
C-Cystein | Pro;
P-Prolin |
| Gln;
Q-Glutamin | Ser;
S-Serin |
| Glu;
E-Glutaminsäure | Thr;
T-Threonin |
| Gly;
G-Glycin | Trp;
W-Tryptophan |
| His;
H-Histidin | Tyr;
Y-Tyrosin |
| Ile;
I-Isoleucin | Val;
V-Valin |
-
Die
Begriffe „DNA" und „Nukleotidsequenz" werden gegeneinander
austauschbar verwendet und sollen ohne Beschränkung alle Formen linearer
Polymere, die Nukleotidbasen umfassen, einschließen, einschließlich gegebenenfalls
RNA.
-
Der
Begriff „Säuger", wie er hier verwendet
wird, bezieht sich auf eine beliebige Säugerspezies (z.B. Mensch, Maus,
Ratte und Affe).
-
Der
Begriff „heterolog" wird hier in bezug
auf Hefe verwendet und bezieht sich somit auf DNA-Sequenzen, Proteine
und andere Materialien, die aus anderen Organismen als Hefe stammen
(z.B. Säuger,
Vögel, Amphibien,
Insekten, Pflanzen), oder auf Kombinationen davon, die nicht natürlicherweise
in der Hefe angetroffen werden.
-
Der
Begriff „stromaufwärts" bzw. „stromabwärts" wird hier unter
Bezug auf die Richtung der Transkription und Translation verwendet,
wobei eine vor einer anderen Sequenz transkribierte oder translatierte
Sequenz als „stromaufwärts" von der letzteren
liegend bezeichnet wird.
-
Alle
G-Protein-gekoppelten Rezeptoren oder Teile davon können ebenso
wie die sie codierenden Nukleotidsequenzen zur Praktizierung der
vorliegenden Erfindung eingesetzt werden. Zu derartigen Rezeptoren gehören beispielsweise,
ohne jedoch darauf beschränkt
zu sein, Adenosinrezeptoren, Somatostatinrezeptoren, Dopaminrezeptoren,
Cholecystokininrezeptoren, muskarinische cholinerge Rezeptoren, α-adrenerge
Rezeptoren, β-adrenerge Rezeptoren,
Opiatrezeptoren, Cannabinoidrezeptoren sowie Rezeptoren für Wachstumshormon
freisetzender Faktor, Glucagon und Serotonin. Der Begriff Rezeptor,
wie er hier verwendet wird, soll Subtypen der genannten Rezeptoren
sowie Mutanten und Homologe davon zusammen mit den diese codierenden
Nukleotidsequenzen umfassen. Dem Fachmann ist ebenso ersichtlich,
daß in
manchen Fällen
nicht der gesamte Rezeptor exprimiert zu werden braucht, um die
gewünschten
Zwecke zu erzielen. Dementsprechend soll der Rezeptor verkürzte Formeln
sowie andere Formvarianten eines gegebenen Rezeptors ohne Beschränkung umfassen.
-
Zur
Praktizierung der folgenden Erfindung können alle DNA-Sequenzen, die
für eine
Gα-Untereinheit (Gα) codieren,
verwendet werden. Zu den Gα-Untereinheiten
gehören
beispielsweise, ohne darauf beschränkt zu sein, Gs-Untereinheiten,
Gi-Untereinheiten, Go-Untereinheiten,
Gz-Untereinheiten sowie Gq-, G11-, G16- und transduzierende Untereinheiten.
Zu den zur Praktizierung der folgenden Erfindung geeigneten G-Proteinen und Untereinheiten
gehören
Subtypen sowie Mutanten und Homologe davon zusammen mit den diese codierenden
DNA-Sequenzen.
-
Einem
Fachmann ist aus den Lehren, wie sie hier dargestellt sind, ersichtlich,
daß die
für die
Konstrukte und Hefezellen der vorliegenden Erfindung geeigneten
G-Proteine heterologe
Gα-Untereinheiten,
Hefe-Gα-Untereinheiten oder
chimärische
Hefe-/heterologe Versionen umfassen können. Dabei ist leicht bestimmbar,
welche Konfiguration sich am besten für eine angemessene Kopplung
an einen bestimmten heterologen Rezeptor eignet, indem man einfach,
wie hier gelehrt, Vektoren konstruiert und die Signalgebung der Ligandenbindung
als Reaktion auf einen gegebenen Test mißt. In bestimmten bevorzugten
Ausführungsformen
ist Gαi2 die Gα-Untereinheit
der Wahl, insbesondere, wenn es sich bei dem heterologen G-gekoppelten-Protein
um einen vollständigen
Somatostatinrezeptor oder einen Teil davon handelt. In diesem Fall
ist es besonders bevorzugt, daß die
Gαi2-Untereinheit an einen Hefe-Gβγ-Komplex gekoppelt
wird. Ebenso können bestimmte
chimärische
Konstrukte eine verbesserte Signaltransduktion im Hinblick auf bestimmte
heterologe Rezeptoren liefern. Dabei ist ein chimärisches
Konstrukt, das aus der Fusion der aminoterminalen Domäne des Hefe-GPA1/SCG1 mit der
carboxyterminalen Domäne
eines heterologen Gαi, Gαs und vor allem Gαi2 hervorgeht,
besonders bevorzugt.
-
Zur
Praktizierung der vorliegenden Erfindung können alle DNA-Sequenzen, die
für eine
Gβγ-Untereinheit
(Gβγ) codieren,
verwendet werden. Zu den zur Praktizierung der vorliegenden Erfindung
geeigneten G-Proteinen und Untereinheiten gehören Subtypen sowie Mutanten
und Homologe davon zusammen mit den diese codierenden DNA-Sequenzen. Die Wirtszellen
können
dabei entweder endogenes Gβγ exprimieren
oder können
zur Expression von heterologem Gβγ (z.B. aus
Säugern)
gegebenenfalls gentechnisch auf die gleiche Weise manipuliert werden,
wie sie zur Expression von heterologem Gα gentechnisch manipuliert würden.
-
Heterologe
DNA-Sequenzen werden in einem Wirt mittels eines Expressions "konstrukts" oder -„vektors" exprimiert. Bei
einem Expressionsvektor handelt es sich um ein replizierbares DNA-Konstrukt,
in dem eine für
die heterologe DNA-Sequenz codierende DNA-Sequenz mit geeigneten
Kontrollsequenzen, die die Expression eines Proteins oder einer
Proteinuntereinheit, das bzw. die von der heterologen DNA-Sequenz
codiert wird, in dem vorgesehenen Wirt beeinflussen können, operativ
verknüpft
ist. Dabei umfassen eukaryontische Kontrollsequenzen im allgemeinen
einen Transkriptionspromotor, doch kann es auch angebracht sein, daß eine für geeignete
mRNA-ribosome Bindungsstellen codierende Sequenz sowie (gegebenenfalls)
Sequenzen, die die Termination der Transkription kontrollieren,
bereitgestellt werden. Zu zur Praktizierung der vorliegenden Erfindung
geeigneten Vektoren gehören
Plasmide, Viren (einschließlich
Bakteriophagen) sowie integrationsfähige DNA-Fragmente (d.h. Fragmente,
die zur Integration in das Wirtsgenom mittels genetischer Rekombination
fähig sind).
Der Vektor kann unabhängig
vom Wirtsgenom replizieren und funktionieren, wie im Fall eines
Plasmids, oder kann in das Genom selbst integrieren, wie im Fall
eines integrationsfähigen DNA-Fragments.
Geeignete Vektoren enthalten Replikon- und Kontrollsequenzen, die
aus mit dem vorgesehenen Expressionswirt kompatiblen Spezies stammen.
So handelt es sich beispielsweise bei einem Promotor, der in einer
Wirtszelle betrieben werden kann, um einen Promotor, der die RNA-Polymerase
dieser Zelle bindet, und bei einer ribosomen Bindungsstelle, die
in einer Wirtszelle betrieben werden kann, um eine Bindungsstelle,
die die endogenen Ribosomen dieser Zelle bindet.
-
DNA-Bereiche
sind operativ assoziiert, wenn sie miteinander funktionell verwandt
sind. So steht beispielsweise ein Promotor in operativer Verknüpfung mit einer
codierenden Sequenz, wenn er die Transkription der Sequenz kontrolliert;
eine Ribosomenbindungsstelle steht in operativer Verknüpfung mit
einer codierenden Sequenz, wenn sie so positioniert ist, daß sie die
Translation gestattet. Im allgemeinen bedeutet operativ verknüpft zusammenhängend sowie
im Fall von Leader-Sequenzen
zusammenhängend
und im Leseraster.
-
Bei
den transformierten Wirtszellen der vorliegenden Erfindung handelt
es sich um Zellen, die mit den unter Verwendung rekombinanter DNA-Techniken
konstruierten Vektoren transformiert oder transfiziert wurden und
die das bzw. die von den heterologen DNA-Sequenzen codierte Protein
oder Proteinuntereinheit exprimieren. Dabei sind verschiedene Hefekulturen
und geeignete Expressionsvektoren zur Transformation von Hefezellen
bekannt. Siehe beispielsweise US-Patent Nr. 4,745,057; US-Patent
Nr. 4,797,359; US-Patent Nr. 4,615,974; US-Patent Nr. 4,880,734; US-Patent Nr.
4,711,844; und US-Patent
Nr. 4,865,989. Unter den Hefen am häufigsten verwendet wird Saccharomyces
cerevisiae, obwohl eine Reihe anderer Hefespezies allgemein verfügbar sind.
Siehe beispielsweise US-Patent Nr. 4,806,472 (Kluveromyces lactis
und Expressionsvektoren dafür);
4,855,231 (Pichia pastoris und Expressionsvektoren dafür). Hefevektoren
können
einen Replikationsursprung aus dem endogenen 2-Mikron-Hefeplasmid
oder eine autonom replizierende Sequenz (ARS), die dem Plasmid die
Fähigkeit
verleiht, in der Hefezelle mit einer hohen Kopienzahl zu replizieren,
zentromere (CEN-) Sequenzen, die die Fähigkeit des Plasmids auf eine
Replikation mit einer nur geringen Kopienzahl in der Hefezelle beschränken, einen
Promotor, die heterologen DNA-Sequenzen codierende DNA, Sequenzen
für die Polyadenylierung
und Transkriptionstermination sowie ein selektionierbares Markergen
enthalten. Beispielhafte Plasmide und Einzelheiten der Materialien
und Methoden zur Herstellung und Verwendung derselben sind im Beispielteil
aufgeführt.
-
Zur
Verwendung in den Konstrukten und Zellen der vorliegenden Erfindung
kann ein beliebiger, in Hefesystemen funktionsfähiger Promotor ausgewählt werden.
Zu geeigneten Promotorsequenzen in Hefevektoren gehören die
Promotoren für
Metallothionein, 3-Phosphoglyceratkinase (PGK) [Hitzeman et al.,
(1980) J. Biol. Chem. 255, 2073] oder andere glykolytische Enzyme
[(Hess et al., (1968) J. Adv. Enzyme Reg. 7, 149]; und Holland et
al., (1978) Biochemistry 17, 4900], wie beispielsweise Enolase,
Glycerinaldehyd-3-phosphat-dehydrogenase, Hexokinase, Pyruvat-decarboxylase,
Phosphofructokinase, Glucose-6-phosphat-isomerase, 3-Phosphoglyceratmutase,
Pyruvatkinase, Triosephosphatisomerase, Phosphoglucoseisomerase
und Glucokinase. Geeignete Vektoren und Promotoren zur Verwendung
bei der Hefeexpression sind ferner bei R. Hitzeman et al., EPO-Veröffentlichung
Nr. 73657 beschrieben. Weitere Promotoren, die den zusätzlichen
Vorteil einer durch Wachstumsbedingungen kontrollierten Transkription
aufweisen, sind die Promotorbereiche für Alkoholdehydrogenase, 1,2-Isocytochrom C, Säurephosphate,
abbauende Enzyme, die mit dem Stickstoffmetabolismus assoziiert
sind, sowie die oben erwähnte
Metallothionein- und Glycerinaldehyd-3-phosphat-dehydrogenase ebenso wie
für die
Maltose- und Galactoseverwertung
verantwortliche Enzyme, wie beispielsweise der durch Galactose induzierbare
Promotor GAL1. Zur Verwendung hier besonders bevorzugt sind der PGK-Promoter,
der GAL1-Promotor und Alkoholdehydrogenase (ADH)-Promotoren. Schließlich können bei der
Konstruktion geeigneter Expressionsplasmide auch die mit diesen
Genen assoziierten Terminationssequenzen in den Expressionsvektor
ligiert werden, und zwar 3' von
den heterologen codierenden Sequenzen, um so für die Polyadenylierung und
Termination der mRNA zu sorgen. Bei der Herstellung der bevorzugten Expressionsvektoren
der vorliegenden Erfindung werden zur Vermittlung der effizientesten
Expression einer gegebenen Nukleinsäuresequenz in der Hefezelle
Translationsinitiationsstellen gewählt [siehe Cigan, M. und T.F.
Donahue 1987, GENE, Band 59, S. 1-18 für eine Beschreibung geeigneter
Translationsinitiationsstellen].
-
Ein
zur Durchführung
der vorliegenden Erfindung geeigneter, besonders bevorzugter Nukleotidexpressionsvektor
umfaßt
eine solche oben erwähnte
Promotorsequenz, die sich stromaufwärts von der Translationsinitiationsstelle
der für
den heterologen G-Protein-gekoppelten
Rezeptor, den sie exprimieren soll, codierenden heterologen Nukleotidsequenz
sowie im korrekten Leseraster damit befindet. Diesbezüglich besonders
bevorzugte Promotoren sind die Promotoren GAL1, PGK und ADH. Die
Positionierung des oben erwähnten
Promotors stromaufwärts
von der gewählten
Translationsinitiationsstelle kann die Expression eines heterologen
Proteins verbessern. In diesen bevorzugten Ausführungsformen wird kein Segment
eines G-Protein-gekoppelten
Rezeptors aus Hefe an das Segment des heterologen G-Protein-gekoppelten
Rezeptors fusioniert. Von den Erfindern der vorliegenden Anmeldung
wurde festgestellt, daß solche
Hybridrezeptoren zur Erzielung der Rezeptorexpression in Hefe nicht
kritisch sind. Dies steht im Gegensatz zu der diesbezüglichen, im
Fachgebiet akzeptierten Lehre [siehe King et al., unten zitiert].
-
Allerdings
wird in bestimmten anderen Ausführungsformen
mindestens ein Fragment des 5'-nichttranslatierten
Bereichs eines Hefegens stromaufwärts vom heterologen G-Protein-gekoppelten
Segment positioniert und mit diesem operativ assoziiert. Hierzu
werden von der vorliegenden Erfindung auch Konstrukte mit geeigneten
Promotoren und Translationsinitiationsstellen, wie oben beschrieben,
bereitgestellt, doch enthalten diese Konstrukte ein Hefesegment,
das mindestens ein Fragment der äußersten
aminoterminalen codierenden Nukleotidsequenz eines G-Protein-gekoppelten
Rezeptors aus Hefe umfaßt,
sowie ein zweites Segment, das stromabwärts vom ersten Segment liegt
und sich im korrekten Leseraster damit befindet, wobei das zweite Segment
eine einen heterologen G-Protein-gekoppelten Rezeptor codierende
Nukleotidsequenz umfaßt. Diesbezüglich kann
das Hefesegment dazu vorgesehen sein, daß es tatsächlich wie eine Reportersequenz wirkt,
statt zur Verbesserung der wirksamen Expression des heterologen
G-Proteins im Hefesystem zu dienen. Somit umfassen bestimmte Ausführungsformen
eine ein Hefesegment eines G-Protein-gekoppelten Rezeptors aus Hefe codierende
Gensequenz, die als ein Reportersegment fungiert, indem sie nämlich für ein Peptid codiert,
das über
herkömmliche
Mittel, wie beispielsweise Antikörperbindung
und dergleichen nachgewiesen werden kann. Diesbezüglich bevorzugt
ist ein vollständiger
Hefe-Pheromonrezeptor oder ein Teil davon, der mit einem heterologen
G-Protein-gekoppelten Rezeptor fusioniert ist und der hauptsächlich als „Epitop-Tag" für den hochspezifischen
Nachweis der Expression des gewünschten
heterologen Rezeptors unter Verwendung von spezifisch gegen die
exprimierte Epitopsequenz gerichteten Antikörpern verwendet werden kann. Bei
der Konstruktion eines solchen Vektors kann das Hefesegment stromaufwärts zum
heterologen Protein positioniert werden, oder es kann als Alternative
ein Fragment der äußersten
aminoterminalen codierenden Sequenz des heterologen G-Protein-gekoppelten
Rezeptors deletiert und das Hefesegment direkt daran fusioniert
werden. In einigen Fällen
werden dabei eine oder mehrere der aminoterminalen Transmembrandomänen oder
intrazellulären
Domänen
des heterologen Proteins deletiert. Als Alternative kann das Hefesegment
direkt an den Aminoterminus des heterologen Rezeptors angefügt werden,
wodurch die Gesamtlänge
des chimärischen
Rezeptorkonstrukts vergrößert wird.
-
Das
erste und das zweite Segment sind operativ mit einem Promotor, wie
beispielsweise dem GAL1-Promotor, der in einer Hefezelle operativ
ist, operativ assoziiert. Codierende Sequenzen für G-Protein-gekoppelte Rezeptoren aus Hefe, die
bei der Konstruktion derartiger Vektoren verwendet werden können, sind
durch die für
Hefe-Pheromonrezeptoren codierenden Gensequenzen beispielhaft dargestellt
(z.B. das STE2-Gen, das für
den α-Faktor-Rezeptor
codiert, und das STE3-Gen, das für
den a-Faktor-Rezeptor codiert).
-
Bestimmte,
hier bereitgestellte bevorzugte chimärische Rezeptoren umfassen
ein Ste2-Proteinsegment aus Hefe, das direkt an einen vollständigen heterologen
G-Proteinrezeptor
oder einen Teil davon fusioniert ist, und vorzugsweise den 5HT1a-Rezeptor,
muskarinischen Rezeptor, α-adrenergen
Rezeptor oder einen Somatostatinrezeptor.
-
Für den Nachweis
der Auswirkungen einer Ligandenbindung kann ein beliebiges aus einer
Vielfalt von Mitteln genutzt werden. So läßt sich beispielsweise die
Messung der Dissoziation von Gα von
Gβγ über herkömmliche
biochemische Techniken messen. Dabei soll jedoch angemerkt werden,
daß die
Bindung eines Liganden an einen Rezeptor eine nachweisbare biologische
Reaktion, die ihrerseits sich möglicherweise
auch zur Messung eignet, entweder auslösen oder blockieren kann. Bei
einer solchen biologischen Reaktion handelt es sich um die Fähigkeit
von Hefezellen zur Paarung. Die Verwendung des pheromoninduzierten
Paarungssignaltransduktionswegs ist ein bevorzugtes Verfahren zum
Nachweis der Ligandenbindungseffekte in den hier vorgestellten Testsystemen,
deren Grundlage nachfolgend ausführlicher
erörtert
wird.
-
In
der Hefe wird von G-Protein-gekoppelten Pheromonrezeptoren ein Entwicklungsprogramm
gesteuert, das in der Paarung (Fusion) haploider a- und α-Zellarten
unter Bildung des a/α-Diploids
kulminiert (für
eine Übersicht,
siehe G.F. Sprague, Jr. und J.W. Thorner, in Molecular Biology and
Cellular Biology of the Yeast Saccharomyces: Band II, Gene Expression).
Der Paarungsprozeß wird
dabei durch extrazelluläre
Peptide, die Paarungspheromone gestartet. Die Zellen des a-Paarungstyps sezernieren α-Faktor,
der eine Antwort in α-Zellen
hervorruft; Zellen des α-Paarungstyps
sezernieren a-Faktor, der nur auf a-Zellen wirkt. Haploide Zellen
reagieren auf die Gegenwart der Peptidpaarungspheromone über die
Wirkung endogener G-Protein-gekoppelter Pheromonrezeptoren
(STE2: α-Faktor-Rezeptor, nur in α-Zellen exprimiert,
und STE3: a-Faktor-Rezeptor,
nur in a-Zellen exprimiert. Beide Rezeptoren wechselwirken mit den
gleichen heterotrimeren G-Proteinen und einer Signaltransduktionskaskade,
die beiden haploiden Zellarten gemeinsam ist. Nach Pheromonbindung
an den Rezeptor macht dieser vermutlich eine Konformationsänderung
durch, die zur Aktivierung des G-Proteins führt. Die α-Untereinheit SCG1/GPA1 übt eine
negative Wirkung auf den Pheromonantwortweg aus, die durch rezeptorabhängige Aktivierung
aufgehoben wird. Man nimmt an, daß der Komplex der βγ-Untereinheiten (STE4,
STE18) das positive Signal auf einen Effektor, möglicherweise STE20, eine putative
Proteinkinase, überträgt [Leberer,
E., Dignard, D., Harcus, D., Thomas, D.Y., Whiteway, M. (1992) EMBO
J. 11, 4815-4824]. Der Effektor aktiviert wiederum nachgeschaltete
Elemente des Signaltransduktionswegs, einschließlich STE5, sowie eine vermutete,
sich aus den Produkten der Gene STE11, STE7, FUS3 und KSS1 zusammensetzende Proteinkinasekaskade,
was letztendlich zum Zellzyklusarrest und zur Transkriptionsinduktion
führt.
Die Hauptschnittstelle zwischen Elementen des Pheromonantwortwegs
und dem Zellzyklusregulationsapparat ist das FAR1-Genprodukt. Bestimmte
rezessive Allele von FAR1 und FUS3 machen nicht den Zellzyklusarrest
als Reaktion auf Pheromon mit, während
sie die pheromonabhängige
Transkription stattfinden lassen. Die pheromonabhängige Transkription
wird durch die Wirkung des sequenzspezifischen DNA-Bindungsproteins
STE12 vemittelt. Die Aktivierung von STE12 führt zur Transkription von Genen,
die eine in cis wirkende DNA-Sequenz, das Pheromonantwortelement,
besitzen. Diese auf Pheromon reagierenden Gene codieren für Produkte,
die für
die Pheromonsynthese (MFa1, MFa2, MFA1, MFA2, STE6, STE13) und die
Reaktion auf Pheromon (STE2, STE3, SCG1/GPA1, FUS3) benötigt werden
und die die Zellassoziation und -fusion (FUS1), den Zellzyklusarrest
(FAR1) und die zur Paarung erforderlichen morphologischen Ereignisse
erleichtern oder daran beteiligt sind. Falls der Paarungsvorgang
nicht vollzogen wird, adaptieren Hefezellen an die Gegenwart von
Pheromon und nehmen das mitotische Wachstum wieder auf. Somit ist
in bestimmten bevorzugten Ausführungsformen das
FUS3- oder FAR1-Gen mutiert oder komplett deletiert, wodurch der
Zellzyklusarrestweg vom Signaltransduktionsweg getrennt und das
fortgesetzte Wachstum der Zellen als Antwort auf die Bindung von
Paarungspheromon an den heterologen Rezeptor gestattet wird. Da
es sich bei FAR1 um einen Hauptfaktor im Zellzyklusregulationsweg
handelt, ist seine Deletion bzw. Mutation in den Expressionskonstrukten
der vorliegenden Erfindung bevorzugt. Mit derartigen Konstrukten
transformierte Hefezellen ergeben hervorragende Hefestämme für Ligandenbindungstests.
-
Es
ist bekannt, daß der
Paarungssignaltransduktionsweg durch mehrere Mechanismen, einschließlich Pheromonabbau
und Modifikation der Funktion des Rezeptors, der G-Proteine und/oder
nachgeschalteter Elemente der Pheromonsignaltransduktion durch die
Produkte der Gene SST2, STE50, AFR1 [Konopka, J.B. (1993) Mol. Cell.
Biol. 13, 6876-6888] sowie SGV1, MSG5 und SIG1, desensibilisiert
wird. Ausgewählte
Mutationen in diesen Genen können
zur Überempfindlichkeit
gegenüber
Pheromon sowie zu einer Unfähigkeit
zur Anpassung an die Gegenwart von Pheromon führen. So stellt beispielsweise die
Einführung
von funktionsstörenden
Mutationen in heterologe G-Protein-gekoppelte Rezeptoren exprimierende
Stämme
eine signifikante Verbesserung gegenüber Wildtypstämmen dar
und ermöglicht
die Entwicklung äußerst empfindlicher
Biotests für
mit den Rezeptoren wechselwirkende Verbindungen. Andere Mutationen,
z.B. STE50, sgv1, ste2, ste3, pik1, msg5, sig1 und afr1, weisen
den ähnlichen
Effekt einer Erhöhung
der Empfindlichkeit des Biotests auf. Dem Fachmann ist ersichtlich,
daß eine
erhöhte
Empfindlichkeit des Testsystems durch die Deletion eines oder mehrerer
dieser oben erwähnten
Gene sowie die Einführung
von deren Expression herunterregulierenden oder in bestimmten Fällen deren Überexpression
bewirkenden Mutationen erreicht wird. Beispielsweise ist bei dem
STE50-Konstrukt die Überexpression
des Gens und nicht die Deletion des Gens gewünscht.
-
Die
Einführung
einer Konstellation von Mutationen im Paarungssignaltransduktionsweg
führt zu
einer Hefezelle, die sich gut zur Expression heterologer G-Protein-gekoppelter
Rezeptoren eignet, welche zu einer funktionellen Reaktion auf ihre
zugehörigen
Liganden fähig
sind, wobei eine biologische Antwort geliefert wird, die die Bindung
des Rezeptors an den Liganden signalisiert.
-
In
Verbindung mit einer oder mehrerer der oben angeführten Mutationen
besteht ein besonders zweckmäßiges Verfahren
zum Nachweis von Ligandenbindung an in Hefezellen exprimierten heterologen
Rezeptor in der Nutzung eines herkömmlichen genetischen Indikatorsystems.
Somit werden in bestimmten bevorzugten Ausführungsformen die Zellen mit
einer zusätzlichen
heterologen Nukleotidsequenz versehen, die einen auf Pheromon reagierenden
Promotor sowie ein stromabwärts
von dem auf Pheromon reagierenden Promotor liegendes und damit operativ
assoziiertes Indikatorgen umfaßt.
Bei Vorliegen einer solchen Sequenz kann der Nachweisschritt durch
Verfolgen der Expression des Indikatorgens in der Zelle erfolgen.
Dabei könnten
verschiedene auf Pheromon reagierende Promotoren zum Einsatz kommen,
beispielsweise ein Promotor, der eines der oben erwähnten auf
Pheromon reagierenden Gene (z.B. mFa1, mFa2, MFA1, MFA2, STE6, STE13) steuert,
der Promotor des Gens BAR1 und der Promotor des Gens FUS1. Ebenfalls
könnte
eines aus einer breiten Vielfalt von Indikatorgenen verwendet werden,
zu denen beispielsweise die Gene HIS3, G418r, URA3, LYS2, CAN1,
CYH2 und LacZ zählen.
Ein besonders bevorzugtes Reportergenkonstrukt wird genutzt, indem man
Transkriptionskontrollelemente eines FUS1-Gens an für das HIS3-Protein
codierende Sequenzen fusioniert und das ursprüngliche FUS1-Gen durch dieses
Reporterkonstrukt ersetzt. Dadurch wird die Expression des HIS3-Genprodukts
unter die Kontrolle des Pheromonsignaltransduktionswegs gestellt.
Hefestämme (his3),
die dieses Konstrukt tragen, können
auf supplementiertem Minimalmedium ohne Histidin schlecht wachsen
und sind gegenüber
einem Inhibitor des HIS3-Genprodukts
empfindlich. In anderen bevorzugten Ausführungsformen tragen Plasmide
eine FUS1-lacZ-Genfusion.
Dabei wird die Expression des FUS1-Gens als Reaktion auf Rezeptoraktivierung
durch Pheromonbindung stimuliert. Daher läßt sich die Signaltransduktion
quantifizieren, indem man die von dem FUS1-lacZ-Reportergen erzeugte β-Galactosidase-Aktivität mißt.
-
An
weiteren sinnvollen Reportergenkonstrukten, die weiterhin unter
der Kontrolle von Elementen des Pheromonsignaltransduktionswegs
stehen, bei denen es sich jedoch um Alternativen zu den oben erörterten Reportersystemen
handelt, können
Signale beteiligt sein, die über
andere heterologe Effektorproteine, die koexprimiert werden, transduziert
werden. Beispielsweise kann 1) die ligandenabhängige Stimulierung einer heterologen
Adenylylcyclase das Überleben
eines Hefestamms, dem aufgrund einer Mutation im Gen cdc35 seine
eigene Adenylylcyclase fehlt, 2) die ligandenabhängige Stimulierung eines heterologen
G-Protein-gekoppelten
Kaliumkanals das Überleben
eines Hefestamms, der nicht in Medium mit einer niedrigen Kaliumkonzentration
wachsen kann [(trk1, trk2), siehe beispielsweise Anderson, J.A.
et al. (1992) Proc. Natl. Acad. Sci. USA 89, 3736-3740], oder 3)
die ligandenabhängige
Stimulierung einer heterologen Phospholipase C (vor allem PLC-β) das Überleben
eines Hefestamms, dem seine eigene PLC fehlt [(plc), siehe beispielsweise
Payne, W.E. und Fitzgerald-Hayes, M. (1993) Mol. Cell Biol. 13,
4351-4363], gestatten.
-
Zur
Praktizierung der vorliegenden Erfindung können alle für eine Adenylylcyclase codierenden DNA-Sequenzen
verwendet werden. Zu den Beispielen für eine Adenylylcyclase gehören das
Produkt des Rutabaga-Gens aus D. melanogaster und die Untereinheitstypen
I-VIII aus Säugern
[für eine Übersicht,
siehe Tang, W.-J. und Gilman, A.G. (1992) Cell 70, 869-872] sowie
Mutanten und Homologe davon zusammen mit den dafür codierenden DNA-Sequenzen,
die sich zur Praktizierung der vorliegenden Erfindung eignen.
-
Zur
Praktizierung der vorliegenden Erfindung können alle für einen G-Protein-gesteuerten
Kaliumkanal codierenden DNA-Sequenzen verwendet werden. Zu den Beispielen
für einen
G-Protein-gesteuerten Kaliumkanal gehören GIRK1 [Kubo, Y., Reuveny,
E., Slesinger, P.A., Jan, Y.N. und Jan, L.Y. (1992) Nature 365, 802-806],
zur Praktizierung der vorliegenden Erfindung geeignete Untereinheiten
sowie Mutanten und Homologe davon zusammen mit den dafür codierenden
DNA-Sequenzen.
-
Zur
Praktizierung der vorliegenden Erfindung können alle für ein Phospholipaseprotein
codierenden DNA-Sequenzen
verwendet werden. Zu den Phospholipaseproteinen (PLC-Proteinen)
gehören
beispielsweise das norpA-Genprodukt aus D. melanogaster und die
PLC-β-Proteine [für eine Übersicht,
siehe Rhee, S.G. und Choi, K.D. (1992) J. Biol. Chem. 267, 12392-12396],
zur Praktizierung der vorliegenden Erfindung geeignete Untereinheiten
sowie Mutanten und Homologe davon zusammen mit den dafür codierenden
DNA-Sequenzen.
-
Vorliegend
wird ein besonders bevorzugtes Hefe-Expressionssystem beschrieben, das SSTR
und ein chimärisches
G-Protein tragende Hefezellen aufweist, deren kontinuierliches Wachstum
vom Vorhandensein von Somatostatin abhängt. Wie oben angemerkt exprimieren
transformierte Wirtszellen der vorliegenden Erfindung die von den
heterologen DNA-Sequenzen codierten Proteine oder Proteinuntereinheiten.
Wird der G-Protein-gekoppelte
Rezeptor exprimiert, so ist er in der Wirtszellmembran lokalisiert
(d.h. er ist darin physikalisch in der korrekten Orientierung sowohl
für die
stereoselektive Bindung von Liganden als auch für die funktionelle Wechselwirkung
mit G-Proteinen auf der zytoplasmatischen Seite der Zellmembran
positioniert). Die Realisierung des hier beschriebenen empfindlichen
und spezifischen Hefe-Expressionssystems erleichtert die Beschreibung
struktureller und funktioneller Aspekte von Rezeptor/Ligand- und
Rezeptor/G-Protein-Wechselwirkungen.
Durch die Modifikation von Elementen des Paarungssignaltransduktionswegs
ermöglichte
leistungsfähige
genetische Selektionsschemata können
zur Identifizierung von Aspekten des Rezeptors, die sich auf Agonistenselektivität, Ligandenstereoselektivität sowie
Determinanten der Agonisten-/Antagonistenbindung
auswirken, eingesetzt werden. Mit Hilfe dieses leistungsfähigen genetischen
Systems kann die Rolle von Proteinen, die die Reaktion von Rezeptoren
und G-Proteinen auf Liganden modifizieren, im Detail verstanden werden.
Wichtig ist, daß durch
das System ein verallgemeinerter Ansatz zur Untersuchung der Funktionsweise und
der Komponenten des G-Protein-gekoppelten
Signaltransduktionssystems ebenso wie ein verallgemeinerter Ansatz
für Screening-Tests
unter Verwendung des G-Protein-gekoppelten Signaltransduktionssystems bereitgestellt
wird. Mit dem vorliegenden Verfahren werden an die Aufnahme eines
von verschiedenen heterologen G-Protein-gekoppelten Rezeptoren angepaßte Expressionskonstrukte
und Testsysteme in Form von "Expressionskassetten" bereitgestellt.
Dabei wird der zu untersuchende heterologe G-Protein-gekoppelte Rezeptor einfach
in die hier bereitgestellten Vektoren inseriert und in Hefezellen
exprimiert. Möglicherweise
an den exprimierten Rezeptor bindende Liganden läßt man in der Art eines beliebigen
herkömmlichen
Tests mit den Zellen in Kontakt treten, wobei sich die Auswirkungen
der Wechselwirkung leicht verfolgen lassen. Die hier vorliegenden
Systeme sind somit bei der Identifizierung von Liganden für "orphan" ["verwaiste"] G-Protein-gekoppelte
Rezeptoren sowie für
die Entdeckung neuer therapeutisch geeigneter Liganden für medizinisch,
tiermedizinisch und landwirtschaftlich wichtige Rezeptoren von enormem
Nutzen.
-
Zur
weiteren Veranschaulichung verschiedener Aspekte der vorliegenden
Erfindung werden die folgenden Beispiele bereitgestellt, die jedoch
nicht als Beschränkung
der Erfindung aufzufassen sind.
-
BEISPIEL 1
-
Funktionelle
Expression von G-α-Proteinen
aus Säugern
in Saccharomyces cerevisiae
-
Zur
Messung der Störung
der Wechselwirkungen von Gα und
Gβγ der Hefe
durch die Expression heterologer Gα-Proteine wird ein empfindlicher Biotest
genutzt. Dabei werden Säuger-Gα-Gene von
2μ- oder zentromertragenden
Plasmiden unter der Kontrolle des konstitutiven PGK- oder des induzierbaren
CUP1-Promotors exprimiert. Die Daten demonstrieren, daß Gαs und
Gαi2 der Ratte sowie ein chimärisches
Hefe/Säuger-Gα auf wirksame
Weise mit Hefe-Gβγ wechselwirken
können.
-
Medien
und Stämme.
Die Anzucht der Bakterienstämme
sowie die Plasmidmanipulationen werden nach Standardverfahren (Maniatis
T., Molecular Cloning (Cold Spring Harbor Laboratory Press, 1982))
durchgeführt.
Die Anzucht und Transformation von Hefestämmen erfolgt wie bei Rose et
al. beschrieben (Rose M.D., Methods in yeast genetics, Cold Spring
Harbor Laboratory Press, 1990). Die in diesen Arbeiten verwendeten Hefestämme (CY414,
MATa ura3-52 trp1 leu2 his3 pep4::HIS3) leiten sich von bei E. Jones
(Jones, E.W., Ann. Rev. Genet 18:233, 1984) beschriebenen Stämmen ab.
CY414 wird nacheinander mit dem FUS1-lacZ-Fusionsplasmid pSB234
(Trueheart, J. et al. Mol. Cell. Biol. 7(7): 2316-2328, 1987) und
Gα-Expressionsplasmiden transformiert.
-
Konstruktion.
der Gα-Expressionsplasmide.
Ratten-cDNA-Klone
für Gαs und
Gαi2 sowie für Fusionen mit dem Hefe-SCG1-Gen sind an
anderer Stelle beschrieben [Kang, Y.-S., Kane, J., Kurjan, J., Stadel, J.M. und
Tipper, D.J. (1990) Mol. Cell. Biol. 10, 2582-2590]. Zur Expression
dieser Gene von Plasmiden mit niedriger Kopienzahl werden XhoI-SalI-Fragmente,
die jede Expressionskassette (einschließlich der PGK-Promotor- und
Terminatorsequenzen) enthalten, isoliert und in das mit XhoI verdaute
CEN-Plasmid pRS414 kloniert. Für die
induzierbare Expression wird das PGK-Promotorsequenzen enthaltende
DNA-Segment durch stromaufwärts
liegende aktivierende Sequenzen aus dem CUP1-Gen ersetzt.
-
β-Galactosidase-Tests.
Kulturen werden auf 5 × 107 Zellen/ml verdünnt und in getrennte Röhrchen aliquotiert.
Zu einer Probe gibt man Pheromon mit einer Endkonzentration von
10–9 M.
Danach werden die Kulturen 4 Std. bei 30°C inkubiert. Die anschließende Messung
der β-Galactosidase-Aktivität erfolgt
wie an anderer Stelle beschrieben (Rose, M.D., Cold Spring Harbor
Laboratory Press, 1990).
-
Plasmide
mit hoher bzw. niedriger Kopienzahl, die die jeweils vom Hefe-PGK-Promotor
exprimierten Gene Hefe-SCG1
oder Säuger-Gαs oder
-Gαi oder chimärisches Hefe/Säuger-Gα tragen,
werden in einen Wildtyp-Hefestamm,
der auch ein eine FUS1-lacZ-Genfusion tragendes Plasmid enthält, transformiert.
Die Expression des FUS1-Gens wird als Reaktion auf die Rezeptoraktivierung
durch Pheromonbindung stimuliert. Daher läßt sich die Signaltransduktion
quantifizieren, indem man die von dem FUS1-lacZ-Reportergen erzeugte β-Galactosidase-Aktivität mißt. Dabei
wird die Störung
der normalen Signaltransduktion durch die Expression eines heterologen
Gα-Proteins
als Abnahme der β-Galactosidase-Aktivität beobachtet.
-
Eingeführte Gα-Gene exprimierende
Stämme
werden auf pheromoninduzierte Genaktivierung getestet. Die Daten
sind als Prozent Wildtyp-Reaktion in 1 dargestellt.
Die FUS1-lacZ-Expressionsniveaus wurden durch die Expression von
allen Gα-Plasmiden
reduziert, wodurch demonstriert wird, daß die Gα-Proteine funktionell an Hefe-Gβγ koppelten.
Für Scg1,
Gαs und Gαi2 wurde eine Dosisabhängigkeit beobachtet. Die Signalgebung
wird durch die Expression von Plasmiden mit hoher Kopienzahl stark
reduziert, was vermuten läßt, daß ein großer Überschuß an heterologem
Gα-Protein vorhanden
ist. Das chimärische
Scg-Gαi2-Protein
reduziert selbst vom Plasmid mit niedriger Kopienzahl die Signalgebung
fast auf die nichtstimulierten Hintergrundniveaus. Mit anderen CEN-Expressionsplasmiden
wird die Signalgebung auf 53 bis 84% der Wildtypniveaus reduziert.
-
Um
eine genauere Kontrolle der Gα-Expression
zu erreichen und die Expression auf ein hinreichend niedriges Niveau
zu reduzieren, so daß minimale
Auswirkungen auf die pheromoninduzierte Signalgebung auftreten,
werden Gα-Gene
(außer
Gαs) unter
die Kontrolle des induzierbaren CUP1-Promotors gestellt und auf Plasmiden
mit niedriger Kopienzahl in Hefe transformiert. Das Niveau der von
diesen Plasmiden vermittelten Repression der Signalgebung hängt von
der Konzentration des dem Medium zugesetzten Cu++4 ab (2). Allerdings
entsprach die Grundexpression (ohne Zugabe von Cu++4) den beobachteten
Niveaus vom PGK-Promotor (1). Das
chimärische
SCG-Gαi2-Protein reduziert
wie im vorherigen Experiment die Signalgebung fast auf Hintergrundniveaus.
-
Die
in 1 und 2 dargestellten Daten deuten
darauf hin, daß alle
untersuchten Gα-Expressionsplasmide
funktionelle Gα-Proteine
produzieren, indem sie alle den Signaltransduktionsweg hemmen. Bei
Verwendung eines konstitutiven Promotors (PGK) zeigen die meisten
Gα-Gene einen dosisabhängigen Effekt, wobei
mit den in hoher Kopienzahl vorliegenden 2-Mikron-Plasmiden die
Signalgebung drastisch reduziert wird (1). Durch
die niedrigere Expression von CEN-Plasmiden werden die Signalgebungsniveaus
bis hinunter zu 16% reduziert (siehe Gi, 1).
Die Expression der Gα-Gene
vom CUP1-Promotor zeigt die erwarteten Dosis/Wirkung-Effekte, wobei die
reduzierte Signalgebung mit erhöhten
Cu++-Konzentrationen korreliert ist (2).
-
BEISPIEL 2
-
Pharmakologische
Bewertung in Saccharomyces cerevisiae exprimierter heterologer G-Protein-gekoppelter Rezeptoren
-
Hefestämme. Die
Anzucht und Transformation von Hefestämmen erfolgt wie bei Rose et
al. beschrieben (Rose M.D., Methods in Yeast Genetics, Cold Spring
Harbor Laboratory Press, 1990). Die in diesen Arbeiten verwendeten
Hefestämme
(CY414, MATa ura3-52 trp1 leu2 his3 pep4ΔHIS3) leiten sich von bei E.
Jones (Jones, E.W., Ann. Rev. Genet 18:233, 1984) beschriebenen Stämmen ab.
-
Nukleinsäuremanipulation.
Die Anzucht der Bakterienstämme
sowie die Plasmidmanipulationen werden nach Standardverfahren [Sambrook,
J., Fritsch, E.F. und Maniatis T., Molecular Cloning, 2. Aufl. (Cold Spring
Harbor Laboratory Press, 1989)] durchgeführt. Die DNA-Sequenzierung wird
mittels "High temperature cycle"-Sequenzierung (Applied Biosystems) durchgeführt.
-
Proteinanalyse.
Die Rezeptorexpressionsstämme
werden in synthetischem Komplettmedium ohne spezifische Nährstoffe
zur Selektion auf Plasmidretention sowie mit 3% Galactose zur Induktion
der Rezeptorgenexpression angezogen. Die Zellen werden pelletiert
und in Lysepuffer (10 mM Natriumhydrogencarbonat pH 7,2, 1 mM EGTA,
1 mM EDTA) gewaschen, anschließend
in Lysepuffer plus Proteaseinhibitoren (5 μg/ml Leupeptin, 10 μg/ml Benzamidin,
10 μg/ml
Bacitracin, 5 μg/ml
Pepstatin, 5 μg/ml
Aprotinin) resuspendiert und durch physikalischen Aufschluß mit Glasperlen
lysiert. Zelltrümmer
werden durch 10minütige
Zentrifugation bei 1000 × g
abgetrennt. Die Membranfraktion wird durch 10minütige Zentrifugation bei 100000 × g isoliert. Dieses
Pellet wird einmal in Lysepuffer plus Inhibitoren gewaschen. Die
Polyacrylamidgelelektrophorese der Hefeextrakte wird nach Standardverfahren
durchgeführt,
mit der Ausnahme, daß die
Proben nicht aufgekocht werden. Die Proteine werden mit der Semi-Dry-Technik
auf Immobilon-P-Millipore-Filter übertragen.
Rezeptorprotein wird unter Verwendung von ECL-Reagentien mit Kaninchen-Anti-Ste2-Antikörpern sichtbar
gemacht.
-
Radioligandenbindungstests.
Die Reaktionen werden in einem Volumen von 0,2 μl mit 5 bis 50 μg Protein
durchgeführt.
Bei den Bindungstests für
Liganden des 5HT1a-Rezeptors oder des β2-adrenergen Rezeptors wird
ein Puffer aus 50 mM Tris pH 7,4, 10 mM MgCl2 verwendet.
Somatostatinbindung wird in einem Puffer von 50 mM HEPES, pH 7,4,
5 mM MgCl2 durchgeführt. Man läßt die Ligandenbindung bis
zum Erreichen des Gleichgewichts bei Raumtemperatur ablaufen und
isoliert anschließend
die Membranfraktionen auf GFC-Glasfaserfiltern. Dabei werden die
folgenden Ligandenendkonzentrationen verwendet: Radioliganden: 3H-Spiperon, 80 nM; 125I-Cyanopindolol, 250
pM; [125I-tyr11]-Somatostatin
14, 250 pM; Kompetitoren: Serotonin, 10 μm; Propanolol, 20 μM; Somatostatin
14, 1 μM.
Es werden 100 μM
des Guanosintriphosphat-Analogs Gpp(NH)p verwendet.
-
Expression
des menschlichen serotonergen Rezeptors 5HT1a. Das für den menschlichen
5HT1a-Rezeptor codierende Gen wird unter Addition der ersten 14
Aminosäuren
des Ste2-Proteins der Hefe modifiziert, in das Expressionsplasmid
pMP3 kloniert und mit pCHI11 bezeichnet. Dieser Stamm mit der Bezeichnung CY382
wird zur Induktion der Rezeptorexpression in galactosehaltigem Medium
angezogen, fraktioniert und über
die Bindung des radioaktiv markierten Antagonisten 3H-Spiperon auf Rezeptoraktivität getestet.
Die Sättigungsbindung
zeigt, daß der
Rezeptor auf hohem Niveau exprimiert wird (Bmax = 3,2 pmol/mg Protein)
und daß er
Spiperon mit einer ähnlichen
Affinität
(Kd = 115 nM; 3) wie der in Säugergeweben
beobachteten (Kd = 20 bis 100 nM) bindet.
-
Zwei
chimärische
Rezeptorgene werden gentechnisch hergestellt: in pCH117 sind für den N-Terminus einschließlich der
ersten beiden Transmembrandomänen
des 5HT1a-Rezeptors codierende Sequenzen durch die entsprechenden
Sequenzen des Ste2-Rezeptors ersetzt, und in pCH118 sind diese Ste2-Sequenzen
direkt an den N-Terminus
des 5HT1a-Rezeptors angefügt,
so daß ein
neuer Rezeptor mit neun Transmembrandomänen entsteht (4).
Diese Rezeptoren exprimierende Stämme werden auf die Bindung
von radioaktiv markiertem Liganden untersucht. Beide Rezeptoren
zeigen spezifische Bindung des 5HT-Rezeptor-Antagonisten 3H-Spiperon (4). Der Austausch
der ersten beiden Transmembrandomänen gegen solche eines nicht verwandten
Rezeptors wirkt sich anscheinend nicht auf die Bindung dieses Liganden
aus. Das Hinzufügen
von Transmembrandomänen
bewirkt keine Bindung, was vermuten läßt, daß dieser ungewöhnliche
Rezeptor eine funktionelle Konformation in der Zellmembran einnehmen
kann. pCHI11, pCHI17 bzw. pCHI18 tragende Stämme produzieren Bmax-Werte
von 3,1, 1,6 bzw. 0,7 pmol/mg. Zwar ergeben diese chimärischen
Rezeptoren im Hinblick auf die Rezeptorstruktur interessante Ergebnisse,
doch werden dadurch die Gesamtniveaus an funktionellen Rezeptoren
in der Zelle nicht gesteigert.
-
Alle
intrazellulären
Sequenzen des 5HT1a-Rezeptors werden zur direkten Kopplung des Rezeptors
an das Hefe-G-Protein
durch entsprechende Sequenzen des Hefe-Ste2-Proteins ersetzt. Der dabei erhaltene
chimärische
Rezeptor CHI16 wird in einem Wildtyp-Hefestamm exprimiert und auf
die hochaffine Bindung von 5HT1a-Rezeptor-Agonisten
untersucht. Eine Agonistenbindung wird nicht nachgewiesen. Allerdings
entspricht das Niveau der Bindung des radioaktiv markierten Spiperons
dem von CHI11, was darauf hindeutet, daß dieser Rezeptor auf hohem
Niveau und in einer funktionellen Konformation exprimiert wird.
-
Expression
des menschlichen β2-adrenergen
Rezeptors. Der menschliche adrenerge Rezeptor wird in der Hefe mit
der Absicht, ihn als Modell zur Optimierung der Expression und G-Protein-Kopplung
zu verwenden, exprimiert. Ein den Rezeptor exprimierender Hefestamm
wird mittels Scatchard-Analyse auf die Bindung des Liganden 125I-Cyanopindolol untersucht. Die Bindung
läßt sich
absättigen
und zeigt einen zu dem bei Säugergeweben
angegebenen Wert ähnlichen
Kd-Wert (23 pM). Danach werden Stämme mit und ohne koexprimiertes
Gαs in Kompetitionstests
untersucht, bei denen die Bindung dieses Radioliganden mit den Agonisten Isoproterenol
oder Epinephrin konkurriert. In beiden Stämmen wurde eine hochaffine
Bindung beobachtet, die erwartungsgemäß nur dann auftritt, wenn der
Rezeptor aktiv an G-Protein gekoppelt wird (5 und 6). Die
extrapolierten Ki-Werte für
diese Liganden (Isoproterenol = 10 nM; Epinephrin = 60 nM) sind
mit den in Säugergeweben
beobachteten Affinitäten
vereinbar und zeigen die erwartete Potency-Reihenfolge. Andere Daten
lassen jedoch vermuten, daß die
hochaffine Bindung von Agonisten an den β2-adrenergen Rezeptor in Hefe
anomal ist. und nicht von einer Kopplung an G-Protein herrührt. Insbesondere wird der
dritte intrazelluläre Loop
(der die primären
Gα-Kontaktpunkte
enthält)
des β2-adrenergen
Rezeptors durch die entsprechende Domäne des Hefe-Ste2-Rezeptors
ersetzt. Dieser Rezeptor zeigt die gleichen Affinitäten für adrenerge
Agonisten, was vermuten läßt, daß der β2-adrenerge Rezeptors
in der Hefe eine ungeeignete Konformation einnimmt.
-
Expression
des Somatostatinrezeptors der Ratte. Die hochaffine Bindung von
Somatostatin an SSTR2 hängt
von der Ausbildung eines Rezeptor/G-Protein-Komplexes ab (Strnad
et al., 1993). Sind SSTR und G-Protein voneinander entkoppelt, so
ist die hochaffine Bindung von [
125I]tyr
11S-14 abgeschwächt. Wie in
8 gezeigt,
läßt sich
die Bindung von [
125I]tyr
11S-14
an in Scg1/Gα
i2 koexprimierender Hefe exprimierten SSTR2 absättigen und
weist eine hohe Affinität
auf. Der berechnete K
d-Wert für in Hefe
exprimierten SSTR2 bindendes [
125I]tyr
11S-14 beträgt 600 pM. Ähnliche Bindungsaffinitäten werden
beobachtet, wenn statt Scg1/Gα
i2 Gα
i2 mit SSTR2 koexprimiert wird. Der in der
Hefe beobachtete K
d-Wert stimmt gut mit
dem berechneten K
d-Wert der [
125I]tyr
11S-14-Bindung
von in Säugerzellen
exprimiertem SSTR2 (Strnad et al., 1993) überein. Es wird gezeigt, daß die Addition
des Hefe-Ste2-Rezeptors an den N-Terminus dieses Rezeptors keine
Auswirkung auf dessen Fähigkeit
zur Bindung von S-14 hat. Die Ste2-Sequenzen fungieren als Tag für die immunchemische Untersuchung
der Rezeptorexpression. Der in
7 gezeigte
Immunoblot veranschaulicht das hohe Niveau der SSTR2-Expression
in drei unterschiedlichen Stämmen.
Den Somatostatinrezeptor SSTR2 sowie unterschiedliche Gα-Proteine
exprimierende Hefestämme
leiten sich von dem Stamm YPH500 ab. Diese Stämme teilen den Genotyp MATa
scg1ΔhisG
lys2-801 ura3-52 leu2Δ1
trp1Δ63
his3Δ200
ade2 SSTR2. Stämme
mit der Bezeichnung CY624 (Gα
i2), CY602 (Gα
s) und
CY603 (Scg1) werden auf die spezifische Bindung von radioaktiv markiertem
Somatostatin-14 (S-14)
untersucht. Alle drei zeigen einen gewissen Grad an Somatostatinbindung
(Tabelle 1). Die hochaffine Bindung dieses Liganden erfordert die
Kopplung des Rezeptors an G-Protein, normalerweise Gαi (Luthin
D.R. 1993; Strnad J. 1993), so daß das hohe Bindungsniveau in
Abwesenheit von Gαi
unerwartet ist. Als Bestätigung
für die
Kopplung des Rezeptors an G-Proteine wird die Bindung in Gegenwart
des nicht hydrolysierbaren Guanosintriphosphat-Analogs Gpp(NH)p
untersucht. Die Zugabe dieser Verbindung hebt die Ligandenbindung
auf (Tabelle 1), wodurch demonstriert wird, daß der SSTR2-Rezeptor an G-Protein gekoppelt
ist. Diese Daten zeigen, daß ein
G-Protein-gekoppelter
Rezeptor aus Säugern
eine funktionelle Wechselwirkung mit einem aus seinem bevorzugten
Gα-Protein
plus den Gβ-
und Gγ-Untereinheiten aus
Hefe zusammengesetzten G-Protein eingehen kann und daß ein heterologer
Rezeptor in der Lage ist, funktionell an ein vollständig aus
Hefe-Untereinheiten
zusammengesetztes G-Protein zu koppeln. TABELLE
1. Bindung von [
125I]-Somatostatin
- a Aus den Ratte-SSTR-Somatostatinrezeptor-Subtyp
und das angegebene Gα-Protein
exprimierenden Hefestämmen
wurden Membranrohextrakte präpariert.
Die maximale Bindung von radioaktiv markiertem Somatostatin 14 wurde
wie im Text beschrieben gemessen. b Bmax-Werte
sind als fmol/mg Gesamtprotein angegeben. c Zur
Entkopplung von Rezeptor und G-Protein wurden Proben mit dem nicht
hydrolysierbaren GTP-Analog Gpp(NH)p versetzt. Die Daten sind als
Prozent gebundener Radioligand verglichen mit unbehandelten Proben
dargestellt.
-
Expression
des muskarinischen Acetylcholinrezeptors aus Drosophila. Einen muskarinischen
Acetylcholinrezeptor aus Drosophila (Dm-mAChR) codierende DNA-Sequenzen
werden durch das Hinzufügen
einer SalI-Stelle in den 5'-codierenden
Sequenzen unter Verwendung von PCR modifiziert. Für die ersten
23 Aminosäuren
des STE2-Genprodukts
codierende DNA-Sequenzen werden an das 5'-Ende
von Dm-mAChR in Form eines BamHI/SalI-Fragments angefügt. Die
modifizierte Dm-mRChR-Sequenz wird in die BamHI-Stelle im Plasmid
pMP3 inseriert, wobei die Expression des Rezeptors unter die Kontrolle
des GAL1-Promotors
gestellt und das Plasmid pMP3-Dm-mAChR gebildet wird. Der Stamm
CY414 wird mit diesem Plasmid transformiert und zur Rezeptorexpression
nach Standardverfahren kultiviert. Von diesen Zellen werden Membranrohpräparationen
hergestellt und auf das Vorhandensein spezifischer Bindungsstellen
für den
muskarinischen Antagonisten 3H-Chinuclidinylbenzilat (10 nM) in
Konkurrenz mit Atropin (50 μM)
getestet. Es werden spezifische Bindungsstellen (Bmax 10 bzw. 30
fmol/mg) beobachtet.
-
Die
Expression von Drosophila-mAChR ist auch mit Immunoblot-Verfahren
nachweisbar. In Übereinstimmung
mit dem aus der Primärsequenz
von mAChR vorhergesagten Molekulargewicht wird unter Verwendung
eines gegen das assoziierte Ste2-Epitop gerichteten Antikörpers ein
reichlich vorhandenes 75 kDa großes Polypeptid in Proteinproben
(30 μg/Spur)
aus Membranrohpräparationen von
mAchR von pMP3 exprimierenden Zellen nachgewiesen (9).
Wesentlich weniger Protein wird nachgewiesen, wenn mAchR von pMP2,
einem Derivat von pMP3 ohne GAL4-Sequenzen, exprimiert wird, womit
keine Bestätigung
einer Expression von mAchR auf hohem Niveau erwartet wird.
-
Expression
eines α2-adrenergen
Rezeptors (α2-AR).
Ein EcoRI-NarI-Fragment aus dem Plasmid pMP3, einschließlich dem
GAL1,10-Promotor-EcoRI-BamHI-Fragment,
für die
ersten 23 Aminosäuren
des STE2-Genprodukts
codierenden und auf einem BamHI-SalI-Fragment liegenden DNA-Sequenzen, dem
SalI-SphI-Polylinker-Fragment aus YEp352 sowie STE7-Terminatorsequenzen,
wird unter Bildung von pLP15 auf pRS424 übertragen. Ein für einen α2A-AR aus
Schwein [Guyer, C.A., Horstman, D.A., Wilson, A.L., Clark, J.D., Cragoe,
E.J. und Limbird, L.E. (1990) J. Biol. Chem. 265, 17307-17317] codierendes
PstI-PvuII-Fragment wird in die PstI-SmaI-Stellen von pLP15 inseriert,
wobei pLP50 gebildet wird. Ein EcoRI-Fragment von GAL4 wird in die
EcoRI-Stelle von pLP50 unter Bildung von pLP60 inseriert. Der Stamm
LY124 [ein Derivat von YPH500 (Stratagene), das das scg1ΔhisG-Allel
enthält
sowie das Plasmid pLP10 [pLP10:pUN75 (Elledge, S. J. und Davis,
R. W. Genetics 87, 189-194) mit dem in die SalI-Stelle inserierten
PGK-Scg1-Gαi2-XhoI-SalI-Fragment aus pPGKH-Scg1Gαi2] trägt, wird
mit pLP60 transformiert und auf Rezeptorexpression nach Standardverfahren kultiviert.
Von diesen Zellen werden Membranrohpräparationen hergestellt und
auf das Vorhandensein spezifischer Bindungsstellen für den α2-AR-Antagonisten
3H-Rauwolscin (200 nM) in Konkurrenz mit Phentolamin (10 μM) getestet.
Es wurden spezifische Bindungsstellen mit einem Bmax zwischen 10
und 84 fmol/mg beobachtet.
-
Die
Expression von Schweine-α2AR
ist auch mit Immunoblot-Verfahren nachweisbar (10). Dabei werden unter Verwendung eines gegen
das assoziierte Ste2-Epitop gerichteten Antikörpers in Proteinproben (30 μg/Spur) aus
Membranrohextrakten von α2AR
von pMP3 exprimierenden Zellen mehrere reichlich vorhandene Polypeptide
nachgewiesen.
-
Beispiel 3
-
Agonistenabhängiges Wachstum
von Hefe als Reaktion auf Somatostatinrezeptor-Agonisten
-
Hefestämme, die
auf Somatostatin reagieren, werden durch Einführung mehrerer Modifikationen
in typische Laborhefestämme
erzeugt. Dabei wird erstens eine für den Somatostatinrezeptor
Subtyp 2 (SSTR2) codierende cDNA in einem Mehrkopien-Hefeplasmid
unter die Kontrolle des galactoseinduzierbaren GAL1-Promotors gestellt
(11). Eine Rezeptorexpression auf hohem Niveau
wird durch induzierbare Koüberexpression
des Transkriptionsaktivierungsproteins GAL4 vom gleichen Plasmid
erreicht. Zweitens wird das endogene Gα-Proteingen GPA1/SCG1 durch
ein sich aus einer aminoterminalen Domäne aus GPA1/SCG1 sowie C-terminalen Sequenzen
aus Ratte-Gαi2
zusammensetzendes chimärisches
Gen ersetzt (12). Es konnte bereits gezeigt
werden, daß die
Expression chimärischer
G-Proteine in Hefe den Wachstumsdefekt von scg1/gpa1-Mutantenzellen
supprimiert [Kang, Y. -S., Kane, J., Kurjan, J., Stadel, J. M. und
Tipper, D. J. (1990) Mol. Cell. Biol. 10, 2582-2590]. Drittens wird
das FAR1-Gen deletiert, was die Fortsetzung des Wachstums bei Vorhandensein
eines aktivierten Paarungssignaltransduktionswegs gestattet. Es
wird vermutet, daß das FAR1-Protein
als primäre
Schnittstelle zwischen dem Paarungssignaltransduktionsweg und dem
Zellzyklusapparat dient [Chang, F. und Herskowitz, I. (1990) Cell
63, 999-1012; Peter,
M., Gartner, A., Horecka, J., Ammerer, G. und Herskowitz, I. (1993)
Cell. Biol. 13, 5659- 5669].
Viertens wird das FUS1-Gen durch ein durch Fusion von Transkriptionskontrollelementen
des FUS1-Gens an
für das
HIS3-Protein codierende Sequenzen gebildetes Reportergenkonstrukt
ersetzt, wodurch die Expression des HIS3-Genprodukts unter die Kontrolle
des Paarungssignaltransduktionswegs gestellt wird. Dieses Konstrukt
tragende Hefestämme
(his3) können
auf supplementiertem Minimalmedium ohne Histidin schwach wachsen
und sind gegenüber
3-Amino-1,2,4-triazol
(AT), einem Inhibitor des HIS3-Genprodukts, empfindlich. Die Rezeptoraktivierung
durch Agonistenbindung führt
zu einer erhöhten
HIS3-Proteinexpression,
einem entsprechenden Anstieg der Resistenz gegenüber AT und daher der Fähigkeit
zum Wachstum auf Medium ohne Histidin und/oder in Gegenwart des
Inhibitors. Die Einstellung des pH-Werts des Wachstumsmediums auf > pH 5,5 verstärkt die
Fähigkeit
solcher Zellen, in Gegenwart eines Agonisten zu wachsen, vermutlich
aufgrund einer erhöhten
Fähigkeit
von Somatostatin zur Bindung an SSTR2.
-
Der
Nutzen des Hefe-Expressionssystems liegt in seiner Anpassungsfähigkeit
an schnelles Massen-Screening. Zur Erleichterung des Screening auf
neue, auf die SSTRs gerichtete Therapeutika wird ein zweckmäßiger Agarplatten-Biotest
entwickelt, bei dem die funktionelle Kopplung der Somatostatinbindung
an Rezeptor und der anschließenden
Aktivierung des Paarungssignaltransduktionswegs als eine Wachstumszone
(Hof) um die aufgetragenen Verbindungen herum nachgewiesen wird
(13). Übernacht-Flüssigkulturen von LY268 [einem
Derivat von YPH500 (Stratagene) MATa ura3-52 lys2-801 ade2 trp1Δ63 his3Δ200 leu2Δ1 far1ΔLYS2 scg1ΔhisG fus1ΔFUS1-HIS3
sst2ΔADE2,
das das SSTR2-Expressionsplasmid
und das SCG1-Gαi2-Expressionsplasmid
pLP82 trägt]
in SC-Dextrose (2%) ohne ura, trp wurden auf SC-Lactat-Medium (2%)
ohne ura und trp und anschließend
auf SC-Galactose-Medium (2%) ohne ura und trp überführt. Die Zellen (2 × 105) werden dann in 30 ml SC-Galactose-Agar
(2%) ohne ura, trp und his ausplattiert (13A obere
Abbildung) oder gleichmäßig auf
der Oberfläche
verteilt (13B, untere Abbildung), die
angegebenen Mengen an ausgewählten
Verbindungen auf auf der Oberfläche
der Agarplatte befindliche Papierscheibchen aufgetragen und 3-5
Tage bei 30°C
inkubiert. Wachstumshöfe
werden um mit verschiedenen Konzentrationen an Somatostatin (S-14) und MK678 [einem
Hexapeptidanalog von Somatostatin, das eine hochaffine Bindung zu
SSTR2 zeigt [Verber, D., Saperstein, R., Nutt, R., Friedinger, R.,
Brady, P., Curley, P., Perlov, D., Paleveda, W., Zacchei, A., Cordes,
E., Anderson, P. und Hirschmann, R. (1981) Life Sci, 35, 1371-1378]
gesättigten Scheibchen
herum beobachtet. Die Hofgröße nimmt
proportional zur aufgetragenen Menge an Agonist zu, wobei sogar
bei der geringsten aufgetragenen Menge (6 nmol S-14) eine signifikante
Reaktion beobachtet wird, was die ausgezeichnete Empfindlichkeit
des Tests demonstriert. Mit dem Träger allein sowie gegenüber Metenkephalin,
einem Opiatrezeptor-Agonisten, wird keine nachweisbare Reaktion
beobachtet.
-
Das
Hefemedium sowie die Kultivierungsbedingungen werden gemäß Standardverfahren
formuliert, und die DNA-vermittelte Transformation der Hefe erfolgt
mit dem LiAc-Verfahren [Sherman, F., Fink, G. R. und Hicks, J. B.
(1986) Methods in Yeast Genetics (Cold Spring Harbor Laboratory
Press)]. LY268 wird mittels sequentieller Insertionsdeletion unter
Verwendung der rekombinanten Allele scg1:ΔhisG, far1ΔLYS2, FUS1ΔHIS3 und sst2ΔADE2 konstruiert.
Dabei wird das scg1ΔhisG-Allel durch Insertion
des hisG-URA3-hisG-Fragments aus pNKY51 [Alani, E., Cao, L. und
Kleckner, N. (1987) Genetics 116, 541-545] zwischen das 5'-EcoRI-HindIII-Fragment
und das 3'-SphI-SnaBI-Fragment
von SCG1/GPA1 zusammengebaut. Nach der DNA-vermittelten Transformation
entsprechender Hefestämme
und der Selektion auf den Austausch des chromosomalen Allels wird
das URA3-Gen entfernt, indem man durch Wachstum auf 5-Fluororotsäure (FOA)
enthaltendem Medium die Rekombination zwischen hisG-Wiederholungen
induziert [Boeke, J., Lacroute, F. und Fink, G. (1984) Mol. Gen.
Genet. 197, 345-346]. Das far1ΔLYS2-Allel
wird konstruiert, indem man zwei Fragmente des FAR1-Gens [Chang,
F. und Herskowitz, I. (1990) Cell 63, 999-1012] aus genomischer Hefe-DNA (Stamm
YPH501, Stratagene) unter Verwendung synthetischer Oligonukleotide,
durch die im 5'-Fragment
an Position 1201 eine EcoRI-Stelle sowie im 3'-Fragment an Position 2017 eine HindIII-Stelle
und in Position 2821 eine SalI-Stelle eingeführt werden, amplifiziert. Die
Fragmente werden in das EcoRI/SalI-Fragment von pBSK (Stratagene) kloniert.
Das vollständige
far1ΔLYS2-Konstrukt
wird mit EcoRI verdaut und zur Hefetransformation verwendet. Ein
für das
FUS1-HIS3-Reportergen codierendes EcoRI-Fragment wird aus pSL1497
[Stevenson, B. J., Rhodes, N., Errede, B. und Sprague, G. F. (1992)
Genes Dev. 6, 1293] herausgetrennt und zur Transformation entsprechender
Hefestämme
verwendet. Das sst2ΔADE2-Allel
[Dietzel, C. und Kurjan, J. (1987) Mol. Cell. Biol. 7, 4169-4177] wird aus einem
mit PCR unter Verwendung von Oligos, mit denen an Position 1 eine
Cla-Stelle und an Position 2518 eine NheI-Stelle plaziert wurde,
amplifizierten 2,5 kb großen
Fragment des ADE2-Gens aufgebaut. Dieses Fragment wird für den Austausch
des internen ClaI-NheI-Fragments in SST2 verwendet. Das sst2ΔADE2-Fragment
wird durch Verdauung mit SalI freigesetzt und zur Transformation
entsprechender Hefestämme
verwendet.
-
Die
aus mehreren Schritten bestehende Konstruktion des SSTR2-Expressionsplasmids
pJH2 (11) wird durch die Insertion
eines SphI/NarI-Fragments des 3'-nichttranslatierten
Bereichs aus dem STE7-Gen [Teague, M. A., Chaleff, D. T. und Errede,
B. (1986) Proc. Natl. Acad. Sci. USA 83, 7371-7375] sowie eines
EcoRI/BamHI-Fragments des GAL1/10-Promotors [Yocum, R. R., Hanley,
S., West, R., and Ptashne, M. (1984) Mol. Cell. Biol. 4, 1985-1998]
in entsprechende Stellen in YEp352 [Hill, J. E., Myers, A. M., Koerner, T.
J. und Tzagoloff, (1986) Yeast 2, 163-167] gestartet, wobei pEK1 erzeugt wird.
Ein für
das offene Leseraster und Transkriptionsterminationssequenzen des
GAL4-Gens codierendes PCR-Produkt wird mit 5'-EcoRI- und 3'-AatII-Stellen enthaltenden Oligos amplifiziert
und in pEK1 inseriert, wobei pMP3 entsteht. Die für Ratte-SSTR2
codierende cDNA [Strnad, J., Eppler, C. M., Corbett, M. und Hadcock,
J. R. (1993) BBRC 191, 968-976] wird mittels PCR unter Verwendung
von Oligonukleotiden, die den für
den Aminoterminus von SSTR2 codierenden DNA-Sequenzen eine BglII-Stelle
sowie direkt hinter der Translationsstoppstelle eine BglII-Stelle hinzufügen, modifiziert.
Für SSTR2
codierende Sequenzen werden als BglII-PCR-Fragment in die BamHI-Stelle
von pMP3 inseriert.
-
Das
Plasmid pLP82 (12) wird konstruiert, indem
man zunächst
das XhoI/EcoRI-Promotorfragment in pPGKH-SCG1-Gαs [Kang, Y. -S., Kane, J., Kurjan,
J., Stadel, J. M. und Tipper, D. J. (1990) Mol. Cell. Biol. 10,
2582-2590] durch ein aus genomischer Hefe-DNA unter Verwendung von Oligonukleotiden,
durch die an den Positionen -200 and -42 5'-XhoI- und 3'-EcoRI-Stellen eingeführt werden, modifiziertes SCG1-Promotorfragment
[Dietzel, C. und Kurjan, J. (1987) Cell 50, 1001-1010] ersetzt,
wobei das Plasmid pLP61 gebildet wird. Das für die Gαs-Domäne codierende BamHI-Fragment
wird durch ein vergleichbares, für
Gαi2 codierendes
Fragment ersetzt, wobei das Plasmid pLP71 gebildet wird. Das für ein unter
der Kontrolle des SCG1-Promotors exprimiertes chimärisches
SCG1-Gαi2-G-Protein
codierendes XhoI/SalI-Fragment von pLP71 wird in die SalI-Stelle
in pRS414 (Stratagene) übertragen,
wobei pLP82 gebildet wird.
-
Das
Plasmid pLP83 wird konstruiert, indem man das EcoRI-Fragment in
pLP71 durch das für
I codierende EcoRI-Fragment aus pPGKH-SCG1 [Kang, Y. -S., Kane,
J., Kurjan, J., Stadel, J. M. und Tipper, D. J. (1990) Mol. Cell.
Biol. 10, 2582-2590] ersetzt, wobei das Plasmid pLP75 gebildet wird.
Das für
SCG1 codierende XhoI/SalI-Fragment wird in die SalI-Stelle in pRS414
(Stratagene) übertragen,
wobei das Plasmid pLP83 gebildet wird.
-
BEISPIEL 4
-
Auswirkungen
der G-Protein-Expression auf die Empfindlichkeit des Biotests
-
Die
Hefestämme
LY268 (pLP82: CEN pSCG1-Scg1-Gαi2),
LY262 (pRS414-PGK-Scg1-Gαi2:
pRS414 mit dem PGK-Scg1-Gαi2-Xho/SalI-Fragment
aus pPGKH-Scg1-Gαi2
in der SalI-Stelle), LY324 (pLP84: 2μ pSCG1-Scg-Gαi2) und LY284 (pRS424-PGK-Scg-Gαi2: pRS424
mit dem PGK-Scg1-Gαi2-Xho/SalI-Fragment aus
pPGKH-Scg1-Gαi2
in der SalI-Stelle) wurden durch Einbringen der genannten Plasmide
in den Stamm LY260 [einem Derivat von YPH500 (Stratagene) MATa ura
3-52 lys2-801 ade2 trp1D63 his3Δ200
leu2α1 far1ΔLYS2 scg1ΔhisG fus1ΔFUS1-HIS3
sst2ΔADE2,
das das SSTR2-Expressionsplasmid trägt] konstruiert. Übernacht-Flüssigkulturen
in SC-Dextrose (2%) ohne ura und trp wurden auf SC-Lactat-Medium
(2%) ohne ura und trp und anschließend auf SC-Galactose-Medium (2%) ohne
ura und trp überführt. Die
Zellen (2 × 105) werden dann in 30 ml SC-Galactose-Agar
(2%) ohne ura, trp und his ausplattiert, die angegebenen Mengen an
ausgewählten
Verbindungen auf auf der Oberfläche
der Agarplatte befindliche Papierscheibchen aufgetragen und 3-5
Tage bei 30°C
inkubiert (14). Das Ausmaß an Wachstum
um S-14 herum hängt
jeweils von dem im jeweiligen Stamm enthaltenen G-Protein- Expressionsplasmid
ab. Das ausgiebigste Wachstum wird als Reaktion auf S-14 bei LY268
(pLP82: CEN pSCG1-Scg1-Gαi2) beobachtet,
ein geringeres Wachstum ist bei den Stämmen LY262 (pRS414-PGK-Scg1-Gαi2) und LY324
(pLP84: 2μ-pSCG1-Scg-Gαi2) zu sehen,
während LY284
(pRS424-PGK-Scg1-Gαi2)
nur wenig nachweisbares Wachstum zeigt. Diese Ergebnisse stehen
im Einklang mit der beobachteten Hemmung pheromonstimulierter Transkriptionsinduktion
durch erhöhte
Mengen an exprimiertem Gα-Protein.
Somit ist eine präzise
Regulation der G-Protein-Expressionsniveaus in heterologe G-Protein-gekoppelte
Rezeptoren exprimierenden Stämmen
für die
Entwicklung und erfolgreiche Realisierung eines Biotests für mit dem
Rezeptor wechselwirkende Verbindungen entscheidend.
-
Das
Plasmid pLP84 wird konstruiert, indem man zunächst das XhoI/EcoRI-Promotorfragment
in pPGKH-SCG1-Gαs [Kang,
Y. -S., Kane, J., Kurjan, J., Stadel, J. M. und Tipper, D. J. (1990)
Mol. Cell. Biol. 10, 2582-2590] durch ein aus genomischer Hefe-DNA
unter Verwendung von Oligonukleotiden, durch die an den Positionen
-200 and -42 5'-XhoI-
und 3'-EcoRI-Stellen
eingeführt
werden, modifiziertes SCG1-Promotorfragment [Dietzel, C. und Kurjan,
J. (1987) Cell 50, 1001-1010] ersetzt, wobei das Plasmid pLP61 gebildet
wird. Das für
die Gαs-Domäne
codierende BamHI-Fragment
wird durch ein vergleichbares für
Gαi2 codierendes Fragment ersetzt, wobei das
Plasmid pLP71 gebildet wird. Das für ein unter der Kontrolle des
SCG1-Promotors exprimiertes chimärisches
SCG1-Gαi2-G-Protein
codierende XhoI/SalI-Fragment aus pLP71 wird in die SalI-Stelle
in pRS424 (Stratagene) übertragen,
wobei pLP84 gebildet wird.
-
BEISPIEL 5
-
Der Somatostatin-Rezeptor
kann ein Signal über
das endogene Hefe-Gα-Protein übermitteln
-
Man
nimmt an, daß SSTR2
in Säugerzellen
an Gαi2 und Gαi3 koppeln kann [Luthin, D. R., Eppler, C. M.
und Linden, J. (1993) J. Biol. Chem. 268, 5990-5996]. Es konnte
jedoch gezeigt werden, daß SSTR2
ein Signal über
das endogene Hefe-Gα-Protein übermitteln
kann, wenn er in entsprechenden Hefestämmen (unten beschrieben) exprimiert
wird. Diese Beobachtung impliziert eine notwendige Kopplung von
SSTR2 an das endogene Gα-Protein. Die Fähigkeit
heterologer G-Protein-gekoppelter
Rezeptoren zur Kopplung an das endogene Gα-Protein bedeutet eine signifikante Verbesserung
der existierenden Technologie und wird im Stand der Technik nicht
für möglich gehalten
(King K., Dohlman, H. G., Thorner, J., Caron, M. G. und Lefkowitz,
R. J. (1990) Science 250, 121-123). Die Hefestämme LY266 (pLP83: CEN pSCG1-Scg1),
LY280 (pRS414-PGK-Scg1: pRS414 mit dem PGK-Scg1-Xho-SalI-Fragment
aus pPGKH-ScgI in der SalI-Stelle), LY326
(pLP86: 2μ-pSCG1-Scg)
und LY282 (pRS424-pPGK-Scg:
pRS424 mit dem PGK-Scg1-Xho-SalI-Fragment aus pPGKH-Scg1 in der
SalI-Stelle) wurden durch Einbringen der genannten Plasmide in den
Stamm LY260 konstruiert. Übernacht-Flüssigkulturen
dieser Stämme,
die nur SCG1/GPA1 exprimieren können,
in SC-Dextrose (2%) ohne ura und trp wurden auf SC-Lactat-Medium
(2%) ohne ura, trp und anschließend
auf SC-Galactose-Medium (2%) ohne ura und trp überführt. Die Zellen (2 × 105) werden dann in 30 ml SC-Galactose-Medium
(2%) ohne ura, trp und his ausplattiert, die angegebenen Mengen
an ausgewählten
Verbindungen auf auf der Oberfläche
der Agarplatte befindliche Papierscheibchen aufgetragen und 3-5
Tage bei 30°C inkubiert.
Wachstumshöfe
werden um mit verschiedenen Konzentrationen an S-14 gesättigten
Scheibchen herum beobachtet, wodurch demonstriert wird, daß ein produktives
Signal über
eine Wechselwirkung zwischen SSTR2 und dem Hefeprotein SCG1/GPA1 übertragen
werden kann (15). Diese Beobachtungen
zeigen, daß ein
einfacher und breit anwendbarer Biotest realisiert werden kann,
bei dem ein beliebiges Mitglied der Klasse der G-Protein-gekoppelten
Rezeptoren in entsprechend modifizierten Hefestämmen exprimiert und zur Kopplung
an das endogene Gα-Protein
veranlaßt
werden kann.
-
Das
Plasmid pLP86 wird konstruiert, indem man das EcoRI-Fragment in
pLP71 durch das für
SCG1 codierende EcoRI-Fragment aus pPGKH-SCG1 [Kang, Y. -S., Kane,
J., Kurjan, J., Stadel, J. M. und Tipper, D. J. (1990) Mol. Cell.
Biol. 10, 2582-2590] ersetzt, wobei das Plasmid pLP75 gebildet wird.
Das für
SCG1 codierende XhoI/SalI-Fragment
wird in die SalI-Stelle in pRS424 (Stratagene) übertragen, wobei das Plasmid
pLP86 gebildet wird.
-
BEISPIEL 6
-
Mutationen in SST2 verbessern
die Empfindlichkeit der Reaktion auf Somatostatin
-
Mutationen
im SST2-Gen führen
zur Supersensitivität
von Zellen, bei denen es sich ansonsten um Wildtypzellen handelt,
gegenüber
Paarungspheromon. Die Auswirkung dieser Mutation auf die in far1-, FUS1-HIS3-Stämmen exprimierten
AT-Resistenzniveaus wird untersucht. (16).
Zellen (5 × 105) aus Übernachtkulturen
von LY230 [einem Derivat von YPH50 (Stratagene) MATa SST2 ura3-52
lys2-801 ade2 trp1Δ63 his3Δ200 leu2Δ1 far1ΔFUS1-HIS3]
und LY238 (einer Modifikation von LY230 sst2ΔADE2) in SCD-ura, trp werden
auf SCD-ura, trp, his plus 10 mM AT ausplattiert und 2 Tage bei
30 °C inkubiert.
LY238 (sst2) zeigt eine erhöhte
AT-Resistenz als Reaktion auf Paarungsfaktor. Dabei wird LY238-Wachstum um Scheibchen
mit 10 pmol Paarungspheromon herum beobachtet, während LY230 (SST2) 1 nmol Paarungsfaktor
benötigt,
so daß ein
signifikantes Wachstum beobachtet werden kann. Somit steigert die
Einführung
von sst2 in diese Stämme die
Empfindlichkeit des Biotests um mindestens das 100fache, wodurch
ebenso eine Erhöhung
der Empfindlichkeit des SSTR-abhängigen
Biotests ermöglicht
wird.
-
Hefestämme, die
SSTR2 exprimieren und ein defektes sst2-Gen tragen, zeigen ein weitaus
stärkeres Wachstum
um Scheibchen mit verschiedenen Somatostatinkonzentrationen herum
als Stämme
mit einem funktionsfähigen
SST2-Gen. Übernachtkulturen
der Stämme
LY268 (sst2, mit pLP82), LY266 (sst2, mit pLP83), LY288 [einem das
SSTR2-Expressionsplasmid und das SCG1-Gαi2-Expressionsplasmid
pLP82 tragenden Derivat von YPH500 (Stratagene) MATa SST2 ura3-52
lys2-801 ade2 trp1Δ63
his3Δ200
leu2Δ1 far1ΔLYS2 scg1ΔhisG fus1ΔFUS1-HIS3]
und LY290 (einer pLP83 enthaltenden Modifikation von LY288) in SC-Dextrose
(2%) ohne ura, trp wurden auf SC-Lactat-Medium (2%) ohne ura und trp und anschließend auf SC-Galactose-Medium
(2%) ohne ura und trp überführt. Die
Zellen (2 × 105) werden dann auf 30 ml SC-Galactose-Platten (2%) ohne
ura, trp und his ausplattiert, die angegebenen Mengen an ausgewählten Verbindungen
auf auf der Oberfläche
der Agarplatte befindliche Papierscheibchen aufgetragen und 3-5
Tage bei 30°C inkubiert.
Wachstumshöfe
werden um mit verschiedenen Konzentrationen an S-14 gesättigten
Scheibchen herum sowohl bei sst2Δ-
als auch SST2-Stämmen
beobachtet (17), doch ist der von
den Stämmen
LY268 und LY266 (sst2) gezeigte Wachstumsgrad deutlich höher als
der für
die Stämme
LY288 und LY290 (SST2) beobachtete. Weiterhin tritt der Herunterregulationseffekt
von SST2 stärker
in denjenigen Stämmen
zutage, die lediglich das SCG1/GPA1-Wildtypprotein exprimieren,
was damit übereinstimmt,
daß man
von SST2 eine festere Wechselwirkung mit dem nativen Protein als
mit dem chimärischen
SCG1-Gαi2-Protein erwartet.
-
BEISPIEL 7
-
Funktionelle Expression
eines Cholecystokinin (CCKB)-Rezeptors der Ratte
in Hefe
-
Cholecystokinin
(CCK) ist ein Haupthormon im Verdauungstrakt, das eine wichtige
Rolle bei der Steuerung der pankreatischen Sekretion und dem Ausstoß von Gallenflüssigkeit
spielt (1). CCK ist ebenfalls eines der am weitesten verbreiteten
Neuropeptide des Gehirns (2). Die CCK-Effekte werden über die
Wirkung von Zelloberflächenrezeptoren
vermittelt, die sich unter Verwendung pharmakologischer Kriterien
in zwei Subtypen, nämlich
CCKA und CCKB, klassifizieren
lassen (3). Durch molekulare Klonierungsarbeiten konnten cDNAs identifiziert
werden, die für
G-Protein-gekoppelte CCKA- (4) bzw. CCKB- (5-8) Rezeptoren codieren. Kürzlich wurden
Verbindungen mit selektiven CCKB-Rezeptor-Antagonisteneigenschaften
und einer starken anxiolytischen Aktivität identifiziert (9). Die funktionelle
Expression von CCKB-Rezeptoren in Hefe sollte
ein schnelles Screening auf neue Verbindungen mit CCKB-Antagonisteneigenschaften
gestatten und die für
die rationale Konstruktion neuer CCKB-Liganden
erforderliche molekulare Charakterisierung struktureller Aspekte
des CCKB-Rezeptors erleichtern.
-
Material und
Methoden
-
Plasmidkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (10)
durchgeführt.
Der Ratte-CCKB-Rezeptor wurde von Rattenhirn-cDNA
mittels PCR unter Verwendung von Oligonukleotidprimern, mit denen
an den 5'- und 3'-Enden BglII-Stellen eingeführt werden
(5'-AAAAGATCTAAAATGGACCTGCTCAAGCTG,
3'-AAAAGATCTTCAGCCAGGCCCCAGTGTGCT),
kloniert. Das CCKB-Rezeptor-Expressionsplasmid
pJH20 wurde konstruiert, indem das mit BglII verdaute PCR-Fragment
in der korrekten Orientierung in das mit BamHI geschnittene pMP3
(11) inseriert wurde. Die in der vorliegenden Arbeit verwendeten
Gα-Protein-Expressionsplasmide
wurden konstruiert, indem für
die 47 carboxyterminalen Aminosäuren
von GPA1 codierende DNA-Sequenzen in pLP83 (11) durch solche für Gαs (pLP122),
Gαi2 (pLP121) ersetzt wurden.
-
Stammkonstruktionen.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standardverfahren (12). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die als Grundlage für alle in
diesem Bericht beschriebenen Experimente verwendeten Hefestämme wurden
mittels sequentieller Insertionsdeletion unter Verwendung rekombinanter
Allele konstruiert. Den Ratte-CCKB-Rezeptor exprimierende
Hefestämme
wurden mittels sequentieller DNA-vermittelter Transformation von
LY296 (MATa ura3-52 trp1Δ63
his3Δ200
leu2Δ1 ade2-101
lys2-801 gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
Ref. 7) mit pJH20 und danach mit den oben beschriebenen Gα-Protein-Expressionsplasmiden
konstruiert.
-
Sättigungsbindungstests
mit radioaktiv markiertem Agonisten. Hefemembranrohextrakte wurden
von Kulturen in der späten
log-Phase mittels Glasperlenlyse und Zentrifugation bei 40000 × g nach
einem veröffentlichten
Verfahren (13) präpariert.
Der Proteingehalt der Membranrohfraktionen wurde mit dem Biorad-Proteintestkit gemäß den Angaben
des Herstellers gemessen. Radioligandenbindungstests wurden gemäß Strnad
et al. (14) mit 3H-CCK-8 (Amersham) in Gegenwart
von 150 mM NaCl ausgeführt.
Als nicht-spezifische Bindung wurde die in Gegenwart von 1 μM CCK-4 beobachtete
Bindung definiert. In aus Zellen ohne CCKB-Rezeptor hergestellten
Membranfraktionen wurde eine vernachlässigbare spezifische Bindung
beobachtet (Daten nicht gezeigt).
-
Biotest.
Ein Funktionstest für
in Hefe exprimierten CCKB-Rezeptor wurde
unter Verwendung einer Modifikation eines Standardverfahrens (11)
ausgeführt.
Dabei wurden Hefestämme über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil und Tryptophan (SCD-ura-trp) angezogen, zur Entfernung
von Glucoseresten gewaschen und über
Nacht in 5 ml SC-Galactose
(2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (50 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium (30 ml, durch Zugabe von
konzentriertem KOH oder NH4OH vor dem Autoklavieren
auf pH 6,8 eingestellt) wurde mit der Übernachtkultur (2 × 104 Zellen/ml) angeimpft und in quadratische
(9 × 9
cm) Petrischalen gegossen. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen der genannten Verbindungen enthaltendem DMSO gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert. Cholecystokinine (CCK-4, CCK-8), Somatostatin (S-14)
und Metenkephalin stammten von Bachem. Oxymetazolin, Isoproterenol
und Carbachol stammten von Sigma.
-
ERGEBNISSE
-
Bindung
von Cholecystokinin an den in Hefe exprimierten Ratte-CCKB-Rezeptor. Die funktionelle Expression des
Ratte-CCKB-Rezeptors auf hohem Niveau in
der Hefe war eine notwendige Voraussetzung für die Entwicklung eines sinnvollen
Biotests. Dabei wurde die Ratte-CCKB-Rezeptor-cDNA unter
die Kontrolle des GAL1-Promotors im Plasmid pJH20 gestellt. Mit
diesem Konstrukt wird auch die induzierbare Überexpression von Gal4p, dem
Transkriptionsaktivierungsprotein für galactoseinduzierbare Gene,
verliehen, was zu deutlich erhöhten
Niveaus an Rezeptorprotein in Membranrohfraktionen im Vergleich
zu einem von einem Plasmid ohne GAL4-Sequenzen exprimierten Rezeptor führt (Daten
nicht gezeigt). CCKB-Rezeptorsequenzen wurden
in pJH20 ohne Modifikation der proteincodierenden Sequenzen eingeführt. Von
King et al. wurde bereits berichtet, daß der Austausch der aminoterminalen
Domäne
des β2-adrenergen
Rezeptors gegen die äquivalente
STE2-Sequenz für
eine effiziente Rezeptorexpression in der Hefe notwendig war (15).
Im Gegensatz dazu benötigt
die funktionelle Expression des CCKB-Rezeptors
in der Hefe keine Addition von Hefesequenzen an den Aminoterminus.
Es wurden die Expression chimärischer
Gα-Proteine,
die sich aus der aminoterminalen βγ-Wechselwirkungsdomäne von Gpa1p
und carboxyterminalen Rezeptorwechselwirkungsdomänen von Ratte-Gαi2 (pLP121)
oder -Gαs (pLP122) zusammensetzen, unter der Kontrolle
des GPA1-Promotors
verleihende Plasmide konstruiert. Hefestämme, die exprimierten CCKB-Rezeptor sowie chimärisches Gαi2-(LY628) bzw. Gαs-
(LY631) Protein enthalten, wurden durch Transformation eines durch
die Deletion von für
Komponenten des Paarungssignaltransduktionswegs codierenden Genen
modifizierten Hefestamms (LY296) mit CCKB-Rezeptor-
und Gα-Protein-Expressionsplasmiden
konstruiert. Die meisten G-Protein-gekoppelten Rezeptoren zeigen
jeweils agonistenabhängige
hoch- und niedrigaffine Zustände.
Die hochaffine Agonistenbindung hängt von der funktionellen Assoziation
des Rezeptors mit einem heterotrimeren G-Protein ab. Falls der Rezeptor nicht
mit dem G-Protein assoziiert oder von diesem entkoppelt ist, liegt
eine niedrigaffine Agonistenbindung vor, die in Sättigungsbindungstests
mit radioaktiv markiertem Agonisten nicht nachweisbar ist. In aus LY631-Zellen
hergestellten Hefe-Membranrohfraktionen
band der Agonist 3H-CCK-8 mit hoher Affinität und auf sättigbare
Weise an den CCKB-Rezeptor (18), womit demonstriert wurde, daß (1) eine
funktionelle ligandenbindende Konformation des CCKB-Rezeptors in der
Hefe exprimiert wurde und (2) der Rezeptor funktionell mit dem chimärischen
Gα-Protein
unter Ausbildung eines hochaffinen Agonistenbindungszustands assoziiert war.
Der in Hefe exprimierte CCKB-Rezeptor zeigte
eine Affinität
für 3H-CCK-8
(Kd = 8 nM), die wesentlich niedriger als
der hochaffine Bindungszustand des in Säugerzellen exprimierten CCKB-Rezeptors (Kd =
100 pM, Ref. 5) war, was vielleicht an einer ineffizienten Wechselwirkung
mit der Rezeptorwechselwirkungsdomäne von Ratte-Gαs lag.
Man würde
erwarten, daß diese
Bindungsparameter den nativen Werten in Extrakten aus das zugehörige Gα-Protein Gαq (5-8) enthaltenden
Zellen stärker ähneln. Die
Gesamtzahl an beobachteten 3H-CCK-8-Bindungsstellen
(Bmax = 206 fmol/mg) stand im Einklang mit
Werten, die für
den α-Paarungspheromon-Rezeptor
der Hefe erhalten wurden (200 fmol/mg, Ref. 16). Bei vielen G-Protein-gekoppelten Rezeptoren ist
die hochaffine Agonistenbindung gegenüber GTP und dessen Analogen
empfindlich. GTP-Analoge induzieren die Dissoziation des Rezeptor/G-Protein-Komplexes,
was zu einem niedrigaffinen Agonistenbindungszustand führt. Die
Zugabe von GppNHp (100 μM),
einem nicht hydrolysierbaren GTP-Analog, zu einem Agonistenbindungstest
reduziert die spezifische Bindung von 3H-CCK-8
an den CCKB-Rezeptor in Membranrohfraktionen
aus LY631-Zellen um mehr als 50%. Diese Ergebnisse stellen einen
weiteren Hinweis auf die funktionelle Kopplung zwischen dem CCKB-Rezeptor und dem chimärischen Gα-Protein dar. Somit zeigt der
in Hefe exprimierte Ratte-CCKB-Rezeptor
Eigenschaften einer hochaffinen Agonistenbindung, die mit den in
Säugergeweben
beobachteten vergleichbar sind.
-
Die
Agonistenselektivität
des CCKB-Rezeptors blieb bei der Expression
in Hefe erhalten. Es wurde ein selektiver und empfindlicher Biotest
entwickelt, bei dem Hefestämme
verwendet werden, die die oben beschriebenen genetischen Modifikationen
sowie die Expression des CCKB-Rezeptors
und chimärischer
Gαi2- und Gαs-Proteine verleihende Plasmide tragen. Eine
dosisabhängige
Wachstumsreaktion von LY628- und LY631-Zellen war um das aufgetragene CCK-4
deutlich erkennbar (19). Der Test
war selektiv: der Durchmesser der Wachstumszonen war zur angegebenen
Affinität
der Liganden für
den CCKB-Rezeptor (CCK-8 > Gastrin > CCK-4) proportional,
was die Fähigkeit
des Biotests zur Unterscheidung zwischen Liganden mit unterschiedlicher
Potency (5-8) widerspiegelt. Nachweisbare Wachstumsreaktionen wurden
weder als Antwort auf verschiedene für andere G-Protein-gekoppelte
Rezeptoren selektive Agonisten (Somatostatin, Metenkephalin, Oxymetazolin,
Isoproterenol, Carbachol) noch für
Hefezellen, denen der CCKB-Rezeptor fehlt,
beobachtet (Daten nicht gezeigt). Eine nachweisbare Reaktion wurde
gegenüber
10 μg CCK-4
beobachtet.
-
DISKUSSION
-
An
den CCK-Rezeptoren wirkende Verbindungen, insbesondere Antagonisten,
können
ein großes
therapeutisches Potential besitzen (3). In der Peripherie machen
die Hemmwirkungen von CCK-Antagonisten
diese zu ausgezeichneten Kandidaten für die Behandlung von Pankreatitis,
Bauchspeicheldrüsenkrebs,
Gallenkolik, Störungen
der Magenentleerung und Reizkolon. Durch CCK-Antagonisten wird die
Entwicklung einer Übersättigung
aufgehoben, so daß sie
sich zur Verbesserung des Appetits bei Patienten mit Anorexie oder
anderen, bei denen eine erhöhte
Nahrungsaufnahme erforderlich ist, eignen könnten. Umgekehrt könnten CCK-Agonisten
als Appetitzügler
geeignet sein. Durch CCK-Antagonisten wird auch die Opiatanalgesie
potenziert, so daß sie
sich zur Verwendung bei der Kontrolle klinischer Schmerzzustände eignen
könnten.
Im ZNS zeigen ausgewählte
CCK-Antagonisten Potential als leistungsfähige Anxiolytika (9). Ferner
lindern CCK-Antagonisten
das mit dem Absetzen von Arzneimitteln assoziierte Angstgefühl und könnten somit
eine Verwendung bei der Behandlung der Entziehung von allgemein
mißbrauchten
Arzneimitteln finden. CCK-Agonisten könnten als
Antipsychotika eingesetzt werden.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Ivy, A.C. und E. Oldberg. 1928. J. Physiol. (London)
86: 599-613.
- 2. Dockray, G.J.R. 1976. Immunochemical evidence of cholecystokinin-like
peptides in brain. Nature 264: 568-570.
- 3. Woodruff, G.N. und J. Hughes. 1991. Cholecystokinin antagonists.
Annu. Rev. Pharmacol. Toxicol. 31: 469-501.
- 4. Wank, S.A., R. Harkins, R.T. Jensen, H. Shapiro, A. de Weerth
und T. Slattery. 1992. Purification, molecular cloning, and function
expression of the cholecystokinin receptor from rat pancreas. Proc.
Natl. Acad. Sci. USA 89: 3125-3129.
- 5. Kopin, A.S., Y-M. Lee, E.W. McBride, L.J. Miller, M. Liu,
H.Y. Lin, L.F. Kolakowski und M. Beinborn. 1992. Expression cloning
and characterization of the canine parietal cell gastrin receptor.
Proc. Natl. Acad. Sci. USA 89: 3605-3609.
- 6. Wank, S.A., J.R. Pisenga und A. de Weerth. 1992. Brain and
gastrointestinal cholecystokinin receptor family: Structure and
function. Proc. Natl. Acad. Sci. USA 89: 8691-8695.
- 7. Lee, Y-M., M. Beinborn, E.W. McBride, M. Lu, L.F. Kolakowski
und A.S. Kopin. 1993. The human brain cholecystokinin-B/gastrin
Receptor. J. Biol. Chem. 268: 8164-8169.
- 8. Ito, M., T. Matsui, T. Taniguchi, T. Tsukamoto, T. Murayama,
N. Arima, H. Nakata, T. Chiba und K. Chibura. 1993. Functional characterization
of a human brain cholecystokinin-B receptor. J. Biol. Chem. 268: 18300-18305.
- 9. Hughes, J., P. Boden, B. Costall, A. Domeney, E. Kelly, D.C.
Horwell, J.C. Hunter, R.D. Pinnock und G.N. Woodruff. 1990. Development
of a class of selective cholecystokinin type B receptor antagonists
having potent anxiolytic activity. Proc. Natl. Acad. Sci. USA 87:
6728-6732.
- 10. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 11. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 12. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
- 13. Blumer, K. J., J. E. Reneke und J. Thorner. 1988. The STE2
gene product is the ligand-binding component of the α-factor receptor
of Saccharomyces cerevisiae. J. Biol. Chem. 263: 10836-10842.
- 14. Strnad, J., C. M. Eppler,, M. Corbett und J. R. Hadcock.
1993. The rat SSTR2 somatostatin receptor subtype is coupled to
inhibition of cyclic AMP accumulation. Biochem. Biophys. Res. Comm.
191: 968-976.
- 15. King, K., H. G. Dohlman, J. Thorner, M. G. Caron und R.J.
Lefkowitz. 1990. Control of yeast mating signal transduction by
a mammalian β2-adrenergic receptor and Gs α subunit.
Science 250: 121-123.
- 16. Weiner, J. L., C. Guttierez-Steil und K. J. Blumer. 1993.
Disruption of receptor-G protein coupling in yeast promotes the
function of an SST2-dependent adaptation pathway. J. Biol. Chem.
268: 8070-8077.
-
BEISPIEL 9
-
Funktionelle Expression
eines Adenosinrezeptors A2a der Ratte in
Hefe
-
Adenosin
wirkt ebenso wie ATP und verwandte purinerge Verbindungen sowohl
als neurohormonales Agens als auch als den Vorgang der Kommunikation
von Zelle zu Zelle steuerndes Autokoid (1). In dieser Rolle reguliert
Adenosin eine große
Bandbreite physiologischer Funktionen, einschließlich Herzschlagfrequenz und Kontraktilität, Tonus
der glatten Muskulatur, Sedation, Freisetzung von Neurotransmittern,
Blutplättchenfunktion,
Lipolyse, Nierenfunktion und Funktion der weißen Blutkörperchen. Dabei werden die
Adenosineffekte über die
Wirkung von Zelloberflächenrezeptoren
vermittelt, die sich unter Anwendung pharmakologischer Kriterien in
drei Subtypen, nämlich
A1, A2a und A2b sowie A3, klassifizieren
lassen. Durch molekulare Klonierungsarbeiten konnten cDNAs identifiziert
werden, die für
G-Protein-gekoppelte A1- (2-5), A2a- und A2b- (6-9) und A3-
(10) Adenosinrezeptoren codieren. Die funktionelle Expression von
Adenosinrezeptoren in Hefe sollte ein schnelles Screening auf neue
Verbindungen mit Adenosin-Agonisten- und -Antagonisteneigenschaften
gestatten und die für
die rationale Konstruktion neuer Adenosinliganden erforderliche
molekulare Charakterisierung struktureller Aspekte des Adenosinrezeptors
erleichtern.
-
MATERIAL UND
METHODEN
-
Plasmidkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (11)
durchgeführt.
Der Ratte-A2a-Adenosinrezeptor (9) wurde
von Rattenhirn-cDNA mittels PCR unter Verwendung von Oligonukleotidprimern,
mit denen an den 5'-
und 3'-Enden BamHI-Stellen
eingeführt
werden (5'-GAAGATCTAAAAAATGGGCTCCTCGGTGTAC,
3'-ACATGCATGCAGATCTTCAGGAAGGGGCAAACTC),
kloniert. Das A2a-Adenosinrezeptor-Expressionsplasmid
pJH21 wurde konstruiert, indem das mit BglII verdaute PCR-Fragment
in der korrekten Orientierung in das mit BamHI geschnittene pMP3
(12) inseriert wurde. Zur konstitutiven Expression des A2a-Adenosinrezeptors in glucosehaltigem Medium
wurde der Expressionsvektor pLP100 konstruiert. Dabei wurden für Transkriptionsregulationssequenzen
aus dem ADH1-Gen (&)
codierende DNA-Fragmente mittels PCR amplifiziert und in pRS426
inseriert. Ein ADH1-Transkriptionsterminatorfragment wurde aus genomischer
Hefe-DNA (YPH501, Stratagene) unter Verwendung synthetischer Oligonukleotide,
mit denen eine 5'-XhoI-
(TTTCTCGAGCGAATTTCTTATGATTT) und eine 3'-KpnI- (TTTGGTACCGGGCCCGGACGGATTACAACAGGT) Stelle
hinzugefügt
wurden, amplifiziert. Ein ADH1-Promotorfragment
wurde aus genomischer Hefe-DNA unter Verwendung synthetischer Oligonukleotide,
mit denen eine 5'-SacI-
(GGGAGCTCTGATGGTGGTACATRACG) und eine 3'-BamHI-
(GGGGGATCCTGTATATGAGATAGTTGA) Stelle hinzugefügt wurden, amplifiziert. Das
A2a-Adenosinrezeptor-Expressionsplasmid pLP116 wurde konstruiert,
indem ein für
den A2a-Adenosinrezeptor codierendes und
unter Verwendung von Oligonukleotiden, mit denen eine 5'-BglII- (AAAGATCTAAAATGGGCTCCTCGGTGTAC)
und eine 3'-SalI- (AAGTCGACTCAGGAAGGGGCAAACTC)
Stelle hinzugefügt
wurden, amplifiziertes PCR-Fragment in das mit BamHI und SalI geschnittene pLP100
inseriert wurde. Die in der vorliegenden Arbeit verwendeten Gα-Protein-Expressionsplasmide
wurden konstruiert, indem für
die 47 carboxyterminalen Aminosäuren
von GPA1 codierende DNA-Sequenzen in pLP83 (12) durch solche für Gαs (pLP122)
und Gαi2 (pLP121) ersetzt wurden.
-
Stammkonstruktionen.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standardverfahren (13). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die als Grundlage für alle in
diesem Bericht beschriebenen Experimente verwendeten Hefestämme wurden
mittels sequentieller Insertionsdeletion unter Verwendung rekombinanter
Allele konstruiert. Den Ratte-A2a-Adenosinrezeptor
exprimierende Hefestämme
wurden mittels sequentieller DNA-vermittelter Transformation von
LY296 (MATa ura3-52 trpiΔ63
his3Δ200
leu2Δ1 ade2-101 lys2-801 gpa1ΔhisG far1ΔLYS2 FUS1-HIS3
sst2ΔAΔE2, Ref.
12) mit A2a-Adenosinrezeptor-Expressionsplasmiden
und danach mit den oben beschriebenen Gα-Protein-Expressionsplasmiden konstruiert.
-
Sättigungsbindungstests
mit radioaktiv markiertem Agonisten. Hefemembranrohextrakte wurden
von Kulturen in der späten
log-Phase mittels Glasperlenlyse und Zentrifugation bei 40000 × g nach
einem veröffentlichten
Verfahren (14) präpariert.
Der Proteingehalt der Membranrohfraktionen wurde mit dem Biorad-Proteintestkit gemäß den Herstellerangaben
gemessen. Radioligandenbindungstests wurden gemäß Strnad et al. (15) mit 3H-NECA (Amersham) ausgeführt. Als nichtspezifische Bindung
wurde die in Gegenwart von 1 μM NECA
beobachtete Bindung definiert. In aus Zellen ohne A2a-Adenosinrezeptor
hergestellten Membranfraktionen wurde eine vernachlässigbare
spezifische Bindung beobachtet (Daten nicht gezeigt).
-
Biotest.
Ein Funktionstest für
den in Hefe exprimierten A2a-Adenosinrezeptor
wurde unter Verwendung einer Modifikation eines Standardverfahrens
(12) ausgeführt.
Dabei wurden Hefestämme über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil und Tryptophan (SCD-ura-trp-Medium) angezogen, zur
Entfernung von Glucoseresten gewaschen und über Nacht in 5 ml SC-Galactose
(2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (50 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium
(30 ml, durch Zugabe von konzentriertem KOH oder NH4OH
vor dem Autoklavieren auf pH 6,8 eingestellt) wurde mit der Übernachtkultur
(2 × 104 Zellen/ml) angeimpft und in quadratischen (9 × 9 cm)
Petrischalen ausplattiert. Zur Expression des A2a-Adenosinrezeptors
in glucosehaltigem Medium wurden der ersten Übernachtkultur Proben entnommen
und in wie oben zusammengesetztem Agarmedium mit Glucose (2%) statt
Galactose getestet. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen der genannten Verbindungen enthaltendem DMSO gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert. Die Adenosinliganden CGS-21680, NECA und DPMA wurden
von RBI bezogen. Somatostatin (S-14) und Metenkephalin stammten
von Bachem. Oxymetazolin, Isoproterenol und Carbachol stammten von
Sigma.
-
ERGEBNISSE
-
Bindung
von Adenosin-Agonisten an den in Hefe exprimierten Ratte-A2a-Adenosinrezeptor. Die funktionelle Expression
des Ratte-A2a-Adenosinrezeptors auf hohem
Niveau in der Hefe war eine notwendige Voraussetzung für die Entwicklung
eines sinnvollen Biotests. Dabei wurde im Plasmid pJH21 die Ratte-A2a-Adenosinrezeptor-cDNA
unter die Kontrolle des induzierbaren GAL1-Promotors gestellt. Mit
diesem Konstrukt wird auch die induzierbare Überexpression von Gal4p, dem
Transkriptionsaktivierungsprotein für galactoseinduzierbare Gene,
verliehen, was zu deutlich erhöhten
Niveaus an Rezeptorprotein in Membranrohfraktionen im Vergleich
zu einem von einem Plasmid ohne GAL4-Sequenzen exprimierten Rezeptor
führt (Daten
nicht gezeigt). Das Plasmid pLP116 verleiht eine konstitutive Expression
des A2a-Adenosinrezeptors auf hohem Niveau unter
der Kontrolle des ADH1-Promotors. Bei beiden Plasmiden wurden für den A2a-Adenosinrezeptor codierende DNA-Sequenzen
ohne Modifikation der proteincodierenden Sequenzen eingeführt. Von
King et al. wurde bereits berichtet, daß der Austausch der aminoterminalen
Domäne
des β2-adrenergen Rezeptors gegen die äquivalente
STE2-Sequenz für
eine effiziente Rezeptorexpression in der Hefe notwendig war (16).
Im Gegensatz dazu benötigt
die funktionelle Expression des A2a-Adenosinrezeptors
in der Hefe keine Addition von Hefesequenzen an den Aminoterminus.
Es wurde ein chimärisches
Gα-Protein,
das sich aus der vorgeschlagenen aminoterminalen βγ-Wechselwirkungsdomäne von Gpa1p
und einer carboxyterminalen Rezeptorwechselwirkungsdomäne von Ratte-Gαs (pLP122)
unter der Kontrolle des GPA1-Promotors zusammensetzt, konstruiert.
Hefestämme,
die exprimierten A2a-Adenosinrezeptor sowie
chimärisches
Gα-Protein
enthalten, wurden durch Transformation eines durch die Deletion
von für
Komponenten des Paarungssignaltransduktionswegs codierenden Genen
modifizierten Hefestamms (LY296) mit A2a-Adenosinrezeptor-
und Gα-Protein-Expressionsplasmiden
konstruiert.
-
Die
meisten G-Protein-gekoppelten Rezeptoren zeigen jeweils agonistenabhängige hoch-
und niedrigaffine Zustände.
Die hochaffine Agonistenbindung hängt von der funktionellen Assoziation
des Rezeptors mit einem heterotrimeren G-Protein ab. Falls der Rezeptor
nicht mit dem G-Protein assoziiert oder von diesem entkoppelt ist,
liegt eine niedrigaffine Agonistenbindung vor, die in Sättigungsbindungstests
mit radioaktiv markiertem Agonisten nicht nachweisbar ist. In Hefe-Membranrohfraktionen
aus pLP116 und pLP122 tragenden Zellen (LY626) band der Agonist 3H-NECA mit hoher Affinität und auf sättigbare Weise an den A2a-Adenosinrezeptor
(20), womit demonstriert wurde, daß (1) eine
funktionelle ligandenbindende Konformation des A2a-Adenosinrezeptors
in der Hefe exprimiert wurde und (2) der Rezeptor funktionell mit
dem chimärischen Gα-Protein
unter Ausbildung eines hochaffinen Agonistenbindungszustands assoziiert
war. Die Gesamtzahl an beobachteten 3H-NECA-Bindungsstellen
(Bmax = 242 fmol/mg) überschritt Werte, die für den α-Paarungspheromon-Rezeptor
der Hefe erhalten worden waren (200 fmol/mg, Ref. 17). Die Affinität von [3H]-NECA
für den
A2a-Adenosinrezeptor in Hefemembranen (Kd-8 μM) ist mit
der in Säugerzellen
beobachteten gleichwertig, was auf eine funktionelle Kopplung zwischen
Rezeptor und G-Protein hindeutet.
-
Die
Agonistenselektivität
des A2a-Adenosinrezeptors blieb bei der
Expression in Hefe erhalten. Es wurde ein selektiver und empfindlicher
Biotest entwickelt, bei dem ein Hefestamm (LY595) verwendet werden,
der die oben beschriebenen genetischen Modifikationen sowie die
Expression des A2a-Adenosinrezeptors (pLP116)
und von GPA1 (pLP83) verleihende Plasmide trägt. Eine dosisabhängige Wachstumsreaktion
von LY595-Zellen war um aufgetragenes CGS-21680, einem A2a-Adenosinrezeptor selektiven Agonisten,
deutlich erkennbar, wobei die Wachstumsreaktion deutlich stärker als
die von auf NECA und DPMA reagierenden Zellen war (21). Der Test war selektiv: der Durchmesser der
Wachstumszonen war zur angegebenen Affinität der Liganden für den A2a-Adenosinrezeptor
(CGS-21680>NECA=DPMA)
proportional, was die Fähigkeit
des Biotests zur Unterscheidung zwischen Liganden mit unterschiedlicher
Potency widerspiegelt. Nachweisbare Wachstumsreaktionen wurden weder
als Antwort auf verschiedene für
andere G-Protein-gekoppelte
Rezeptoren selektive Agonisten (Somatostatin, Metenkephalin, Oxymetazolin,
Isoproterenol, Carbachol) noch für
Hefezellen, denen der A2a-Adenosinrezeptor
fehlt, beobachtet (Daten nicht gezeigt). Eine nachweisbare Reaktion wurde
gegenüber
10 μg CGS-21680
beobachtet.
-
DISKUSSION
-
Für Verbindungen,
die die Funktion der Adenosinrezeptoren modulieren (1), gibt es
viele therapeutische Anwendungsmöglichkeiten.
Adenosin-Agonisten können
bei der Behandlung epileptischer Anfälle und zur Verhinderung einer
neuronalen Schädigung
bei Schlaganfall und neurodegenerativen Erkrankungen geeignet sein.
Die antidysrhythmische Wirkung von Adenosin läßt vermuten, daß Adenosin-Agonisten
bei der Behandlung der Komplex-Tachykardie wirksam sein könnten. A2-Adenosin-Agonisten besitzen eine starke sedative,
antikonvulsive und anxiolytische Aktivität. A2a-Adenosin-selektive
Agonisten können
für die
Stimulierung der Lipolyse in Fettgewebe geeignet sein, was ihnen
eine Eignung als Therapien zur Gewichtsabnahme oder als Antidiabetika
sowie bei der Verbesserung der Fleischqualität landwirtschaftlicher Nutztiere
verleiht. A1-Adenosin-Antagonisten können bei der Behandlung von
akuter Nierenfehlfunktion geeignet sein. A3-Adenosin-Antagonisten können bei
der Modulation der Mastzellen-Degranulierung
zur Behandlung entzündlicher Erkrankungen,
einschließlich
Asthma, nützlich
sein.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Jacobsen, K.A., P.J.M. van Galen und M. Williams. 1992.
Adenosine receptors: Pharmacology, structureactivity relationships,
and therapeutic potential. J. Med. Chem. 35: 407-422.
- 2. Libert, F., S.N. Schiffmann, A. Lefort, M. Parmentier, C.
Gerard, J.E. Dumont, J.-J. Vanderhaeghen und G. Vassart. 1991. The
orphan receptor cDNA RDC7 encodes an A1 adenosine receptor. EMBO
J. 10: 1677-1682.
- 3. Mahan, L.C., L.D. McVittie, E.M. Smyk-Randal, H. Nakata,
F.J. Monsma, C.R. Green und D.R. Sibley. 1991. Cloning and expression
of an A1 adenosine receptor from rat brain.
Mol. Pharmacol: 40: 1-7.
- 4. Olah, M.E., H. Ren, J. Ostrowski, K.A. Jacobsen und G.L.
Stiles. 1992. Cloning, expression and characterization of the unique
bovine A1 adenosine receptor. J. Biol. Chem.
267: 10764-10770.
- 5. Tucker, A.L., J. Linden, A.S. Robeva, D.D. D'angelo und K.R. Lynch.
1992. Cloning and expression of a bovine adenosine A1 receptor
cDNA. FEBS Lett. 297: 107-111.
- 6. Maenhaut, C., J. van Sande, F. Libert, M. Abramowicz, M.
Parmentier, J.-J. E. Dumont, G. Vassart und S Schiffmann. 1990.
RDC8 codes for an adenosine A2 receptor with physiological constitutive
activity. Bioch. Biophys. Res. Comm. 173: 1169-1178.
- 7. Pierce, K.D., Furlong, T.J., L.A. Stehle und J. Shine. 1992.
Molecular cloning and expression of an adenosine A2b receptor from
human brain. Bioch. Biophys. Res. Comm. 187: 86-93.
- 8. Chern, Y., K. King, H.-L. Lai und H.-T. Lai. 1992. Molecular
cloning of a novel adenosine receptor gene from rat brain. Bioch.
Biophys. Res. Comm. 185: 304-309.
- 9. Stehle, J.H., S.A. Rivkees, J.J. Lee, D.R. Weaver, J.D. Deeds
und S.M. Reppert. 1992. Molecular cloning and expression of the
cDNA for a novel A2 adenosine receptor subtype.
Mol. Endocrinol. 6: 384-393.
- 10. Zhou, Q.-Y., C. Li, M.E. Olah, R.A. Johnson, G.L. Stiles
und O. Civelli. 1992. Molecular cloning and characterization of
an adenosine receptor: The A3 adenosine receptor. Proc. Natl. Acad.
Sci. USA 89: 7432-7436.
- 11. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 12. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 13. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
- 14. Blumer, K. J., J. E. Reneke und J. Thorner. 1988. The STE2
gene product is the ligand-binding component of the α-factor receptor
of Saccharomyces cerevisiae. J. Biol. Chem. 263: 10836-10842.
- 15. Strnad, J., C. M. Eppler,, M. Corbett und J. R. Hadcock.
1993. The rat SSTR2 somatostatin receptor subtype is coupled to
inhibition of cyclic AMP accumulation. Biochem. Biophys. Res. Comm.
191: 968-976.
- 16. King, K., H. G. Dohlman, J. Thorner, M. G. Caron und R.J.
Lefkowitz. 1990. Control of yeast mating signal transduction by
a mammalian β2-adrenergic receptor and Gs α subunit.
Science 250: 121-123.
- 17. Weiner, J. L., C. Guttierez-Steil und K. J. Blumer. 1993.
Disruption of receptor-G protein coupling in yeast promotes the
function of an SST2-dependent adaptation pathway. J. Biol. Chem.
268: 8070-8077.
-
BEISPIEL 8
-
Funktionelle Expression
eines Somatostatin-Subtyp-5-Rezeptors
der Ratte in Hefe
-
Das
zyklische Tetradecapeptid Somatostatin ist ein starker Inhibitor
der Sekretion mehrerer Hormone, einschließlich Wachstumshormon aus der
Hypophyse, Glucagon und Insulin aus der Bauchspeicheldrüse und Gastrin
aus dem Darm. Somatostatin wirkt auch als Neurotransmitter, und
es konnte gezeigt werden, daß es breite
modulatorische Effekte im ZNS und in peripheren Geweben besitzt
(1). Die Somatostatineffekte werden über die Bindung des Hormons
an hochaffine, plasmamembranständige
Somatostatinrezeptoren (SSTR) transduziert (2). Die in fünf verschiedenen
Subtypen (SSTR1-5) codierten SSTR, was teilweise die gewebespezifischen
Unterschiede in den Reaktionen auf Somatostatin erklärt (3-10),
umfassen eine Unterfamilie der Superfamilie der Sieben-Transmembrandomänen-, G-Protein-gekoppelten
Rezeptoren, die Reaktionen auf eine breite Vielfalt extrazellulärer Signale
vermittelt. Die funktionelle Expression von SSTR5 in Hefe sollte ein
schnelles Screening auf neue subtypenselektive Somatostatin-Agonisten
und Verbindungen mit Antagonisteneigenschaften gestatten und die
für die
rationale Konstruktion neuer Somatostatinliganden erforderliche molekulare
Charakterisierung struktureller Aspekte des SSTR5 erleichtern.
-
MATERIAL UND
METHODEN
-
Plasmidkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (11)
durchgeführt.
Der Ratte-SSTR5 (7) wurde aus genomischer Ratten-DNA mittels PCR
unter Verwendung von Oligonukleotidprimern, mit denen an den 5'- und 3'-Enden BglII-Stellen
eingeführt
werden (5'-AAAAAGATCTAAAATGGAGCCCCTCTCTCTG,
3'-AGCAGATCTTCAGATCCCAGAAGACAAC),
kloniert. Das SSTR5-Expressionsplasmid pJH19 wurde konstruiert,
indem das mit BglII verdaute PCR-Fragment in der korrekten Orientierung
in das mit BamHI geschnittene pMP3 (12) inseriert wurde. Die in
der vorliegenden Arbeit verwendeten Gα-Protein-Expressionsplasmide wurden konstruiert,
indem für
die 47 carboxyterminalen Aminosäuren
von GPA1 codierende DNA-Sequenzen in pLP83 (12) durch solche für Gαs (pLP122)
und Gαi2 (pLP121) ersetzt wurden.
-
Stammkonstruktionen.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standardverfahren (13). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die als Grundlage für alle in
diesem Bericht beschriebenen Experimente verwendeten Hefestämme wurden
mittels sequentieller Insertionsdeletion unter Verwendung rekombinanter
Allele konstruiert. SSTR5 exprimierende Hefestämme wurden mittels sequentieller DNA-vermittelter Transformation
von LY296 (MATa ura3-52 trp1Δ63
his3Δ200
leu2Δ1 ade2-101
lys2-801 gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
Ref. 12) mit pJH19 und danach mit den oben beschriebenen Gα-Protein-Expressionsplasmiden
konstruiert.
-
Biotest.
Ein Funktionstest für
den in Hefe exprimierten SSTR5 wurde unter Verwendung einer Modifikation
eines Standardverfahrens (12) ausgeführt. Dabei wurden Hefestämme über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil und Tryptophan (SCD-ura-trp-Medium) angezogen, zur
Entfernung von Glucoseresten gewaschen und über Nacht in 5 ml SC-Galactose (2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (55 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium
(30 μl,
durch Zugabe von konzentriertem KOH oder NH4OH
vor dem Autoklavieren auf pH 6,8 eingestellt) wurde mit der Übernachtkultur
(2 × 104 Zellen/ml) angeimpft und in quadratischen
(9 × 9
cm) Petrischalen ausplattiert. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen der genannten Verbindungen enthaltendem sterilem Wasser gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert. Somatostatin (S-14, S-28) und Metenkephalin sowie CCK-8
stammten von Bachem. Oxymetazolin, Isoproterenol und Carbachol stammten
von Sigma.
-
ERGEBNISSE
-
Somatostatin-abhängige Wachstumsreaktion
von den SSTR5 exprimierenden Hefezellen. Die funktionelle Expression
des SSTR5 auf hohem Niveau in der Hefe war eine notwendige Voraussetzung
für die
Entwicklung eines sinnvollen Biotests. Dabei wurde im Plasmid pJH19
die SSTR5-cDNA unter die Kontrolle des induzierbaren GAL1-Promotors gestellt.
Mit diesem Konstrukt wird auch die induzierbare Überexpression von Gal4p, dem
Transkriptionsaktivierungsprotein für galactoseinduzierbare Gene,
verliehen, was zu deutlich erhöhten
Niveaus an Rezeptorprotein in Membranrohfraktionen im Vergleich
zu einem von einem Plasmid ohne GAL4-Sequenzen exprimierten Rezeptor führt (Daten
nicht gezeigt). SSTR5-Sequenzen wurden in pJH19 ohne Modifikation
der proteincodierenden Sequenzen eingeführt. Von King et al. wurde
bereits berichtet, daß der
Austausch der aminoterminalen Domäne des β2-adrenergen Rezeptors gegen die äquivalente
STE2-Sequenz für
eine effiziente Rezeptorexpression in der Hefe notwendig war (15).
Im Gegensatz dazu benötigt
die funktionelle Expression von SSTR5 in der Hefe keine Addition
von Hefesequenzen an den Aminoterminus. Es wurde ein chimärisches
Gα-Protein,
das sich aus der vorgeschlagenen aminoterminalen β2-Wechselwirkungsdomäne von Gpa1p
und einer carboxyterminalen Rezeptorwechselwirkungsdomäne von Ratte-Gαi2 (pLP121) unter
der Kontrolle des GPA1-Promotors zusammensetzt, konstruiert. Ein
Hefestamm (LY620), der exprimierten SSTR5 sowie chimärisches
Gα-Protein
enthält,
wurde durch Transformation eines durch die Deletion von für Komponenten
des Paarungssignaltransduktionswegs codierenden Genen modifizierten
Hefestamms (LY296) mit SSTR5- (pJH19) und Gα-Protein-Expressionsplasmiden
(pLP121) konstruiert. Eine dosisabhängige Wachstumsreaktion von
LY620-Zellen war um das aufgetragene S-14 herum deutlich erkennbar
(22). Nachweisbare Wachstumsreaktionen wurden weder
als Antwort auf verschiedene für
andere G-Protein-gekoppelte
Rezeptoren selektive Agonisten (CCK 8, Metenkephalin, Oxymetazolin,
Isoproterenol, Carbachol) noch für
Hefezellen, denen der SSTR5 fehlt, beobachtet (Daten nicht gezeigt).
Eine nachweisbare Reaktion wurde gegenüber 60 nmol S-14 beobachtet.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Brazeau, P., W. Vale, R. Burgus, N. Ling, M. Butcher,
J. Rivier und R. Guillemin. 1973. Hypothalamic polypeptide that
inhibits the secretion of immunoreactive pituitary growth hormone.
Science 129: 77-79.
- 2. Raisine, T. und G. I. Bell. 1993. Molecular biology of somatostatin
receptors. Trends Neurosci. 16: 34-38.
- 3. Meyerhof, W., H.-J. Paust, C. Schonrock und D. Richter. 1991.
Cloning of a cDNA encoding a novel putative G protein-coupled receptor
expressed in specific rat brain regions. DNA Cell Biol. 10: 689-694.
- 4. Bruno, J. F., Y. Xu, J. Song und M. Berelowitz. 1992. Molecular
cloning and functional expression of a brain specific somatostatin
receptor. Proc. Natl. Acad. Sci. USA 89: 11151-11155.
- 5. Kluxen, F.-W., C. Bruns und H. Lubbert. 1992. Expression
cloning of a rat brain somatostatin receptor. Proc. Natl. Acad.
Sci. USA 89: 4618-4622.
- 6. Li, X.-J., M. Forte, R. A. North, C. A. Ross und S. H. Snyder.
1992. Cloning and expression of a rat somatostatin receptor enriched
in brain. J. Biol. Chem. 267: 21307-21312.
- 7. O'Carrol,
A.-M., S. J. Lolait, M. Konig und L. Mahan. 1992. Molecular cloning
and expression of a pituitary somatostatin receptor with preferential
affinity for somatostatin-28. Mol. Pharmacol. 42: 939-946.
- 8. Yasuda, K., S. Rens-Domiano, C. D. Breder, S. F. Law, C.
B. Saper, T. Reisine und G. I. Bell. 1992. Cloning of a novel somatostatin
receptor, SSTR3, coupled to adenylylcyclase. J. Biol. Chem. 267
(28): 20422-20428.
- 9. Yamada, Y., S. R. Post, K. Wang, H. S. Tager, G. I. Bell
und S. Seino. 1992. Cloning and functional characterization of a
family of human and mouse somatostatin receptors expressed in brain,
gastrointestinal tract, and kidney. Proc. Natl. Acad. Sci. USA 89:
251-255.
- 10. Strnad, J., C. M. Eppler,, M. Corbett and J. R. Hadcock.
1993. The rat SSTR2 somatostatin receptor subtype is coupled to
inhibition of cyclic AMP accumulation. Biochem. Biophys. Res. Comm.
191: 968-976.
- 11. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 12. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 13. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
- 14. Blumer, K. J., J. E. Reneke und J. Thorner. 1988. The STE2
gene product is the ligand-binding component of the α-factor receptor
of Saccharomyces cerevisiae. J. Biol. Chem. 263: 10836-10842.
- 15. King, K., H. G. Dohlman, J. Thorner, M. G. Caron und R.J.
Lefkowitz. 1990. Control of yeast mating signal transduction by
a mammalian β2-adrenergic receptor and Gα α subunit.
Science 250: 121-123.
- 16. Weiner, J. L., C. Guttierez-Steil und K. J. Blumer. 1993.
Disruption of receptor-G protein coupling in yeast promotes the
function of an SST2-dependent adaptation pathway. J. Biol. Chem.
268: 8070-8077.
-
Beispiel 10
-
Funktionelle Expression
des Somatostatin-Subtyp-2-Rezeptors
(SSTR2) des Schweins in Hefe
-
Das
zyklische Tetradecapeptid Somatostatin ist ein starker Inhibitor
der Sekretion mehrerer Hormone, einschließlich Wachstumshormon aus der
Hypophyse, Glucagon und Insulin aus der Bauchspeicheldrüse und Gastrin
aus dem Darm. Somatostatin wirkt auch als Neurotransmitter, und
es konnte gezeigt werden, daß es breite
modulatorische Effekte im ZNS und in peripheren Geweben besitzt
(1). Die Somatostatineffekte werden über die Bindung des Hormons
an hochaffine, plasmamembranständige
Somatostatinrezeptoren (SSTR) transduziert (2). Die in fünf verschiedenen
Subtypen (SSTR1-5) codierten SSTR, was teilweise die gewebespezifischen
Unterschiede in den Reaktionen auf Somatostatin erklärt (3-11),
umfassen eine Unterfamilie der Superfamilie der Sieben-Transmembrandomänen-, G-Protein-gekoppelten
Rezeptoren, die Reaktionen auf eine breite Vielfalt extrazellulärer Signale
vermittelt. Die funktionelle Expression von Schwein-SSTR2 in Hefe
sollte ein schnelles Screening auf neue subtypenselektive Somatostatin-Agonisten
und Verbindungen mit Antagonisteneigenschaften gestatten und die
für die
rationale Konstruktion neuer Somatostatinliganden erforderliche
molekulare Charakterisierung struktureller Aspekte des Schwein-SSTR2 erleichtern.
In Screens mit hohem Durchsatz auf Mechanismusbasis identifizierte
Verbindungen stellen Anhaltspunkte für neue wachstumsverbessernde
Agentien zur Verwendung in Schweinen dar.
-
MATERIAL UND
METHODEN
-
Plasmidkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (12)
durchgeführt.
Der Schwein-SSTR2 (11) wurde aus einer cDNA-Bank von menschlichem
Gehirn mittels PCR unter Verwendung von Oligonukleotidprimern, mit
denen an den 5'-
und 3'-Enden BglII-Stellen
eingeführt werden
(5'-AAAAGATCTAAAATGTCCATTCCATTTGAC,
3'-AAAAGGTACCAGATCTTCAGATACTGGTTTGGAG),
kloniert. Das Schwein-SSTR2-Expressionsplasmid pJH18 wurde konstruiert,
indem das mit BglII verdaute PCR-Fragment in der korrekten Orientierung
in das mit BamHI geschnittene pMP3 (13) inseriert wurde.
-
Stammkonstruktionen.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standardverfahren (14). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die als Grundlage für alle in
diesem Bericht beschriebenen Experimente verwendeten Hefestämme wurden
mittels sequentieller Insertionsdeletion unter Verwendung rekombinanter
Allele konstruiert. Den Schwein-SSTR2 exprimierende Hefestämme wurden
mittels sequentieller DNA-vermittelter Transformation von LY296
(MATa ura3-52 trp1Δ63
his3Δ200
leu2Δ1 ade2-101 lys2-801
gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
Ref. 13) mit dem chimärischen
Gαi2-Protein-Expressionsplasmid pLP82 (13)
und danach mit pJH18 oder pJH17 konstruiert.
-
Sättigungsbindungstests
mit radioaktiv markiertem Agonisten. Hefemembranrohextrakte wurden
von Kulturen in der späten
log-Phase mittels Glasperlenlyse und Zentrifugation bei 40000 × g nach
einem veröffentlichten
Verfahren (15) präpariert.
Der Proteingehalt der Membranrohfraktionen wurde mit dem Biorad- Proteintestkit gemäß den Herstellerangaben
gemessen. Radioligandenbindungstests wurden gemäß Strnad et al. (10) mit radioaktiv
markiertem Somatostatin (125I-tyr11-S-14,
Amersham) ausgeführt.
Als nicht-spezifische Bindung wurde die in Gegenwart von 1 μM S-14 beobachtete
Bindung definiert. In aus Zellen ohne Schwein-SSTR2 hergestellten
Membranfraktionen wurde eine vernachlässigbare spezifische Bindung
beobachtet (Daten nicht gezeigt).
-
Biotest.
Ein Funktionstest für
den in Hefe exprimierten Schwein-SSTR2 wurde unter Verwendung einer Modifikation
eines Standardverfahrens (13) ausgeführt. Dabei wurden Hefestämme über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil und Tryptophan (SCD-ura-trp-Medium) angezogen, zur
Entfernung von Glucoseresten gewaschen und über Nacht in 5 ml SC-Galactose (2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (55 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium
(30 ml, durch Zugabe von konzentriertem KOH oder NH4OH
vor dem Autoklavieren auf pH 6,8 eingestellt) wurde mit der Übernachtkultur
(2 × 104 Zellen/ml) angeimpft und in quadratischen
(9 × 9
cm) Petrischalen ausplattiert. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen der genannten Verbindungen enthaltendem sterilem Wasser gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert. Somatostatin (S-14, S-28) und Metenkephalin stammten
von Bachem. Oxymetazolin, Isoproterenol und Carbachol stammten von
Sigma. MK678 und Sandostatin wurden synthetisiert.
-
ERGEBNISSE
-
Bindung
von Somatostatin an den in Hefe exprimierten Schwein-SSTR2-Rezeptor.
Die funktionelle Expression des Schwein-SSTR2-Rezeptors auf hohem
Niveau in der Hefe war eine notwendige Voraussetzung für die Entwicklung eines
sinnvollen Biotests. Dabei wurde im Plasmid pJH17 und 18 die Schwein-SSTR2-cDNA
unter die Kontrolle des GAL1-Promotors gestellt. Mit diesen Konstrukten
wird auch die induzierbare Überexpression
von Gal4p, dem Transkriptionsaktivierungsprotein für galactoseinduzierbare
Gene, verliehen, was zu deutlich erhöhten Niveaus an Rezeptorprotein
in Membranrohfraktionen im Vergleich zu einem von einem Plasmid
ohne GAL4-Sequenzen
exprimierten Rezeptor führt
(Daten nicht gezeigt). Die Schwein-SSTR2-Rezeptor-Sequenzen wurden
in pJH18 ohne Modifikation der proteincodierenden Sequenzen eingeführt. Von King
et al. wurde bereits berichtet, daß der Austausch der aminoterminalen
Domäne
des β2-adrenergen Rezeptors gegen die äquivalente
STE2-Sequenz für eine effiziente
Rezeptorexpression in der Hefe notwendig war (16). Im Gegensatz
dazu benötigt
die funktionelle Expression des Schwein-SSTR2-Rezeptors in der Hefe keine
Addition von Hefesequenzen an den Aminoterminus. Es wurde ein chimärisches
Gα-Protein,
das sich aus der vorgeschlagenen aminoterminalen βγ-Wechselwirkungsdomäne von Gpa1p
und einer carboxyterminalen Rezeptorwechselwirkungsdomäne von Ratte-Gαi2 (pLP82)
unter der Kontrolle des GPA1-Promotors
zusammensetzt, konstruiert. Hefestämme, die exprimierten Schwein-SSTR2
sowie chimärisches
Gα-Protein enthalten,
wurden durch Transformation eines durch die Deletion von für Komponenten
des Paarungssignaltransduktionswegs codierenden Genen modifizierten
Hefestamms (LY296) mit Expressionsplasmiden für Schwein-SSTR2 (pJH17, pJH18)
und Ga-Protein (pLP82) konstruiert.
-
Die
meisten G-Protein-gekoppelten Rezeptoren zeigen jeweils agonistenabhängige hoch-
und niedrigaffine Zustände.
Die hochaffine Agonistenbindung hängt von der funktionellen Assoziation
des Rezeptors mit einem heterotrimeren G-Protein ab. Falls der Rezeptor
nicht mit dem G-Protein assoziiert oder von diesem entkoppelt ist,
liegt eine niedrigaffine Agonistenbindung vor, die in Sättigungsbindungstests
mit radioaktiv markiertem Agonisten nicht nachweisbar ist. In Hefe-Membranrohfraktionen
aus pJH17 tragenden Zellen band der Agonist 125I-tyr11-S-14 mit hoher Affinität und auf sättigbare Weise an den Schwein-SSTR2,
womit demonstriert wurde, daß (1)
eine funktionelle 1igandenbindende Konformation des Schwein-SSTR2
in der Hefe exprimiert wurde und (2) der Rezeptor funktionell mit
dem chimärischen
Gα-Protein
unter Ausbildung eines hochaffinen Agonistenbindungszustands assoziiert
war. Die Gesamtzahl an beobachteten 125I-tyr11-S-14-Bindungsstellen (Bmax = 146 fmol/mg) stand im Einklang mit
Werten, die für
den α-Paarungspheromon-Rezeptor
der Hefe erhalten worden waren (200 fmol/mg, Ref. 17).
-
Die
Agonistenselektivität
des Schwein-SSTR2 blieb bei der Expression in Hefe erhalten. Es
wurde ein selektiver und empfindlicher Biotest entwickelt, bei dem
ein Hefestamm (LY474) verwendet wird, der die oben beschriebenen
genetischen Modifikationen sowie die Expression des Schwein-SSTR2
(pJH18) und eines chimärischen
Gpa1-Gαi2-Proteins (pLP82) verleihende Plasmide
trägt.
Eine dosisabhängige
Wachstumsreaktion von LY474-Zellen war um aufgetragenes S-14, MK678
und Sandostatin deutlich erkennbar (23).
Der Test war selektiv: der Durchmesser der Wachstumszonen war zur
angegebenen Affinität
der Liganden für
den Schwein-SSTR2
(S-14=MK678>Sandostatin)
proportional, was die Fähigkeit
des Biotests zur Unterscheidung zwischen Liganden mit unterschiedlicher
Potency widerspiegelt (18). Nachweisbare Wachstumsreaktionen wurden
weder als Antwort auf verschiedene für andere G-Protein-gekoppelte Rezeptoren
selektive Agonisten (Metenkephalin, Oxymetazolin, Isoproterenol,
Carbachol) noch für
Hefezellen, denen der Schwein-SSTR2 fehlt, beobachtet (Daten nicht
gezeigt). Eine nachweisbare Reaktion wurde gegenüber nur 60 pmol S-14 beobachtet,
wodurch die außerordentliche
Empfindlichkeit des Biotests veranschaulicht wird.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Brazeau, P., W. Vale, R. Burgus, N. Ling, M. Butcher,
J. Rivier und R. Guillemin. 1973. Hypothalamic polypeptide that
inhibits the secretion of immunoreactive pituitary growth hormone.
Science 129: 77-79.
- 2. Reisine, T. und G. I. Bell. 1993. Molecular biology of somatostatin
receptors. Trends Neurosci. 16: 34-38.
- 3. Meyerhof, W., H.-J. Paust, C. Schonrock und D. Richter. 1991.
Cloning of a cDNA encoding a novel putative G protein-coupled receptor
expressed in specific rat brain regions. DNA Cell Biol. 10: 689-694.
- 4. Bruno, J. F., Y. Xu, J. Song und M. Berelowitz. 1992. Molecular
cloning and functional expression of a brain specific somatostatin
receptor. Proc. Natl. Acad. Sci. USA 89: 11151-11155.
- 5. Kluxen, F.-W., C. Bruns und H. Lobbert. 1992. Expression
cloning of a rat brain somatostatin receptor. Proc. Natl. Acad.
Sci. USA 89: 4618-4622.
- 6. Li, X.-J., M. Forte, R. A. North, C. A. Ross und S. H. Snyder.
1992. Cloning and expression of a rat somatostatin receptor enriched
in brain. J. Biol. Chem. 267: 21307-21312.
- 7. O'Carrol,
A.-M., S. J. Lolait, M. Konig und L. Mahan. 1992. Molecular cloning
and expression of a pituitary somatostatin receptor with preferential
affinity for somatostatin-28. Mol. Pharmacol. 42: 939-946.
- 8. Yasuda, K., S. Rens-Domiano, C. D. Breder, S. F. Law, C.
B. Saper, T. Reisine und G. I. Bell. 1992. Cloning of a novel somatostatin
receptor, SSTR3, coupled to adenylylcyclase. J. Biol. Chem. 267
(28): 20422-20428.
- 9. Yamada, Y., S. R. Post, K. Wang, H. S. Tager, G. I. Bell
und S. Seino. 1992. Cloning and functional characterization of a
family of human and mouse somatostatin receptors expressed in brain,
gastrointestinal tract, and kidney. Proc. Natl. Acad. Sci. USA 89:
251-255.
- 10. Strnad, J., C. M. Eppler, M. Corbett und J. R. Hadcock.
1993. The rat SSTR2 somatostatin receptor subtype is coupled to
inhibition of cyclic AMP accumulation. Biochem. Biophys. Res. Comm.
191: 968-976.
- 11. Matsumoto, K., Y. Yokogoshi, Y. Fujinaka, C. Z. Xhang und
S. Saito. 1994. Molecular cloning and sequencing of porcine somatostatin
receptor 2. Biochem. Biophys. Res. Comm. 199: 298-305.
- 12. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 13. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 14. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
- 15. Blumer, K. J., J. E. Reneke und J. Thorner. 1988. The STE2
gene product is the ligand-binding component of the α-factor receptor
of Saccharomyces cerevisiae. J. Biol. Chem. 263: 10836-10842.
- 16. King, K., H. G. Dohlman, J. Thorner, M. G. Caron und R.J.
Lefkowitz. 1990. Control of yeast mating signal transduction by
a mammalian β2-adrenergic receptor and Gs α subunit.
Science 250: 121-123.
- 17. Weiner, J. L., C. Guttierez-Steil und K. J. Blumer. 1993.
Disruption of receptor-G protein coupling in yeast promotes the
function of an SST2-dependent adaptation pathway. J. Biol. Chem.
268: 8070-8077.
- 18. Marbach, P., W. Bauer und U. Briner. 1988. Structure-function
relationships of somatostatin analogs. Horm. Res. 29: 54-58.
-
BEISPIEL 11
-
Die Empfindlichkeit der
Antwort gegenüber
Agonisten wird durch die Deletion von MSG5 erhöht.
-
Die
Reaktionsfähigkeit
eines Signaltransduktionssystems gegenüber einem Dauerreiz nimmt mit
der Zeit ab. Dieses Phänomen,
das unter dem Namen Desensibilisierung oder Adaption bekannt ist,
ist ein allgemeines Kennzeichen eines Signalantwortsystems. Für den Paarungssignaltransduktionsweg
der Hefe wurden mehrere molekulare Mechanismen für die Adaption beschrieben
(1). Mutationen im SST2-Gen vermitteln Adaptionsdefekte sowie eine
erhöhte
Paarungspheromonempfindlichkeit (2,3). Die Reaktion von den Ratte-SSTR2
funktionell exprimierenden Hefezellen auf appliziertes Somatostatin
ist in sst2-Mutantenzellen stark erhöht (4). Man würde erwarten,
daß Mutationen
in anderen Genen, deren Produkte eine Rolle bei der Adaptionsantwort
spielen, ähnliche
Effekte hervorrufen. Durch Mutationen im MSG5-Gen, das für eine putative Protein-Tyrosinphosphatase
codiert, wird die Empfindlichkeit gegenüber Paarungspheromon stark
erhöht
(5). In der vorliegenden Arbeit führt die Deletion von MSG5 in
den Ratte-SSTR2 exprimierenden Zellen zu einem starken Anstieg der
Empfindlichkeit gegenüber
Somatostatin. Der Effekt der MSG5-Mutation ist bei einer SST2-Deletionsmutation
additiv. Die sst2-msg5-Doppelmutantenzellen bilden die Grundlage
für einen äußerst empfindlichen
Biotest auf Verbindungen, die mit G-Protein-gekoppelten Rezeptoren
und G-Proteinen wechselwirken.
-
MATERIAL UND
METHODEN
-
Stammkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (6)
durchgeführt.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standard verfahren (7). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die in diesen Experimenten
beschriebenen Hefestämme
wurden unter Verwendung des rekombinanten msg5ΔLeu2-Allels in pS/PDel und Multikopien-YEpMSG5
(5) konstruiert. Veränderte
MSG5-Niveaus tragende Hefestämme
wurden über
DNA-vermittelte Hefetransformation von LY268 (MATa ura3-52 trp1D63
his3D200 leu2D1 ade2-101 lys2-801 gpa1ΔhisG far1ΔLYS2 FUS1-HIS3 sst2ΔADE2, pJH2,
pLP82) unter Erhalt von MPY459 (LY268 msg5ΔLeu2 sst2ΔADE2) und MPY467 (LY268 YEpMSG5)
sowie von LY288 (LY268 SST2) unter Erhalt von MPY458 (LY288 msg5ΔLeu2 SST2)
und MPY466 (LY288 YEpMSG5) konstruiert (4).
-
Biotest.
Ein Funktionsbiotest für
den in Hefe exprimierten Ratte-SSTR2 wurde unter Verwendung einer Modifikation
eines Standardverfahrens (4) ausgeführt. Dabei wurden Hefestämme über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil, Tryptophan und Leucin (SCD-ura-trp-leu-Medium) angezogen,
zur Entfernung von Glucoseresten gewaschen und über Nacht in 5 ml SC-Galactose
(2%)-ura-trp-leu-Flüssigmedium
angezogen. Geschmolzenes (55 °C)
SC-Galactose (2%)-ura-trp-leu-his-Agarmedium (35 ml, durch Zugabe
von konzentriertem NH4OH vor dem Autoklavieren
auf pH 6,8 eingestellt) wurde mit der Übernachtkultur (2 × 104 Zellen/ml) angeimpft und in quadratischen
(9 × 9
cm) Petrischalen ausplattiert. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen des Somatostatins (S-14) enthaltendem sterilem Wasser gesättigt. Die Platten
wurden 3 Tage bei 30 °C
inkubiert. Somatostatin (S-14) stammte von Bachem.
-
ERGEBNISSE
-
Die
Empfindlichkeit gegenüber
Ligand wird durch Deletion von MSG5 gesteigert. Die Effekte von Änderungen
in der Expression des MSG5-Genprodukts wurden analysiert, indem
die Wachstumsreaktion von den Ratte-SSTR2 exprimierenden Zellen
gegenüber
S-14 verglichen wurde (24).
Man würde
erwarten, daß Mutationen,
durch die die MSG5-Adaptionsfunktion aufgehoben wird, zu einer erhöhten Empfindlichkeit des
Biotests gegenüber
aufgetragenem S-14 führt,
während
die Überexpression
von MSG5 die Wachstumsreaktion abschwächen sollte. Wie erwartet wurde
bei LY288 (SST2 MSG5) eine dosisabhängige Wachstumsreaktion gegenüber aufgetragenem
S-14 beobachtet. In Übereinstimmung
mit den Erwartungen führt
die Deletion des MSG5-Gens in MPY458 zu einer wesentlichen Verbesserung
der Empfindlichkeit des Biotests. Die Wachstumsreaktion von MPY458
ist mit der von LY268 (sst2ΔADE2,
MSG5) gezeigten vergleichbar. Bei der Doppelmutante MPY459 (msg5ΔLeu2 sst2ΔADE2), die
eine weitere Verbesserung der Wachstumsreaktion zeigte, wurden die
Effekte von Mutationen in beiden Genen beobachtet. Durch die Überexpression
von MSG5 in SST2- (MPY466) und sst2ΔADE2- (MPY467) Stämmen wurde
die Wachstumsreaktion stark reduziert.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Sprague, G. F. und J. W. Thorner. 1992. Pheromone response
and signal transduction during the mating process of Saccharomyces
cerevisiae, 657-744. In J. R. Pringle, E. W. Jones and J. R. Broach,
Gene expression, 2. Cold Spring Harbor Laboratory Press, Cold Spring
Harbor, NY.
- 2. Chan, R. K. und C. A. Otte. 1982. Isolation and genetic analysis
of Saccharomyces cerevisiae mutants supersensitive to G1 arrest
by α factor
and a factor pheromones. Mol. Cell. Biol. 2: 11-20.
- 3. Chan, R. K. und C. A. Otte. 1982. Physiological characterization
of Saccharomyces cerevisiae mutants supersensitive to G1 arrest
by α factor
and a factor pheromones. Mol. Cell. Biol. 2: 21-29.
- 4. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 5. Doi, K., A. Gartner, G. Ammerer, B. Errede, H. Shinkawa,
K. Sugimoto und K. Matsumoto. 1994. MSG5, a novel protein phosphatase
promotes adaptation to pheromone response in S. cerevisiae. EMBO
J. 13: 61-70.
- 6. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 7. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
-
BEISPIEL 12
-
Funktionelle Expression
eines menschlichen GRF (Growth Hormone Release Factor) -Rezeptors
in Hefe
-
Bei
dem GRF (Growth Hormone Release Factor) handelt es sich um einen
starken Stimulator der Sekretion von Wachstumshormon aus der Hypophyse
(1). Die GRF-Effekte werden über
die Bindung des Hormons an hochaffine, plasmamembranständige GRF-Rezeptoren
transduziert. Der GRF-Rezeptor sowie verwandte Rezeptoren der Secretin-Klasse bilden eine
Unterfamilie der Superfamilie der Sieben-Transmembrandomänen-, G-Protein-gekoppelten
Rezeptoren, die Reaktionen auf eine breite Vielfalt extrazellulärer Signale vermittelt,
und zeichnen sich durch das Vorhandensein einer großen aminoterminalen
Ligandenbindungsdomäne
aus (2). Die funktionelle Expression des menschlichen GRF-Rezeptors
(3) in Hefe sollte ein schnelles Screening auf neue speziesselektive
Agonisten gestatten und die für
die rationale Konstruktion neuer Liganden des GRF-Rezeptors erforderliche
molekulare Charakterisierung erleichtern. GRF-Agonisten repräsentieren
eine neue Klasse wachstumsfördernder
Agentien zur Verwendung in landwirtschaftlichen Nutztieren und könnten eine
therapeutische Anwendung beim Menschen bei der Kontrolle des Wachstums
von kleinwüchsigen
Kindern finden.
-
MATERIAL UND
METHODEN
-
Plasmidkonstruktionen.
Alle molekularbiologischen Manipulationen wurden gemäß Standardverfahren (4)
durchgeführt.
Der menschliche GRF-Rezeptor (3) wurde aus einer cDNA-Bank von menschlichem
Gehirn mittels PCR unter Verwendung von Oligonukleotidprimern, mit
denen an den 5'-
und 3'-Enden BamHI-Stellen eingeführt werden
(5'-ATAGGATCCAAAATGGACCGCCGGATGTGGGGG,
3'-ATATGGATCCCTAGCACATAGATGTCAG),
kloniert. Das GRF-Rezeptor-Expressionsplasmid
pJH25 wurde konstruiert, indem das mit BamHI verdaute PCR-Fragment
in der korrekten Orientierung in das mit BamHI geschnittene pMP3
(5) inseriert wurde. Die in der vorliegenden Arbeit verwendeten
Ga-Protein-Expressionsplasmide wurden konstruiert,
indem für
die 47 carboxyterminalen Aminosäuren
von GPA1 codierende DNA-Sequenzen in pLP83 (12) durch solche für Gαs (pLP122)
ersetzt wurden.
-
Stammkonstruktionen.
Die Konstruktion der Hefestämme
sowie die Formulierung der Wachstumsmedien und Kultivierungsbedingungen
erfolgten nach Standardverfahren (6). Die DNA-vermittelte Hefetransformation
wurde mit dem Lithiumacetatverfahren durchgeführt. Die als Grundlage für alle in
diesem Bericht beschriebenen Experimente verwendeten Hefestämme wurden
mittels sequentieller Insertionsdeletion unter Verwendung rekombinanter
Allele konstruiert. Den menschlichen GRF-Rezeptor exprimierende Hefestämme wurden
mittels sequentieller DNA-vermittelter Transformation von LY296
(MATa ura3-52 trp1Δ63
his3Δ200
leu2Δ1 ade2-101
lys2-801 gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
Ref. 5) mit pJH25 und danach mit dem chimärischen Gas-Protein-Expressionsplasmid
pLP122 (5) konstruiert.
-
Biotest.
Ein Funktionstest für
den in Hefe exprimierten menschlichen GRF-Rezeptor wurde unter Verwendung
einer Modifikation eines Standardverfahrens (5) ausgeführt. Dabei
wurden Hefestämme über Nacht in
2 ml synthetischem komplettem Flüssigmedium
mit Glucose (2%) und ohne Uracil und Tryptophan (SCD-ura-trp-Medium)
angezogen, zur Entfernung von Glucoseresten gewaschen und über Nacht
in 5 ml SC-Galactose (2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (55 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium
(30 ml, durch Zugabe von konzentriertem KOH oder NH4OH
vor dem Autoklavieren auf pH 6,8 eingestellt) wurde mit der Übernachtkultur
(2 × 104 Zellen/ml) angeimpft und in quadratische (9 × 9 cm)
Petrischalen gegossen. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die angegebenen
Mengen der genannten Verbindungen enthaltendem sterilem Wasser gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert. Menschlicher GRF (hGRF (1-29)-NH2),
(D-ala2)-hGRF (1-29)-NH2 und Metenkephalin stammten von Bachem.
Oxymetazolin, Isoproterenol und Carbachol stammten von Sigma.
-
ERGEBNISSE
-
Bindung
von GRF an den in Hefe exprimierten menschlichen GRF-Rezeptor. Die
funktionelle Expression des menschlichen GRF-Rezeptors auf hohem
Niveau in der Hefe war eine notwendige Voraussetzung für die Entwicklung
eines sinnvollen Biotests. Dabei wurde im Plasmid pJH25 die GRF-Rezeptor-cDNA
unter die Kontrolle des GAL1-Promotors gestellt. Mit diesen Konstrukten
wird auch die induzierbare Überexpression
von Gal4p, dem Transkriptionsaktivierungsprotein für galactoseinduzierbare
Gene, verliehen, was zu deutlich erhöhten Niveaus an Rezeptorprotein
in Membranrohfraktionen im Vergleich zu einem von einem Plasmid
ohne GAL4-Sequenzen
exprimierten Rezeptor führt
(Daten nicht gezeigt). Die GRF-Rezeptor-Sequenzen wurden in pJH25
ohne Modifikation der proteincodierenden Sequenzen eingeführt. Von
King et al. wurde bereits berichtet, daß der Austausch der aminoterminalen
Domäne
des β2-adrenergen
Rezeptors gegen die äquivalente STE2-Sequenz
für eine
effiziente Rezeptorexpression in der Hefe notwendig war (9). Im
Gegensatz dazu benötigt
die funktionelle Expression des GRF-Rezeptors in der Hefe keine
Addition von Hefesequenzen an den Aminoterminus. Es wurde ein chimärisches
Gα-Protein,
das sich aus der vorgeschlagenen aminoterminalen βγ-Wechselwirkungsdomäne von Gpa1p
und einer carboxyterminalen Rezeptorwechselwirkungsdomäne von Ratte-Gas (pLP122) unter der Kontrolle des GPA1-Promotors
zusammensetzt, konstruiert. Hefestämme, die exprimierten GRF-Rezeptor
sowie chimärisches
Ga-Protein enthalten, wurden durch Transformation
eines durch die Deletion von für
Komponenten des Paarungssignaltransduktionswegs codierenden Genen
modifizierten Hefestamms (LY296) mit Expressionsplasmiden für menschlichen
GRF-Rezeptor (pJH25) und chimärisches
Gpa1-Gαs-Protein (pLP122) konstruiert.
-
Die
Agonistenselektivität
des menschlichen GRF-Rezeptors
blieb bei der Expression in Hefe erhalten. Es wurde ein selektiver
und empfindlicher Biotest entwickelt, bei dem ein Hefestamm (CY990)
verwendet wird, der die oben beschriebenen genetischen Modifikationen
sowie die Expression des menschlichen GRF-Rezeptors (pJH25) und
eines chimärischen
Gpa1-Gαs-Proteins
(pLP122) verleihende Plasmide trägt.
Eine dosisabhängige
Wachstumsreaktion von CY990-Zellen war um ein aufgetragenes Agonistenanalog
von GRF [hGRF (1-29)-NH2] herum deutlich erkennbar [25A], die durch die Koapplikation eines Antagonistenanalogs [(D-arg2)-hGRF
(1-29)-NH2] gehemmt wurde [25B]. Der Test war selektiv: nachweisbare Wachstumsreaktionen
wurden weder als Antwort auf verschiedene für andere G-Protein-gekoppelte Rezeptoren
selektive Agonisten (Metenkephalin, Oxymetazolin, Isoproterenol,
Carbachol) noch für
Hefezellen, denen der GRF-Rezeptor fehlt, beobachtet (Daten nicht
gezeigt). Eine nachweisbare Reaktion wurde gegenüber 20 nmol GRF beobachtet,
wodurch die Empfindlichkeit des Biotests veranschaulicht wird.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Bohlen, P. F. Esch, P. Brazeau, N. Ling und Guillemin.
1983. Isolation and characterization of the porcine hypothalamic
growth hormone releasing factor. Biochem. Biophys. Res. Comm. 116:
726-734.
- 2. Segre, G. V, und S. R. Goldring. 1993. Receptors for secretin,
calcitonin, parathyroid hormone (PTH)/PTH-related peptide, vasoactive
intestinal peptide, glucagonlike peptide 1, growth hormone releasing hormone,
and glucagon belong to a newly discovered G protein linked receptor
family. Trends Endo. Metab. 4: 309-314.
- 3. Gaylinn, B. D., J. K. Harrison, J. R. Zysk, C. E. Lyons,
K. R. Lynch und M. O. Thorner. 1993. Molecular cloning and expression
of a human anterior pituitary receptor for growth hormonereleasing
hormone. Mol. Endocrinol. 7: 77-84.
- 4. Sambrook, J., E. F. Fritsch und T. Maniatis. 1989. Molecular
Cloning, A Laboratory Handbook. Cold Spring Harbor Press. Cold Spring
Harbor, NY.
- 5. Price, L.A., E.M. Kajkowski, J.R. Hadcock, B.A. Ozenberger
und M.H. Pausch. 1995. Yeast cell growth in response to agonist
dependent activation of a mammalian somatostatin receptor. Eingereicht.
- 6. Rose, M., F. Winston und P. Hieter. 1990. Methods in Yeast
Genetics. Cold Spring Harbor Press. Cold Spring Harbor, NY.
- 7. Blumer, K. J., J. E. Reneke und J. Thorner. 1988. The STE2
gene product is the ligand-binding component of the α-factor receptor
of Saccharomyces cerevisiae. J. Biol. Chem. 263: 10836-10842.
- 8. Strnad, J., C. M. Eppler, M. Corbett und J. R. Hadcock. 1993.
The rat SSTR2 somatostatin receptor subtype is coupled to inhibition
of cyclic AMP accumulation. Biochem. Biophys. Res. Comm. 191: 968-976.
- 9. King, K., H. G. Dohlman, J. Thorner, M. G. Caron und R.J.
Lefkowitz. 1990. Control of yeast mating signal transduction by
a mammalian β2-adrenergic receptor and Gs α subunit.
Science 250: 121-123.
- 10. Weiner, J. L., C. Guttierez-Steil und K. J. Blumer. 1993.
Disruption of receptor-G protein coupling in yeast promotes the
function of an SST2-dependent adaptation pathway. J. Biol. Chem.
268: 8070-8077.
-
BEISPIEL 13
-
Die Empfindlichkeit des
Hefe-Biotests wird durch die Überexpression
von STE50 verbessert.
-
Für den Paarungssignaltransduktionsweg
der Hefe wurden mehrere molekulare Adaptionsmechanismen beschrieben
(1). Veränderungen
an einem oder mehreren dieser Mechanismen sollten der Verbesserung der
Empfindlichkeit eines Biotests dienen, und zwar durch Veränderung
von Desensibilisierungswegen und daher Verlängerung des durch Agonistenbindung
an den Rezeptor initiierten Signals. Die Auswirkungen einer sst2-Mutation auf die
Empfindlichkeit des Hefe-Biotests wurden bereits beschrieben (Beispiel
6). Es wurde vorhergesagt, daß eine
als Alternative zur genetischen Modifikation an sst2 vorgesehene Überexpression
des Hefegens STE50 ähnliche
Auswirkungen haben sollte (2), allerdings über einen unterschiedlichen
Wirkmechanismus (2,3). Das STE50-Gen wurde isoliert und unter die
Kontrolle eines starken konstitutiven Promotors in einem Plasmid
mit hoher Kopienzahl gestellt, was zu einer signifikanten Überexpression
des Gens führte.
Es stellte sich heraus, daß auf
eine Reaktion gegenüber
dem Säugerhormon
Somatostatin über
einen exprimierten SSTR2-Somatostatinrezeptor hin manipulierte Hefe
eine robustere Reaktion auf Hormon zeigte, wenn STE50 überexprimiert
wurde.
-
MATERIAL UND
METHODEN
-
Konstruktion
des STE50-Expressionsplasmids. Die Anzucht der Bakterienstämme und
die Plasmidmanipulationen wurden nach Standardverfahren durchgeführt (4).
Die proteincodierenden Sequenzen für STE50 wurden mittels Polymerasekettenreaktion
(PCR) unter Verwendung von durch Untersuchung der veröffentlichten
Sequenz (2) ausgewählten
Oligonukleotiden amplifiziert. Das Sense-Oligonukleotid (5'-GTCGACAAATCAG ATG GAG GAC GGT AAA CAG G-3') enthielt das Translationsstartcodon
(unterstrichen) sowie eine SalI-Restriktionsstelle und das Antisense-Oligonukleotid
(5'-GAGCTCA TTA GAG TCT TCC ACC GGG GG-3') das Translationsstoppcodon
(unterstrichen) sowie eine SacI-Restriktionsstelle. Diese Oligonukleotide wurden
als Primer in einer Standard-PCR zur Amplifikation von STE50 aus
genomischer Saccharomyces cerevisiae-DNA eingesetzt. Das 1100 Basenpaar
große
Amplifikationsprodukt wurde in den Vektor pCR2 (Invitrogen Corp.,
San Diego, CA, USA) kloniert und durch DNA-Sequenzierung bestätigt. Die
STE50-Sequenzen wurden dann auf einem SalI-SacI-Restriktionsfragment
isoliert und in einen pADH-Expressionsvektor (5) kloniert, wodurch
die Expression von STE50 unter die Kontrolle des starken konstitutiven
ADH1-Promotors gestellt wurde. Dieses Plasmid wurde mit pOZ162 bezeichnet.
-
Hefestammkonstruktion.
Die Anzucht und Transformation von Hefestämmen wurde wie bei Rose et
al. (6) beschrieben durchgeführt.
Der SSTR2-Somatostatinrezeptor-Expressionsstamm LY268 (MATa ura3-52 trp1Δ63 his3Δ200 leu2Δ1 ade2-101
lys2-801 gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
pJH2, pLP82) wurde in vorhergehenden Beispielen sowie bei Price
et al. (7) beschrieben. Der Stamm LY268 wurde entweder mit dem STE50-Expressionsplasmid
pOZ162 oder dem pADH-Vektor transformiert. Diese Stämme werden
mit CY560 bzw. CY562 bezeichnet.
-
Biotest.
Der Biotest für
in Hefe exprimierten SSTR2-Somatostatinrezeptor
wurde in vorhergehenden Beispielen sowie bei Price et al. (7) beschrieben.
In Kürze:
Hefestämme
wurden über
Nacht in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil, Tryptophan und Leucin (SCD-ura-trp-leu) angezogen,
zur Entfernung von Glucoseresten gewaschen und über Nacht in 5 ml SC-Galactose
(2%)-ura-trp-leu-Flüssigmedium
angezogen. Geschmolzenes (52 °C)
SC-Galactose (2%)-ura-trp-leu-his-Agarmedium
(30 ml, durch Zugabe von KOH vor dem Autoklavieren auf pH 6,8 eingestellt) wurde
mit 0,06 ml der Übernachtkultur
angeimpft, so daß sich
eine endgültige
Zelldichte von ungefähr
105 Zellen/ml ergab, und in quadratische
(9 × 9
cm) Petrischalen gegossen. Auf die Oberfläche des verfestigten Agars wurden
sterile Filterscheibchen gelegt und mit 10 μl die angegebenen Mengen an
Somatostatin-14 (Bachem Bioscience Inc., Philadelphia, PA, USA)
oder α-Paarungspheromon
(Sigma, St. Louis, MO, USA) enthaltendem sterilem Wasser gesättigt. Die
Platten wurden 3 Tage bei 30 °C
inkubiert.
-
ERGEBNISSE
-
Die
Auswirkung der STE50-Überexpression
auf die Empfindlichkeit des Hefe-Biotests wurde untersucht, indem
sich nur im Niveau der STE50-Expression unterscheidende Stämme verglichen
wurden (26). Es wurden Biotestplatten
hergestellt, die entweder den STE50-Überexpressionsstamm CY560 oder
den Kontrollstamm CY562 enthielten. Die Reaktionen dieser Stämme auf
Somatostatin oder Hefepheromon wurden wie in Material und Methoden
beschrieben untersucht. Beide Stämme
wiesen sehr schwache Reaktionen gegenüber Hefepheromon auf, da das
Gα-wildtyphefegen
GPA1 unterbrochen und durch ein ein chimärisches Gpa1/Gαi2-Protein
exprimierendes Gen funktionell ersetzt worden war (7). Dieses chimärische Gα-Protein kann
mit dem Hefepheromonrezeptor keine effiziente Wechselwirkung eingehen.
Die Reaktion dieser Zellen auf Somatostatin ist jedoch stark (26). Wie vorhergesagt führte die Überexpression
von STE50 zu einer robusteren Reaktion (26a).
Durch diese Daten wird demonstriert, daß die Überexpression von STE50 eine Überempfindlichkeit
gegenüber
Liganden, die über
an den Hefe-Signaltransduktionsweg gekoppelte G-Protein-gekoppelte
Rezeptoren wirken, hervorruft, selbst wenn der Ligand und der Rezeptor
aus einer heterologen Quelle stammen.
-
IN DIESEM BEISPIEL ZITIERTE
LITERATURSTELLEN
-
- 1. Sprague GF, Thorner JW. Pheromone response and signal
transduction during the mating process of Saccharomyces cerevisiae.
In: The molecular and cellular biology of the yeast Saccharomyces.
EW Jones JR Pringle und JR Broach, Hrsg. Cold Spring Harbor Laboratory
Press, 1992.
- 2. Ramezani-Rad M, Xu G, Hollenberg CP 1992. STE50, a novel
gene required for activation of conjugation at an early step in
mating in Saccharomyces cerevisiae. Mol Gen Genet 236:145-154.
- 3. Chan RK, Otte CA 1982. Isolation and genetic analysis of
Saccharomyces cerevisiae mutants supersensitive to G1 arrest by α factor and α factor pheromones.
Mol Cell Biol 2: 11-20.
- 4. Maniatis T, Fritsch EF, Sambrook J. Molecular cloning. Cold
Spring Harbor Laboratory Press, 1982.
- 5. Martin GA, Viskochil D, Bollag G et al. 1990. The GAP-related
domain of the neurofibromatosis type 1 gene product interacts with
ras p21. Cell 63:843-849.
- 6. Rose MD, Winston F, Hieter P. Methods in yeast genetics.
Cold Spring Harbor Laboratory Press, 1990.
- 7. Price LA, Kajkowski EM, Hadcock JA, Ozenberger BA, Pausch
MH 1995. Yeast cell growth in response to agonist-dependent activation
of a mammalian somatostatin receptor. Eingereicht.
-
BEISPIEL 14
-
IDENTIFIZIERUNG VON VERBINDUNGEN
MIT SOMATOSTATINREZEPTOR-AGONISTEN- UND/ODER -ANTAGONISTENEIGENSCHAFTEN
-
Neue
subtypselektive Verbindungen mit Somatostatinagonisteneigenschaften
besitzen ein signifikantes therapeutisches Potential beim Nachweis
und bei der Behandlung verschiedener Krebsarten. Verbindungen mit
Somatostatinagonisteneigenschaften können sich zur Förderung
der Wachstumshormonausschüttung in
landwirtschaftlichen Spezies eignen. Eine erhöhte Wachstumshormonausschüttung kann
zu beachtlichen Verbesserungen der Wachstumsleistung und Fleischqualität führen. Hierzu
wurde ein auf einen Mechanismus auf Hefebasis beruhender Screening-Test
entwickelt, um auf solche Verbindungen zu testen, die wünschenswerte
Somatostatinagonisten- und/oder -antagonisteneigenschaften besitzen.
-
Biotest.
Ein für
den Nachweis von Verbindungen mit Somatostatinagonisten- und/oder
-antagonisteneigenschaften vorgesehener Biotest wurde unter Verwendung
eines den Ratte-SSTR2 funktionell exprimierenden Hefestamms (LY
364 MATa ura3-52 trp1Δ63
his3Δ200
leu2Δ1 ade2-101
lys2-801 gpa1ΔhisG
far1ΔLYS2 FUS1-HIS3
sst2ΔADE2,
pJH2, pLP82) mobilisiert. Der Test wurde unter Verwendung einer
Modifikation eines Standardverfahrens ausgeführt. Dabei wurde LY364 über Nacht
in 2 ml synthetischem komplettem Flüssigmedium mit Glucose (2%)
und ohne Uracil und Tryptophan (SCD-ura-trp-Medium) angezogen, zur Entfernung
von Glucoseresten gewaschen und über
Nacht in 5 ml SC-Galactose
(2%)-ura-trp-Flüssigmedium
angezogen. Geschmolzenes (55 °C)
SC-Galactose (2%)-ura-trp-his-Agarmedium
(150 ml, durch Zugabe von konzentriertem (2 × 104 Zellen/ml)
auf pH 6,8 eingestellt und in quadratischen (500 cm2)
Petrischalen ausplattiert. Für
den Antagonistentest wurde dem geschmolzenen Agar vor dem Gießen Somatostatin
(20 nM S-14) zugesetzt. Auf die Oberfläche des verfestigten Agars
wurden sterile Filterscheibchen gelegt und mit 10 μl die Kandidatenverbindungen
enthaltendem sterilem Wasser gesättigt.
Die Platten wurden 3 Tage bei 30 °C
inkubiert.
-
Ergebnisse.
Mit einem primären
Screening erhaltene aktive Verbindungen wurden erneut getestet,
wobei die Ergebnisse in 27 dargestellt
sind. Dabei zeigt die linke Abbildung die Ergebnisse eines Tests
auf Verbindungen mit Somatostatinagonisteneigenschaften. Vier Verbindungen
zeigten eine von Verbindungen mit Somatostatinagonisteneigenschaften
erwartete beträchtliche
wachstumsfördernde
Aktivität.
Bei den in den vier Positionen unten links vorhandenen Verbindungen
handelt es sich um als Kontrolle aufgetragene unterschiedliche Mengen
an Somatostatin. Die rechte Abbildung zeigt die Ergebnisse eines
Tests auf Verbindungen mit Somatostatinantagonistenaktivität. Im Antagonisten-Biotest wird dem
geschmolzenen Agar vor dem Gießen
Somatostatin zugesetzt. Auf diese Weise wird bei allen Zellen auf
der Platte als Reaktion auf Somatostatin Wachstum induziert. Mit
der Diffusion der aufgetragenen aktiven Verbindungen mit Antagonisteneigenschaften in
das Agarmedium und deren Inkontakttreten mit den Zellen darin wird
die durch Somatostatin induzierte Wachstums reaktion unterbrochen,
wordurch eine klare Zone mit gehemmtem Wachstum entsteht. Mehrere Verbindungen
zeigten nachweisbare wachstumshemmende Eigenschaften.
-
BEISPIEL 15
-
Die
Signalgebungseffizienz als Reaktion auf Somatostatin wird durch
die Fusion von STE2-Sequenzen an den Aminoterminus von SSTR2 reduziert.
-
Die
funktionelle Expression von G-Protein-gekoppelten Rezeptoren im
allgemeinen und des SSTR2 im besonderen auf hohem Niveau war eine
notwendige Voraussetzung für
die Entwicklung eines sinnvollen Biotests. Von King et al. wurde
berichtet, daß der
Austausch der aminoterminalen Domäne des β2-adrenergen Rezeptors
gegen äquivalente
STE2-Sequenz für
eine effiziente Rezeptorexpression in der Hefe notwendig war. Um
diese Hypothese sowie die Auswirkung von STE2-Sequenzen auf die
Expression des Somatostatin-Rezeptors in der Hefe zu testen, wurde
die Ratte-SSTR2-cDNA in den Plasmiden pJH1 und pJH2 unter die Kontrolle
des GAL1-Promotors gestellt. Mit diesen Konstrukten wird die induzierbare Überexpression
von Gal4p, dem Transkriptionsaktivierungsprotein für galactoseinduzierbare
Gene, verliehen, was zu deutlich erhöhten Niveaus an Rezeptorprotein
in Membranrohfraktionen im Vergleich zu einem von einem Plasmid
ohne GAL4-Sequenzen exprimierten Rezeptor führt (Daten nicht gezeigt).
Im SSTR2-Expressionsplasmid pJH1 wurden für die ersten 13 Aminosäuren von
SSTR2 codierende DNA-Sequenzen durch für die ersten 23 Aminosäuren von
STE2 codierende Sequenz ersetzt (11).
Die Ratte-SSTR2-Sequenzen wurden in pJH2 ohne Modifikation der proteincodierenden
Sequenzen eingeführt.
Hefestämme
mit diesen Konstrukten (LY322: MATa ura3-52 trp1Δ63 his3Δ200 leu2Δ1 ade2-101 lys2-801 gpa1ΔhisG far1ΔLYS2 FUS1-HIS3
sst2ΔADE2, pJH1,
pLP82; LY268: MATa ura3-52 trp1Δ63
his3Δ200
ade2-101 lys2-801 gpa1ΔhisG
far1ΔLYS2
FUS1-HIS3 sst2ΔADE2,
pJH2, pLP82) tragen ein Plasmid (pLP82), durch das die Expression
eines chimärischen
Gα-Protein,
das sich aus der vorgeschlagenen aminoterminalen βγ-Wechselwirkungsdomäne von Gpa1p
und einer carboxyterminalen Rezeptorwechselwirkungsdomäne von Ratte-Gαi2 unter
der Kontrolle des GPA1-Promotors zusammensetzt, vermittelt wird.
Es wurde die Stärke
der Reaktion dieser Stämme
auf appliziertes Somatostatin (S-14) gemessen (28).
LY268-Zellen zeigten eine robuste Wachstumsreaktion auf appliziertes
S-14, womit demonstriert wird, daß für die funktionelle Expression
des Ratte-SSTR2 in der Hefe keine STE2-Sequenzen benötigt werden
(28A). Die Wachstumsreaktion von LY268-Zellen war
wesentlich stärker
als die von LY322-Zellen gezeigte (28B).
Der einzige Unterschied zwischen diesen Stämmen besteht im Vorhandensein
von STE2-Sequenzen im in LY322 vorliegenden pJH1. Somit wird durch
den Austausch des Aminoterminus von SSTR2 gegen das äquivalente
STE2-Segment die
Effizienz der Signalgebung als Reaktion auf appliziertes Somatostatin
stark reduziert. Trotz der Beobachtungen von King et al. benötigen in
Hefe exprimierte heterologe G-Protein-gekoppelte Rezeptoren für die funktionelle
Expression keinerlei aminoterminale proteincodierende Sequenzen
von Hefeproteinen.