-
Konjugierte Linolsäure (CLA)
wird in vielen Literaturstellen als eine Mischung mit einer Anzahl
von Vorteilen für
die Gesundheit beschrieben. Vor allem WARF hat viele Patentanmeldungen
auf diese Vorteile hinterlegt.
-
Konjugierte Linolsäure ist
jedoch nicht eine Einzelverbindung, sondern besteht aus einer grossen
Zahl von Isomeren. Diese Isomeren umfassen Isomere, worin die 2
Doppelbindungen verschiedene Positionen im Fettsäuremolekül einnehmen, aber auch Isomere
basierend auf cis/trans-Isomere.
-
Bis jetzt legen alle Referenzen über konjugierte
Linolsäure
nahe, dass die berichteten Effekte auf die Gesundheit auf der Gegenwart
von mindestens einer cis-Doppelbindung
im System beruhen. Vor allem die cis9trans11- und trans10cis12-Isomeren
werden für
die nützlichen
Wirkungen verantwortlich gemacht. Das kann z. B. aus den folgenden
Dokumenten geschlossen werden: WO 99/29317; WO 96/34855, aber auch
aus wissenschaftlichen Publikationen, wie Poultry Science 72 (1993),
S. 1301–1305
oder J Lipid Research 40 (1999), S. 1426-33 oder Lipids 33 (5) 1998,
S. 521–7.
Im Gegensatz dazu zeigt Lipids 34 (3) 1999, S. 235–41, dass trans9trans11-CLA überhaupt
keine biologische Wirkung aufweist.
-
Wir untersuchten, ob diese Wirkungen
wirklich auf den oben genannten Isomeren beruhen oder ob andere
Isomere von CLA zu diesen bekannten Wirkungen beitragen oder neue
Wirkungen entfalten. Diese Studie resultierte im überraschenden
Befund, dass in in-vitro-Versuchen, insbesondere die tt-CLA-Verbindungen (d.
h. konjugierte Linolsäure-Isomere,
worin alle Bindungen trans Doppelbindungen sind) nützliche
Eigenschaften, insbesondere anti-inflammatorische Eigenschaften,
besitzen. Darüber
hinaus fanden wir, dass ein tt-CLA-Isomerengemisch, welches vorwiegend trans9trans11- und trans10trans12-Isomeren
enthält,
die stärkste biologische
Wirkung entfaltet.
-
Unsere Erfindung betrifft deshalb
in erster Linie die Verwendung einer Mischung zur Herstellung eines Nahrungsmittels
oder eines Nahrungsmittelzusatzes, wobei die Mischung 1 bis 100,
vorzugsweise 5 bis 90, am bevorzugtesten 20 bis 85 Gewichts% (basierend
auf der Gesamtmischung) an Isomeren von trans/trans konjugierter
Linolsäure
(=tt-CLA) enthält,
was mit13C-Magnetresonanz gemessen wurde,
und die tt-CLA zur Herstellung eines Nahrungsmittels oder Nahrungsmittelzusatzes
mit antiinflammatorischen Eigenschaften eingesetzt wird.
-
Gemäss einer anderen Ausführungsform
unserer Erfindung können
diese Mischungen auch als Additiv in einem Nahrungsmittel oder als
Nahrungsmittelzusatz eingesetzt werden, vorzugsweise in eingekapselter Form,
um diese Produkte mit antiinflammatorischen Eigenschaften zu versehen.
Gleichzeitig wurde gefunden, dass die Verwendung dieser tt-reichen
CLA- Mischungen in einer Verbesserung der physikalischen Eigenschaften
resultiert, wie verbesserte Härte,
Textur, Festigkeit und besserer Anteil Luft im Produkt (overrun)
von Nahrungsmitteln.
-
Das Gefühl sowie das Zusammenschmelzen
im Munde und die Freigabe von Aromastoffen werden durch die tt-CLA
nicht negativ beeinflusst. Zusätzlich
sind die Produkte leichter zu verarbeiten und weisen bessere Belüftungseigenschaften
auf.
-
Es ist bevorzugt, dass die erfindungsgemässen tt-CLA-Mischungen
einen relativ hohen Gehalt an tt-CLA aufweisen. Deshalb bevorzugen
wir die Verwendung einer Mischung, welche, mit 13C-Magnetresonanztechnik
gemessen, einen Gehalt von 5 bis 90 Gewichts% (der Gesamtmischung)
an tt-CLA-Isomeren aufweist, während
die CLA-Isomeren cis9trans11 und
trans10cis12 in
einem Gewichtsverhältnis
von: (t9t11 + t10t12) : (c9t11 + t10c12) von mehr als 3 : 1, vorzugsweise mehr
als 5 : 1, am bevorzugtesten von mehr als 7.5 : 1, vorliegen.
-
Die 13C-Magnetresonanztechnik
zur Bestimmung der Isomerenverteilung in der CLA ist aus Davis,
A. L. et al Chemistry and physics of Lipids, 97, (1999), S. 155–65 bekannt.
-
Die tt-reichen CLA-Gemische, welche
gemäss
Erfindung eingesetzt werden können,
können
aus freien Fettsäuren,
Mono-, Di- oder Triglyceriden und Alkylestern von CLA ausgewählt werden.
-
Obwohl während der Herstellung von CLA-Isomerengemischen
immer auch tt-CLA
in gewissen (geringen) Mengen produziert wird, wäre es sehr nützlich,
wenn Konzentrate zugänglich
wären,
da diese die Dosierung in Nahrungsmittel erleichtern und insbesondere
die Herstellung von wirksamen Nahrungsmittelzusätzen ermöglichen würden. Deshalb haben wir auch
untersucht, ob wir Konzentrate von tt-CLA erhalten könnten. Diese Untersuchungen
führten
zu einer weiteren Ausführungsform
unserer Erfindung, nämlich
zu Mischungen mit antiinflammatorischen Eigenschaften, welche CLA-Isomere
enthalten, wobei die Mischung mehr als 10 Gewichts%, vorzugsweise
mehr als 25 Gewichts%, ganz besonders bevorzugt mehr als 50 Gewichts%
CLA-Isomere enthält,
von denen wiederum mehr als 55, vorzugsweise mehr als 60, besonders
bevorzugt mehr als 65 Gewichts% (der Gesamt-CLA-Isomeren) tt-CLA-Isomeren
sind, was mit 13C-Magnetresonanztechnik gemessen wurde.
-
Bevorzugte Mischungen, die wir erhalten
haben, sind solche, in denen die tt-CLA-Isomeren t9t11 und t10t12 in einem Gewichtsverhältnis von t9t11 : t10t12 von weniger als 2.3 : 1, vorzugsweise
weniger als 1.8 : 1, am meisten bevorzugt weniger als 1.0 : 1 vorliegen
(mit13C-Magnetresonanztechnik gemessen).
-
Andere bevorzugte Mischungen enthalten
zusätzlich
zu den tt-Isomeren c9t11-
und t10c12-CLA-Isomere in
einem Gewichtsverhältnis
von (total t9t11 +
t10t12) : (c9t11 + t10c12) von mehr als 3 : 1, vorzugsweise mehr
als 5 : 1, am meisten bevorzugt mehr als 7.5 : 1, was mit13C-Magentresonanztechnik gemessen wurde.
-
Die tt-CLA-Mischung gemäss der Erfindung
kann geeigneterweise in Nahrungsmitteln verwendet werden. Obwohl
die tt-CLA-Mischungen in jeder Form vorliegen könnten (d. h. freie Säure/Glyceride/Alkylester
mit Alkylgruppen mit 2–20,
vorzugsweise 2–8,
Kohlenstoffatomen), bevorzugen wir die Verwendung dieser Mischungen
als Glyceride, da auf diese Weise die besten Eigenschaften des Nahrungsmittels
bezüglich
dem Gefühl
im Munde erreicht werden können.
-
Teil unserer Erfindung sind deshalb
auch Nahrungsmittel, vorzugsweise ausgewählt aus Konditoreiwaren, Brotaufstrichen,
Saucen, Salatsaucen, Mayonnaise, Käse, Speiseeis, Teig, Backwaren,
Füllungen
und Cremen, enthaltend eine wirksame Menge einer Mischung mit 1
bis 100 Gewichts% tt-CLA, vorzugsweise in Form eines Mono- und/oder
Di- und/oder Tri-glycerids. Am meisten bevorzugt sind Nahrungsmittel,
welche eine wirksame Menge an bevorzugter CLA-Mischung, wie oben
definiert, enthalten. Eine wirksame Menge wird als die Menge definiert,
welche der empfohlenen täglichen
Menge entspricht, die mit 1–5
Mahlzeiten pro Tag erreicht wird.
-
Eine sehr zweckmässige Methode, einem Benutzer
eine wirksame Menge unserer tt-CLA
zu verabreichen, besteht darin, unserem Benutzer Nahrungsmittelzusätze bereitzustellen,
welche eine wirksame Dosis an tt-CLA enthalten. Ebenfalls Teil unserer
Erfindung sind deshalb Nahrungsmittelzusätze, in denen die tt-reiche CLA
in einem in Nahrungsmittel zugelassenen Mittel zur Einkapselung,
wie Zucker, Lactose Stärke,
modifizierte Stärke,
Gelatine, Cyclodextrin, Proteine und Cellulose, eingekapselt ist
-
Die Nahrungsmittelzusätze können auch
mit anderen Nahrungsmittelbestandteilen verstärkt werden. Diese Bestandteile
können
ausgewählt
werden aus den Vitaminen A, B, C, D, E und K, Mineralien, wie Kalzium,
Kalium, Magnesium, Eisen, Kupfer, Zink, Selen und Anti-oxidantien,
wie Tocopherole und Polyphenole.
-
Die tt-reiche CLA-Isomeren-Mischung
kann nach einem Verfahren hergestellt werden, gemäss welchem
-
- i) eine Mischung mit einem Gesamtgehalt an
unkonjugiertem C 18 : 2 von mehr als 55 Gewichts% durch eine Behandlung
mit einem Schwefel-Nickel-Katalysator
bei einer Temperatur von 100 bis 180°C in Abwesenheit von Wasserstoff
konjugiert und isomerisiert wird,
- ii) das in Schritt i) gebildete Produkt einer Lösungsmittel-Fraktionierung
mit Aceton in einem Gewichtsverhältnis
von Aceton zu CLA-Produkt von 10 : 1 bis 1 : 1 bei einer Temperatur
von –25
bis –100°C unterworfen wird,
worauf eine Stearin-(oder Kopf)-Fraktion als erfindungsgemässes Produkt
isoliert wird.
-
Ein Alternativverfahren zur Herstellung
dieser Mischungen besteht in der Anreicherung eines Gemisches verschiedener
Isomeren von konjugierter Linolsäure
in den tt-CLA-Isomeren, wobei ein Gemisch enthaltend mindestens
1 Gewichts% tt-CLA
in Beimischung mit anderen CLA-Isomeren einer enzymatischen Umwandlung
unterworfen wird, welche ausgewählt
ist aus i) partieller Hydrolyse eines Glycerid-Gemisches oder eines Gemisches von Estern
mit kurzkettigen Alkoholen, ii) partieller Veresterung eines Gemisches
von freien Fettsäuren
mit Glycerol oder einem Glycerid, iii) partieller Glycerolyse eines
Glyceridgemisches und iv) partieller Veresterung eines Alkohols
mit einem freien CLA-Isomeren, wobei ein Enzym verwendet wird, welches tt-CLA
von anderen CLA-Isomeren unterscheiden kann, und danach das Reaktionsprodukt
mit physikalischen Methoden abgetrennt wird, wobei eine Fraktion
als Reaktionsprodukt abgetrennt wird, welche mit tt-CLA angereichert
ist.
-
Enzyme, welche im obigen Verfahren
eingesetzt werden können,
sind Lipase von Candida rugosa, Lipase CL, Lipase SL, Lipase OF
und Lipase von Geotrichum candidum B, Lipozym IM, Lipozym M.
-
EXPERIMENTELLER
TEIL
-
Die anti-inflammatorischen Eigenschaften
wurden in in vitro-Tests bestimmt, in denen die Produktion von Prostaglandin
E2 (=PGE2) durch menschliche Haut-Fibroblasten, Endothel-Zellen
von Blutgefässen
(HUVECS=Human Umbilicial Vein Endothelial Cells) und Blut nach Stimulation
mit dem Entzündungsauslöser PMA
gemessen wird. Eine Reduktion des PGE2-Spiegels zeigt eine anti-inflammatorische
Wirkung an.
-
Primäre menschliche Vorhaut-Fibroblasten
in Passage 2 (P2) wurden auf Kulturplatten mit 96 Vertiefungen mit
10000 Zellen/Vertiefung angeimpft und 24 Stunden in einer Atmosphäre von 5%
Kohlendioxid in Dulbeccos Modified Eagles Medium (DMEM), welchem
10% foetales Kälberserum
zugesetzt worden ist, kultiviert. Angereicherte tt-CLA (enthaltend
84 Gewichts% tt-CLA in einem Verhältnis von (t9t11 + t10t12) : (c9t11 + t10c12) von 15 wurde auf 3 Kulturplatten zu frischem
Zellmedium in Ethanol gegeben (Endkonzentration 1%) und für weitere
24 Stunden inkubiert. Phorbal-myristat-acetat (PMA, Sigma) in Ethanol/Zellmedium
wurde zum Medium (Endkonzentration 10 nm) gegeben, und die Zellen
weitere 24 Stunden inkubiert. PMA ist ein externer Stressfaktor,
welcher in den Zellen oxidativen Stress und Entzündungsreaktionen induziert.
Das Medium wurde dann sofort wie unten beschrieben analysiert.
-
Prostaglandin-E2-Versuch (PGE2) Volumina
von 50 μl
Kulturmedium wurden für
den PGE2-Versuch entnommen, nachdem die Kulturplatte leicht geschüttelt worden
ist. Der Gehalt an PGE2 im Medium wurde mit einem Biotrak- PGE2-Immunoassay- Kit (Amersham, UK)
bestimmt. Der Assay beruht auf dem Wettbewerb zwischen unmarkiertem
PGE2 in der Probe und einer bestimmten Menge von mit Meerrettichperoxidase
markiertem PGE2 für
eine beschränkte
Menge an fixiertem PGE2-spezifischem Antikörper. Konzentrationen von unmarkierten
PGE2- Proben wurden nach einer Standardkurve bestimmt, welche gleichzeitig
erhalten wurde.
-
Resultate:
-
Die untenstehende Graphik (1) zeigt, dass Behandeln
von Zellen mit einem Entzündungsauslöser, wie
PMA (Phorbol-myristyl-acetat), eine Zunahme der Entzündungsreaktion
verursacht, was über
die Produktion von Prostaglandin E2 (PGE2) gemessen wurde. tt-CLA
reduziert sogar bei einem Gehalt von 10 ng/ml die Entzündungsreaktion
drastisch, was über
die PGE2-Produktion gemessen wurde (1).
-gute
anti-inflammatorische Aktivität.
-
Beispiel 1
-
10g Sonnenblumenöl wurden mit 1 g mit Schwefel
vergiftetem Nickel-Hydrierkatalysator
vermischt. Das Gemisch wurde unter einer Stickstoffdecke in einem
Glasgefäss
mit magnetischem Rührer
bei 180°C
gerührt.
-
Nach 6 Stunden wurde eine Probe entnommen,
mit einem geeigneten Lösungsmittel
extrahiert und filtriert. Die Fettsäuremischung des Triglycerids
enthielt 45% konjugierte Linolsäure
(CLA), von der 50% tt-CLA war, was mit FAME GC bestimmt wurde. Die
Hauptisomeren der tt-CLA waren gemäss Bestimmung mit 13C-NMR
trans9trans11 und
trans10trans12,
welche zusammen 60% der gesamten tt-CLA ausmachten.
-
Beispiel 2
-
Konjugierte Linolsäure wurde
wie in Beispiel 1 beschrieben hergestellt. Ein angereichertes Produkt wurde
nach dem nachstehenden Verfahren hergestellt. 5g CLA wurden unter
Rühren
zu 30g Aceton in einem Glasgefäss
gegeben, und die Temperatur langsam auf –58°C gekühlt. Die Stearin-Fraktion wurde
unter Vakuum abfiltriert und mit vorgekühltem Aceton gewaschen. Die
Fettsäure-Mischung
enthielt gemäss 13C-NMR 33% CLA, von denen 86.6% tt-CLA waren.
Die Hauptisomeren der tt-CLA waren gemäss 13C-NMR trans9trans11 und trans10trans12, welche
zusammen 67% der gesamten tt-CLA ausmachten. Dieses Produkt wurde
im obigen Test auf anti-inflammatorische Eigenschaften eingesetzt.
-
Beispiel 3
-
Konjugierte Linolsäure wurde
durch Isomerisation mit Alkali wie vorher beschrieben hergestellt,
WO 9718320, und lieferte ein Produkt, welches 80% CLA enthielt.
Die zwei Hauptisomeren wurden mit FAME GC als cis9trans11- und trans10cis12-Isomere bestimmt, welche zusammen 95%
der gesamten tt-CLA ausmachten.
-
20g dieses Materials wurden für 4 Stunden
unter einer Stickstoffdecke auf 250°C erhitzt. Die Fettsäuremischung
wurde mittels FAME GC bestimmt und enthielt 67% CLA, von denen 30%
tt-CLA waren.
-
Beispiel 5
-
Konjugierte Linolsäure wurde
wie in Beispiel 1 beschrieben hergestellt. Ein angereichertes Produkt wurde
hergestellt, indem 2g dieser CLA zu 2g Wasser und 3'000 LU von Lipase
B von Geotrichum candidum gegeben wurden. Das Gemisch wurde unter
Rühren
bei 35°C
gehalten. Die Fettsäuremischung
der Glyceride wurde mit FAME GC bestimmt und enthielt 50 Gewichts%
CLA, von denen 57% tt-CLA waren. Definitionen
von in den Beispielen 6 und 7 verwendeten Produkten
| InES: | Untereinander
verestertes Palmöl-Stearin-/Palmkern-Stearin-Fett |
| Pof
IV65: | Palm-Olein-Fraktion
mit einem Jod-Wert von 65 |
| SF: | Sonnenblumenöl |
| tt-CLA: | tt-CLA-enthaltendes
Oel |
| CN: | Kokosnussöl |
-
Beispiel 6 Herstellung
von Margarine
-
a) Formulierung
-
Wässrige Phase
| Wasser | 18.48% |
| Kaliumsorbat | 0.15 |
| Zitronensäure | 0.07 |
| SMP | 1.0 |
-
-
b) Verfahrensbedingungen
-
Die Verfahrenslinie wurde konfiguriert
als:
Vormischen – Pumpen – A1-Einheit – C1-Einheit – A2-Einheit
-
Die Temperatur für das Vormischen betrug 60°C und die
Rührgeschwindigkeit
60 Umdrehungen pro Minute. Alle Einheiten wurden auf 15°C eingestellt
, und die Rührgeschwindigkeit
betrug 1000 Umdrehungen pro Minute. Der Durchlauf betrug 50 g/Min.
bei Verwendung einer Pumpe mit gleichbleibender Pumpgeschwindigkeit.
-
Für
alle Produkte wurde durch langsame Zugabe der hergestellten wässrigen
Phase zur Oelphase in einem Vormisch-Tank eine grobe Vormischung
hergestellt. Ein 2kg-Batch
wurde eingesetzt.
-
Vor dem Pumpen wurde das Gemisch
15 Minuten gerührt.
Nach dem Pumpen liess man die Linie 15 Minuten laufen bevor ein
Produkt gesammelt wurde.
-
Die folgenden Verfahrensparameter
wurden bestimmt:
-
-
Alle Gefässe wurden bei 5°C gelagert.
Nach einem Tag wurde von jedem ein Gefäss bei 5°C, 10°C, 15°C und 20°C gelagert und nach einer Woche
evaluiert.
-
Alle Proben liessen sich ohne sichtbaren
Wasserverlust leicht streichen. Alle Produkte waren von ausgezeichneter
Qualität
und ergaben sehr gute Werte für
Härte (C-Wert),
Kragen (Collar) und Leitfähigkeit
bei allen Lagertemperaturen.
-
-
-
-
-
Beispiel 7 Herstellung
von Speiseeis
-
Tabelle
1: Rezept
Das folgende Rezept wurde angewendet (Vgl. Tabelle
1)
-
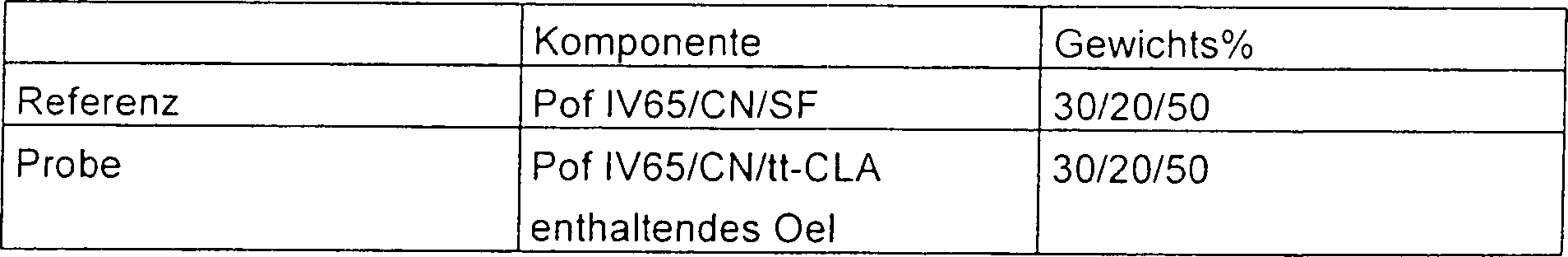
Die verwendeten Fettgemische sind
in Tabelle 2 beschrieben.
-
-
Der Zucker, das Milchpulver und die
Dextrose wurden gemischt und zum Wasser gegeben. Das Gemisch wurde
auf 70°C
erhitzt, und der klare Sirup zugegeben. Dann wurde das Fettgemisch
und der Emulgator zugegeben. Die Emulsion wurde mit einem Ultra-Turrax
gerührt,
auf 20°C
abgekühlt
und dann wieder mit dem Ultra-Turrax gerührt. Die Emulsion wurde über Nacht
im Kühlschrank
bei 7°C
gelassen. Die Maschine zur Herstellung von Speiseeis wurde für 24 Stunden
bei –28°C gehalten.
Die Emulsion wurde danach in der Maschine während 40 Minuten bis zum Erreichen
der tiefsten Temperatur gerührt.
Das erhaltene Speiseeis wurde für mindestens
3 Tage bei –18°C gelagert
und dann evaluiert.
-
Aus Tabelle 3 kann ersehen werden,
dass die erfindungsgemässen
Produkte eine bessere Härte
und einen höheren
Anteil Luft im Produkt (overrun) aufweisen.
-
-
Geschmackstest
-
Sieben Testpersonen haben die Festigkeit
der Probe im Vergleich zu einem Referenzmuster getestet. Für fünf dieser
sieben Testpersonen hatte die Probe mit der tt-CLA eine höhere Festigkeit
-
1.
Referenz mit SF – tt-CLA