DE10342828A1 - Hochreines, pyrogen hergestelltes Siliciumdioxid - Google Patents
Hochreines, pyrogen hergestelltes Siliciumdioxid Download PDFInfo
- Publication number
- DE10342828A1 DE10342828A1 DE10342828A DE10342828A DE10342828A1 DE 10342828 A1 DE10342828 A1 DE 10342828A1 DE 10342828 A DE10342828 A DE 10342828A DE 10342828 A DE10342828 A DE 10342828A DE 10342828 A1 DE10342828 A1 DE 10342828A1
- Authority
- DE
- Germany
- Prior art keywords
- silica
- high purity
- silicon tetrachloride
- purity
- metals
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B33/00—Silicon; Compounds thereof
- C01B33/113—Silicon oxides; Hydrates thereof
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B33/00—Silicon; Compounds thereof
- C01B33/113—Silicon oxides; Hydrates thereof
- C01B33/12—Silica; Hydrates thereof, e.g. lepidoic silicic acid
- C01B33/18—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof
- C01B33/181—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof by a dry process
- C01B33/183—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof by a dry process by oxidation or hydrolysis in the vapour phase of silicon compounds such as halides, trichlorosilane, monosilane
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03B—MANUFACTURE, SHAPING, OR SUPPLEMENTARY PROCESSES
- C03B19/00—Other methods of shaping glass
- C03B19/12—Other methods of shaping glass by liquid-phase reaction processes
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C1/00—Ingredients generally applicable to manufacture of glasses, glazes, or vitreous enamels
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C1/00—Ingredients generally applicable to manufacture of glasses, glazes, or vitreous enamels
- C03C1/02—Pretreated ingredients
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03B—MANUFACTURE, SHAPING, OR SUPPLEMENTARY PROCESSES
- C03B2201/00—Type of glass produced
- C03B2201/02—Pure silica glass, e.g. pure fused quartz
- C03B2201/03—Impurity concentration specified
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P40/00—Technologies relating to the processing of minerals
- Y02P40/50—Glass production, e.g. reusing waste heat during processing or shaping
- Y02P40/57—Improving the yield, e-g- reduction of reject rates
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Geochemistry & Mineralogy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Chemistry (AREA)
- Glass Compositions (AREA)
- Silicon Compounds (AREA)
- Glass Melting And Manufacturing (AREA)
Abstract
Hochreines, pyrogen hergestelltes Siliciumdioxid mit Metallgehalten von kleiner 0,2 mug/g wird hergestellt, indem man ein Siliciumtetrachlorid mit Metallgehalten kleiner 30 ppb mittels Flammenhydrolyse umsetzt. DOLLAR A Das Siliziumdioxid kann zur Herstellung von hochreinen Gläsern mittels des Sol-Gel-Verfahrens eingesetzt werden.
Description
- Die Erfindung betrifft ein hochreines, pyrogen hergestelltes Siliciumdioxid, ein Verfahren zu seiner Herstellung sowie seine Verwendung.
- Kieselglas kann vorteilhaft für viele Einsatzzwecke, wie Crucibles, Boards und Quarzröhren zur Herstellung von Halbleitern eingesetzt werden, seitdem es möglich ist, dieses Kieselglas in hoher Reinheit herzustellen.
- Weiterhin wird das Siliciumdioxidglas für die Glasgeräte in der Chemie oder für die Photozelle verwendet. Es kann zur Herstellung von Lichtleitfasern verwendet werden.
- Es ist bekannt Siliciumdioxidglas zum Beispiel in Form eines Monolithen herzustellen, indem man Siliciumalkoxid hydrolysiert, pyrogene Kieselsäure zu der hydrolysierten Lösung hinzugibt, die Mischung zu einem Gel gellieren läßt, das Gel trocknet und das erhaltene trockne Gel sintert (
US 4,681,615 ,US 4,801,318 ). - Bei dem bekannten Verfahren können bekannte pyrogen hergestellte Siliciumdioxide eingesetzt werden.
- Die bekannten pyrogenen Kieselsäuren weisen den Nachteil auf, daß sie für die besonders hohen Ansprüche an die Reinheit des Glases noch zu viele Fremdelemente enthalten.
- Gegenstand der Erfindung ist ein hochreines, pyrogen hergestelltes Siliciumdioxid, welches gekennzeichnet ist durch einen Gehalt an Metallen von kleiner 9 ppm.
-
- Der Gesamtmetallgehalt kann dann 3252 ppb (~ 3,2 ppm) oder kleiner betragen.
-
- Der Gesamtmetallgehalt kann dann 1033 ppb (~ 1,03 ppm) oder kleiner betragen.
- Ein weiterer Gegenstand der Erfindung ist ein Verfahren zur Herstellung des hochreinen, pyrogen hergestellten Siliciumdioxides, welches dadurch gekennzeichnet ist, daß man Siliciumtetrachlorid auf bekannte Weise mittels Hochtemperaturhydrolyse zu Siliciumdioxid in der Flamme umsetzt und dabei ein Siliciumtetrachlorid verwendet, welches einen Metallgehalt von kleiner 30 ppb aufweist.
-
- Siliciumtetrachlorid mit diesem niedrigen Metallgehalt kann gemäß
DE 100 30 251 oder gemäßDE 100 30 252 hergestellt werden. - Das prinzipielle Verfahren zur Herstellung von pyrogenem Siliciumdioxid, ausgehend von Siliciumtetrachlorid, das im Gemisch mit Wasserstoff und Sauerstoff umgesetzt wird, ist bekannt aus Ullmanns Enzyklopädie der technischen Chemie, 4. Auflage, Band 21, Seite 464 ff. (1982).
- Metallgehalt des erfindungsgemäßen Siliciumdioxides liegt im ppm-Bereich und darunter (ppb-Bereich).
- Das erfindungsgemäße pyrogen hergestellte Siliciumdioxid kann bei den verschiedensten Glasherstellungsmethoden, wie zum Beispiel dem Sol-Gel-Verfahren eingesetzt werden. Derartige Sol-Gel-Verfahren sind bekannt aus
US 4,681,615 oderUS 4,801,318 . - Das erfindungsgemäße pyrogen hergestellte Siliciumdioxid eignet sich vorteilhaft zur Herstellung von Spezialgläsern mit hervorragenden optischen Eigenschaften.
- Die mittels dem erfindungsgemäßen Siliciumdioxid hergestellten Gläser weisen eine besonders geringe Adsorption im tiefen UV-Bereich auf.
- Beispiel 1 (Vergleichsbeispiel)
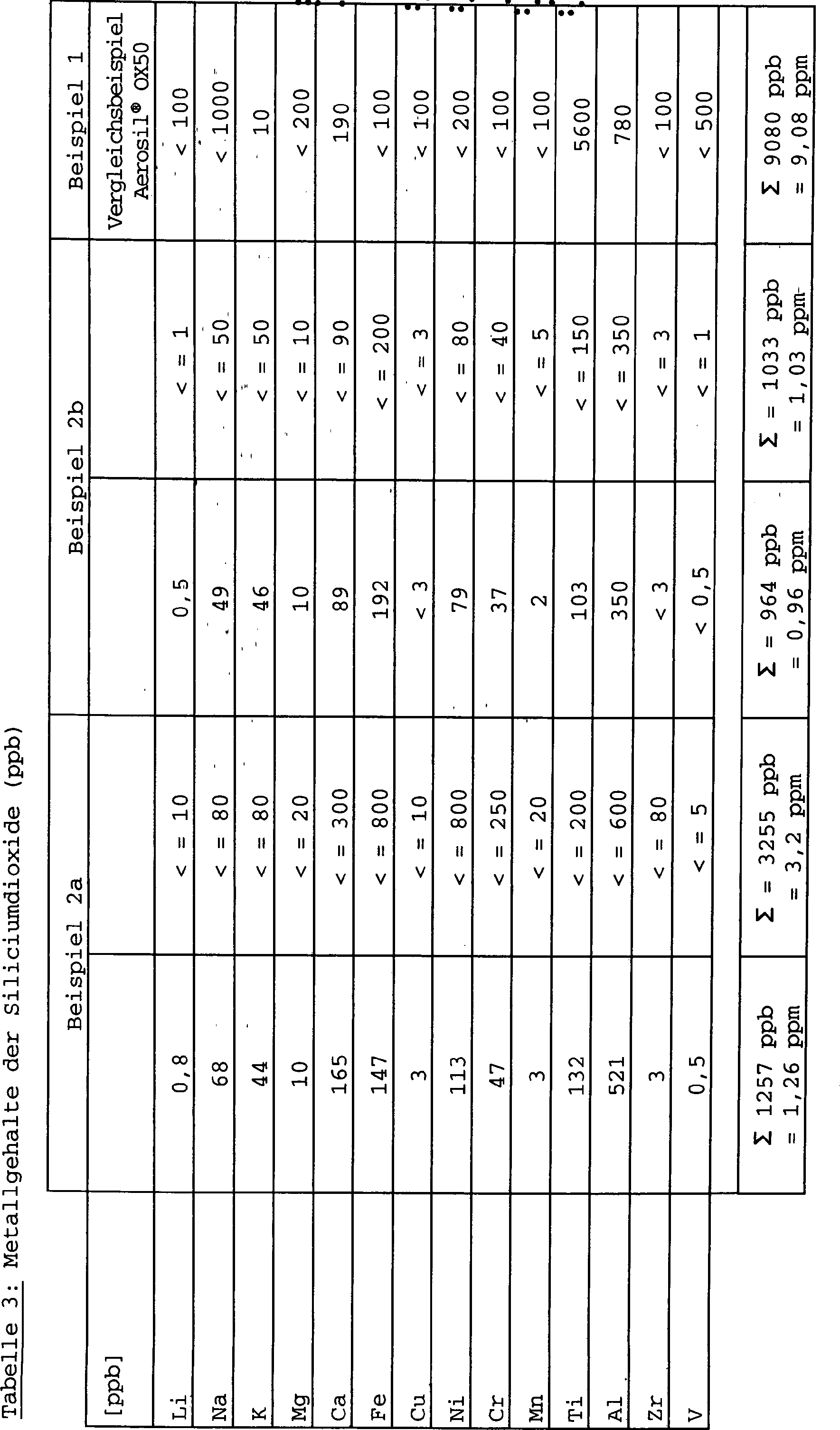
- 500 kg/h SiCl4 einer Zusammensetzung gemäß Tabelle 1 werden bei ca. 90 °C verdampft und in das Zentralrohr eines Brenners bekannter Bauart überführt. In dieses Rohr werden zusätzlich 190 Nm3/h Wasserstoff sowie 326 Nm3/h Luft mit einem Sauerstoffanteil von 35 Vol% gegeben. Dieses Gasgemisch wird entzündet und brennt im Flammrohr des wassergekühlten Brenners. In eine die Zentraldüse umgebende Manteldüse werden zur Vermeidung von Anbackungen zusätzlich 15 Nm3/h Wasserstoff gegeben. In das Flammrohr wird außerdem zusätzlich 250 Nm3/h Luft normaler Zusammensetzung gegeben. Nach der Abkühlung der Reaktionsgase wird das pyrogene Siliciumdioxidpulver von den salzsäurehaltigen Gasen mittels eines Filters und/oder eines Zyklons abgetrennt. In einer Entsäuerungseinheit wird das pyrogene Siliciumdioxidpulver mit Wasserdampf und Luft behandelt, um es von anhaftender Salzsäure zu befreien. Die Metallgehalte sind in der Tabelle 3 wiedergegeben.
- Beispiel 2 (Ausführungsbeispiel)
- 500 kg/h SiCl4 einer Zusammensetzung gemäß Tabelle 2 werden bei ca. 90 °C verdampft und in das Zentralrohr eines Brenners bekannter Bauart überführt. In dieses Rohr werden zusätzlich 190 Nm3/h Wasserstoff sowie 326 Nm3/h Luft mit einem Sauerstoffanteil von 35 Vol% gegeben. Dieses Gasgemisch wird entzündet und brennt im Flammrohr des wassergekühlten Brenners. In eine die Zentraldüse umgebende Manteldüse werden zur Vermeidung von Anbackungen zusätzlich 15 Nm3/h Wasserstoff gegeben. In das Flammrohr wird außerdem zusätzlich 250 Nm3/h Luft normaler Zusammensetzung gegeben. Nach der Abkühlung der Reaktionsgase wird das pyrogene Siliciumdioxidpulver von den salzsäurehaltigen Gasen mittels eines Filters und/oder eines Zyklons abgetrennt. In einer Entsäuerungseinheit wird das pyrogene Siliciumdioxidpulver mit Wasserdampf und Luft behandelt, um es von anhaftender Salzsäure zu befreien.
- Die Metallgehalte sind in der Tabelle 3 wiedergegeben.
- Meßmethode
- Die erhaltenen pyrogen hergestellten Siliciumdioxide werden in Bezug auf ihren Metallgehalt analysiert. Die Proben werden in einer Säurelösung, die hauptsächlich aus HF besteht, gelöst.
- Das SiO2 reagiert mit dem HF und bildet SiF4 + H2O. Das SiF4 verdampft und läßt die zu bestimmenden Metalle vollständig in der Säure zurück. Die einzelnen Proben werden mit destilliertem Wasser verdünnt und mittels der Perkin Elmer Optima 3000 DV Inductively Coupled Plasma-Atomic Emission Spectroscopy (ICP-AES) gegen einen internen Standard analysiert. Die Ungenauigkeit der Werte rührt von Proben-Affekten, Spektral Interferencen und der Begrenztheit der Meßmethode her. Größere Elemente haben eine relative Ungenauigkeit von ± 5 %, während die kleineren Elemente eine relative Ungenauigkeit von ± 15 % aufweisen.
Claims (6)
- Hochreines, pyrogen hergestelltes Siliciumdioxid, gekennzeichnet durch einen Gehalt an Metallen von kleiner 9 ppm.
- Verfahren zur Herstellung des hochreinen, pyrogen hergestellten Siliciumdioxides gemäß den Ansprüchen 1 oder 2, dadurch gekennzeichnet, daß man Siliciumtetrachlorid auf bekannte Weise mittels Hochtemperaturhydrolyse zu Siliciumdioxid in der Flamme umsetzt und dabei ein Siliciumtetrachlorid verwendet, welches einen Metallgehalt von kleiner 30 ppb aufweist.
- Verfahren zur Herstellung des hochreinen, pyrogen hergestellten Siliciumdioxides gemäß Anspruch 3, dadurch gekennzeichnet, daß man Siliciumtetrachlorid auf bekannter Waise mittels Hochtemperaturhydrolyse zu Siliciumdioxid in der Flamme umsetzt und dabei ein Siliciumtetrachlorid verwendet, welches neben Siliciumtetrachlorid den folgenden Gehalt an Metallen aufweist:
- Verwendung des hochreinen, pyrogen hergestellten Siliciumdioxides gemäß Anspruch 1 zur Herstellung von Gläsern.
- Verwendung des hochreinen, pyrogen hergestellten Siliciumdioxides gemäß Anspruch 5 zur Herstellung von Gläsern mittels dem Sol-Gel-Verfahren.
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10342828A DE10342828A1 (de) | 2003-09-17 | 2003-09-17 | Hochreines, pyrogen hergestelltes Siliciumdioxid |
| PCT/EP2004/010335 WO2005026068A2 (en) | 2003-09-17 | 2004-09-16 | High-purity pyrogenically prepared silicon dioxide |
| CNA2004800268452A CN1863733A (zh) | 2003-09-17 | 2004-09-16 | 高纯度的热解制备的二氧化硅 |
| KR1020067005468A KR100789124B1 (ko) | 2003-09-17 | 2004-09-16 | 발열 제조된 고순도 이산화규소, 이의 제조방법 및 이를 이용하여 수득한 실리카 유리 및 성형품 |
| EP04786950A EP1663888A2 (de) | 2003-09-17 | 2004-09-16 | Hochreines pyrogen hergestelltes siliciumdioxid |
| JP2006526581A JP4903045B2 (ja) | 2003-09-17 | 2004-09-16 | 熱分解により製造された高純度の二酸化ケイ素 |
| US10/571,332 US20070003770A1 (en) | 2003-09-17 | 2004-09-16 | High-purity pyrogenically prepared silicon dioxide |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10342828A DE10342828A1 (de) | 2003-09-17 | 2003-09-17 | Hochreines, pyrogen hergestelltes Siliciumdioxid |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE10342828A1 true DE10342828A1 (de) | 2005-04-14 |
Family
ID=34305816
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE10342828A Withdrawn DE10342828A1 (de) | 2003-09-17 | 2003-09-17 | Hochreines, pyrogen hergestelltes Siliciumdioxid |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20070003770A1 (de) |
| EP (1) | EP1663888A2 (de) |
| JP (1) | JP4903045B2 (de) |
| KR (1) | KR100789124B1 (de) |
| CN (1) | CN1863733A (de) |
| DE (1) | DE10342828A1 (de) |
| WO (1) | WO2005026068A2 (de) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1700831A1 (de) | 2005-03-09 | 2006-09-13 | Novara Technology S.R.L. | Verfahren zur Herstellung von Monolithen durch ein Sol-Gel Verfahren |
| EP1700830A1 (de) | 2005-03-09 | 2006-09-13 | Novara Technology S.R.L. | Prozess für die Herstellung von Monolithen mittels eines Sol-Gel Prozesses |
| EP1700829A1 (de) | 2005-03-09 | 2006-09-13 | Degussa AG | Verfahren zum Herstellen eines Glasmonolithes mittels eines Sol-Gel-Verfahrens |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2028228B1 (de) | 2004-10-25 | 2018-12-12 | IGM Group B.V. | Funktionalisierte Nanopartikel |
| EP1700824A1 (de) * | 2005-03-09 | 2006-09-13 | Degussa AG | Granulate basierend auf pyrogen hergestelles silicon dioxid, sowie Verfahren zu deren Herstellung und Verwendung dergleichen |
| EP1717202A1 (de) * | 2005-04-29 | 2006-11-02 | Degussa AG | Sinterwerkstoffe aus Siliciumdioxid |
| CN102167334A (zh) * | 2011-03-18 | 2011-08-31 | 中国恩菲工程技术有限公司 | 多晶硅副产物四氯化硅处理方法 |
| JP5737265B2 (ja) * | 2012-10-23 | 2015-06-17 | 信越化学工業株式会社 | 珪素酸化物及びその製造方法、負極、ならびにリチウムイオン二次電池及び電気化学キャパシタ |
| JP6355729B2 (ja) * | 2013-07-11 | 2018-07-11 | エボニック デグサ ゲーエムベーハーEvonik Degussa GmbH | 可変の粘度を有するケイ酸の製造方法 |
| CN104568535A (zh) * | 2013-10-29 | 2015-04-29 | 中芯国际集成电路制造(上海)有限公司 | Vpd样品收集方法 |
| FR3097802B1 (fr) | 2019-06-27 | 2021-07-02 | Qwarzo | Machine et procede pour la production de touillettes ou de batonnets de melange pour boissons |
| CN110790489A (zh) * | 2019-11-28 | 2020-02-14 | 福建工程学院 | 一种低维材料掺杂的无水解凝胶玻璃的制备方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4681615A (en) * | 1982-12-23 | 1987-07-21 | Seiko Epson Kabushiki Kaisha | Silica glass formation process |
| DE3703079A1 (de) * | 1987-02-03 | 1988-08-11 | Rolf Dipl Chem Dr Rer Bruening | Verfahren zur herstellung von wasserfreiem synthetischem siliciumdioxid |
| DE10211958A1 (de) * | 2002-03-18 | 2003-10-16 | Wacker Chemie Gmbh | Hochreines Silica-Pulver, Verfahren und Vorrichtung zu seiner Herstellung |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2898391A (en) * | 1953-12-15 | 1959-08-04 | Degussa | Natural rubber composition containing a pyrogenically formed mixture of silica and another metal oxide and process of preparation |
| US3391997A (en) * | 1964-12-21 | 1968-07-09 | Cabot Corp | Pyrogenic silica production |
| US4282196A (en) * | 1979-10-12 | 1981-08-04 | Bell Telephone Laboratories, Incorporated | Method of preparing optical fibers of silica |
| US4372834A (en) * | 1981-06-19 | 1983-02-08 | Bell Telephone Laboratories, Incorporated | Purification process for compounds useful in optical fiber manufacture |
| CS223494B1 (cs) * | 1982-02-09 | 1983-10-28 | Jaromir Plesek | Způsob čištění kovalentníeh anorganických halogenidů pro optická vlakna |
| US4961767A (en) * | 1987-05-20 | 1990-10-09 | Corning Incorporated | Method for producing ultra-high purity, optical quality, glass articles |
| US4789389A (en) * | 1987-05-20 | 1988-12-06 | Corning Glass Works | Method for producing ultra-high purity, optical quality, glass articles |
| US5165907A (en) * | 1988-04-14 | 1992-11-24 | Imcera Group Inc. | Method of production of high purity silica and ammonium fluoride |
| DD298493A5 (de) * | 1989-01-02 | 1992-02-27 | Chemiewerk Bad Koestritz Gmbh,De | Verfahren zur herstellung von kieselsaeure hnher reinheit |
| JPH0717370B2 (ja) * | 1989-11-30 | 1995-03-01 | イー・アイ・デュポン・ドゥ・メムール・アンド・カンパニー | 高純度ケイ酸水溶液の製造方法 |
| US5063179A (en) * | 1990-03-02 | 1991-11-05 | Cabot Corporation | Process for making non-porous micron-sized high purity silica |
| JPH0431334A (ja) * | 1990-05-25 | 1992-02-03 | Tosoh Corp | 遠紫外線透過石英ガラスおよびその製造方法 |
| JP2980510B2 (ja) * | 1994-01-28 | 1999-11-22 | 信越石英株式会社 | 紫外線ランプ用高純度シリカガラスおよびその製造方法 |
| DE4419234A1 (de) * | 1994-06-01 | 1995-12-07 | Wacker Chemie Gmbh | Verfahren zur Silylierung von anorganischen Oxiden |
| JP2542797B2 (ja) * | 1994-09-29 | 1996-10-09 | 日本化学工業株式会社 | 高純度シリカの製造方法 |
| WO1996021617A1 (fr) * | 1995-01-12 | 1996-07-18 | Mitsubishi Chemical Corporation | Gel de silice, poudre de verre de quartz synthetique, moulage de verre de quartz et leur procedes de production |
| DE19855816A1 (de) * | 1998-12-03 | 2000-06-08 | Heraeus Quarzglas | Verfahren für die Reinigung von Si0¶2¶-Körnung und Vorrichtung zur Durchführung des Verfahrens |
| DE10030251A1 (de) * | 2000-06-20 | 2002-01-03 | Degussa | Abtrennung von Metallchloriden aus gasförmigen Reaktionsgemischen der Chlorsilan-Synthese |
| WO2003008332A1 (fr) * | 2001-07-19 | 2003-01-30 | Mitsubishi Chemical Corporation | Poudre de quartz de grande purete, procede de fabrication et article obtenu a partir de cette poudre |
| JP3970692B2 (ja) * | 2002-05-31 | 2007-09-05 | 信越化学工業株式会社 | プリフォーム製造方法 |
-
2003
- 2003-09-17 DE DE10342828A patent/DE10342828A1/de not_active Withdrawn
-
2004
- 2004-09-16 KR KR1020067005468A patent/KR100789124B1/ko active IP Right Grant
- 2004-09-16 US US10/571,332 patent/US20070003770A1/en not_active Abandoned
- 2004-09-16 EP EP04786950A patent/EP1663888A2/de not_active Withdrawn
- 2004-09-16 JP JP2006526581A patent/JP4903045B2/ja not_active Expired - Lifetime
- 2004-09-16 CN CNA2004800268452A patent/CN1863733A/zh active Pending
- 2004-09-16 WO PCT/EP2004/010335 patent/WO2005026068A2/en active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4681615A (en) * | 1982-12-23 | 1987-07-21 | Seiko Epson Kabushiki Kaisha | Silica glass formation process |
| DE3703079A1 (de) * | 1987-02-03 | 1988-08-11 | Rolf Dipl Chem Dr Rer Bruening | Verfahren zur herstellung von wasserfreiem synthetischem siliciumdioxid |
| DE10211958A1 (de) * | 2002-03-18 | 2003-10-16 | Wacker Chemie Gmbh | Hochreines Silica-Pulver, Verfahren und Vorrichtung zu seiner Herstellung |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1700831A1 (de) | 2005-03-09 | 2006-09-13 | Novara Technology S.R.L. | Verfahren zur Herstellung von Monolithen durch ein Sol-Gel Verfahren |
| EP1700830A1 (de) | 2005-03-09 | 2006-09-13 | Novara Technology S.R.L. | Prozess für die Herstellung von Monolithen mittels eines Sol-Gel Prozesses |
| EP1700829A1 (de) | 2005-03-09 | 2006-09-13 | Degussa AG | Verfahren zum Herstellen eines Glasmonolithes mittels eines Sol-Gel-Verfahrens |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2007505808A (ja) | 2007-03-15 |
| WO2005026068A2 (en) | 2005-03-24 |
| JP4903045B2 (ja) | 2012-03-21 |
| KR100789124B1 (ko) | 2007-12-28 |
| US20070003770A1 (en) | 2007-01-04 |
| KR20060087570A (ko) | 2006-08-02 |
| CN1863733A (zh) | 2006-11-15 |
| EP1663888A2 (de) | 2006-06-07 |
| WO2005026068A3 (en) | 2006-04-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3390304B1 (de) | Sprühgranulieren von siliziumdioxid bei der herstellung von quarzglas | |
| EP3390303B1 (de) | Herstellung von quarzglaskörpern mit taupunktkontrolle im schmelzofen | |
| DE10342828A1 (de) | Hochreines, pyrogen hergestelltes Siliciumdioxid | |
| DE602005003198T2 (de) | Verfahren zur Herstellung von Monolithen durch ein Sol-Gel Verfahren | |
| EP1686093B1 (de) | Pyrogen hergestelltes Siliciumdioxidpulver | |
| EP3390302B1 (de) | Herstellung eines quarzglaskörpers in einem schmelztiegel aus refraktärmetall | |
| DE602005002265T2 (de) | Durch flammenhydrolyse hergestelltes silicium-titan-mischoxidpulver | |
| WO2017103156A2 (de) | Herstellung von quarzglaskörpern aus siliziumdioxidpulver | |
| WO2017103168A1 (de) | Gasspülung für schmelzofen und herstellungsverfahren für quarzglas | |
| EP3390305A1 (de) | Herstellung von quarzglaskörpern aus siliziumdioxidgranulat | |
| EP3390294A1 (de) | Verringern des erdalkalimetallgehalts von siliziumdioxidgranulat durch behandlung von kohlenstoffdotiertem siliziumdioxidgranulat bei hoher temperatur | |
| WO2017103133A9 (de) | Herstellen und nachbehandeln eines quarzglaskörpers | |
| EP3390296A2 (de) | Herstellung eines quarzglaskörpers in einem mehrkammerofen | |
| WO2017103124A2 (de) | Erhöhen des siliziumgehalts bei der herstellung von quarzglas | |
| WO2017103167A2 (de) | Verringern des kohlenstoffgehalts von siliziumdioxidgranulat und herstellung eines quarzglaskörpers | |
| EP3390300A1 (de) | Herstellung eines quarzglaskörpers in einem stehendem sintertiegel | |
| EP3390306A2 (de) | Herstellung eines quarzglaskörpers in einem hängenden sintertiegel | |
| WO2017103153A9 (de) | Glasfasern und vorformen aus quarzglas mit geringem oh-, cl- und al-gehalt | |
| WO2017103112A9 (de) | Herstellung eines quarzglaskörpers in einem hängenden blechtiegel | |
| EP1083146A1 (de) | Bakterizides, mit Silber dotiertes Siliciumdioxid | |
| EP1991502B1 (de) | Verfahren zur wiederverwertung von hochsiedenden verbindungen innerhalb eines chlorsilanverbundes | |
| CH493610A (de) | Verfahren zur Herstellung feinverteilter Oxyde von Metallen oder Metalloiden | |
| DE102009029640A1 (de) | Verfahren zur Oberflächenmodifizierung von Metalloxidpartikeln | |
| EP3156459B1 (de) | Siliciumdioxidpulver mit grosser porenlänge | |
| DE10134382A1 (de) | Mit Erbiumoxid dotierte pyrogene Oxide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OP8 | Request for examination as to paragraph 44 patent law | ||
| 8127 | New person/name/address of the applicant |
Owner name: DEGUSSA GMBH, 40474 DUESSELDORF, DE |
|
| 8127 | New person/name/address of the applicant |
Owner name: EVONIK DEGUSSA GMBH, 40474 DUESSELDORF, DE |
|
| 8130 | Withdrawal |