CN116194109A - 抗体-药物缀合物和atm抑制剂的组合 - Google Patents
抗体-药物缀合物和atm抑制剂的组合 Download PDFInfo
- Publication number
- CN116194109A CN116194109A CN202180050399.2A CN202180050399A CN116194109A CN 116194109 A CN116194109 A CN 116194109A CN 202180050399 A CN202180050399 A CN 202180050399A CN 116194109 A CN116194109 A CN 116194109A
- Authority
- CN
- China
- Prior art keywords
- cancer
- methyl
- antibody
- imidazo
- pharmaceutical product
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6855—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from breast cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
提供了用于组合施用抗HER2抗体‑药物缀合物与ATM抑制剂的药物产品。该抗HER2抗体‑药物缀合物为其中由下式(其中A表示与抗体的连接位置)表示的药物接头经由硫醚键与抗HER2抗体缀合的抗体‑药物缀合物。还提供了治疗用途和方法,其中该抗体‑药物缀合物和该ATM抑制剂被组合施用于受试者:式(I):
Description
【技术领域】
本披露涉及一种药物产品,该药物产品用于与ATM抑制剂组合施用特异性抗体-药物缀合物,该特异性抗体-药物缀合物具有经由接头结构与抗HER2抗体缀合的抗肿瘤药物;并且本披露涉及一种治疗用途和方法,其中将该特异性抗体-药物缀合物和ATM抑制剂组合施用于受试者。
【背景技术】
ATM(共济失调毛细血管扩张症突变激酶)是丝氨酸/苏氨酸蛋白激酶,该激酶最初被鉴定为共济失调毛细血管扩张症中突变的基因的产物。共济失调毛细血管扩张症位于人染色体11q22-23上并且编码约350kDa的一个大蛋白质,其由磷脂酰肌醇(“PI”)3-激酶样丝氨酸/苏氨酸激酶结构域的存在来表征,该结构域的侧翼为调节ATM激酶活性和功能的FRAP-ATM-TRRAP结构域和FATC结构域。ATM激酶已被确定为通过双链断裂引起的DNA损伤应答的主要参与者。它主要在S/G2/M细胞周期过渡中并在坍塌复制叉处起作用以引发细胞周期检查点、染色质修饰、HR修复以及促存活信号级联放大,以便在DNA损伤后保持细胞完整性(拉文(Lavin),M.F.;Rev.Mol.Cell Biol.[分子细胞生物学述评]2008,759-769)。ATM激酶响应于由常见抗癌治疗如电离辐射和拓扑异构酶-II抑制剂(多柔比星,依托泊苷)所造成的直接的双链断裂,而且通过复制过程中的单链断裂至双链断裂转换还响应于拓扑异构酶-I抑制剂(例如伊立替康和托泊替康)。ATM激酶抑制可以增强任何这些试剂的活性,并且结果是ATM激酶抑制剂预期在癌症的治疗中是有用的。例如,WO 2017/046216中公开了ATM抑制剂的示例。
由与抗体缀合的细胞毒性药物组成的抗体-药物缀合物(ADC)可以选择性地将药物递送至癌细胞,并且因此预期会引起药物在癌细胞内累积并杀死癌细胞(Ducry,L.等人,Bioconjugate Chem.[生物共轭化学](2010)21,5-13;Alley,S.C.等人,Current Opinionin Chemical Biology[当代化学生物学观点](2010)14,529-537;Damle N.K.ExpertOpin.Biol.Ther.[生物治疗专家观点](2004)4,1445-1452;Senter P.D.等人,NatureBiotechnology[自然-生物技术](2012)30,631-637;Burris HA.等人,J.Clin.Oncol.[临床肿瘤学杂志](2011)29(4):398-405)。
一种此类抗体-药物缀合物为德卢替康-曲妥珠单抗(trastuzumab deruxtecan),其由靶向HER2的抗体和依喜替康的衍生物组成(Ogitani Y.等人,Clinical CancerResearch[临床癌症研究](2016)22(20),5097-5108;Ogitani Y.等人,Cancer Science[癌症科学](2016)107,1039-1046)。
尽管抗体-药物缀合物和ATM抑制剂具有治疗潜力,但尚未发表文献,描述表明抗体-药物缀合物和ATM抑制剂组合使用的优异效果的测试结果,或任何表明此类测试结果的科学依据。此外,在缺乏测试结果的情况下,存在一种可能性,即抗体-药物缀合物与另一种癌症治疗剂(如ATM抑制剂)的组合施用可能会导致负相互作用和/或亚加合性治疗结果,并且因此不能期望通过这种组合治疗来获得优异或卓越的效果。
因此,仍然需要改进的治疗组合物和方法,其可以增强现有癌症治疗剂的功效、增加治疗响应的持久性和/或降低剂量依赖性毒性。
【发明内容】
本披露中使用的抗体-药物缀合物(包括拓扑异构酶I抑制剂依喜替康的衍生物的抗HER2抗体-药物缀合物)已被证实当单独施用时,在治疗某些癌症诸如乳腺癌和胃癌时表现出优异的抗肿瘤效果。然而,需要提供药物和治疗,其可以在癌症治疗中获得优异的抗肿瘤效果,例如增强的功效、增加的治疗响应持久性和/或降低的剂量依赖性毒性。通过抑制由本披露的抗体-药物缀合物引入的双链断裂引起的DNA损伤响应,ATM抑制剂可在与抗体-药物缀合物组合施用时进一步增强抗肿瘤功效。
本披露提供了一种药物产品,该药物产品可通过将抗HER2抗体-药物缀合物与ATM抑制剂组合施用而在癌症治疗中表现出优异的抗肿瘤效果。本披露还提供了一种治疗用途和方法,其中将抗HER2抗体-药物缀合物和ATM抑制剂组合施用于受试者。
具体地,本披露涉及以下[1]至[52]:
[1]一种药物产品,该药物产品包含用于组合施用的抗HER2抗体-药物缀合物和ATM抑制剂,其中该抗HER2抗体-药物缀合物为其中由下式表示的药物-接头经由硫醚键与抗HER2抗体缀合的抗体-药物缀合物,
其中A表示与抗体的连接位置;
[2]如[1]所述的药物产品,其中该ATM抑制剂为由下式(I)表示的化合物:
其中:
R1是甲基;
R2是氢或甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟,
或其药学上可接受的盐;
[3]如[2]所述的药物产品,其中,在式(I)中,R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
[4]如[2]或[3]所述的药物产品,其中在式(I)中,R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
[5]如[2]至[4]中任一项所述的药物产品,其中,在式(I)中,R3是氢;
[6]如[2]至[5]中任一项所述的药物产品,其中,在式(I)中,R4是甲基;
[7]如[2]至[6]中任一项所述的药物产品,其中在该具有式(I)的化合物中,R5是氟;
[8]如[2]所述的药物产品,其中,在式(I)中:
R1是甲基;
R2是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是甲基;并且
R5是氢或氟;
[9]如[2]所述的药物产品,其中该ATM抑制剂为AZD1390,也称为AZ13791971,由下式表示:
或其药学上可接受的盐;
[10]如[1]至[9]中任一项所述的药物产品,其中该抗HER2抗体是包含重链和轻链的抗体,该重链包含:由SEQ ID NO:3[=SEQ ID NO:1的氨基酸残基26至33]表示的氨基酸序列组成的CDRH1、由SEQ ID NO:4[=SEQ ID NO:1的氨基酸残基51至58]表示的氨基酸序列组成的CDRH2和由SEQ ID NO:5[=SEQ ID NO:1的氨基酸残基97至109]表示的氨基酸序列组成的CDRH3,该轻链包含:由SEQ ID NO:6[=SEQ ID NO:2的氨基酸残基27至32]表示的氨基酸序列组成的CDRL1、由SEQ ID NO:7[=SEQ ID NO:2的氨基酸残基50至52]的氨基酸残基1至3所组成的氨基酸序列组成的CDRL2和由SEQ ID NO:8[=SEQ ID NO:2的氨基酸残基89至97]表示的氨基酸序列组成的CDRL3;
[11]如[1]至[9]中任一项所述的药物产品,其中抗HER2抗体是包含重链和轻链的抗体,该重链包含由SEQ ID NO:9[=SEQ ID NO:1的氨基酸残基1至120]表示的氨基酸序列组成的重链可变区,该轻链包含由SEQ ID NO:10[=SEQ ID NO:2的氨基酸残基1至107]表示的氨基酸序列组成的轻链可变区;
[12]如[1]至[9]中任一项所述的药物产品,其中抗HER2抗体是包含重链和轻链的抗体,该重链由SEQ ID NO:1表示的氨基酸序列组成,该轻链由SEQ ID NO:2表示的氨基酸序列组成;
[13]如[1]至[9]中任一项所述的药物产品,其中抗HER2抗体是包含重链和轻链的抗体,该重链由SEQ ID NO:11[=SEQ ID NO:1的氨基酸残基1至449]表示的氨基酸序列组成,该轻链由SEQ ID NO:2表示的氨基酸序列组成;
[14]如[1]至[13]中任一项所述的药物产品,其中抗HER2抗体-药物缀合物由下式表示:
其中‘抗体’指示经由硫醚键与药物-接头缀合的抗HER2抗体,并且n指示抗体-药物缀合物中每个抗体分子缀合的药物-接头的平均单元数,其中n在7至8的范围内;
[15]如[1]至[14]中任一项所述的药物产品,其中抗HER2抗体-药物缀合物为德卢替康-曲妥珠单抗(DS-8201);
[16]如[1]至[15]中任一项所述的药物产品,其中该产品是包含抗HER2抗体-药物缀合物和ATM抑制剂的组合物,用于同时施用;
[17]如[1]至[15]中任一项所述的药物产品,其中该产品是组合制剂,该组合制剂包含抗HER2抗体-药物缀合物和ATM抑制剂,用于顺序或同时施用;
[18]如[1]至[17]中任一项所述的药物产品,其中该产品用于治疗癌症;
[19]如[18]所述的药物产品,其中该癌症为选自由以下组成的组中的至少一种:乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤;
[20]如[18]所述的药物产品,其中该癌症为乳腺癌;
[21]如[20]所述的药物产品,其中该乳腺癌具有IHC 3+的HER2状态评分;
[22]如[20]所述的药物产品,其中该乳腺癌为HER2低表达乳腺癌;
[23]如[20]所述的药物产品,其中该乳腺癌具有IHC 2+的HER2状态评分;
[24]如[20]所述的药物产品,其中该乳腺癌具有IHC 1+的HER2状态评分;
[25]如[20]所述的药物产品,其中该乳腺癌具有IHC>0且<1+的HER2状态评分;
[26]如[20]所述的药物产品,其中该乳腺癌为三阴性乳腺癌;
[27]如[18]所述的药物产品,其中该癌症为胃癌;
[28]如[18]所述的药物产品,其中该癌症为结直肠癌;
[29]如[18]所述的药物产品,其中该癌症为肺癌;
[30]如[29]所述的药物产品,其中该肺癌是非小细胞肺癌;
[31]如[18]所述的药物产品,其中该癌症为胰腺癌;
[32]如[18]所述的药物产品,其中该癌症为卵巢癌;
[33]如[18]所述的药物产品,其中该癌症为前列腺癌;
[34]如[18]所述的药物产品,其中该癌症为肾癌;
[35]如[1]至[17]中任一项所定义的药物产品,该药物产品用于治疗癌症的用途中;
[36]用于如[35]所述使用的药物产品,其中该癌症如[19]至[34]中任一项所定义;
[37]抗HER2抗体-药物缀合物或ATM抑制剂在制备药物中的用途,该药物用于组合施用该抗HER2抗体-药物缀合物和该ATM抑制剂以治疗癌症,其中该抗HER2抗体-药物缀合物和该ATM抑制剂如[1]至[15]中任一项所定义;
[38]如[37]所述的用途,其中该癌症如[19]至[34]中任一项所定义;
[39]如[37]或[38]所述的用途,其中该药物是包含抗HER2抗体-药物缀合物和ATM抑制剂的组合物,用于同时施用;
[40]如[37]或[38]所述的用途,其中该药物是组合制剂,该组合制剂包含抗HER2抗体-药物缀合物和ATM抑制剂,用于顺序或同时施用;
[41]一种抗HER2抗体-药物缀合物,其与ATM抑制剂组合使用用于治疗癌症,其中抗HER2抗体-药物缀合物和ATM抑制剂如[1]至[15]中任一项所定义;
[42]用于如[41]所述使用的抗HER2抗体-药物缀合物,其中该癌症如[19]至[34]中任一项所定义;
[43]用于如[41]或[42]所述使用的抗HER2抗体-药物缀合物,其中该使用包括按顺序施用抗HER2抗体-药物缀合物和ATM抑制剂;
[44]用于如[41]或[42]所述使用的抗HER2抗体-药物缀合物,其中该使用包括同时施用抗HER2抗体-药物缀合物和ATM抑制剂;
[45]一种ATM抑制剂,其与抗HER2抗体-药物缀合物组合使用用于治疗癌症,其中该抗HER2抗体-药物缀合物和该ATM抑制剂如[1]至[15]中任一项所定义;
[46]用于如[45]所述使用的ATM抑制剂,其中该癌症如[19]至[34]中任一项所定义;
[47]用于如[45]或[46]所述使用的ATM抑制剂,其中该使用包括按顺序施用抗HER2抗体-药物缀合物和ATM抑制剂;
[48]用于如[45]或[46]所述使用的ATM抑制剂,其中该使用包括同时施用抗HER2抗体-药物缀合物和ATM抑制剂;
[49]一种治疗癌症的方法,该方法包括向有需要的受试者组合施用如[1]至[15]中任一项所定义的抗HER2抗体-药物缀合物和ATM抑制剂组合;
[50]如[49]所述的方法,其中该癌症如[19]至[34]中任一项所定义;
[51]如[49]或[50]所述的方法,其中该方法包括按顺序施用该抗HER2抗体-药物缀合物和该ATM抑制剂;并且
[52]如[49]或[50]所述的方法,其中该方法包括同时施用该抗HER2抗体-药物缀合物和该ATM抑制剂。
[披露的有利效果]
本披露提供了一种药物产品,其中组合施用抗HER2抗体-药物缀合物和ATM抑制剂,该抗HER2抗体-药物缀合物具有经由接头结构与抗HER2抗体缀合的抗肿瘤药物;并且本披露提供了一种治疗用途和方法,其中将该特异性抗体-药物缀合物和ATM抑制剂组合施用于受试者。因此,本披露可以提供在癌症治疗中可以获得优异抗肿瘤效果的药物和治疗。
【附图说明】
[图1]图1是显示抗HER2抗体的重链的氨基酸序列(SEQ ID NO:1)的图。
[图2]图2是显示抗HER2抗体的轻链的氨基酸序列(SEQ ID NO:2)的图。
[图3]图3是显示重链CDRH1的氨基酸序列(SEQ ID NO:3[=SEQ ID NO:1的氨基酸残基26至33])的图。
[图4]图4是显示重链CDRH2的氨基酸序列(SEQ ID NO:4[=SEQ ID NO:1的氨基酸残基51至58])的图。
[图5]图5是显示重链CDRH3的氨基酸序列(SEQ ID NO:5[=SEQ ID NO:1的氨基酸残基97至109])的图。
[图6]图6是显示轻链CDRL1的氨基酸序列(SEQ ID NO:6[=SEQ ID NO:2的氨基酸残基27至32])的图。
[图7]图7是显示包含轻链CDRL2(SAS)的氨基酸序列的氨基酸序列(SEQ ID NO:7[=SEQ ID NO:2的氨基酸残基50至56])的图。
[图8]图8是显示轻链CDRL3的氨基酸序列(SEQ ID NO:8[=SEQ ID NO:2的氨基酸残基89至97])的图。
[图9]图9是显示重链可变区的氨基酸序列(SEQ ID NO:9[=SEQ ID NO:1的氨基酸残基1至120])的图。
[图10]图10是显示轻链可变区的氨基酸序列(SEQ ID NO:10[=SEQ ID NO:2的氨基酸残基1至107])的图。
[图11]图11是显示重链的氨基酸序列(SEQ ID NO:11[=SEQ ID NO:1的氨基酸残基1至449])的图。
[图12A和12B]图12A和12B是示出在三个具有不同HER2表达的乳腺癌细胞系和一个具有高HER2表达的胃细胞系中,通过将DS-8201与AZD1390(AZ13791971;ATM抑制剂)组合的高通量筛选而获得的组合矩阵的图。
[图13]图13是示出关于(A)相对总细胞计数作为对照百分比和(B)Loewe、Bliss和HSA评分,在HER2高KPL4细胞系中DS-8201和AZD1390的组合的协同矩阵的图。
[图14]图14是示出在(A)HER2高KPL4细胞系和(B)HER2阴性MDA-MB-468细胞系中DS-8201与AZD1390的组合的治疗后剩余总细胞与时间零相比的变化的图。
[图15]图15是示出在(A)HER2高KPL4细胞系或(B)HER2低MDA-MB-468细胞系中DS-8201与AZD1390组合的ATM依赖性KAP1 pSer824信号传导、DNA双链断裂损伤(γH2AX)生物标志物的诱导或细胞数百分比(相对于溶剂对照)的图。
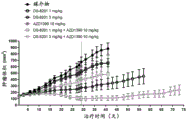
[图16]图16是示出皮下植入NCI-N87肿瘤的雌性裸小鼠治疗组的肿瘤体积随时间变化的图,该小鼠用1mg/kg或3mg/kg DS-8201单独治疗,并用与10mg/kg AZD1390的组合进行治疗。
[图17]图17是示出在(A)NCI-N87(胃癌)和(B)KPL4(乳腺癌)细胞系中将DS-8201或依喜替康甲磺酸盐与AZD1390组合的抗体印迹图像的图。
[图18]在图18中,(A)和(B)是示出在HER2高NCI-H2170(肺癌)细胞系中通过将DS-8201和AZD1390(ATM抑制剂)组合的高通量筛选获得的组合矩阵的图。
为了更容易地理解本披露,首先定义某些术语。另外的定义贯穿详细说明列出。
在详细描述本披露之前,应理解的是本披露不限于特定的组合物或方法步骤,因为这些组合物或方法步骤可以变化。如在本说明书和随附权利要求书中所使用,除非上下文另外明确说明,否则单数形式“一个/种(a/an)”和“该/所述(the)”包括复数参考对象。术语“一个”(或“一种”)以及术语“一个或多个”和“至少一个”在本文可以互换使用。
此外,“和/或”在本文使用时被认为是两个所指定的特征或组分中每一者与或不与另一者一起的具体披露。因此,术语“和/或”如在词组如“A和/或B”中使用时在此旨在包括“A和B”、“A或B”、“A”(单独)、以及“B”(单独)。同样,如在诸如“A、B和/或C”等短语中所用的术语“和/或”意图涵盖以下方面中的每一个:A、B、和C;A、B或C;A或C;A或B;B或C;A和C;A和B;B和C;A(单独);B(单独);和C(单独)。
除非另外定义,否则本文使用的所有技术和科学术语具有如本披露所属领域的普通技术人员通常理解的相同含义。例如,Concise Dictionary of Biomedicine andMolecular Biology[简明生物医学和分子生物学词典],Juo,Pei-Show,第2版,2002,CRCPress[CRC出版社];Dictionary of Cell and Molecular Biology[细胞和分子生物学词典],第3版,1999,Academic Press[学术出版社];以及Oxford Dictionary OfBiochemistry And Molecular Biology[生物化学和分子生物学牛津词典],修订版,2000,Oxford University Press[牛津大学出版社]为技术人员提供了在本披露中使用的许多术语的通用词典注释。
单位、前缀和符号是以它们的国际单位系统(Système International deUnites)(SI)接受的形式表示。数值范围包括限定该范围的数字。
应当理解,无论在什么情况下本文用语言“包含”描述各个方面时,也提供了用“由……组成”和/或“主要由……组成”描述的其他类似方面。术语“抑制”、“阻止”、以及“阻遏”在此可互换地使用,并且指生物活性的任何统计学显著的降低,包括活性的完全阻止。例如,“抑制”可以指生物活性的约10%、20%、30%、40%、50%、60%、70%、80%、90%或100%的降低。细胞增生可以使用本领域公认的技术测定,其测量的细胞分裂速率,和/或经历细胞分裂的细胞群中细胞的分数、和/或由于终末分化或细胞死亡(例如,胸苷掺入)自细胞群的细胞损失的速率。
术语“受试者”是指有待成为特定治疗的接受者的任何动物(例如,哺乳动物),包括但不限于人类、非人类灵长动物、啮齿类等。典型地,术语“受试者”和“患者”在本文关于人类受试者可互换地使用。
术语“药物产品”是指此类制剂,其形式允许活性成分的生物活性,或者作为含有所有活性成分的组合物(用于同时施用),或者作为各自含有至少一种但不是所有活性成分的单独组合物的组合(组合制剂)(用于顺序或同时施用),并且其不含有对将施用该产品的受试者具有不可接受的毒性的额外组分。此类产品可以是无菌的。“同时施用”是指活性成分同时施用。“顺序施用”是指活性成分按任一顺序、以各次施用之间的时间间隔相继地施用。时间间隔可以是例如小于24小时,优选小于6小时,更优选小于2小时。
术语如“治疗(treating或treatment或to treat)”或“减轻(alleviating或toalleviate)”是指(1)使得诊断的病理性病症或障碍被治愈、减缓、减轻症状、和/或停止进展的治疗措施以及(2)防止和/或减缓所靶向的病理学病症或障碍的发展的预防性或防止性措施。因此,需要治疗的那些包括已患有障碍的那些;倾向于患有障碍的那些;以及在他们中需要预防障碍的那些。在某些方面中,如果患者示出例如,总的、部分的、或瞬时的某一类型癌症的缓解,则根据本披露的方法成功“治疗”了该受试者的癌症。
术语“癌症”、“肿瘤”、“癌性”、和“恶性”指或描述在哺乳动物中典型地是特征为不受控制的细胞生长的生理病症。癌症的实例包括但不限于乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤。癌症包括血液系统恶性肿瘤,如急性髓性白血病、多发性骨髓瘤、慢性淋巴细胞性白血病、弥漫性大B细胞淋巴瘤、伯基特淋巴瘤、滤泡性淋巴瘤以及实体瘤如乳腺癌、肺癌、成神经细胞瘤和结肠癌。
术语“细胞毒剂”如在此使用的是广泛定义的并且是指抑制或阻止细胞的功能和/或造成细胞破坏(细胞死亡)、和/或施加抗肿瘤/抗增生作用的一种物质。例如,细胞毒性试剂直接或间接阻止赘生性肿瘤细胞的发育、成熟、或扩散。该术语还包括仅引起抑制细胞生长效应并且不仅仅是细胞毒性效应的此类试剂。该术语包括如下指出的化疗剂,连同其他HER2拮抗剂、抗血管生成剂、酪氨酸激酶抑制剂、蛋白激酶A抑制剂,细胞因子家族的成员、放射性同位素、以及毒素如细菌、真菌、植物或动物来源的酶促活性毒素。术语“化疗剂”是包括天然或合成的化学化合物的术语“细胞毒剂”的子集。
根据本披露的方法或用途,本披露的化合物可以施用于患者,以促进对于癌症的积极治疗响应。术语对于癌症治疗的“积极治疗响应”是指与该疾病相关的症状的改进。例如,疾病的改进可以表征为完全响应。术语“完全响应”是指没有临床上可检测的疾病,并且任何先前的测试结果都正常。可替代地,疾病的改善可以被归类为部分响应。“积极治疗响应”涵盖从本披露的化合物的给予得到的癌症的进展和/或持续时间的减少或抑制,癌症的严重性的减少或改进、和/或其一种或多种症状的改进。在具体方面中,此类术语是指给予本披露的化合物之后以下一种、两种或三种或更多种结果:
(1)癌細胞群的穩定化、減少或消除;
(2)癌症生长的稳定或减少;
(3)癌症形成受损;
(4)原发性、区域性和/或转移性癌症的根除、去除,或控制;
(5)死亡率降低;
(6)无疾病、无复发、无进展、和/或总存活、持续时间或比率的增加;
(7)响应率、响应的持久性或响应或处于缓解的患者数量的增加;
(8)住院率的降低,
(9)住院时间的减少,
(10)癌症的尺寸维持并且不增加或增加少于10%、优选小于5%、优选小于4%、优选小于2%,以及
(11)处于缓解的患者数量的增加。
(12)否则治疗癌症要求的辅助治疗(如,化疗或激素治疗)的数目的减少。
临床响应可以使用筛选技术评定,如PET、磁共振成像(MRI)扫描、x-射线照相成像、计算机断层成像(CT)扫描、流式细胞计量术或荧光活化细胞分选仪(FACS)分析、组织学、宏观病理学、和血液化学,包括但不限于可通过ELISA、RIA、层析、以及类似物检测的变化。除了这些积极治疗响应之外,正经受治疗的受试者可以经历与该疾病相关的症状的改进的有益效果。
如在此所使用的,短语“有效量”意指一种化合物或组合物的足以显著和积极改变有待治疗的症状和/或病症(例如,提供积极临床响应)的量。用于药物产品中的活性成分的有效量将随所治疗的特定病症、病症的严重程度、治疗的持续时间、同步治疗的性质、所采用的一种或多种特定活性成分、所利用的一种或多种特定药学上可接受的赋形剂/载剂、以及处于主治医生的知识和专业知识范围内的类似因素而变化。特别是,与抗体-药物缀合物组合用于治疗癌症的具有式(I)化合物的有效量是以下量,其使得该组合足以对症缓解温血动物如人的癌症症状,以减缓癌症进展,或降低具有癌症症状的患者恶化的风险。
在使用术语“任选地”时,意指随后的特征可以发生或可以不发生。因此,使用术语“任选地”包括特征存在的情况、以及还有特征不存在的情况。例如,基团“任选地被一个甲氧基取代”包括具有和不具有甲氧基取代基的基团。
术语“被取代的”意指在指定基团上的一个或多个氢(例如1或2个氢,或替代地1个氢)被指示的一个或多个取代基(例如1或2个取代基,或替代地1个取代基)替代,其条件是具有取代基的任一个或多个原子保持允许的化合价。取代基组合仅涵盖稳定的化合物以及稳定的合成中间体。“稳定的”是指相关的化合物或中间体足够稳固以便分离并且具有作为合成中间体或作为具有潜在治疗效用的试剂的效用。如果基团未被描述为“被取代的”或“任选地被取代的”,则应视为未被取代的(即,在指定基团上的氢都尚未被替代)。
术语“药学上可接受的”用于指定对象(例如盐、剂型或赋形剂)是适合在患者中使用的。药学上可接受的盐的实例列表可以发现于:Handbook of Pharmaceutical Salts:Properties,Selection and Use[药用盐手册:特性、选择和用途],P.H.Stahl和C.G.Wermuth编辑,魏因海姆/苏黎世:Wiley-VCH/VHCA出版社[Weinheim/Zürich:Wiley-VCH/VHCA],2002。例如,具有式(I)或(II)的化合物的合适的药学上可接受的盐是酸加成盐。具有式(I)或(II)的化合物的酸加成盐可以通过在技术人员已知的条件下,使该化合物与合适的无机酸或有机酸接触来形成。酸加成盐例如可以使用选自由以下组成的组的无机酸来形成:盐酸、氢溴酸、硫酸以及磷酸。酸加成盐还可以使用选自由以下组成的组的有机酸来形成:三氟乙酸、柠檬酸、马来酸、草酸、乙酸、甲酸、苯甲酸、富马酸、琥珀酸、酒石酸、乳酸、丙酮酸、甲磺酸、苯磺酸以及对甲苯磺酸。
因此,在具有式(I)或(II)的化合物或其药学上可接受的盐的一个实施例中,该药学上可接受的盐是盐酸盐、氢溴酸盐、硫酸盐、磷酸盐、三氟乙酸盐、柠檬酸盐、马来酸盐、草酸盐、乙酸盐、甲酸盐、苯甲酸盐、富马酸盐、琥珀酸盐、酒石酸盐、乳酸盐、丙酮酸盐、甲磺酸盐、苯磺酸盐或对甲苯磺酸盐。在具有式(I)或(II)的化合物或其药学上可接受的盐的另一个实施例中,药学上可接受的盐是甲磺酸盐。在具有式(I)或(II)的化合物或其药学上可接受的盐的另一个实施例中,该药学上可接受的盐是单甲磺酸盐,即具有式(I)或(II)的化合物与甲磺酸的化学计量是1:1。
本说明书中描述的化合物和盐可以以溶剂化形式和非溶剂化形式存在。例如,溶剂化形式可以是水合形式,如半水合物、一水合物、二水合物、三水合物或其替代量。本披露涵盖了具有式(I)或(II)的化合物的所有此类溶剂化和非溶剂化形式,具体地是就此类形式具有ATM激酶抑制活性的程度而言。
本说明书中所描述的化合物和盐的原子可以作为它们的同位素存在。本披露涵盖了具有式(I)或(II)的所有化合物,其中原子被其同位素中的一个或多个替换(例如具有式(I)或(II)的化合物,其中一个或多个碳原子是11C或13C碳同位素,或其中一个或多个氢原子是2H或3H同位素,或其中一个或多个氟原子是18F同位素)。
本说明书中所描述的化合物和盐可以按互变异构体的混合物存在。“互变异构体”是结构异构体,其存在于由氢原子的迁移产生的平衡中。本披露包括具有式(I)或(II)的化合物的所有互变异构体,具体地是就此类互变异构体具有ATM激酶抑制活性的程度而言。
本说明书中所描述的化合物和盐可以借助一个或多个不对称碳原子而以光学活性形式或外消旋形式存在。本披露包括具有ATM激酶抑制活性的具有式(I)或(II)的化合物的任何光学活性或外消旋形式。光学活性形式的合成可以通过本领域中熟知的有机化学标准技术进行,例如通过使用光学活性物质合成或通过拆分外消旋形式。
因此,在具有式(I)或(II)的化合物或其药学上可接受的盐的一个实施例中,该化合物是对映异构体过量(%ee)≥95%、≥98%或≥99%的单一光学异构体。在另一个实施例中,单一光学异构体以对映异构体过量(%ee)≥99%存在。
本说明书中所述的化合物和盐可以是晶体,并且可以展示一种或多种结晶形式。本披露涵盖了具有式(I)或(II)的化合物的任何晶体或非晶形形式,或这此类形式的混合物,它们都具有ATM激酶抑制活性。
【具体实施方式】
在下文中,描述了用于实施本披露的优选方式。给出下面描述的实施例仅仅是为了说明本披露的典型实施例的一个实例,而不是为了限制本披露的范围。
1.抗体-药物缀合物
本披露中使用的抗体-药物缀合物为其中由下式表示的药物-接头经由硫醚键与抗HER2抗体缀合的抗体-药物缀合物,
其中A表示与抗体的连接位置。
在本披露中,抗体-药物缀合物中由接头和药物组成的部分结构被称为“药物-接头”。药物-接头与抗体中链间二硫键位点(重链之间的两个位点,以及重链和轻链之间的两个位点)形成的巯基(换句话说,半胱氨酸残基的硫原子)相连。
本披露的药物-接头包括依喜替康(IUPAC名称:(1S,9S)-1-氨基-9-乙基-5-氟-1,2,3,9,12,15-六氢-9-羟基-4-甲基-10H,13H-苯并[de]吡喃并[3',4':6,7]吲哚嗪并[1,2-b]喹啉-10,13-二酮,(也表示为化学名:(1S,9S)-1-氨基-9-乙基-5-氟-2,3-二氢-9-羟基-4-甲基-1H,12H-苯并[de]吡喃并[3',4':6,7]吲哚嗪并[1,2-b]喹啉-10,13(9H,15H)-二酮)),其为拓扑异构酶I抑制剂,作为成分。依喜替康是具有抗肿瘤作用的喜树碱衍生物,由下式表示:
本披露中使用的抗HER2抗体-药物缀合物也可以由下式表示:
在此,药物-接头经由硫醚键与抗HER2抗体(“抗体-”)缀合。N的含义与所谓的缀合药物分子的平均数(DAR;药物与抗体比率)的含义相同,并指示每个抗体分子所缀合的药物-接头的平均单元数。
在迁移到癌细胞中后,本披露中使用的抗HER2抗体-药物缀合物在接头部分被切割,以释放由下式表示的化合物:
推测该化合物是本披露中使用的抗体-药物缀合物的抗肿瘤活性的原始来源,并且已经证实其具有拓扑异构酶I抑制作用(Ogitani Y.等人,Clinical Cancer Research[临床癌症研究],2016年10月,15;22(20):5097-5108,Epub 2016年3月29日)。
已知本披露中使用的抗HER2抗体-药物缀合物具有旁观者效应(Ogitani Y.等人,Cancer Science[癌症科学](2016)107,1039-1046)。旁观者效应通过以下过程发挥作用,即本发明中使用的抗体-药物缀合物在表达靶标的癌细胞中被内化,然后释放的化合物也对存在于其周围且不表达靶标的癌细胞发挥抗肿瘤作用。即使当抗HER2抗体-药物缀合物与根据本披露的ATM抑制剂组合使用时,这种旁观者效应也作为优异的抗肿瘤效果而发挥作用。
2.抗体-药物缀合物中的抗体
本披露中使用的抗体-药物缀合物中的抗HER2抗体可以来自任何物种,并且优选为来自人、大鼠、小鼠或兔的抗HER2抗体。在抗体为来自除人类物种以外的物种的情况下,优选使用众所周知的技术将其嵌合化或人源化。抗HER2抗体可以为多克隆抗体或单克隆抗体,并且优选为单克隆抗体。
本披露中使用的抗体-药物缀合物中的抗体是优选具有能够靶向癌细胞的特性的抗HER2抗体,并且优选是具有例如识别癌细胞的特性、与癌细胞结合的特性、在癌细胞中内化的特性和/或针对癌细胞的杀细胞活性的抗体。
抗HER2抗体对癌细胞的结合活性可以使用流式细胞术来证实。抗体到癌细胞中的内化可以使用以下来证实:(1)使用与治疗性抗体结合的二级抗体(荧光标记的)在荧光显微镜下观察掺入细胞中的抗体的测定(Cell Death and difference[细胞死亡与差异](2008)15,751-761),(2)使用与治疗性抗体结合的二级抗体(荧光标记的)测量掺入细胞中的荧光强度的测定(Molecular Biology of the Cell[细胞分子生物学],第15卷,5268-5282,2004年12月),或(3)使用与治疗性抗体结合的免疫毒素的Mab-ZAP测定,其中该毒素在掺入细胞后释放以抑制细胞生长(Bio technologies[生物技术]28:162-165,2000年1月)。作为免疫毒素,可以使用白喉毒素催化结构域和蛋白G的重组复合蛋白。
通过测定对抗细胞生长的抑制活性,可以在体外证实抗HER2抗体的抗肿瘤活性。例如,培养过表达作为抗体的靶蛋白的HER2的癌细胞系,并将抗体以不同浓度加入培养系统中,以测定对抗病灶形成、集落形成和球状体生长的抑制活性。可以在体内证实抗肿瘤活性,例如,通过将抗体施用于具有移植的高表达靶蛋白的癌细胞系的裸鼠,并测定癌细胞的变化。
由于在抗HER2抗体-药物缀合物中缀合的化合物发挥抗肿瘤作用,优选但非必须的是抗HER2抗体本身应该具有抗肿瘤作用。为了特异性和选择性地发挥抗肿瘤化合物对癌细胞的细胞毒活性,重要且也是优选的是,抗HER2抗体应该具有内化以迁移到癌细胞中的特性。
本披露中使用的抗体-药物缀合物中的抗HER2抗体可以通过本领域已知的方法获得。例如,可以使用本领域通常实施的方法获得本披露的抗体,该方法涉及用抗原多肽对动物进行免疫,并收集和纯化体内产生的抗体。抗原的来源不限于人类,并且动物可以用来源于非人类动物如小鼠、大鼠等的抗原进行免疫。在这种情况下,可以测试与获得的异源抗原结合的抗体与人类抗原的交叉反应性,以筛选适用于人类疾病的抗体。
或者,根据本领域已知的方法,将产生针对该抗原的抗体的抗体产生细胞与骨髓瘤细胞融合(例如,Kohler和Milstein,Nature[自然](1975)256,第495-497页;和Kennet,R.编辑,Monoclonal Antibodies[单克隆抗体],第365-367页,Plenum Press[普莱纽姆出版社],纽约(1980))以建立杂交瘤,从杂交瘤中可以继而获得单克隆抗体。
可以通过基因工程改造宿主细胞以产生编码抗原蛋白的基因来获得抗原。具体而言,制备允许抗原基因表达的载体,并将其转移至宿主细胞,从而表达该基因。如此表达的抗原可以被纯化。也可以通过用上述基因工程改造的抗原表达细胞或表达抗原的细胞系对动物进行免疫的方法来获得抗体。
本披露使用的抗体-药物缀合物中的抗HER2抗体优选为通过人工修饰以降低对人的异源抗原性而获得的重组抗体,例如嵌合抗体或人源化抗体,或者优选为仅具有来源于人的抗体的基因序列的抗体,即人抗体。这些抗体可以用已知的方法生产。
作为嵌合抗体,可以例举其中抗体可变区和恒定区来自不同物种的抗体,例如其中小鼠或大鼠来源的抗体可变区与人源性抗体恒定区连接的嵌合抗体(Proc.Natl.Acad.Sci.USA[美国国家科学院院刊],81,6851-6855,(1984))。
作为人源化抗体,可以例举通过仅将异源抗体的互补决定区(CDR)整合到人源性抗体中获得的抗体(Nature[自然](1986)321,第522-525页),和通过CDR移植方法将异源抗体框架的一部分氨基酸残基以及异源抗体的CDR序列移植到人抗体中获得的抗体(WO 90/07861),和使用基因转化诱变策略(美国专利号5821337)进行人源化的抗体。
作为人抗体,可以例举通过使用产生人抗体的小鼠产生的抗体,该小鼠具有包含人抗体的重链和轻链的基因的人染色体片段(参见Tomizuka,K.等人,Nature Genetics[自然遗传学](1997)16,第133-143页;Kuroiwa,Y.等人,Nucl.Acids Res.[核酸研究](1998)26,第3447-3448页;Yoshida,H.等人,Animal Cell Technology:Basic and AppliedAspects[动物细胞技术:基础和应用方面]第10卷,第69-73页(Kitagawa,Y.,Matsuda,T.和Iijima,S.编辑),Kluwer Academic Publishers[克吕韦尔学术出版社],1999;Tomizuka,K.等人,Proc.Natl.Acad.Sci.USA [美国国家科学院院刊](2000)97,第722-727页,等等)。作为替代,可以例举通过噬菌体展示获得的抗体,该抗体选自人抗体库(参见Wormstone,I.M.等人,Investigative Ophthalmology&Visual Science[调查性眼科与视觉科学](2002)43(7),第2301-2308页;Carmen,S.等人,Briefings in Functional Genomics andProteomics[功能基因组学和蛋白质组学简介](2002),1(2),第189-203页;Siriwardena,D.等人,Ophthalmology[眼科学](2002)109(3),第427-431页,等等)。
在本披露中,还包括在本披露中使用的抗体-药物缀合物中的抗HER2抗体的修饰变体。修饰变体是指通过对根据本披露的抗体进行化学或生物修饰而获得的变体。化学修饰变体的实例包括包含化学部分与氨基酸骨架连接的变体、包含化学部分与N连接或O连接的碳水化合物链连接的变体等。生物修饰变体的实例包括通过翻译后修饰(如N连接或O连接的糖基化、N或C末端加工、脱酰胺、天冬氨酸异构化或甲硫氨酸氧化)获得的变体,以及通过在原核宿主细胞中表达而在N末端添加甲硫氨酸残基的变体。此外,经标记以使得能够检测或分离根据本披露的抗体或抗原的抗体,例如酶标记的抗体、荧光标记的抗体和亲和标记的抗体也包括在修饰变体的含义中。根据本披露的抗体的这种修饰变体可用于提高抗体的稳定性和血液滞留性、降低其抗原性、检测或分离抗体或抗原,等等。
此外,通过调节与根据本披露的抗体连接的聚糖的修饰(糖基化、去糖基化等),有可能增强抗体依赖性细胞毒活性。作为调节抗体的聚糖修饰的技术,在WO 99/54342、WO00/61739、WO 02/31140、WO 2007/133855、WO 2013/120066等中公开的技术是已知的。然而,该技术不限于此。在根据本披露的抗HER2抗体中,还包括其中聚糖的修饰受到调节的抗体。
已知在培养的哺乳动物细胞中产生的抗体的重链的羧基末端处的赖氨酸残基缺失(Journal of Chromatography A[色谱法杂志A辑],705:129-134(1995)),并且还已知在培养的哺乳动物细胞中产生的抗体的重链的羧基末端的处两个氨基酸残基(甘氨酸和赖氨酸)缺失,并且新位于羧基末端处的脯氨酸残基被酰胺化(Analytical Biochemistry[分析生物化学],360:75-83(2007))。然而,重链序列的这种缺失和修饰不影响抗体的抗原结合亲和力和效应子功能(补体的激活、抗体依赖性细胞毒性等)。因此,在根据本披露的抗HER2抗体中,也包括经过这种修饰的抗体和抗体的功能片段,并且还包括其中在重链的羧基末端处缺失了一个或两个氨基酸的缺失变体、通过缺失变体的酰胺化获得的变体(例如,其中羧基末端脯氨酸残基已经酰胺化的重链)等。根据本披露的在抗HER2抗体的重链的羧基末端处具有缺失的缺失变体的类型不限于上述变体,只要抗原结合亲和力和效应子功能是保全的。构成根据本披露的抗体的两条重链可以是选自由全长重链和上述缺失变体组成的组中的一种类型,或者可以是从中选择的两种类型的组合。每种缺失变体的量的比率可以受产生根据本披露的抗HER2抗体的培养的哺乳动物细胞的类型和培养条件影响;然而,作为优选可以例举其中在根据本披露的抗体的两条重链中,羧基末端处的一个氨基酸残基已经缺失的抗体。
作为根据本披露的抗HER2抗体的同种型,例如,可以例举IgG(IgG1、IgG2、IgG3、IgG4),并且作为优选可以例举IgG1或IgG2。
在本披露中,术语“抗HER2抗体”是指与HER2(人表皮生长因子受体2型;ErbB-2)特异性结合的抗体,并且优选具有通过与HER2结合而在表达HER2的细胞中内化的活性。
抗HER2抗体的实例包括曲妥珠单抗(美国专利号5821337)和帕妥珠单抗(WO 01/00245),并且作为优选可以例举曲妥珠单抗。
3.抗体-药物缀合物的生产
用于生产根据本披露的抗HER2抗体-药物缀合物的药物-接头中间体由下式表示:
药物-接头中间体可以表示为化学名称为N-[6-(2,5-二氧代-2,5-二氢-1H-吡咯-1-基)己酰基]甘氨酰-甘氨酰-L-苯基丙氨酰基-N-[(2-{[(1S,9S)-9-乙基-5-氟-9-羟基-4-甲基-10,13-二氧代-2,3,9,10,13,15-六氢-1H,12H-苯并[de]吡喃并[3',4':6,7]吲哚嗪并[1,2-b]喹啉-1-基]氨基}-2-氧代乙氧基)甲基]甘氨酰胺,并且可以参照WO 2014/057687、WO 2015/098099、WO 2015/115091、WO 2015/155998、WO 2019/044947中的描述来生产。
本披露中使用的抗HER2抗体-药物缀合物可以通过使上述药物-接头中间体和具有巯基(也称为巯基)的抗HER2抗体反应来生产。
具有巯基的抗HER2抗体可以通过本领域公知的方法获得(Hermanson,G.T,Bioconjugate Techniques[生物缀合技术],第56-136页,第456-493页,Academic Press[学术出版社](1996))。例如,通过对抗体中的每个链间二硫化物使用0.3至3摩尔当量的还原剂如三(2-羧乙基)膦盐酸盐(TCEP),并在含有螯合剂如乙二胺四乙酸(EDTA)的缓冲溶液中与抗体反应,可以获得抗体中链间二硫化物部分或完全还原的具有巯基的抗HER2抗体。
此外,通过对每个具有巯基的抗HER2抗体使用2至20摩尔当量的药物-接头中间体,可以生产其中每个抗体分子缀合2至8个药物分子的抗HER2抗体-药物缀合物。
生产的抗体-药物缀合物的每个抗HER2抗体分子的缀合药物分子平均数可例如通过以下测定:基于抗体-药物缀合物及其缀合前体在280nm和370nm两个波长下的UV吸光度测量的计算方法(UV方法)或基于通过用还原剂处理抗体-药物缀合物获得的片段的HPLC测量的定量的计算方法(HPLC方法)。
可以参考WO 2014/057687、WO 2015/098099、WO 2015/115091、WO 2015/155998、WO 2017/002776、WO 2018/212136等中的描述来进行抗HER2抗体和药物-接头中间体之间的缀合以及抗体-药物缀合物的每个抗体分子的缀合药物分子平均数的计算。
在本披露中,术语“抗HER2抗体-药物缀合物”是指以下抗体-药物缀合物,其使得根据本披露的抗体-药物缀合物中的抗体是抗HER2抗体。
抗HER2抗体优选为包含以下重链和轻链的抗体,该重链包含:由SEQ ID NO:1的氨基酸残基26至33所组成的氨基酸序列组成的CDRH1、由SEQ ID NO:1的氨基酸残基51至58所组成的氨基酸序列组成的CDRH2和由SEQ ID NO:1的氨基酸残基97至109所组成的氨基酸序列组成的CDRH3,该轻链包含:由SEQ ID NO:2的氨基酸残基27至32所组成的氨基酸序列组成的CDRL1、由SEQ ID NO:2的氨基酸残基50至52所组成的氨基酸序列组成的CDRL2和由SEQID NO:2的氨基酸残基89至97所组成的氨基酸序列组成的CDRL3,并且更优选为包含以下重链和轻链的抗体,该重链包含:由SEQ ID NO:1的氨基酸残基1至120所组成的氨基酸序列组成的重链可变区,该轻链包含由SEQ ID NO:2的氨基酸残基1至107所组成的氨基酸序列组成的轻链可变区,并且甚至更优选为包含由SEQ ID NO:1表示的氨基酸序列组成的重链和由SEQ ID NO:2表示的氨基酸序列组成的轻链的抗体,或者为包含由SEQ ID NO:1的氨基酸残基1至449组成的重链和由SEQ ID NO:2的所有氨基酸残基1至214组成的轻链的抗体。
在抗HER2抗体-药物缀合物中,每个抗体分子缀合的药物-接头的平均单元数优选为2至8,更优选为3至8,甚至更优选为7至8,甚至更优选为7.5至8,并且甚至更优选为约8。
本披露中使用的抗HER2抗体-药物缀合物可以参考WO 2015/115091等中的描述来生产。
在优选的实施例中,抗HER2抗体-药物缀合物为德卢替康-曲妥珠单抗(DS-8201)。
4.ATM抑制剂
在本披露中,术语“ATM抑制剂”是指抑制ATM(共济失调毛细血管扩张症突变激酶)的药剂。本披露中的ATM抑制剂可以选择性地抑制ATM激酶,或可以非选择性地抑制ATM并且还抑制ATM以外的激酶。优选地,本披露中的ATM抑制剂选择性地抑制ATM。本披露中的ATM抑制剂没有特别限制,只要其是具有所述特征的药剂即可,其优选的示例可以包括在WO2017/046216、WO 2015/170081、WO 2018/167203、WO 2017/153578、WO 2017/162611、WO2017/162605、WO 2017/174446、WO 2017/076895、WO 2017/076898、WO 2017/194632、WO2019/057757中公开的那些。
在本披露中使用的ATM抑制剂的其他实施例中,该ATM抑制剂是选自以下的化合物:
AZD1390:
7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮(WO 2017/046216:实例2)以及其氘化形式:
4,6-二氘-7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮,和
4-氘-7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
AZD0156
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮(WO 2015/170081:实例1);
M4076
8-(1,3-二甲基-1H-吡唑-4-基)-1-(3-氟-5-甲氧基-吡啶-4-基)-7-甲氧基-3-甲基-1,3-二氢咪唑并[4,5-c]喹啉-2-酮(WO 2016/155884);
M3541
3-氟-4-[7-甲氧基-3-甲基-8-(1-甲基-1H-吡唑-4-基)-2-氧代-2,3-二氢-1H-咪唑并[4,5-c]喹啉-1-基]苯甲腈(WO 2012/028233);
KU-55933
2-(4-吗啉基)-6-(1-噻蒽基)-4H-吡喃-4-酮(CAS号587871-26-9;WO2003070726A1);
KU-60019:
2-[(2R,6S)-2,6-二甲基-4-吗啉基]-N-{5-[6-(4-吗啉基)-4-氧代-4H-吡喃-2-基]-9H-噻吨-2-基}乙酰胺(CAS号925701-49-1);
KU-59403
3-(4-甲基-1-哌嗪基)-N-{6-[6-(4-吗啉基)-4-氧代-4H-吡喃-2-基]-2-噻蒽基}丙酰胺(WO 2005016919);
CP466722
2-(6,7-二甲氧基喹唑啉-4-基)-5-(2-吡啶基)-1,2,4-三唑-3-胺(CAS号1080622-86-1);
NVP-BEZ235
2-甲基-2-[4-[3-甲基-2-氧代-8-(3-喹啉基)咪唑并[4,5-c]喹啉-1-基]苯基]丙腈(达克利司(dactolisib);CAS号915019-65-7;WO 2006/122806);
6-[6-(甲氧基甲基)-3-吡啶基]-4-[[(1S)-1-四氢吡喃-4-基乙基]氨基]喹啉-3-甲酰胺
(Degorce等人,J Med Chem[药物化学杂志],2016,59,6281);
7-氟-6-[6-(甲氧基甲基)-3-吡啶基]-4-[[(1S)-1-(1-甲基吡唑-3-基)乙基]氨基]喹啉-3-甲酰胺(Degorce等人,J Med Chem[药物化学杂志],2016,59,6281);
6-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-N-甲基-4-[[(1S)-1-四氢吡喃-4-基乙基]氨基]噌啉-3-甲酰胺(Barlaam等人,Med Chem Lett[药物化学快报],2018,9,809-814);
N-甲基-4-(6-苯基咪唑并[1,2-a]吡嗪-3-基)苯甲酰胺(Valerie等人,Mol CanTher[分子癌症疗法],2018,1637);
1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮(WO 2019/057757);并且
2-(7-甲氧基-9H-噻吨-4-基)-6-吗啉-吡喃-4-酮(J.Med.Chem[药物化学杂志],2019,62,2988)。
根据本披露中使用的ATM抑制剂的优选实施例,该ATM抑制剂为由下式(I)表示的化合物:
其中:
R1是甲基;
R2是氢或甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟,
或其药学上可接受的盐。
在提及“R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环”的情况下,这意味着R1和R2基团经由碳-碳共价键连接以形成适当长度的未经取代的亚烷基链,从而形成对应的环。例如,当R1和R2连同它们所键合的氮原子一起形成吡咯烷基环时,R1和R2一起表示未经取代的亚丁基链,该亚丁基链在两个末端碳处附接至式(I)中的相关的氮原子。
式(I)中的可变基团的一些值如下。此类值可与本文定义的任何定义、权利要求或实施例结合使用以提供具有式(I)的化合物的另外实施例:
a)R1是甲基。
b)R2是甲基。
c)R2是氢。
d)R1是甲基并且R2是氢或甲基。
e)R1和R2均是甲基。
f)R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环。
g)R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基环。
h)R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成吡咯烷基环。
i)R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成哌啶基环。
j)R1和R2均是甲基。
k)R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环。
l)R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基环。
m)R1和R2连同它们所键合的氮原子一起形成吡咯烷基环。
n)R1和R2连同它们所键合的氮原子一起形成哌啶基环。
o)R3和R5均是氢。
p)R3和R5均是氟。
q)R3是氢。
r)R3是氟。
s)R4是氢。
t)R4是甲基。
u)R5是氢。
v)R5是氟。
在一个实施例中,该化合物由式(I),或其药学上可接受的盐表示,其中:
R1是甲基;
R2是氢或甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟。
在另一个实施例中,该化合物由式(I),或其药学上可接受的盐表示,其中:
R1是甲基;
R2是氢或甲基;
R3是氢;
R4是氢或甲基;并且
R5是氢。
在另一个实施例中,该化合物由式(I),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
7-氟-1-异丙基-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-异丙基-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[2-氟-6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[2-氟-6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-8-[2-氟-6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-8-[2-氟-6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-2-氟-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-2-氟-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3H-咪唑并[4,5-c]喹啉-2-酮;并且
7-氟-1-异丙基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-3H-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,由式(I)表示的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮,或其药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,根据式(I)的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮,或其药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,根据式(I)的化合物是8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮,或其药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,根据式(I)的化合物是8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-氧化哌啶-1-鎓-1-基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮,或其药学上可接受的盐。
在另一个实施例中,由式(I)表示的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-氧化哌啶-1-鎓-1-基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,根据式(I)的化合物是7-氟-1-异丙基-3-甲基-8-[6-[3-(1-氧化哌啶-1-鎓-1-基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
根据本披露中使用的ATM抑制剂的其他优选实施例,该ATM抑制剂为由下式(II)表示的化合物:
其中:
Q是环丁基或环戊基环,该环丁基或环戊基环各自任选地被一个羟基或甲氧基基团取代,或Q是氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环,该氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环各自任选地被一个甲基基团取代;
R1是甲基;
R2是氢或甲基;或R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟,
或其药学上可接受的盐。
术语“环丁基环”和“环戊基环”指代不包含杂原子的碳环。1-甲氧基环丁-3-基基团和3-甲氧基环丁-1-基基团具有相同的结构,如下所示。
顺式-1-甲氧基-环丁-3-基基团等同于顺式-3-甲氧基-环丁-1-基并且具有以下结构:
相同的惯例适用于其他环丁基基团,例如1-羟基环丁-3-基基团和3-羟基环丁-1-基基团。
以类似的方式,1-甲氧基环戊-3-基基团和3-甲氧基环戊-1-基基团具有相同的结构,如下所示。
术语“氧杂环丁烷基环”包括氧杂环丁烷-2-基和氧杂环丁烷-3-基基团,其结构在下文示出。
术语“四氢呋喃基环”包括四氢呋喃-2-基和四氢呋喃-3-基基团,其结构在下文示出。
术语“氧杂环己烷基环”包括氧杂环己烷-2-基、氧杂环己烷-3-基、和氧杂环己烷-4-基基团,其结构在下文示出。
在以上结构中,虚线指示相关基团的键合位置。
氧杂环己烷基环还可以称为四氢吡喃基环。类似地,氧杂环己烷-4-基环可以称为四氢吡喃-4-基环;氧杂环己烷-3-基环可以称作四氢吡喃-3-基环,并且氧杂环己烷-2-基环可以称作四氢吡喃-2-基环。
在提及“R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环”的情况下,这意味着R1和R2基团经由碳-碳共价键连接以形成适当长度的未经取代的亚烷基链,从而形成对应的环。
式(II)中的可变基团的一些值如下。此类值可与本文定义的任何定义、权利要求或实施例结合使用以提供具有式(II)的化合物的另外实施例:
a)Q是环丁基或环戊基环,该环丁基或环戊基环各自被一个羟基或甲氧基基团取代,或Q是氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环,该氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环各自任选地被一个甲基基团取代。
b)Q是环丁基环,该环丁基环被一个羟基或甲氧基基团取代,或Q是氧杂环丁烷基或氧杂环己烷基环,该氧杂环丁烷基或氧杂环己烷基环各自任选地被一个甲基基团取代。
c)Q是环丁基环,该环丁基环被一个羟基或甲氧基基团取代,或Q是氧杂环丁烷基或氧杂环己烷基环。
d)Q是环丁基、1-甲氧基-环丁-3-基、1-羟基-环丁-3-基、3-甲氧基环戊-1-基、氧杂环丁烷-3-基、四氢呋喃-3-基、氧杂环己烷-3-基、氧杂环己烷-4-基或4-甲基氧杂环己烷-4-基。
e)Q是1-甲氧基-环丁-3-基、1-羟基-环丁-3-基、3-甲氧基环戊-1-基、氧杂环丁烷-3-基、氧杂环己烷-3-基、氧杂环己烷-4-基或4-甲基氧杂环己烷-4-基。
f)Q是1-甲氧基-环丁-3-基、1-羟基-环丁-3-基或氧杂环己烷-4-基。
g)Q是顺式-1-甲氧基-环丁-3-基或氧杂环己烷-4-基。
h)Q是环丁基或环戊基环,该环丁基或环戊基环各自任选地被一个羟基或甲氧基基团取代。
i)Q是环丁基或环戊基环,该环丁基或环戊基环各自任选地被一个甲氧基基团取代。
j)Q是被一个羟基或甲氧基基团取代的环丁基环。
k)Q是环丁基、1-羟基-环丁-3-基或1-甲氧基-环丁-3-基。
l)Q是环丁基。
m)Q是被一个羟基或甲氧基基团取代的环戊基环。
n)Q是被一个甲氧基基团取代的环戊基环。
o)Q是3-甲氧基环戊-1-基。
p)Q是1-羟基-环丁-3-基或1-甲氧基-环丁-3-基。
q)Q是顺式-1-羟基-环丁-3-基或顺式-1-甲氧基-环丁-3-基。
r)Q是顺式-1-甲氧基-环丁-3-基。
s)Q是氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环,该氧杂环丁烷基、四氢呋喃基或氧杂环己烷基环各自任选地被一个甲基基团取代。
t)Q是氧杂环丁烷基或氧杂环己烷基环,该氧杂环丁烷基或氧杂环己烷基环各自任选地被一个甲基基团取代。
u)Q是氧杂环丁烷基或四氢呋喃基环。
v)Q是氧杂环丁烷基环。
w)Q是氧杂环丁烷-3-基。
x)Q是四氢呋喃基环。
y)Q是四氢呋喃-3-基。
z)Q是任选地被一个甲基基团取代的氧杂环己烷基环。
aa)Q是氧杂环己烷基环。
bb)Q是氧杂环己烷-4-基。
cc)R1是甲基。
dd)R2是甲基。
ee)R2是氢。
ff)R1是甲基并且R2是氢或甲基。
gg)R1和R2均是甲基;或R1和R2一起形成吡咯烷基环。
hh)R1和R2均是甲基。
ii)R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环。
jj)R1和R2一起形成氮杂环丁烷基环。
kk)R1和R2一起形成吡咯烷基环。
ll)R1和R2一起形成哌啶基环。
mm)R3和R5均是氢。
nn)R3是氢。
oo)R3是氟。
pp)R4是氢。
qq)R4是甲基。
rr)R5是氢。
ss)R5是氟。
在一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中:
Q是环丁基、1-甲氧基-环丁-3-基、1-羟基-环丁-3-基、3-甲氧基环戊-1-基、氧杂环丁烷-3-基、四氢呋喃-3-基、氧杂环己烷-3-基、氧杂环己烷-4-基或4-甲基氧杂环己烷-4-基;
R1是甲基;
R2是氢或甲基;或R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中:
Q是1-甲氧基-环丁-3-基、1-羟基-环丁-3-基、3-甲氧基环戊-1-基、氧杂环丁烷-3-基、氧杂环己烷-3-基、氧杂环己烷-4-基或4-甲基氧杂环己烷-4-基;
R1是甲基;
R2是氢或甲基;或R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中:
Q是1-甲氧基-环丁-3-基、1-羟基-环丁-3-基或3-甲氧基环戊-1-基;
R1是甲基;
R2是氢或甲基;或R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中:
Q是氧杂环丁烷-3-基、氧杂环己烷-3-基、氧杂环己烷-4-基或4-甲基氧杂环己烷-4-基;
R1是甲基;
R2是氢或甲基;或R1和R2一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中:
Q是顺式-1-甲氧基-环丁-3-基或氧杂环己烷-4-基;
R1是甲基;
R2是甲基或氢;
R3是氢;
R4是甲基或氢;并且
R5是氢。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
1-(3-顺式-羟基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮;
7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3R)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;并且
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[3-(甲基氨基)丙氧基]-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮
3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-(氧杂环丁烷-3-基)-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[2-氟-6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1R,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;并且
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1S,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
1-(3-顺式-羟基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3R)-氧杂环己烷-3-基]-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮;
7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3R)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;并且
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(4-甲基氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-7-氟-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)-3H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-羟基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
1-(3-顺式-羟基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
8-[6-(3-二甲基氨基丙氧基)-2-氟吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3R)-氧杂环己烷-3-基]-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3S)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
3-甲基-1-[(3R)-氧杂环己烷-3-基]-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-[(3R)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-8-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]-3H-咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-(氧杂环己烷-4-基)-8-[6-(3-哌啶-1-基丙氧基)吡啶-3-基]咪唑并[5,4-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮;
3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]-1-[(3S)-氧杂环己烷-3-基]咪唑并[5,4-c]喹啉-2-酮;并且
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-(3-甲基氨基丙氧基)吡啶-3-基]咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
7-氟-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[3-(甲基氨基)丙氧基]-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮
13-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3R)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-1-(氧杂环丁烷-3-基)-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(氮杂环丁烷-1-基)丙氧基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[2-氟-6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-8-[6-(3-吡咯烷-1-基丙氧基)-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1R,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;并且
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-[(1S,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,该化合物由式(II),或其药学上可接受的盐表示,其中该化合物选自由以下项组成的组:
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮;并且
8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基咪唑并[4,5-c]喹啉-2-酮。
在一个实施例中,提供了8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮,或其药学上可接受的盐。
在一个实施例中,提供了8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮。
在一个实施例中,提供了8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-1-(顺式-3-甲氧基环丁基)-3-甲基咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
在另一个实施例中,由式(II)表示的化合物是8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮,或其药学上可接受的盐。
在另一个实施例中,由式(II)表示的化合物是8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮。
在另一个实施例中,根据式(II)的化合物是8-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-3-甲基-1-(氧杂环己烷-4-基)咪唑并[5,4-c]喹啉-2-酮的药学上可接受的盐。
在另一个实施例中,由式(II)表示的化合物是1-(顺式-3-甲氧基环丁基)-3-甲基-8-{6-[3-(吡咯烷-1-基)丙氧基]吡啶-3-基}-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮、或其药学上可接受的盐。
在另一个实施例中,由式(II)表示的化合物是1-(顺式-3-甲氧基环丁基)-3-甲基-8-{6-[3-(吡咯烷-1-基)丙氧基]吡啶-3-基}-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮。
在另一个实施例中,根据式(II)的化合物是1-(顺式-3-甲氧基环丁基)-3-甲基-8-{6-[3-(吡咯烷-1-基)丙氧基]吡啶-3-基}-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮的药学上可接受的盐。
在优选的实施例中,本披露中使用的ATM抑制剂为具有式(I)的化合物,其中该化合物为由下式表示的AZD1390:
或其药学上可接受的盐。
在另一个优选的实施例中,本披露中使用的ATM抑制剂为具有式(II)的化合物,其中该化合物为由下式表示的AZD0156:
或其一种药学上可接受的盐。
ATM抑制剂,如具有式(I)和式(II)的化合物可以通过本领域已知的方法(如WO2017/046216和WO 2015/170081中公开的)来制备。
应当理解,具有式(I)和式(II)的化合物以及本文提及的其他ATM抑制剂可以涵盖具有一个或多个同位素取代的化合物。例如,H可以为任何同位素形式,包括1H、2H(D)、和3H(T);C可以为任何同位素形式,包括12C、13C、和14C;O可以为任何同位素形式,包括16O和18O;等等。
特别地,如WO 2018/167203中所述,7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮(AZD1390)可以作为4,6-二氘-7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮存在,其具有以下化学结构:
另选地,也如WO2018/167203中所述,AZD1390可以作为4-氘-7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮存在,其具有以下化学结构:
可根据本披露使用的ATM抑制剂的其他示例为:
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-异丙基-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(氮杂环丁烷-1-基)丙氧基]苯基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(氮杂环丁烷-1-基)丙氧基]苯基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-1-[反式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
1-[反式-3-甲氧基环戊基]-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-(反式-4-甲氧基环己基)-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(氮杂环丁烷-1-基)丙氧基]苯基]-7-氟-1-[反式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(顺式-4-甲氧基环己基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(顺式-4-甲氧基环己基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-4-甲氧基环己基)-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[反式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[反式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-[反式-3-甲氧基环己基]-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[顺式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[顺式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[顺式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-1-[顺式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-[顺式-3-甲氧基环己基]-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
1-[顺式-3-甲氧基环己基]-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
1-(反式-3-甲氧基环丁基)-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-(3-(顺式)甲氧基环丁基)-3-甲基-8-[4-(2-吡咯烷-1-基乙氧基)苯基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-(2-吡咯烷-1-基乙氧基)苯基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[4-(2-吡咯烷-1-基乙氧基)苯基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[4-[2-(二甲基氨基)乙氧基]苯基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-1-(3-(顺式)甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[4-[2-(二甲基氨基)乙氧基]苯基]-7-氟-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3S)-四氢呋喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(反式-4-甲氧基环己基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3S)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-1-[反式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-1-(反式-4-甲氧基环己基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-7-氟-1-[反式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-[反式-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
1-环丁基-8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-3-甲基-1-(氧杂环丁烷-3-基)咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-7-氟-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-7-氟-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)-1-哌啶基]-3-吡啶基]-7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(顺式-4-甲氧基环己基)-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-[(顺式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[顺式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-1-[顺式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[反式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-[反式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)氮杂环丁烷-1-基]-3-吡啶基]-1-[反式-3-甲氧基环己基]-3-甲基-咪唑并[4,5-c]喹啉-2-酮;
7-氟-1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-[4-(甲基氨基)-1-哌啶基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[4-(甲基氨基)-1-哌啶基]-3-吡啶基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
3-甲基-8-[6-[4-(甲基氨基)-1-哌啶基]-3-吡啶基]-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]喹啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-[4-(甲基氨基)-1-哌啶基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮;并且
3-甲基-8-[6-[4-(甲基氨基)-1-哌啶基]-3-吡啶基]-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-2-酮。
(R)-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(S)-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(S)-7-氟-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(R)-7-氟-8-(2-氟-6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(S)-7-氟-8-(2-氟-6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(R)-8-(2-氟-6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(S)-8-(2-氟-6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
(R)-7-氟-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1-(四氢-2H-吡喃-3-基)-1H-咪唑并[4,5-c]喹啉-2(3H)-酮;
外消旋-1-(3,3-二甲基四氢-2H-吡喃-4-基)-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(R)-1-(3,3-二甲基四氢-2H-吡喃-4-基)-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(S)-1-(3,3-二甲基四氢-2H-吡喃-4-基)-8-(6-(甲氧基甲基)吡啶-3-基)-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(S)-8-(6-(甲氧基甲基)吡啶-3-基)-1-(四氢-2H-吡喃-3-基)-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1R)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-6-[2-氟-6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[2-氟-6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[2-氟-6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1R)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1R)-1-(1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-4-{[(1S)-1-(4-氟-1-甲基-1H-吡唑-3-基)乙基]氨基}-6-(6-[甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
7-氟-4-{[(1R)-1-(4-氟-1-甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(4-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1R)-1-(4-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
7-氟-6-[6-(羟甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1R)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-7-氟-6-[6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
6-[2-氟-6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[2-氟-6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1R)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[2-氟-6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
6-[6-(羟甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
4-{[(1S)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1R)-1-(1,4-二甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(羟甲基)吡啶-3-基]喹啉-3-甲酰胺;
4-{[(1S)-1-(4-氟-1-甲基-1H-吡唑-3-基)乙基]氨基}-6-[6-(甲氧基甲基)吡啶-3-基]喹啉-3-甲酰胺;
6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1S)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
6-[6-(甲氧基甲基)吡啶-3-基]-4-{[(1R)-1-(1-甲基-1H-吡唑-3-基)乙基]氨基}喹啉-3-甲酰胺;
6-[2-氟-6-(甲氧基甲基)-3-吡啶基]-4-[[(1S)-1-(4-氟-1-甲基-吡唑-3-基)乙基]氨基]喹啉-3-甲酰胺;
6-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-N-甲基-4-[[(1S)-1-(氧杂环己烷-4-基)乙基]氨基]噌啉-3-甲酰胺;
6-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-4-[[(1S)-1-(氧杂环己烷-4-基)乙基]氨基]噌啉-3-甲酰胺;
4-[[(1S)-1-(氧杂环己烷-4-基)乙基]氨基]-6-[6-(3-吡咯烷-1-基丙氧基)吡啶-3-基]噌啉-3-甲酰胺;
6-[6-(3-甲基氨基丙氧基)吡啶-3-基]-4-[[(1S)-1-(氧杂环己烷-4-基)乙基]氨基]噌啉-3-甲酰胺;
N-甲基-6-[6-(3-甲基氨基丙氧基)吡啶-3-基]-4-[[(1S)-1-(氧杂环己烷-4-基)乙基]氨基]噌啉-3-甲酰胺;
6-[6-(3-二甲基氨基丙氧基)吡啶-3-基]-N-甲基-4-[[(1R)-1-(氧杂环己烷-4-基)乙基]氨基]噌啉-3-甲酰胺;
N,N-二甲基-3-[[5-(3-甲基-2-氧代-1-四氢吡喃-4-基-咪唑并[4,5-c]喹啉-8-基)-2-吡啶基]氧基]丙烷-1-胺氧化物;
8-(6-(3-(4-氟哌啶-1-基)丙氧基)吡啶-3-基)-1-异丙基-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(S)-8-(6-(3-(3-氟吡咯烷-1-基)丙氧基)吡啶-3-基)-1-异丙基-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
(R)-8-(6-(3-(3-氟吡咯烷-1-基)丙氧基)吡啶-3-基)-1-异丙基-3-甲基-1,3-二氢-2H-咪唑并[4,5-c]喹啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3S)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]-1-四氢吡喃-4-基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3-甲基-8-[4-(3-吡咯烷-1-基丙氧基)苯基]咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3-甲基-8-(4-(3-(哌啶-1-基)丙氧基)苯基)-1,3-二氢-2H-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(4-氟-1-哌啶基)丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-[(3R)-3-氟吡咯烷-1-基]丙氧基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3-甲基-8-[2-甲基-6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
1-(反式-3-甲氧基环丁基)-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(4-氟-1-哌啶基)丙氧基]-3-吡啶基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(4-氟-1-哌啶基)丙氧基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-[(3R)-3-氟吡咯烷-1-基]丙氧基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(4-氟-1-哌啶基)丙氧基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-3-甲基-1-(1-甲基环丙基)咪唑并[4,5-c]噌啉-2-酮;
3-甲基-1-(1-甲基环丙基)-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(4-氟-1-哌啶基)丙氧基]-3-吡啶基]-3-甲基-1-(1-甲基环丙基)咪唑并[4,5-c]噌啉-2-酮;
3-甲基-1-(1-甲基环丙基)-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-[(3S)-3-氟吡咯烷-1-基]丙氧基]-3-吡啶基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
1-(顺式-3-甲氧基环丁基)-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-[(3S)-3-氟吡咯烷-1-基]丙氧基]-3-吡啶基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-[(4S)-3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-[(4R)-3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮
1-[3,3-二甲基四氢吡喃-4-基]-3-甲基-8-{4-[3-(1-哌啶基)丙氧基]苯基}-1,3-二氢-2H-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(4S)-3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-[(4R)-3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
7-氟-1-异丙基-3-甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
8-[4-[3-(二甲基氨基)丙氧基]苯基]-1-异丙基-3,7-二甲基-咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3,7-二甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-异丙基-3,7-二甲基-咪唑并[4,5-c]噌啉-2-酮;
1-异丙基-3,7-二甲基-8-[4-[3-(1-哌啶基)丙氧基]苯基]咪唑并[4,5-c]噌啉-2-酮;
3-(二氟甲基)-8-[6-[3-(二甲基氨基)丙氧基]-3-吡啶基]-1-异丙基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-[3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(反式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-3-甲基-1-四氢吡喃-4-基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[4-(二甲基氨基)-1-哌啶基]-3-吡啶基]-1-(顺式-3-甲氧基环丁基)-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-1-[3,3-二甲基四氢吡喃-4-基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-1-[(1R,3R)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-1-[(1S,3S)-3-甲氧基环戊基]-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-3-甲基-1-[(3R)-四氢吡喃-3-基]咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-7-氟-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[6-[(3R)-3-(二甲基氨基)吡咯烷-1-基]-3-吡啶基]-1-异丙基-3,7-二甲基-咪唑并[4,5-c]噌啉-2-酮;
8-[4-[4-(二甲基氨基)-1-哌啶基]苯基]-1-异丙基-3,7-二甲基-咪唑并[4,5-c]噌啉-2-酮;并且
8-[6-[3-(二甲基氨基)丙氧基]-2-氟-3-吡啶基]-1-异丙基-3-甲基-咪唑并[4,5-c]噌啉-2-酮。
5.抗体-药物缀合物和ATM抑制剂的组合
在本披露的第一个组合实施例中,与ATM抑制剂组合的抗HER2抗体-药物缀合物为其中由下式表示的药物-接头经由硫醚键与抗HER2抗体缀合的抗体-药物缀合物,
其中A表示与抗体的连接位置。
在另一个组合实施例中,将如上文针对第一个组合实施例所定义的抗HER2抗体-药物缀合物与ATM抑制剂组合,该ATM抑制剂为由下式(I)表示的化合物:
其中:
R1是甲基;
R2是氢或甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是氢或甲基;并且
R5是氢或氟,
或其药学上可接受的盐;
在另一个组合实施例中,将如上文定义的抗HER2抗体-药物缀合物与ATM抑制剂组合,该ATM抑制剂为如上文定义的由式(I)表示的化合物,其中,在式(I)中,R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中,在式(I)中,R1和R2与它们键合的氮原子一起形成氮杂环丁基、吡咯烷基或哌啶基环;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中,在式(I)中,R3是氢;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中,在式(I)中,R4是甲基;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中,在式(I)中,R5是氟;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中,在式(I)中:
R1是甲基;
R2是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是甲基;并且
R5是氢或氟;
在另一个组合实施例中,将如上文所定义的抗HER2抗体-药物缀合物与如上文所定义的ATM抑制剂组合,其中ATM抑制剂为由下式表示的AZD1390:
或其药学上可接受的盐。
在上述每个组合实施例的实施例中,抗HER2抗体包含重链和轻链,该重链包含:由SEQ ID NO:3表示的氨基酸序列组成的CDRH1、由SEQ ID NO:4表示的氨基酸序列组成的CDRH2和由SEQ ID NO:5表示的氨基酸序列组成的CDRH3,该轻链包含:由SEQ ID NO:6表示的氨基酸序列组成的CDRL1、由SEQ ID NO:7的氨基酸残基1至3所组成的氨基酸序列组成的CDRL2和由SEQ ID NO:8表示的氨基酸序列组成的CDRL3。在上述每个组合实施例的另一个实施例中,抗HER2抗体包含重链和轻链,该重链包含由SEQ ID NO:9表示的氨基酸序列组成的重链可变区,该轻链包含由SEQ ID NO:10表示的氨基酸序列组成的轻链可变区。在上述每个组合实施例的另一个实施例中,抗HER2抗体包含重链和轻链,该重链由SEQ ID NO:1表示的氨基酸序列组成,该轻链由SEQ ID NO:2表示的氨基酸序列组成。在上述每个组合实施例的另一个实施例中,抗HER2抗体包含重链和轻链,该重链由SEQ ID NO:11表示的氨基酸序列组成,该轻链由SEQ ID NO:2表示的氨基酸序列组成。
在本披露的一个特别优选的组合实施例中,抗HER2抗体-药物缀合物为德卢替康-曲妥珠单抗(DS-8201),并且ATM抑制剂为由下式表示的化合物:
6.治疗组合用途和方法
下文描述了一种药物产品以及治疗用途和方法,其中将根据本披露的抗HER2抗体-药物缀合物和ATM抑制剂组合施用。
本披露的药物产品和治疗用途和方法的特征在于将抗HER2抗体-药物缀合物和ATM抑制剂作为活性组分单独地包含在不同的配制剂中,并同时或在不同的时间施用,或者其特征在于将抗体-药物缀合物和ATM抑制剂作为活性组分包含在单一配制剂中并施用。
在本披露的药物产品和治疗方法中,本披露中使用的单一ATM抑制剂可以与抗HER2抗体-药物缀合物组合施用,或者两种或更多种不同的ATM抑制剂可以与抗体-药物缀合物组合施用。
本披露的药物产品和治疗方法可用于治疗癌症,并且可优选用于治疗至少一种选自以下组成的组中的癌症:乳腺癌(包括三阴性乳腺癌和腔内乳腺癌)、胃癌(也称为胃腺癌)、结直肠癌(又称结直肠癌,并且包括结肠癌和直肠癌)、肺癌(包括小细胞肺癌和非小细胞肺癌)、食管癌、头颈癌(包括唾液腺癌和咽喉癌)、食管胃连接部腺癌、胆道癌(包括胆管癌)、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤,并且可以更优选地用于治疗至少一种选自以下组成的组中的癌症:乳腺癌、胃癌、结直肠癌、肺癌(优选非小细胞肺癌)、胰腺癌、卵巢癌、前列腺癌和肾癌。
HER2肿瘤标记物的存在或不存在可以通过以下确定:例如,通过从癌症患者收集肿瘤组织以制备福尔马林固定的石蜡包埋的(FFPE)标本,并对该标本进行基因产物(蛋白质)测试,例如,用免疫组织化学(IHC)法、流式细胞仪或蛋白质印迹法,或进行基因转录测试,例如,用原位杂交(ISH)法、定量PCR法(q-PCR)或微阵列分析,或者通过从癌症患者收集无细胞循环肿瘤DNA(ctDNA)并用如下一代测序(NGS)的方法对ctDNA进行测试。
本披露的药物产品和治疗方法可用于癌症,该癌症可以是HER2过表达癌症(高或中度)或者可以是HER2低表达癌症。
在本披露中,术语“过表达HER2的癌症”没有特别限制,只要它被本领域技术人员认为是过表达HER2的癌症。过表达HER2的癌症的优选实例可包括在IHC法中HER2表达评分为3+的癌症,和在IHC法中HER2表达评分为2+并在原位杂交法(ISH)中HER2表达被确定为阳性的癌症。本披露的原位杂交方法包括荧光原位杂交方法(FISH)和双色原位杂交方法(DISH)。
在本披露中,术语“低表达HER2的癌症”没有特别限制,只要它被本领域技术人员认为是低表达HER2的癌症。低表达HER2的癌症的优选实例可包括在IHC法中HER2表达评分为2+且在原位杂交法中HER2表达被确定为阴性的癌症,以及在IHC法中HER2表达评分为1+的癌症。
通过IHC法对HER2表达程度评分的方法,或通过原位杂交法确定HER2表达为阳性或阴性的方法没有特别限制,只要其是本领域技术人员所认可的。该方法的实例可以包括在第4版乳腺癌HER2检测指南(由日本病理学委员会(Japanese Pathology Board)开发,用于HER2在乳腺癌中的最佳应用)中描述的方法。
该癌症(特别是关于乳腺癌的治疗)可以为过表达HER2(高或中等)或低表达的乳腺癌,或三阴性乳腺癌,和/或可以具有IHC 3+、IHC 2+、IHC 1+或IHC>0且<1+的HER2状态评分。
本披露的药物产品和治疗方法可优选用于哺乳动物,但更优选用于人类。
本披露的药物产品和治疗方法的抗肿瘤效果可以通过以下来证实:将癌细胞移植到受试动物以制备模型并通过应用本披露的药物产品和治疗方法测量肿瘤体积的减小或生命延长效果。然后,可以通过比较单独施用本披露中使用的抗体-药物缀合物和单独施用ATM抑制剂的抗肿瘤效果,确认本披露中使用的抗体-药物缀合物和ATM抑制剂的组合使用的效果。
本披露的药物产品和治疗方法的抗肿瘤效果可以在临床试验中使用实体瘤反应评估标准(RECIST)、WHO评估方法、Macdonald评估方法、体重测量和其他方法中的任何一种评估方法来确认,并且可以基于完全响应(CR)、部分响应(PR);疾病进展(PD)、客观响应率(ORR)、响应持续时间(DoR)、无进展存活(PFS)、总存活(OS)等的指数来确定。
通过使用上述方法,可以证实本披露的药物产品和治疗方法在抗肿瘤效果上优于现有的用于癌症治疗的药物产品和治疗方法。
本披露的药物产品和治疗方法可以延迟癌细胞的发展,抑制其生长,并进一步杀死癌细胞。这些作用可以使癌症患者摆脱由癌症引起的症状,或者改善癌症患者的生活质量(QOL),并通过维持癌症患者的生命而达到治疗效果。即使本披露的药物产品和治疗方法不能实现杀死癌细胞,它们也可以通过抑制或控制癌细胞的生长来实现癌症患者的更高QOL,同时实现更长期的存活。
可以预期本发明的药物产品通过作为全身疗法应用于患者以及另外通过局部应用于癌组织来发挥治疗效果。
本披露的药物产品可以含有至少一种药学上合适的成分来施用。可根据本披露中使用的抗体-药物缀合物和ATM抑制剂的剂量、施用浓度等,从本领域中通常使用的配制剂添加剂等中适当地选择和应用药学上合适的成分。本披露中使用的抗HER2抗体-药物缀合物可以例如作为包含缓冲剂如组氨酸缓冲剂、媒介物如蔗糖和海藻糖以及表面活性剂如聚山梨醇酯80和20的药物产品进行施用。本披露中使用的包含抗体-药物缀合物的药物产品可以优选用作注射剂,可以更优选用作含水注射剂或冻干注射剂,并且可以甚至更优选用作冻干注射剂。
在本披露中使用的含有抗HER2抗体-药物缀合物的药物产品是含水注射剂的情况下,该含水注射剂可以优选用合适的稀释剂稀释,然后作为静脉输注施用。稀释剂的实例可以包括葡萄糖溶液和生理盐水,可以优选例举葡萄糖溶液,并且可以更优选例举5%的葡萄糖溶液。
在本披露的药物产品是冻干注射剂的情况下,预先溶解在注射用水中的所需量的冻干注射剂可以优选用合适的稀释剂稀释,然后作为静脉输注施用。稀释剂的实例可以包括葡萄糖溶液和生理盐水,可以优选例举葡萄糖溶液,并且可以更优选例举5%的葡萄糖溶液。
适用于施用本披露的药物产品的施用途径的实例可包括静脉内、皮内、皮下、肌内和腹膜内途径,并且优选静脉内途径。
本披露中使用的抗HER2抗体-药物缀合物可以以1天至180天的间隔施用于人,可以优选以一周、两周、三周或四周的间隔施用,并且可以更优选以三周的间隔施用。本披露中使用的抗HER2抗体-药物缀合物可以以每次施用约0.001mg/kg至100mg/kg的剂量施用,并且可以优选以每次施用0.8mg/kg至12.4mg/kg的剂量施用。例如,抗HER2抗体-药物缀合物可以以0.8mg/kg、1.6mg/kg、3.2mg/kg、5.4mg/kg、6.4mg/kg、7.4mg/kg或8mg/kg的剂量每三周施用一次,并且可以优选以5.4mg/kg或6.4mg/kg的剂量每三周施用一次。
具有式(I)或(II)的化合物通常将以范围为2.5-5000mg/m2动物体表面积、或约0.05-100mg/kg内的单位剂量施用于温血动物,并且这通常提供治疗有效剂量。单位剂型如片剂或胶囊剂通常将含有例如0.1-250mg的活性成分。日剂量将必然随所治疗的宿主、具体的施用途径、共施用的任何治疗、以及正在治疗的疾病的严重性而变化。因此,治疗任何具体患者的执业医生可以确定最佳剂量。
药物产品可处于适合于以下的形式:口服使用(例如作为片剂、锭剂、硬或软胶囊、水性或油性悬浮液、乳剂、可分散粉剂或颗粒剂、糖浆剂或酏剂),局部使用(例如作为乳膏、软膏剂、凝胶剂、或者水性或油性溶液或悬浮液),通过吸入施用(例如作为细碎粉末或液体气雾剂),通过吹入施用(例如作为细碎粉末),或肠胃外施用(例如作为用于静脉内、皮下、肌内或肌内给药的无菌水性或油性溶液),或作为用于直肠给药的栓剂。组合物可以通过本领域熟知的常规程序来获得。旨在用于口服使用的组合物可含有另外的组分,例如,一种或多种着色剂、甜味剂、调味剂和/或防腐剂。
特定疾病状态的治疗性治疗所需的剂量大小将必然改变,这取决于所治疗的受试者、施用途径和正在治疗的疾病的严重性。具有式(I)或(II)的化合物通常以范围为2.5-5000mg/m2动物体表面积、或约0.05-100mg/kg内的单位剂量施用于温血动物,并且这通常提供治疗有效剂量。单位剂型如片剂或胶囊剂通常将含有例如0.1-250mg的活性成分。
本披露的药物产品和治疗方法可用作与外科手术结合的辅助化疗。本披露的药物产品可以在外科手术之前为了减小肿瘤大小的目的而施用(称为术前辅助化疗或新辅助治疗),或者可以在外科手术之后为了防止肿瘤复发的目的而施用(称为术后辅助化疗或辅助治疗)。
[实例]
鉴于下面示出的实例具体描述本披露。然而,本披露不限于这些。此外,决不能以限制的方式对其进行解释。
实例1:抗体-药物缀合物的生产
根据WO 2015/115091中描述的生产方法,并使用抗HER2抗体(包含由SEQ ID NO:11表示的氨基酸序列(SEQ ID NO:1的氨基酸残基1至449)组成的重链和由SEQ ID NO:2的所有氨基酸残基1至214所组成的氨基酸序列组成的轻链的抗体),生产其中由下式表示的药物-接头经由硫醚键与抗HER2抗体缀合的抗HER2抗体-药物缀合物(DS-8201:德卢替康-曲妥珠单抗),
其中A表示与抗体的连接位置。抗体-药物缀合物的DAR为7.7或7.8。
实例2:ATM抑制剂的生产
根据WO 2017/046216)中描述的生产方法制备具有式(I)的ATM抑制剂。具体地,7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮:
可根据WO 2017/046216的实例2进行制备。
实例3:抗肿瘤测试(1)
抗体-药物缀合物DS-8201(德卢替康-曲妥珠单抗)与ATM抑制剂AZD1390(7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮)的组合
方法:
运行高通量组合筛选,其中三种具有不同HER2表达的乳腺癌细胞系和一种具有高HER2表达的胃细胞系(表1)用DS-8201和AZD1390(ATM抑制剂)的组合进行治疗。
表1
| 细胞系 | HER2表达 | 癌症类型 |
| KPL-4 | 高 | 乳腺癌(HER2+) |
| NCI-N87 | 高 | 胃癌 |
| MDA-MB-468 | 低 | 乳腺癌(TNB) |
| T47D | 低 | 乳腺癌(ER+) |
屏幕上的读数是7天细胞滴度-glo细胞活力测定,以每个组合的6x 6剂量响应矩阵进行(DS-8201的5点对数连续稀释,以及伴侣的半对数连续稀释)。
此外,曲妥珠单抗和依喜替康(DNA拓扑异构酶I抑制剂)也与AZD1390平行筛选。
基于ΔEmax和HSA协同评分的组合来评估组合活性。
结果:
结果显示在图12A和12B以及表2中。
图12A示出测量的细胞活力信号的矩阵。X轴代表药物A(DS-8201),并且Y轴代表药物B(AZD1390)。方框中的值代表在第7天用药物A+B处理的细胞与DMSO对照的比率。将所有值标准化为第0天的细胞活力值。0和100之间的值代表%生长抑制,并且高于100的值代表细胞死亡。
图12B示出HSA超额矩阵。框中的值代表由HSA(最高单一药剂)模型计算的超额值。
下表2显示了HSA协同评分和Loewe加性评分:
表2
如果两种化合物通过相同的机制作用于相同的分子靶标,则Loewe剂量加性预测预期的响应。它基于化合物之间零相互作用的假设计算加性,并且它独立于剂量-响应关系的性质。
HSA(最高单一药剂)[Berenbaum 1989]量化了两种单一化合物在其相应浓度下的较高效果。将组合效果与组合中所用浓度的每种单一药剂的效果进行比较。超过最高单一药剂效果表明协同作用。HSA不要求化合物影响相同的靶标。
超额矩阵:对于浓度矩阵中的每个孔,将测量值或拟合值与每个浓度对的预测非协同值进行比较。预测值由选择的模型决定。预测值和观察值之间的差异可能表明协同作用或拮抗作用,并显示在超额矩阵中。超额矩阵值通过组合评分超额量和协同评分进行总结。
如图12A和12B以及表2所示,AZD1390(AZ13791971)与DS-8201的组合在EMAX(0.3μM AZD1390和10μg/ml(0.064μM)DS-8201)下在HER2+细胞系KPL4和NCI-N87中显示出协同活性和细胞死亡增加。在更低的浓度下也观察到组合活性。单一药剂AZD1390在选定的浓度范围内没有活性。此外,AZD1390和DS-8201在HER2低细胞系MDA-MB-468和T47D中在DS-8201Emax下显示出组合活性。
结果表明,使用AZD1390的ATM抑制增强了DS-8201在体外高和低HER2表达细胞系两者中的抗肿瘤功效。AZD1390在HER2高细胞系中显示出协同组合活性和细胞死亡增加。在HER2低的癌细胞系中也观察到有益的组合活性。
实例4:抗肿瘤测试(2)
抗体-药物缀合物DS-8201(德卢替康-曲妥珠单抗)与ATM抑制剂AZD1390(7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮)的组合
DS-8201或依喜替康甲磺酸盐在具有不同HER2表达水平的癌细胞系中单独进行测试并与AZD1390组合进行测试。
方法:
将在各自条件下生长的细胞以最佳密度铺在96孔板中,以允许在测定期间进行线性增殖(4天至8天;治疗持续时间取决于每个细胞系的生长率)。铺板后,立即给细胞施用所示化合物,总体积为200μL/孔,并置于培养箱中。以每个组合6x 8的浓度响应矩阵进行组合。在终点,将细胞在室温下在2% PFA中固定20分钟。为了获得处理开始时的细胞数量,每个实验使用一个额外的板,并在细胞附着后固定。然后将细胞在含0.5% Triton-X100的PBS中渗透10分钟。PBS洗涤后,将细胞在RT下在含5% FBS的PBS中封闭1h,并在4℃下与5%FBS+0.05%triton中的一级抗体一起孵育过夜。在PBS中洗涤3次后,细胞在室温下与具有Hoechst33258的5% FBS+0.05%triton中的二级抗体一起孵育1h。在PBS中洗涤3次后,用Cellinsight仪器以10x物镜和9个视野/孔扫描细胞。基于细胞核Hoechst染色和研究的其他生物标记物的细胞核强度,使用Columbus针对细胞计数对图像进行分析。与溶剂对照相比,总细胞数/孔用于计算每个孔中的相对生长。为了计算协同评分,使用Combenefit软件分析生长抑制数据(Di Veroli GY等人,Bioinformatics[生物信息学]2016,32(18),2866-8)。也相对于溶剂对照表达IF生物标记物的核强度总和的平均值/孔。
结果:
结果示于图13至15以及表3和表4中。
下表3示出DS-8201、依喜替康和AZD1390对体外研究中使用的细胞系的单一治疗活性:
表3
*Nd:未确定
图13示出在HER2高KPL4细胞系中DS-8201和AZD1390的组合的协同矩阵。
在图13中,(A)示出相对总细胞(核)计数占DMSO媒介物对照的百分比(对照=100%,无剩余细胞=0%;暗区是总细胞计数非常低的区域),并且(B)示出针对Loewe、Bliss和HSA评分的计算的协同矩阵(更高=更多协同作用;暗区是具有高组合协同作用的区域)。
下表4示出DS-8201与AZD1390组合的协同评分(Loewe、Bliss和HSA)的总和:
表4
图14示出针对DS-8201与AZD1390的组合,在(A)HER2高KPL4细胞系和(B)HER2阴性MDA-MB-468细胞系中治疗4至8天后剩余的总细胞与时间零相比的倍数变化。正值指示生长(倍数增加),零值指示细胞抑制,并且负值表示净细胞损失和细胞死亡的替代物。方框区域显示了与单一疗法相比,组合的细胞抑制或细胞损失的区域。
图15示出在(A)HER2高KPL4细胞系或(B)HER2低MDA-MB-468细胞系中DS-8201与AZD1390组合的ATM依赖性KAP1 pSer824信号传导、DNA双链断裂损伤(γH2AX)生物标志物的诱导或细胞数百分比(相对于溶剂对照)。方框区域显示了与单一疗法相比,组合的DNA损害响应、DNA损害或细胞损失的诱导增加的区域。
根据上文结果,在高HER2 KPL4乳腺癌细胞系模型中,在临床相关浓度的DS-8201(和依喜替康)与ATM抑制剂AZD1390组合时,观察到协同活性和细胞死亡。此外,DS-8201(和依喜替康)以浓度依赖的方式诱导ATM(KAP1 pSer824)活化和DNA链断裂(γH2AX)的生物标志物,其与AZD1390组合被进一步增强。在HER2阴性MDA-MB-468乳腺癌细胞系中,在组合DS-8201中观察到弱组合活性和差的DNA损害响应途径活化,而依喜替康仍显示组合活性,支持DS-8201的HER2和肿瘤靶向依赖性,但无依喜替康不是如此。这些数据显示当与依赖于肿瘤HER2表达的ATM抑制剂AZD1390组合时,DS-8201活性的强力增强,并且因此与无拓扑异构酶I抑制剂相比,可以提供增加的治疗指数。
实例5:抗肿瘤测试(3)-体内
抗体-药物缀合物DS-8201(德卢替康-曲妥珠单抗)与ATM抑制剂AZD1390(7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮)的组合
方法:
使用5周龄至8周龄的雌性裸鼠(Charles River[查尔斯河]),在进入研究前适应环境7天。将1x107个NCI-N87肿瘤细胞(基质胶中1:1)皮下植入雌性裸小鼠的侧腹。当肿瘤达到约150mm3时,将大小相似的肿瘤随机分配到治疗组,如表5所示:
表5
根据给药当天的个体体重计算每只动物的化合物剂量。在DS-8201给药后24小时施用AZD1390。除非另有说明,否则给药持续时间为28天(1个周期)。
3mg/kg和1mg/kg DS-8201的配制剂
在给药当天通过在25mM组氨酸缓冲液、9%蔗糖(pH5.5)中将DS-8201储备液(20.1mg/ml)稀释至0.6mg/ml,并分别将3mg/kg和1mg/kg给药溶液稀释至0.2mg/ml来制备DS-8201的给药溶液。在以5ml/kg的给药体积经由IV注射进行施用之前,使用移液管将每种给药溶液充分混合。
10mg/kg AZD1390的配制剂
为了配制10mg/kg给药溶液,制备1mg/ml AZD1390的最终浓度,这导致PO给药的给药体积为10ml/kg。最初在含有0.1%吐温80的0.5% HPMC(溶媒)中制备5mg/ml给药溶液。将化合物搅拌过夜,然后在给药当天进一步稀释至1mg/ml给药溶液。将给药溶液避光并在室温下保持至多4天,并不断混合。10mg/kg AZD1390的最终给药基质是白色悬浮液。
测量
通过比较对照组和治疗组的肿瘤体积的几何平均变化来评估从研究开始到肿瘤测量当天的肿瘤生长抑制(TGI)。肿瘤消退计算为肿瘤体积相对于基线(治疗前)值的减少百分比:
%消退=(1–RTV)*100%,
其中RTV=几何平均相对肿瘤体积。
在最终测量当天,使用(log(相对肿瘤体积)=log(最终体积/开始体积))的单尾t检验来评估统计显著性,与溶媒对照进行比较。
结果:
用DS-8201和/或AZD1390治疗的肿瘤体积如图16所示。数据表示治疗组的肿瘤体积随时间的变化。图16中的虚线表示给药周期的结束。有关完整剂量和时间表信息,参考上表5。显示的值是均值±SEM;对于媒介物治疗的小鼠,最初n=10,对于所有其他治疗组,n=8。
在NCI-N87异种移植物中,单独使用DS-8201或AZD1390或者使用DS-8201与AZD1390的组合治疗后的TGI最佳响应(最大TGI/消退)如表6所示:表6
在治疗后第33天,用3mg/kg DS-8201的单一疗法显示84%的最大肿瘤生长抑制(TGI)。在1mg/kg时,DS-8201在处理后第37天显示22%的最大TGI值。在治疗后第40天,AZD1390单一疗法达到了37%的最大TGI。与溶媒治疗的对照小鼠相比,以1mg/kg DS-8201的组合治疗导致NCI-N87肿瘤负荷的显著降低,其中在治疗后40天,观察到DS-8201 1mg/kg+AZD1390具有82%的最大TGI的显著效果。
使用更高的DS-8201 3mg/kg与AZD1390的组合治疗实现了肿瘤消退,其中在治疗后第33天最大TGI为143%,并且显示出比任一单一疗法更好的响应。
所有治疗组均耐受,并且在媒介物、单一疗法或组合组之间未观察到平均体重的一致差异。
实例6:ATM信号传导的抑制
DS-8201与ATM抑制剂AZD1390的组合
方法
胃癌NCI-N87和乳腺癌KPL4细胞系在补充有10% FCS的RPMI 1640中于37℃、含5% CO2的湿润培养箱中培养。将细胞以最佳密度铺在6孔板中,以允许在测定期间进行线性增殖。铺板后两天,给细胞施用指定的化合物(单独的AZD1390,或与DS-8201或依喜替康甲磺酸盐组合)并放回培养箱中。给药后7h、24h或48h,通过在含有蛋白酶和磷酸酶抑制剂的50mM Tris-HCl pH 7.5、2% SDS中裂解获得全细胞提取物。裂解物在95℃下煮沸5分钟。使用Nanodrop在240nm处测量蛋白质浓度,并将50μg裂解物加载于4-12% Bis Tris凝胶中。使用iblot2转移蛋白质。一级抗体(见表7)于4℃在3%牛奶TBS-吐温0.05%中孵育过夜,并且HRP缀合的二级抗体在室温下孵育1小时。使用G-box对印迹进行成像。
表7
结果:
结果以抗体印迹图像的形式显示在图17中,该图像是在(A)NCI-N87(胃癌)和(B)KPL4(乳腺癌)细胞系中单独使用AZD1390或与DS-8201(或依喜替康甲磺酸盐)组合使用而获得的。
在Her2高NCI-N87和KPL4中,暴露于30μg/mL DS-8201或弹头(依喜替康甲磺酸盐)诱导ATM途径的活化,如pATM-S1981、pChk2-T68和pKap1-S824的增加所示。与100nMAZD1390结合抑制pATM、pChk2和pKAP1的活化,同时加剧DNA损伤(pRPA,gH2AX),最终导致细胞死亡增加(cCasp3)。
因此,显示AZD1390抑制DS-8201诱导的ATM信号传导。
实例7:抗肿瘤测试(4)
抗体-药物缀合物DS-8201(德卢替康-曲妥珠单抗)与ATM抑制剂AZD1390(7-氟-1-异丙基-3-甲基-8-[6-[3-(1-哌啶基)丙氧基]-3-吡啶基]咪唑并[4,5-c]喹啉-2-酮)的组合
方法:
进行高通量组合筛选,其中用DS-8201和AZD1390的组合治疗具有高HER2表达的肺癌细胞系(表8)。
表8
| 细胞系 | HER2表达 | 癌症类型 |
| NCI-H2170 | 高 | 鳞状非小细胞肺癌 |
屏幕的读数是7天细胞滴度-glo细胞活力测定,以每个组合的6x6剂量响应矩阵进行(DS-8201和AZD1390都以半对数连续稀释使用)。
基于ΔEmax和HSA协同评分的组合来评估组合活性。
结果:
结果显示在图18A和18B以及表9中。
图18A示出测量的细胞活力信号的矩阵。X轴代表药物A(DS-8201),并且Y轴代表药物B(AZD1390)。方框中的值代表在第7天用药物A+B处理的细胞与DMSO对照的比率。将所有值标准化为第0天的细胞活力值。0和100之间的值代表%生长抑制,并且高于100的值代表细胞死亡。
图18B示出HSA超额矩阵。框中的值代表由HSA(最高单一药剂)模型计算的超额值。
下表9示出HSA加性评分和Loewe协同评分:
表9
从图18A和18B以及表9可以看出,AZD1390与DS-8201协同作用,并且也增加了HER2高肺细胞系中的细胞死亡。
前述书面说明书被认为是足以使得本领域的技术人员能够实践这些实施例。前述描述和实例详述了某些实施例并且描述了诸位发明人所期望的最佳方式。然而,将会了解的是无论前述内容可以如何详述出现在本文中,能以许多方式实践这些实施例并且权利要求书包括其任何等效物。
序列列表的自由文本
SEQ ID NO:1-抗HER2抗体的重链的氨基酸序列
SEQ ID NO:2-抗HER2抗体的轻链的氨基酸序列
SEQ ID NO:3-重链CDRH1的氨基酸序列[=SEQ ID NO:1的氨基酸残基26至33]
SEQ ID NO:4-重链CDRH2的氨基酸序列[=SEQ ID NO:1的氨基酸残基51至58]
SEQ ID NO:5-重链CDRH3的氨基酸序列[=SEQ ID NO:1的氨基酸残基97至109]
SEQ ID NO:6-轻链CDRL1的氨基酸序列[=SEQ ID NO:2的氨基酸残基27至32]
SEQ ID NO:7-包含轻链CDRL2(SAS)的氨基酸序列的氨基酸序列[=SEQ ID NO:2的氨基酸残基50至56]
SEQ ID NO:8-轻链CDRL3的氨基酸序列[=SEQ ID NO:2的氨基酸残基89至97]
SEQ ID NO:9-重链可变区的氨基酸序列[=SEQ ID NO:1的氨基酸残基1至120]
SEQ ID NO:10-轻链可变区的氨基酸序列[=SEQ ID NO:2的氨基酸残基1至107]
SEQ ID NO:11-重链的氨基酸序列[=SEQ ID NO:1的氨基酸残基1至449]
Claims (89)
3.如权利要求2所述的药物产品,其中,在式(I)中,R1和R2均是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环。
4.如权利要求2或权利要求3所述的药物产品,其中,在式(I)中,R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环。
5.如权利要求2至4中任一项所述的药物产品,其中,在式(I)中,R3是氢。
6.如权利要求2至5中任一项所述的药物产品,其中,在式(I)中,R4是甲基。
7.如权利要求2至6中任一项所述的药物产品,其中,在式(I)中,R5是氟。
8.如权利要求2所述的药物产品,其中,在式(I)中:
R1是甲基;
R2是甲基;或R1和R2连同它们所键合的氮原子一起形成氮杂环丁烷基、吡咯烷基或哌啶基环;
R3是氢或氟;
R4是甲基;并且
R5是氢或氟。
10.如权利要求1至9中任一项所述的药物产品,其中该抗HER2抗体是包含重链和轻链的抗体,该重链包含:由SEQ ID NO:3表示的氨基酸序列组成的CDRH1、由SEQ ID NO:4表示的氨基酸序列组成的CDRH2和由SEQ ID NO:5表示的氨基酸序列组成的CDRH3,该轻链包含:由SEQ ID NO:6表示的氨基酸序列组成的CDRL1、由SEQ ID NO:7的氨基酸残基1至3所组成的氨基酸序列组成的CDRL2和由SEQ IDNO:8表示的氨基酸序列组成的CDRL3。
11.如权利要求1至9中任一项所述的药物产品,其中该抗HER2抗体是包含重链和轻链的抗体,该重链包含由SEQ ID NO:9表示的氨基酸序列组成的重链可变区,该轻链包含由SEQ ID NO:10表示的氨基酸序列组成的轻链可变区。
12.如权利要求1至9中任一项所述的药物产品,其中该抗HER2抗体是包含重链和轻链的抗体,该重链由SEQ ID NO:1表示的氨基酸序列组成,该轻链由SEQ IDNO:2表示的氨基酸序列组成。
13.如权利要求1至9中任一项所述的药物产品,其中该抗HER2抗体是包含重链和轻链的抗体,该重链由SEQ ID NO:11表示的氨基酸序列组成,该轻链由SEQ IDNO:2表示的氨基酸序列组成。
15.如权利要求1至14中任一项所述的药物产品,其中该抗HER2抗体-药物缀合物为德卢替康-曲妥珠单抗(DS-8201)。
16.如权利要求1至15中任一项所述的药物产品,其中该产品是包含该抗HER2抗体-药物缀合物和该ATM抑制剂的组合物,用于同时施用。
17.如权利要求1至15中任一项所述的药物产品,其中该产品是组合制剂,该组合制剂包含该抗HER2抗体-药物缀合物和该ATM抑制剂,用于顺序或同时施用。
18.如权利要求1至17中任一项所述的药物产品,其中该产品用于治疗癌症。
19.如权利要求18所述的药物产品,其中该癌症为选自由以下组成的组中的至少一种:乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤。
20.如权利要求18所述的药物产品,其中该癌症为乳腺癌。
21.如权利要求20所述的药物产品,其中该乳腺癌具有IHC 3+的HER2状态评分。
22.如权利要求20所述的药物产品,其中该乳腺癌为HER2低表达乳腺癌。
23.如权利要求20所述的药物产品,其中该乳腺癌具有IHC 2+的HER2状态评分。
24.如权利要求20所述的药物产品,其中该乳腺癌具有IHC 1+的HER2状态评分。
25.如权利要求20所述的药物产品,其中该乳腺癌具有IHC>0且<1+的HER2状态评分。
26.如权利要求20所述的药物产品,其中该乳腺癌为三阴性乳腺癌。
27.如权利要求18所述的药物产品,其中该癌症为胃癌。
28.如权利要求18所述的药物产品,其中该癌症为结直肠癌。
29.如权利要求18所述的药物产品,其中该癌症为肺癌。
30.如权利要求29所述的药物产品,其中该肺癌为非小细胞肺癌。
31.如权利要求18所述的药物产品,其中该癌症为胰腺癌。
32.如权利要求18所述的药物产品,其中该癌症为卵巢癌。
33.如权利要求18所述的药物产品,其中该癌症为前列腺癌。
34.如权利要求18所述的药物产品,其中该癌症为肾癌。
35.如权利要求1至17中任一项所述的药物产品,该药物产品用于在治疗癌症中使用。
36.用于如权利要求35所述使用的药物产品,其中该癌症为选自由以下组成的组中的至少一种:乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤。
37.用于如权利要求35所述使用的药物产品,其中该癌症为乳腺癌。
38.用于如权利要求37所述使用的药物产品,其中该乳腺癌具有IHC 3+的HER2状态评分。
39.用于如权利要求37所述使用的药物产品,其中该乳腺癌为HER2低表达乳腺癌。
40.用于如权利要求37所述使用的药物产品,其中该乳腺癌具有IHC 2+的HER2状态评分。
41.用于如权利要求37所述使用的药物产品,其中该乳腺癌具有IHC 1+的HER2状态评分。
42.用于如权利要求37所述使用的药物产品,其中该乳腺癌具有IHC>0且<1+的HER2状态评分。
43.用于如权利要求37所述使用的药物产品,其中该乳腺癌为三阴性乳腺癌。
44.用于如权利要求35所述使用的药物产品,其中该癌症为胃癌。
45.用于如权利要求35所述使用的药物产品,其中该癌症为结直肠癌。
46.用于如权利要求35所述使用的药物产品,其中该癌症为肺癌。
47.用于如权利要求46所述使用的药物产品,其中该肺癌为非小细胞肺癌。
48.用于如权利要求35所述使用的药物产品,其中该癌症为胰腺癌。
49.用于如权利要求35所述使用的药物产品,其中该癌症为卵巢癌。
50.用于如权利要求35所述使用的药物产品,其中该癌症为前列腺癌。
51.用于如权利要求35所述使用的药物产品,其中该癌症为肾癌。
52.抗HER2抗体-药物缀合物或ATM抑制剂在制备药物中的用途,该药物用于组合施用该抗HER2抗体-药物缀合物和该ATM抑制剂以治疗癌症,其中该抗HER2抗体-药物缀合物和该ATM抑制剂如权利要求1至15中任一项所定义。
53.如权利要求52所述的用途,其中该癌症为选自由以下组成的组中的至少一种:乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤。
54.如权利要求52所述的用途,其中该癌症为乳腺癌。
55.如权利要求54所述的用途,其中该乳腺癌具有IHC 3+的HER2状态评分。
56.如权利要求54所述的用途,其中该乳腺癌为HER2低表达乳腺癌。
57.如权利要求54所述的用途,其中该乳腺癌具有IHC 2+的HER2状态评分。
58.如权利要求54所述的用途,其中该乳腺癌具有IHC 1+的HER2状态评分。
59.如权利要求54所述的用途,其中该乳腺癌具有IHC>0且<1+的HER2状态评分。
60.如权利要求54所述的用途,其中该乳腺癌为三阴性乳腺癌。
61.如权利要求52所述的用途,其中该癌症为胃癌。
62.如权利要求52所述的用途,其中该癌症为结直肠癌。
63.如权利要求52所述的用途,其中该癌症为肺癌。
64.根据权利要求63所述的用途,其中该肺癌为非小细胞肺癌。
65.如权利要求52所述的用途,其中该癌症为胰腺癌。
66.如权利要求52所述的用途,其中该癌症为卵巢癌。
67.如权利要求52所述的用途,其中该癌症为前列腺癌。
68.如权利要求52所述的用途,其中该癌症为肾癌。
69.如权利要求52至68中任一项所述的用途,其中该药物是包含该抗HER2抗体-药物缀合物和该ATM抑制剂的组合物,用于同时施用。
70.如权利要求52至68中任一项所述的用途,其中该药物是组合制剂,该组合制剂包含该抗HER2抗体-药物缀合物和该ATM抑制剂,用于顺序或同时施用。
71.一种治疗癌症的方法,该方法包括向有需要的受试者组合施用如权利要求1至15中任一项所定义的抗HER2抗体-药物缀合物和ATM抑制剂。
72.如权利要求71所述的方法,其中该癌症为选自由以下组成的组中的至少一种:乳腺癌、胃癌、结直肠癌、肺癌、食管癌、头颈癌、食管胃连接部腺癌、胆道癌、佩吉特病、胰腺癌、卵巢癌、子宫癌肉瘤、尿路上皮癌、前列腺癌、膀胱癌、胃肠间质瘤、消化道间质瘤、子宫颈癌、鳞状细胞癌、腹膜癌、肝癌、肝细胞癌、子宫体癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤、神经胶质瘤、多形性胶质母细胞瘤、骨肉瘤、肉瘤和黑色素瘤。
73.如权利要求71所述的方法,其中该癌症为乳腺癌。
74.如权利要求73所述的方法,其中该乳腺癌具有IHC 3+的HER2状态评分。
75.如权利要求73所述的方法,其中该乳腺癌为HER2低表达乳腺癌。
76.如权利要求73所述的方法,其中该乳腺癌具有IHC 2+的HER2状态评分。
77.如权利要求73所述的方法,其中该乳腺癌具有IHC 1+的HER2状态评分。
78.如权利要求73所述的方法,其中该乳腺癌具有IHC>0且<1+的HER2状态评分。
79.如权利要求73所述的方法,其中该乳腺癌为三阴性乳腺癌。
80.如权利要求71所述的方法,其中该癌症为胃癌。
81.如权利要求71所述的方法,其中该癌症为结直肠癌。
82.如权利要求71所述的方法,其中该癌症为肺癌。
83.如权利要求82所述的方法,其中该肺癌为非小细胞肺癌。
84.如权利要求71所述的方法,其中该癌症为胰腺癌。
85.如权利要求71所述的方法,其中该癌症为卵巢癌。
86.如权利要求71所述的方法,其中该癌症为前列腺癌。
87.如权利要求71所述的方法,其中该癌症为肾癌。
88.如权利要求71至87中任一项所述的方法,其中该方法包括按顺序施用该抗HER2抗体-药物缀合物和该ATM抑制剂。
89.如权利要求71至87中任一项所述的方法,其中该方法包括同时施用该抗HER2抗体-药物缀合物和该ATM抑制剂。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063043474P | 2020-06-24 | 2020-06-24 | |
| US63/043474 | 2020-06-24 | ||
| PCT/IB2021/055549 WO2021260580A1 (en) | 2020-06-24 | 2021-06-23 | Combination of antibody-drug conjugate and atm inhibitor |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116194109A true CN116194109A (zh) | 2023-05-30 |
Family
ID=76730927
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180050399.2A Pending CN116194109A (zh) | 2020-06-24 | 2021-06-23 | 抗体-药物缀合物和atm抑制剂的组合 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20230256110A1 (zh) |
| EP (1) | EP4171651A1 (zh) |
| JP (1) | JP2023539715A (zh) |
| CN (1) | CN116194109A (zh) |
| TW (1) | TW202216209A (zh) |
| WO (1) | WO2021260580A1 (zh) |
Family Cites Families (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| DE69233254T2 (de) | 1991-06-14 | 2004-09-16 | Genentech, Inc., South San Francisco | Humanisierter Heregulin Antikörper |
| PT1071700E (pt) | 1998-04-20 | 2010-04-23 | Glycart Biotechnology Ag | Modificação por glicosilação de anticorpos para melhorar a citotoxicidade celular dependente de anticorpos |
| CA2376596C (en) | 1999-06-25 | 2009-10-06 | Genentech, Inc. | Humanized anti-erbb2 antibodies and treatment with anti-erbb2 antibodies |
| CA2785941C (en) | 2000-10-06 | 2017-01-10 | Kyowa Hakko Kirin Co., Ltd. | Antibody composition-producing cell |
| JP2005521689A (ja) | 2002-02-25 | 2005-07-21 | クドス ファーマシューティカルズ リミテッド | Atm阻害剤として有用なピラノン |
| CA2534300A1 (en) | 2003-08-13 | 2005-02-24 | Kudos Pharmaceuticals Limited | Aminopyrones and their use as atm inhibitors |
| GB0510390D0 (en) | 2005-05-20 | 2005-06-29 | Novartis Ag | Organic compounds |
| CA2647632C (en) | 2006-03-27 | 2017-06-27 | University Of Maryland Biotechnology Institute | Glycoprotein synthesis and remodeling by enzymatic transglycosylation |
| DE102010035744A1 (de) | 2010-08-28 | 2012-03-01 | Merck Patent Gmbh | Imidazolonylchinoline |
| CA2862925C (en) | 2012-02-10 | 2020-01-21 | University Of Maryland, Baltimore | Chemoenzymatic glycoengineering of antibodies and fc fragments thereof |
| SG10201804788XA (en) | 2012-10-11 | 2018-07-30 | Daiichi Sankyo Co Ltd | Antibody-drug conjugate |
| ES2703903T3 (es) | 2013-12-25 | 2019-03-13 | Daiichi Sankyo Co Ltd | Conjugado de fármaco-anticuerpo anti-trop2 |
| SG11201603960XA (en) * | 2014-01-31 | 2016-07-28 | Daiichi Sankyo Co Ltd | Anti-her2 antibody-drug conjugate |
| WO2015155998A1 (en) | 2014-04-10 | 2015-10-15 | Daiichi Sankyo Company, Limited | Anti-her3 antibody-drug conjugate |
| NO2714752T3 (zh) | 2014-05-08 | 2018-04-21 | ||
| CA2981365A1 (en) | 2015-04-02 | 2016-10-06 | Merck Patent Gmbh | Imidazolonylquinolines and the use thereof as atm kinase inhibitors |
| KR20180021723A (ko) | 2015-06-29 | 2018-03-05 | 다이이찌 산쿄 가부시키가이샤 | 항체-약물 콘주게이트의 선택적 제조 방법 |
| GB201516504D0 (en) | 2015-09-17 | 2015-11-04 | Astrazeneca Ab | Imadazo(4,5-c)quinolin-2-one Compounds and their use in treating cancer |
| GB201519406D0 (en) | 2015-11-03 | 2015-12-16 | Astrazeneca Ab | Imidazo[4,5-c]quinolin-2-one compounds and their use in treating cancer |
| GB201519568D0 (en) | 2015-11-05 | 2015-12-23 | Astrazeneca Ab | Imidazo[4,5-c]quinolin-2-one compounds and their use in treating cancer |
| GB201604182D0 (en) | 2016-03-11 | 2016-04-27 | Astrazeneca Ab | Imidazo[4,5-c]quinolin-2-one compounds and their use in treating cancer |
| CN108884084A (zh) | 2016-03-21 | 2018-11-23 | 阿斯利康(瑞典)有限公司 | 噌啉-4-胺化合物及其在治疗癌症中的用途 |
| WO2017162611A1 (en) | 2016-03-21 | 2017-09-28 | Astrazeneca Ab | Quinoline-3-carboxamide compounds and their use in treating cancer |
| EA201891866A1 (ru) | 2016-04-07 | 2019-04-30 | Астразенека Аб | N,N-ДИМЕТИЛ-3-[[5-(3-МЕТИЛ-2-ОКСО-1-ТЕТРАГИДРОПИРАН-4-ИЛ-ИМИДАЗО[4,5-c]ХИНОЛИН-8-ИЛ)-2-ПИРИДИЛ]ОКСИ]ПРОПАН-1-АМИНОКСИД В КАЧЕСТВЕ МОДУЛЯТОРА АТМ-КИНАЗЫ (МУТАЦИИ АТАКСИИ-ТЕЛЕАНГИЭКТАЗИИ) ДЛЯ ЛЕЧЕНИЯ РАКА |
| GB201608227D0 (en) | 2016-05-11 | 2016-06-22 | Astrazeneca Ab | Imidazo[4,5-c]quinolin-2-one compounds and their use in treating cancer |
| JOP20190209A1 (ar) | 2017-03-16 | 2019-09-12 | Astrazeneca Ab | مركبات إيميدازو [ 4، 5-c ] كينولين-2-أون ديوترومية واستخدامها في علاج السرطان |
| TWI794230B (zh) | 2017-05-15 | 2023-03-01 | 日商第一三共股份有限公司 | 抗cdh6抗體及抗cdh6抗體-藥物結合物、以及其製造方法 |
| SG11202000997YA (en) | 2017-08-31 | 2020-03-30 | Daiichi Sankyo Co Ltd | Improved method for producing antibody-drug conjugate |
| CN111344293A (zh) | 2017-09-20 | 2020-06-26 | 阿斯利康(瑞典)有限公司 | 1,3-二氢咪唑并[4,5-c]噌啉-2-酮化合物及其在治疗癌症中的用途 |
-
2021
- 2021-06-23 EP EP21736709.3A patent/EP4171651A1/en active Pending
- 2021-06-23 WO PCT/IB2021/055549 patent/WO2021260580A1/en unknown
- 2021-06-23 CN CN202180050399.2A patent/CN116194109A/zh active Pending
- 2021-06-23 JP JP2022580310A patent/JP2023539715A/ja active Pending
- 2021-06-23 US US18/012,900 patent/US20230256110A1/en active Pending
- 2021-06-23 TW TW110122960A patent/TW202216209A/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP4171651A1 (en) | 2023-05-03 |
| JP2023539715A (ja) | 2023-09-19 |
| US20230256110A1 (en) | 2023-08-17 |
| WO2021260580A1 (en) | 2021-12-30 |
| TW202216209A (zh) | 2022-05-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3903828A1 (en) | Combination of antibody-drug conjugate and kinase inhibitor | |
| RU2769700C2 (ru) | Дуокармициновые adc, демонстрирующие улучшенную противоопухолевую активность in vivo | |
| US20210290775A1 (en) | Combination of antibody-drug conjugate and tubulin inhibitor | |
| EP3909580A1 (en) | Combination of antibody-drug conjugate with parp inhibitor | |
| US20230372527A1 (en) | Combination of antibody-drug conjugate and parp1 selective inhibitor | |
| US20210290777A1 (en) | Treatment of metastatic brain tumor by administration of antibody-drug conjugate | |
| US20230233540A1 (en) | Combination of antibody-drug conjugate and cdk9 inhibitor | |
| US20230256110A1 (en) | Combination of antibody-drug conjugate and atm inhibitor | |
| WO2021260583A1 (en) | Combination of antibody-drug conjugate and dna-pk inhibitor | |
| WO2021260582A1 (en) | Combination of antibody-drug conjugate and aurora b inhibitor | |
| US20230330243A1 (en) | Combination of antibody-drug conjugate and atr inhibitor | |
| Spencer et al. | A phase I trial of riluzole and sorafenib in patients with advanced solid tumors: CTEP# 8850 | |
| WO2023126822A1 (en) | Combination of antibody-drug conjugate and rasg12c inhibitor | |
| CA3238116A1 (en) | Combination of antibody-drug conjugate and parp1 selective inhibitor | |
| WO2023126823A1 (en) | Combination of antibody-drug conjugate and atr inhibitor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |