CN111228362B - 双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 - Google Patents
双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 Download PDFInfo
- Publication number
- CN111228362B CN111228362B CN202010136104.0A CN202010136104A CN111228362B CN 111228362 B CN111228362 B CN 111228362B CN 202010136104 A CN202010136104 A CN 202010136104A CN 111228362 B CN111228362 B CN 111228362B
- Authority
- CN
- China
- Prior art keywords
- infection
- pharyngitis
- application
- shuangyang
- particles
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/81—Solanaceae (Potato family), e.g. tobacco, nightshade, tomato, belladonna, capsicum or jimsonweed
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/56—Materials from animals other than mammals
- A61K35/63—Arthropods
- A61K35/64—Insects, e.g. bees, wasps or fleas
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/28—Asteraceae or Compositae (Aster or Sunflower family), e.g. chamomile, feverfew, yarrow or echinacea
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/28—Asteraceae or Compositae (Aster or Sunflower family), e.g. chamomile, feverfew, yarrow or echinacea
- A61K36/288—Taraxacum (dandelion)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/53—Lamiaceae or Labiatae (Mint family), e.g. thyme, rosemary or lavender
- A61K36/534—Mentha (mint)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/53—Lamiaceae or Labiatae (Mint family), e.g. thyme, rosemary or lavender
- A61K36/538—Schizonepeta
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
Landscapes
- Health & Medical Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Botany (AREA)
- Medical Informatics (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Alternative & Traditional Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Virology (AREA)
- Insects & Arthropods (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Molecular Biology (AREA)
- Pulmonology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Animal Husbandry (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
本发明公开了一种双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用。本发明可以有效抑制冠状病毒的生长,从而使得双羊喉痹通颗粒具有在治疗由冠状病毒感染引发的疾病中的新用途。
Description
技术领域
本发明涉及一种双羊喉痹通颗粒的应用,特别是一种双羊喉痹通 颗粒在治疗冠状病毒感染引发的疾病中的应用。
背景技术
双羊喉痹通颗粒的主要成分有野烟叶、羊耳菊、矮地茶、羊奶奶 叶、僵蚕、荆芥、薄荷,辅料为蔗糖;其主要的用途为清热解毒,利 咽止痛,用于急喉痹(急性咽炎)、急乳蛾(急性扁桃体炎)所致的咽喉 肿痛。
而新型冠状病毒,属于β属的冠状病毒,有包膜,其基因特征与 SARSr-CoV和MERSr-CoV有明显区别,目前研究显示与蝙蝠SARS样 冠状病毒同源性达85%以上。其传染源主要是新型冠状病毒感染的患 者,传播途径主要依靠呼吸道飞沫和接触传播,临床表现以发热、乏 力、干咳为主要表现。在新型冠状病毒感染的肺炎治疗方案(试运行 第六版)中,公开了目前针对该病毒的一些治疗手段,包括抗菌药物 治疗、抗病毒治疗和中医治疗等。由于本病属于中医疫病范畴,根据 临床表现的不同,可以选用相应的中药进行治疗,具体地:在医学观 察期,可以使用藿香正气胶囊、金花清感颗粒、连花清瘟胶囊、疏风 解毒胶囊、防风通圣丸等进行治疗;在临床治疗期,针对轻型患者, 推荐处方:生麻黄6g、生石膏15g、杏仁9g、羌活15g、葶苈子15g、 贯众9g、地龙15g、徐长卿15g、藿香、佩兰9g、仓术15g、云苓45g、 生白术30g、焦三仙各9g、厚朴15g、焦槟榔9g、煨草果9g、生姜 15g;针对普通型患者,推荐处方:仓术15g、陈皮10g、厚朴10g、 藿香10g、草果6g、生麻黄6g、羌活10g、生姜10g、槟榔10g;针 对重型患者,推荐处方:生麻黄6g、杏仁9g、生石膏15g、甘草3g、 藿香10g(后下)、厚朴10g、仓术15g、草果10g、法半夏9g、茯 苓15g、生大黄5g(后下)、生黄芪10g、葶苈子10g、赤芍10g; 危重型患者,推荐处方:人参15g、黑顺片10g(先煎)、山茱萸15g, 送服苏合香丸或安宫牛黄丸。然而,截止目前,公众所能获知的专利、 文献、刊物等资料中,均未公开将双羊喉痹通颗粒用于治疗冠状病毒 感染引发的疾病中的用途。
发明内容
本发明的目的在于,提供一种双羊喉痹通颗粒在治疗冠状病毒感 染引发的疾病中的应用。本发明可以有效抑制冠状病毒的生长,从而 使得双羊喉痹通颗粒具有在治疗由冠状病毒感染引发的疾病中的新 用途。
本发明的技术方案:双羊喉痹通颗粒在治疗冠状病毒感染引发的 疾病中的应用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,所述的双羊喉痹通颗粒对人类冠状病毒HCoV-229E株具有抑制 作用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,双羊喉痹通颗粒在治疗人类冠状病毒HCoV-229E株感染引发的 呼吸道感染疾病中的应用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,双羊喉痹通颗粒在治疗人类冠状病毒HCoV-229E株感染引发的 小鼠呼吸道感染疾病中的应用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,所述的双羊喉痹通颗粒对大鼠冠状病毒8190株具有抑制作用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,双羊喉痹通颗粒在治疗大鼠冠状病毒8190株感染引发的呼吸 道感染疾病中的应用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,双羊喉痹通颗粒在治疗人类冠状病毒HCoV-229E株感染引发的 大鼠呼吸道感染疾病中的应用。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,所述双羊喉痹通颗粒的临床用量为24-36g/60kg/d。
前述的双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应 用中,所述双羊喉痹通颗粒的临床用量为30g/60kg/d。
与现有技术相比,本发明可以有效抑制冠状病毒的生长,从而使 得双羊喉痹通颗粒具有在治疗由冠状病毒感染引发的疾病中的新用 途。
使用双羊喉痹通颗粒在治疗由冠状病毒感染引发的疾病中具有 良好的治疗效果,其药物疗效可通过双羊喉痹通颗粒抗冠状病毒的体 外细胞实验来表现。
以下是本发明的实验例。
实验例1:双羊喉痹通颗粒抗冠状病毒的体外细胞实验
1、试验材料
1.1、细胞株:人肺癌细胞A549购自北京北纳创联生物技术研 究院,本室传代,液氮保存备用。
1.2、病毒株:人类冠状病毒(HCoV-229E),由中国医学科学 院医药生物技术研究所提供,本实验室传代,-80℃冰箱保存备用
1.3受试药物
名称:双羊喉痹通颗粒
批号:20200202
规格:10g/袋
用法用量:10g/次,3次/日
生产厂家:贵州百灵企业集团制药股份有限公司
1.4、试验试剂
1.5、试验仪器
2、试验方法及结果
2.1、药物制备
2.2、药物对体外培养A549细胞的毒性试验
将配制后浓度的药物用培养液做2倍倍比稀释,共7个稀释 度,加到已长成单层的A549细胞培养板中,100μL/孔,每个稀释 度做3个复孔,同时设正常细胞对照。将培养板置37℃,5%CO2培 养箱中培养,每日倒置显微镜下观察细胞病变情况,连续96h,确定 细胞不出现明显病变的最低稀释倍数(最大无毒浓度TC0),并按 Reed-Muench法计算50%细胞毒性浓度(TC50)。
表1.药物对体外培养A549细胞的毒性作用
表2 药物对体外培养A549细胞的毒性作用
表1、2结果显示了药物的最大无毒浓度(TC0),以下试验时 采用TC0浓度以下的6个浓度进行。
2.3、药物在体外培养A549细胞上对人类冠状病毒(HCoV-229E) 的抑制作用
取已长成单层细胞的培养板,倒掉培养液,用细胞维持液冲洗细 胞面3遍后,接种HCoV-229E病毒液,100TCID50,100μL/孔,置 37℃5%CO2培养箱中吸附1h后,依次加入无毒浓度以下7个稀 释度的各药液,100μL/孔,同时设正常细胞对照和病毒对照。置37℃ 5%CO2培养箱中培养,每日倒置显微镜下观察细胞病变情况,96小 时后病毒对照组细胞病变为+++~~++++时记录试验结果;并取上清液 检测病毒核酸和细胞活力。
细胞病变按6级标准判断:
-:细胞生长正常,无病变出现;
±:细胞病变少于整个单层的10%;
+:细胞病变约占整个单层细胞的25%以下;
++:细胞病变约占整个单层细胞的50%以下;
+++:细胞病变约占整个单层细胞的75%以下;
++++:细胞病变约占整个单层细胞的75%以上。
按Reed-Muench计算50%抑制浓度(IC50)和治疗指数(TI), TI=TC50/IC50
2.3.1、病毒核酸检测方法(RT-PCR法):
细胞中核酸裂解处理
1)按照说明书将各个试剂配好备用;2)吸取560μl配制好的 Buffer AVL-carrierRNA至1.5ml的离心管中;3)加入140μl细胞 培养上清液至第2)步准备好的管中,涡旋振荡15秒;4)室温下 (15-25℃)孵育10分钟;5)快速离心以去除附着于内壁与内盖的 水滴;6)加入560μl乙醇(96-100%)至样本中,短暂离心15秒混 匀,混匀后,快速离心去除附着于内壁与内盖的水滴;7)小心吸取 630μl上一步获得的溶液至QIAamp Mini column上(柱子放置于1 个2毫升的收集管内),小心不要碰到柱子的边缘,盖上盖子,6000 x g(8000rpm)下离心1分钟。将QIAamp Mini column移至一个新 的2ml收集管,丢弃带有流出液的旧管;8)小心打开盖子,重复第 7步操作;9)小心打开盖子,加入500μl Buffer AW1,盖上盖子,6000x g(8000rpm)下离心1分钟,将QIAamp Mini column移至 一个新的2ml收集管,丢弃带有流出液的旧管;10)小心打开盖子, 加入500μl Buffer AW2,盖上盖子全速离心(20000xg;14000rpm) 3分钟;11)将柱子放在一个干净的1.5ml的离心管,丢弃含有流出 液的旧管,小心打开盖子,加60μl平衡好的Buffer AVE至膜上,盖 上盖子,室温下孵育一分钟,6000xg(8000rpm)离心1分钟,于-20℃ 1月或-80℃下保存1年。
核酸测定:
对照品核酸处理:DEPC-H2O作为阴性对照。阳性对照品进行10、 100、1000倍梯度稀释。
试剂配制:取n×18μl HCoV-229E核酸荧光PCR检测混合液, n×1μl内部对照品,与n×1μl RT-PCR酶(n为反应管数),振荡 混匀数秒,3000rpm离心数秒。
加样:取上述混合液20μl置于PCR管中,然后将样品核酸提 取液、DEPC-H2O、阳性对照品各5μl分别加入PCR管中,改进管盖, 离心数秒使所有液体置于底部,立即进行PCR扩增反应。
PCR扩增:反应管置于定量荧光PCR仪上,循环参数设置为: 45℃×10min;95℃×15min;再按95℃×15sec→60℃×60sec,循 环40次;单点荧光检测在60℃,反应体系为25μl。
荧光通道检测选择:选用FAM和HEX/VIC/JOE通道。
备注:使用ABI系列PCR仪,请务必于passive reference和 quencher处均选择“none”。
计算方法
| 通道 | Ct值 | 结果判断 | |
| 1 | FAM | UNDET或40 | 样本低于检测值限,报告为阴性 |
| 2 | FAM | ≦38 | 报告为阳性 |
| 3 | FAM | 38~40 | 复检一次,如仍为38~40,则报告为阴性 |
2.3.2、细胞活力检测方法(CCK8法):
检测原理:CCK8检测试剂盒,是一种基于WST-8(化学名:2-(2- 甲氧基-4-硝苯基)-3-(4-硝苯基)-5-(2,4-二磺基苯)-2H-四唑单钠 盐)的广泛应用于细胞增殖和细胞毒性的快速高灵敏度检测试剂盒, 工作原理为:在电子耦合试剂存在的情况下,WST-8可以被线粒体内 的脱氢酶还原生成高度水溶性的橙黄色的甲臜产物(formazan)。颜 色的深浅与细胞的增殖成正比,与细胞毒性成反比。使用酶标仪在 450nm波长处测定OD值,间接反映活细胞数量。
检测方法:将已接种HCoV-229E病毒液并加入不同浓度各药液 的A549细胞继续培养96h后,吸去上清液,向96孔板每孔加入 含10%CCK8溶液的DMEM培养液100μL。将培养板在培养箱内继续 孵育1小时,用酶标仪测定在450nm处的吸光度值。
表3.药物在体外培养A549细胞上HCoV-229E的抑制作用
表4.药物在体外培养A549细胞上HCoV-229E的抑制作用
表3、4结果显示:药物在不同浓度下对HCoV-229E致体外培 养A549细胞病变有不同程度的抑制作用。
表5.药物在体外培养A549细胞上HCoV-229E的抑制作用
表5结果显示:细胞对照组无HCoV-229E病毒核酸表达;病毒 感染后对照组可检测出HCoV-229E病毒核酸表达;双羊喉痹通颗粒 在3.91ug/ml剂量时可明显降低HCoV-229E病毒核酸表达。
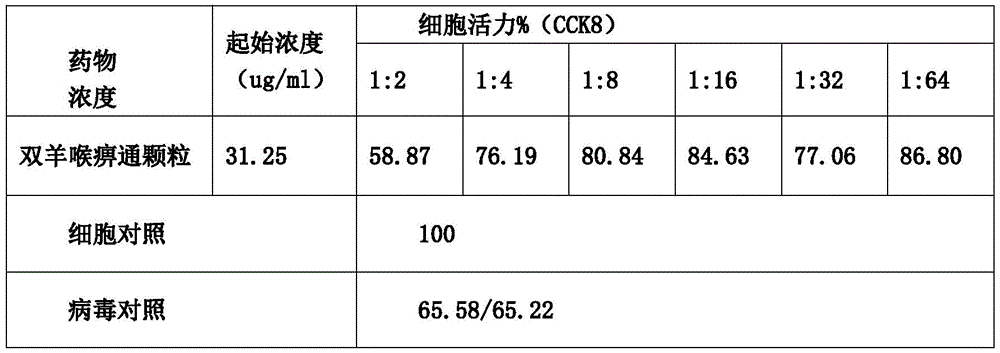
表6.药物在体外培养A549细胞上HCoV-229E的抑制作用
表6结果显示:细胞对照组活力为100%,说明细胞状态良好; 病毒感染后对照组细胞活力明显降低,与CPE结果相吻合。
3、小结
采用人类冠状病毒229E(HCoV-229E)感染A549细胞,通过观 察药物的TC0、TC50、IC50、TI,病毒核酸表达量以及培养细胞活力, 综合评价药物在体外对HCoV-229E的抑制作用。
结果显示:双羊喉痹通颗粒在体外对人类冠状病毒229E (HCoV-229E)有明显抑制作用。
具体实施方式
下面结合实施例对本发明作进一步的说明,但并不作为对本发明 限制的依据。
实施例1。双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的 应用。
所述双羊喉痹通颗粒的人临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的人临床用量为30g/60kg/d。
口服,一次10g,一日三次。禁忌:孕妇禁用。糖尿病患者禁服。 注意事项:1、忌烟酒、辛辣、鱼腥食物。2、不宜在服药期间同时服 用温补性中药。3、儿童应在医师指导下服用。4、脾虚大便溏者慎用。 5、属风寒感冒咽痛者,症见恶寒发热、无汗、鼻流清涕者慎用。6、扁桃体有化脓及全身高热者应去医院就诊。7、服药3天症状无缓解, 应去医院就诊。8、对本品过敏者禁用,过敏体质者慎用。9、本品性 状发生改变时禁止使用。10、儿童必须在成人监护下使用。11、请将 本品放在儿童不能接触的地方。12、如正在使用其他药品,使用本品 前请咨询医师或药师。
实施例2。双羊喉痹通颗粒在治疗人类冠状病毒(HCoV-229E株) 感染引发的疾病中的应用。
所述的双羊喉痹通颗粒对人类冠状病毒HCoV-229E株具有抑制 作用。
所述双羊喉痹通颗粒的人临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的人临床用量为30g/60kg/d。
口服,一次10g,一日三次。禁忌:孕妇禁用。糖尿病患者禁服。 注意事项:1、忌烟酒、辛辣、鱼腥食物。2、不宜在服药期间同时服 用温补性中药。3、儿童应在医师指导下服用。4、脾虚大便溏者慎用。 5、属风寒感冒咽痛者,症见恶寒发热、无汗、鼻流清涕者慎用。6、扁桃体有化脓及全身高热者应去医院就诊。7、服药3天症状无缓解, 应去医院就诊。8、对本品过敏者禁用,过敏体质者慎用。9、本品性 状发生改变时禁止使用。10、儿童必须在成人监护下使用。11、请将 本品放在儿童不能接触的地方。12、如正在使用其他药品,使用本品 前请咨询医师或药师。
实施例3。双羊喉痹通颗粒在治疗人类冠状病毒HCoV-229E株感 染引发的呼吸道感染疾病中的应用。
所述双羊喉痹通颗粒的人临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的人临床用量为30g/60kg/d。
口服,一次10g,一日三次。禁忌:孕妇禁用。糖尿病患者禁服。 注意事项:1、忌烟酒、辛辣、鱼腥食物。2、不宜在服药期间同时服 用温补性中药。3、儿童应在医师指导下服用。4、脾虚大便溏者慎用。 5、属风寒感冒咽痛者,症见恶寒发热、无汗、鼻流清涕者慎用。6、扁桃体有化脓及全身高热者应去医院就诊。7、服药3天症状无缓解, 应去医院就诊。8、对本品过敏者禁用,过敏体质者慎用。9、本品性 状发生改变时禁止使用。10、儿童必须在成人监护下使用。11、请将 本品放在儿童不能接触的地方。12、如正在使用其他药品,使用本品 前请咨询医师或药师。
实施例4。双羊喉痹通颗粒在治疗人类冠状病毒HCoV-229E株感 染引发的小鼠呼吸道感染疾病中的应用。
所述双羊喉痹通颗粒的临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的临床用量为30g/60kg/d。
口服,一次10g,一日三次。
实施例5。双羊喉痹通颗粒在治疗大鼠冠状病毒8190株感染引 发的疾病中的应用。
所述双羊喉痹通颗粒的人临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的人临床用量为30g/60kg/d。
口服,一次10g,一日三次。禁忌:孕妇禁用。糖尿病患者禁服。 注意事项:1、忌烟酒、辛辣、鱼腥食物。2、不宜在服药期间同时服 用温补性中药。3、儿童应在医师指导下服用。4、脾虚大便溏者慎用。 5、属风寒感冒咽痛者,症见恶寒发热、无汗、鼻流清涕者慎用。6、扁桃体有化脓及全身高热者应去医院就诊。7、服药3天症状无缓解, 应去医院就诊。8、对本品过敏者禁用,过敏体质者慎用。9、本品性 状发生改变时禁止使用。10、儿童必须在成人监护下使用。11、请将 本品放在儿童不能接触的地方。12、如正在使用其他药品,使用本品 前请咨询医师或药师。
实施例6。双羊喉痹通颗粒在治疗大鼠冠状病毒8190株感染引 发的呼吸道感染疾病中的应用。
所述双羊喉痹通颗粒的人临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的人临床用量为30g/60kg/d。
口服,一次10g,一日三次。禁忌:孕妇禁用。糖尿病患者禁服。 注意事项:1、忌烟酒、辛辣、鱼腥食物。2、不宜在服药期间同时服 用温补性中药。3、儿童应在医师指导下服用。4、脾虚大便溏者慎用。 5、属风寒感冒咽痛者,症见恶寒发热、无汗、鼻流清涕者慎用。6、扁桃体有化脓及全身高热者应去医院就诊。7、服药3天症状无缓解, 应去医院就诊。8、对本品过敏者禁用,过敏体质者慎用。9、本品性 状发生改变时禁止使用。10、儿童必须在成人监护下使用。11、请将 本品放在儿童不能接触的地方。12、如正在使用其他药品,使用本品 前请咨询医师或药师。
实施例7。双羊喉痹通颗粒在治疗大鼠冠状病毒8190株感染引 发的大鼠呼吸道感染疾病中的应用。
所述双羊喉痹通颗粒的临床用量为24-36g/60kg/d。
优选为:所述双羊喉痹通颗粒的临床用量为30g/60kg/d。
口服,一次10g,一日三次。
Claims (5)
1.双羊喉痹通颗粒在制备治疗人类冠状病毒HCoV-229E株感染引发的呼吸道感染疾病药物中的应用。
2.根据权利要求1所述的双羊喉痹通颗粒在制备治疗人类冠状病毒HCoV-229E株感染引发的呼吸道感染疾病药物中的应用,其特征在于:所述呼吸道感染疾病为小鼠呼吸道感染疾病。
3.根据权利要求1所述的双羊喉痹通颗粒在制备治疗人类冠状病毒HCoV-229E株感染引发的呼吸道感染疾病药物中的应用,其特征在于:所述呼吸道感染疾病为大鼠呼吸道感染疾病。
4.根据权利要求1至3中任一项所述的双羊喉痹通颗粒在制备治疗人类冠状病毒HCoV-229E株感染引发的呼吸道感染疾病药物中的应用,其特征在于:所述双羊喉痹通颗粒的临床用量为24-36g/60kg/d。
5.根据权利要求4所述的双羊喉痹通颗粒在制备治疗人类冠状病毒HCoV-229E株感染引发的呼吸道感染疾病药物中的应用,其特征在于:所述双羊喉痹通颗粒的临床用量为30g/60kg/d。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010136104.0A CN111228362B (zh) | 2020-03-02 | 2020-03-02 | 双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010136104.0A CN111228362B (zh) | 2020-03-02 | 2020-03-02 | 双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN111228362A CN111228362A (zh) | 2020-06-05 |
| CN111228362B true CN111228362B (zh) | 2022-01-14 |
Family
ID=70878847
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202010136104.0A Active CN111228362B (zh) | 2020-03-02 | 2020-03-02 | 双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN111228362B (zh) |
-
2020
- 2020-03-02 CN CN202010136104.0A patent/CN111228362B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN111228362A (zh) | 2020-06-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN111870657B (zh) | 一种中药组合物在制备治疗或预防冠状病毒感染的药物中的应用 | |
| CN111297969A (zh) | 柴银制剂在制备抗冠状病毒药物中的应用及其制备方法 | |
| CN101618193B (zh) | 一种抗病毒的中药组合物 | |
| WO2021212721A1 (zh) | 祛湿宣肺中药组合物及其应用 | |
| CN111150755B (zh) | 具有防治病毒性疾病的中药组合物及其应用 | |
| CN111991480A (zh) | 用于预防新型冠状病毒肺炎感染的中药组合物 | |
| CN111228362B (zh) | 双羊喉痹通颗粒在治疗冠状病毒感染引发的疾病中的应用 | |
| CN108186866B (zh) | 金贝口服液在抗病毒中的应用 | |
| CN111632116A (zh) | 一种抗病毒性感冒中药制剂的制备方法 | |
| CN100353953C (zh) | 治疗口腔、咽喉疾病的中药制剂及其制备方法 | |
| CN103356812B (zh) | 一种了哥王颗粒 | |
| CN102198192B (zh) | 一种防治甲流的中药组合物及其应用 | |
| CN102240328B (zh) | 一种治疗感冒的中药及其制备方法 | |
| CN1318077C (zh) | 一种抗病毒的中药复方制剂及其制备方法和用途 | |
| CN108245586B (zh) | 小儿解感颗粒在抗病毒中的应用 | |
| CN100398097C (zh) | 一种四季三黄新制剂和制备方法及用途 | |
| CN113101331A (zh) | 一种百里香药茶及其制备方法和应用 | |
| CN116966244B (zh) | 一种防治新型冠状病毒感染的中药组合物及其制备方法和应用 | |
| CN113967230B (zh) | 治疗马腺疫的中药组合物 | |
| CN115282243B (zh) | 一种治疗小儿急性支气管炎的中药组合物及其制备方法 | |
| CN114712452A (zh) | 一种中药组合物在制备抗sars病毒药物中的应用 | |
| CN103356813B (zh) | 一种了哥王胶囊 | |
| CN116509931B (zh) | 一种抑制hiv病毒感染的中药组合物及其制备方法 | |
| CN113440562B (zh) | 复方鱼腥草合剂在制备预防或治疗冠状病毒药物中的应用 | |
| CN114668805B (zh) | 组合物在制备药物中的用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant | ||
| TR01 | Transfer of patent right | ||
| TR01 | Transfer of patent right |
Effective date of registration: 20230926 Address after: 550025 Changba Industrial Zone, Guiyang Economic and Technological Development Zone, Guizhou Province Patentee after: Guizhou Bailing Enterprise Group Zhengxin Pharmaceutical Co.,Ltd. Address before: 561000 No.212 Xihang Road, economic and Technological Development Zone, Anshun City, Guizhou Province Patentee before: GUIZHOU BAILING ENTERPRISE GROUP PARMACEUTIAL Co.,Ltd. |