CN111093660A - 用于治疗癌症的组合疗法 - Google Patents
用于治疗癌症的组合疗法 Download PDFInfo
- Publication number
- CN111093660A CN111093660A CN201880057161.0A CN201880057161A CN111093660A CN 111093660 A CN111093660 A CN 111093660A CN 201880057161 A CN201880057161 A CN 201880057161A CN 111093660 A CN111093660 A CN 111093660A
- Authority
- CN
- China
- Prior art keywords
- inhibitor
- pharmaceutically acceptable
- agents
- acceptable salt
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/475—Quinolines; Isoquinolines having an indole ring, e.g. yohimbine, reserpine, strychnine, vinblastine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/52—Purines, e.g. adenine
- A61K31/522—Purines, e.g. adenine having oxo groups directly attached to the heterocyclic ring, e.g. hypoxanthine, guanine, acyclovir
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/555—Heterocyclic compounds containing heavy metals, e.g. hemin, hematin, melarsoprol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/243—Platinum; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
Abstract
本披露涉及用于治疗癌症的方法、用于使用的化合物和药物,所述方法包括向有需要的受试者施用治疗有效量的第一药剂和各自处于治疗有效量的一种或多种第二药剂。在一些实施例中,所述第一药剂包括EZH2抑制剂。在某些实施例中,所述第一药剂是他泽美司他或其药学上可接受的盐,并且本披露的方法用于治疗肺癌,例如非小细胞肺癌。
Description
相关申请
本申请要求于2017年9月5日提交的美国临时申请号62/554,484的优先权和权益,将其内容通过引用以其全文结合在此。
技术领域
本发明涉及包括以下各项的组合物:人类组蛋白甲基转移酶EZH2的抑制剂、催化组蛋白H3(H3-K27)上赖氨酸27的一至三甲基化的PRC2复合体的催化亚基、以及一种或多种其他治疗剂,特别是抗癌药剂,并且涉及用于治疗癌症的组合疗法方法。
背景技术
组合疗法治疗癌症已变得更加常见,部分原因是由于通过多途径攻击疾病的已知优势。虽然在过去的几十年中已经确定了许多有效的组合疗法治疗,鉴于每年由癌症造成的持续大量的死亡,仍然对确定用于抗癌治疗的有效治疗方案存在持续的需要。
发明内容
本披露是基于这样的发现:EZH2组蛋白甲基转移酶抑制剂和其他抗癌剂可以组合用于治疗某些肿瘤,并且具有比那些通过单独使用EZH2组蛋白甲基转移酶抑制剂和抗癌剂治疗肿瘤取得更优的结果。因此,本披露提供了一种包含EZH2组蛋白甲基转移酶抑制剂和一种或多种其他治疗剂的组合物,以及它们的使用来治疗疾病(例如癌症)的方法,其中该过程可以受调节组蛋白或其他蛋白质的甲基化状态的影响。在某些实施例中,本披露提供了一种组合物,该组合物包含EZH2组蛋白甲基转移酶抑制剂他泽美司他(tazemetostat)或其药学上可接受的盐和一种或多种第二抗癌剂。在某些实施例中,本披露提供了一种组合物,该组合物包含EZH2组蛋白甲基转移酶抑制剂他泽美司他或其药学上可接受的盐和第二抗癌剂,用于治疗肺癌,例如非小细胞肺癌。
本披露的一些方面提供了用于治疗癌症的方法、策略、治疗方式、组合物、和组合。在一些实施例中,本披露提供了多种方法,所述方法包括向有需要的受试者施用(a)治疗有效量的第一药剂,其中该第一药剂包括EZH2抑制剂,和(b)治疗有效量的一种或多种第二药剂。在一些实施例中,EZH2抑制剂是本文提供的EZH2抑制剂。例如,并且非限制,在一些实施例中,EZH2抑制剂是具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物,或其药学上可接受的盐。在一些示例性实施例中,EZH2抑制剂是具有式(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb)的化合物,或其药学上可接受的盐。
在一些实施例中,本披露提供了用于治疗癌症的多种方法,所述方法包括向有需要的受试者施用(a)治疗有效量的第一药剂,其中该第一药剂包括化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb),或其药学上可接受的盐,和(b)治疗有效量的一种或多种第二药剂。在某些实施例中,该第一药剂和/或第二药剂可以包括药学上可接受的载体。在一些实施例中,对于该第一和第二药剂,该药学上可接受的载体是相同的,或者在该第一和第二药剂之间,该药学上可接受的载体是不同的。
在一些实施例中,本披露提供了用于治疗癌症的多种方法。所述方法包括向有需要的受试者施用(a)治疗有效量的第一药剂,其中该第一药剂包括他泽美司他或其药学上可接受的盐,和(b)治疗有效量的一种或多种第二药剂。在某些实施例中,该第一药剂和/或第二药剂可以包括药学上可接受的载体。在一些实施例中,对于该第一和第二药剂,该药学上可接受的载体是相同的,或者在该第一和第二药剂之间,该药学上可接受的载体是不同的。
在一些实施例中,该一种或多种第二药剂包括两种或更多种第二药剂(例如两种、三种、四种、或五种、或更多种不同的第二药剂)。典型地,所述一种或多种第二药剂包括治疗剂,例如化学治疗剂、免疫肿瘤学药剂、和护理标准剂或此类药剂的组合。
本披露的一些方面提供了用于治疗有需要的受试者中的癌症的EZH2抑制剂,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用于治疗有需要的受试者中的癌症的具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物,或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用于治疗有需要的受试者中的癌症的化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb),或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用于治疗有需要的受试者中的癌症的他泽美司他,或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
本披露的一些方面提供了用作用于治疗有需要的受试者中的癌症的药物的EZH2抑制剂,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用作用于治疗有需要的受试者中的癌症的药物的具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物,或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用作用于治疗有需要的受试者中的癌症的药物的化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb),或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了用作用于治疗有需要的受试者中的癌症的药物的他泽美司他,或其药学上可接受的盐,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
本披露的一些方面提供了EZH2抑制剂用于制造用于治疗有需要的受试者中的癌症的药物的用途,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物,或其药学上可接受的盐用于制造用于治疗有需要的受试者中的癌症的药物的用途,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb),或其药学上可接受的盐用于制造用于治疗有需要的受试者中的癌症的药物的用途,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
在一些实施例中,本披露提供了他泽美司他,或其药学上可接受的盐用于制造用于治疗有需要的受试者中的癌症的药物的用途,其中还向该受试者施用治疗有效量的一种或多种第二药剂。
本披露的一些方面提供了EZH2抑制剂,用于与治疗有效量的一种或多种第二药剂组合用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物或其药学上可接受的盐,用于与治疗有效量的一种或多种第二药剂组合用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb),或其药学上可接受的盐,用于与治疗有效量的一种或多种第二药剂组合用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了他泽美司他,或其药学上可接受的盐,用于与治疗有效量的一种或多种第二药剂组合用于治疗有需要的受试者中的癌症。
本披露的一些方面提供了EZH2抑制剂,其用作药物,用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物,或其药学上可接受的盐,用作药物,用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb)或其药学上可接受的盐的用途,所述用途是用作药物,用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了他泽美司他或其药学上可接受的盐的用途,所述用途是用作药物,用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
本披露的一些方面提供了EZH2抑制剂在制造药物中的用途,该药物用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了具有式(I)、(II)、(III)、(IVa)、(IVb)、(V)、或(VIa)的化合物或其药学上可接受的盐在制造药物中的用途,该药物用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb)或其药学上可接受的盐在制造药物中的用途,该药物用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,本披露提供了他泽美司他或其药学上可接受的盐在制造药物中的用途,该药物用于与治疗有效量的一种或多种第二药剂的组合疗法,用于治疗有需要的受试者中的癌症。
在一些实施例中,EZH2抑制剂的治疗有效量是约100mg至约1600mg之间的量,包括端值在内。在某些实施例中,EZH2抑制剂的治疗有效量是约100mg、约200mg、约400mg、约800mg、或约1600mg。在某些实施例中,EZH2抑制剂的治疗有效量是约800mg。
在一些实施例中,化合物(A)、(B)、(C)、(D)、(E)、(F)、(G)、(Ga)、或(Gb)或其药学上可接受的盐的治疗有效量是约100mg至约1600mg之间,包括端值在内。在某些实施例中,他泽美司他或其药学上可接受的盐的治疗有效量是约100mg、200mg、400mg、800mg、或约1600mg。在某些实施例中,他泽美司他或其药学上可接受的盐的治疗有效量是约800mg。
在一些实施例中,他泽美司他或其药学上可接受的盐的治疗有效量是约100mg至约1600mg之间,包括端值在内。在某些实施例中,他泽美司他,或其药学上可接受的盐的治疗有效量是约100mg、200mg、400mg、800mg、或约1600mg。在某些实施例中,他泽美司他或其药学上可接受的盐的治疗有效量是约800mg。
在一些实施例中,作为单剂量,或经过一段时间以多剂量,例如每天两次(BID)、每天三次等施用治疗有效量的EZH2抑制剂。例如,并且非限制,在一些实施例中,经过一周和六个月之间的时段,每天两次,以约100mg至约1600mg之间的剂量,施用本文提供的EZH2抑制剂。
在一些实施例中,每天两次(BID),例如以每次施用800mg或1600mg的剂量,施用治疗有效量的他泽美司他或其药学上可接受的盐。
在一些实施例中,口服施用治疗有效量的EZH2抑制剂。例如,在一些实施例中,作为胶囊或片剂施用治疗有效量的他泽美司他或其药学上可接受的盐。
在一些实施例中,口服施用治疗有效量的EZH2抑制剂,例如他泽美司他或其药学上可接受的盐。例如,在一些实施例中,作为胶囊或片剂,或作为液体悬浮液,口服施用治疗有效量的EZH2抑制剂,例如他泽美司他或其药学上可接受的盐。在一些实施例中,胃肠外,例如静脉内施用治疗有效量的EZH2抑制剂。例如,在一些实施例中,作为注射溶液或悬浮液,胃肠外施用治疗有效量的EZH2抑制剂。
本文提供的方法的一些实施例包括治疗肺癌,例如非小细胞肺癌。本文提供的方法的一些实施例包括用EZH2抑制剂,例如他泽美司他或其药学上可接受的盐,并且用一种或多种第二药剂(例如一种、两种、三种、四种、或五种不同的第二药剂)治疗肺癌,例如非小细胞肺癌。本文提供的方法的一些实施例包括用EZH2抑制剂,例如用他泽美司他或其药学上可接受的盐,并且用两种或更多种第二药剂(例如两种、三种、四种、或五种不同的第二药剂)治疗肺癌,例如非小细胞肺癌。
本文提供的化合物的一些实施例包括多种化合物,用于治疗肺癌,例如非小细胞肺癌。本文提供的化合物的一些实施例包括他泽美司他或其药学上可接受的盐,和一种或多种第二药剂(例如一种、两种、三种、四种、或五种不同的第二药剂),用于治疗肺癌,例如非小细胞肺癌。本文提供的化合物的一些实施例包括他泽美司他,或其药学上可接受的盐,和两种或更多种第二药剂(例如两种、三种、四种、或五种不同的第二药剂),用于治疗肺癌,例如非小细胞肺癌。
本文提供的化合物的一些实施例包括多种化合物,用作用于治疗肺癌,例如非小细胞肺癌的药物。本文提供的化合物的一些实施例包括他泽美司他或其药学上可接受的盐,和一种或多种第二药剂(例如一种、两种、三种、四种、或五种不同的第二药剂),用作用于治疗肺癌,例如非小细胞肺癌的药物。本文提供的化合物的一些实施例包括他泽美司他或其药学上可接受的盐,和两种或更多种第二药剂(例如两种、三种、四种、或五种不同的第二药剂),用作用于治疗肺癌,例如非小细胞肺癌的药物。
本文提供的化合物的用途的一些实施例包括多种化合物在制造药物中的用途,该药物用于治疗肺癌,例如非小细胞肺癌。本文提供的化合物的用途的一些实施例包括他泽美司他或其药学上可接受的盐,和一种或多种第二药剂(例如一种、两种、三种、四种、或五种不同的第二药剂),用于制造药物,该药物用于治疗肺癌,例如非小细胞肺癌。本文提供的化合物的用途的一些实施例包括他泽美司他,或其药学上可接受的盐,和两种或更多种第二药剂(例如两种、三种、四种、或五种不同的第二药剂)在制造药物中的用途,该药物用于治疗肺癌,例如非小细胞肺癌。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括烷化剂或类烷化剂、抗肿瘤剂、有丝分裂抑制剂、微管蛋白聚合抑制剂、抗代谢药、DNA甲基转移酶(DNMT)抑制剂、组蛋白脱乙酰酶(HDAC)抑制剂、拓扑异构酶抑制剂、表皮生长因子受体(EFGR)抑制剂、EFGR和ErbB2的抑制剂、EFGR和人表皮生长因子受体2(Her2)的抑制剂、间变性淋巴瘤激酶(ALK)抑制剂、ALK和ROS1的抑制剂、ALK和EGFR的抑制剂、细胞周期蛋白依赖性激酶(CDK)4/6抑制剂、促分裂原活化蛋白激酶(MEK)抑制剂、BRAF抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂、Wee1抑制剂、聚(ADP-核糖)聚合酶(PARP)抑制剂、糖皮质激素受体激动剂、维甲酸受体激动剂、CBP/p300抑制剂、或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括烷化剂或类烷化剂。因此,在本披露的一些实施例中,与烷化剂或类烷化剂组合施用EZH2抑制剂(例如他泽美司他)。是烷化剂或类烷化剂的示例性第二药剂包括但不限于顺铂。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括抗肿瘤剂。因此,在本披露的一些实施例中,与抗肿瘤剂组合施用EZH2抑制剂(例如他泽美司他)。是抗肿瘤剂的示例性第二药剂包括但不限于奥沙利铂。
在本披露的某些实施例中,并且特别是其中癌症是非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括有丝分裂抑制剂。因此,在本披露的一些实施例中,与有丝分裂抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是有丝分裂抑制剂的示例性第二药剂包括但不限于紫杉醇、多西他赛、或长春碱。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括微管蛋白聚合抑制剂。因此,在本披露的一些实施例中,与微管蛋白聚合抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是微管蛋白聚合抑制剂的示例性第二药剂包括但不限于长春瑞滨。
在本披露的某些实施例中,并且特别是其中癌症是非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括抗代谢药。在另外的实施例中,所述一种或多种第二药剂包括叶酸型的抗代谢药。是抗代谢药的示例性第二药剂包括但不限于吉西他滨。是叶酸型的抗代谢药的示例性第二药剂包括但不限于甲氨蝶呤、培美曲塞或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括DNA甲基转移酶(DNMT)抑制剂。因此,在本披露的一些实施例中,与DNA甲基转移酶(DNMT)抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是DNA甲基转移酶(DNMT)抑制剂的示例性第二药剂包括但不限于地西他滨、阿扎胞苷、或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括组蛋白脱乙酰酶(HDAC)抑制剂。因此,在本披露的一些实施例中,与HDAC抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是HDAC抑制剂的示例性第二药剂包括但不限于伏立诺他。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括拓扑异构酶抑制剂。因此,在本披露的一些实施例中,与拓扑异构酶抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是拓扑异构酶抑制剂的示例性第二药剂包括但不限于伊立替康、依托泊苷或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括表皮生长因子受体(EFGR)抑制剂。因此,在本披露的一些实施例中,与EFGR抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是EFGR抑制剂的示例性第二药剂包括但不限于埃罗替尼、吉非替尼、AZD9291、或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括表皮生长因子受体(EFGR)和ErbB2的抑制剂。因此,在本披露的一些实施例中,与EFGR和ErbB2的抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是EFGR和ErbB2的抑制剂的示例性第二药剂包括但不限于拉帕替尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括表皮生长因子受体(EFGR)和人表皮生长因子受体2(Her2)的抑制剂。因此,在本披露的一些实施例中,与EFGR和Her2的抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是EFGR和Her2的抑制剂的示例性第二药剂包括但不限于阿法替尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括间变性淋巴瘤激酶(ALK)抑制剂。因此,在本披露的一些实施例中,与ALK抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是ALK抑制剂的示例性第二药剂包括但不限于色瑞替尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括间变性淋巴瘤激酶(ALK)和ROS1的抑制剂。因此,在本披露的一些实施例中,与ALK和ROS1的抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是ALK和ROS1的抑制剂的示例性第二药剂包括但不限于克唑替尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括间变性淋巴瘤激酶(ALK)和表皮生长因子受体(EFGR)的抑制剂。因此,在本披露的一些实施例中,与抑制剂ALK和EFGR组合施用EZH2抑制剂(例如他泽美司他)。是ALK和EFGR的抑制剂的示例性第二药剂包括但不限于布加替尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括细胞周期蛋白依赖性激酶(CDK)4/6抑制剂。因此,在本披露的一些实施例中,与周细胞周期蛋白依赖性激酶(CDK)4/6抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是周细胞周期蛋白依赖性激酶(CDK)4/6抑制剂的示例性第二药剂包括但不限于阿贝西尼、帕博西尼、瑞博西尼、或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括促分裂原活化蛋白激酶(MEK)抑制剂。因此,在本披露的一些实施例中,与MEK抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是MEK抑制剂的示例性第二药剂包括但不限于曲美替尼、司美替尼、或其组合。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括BRAF抑制剂。因此,在本披露的一些实施例中,与BRAF抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是BRAF抑制剂的示例性第二药剂包括但不限于威罗菲尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括磷脂酰肌醇3-激酶(PI3K)抑制剂。因此,在本披露的一些实施例中,与PI3K抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是PI3K抑制剂的示例性第二药剂包括但不限于匹替利司或BKM-120。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括Wee1抑制剂。因此,在本披露的一些实施例中,与Wee1抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是Wee1抑制剂的示例性第二药剂包括但不限于MK-1775。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括聚(ADP-核糖)聚合酶(PARP)抑制剂。因此,在本披露的一些实施例中,与PARP抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是PARP抑制剂的示例性第二药剂包括但不限于维利帕尼。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括糖皮质激素受体激动剂。因此,在本披露的一些实施例中,与糖皮质激素受体激动剂组合施用EZH2抑制剂(例如他泽美司他)。是糖皮质激素受体激动剂的示例性第二药剂包括但不限于泼尼松龙。
在本披露的某些实施例中,并且特别是其中癌症是肺癌,例如非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括维甲酸受体激动剂。因此,在本披露的一些实施例中,与维甲酸受体激动剂组合施用EZH2抑制剂(例如他泽美司他)。是维甲酸受体激动剂的示例性第二药剂包括但不限于ATRA。
在本披露的某些实施例中,并且特别是其中癌症是非小细胞肺癌的那些实施例中,所述一种或多种第二药剂包括CBP/p300抑制剂。因此,在本披露的一些实施例中,与CBP/p300抑制剂组合施用EZH2抑制剂(例如他泽美司他)。是CBP/p300抑制剂受体激动剂的示例性第二药剂包括但不限于以下化合物H。
或其药学上可接受的盐。
化合物H,(N-(4-氟苄基)-2-[(3'R,4S)-3'-氟-5'-{1-[2-(甲氨基)-2-氧代乙基]-1H-吡唑-4-基}-2,5-二氧代-2',3'-二氢-1H-螺[咪唑啉-4,1'-茚]-1-基]-N-[(2S)-1,1,1-三氟丙-2-基]乙酰胺,描述于WO2016/044770中,将其全部内容通过引用结合在此。
在一些实施例中,以每天0.01mg/kg至每天约1000mg/kg的剂量施用本披露的第二抗癌剂。
在一些实施例中,同时施用治疗有效量的EZH2抑制剂和第二药剂。可替代地,顺序施用治疗有效量的EZH2抑制剂和一种或多种第二药剂。在某些实施例中,在一种或多种第二药剂之前施用EZH2抑制剂。在某些实施例中,在EZH2抑制剂之前施用一种或多种第二药剂。
在其中组合施用EZH2抑制剂(例如他泽美司他)和一种或多种第二药剂的一些实施例中,同时施用EZH2抑制剂和第二药剂。在其中组合施用EZH2抑制剂(例如他泽美司他)和一种或多种第二药剂的一些实施例中,顺序施用EZH2抑制剂和第二药剂。在其中组合施用EZH2抑制剂(例如他泽美司他)和一种或多种第二药剂的一些实施例中,在一种或多种第二药剂之前施用EZH2抑制剂。在其中组合施用EZH2抑制剂(例如他泽美司他)和一种或多种第二药剂的一些实施例中,在EZH2抑制剂之前施用一种或多种第二药剂。
在其中组合施用EZH2抑制剂(例如他泽美司他)和一种或多种第二药剂的一些实施例中,同时施用治疗有效量的EZH2抑制剂,例如他泽美司他或其药学上可接受的盐,和第二药剂。可替代地,顺序施用治疗有效量的EZH2抑制剂,例如他泽美司他或其药学上可接受的盐,和一种或多种第二药剂。在某些实施例中,在一种或多种第二药剂之前施用EZH2抑制剂,例如他泽美司他或其药学上可接受的盐。在某些实施例中,在EZH2抑制剂,例如他泽美司他或其药学上可接受的盐之前施用一种或多种第二药剂。
在本披露的某些实施例中,EZH2抑制剂是以下具有式(VIa)的化合物。
在一些实施例中,具有式(VIa)的化合物可包以括以下特征中的一者或多者:
Ra和Rb各自独立地是H或C1-C6烷基。
Ra和Rb与其所附接的N原子一起是具有0或1个另外的杂原子的4至7元杂环烷基环、任选地经一个或多个-Q3-T3取代的C1-C6烷基和4至12元(例如,4至7元)杂环烷基环。
Q3是键或未经取代或经取代的C1-C3烷基接头。
T3是H、卤素、4至7元杂环烷基、C1-C3烷基、ORd、COORd、-S(O)2Rd、或-NRdRe,Rd和Re各自独立地是H或C1-C6烷基。
R7是C1-C6烷基、C3-C8环烷基或4至12元(例如,4至7元)杂环烷基,这些基团各自任选地经一个或多个-Q5-T5取代。例如,R7不是H。
R7是任选地经一个或多个-Q5-T5取代的4至7元杂环烷基。
R7是哌啶基、四氢吡喃、环戊基、或环己基,这些基团各自任选地经一个Q5-T5取代。
T5是H、卤素、C1-C6烷基、C1-C6烷氧基、C3-C8环烷基、C6-C10芳基、或4至12元(例如,4至7元)杂环烷基。
Q5是键,并且T5是C1-C6烷基、C3-C8环烷基、或4至12元(例如,4至7元)杂环烷基。
Q5是CO、S(O)2、或NHC(O);并且T5是C1-C6烷基、C1-C6烷氧基、C3-C8环烷基、或4至12元(例如,4至7元)杂环烷基。
Q5是C1-C3烷基接头,并且T5是H或C6-C10芳基。
Q5是C1-C3烷基接头,并且T5是C3-C8环烷基、4至7元杂环烷基、或S(O)qRq。
R7是环戊基或环己基,这些基团各自任选地经一个Q5-T5取代。
Q5是NHC(O),并且T5是C1-C6烷基或C1-C6烷氧基。
R7是异丙基。
R2和R4各自独立地是H或任选地经氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、或C6-C10芳基取代的C1-C6烷基。
R8是H、甲基、或乙基。
R8是甲基。
R8是乙基。
R8是4至7-杂环烷基,例如,四氢吡喃。
在本披露的某些实施例中,具有式(VIa)的化合物是具有以下式的他泽美司他(本文也称为化合物(A),并且也称为化合物44、EPZ-6438、和E7438):
或其药学上可接受的盐或溶剂化物。
可以通过任何适当的途径,包括但不限于肠内途径,和非肠道途径,例如口服途径、静脉途径、肌内途径、以及通过粘膜组织直接吸收,施用本披露的治疗剂(包括第一药剂和/或一种或多种第二药剂)。可以通过相同途径或通过不同途径施用这些治疗剂。
用于本披露所展示的组合疗法的方法、或化合物或药物可以导致协同效应,其中治疗剂(例如EZH2抑制剂,例如他泽美司他或其药学上可接受的盐,和一种或多种第二抗癌剂)的组合的效果大于由作为单一药剂的治疗剂中任一种的施用所导致的效果的总和。协同效应还可以是任何治疗剂作为单一药剂施用时所不能达到的效果。协同效应可以包括但不限于治疗癌症,例如非小细胞肺癌的效果,例如通过减小肿瘤尺寸、减少受试者中或从受试者获得的样品中恶性细胞的数量或频率,抑制肿瘤生长,抑制恶性细胞的生长、生存、或增生,或增加受试者的生存期。协同效应还可以包括降低癌症细胞活力、诱发癌症细胞死亡、和抑制或延迟癌症细胞生长。
在一些实施例中,如本披露提供的受试者患有癌症,包括但不限于非小细胞肺癌。受试者可以是任何物种;然而,受试者优选地是人类。在一些实施例中,受试者可以患有特征在于任何阶段的癌症,包括但不限于阶段0、I、II、III、和IV。在一些实施例中,受试者的癌症是原发性或继发性肿瘤。受试者的癌症可以是转移性的。受试者的癌症可以已经从另一个原发位置转移至继发位置。在一些实施例中,受试者的非小细胞肺癌可以转移,或可以已经转移,从骨髓的一个区域至另一个区域。
在一些实施例中,如本文提供的受试者,例如患有非小细胞肺癌的受试者,可以表达野生型EZH2。
在一些实施例中,如本文提供的受试者,例如患有非小细胞肺癌的受试者,可以表达突变型EZH2。例如,突变体EZH2包括一个或多个突变,其中该突变是取代、点突变、无义突变、错义突变、缺失、或插入。本披露的突变型EZH2可以包括在底物口袋结构域中的突变。突变体EZH2可在氨基酸Y641处具有取代。在一些实施例中,突变型EZH2具有以下突变之一:苯丙氨酸(F)取代在氨基酸位置641处的野生型残基酪氨酸(Y)(Y641F);组氨酸(H)取代在氨基酸位置641处的野生型残基酪氨酸(Y)(Y641H);天冬酰胺(N)取代在氨基酸位置641处的野生型残基酪氨酸(Y)(Y641N);丝氨酸(S)取代在氨基酸位置641处的野生型残基酪氨酸(Y)(Y641S);以及半胱氨酸(C)取代在氨基酸位置641处的野生型残基酪氨酸(Y)(Y641C)。
在一些实施例中,EZH2突变体可以包括但不限于:甘氨酸(G)取代野在氨基酸位置677处的生型残基丙氨酸(A)(A677G);缬氨酸(V)取代在氨基酸位置687处的野生型残基丙氨酸(A)(A687V);甲硫氨酸(M)取代在氨基酸位置674处的野生型残基缬氨酸(V)(V674M);组氨酸(H)取代在氨基酸位置685处的野生型残基精氨酸(R)(R685H);半胱氨酸(C)取代在氨基酸位置685处的野生型残基精氨酸(R)(R685C);丝氨酸(S)取代在氨基酸位置322处的野生型残基天冬酰胺(N)(N322S),谷氨酰胺(Q)取代在氨基酸位置288处的野生型残基精氨酸(R)(R288Q),异亮氨酸(I)取代在氨基酸位置573处的野生型残基苏氨酸(T)(T573I),谷氨酸(E)取代在氨基酸位置664处的野生型残基天冬氨酸(D)(D664E),谷氨酰胺(Q)取代在氨基酸位置458处的野生型残基精氨酸(R)(R458Q),赖氨酸(K)取代在氨基酸位置249处的野生型残基谷氨酸(E)(E249K),半胱氨酸(C)取代在氨基酸位置684处的野生型残基精氨酸(R)(R684C),组氨酸(H)取代在氨基酸位置628处的野生型残基精氨酸(R)(R628H),组氨酸(H)取代在氨基酸位置501处的野生型残基谷氨酰胺(Q)(Q501H),天冬酰胺(N)取代在氨基酸位置192处的野生型残基天冬氨酸(D)(D192N),缬氨酸(V)取代在氨基酸位置664处的野生型残基天冬氨酸(D)(D664V),亮氨酸(L)取代在氨基酸位置704处的野生型残基缬氨酸(V)(V704L),丝氨酸(S)取代在氨基酸位置132处的野生型残基脯氨酸(P)(P132S),赖氨酸(K)取代在氨基酸位置669处的野生型残基谷氨酸(E)(E669K),苏氨酸(T)取代在氨基酸位置255处的野生型残基丙氨酸(A)(A255T),缬氨酸(V)取代在氨基酸位置726处的野生型残基谷氨酸(E)(E726V),酪氨酸(Y)取代在氨基酸位置571处的野生型残基半胱氨酸(C)(C571Y),半胱氨酸(C)取代在氨基酸位置145处的野生型残基苯丙氨酸(F)(F145C),苏氨酸(T)取代在氨基酸位置693处的野生型残基天冬酰胺(N)(N693T),丝氨酸(S)取代在氨基酸位置145处的野生型残基苯丙氨酸(F)(F145S),组氨酸(H)取代在氨基酸位置109处的野生型残基谷氨酰胺(Q)(Q109H),半胱氨酸(C)取代在氨基酸位置622处的野生型残基苯丙氨酸(F)(F622C),精氨酸(R)取代在氨基酸位置135处的野生型残基甘氨酸(G)(G135R),谷氨酰胺(Q)取代在氨基酸位置168处的野生型残基精氨酸(R)(R168Q),精氨酸(R)取代在氨基酸位置159处的野生型残基甘氨酸(G)(G159R),半胱氨酸(C)取代在氨基酸位置310处的野生型残基精氨酸(R)(R310C),组氨酸(H)取代在氨基酸位置561处的野生型残基精氨酸(R)(R561H),组氨酸(H)取代在氨基酸位置634处的野生型残基精氨酸(R)(R634H),精氨酸(R)取代在氨基酸位置660处的野生型残基甘氨酸(G)(G660R),半胱氨酸(C)取代在氨基酸位置181处的野生型残基酪氨酸(Y)(Y181C),精氨酸(R)取代在氨基酸位置297处的野生型残基组氨酸(H)(H297R),丝氨酸(S)取代在氨基酸位置612处的野生型残基半胱氨酸(C)(C612S),酪氨酸(Y)取代在氨基酸位置694处的野生型残基组氨酸(H)(H694Y),丙氨酸(A)取代在氨基酸位置664处的野生型残基天冬氨酸(D)(D664A),苏氨酸(T)取代在氨基酸位置150处的野生型残基异亮氨酸(I)(I150T),精氨酸(R)取代在氨基酸位置264处的野生型残基异亮氨酸(I)(I264R),亮氨酸(L)取代在氨基酸位置636处的野生型残基脯氨酸(P)(P636L),苏氨酸(T)取代在氨基酸位置713处的野生型残基异亮氨酸(I)(I713T),脯氨酸(P)取代在氨基酸位置501处的野生型残基谷氨酰胺(Q)(Q501P),谷氨酰胺(Q)取代在氨基酸位置243处的野生型残基赖氨酸(K)(K243Q),天冬氨酸(D)取代在氨基酸位置130处的野生型残基谷氨酸(E)(E130D),甘氨酸(G)取代在氨基酸位置509处的野生型残基精氨酸(R)(R509G),组氨酸(H)取代在氨基酸位置566处的野生型残基精氨酸(R)(R566H),组氨酸(H)取代在氨基酸位置677处的野生型残基天冬氨酸(D)(D677H),天冬酰胺(N)取代在氨基酸位置466处的野生型残基赖氨酸(K)(K466N),组氨酸(H)取代在氨基酸位置78处的野生型残基精氨酸(R)(R78H),甲硫氨酸(M)取代在氨基酸位置1处的野生型残基赖氨酸(K)(K6M),亮氨酸(L)取代在氨基酸位置538处的野生型残基丝氨酸(S)(S538L),谷氨酰胺(Q)取代在氨基酸位置149处的野生型残基亮氨酸(L)(L149Q),缬氨酸(V)取代在氨基酸位置252处的野生型残基亮氨酸(L)(L252V),缬氨酸(V)取代在氨基酸位置674处的野生型残基亮氨酸(L)(L674V),缬氨酸(V)取代在氨基酸位置656处的野生型残基丙氨酸(A)(A656V),天冬氨酸(D)取代在氨基酸位置731处的野生型残基丙氨酸(A)(Y731D),苏氨酸(T)取代在氨基酸位置345处的野生型残基丙氨酸(A)(A345T),天冬氨酸(D)取代在氨基酸位置244处的野生型残基丙氨酸(A)(Y244D),色氨酸(W)取代在氨基酸位置576处的野生型残基半胱氨酸(C)(C576W),赖氨酸(K)取代在氨基酸位置640处的野生型残基天冬酰胺(N)(N640K),赖氨酸(K)取代在氨基酸位置675处的野生型残基天冬酰胺(N)(N675K),酪氨酸(Y)取代在氨基酸位置579处的野生型残基天冬氨酸(D)(D579Y),异亮氨酸(I)取代在氨基酸位置693处的野生型残基天冬酰胺(N)(N693I),和/或赖氨酸(K)取代在氨基酸位置693处的野生型残基天冬酰胺(N)(N693K)。
EZH2的其他突变可以包括:在氨基酸位置730、391、461、441、235、254、564、662、715、405、685、64、73、656、718、374、592、505、730、或363处,或核酸序列的相应核苷酸位置处的移码;在氨基酸位置148和149处的谷氨酸(E)和亮氨酸(L)的缺失,或者在氨基酸位置733、25、317、62、553、328、58、207、123、63、137、或60处的无义突变。
除非另有定义,否则本文所用的所有技术和科学术语都具有与本披露所属领域的普通技术人员通常所理解的相同的含义。在本说明书中,单数形式也包括复数形式,除非上下文另有明确指示。尽管在本披露的实践或测试中可以使用与本文所述的那些相似或等效的方法和材料,但是下文描述了一些示例性的、非限制性的适合的方法和材料。本文提及的所有出版物、专利申请、专利和其他参考文献均通过援引并入本文。本文所引用的参考文献不被视为所要求保护的发明的现有技术。在发生冲突的情况下,以本说明书(包括定义)为准。另外,这些材料、方法和实例仅是说明性的并且不旨在进行限制。
根据以下详细描述和权利要求书,本发明的其他特征和优点将变得显而易见。
附图说明
本专利或申请文件含有至少一张彩色附图。具有一张或多张彩色附图的本专利或专利申请公开的副本将根据请求并在支付必要的费用后由专利局提供。
以上和另外特征将从结合附图时进行的以下详细描述而得以更清楚理解。
图1是概述实例1的实验程序的示意图。
图2是一组图,说明在A427细胞中,地西他滨与EZH2抑制剂(他泽美司他)的协同。图A是体外测定的剂量矩阵。图B显示了他泽美司他与地西他滨的组合的Loewe过量矩阵。图C显示了他泽美司他与地西他滨组合的等效线图。
图3是一组图,说明在A427细胞中,曲美替尼与EZH2抑制剂(他泽美司他)的协同。图A是体外测定的剂量矩阵。图B显示了他泽美司他与曲美替尼的组合的Loewe过量矩阵。图C显示了他泽美司他与曲美替尼组合的等效线图。
图4是一组图,说明在A427细胞中,帕博西尼与EZH2抑制剂(他泽美司他)的协同。图A是体外测定的剂量矩阵。图B显示了他泽美司他与帕博西尼的组合的Loewe过量矩阵。图C显示了他泽美司他与帕博西尼组合的等效线图。
图5是一组图,说明在A427细胞中,色瑞替尼与EZH2抑制剂(他泽美司他)的协同。图A是体外测定的剂量矩阵。图B显示了他泽美司他与色瑞替尼的组合的Loewe过量矩阵。图C显示了他泽美司他与色瑞替尼组合的等效线图。
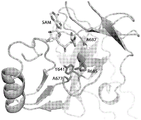
图6是EZH2蛋白结构的说明。
具体实施方式
本披露的一些方面提供了用于组合疗法的方法、策略、组合物、和组合,该组合疗法用于治疗受试者中的癌症,例如非小细胞肺癌,包括向受试者施用EZH2抑制剂和第二抗癌剂。在一些实施例中,该EZH2抑制剂是本文提供的化合物。在一些实施例中,该EZH2抑制剂是他泽美司他或其药学上可接受的盐。在一些实施例中,该EZH2抑制剂与第二抗癌剂协同的组合实现了希望的临床效果。
EZH2
EZH2是一种组蛋白甲基转移酶,它是PRC2复合物的催化亚基,该复合物催化组蛋白H3上的赖氨酸27(H3-K27)的单至三甲基化。组蛋白H3-K27三甲基化是一种抑制接近组蛋白修饰位点的特定基因的转录的机制。已知这种三甲基化是在癌症(如前列腺癌)中具有改变的表达的癌症标志物(参见例如美国专利申请公开号2003/0175736;通过援引以其全文并入本文)。其他研究提供了异常调节的EZH2表达、转录抑制与肿瘤性转化之间的功能联系的证据。Varambally等人(2002)Nature[自然]419(6907):624-9Kleer等人(2003)ProcNatl Acad Sci USA[美国国家科学院院刊]100(20):11606-11。
先前已经描述了人EZH2核酸和多肽。参见例如Chen等人(1996)Genomics[基因组学]38:30-7[746个氨基酸];Swiss-Prot登录号Q15910[746个氨基酸];GenBank登录号NM_004456和NP_004447(同种型a[751个氨基酸]);以及GenBank登录号NM_152998和NP_694543(同种型b[707个氨基酸]),它们各自通过援引以其全文并入本文。
还出于本申请的目的,人类EZH2的Y641突变体,和相等地,EZH2的Y641突变体应被理解为是指人类EZH2中对应于野生型人类EZH2的Y641的氨基酸残基被除酪氨酸外的氨基酸残基取代。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被除酪氨酸外的氨基酸残基取代。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被苯基丙氨酸(F)取代。对应于这些实施例的EZH2的Y641突变体本文被称为Y641F突变体,或等同地,Y641F。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被组氨酸(H)取代。对应于这些实施例的EZH2的Y641突变体本文被称为Y641H突变体,或等同地,Y641H。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被天冬酰胺(N)取代。对应于这些实施例的EZH2的Y641突变体本文被称为Y641N突变体,或等同地,Y641N。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被丝氨酸(S)取代。对应于这些实施例的EZH2的Y641突变体本文被称为Y641S突变体,或等同地,Y641S。
在一些实施例中,EZH2的Y641突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的Y641的单个氨基酸残基被半胱氨酸(C)取代。对应于这些实施例的EZH2的Y641突变体本文被称为Y641C突变体,或等同地,Y641C。
在一些实施例中,EZH2的A677突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的A677的单个氨基酸残基被非丙氨酸的氨基酸,优选是甘氨酸(G)取代。对应于这些实施例的EZH2的A677突变体本文被称为A677突变体,并且优选是A677G突变体,或等同地,A677G。
在一些实施例中,EZH2的A687突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的A687的单个氨基酸残基被非丙氨酸的氨基酸,优选是缬氨酸(V)取代。对应于这些实施例的EZH2的A687突变体本文被称为A687突变体,并且优选是A687V突变体,或等同地,A687V。
在一些实施例中,EZH2的R685突变体的氨基酸序列不同于野生型人类EZH2的氨基酸序列,不同之处仅是相应于野生型人类EZH2的R685的单个氨基酸残基被非丙氨酸的氨基酸,优选是组氨酸(H)或半胱氨酸(C)取代。对应于这些实施例的EZH2的R685突变体本文被称为R685突变体,并且优选是R685C突变体或R685H突变体,或等同地,R685H或R685C。
对EZH2杂合的细胞预期会显示一个恶性表型,这是因为通过WT酶有效的形成H3-K27me1,并且随后通过突变体酶的形式有效的将这个源种类转换成H3-K27me2,以及特别是,H3-K27me3。
先前的结果指向对执行H3-K27单甲基化的酶之间的酶偶合以及对EZH2导致滤泡性淋巴瘤和弥漫性大B细胞淋巴瘤中发病机理的某些突变体形式的依赖性。例如,表达Y641突变体EZH2的细胞对小分子EZH2抑制剂可能比表达WT EZH2的细胞更敏感。具体而言,表达Y641突变体EZH2的细胞在EZH2抑制剂治疗后显示减少的生长、分裂或增生,甚至发生细胞凋亡或坏死。相比之下,表达WT EZH2的细胞不响应于EZH2抑制剂的抗增生作用(美国专利申请号13/230,703(现为美国专利8,895,245);通过引用以其全文结合在此)。
本披露的一些方面涉及通过向表达野生型或突变型EZH2的受试者施用与适合同时地、顺序地、或交替地一起施用的第二抗癌剂组合的治疗有效量如本文所述的EZH2抑制剂(例如,具有式(I)-(VIa)的化合物(优选地他泽美司他)),来治疗或缓解受试者的癌症或癌前病症的症状。
本发明的一些方面涉及在受试者中抑制H3-K27转化成三甲基化的H3-K27。该抑制可能涉及在受试者中抑制非甲基化的H3-K27转化成单甲基化H3-K27、单甲基化H3-K27转化成二甲基化H3-K27、二甲基化H3-K27转化成三甲基化H3-K27、或其任何组合,包括,例如单甲基化H3-K27转化成二甲基化H3-K27和二甲基化H3-K27转化成三甲基化H3-K27。如本文所用,未甲基化H3-K27是指其中没有甲基与赖氨酸27的氨基共价连接的组蛋白H3。如本文所用,单甲基化H3-K27是指其中单个甲基与赖氨酸27的氨基共价连接的组蛋白H3。单甲基化H3-K27在本文中也被称为H3-K27me1。如本文所用,二甲基化H3-K27是指其中两个甲基与赖氨酸27的氨基共价连接的组蛋白H3。二甲基化H3-K27在本文中也被称为H3-K27me2。如本文所用,三甲基化H3-K27是指其中三个甲基与赖氨酸27的氨基共价连接的组蛋白H3。三甲基化H3-K27在本文中也被称为H3-K27me3。
组蛋白H3是136个氨基酸长的蛋白质,其序列是已知的。参见例如,GenBank登录号CAB02546,其内容通过引用结合在此。如本文进一步披露的,除全长组蛋白H3外,包含对应于全长组蛋白H3的K27的赖氨酸残基的组蛋白H3的肽片段可以用作EZH2的底物(并且同样用于EZH2的突变体形式)以评估H3-K27m1至H3-K27m2的转化,以及H3-K27m2至H3-K27m3的转化。在一些实施例中,这种肽片段对应于组蛋白H3的氨基酸残基21-44。
EZH2抑制剂
适合根据本披露使用的示例性EZH2抑制剂包括具有式(I)-(VIa)的化合物。适用于本披露方法的具有式(I)-(VIa)的其他化合物描述于美国公开案20120264734中,将其内容通过引用以其全文而特此结合。
在一些实施例中,本披露的EZH2抑制剂可以具有以下式I:
R701是H、F、OR707、NHR707、-(C≡C)-(CH2)n7-R708、苯基、5或6元杂芳基、C3-8环烷基或含有1-3个杂原子的4-7元杂环烷基,其中苯基、5或6元杂芳基、C3-8环烷基或4-7元杂环烷基各自独立地任选地被一个或多个选自以下的基团取代:卤素、C1-3烷基、OH、O-C1-6烷基、NH-C1-6烷基和被C3-8环烷基或含有1-3个杂原子的4-7元杂环烷基取代的C1-3烷基,其中O-C1-6烷基和NH-C1-6烷基各自任选地被羟基、O-C1-3烷基或NH-C1-3烷基取代,O-C1-3烷基和NH-C1-3烷基各自任选地被O-C1-3烷基或NH-C1-3烷基进一步取代;
R702和R703各自独立地是H、卤素、C1-4烷基、C1-6烷氧基或C6-C10芳氧基,这些基团各自任选地被一个或多个卤素取代;
R704和R705各自独立地是C1-4烷基;
R706是经N(C1-4烷基)2取代的环己基,其中一个或两个C1-4烷基经C1-6烷氧基取代;或R706是四氢吡喃基;
R707是任选地被一个或多个选自以下的基团取代的C1-4烷基:羟基、C1-4烷氧基、氨基、单或二-C1-4烷基氨基、C3-8环烷基和含有1-3个杂原子的4-7元杂环烷基,其中C3-8环烷基或4-7元杂环烷基各自独立地任选地被C1-3烷基进一步取代;
R708是任选地被一个或多个选自以下的基团取代的C1-4烷基:OH、卤素和C1-4烷氧基、含有1-3个杂原子的4-7元杂环烷基或O-C1-6烷基,其中4-7元杂环烷基可任选地被OH或C1-6烷基进一步取代;并且
n7是0、1或2。
例如,R706是被N(C1-4烷基)2取代的环己基,其中一个C1-4烷基未被取代且另一个被甲氧基取代。
在一些实施例中,本披露的EZH2抑制剂可以具有以下式II:
例如,R702是甲基或异丙基并且R703是甲基或甲氧基。
例如,R704是甲基。
例如,R701是OR707并且R707是任选地被OCH3或吗啉取代的C1-3烷基。
例如,R701是H或F。
例如,R701是四氢吡喃基、苯基、吡啶基、嘧啶基、吡嗪基、咪唑基或吡唑基,这些基团各自任选地被以下基团取代:甲基、甲氧基、被吗啉取代的乙基、或-OCH2CH2OCH3。
例如,R708是吗啉、哌啶、哌嗪、吡咯烷、二氮杂环庚烷或氮杂环丁烷,这些基团各自任选地被以下基团取代:OH或C1-6烷基。
例如,R708是吗啉
例如,R708是被C1-6烷基取代的哌嗪。
例如,R708是甲基、叔丁基或C(CH3)2OH。
在一些实施例中,本披露的EZH2抑制剂可以具有以下式III:
在该式中:
R801是C1-6烷基、C2-6烯基、C2-6炔基、C3-8环烷基、含有1-3个杂原子的4-7元杂环烷基、苯基或5或6元杂芳基,这些基团各自被O-C1-6烷基-Rx或NH-C1-6烷基-Rx取代,其中Rx是羟基、O-C1-3烷基或NH-C1-3烷基,并且Rx任选地被O-C1-3烷基或NH-C1-3烷基进一步取代,但Rx是羟基时除外;或R801是被-Q2-T2取代的苯基,其中Q2是键或任选地被卤素、氰基、羟基或C1-C6烷氧基取代的C1-C3烷基接头,并且T2是任选地被取代的4至12元杂环烷基;并且R801任选地被进一步取代;
R802和R803各自独立地是H、卤素、C1-4烷基、C1-6烷氧基或C6-C10芳氧基,这些基团各自任选地被一个或多个卤素取代;
R804和R805各自独立地是C1-4烷基;并且
R806是-Qx-Tx,其中Qx是键或C1-4烷基接头,Tx是H、任选地被取代的C1-4烷基、任选地被取代的C3-C8环烷基或任选地被取代的4至14元杂环烷基。
例如,Qx和Q2各自独立地是键或甲基接头,并且Tx和T2各自独立地是四氢吡喃基、被1、2或3个C1-4烷基取代的哌啶基或被N(C1-4烷基)2取代的环己基,其中C1-4烷基中的一者或两者任选地被C1-6烷氧基取代;
例如,R806是被N(C1-4烷基)2取代的环己基,或者R806是四氢吡喃基。
例如,R801是被O-C1-6烷基-Rx取代的苯基或5或6元杂芳基,或者R801是被CH2-四氢吡喃基取代的苯基。
本披露的EZH2抑制剂可以具有以下式IVa或IVb:
例如,R807是-CH2CH2OH、-CH2CH2OCH3或-CH2CH2OCH2CH2OCH3。
例如,R802是甲基或异丙基并且R803是甲基或甲氧基。
例如,R804是甲基。
本披露的EZH2抑制剂可以具有以下式(V):
在该式中:
R2、R4和R12各自独立地是C1-6烷基;
R6是C6-C10芳基或5或6元杂芳基,这些基团各自任选地被一个或多个-Q2-T2取代,其中Q2是键或任选地被卤素、氰基、羟基或C1-C6烷氧基取代的C1-C3烷基接头,并且T2是H、卤素、氰基、-ORa、-NRaRb、-(NRaRbRc)+A-、-C(O)Ra、-C(O)ORa、-C(O)NRaRb、-NRbC(O)Ra、-NRbC(O)ORa、-S(O)2Ra、-S(O)2NRaRb或RS2,其中Ra、Rb和Rc各自独立地是H或RS3,A-是药学上可接受的阴离子,RS2和RS3各自独立地是C1-C6烷基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基或5或6元杂芳基,或Ra和Rb与它们所附接的N原子一起形成具有0或1个另外的杂原子的4至12元杂环烷基环,并且RS2、RS3以及由Ra和Rb形成的4至12元杂环烷基环各自任选地被一个或多个-Q3-T3取代,其中Q3是键或各自任选地被卤素、氰基、羟基或C1-C6烷氧基取代的C1-C3烷基接头,并且T3选自由以下组成的组:卤素、氰基、C1-C6烷基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基、5或6元杂芳基、ORd、COORd、-S(O)2Rd、-NRdRe和-C(O)NRdRe,Rd和Re各自独立地是H或C1-C6烷基,或者-Q3-T3是氧代;或任何两个相邻的-Q2-T2与它们所附接的原子一起形成5或6元环,该环任选地含有1-4个选自N、O和S的杂原子并且任选地被一个或多个选自由以下组成的组的取代基取代:卤素、羟基、COOH、C(O)O-C1-C6烷基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基和5或6元杂芳基;
R7是-Q4-T4,其中Q4是键、C1-C4烷基接头或C2-C4烯基接头,每个接头任选地被卤素、氰基、羟基或C1-C6烷氧基取代,并且T4是H、卤素、氰基、NRfRg、-ORf、-C(O)Rf、-C(O)ORf、-C(O)NRfRg、-C(O)NRfORg、-NRfC(O)Rg、-S(O)2Rf或RS4,其中Rf和Rg各自独立地是H或RS5,RS4和RS5各自独立地是C1-C6烷基、C2-C6烯基、C2-C6炔基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基或5或6元杂芳基,并且RS4和RS5各自任选地被一个或多个-Q5-T5取代,其中Q5是键、C(O)、C(O)NRk、NRkC(O)、S(O)2或C1-C3烷基接头,Rk是H或C1-C6烷基,并且T5是H、卤素、C1-C6烷基、羟基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基、5或6元杂芳基或S(O)qRq,其中q是0、1或2并且Rq是C1-C6烷基、C2-C6烯基、C2-C6炔基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基或5或6元杂芳基,并且T5任选地被一个或多个选自由以下组成的组的取代基取代:卤素、C1-C6烷基、羟基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基和5或6元杂芳基,但T5是H、卤素、羟基或氰基时除外;或者-Q5-T5是氧代;并且
R8是H、卤素、羟基、COOH、氰基、RS6、ORS6或COORS6,其中RS6是C1-C6烷基、C2-C6烯基、C2-C6炔基、C3-C8环烷基、4至12元杂环烷基、氨基、单-C1-C6烷基氨基或二-C1-C6烷基氨基,并且RS6任选地被一个或多个选自由以下组成的组的取代基取代:卤素、羟基、COOH、C(O)O-C1-C6烷基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基和二-C1-C6烷基氨基;或R7和R8与它们所附接的N原子一起形成具有0至2个另外的杂原子的4至11元杂环烷基环,并且由R7和R8形成的4至11元杂环烷基环任选地被一个或多个-Q6-T6取代,其中Q6是键、C(O)、C(O)NRm、NRmC(O)、S(O)2或C1-C3烷基接头,Rm是H或C1-C6烷基,并且T6是H、卤素、C1-C6烷基、羟基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基、5或6元杂芳基或S(O)pRp,其中p是0、1或2并且Rp是C1-C6烷基、C2-C6烯基、C2-C6炔基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基或5或6元杂芳基,并且T6任选地被一个或多个选自由以下组成的组的取代基取代:卤素、C1-C6烷基、羟基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基、C3-C8环烷基、C6-C10芳基、4至12元杂环烷基和5或6元杂芳基,但T6是H、卤素、羟基或氰基时除外;或者-Q6-T6是氧代。
例如,R6是C6-C10芳基或5或6元杂芳基,这些基团各自任选地独立地被一个或多个-Q2-T2取代,其中Q2是键或C1-C3烷基接头,并且T2是H、卤素、氰基、-ORa、-NRaRb、-(NRaRbRc)+A-、-C(O)NRaRb、-NRbC(O)Ra、-S(O)2Ra或RS2,其中Ra和Rb各自独立地是H或RS3,RS2和RS3各自独立地是C1-C6烷基,或Ra和Rb与它们所附接的N原子一起形成具有0或1个另外的杂原子的4至7元杂环烷基环,并且RS2、RS3以及由Ra和Rb形成的4至7元杂环烷基环各自任选地独立地被一个或多个-Q3-T3取代,其中Q3是键或C1-C3烷基接头并且T3选自由以下组成的组:卤素、C1-C6烷基、4至7元杂环烷基、ORd、-S(O)2Rd和-NRdRe,Rd和Re各自独立地是H或C1-C6烷基,或者-Q3-T3是氧代;或任何两个相邻的-Q2-T2与它们所附接的原子一起形成任选地含有1-4个选自N、O和S的杂原子的5或6元环。
在一些实施例中,本披露的EZH2抑制剂可以具有以下式(VIa):
或其药学上可接受的盐或酯,其中R7、R8、Ra和Rb在本文中定义。
具有式(VIa)的化合物可包括以下特征中的一者或多者:
例如,Ra和Rb各自独立地是H或任选地被一个或多个-Q3-T3取代的C1-C6烷基。
例如,Ra和Rb中的一者是H。
例如,Ra和Rb与它们所附接的N原子一起形成具有0或1个除N原子以外的另外的杂原子的4至7元杂环烷基环(例如,氮杂环丁烷基、吡咯烷基、咪唑烷基、吡唑烷基、噁唑烷基、异噁唑烷基、三唑烷基、哌啶基、1,2,3,6-四氢吡啶基、哌嗪基、吗啉基、1,4-二氮杂环庚烷基、1,4-氧氮杂环庚烷基、2-氧杂-5-氮杂双环[2.2.1]庚烷基、2,5-二氮杂双环[2.2.1]庚烷基等),并且该环任选地被一个或多个-Q3-T3取代。
例如,Ra和Rb与它们所附接的N原子一起形成氮杂环丁烷基、吡咯烷基、咪唑烷基、吡唑烷基、噁唑烷基、异噁唑烷基、三唑烷基、四氢呋喃基、哌啶基、1,2,3,6-四氢吡啶基、哌嗪基或吗啉基,并且该环任选地被一个或多个-Q3-T3取代。
例如,一个或多个-Q3-T3是氧代。
例如,Q3是键或未取代或取代的C1-C3烷基接头。
例如,T3是H、卤素、4至7元杂环烷基、C1-C3烷基、ORd、COORd、-S(O)2Rd、或-NRdRe。
例如,Rd和Re各自独立地是H或C1-C6烷基。
例如,R7是C3-C8环烷基或4至7元杂环烷基,这些基团各自任选地被一个或多个-Q5-T5取代。
例如,R7是哌啶基、四氢吡喃、四氢-2H-噻喃基、环戊基、环己基、吡咯烷基或环庚基,这些基团各自任选地被一个或多个-Q5-T5取代。
例如,R7是环戊基、环己基、或四氢-2H-噻喃基,这些基团各自任选地被一个或多个-Q5-T5取代。
例如,各自地,Q5是NHC(O),并且T5是C1-C6烷基或C1-C6烷氧基
例如,一个或多个-Q5-T5是氧代。
例如,R7是1-氧化物-四氢-2H-噻喃基或1,1-二氧化物-四氢-2H-噻喃基。
例如,Q5是键,并且T5是氨基、单-C1-C6烷基氨基、二-C1-C6烷基氨基。
例如,Q5是CO、S(O)2、或NHC(O);并且T5是C1-C6烷基、C1-C6烷氧基、C3-C8环烷基、或4至7元杂环烷基。
例如,R8是H或任选地被一个或多个选自由以下组成的组的取代基取代的C1-C6烷基:卤素、羟基、COOH、C(O)O-C1-C6烷基、氰基、C1-C6烷氧基、氨基、单-C1-C6烷基氨基和二-C1-C6烷基氨基。
例如,R8是H、甲基或乙基。
在一些实施例中,EZH2抑制剂是他泽美司他(本文也称为化合物44或化合物(A)):
或其立体异构体、溶剂化物、或药学上可接受的盐。
在一些实施例中,EZH2抑制剂是:
在某些实施例中,EZH2抑制剂是化合物F:
在一些实施例中,EZH2抑制剂是具有以下式的GSK-126:
在某些实施例中,EZH2抑制剂是化合物G:
在某些实施例中,可以用于本文所呈现的任何方法中的化合物(例如,EZH2抑制剂)是化合物Ga-Gc中的任一个:
在一些实施例中,EZH2抑制剂可包含CPI-1205或GSK343、基本上由其组成或由其组成。
用于本文提供的方法、策略、组合物、和/或组合的另外适合的EZH2抑制剂对于本领域技术人员来说将是显而易见的。在本文提供的策略、治疗方式、方法、组合、和组合物的一些实施例中,该EZH2抑制剂是US 8,536,179(描述了GSK-126等化合物并且对应于WO2011/140324)中所述的EZH2抑制剂,其各自的全部内容通过援引以其全文并入本文。
在本文提供的策略、治疗方式、方法、组合、和组合物的一些实施例中,该EZH2抑制剂是公布为WO 2014/124418的PCT/US2014/015706、公布为WO2013/120104的PCT/US2013/025639以及公布为US 2015/0368229的US14/839,273中所述的EZH2抑制剂,其各自的全部内容通过援引以其全文并入本文。
在一些实施例中,本披露的化合物是化合物自身,即游离碱或“裸”分子。在一些实施例中,该化合物是其盐,例如,药学上可接受的盐,例如裸分子的单-HCl盐或三-HCl盐、单-HBr盐或三-HBr盐。基于本披露和本领域的知识,本文提供的化合物的药学上可接受的盐对于本领域技术人员来说将是显而易见的。本披露在此方面不受限制。
本披露的具有式VIa的代表性化合物包括表1中列出的化合物。
表1
如本文所用,“烷基”、“C1、C2、C3、C4、C5或C6烷基”或“C1-C6烷基”旨在包括C1、C2、C3、C4、C5或C6直链(线性)饱和脂肪族烃基和C3、C4、C5或C6支链饱和脂肪族烃基。例如,C1-C6烷基旨在包括C1、C2、C3、C4、C5和C6烷基。烷基的实例包括具有一至六个碳原子的部分,例如但不限于甲基、乙基、正丙基、异丙基、正丁基、仲丁基、叔丁基、正戊基、仲戊基或正己基。
在一些实施例中,直链或支链烷基具有六个或更少碳原子(例如,对于直链为C1-C6,对于支链为C3-C6),并且在一些实施例中,直链或支链烷基具有四个或更少碳原子。
如本文所用,术语“环烷基”是指具有3至30个碳原子(例如,C3-C10)的饱和或不饱和非芳族烃单环或多环(例如,稠合环、桥接环或螺环)系统。环烷基的实例包括但不限于环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环戊烯基、环己烯基、环庚烯基和金刚烷基。除非另外指定,否则术语“杂环烷基”是指具有一个或多个杂原子(例如O、N、S或Se)的饱和或不饱和非芳族3-8元单环、7-12元二环(稠合环、桥接环或螺环)或11-14元三环系统(稠合环、桥接环或螺环)。杂环烷基的实例包括但不限于哌啶基、哌嗪基、吡咯烷基、二噁烷基、四氢呋喃基、异吲哚啉基、二氢吲哚基、咪唑烷基、吡唑烷基、噁唑烷基、异噁唑烷基、三唑烷基、四氢呋喃基、环氧乙烷基、氮杂环丁烷基、氧杂环丁基、硫杂环丁基、1,2,3,6-四氢吡啶基、四氢吡喃基、二氢吡喃基、吡喃基、吗啉基、1,4-二氮杂环庚烷基、1,4-氧杂氮杂环庚烷基、2-氧杂-5-氮杂双环[2.2.1]庚烷基、2,5-二氮杂双环[2.2.1]庚烷基、2-氧杂-6-氮杂螺[3.3]庚烷基、2,6-二氮杂螺[3.3]庚烷基、1,4-二氮杂-8-氮杂螺[4.5]癸烷基等。
术语“任选取代的烷基”是指未取代的烷基或具有替代烃主链的一个或多个碳上的一个或多个氢原子的指定取代基的烷基。此类取代基可以包括例如烷基、烯基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。
“芳基烷基”或“芳烷基”部分是被芳基取代的烷基(例如,苯基甲基(苄基))。“烷基芳基”部分是被烷基取代的芳基(例如,甲基苯基)。
如本文所用,“烷基接头”旨在包括C1、C2、C3、C4、C5或C6直链(线性)饱和二价脂肪族烃基和C3、C4、C5或C6支链饱和脂肪族烃基。例如,C1-C6烷基接头旨在包括C1、C2、C3、C4、C5和C6烷基接头基团。烷基接头的实例包括具有一至六个碳原子的部分,例如但不限于甲基(-CH2-)、乙基(-CH2CH2-)、正丙基(-CH2CH2CH2-)、异丙基(-CHCH3CH2-)、正丁基(-CH2CH2CH2CH2-)、仲丁基(-CHCH3CH2CH2-)、异丁基(-C(CH3)2CH2-)、正戊基(-CH2CH2CH2CH2CH2-)、仲戊基(-CHCH3CH2CH2CH2-)或正己基(-CH2CH2CH2CH2CH2CH2-)。
“烯基”包括在长度和可能的取代方面与上述烷基类似但含有至少一个双键的不饱和脂肪族基团。例如,术语“烯基”包括直链烯基基团(例如,乙烯基、丙烯基、丁烯基、戊烯基、己烯基、庚烯基、辛烯基、壬烯基、癸烯基)和支链烯基基团。在某些实施例中,直链或支链烯基基团在其主链中具有六个或更少碳原子(例如,对于直链为C2-C6,对于支链为C3-C6)。术语“C2-C6”包括含有二至六个碳原子的烯基基团。术语“C3-C6”包括含有三至六个碳原子的烯基基团。
术语“任选取代的烯基”是指未取代的烯基或具有替代一个或多个烃主链碳原子上的一个或多个氢原子的指定取代基的烯基。此类取代基可以包括例如烷基、烯基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、杂环基、烷基芳基或者芳族或杂芳族部分。
“炔基”包括在长度和可能的取代方面与上述烷基类似但含有至少一个三键的不饱和脂肪族基团。例如,“炔基”包括直链炔基基团(例如,乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基、辛炔基、壬炔基、癸炔基)和支链炔基基团。在某些实施例中,直链或支链炔基基团在其主链中具有六个或更少的碳原子(例如,对于直链为C2-C6,对于支链为C3-C6)。术语“C2-C6”包括含有二至六个碳原子的炔基基团。术语“C3-C6”包括含有三至六个碳原子的炔基基团。
术语“任选取代的炔基”是指未取代的炔基或具有替代一个或多个烃主链碳原子上的一个或多个氢原子的指定取代基的炔基。此类取代基可以包括例如烷基、烯基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。
其他任选取代的部分(例如任选取代的环烷基、杂环烷基、芳基或杂芳基)包括未取代的部分和具有指定取代基中的一者或多者的部分两者。例如,取代的杂环烷基包括被一个或多个烷基基团取代的那些,例如2,2,6,6-四甲基-哌啶基和2,2,6,6-四甲基-1,2,3,6-四氢吡啶基。
“芳基”包括具有芳香性的基团,包括“共轭”或具有至少一个芳族环且在环结构中不含有任何杂原子的多环系统。实例包括苯基、苄基、1,2,3,4-四氢萘基等。
“杂芳基”基团是如上所定义的芳基基团,但在环结构中具有一至四个杂原子,并且还可被称为“芳基杂环”或“杂芳族”。如本文所用,术语“杂芳基”旨在包括由碳原子以及一个或多个独立地选自由氮、氧和硫组成的组的杂原子(例如1或1-2或1-3或1-4或1-5或1-6个杂原子,或例如1、2、3、4、5或6个杂原子)组成的稳定的5、6或7元单环或7、8、9、10、11或12元双环芳族杂环。氮原子可以是取代的或未取代的(即,N或NR,其中R是H或如所定义的其他取代基)。氮和硫杂原子可任选地被氧化(即,N→O和S(O)p,其中p=1或2)。应注意,芳族杂环中S和O原子的总数不大于1。
杂芳基基团的实例包括吡咯、呋喃、噻吩、噻唑、异噻唑、咪唑、三唑、四唑、吡唑、噁唑、异噁唑、吡啶、吡嗪、哒嗪、嘧啶等。
另外,术语“芳基”和“杂芳基”包括多环芳基和杂芳基,例如三环、二环,例如萘、苯并噁唑、苯并二噁唑、苯并噻唑、苯并咪唑、苯并噻吩、亚甲基二氧苯基、喹啉、异喹啉、萘啶、吲哚、苯并呋喃、嘌呤、苯并呋喃、脱氮杂嘌呤、中氮茚。
在多环芳族环的情况下,仅需要环中的一者是芳族(例如,2,3-二氢吲哚),但所有环都可以是芳族(例如,喹啉)。第二环也可以是稠合或桥接的。
环烷基、杂环烷基、芳基或杂芳基环可以在一个或多个环位置(例如,成环碳或杂原子,例如N)被如上所述的此类取代基取代,这些取代基例如烷基、烯基、炔基、卤素、羟基、烷氧基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、烷基氨基羰基、芳烷基氨基羰基、烯基氨基羰基、烷基羰基、芳基羰基、芳烷基羰基、烯基羰基、烷氧基羰基、氨基羰基、烷基硫羰基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。芳基和杂芳基也可以与不是芳族的脂环族环或杂环稠合或桥接,以形成多环系统(例如,四氢化萘、亚甲基二氧苯基)。
如本文所用,“碳环”或“碳环的环”旨在包括具有指定碳数的任何稳定单环、双环或三环的环,其中任一个可以是饱和、不饱和或芳族的。碳环包括环烷基和芳基。例如,C3-C14碳环旨在包括具有3、4、5、6、7、8、9、10、11、12、13或14个碳原子的单环、双环或三环。碳环的实例包括但不限于环丙基、环丁基、环丁烯基、环戊基、环戊烯基、环己基、环庚烯基、环庚基、环庚烯基、金刚烷基、环辛基、环辛烯基、环辛二烯基、芴基、苯基、萘基、茚满基、金刚烷基和四氢萘基。桥接环也包括在碳环的定义中,包括例如[3.3.0]二环辛烷、[4.3.0]二环壬烷、[4.4.0]二环癸烷和[2.2.2]二环辛烷。当一个或多个碳原子连接两个不相邻的碳原子时,会发生桥接环。在一些实施例中,桥环是一个或两个碳原子。应注意,桥总是将单环转化成三环。当环被桥接时,针对该环所列举的取代基也可以存在于桥上。还包括稠合(例如,萘基、四氢萘基)环和螺环。
如本文所用,“杂环”或“杂环基”包括含有至少一个环杂原子(例如,N、O或S)的任何环结构(饱和、不饱和或芳族)。杂环包括杂环烷基和杂芳基。杂环的实例包括但不限于吗啉、吡咯烷、四氢噻吩、哌啶、哌嗪、氧杂环丁烷、吡喃、四氢吡喃、氮杂环丁烷和四氢呋喃。
杂环基的实例包括但不限于吖啶基、吖辛因基、苯并咪唑基、苯并呋喃基、苯并硫代呋喃基、苯并噻吩基、苯并噁唑基、苯并噁唑啉基、苯并噻唑基、苯并三唑基、苯并四唑基、苯并异噁唑基、苯并异噻唑基、苯并咪唑啉基、咔唑基、4aH-咔唑基、咔啉基、色满基、色烯基、噌啉基、十氢喹啉基、2H,6H-1,5,2-二噻嗪基、二氢呋喃并[2,3-b]四氢呋喃、呋喃基、呋咱基、咪唑烷基、咪唑啉基、咪唑基、1H-吲唑基、吲哚烯基、二氢吲哚基、吲嗪基、吲哚基、3H-吲哚基、靛吲哚基、异苯并呋喃基、异苯并二氢吡喃基、异吲唑基、异吲哚啉基、异吲哚基、异喹啉基、异噻唑基、异噁唑基、亚甲基二氧苯基、吗啉基、萘啶基、八氢异喹啉基、噁二唑基、1,2,3-噁二唑基、1,2,4-噁二唑基、1,2,5-噁二唑基、1,3,4-噁二唑基、1,2,4-噁二唑5(4H)-酮、噁唑烷基、噁唑基、羟吲哚基、嘧啶基、菲啶基、菲咯啉基、吩嗪基、吩噻嗪基、吩噁噻基、吩噁嗪基、酞嗪基、哌嗪基、哌啶基、哌啶酮基、4-哌啶酮基、胡椒基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑烷基、吡唑啉基、吡唑基、哒嗪基、吡啶并噁唑、吡啶并咪唑、吡啶并噻唑、吡啶基(pyridinyl)、吡啶基(pyridyl)、嘧啶基、吡咯烷基、吡咯啉基、2H-吡咯基、吡咯基、喹唑啉基、喹啉基、4H-喹嗪基、喹噁啉基、奎宁环基、四氢呋喃基、四氢异喹啉基、四氢喹啉基、四唑基、6H-1,2,5-噻二嗪基、1,2,3-噻二唑基、1,2,4-噻二唑基、1,2,5-噻二唑基、1,3,4-噻二唑基、噻蒽基、噻唑基、噻吩基、噻吩并噻唑基、噻吩并噁唑基、噻吩并咪唑基、噻吩基、三嗪基、1,2,3-三唑基、1,2,4-三唑基、1,2,5-三唑基、1,3,4-三唑基和呫吨基。
如本文所用,术语“被取代”意指指定原子上的任何一个或多个氢被来自所指示基团中的选择物替代,前提条件是不超过指定原子的正常化合价,并且该取代产生稳定的化合物。当取代基是氧代或酮基(即,=O)时,则原子上的2个氢原子被替代。酮基取代基不存在于芳族部分上。如本文所用,环双键是在两个相邻环原子之间形成的双键(例如,C=C、C=N或N=N)。“稳定化合物”和“稳定结构”意在指示足够稳健以经受得住从反应混合物中分离至有用纯度并配制成有效治疗剂的化合物。
当与取代基连接的键显示为与连接环中两个原子的键交叉时,则这样的取代基可与环中的任何原子键合。当列出取代基而未指明该取代基通过其键合到给定式的化合物的其余部分的原子时,则该取代基可通过该式中的任何原子键合。取代基和/或变量的组合是允许的,但仅当这种组合产生稳定的化合物时。
当任何变量(例如,R1)在化合物的任何成分或通式中出现超过一次时,其在每次出现时的定义都独立于其在每次其他出现时的定义。因此,例如,如果显示基团被0-2个R1部分取代,则该基团可任选地被至多两个R1部分取代,并且R1在每次出现时独立地选自R1的定义。同样,取代基和/或变量的组合是允许的,但仅当这种组合产生稳定的化合物时。
术语“羟基”(“hydroxy”或“hydroxyl”)包括具有-OH或-O-的基团。
如本文所用,“卤”或“卤素”是指氟、氯、溴和碘。术语“全卤代”通常是指其中所有氢原子均被卤素原子替代的部分。术语“卤代烷基”或“卤代烷氧基”是指被一个或多个卤素原子取代的烷基或烷氧基。
术语“羰基”包括含有通过双键键合到氧原子的碳的化合物和部分。含有羰基的部分的实例包括但不限于醛、酮、羧酸、酰胺、酯、酸酐等。
术语“羧基”是指-COOH或其C1-C6烷基酯。
“酰基”包括含有酰基(R-C(O)-)或羰基基团的部分。“取代的酰基”包括其中一个或多个氢原子被以下基团替代的酰基基团:例如烷基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。
“芳酰基”包括具有与羰基基团结合的芳基或杂芳族部分的部分。芳酰基基团的实例包括苯基羧基、萘基羧基等。
“烷氧基烷基”、“烷基氨基烷基”和“硫代烷氧基烷基”包括如上文所述的其中氧、氮或硫原子替代一个或多个烃主链碳原子的烷基基团。
术语“烷氧基”(“alkoxy”或“alkoxyl”)包括共价连接到氧原子的取代的和未取代的烷基、烯基和炔基。烷氧基基团或烷氧基团的实例包括但不限于甲氧基、乙氧基、异丙氧基、丙氧基、丁氧基和戊氧基基团。取代的烷氧基基团的实例包括卤化烷氧基基团。烷氧基基团可被以下基团取代:例如烯基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、磷酸根、膦酸基、次膦酸基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。卤素取代的烷氧基基团的实例包括但不限于氟甲氧基、二氟甲氧基、三氟甲氧基、氯甲氧基、二氯甲氧基和三氯甲氧基。
术语“醚”或“烷氧基”包括含有与两个碳原子或杂原子键合的氧的化合物或部分。例如,该术语包括“烷氧基烷基”,其是指共价键合到与烷基基团共价键合的氧原子的烷基、烯基或炔基。
术语“酯”包括含有结合到与羰基基团碳键合的氧原子的碳或杂原子的化合物或部分。术语“酯”包括烷氧基羧基基团,例如甲氧基羰基、乙氧基羰基、丙氧基羰基、丁氧基羰基、戊氧基羰基等。
术语“硫代烷基”包括含有与硫原子连接的烷基基团的化合物或部分。硫代烷基基团可被以下基团取代:例如烷基、烯基、炔基、卤素、羟基、烷基羰氧基、芳基羰氧基、烷氧基羰氧基、芳氧基羰氧基、羧酸根、羧酸、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫羰基、烷氧基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基和烷基芳基氨基)、酰氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基)、脒基、亚氨基、巯基、烷硫基、芳硫基、硫代羧酸根、硫酸根、烷基亚磺酰基、磺酸基、氨磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基或者芳族或杂芳族部分。
术语“硫代羰基”或“硫代羧基”包括含有通过双键与硫原子键合的碳的化合物和部分。
术语“硫醚”包括含有与两个碳原子或杂原子键合的硫原子的部分。硫醚的实例包括但不限于烷硫代烷基、烷硫代烯基和烷硫代炔基。术语“烷硫代烷基”包括具有键合到与烷基基团键合的硫原子的烷基、烯基或炔基的部分。类似地,术语“烷硫代烯基”是指其中烷基、烯基或炔基基团键合到与烯基基团共价键合的硫原子的部分;并且“烷硫代炔基”是指其中烷基、烯基或炔基基团键合到与炔基基团共价键合的硫原子的部分。
如本文所用“胺”或“氨基”是指未取代或取代的-NH2。“烷基氨基”包括其中-NH2的氮与至少一个烷基基团结合的化合物的基团。烷基氨基的实例包括苄基氨基、甲基氨基、乙基氨基、苯乙基氨基等。“二烷基氨基”包括其中-NH2的氮与至少两个另外的烷基基团结合的基团。二烷基氨基基团的实例包括但不限于二甲基氨基和二乙基氨基。“芳基氨基”和“二芳基氨基”包括其中氮分别与至少一个或两个芳基结合的基团。“氨基芳基”和“氨基芳氧基”是指被氨基取代的芳基和芳氧基。“烷基芳基氨基”、“烷基氨基芳基”或“芳基氨基烷基”是指与至少一个烷基和至少一个芳基结合的氨基基团。“烷氨基烷基”是指结合到还与烷基基团结合的氮原子的烷基、烯基或炔基。“酰氨基”包括其中氮与酰基结合的基团。酰氨基的实例包括但不限于烷基羰基氨基、芳基羰基氨基、氨基甲酰基和脲基。
术语“酰胺”或“氨基羧基”包括含有与羰基或硫代羰基基团的碳结合的氮原子的化合物或部分。该术语包括“烷氨基羧基”,其包括结合到与羰基或硫代羰基基团的碳结合的氨基的烷基、烯基或炔基。它还包括“芳基氨基羧基”基团,其包括结合到与羰基或硫代羰基基团的碳结合的氨基的芳基或杂芳基部分。术语“烷基氨基羧基”、“烯基氨基羧基”、“炔基氨基羧基”和“芳基氨基羧基”包括其中烷基、烯基、炔基和芳基部分分别与氮原子结合的部分,该氮原子又与羰基基团的碳结合。酰胺可被以下取代基取代:例如直链烷基、支链烷基、环烷基、芳基、杂芳基或杂环。酰胺基上的取代基可被进一步取代。
可以通过用氧化剂(例如,3-氯过氧苯甲酸(mCPBA)和/或过氧化氢)处理将含有氮的本披露化合物转化成N-氧化物以得到本披露的其他化合物。因此,当化合价和结构允许时,所有示出和要求保护的含氮化合物被认为包括所示的化合物及其N-氧化物衍生物(其可被指定为N→O或N+-O-)两者。此外,在其他情况下,本披露的化合物中的氮可以被转化成N-羟基或N-烷氧基化合物。例如,N-羟基化合物可通过用例如m-CPBA的氧化剂氧化母体胺来制备。当化合价和结构允许时,所有示出和要求保护的含氮化合物还被认为涵盖所示化合物及其N-羟基(即,N-OH)和N-烷氧基(即,N-OR,其中R是取代的或未取代的C1-C6烷基、C1-C6烯基、C1-C6炔基、3-14元碳环或3-14元杂环)衍生物两者。
“异构现象”意指具有相同分子式但其原子的键合顺序或其原子的空间排列不同的化合物。其原子的空间排列不同的异构体称为“立体异构体”。不互为镜像的立体异构体称为“非对映异构体”,互为非重叠镜像的立体异构体称为“对映异构体”或有时也称为旋光异构体。含有等量相反手性的单个对映体形式的混合物称为“外消旋混合物”。
与四个不同取代基键合的碳原子称为“手性中心”。
“手性异构体”意指具有至少一个手性中心的化合物。具有多于一个手性中心的化合物可以单独的非对映体形式或以非对映体混合物形式存在,称为“非对映体混合物”。当存在一个手性中心时,立体异构体可通过该手性中心的绝对构型(R或S)来表征。绝对构型是指与手性中心附接的取代基的空间排列。根据Cahn、Ingold和Prelog的顺序规则对与所考虑的手性中心连接的取代基进行排序。(Cahn等人,Angew.Chem.Inter.Edit.[德国应用化学]1966,5,385;勘误表511;Cahn等人,Angew.Chem.[德国应用化学]1966,78,413;Cahn和Ingold,J.Chem.Soc.[美国化学学会期刊]1951(伦敦),612;Cahn等人,Experientia[实验]1956,12,81;Cahn,J.Chem.Educ.[化学教育杂志]1964,41,116)。
“几何异构体”意指这样的非对映异构体,它们的存在导致围绕双键或环烷基接头(例如,1,3-环丁基)的旋转受阻。这些构型的名称通过前缀顺式和反式、或Z和E来区分,这些前缀指示根据卡恩-英戈尔德-普雷洛格(Cahn-Ingold-Prelog)规则这些基团位于分子中双键的同侧或对侧。
应理解,本披露的化合物可以描绘为不同手性异构体或几何异构体。还应理解的是,在化合物具有手性异构体或几何异构体形式时,所有异构体形式均旨在被包括于本披露的范围内,并且化合物的命名不排除任何异构体形式。
此外,本发明中讨论的结构和其他化合物包括其所有阻转异构体。“阻转异构体”是一种其中两个异构体的原子在空间上排列不同的立体异构体。阻转异构体的存在是由于大基团围绕中心键的旋转受阻而导致的受限旋转。此类阻转异构体典型地作为混合物存在,然而由于色谱技术的最新进展,已经可能在选择的情况下分离两种阻转异构体的混合物。
“互变异构体”是平衡地存在并且易于从一种异构形式转化为另一种异构体形式的两种或更多种结构异构体中的一种。这种转化导致氢原子的形式迁移,伴随着相邻共轭双键的转化。互变异构体以互变异构体的混合物组形式存在于溶液中。在可能存在互变异构的溶液中,将达到互变异构体的化学平衡。互变异构体的确切比率取决于若干因素,包括温度、溶剂和pH。可通过互变异构作用相互转化的互变异构体的概念被称为互变异构现象。
在可能的多种类型的互变异构现象中,通常观察到两种。在酮-烯醇互变异构现象中,同时发生电子和氢原子的移动。由于糖链分子中的醛基(-CHO)与同一分子中的一个羟基(-OH)反应,使其成为葡萄糖所表现出的环状(环形)形式,从而产生了环-链互变异构现象。
常见的互变异构对是:酮-烯醇、酰胺-腈、内酰胺-内酰亚胺、杂环中(例如,在例如鸟嘌呤、胸腺嘧啶和胞嘧啶的核碱基中)的酰胺-亚胺酸互变异构、亚胺-烯胺和烯胺-烯胺。酮-烯醇平衡的一个实例是吡啶-2(1H)-酮与对应的吡啶-2-醇之间的平衡,如下所示。
应理解,本披露的化合物可以描绘为不同互变异构体。还应当理解的是,在化合物具有互变异构形式时,所有互变异构形式都旨在被包括于本披露的范围内,并且化合物的命名不排除任何互变异构体形式。
本文所披露的具有式(I)-(VIa)的化合物包括化合物自身,以及其盐和其溶剂化物(若适用)。例如,可在阴离子与芳基取代的或杂芳基取代的苯化合物上的带正电荷的基团(例如,氨基)之间形成盐。适合的阴离子包括氯离子、溴离子、碘离子、硫酸根、硫酸氢根、氨基磺酸根、硝酸根、磷酸根、柠檬酸根、甲磺酸根、三氟乙酸根、谷氨酸根、葡糖醛酸根、戊二酸根、苹果酸根、马来酸根、琥珀酸根、富马酸根、酒石酸根、甲苯磺酸根、水杨酸根、乳酸根、萘磺酸根和乙酸根(例如,三氟乙酸根)。术语“药学上可接受的阴离子”是指适于形成药学上可接受的盐的阴离子。同样,也可在阳离子与芳基取代的或杂芳基取代的苯化合物上的带负电荷的基团(例如,羧酸根)之间形成盐。适合的阳离子包括钠离子、钾离子、镁离子、钙离子和铵阳离子(例如四甲基铵离子)。芳基取代的或杂芳基取代的苯化合物还包括那些含有季氮原子的盐。在盐形式中,应理解,化合物与盐的阳离子或阴离子的比例可为1:1或除1:1外的任何比例,例如3:1、2:1、1:2或1:3。
另外,本披露的化合物(例如,化合物的盐)可以水合或非水合(无水)形式或作为与其他溶剂分子的溶剂化物而存在。水合物的非限制性实例包括一水合物、二水合物等。溶剂化物的非限制性实例包括乙醇溶剂化物、丙酮溶剂化物等。
“溶剂化物”意指含有化学计量量或非化学计量量的溶剂的溶剂加成形式。一些化合物具有在结晶固态中捕获固定摩尔比的溶剂分子的倾向,从而形成溶剂化物。如果溶剂是水,则所形成的溶剂化物是水合物;并且如果溶剂是醇,则所形成的溶剂化物是醇化物。水合物是通过一分子或多分子水与一分子物质组合形成的,其中水保持其分子状态为H2O。
如本文所用,术语“类似物”是指在结构上与另一化合物类似但在组成上略有不同的化合物(如一个原子被不同元素的原子替代或存在特定官能团,或一个官能团被另一官能团替代)。因此,类似物是与参考化合物在功能和外观上相似或可比但在结构或来源上不相似或不可比的化合物。
如本文所定义,术语“衍生物”是指具有共同的核心结构,并且被如本文所述的不同基团取代的化合物。例如,由式(I)表示的所有化合物均是芳基或杂芳基取代的苯化合物,并且具有式(I)作为共同核心。
术语“生物电子等排体”是指通过原子或原子团由大概相似的另一原子或原子团交换所得的化合物。生物电子等排置换的目标是产生具有与母体化合物相似的生物学特性的新化合物。生物电子等排置换可以基于物理化学或拓扑学。羧酸生物电子等排体的实例包括但不限于酰基磺酰亚胺、四唑、磺酸酯和膦酸酯。参见例如,Patani和LaVoie,Chem.Rev.[化学评论]96,3147-3176,1996。
本披露旨在包括本披露化合物中存在的原子的所有同位素。同位素包括原子数相同但质量数不同的那些原子。作为一般实例而非限制,氢的同位素包括氚和氘,并且碳的同位素包括C-13和C-14。
如本文所述的,本披露的具有式(I)-(VIa)的任何化合物可以是EZH2抑制剂。
在本发明的某些方面,当EZH2的抑制剂抑制突变体EZH2的组蛋白甲基转移酶活性比它抑制野生型EZH2的组蛋白甲基转移酶活性更有效时,EZH2的抑制剂“选择性地抑制”突变体EZH2的组蛋白甲基转移酶活性。例如,在一些实施例中,该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少40%。在一些实施例中该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少50%。在一些实施例中该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少60%。在一些实施例中该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少70%。在一些实施例中该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少80%。在一些实施例中该选择性抑制剂对突变型EZH2的IC50比对野生型EZH2的IC50低至少90%。
在一些实施例中,突变型EZH2的选择性抑制剂对野生型EZH2基本上没有抑制作用。
在本发明的某些方面,该抑制剂(例如本文披露的化合物)抑制从H3-K27me2至H3-K27me3的转化。在一些实施例中,认为该抑制剂抑制H3-K27的三甲基化。由于H3-K27me1向H3-K27me2的转化先于H3-K27me2向H3-K27me3的转化,因此H3-K27me1向H3-K27me2的转化抑制剂自然也抑制H3-K27me2向H3-K27me3的转化,即其抑制H3-K27的三甲基化。也有可能抑制H3-K27me2向H3-K27me3的转化而不抑制H3-K27me1向H3-K27me2的转化。这种类型的抑制尽管不会抑制H3-K27的二甲基化,但也将导致H3-K27三甲基化的抑制。
在一些实施例中,该抑制剂(例如本文披露的化合物)抑制H3-K27me1向H3-K27me2的转化以及H3-K27me2向H3-K27me3的转化。这样的抑制剂可直接抑制单独的H3-K27me1向H3-K27me2的转化。替代性地,这样的抑制剂可直接抑制H3-K27me1向H3-K27me2的转化以及H3-K27me2向H3-K27me3的转化。
在本发明的某些方面,该EZH2抑制剂(例如本文披露的化合物)抑制组蛋白甲基转移酶活性。组蛋白甲基转移酶活性的抑制可使用任何适合的方法来检测。抑制可以例如根据组蛋白甲基转移酶活性的速率或作为组蛋白甲基转移酶活性的产物来测量。
相比适合的对照该抑制是一种可测量的抑制。在一些实施例中,与合适的对照相比,抑制是至少10%的抑制。即,使用抑制剂时酶活性的比率或产物的量是少于或等于不使用抑制剂时产生的相应的比率和量的90%。在各种其他实施例中,相比适合的对照,抑制是至少20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或95%抑制。在一些实施例中,与适合的对照相比,抑制是至少99%的抑制。即,使用抑制剂时酶活性的比率或产物的量是少于或等于不使用抑制剂时产生的相应的比率和量的1%。
本披露的组合物可以包含具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种其他治疗剂或其药学上可接受的盐。本披露提供了用于具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种治疗剂或其药学上可接受的盐(作为共同配制品或单独的配制品)的施用,其中配制品的施用是同时的、顺序的或交替的。在某些实施例中,其他治疗剂可以是被本技术领域认为是对治疗正在经本披露的组合物治疗的疾病或病状有用的药剂。在一些实施例中,其他治疗剂可以是未被本技术领域认为是对治疗正在经本披露的组合物治疗的疾病或病状有用的药剂。在一些方面,其他治疗剂可以是赋予本披露的组合物有益属性的药剂(例如,影响组合物粘性的药剂)。对本披露的组合物有益的属性包括但不限于从具有式(I)-(VIa)的化合物与一种或多种其他治疗剂的组合产生的药剂代谢动力学或药效学共同作用。
以下阐述的治疗剂是为了说明的目的,而不是意在限制。本披露包括从以下列表中选出的至少一种其他治疗剂。本披露可以包括多于一种其他治疗剂,例如,两种、三种、四种、或五种其他治疗剂以至于本披露的组合物可以执行其预期功能。
在一些实施例中,该其他治疗剂是抗癌剂。在一些实施例中,该抗癌剂是影响组蛋白修饰的化合物,例如HDAC抑制剂(例如或)。在某些实施例中,抗癌剂选自下组,该组由以下各项组成:化学治疗剂(例如2CdA、5-FU、6-巯基嘌呤、6-TG、AbraxaneTM、放线菌素D、全反式维甲酸、氨甲蝶呤、阿糖胞苷、Azacitadine、BCNU、氯法拉滨、ClolarTM、盐酸柔红霉素、DIC、 磷酸依托泊苷、 六甲嘧胺、伊沙匹隆、L-天冬酰胺酶、脂质体阿糖胞苷、L-PAM、Lysodren、马磷酰胺、光辉霉素(mithracin)、丝裂霉素C、尼洛替尼、氮芥子气、具有卡莫司汀植入物的prolifeprospan 20、 TESPA、VidazaTM、硫酸长春新碱、VM 26、以及);生物制剂(例如α干扰素、卡介苗、埃罗替尼、白介素-2、来那度胺、 TarcevaTM、以及ZevalinTM);皮质类固醇(例如地塞米松磷酸钠、和);糖皮质激素受体激动剂(例如或);激素疗法(例如 PlenaxisTM以及);以及放射性药剂(如以及Samarium SM-153);免疫调节药物(例如和);蛋白酶体抑制剂(例如和);bcl-2抑制剂(例如)。
在一些实施例中,该其他治疗剂是选自包括以下各项的组的化学治疗剂(也称为抗肿瘤剂或抗增生剂):烷基化剂;抗生素;抗代谢药;解毒剂;干扰素;多克隆或单克隆抗体;EGFR抑制剂;HER2抑制剂;组蛋白脱乙酰酶抑制剂;激素;有丝分裂抑制剂;MTOR抑制剂;多激酶抑制剂;丝氨酸/苏氨酸激酶抑制剂;酪氨酸激酶抑制剂;VEGF/VEGFR抑制剂;紫杉烷或紫杉烷衍生物、芳香酶抑制剂、蒽环霉素、微管靶向药物、拓扑异构酶毒物药剂、分子靶标或酶的抑制剂(例如,激酶或蛋白质甲基转移酶)、胞苷类似物药物或列于www.cancer.org/docroot/cdg/cdg_0.asp的任何化学治疗剂、抗肿瘤剂或抗增生剂。
示例性抗代谢药包括但不限于氟尿嘧啶卡培他滨羟基脲巯基嘌呤培美曲塞(Alimta);氟达拉滨奈拉滨克拉屈滨(Cladribine);氯法拉滨阿糖胞苷地西他滨阿糖胞苷脂质体羟基脲普拉曲沙氟尿苷吉西他滨克拉屈滨氟达拉滨甲氨蝶呤甲氨蝶呤硫鸟嘌呤TS-1或阿糖胞苷
示例性抗代谢药包括叶酸型的抗代谢药,包括但不限于吉西他滨、甲氨蝶呤、和培美曲塞。
示例性激素包括但不限于它莫西芬(Soltamox;);雷洛昔芬甲地孕酮亮丙瑞林(Lupron );氟维司群来曲唑曲普瑞林(TrelstarTrelstar);依西美坦戈舍瑞林比卡鲁胺阿那曲唑氟甲睾酮甲羟孕酮雌氮芥氟他胺托瑞米芬地加瑞克尼鲁米特阿巴瑞克或睾内酯
示例性微管靶向药物包括但不限于紫杉醇、多西他赛、长春新碱、长春碱、诺考达唑、埃博霉素以及诺维本。
示例性拓扑异构酶毒物药剂/拓扑异构酶抑制剂包括但不限于伊立替康、替尼泊苷、依托泊苷、阿霉素、喜树碱、柔红霉素、更生霉素、米托蒽醌、安吖啶、表柔比星以及伊达比星。
示例性紫杉烷或紫杉烷衍生物包括但不限于紫杉醇和多西他赛。
示例性一般化学治疗剂、抗肿瘤剂、抗增生剂包括但不限于六甲蜜胺(Hexalen);异维A酸(Accutane;Amnesteem;Claravis;Sotret);维甲酸阿扎胞苷硼替佐米天冬酰胺酶依鲁替尼左旋咪唑米托坦丙卡巴肼(Matulane);培门冬酶地尼白介素-毒素连接物卟吩姆阿地白介素来那度胺贝沙罗汀沙利多迈坦罗莫司三氧化二砷维替泊芬含羞草氨酸(1M替加氟-0.4M 5-氯-2,4-二羟基嘧啶-1M氧嗪酸钾)、或洛伐他汀。
在一些方面,该其他治疗剂是化学治疗剂或细胞因子,例如G-CSF(粒细胞集落刺激因子)。
在另外的方面,该其他治疗剂可以是标准化学疗法组合,例如但不限于CMF(环磷酰胺、甲氨蝶呤和5-氟尿嘧啶)、CAF(环磷酰胺、阿霉素和5-氟尿嘧啶)、AC(阿霉素和环磷酰胺)、FEC(5-氟尿嘧啶、表柔比星和环磷酰胺)、ACT或ATC(阿霉素、环磷酰胺和紫杉醇)、利妥昔单抗、Xeloda(卡培他滨)、顺铂(CDDP)、卡铂、TS-1(摩尔比为1:0.4:1的替加氟、吉美司特和奥斯他特钾)、喜树碱-11(CPT-11、伊立替康或CamptosarTM)、CHOP(环磷酰胺、羟基柔红霉素、长春新碱(oncovin)、和强的松或泼尼松龙)、R-CHOP(利妥昔单抗、环磷酰胺,羟基柔红霉素、长春新碱、强的松或泼尼松龙)、CVP(环磷酰胺、长春新碱、和强的松)、超-CVAD(超分割环磷酰胺、长春新碱、阿霉素、和强的松)或CMFP(环磷酰胺、甲氨蝶呤、5-氟尿嘧啶和强的松)。
在其他方面,该其他治疗剂可以是酶(例如受体或非受体激酶)的抑制剂。受体或非受体激酶是例如,酪氨酸激酶或丝氨酸/苏氨酸激酶。本文所述的激酶抑制剂是小分子、多核酸、多肽、或抗体。
示例性激酶抑制剂包括但不限于阿法替尼(靶向EFGR/Her2)、贝伐单抗(靶向VEGF)、BIBW 2992(靶向EGFR和ErbB2)、布加替尼(靶向ALK和EFGR)、色瑞替尼(靶向ALK)、克唑替尼(靶向ALK和ROS1)、西妥昔单抗/Erbitux(靶向ErbB1)、伊马替尼/Gleevic(靶向Bcr-Abl)、曲妥珠单抗(靶向ErbB2)、吉非替尼/Iressa(靶向EGFR)、兰尼单抗(靶向VEGF)、哌加他尼(靶向VEGF)、埃罗替尼/Tarceva(靶向ErbB1)、尼洛替尼(靶向Bcr-Abl)、拉帕替尼(靶向ErbB1和ErbB2/Her2)、GW-572016/二甲苯磺酸拉帕替尼(靶向HER2/ErbB2)、帕尼单抗/Vectibix(靶向EGFR)、凡德他尼(靶向RET/VEGFR)、E7080(包括RET和VEGFR多个靶向)、Herceptin(靶向HER2/ErbB2)、PKI-166(靶向EGFR)、卡纳替尼/CI-1033(靶向EGFR)、舒尼替尼/SU-11464/Sutent(靶向EGFR和FLT3)、马妥珠单抗/Emd7200(靶向EGFR)、EKB-569(靶向EGFR)、Zd6474(靶向EGFR和VEGFR)、PKC-412(靶向VEGR和FLT3)、伐他拉尼/Ptk787/ZK222584(靶向VEGR)、CEP-701(靶向FLT3)、SU5614(靶向FLT3)、MLN518(靶向FLT3)、XL999(靶向FLT3)、VX-322(靶向FLT3)、Azd0530(靶向SRC)、BMS-354825(靶向SRC)、SKI-606(靶向SRC)、CP-690(靶向JAK)、AG-490(靶向JAK)、WHI-P154(靶向JAK)、WHI-P131(靶向JAK)、索拉非尼/Nexavar(靶向RAF激酶、VEGFR-1、VEGFR-2、VEGFR-3、PDGFR-β、KIT、FLT-3、以及RET)、达沙替尼/Sprycel(BCR/ABL和Src)、AC-220(靶向Flt3)、AC-480(靶向所有HER蛋白质,“panHER”)、二磷酸莫替沙尼(靶向VEGF1-3、PDGFR、和c-kit)、狄诺塞(靶向RANKL,抑制SRC)、AMG888(靶向HER3)、以及AP24534(包括Flt3多个靶向)。
示例性丝氨酸/苏氨酸激酶抑制剂包括但不限于雷帕呜(靶向mTOR/FRAP1)、地磷莫司(靶向mTOR)、Certican/依维莫司(靶向mTOR/FRAP1)、AP23573(靶向mTOR/FRAP1)、Eril/法舒地尔盐酸化物(靶向RHO)、阿贝西尼(靶向CDK)、帕博西尼(靶向CDK)、瑞博西尼(靶向CDK)、黄酮吡多(靶向CDK)、塞利西利/CYC202/Roscovitrine(靶向CDK)、SNS-032/BMS-387032(靶向CDK)、芦波妥林(靶向PKC)、Pkc412(靶向PKC)、苔藓抑素(靶向PKC)、KAI-9803(靶向PKC)、SF1126(靶向PI3K)、匹替利司(靶向PI3K)、BKM-120(靶向PI3K)、VX-680(靶向极光激酶)、Azd1152(靶向极光激酶)、Arry-142886/AZD-6244(靶向MAP/MEK)、AZD9291(靶向EFGR)、SCIO-469(靶向MAP/MEK)、GW681323(靶向MAP/MEK)、CC-401(靶向JNK)、CEP-1347(靶向JNK)、MK-1775(靶向Wee)、维利帕尼(靶向PARP)、地西他滨(靶向DNMT)、阿扎胞苷(靶向DNMT)、以及PD 332991(靶向CDK)。
示例性酪氨酸激酶抑制剂包括但不限于埃罗替尼(Tarceva);吉非替尼(Iressa);伊马替尼(Gleevec);索拉非尼(Nexavar);舒尼替尼(Sutent);曲妥珠单抗(Herceptin);贝伐单抗(Avastin);利妥昔单抗(Rituxan);拉帕替尼(Tykerb);西妥昔单抗(Erbitux);帕尼单抗(Vectibix);依维莫司(Afinitor);阿仑单抗(Campath);吉妥珠单抗(Mylotarg);坦罗莫司(Torisel);帕唑帕尼(Votrient);达沙替尼(Sprycel);尼洛替尼(Tasigna);伐他拉尼(Ptk787;ZK222584);CEP-701;SU5614;MLN518;XL999;VX-322;Azd0530;BMS-354825;SKI-606CP-690;AG-490;WHI-P154;WHI-P131;AC-220;或AMG888。适合与具有式(I)-(VIa)的化合物或其药学上可接受的盐组合使用的其他治疗剂的更多实例在2014年5月13日提交的共同未决的美国申请号61/992,881、2014年12月8日提交的国际申请号PCT/US2014/069167中公开,将其各自的内容通过引用以其全文结合在此。
示例性微管蛋白聚合抑制剂包括但不限于长春瑞滨。
示例性促分裂原活化蛋白激酶(MEK)抑制剂包括但不限于曲美替尼、和司美替尼。
示例性BRAF抑制剂包括但不限于威罗菲尼。
可以是维甲酸受体激动剂的示例性第二药剂包括但不限于ATRA。
可以是CBP/p300抑制剂受体激动剂的示例性第二药剂包括但不限于化合物H,或其药学上可接受的盐。
在一些实施例中,该其他治疗剂是多效性途径修饰剂。示例性多效性途径修饰剂包括但不限于CC-122。
本披露提供用于组合疗法的方法,其中向需要治疗疾病或癌症的受试者施用一种组合物,该组合物包含具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种其他治疗剂。本披露提供了用作用于组合疗法的药物的组合物,其中该组合物包含具有式(I)-(VIa)的化合物或其药学上可接受的盐,并且与一种或多种其他治疗剂组合地向需要治疗疾病或癌症的受试者施用。本披露进一步提供了组合物用于制造用于组合疗法的药物的用途,其中该组合物包含具有式(I)-(VIa)的化合物或其药学上可接受的盐,并且与一种或多种其他治疗剂组合地向需要治疗疾病或癌症的受试者施用。组合疗法还可以是被施用癌症细胞以抑制增生或诱导细胞死亡。在一些方面,在施用包含具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种其他治疗剂的本披露的组合物之后,施用具有式(I)-(VIa)的化合物或其药学上可接受的盐。在一些方面,在施用包含具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种其他治疗剂的本披露的组合物之前,施用具有式(I)-(VIa)的化合物或其药学上可接受的盐。在一些方面,在施用一种或多种其他治疗剂之后,施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,以至于这些其他治疗剂是在单一的组合物中或在两种或更多种组合物中被施用,例如,同时地、顺序地、或交替地被施用。在一个方面,在施用一种或多种其他治疗剂之前施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,以至于这些其他治疗剂是在单一的组合物中或在两种或更多种组合物中被施用,例如,同时地、顺序地、或交替地被施用。
在一些方面,在施用包含他泽美司他或其药学上可接受的盐和一种或多种其他治疗剂的本披露的组合物之后,施用他泽美司他或其药学上可接受的盐。在一些方面,在施用包含他泽美司他或其药学上可接受的盐和一种或多种其他治疗剂的本披露的组合物之前,施用他泽美司他或其药学上可接受的盐。在一些方面,在施用一种或多种其他治疗剂之后,施用他泽美司他或其药学上可接受的盐,以至于这些其他治疗剂是在单一的组合物中或在两种或更多种组合物中被施用,例如,同时地、顺序地、或交替地被施用。在一些方面,在施用一种或多种其他治疗剂之前,施用他泽美司他或其药学上可接受的盐,以至于这些其他治疗剂是在单一的组合物中或在两种或更多种组合物中被施用,例如,同时地、顺序地、或交替地被施用。
在一些实施例中,与以下组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物:类烷化剂、抗肿瘤剂、有丝分裂抑制剂、微管蛋白聚合抑制剂、抗代谢药、DNA甲基转移酶(DNMT)抑制剂、组蛋白脱乙酰酶(HDAC)抑制剂、拓扑异构酶抑制剂、表皮生长因子受体(EFGR)抑制剂、EFGR和ErbB2的抑制剂、EFGR和人表皮生长因子受体2(Her2)的抑制剂、间变性淋巴瘤激酶(ALK)抑制剂、ALK和ROS1的抑制剂、ALK和EGFR的抑制剂、细胞周期蛋白依赖性激酶(CDK)4/6抑制剂、促分裂原活化蛋白激酶(MEK)抑制剂、BRAF抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂、Wee1抑制剂、聚(ADP-核糖)聚合酶(PARP)抑制剂、糖皮质激素受体激动剂、维甲酸受体激动剂、CBP/p300抑制剂、或其组合。
在一些实施例中,与以下组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物:类烷化剂、抗肿瘤剂、有丝分裂抑制剂、微管蛋白聚合抑制剂、抗代谢药、DNA甲基转移酶(DNMT)抑制剂、组蛋白脱乙酰酶(HDAC)抑制剂、拓扑异构酶抑制剂、表皮生长因子受体(EFGR)抑制剂、EFGR和ErbB2的抑制剂、EFGR和人表皮生长因子受体2(Her2)的抑制剂、间变性淋巴瘤激酶(ALK)抑制剂、ALK和ROS1的抑制剂、ALK和EGFR的抑制剂、细胞周期蛋白依赖性激酶(CDK)4/6抑制剂、促分裂原活化蛋白激酶(MEK)抑制剂、BRAF抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂、Wee1抑制剂、聚(ADP-核糖)聚合酶(PARP)抑制剂、糖皮质激素受体激动剂、维甲酸受体激动剂、CBP/p300抑制剂、或其组合。
在一些实施例中,与以下组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物:顺铂、奥沙利铂、紫杉醇、多西他赛、长春瑞滨、吉西他滨、地西他滨、阿扎胞苷、伏立诺他、伊立替康、依托泊苷、长春碱、埃罗替尼、吉非替尼、拉帕替尼、阿法替尼、AZD9291、克唑替尼、色瑞替尼、布加替尼、阿贝西尼、帕博西尼、瑞博西尼、甲氨蝶呤、培美曲塞、曲美替尼、司美替尼、威罗菲尼、匹替利司、BKM-120、MK-1775、维利帕尼、泼尼松龙、ATRA、化合物H或其药学上可接受的盐、或其组合。
在一些实施例中,与以下组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物:顺铂、奥沙利铂、紫杉醇、多西他赛、长春瑞滨、吉西他滨、地西他滨、阿扎胞苷、伏立诺他、伊立替康、依托泊苷、长春碱、埃罗替尼、吉非替尼、拉帕替尼、阿法替尼、AZD9291、克唑替尼、色瑞替尼、布加替尼、阿贝西尼、帕博西尼、瑞博西尼、甲氨蝶呤、培美曲塞、曲美替尼、司美替尼、威罗菲尼、匹替利司、BKM-120、MK-1775、维利帕尼、泼尼松龙、ATRA、化合物H或其药学上可接受的盐、或其组合。
在一些实施例中,与烷化剂或类烷化剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与顺铂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与烷化剂或类烷化剂激动剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与顺铂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与抗肿瘤剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与奥沙利铂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与抗肿瘤剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与奥沙利铂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与有丝分裂抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与紫杉醇、多西他赛、长春碱、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与有丝分裂抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与紫杉醇、多西他赛、长春碱、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与微管蛋白聚合抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与长春瑞滨组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与微管蛋白聚合抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与长春瑞滨组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与抗代谢药组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与吉西他滨组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与抗代谢药组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与吉西他滨组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与叶酸型的抗代谢药组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与甲氨蝶呤、培美曲塞、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与叶酸型的抗代谢药组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与甲氨蝶呤、培美曲塞、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与DNA甲基转移酶(DNMT)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与地西他滨、阿扎胞苷、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与DNA甲基转移酶(DNMT)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与地西他滨、阿扎胞苷、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与组蛋白脱乙酰酶(HDAC)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与伏立诺他组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与组蛋白脱乙酰酶(HDAC)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与伏立诺他组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与拓扑异构酶抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与伊立替康、依托泊苷、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与拓扑异构酶抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与伊立替康、依托泊苷、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与埃罗替尼、吉非替尼、AZD9291、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与埃罗替尼、吉非替尼、AZD9291、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)和ErbB2的抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与拉帕替尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)和ErbB2的抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与拉帕替尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)和人表皮生长因子受体2(Her2)的抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与阿法替尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与表皮生长因子受体(EFGR)和人表皮生长因子受体2(Her2)的抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与阿法替尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与色瑞替尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与色瑞替尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)抑制剂和ROS1的抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与克唑替尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)抑制剂和ROS1的抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与克唑替尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)和表皮生长因子受体(EFGR)的抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与布加替尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与间变性淋巴瘤激酶(ALK)和表皮生长因子受体(EFGR)的抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与布加替尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与细胞周期蛋白依赖性激酶(CDK)4/6抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与阿贝西尼、帕博西尼、瑞博西尼、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与细胞周期蛋白依赖性激酶(CDK)4/6抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与阿贝西尼、帕博西尼、瑞博西尼、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与促分裂原活化蛋白激酶(MEK)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与曲美替尼、司美替尼、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与促分裂原活化蛋白激酶(MEK)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与曲美替尼、司美替尼、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与BRAF抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与威罗菲尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与BRAF抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与威罗菲尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与磷脂酰肌醇3-激酶(PI3K)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与匹替利司、BKM-120、或其组合进行组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与磷脂酰肌醇3-激酶(PI3K)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与匹替利司、BKM-120、或其组合进行组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与Wee1抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与MK-1775组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与Wee1抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与MK-1775组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与聚(ADP-核糖)聚合酶(PARP)抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与维利帕尼组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与聚(ADP-核糖)聚合酶(PARP)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与维利帕尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与聚(ADP-核糖)聚合酶(PARP)抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与维利帕尼组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与糖皮质激素受体激动剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与泼尼松龙组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与糖皮质激素受体激动剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与泼尼松龙组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与维甲酸受体激动剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与ATRA组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与维甲酸受体激动剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与ATRA组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与CBP/p300抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与化合物H组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与CBP/p300抑制剂组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。例如,与化合物H的药学上可接受的盐组合地施用具有式(I)-(VIa)的化合物或其药学上可接受的盐,或包含具有式(I)-(VIa)的化合物或其药学上可接受的盐的组合物。
在一些实施例中,与CBP/p300抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与化合物H组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在一些实施例中,与CBP/p300抑制剂组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。例如,与化合物H的药学上可接受的盐组合地施用他泽美司他或其药学上可接受的盐,或包含他泽美司他或其药学上可接受的盐的组合物。
在某些实施例中,“组合疗法”旨在包括以顺序方式施用这些治疗剂,其中在不同时间施用每种治疗剂,以及同时或以基本上同时的方式施用这些治疗剂或这些治疗剂中的至少两种。可以例如通过向受试者施用具有固定比率的每种治疗剂的单一胶囊或以针对这些治疗剂中的每种的多个单一胶囊来完成基本上同时施用。依次或基本上同时施用每一治疗剂,可通过任何适当的途径来实现,包括但不限于口服途径、静脉途径、肌内途径、并通过粘膜组织直接吸收。可以通过相同途径或通过不同途径施用这些治疗剂。例如,可以通过静脉注射施用选定组合的第一治疗剂,同时可以口服地施用该组合的其他治疗剂。可替代地,例如,可以口服地施用所有治疗剂或可以通过静脉注射施用所有治疗剂。也可以交替地施用治疗剂。
在本发明的某些方面,本披露所展示的组合疗法可以在疾病或癌症治疗中产生协同效应。“协同效应”被定义为治疗剂的组合的功效比任何给定的药剂单独的效果的总和要大。协同效应还可以是任何化合物或其他治疗剂作为单一药剂施用时所不能达到的效果。协同效应可以包括但不限于通过减小肿瘤尺寸、抑制肿瘤生长或增加受试者存活来治疗癌症的效果。协同效应还可以包括降低癌症细胞活力、诱发癌症细胞死亡、和抑制或延迟癌症细胞生长。
在本发明的某些方面,“组合疗法”也包括进一步组合其他生物活性成分和非药物治疗(例如,手术或放射治疗)来施用如上文描述的治疗剂。当组合疗法进一步包括非药物治疗时,所述非药物治疗可在任何适合时间进行,只要实现治疗剂与非药物治疗的组合的共同作用的有益效果即可。例如,在适当的情况下,当非药物治疗暂时从治疗剂的施用中移除时(也许是几天或甚至几个星期),仍然能获得有益的效果。
在其他方面,本披露的组合物或其药学上可接受的盐、溶剂化物、类似物或衍生物可与放射疗法组合施用。放射治疗也能与本披露的组合物和本文所述的作为多药剂治疗的一部分的其他化学治疗剂组合施用。
在一些实施例中,可以通过以下实现组合疗法:施用两种或更多种药剂,例如具有式(I)-(VIa)的化合物和如本文所述的一种或多种其他治疗剂,其中将具有式(I)-(VIa)的化合物与一种或多种其他治疗剂分开地配制并且施用。在一些实施例中,通过以单一配制品施用两种或更多种药剂来实现组合治疗。组合疗法也包括其他的组合。例如,两种药剂可以一起配制和与含有第三药剂的单独配制品一起施用。然而,在一些实施例中,组合疗法中的两种或更多种药剂可以同时施用,它们不需要如此。例如,施用第一药剂(或药剂的组合)可以先于施用一种或多种第二药剂(例如药剂的组合)几分钟、几小时、几天、或几个星期。因此,两种或更多种药剂可以在间隔几分钟内施用,或间隔1、2、3、6、9、12、15、18、或24小时内施用,或间隔1、2、3、4、5、6、7、8、9、10、12、14天施用,或间隔2、3、4、5、6、7、8、9、或10星期施用。在一些情况下可能是甚至更长的间隔。然而在许多情况下,最好是在组合疗法中使用的两种或更多种药剂可以同时存在于病人的体内,这不必如此。
在一些实施例中,两种或更多种药剂,例如具有式(I)-(VIa)的化合物和如本文所述的一种或多种其他治疗剂的施用方案是不同的。例如,在一些实施例中,第一药剂,例如如本文提供的EZH2抑制剂是每天施用,例如按100mg和1600mg之间的剂量每天两次,并且一种或多种第二药剂,例如本文提供的抗癌剂,是每周一次、每两周一次施用、每三周一次施用、或每四周一次施用。在一些实施例中,一种药剂,例如EZH2抑制剂是经一个治疗期连续施用,例如每天(例如BID),持续一个月、两个月、三个月、四个月、等的时段,同时一种或多种第二药剂,例如本文提供的抗癌剂,是在此时段期间施用,其中顺序的治疗期由非治疗期隔开,例如两周的治疗,随后是一周的非治疗。可以通过具有与其他药剂的至少一个治疗期重叠的一种药剂的至少一个治疗期,在这样的实施例中实现组合治疗。
本披露还提供了药物组合物,这些药物组合物包含具有式(I)-(VIa)的化合物或其药学上可接受的盐以及本文披露的一种或多种其他治疗剂,并且混合药学上适合剂量的载体或赋形剂来治疗或预防的如本文所述的疾病或病状。在一些方面,本披露还提供了包含以治疗或预防如本文所述的疾病或病症的剂量与药学上适合的载体或一种或多种赋形剂混合的表I的任何化合物或其药学上可接受的盐和一种或多种治疗剂的药物组合物。在其他方面,本披露还提供了包含以治疗或预防如本文所述的疾病或病症的剂量与药学上适合的载体或一种或多种赋形剂混合的他泽美司他
或其药学上可接受的盐和一种或多种其他治疗剂的药物组合物。本披露的药物组合物还可与其他治疗剂或治疗方式同时、相继或交替地组合施用。
本披露的组合物的混合物也可以作为简单的混合物或以适合的配制的药物组合物向患者施用。例如,本发明的一些方面涉及药物组合物,该药物组合物包含:治疗有效剂量的具有式(I)-(VIa)的EZH2抑制剂或其药学上可接受的盐、水合物、对映异构体或立体异构体;一种或多种其他治疗剂以及药学上可接受的稀释剂或载体。
“药物组合物”是含有适于施用于受试者的形式的本披露的化合物的配制品。具有式(I)-(VIa)的化合物(例如他泽美司他)和本文所述的一种或多种其他治疗剂可各自单独地配制或以活性成分的任何组合配制在多种药物组合物中。因此,可基于每种药物组合物的剂型适当地选择一种或多种施用途径。替代性地,可将具有式(I)-(VIa)的化合物(例如他泽美司他)和本文所述的一种或多种其他治疗剂配制成一种药物组合物。
在一些实施例中,适用于本文提供的方法、策略、治疗方式、组合物、或组合的药物组合物是散装的或单位剂型。单位剂型可以是多种形式中的任一种,包括例如胶囊、囊剂、IV袋、片剂、气溶胶吸入器上的单泵或小瓶或安瓿。单位剂量组合物中的活性成分(例如,所披露的化合物或其盐、水合物、溶剂化物或异构体、或此类化合物的组合的配制品)的量是有效量,并且根据所涉及的具体治疗而变化。本领域的技术人员将理解,有时有必要根据患者的年龄和病症对剂量进行常规改变。剂量还将取决于施用途径。考虑了多种途径,包括口服、经肺、经直肠、肠胃外、经皮、皮下、静脉内、肌内、腹膜内、吸入、经颊、舌下、胸膜内、鞘内、鼻内等。用于局部或经皮施用本发明的化合物的剂型包括散剂、喷雾剂、软膏剂、糊剂、乳膏剂、洗剂、凝胶剂、溶液、贴剂以及吸入剂。在一些实施例中,将活性化合物在无菌条件下与药学上可接受的载体以及与所需的任何防腐剂、缓冲剂或推进剂混合。
如本文所用,短语“药学上可接受的”是指在合理的医学判断范围内适用于与人和动物的组织接触而无过度毒性、刺激、过敏反应或其他问题或并发症的与合理的利益/风险比相称的那些化合物、阴离子、阳离子、材料、组合物、载体和/或剂型。
“药学上可接受的赋形剂”意指用于制备药物组合物的赋形剂,该赋形剂通常是安全的、无毒性的并且在生物学上或其他方面都不是不期望的,并且包括兽医用途以及人类药学用途可接受的赋形剂。如说明书和权利要求书中所用的“药学上可接受的赋形剂”包括一种和多于一种这样的赋形剂。
本发明的药物组合物被配制成与其预期的施用途径相容。施用途径的实例包括肠胃外,例如静脉内、皮内、皮下、口服(例如,吸入)、经皮(局部)和经粘膜施用。用于肠胃外、皮内或皮下应用的溶液或悬浮液包含以下组分:无菌稀释剂,例如注射用水、盐水溶液、不挥发油、聚乙二醇、甘油、丙二醇或其他合成溶剂;抗菌剂,例如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,例如抗坏血酸或亚硫酸氢钠;螯合剂,例如乙二胺四乙酸;缓冲剂,例如乙酸盐、柠檬酸盐或磷酸盐,以及用于张力调节的试剂,例如氯化钠或右旋糖。可用酸或碱(例如盐酸或氢氧化钠)调节pH。肠胃外制剂可以封装在由玻璃或塑料制成的安瓿、一次性注射器或多剂量小瓶中。
本发明的组合物可以许多目前用于化学治疗的熟知的方法施用受试者。例如,对于治疗癌症,本发明的化合物可以直接被注射进肿瘤,注射进血流或体腔或口服或使用贴剂应用于皮肤。选择的剂量应该足以构成有效治疗,但不会高到引起不可接受的副作用。应优选地在治疗期间和治疗后的合理期间内密切监测疾病病症(例如,癌症、癌前病变等)的状况和患者的健康状况。
如本文所用,术语“治疗有效量”是指用于治疗、改善或预防已识别的疾病或病症或表现出可检测的治疗或抑制作用的药剂的量。该作用可以通过本领域已知的任何测定方法来检测。用于受试者的精确有效量将取决于受试者的体重、体型和健康状况;病症的性质和程度;以及选择用于施用的治疗剂或治疗剂的组合。对于给定情况的治疗有效量可以通过临床医师的技能和判断范围内的常规实验来确定。在一些方面,待治疗的疾病或病症是癌症。在其他方面,待治疗的疾病或病症是细胞增生性障碍。
在某些实施例中,与单独使用每种药剂的单一疗法相比,当组合使用时,组合使用的每种药剂的治疗有效量将更低。这种较低的治疗有效量可提供治疗方案的较低毒性。
对于任何化合物,治疗有效量最初可以在细胞培养测定(例如,肿瘤细胞的细胞培养测定)中或者在动物模型(通常是大鼠、小鼠、兔、狗或猪)中估算。动物模型也可用于确定适合的浓度范围和施用途径。然后,可使用这样的信息来确定在人体内施用的有效剂量和途径。治疗/预防效力和毒性可通过标准药学程序在细胞培养物或实验动物中测定,例如ED50(对50%群体治疗有效的剂量)和LD50(对50%群体致死的剂量)。毒性与治疗效果之间的剂量比是治疗指数,并且它可以表达为比值LD50/ED50。优选表现出大治疗指数的药物组合物。剂量可在此范围内变化,这取决于所采用的剂型、患者的敏感性和施用途径。
调整剂量和施用以提供足够水平的一种或多种活性剂或维持期望的效果。可考虑的因素包括疾病状况的严重性、受试者的一般健康状况、受试者的年龄、体重和性别、饮食、施用的时间和频率、一种或多种药物组合、反应敏感性以及对疗法的耐受性/响应。长效药物组合物可以每3至4天、每周或每两周一次施用,这取决于特定配制品的半衰期和清除率。
含有本披露活性化合物的药物组合物可以通常已知的方式制备,例如借助常规的混合、溶解、制粒、制糖衣、磨粉、乳化、包封、包埋或冻干工艺的方式。药物组合物可以常规方式使用一种或多种药学上可接受的载体(包括赋形剂和/或助剂)来配制,这些载体促进将活性化合物加工成药学上可用的制剂。当然,适当的配制品取决于所选择的施用途径。
适于注射使用的药物组合物包括无菌水溶液(水溶性时)或分散液和用于临时制备无菌注射溶液或分散液的无菌粉末。对于静脉内施用,适合的载体包括生理盐水、抑菌水、Cremophor ELTM(新泽西州帕西帕尼的巴斯夫公司(BASF,Parsippany,N.J.))或磷酸盐缓冲盐水(PBS)。在所有情况下,组合物必须是无菌的,并且应具有一定程度的流动性,以至于易于注射。它必须在生产和储存条件下保持稳定,并且必须进行防腐处理以防止微生物(例如细菌和真菌)的污染。载体可以是含有例如以下物质的溶剂或分散介质:水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)及其适合的混合物。可例如通过使用例如卵磷脂的包衣、通过在分散液的情况下保持期望的粒径以及通过使用表面活性剂来保持适当的流动性。防止微生物的作用可以通过各种抗细菌剂和抗真菌剂(例如对羟苯甲酸酯、三氯叔丁醇、苯酚、抗坏血酸、硫柳汞等)来实现。在许多情况下,优选在组合物中包括等渗剂,例如糖、多元醇(例如甘露醇和山梨糖醇)以及氯化钠。通过在组合物中包括延迟吸收的试剂(例如,单硬脂酸铝和明胶),可实现可注射组合物的延长吸收。
无菌可注射溶液可通过将所需量的活性化合物与以上列举的成分中的一种或其组合一起掺入到适当的溶剂中,根据需要随后过滤灭菌来制备。通常,通过将活性化合物掺入到无菌媒介物中来制备分散液,该无菌媒介物含有基础分散介质和来自以上列举的那些的所需其他成分。在用于制备无菌注射溶液的无菌粉末的情况下,制备方法是真空干燥和冷冻干燥,其从其先前无菌过滤的溶液中产生活性成分和任何其他所需成分的粉末。
口服组合物通常包含惰性稀释剂或可食用的药学上可接受的载体。它们可封装在明胶胶囊中或压成片剂。出于口服治疗施用的目的,可将活性化合物与赋形剂结合并以片剂、锭剂或胶囊剂的形式使用。口服组合物也可使用流体载体制备以用作漱口剂,其中流体载体中的化合物经口服施用和漱口并吐出或吞咽。药学上相容的粘合剂和/或佐剂材料可作为组合物的一部分包括在内。片剂、丸剂、胶囊剂、锭剂等可含有任何以下成分或具有类似性质的化合物:粘合剂,例如微晶纤维素、黄蓍胶或明胶;赋形剂,例如淀粉或乳糖;崩解剂,例如海藻酸、Primogel或玉米淀粉;润滑剂,例如硬脂酸镁或Streets;助流剂,例如胶体二氧化硅;甜味剂,例如蔗糖或糖精;或调味剂,例如薄荷、水杨酸甲酯或橙味剂。
对于通过吸入施用,将这些化合物以气溶胶喷雾的形式从加压的容器或分配器中递送,这些容器或分配器含有适合的推进剂(例如像二氧化碳的气体)或喷雾器。
全身施用也可通过经粘膜或经皮的方式进行。对于经粘膜或经皮施用,在配制品中使用适合于待渗透的屏障的渗透剂。此类渗透剂通常是本领域已知的,并且包括例如用于经粘膜施用的洗涤剂、胆汁盐和夫西地酸衍生物。经粘膜施用可通过使用鼻喷雾剂或栓剂来实现。对于经皮施用,将活性化合物配制成软膏剂、油膏剂、凝胶剂或乳膏剂,如本领域通常已知的。
活性化合物可与药学上可接受的载体一起制备,这些载体将保护化合物免于从体内快速消除,例如控释配制品,包括植入物和微囊递送系统。可使用可生物降解的生物相容性聚合物,例如乙烯乙酸乙烯酯、聚酐、聚乙醇酸、胶原、聚原酸酯和聚乳酸。此类配制品的制备方法对本领域技术人员而言是显而易见的。这些材料也可从阿尔扎公司(AlzaCorporation)和新星制药有限公司(Nova Pharmaceuticals,Inc.)商购获得。脂质体悬浮液(包括以针对抗病毒抗原的单克隆抗体靶向受感染细胞的脂质体)也可以用作药学上可接受的载体。这些可根据本领域技术人员已知的方法来制备,例如,如在美国专利号4,522,811中所述的。
以剂量单位形式配制口服或肠胃外组合物是特别有利的,以易于施用和剂量统一。如本文所用,剂量单位形式是指适合作为用于待治疗受试者的单一剂量的物理上离散的单位;每单元含有经计算与所需的药物载体一起产生期望的治疗效果的预定量的活性化合物。对于本发明的单位剂型的规格被指示为并且直接取决于活性化合物的独特特征和有待实现的特定治疗效果。
在治疗应用中,本文所述的EZH2抑制剂、本文所述的其他治疗剂、包含具有式(I)-(VIa)的化合物和一种或多种其他治疗剂的组合物、或在按照本发明使用的药物组合物的剂量变化,在影响所选剂量的其他因素中,取决于药剂、接受的患者的年龄、体重和临床状况,以及施用治疗的临床医师或执业医师的经验和判断。通常,剂量应该足以导致肿瘤的生长减慢、并且优选消退,并且还优选地使癌症完全消退。剂量的范围可以是从每天约0.01mg/kg至每天约5000mg/kg。在一些方面,剂量的范围可以是从每天约1mg/kg至每天约1000mg/kg。在一些方面,剂量的范围将为约0.1mg/天至约50g/天;约0.1mg/天至约25g/天;约0.1mg/天至约10g/天;约0.1mg至约3g/天;或约0.1mg至约1g/天,呈单一、分开或连续剂量(该剂量可以针对患者的以kg计的体重、以m2计的体表面积和以岁计的年龄来调整)。药剂的有效量是这样的量,该量提供如由临床医师或其他有资格的观察者注意到的客观上可识别的改善。例如,可参考肿瘤的直径来测量患者的肿瘤消退。肿瘤直径的减小指示消退。消退还通过治疗停止后肿瘤不再出现来指示。如本文所用,术语“剂量有效方式”是指在受试者或细胞中产生期望生物学效应的活性化合物的量。
药物组合物可以同施用说明书一起被包括在容器、包装、或分配器中。
本披露的组合物能够进一步形成盐。本披露的组合物每个分子能够形成多于一个(例如单-、二-、三-)盐。所有这些形式也被考虑在要求保护的发明的范围内。
如本文所用,“药学上可接受的盐”是指本披露的化合物的衍生物,其中母体化合物通过制造其酸或碱的盐来修饰。药学上可接受的盐的实例包括但不限于碱性残基(例如胺)的矿物盐或有机酸盐、酸性残基(例如羧酸)的碱盐或有机盐等。药学上可接受的盐包括例如由无毒的无机酸或有机酸形成的母体化合物的常规无毒盐或季铵盐。例如,此类常规无毒盐包括但不限于源自无机酸和有机酸的那些,这些无机酸和有机酸选自2-乙酰氧基苯甲酸、2-羟基乙烷磺酸、乙酸、抗坏血酸、苯磺酸、苯甲酸、重碳酸、碳酸、柠檬酸、依地酸、乙二磺酸、1,2-乙磺酸、富马酸、葡庚糖酸、葡糖酸、谷氨酸、乙醇酸、乙二醇阿散酸、己基间苯二酚酸、海巴酸、氢溴酸、盐酸、氢碘酸、羟基马来酸、羟萘甲酸、羟乙基磺酸、乳酸、乳糖酸、月桂基磺酸、马来酸、苹果酸、扁桃酸、甲烷磺酸、萘磺酸、硝酸、草酸、扑酸、泛酸、苯乙酸、磷酸、聚半乳糖醛酸、丙酸、水杨酸、硬脂酸、次乙酸、琥珀酸、氨基磺酸、对氨基苯磺酸、硫酸、鞣酸、酒石酸、甲苯磺酸,以及常见的氨基酸,例如甘氨酸、丙氨酸、苯丙氨酸、精氨酸等。
药学上可接受的盐的其他实例包括己酸、环戊烷丙酸、丙酮酸、丙二酸、3-(4-羟基苯甲酰基)苯甲酸、肉桂酸、4-氯苯磺酸、2-萘磺酸、4-甲苯磺酸、樟脑磺酸、4-甲基二环-[2.2.2]-辛-2-烯-1-甲酸、3-苯基丙酸、三甲基乙酸、叔丁基乙酸、粘糠酸等。本披露还涵盖当母体化合物中存在的酸性质子被例如碱金属离子、碱土离子或铝离子的金属离子替代、或与例如乙醇胺、二乙醇胺、三乙醇胺、氨丁三醇、N-甲基葡糖胺等的有机碱配位时形成的盐。
应当理解,所有对药学上可接受的盐的提及均包括相同盐的溶剂加成形式(溶剂化物)。
本披露的组合物还可被制备成酯,例如药学上可接受的酯。例如,可将化合物中的羧酸官能团转化为其相应的酯,例如甲基、乙基或其他酯。而且,可将化合物中的醇基团可转化为其相应的酯,例如乙酸酯、丙酸酯或其他酯。
组合物或其药学上可接受的盐或溶剂化物的施用方式有口服、经鼻、经皮、经肺、吸入、经颊、舌下、腹腔内、皮下、肌内、静脉内、直肠、胸膜内、鞘内和肠胃外。在一些实施例中,该化合物口服施用。本领域技术人员应认识到某些施用途径的优点。
根据多种因素来选择利用这些化合物的剂量方案,这些因素包括患者的类型、种类、年龄、体重、性别和医学病症;待治疗病症的严重程度;施用途径;患者的肾功能和肝功能;以及所采用的具体化合物或其盐。普通技术的医师或兽医可容易地确定并开出预防、抵抗或阻止病症进展所需的药物有效量。
本发明披露的化合物的配制和施用技术可见于Remington:the Science andPractice of Pharmacy[雷明顿:药学科学与实践],第19版,麦克出版公司(MackPublishing Co.),伊斯顿,宾夕法尼亚州(1995)。在一些实施例中,本文所述的化合物及其药学上可接受的盐与药学上可接受的载体或稀释剂组合用于药物制剂中。适合的药学上可接受的载体包括惰性固体填充剂或稀释剂和无菌水溶液或有机溶液。这些化合物将以足以提供在本文所述范围内的期望剂量的量存在于此类药物组合物中。
除非另外指明,否则本文中使用的所有百分比和比率均以重量计。本披露的其他特征和优点从不同实例中显而易见。所提供的实例说明了在实践本披露中有用的不同组分和方法。这些实例并不限制要求保护的发明。基于本披露,技术人员可识别和采用可用于实践本披露的其他组分和方法。
如本文所用,“对其有需要的受试者”是具有EZH2介导的蛋白质甲基化起作用的疾病的受试者,或者相对于大的群体具有增加的发展这样的疾病风险的受试者。在一些实施例中,有需要的受试者患有癌症。“受试者”包括哺乳动物。哺乳动物可以是例如任何哺乳动物,例如人、灵长类、鸟、小鼠、大鼠、家禽、狗、猫、牛、马、山羊、骆驼、绵羊或猪。在一些实施例中,该哺乳动物是人。
本披露的受试者包括已经被诊断为癌症或癌前病症、具有癌症或癌前病症的症状、或具有发展癌症或癌前病症的风险的任何人类受试者。本披露的受试者包括表达突变体EZH2的任何人类受试者。例如,突变体EZH2包括一个或多个突变,其中该突变是取代、点突变、无义突变、错义突变、缺失、或插入或任何其他本文所述的EZH2突变。
有需要的受试者可患有难治性或抗性癌症。“难治性或抗性的癌症”意味着癌症对治疗不响应。该癌症可在治疗开始时就有抗性,或可在治疗期间变得有抗性。在一些实施例中,有需要的受试者的癌症在最近的疗法缓解后复发。在一些实施例中,有需要的受试者接受了所有已知的用于癌症治疗的有效疗法并失败。在一些实施例中,有需要的受试者接受了至少一种先前疗法。在某些实施例中,先前疗法是单一疗法。在某些实施例中,先前疗法是组合疗法。
在一些实施例中,有需要的受试者可能患有由先前疗法引起的继发性癌症。“继发性癌症”是指由于先前的致癌疗法(例如化学疗法)或由其引起的癌症。
该受试者还可表现出对EZH2组蛋白甲基转移酶抑制剂或任何其他治疗剂的抗性。
本文使用的术语“响应性”是与术语“响应”、“敏感”、和“敏感性”可互换,并且它是指当施用本发明的组合物时受试者表现出治疗响应,例如,受试者的肿瘤细胞或肿瘤组织经受细胞凋亡和/或坏死,和/或显示降低的生长、分裂或增生。该术语也指当施用本发明的组合物时,受试者相对于大的群体会或具有更高的概率表现治疗响应,例如,受试者的肿瘤细胞或肿瘤组织经受细胞凋亡和/或坏死和/或显示降低的生长、分裂或增生。
所谓“样品”意思是源自受试者的任何生物样品,包括但不限于细胞、组织样品、体液(包括但不限于粘液、血液、血浆、血清、尿液、唾液、和精液)、肿瘤细胞、以及肿瘤组织。在一些实施例中,样品选自骨髓、外周血细胞、血液、血浆和血清。样品可由接受治疗或测试的受试者提供。替代性地,样品可由医师根据本领域的常规实践获得。
如本文所用,“正常细胞”是不能被分类为“细胞增生性障碍”的一部分的细胞。正常细胞缺乏可导致不希望病症或疾病的发展的不受调节的生长或异常生长或两者。在一些实施例中,正常细胞具有正常运转的细胞周期检查点控制机制。
如本文所用,“接触细胞”是指其中化合物或其他物质的组合物与细胞直接接触或足够接近以在细胞中诱导期望的生物效应的情况。
如本文所用,“候选化合物”是指已经或将要在一个或多个体外或体内生物测试中测定,以确定该化合物是否可能在细胞、组织、系统、动物或人类中引起正在被研究人员或临床医师所寻求的期望的生物学或医学响应的本披露的化合物或其药学上可接受的盐或溶剂化物。候选化合物是本披露的化合物、或其药学上可接受的盐或溶剂化物。该生物学或医学响应可以是癌症的治疗。该生物学或医学响应可以是细胞增生性障碍的治疗或预防。体外或体内生物测定可以包括但不限于酶活性测定、电泳迁移率变动测定、报告基因测定、体外细胞活力测定、以及本文所述的测定。
如本文所用,“治疗”(“treating”或“treat”)描述了出于防治疾病、病症或障碍的目的对患者的管理和护理,并包括施用本披露的化合物或其药学上可接受的盐或溶剂化物,以减轻疾病、病症或障碍的症状或并发症,或消除疾病、病症或障碍。
本披露的组合物或其药学上可接受的盐或溶剂化物,还可以用于预防疾病、病症或障碍。如本文所用,“预防”(“preventing”或“prevent”)描述了减少或消除疾病、病症或障碍的症状或并发症的发作。
本文使用的“减轻”一词是指用来描述一个过程,其中障碍的体征或症状的严重性降低。重要的是,体征或症状可以减轻而不被消除。在一些实施例中,施用本发明的药物组合物导致体征或症状的消除,然而,不需要消除。有效剂量预期降低体征或症状的严重性。例如,可能发生在多个位置的病症例如癌症的体征或症状得以减轻的条件是该癌症的严重性在多个位置中的至少一个内下降了。
如本文所用,术语“严重性”是指描述癌症从癌前期或良性的状态转变成恶性状态的潜力。可替代地或另外地,严重性是指例如根据TNM分期系统(由国际抗癌联盟(UICC)和美国癌症组合委员会(AJCC)接受)或者由其他技术领域公认的方法描述的癌症阶段。癌症阶段指的是基于因素例如原发肿瘤的位置、肿瘤尺寸、肿瘤数和受累的淋巴结(癌症扩散到淋巴结)癌症的程度或严重性。可替代地或另外地,严重性是指由本领域公认的方法(参见,美国国家癌症研究所,www.cancer.gov)描述的肿瘤分级。肿瘤等级是按照癌细胞在显微镜下的外观和肿瘤生长和扩散的可能速度,用于癌细胞分类的系统。当判断肿瘤等级的时候,包括细胞的结构和生长方式的很多因素被考虑。用于确定肿瘤等级的具体因素因每个类型癌症的不同而不同。严重性还描述了一种组织学分级,也称为分化,其是指有多少肿瘤细胞类似于同一组织类型的正常细胞(参见,美国国家癌症研究所,www.cancer.gov)。此外,严重性描述了一种核级,其是指肿瘤细胞中的核的大小和形状以及正在分裂的肿瘤细胞的百分比(参见,美国国家癌症研究所,www.cancer.gov)。
本发明的其他方面,严重性描述了肿瘤已分泌生长因子、降低细胞外基质、成为血管、失去粘附到并列组织或转移的程度。此外,严重性描述了原发肿瘤已经转移的位置的数量。最后,严重性包括治疗不同类型和位置的肿瘤的难度。例如,不能手术的肿瘤、那些更多的接近多个身体系统(血液学和免疫学肿瘤)的那些癌症、和最抵抗传统治疗的那些被认为是最严重的。在这些情况下,延长受试者的预期寿命和/或减轻疼痛,减少癌性细胞的比例或者限制细胞于一个系统,以及改善癌症阶段/肿瘤分级/组织学分级/核级被认为是减轻癌症的体征或症状。
如本文所用,术语“症状”被定义为疾病、病、损伤或某些在体内不正常的指示。症状被经历该症状的个人感觉到或注意到,但可能不容易被其他人注意。其他人被定义为非医护人员。
如本文所用,术语“体征”也被定义为某些在体内不正常的指示。但体征被定义为可以由医生、护士、或其他卫生保健专业人士可以看出的事物。
非小细胞肺癌
肺癌是第二最常见形式的癌症,并且是癌症相关死亡率的主要原因。非小细胞肺癌(NSCLC)是最常见形式的肺癌,占所有肺癌病例的85%。多数患者患有晚期阶段III或IVNSCLC,分别具有24%和4%的5年生存率。因为疾病表现出的晚期性质,所以手术切除通常不是一个选项。对于大部分患者,疗法涉及化学疗法和/或放射治疗。基于疾病阶段、患者表现标准和地理区域偏好,化学疗法的选择是高度可变的。在多数情况下,化学疗法是基于一对药物,该对药物包括铂化剂例如顺铂或卡铂,和第二细胞毒性药物,例如吉西他滨、依托泊苷或多西他赛。对于少数患者,疗法可以包括用靶向突变的或失调的特定蛋白(例如ALK和EGFR)的药剂(例如克唑替尼、吉非替尼和埃罗替尼)进行治疗。基于遗传的或蛋白质组学的标志物,选择用于这些靶向治疗的患者。在晚期NSCLC临床研究中已经评估了大量药剂,然而,在基于化学疗法的治疗中,大部分已经显示非常小的益处,其中中位总体存活期典型地小于11个月。因此,对于改善非小细胞肺癌治疗的新策略,存在极大需求。
癌症
“癌细胞”或“癌性细胞”是体现出细胞增生性障碍即癌症的细胞。任何可重复使用的测量方法均可用于识别癌细胞或癌前细胞。癌细胞或癌前细胞可通过组织样品(例如,活检样品)的组织学分型或分级来识别。癌细胞或癌前细胞可通过使用适当的分子标志物来识别。
示例性癌症包括但不限于肾上腺皮质癌、AIDS相关癌症、AIDS相关淋巴瘤、肛门癌、直肠肛管癌、肛管癌、阑尾癌、儿童小脑星形细胞瘤、儿童脑星形细胞瘤、基底细胞癌、皮肤癌(非黑色素瘤)、胆管癌、肝外胆管癌、肝内胆管癌、膀胱癌、泌尿膀胱癌、骨和关节恶性肿瘤、骨肉瘤和恶性纤维组织细胞瘤、脑癌、脑肿瘤、脑干胶质瘤、小脑星形细胞瘤、脑星形细胞瘤/恶性胶质瘤、室管膜瘤、成神经管细胞瘤、幕上原始神经外胚层肿瘤、视觉通路和下丘脑胶质瘤、乳腺癌、支气管腺瘤/类癌、类癌肿瘤、胃肠道、神经系统癌、神经系统淋巴瘤、中枢神经系统癌、中枢神经系统淋巴瘤、宫颈癌、儿童癌症、慢性淋巴细胞性白血病、慢性髓细胞性白血病、慢性骨髓增生性疾病、结肠癌、结直肠癌、皮肤T细胞淋巴瘤、淋巴性肿瘤、蕈样真菌病、Seziary综合征、子宫内膜癌、食管癌、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、肝外胆管癌、眼癌、眼内黑色素瘤、视网膜母细胞瘤、胆囊癌、胃癌(gastric cancer或stomach cancer)、胃肠道类癌肿瘤、胃肠道间质瘤(GIST)、生殖细胞肿瘤、卵巢生殖细胞瘤、妊娠滋养细胞肿瘤胶质瘤、头颈癌、肝细胞(肝)癌、霍奇金淋巴瘤、下咽癌、眼内黑色素瘤、眼癌、胰岛细胞瘤(内分泌胰腺)、卡波西肉瘤、肾脏癌(kidney cancer)、肾癌(renalcancer)、肾癌、喉癌、急性成淋巴细胞性白血病、急性髓细胞性白血病、慢性淋巴细胞白血病、慢性骨髓性白血病、毛细胞白血病、唇和口腔癌、肝癌、肺癌、非小细胞肺癌、小细胞肺癌、AIDS相关淋巴瘤、非霍奇金淋巴瘤、原发性中枢神经系统淋巴瘤、套细胞淋巴瘤、华氏巨球蛋白血症(Waldenstram macroglobulinemia)、成神经管细胞瘤、黑色素瘤、眼内(眼)黑色素瘤、默克细胞癌(merkel cell carcinoma)、恶性间皮瘤、间皮瘤、转移性鳞状细胞颈癌、口腔癌(mouth cancer)、舌癌、多发性内分泌肿瘤综合征、蕈样真菌病、骨髓增生异常综合征、骨髓增生异常/骨髓增生性疾病、慢性粒细胞性白血病、急性骨髓性白血病、多发性骨髓瘤、慢性骨髓增生性疾病、鼻咽癌、神经母细胞瘤、口腔癌(oral cancer)、口腔癌(oralcavity cancer)、口咽癌、卵巢癌、卵巢上皮癌、卵巢低恶性瘤、胰腺癌、胰岛细胞胰腺癌、鼻窦和鼻腔癌、甲状旁腺癌、阴茎癌、咽喉癌、嗜铬细胞瘤、松果体母细胞瘤和幕上原始神经外胚层肿瘤、垂体肿瘤、浆细胞肿瘤/多发性骨髓瘤、胸膜肺母细胞瘤、前列腺癌、直肠癌、肾盂和输尿管、移行细胞癌、视网膜母细胞瘤、横纹肌肉瘤、唾液腺癌、尤文氏肿瘤家族、卡波西肉瘤、软组织肉瘤、子宫癌、子宫肉瘤、皮肤癌(非黑色素瘤)、皮肤癌(黑色素瘤)、默克细胞皮肤癌、小肠癌、软组织肉瘤、鳞状细胞癌、胃癌(stomach cancer或gastric cancer)、幕上原始神经外胚层肿瘤、睾丸癌、喉癌、胸腺瘤、胸腺瘤和胸腺癌、甲状腺癌、肾盂和输尿管等泌尿器官的移行细胞癌、妊娠滋养细胞肿瘤、尿道癌、子宫内膜癌、子宫肉瘤、宫体癌、阴道癌、外阴癌、和肾母细胞瘤。
“血液系统的细胞增生性障碍”是涉及血液系统的细胞的细胞增生性障碍。血液系统的细胞增生性障碍可以包括淋巴瘤、白血病、髓样肿瘤、肥大细胞肿瘤、脊髓发育不良、良性单克隆丙种球蛋白病、淋巴瘤样肉芽肿、淋巴瘤样丘疹病、真性红细胞增多症、慢性髓细胞白血病、特发性髓样化生、以及特发性血小板增多症。血液系统的细胞增生性障碍可包括血液系统的细胞的增生、异型增生和化生。在一些实施例中,本披露的组合物可用于治疗选自本披露的血液学癌症或本披露的血液细胞增生性障碍组成的组的癌症。本披露的血液癌症可包括多发性骨髓瘤、淋巴瘤(包括霍奇金淋巴瘤、非霍奇金淋巴瘤(例如套细胞淋巴瘤)、儿童期淋巴瘤以及淋巴细胞和皮肤起源的淋巴瘤)、白血病(包括儿童期白血病、毛细胞白血病、急性淋巴细胞性白血病、急性髓细胞性白血病、慢性淋巴细胞性白血病、慢性髓细胞性白血病、慢性骨髓性白血病和肥大细胞白血病)、髓样瘤和肥大细胞瘤。
“肺的细胞增生性障碍”是涉及肺细胞的细胞增生性障碍。肺的细胞增生性障碍可包括影响肺细胞的所有形式的细胞增生性障碍。肺的细胞增生性障碍可包括肺癌、肺的癌前期或癌前病症、肺的良性生长或病变和肺的恶性生长或病变以及除肺外的身体组织和器官中的转移性病变。在一些实施例中,本披露的组合物用于治疗肺癌或肺的细胞增生性障碍。肺癌可包括肺的所有形式的癌症。肺癌可包括恶性肺肿瘤、原位癌、典型的类癌肿瘤和非典型的类癌肿瘤。肺癌可包括小细胞肺癌(“SCLC”)、非小细胞肺癌(“NSCLC”)、鳞状细胞癌、腺癌、小细胞癌、大细胞癌、腺鳞状细胞癌和间皮癌。肺癌可包括“瘢痕癌”、细支气管肺泡癌、巨细胞癌、梭形细胞癌和大细胞神经内分泌癌。肺癌可包括具有组织学和超微结构异质性(例如,混合细胞类型)的肺肿瘤。
肺的细胞增生性障碍可包括影响肺细胞的所有形式的细胞增生性障碍。肺的细胞增生性障碍可以包括肺癌、肺的癌前病症。肺的细胞增生性障碍可包括肺的增生、化生和异型增生。肺的细胞增生性障碍可以包括石棉诱导的增生、鳞状化生、和良性反应性间皮化生。肺的细胞增生性障碍可包括柱状上皮被分层的鳞状上皮替代和粘膜异型增生。暴露于吸入性有害环境物质(例如香烟烟雾和石棉)的个体发生肺细胞增生性障碍的风险可能会增加。可能使个体容易发展成肺细胞增生性障碍的先前的肺部疾病可包括慢性间质性肺病、坏死性肺病、硬皮病、类风湿病、结节病、间质性肺炎、肺结核、反复性肺炎、特发性肺纤维化、肉芽肿、石棉沉滞症、纤维性肺泡炎和霍奇金病。
“结肠的细胞增生性障碍”是涉及结肠细胞的细胞增生性障碍。在一些实施例中,结肠的细胞增生性障碍是结肠癌。在一些实施例中,本披露的组合物用于治疗结肠癌或结肠的细胞增生性障碍。结肠癌可包括结肠的所有形式的癌症。结肠癌可包括散发性和遗传性结肠癌。结肠癌可包括恶性结肠肿瘤、原位癌、典型的类癌肿瘤和非典型的类癌肿瘤。结肠癌可包括腺癌、鳞状细胞癌和腺鳞状细胞癌。结肠癌可与选自由以下组成的组的遗传综合征有关:遗传性非息肉性结直肠癌、家族性腺瘤性息肉病、加德纳氏综合征、波伊茨-耶格综合征、Turcot综合征和青少年息肉病。结肠癌可由选自由以下组成的组的遗传综合征引起:遗传性非息肉性结直肠癌、家族性腺瘤性息肉病、加德纳氏综合征、波伊茨-耶格综合征、Turcot综合征和青少年息肉病。
结肠的细胞增生性障碍可包括影响结肠细胞的所有形式的细胞增生性障碍。结肠的细胞增生性障碍可包括结肠癌、结肠的癌前病症、结肠的腺瘤性息肉和结肠的异时性病变。结肠的细胞增生性障碍可包括腺瘤。结肠的细胞增生性障碍的特征可能在于结肠的增生、化生和异型增生。可使个体易于发展结肠的细胞增生性障碍的先前的结肠病可包括先前的结肠癌。可使个体易于发展结肠的细胞增生性障碍的当前疾病可包括克罗恩病和溃疡性结肠炎。结肠的细胞增生性障碍可能与选自由p53、ras、FAP和DCC组成的组的基因中的突变有关。由于选自由p53、ras、FAP和DCC组成的组的基因中存在突变,因此个体可能具有升高的发展结肠的细胞增生性障碍的风险。
“胰腺的细胞增生性障碍”是涉及胰腺细胞的细胞增生性障碍。胰腺的细胞增生性障碍可包括影响胰腺细胞的所有形式的细胞增生性障碍。胰腺的细胞增生性障碍可以包括胰腺癌、胰腺的癌前期或癌前病症、胰腺增生、和胰腺的发育异常、胰腺的良性生长或病灶、和胰腺的恶性生长或病灶,以及身体除胰腺外的组织和器官中的转移病灶。胰腺癌包括胰腺的所有形式的癌症。胰腺癌可包括导管腺癌、腺鳞癌、多形巨细胞癌、粘液腺癌、破骨细胞样巨细胞癌、粘液性囊腺癌、腺泡癌、未分类大细胞癌、小细胞癌、胰腺母细胞瘤、乳头状瘤、粘液性囊腺瘤、乳头状囊性瘤和浆液性囊腺瘤。胰腺癌还可包括具有组织学和超微结构异质性(例如,混合细胞类型)的胰腺肿瘤。
“前列腺的细胞增生性障碍”是涉及前列腺细胞的细胞增生性障碍。前列腺的细胞增生性障碍可包括影响前列腺细胞的所有形式的细胞增生性障碍。前列腺的细胞增生性障碍可包括前列腺癌、前列腺的癌前期或癌前病症、前列腺的良性生长或病变、前列腺的恶性生长或病变以及除前列腺外的身体组织和器官中的转移性病变。前列腺的细胞增生性障碍可包括前列腺的增生、化生和异型增生。
“皮肤的细胞增生性障碍”是涉及皮肤细胞的细胞增生性障碍。皮肤的细胞增生性障碍可包括影响皮肤细胞的所有形式的细胞增生性障碍。皮肤的细胞增生性障碍可包括皮肤的癌前期或癌前病症、皮肤的良性生长或病变、黑色素瘤、恶性黑色素瘤和皮肤的其他恶性生长或病变以及除皮肤外的身体组织和器官中的转移性病变。皮肤的细胞增生性障碍可包括皮肤的增生、化生和异型增生。
“卵巢的细胞增生性障碍”是涉及卵巢细胞的细胞增生性障碍。卵巢的细胞增生性障碍可包括影响卵巢细胞的所有形式的细胞增生性障碍。卵巢的细胞增生性障碍可包括卵巢的癌前期或癌前病症、卵巢的良性生长或病变、卵巢癌、卵巢的恶性生长或病变以及除卵巢外的身体组织和器官中的转移性病变。皮肤的细胞增生性障碍可包括卵巢细胞的增生、化生和异型增生。
“乳腺的细胞增生性障碍”是涉及乳腺细胞的细胞增生性障碍。乳腺的细胞增生性障碍可包括影响乳腺细胞的所有形式的细胞增生性障碍。乳腺的细胞增生性障碍可包括乳腺癌、乳腺的癌前期或癌前病症、乳腺的良性生长或病变和乳腺的恶性生长或病变以及除乳腺外的身体组织和器官中的转移性病变。乳腺的细胞增生性障碍可包括乳腺的增生、化生和异型增生。
乳腺的细胞增生性障碍可以是乳腺的癌前病症。在一些实施例中,本披露的组合物用于治疗乳腺的癌前病症。乳腺的癌前病症可包括乳腺的异型增生、原位导管癌(DCIS)、导管内癌、原位小叶癌(LCIS)、小叶瘤变和乳腺的0期或0级生长或病变(例如,0期或0级乳腺癌或原位癌)。乳腺的癌前病症可根据美国癌症联合委员会(AJCC)所接受的TNM分类方案来分级,其中原发性肿瘤(T)已被指定为T0或Tis期;并且其中区域淋巴结(N)已被指定为N0期;并且其中远处转移(M)已被指定为M0期。
乳腺的细胞增生性障碍可以是乳腺癌。在一些实施例中,本披露的组合物用于治疗乳腺癌。乳腺癌包括乳腺的所有形式的癌症。乳腺癌可包括原发性上皮性乳腺癌。乳腺癌可包括其中乳腺与其他肿瘤(例如淋巴瘤、肉瘤或黑色素瘤)相关的癌症。乳腺癌可包括乳癌、乳腺导管癌、乳腺小叶癌、乳腺未分化癌、乳腺叶状囊肉瘤、乳腺血管肉瘤和乳腺原发性淋巴瘤。乳腺癌可包括I、II、IIIA、IIIB、IIIC和IV期乳腺癌。乳腺导管癌可包括侵入性癌、具有主要导管内成分的原位侵入性癌、炎性乳腺癌、以及具有选自由以下组成的组的组织类型的乳腺导管癌:粉刺、粘液(胶质)、髓质、具有淋巴细胞浸润的髓质、乳头状、硬化和管状。乳腺的小叶癌可包括具有主要原位成分的侵入性小叶癌、侵入性小叶癌和浸润性小叶癌。乳腺癌可包括佩吉特氏病、具有导管内癌的佩吉特氏病和具有侵入性导管癌的佩吉特氏病。乳腺癌可包括具有组织学和超微结构异质性(例如,混合细胞类型)的乳腺肿瘤。
待治疗的癌症可根据美国癌症联合委员会(AJCC)TNM分类系统来分期,其中肿瘤(T)已被指定为TX、T1、T1mic、T1a、T1b、T1c、T2、T3、T4、T4a、T4b、T4c、或T4d期;并且其中区域淋巴结(N)已被指定为NX、N0、N1、N2、N2a、N2b、N3、N3a、N3b、或N3c期;并且其中远处转移(M)可被指定为MX、M0、或M1期。待治疗的癌症可根据美国癌症联合委员会(AJCC)分类来分期,分为I期、IIA期、IIB期、IIIA期、IIIB期、IIIC期或IV期。待治疗的癌症可根据AJCC分类来指定等级,分为GX级(例如,不能评估的等级)、1级、2级、3级或4级。待治疗的癌症可根据AJCC病理分类(pN)来分级,分为pNX、pN0、PN0(I-)、PN0(I+)、PN0(mol-)、PN0(mol+)、PN1、PN1(mi)、PN1a、PN1b、PN1c、pN2、pN2a、pN2b、pN3、pN3a、pN3b、或pN3c。
待治疗的癌症可包括已确定直径小于或等于约2厘米的肿瘤。待治疗的癌症可包括已确定直径为约2厘米至约5厘米的肿瘤。待治疗的癌症可包括已确定直径大于或等于约3厘米的肿瘤。待治疗的癌症可包括已确定直径大于5厘米的肿瘤。待治疗的癌症可通过微观外观分类为高度分化、中度分化,低分化或未分化。待治疗的癌症可以关于有丝分裂计数(例如,细胞分裂量)或核多态性(例如,细胞变化)通过微观外观分类。待治疗的癌症可通过微观外观被分类为与坏死区域(例如,死亡或退化细胞的区域)有关。待治疗的癌症可被分类为具有异常核型、具有异常数量的染色体或具有一个或多个外观异常的染色体。待治疗的癌症可被分类为非整倍体、三倍体、四倍体或具有改变的倍数性。待治疗的癌症可被分类为具有染色体易位、或整个染色体的缺失或复制、或染色体的一部分的缺失、复制或扩增区域。
待治疗的癌症可通过DNA细胞计数、流式细胞计数或图像细胞计数来评估。待治疗的癌症可被分型为具有10%、20%、30%、40%、50%、60%、70%、80%、或90%的处于细胞分裂合成阶段(例如,处于细胞分裂的S期)的细胞。待治疗的癌症可被分型为具有低S期分率或高S期分率。
癌症是一组可以导致几乎所有的体征或症状的疾病。症状和体征将取决于癌症在哪里、癌症的尺寸、它对附近器官或结构有多大的影响。如果癌症传播(发生转移),那么症状可出现在身体的不同部位。
其中EZH2介导的蛋白质甲基化起作用的病症可以是神经系统疾病。因此,本发明的化合物还可以用于治疗神经疾病,例如癫痫、精神分裂症、双相性精神障碍或其他心理和/或精神障碍、神经病、骨骼肌萎缩、以及神经变性疾病(例如,神经变性疾病)。示例性神经变性疾病包括:阿尔茨海默病、肌萎缩性侧索硬化(ALS)、和帕金森氏病。另一类神经变性疾病包括至少部分地由聚谷氨酰胺的聚集引起的疾病。此类疾病包括:亨廷顿氏病、脊髓延髓性肌肉萎缩(SBMA或肯尼迪氏病)、齿状核红核苍白球路易体萎缩(DRPLA)、脊髓小脑性共济失调1(SCA1)、脊髓小脑性共济失调2(SCA2)、马-约病(MJD;SCA3)、脊髓小脑性共济失调6(SCA6)、脊髓小脑性共济失调7(SCA7)、以及脊髓小脑性共济失调12(SCA12)。
可使用本文所述的组合物和方法来治疗或预防其中由EZH2介导的表观遗传甲基化起作用的任何其他疾病。
对癌症进行治疗可导致肿瘤尺寸的减小。肿瘤尺寸的减小也可被称为“肿瘤消退”。在一些实施例中,在治疗后,肿瘤尺寸相对于治疗前的肿瘤尺寸减小5%或更多;在一些实施例中,肿瘤尺寸减小10%或更多;减小20%或更多;减小30%或更多;减小40%或更多;减小50%或更多;或减小75%或更多。肿瘤的大小可通过任何可重复的测量方式来测量。肿瘤的大小可被测量为肿瘤的直径。
对癌症进行治疗可导致肿瘤体积的减小。在一些实施例中,在治疗后,肿瘤体积相对于治疗前的肿瘤尺寸减小5%或更多;在一些实施例中,肿瘤体积减小10%或更多;减小20%或更多;减小30%或更多;减小40%或更多;甚至减小50%或更多;并且最优选地,减小多于75%或更多。肿瘤体积可通过任何可重复的测量方式来测量。
治疗癌症可导致肿瘤数量的减少。在一些实施例中,在治疗后,肿瘤数量相对于治疗前的数量减少5%或更多;在一些实施例中,肿瘤数量减少10%或更多;减少20%或更多;减少30%或更多;减少40%或更多;甚至减少50%或更多;并且最优选地,减少多于75%。肿瘤的数量可通过任何可重复的测量方式来测量。肿瘤的数量可通过计数肉眼或在指定的放大率下可见的肿瘤来测量。在一些实施例中,指定的放大率是2x、3x、4x、5x、10x、或50x。
对癌症进行治疗可导致远离原发性肿瘤部位的其他组织或器官中的转移性病变的数量减少。在一些实施例中,在治疗后,转移病灶数量相对于治疗前的数量减少5%或更多;在一些实施例中,转移病灶数量减少10%或更多;减少20%或更多;减少30%或更多;减少40%或更多;减少50%或更多;并且最优选地,减少多于75%。转移性病变的数量可通过任何可重复的测量方式来测量。转移性病变的数量可通过计数肉眼或在指定的放大率下可见的肿瘤来测量。在一些实施例中,指定的放大率是2x、3x、4x、5x、10x、或50x。
对癌症进行治疗可导致接受治疗的受试者群体的平均存活时间与仅接受载体的群体相比增加。在一些实施例中,平均存活时间延长超过30天;超过60天;超过90天;并且最优选地,增加超过120天。群体的平均存活时间的增加可通过任何可重复的方式来测量。群体的平均存活时间的增加可例如通过在开始使用活性化合物治疗后计算群体的平均存活长度来测量。群体的平均存活时间的增加可例如通过在使用活性化合物完成第一轮治疗后计算群体的平均存活长度来测量。
对癌症进行治疗可导致接受治疗的受试者群体的平均存活时间与未接受治疗的受试者群体相比增加。在一些实施例中,平均存活时间延长超过30天;超过60天;超过90天;并且最优选地,增加超过120天。群体的平均存活时间的增加可通过任何可重复的方式来测量。群体的平均存活时间的增加可例如通过在开始使用活性化合物治疗后计算群体的平均存活长度来测量。群体的平均存活时间的增加可例如通过在使用活性化合物完成第一轮治疗后计算群体的平均存活长度来测量。
对癌症进行治疗可导致接受治疗的受试者群体的平均存活时间与接受不是本披露的化合物或其药学上可接受的盐、溶剂化物、类似物或衍生物的药物的单一疗法的群体相比增加。在一些实施例中,平均存活时间延长超过30天;超过60天;超过90天;并且最优选地,增加超过120天。群体的平均存活时间的增加可通过任何可重复的方式来测量。群体的平均存活时间的增加可例如通过在开始使用活性化合物治疗后计算群体的平均存活长度来测量。群体的平均存活时间的增加可例如通过在使用活性化合物完成第一轮治疗后计算群体的平均存活长度来测量。
对癌症进行治疗可导致接受治疗的受试者群体的死亡率与仅接受载体的群体相比降低。对癌症进行治疗可导致接受治疗的受试者群体的死亡率与未接受治疗的群体相比降低。对癌症进行治疗可导致接受治疗的受试者群体的死亡率与接受不是本披露的化合物或其药学上可接受的盐、溶剂化物、类似物或衍生物的药物的单一疗法的群体相比降低。在一些实施例中,死亡率降低超过2%;超过5%;超过10%;并且最优选地,降低超过25%。接受治疗的受试者群体的死亡率的降低可通过任何可重复的方式来测量。群体的死亡率的降低可例如通过在开始使用活性化合物治疗后计算每单位时间内群体的疾病相关死亡的平均数量来测量。群体的死亡率的降低可例如通过在使用活性化合物完成第一轮治疗后计算每单位时间内群体的疾病相关死亡的平均数量来测量。
对癌症进行治疗可导致肿瘤生长速率降低。在一些实施例中,在治疗后,肿瘤生长速率相对于治疗之前的数值降低至少5%;在一些实施例中,肿瘤生长速率降低至少10%;降低至少20%;降低至少30%;降低至少40%;降低至少50%;降低至少50%;并且最优选地,降低至少75%。肿瘤生长速率可通过任何可重复的测量方式来测量。肿瘤生长速率可根据每单位时间内肿瘤直径的变化来测量。
对癌症进行治疗可导致肿瘤再生长率降低。在一些实施例中,在治疗后,肿瘤再生长低于5%;在一些实施例中,肿瘤再生长低于10%;低于20%;低于30%;低于40%;低于50%;低于50%;并且最优选地,低于75%。肿瘤再生长率可通过任何可重复的测量方式来测量。肿瘤再生长率例如通过测量在治疗后的先前肿瘤缩小后肿瘤直径的增加来测量。停止治疗后肿瘤复发失败指示肿瘤再生长率的降低。
对细胞增生性障碍进行治疗或预防可导致细胞增生速率降低。在一些实施例中,在治疗后,细胞增生速率降低至少5%;至少10%;至少20%;至少30%;至少40%;至少50%;甚至至少50%;并且最优选地,至少75%。细胞增生速率可通过任何可重复的测量方式来测量。细胞增生速率例如通过测量每单位时间内组织样品中分裂细胞的数量来测量。
对细胞增生性障碍进行治疗或预防可导致增生细胞的比例下降。在一些实施例中,在治疗后,增生细胞的比例下降至少5%;至少10%;至少20%;至少30%;至少40%;至少50%;至少50%;并且最优选地,至少75%。增生细胞的比例可通过任何可重复的测量方式来测量。在一些实施例中,增生细胞的比例例如通过定量组织样品中分裂细胞的数量相对于非分裂细胞的数量来测量。
增生细胞的比例可等同于有丝分裂指数。
对细胞增生性障碍进行治疗或预防可导致细胞增生的面积或区域大小减少。在一些实施例中,在治疗后,细胞增生的面积或区域的大小相对于其治疗前的大小减少至少5%;减少至少10%;减少至少20%;减少至少30%;减少至少40%;减少至少50%;减少至少50%;并且最优选地,减少至少75%。细胞增生的面积或区域大小可通过任何可重复的测量方式来测量。细胞增生的面积或区域大小可被测量为细胞增生面积或区域的直径或宽度。
对细胞增生性障碍进行治疗或预防可以导致增生细胞,例如恶性细胞的存活或活力的降低。在一些实施例中,在治疗后,相对于治疗前的存活或活力的比率,增生细胞的存活或活力减少至少5%;减少至少10%;减少至少20%;减少至少30%;减少至少40%;减少至少50%;减少至少50%;以及减少至少75%,减少至少80%,减少至少90%,减少至少95%,减少至少99%。增生细胞的存活或活力的比率可以通过任何可重复的测量方式来测量。本文描述了用于测量细胞活力、存活、和增生速率的一些示例性适合的测定,并且基于本披露和本领域的知识,另外的适合的测定对于本领域技术人员来说将是显而易见的。在一些示例性实施例中,例如通过相对于初始细胞数量,在某一治疗时间后,量化剩余细胞的数量,来测量增生细胞的存活的比率。在一些实施例中,例如,在体外细胞活力测定中,测量细胞活力。
对细胞增生性障碍进行治疗或预防可导致具有异常外观或形态的细胞的数量或比例减少。在一些实施例中,在治疗后,具有异常形态的细胞数相对于其在治疗之前的数量减少至少5%;减少至少10%;减少至少20%;减少至少30%;减少至少40%;减少至少50%;减少至少50%;并且最优选地,减少至少75%。异常的细胞外观或形态可通过任何可重复的测量方法来测量。异常的细胞形态可通过显微镜(例如使用倒置的组织培养显微镜)来测量。异常细胞形态可以采取核多形性的形式。
如本文所用,术语“选择性地”是指倾向于在一个群体中比在另一群体中以更高的频率发生。比较的群体可以是细胞群体。在一些实施例中,本披露的化合物或其药学上可接受的盐或溶剂化物选择性地作用于癌症或癌前细胞,而不作用于正常细胞。在一些实施例中,本披露的化合物或其药学上可接受的盐或溶剂化物选择性地起作用以调节一种分子靶标(例如,靶蛋白甲基转移酶),但不显著调节另一分子靶标(例如,非靶蛋白甲基转移酶)。本发明还提供了一种选择性地抑制酶(如蛋白质甲基转移酶)的活性的方法。在一些实施例中,如果事件在群体A中的发生频率大于在群体B中发生频率的两倍,那么相对于群体B,所述事件选择性地发生于群体A中。如果事件在群体A中的发生频率大于5倍,那么所述事件选择性地发生。如果事件在群体A中的发生频率大于群体B的十倍;大于五十倍;大于100倍;并且最优选地,在群体A中的频率大于1000倍,那么所述事件选择性地发生。例如,如果细胞死亡在癌细胞中的发生频率大于正常细胞的两倍,那么将认为细胞死亡在癌细胞中选择性地发生。
本披露的组合物(例如,包含具有式(I)-(VIa)的化合物或其药学上可接受的盐和一种或多种其他治疗剂(例如强的松)的组合物)可以调节分子靶标(例如,靶蛋白甲基转移酶)的活性。调节是指刺激或抑制分子靶标的活性。在一些实施例中,如果相对于在相同条件下但仅缺少本披露的化合物或其药学上可接受的盐或溶剂化物的存在的情况下的分子靶标的活性,化合物刺激或抑制分子靶标的活性至少2倍,则本披露的化合物或其药学上可接受的盐或溶剂化物调节该分子靶标的活性。在一些实施例中,如果相对于在相同条件下但仅缺少本披露的化合物或其药学上可接受的盐或溶剂化物的存在的情况下的分子靶标的活性,化合物刺激或抑制分子靶标的活性至少5倍、至少10倍、至少20倍、至少50倍、至少100倍,则本披露的化合物或其药学上可接受的盐或溶剂化物调节该分子靶标的活性。分子靶标的活性可通过任何可重复的方式来测量。分子靶标的活性可在体外或体内测量。例如,分子靶标的活性可通过酶活性测定或DNA结合测定在体外测量,或者分子靶标的活性可通过报告基因表达测定在体内测量。
如果相对于在相同条件下但仅缺少本披露的化合物的存在的情况下的分子靶标的活性,化合物的添加不刺激或不抑制分子靶标的活性大于10%,则本披露的组合物不显著调节该分子靶标的活性。
如本文所用,术语“同工酶选择性”意指与酶的第二同种型相比优先抑制或刺激酶的第一同种型(例如,与蛋白甲基转移酶同工酶β相比优先抑制或刺激蛋白甲基转移酶同工酶α)。在一些实施例中,本披露的化合物或其药学上可接受的盐或溶剂化物在实现生物效应所需的剂量上表现出最小四倍的差异、优选十倍的差异、更优选五十倍的差异。在一些实施例中,本披露的化合物或其药学上可接受的盐或溶剂化物在抑制范围内表现出这种差异,并且该差异以IC50即对感兴趣的分子靶标的50%抑制为例。
向细胞或有需要的受试者施用本披露的组合物可导致感兴趣的蛋白甲基转移酶活性的调节(即刺激或抑制)。
向细胞或有需要的受试者施用本披露的化合物(例如,包含具有式(I)-(VIa)的任何化合物或其药学上可接受的盐和一种或多种其他治疗剂(例如强的松)的组合物)导致细胞内靶标(例如底物)活性的调节(即刺激或抑制)。可用本披露的化合物调节若干细胞内靶标,包括但不限于蛋白质甲基转移酶。
激活是指使物质组合物(例如,蛋白质或核酸)处于适合执行期望生物功能的状态。能够被激活的物质组合物也具有非激活的状态。激活的物质组合物可以具有抑制或刺激的生物学功能或两者。
提高是指物质组合物(例如,蛋白质或核酸)的期望的生物学活性的增加。提高可以通过物质组合物的浓度增加而发生。
治疗癌症或细胞增生性障碍可导致细胞死亡,并且优选地细胞死亡导致群体中细胞数量减少至少10%。在一些实施例中,细胞死亡意指减少至少20%;减少至少30%;减少至少40%;减少至少50%;最优选地,减少至少75%。群体中细胞数量可通过任何可重复的方式来测量。群体中细胞数量可通过荧光激活细胞分选(FACS)、免疫荧光显微镜和光学显微镜来测量。测量细胞死亡的方法如Li等人,Proc Natl Acad Sci USA.[美国国家科学院院刊]100(5):2674-8,2003中所示。在一些方面,细胞死亡通过细胞凋亡发生。
在一些实施例中,本披露的组合物或其药学上可接受的盐或溶剂化物的有效量是对正常细胞没有显著的细胞毒性。如果施用治疗有效量的化合物不会引起正常细胞大于10%的细胞死亡,那么治疗有效量的化合物对正常细胞没有显著的细胞毒性。如果施用治疗有效量的化合物不会引起正常细胞大于10%的细胞死亡,那么治疗有效量的化合物不会显著地影响正常细胞的活力。在一些方面,细胞死亡通过细胞凋亡发生。
使细胞接触本披露的组合物或其药学上可接受的盐或溶剂化物可选择性地诱发或激活癌细胞的细胞死亡。向有需要的受试者施用本披露的化合物或其药学上可接受的盐或溶剂化物可选择性地诱发或激活癌细胞的细胞死亡。使细胞接触本披露的组合物或其药学上可接受的盐或溶剂化物可选择性地诱发受细胞增生性障碍影响的一种或多种细胞的细胞死亡。在一些实施例中,向有需要的受试者施用本披露的组合物或其药学上可接受的盐或溶剂化物选择性地诱发受细胞增生性障碍影响的一种或多种细胞的细胞死亡。
本披露内容涉及通过向有需要的受试者施用本披露内容的组合物或其药学上可接受的盐或溶剂化物来治疗或预防癌症的方法,其中,施用本披露内容的组合物或其药学上可接受的盐或溶剂化物导致以下中的一项或多项:通过在细胞周期的一个或多个阶段(例如,G1期、G1/S期、G2/M期)中的细胞累积、或诱导细胞的衰老、或促进肿瘤细胞分化来阻止癌细胞的增生;通过细胞毒性、坏死或凋亡促进癌细胞的细胞死亡,而不引起大量正常细胞的细胞死亡,并且在动物中抗肿瘤活性具有至少2的治疗指数。如本文所用,“治疗指数”是最大耐受剂量除以有效剂量。
本领域技术人员可以参考一般参考文献来详细描述本文讨论的已知技术或等同技术。这些文献包括:Ausubel等人,Current Protocols in Molecular Biology[分子生物学实验指南],约翰威利父子公司(John Wiley and Sons,Inc.)(2005);Sambrook等人,Molecular Cloning,A Laboratory Manual[分子克隆,实验室手册](第3版),冷泉港出版社(Cold Spring Harbor Press),冷泉港,纽约(2000);Coligan等人,Current Protocolsin Immunology[免疫学实验指南],约翰威利父子公司(John Wiley&Sons),纽约;Enna等人,Current Protocols in Pharmacology[药物学实验指南],约翰威利父子公司(JohnWiley&Sons),纽约;Fingl等人,The Pharmacological Basis of Therapeutics[治疗学的药理学基础](1975),Re mington's Pharmaceutical Sciences[雷明顿制药科学],麦克出版公司(Mack Publishing Co.),伊斯顿,宾夕法尼亚州,第18版(1990)。当然,在制备或使用本发明的方面中可参考这些文献。
实例1:EZH2非小细胞肺癌体外组合研究
方法:使用乳腺癌细胞系进行了体外研究,以评估他泽美司他与第二药剂的组合的抗增生作用。进行了初始增生研究,以确定每种细胞系中他泽美司他的IC50。对于筛选,使用的他泽美司他的括号内浓度在IC50值左右。如果未达到50%抑制浓度,则从10μM开始测试他泽美司他。
为了研究他泽美司他和第二药剂的双重组合对细胞增生的影响,将处于对数线性期生长速率的细胞在烧瓶中用不同浓度的他泽美司他或DMSO预处理7天,铺板在不存在化合物的384孔板中,并在第8天用他泽美司他或DMSO和系列稀释的第二药剂共同处理另外6天(如图1所示)。在第15天,使用Cell Titer Glo显影用于终点分析的板,以测量ATP含量,将其用作细胞活力的指标。在整个测定中,DMSO浓度保持恒定在0.15%v/v。
细胞系:所有细胞系获得自美国典型培养物保藏中心(ATCC;罗克维尔,马里兰州)。在含有以下组分的DMEM:F12培养基中培养NCI-H1573:0.02mg/ml胰岛素、0.01mg/ml转铁蛋白、25nM亚硒酸钠、50nM氢化可的松、1ng/ml表皮生长因子、0.01mM乙醇胺、0.01mM磷酸乙醇胺、100pM三碘甲状腺原氨酸、0.5%(w/v)牛血清白蛋白、0.5mM丙酮酸钠、4.5mM L-谷氨酰胺和1%v/v Pen/Strep。在EMEM+10%胎牛血清(FBS)+1%v/v青霉素/链霉素(P/S)中培养A427、Calu-3、Calu-6细胞系。在F-12K+10%FBS+1%v/v P/S中培养A549细胞。在HITES+5%FBS+1%v/v P/S中培养NCI-H1793。在RPMI-1640+10%FBS中培养HCC827、NCI-H838、NCI-H460、NCI-H661、NCI-H23、NCI-H1299、NCI-H1703、NCI-H1993、NCI-H2030、NCI-H2122和NCI-H522细胞系。
协同作用的分析:使用CHALICE软件(视界发现公司(Horizon Discovery),剑桥,英国)对组合效应和协同作用定量进行了分析,并使用Loewe方法确定了协同作用(Lehar等人,Mol Syst Biol[分子系统生物学]2007;3:80)。Loewe量大于1表示协同作用,而量<-1表示“拮抗作用”。-1和1之间的值表示“加和作用”。如果单一药剂及其组合都不能达到50%抑制浓度,则它被视为“无效”。
他泽美司他和若干护理标准药物以及靶向疗法之间的组合效应的分析结果显示在表2中。
示例性实施例
实施例1.一种用于治疗非小细胞肺癌(NSCLC)的方法,所述方法包括向有需要的受试者施用:
(a)治疗有效量的第一药剂,其中所述第一药剂包括EZH2抑制剂,和
(b)治疗有效量的一种或多种第二药剂。
实施例2.如实施例1所述的方法,其中所述EZH2抑制剂是他泽美司他或其药学上可接受的盐。
实施例3.如实施例1所述的方法,其中治疗有效量的所述EZH2抑制剂是约100mg和约1600mg之间,包括端值在内。
实施例4.如实施例3所述的方法,其中治疗有效量的所述EZH2抑制剂是约100mg、约200mg、约400mg、约800mg、或约1600mg。
实施例5.如实施例4所述的方法,其中治疗有效量的所述EZH2抑制剂是约800mg。
实施例6.如实施例2所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约100mg和约1600mg之间,包括端值在内。
实施例7.如实施例6所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约100mg、约200mg、约400mg、约800mg、或约1600mg。
实施例8.如实施例7所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约800mg。
实施例9.如前述实施例中任一项所述的方法,其中每天两次(BID)施用治疗有效量的所述EZH2抑制剂。
实施例10.如前述实施例中任一项所述的方法,其中口服施用治疗有效量的所述EZH2抑制剂。
实施例11.如实施例10所述的方法,其中作为胶囊或片剂施用治疗有效量的所述EZH2抑制剂。
实施例12.一种抑制或降低癌细胞的生长、活力、存活、或增生的方法,所述方法包括使所述细胞与以下接触:
(a)有效量的EZH2抑制剂,和
(b)一种或多种第二药剂。
实施例13.如实施例12所述的方法,其中所述癌细胞是非小细胞肺癌(NSCLC)细胞。
实施例14.如实施例12或13所述的方法,其中所述EZH2抑制剂是他泽美司他或其药学上可接受的盐。
实施例15.如实施例12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少50%的量。
实施例16.如实施例12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少70%的量。
实施例17.如实施例12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少90%的量。
实施例18.如实施例12-14中任一项所述的方法,其中所述接触是体外的或离体的。
实施例19.如实施例12-14中任一项所述的方法,其中所述接触是体内的,这是通过向携带所述癌细胞的受试者施用所述EZH2抑制剂和所述一种或多种第二药剂。
实施例20.如实施例1-19中任一项所述的方法,其中所述一种或多种第二药剂包括护理标准剂。
实施例21.如实施例1-19中任一项所述的方法,其中所述一种或多种第二药剂包括烷化剂或类烷化剂、抗肿瘤剂、有丝分裂抑制剂、微管蛋白聚合抑制剂、抗代谢药、DNA甲基转移酶(DNMT)抑制剂、组蛋白脱乙酰酶(HDAC)抑制剂、拓扑异构酶抑制剂、表皮生长因子受体(EFGR)抑制剂、EFGR和ErbB2的抑制剂、EFGR和人表皮生长因子受体2(Her2)的抑制剂、间变性淋巴瘤激酶(ALK)抑制剂、ALK和ROS1的抑制剂、ALK和EGFR的抑制剂、细胞周期蛋白依赖性激酶(CDK)4/6抑制剂、促分裂原活化蛋白激酶(MEK)抑制剂、BRAF抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂、Wee1抑制剂、聚(ADP-核糖)聚合酶(PARP)抑制剂、糖皮质激素受体激动剂、维甲酸受体激动剂、CBP/p300抑制剂、或其组合。
实施例22.如实施例21所述的方法,其中所述一种或多种第二药剂包括烷化剂或类烷化剂。
实施例23.如实施例22所述的方法,其中所述一种或多种第二药剂包括顺铂。
实施例24.如实施例21所述的方法,其中所述一种或多种第二药剂包括抗肿瘤剂。
实施例25.如实施例24所述的方法,其中所述一种或多种第二药剂包括奥沙利铂。
实施例26.如实施例21所述的方法,其中所述一种或多种第二药剂包括有丝分裂抑制剂。
实施例27.如实施例26所述的方法,其中所述一种或多种第二药剂包括紫杉醇、多西他赛、长春碱、或其组合。
实施例28.如实施例21所述的方法,其中所述一种或多种第二药剂包括微管蛋白聚合抑制剂。
实施例29.如实施例28所述的方法,其中所述一种或多种第二药剂包括长春瑞滨。
实施例30.如实施例21所述的方法,其中所述一种或多种第二药剂包括抗代谢药。
实施例31.如实施例30所述的方法,其中所述一种或多种第二药剂包括吉西他滨。
实施例32.如实施例30所述的方法,其中所述一种或多种第二药剂包括叶酸型的抗代谢药。
实施例33.如实施例32所述的方法,其中所述一种或多种第二药剂包括甲氨蝶呤、培美曲塞、或其组合。
实施例34.如实施例21所述的方法,其中所述一种或多种第二药剂包括DNA甲基转移酶(DNMT)抑制剂。
实施例35.如实施例34所述的方法,其中所述一种或多种第二药剂包括地西他滨、阿扎胞苷、或其组合。
实施例36.如实施例21所述的方法,其中所述一种或多种第二药剂包括组蛋白脱乙酰酶(HDAC)抑制剂。
实施例37.如实施例36所述的方法,其中所述一种或多种第二药剂包括伏立诺他。
实施例38.如实施例21所述的方法,其中所述一种或多种第二药剂包括拓扑异构酶抑制剂。
实施例39.如实施例38所述的方法,其中所述一种或多种第二药剂包括伊立替康、依托泊苷、或其组合。
实施例40.如实施例21所述的方法,其中所述一种或多种第二药剂包括表皮生长因子受体(EFGR)抑制剂。
实施例41.如实施例40所述的方法,其中所述一种或多种第二药剂包括埃罗替尼、吉非替尼、AZD9291、或其组合。
实施例42.如实施例21所述的方法,其中所述一种或多种第二药剂包括EFGR和ErbB2的抑制剂。
实施例43.如实施例42所述的方法,其中所述一种或多种第二药剂包括拉帕替尼。
实施例44.如实施例21所述的方法,其中所述一种或多种第二药剂包括EFGR和人表皮生长因子受体2(Her2)的抑制剂。
实施例45.如实施例44所述的方法,其中所述一种或多种第二药剂包括阿法替尼。
实施例46.如实施例21所述的方法,其中所述一种或多种第二药剂包括间变性淋巴瘤激酶(ALK)抑制剂。
实施例47.如实施例46所述的方法,其中所述一种或多种第二药剂包括色瑞替尼。
实施例48.如实施例21所述的方法,其中所述一种或多种第二药剂包括ALK和ROS1的抑制剂。
实施例49.如实施例48所述的方法,其中所述一种或多种第二药剂包括克唑替尼。
实施例50.如实施例21所述的方法,其中所述一种或多种第二药剂包括ALK和EFGR的抑制剂。
实施例51.如实施例50所述的方法,其中所述一种或多种第二药剂包括布加替尼。
实施例52.如实施例21所述的方法,其中所述一种或多种第二药剂包括细胞周期蛋白依赖性激酶(CDK)4/6抑制剂。
实施例53.如实施例52所述的方法,其中所述一种或多种第二药剂包括阿贝西尼、帕博西尼、瑞博西尼、或其组合。
实施例54.如实施例21所述的方法,其中所述一种或多种第二药剂包括促分裂原活化蛋白激酶(MEK)抑制剂。
实施例55.如实施例54所述的方法,其中所述一种或多种第二药剂包括曲美替尼、司美替尼、或其组合。
实施例56.如实施例21所述的方法,其中所述一种或多种第二药剂包括BRAF抑制剂。
实施例57.如实施例56所述的方法,其中所述一种或多种第二药剂包括威罗菲尼。
实施例58.如实施例21所述的方法,其中所述一种或多种第二药剂包括磷脂酰肌醇3-激酶(PI3K)抑制剂。
实施例59.如实施例58所述的方法,其中所述一种或多种第二药剂包括匹替利司、BKM-120、或其组合。
实施例60.如实施例21所述的方法,其中所述一种或多种第二药剂包括Wee1抑制剂。
实施例61.如实施例60所述的方法,其中所述一种或多种第二药剂包括MK-1775。
实施例62.如实施例21所述的方法,其中所述一种或多种第二药剂包括聚(ADP-核糖)聚合酶(PARP)抑制剂。
实施例63.如实施例62所述的方法,其中所述一种或多种第二药剂包括维利帕尼。
实施例64.如实施例21所述的方法,其中所述一种或多种第二药剂包括糖皮质激素受体激动剂。
实施例65.如实施例64所述的方法,其中所述一种或多种第二药剂包括泼尼松龙。
实施例66.如实施例21所述的方法,其中所述一种或多种第二药剂包括维甲酸受体激动剂。
实施例67.如实施例66所述的方法,其中所述一种或多种第二药剂包括ATRA。
实施例68.如实施例21所述的方法,其中所述一种或多种第二药剂包括CBP/p300抑制剂。
实施例69.如实施例68所述的方法,其中所述一种或多种第二药剂包括化合物H:
或其药学上可接受的盐。
实施例70.如前述实施例中任一项所述的方法,其中顺序施用所述EZH2抑制剂和所述一种或多种第二药剂。
实施例71.如前述实施例中任一项所述的方法,其中在所述一种或多种第二药剂之前施用所述EZH2抑制剂。
实施例72.如前述实施例中任一项所述的方法,其中在所述EZH2抑制剂之前施用所述一种或多种第二药剂。
实施例73.如前述实施例中任一项所述的方法,其中所述EZH2抑制剂是他泽美司他的药学上可接受的盐。
本文引用的所有出版物和专利文献均通过援引并入本文,如同每个这样的出版物或文献被明确地和单独地指示通过援引并入本文。出版物和专利文献的引用不旨在承认任何出版物和专利文献是相关的现有技术,也不构成对其内容或日期的任何承认。现在已经通过书面描述的方式描述了本发明,本领域的技术人员将认识到,可在各种实施例中实践本发明,并且前述描述和下文的实例是出于说明的目的,并不限制随后的权利要求。如果使用细胞系或基因的名称,除非另有说明或从上下文中明显可见,否则缩写和名称符合美国典型培养物保藏中心(ATCC)或国家生物技术信息中心(NCBI)的命名法。
在不背离本发明的精神或本质特征的情况下,本发明可以以其他具体形式体现。因此,前述实施例在所有方面都应被认为是说明性的,而不是对本文所述的发明的限制。因此本发明的范围是由所附权利要求书而非前述说明书指示的,并且属于权利要求书的含义和等效范围内的所有变化意图被包含在其中。
Claims (73)
1.一种用于治疗非小细胞肺癌(NSCLC)的方法,所述方法包括向有需要的受试者施用:
(a)治疗有效量的第一药剂,其中所述第一药剂包括EZH2抑制剂,和
(b)治疗有效量的一种或多种第二药剂。
2.如权利要求1所述的方法,其中所述EZH2抑制剂是他泽美司他或其药学上可接受的盐。
3.如权利要求1所述的方法,其中治疗有效量的所述EZH2抑制剂是约100mg和约1600mg之间,包括端值在内。
4.如权利要求3所述的方法,其中治疗有效量的所述EZH2抑制剂是约100mg、约200mg、约400mg、约800mg、或约1600mg。
5.如权利要求4所述的方法,其中治疗有效量的所述EZH2抑制剂是约800mg。
6.如权利要求2所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约100mg和约1600mg之间,包括端值在内。
7.如权利要求6所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约100mg、约200mg、约400mg、约800mg、或约1600mg。
8.如权利要求7所述的方法,其中治疗有效量的他泽美司他或其药学上可接受的盐是约800mg。
9.如前述权利要求中任一项所述的方法,其中每天两次(BID)施用治疗有效量的所述EZH2抑制剂。
10.如前述权利要求中任一项所述的方法,其中口服施用治疗有效量的所述EZH2抑制剂。
11.如权利要求10所述的方法,其中作为胶囊或片剂施用治疗有效量的所述EZH2抑制剂。
12.一种抑制或降低癌细胞的生长、活力、存活、或增生的方法,所述方法包括使所述细胞与以下接触:
(a)有效量的EZH2抑制剂,和
(b)一种或多种第二药剂。
13.如权利要求12所述的方法,其中所述癌细胞是非小细胞肺癌(NSCLC)细胞。
14.如权利要求12或13所述的方法,其中所述EZH2抑制剂是他泽美司他或其药学上可接受的盐。
15.如权利要求12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少50%的量。
16.如权利要求12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少70%的量。
17.如权利要求12-14中任一项所述的方法,其中有效量的所述EZH2抑制剂是足以抑制或降低非小细胞肺癌细胞的生长、活力、存活、或增生至少90%的量。
18.如权利要求12-14中任一项所述的方法,其中所述接触是体外的或离体的。
19.如权利要求12-14中任一项所述的方法,其中所述接触是体内的,这是通过向携带所述癌细胞的受试者施用所述EZH2抑制剂和所述一种或多种第二药剂。
20.如权利要求1-19中任一项所述的方法,其中所述一种或多种第二药剂包括护理标准剂。
21.如权利要求1-19中任一项所述的方法,其中所述一种或多种第二药剂包括烷化剂或类烷化剂、抗肿瘤剂、有丝分裂抑制剂、微管蛋白聚合抑制剂、抗代谢药、DNA甲基转移酶(DNMT)抑制剂、组蛋白脱乙酰酶(HDAC)抑制剂、拓扑异构酶抑制剂、表皮生长因子受体(EFGR)抑制剂、EFGR和ErbB2的抑制剂、EFGR和人表皮生长因子受体2(Her2)的抑制剂、间变性淋巴瘤激酶(ALK)抑制剂、ALK和ROS1的抑制剂、ALK和EGFR的抑制剂、细胞周期蛋白依赖性激酶(CDK)4/6抑制剂、促分裂原活化蛋白激酶(MEK)抑制剂、BRAF抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂、Wee1抑制剂、聚(ADP-核糖)聚合酶(PARP)抑制剂、糖皮质激素受体激动剂、维甲酸受体激动剂、CBP/p300抑制剂、或其组合。
22.如权利要求21所述的方法,其中所述一种或多种第二药剂包括烷化剂或类烷化剂。
23.如权利要求22所述的方法,其中所述一种或多种第二药剂包括顺铂。
24.如权利要求21所述的方法,其中所述一种或多种第二药剂包括抗肿瘤剂。
25.如权利要求24所述的方法,其中所述一种或多种第二药剂包括奥沙利铂。
26.如权利要求21所述的方法,其中所述一种或多种第二药剂包括有丝分裂抑制剂。
27.如权利要求26所述的方法,其中所述一种或多种第二药剂包括紫杉醇、多西他赛、长春碱、或其组合。
28.如权利要求21所述的方法,其中所述一种或多种第二药剂包括微管蛋白聚合抑制剂。
29.如权利要求28所述的方法,其中所述一种或多种第二药剂包括长春瑞滨。
30.如权利要求21所述的方法,其中所述一种或多种第二药剂包括抗代谢药。
31.如权利要求30所述的方法,其中所述一种或多种第二药剂包括吉西他滨。
32.如权利要求30所述的方法,其中所述一种或多种第二药剂包括叶酸型的抗代谢药。
33.如权利要求32所述的方法,其中所述一种或多种第二药剂包括甲氨蝶呤、培美曲塞、或其组合。
34.如权利要求21所述的方法,其中所述一种或多种第二药剂包括DNA甲基转移酶(DNMT)抑制剂。
35.如权利要求34所述的方法,其中所述一种或多种第二药剂包括地西他滨、阿扎胞苷、或其组合。
36.如权利要求21所述的方法,其中所述一种或多种第二药剂包括组蛋白脱乙酰酶(HDAC)抑制剂。
37.如权利要求36所述的方法,其中所述一种或多种第二药剂包括伏立诺他。
38.如权利要求21所述的方法,其中所述一种或多种第二药剂包括拓扑异构酶抑制剂。
39.如权利要求38所述的方法,其中所述一种或多种第二药剂包括伊立替康、依托泊苷、或其组合。
40.如权利要求21所述的方法,其中所述一种或多种第二药剂包括表皮生长因子受体(EFGR)抑制剂。
41.如权利要求40所述的方法,其中所述一种或多种第二药剂包括埃罗替尼、吉非替尼、AZD9291、或其组合。
42.如权利要求21所述的方法,其中所述一种或多种第二药剂包括EFGR和ErbB2的抑制剂。
43.如权利要求42所述的方法,其中所述一种或多种第二药剂包括拉帕替尼。
44.如权利要求21所述的方法,其中所述一种或多种第二药剂包括EFGR和人表皮生长因子受体2(Her2)的抑制剂。
45.如权利要求44所述的方法,其中所述一种或多种第二药剂包括阿法替尼。
46.如权利要求21所述的方法,其中所述一种或多种第二药剂包括间变性淋巴瘤激酶(ALK)抑制剂。
47.如权利要求46所述的方法,其中所述一种或多种第二药剂包括色瑞替尼。
48.如权利要求21所述的方法,其中所述一种或多种第二药剂包括ALK和ROS1的抑制剂。
49.如权利要求48所述的方法,其中所述一种或多种第二药剂包括克唑替尼。
50.如权利要求21所述的方法,其中所述一种或多种第二药剂包括ALK和EFGR的抑制剂。
51.如权利要求50所述的方法,其中所述一种或多种第二药剂包括布加替尼。
52.如权利要求21所述的方法,其中所述一种或多种第二药剂包括细胞周期蛋白依赖性激酶(CDK)4/6抑制剂。
53.如权利要求52所述的方法,其中所述一种或多种第二药剂包括阿贝西尼、帕博西尼、瑞博西尼、或其组合。
54.如权利要求21所述的方法,其中所述一种或多种第二药剂包括促分裂原活化蛋白激酶(MEK)抑制剂。
55.如权利要求54所述的方法,其中所述一种或多种第二药剂包括曲美替尼、司美替尼、或其组合。
56.如权利要求21所述的方法,其中所述一种或多种第二药剂包括BRAF抑制剂。
57.如权利要求56所述的方法,其中所述一种或多种第二药剂包括威罗菲尼。
58.如权利要求21所述的方法,其中所述一种或多种第二药剂包括磷脂酰肌醇3-激酶(PI3K)抑制剂。
59.如权利要求58所述的方法,其中所述一种或多种第二药剂包括匹替利司、BKM-120、或其组合。
60.如权利要求21所述的方法,其中所述一种或多种第二药剂包括Wee1抑制剂。
61.如权利要求60所述的方法,其中所述一种或多种第二药剂包括MK-1775。
62.如权利要求21所述的方法,其中所述一种或多种第二药剂包括聚(ADP-核糖)聚合酶(PARP)抑制剂。
63.如权利要求62所述的方法,其中所述一种或多种第二药剂包括维利帕尼。
64.如权利要求21所述的方法,其中所述一种或多种第二药剂包括糖皮质激素受体激动剂。
65.如权利要求64所述的方法,其中所述一种或多种第二药剂包括泼尼松龙。
66.如权利要求21所述的方法,其中所述一种或多种第二药剂包括维甲酸受体激动剂。
67.如权利要求66所述的方法,其中所述一种或多种第二药剂包括ATRA。
68.如权利要求21所述的方法,其中所述一种或多种第二药剂包括CBP/p300抑制剂。
70.如前述权利要求中任一项所述的方法,其中顺序地施用所述EZH2抑制剂和所述一种或多种第二药剂。
71.如前述权利要求中任一项所述的方法,其中在所述一种或多种第二药剂之前施用所述EZH2抑制剂。
72.如前述权利要求中任一项所述的方法,其中在所述EZH2抑制剂之前施用所述一种或多种第二药剂。
73.如前述权利要求中任一项所述的方法,其中所述EZH2抑制剂是他泽美司他的药学上可接受的盐。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762554484P | 2017-09-05 | 2017-09-05 | |
| US62/554,484 | 2017-09-05 | ||
| PCT/US2018/049516 WO2019050924A1 (en) | 2017-09-05 | 2018-09-05 | POLY THERAPY FOR THE TREATMENT OF CANCER |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN111093660A true CN111093660A (zh) | 2020-05-01 |
Family
ID=65635164
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880057161.0A Pending CN111093660A (zh) | 2017-09-05 | 2018-09-05 | 用于治疗癌症的组合疗法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US11452727B2 (zh) |
| EP (1) | EP3678663A4 (zh) |
| JP (2) | JP7399079B2 (zh) |
| CN (1) | CN111093660A (zh) |
| CA (1) | CA3074720A1 (zh) |
| WO (1) | WO2019050924A1 (zh) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111093660A (zh) * | 2017-09-05 | 2020-05-01 | Epizyme股份有限公司 | 用于治疗癌症的组合疗法 |
| CN111217802B (zh) * | 2018-11-27 | 2021-10-08 | 海创药业股份有限公司 | 一类组蛋白乙酰化酶p300抑制剂及其用途 |
| US20220362254A1 (en) * | 2019-08-22 | 2022-11-17 | Thomas Jefferson University | Methods for reprogramming cancer cells |
| TW202114670A (zh) * | 2019-09-30 | 2021-04-16 | 大陸商江蘇恒瑞醫藥股份有限公司 | 一種ezh2抑制劑與cdk4/6抑制劑聯合在製備治療腫瘤藥物中的用途 |
| CN112870366B (zh) * | 2019-11-29 | 2023-01-24 | 江苏恒瑞医药股份有限公司 | Ezh2抑制剂在制备治疗肿瘤药物中的新用途 |
| CN112870367B (zh) * | 2019-11-29 | 2023-01-20 | 江苏恒瑞医药股份有限公司 | Ezh2抑制剂、cdk4/6抑制剂和mek抑制剂在制备治疗肿瘤药物中的用途 |
| BR112023021015A2 (pt) * | 2021-04-21 | 2023-12-19 | Bristol Myers Squibb Co | Métodos de tratamento de linfoma não hodgkin usando 2-(2,6-dioxopiperidin-3-il)-4-((2-fluoro-4-((3-morfolinoazetidin-1-il)metil)benzil)amino) isoindolina-1,3-diona |
| WO2023011533A1 (en) * | 2021-08-04 | 2023-02-09 | Cullgen (Shanghai) , Inc. | Compositions and methods of combination therapy for targeting lymphoma |
| EP4151208A1 (en) * | 2021-09-17 | 2023-03-22 | Universite De Bordeaux | Novel synergistic combinations and methods of uses thereof for treating cancers |
| WO2024059696A1 (en) * | 2022-09-15 | 2024-03-21 | Recurium Ip Holdings, Llc | Combinations |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016168856A1 (en) * | 2015-04-17 | 2016-10-20 | Boston Biomedical, Inc. | Methods for treating cancer |
| WO2017132518A1 (en) * | 2016-01-29 | 2017-08-03 | Epizyme, Inc. | Combination therapy for treating cancer |
Family Cites Families (44)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102061353B1 (ko) | 2010-09-10 | 2020-01-02 | 에피자임, 인코포레이티드 | 인간 ezh2의 억제제 및 이의 사용 방법 |
| EP2681216B1 (en) | 2011-02-28 | 2017-09-27 | Epizyme, Inc. | Substituted 6,5-fused bicyclic heteroaryl compounds |
| TW201733984A (zh) | 2011-04-13 | 2017-10-01 | 雅酶股份有限公司 | 經取代之苯化合物 |
| JO3438B1 (ar) * | 2011-04-13 | 2019-10-20 | Epizyme Inc | مركبات بنزين مستبدلة بأريل أو أريل غير متجانس |
| EP2825161B1 (en) | 2012-03-12 | 2019-01-02 | Epizyme, Inc. | Inhibitors of human ezh2, and methods of use thereof |
| LT3184523T (lt) | 2012-04-13 | 2020-02-10 | Epizyme Inc | N-((4,6-dimetil-2-okso-1,2-dihidropiridin-3-il)metil)-5-(etil (tetrahidro-2h-piran-4-il)amino)-4-metil-4'-(morfolinometil)-[1,1'-bifenil]-3-karboksamido hidrobromidas, skirtas naudoti hematologinės sistemos proliferacinio sutrikimo gydymui |
| CN104768555B (zh) * | 2012-04-13 | 2018-10-30 | Epizyme股份有限公司 | 用于治疗癌症的联合治疗 |
| TWI588131B (zh) | 2012-10-15 | 2017-06-21 | 雅酶股份有限公司 | 經取代苯化合物 |
| RU2018145311A (ru) | 2012-10-15 | 2019-02-18 | Эпизайм, Инк. | Способы лечения рака |
| CA2894216A1 (en) | 2012-12-21 | 2014-06-26 | Epizyme, Inc. | 1,4-pyridone compounds |
| CA2894222A1 (en) | 2012-12-21 | 2014-06-26 | Epizyme, Inc. | 1,4-pyridone bicyclic heteroaryl compounds |
| CN105307683A (zh) | 2013-03-14 | 2016-02-03 | 基因泰克公司 | 治疗癌症和预防癌症药物抗性的方法 |
| CA2903572A1 (en) | 2013-03-15 | 2014-10-23 | Epizyme, Inc. | Substituted benzene compounds |
| WO2014144747A1 (en) | 2013-03-15 | 2014-09-18 | Epizyme, Inc. | Substituted 6,5-fused bicyclic heteroaryl compounds |
| US10150764B2 (en) | 2013-07-19 | 2018-12-11 | Epizyme, Inc. | Substituted benzene compounds |
| WO2015010078A2 (en) | 2013-07-19 | 2015-01-22 | Epizyme, Inc. | Substituted 6,5-fused bicyclic heteroaryl compounds |
| PL3057962T3 (pl) | 2013-10-16 | 2024-01-29 | Epizyme, Inc. | Postać soli chlorowodorku do inhibicji ezh2 |
| US20160228447A1 (en) | 2013-10-18 | 2016-08-11 | Epizyme, Inc. | Method of treating cancer |
| US20160303135A1 (en) | 2013-12-06 | 2016-10-20 | Epizyme, Inc. | Combination therapy for treating cancer |
| KR20230031963A (ko) | 2014-06-17 | 2023-03-07 | 에피자임, 인코포레이티드 | 림프종 치료를 위한 ezh2 억제제 |
| US20170217941A1 (en) | 2014-06-25 | 2017-08-03 | Epizyme, Inc. | Substituted benzene and 6,5-fused bicyclic heteroaryl compounds |
| US20160235716A1 (en) | 2014-09-18 | 2016-08-18 | Abbvie Inc. | Spirocyclic hat inhibitors and methods for their use |
| BR112017007738B1 (pt) | 2014-10-16 | 2023-04-11 | Epizyme, Inc | Método para determinar a probabilidade de eficácia de um tratamento e método para triagem da eficácia de um tratamento compreendendo um inibidor de ezh2 |
| CN116650500A (zh) | 2014-11-17 | 2023-08-29 | Epizyme股份有限公司 | 治疗癌症的方法 |
| JP2018513865A (ja) * | 2015-04-20 | 2018-05-31 | エピザイム,インコーポレイティド | 癌を処置するための併用療法 |
| CA2988816A1 (en) | 2015-06-10 | 2016-12-15 | Epizyme, Inc. | Ezh2 inhibitors for treating lymphoma |
| US10493076B2 (en) | 2015-08-24 | 2019-12-03 | Epizyme, Inc. | Method for treating cancer |
| KR20180054793A (ko) | 2015-09-25 | 2018-05-24 | 에피자임, 인코포레이티드 | 악성 간상소체 종양 또는 고칼슘혈증형 난소의 소세포 암을 치료하는 방법 |
| CA3000983A1 (en) | 2015-10-06 | 2017-04-13 | The Regents Of The University Of Colorado, A Body Corporate | Method of treating medulloblastoma with an ezh2 inhibitor |
| US20190070188A1 (en) | 2015-11-06 | 2019-03-07 | Epizyme, Inc. | Pediatric dosing for treatment of cancer with an ezh2 inhibitor |
| CN108368553A (zh) * | 2015-11-20 | 2018-08-03 | 斯特拉斯堡大学 | 确定癌症患者的个性化治疗策略的方法 |
| US20210052595A1 (en) | 2015-12-07 | 2021-02-25 | Epizyme, Inc. | Inhibitors of ezh2 and methods of use thereof |
| CN108430993A (zh) | 2015-12-17 | 2018-08-21 | 吉利德科学公司 | Tank-结合激酶抑制剂化合物 |
| WO2017139404A1 (en) | 2016-02-08 | 2017-08-17 | Epizyme, Inc. | Methods of treating cancer |
| EP3464643A4 (en) * | 2016-06-01 | 2020-04-01 | Epizyme Inc | USE OF EZH2 INHIBITORS FOR THE TREATMENT OF CANCER |
| US11147819B2 (en) | 2016-06-17 | 2021-10-19 | Epizyme, Inc. | EZH2 inhibitors for treating cancer |
| JP7208898B2 (ja) | 2016-12-02 | 2023-01-19 | エピザイム,インコーポレイティド | 癌を処置するための併用療法 |
| JP7324144B2 (ja) * | 2017-02-02 | 2023-08-09 | エピザイム,インコーポレイティド | 癌処置様式 |
| US11642346B2 (en) * | 2017-03-31 | 2023-05-09 | Epizyme, Inc. | Combination therapy for treating cancer |
| AU2018254577A1 (en) * | 2017-04-21 | 2019-12-05 | Epizyme, Inc. | Combination therapies with EHMT2 inhibitors |
| JP2020522687A (ja) | 2017-06-02 | 2020-07-30 | エピザイム,インコーポレイティド | 癌を処置するためのezh2阻害剤の使用 |
| US20230201212A1 (en) | 2017-06-13 | 2023-06-29 | Epizyme, Inc. | Inhibitors of ezh2 and methods of use thereof |
| CN111093660A (zh) * | 2017-09-05 | 2020-05-01 | Epizyme股份有限公司 | 用于治疗癌症的组合疗法 |
| BR112022016573A2 (pt) * | 2020-02-19 | 2022-11-08 | Epizyme Inc | Inibidores de setd2 e métodos e usos relacionados, incluindo terapias de combinação |
-
2018
- 2018-09-05 CN CN201880057161.0A patent/CN111093660A/zh active Pending
- 2018-09-05 US US16/644,202 patent/US11452727B2/en active Active
- 2018-09-05 JP JP2020512822A patent/JP7399079B2/ja active Active
- 2018-09-05 WO PCT/US2018/049516 patent/WO2019050924A1/en unknown
- 2018-09-05 CA CA3074720A patent/CA3074720A1/en active Pending
- 2018-09-05 EP EP18853157.8A patent/EP3678663A4/en active Pending
-
2022
- 2022-08-22 US US17/892,651 patent/US20230000877A1/en active Pending
-
2023
- 2023-10-06 JP JP2023174378A patent/JP2024001203A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016168856A1 (en) * | 2015-04-17 | 2016-10-20 | Boston Biomedical, Inc. | Methods for treating cancer |
| WO2017132518A1 (en) * | 2016-01-29 | 2017-08-03 | Epizyme, Inc. | Combination therapy for treating cancer |
Non-Patent Citations (1)
| Title |
|---|
| EPIZYME INC: "Epizyme Expands Clinical Collaboration to Study Tazemetostat and TECENTRIQ® Combination in NSCLC", 《WWW.GLOBENEWSWIRE.COM/NEWS-RELEASE/2017/06/26/1028871/0/EN/EPIZYME-EXPANDS-CLINICAL-COLLABORATION-TO-STUDY-TAZEMETOSTAT-AND-TECENTRIQ-COMBINATION-INNSCLC-HEML?PRINT=1》 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3678663A1 (en) | 2020-07-15 |
| CA3074720A1 (en) | 2019-03-14 |
| EP3678663A4 (en) | 2021-06-02 |
| JP2020532556A (ja) | 2020-11-12 |
| JP7399079B2 (ja) | 2023-12-15 |
| US20210060025A1 (en) | 2021-03-04 |
| US11452727B2 (en) | 2022-09-27 |
| US20230000877A1 (en) | 2023-01-05 |
| JP2024001203A (ja) | 2024-01-09 |
| WO2019050924A1 (en) | 2019-03-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN111093660A (zh) | 用于治疗癌症的组合疗法 | |
| US20210053948A1 (en) | Combination therapy for treating cancer | |
| US11951108B2 (en) | Combination therapy for treating cancer | |
| US20220160721A1 (en) | Methods of treating cancer | |
| AU2014236348B2 (en) | Combination therapy for treating cancer | |
| JP2021130700A (ja) | 癌を処置するための併用療法 | |
| JP7208898B2 (ja) | 癌を処置するための併用療法 | |
| JP2017532312A (ja) | 癌を治療するための併用療法 | |
| CN110944628A (zh) | 使用ezh2抑制剂治疗癌症 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |