CN109154002B - 用于治疗显性视网膜色素变性的aav载体 - Google Patents
用于治疗显性视网膜色素变性的aav载体 Download PDFInfo
- Publication number
- CN109154002B CN109154002B CN201780014309.8A CN201780014309A CN109154002B CN 109154002 B CN109154002 B CN 109154002B CN 201780014309 A CN201780014309 A CN 201780014309A CN 109154002 B CN109154002 B CN 109154002B
- Authority
- CN
- China
- Prior art keywords
- rna
- rho
- sequence
- vector
- gene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 208000007014 Retinitis pigmentosa Diseases 0.000 title claims abstract description 19
- 238000011282 treatment Methods 0.000 title description 18
- 239000013607 AAV vector Substances 0.000 title description 5
- 101150079354 rho gene Proteins 0.000 claims abstract description 64
- 230000002452 interceptive effect Effects 0.000 claims abstract description 57
- 239000000203 mixture Substances 0.000 claims abstract description 53
- 150000007523 nucleic acids Chemical class 0.000 claims abstract description 37
- 230000014509 gene expression Effects 0.000 claims abstract description 25
- 102100040756 Rhodopsin Human genes 0.000 claims description 209
- 108091027967 Small hairpin RNA Proteins 0.000 claims description 201
- 239000004055 small Interfering RNA Substances 0.000 claims description 91
- 239000013598 vector Substances 0.000 claims description 58
- 108020004459 Small interfering RNA Proteins 0.000 claims description 39
- 229920002477 rna polymer Polymers 0.000 claims description 22
- 108091070501 miRNA Proteins 0.000 claims description 20
- 101000611338 Homo sapiens Rhodopsin Proteins 0.000 claims description 19
- 239000002679 microRNA Substances 0.000 claims description 16
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 15
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 claims description 12
- 239000013603 viral vector Substances 0.000 claims description 11
- 238000004519 manufacturing process Methods 0.000 claims description 9
- 230000000692 anti-sense effect Effects 0.000 claims description 8
- 230000009452 underexpressoin Effects 0.000 claims description 8
- 230000001939 inductive effect Effects 0.000 claims description 7
- 241000124008 Mammalia Species 0.000 claims description 6
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 6
- 102000014450 RNA Polymerase III Human genes 0.000 claims description 6
- 108010078067 RNA Polymerase III Proteins 0.000 claims description 6
- 229940035893 uracil Drugs 0.000 claims description 6
- 108091026821 Artificial microRNA Proteins 0.000 claims description 5
- 102000009572 RNA Polymerase II Human genes 0.000 claims description 5
- 108010009460 RNA Polymerase II Proteins 0.000 claims description 5
- 239000003814 drug Substances 0.000 claims description 5
- 108091081021 Sense strand Proteins 0.000 claims description 4
- 241000283984 Rodentia Species 0.000 claims description 3
- 239000002671 adjuvant Substances 0.000 claims description 3
- 238000002360 preparation method Methods 0.000 claims description 3
- 239000000969 carrier Substances 0.000 claims description 2
- 239000013613 expression plasmid Substances 0.000 claims description 2
- 102000039446 nucleic acids Human genes 0.000 abstract description 35
- 108020004707 nucleic acids Proteins 0.000 abstract description 35
- 238000000034 method Methods 0.000 abstract description 32
- 201000007737 Retinal degeneration Diseases 0.000 abstract description 19
- 108091032973 (ribonucleotides)n+m Proteins 0.000 abstract description 15
- 102000040650 (ribonucleotides)n+m Human genes 0.000 abstract description 15
- 108700028369 Alleles Proteins 0.000 abstract description 9
- 101800001318 Capsid protein VP4 Proteins 0.000 abstract description 8
- 108090000820 Rhodopsin Proteins 0.000 description 203
- NCYCYZXNIZJOKI-IOUUIBBYSA-N 11-cis-retinal Chemical compound O=C/C=C(\C)/C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C NCYCYZXNIZJOKI-IOUUIBBYSA-N 0.000 description 185
- 108090000623 proteins and genes Proteins 0.000 description 91
- 241000282472 Canis lupus familiaris Species 0.000 description 76
- 241000702423 Adeno-associated virus - 2 Species 0.000 description 73
- 241000282465 Canis Species 0.000 description 63
- 238000002347 injection Methods 0.000 description 61
- 239000007924 injection Substances 0.000 description 61
- 208000002352 blister Diseases 0.000 description 55
- 239000002245 particle Substances 0.000 description 51
- 102000004169 proteins and genes Human genes 0.000 description 45
- 230000015572 biosynthetic process Effects 0.000 description 43
- 238000003786 synthesis reaction Methods 0.000 description 42
- 210000004027 cell Anatomy 0.000 description 41
- 102000040430 polynucleotide Human genes 0.000 description 41
- 108091033319 polynucleotide Proteins 0.000 description 41
- 239000002157 polynucleotide Substances 0.000 description 41
- 230000003612 virological effect Effects 0.000 description 38
- 238000001574 biopsy Methods 0.000 description 37
- 210000001525 retina Anatomy 0.000 description 35
- 238000003197 gene knockdown Methods 0.000 description 34
- 108020004999 messenger RNA Proteins 0.000 description 34
- 230000002207 retinal effect Effects 0.000 description 28
- 238000001262 western blot Methods 0.000 description 23
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 20
- 239000013612 plasmid Substances 0.000 description 20
- 230000004258 retinal degeneration Effects 0.000 description 18
- 101100518359 Homo sapiens RHO gene Proteins 0.000 description 17
- 238000010186 staining Methods 0.000 description 17
- 239000000284 extract Substances 0.000 description 16
- 238000011002 quantification Methods 0.000 description 16
- 230000000670 limiting effect Effects 0.000 description 15
- 108091008695 photoreceptors Proteins 0.000 description 15
- 238000013381 RNA quantification Methods 0.000 description 14
- 238000004458 analytical method Methods 0.000 description 14
- 238000001727 in vivo Methods 0.000 description 13
- 108090000565 Capsid Proteins Proteins 0.000 description 12
- 102100023321 Ceruloplasmin Human genes 0.000 description 12
- 108020004414 DNA Proteins 0.000 description 12
- 238000010790 dilution Methods 0.000 description 12
- 239000012895 dilution Substances 0.000 description 12
- 238000003119 immunoblot Methods 0.000 description 12
- 201000010099 disease Diseases 0.000 description 11
- 239000005090 green fluorescent protein Substances 0.000 description 11
- 238000003384 imaging method Methods 0.000 description 11
- 238000006467 substitution reaction Methods 0.000 description 11
- 239000002299 complementary DNA Substances 0.000 description 10
- 239000002773 nucleotide Substances 0.000 description 10
- 125000003729 nucleotide group Chemical group 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- 101000785755 Homo sapiens Arrestin-C Proteins 0.000 description 9
- 208000035475 disorder Diseases 0.000 description 9
- 238000002474 experimental method Methods 0.000 description 9
- NYHBQMYGNKIUIF-UUOKFMHZSA-N Guanosine Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O NYHBQMYGNKIUIF-UUOKFMHZSA-N 0.000 description 8
- 108010033040 Histones Proteins 0.000 description 8
- 108091026890 Coding region Proteins 0.000 description 7
- 230000001154 acute effect Effects 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 238000003364 immunohistochemistry Methods 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 108090000765 processed proteins & peptides Proteins 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 102000006947 Histones Human genes 0.000 description 6
- 230000009471 action Effects 0.000 description 6
- 238000005520 cutting process Methods 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 230000035772 mutation Effects 0.000 description 6
- 238000010606 normalization Methods 0.000 description 6
- 102000004196 processed proteins & peptides Human genes 0.000 description 6
- 241001634120 Adeno-associated virus - 5 Species 0.000 description 5
- 241000972680 Adeno-associated virus - 6 Species 0.000 description 5
- 238000009010 Bradford assay Methods 0.000 description 5
- 238000001190 Q-PCR Methods 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 241000700605 Viruses Species 0.000 description 5
- 230000002583 anti-histone Effects 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 230000000903 blocking effect Effects 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 239000007853 buffer solution Substances 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 5
- 238000011156 evaluation Methods 0.000 description 5
- 238000011068 loading method Methods 0.000 description 5
- 230000014759 maintenance of location Effects 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 239000002105 nanoparticle Substances 0.000 description 5
- 239000008188 pellet Substances 0.000 description 5
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 5
- 229920001184 polypeptide Polymers 0.000 description 5
- -1 rRNA Proteins 0.000 description 5
- 238000007920 subcutaneous administration Methods 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 108090000994 Catalytic RNA Proteins 0.000 description 4
- 102000053642 Catalytic RNA Human genes 0.000 description 4
- MIKUYHXYGGJMLM-GIMIYPNGSA-N Crotonoside Natural products C1=NC2=C(N)NC(=O)N=C2N1[C@H]1O[C@@H](CO)[C@H](O)[C@@H]1O MIKUYHXYGGJMLM-GIMIYPNGSA-N 0.000 description 4
- NYHBQMYGNKIUIF-UHFFFAOYSA-N D-guanosine Natural products C1=2NC(N)=NC(=O)C=2N=CN1C1OC(CO)C(O)C1O NYHBQMYGNKIUIF-UHFFFAOYSA-N 0.000 description 4
- 241000702421 Dependoparvovirus Species 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 241000699670 Mus sp. Species 0.000 description 4
- 208000027418 Wounds and injury Diseases 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 239000004568 cement Substances 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000030279 gene silencing Effects 0.000 description 4
- 229940029575 guanosine Drugs 0.000 description 4
- 208000014674 injury Diseases 0.000 description 4
- 238000007918 intramuscular administration Methods 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- 150000002632 lipids Chemical class 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 238000003762 quantitative reverse transcription PCR Methods 0.000 description 4
- 239000013646 rAAV2 vector Substances 0.000 description 4
- 101150066583 rep gene Proteins 0.000 description 4
- 108091092562 ribozyme Proteins 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 230000008685 targeting Effects 0.000 description 4
- 238000012876 topography Methods 0.000 description 4
- 238000011269 treatment regimen Methods 0.000 description 4
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 3
- 101150044789 Cap gene Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 102000010175 Opsin Human genes 0.000 description 3
- 108050001704 Opsin Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 238000011529 RT qPCR Methods 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 210000000234 capsid Anatomy 0.000 description 3
- 210000005056 cell body Anatomy 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 238000011532 immunohistochemical staining Methods 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000007912 intraperitoneal administration Methods 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 230000008832 photodamage Effects 0.000 description 3
- 210000000608 photoreceptor cell Anatomy 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000000717 retained effect Effects 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 241001655883 Adeno-associated virus - 1 Species 0.000 description 2
- 241000202702 Adeno-associated virus - 3 Species 0.000 description 2
- 241000580270 Adeno-associated virus - 4 Species 0.000 description 2
- 241001164825 Adeno-associated virus - 8 Species 0.000 description 2
- 241000282709 Aotus trivirgatus Species 0.000 description 2
- 241000282672 Ateles sp. Species 0.000 description 2
- 201000004569 Blindness Diseases 0.000 description 2
- 102100032982 CCR4-NOT transcription complex subunit 9 Human genes 0.000 description 2
- 101150032562 CNOT9 gene Proteins 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 2
- ZTPNVPPLIDWEGE-UHFFFAOYSA-N P.S.S Chemical compound P.S.S ZTPNVPPLIDWEGE-UHFFFAOYSA-N 0.000 description 2
- 102100035591 POU domain, class 2, transcription factor 2 Human genes 0.000 description 2
- 101710084411 POU domain, class 2, transcription factor 2 Proteins 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 229920002873 Polyethylenimine Polymers 0.000 description 2
- 241000288961 Saguinus imperator Species 0.000 description 2
- 241000282695 Saimiri Species 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000007850 degeneration Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- MWRBNPKJOOWZPW-CLFAGFIQSA-N dioleoyl phosphatidylethanolamine Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(COP(O)(=O)OCCN)OC(=O)CCCCCCC\C=C/CCCCCCCC MWRBNPKJOOWZPW-CLFAGFIQSA-N 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 238000013401 experimental design Methods 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 241001515942 marmosets Species 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 238000009126 molecular therapy Methods 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 230000001537 neural effect Effects 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 2
- 210000000880 retinal rod photoreceptor cell Anatomy 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 231100001274 therapeutic index Toxicity 0.000 description 2
- 238000010361 transduction Methods 0.000 description 2
- 230000026683 transduction Effects 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- 241000701161 unidentified adenovirus Species 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- 238000012800 visualization Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- 241001164823 Adeno-associated virus - 7 Species 0.000 description 1
- 101100524317 Adeno-associated virus 2 (isolate Srivastava/1982) Rep40 gene Proteins 0.000 description 1
- 101100524319 Adeno-associated virus 2 (isolate Srivastava/1982) Rep52 gene Proteins 0.000 description 1
- 101100524321 Adeno-associated virus 2 (isolate Srivastava/1982) Rep68 gene Proteins 0.000 description 1
- 101100524324 Adeno-associated virus 2 (isolate Srivastava/1982) Rep78 gene Proteins 0.000 description 1
- 108020005544 Antisense RNA Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000003910 Baronia <angiosperm> Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 102000049320 CD36 Human genes 0.000 description 1
- 108010045374 CD36 Antigens Proteins 0.000 description 1
- 101001086434 Canis lupus familiaris Rhodopsin Proteins 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 241000867610 Chlorocebus pygerythrus Species 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 101150066038 E4 gene Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 102000004437 G-Protein-Coupled Receptor Kinase 1 Human genes 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 241000282575 Gorilla Species 0.000 description 1
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 1
- VSNHCAURESNICA-UHFFFAOYSA-N Hydroxyurea Chemical compound NC(=O)NO VSNHCAURESNICA-UHFFFAOYSA-N 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- 241000282553 Macaca Species 0.000 description 1
- 108700011259 MicroRNAs Proteins 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241000282520 Papio Species 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- 229940079156 Proteasome inhibitor Drugs 0.000 description 1
- 102000017143 RNA Polymerase I Human genes 0.000 description 1
- 108010013845 RNA Polymerase I Proteins 0.000 description 1
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 102000005801 Rod Opsins Human genes 0.000 description 1
- 108010005063 Rod Opsins Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 108020004566 Transfer RNA Proteins 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000010775 animal oil Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 229960001467 bortezomib Drugs 0.000 description 1
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N chembl421 Chemical compound C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000000779 depleting effect Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000000925 erythroid effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 230000009368 gene silencing by RNA Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229960001330 hydroxycarbamide Drugs 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 238000000185 intracerebroventricular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- NBQNWMBBSKPBAY-UHFFFAOYSA-N iodixanol Chemical compound IC=1C(C(=O)NCC(O)CO)=C(I)C(C(=O)NCC(O)CO)=C(I)C=1N(C(=O)C)CC(O)CN(C(C)=O)C1=C(I)C(C(=O)NCC(O)CO)=C(I)C(C(=O)NCC(O)CO)=C1I NBQNWMBBSKPBAY-UHFFFAOYSA-N 0.000 description 1
- 229960004359 iodixanol Drugs 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- RCRODHONKLSMIF-UHFFFAOYSA-N isosuberenol Natural products O1C(=O)C=CC2=C1C=C(OC)C(CC(O)C(C)=C)=C2 RCRODHONKLSMIF-UHFFFAOYSA-N 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 238000011369 optimal treatment Methods 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920000724 poly(L-arginine) polymer Polymers 0.000 description 1
- 108010011110 polyarginine Proteins 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 108010055896 polyornithine Proteins 0.000 description 1
- 229920002714 polyornithine Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000003207 proteasome inhibitor Substances 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 210000002763 pyramidal cell Anatomy 0.000 description 1
- 239000002510 pyrogen Substances 0.000 description 1
- 239000013608 rAAV vector Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 210000004358 rod cell outer segment Anatomy 0.000 description 1
- 102200141512 rs104893768 Human genes 0.000 description 1
- 102200141461 rs104893769 Human genes 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 230000011218 segmentation Effects 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 230000037432 silent mutation Effects 0.000 description 1
- 229920002379 silicone rubber Polymers 0.000 description 1
- 239000004945 silicone rubber Substances 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 239000012096 transfection reagent Substances 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 241000701447 unidentified baculovirus Species 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 108700026220 vif Genes Proteins 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1138—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against receptors or cell surface proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/12—Type of nucleic acid catalytic nucleic acids, e.g. ribozymes
- C12N2310/122—Hairpin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
- C12N2310/141—MicroRNAs, miRNAs
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
- C12N2310/531—Stem-loop; Hairpin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2330/00—Production
- C12N2330/50—Biochemical production, i.e. in a transformed host cell
- C12N2330/51—Specially adapted vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Medicinal Chemistry (AREA)
- Virology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Ophthalmology & Optometry (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Immunology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Pigments, Carbon Blacks, Or Wood Stains (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Paper (AREA)
Abstract
本公开内容的一些方面涉及用于治疗视网膜色素变性的方法和组合物。在一些方面,本公开内容提供了用于向对象递送干扰核酸(例如干扰RNA)以降低所述对象中内源性rho基因的一个或两个等位基因(例如与视网膜色素变性相关的突变rho等位基因)的表达的组合物和方法。在一些实施方案中,还向所述对象递送对所述干扰核酸具有抗性的替代rho基因。
Description
相关申请的交叉引用
本申请要求于2016年3月1日提交的美国临时专利申请No.62/302,122和于2016年9月22日提交的美国临时专利申请No.62/398,451的权益,其各自的内容通过引用整体并入本文。
政府支持
本发明是在由国立卫生研究院(National Institutes of Health)授予的基金号R24-EY022012的政府支持下完成的。政府在本发明中具有某些权利。
背景技术
常染色体显性视网膜色素变性(autosomal dominant retinitis pigmentosa,adRP)是致盲性疾病,其影响1/12,000的人。这些个体中的相当大部分在视网膜中感光细胞的集光色素蛋白(light harvesting pigment protein)视紫红质的基因(rho)中携带突变。该疾病是显性的,因为从任一亲本遗传该突变基因均导致视网膜变性和最终失明。在rho中鉴定的超过100种不同的突变导致失明。目前还没有批准的用于adRP的药物或基因治疗性治疗。因此,需要适合adRP和相关病症的任何和所有原因的有效治疗选择。
发明概述
本申请的一些方面涉及用于在对象中(例如,在人中)治疗视网膜色素变性(例如,显性视网膜色素变性)的组合物和方法。在一些实施方案中,通过向对象(例如,向患有视网膜色素变性的对象,例如向患有显性视网膜色素变性的人)施用干扰RNA分子使对象的视紫红质基因(rho基因)的一个或两个等位基因沉默。在一些实施方案中,还向对象施用替代rho基因(replacement rho gene)以提供功能性RHO蛋白以恢复对象的光感受器功能。在一些实施方案中,替代rho基因相对于内源性基因等位基因具有一个或更多个核苷酸替换,其使替代基因对干扰RNA的作用具有抗性。在一些实施方案中,替代rho基因是人rho基因(例如,野生型人rho基因),其包含使该基因对由干扰RNA分子介导的降解具有抗性(也称为“硬化”)的一个或更多个(例如,1、2、3、4、5个或更多个)替换。在一些实施方案中,该一个或更多个核苷酸替换在rho基因的编码序列中。在一些实施方案中,该一个或更多个核苷酸替换是沉默的(例如,其不改变RHO蛋白的氨基酸序列)。在一些实施方案中,该一个或更多个替换引入氨基酸变化,但所得RHO蛋白仍具有足够的功能以在治疗上有效(以恢复或维持至少部分视力或正常视力)。
在一些实施方案中,可使用任何合适的技术来向对象递送干扰RNA和/或替代基因。在一些实施方案中,以编码干扰RNA的基因的形式向对象提供干扰RNA。在一些实施方案中,编码干扰RNA的基因以重组腺相关病毒(recombinant adeno-associated virus,rAAV)向对象提供。在一些实施方案中,替代基因以rAAV向对象提供。在一些实施方案中,编码干扰RNA的基因和替代基因以同一rAAV提供(例如其均在以AAV末端反向重复(invertedterminal repeat,ITR)为侧翼的同一重组基因组上编码)。在一些实施方案中,这两种基因在同一启动子的控制之下。在一些实施方案中,基因在两种不同启动子的控制之下。在一些实施方案中,编码干扰RNA的基因和替代基因以不同的rAAV提供。
在一些实施方案中,干扰RNA是合成核糖核酸(RNA)分子,其包含:
a)序列CUGCCUACAUGUUUCUGCU(SEQ ID NO:1)的有义链和序列AGCAGAAACAUGUAGGCAG(SEQ ID NO:2)的反义链;
b)序列CCUACAUGUUUCUGCUGAU(SEQ ID NO:3)的有义链和序列AUCAGCAGAAACAUGUAGG(SEQ ID NO:4)的反义链;
c)序列GCAUGGUCAUCAUCAUGGU(SEQ ID NO:5)的有义链和序列ACCAUGAUGAUGACCAUGC(SEQ ID NO:6)的反义链;或
d)序列GUGGCAUUCUACAUCUUCA(SEQ ID NO:7)的有义链和序列UGAAGAUGUAGAAUGCCAC(SEQ ID NO:8)的反义链。
在一些实施方案中,合成RNA分子是小干扰RNA(small interfering RNA,siRNA)。在一些实施方案中,干扰RNA是小发夹RNA(small hairpin RNA,shRNA)。在一些实施方案中,shRNA包含具有序列UCAAGAG(SEQ ID NO:9)的RNA或序列UGUGCUU(SEQ ID NO:10)的RNA的环。
在一些实施方案中,合成RNA分子是人工微RNA(micro RNA,miRNA)。在一些实施方案中,人工miRNA具有以下RNA序列:UGCUGUUGACAGUGAGCGA(X)nUAGUGAAGCCACAGAUGUA(Y)nCUGCCUACUGC
CUCGGA(SEQ ID NO:19),其中:
a)(X)n包含SEQ ID NO:1且(Y)n包含SEQ ID NO:2;
b)(X)n包含SEQ ID NO:3且(Y)n包含SEQ ID NO:4;
c)(X)n包含SEQ ID NO:5且(Y)n包含SEQ ID NO:6;或
d)(X)n包含SEQ ID NO:7且(Y)n包含SEQ ID NO:8。
在一些实施方案中,在上文或本申请其他部分描述的合成RNA还在5′和/或3′端包含未配对的突出端序列(overhang sequence)。在一些实施方案中,未配对的突出端序列包含重复碱基的序列。在一些实施方案中,重复碱基的序列包含重复尿嘧啶(U)碱基。在一些实施方案中,未配对的突出端序列是UU。
在一些实施方案中,组合物(例如,用于施用于对象的组合物)包含一种或更多种(例如,2、3或4种)在上文或本申请其他部分描述的干扰RNA(例如,合成RNA分子)。在一些实施方案中,组合物(例如,用于施用于对象的组合物)包含编码一种或更多种(例如,2、3或4种)在上文或本申请其他部分描述的干扰RNA(例如,合成RNA分子)的核酸(例如,DNA)。
在一些实施方案中,组合物还包含一种或更多种生理学上可接受的载体和/或一种或更多种生理学上可接受的辅料。
在一些实施方案中,载体编码一种或更多种(1、2、3或4种或者更多种)shRNA和/或人工miRNA(例如,在上文或本文其他部分描述的)。在一些实施方案中,shRNA具有SEQ IDNO:11至18中一种或更多种的序列。
在一些实施方案中,载体编码替代rho基因。
在一些实施方案中,载体编码替代rho基因和/或一种或更多种shRNA和/或人工miRNA(例如,在上文或本文其他部分描述的)。
在一些实施方案中,载体是表达质粒。在一些实施方案中,载体是重组病毒基因组(例如,rAAV基因组)。在一些实施方案中,载体是病毒载体。在一些实施方案中,病毒载体包含rAAV基因组。
在一些实施方案中,在对象中降低RHO表达的方法包括向该对象施用包含一种或更多种干扰RNA和/或一种或更多种载体的组合物,所述载体各自编码(例如,能够表达)在上文或本文其他部分描述的一种或更多种干扰RNA。
在一些实施方案中,在对象中治疗视网膜色素变性(retinitis pigmentosa,RP)的方法包括向该对象施用包含干扰RNA或表达干扰RNA的载体的组合物和包含重组rho基因(例如编码重组rho基因的载体)的组合物二者,其中所述rho基因对干扰RNA的靶向具有抗性。
在一些实施方案中,重组rho基因使用rAAV递送。在一些实施方案中,干扰RNA和重组rho基因使用同一rAAV递送。在一些实施方案中,干扰RNA和重组rho基因二者在单启动子序列的表达控制之下。在一些实施方案中,干扰RNA和重组rho基因各自在独立启动子序列(例如,组成型或诱导型启动子)的表达控制之下。在一些实施方案中,干扰RNA和/或经修饰rho基因在人启动子或不同物种的启动子(例如,病毒启动子、原核生物启动子或真核生物启动子,例如来自非人灵长类、啮齿动物、狗、猫、猪或其他物种的启动子)的表达控制之下(例如,与其有效连接)。在一些实施方案中,启动子是RNA聚合酶III启动子(例如,H1RNA聚合酶III启动子)或RNA聚合酶II启动子、或RNA聚合酶I启动子。在一些实施方案中,干扰RNA是shRNA,并且该shRNA在RNA聚合酶III启动子(例如,H1RNA聚合酶III启动子)的表达控制之下。在一些实施方案中,干扰RNA是人工miRNA,并且该人工miRNA在RNA聚合酶II启动子的表达控制之下。在一些实施方案中,重组rho基因在组成型或诱导型启动子(例如,人启动子、眼特异性启动子)的表达控制之下。在一些实施方案中,组成型或诱导型启动子是小鼠启动子(例如,小鼠视蛋白(mouse opsin,MOPS)启动子)。
在一些实施方案中,对象是哺乳动物。在一些实施方案中,哺乳动物是啮齿动物或狗。在一些实施方案中,哺乳动物是人(例如,患有或已知患有(例如被诊断为患有)视网膜色素变性(例如显性视网膜色素变性)的人)。这些和其他方面在以下附图、实例和权利要求书中进行描述。
附图简述
附图和以下简述提供了本文中所述组合物和方法的一些方面的非限制性实例。
图1A-C示出了通过FACS(荧光激活细胞分选(fluorescence-activated cellsorting))测量的GFP标记的人视紫红质的敲减。该实验以三个生物学重复在293T细胞中进行。将500ng GFP标记的人RHO cDNA与不同的siRNA共转染。转染使用2000转染试剂进行。对照是购自Dharmacon的非靶向siRNA。将样品孵育72小时,然后通过流式细胞术分析,首先针对前向和侧向散射设门以排除非活颗粒,然后针对高于自发荧光的GFP表达设门。经对照siRNA处理的GFP阳性细胞的数目设定为100%。
图2示出了通过shRNA的RHO敲减。该实验以三个生物学重复在293T细胞中进行。将200ng GFP标记的人视紫红质与包含由H1启动子驱动的shRNA131、765或820的pUC57共转染。将样品孵育72小时,并且如图1中通过流式细胞术测量RHO敲减。
图3显示,shRNA切割突变和野生型RHO RNA二者。该实验以两个生物学重复和三个qRT-PCR重复在293T细胞中进行。使用2000将200ng GFP标记的人视紫红质(WT、T17M或P23H)与rAAV-H1-shRNA质粒(131(SEQ ID NO:11)、765(SEQ ID NO:15)或820(SEQ ID NO:17))共转染。非靶向shRNA被设计成用于降解不相关的光转导蛋白(视杆(rod)环GMP门控离子通道的亚基)。将样品孵育48小时,然后进行处理用于qRT-PCR分析。
图4示出了在miR30(SEQ ID NO:28)的序列环境中的siRNA131有义链(SEQ ID NO:1)和反义链(SEQ ID NO:2)。在从RNA聚合酶II启动子表达之后,siRNA将通过酶(细胞核中的Drosha和细胞质中的Dicer)从前体切除。
图5A-5C示出了(图5A)取自犬视网膜的泡(bleb)区域和非泡(non-bleb)区域的活检钻取物(biopsy punch)的视紫红质免疫印迹。图5B示出了相对于组蛋白归一化的视紫红质单体量的定量。图5C是显示经归一化量的表。
图6A-6B示出了犬RHO RNA的绝对数。图6A是犬RHO RNA的绝对数的图。图6B是显示绝对RNA数的表。
图7A-7C示出了(图7A)取自犬视网膜的泡区域和非泡区域的活检钻取物的视紫红质免疫印迹。图7B示出了相对于组蛋白归一化的视紫红质单体量的定量。图7C是显示经归一化量的表。
图8A-8B示出了犬RHO RNA的绝对数。图8A是犬RHO RNA的绝对数的图。图8B是显示绝对RNA数的表。
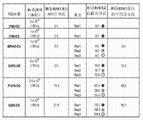
图9描绘了在shRNA与内源性人或硬化(hardened)RHO mRNA的靶序列之间发生的示例性碱基配对。所有shRNA均与狗的RHO mRNA的靶序列完美地碱基配对。白框:shRNA与内源性狗以及硬化RHO mRNA之间的错配。深灰色框:在RNA中鸟苷与尿嘧啶之间发生的弱摆动碱基配对。浅灰色框:仅shRNA与硬化RHO mRNA之间的错配。从上到下,序列分别对应于SEQID NO:29至37。
图10描绘了在shRNA134与内源性人或硬化RHO131mRNA的靶序列之间发生的示例性碱基配对。shRNA 131和134的靶序列接近度使得能够使用相同的硬化RHO131。深灰色框:在RNA中鸟苷与尿嘧啶之间发生的弱摆动碱基配对。浅灰色框:仅shRNA与硬化RHO mRNA之间的错配。从上到下,序列分别对应于SEQ ID NO:38至40。
图11描绘了编码GFP标记的人RHO的质粒的示例性图谱。
图12A-12C示出了编码siRNA(图12A和12B)和人RHO(图12C)的质粒的图谱的非限制性实例。
图13A-13E示出了在WT RHO+/+狗中视网膜下注射不同病毒滴度的AAV2/5-sc-H1-shRNA820下视紫红质敲减的RNA和蛋白质分析。图13A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈(dottedcircle)表示用于每个western印迹重复的泡/经处理和非泡/未经处理区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图13B示出了条形图,其显示作为在同一视网膜的未经处理区域中测量的水平的百分比的经处理区域中剩余的犬视紫红质RNA。图13C示出了免疫印迹,其显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中视紫红质的量。组蛋白H3用于归一化。条形图示出了作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质蛋白。图13D是显示报道为剩余RNA或蛋白质的百分比的来自每个实验的数值的表。图13E是显示报道为RNA或蛋白质的敲减百分比的来自每个实验的数值的另一个表。
图14A-14D示出了在WT狗中视网膜下注射不同滴度的AAV2/5-sc-H1-shRNA820之后ONL和ELM/IS/OS完整性的评估。图14A示出了ONL厚度图;图14B示出了经归一化强度的ELM/IS/OS图;图14C示出了ONL厚度值;并且图14D示出了ELM/IS/OS层的经归一化强度的值。
图15A-15E示出了在突变体RHOT4R/+狗中视网膜下注射不同病毒滴度的AAV2/5-sc-H1-shRNA820下视紫红质敲减的RNA和蛋白质分析。图15A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈表示用于每个western印迹重复的泡区域和非泡区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图15B是显示作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质RNA的量的条形图。图15C是免疫印迹,其显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中犬视紫红质的量。组蛋白H3用于归一化。条形图示出了作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质蛋白的量。图15D是显示报道为剩余RNA或蛋白质的百分比的来自每个实验的数值的表。图15E是显示报道为RNA或蛋白质的敲减百分比的来自每个实验的数值的另一个表。
图16A-16D示出了OCT B扫描,其涵盖在暴露于引起突变体RHOT4R/+狗中急性视网膜变性的短暂光剂量之后2周RHOT4R/+狗的经处理(经不同病毒滴度的AAV2/5-sc-H1-shRNA820处理)和未经处理的视网膜区域。(图16A)经1×1012vg/ml处理的狗的OCT扫描。(图16B)经5×1011vg/ml处理的狗的OCT扫描。(图16C)经2.5×1011vg/ml处理的狗的OCT扫描。(图16D)经1×1011vg/ml处理的狗的OCT扫描。
图17A-17B示出了来自经AAV2/5-sc-H1-shRNA820处理的RHOT4R/+的ONL厚度地形图,其显示针对光诱导的视网膜变性的保护。(图17A)未经处理的WT对照狗的ONL厚度图(左图)和经5E+11vg/ml的AAV2/5-sc-H1-shRNA820处理的EM411-OS的ONL厚度图,并且示出了在光诱导的损伤之后数周经处理/泡区域中保持的ONL厚度。黑色和白色曲线显示如在视网膜下注射之后立即看到的泡的界限。下面的图示出了具有颜色为较深灰色(中间带)的ONL的OCT B扫描用于可视化目的。(图17B)选择在泡外部和内部的位点用于ONL厚度测量。
图18示出了视网膜下不同病毒滴度的AAV2/5-sc-H1-shRNA820的突变体RHOT4R/+视网膜的经处理(Tx)和未经处理(UnTx)区域的组织学(H&E染色)和免疫组织化学(视紫红质染色为绿色并且在图18的下图中显示为浅染色;人视锥拘留蛋白(human cone arrestin)染色为红色并且在图18的下图中显示为灰色染色)。
图19A-19F示出了在突变体RHOT4R/+狗中视网膜下注射5×1011vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820下视紫红质敲减和替代的RNA和蛋白质分析。图19A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈表示用于每个western印迹重复的经处理(Tx)和未经处理(UnTx)区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图19B示出了免疫印迹,其显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中总视紫红质(犬+人RHO820)的量。组蛋白H3用于归一化。条形图示出了经处理和未经处理区域中剩余视紫红质蛋白的百分比。注意EM424-OD和EM425-OD的经处理区域中较低MW条带(对应于突变体T4R RHO蛋白)的损失。图19C是显示用于蛋白质定量的每对钻取物的数值的表。图19D是显示作为在未经处理区域中测量的犬RHO RNA水平的百分比的经处理区域中剩余犬视紫红质RNA的条形图。图19E是显示作为在未经处理区域中测量的犬RHO RNA水平的百分比的经处理区域中人RHO820的水平的条形图。图19F是显示用于RNA定量的每对钻取物的数值的表。
图20A-20C示出了体内视网膜成像,其显示在经5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820处理的突变体RHOT4R/+视网膜区域中针对光诱导的视网膜变性的保护。图20A示出了en face cSLO复合图,其显示在光暴露之后2周被保护免受变性的视网膜区域(边界由白色箭头界定)。浅灰色箭头表示图20B中所示的OCT B扫描在经处理区域中的位置,深灰色箭头表示图20C中所示的OCT B扫描在未经处理区域中的位置。图20B示出了注射之前、注射之后11周和注射之后13周/光暴露之后2周经处理区域中的OCT B扫描。在注射病毒载体之后的这两个时间点在整个经处理区域均保持ONL厚度。图20B和30V示出了注射之前、注射之后11周和注射之后13周/光暴露之后2周未经处理区域中的OCT B扫描。ONL被保持直至注射之后11周,但在光暴露之后2周完全丧失。
图21示出了来自经5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820处理的两个RHOT4R/+的ONL厚度的地形图,其显示针对光诱导的视网膜变性的保护。
图22示出了视网膜下注射有5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820的突变体RHOT4R/+视网膜的经处理区域、过渡区和未经处理区域的免疫组织化学(视紫红质染色为绿色并且在图22的图中显示为浅染色;人视锥拘留蛋白染色为红色并且在图22的图中显示为灰色染色)。
发明详述
本申请的一些方面提供了可用于在对象中(例如,在患有显性视网膜色素变性的对象中)治疗视网膜色素变性的方法和组合物。
在一些实施方案中,使用RNA干扰来降低或抑制内源性视紫红质(例如,突变和正常视紫红质)的表达,并且通过递送被改造以移除RNA抑制剂的靶位点的正常蛋白的基因来替代丢失的蛋白质。
在一些实施方案中,单腺相关病毒(AAV)载体用于递送RNA剂(例如,小发夹RNA或人工微RNA)和重组RHO基因二者。
在一些实施方案中,小发夹RNA、人工微RNA(a-miR)和/或RNA酶(核酶)可设计成通过靶向小鼠、人和狗中共有的序列来降解视紫红质mRNA。这样的分子可用于在细胞培养物、小鼠和/或狗中测试抑制,以开发可在人患者中起作用的抑制剂。
在一些实施方案中,提供了靶向人和狗视紫红质mRNA二者的小干扰核酸(例如,RNA)。在一些实施方案中,提供了四种消化人和犬视紫红质(RHO)mRNA的小干扰RNA,用于耗尽人和动物中内源性产生的视紫红质的目的。在一些实施方案中,这些干扰RNA靶向患有由RHO中突变引起的显性遗传形式的视网膜色素变性的对象中的视紫红质表达。这些突变中的一些导致蛋白质的毒性形式,其合成必须被沉默以防止视网膜变性。
在一些实施方案中,干扰核酸(例如,RNA)被设计成靶向对突变rho基因具有特异性的序列(例如,其与存在于突变rho基因中而不存在于野生型rho基因中的序列互补)。然而,在一些实施方案中,干扰核酸被设计成靶向突变内源性rho基因中的野生型序列(例如,在不被干扰核酸靶向的其他位置具有一个或更多个突变)。在另一些实施方案中,提供对干扰核酸具有抗性的功能性(例如,野生型)rho基因以恢复对象中的RHO活性,并且从而治疗与被干扰核酸靶向的突变内源性rho等位基因相关的疾病或病症的一种或更多种症状。
在一些实施方案中,一种或更多种干扰RNA可作为由启动子(例如,RNA聚合酶III启动子或其他合适的组成型或诱导型启动子)驱动的短发夹RNA(shRNA)或作为由启动子(例如,使用RNA聚合酶II启动子或其他合适的组成型或诱导型启动子)驱动的人工微RNA(miRNA)使用腺相关病毒(AAV)载体递送。
在一些实施方案中,同一载体表达编码正常视紫红质但对由病毒表达的siRNA的作用具有抗性的基因(cDNA)。
表1至4中提供了干扰RNA的一些非限制性实例。
表1:小干扰RNA(siRNA)
| SEQ ID NO: | 名称 | RNA序列 |
| 1 | RHO131-S | CUGCCUACAUGUUUCUGCU |
| 2 | RHO131-A | AGCAGAAACAUGUAGGCAG |
| 3 | RHO134-S | CCUACAUGUUUCUGCUGAU |
| 4 | RHO134-A | AUCAGCAGAAACAUGUAGG |
| 5 | RHO765-S | GCAUGGUCAUCAUCAUGGU |
| 6 | RHO765-A | ACCAUGAUGAUGACCAUGC |
| 7 | RHO820-S | GUGGCAUUCUACAUCUUCA |
| 8 | RHO820-A | UGAAGAUGUAGAAUGCCAC |
表2:发夹环RNA
| SEQ ID NO: | RNA序列 |
| 9 | UCAAGAG |
| 10 | UGUGCUU |
表3:小发夹RNA(shRNA)
表4:微RNA(miRNA)
在一些实施方案中,硬化的正常(例如,野生型)视紫红质(rho)基因可具有以下序列,其基于人rho基因(例如,具有登录号NG_009115.1所示的序列;所述序列也示于SEQ IDNO:41中)或者mRNA或其蛋白质编码部分(例如,由SEQ ID NO:41的核苷酸5001-5456连接至7238-7406连接至8613-8778连接至8895-9134连接至9970-11706编码的mRNA或其蛋白质编码部分,例如由SEQ ID NO:41的核苷酸5096-5456连接至7238-7406连接至8613-8778连接至8895-9134连接至9970-10080组成的编码序列)。在一些实施方案中,正常rho基因的序列被修饰成包含一个或更多个(例如,2、3、4、5、6、7、8、9、10个或更多个)突变,所述突变使替代rho基因对用作敲减剂以降低治疗对象中突变内源性rho基因表达的一种或更多种干扰RNA具有抗性。然而,在一些实施方案中,如果具有未修饰的正常(例如,野生型)序列的重组rho基因与在所治疗对象中靶向的内源性rho基因或等位基因具有不同的序列和如果所使用的敲减剂被设计成靶向内源性rho基因或等位基因而不是所提供的重组rho基因,则可使用具有未修饰的正常(例如,野生型)序列的重组rho基因。在一些实施方案中,可使用来自与治疗对象不同的物种的rho基因。然而,在一些实施方案中,rho基因(例如,经修饰的rho基因)可来自与所治疗对象相同的物种。在一些实施方案中,重组rho基因中的一个或更多个修饰改变编码序列的核酸序列,但不改变编码的蛋白质(例如,其是沉默突变,例如在密码子的第三位,其可包含两种或更多种不同核苷酸中的一种而不改变编码的氨基酸)。在一些实施方案中,重组rho基因不包含野生型rho基因的内含子序列。在一些实施方案中,重组rho基因编码已被修饰成对干扰RNA具有抗性的rho基因的mRNA(或其蛋白质编码部分)。在一些实施方案中,重组rho基因包含已被修饰成对干扰RNA具有抗性的野生型编码序列。在一些实施方案中,经修饰的野生型编码序列与不是来源于野生型rho mRNA的上游和/或下游mRNA序列一起提供。在一些实施方案中,重组替代rho基因包含SEQ ID NO:42。SEQ IDNO:42(示于下文)编码对被称为820的干扰RNA的一个实例(例如,如本文中所述的siRNA820或shRNA820)具有抗性的mRNA序列的一部分。如图9中所示,本文中所述的820干扰RNA序列靶向内源性人rho mRNA中的对应序列,但是SEQ ID NO:42包含使其对820干扰RNA的靶向具有抗性的四个替换(在下文中加有下划线且粗体,其对应于SEQ ID NO:41的第9014、9017、9020和9023位)。SEQ ID NO:42中的编码序列开始于SEQ ID NO:42的第88位。在一些实施方案中,所递送的重组rho基因可包含SEQ ID NO:42的编码序列(例如,开始于SEQ ID NO:42的第88位),但具有不同的上游mRNA序列。在一些实施方案中,重组rho基因可具有一个或更多个其他序列修饰(作为补充或替代)以使其对另外或替代的干扰RNA(例如,本文中提供了其序列的其他干扰RNA)具有抗性。在一些实施方案中,可使用靶向对象中内源性rho编码序列的不同区域的一种或更多种干扰RNA。
SEQ ID NO:42(经修饰的“硬化”重组人rho基因的一个非限制性实例):
因此,本文中的组合物可施用于需要治疗的对象。在一些实施方案中,所述对象患有或被怀疑患有脑和/或眼的一种或更多种病症、疾病或障碍。在一些实施方案中,所述对象患有或被怀疑患有本文中所公开的病症、疾病和障碍中的一种或更多种。在一些实施方案中,所述对象具有一个或更多个内源性突变rho等位基因(例如,与眼或视网膜的疾病或病症相关或者引起眼或视网膜的疾病或病症)。在一些实施方案中,所述对象具有至少一个显性突变rho等位基因(例如,其引起显性视网膜色素变性)。在一些实施方案中,所述对象是人。在一些实施方案中,所述对象是非人灵长类。非人灵长类对象的一些非限制性实例包括猕猴(例如,食蟹猕猴或恒河猕猴)、狨猴(marmoset)、绢毛猴(tamarin)、蜘蛛猴(spidermonkey)、枭猴(owl monkey)、长尾猴(vervet monkey)、松鼠猴(squirrel monkey)、狒狒、大猩猩、黑猩猩和猩猩。另一些示例性对象包括家养动物,例如狗和猫;家畜,例如马、牛、猪、绵羊、山羊和鸡;以及其他动物,例如小鼠、大鼠、豚鼠和仓鼠。
在一些实施方案中,施用于细胞或对象的rAAV颗粒的剂量可以在以下数量级上:106至1014个颗粒/mL或103至1015个颗粒/mL,或者其任一范围之间的任何值,例如,约106、107、108、109、1010、1011、1012、1013或1014个颗粒/mL。在一个实施方案中,施用高于1013个颗粒/mL的rAAV颗粒。在一些实施方案中,施用于对象的rAAV颗粒的剂量可以在以下数量级上:106至1014个载体基因组(vg)/mL或103至1015vg/mL,或者其任一范围之间的任何值,例如,约106、107、108、109、1010、1011、1012、1013或1014vg/mL。在一个实施方案中,施用高于1013vg/mL的rAAV颗粒。rAAV颗粒可作为单剂量施用,或者可根据需要分成两次或更多次施用,以实现对所治疗特定疾病或病症的治疗。在一些实施方案中,以一定剂量向对象递送0.0001mL至10mL(例如,0.0001mL、0.001mL、0.01mL、0.1mL、1mL、10mL)。
在一些实施方案中,rAAV病毒滴度为1×1010vg/ml至5×1013vg/ml。在一些实施方案中,rAAV病毒滴度可以是1×1010、2.5×1010、5×1010、1×1011、2.5×1011、5×1011、1×1012、2.5×1012、5×1012、1×1013、2.5×1013或5×1013vg/mL。在一些实施方案中,病毒滴度小于1×1010vg/mL。在一些实施方案中,rAAV病毒滴度大于1×1015vg/ml。在一个实施方案中,rAAV颗粒大于5×1013vg/ml。在一些实施方案中,rAAV病毒滴度通过本文中进一步描述的方法(例如,视网膜下或玻璃体内)施用。
rAAV颗粒可作为单剂量施用,或者可根据需要分成两次或更多次施用,以实现对所治疗特定疾病或病症的治疗。在一些实施方案中,向对象的一只或两只眼施用1至500微升本申请中描述的组合物。例如,在一些实施方案中,可向每只眼施用约1、约10、约50、约100、约200、约300、约400或约500微升。然而,应当理解,在一些实施方案中可施用更小或更大的体积。
在一些实施方案中,本公开内容提供了在可药用溶液中的本文中公开的一种或更多种基于rAAV的组合物的制剂,其用于单独或与一种或更多种其他治疗方式组合施用于细胞或动物并且特别地用于治疗影响人的人细胞、组织和疾病。
如果期望的话,rAAV颗粒或核酸载体也可与其他药剂(例如蛋白质或多肽或多种药物活性剂)组合施用,包括治疗性多肽、生物活性片段、或其变体的一次或更多次全身或局部施用。事实上,对也可包含在内的其他组分几乎没有限制,只要另外的药剂在与靶细胞或宿主组织接触之后不引起显著的不利影响即可。因此,rAAV颗粒可根据特定情况的需要与多种其他药剂一起递送。这样的组合物可从宿主细胞或其他生物来源中纯化,或者作为替代地可如本文中所述化学合成。
可药用赋形剂和载体溶液的配制对于本领域技术人员来说是公知的,用于在多种治疗方案中使用本文中所描述的特定组合物的合适给药和治疗方案的开发也如此,所述治疗方案包括例如经口、肠胃外、静脉内、鼻内、关节内和肌内施用和配制。
通常来说,这些制剂可包含至少约0.1%或更多的治疗剂(例如,rAAV颗粒或宿主细胞),但是活性成分的百分比当然可变化并且可方便地介于总制剂的重量或体积的约1%或2%和约70%或80%或更多之间。当然,每种治疗上可用的组合物中治疗剂(例如,rAAV颗粒)的量可以以这样的方式制备使得在任何给定单位剂量的化合物中获得合适的剂量。制备这样的药物制剂领域的技术人员将考虑例如溶解度、生物利用度、生物半衰期、施用途径、产品保质期以及其他药理学考虑因素的因素,并且这样,多种剂量和治疗方案可以是期望的。
在某些情况下,将期望如下递送在本文中公开的适当配制药物组合物中的rAAV颗粒或宿主细胞:皮下、眼内、玻璃体内、肠胃外、皮下、静脉内、脑室内、肌内、鞘内、经口、腹膜内、通过经口或经鼻吸入、或通过经由直接注射来直接注射至一种或更多种细胞、组织或器官。
适于可注射使用的rAAV颗粒或宿主细胞组合物的药物形式包括无菌水溶液或分散体。在一些实施方案中,所述形式是无菌的并且在存在易注射性的程度上是流体。在一些实施方案中,所述形式在制备和储存条件下是稳定的,并且被保护以免于微生物(例如细菌和真菌)的污染作用。载体可以是包含以下的溶剂或分散介质:例如水、盐水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇,等)、其合适混合物、和/或植物油。可维持适当的流动性,例如通过使用包衣(例如卵磷脂)、在分散体的情况下通过维持所需的颗粒尺寸和通过使用表面活性剂来维持。
术语“载体”是指与rAAV颗粒或宿主细胞一起施用的稀释剂、辅料、赋形剂或载剂。这样的药用载体可以是无菌液体,例如水和油,包括以下那些:石油,例如矿物油;植物油,例如花生油、豆油和芝麻油;动物油;或合成来源的油。盐水溶液以及葡萄糖水溶液和甘油溶液也可用作液体载体。
本公开内容的组合物可通过标准途径施用于所治疗对象,所述标准途径包括但不限于经肺、鼻内、经口、吸入、肠胃外(例如静脉内)、局部、经皮、皮内、经黏膜、腹膜内、肌内、囊内、眶内(intraorbital)、玻璃体内、心内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊柱内、硬膜外和胸骨内注射。
本公开内容的组合物可通过多种途径递送至眼。其可眼内递送,通过局部施用于眼来递送或者通过眼内注射到例如玻璃体(玻璃体内注射)或视网膜下(视网膜下注射)光感受器间空间(inter-photoreceptor space)来递送。在一些实施方案中,将其递送至视杆感光细胞(rod photoreceptor cell)。或者,其可通过插入或注射到眼周围的组织中而局部递送。其可通过经口途径或通过皮下、静脉内或肌内注射而全身递送。或者,其可通过导管或通过植入物递送,其中这样的植入物由多孔、无孔或凝胶材料(包括膜例如硅橡胶膜或纤维、生物可降解聚合物或蛋白质材料)制成。其可在病症发作之前施用以防止其发生,例如在对眼进行手术期间施用;或者在病理状况发作之后立即施用或者在急性或拖延性病症发生期间施用。
对于可注射水溶液的施用,例如,如果需要的话,溶液可适当地缓冲,并且液体稀释剂首先用足够的盐水或葡萄糖使其等张。这些特定的水溶液尤其适于静脉内、肌内、玻璃体内、皮下和腹膜内施用。就此而言,可使用的无菌水性介质将是本领域技术人员根据本公开内容已知的。例如,可将一个剂量溶解在1ml等张NaCl溶液中,并且将其添加至1000ml的皮下灌注流体中或者注射在建议的输注部位(参见例如,“Remington′s PharmaceuticalSciences”第15版,第1035-1038和1570-1580页)。根据被治疗对象的病症,必然将发生一定的剂量变化。无论如何,负责施用的人员将确定个体对象的合适剂量。此外,对于人施用,制剂应符合例如FDA生物制品标准办公室(FDA Office of Biologics standards)所要求的无菌性、致热原性以及一般安全性和纯度标准。
无菌可注射溶液如下制备:将所需量的rAAV颗粒或宿主细胞与上文中列举的数种其他成分(如有需要的话)一起并入合适的溶剂中,然后无菌过滤。通常来说,分散体通过将多种经灭菌活性成分并入到包含基础分散介质和来自上文中列举的那些的所需其他成分的无菌载剂中来制备。在用于制备无菌可注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥技术,这由其经预先无菌过滤的溶液产生活性成分加任何另外期望成分的粉末。
rAAV颗粒、核酸载体或宿主细胞组合物的量和这样的组合物的施用时间将在受益于本教导的技术人员的范围内。然而,可能的是,治疗有效量的所公开组合物的施用可通过单次施用(例如单次注射足够数量的感染性颗粒)来实现以向进行这样的治疗的患者提供治疗益处。或者,在一些情况下,可期望在相对短或相对延长的时间段内提供rAAV颗粒或宿主细胞组合物的多次或连续施用,如可由监督此类组合物之施用的医疗从业人员确定。
在一些实施方案中,视杆细胞(rod cell)在使细胞视紫红质基因表达沉默之后保持结构完整和/或存活。在一些实施方案中,其中细胞视紫红质基因表达被沉默的视杆细胞具有在正常情况下包含视紫红质的缩短外段。在一些实施方案中,外段的长度可使用外源添加的(硬化)视紫红质基因来维持或恢复(例如,部分地或完全地),所述视紫红质基因的表达对使用本申请中描述的组合物的沉默具有抗性。
所述组合物可单独或者与一种或更多种另外的活性成分组合包含rAAV颗粒或宿主细胞,所述活性成分可从天然或重组来源获得或者化学合成。在一些实施方案中,rAAV颗粒与蛋白酶体抑制剂(例如硼替佐米)或羟基脲在同一组合物中或作为同一治疗方案的一部分施用而组合施用。
“治疗”疾病如该术语在本文中使用的意指降低对象经历的疾病或病症的至少一种体征或症状的频率或严重程度。上述组合物通常以有效量(即能够产生期望结果的量)施用于对象。所述期望结果将取决于所施用的活性剂。例如,rAAV颗粒的有效量可以是能够将异源核酸转移至宿主器官、组织或细胞的颗粒的量。
用于本公开内容方法的组合物的毒性和效力可通过使用培养物或实验动物中的细胞通过标准药学操作确定LD50(对群体中50%致死的剂量)来确定。毒性和效力之间的剂量比是治疗指数并且其可表示为LD50/ED50比。显示出大治疗指数的那些组合物是优选的。虽然可使用表现出毒性副作用的那些,但应注意设计使这些副作用的潜在损害最小化的递送系统。如本文中所述的组合物的剂量通常在包括ED50且具有很小毒性或无毒性的范围内。剂量可在该范围内变化,这取决于所采用的剂量形式和所使用的施用途径。
本公开内容的一些方面涉及用于将包含目的基因的一种或更多种核酸载体递送到多种组织、器官和/或细胞中的重组腺相关病毒(rAAV)颗粒。在一些实施方案中,rAAV颗粒包含如本文中所述的rAAV衣壳蛋白,其例如包含一个或更多个氨基酸替换。在一些实施方案中,目的基因编码目的多肽或目的蛋白质(例如治疗性多肽或蛋白质)。在一些实施方案中,目的基因编码目的RNA(例如,治疗性mRNA、siRNA、shRNA、微RNA、反义RNA、tRNA、rRNA或核酶)。在一些实施方案中,目的基因是替代基因(例如,眼特异性基因、功能性基因、功能性RHO基因)。在一些实施方案中,目的基因包含或编码目的RNA(例如,微RNA、siRNA、shRNA)和目的替代基因(例如,眼特异性基因、功能性基因、功能性RHO基因)。在一些实施方案中,功能性RHO基因包含含有沉默核苷酸替换的RHO基因,所述沉默核苷酸替换使其不能够被目的RNA(例如,微RNA、siRNA、shRNA)降解。在一些实施方案中,目的RNA和目的替代基因在同一启动子的控制之下。在一些实施方案中,目的RNA和目的替代基因在单独启动子的控制之下。可使用任何合适的启动子,例如但不限于病毒启动子(例如,CMV或其他病毒启动子)、微生物(例如酵母或细菌)启动子或真核生物(例如,哺乳动物)启动子。
重组AAV(rAAV)颗粒可至少包含:(a)一个或更多个异源核酸区,其包含编码目的基因(例如,目的RNA和/或目的替代基因)的序列;以及(b)一个或更多个包含末端反向重复(ITR)序列(例如,野生型ITR序列或经改造ITR序列)的区域,其在一个或更多个异源核酸区侧翼。在一些实施方案中,核酸载体的尺寸为4kb至5kb(例如,尺寸为4.2kb至4.7kb)。该核酸载体可被病毒衣壳(例如AAV1、AAV2、AAV3、AAV4或AAV5衣壳)衣壳化,所述衣壳可包含如本文中所述的经修饰衣壳蛋白。在一些实施方案中,核酸载体是环状的。在一些实施方案中,核酸载体是单链的。在一些实施方案中,核酸载体是双链的。在一些实施方案中,双链核酸载体可以是例如自身互补载体,其包含与核酸载体另一区域互补开始形成核酸载体的双链的核酸载体区域。
rAAV颗粒可以是任何AAV血清型的,包括任何衍生物或假型(pseudotype)(例如,1、2、3、4、5、6、7、8、9、10、2/1、2/5、2/8、或2/9)。如本文中所用,rAAV病毒载体(例如,rAAV颗粒)的血清型是指重组病毒的衣壳蛋白的血清型。在一些实施方案中,rAAV颗粒不是AAV2。在一些实施方案中,rAAV颗粒是AAV2。在一些实施方案中,rAAV颗粒是AAV6。在一些实施方案中,rAAV颗粒是包含如本文中所述的rAAV衣壳蛋白的AAV6血清型。衍生物和假型的一些非限制性实例包括rAAV2/1、rAAV2/5、rAAV2/8、rAAV2/9、AAV2-AAV3杂合体、AAVrh.10、AAVhu.14、AAV3a/3b、AAVrh32.33、AAV-HSC15、AAV-HSC17、AAVhu.37、AAVrh.8、CHt-P6、AAV2.5、AAV6.2、AAV2i8、AAV-HSC15/17、AAVM41、AAV9.45、AAV6(Y445F/Y731F)、AAV2.5T、AAV-HAE1/2、AAV克隆32/83、AAVShH10、AAV2(Y->F)、AAV8(Y733F)、AAV2.15、AAV2.4、AAVM41和AAVr3.45。这样的AAV血清型和衍生物/假型以及产生这样的衍生物/假型的方法是本领域中已知的(参见例如,Mol Ther.2012年4月;20(4):699-708.doi:10.1038/mt.2011.287.电子出版于2012年01月24日.The AAV vector toolkit:poised at theclinical crossroads.Asokan A1,Schaffer DV,Samulski RJ.)。在一些实施方案中,rAAV颗粒是假型化rAAV颗粒,其包含:(a)包含来自一种血清型(例如,AAV2)的ITR的核酸载体和(b)包含来源于另一种血清型(例如,AAV1、AAV3、AAV4、AAV5、AAV6、AAV7、AAV8、AAV9或AAV10)的衣壳蛋白的衣壳。用于产生和使用假型化rAAV载体的方法是本领域中已知的(参见例如,Duan等,J.Virol.,75:7662-7671,2001;Halbert等,J.Virol.,74:1524-1532,2000;Zolotukhin等,Methods,28:158-167,2002;和Auricchio等,Hum.Molec.Genet.,10:3075-3081,2001)。
产生rAAV颗粒和核酸载体的方法也是本领域中已知的并且可商购获得(参见例如,Zolotukhin等.Production and purification of serotype 1,2,and 5recombinantadeno-associated vital vectors.Methods 28(2002)158-167;以及美国专利公布号US20070015238和US20120322861,其通过引用并入本文;以及可从ATCC和Cell Biolabs,Inc.获得的质粒和试剂盒)。例如,包含核酸载体的质粒可与例如包含rep基因(例如,其编码Rep78、Rep68、Rep52和Rep40)和cap基因(例如,其编码VP1、VP2和VP3,包括如本文中所述的经修饰VP3区)的一种或更多种辅助质粒组合,并且转染到生产细胞系中,使得rAAV颗粒可被包装并随后纯化。
在一些实施方案中,一种或更多种辅助质粒包括包含rep基因和cap基因(例如,其编码如本文中所述的rAAV衣壳蛋白)的第一辅助质粒,以及包含E1a基因、E1b基因、E4基因、E2a基因和VA基因的第二辅助质粒。在一些实施方案中,rep基因是来源于AAV2或AAV6的rep基因,并且cap基因来源于AAV2或AAV6且可包括对该基因的修饰以产生本文中所述的经修饰衣壳蛋白。辅助质粒和制备这样的质粒的方法是本领域中已知的并且可商购获得(参见例如来自PlasmidFactory,Bielefeld,Germany的pDM、pDG、pDP1rs、pDP2rs、pDP3rs、pDP4rs、pDP5rs、pDP6rs、pDG(R484E/R585E)和pDP8.ape质粒;可从以下获得的其他产品和服务:Vector Biolabs,Philadelphia,PA;Cellbiolabs,San Diego,CA;AgilentTechnologies,Santa Clara,Ca;和Addgene,Cambridge,MA;pxx6;Grimm等.(1998),NovelTools for Production and Purification of Recombinant Adenoassociated VirusVectors,Human Gene Therapy,第9卷,2745-2760;Kern,A.等.(2003),Identification ofa Heparin-Binding Motif on Adeno-Associated Virus Type 2Capsids,Journal ofVirology,第77卷,11072-11081;Grimm等(2003),Helper Virus-Free,OpticallyControllable,and Two-Plasmid-Based Production of Adeno-associated VirusVectors of Serotypes 1to 6,Molecular Therapy,第7卷,839-850;Kronenberg等.(2005),A Conformational Change in the Adeno-Associated Virus Type 2CapsidLeads to the Exposure of Hidden VP1 N Termini,Journal of Virology,第79卷,5296-5303;以及Moullier,P.和Snyder,R.O.(2008),International efforts forrecombinant adeno-associated viral vector reference standards,MolecularTherapy,第16卷,1185-1188)。
接下来描述一种示例性的非限制性rAAV颗粒产生方法。产生或获得一种或更多种辅助质粒,其包含所期望AAV血清型的rep和cap ORF以及在其天然启动子的转录控制之下的腺病毒VA、E2A(DBP)和E4基因。cap ORF还可包含一个或更多个修饰以产生如本文中所述的经修饰衣壳蛋白。通过CaPO4介导的转染、脂质或聚合物分子(例如聚乙烯亚胺(PEI))用辅助质粒和包含本文中所述核酸载体的质粒转染HEK293细胞(可从获得)。然后,将HEK293细胞孵育至少60小时以允许rAAV颗粒产生。或者,在另一个实例中,用包含核酸载体的单重组杆状病毒感染基于Sf9的生产稳定细胞系。作为另一个替选方案,在另一个实例中,用包含核酸载体的HSV和任选地一种或更多种辅助HSV感染HEK293或BHK细胞系,所述辅助HSV包含如本文中所述的rep和cap ORF以及在其天然启动子的转录控制之下的腺病毒VA、E2A(DBP)和E4基因。然后,将HEK293、BHK或Sf9细胞孵育至少60小时以允许rAAV颗粒产生。然后,可使用本领域中已知或本文中描述的任何方法,例如通过碘克沙醇分步梯度、CsCl梯度、色谱或聚乙二醇(PEG)沉淀来纯化rAAV颗粒。
本公开内容还考虑包含至少一种所公开的rAAV颗粒或核酸载体的宿主细胞。这样的宿主细胞包括哺乳动物宿主细胞,其中优选人宿主细胞,并且可以是分离的、在细胞或组织培养物中的。在经遗传修饰的动物模型(例如,小鼠)的情况下,经转化的宿主细胞可包含在非人动物自身的体内。在一些实施方案中,宿主细胞是红系谱系的细胞,例如CD36+爆发型形成单位-红系(burst-forming units-erythroid,BFU-E)细胞或集落形成单位-红系(colony-forming unit-erythroid,CFUE-E)祖细胞。
在一些实施方案中,将本文中所述的组合物(例如,siRNA、shRNA和/或目的替代基因)配制在纳米粒中。在一些实施方案中,将本文中所述的组合物(例如,siRNA、shRNA和/或目的替代基因)配制在脂质纳米粒中。在一些实施方案中,将本文中所述的组合物(例如,siRNA、shRNA和/或目的替代基因)配制在称为阳离子脂质纳米粒的脂质-聚阳离子复合物中。脂质纳米粒的形成可通过本领域中已知和/或如美国公布No.20120178702(其通过引用整体并入本文)中所述的方法来实现。作为一个非限制性实例,聚阳离子可包括阳离子肽或多肽,例如但不限于聚赖氨酸、聚鸟氨酸和/或聚精氨酸,以及国际公布No.WO2012013326或美国专利公布No.US20130142818中描述的阳离子肽;其各自通过引用整体并入本文。在一些实施方案中,将本文中所述的组合物(例如,siRNA、shRNA和/或目的替代基因)配制在包含非阳离子脂质的脂质纳米粒中,所述非阳离子脂质例如但不限于胆固醇或二油酰磷脂酰乙醇胺(DOPE)。
实施例
实施例1:敲减RHO的短干扰RNA(siRNA)的鉴定
使用由Khvorova及同事描述的短干扰RNA(siRNA)设计原理4,5,设计了14种siRNA用于特异性地切割狗siRNA,其中12种也靶向人视紫红质mRNA。在进行之前,使用NCBIBlast实用程序(blast.ncbi.nlm.nih.gov/Blast.cgi)针对NCBI人RefSeq数据库筛选siRNA的第2至19位。排除了两种潜在的siRNA,因为其与可能在视网膜中表达的其他基因紧密匹配。10种siRNA的RNA形式与用作对照的非靶向siRNA一起从GE Healthcare Dharmacon订购。这些在表达与绿色荧光蛋白(GFP,图11中描绘的示例性质粒图谱)融合的人RHO的细胞中测试,并且通过荧光激活细胞分选(FACS)测量绿色荧光细胞的减少。基本原理是对RHOmRNA的切割将降低GFP的产生。虽然所有siRNA都是基于siRNA的当前设计原理设计的,但是测试的10种中只有3种导致降低30%或更多(图1A-C)。
为了确定这些siRNA作为从RNA聚合酶III启动子表达并且通过AAV递送的小发夹RNA会是有效的,克隆了表达三种siRNA的用于shRNA的DNA序列(图2)。令人感兴趣的是,使用siRNA的相对RHO敲减并不准确地预测使用shRNA的相对RHO抑制,因为siRNA 131(SEQ IDNO:1)是最有效的siRNA,但是测试的shRNA的效率最低。简单转染作为RNA的siRNA可无法准确地预测设计成通过转录和加工产生相同siRNA的shRNA的有效性。
为了确定shRNA在切割野生型(正常)和突变RHO方面均是有效的,使用定量逆转录PCR(qRT-PCR)作为测定测试在AAV载体中克隆的相同三种shRNA消化野生型和两种不同突变RHO mRNA的能力(图3)。
表5列出了对应于鉴定为能够切割RHO的shRNA序列的RNA序列(包括有义链、环、反义链和突出端)。每条序列示出具有粗体且加有下划线以强调的两种替选环序列,其中突出端为斜体且加有下划线以强调。
表5:小发夹RNA(shRNA)
siRNA也可作为类似于图4中结构的结构的人工微RNA7递送。图4的示例性微RNA包含RHO131的有义链(100)和反义链(101)(分别为SEQ ID NO:1和2)。这种表达模式的优点是可通过使用特定的启动子序列使siRNA的产生成为细胞类型特异性的。在这种情况下,人视紫红质基因的近端启动子或人视紫红质激酶启动子将用于限制感光细胞的表达。
实施例2:RHO+/+狗中RHO KD的分析
狗2190(rcd1携带者)以表6中列出的浓度接受AAV2/5-sc-H1-shRNA-Rho131的视网膜下注射。在注射之后8周将狗终止。从每只眼的泡和非泡区域二者收集数个3mm神经视网膜活检钻取物。
表6:狗2190
本文中描述的AAV2/5-sc-H1-shRNA构建体的一些非限制性实例还可称为AAV2/5-sc-MOP500rGFP-shRNA构建体。AAV2/5表示编码shRNA的核酸以AAV2 ITR为侧翼,并且在包含AAV5衣壳蛋白的rAAV颗粒中提供。在一些实施方案中,本文中所述的任何干扰RNA和本文中所述的任何重组RHO基因可在rAAV颗粒(例如,包含AAV5衣壳蛋白)中的同一AAV核酸(例如,以AAV2 ITR为侧翼)上提供。在一些实施方案中,本文中所述的任何干扰RNA和本文中所述的任何重组RHO基因可在衣壳化在不同rAAV颗粒(例如,各自包含AAV5衣壳蛋白,或者各自具有来自不同AAV血清型的衣壳蛋白)中的不同AAV核酸(例如,各自以AAV2ITR为侧翼,或者各自以来自不同AAV血清型的ITR为侧翼)上提供。
Western印迹分析:
将来自每只眼的两种活检钻取物(代表泡或非泡区域)在50μl Lewin缓冲溶液A(含有蛋白酶抑制剂)中在冰上孵育15分钟。以40%振幅、15secON/10secOFF X8脉冲对样品进行声处理。然后,将样品离心并弃去沉淀。通过Bradford法测量上清液中的蛋白质浓度。对1μg总蛋白质进行免疫印迹以使视紫红质可视化(使用的抗体:Millipore MAB5356,在封闭缓冲液中1∶1000稀释),使用抗组蛋白抗体(Abcam ab1791,1∶3000稀释)作为上样对照(图5A)并且使信号归一化(图5B)。泡与非泡区域之间的RHO蛋白量之间的比较与实验设计不一致(图5C)。
犬视网膜中犬视紫红质RNA的绝对定量:
为了确定核酶处理之后视网膜中存在的视紫红质RNA的绝对量,使用Q-PCR标准曲线法进行绝对定量。使用已知量的犬RHO cDNA的稀释系列构建标准曲线。基于该标准曲线计算每个样品中犬RHO RNA的总量(图6A)。
用AAV2/5-sc-H1-shRNA-Rho131观察到犬RHO的部分敲减。在使用的最高浓度下,蛋白质水平降低37%,而RNA降低接近50%(图6B)。
实施例3:RHO+/+狗中RHO KD的进一步分析
狗2194(rcd1携带者)以表7中列出的浓度接受AAV2/5-sc-H1-shRNA-Rho820的视网膜下注射。在注射之后8周将狗终止。从每只眼的泡和非泡区域二者收集数个3mm神经视网膜活检钻取物。
表7:狗2194
Western印迹分析:
将来自每只眼的两种活检钻取物(代表泡或非泡区域)在50μl Lewin缓冲溶液A(含有蛋白酶抑制剂)中在冰上孵育15分钟。以40%振幅、15secON/10secOFF X8脉冲对样品进行声处理。然后,将样品离心并弃去沉淀。通过Bradford法测量上清液中的蛋白质浓度。对1μg总蛋白质进行免疫印迹以使视紫红质可视化(使用的抗体:Millipore MAB5356,在封闭缓冲液中1∶1000稀释)。使用抗组蛋白抗体(Abcam ab1791,1∶3000稀释)作为上样对照(图7A)并且使信号归一化(图7B)。泡与非泡区域之间的RHO蛋白量之间的比较与实验设计不一致(图7C)。
犬视网膜中犬视紫红质RNA的绝对定量:
为了确定核酶处理之后视网膜中存在的视紫红质RNA的绝对量,使用Q-PCR标准曲线法进行绝对定量。使用已知量的犬RHO cDNA的稀释系列构建标准曲线。基于该标准曲线计算每个样品中犬RHO RNA的总量(图8A)。
用AAV2/5-sc-H1-shRNA-Rho820观察到犬RHO RNA和蛋白质的完全敲减,即使在1×1012vg/ml的较低剂量下也是如此(图8B)。
实施例4:替代基因的硬化mRNA序列
在一些实施方案中,替代基因(例如,替代RHO)的mRNA可在一个或更多个位置被修饰成使其“硬化”(即,使其对通过siRNA的降解具有抗性)。在一些实施方案中,相对于提供用于敲减内源性基因(例如,RHO基因)的siRNA,可在替代基因中包含一个或更多个沉默核苷酸替换。图9和10提供了可引入到替代RHO mRNA中的核苷酸替换的一些非限制性实例。应当理解,替代RHO基因可包含这些替换中的一个或更多个。
图9描绘了在每种shRNA与内源性人或硬化RHO mRNA的靶序列之间发生的碱基配对的代表。所有shRNA均与狗的RHO mRNA的靶序列完美地碱基配对。白框:shRNA与内源性狗以及硬化RHO mRNA之间的错配。深灰色框:在RNA中鸟苷与尿嘧啶之间发生的弱摆动碱基配对。浅灰色框:仅shRNA与硬化RHO mRNA之间的错配。
图10描绘了在shRNA134与内源性人或硬化RHO131 mRNA的靶序列之间发生的碱基配对的代表。shRNA 131和134的靶序列接近度使得能够使用相同的硬化RHO131。深灰色框:在RNA中鸟苷与尿嘧啶之间发生的弱摆动碱基配对。浅灰色框:仅shRNA与硬化RHO mRNA之间的错配。
实施例5:编码siRNA和替代基因
在一些实施方案中,可期望提供在DNA载体中编码的siRNA。图12A-B描绘了在DNA载体中编码的siRNA(例如,shRNA)的一些非限制性实例。在一些实施方案中,如图12A-B中所示的示例性质粒图谱中进一步描绘的,DNA载体还可编码在siRNA(例如,shRNA)侧翼的末端反向重复(ITR)序列。在一些实施方案中,编码以ITR序列为侧翼的siRNA的DNA载体可用于产生包含siRNA的重组AAV颗粒。
在一些实施方案中,可期望提供在DNA载体中编码的替代RHO mRNA。图12C描绘了在DNA载体中编码的替代RHO mRNA(例如,人RHO)的一个非限制性实例。在一些实施方案中,如图12C所示的示例性质粒图谱中进一步描绘的,DNA载体还可编码在替代RHO mRNA(例如,人RHO)侧翼的ITR序列。在一些实施方案中,编码以ITR序列为侧翼的替代RHO mRNA的DNA载体可用于产生包含人rho的重组AAV颗粒。在一些实施方案中,可提供类似的DNA载体,其包含以ITR序列为侧翼的替代rho基因和编码一种或更多种干扰RNA的一个或更多个序列二者。在一些实施方案中,干扰RNA和/或替代rho基因与启动子(例如,RNA聚合酶III启动子、或H1RNA聚合酶III启动子、或如本申请中所述的其他启动子)有效偶联。图12A-C中所示的干扰RNA和/或替代rho基因在H1RNA聚合酶III启动子的控制之下。图12A-C的构建体还包含MOP500-rGFP(在GFP的反向序列(rGFP)(因此不表达)上游的小鼠视杆视蛋白启动子(MOP500)的-385/+86部分)并且可称为H1构建体或MOP500构建体。然而,不需要MOP500(例如,MOP500-rGFP)部分。因此,质粒或rAAV核酸可编码如本文中所述的干扰RNA和/或经修饰rho基因,其各自在没有小鼠视蛋白启动子和/或没有任何GFP编码序列(在任一方向上)下在相同或不同启动子(例如,H1启动子)的控制之下。
实施例6:对在WT RHO+/+狗中用shRNA820进行RHO KD的分析
实施例6包括:鉴定在WT狗中视网膜下注射之后使视紫红质表达高效地沉默的携带shRNA820敲减试剂的AAV2/5的病毒滴度,通过WT狗中体内视网膜成像证明在视网膜下注射AAV2/5-sc-H1-shRNA820之后包含光感受器的层(ONL)保持但包含视紫红质的层减小,鉴定在突变体RHOT4R/+狗(RHO-ADRP的天然模型)中视网膜下注射之后使视紫红质表达高效地沉默的携带shRNA820敲减试剂的AAV2/5的病毒滴度,鉴定在突变体RHOT4R/+狗中赋予光感受器以针对光诱导的视网膜变性的保护的AAV2/5-sc-H1-shRNA820的病毒滴度,证明视紫红质表达的高效敲减导致视杆中的外段的损失。由于外段的保留对于光转导(视杆将光转换成电信号的机制)是关键的,因此对RHO-ADRP的最佳治疗应降低天然RHO但保留外段结构。这些结果表明,敲减方法是不够的,并且主张使用组合的敲减和替代策略。
五只WT RHO+/+狗以如下表8中所示的病毒浓度(1×1011至5×1012vg/ml)在两只眼中均接受AAV2/5-sc-H1-shRNA-Rho820的视网膜下注射。
表8:在WT RHO+/+狗中用shRNA820进行的RHO KD
在注射之后6-8周,进行体内视网膜成像(cSLO/OCT),并随后终止狗。从两只眼(狗2194)或仅从OS眼(其他狗)的泡/经处理和非泡/未经处理区域二者中收集数个3mm神经视网膜活检钻取物,以通过western印迹测量犬视紫红质的表达水平并且通过qPCR分析测量RHO RNA。将OD眼固定,包埋在最佳切割温度介质中并进行处理用于组织学和免疫组织化学染色。
Western印迹分析:
将代表泡或非泡区域的多达三对活检钻取物在50ul Lewin缓冲溶液A(含有蛋白酶抑制剂)中在冰上孵育15分钟。以40%振幅、15secON/10secOFF X8脉冲对样品进行声处理。然后,将样品离心并弃去沉淀。通过Bradford法测量上清液中的蛋白质浓度。将样品储存在-20℃。将1ug总蛋白质加载到凝胶上以使视紫红质可视化(使用的抗体:MilliporeMAB5356,在Odyssey封闭缓冲液中1:1000稀释)。使用抗组蛋白H3抗体(Abcam ab1791,1∶3000稀释)作为上样对照并且使信号归一化。
犬视网膜中犬视紫红质RNA的绝对定量:
为了确定shRNA820处理之后视网膜中存在的视紫红质RNA的绝对量,使用Q-PCR标准曲线法进行绝对定量。使用已知量的犬RHO cDNA的稀释系列构建标准曲线。使用0.1纳克的总cDNA进行定量。基于该标准曲线计算每个样品中犬RHO RNA的总量。
通过体内视网膜成像对注射有不同病毒滴度的AAV2/5-sc-H1-shRNA820的WT RHO+/+狗的眼中视网膜完整性的评价。
使用通过cSLO/OCT的体内视网膜成像评估视网膜下注射不同滴度的AAV2/5-sc-H1-shRNA820之后6至8周ONL的视网膜完整性。ONL厚度的地形图显示该层在所有滴度下都得到保持。外界膜(external limiting membrane,ELM)、内段(inner segment,IS)和外段(outer segment,OS)的分割揭示对应于注射1×1012vg/ml和5×1012vg/ml滴度的眼中泡区域的区域中的信号强度降低。这些结果表明作为RHO沉默的结果光感受器OS和IS缩短,并且可用于评估RHO KD在体内的效力。图13A-13E示出了在WT RHO+/+狗中视网膜下注射不同病毒滴度的AAV2/5-sc-H1-shRNA820下视紫红质敲减的RNA和蛋白质分析。图13A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈表示用于每个western印迹重复的泡/经处理和非泡/未经处理区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图13B示出了条形图,其显示作为在同一视网膜的未经处理区域中测量的水平的百分比的经处理区域中剩余的犬视紫红质RNA。图13C示出了免疫印迹,其显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中视紫红质的量。组蛋白H3用于归一化。条形图示出了作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质蛋白。图13D-13E示出了显示来自每个实验的数值的表(报道为剩余RNA或蛋白质的百分比,以及作为替代地分别报道为RNA或蛋白质的敲减百分比)。
图14A-14D示出了在WT狗中视网膜下注射不同滴度的AAV2/5-sc-H1-shRNA820之后ONL和ELM/IS/OS完整性的评估。图14A示出了ONL厚度图;图14B示出了经归一化强度的ELM/IS/OS图;图14C示出了ONL厚度值;并且图14D示出了ELM/IS/OS层的经归一化强度的值。这些结果表明作为RHO沉默的结果光感受器OS和IS缩短,并且可用于评估RHO KD在体内的效力。
在以低至1×1012vg/ml的病毒滴度视网膜下注射AAV2/5-sc-H1-shRNA820的WT狗中观察到犬RHO RNA和蛋白质的完全敲减。即使在最高的病毒浓度下也未观察到ONL厚度的减小,这表明视紫红质的敲减不诱导感光细胞死亡。在以诱导100%视紫红质KD的高病毒滴度注射的眼的经处理/泡区域中观察到ELM/IS/OS层的OCT反射率降低。该观察结果与这些层的变薄相容,并且可用作KD效率的体内结果量度。
实施例7:对在RHOT4R/+突变体狗中用shRNA820进行RHO KD的分析
四只RHOT4R/+狗以如下表9中所示的病毒浓度在两只眼中均接受AAV2/5-sc-H1-shRNA-Rho820的视网膜下注射。
表9:在RHOT4R/+突变体狗中用shRNA820进行的RHO KD
在注射之后8周进行cSLO/OCT,并且对所有狗的OS眼进行光暴露(在1mW/cm2下1分钟)以触发光诱导的视网膜变性。在光暴露之后2周对所有狗再次进行cSLO/OCT,以评估处理所赋予的任何挽救效果。终止狗并且从OD眼的泡/经处理和非泡/未经处理区域收集数个3mm神经视网膜活检钻取物,以通过western印迹测量犬视紫红质的表达水平并且通过qPCR分析测量RHO RNA。将OS眼固定,包埋在最佳切割温度介质中并进行处理用于组织学和免疫组织化学染色。
Western印迹分析:
将来自每只OS眼的三对活检钻取物(代表泡/经处理或非泡/未经处理视网膜区域)在50ul Lewin缓冲溶液A(含有蛋白酶抑制剂)中在冰上孵育15分钟。以40%振幅、15secON/10secOFF X8脉冲对样品进行声处理。然后,将样品离心并弃去沉淀。通过Bradford法测量上清液中的蛋白质浓度。将样品储存在-20℃。将1ug总蛋白质加载到凝胶上以使视紫红质可视化(使用的抗体:Millipore MAB5356,在Odyssey封闭缓冲液中1∶1000稀释)。使用抗组蛋白H3抗体(Abcam ab1791,1∶3000稀释)作为上样对照并且使信号归一化。
犬视网膜中犬视紫红质RNA的绝对定量:
为了确定shRNA820处理之后视网膜中存在的视紫红质RNA的绝对量,使用Q-PCR标准曲线法进行绝对定量。使用已知量的犬RHO cDNA的稀释系列构建标准曲线。使用0.1纳克的总cDNA进行定量。基于该标准曲线计算每个样品中犬RHO RNA的总量。
通过体内视网膜成像对注射有不同病毒滴度的AAV2/5-shRNA820的突变体RHOT4R/+狗的眼中从光诱导损伤的光感受器挽救的评价。
在注射之后8周(光暴露之前)通过cSLO/OCT成像检查来自以1×1012vg/ml降至1×1011vg/ml的病毒滴度视网膜下注射的突变体RHOT4R/+狗的眼。泡/经处理区域中的ONL厚度被保持,表明shRNA820在此期间没有引起光感受器的任何损失。使用对先前显示在RHO T4R突变体中引起急性视网膜变性但在WT狗中则不引起的强度(角膜辐照度为1mW/cm2)的白光暴露1分钟来评估由AAV2/5-sc-H1-shRNA820在经处理/泡区域中赋予的保护水平。对于每只眼,周围的非泡/未经处理区域用作内部对照。在光暴露之后两周,对视网膜重新成像,并且在注射有1×1012vg/ml和5×1011vg/ml滴度的眼的泡/经处理区域中显示出良好的ONL厚度保持。在2.5×1011vg/ml滴度下观察到非常轻微的挽救,且在1×1011vg/ml滴度下则没有观察到。
图15A-15E示出了在突变体RHOT4R/+狗中视网膜下注射不同病毒滴度的AAV2/5-sc-H1-shRNA820下视紫红质敲减的RNA和蛋白质分析。图15A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈表示用于每个western印迹重复的泡区域和非泡区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图15B是显示作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质RNA的量的条形图。图15C是显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中犬视紫红质的量的免疫印迹。组蛋白H3用于归一化。条形图示出了作为在同一视网膜的未经处理区域中测量的水平的百分比的剩余犬视紫红质蛋白的量。图15D-15E是显示来自每个实验的数值的表(报道为剩余RNA或蛋白质的百分比,以及作为替代地分别报道为RNA或蛋白质的敲减百分比)。
图16A-16D示出了OCT B扫描,其涵盖在暴露于引起突变体RHOT4R/+狗中急性视网膜变性的短暂光剂量之后2周RHOT4R/+狗的经处理(经不同病毒滴度的AAV2/5-sc-H1-shRNA820处理)和未经处理的视网膜区域。(图16A)经1×1012vg/ml处理的狗的OCT扫描。(图16B)经5×1011vg/ml处理的狗的OCT扫描。(图16C)经2.5×1011vg/ml处理的狗的OCT扫描。(图16D)经1×1011vg/ml处理的狗的OCT扫描。图17A-17B示出了来自经AAV2/5-sc-shRNA820处理的RHOT4R/+的ONL厚度地形图,其显示针对光诱导的视网膜变性的保护。(图17A)未经处理的WT对照狗的ONL厚度图(左图)和经5E+11vg/ml的AAV2/5-sc-shRNA820处理的EM411-OS的ONL厚度图,并且示出了在光诱导的损伤之后数周经处理/泡区域中保持的ONL厚度。黑色和白色曲线显示如在视网膜下注射之后立即看到的泡的界限。下面的图示出了具有颜色为较深灰色(中间带)的ONL的OCT B扫描用于可视化目的。(图17B)选择在泡外部和内部的位点用于ONL厚度测量。
在1×1012和5×1011vg/ml病毒滴度的AAV2/5-shRNA-Rho820下观察到犬RHO RNA和蛋白质(通过western印迹)的完全敲减。用1×1012和5×1011vg/ml病毒滴度的AAV2/5-shRNA-Rho820实现对包含光感受器的细胞体的外核层(outer nuclear layer,ONL)的完全挽救。
通过组织学和免疫组织化学对注射有不同病毒滴度的AAV2/5-sc-H1-shRNA820的突变体RHOT4R/+狗的眼中针对光诱导损伤的光感受器保护的评价。
检查来自上表中列出的同一突变体RHOT4R/+狗的眼,其以1×1012降至1×1011vg/ml的病毒滴度视网膜下注射并且随后光暴露(在注射之后8周时)于持续1分钟的一定强度(角膜辐照度为1mW/cm2)的白光。该光剂量先前显示在RHO T4R突变体中引起急性视网膜变性但在WT狗中则不引起。组织学和免疫组织化学用于评估由AAV2/5-sc-H1-shRNA820在经处理/泡区域中赋予的保护水平。对于每只眼,周围的非泡/未经处理区域用作内部对照。使用针对视紫红质(RHO)和人视锥拘留蛋白(human cone arrestin,hCA)的抗体评估视杆外段和视锥形态的完整性。图18示出了视网膜下注射有不同病毒滴度的AAV2/5-sc-H1-shRNA820的突变体RHOT4R/+视网膜的经处理(Tx)和未经处理(UnTx)区域的组织学(H&E染色)和免疫组织化学(视紫红质染色为绿色并且在图18的下图中显示为较浅染色;人视锥拘留蛋白染色为红色并且在图18的下图中显示为灰色染色)。在光暴露之后两周,观察到注射有1×1012vg/ml和5×1011vg/ml滴度的眼的泡/经处理区域中ONL厚度的良好保持,而在2.5×1011vg/ml下ONL厚度略微减小,并且在1×1011vg/ml滴度下未观察到保护。与在1×1012和5×1011vg/ml滴度下的视紫红质表达的非常高效敲减一致,与视紫红质表达降低组合地在H&E切片上观察到视杆OS长度的减小。
在1×1012和5×1011vg/ml病毒滴度的AAV2/5-sc-H1-shRNA820下观察到犬RHORNA和蛋白质(通过western印迹)的完全敲减。用1×1012和5×1011vg/ml病毒滴度的AAV2/5-sc-H1-shRNA820实现对包含光感受器的细胞体的外核层(outer nuclear layer,ONL)的完全保护。作为有效RHO敲减的结果的视杆中外段结构的损失主张需要组合的KD和替代策略以允许经处理的视杆保留外段并且保持功能性。
实施例8:
该实施例使用RHO-ADRP提供了支持基因治疗的数据。其包括在突变体RHOT4R/+狗中测试将shRNA820敲减试剂和替代试剂RHO820(=硬化人RHO mRNA)二者组合的AAV2/5载体构建体(AAV2/5-sc-HOP-RHO820-H1-shRNA820),鉴定导致内源性犬RHO高效敲减以及替代硬化人RHO(RHO820)高效表达的AAV2/5-sc-HOP-RHO820-H1-shRNA820的病毒滴度,证明AAV2/5-sc-HOP-RHO820-H1-shRNA820在突变体RHOT4R/+狗中赋予光感受器以针对光诱导的视网膜变性的保护,以及证明在经AAV2/5-sc-HOP-RHO820-H1-shRNA820处理的视网膜区域中实现视杆外段的保留。
对在RHOT4R/+突变体狗中用shRNA820和RHO820进行RHO KD&替代的分析:
两只RHOT4R/+狗以如下表中所示的病毒浓度在两只眼中均接受AAV2/5-sc-HOP-RHO820-H1-shRNA820的视网膜下注射(表10)。
表10
HOP:人视蛋白启动子;H1:H1RNA聚合酶III启动子
在注射之后11周时进行体内视网膜成像(cSLO/OCT),并且对两只狗的OS眼进行光暴露(在1mW/cm2下1分钟)以触发光诱导的视网膜变性。在光暴露之后2周对所有狗再次进行cSLO/OCT以评估处理所赋予的任何挽救效果。终止狗并且从OD眼的泡/经处理和非泡/未经处理区域二者收集数个3mm神经视网膜活检钻取物以通过western印迹测量视紫红质的表达水平并且通过qPCR分析测量犬和人RHO RNA。将OS眼固定,包埋在最佳切割温度介质中并进行处理用于组织学和免疫组织化学染色。
Western印迹分析:
将来自每只OD眼的三对活检钻取物(代表泡/经处理或非泡/未经处理视网膜区域)在50ul Lewin缓冲溶液A(含有蛋白酶抑制剂)中在冰上孵育15分钟。以40%振幅、15secON/10secOFF X8脉冲对样品进行声处理。然后,将样品离心并弃去沉淀。通过Bradford法测量上清液中的蛋白质浓度。将样品储存在-20℃。将1ug总蛋白质加载到凝胶上以使视紫红质可视化(使用的抗体:Millipore MAB5356,在Odyssey封闭缓冲液中1∶1000稀释)。注意,该抗体检测犬和人RHO二者。由于Asn2处糖基化的丧失,突变体T4R视紫红质由于其具有可在免疫印迹上检测到的较低MW而可与WT(犬或人)RHO蛋白区分开。因此,来自杂合突变体RHOT4R/+的RHO免疫印迹显示出对应于WT(高MW)和突变体T4R(低MW)RHO蛋白的两个条带。使用抗组蛋白H3抗体(Abcam ab1791,1∶3000稀释)作为上样对照并且使信号归一化。
犬视网膜中犬和人视紫红质RNA的绝对定量:
为了确定在用AAV2/5-sc-HOP-RHO820-H1-shRNA820处理之后视网膜中存在的内源性犬视紫红质RNA和人RHO820 RNA二者的绝对量,使用Q-PCR标准曲线法进行绝对定量。使用已知量的犬和人RHO cDNA的稀释系列构建标准曲线。使用0.1纳克的总cDNA进行定量。基于该标准曲线计算每个样品中犬RHO和人RHO820 RNA的总量。
图19A-19F示出了在突变体RHOT4R/+狗中视网膜下注射5×1011vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820下视紫红质敲减和替代的RNA和蛋白质分析。图19A示出了视网膜图谱,其显示用于western印迹分析和RNA定量的活检钻取物的位置。成对的深灰色、灰色和有点圆圈表示用于每个western印迹重复的经处理(Tx)和未经处理(UnTx)区域中活检钻取物的位置,而黑色圆圈表示用于RNA定量的活检钻取物的位置。图19B示出了免疫印迹,其显示取自犬视网膜的经处理(Tx)和未经处理(UnTx)区域的活检钻取物中总视紫红质(犬+人RHO820)的量。组蛋白H3用于归一化。条形图示出了经处理和未经处理区域中剩余视紫红质蛋白的百分比。注意EM424-OD和EM425-OD的经处理区域中较低MW条带(对应于突变体T4R RHO蛋白)的损失。图19C是显示用于蛋白质定量的每对钻取物的数值的表。图19D是显示作为在未经处理区域中测量的犬RHO RNA水平的百分比的经处理区域中剩余犬视紫红质RNA的条形图。图19E是显示作为在未经处理区域中测量的犬RHO RNA水平的百分比的经处理区域中人RHO820的水平的条形图。图19F是显示用于RNA定量的每对钻取物的数值的表。
通过体内视网膜成像对以5×1011vg/ml视网膜下注射AAV2/5-sc-HOP-RHO820-H1-shRNA820的突变体RHOT4R/+狗的眼中针对光诱导损伤的光感受器保护的评价:
在注射之前、注射之后11周(光暴露之前)和光损伤之后2周通过cSLO/OCT成像检查来自以5×1011vg/ml病毒滴度视网膜下注射的2只突变体RHOT4R/+狗的眼。使用对先前显示在RHO T4R突变体中引起急性视网膜变性但在WT狗中则不引起的强度(角膜辐照度为1mW/cm2)的白光暴露1分钟来评估由AAV2/5-sc-HOP-RHO820-H1-shRNA820载体在经处理/泡区域中赋予的保护水平。在所有注射之后时间点均保持泡/经处理区域中的ONL厚度,表明该载体构建体无毒并且在此期间没有光感受器的损失。对于每只眼,周围的非泡/未经处理区域用作内部对照。在光暴露之后两周,在两只注射眼中的泡/经处理区域中均完全保持ONL厚度。
图20A-20C示出了体内视网膜成像,其显示在经5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820处理的突变体RHOT4R/+视网膜区域中针对光诱导的视网膜变性的保护。图20A示出了en face cSLO复合图,其显示在光暴露之后2周被保护免受变性的视网膜区域(边界由白色箭头界定)。浅灰色箭头表示图20B中所示的OCT B扫描在经处理区域中的位置,深灰色箭头表示图20C中所示的OCT B扫描在未经处理区域中的位置。图20B示出了注射之前、注射之后11周和注射之后13周/光暴露之后2周经处理区域中的OCT B扫描。在注射病毒载体之后的这两个时间点在整个经处理区域均保持ONL厚度。图20B和30V示出了注射之前、注射之后11周和注射之后13周/光暴露之后2周未经处理区域中的OCT B扫描。ONL被保持直至注射之后11周,但在光暴露之后2周完全丧失。图21示出了来自经5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820处理的两个RHOT4R/+的ONL厚度的地形图,其显示针对光诱导的视网膜变性的保护。
通过组织学和免疫组织化学对以5×1011/vg/ml滴度注射AAV2/5-sc-HOP-RHO820-H1-shRNA820的突变体RHOT4R/+狗的眼中针对光诱导损伤的光感受器保护的评价:
检查来自上文中列出的同一突变体RHOT4R/+狗的眼,其被视网膜下注射5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820并且随后光暴露(在注射之后11周时)于持续1分钟的一定强度(角膜辐照度为1mW/cm2)的白光。该光剂量先前显示在RHO T4R突变体中引起急性视网膜变性但在WT狗中则不引起。
使用免疫组织化学评估由AAV2/5-sc-HOP-RHO820-H1-shRNA820在经处理/泡区域中赋予的保护水平。对于每只眼,周围的非泡/未经处理区域用作内部对照。针对视紫红质(RHO)和人视锥拘留蛋白(hCA)的抗体用于评估视杆外段和视锥形态的完整性。在光暴露之后两周,在注射有5×1011vg/ml滴度的眼的泡/经处理区域中实现ONL厚度的优异保持。除在用敲减试剂shRNA820处理视网膜时观察到的之外并且与之相反,用AAV2/5-sc-HOP-RHO820-H1-shRNA820构建体实现视杆外段的保留。
图22示出了视网膜下注射有5×1011/vg/ml滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820的突变体RHOT4R/+视网膜的经处理区域、过渡区和未经处理区域的免疫组织化学(视紫红质染色为绿色并且在图22的图中显示为较浅染色;人视锥拘留蛋白染色为红色并且在图22的图中显示为灰色染色)。在经处理区域中,外核层(ONL)厚度和视杆外段(OS)完全保留,而在未经处理区域中,所有视杆都已损失,并且ONL减小至单排锥细胞体。在过渡区看到经处理区域和未经处理区域之间的明确边界。
用5×1011vg/ml病毒滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820实现犬RHO RNA和蛋白质(通过western印迹)的完全敲减。当与犬视网膜中的正常RHO水平相比时,在mRNA(118%至130%)和蛋白质(30%至33%)水平均实现硬化RHO820的高效替代。用5×1011vg/ml病毒滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820实现对包含光感受器的细胞体的外核层(ONL)的完全保护。用5×1011vg/ml病毒滴度的AAV2/5-sc-HOP-RHO820-H1-shRNA820实现作为用RHO820进行高效RHO替代之结果的视杆外段的完全保留。
参考文献:
1.Mao H,Gorbatyuk Ms,Rossmiller B,Hauswirth WW,Lewin AS,Long-TermRescue of Retinal Structure and Function by Rhodopsin RNA Replacement with aSingle Adeno-Associated Viral Vector in P23H RHO Transgenic Mice.Hum GeneTher.2012;23:356-366.
2.Rossmiller B,Mao H,Lewin AS,Gene therapy in animal models ofautosomal dominant retinitis Pigmentosa.Mol Vis.2012;18:2479-2496.
3,Gorbatyuk M,Justilien V,Liu J,Hauswirth WW,Lewin AS.Suppression ofmouse rhodopsin expression in vivo by AAV mediated siRNA delivery.VisionRes.2007;47:1202-1208.
4.Khvorova A,Reynolds A,Jayasena SD.Functional siRNAs and miRNAsexhibit strand bias.Cell.2003;115:209-216.
5.Reynolds A,Leake D,Boese Q,Scaringe S,Marshall WS,KhvorovaA.Rational siRNA design for RNA interference.Nat Biotechnol.2004;22:326-330.
6.Jensen SMR,Schmitz A,Pedersen FS,Kjems J+,Bramsen JB.FunctionalSelection of shRNA Loops from Randomized Retroviral Libraries.PLoS ONE.2012;7:e43095.
7.Zhou H,Xia XG,Xu Z.An RNA polymerase II construct synthesizesshort-hairpin RNA with a quantitative indicator and mediates highly efficientRNAi.Nucleic Acids Res.
2005;33:e62-e70.
等同方案
虽然本文中已描述并举例说明了本发明的数个实施方案,但是本领域普通技术人员将容易预见用于进行本文中所述的功能和/或获得本文中所述的结果和/或一个或更多个优点的多种其他手段和/或结构,并且每个这样的变化方案和/或修改方案均被视为在本文中所述的本发明实施方案的范围之内。更一般地,本领域技术人员将容易理解,本文中描述的所有参数、尺寸、材料和构造意为示例性的且实际的参数、尺寸、材料和/或构造将取决于使用本发明教导的具体应用。本领域技术人员将认识到或能够仅使用常规实验即可确定本文中所描述的本发明具体实施方案的许多等同方案。因此,应理解的是,前述实施方案仅通过实例的方式给出,且在所附权利要求书及其等效文件的范围之内,可相对于具体描述和要求保护的以其他方式来实施本发明实施方案。本公开内容的本发明实施方案涉及本文中所述的每个单独的特征、系统、制品、材料、套件和/或方法。此外,如果这样的特征、系统、制品、材料、套件和/或方法不相互不一致,则两个或更多个这样的特征、系统、制品、材料、套件和/或方法的任意组合也包括在本公开内容的本发明范围内。
本文中限定和使用的所有定义均应理解为超过字典定义、通过引用并入的文件中的定义和/或所限定术语的一般含义。
本文中公开的所有参考文献、专利和专利申请均针对其各自被引用的主题而通过引用并入,其在一些情况下可涵盖文件的全部内容。
除非明确指出相反,否则如本文中在说明书和权利要求书中使用的没有数量词修饰的名词应理解为意指“至少一个/种”。
如本文中在说明书和权利要求书中使用的短语“和/或”应被理解为意指如此连接的要素(即,在一些情况下联合存在而在另一些情况下分开存在的要素)中的“任一个或两个”。用“和/或”列出的多个要素应以相同的方式解释,即如此连接的要素中的“一个或更多个”。除通过“和/或”子句所具体确定的要素之外,其他要素也可任选地存在,无论是否与具体确定的那些元素相关。因此,作为一个非限制性实例,当与开放式语言(例如“包含/包括”)联合使用时对“A和/或B”的提及在一个实施方案中可指仅A(任选地包括除B之外的要素);在另一个实施方案中,可指仅B(任选地包括除A之外的要素);在另一个实施方案中,可指A和B二者(任选地包括其他要素)等。
如本文中在说明书和权利要求书中使用的“或/或者”应被理解为与如上限定的“和/或”具有相同的含义。例如,当分离列表中的项目时,“或/或者”或“和/或”应被解释为包括性的,即包括多个要素或要素列表中的至少一个,但是也包括多于一个,任选地包括另外的未列出项目。只有明确指出相反的术语(例如“仅之一”或“恰好之一”,或者,在权利要求书中使用时,“由......组成”)才将指包括多个要素或要素列表中的恰好一个要素。一般而言,当之前有排他性的术语(例如“任一”、“之一”、“仅之一”或“恰好之一”)时,本文中使用的术语“或/或者”应仅解释为表示排他性的替代选择(即“一个或另一个但不是二者”)。当在权利要求书中使用时,“基本上由......组成”应具有其在专利法领域中所使用的普通含义。
如本文中在说明书和权利要求书中使用的,关于一个或更多个要素的列表的短语“至少一个”应理解为意指选自要素列表中任意一个或更多个要素中的至少一个要素,但是不一定包括要素列表内具体列出的各个要素和每个要素中的至少一个,并且不排除要素列表中要素的任意组合。该定义还允许可任选地存在除短语“至少一个”所指在要素列表内明确确定的要素之外的要素,不论与那些明确确定的要素是否相关。因此,作为一个非限制性实例,“A和B中的至少一个”(或等同地,“A或B中的至少一个”或等同地,“A和/或B中的至少一个”)在一个实施方案中可以指,至少一个A,任选地包括多于一个A,而不存在B(且任选地包括除B之外的要素);在另一个实施方案中,可以指至少一个B,任选地包括多于一个B,而不存在A(且任选地包括除A之外的要素);在另一个实施方案中,可以指至少一个A,任选地包括多于一个A,以及至少一个B,任选地包括多于一个B(且任选地包括其他要素)等。
还应当理解,除非明确指出相反,否则在本文中要求保护的包括多于一个步骤或动作的任何方法中,方法的步骤或动作的顺序不一定局限于方法的步骤或动作被记载的顺序。
在权利要求书以及在上述说明书中,所有的连接词例如“包含”、“包括”、“携带”、“具有”、“含有”、“涉及”、“容纳”、“由...构成”等应理解为是开放式的,即意指包括但不限于。仅连接词“由......组成”和“基本上由...组成”应分别是封闭式或半封闭式连接词,如美国专利局专利审查程序手册2111.03部分中所述。应当理解,在本文件中使用开放式连接词(例如,“包含”)描述的实施方案在一些替代实施方案中也被考虑为“由通过开放式连接词描述的特征组成”和“基本上由其组成”。例如,如果本公开内容描述“包含A和B的组合物”,则本公开内容还考虑以下替代实施方案:“由A和B组成的组合物”和“基本上由A和B组成的组合物”。
序列表
<110> 佛罗里达大学研究基金会有限公司
宾夕法尼亚大学托管会
<120> 用于治疗显性视网膜色素变性的AAV载体
<130> U1197.70073WO00
<140> 尚未分配
<141> 与此同时
<150> US 62/398,451
<151> 2016-09-22
<150> US 62/302,122
<151> 2016-03-01
<160> 42
<170> PatentIn version 3.5
<210> 1
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 1
cugccuacau guuucugcu 19
<210> 2
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 2
agcagaaaca uguaggcag 19
<210> 3
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 3
ccuacauguu ucugcugau 19
<210> 4
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 4
aucagcagaa acauguagg 19
<210> 5
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 5
gcauggucau caucauggu 19
<210> 6
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 6
accaugauga ugaccaugc 19
<210> 7
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 7
guggcauucu acaucuuca 19
<210> 8
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 8
ugaagaugua gaaugccac 19
<210> 9
<211> 7
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 9
ucaagag 7
<210> 10
<211> 7
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 10
ugugcuu 7
<210> 11
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 11
cugccuacau guuucugcuu caagagagca gaaacaugua ggcag 45
<210> 12
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 12
cugccuacau guuucugcuu gugcuuagca gaaacaugua ggcag 45
<210> 13
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 13
ccuacauguu ucugcugauu caagagauca gcagaaacau guagg 45
<210> 14
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 14
ccuacauguu ucugcugauu gugcuuauca gcagaaacau guagg 45
<210> 15
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 15
gcauggucau caucaugguu caagagacca ugaugaugac caugc 45
<210> 16
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 16
gcauggucau caucaugguu gugcuuacca ugaugaugac caugc 45
<210> 17
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 17
guggcauucu acaucuucau caagagugaa gauguagaau gccac 45
<210> 18
<211> 45
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 18
guggcauucu acaucuucau gugcuuugaa gauguagaau gccac 45
<210> 19
<211> 93
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<220>
<221> misc_feature
<222> (20)..(38)
<223> n是a、c、g、u或不存在
<220>
<221> misc_feature
<222> (58)..(76)
<223> n是a、c、g、u或不存在
<400> 19
ugcuguugac agugagcgan nnnnnnnnnn nnnnnnnnua gugaagccac agauguannn 60
nnnnnnnnnn nnnnnncugc cuacugccuc gga 93
<210> 20
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 20
cugccuacau guuucugcuu caagagagca gaaacaugua ggcaguu 47
<210> 21
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 21
cugccuacau guuucugcuu gugcuuagca gaaacaugua ggcaguu 47
<210> 22
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 22
ccuacauguu ucugcugauu caagagauca gcagaaacau guagguu 47
<210> 23
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 23
ccuacauguu ucugcugauu gugcuuauca gcagaaacau guagguu 47
<210> 24
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 24
gcauggucau caucaugguu caagagacca ugaugaugac caugcuu 47
<210> 25
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 25
gcauggucau caucaugguu gugcuuacca ugaugaugac caugcuu 47
<210> 26
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 26
guggcauucu acaucuucau caagagugaa gauguagaau gccacuu 47
<210> 27
<211> 47
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 27
guggcauucu acaucuucau gugcuuugaa gauguagaau gccacuu 47
<210> 28
<211> 89
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 28
ugcuguugac agugagcgac ugccuacaug uuucugcugu gaagccacag augagcagaa 60
acauguaggc agcugccuac ugccucgga 89
<210> 29
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 29
ccgccuauau guuccuccu 19
<210> 30
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 30
agcagaaaca uguaggcag 19
<210> 31
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 31
ccgccuacau guuucugcu 19
<210> 32
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 32
gcauggugau aauaauggu 19
<210> 33
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 33
accaugauga ugaccaugc 19
<210> 34
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 34
gcauggucau caucauggu 19
<210> 35
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 35
guggcuuuuu auauauuca 19
<210> 36
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 36
ugaagaugua gaaugccac 19
<210> 37
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 37
guggcauucu acaucuuca 19
<210> 38
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 38
ccuauauguu ccuccucau 19
<210> 39
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 39
aucagcagaa acauguagg 19
<210> 40
<211> 19
<212> RNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 40
ccuacauguu ucugcugau 19
<210> 41
<211> 13706
<212> DNA
<213> 人
<400> 41
gtgggggacc aggagaaaga aagccaagga agaggaggag gaggaggaga aggaggagaa 60
ggatgctgac ctagcagctc ctctcacagc agctcctctc ttgcagaggc tgaagagcga 120
tttgtgccct gcaagctaag cccctaatcc accgaggcaa aggcaaagcc cctagccggg 180
ctcccgaggg ctgggactcg ggtgccccaa gatggctgca tccagccatc ttggcttaga 240
aagcccccca catgccagct tggccaacac ccacaccatg ggtttctctg gactgcccga 300
cacaaggtgt gggtgctggc caggcctgtg ttcaaatccc agctctgcag aggaactttg 360
accctgcata ccccagattc ctcagtggtc agtggggagt tagaccctct tcataggggg 420
caggaggagt tgttcattca ttcaacaaat gtttattgaa cacctcctat gggttgtgag 480
ctcagaggca gcgatgaaca ggccaggctg gtcctgcatt ctagaaatag atgggaagtc 540
agtcaataag tagacaaatg aggccaggtg tggtggcatg cctgtagacc cagttactcg 600
ggatgctgag gtaggaggat cacttgagcc taggacagga attcaaggct gcagtaagct 660
atgattgcgc cactgcactc cagcctgggc aacagagcaa gactcatctc taaaaaacat 720
ttaaaaattg ttttaagaag acaaatgaga tagtcgctga tggtaatgac tgtgtaaaaa 780
ctgaacatgg ctgggtgtgg ttgctcacac ctataatctc agcactttgg gaggctgaga 840
ttacagcctc ccaagtggct cccaaggcag gaggatcact tgagcctggg agttagagaa 900
cagcttggac aatataggga gagcccaact ctacaaaaat gaaaataaat tagccaggca 960
tggtggcaca caccaatggt cccagctact caggggttga ggtggtggac cgcttgagcc 1020
caggaggttg aggctgcagt gagccatgat catgccgctg cactccaacc tgagtcacag 1080
agtgataccc tgtctcaaaa aacaataggc caggtgtggt ggctcacgcc tgtaacccca 1140
gcactttggg aggccgaggc ggatggatca cttgagatca ggagttagag accagcctgg 1200
ctaacatggc aaaatcctgt ctgtactaaa aatataaaaa ttagccaggc atggcagtac 1260
atgcctgtag tcctggttac ttgggaggct aaggcaggag aatcgcttga acccaggaag 1320
aggaggttgc agtgagccaa gatcacacca ctgcactcca gcttgggtga cagagtgaga 1380
ccctgtctca aaacagctaa acctggtggg ggtgcctggt gtgtaggatg gtcaggggtg 1440
gtctctccaa ggacatgagt gtgagcggag acctgaagga gactcaggaa gagattaata 1500
ctgtcagcaa caaatatatt gatcacttac aagcactccc aataatccta ttaggtaggc 1560
actattatca ttcccatttt acagagtgga gaaccgaagc acactctcgg gagggcgggg 1620
tagctggctg cacccaggct gtgtagcctc agtccagatg taagggtggg tggaaaagag 1680
ccttgcccaa tgagggagaa cagtgaaacc aaggccatag ggtctaaaga ttcacgaacc 1740
aggctctcat ggagaaagca ggtgaggttt actgtataga tgggtgtgcc cctaccccac 1800
actgaggctt cctcgtctga gcaaactgag gcccagagag gggaaggaag caggactacc 1860
atggtgactc aaagaccagc tagaatccag cctcctctcc tcgaggcttc cactgcccca 1920
cgccaggcct gtgtgactca gtctagggcc tttccattac cccagctaaa cctttcttta 1980
gtcatttata ccatggtgtg aatggctggc tggtctttcc tgagagctat ctttgatgag 2040
gggagggagg catagccagg tttgggaagc tgatacccca ggaagcccag ttgactgtgt 2100
gggttatagc ccaggctgtc actgatttgt aacgggacct gagcaactct gcagagctag 2160
gcctcagtct tttcatctgc aaaatggata tagcagagat ggtcagagta ggtgacttcg 2220
aatgaccctt ccagctcact atgagtctgt tttcctgaac aaagagcatt ttttgtttaa 2280
aaaaaaattt cttgggccgg acacggtggt tcactcctat aatcctggca ctttgggagg 2340
ccgaggaggg tggatcgctt gagccaggag ttcaggacca gcctgggcaa catagcgaga 2400
ctccacccct acaaaaaata caaaaactag tggtgtgcac ttgtggtccc agctactcag 2460
gaggctgagg tgagaggatc gcttgagccc aggaggcaga ggctacagtg agctatgatt 2520
gtggcactgc actccagcct gggcgacaga gaccttgtct caaaactttt tttttcttcg 2580
tcaagcttta cagaataaag agcactgtca cctcagtgat ggctgttagt tccccatcac 2640
cagggctcca tgaggttgca attgtgaaac tcacaaagga ggaacctgag acagagaggg 2700
gaagtactga gatcatctag gtccattccc ccactcactc gttcattcaa caaatattca 2760
ggagcacctt ctaggtgcca ggccctggag acacatcagt gaacaaaaca gacatcatcc 2820
cacctctttc cactacaggc caagcaccat gctggtctct gggaaccctg ttgtgagcaa 2880
gacagaccca ggcttaccct tgtggactca tgttacaggc agggagacgg gcacaaaaca 2940
caaataaaaa gcttccatgc tgtcagaagc actatgcaaa aagcaagatg ctgaggtact 3000
gctaagctgt gtgggatggg ggctcagccc ggccagggag gggccagttg tgggtcagtc 3060
ttgacccaag gcatccagga caccctcctt ctggccatga gggtccacgt cagaatcaaa 3120
ccctcacctt aacctcatta gcgttgggca taatcaccag gccaagcgcc ttaaactacg 3180
agaggcccca tcccacccgc cctgccttag ccctgccacg tgtgccaaac gctgttagac 3240
ccaacaccac ccaggccagg tagggggctg gagcccaggt gggctgcagg gaagggggca 3300
ctcttctgag cagacagatc tgggaatcct gggtgggaag agagacagtg agagagagat 3360
taagggatat ttcccaggca tcagggcttt gcactctcag gggtccttcc gcctggatgt 3420
ccttcccctg aagcttcctc ctgttgttcc gttctcagct caagctccag cttctcagag 3480
aagcctcctg tgttgggagt ggctgcgact gaactgtccc tactgttatt cgctcttcta 3540
tttgtttgtg gtccctgtgc cccctcaccc cacaaaaaca ctggcttctt gtgagcagga 3600
gcttgctctt tcgtgtaccc tgtgtgtccc caaggaccaa gcaccttgtc tgggccacag 3660
taggtgctca atacacatgt tggctggaca gtggtcactg agcggccgca cgtcgggcac 3720
tctcagcact tgcacaggcc gccccagaca ccccacttca ttcctgggag gtgtcatcat 3780
gttgcttgga cgacggggag agggggacct gccagtgttg gcctccattt tcccccagtc 3840
atctgccccc aaggctctga ctactttctt tctcacggta catcctgcta ttctggaatc 3900
ggccctcgtg gggccacctg gtacatggca tttgaggccc tcgtggctga ttaggcctcc 3960
cccaacagtg ccctgtctgc tgcctccagg gccagcctcc ccttcagact ggagtcccct 4020
gaagggttct gcccctcccc tgctctggta gccccctcca tcctccctcc ctccactcca 4080
tctttggggg catttgagtc acctttctac accagtgatc tgcccaagcc actgctcact 4140
ttcctctgga taaagccagg ttccccggcc tagcgttcaa gacccattac aactgccccc 4200
agcccagatc ttccccacct agccacctgg caaactgctc cttctctcaa aggcccaaac 4260
atggcctccc agactgcaac ccccaggcag tcaggccctg tctccacaac ctcacagcca 4320
ccctggacgg aatctgcttc ttcccacatt tgagtcctcc tcagcccctg agctcctctg 4380
ggcagggctg tttctttcca tctttgtatt cccaggggcc tgcaaataaa tgtttaatga 4440
acgaacaaga gagtgaattc caattccatg caacaaggat tgggctcctg ggccctaggc 4500
tatgtgtctg gcaccagaaa cggaagctgc aggttgcagc ccctgccctc atggagctcc 4560
tcctgtcaga ggagtgtggg gactggatga ctccagaggt aacttgtggg ggaacgaaca 4620
ggtaaggggc tgtgtgacga gatgagagac tgggagaata aaccagaaag tctctagctg 4680
tccagaggac atagcacaga ggcccatggt ccctatttca aacccaggcc accagactga 4740
gctgggacct tgggacagac aagtcatgca gaagttaggg gaccttctcc tcccttttcc 4800
tggatcctga gtacctctcc tccctgacct caggcttcct cctagtgtca ccttggcccc 4860
tcttagaagc caattaggcc ctcagtttct gcagcgggga ttaatatgat tatgaacacc 4920
cccaatctcc cagatgctga ttcagccagg agcttaggag ggggaggtca ctttataagg 4980
gtctgggggg gtcagaaccc agagtcatcc agctggagcc ctgagtggct gagctcaggc 5040
cttcgcagca ttcttgggtg ggagcagcca cgggtcagcc acaagggcca cagccatgaa 5100
tggcacagaa ggccctaact tctacgtgcc cttctccaat gcgacgggtg tggtacgcag 5160
ccccttcgag tacccacagt actacctggc tgagccatgg cagttctcca tgctggccgc 5220
ctacatgttt ctgctgatcg tgctgggctt ccccatcaac ttcctcacgc tctacgtcac 5280
cgtccagcac aagaagctgc gcacgcctct caactacatc ctgctcaacc tagccgtggc 5340
tgacctcttc atggtcctag gtggcttcac cagcaccctc tacacctctc tgcatggata 5400
cttcgtcttc gggcccacag gatgcaattt ggagggcttc tttgccaccc tgggcggtat 5460
gagccgggtg tgggtggggt gtgcaggagc ccgggagcat ggaggggtct gggagagtcc 5520
cgggcttggc ggtggtggct gagaggcctt ctcccttctc ctgtcctgtc aatgttatcc 5580
aaagccctca tatattcagt caacaaacac cattcatggt gatagccggg ctgctgtttg 5640
tgcagggctg gcactgaaca ctgccttgat cttatttgga gcaatatgcg cttgtctaat 5700
ttcacagcaa gaaaactgag ctgaggctca aagaagtcaa gcgccctgct ggggcgtcac 5760
acagggacgg gtgcagagtt gagttggaag cccgcatcta tctcgggcca tgtttgcagc 5820
accaagcctc tgtttccctt ggagcagctg tgctgagtca gacccaggct gggcactgag 5880
ggagagctgg gcaagccaga cccctcctct ctgggggccc aagctcaggg tgggaagtgg 5940
attttccatt ctccagtcat tgggtcttcc ctgtgctggg caatgggctc ggtcccctct 6000
ggcatcctct gcctcccctc tcagcccctg tcctcaggtg cccctccagc ctccctgccg 6060
cgttccaagt ctcctggtgt tgagaaccgc aagcagccgc tctgaagcag ttcctttttg 6120
ctttagaata atgtcttgca tttaacagga aaacagatgg ggtgctgcag ggataacaga 6180
tcccacttaa cagagaggaa aactgaggca gggagagggg aagagactca tttagggatg 6240
tggccaggca gcaacaagag cctaggtctc ctggctgtga tccaggaata tctctgctga 6300
gatgcaggag gagacgctag aagcagccat tgcaaagctg ggtgacgggg agagcttacc 6360
gccagccaca agcgtctctc tgccagcctt gccctgtctc ccccatgtcc aggctgctgc 6420
ctcggtccca ttctcaggga atctctggcc attgttgggt gtttgttgca ttcaataatc 6480
acagatcact cagttctggc cagaaggtgg gtgtgccact tacgggtggt tgttctctgc 6540
agggtcagtc ccagtttaca aatattgtcc ctttcactgt taggaatgtc ccagtttggt 6600
tgattaacta tatggccact ctccctatgg aacttcatgg ggtggtgagc aggacagatg 6660
tctgaattcc atcatttcct tcttcttcct ctgggcaaaa cattgcacat tgcttcatgg 6720
ctcctaggag aggcccccac atgtccgggt tatttcattt cccgagaagg gagagggagg 6780
aaggactgcc aattctgggt ttccaccacc tctgcattcc ttcccaacaa ggaactctgc 6840
cccacattag gatgcattct tctgctaaac acacacacac acacacacac acacaacaca 6900
cacacacaca cacacacaca cacacacaca aaactcccta ccgggttccc agttcaatcc 6960
tgaccccctg atctgattcg tgtcccttat gggcccagag cgctaagcaa ataacttccc 7020
ccattccctg gaatttcttt gcccagctct cctcagcgtg tggtccctct gccccttccc 7080
cctcctccca gcaccaagct ctctccttcc ccaaggcctc ctcaaatccc tctcccactc 7140
ctggttgcct tcctagctac cctctccctg tctagggggg agtgcaccct ccttaggcag 7200
tggggtctgt gctgaccgcc tgctgactgc cttgcaggtg aaattgccct gtggtccttg 7260
gtggtcctgg ccatcgagcg gtacgtggtg gtgtgtaagc ccatgagcaa cttccgcttc 7320
ggggagaacc atgccatcat gggcgttgcc ttcacctggg tcatggcgct ggcctgcgcc 7380
gcacccccac tcgccggctg gtccaggtaa tggcactgag cagaagggaa gaagctccgg 7440
gggctctttg tagggtcctc cagtcaggac tcaaacccag tagtgtctgg ttccaggcac 7500
tgaccttgta tgtctcctgg cccaaatgcc cactcagggt aggggtgtag ggcagaagaa 7560
gaaacagact ctaatgttgc tacaagggct ggtcccatct cctgagcccc atgtcaaaca 7620
gaatccaaga catcccaacc cttcaccttg gctgtgcccc taatcctcaa ctaagctagg 7680
cgcaaattcc aatcctcttt ggtctagtac cccgggggca gccccctcta accttgggcc 7740
tcagcagcag gggaggccac accttcctag tgcaggtggc catattgtgg ccccttggaa 7800
ctgggtccca ctcagcctct aggcgattgt ctcctaatgg ggctgagatg agacacagtg 7860
gggacagtgg tttggacaat aggactggtg actctggtcc ccagaggcct catgtccctc 7920
tgtctccaga aaattcccac tctcacttcc ctttcctcct cagtcttgct agggtccatt 7980
tcttacccct tgctgaattt gagcccaccc cctggacttt ttccccatct tctccaatct 8040
ggcctagttc tatcctctgg aagcagagcc gctggacgct ctgggtttcc tgaggcccgt 8100
ccactgtcac caatatcagg aaccattgcc acgtcctaat gacgtgcgct ggaagcctct 8160
agtttccaga agctgcacaa agatccctta gatactctgt gtgtccatct ttggcctgga 8220
aaatactctc accctggggc taggaagacc tcggtttgta caaacttcct caaatgcaga 8280
gcctgagggc tctccccacc tcctcaccaa ccctctgcgt ggcatagccc tagcctcagc 8340
gggcagtgga tgctggggct gggcatgcag ggagaggctg ggtggtgtca tctggtaacg 8400
cagccaccaa acaatgaagc gacactgatt ccacaaggtg catctgcatc cccatctgat 8460
ccattccatc ctgtcaccca gccatgcaga cgtttatgat ccccttttcc agggagggaa 8520
tgtgaagccc cagaaagggc cagcgctcgg cagccacctt ggctgttccc aagtccctca 8580
caggcagggt ctccctacct gcctgtcctc aggtacatcc ccgagggcct gcagtgctcg 8640
tgtggaatcg actactacac gctcaagccg gaggtcaaca acgagtcttt tgtcatctac 8700
atgttcgtgg tccacttcac catccccatg attatcatct ttttctgcta tgggcagctc 8760
gtcttcaccg tcaaggaggt acgggccggg gggtgggcgg cctcacggct ctgagggtcc 8820
agcccccagc atgcatctgc ggctcctgct ccctggagga gccatggtct ggacccgggt 8880
cccgtgtcct gcaggccgct gcccagcagc aggagtcagc caccacacag aaggcagaga 8940
aggaggtcac ccgcatggtc atcatcatgg tcatcgcttt cctgatctgc tgggtgccct 9000
acgccagcgt ggcattctac atcttcaccc accagggctc caacttcggt cccatcttca 9060
tgaccatccc agcgttcttt gccaagagcg ccgccatcta caaccctgtc atctatatca 9120
tgatgaacaa gcaggtgcct actgcgggtg ggagggcccc agtgccccag gccacaggcg 9180
ctgcctgcca aggacaagct acttcccagg gcaggggagg gggctccatc agggttactg 9240
gcagcagtct tgggtcagca gtcccaatgg ggagtgtgtg agaaatgcag attcctggcc 9300
ccactcagaa ctgctgaatc tcagggtggg cccaggaacc tgcatttcca gcaagccctc 9360
cacaggtggc tcagatgctc actcaggtgg gagaagctcc agtcagctag ttctggaagc 9420
ccaatgtcaa agtcagaagg acccaagtcg ggaatgggat gggccagtct ccataaagct 9480
gaataaggag ctaaaaagtc ttattctgag gggtaaaggg gtaaagggtt cctcggagag 9540
gtacctccga ggggtaaaca gttgggtaaa cagtctctga agtcagctct gccattttct 9600
agctgtatgg ccctgggcaa gtcaatttcc ttctctgtgc tttggtttcc tcatccatag 9660
aaaggtagaa agggcaaaac accaaactct tggattacaa gagataattt acagaacacc 9720
cttggcacac agagggcacc atgaaatgtc acgggtgaca cagccccctt gtgctcagtc 9780
cctggcatct ctaggggtga ggagcgtctg cctagcaggt tccctccagg aagctggatt 9840
tgagtggatg gggcgctgga atcgtgaggg gcagaagcag gcaaagggtc ggggcgaacc 9900
tcactaacgt gccagttcca agcacactgt gggcagccct ggccctgact caagcctctt 9960
gccttccagt tccggaactg catgctcacc accatctgct gcggcaagaa cccactgggt 10020
gacgatgagg cctctgctac cgtgtccaag acggagacga gccaggtggc cccggcctaa 10080
gacctgccta ggactctgtg gccgactata ggcgtctccc atcccctaca ccttccccca 10140
gccacagcca tcccaccagg agcagcgcct gtgcagaatg aacgaagtca cataggctcc 10200
ttaatttttt tttttttttt aagaaataat taatgaggct cctcactcac ctgggacagc 10260
ctgagaaggg acatccacca agacctactg atctggagtc ccacgttccc caaggccagc 10320
gggatgtgtg cccctcctcc tcccaactca tctttcagga acacgaggat tcttgctttc 10380
tggaaaagtg tcccagctta gggataagtg tctagcacag aatggggcac acagtaggtg 10440
cttaataaat gctggatgga tgcaggaagg aatggaggaa tgaatgggaa gggagaacat 10500
atctatcctc tcagaccctc gcagcagcag caactcatac ttggctaatg atatggagca 10560
gttgtttttc cctccctggg cctcactttc ttctcctata aaatggaaat cccagatccc 10620
tggtcctgcc gacacgcagc tactgagaag accaaaagag gtgtgtgtgt gtctatgtgt 10680
gtgtttcagc actttgtaaa tagcaagaag ctgtacagat tctagttaat gttgtgaata 10740
acatcaatta atgtaactag ttaattacta tgattatcac ctcctgatag tgaacatttt 10800
gagattgggc attcagatga tggggtttca cccaaccttg gggcaggttt ttaaaaatta 10860
gctaggcatc aaggccagac cagggctggg ggttgggctg taggcaggga cagtcacagg 10920
aatgcagaat gcagtcatca gacctgaaaa aacaacactg ggggaggggg acggtgaagg 10980
ccaagttccc aatgagggtg agattgggcc tggggtctca cccctagtgt ggggccccag 11040
gtcccgtgcc tccccttccc aatgtggcct atggagagac aggcctttct ctcagcctct 11100
ggaagccacc tgctcttttg ctctagcacc tgggtcccag catctagagc atggagcctc 11160
tagaagccat gctcacccgc ccacatttaa ttaacagctg agtccctgat gtcatcctta 11220
tctcgaagag cttagaaaca aagagtggga aattccactg ggcctacctt ccttggggat 11280
gttcatgggc cccagtttcc agtttccctt gccagacaag cccatcttca gcagttgcta 11340
gtccattctc cattctggag aatctgctcc aaaaagctgg ccacatctct gaggtgtcag 11400
aattaagctg cctcagtaac tgctccccct tctccatata agcaaagcca gaagctctag 11460
ctttacccag ctctgcctgg agactaaggc aaattgggcc attaaaagct cagctcctat 11520
gttggtatta acggtggtgg gttttgttgc tttcacactc tatccacagg atagattgaa 11580
actgccagct tccacctgat ccctgaccct gggatggctg gattgagcaa tgagcagagc 11640
caagcagcac agagtcccct ggggctagag gtggaggagg cagtcctggg aatgggaaaa 11700
accccaactt tggggtcata gaggcacagg taacccataa aactgcaaac aagctttgtc 11760
acctctcaga gcttccttat ctgcaaaaaa gaatcttaaa actgaccttg gctgggcaca 11820
gtggctcaca cctctaatcc cagcactttg ggaggccaag gtgggcagat cacgaggtca 11880
ggagtttgag accagcctga ccaacacggt gaaaccctgt ctctactaaa aatacaaaaa 11940
tcagctgggc atggtggcgc gtgcctgtaa tcccagctat tcagtgggct gaggcaggag 12000
aatcgcttga acctgggagg tggaggttgc agtgagccga gattgcgcca ctgcactcca 12060
gcctgagcaa cagagggaca gtctgtctcc aaacaaaaca aaacaaacaa acaaacaaac 12120
aaacaaacaa aaaacaacaa caaaaaaacc acttgatcct aaggggatta gatgcgactg 12180
tggactttaa gtggccagcc tactgcctgg catgcagcag atgagactat ggcaatactg 12240
ggcttcagct cagagctggc cttactagag accctgtccc aaaggggaaa aggatggagc 12300
taaagctccc gagagtcacc ccctcctccg aggtgagaaa ggagggcagg agcatgagat 12360
agccgatcct cggtgccttg gtgaggctgg ggcaaatcat gctgggatct ctatcattgt 12420
ccctctttac tgtgactcac tagataatat cagtcaggat acttttggtc acaagtgata 12480
ggaaatccaa ctcatttggg ctgaagcaaa agggacacat tgttggctca catgaacaaa 12540
aagcccgggg cttcaggcac agggtatcac catgactgag atggggatta attctgtgat 12600
tggccaagtc taggtcacct gatcatacgt aactcattta tgcctgaggt tgcaattttt 12660
tggatttttg caatcagacc ttggcgatga ccttgagcag taggatataa ataactccca 12720
catgcttagc gttccaataa tggaatacta ggcatacgca ggtctaactg catcaccatg 12780
gctggaatgg ggattcatcc tctgattggt cagacctagg tcacatgctc accctgcagc 12840
ccaagcaggc tgaatgggga gaggtaggtt tcacaaagga aagcccaggt gctgttacct 12900
gaagtaggag ggcaggaggc agggtgagca gagccaacat caacccagag ggaatggaat 12960
ctaagttggt gttttctggg cacgtggctg gaccaggcct ccctccctca tcatctcagg 13020
gacatgaggg agaagattcc tatgggtggt cccgaaggtc tcaccctttg ttttggatgc 13080
tgtgttgggc cagggtggca gtgggtggga cagtggcatc ttagctgccc tgacttgcag 13140
gcagcccatt ccagctcccc gccccaaccc caacccagcc cactttttct gagaaatggt 13200
acatttgccc cagcctcatg tccagaggaa aattttactc taacaccaga acattctctg 13260
gtttgtcctg atagacaaga aagcctccac ctccttaatt tacaaatgac ttgacagctg 13320
cttcgtgggc acttgcatac ataaagagaa ggagctgctg ccttaagttg cagcaagttt 13380
ggccccacct catctccagg cagccagcag atgtacagag tgcctcttgg gtacaatggc 13440
agctccattc aaccaaacct gagcaagctg accccatgcc agaatgcact ggggactcgg 13500
agatgaattg gagcctagag accaagtctc taggctatga cctgggctgc ctcacggcca 13560
cagagctctg tcacgccaag ggagagatgc acccctgaaa gcctgaggtg ccccataagg 13620
agagagtggg tgcccttccc aactatgtag cttcagggca agttctcttt ctttcttttt 13680
ctttctttct ctttctttct ttcttt 13706
<210> 42
<211> 1134
<212> DNA
<213> 人工序列
<220>
<223> 合成多核苷酸
<400> 42
ccagctggag ccctgagtgg ctgagctcag gccttcgcag cattcttggg tgggagcagc 60
cacgggtcag ccacaagggc cacagccatg aatggcacag aaggccctaa cttctacgtg 120
cccttctcca atgcgacggg tgtggtacgc agccccttcg agtacccaca gtactacctg 180
gctgagccat ggcagttctc catgctggcc gcctacatgt ttctgctgat cgtgctgggc 240
ttccccatca acttcctcac gctctacgtc accgtccagc acaagaagct gcgcacgcct 300
ctcaactaca tcctgctcaa cctagccgtg gctgacctct tcatggtcct aggtggcttc 360
accagcaccc tctacacctc tctgcatgga tacttcgtct tcgggcccac aggatgcaat 420
ttggagggct tctttgccac cctgggcggt gaaattgccc tgtggtcctt ggtggtcctg 480
gccatcgagc ggtacgtggt ggtgtgtaag cccatgagca acttccgctt cggggagaac 540
catgccatca tgggcgttgc cttcacctgg gtcatggcgc tggcctgcgc cgcaccccca 600
ctcgccggct ggtccaggta catccccgag ggcctgcagt gctcgtgtgg aatcgactac 660
tacacgctca agccggaggt caacaacgag tcttttgtca tctacatgtt cgtggtccac 720
ttcaccatcc ccatgattat catctttttc tgctatgggc agctcgtctt caccgtcaag 780
gaggccgctg cccagcagca ggagtcagcc accacacaga aggcagagaa ggaggtcacc 840
cgcatggtca tcatcatggt catcgctttc ctgatctgct gggtgcccta cgccagcgtg 900
gctttttata tattcaccca ccagggctcc aacttcggtc ccatcttcat gaccatccca 960
gcgttctttg ccaagagcgc cgccatctac aaccctgtca tctatatcat gatgaacaag 1020
cagttccgga actgcatgct caccaccatc tgctgcggca agaacccact gggtgacgat 1080
gaggcctctg ctaccgtgtc caagacggag acgagccagg tggccccggc ctaa 1134
Claims (31)
1.合成核糖核酸(RNA)分子,其包含:
序列GUGGCAUUCUACAUCUUCA(SEQ ID NO:7)的有义链和序列UGAAGAUGUAGAAUGCCAC(SEQID NO:8)的反义链。
2.权利要求1所述的合成RNA分子,其中所述RNA是小干扰RNA(siRNA)。
3.权利要求1所述的合成RNA分子,其中所述RNA是小发夹RNA(shRNA)。
4.权利要求3所述的shRNA,其具有包含序列UCAAGAG(SEQ ID NO:9)的RNA或序列UGUGCUU(SEQ ID NO:10)的RNA的环。
5.权利要求1所述的合成RNA分子,其中所述RNA是人工微RNA(miRNA)。
6.权利要求5所述的人工miRNA,其中所述人工miRNA包含序列UGCUGUUGACAGUGAGCGA(X)nUAGUGAAGCCACAGAUGUA(Y)nCUGCCUACUGCCUCGGA(SEQ ID NO:19)的RNA,并且其中:
(X)n包含SEQ ID NO:7且(Y)n包含SEQ ID NO:8。
7.权利要求1至6中任一项所述的合成RNA,其还在5′和/或3′端包含未配对的突出端序列。
8.权利要求7所述的合成RNA,其中所述未配对的突出端序列包含重复碱基的序列。
9.权利要求8所述的合成RNA,其中所述重复碱基的序列包含重复尿嘧啶(U)碱基。
10.权利要求9所述的合成RNA,其中所述未配对的突出端序列是UU。
11.组合物,其包含权利要求1至10中任一项所述的合成RNA。
12.权利要求11所述的组合物,其还包含一种或更多种生理学上可接受的载体和/或一种或更多种生理学上可接受的辅料。
13.载体,其编码:
a)权利要求3或4所述的shRNA;或者
b)权利要求5或6所述的人工miRNA。
14.权利要求13所述的载体,其中所述shRNA选自SEQ ID NO:11至18中的任一种。
15.权利要求13至14中任一项所述的载体,其中所述载体是表达质粒。
16.权利要求13至14中任一项所述的载体,其中所述载体是病毒载体。
17.权利要求16所述的病毒载体,其中所述病毒载体包含腺相关病毒载体。
18.权利要求11至12所述的组合物或权利要求13至17所述的载体用于制备用于在对象中降低RHO表达的药物的用途。
19.a)权利要求11至12所述的组合物或权利要求13至17所述的载体;以及
b)重组RHO基因,其不包含被a)的所述组合物或所述载体的干扰RNA靶向的序列,
用于制备用于在对象中治疗视网膜色素变性(RP)的药物的用途。
20.权利要求19所述的用途,其中所述重组RHO基因使用rAAV递送。
21.权利要求20所述的用途,其中所述干扰RNA和所述重组RHO基因使用同一rAAV递送。
22.权利要求21所述的用途,其中所述干扰RNA和所述重组RHO基因二者在单启动子序列的表达控制之下。
23.权利要求22所述的用途,其中所述干扰RNA和所述重组RHO基因各自在独立启动子序列的表达控制之下。
24.权利要求23所述的用途,其中所述干扰RNA是shRNA,并且其中所述shRNA在RNA聚合酶III启动子的表达控制之下。
25.权利要求23所述的用途,其中所述干扰RNA是人工miRNA,并且其中所述人工miRNA在RNA聚合酶II启动子的表达控制之下。
26.权利要求24或25所述的用途,其中所述重组RHO基因在组成型或诱导型启动子的表达控制之下。
27.权利要求19至25中任一项所述的用途,其中所述对象是哺乳动物。
28.权利要求27所述的用途,其中所述哺乳动物是啮齿动物或狗。
29.权利要求27所述的用途,其中所述哺乳动物是人。
30.权利要求19至25中任一项所述的用途,其中所述重组RHO基因包含SEQ ID NO:42的核酸序列的第88-1134位核菅酸。
31.权利要求19-25中任一项所述的用途,其中所述重组RHO基因包含SEQ ID NO:42。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202210934990.0A CN115896106A (zh) | 2016-03-01 | 2017-03-01 | 用于治疗显性视网膜色素变性的aav载体 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662302122P | 2016-03-01 | 2016-03-01 | |
| US62/302,122 | 2016-03-01 | ||
| US201662398451P | 2016-09-22 | 2016-09-22 | |
| US62/398,451 | 2016-09-22 | ||
| PCT/US2017/020289 WO2017151823A1 (en) | 2016-03-01 | 2017-03-01 | Aav vectors for treatment of dominant retinitis pigmentosa |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202210934990.0A Division CN115896106A (zh) | 2016-03-01 | 2017-03-01 | 用于治疗显性视网膜色素变性的aav载体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109154002A CN109154002A (zh) | 2019-01-04 |
| CN109154002B true CN109154002B (zh) | 2022-08-30 |
Family
ID=59743213
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202210934990.0A Pending CN115896106A (zh) | 2016-03-01 | 2017-03-01 | 用于治疗显性视网膜色素变性的aav载体 |
| CN201780014309.8A Active CN109154002B (zh) | 2016-03-01 | 2017-03-01 | 用于治疗显性视网膜色素变性的aav载体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202210934990.0A Pending CN115896106A (zh) | 2016-03-01 | 2017-03-01 | 用于治疗显性视网膜色素变性的aav载体 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US11118185B2 (zh) |
| EP (2) | EP4119668A1 (zh) |
| JP (2) | JP7272795B2 (zh) |
| CN (2) | CN115896106A (zh) |
| AU (2) | AU2017227776C1 (zh) |
| CA (1) | CA3014671A1 (zh) |
| ES (1) | ES2923877T3 (zh) |
| IL (2) | IL302455A (zh) |
| WO (1) | WO2017151823A1 (zh) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4119668A1 (en) | 2016-03-01 | 2023-01-18 | University of Florida Research Foundation, Inc. | Aav vectors for treatment of dominant retinitis pigmentosa |
| JP7385282B2 (ja) * | 2017-11-07 | 2023-11-22 | ザ・ユニヴァーシティ・オヴ・ノース・キャロライナ・アト・チャペル・ヒル | 環状rna分子のための方法及び組成物 |
| WO2019222354A1 (en) * | 2018-05-15 | 2019-11-21 | University Of Washington | Compositions and methods for reducing spliceopathy and treating rna dominance disorders |
| EP3802836A4 (en) * | 2018-06-01 | 2022-10-19 | University of Florida Research Foundation, Incorporated | COMPOSITIONS AND METHODS FOR THE TREATMENT OF DOMINANT RETINITIS PIGMENTOSA |
| GB201817469D0 (en) * | 2018-10-26 | 2018-12-12 | Univ Oxford Innovation Ltd | Gene therapy for retinal disease |
| CN111518813B (zh) * | 2019-02-03 | 2023-04-28 | 武汉纽福斯生物科技有限公司 | 视紫红质的编码序列、其表达载体构建及其应用 |
| CN113038971B (zh) * | 2020-04-21 | 2022-06-24 | 北京中因科技有限公司 | RHO-adRP基于基因编辑的方法和组合物 |
| CN111926044B (zh) * | 2020-10-12 | 2021-01-22 | 北京大学第三医院(北京大学第三临床医学院) | 结合突变rho基因的核酸分子和试剂盒 |
| AU2022214429A1 (en) | 2021-02-01 | 2023-09-14 | Regenxbio Inc. | Gene therapy for neuronal ceroid lipofuscinoses |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009035792A1 (en) * | 2007-08-03 | 2009-03-19 | Melba Ketchum | Compositions, methods and systems for the simultaneous determination of parentage, identity, sex, genotype and/or phenotype and breed determination in animals |
| WO2015143418A2 (en) * | 2014-03-21 | 2015-09-24 | Genzyme Corporation | Gene therapy for retinitis pigmentosa |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5795587A (en) | 1995-01-23 | 1998-08-18 | University Of Pittsburgh | Stable lipid-comprising drug delivery complexes and methods for their production |
| GB9606961D0 (en) | 1996-04-02 | 1996-06-05 | Farrar Gwyneth J | Genetic strategy III |
| US20040234999A1 (en) | 1996-04-02 | 2004-11-25 | Farrar Gwenyth Jane | Genetic suppression and replacement |
| US8551970B2 (en) | 1996-04-02 | 2013-10-08 | Optigen Patents Limited | Genetic suppression and replacement |
| US20070015238A1 (en) | 2002-06-05 | 2007-01-18 | Snyder Richard O | Production of pseudotyped recombinant AAV virions |
| WO2004094606A2 (en) * | 2003-04-18 | 2004-11-04 | The Trustees Of The University Of Pennsylvania | COMPOSITIONS AND METHODS FOR siRNA INHIBITION OF ANGIOPOIETIN 1 AND 2 AND THEIR RECEPTOR TIE2 |
| US20070009899A1 (en) | 2003-10-02 | 2007-01-11 | Mounts William M | Nucleic acid arrays for detecting gene expression in animal models of inflammatory diseases |
| WO2005090572A2 (en) | 2004-03-24 | 2005-09-29 | Oncotherapy Science, Inc. | Compositions and methods for treating pancreatic cancer |
| US20080221057A1 (en) | 2007-02-16 | 2008-09-11 | Wyeth | Secreted protein ccdc80 regulates adipocyte differentiation |
| US20120322861A1 (en) | 2007-02-23 | 2012-12-20 | Barry John Byrne | Compositions and Methods for Treating Diseases |
| ES2907452T3 (es) * | 2007-04-12 | 2022-04-25 | The Provost Fellows Found Scholars & The Other Members Of Board Of The College Of The Holy & Undiv T | Supresión y reemplazo genético |
| WO2010127209A2 (en) | 2009-04-30 | 2010-11-04 | The Research Foundation Of State University Of New York | Compositions and methods for therapy of macular degeneration |
| US8968746B2 (en) | 2010-07-30 | 2015-03-03 | Curevac Gmbh | Complexation of nucleic acids with disulfide-crosslinked cationic components for transfection and immunostimulation |
| CN102061308B (zh) | 2010-10-29 | 2013-05-08 | 北京未名凯拓作物设计中心有限公司 | 一种用百草枯筛选转基因植物的方法 |
| CN102061305B (zh) * | 2010-12-15 | 2012-07-18 | 深圳市百恩维生物科技有限公司 | 一种多ShRNA高效协同沉默基因方法及载体 |
| US20130064815A1 (en) * | 2011-09-12 | 2013-03-14 | The Trustees Of Princeton University | Inducing apoptosis in quiescent cells |
| WO2013175446A1 (en) * | 2012-05-25 | 2013-11-28 | Commissariat A L'energie Atomique Et Aux Energies Alternatives | Vector for the selective silencing of a gene in astrocytes |
| WO2014138792A1 (en) | 2013-03-14 | 2014-09-18 | Commonwealth Scientific And Industrial Research Organisation | Double-stranded rna |
| US10426789B2 (en) | 2015-02-26 | 2019-10-01 | Ionis Pharmaceuticals, Inc. | Allele specific modulators of P23H rhodopsin |
| WO2016176690A2 (en) | 2015-04-30 | 2016-11-03 | The Trustees Of Columbia University In The City Of New York | Gene therapy for autosomal dominant diseases |
| US11096955B2 (en) | 2016-02-09 | 2021-08-24 | Fondazione Telethon | Synthetic promoters and uses thereof |
| US20170348387A1 (en) | 2016-02-29 | 2017-12-07 | The Trustees Of The University Of Pennsylvania | Aav-mediated gene therapy for nphp5 lca-ciliopathy |
| EP4119668A1 (en) | 2016-03-01 | 2023-01-18 | University of Florida Research Foundation, Inc. | Aav vectors for treatment of dominant retinitis pigmentosa |
-
2017
- 2017-03-01 EP EP22170988.4A patent/EP4119668A1/en active Pending
- 2017-03-01 JP JP2018545818A patent/JP7272795B2/ja active Active
- 2017-03-01 ES ES17760752T patent/ES2923877T3/es active Active
- 2017-03-01 US US16/081,307 patent/US11118185B2/en active Active
- 2017-03-01 CN CN202210934990.0A patent/CN115896106A/zh active Pending
- 2017-03-01 CA CA3014671A patent/CA3014671A1/en active Pending
- 2017-03-01 CN CN201780014309.8A patent/CN109154002B/zh active Active
- 2017-03-01 AU AU2017227776A patent/AU2017227776C1/en active Active
- 2017-03-01 EP EP17760752.0A patent/EP3423582B1/en active Active
- 2017-03-01 WO PCT/US2017/020289 patent/WO2017151823A1/en active Application Filing
- 2017-03-01 IL IL302455A patent/IL302455A/en unknown
- 2017-03-01 IL IL261014A patent/IL261014B2/en unknown
-
2021
- 2021-05-21 US US17/327,609 patent/US20210324387A1/en active Pending
-
2022
- 2022-09-29 JP JP2022156496A patent/JP2022185052A/ja active Pending
-
2023
- 2023-09-27 AU AU2023237106A patent/AU2023237106A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009035792A1 (en) * | 2007-08-03 | 2009-03-19 | Melba Ketchum | Compositions, methods and systems for the simultaneous determination of parentage, identity, sex, genotype and/or phenotype and breed determination in animals |
| WO2015143418A2 (en) * | 2014-03-21 | 2015-09-24 | Genzyme Corporation | Gene therapy for retinitis pigmentosa |
Non-Patent Citations (2)
| Title |
|---|
| A CHOP-regulated microRNA controls rhodopsin expression;Shannon Behrman等;《J Cell Biol.》;20110321;第192卷(第6期);919-927 * |
| 视紫红质基因突变相关的视网膜色素变性;江海波等;《国际眼科纵览》;20141222;第38卷(第6期);391-394 * |
Also Published As
| Publication number | Publication date |
|---|---|
| IL261014A (en) | 2018-10-31 |
| AU2023237106A1 (en) | 2023-10-19 |
| IL261014B2 (en) | 2023-10-01 |
| EP3423582A4 (en) | 2019-11-13 |
| JP2019511216A (ja) | 2019-04-25 |
| AU2017227776A1 (en) | 2018-08-23 |
| CN109154002A (zh) | 2019-01-04 |
| IL261014B1 (en) | 2023-06-01 |
| EP3423582A1 (en) | 2019-01-09 |
| AU2017227776C1 (en) | 2024-01-25 |
| EP3423582B1 (en) | 2022-05-04 |
| JP2022185052A (ja) | 2022-12-13 |
| JP7272795B2 (ja) | 2023-05-12 |
| ES2923877T3 (es) | 2022-10-03 |
| AU2017227776B2 (en) | 2023-07-06 |
| CN115896106A (zh) | 2023-04-04 |
| US20210324387A1 (en) | 2021-10-21 |
| WO2017151823A1 (en) | 2017-09-08 |
| US11118185B2 (en) | 2021-09-14 |
| US20190093111A1 (en) | 2019-03-28 |
| CA3014671A1 (en) | 2017-09-08 |
| EP4119668A1 (en) | 2023-01-18 |
| IL302455A (en) | 2023-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109154002B (zh) | 用于治疗显性视网膜色素变性的aav载体 | |
| KR102373765B1 (ko) | 벡터 제조 및 유전자 전달을 위한 캡시드-결핍 aav 벡터, 조성물 및 방법 | |
| ES2856403T3 (es) | Composiciones a base de rAAV y procedimientos para el tratamiento de la esclerosis lateral amiotrofica | |
| JP7428664B2 (ja) | 合成肝臓指向性アデノ随伴ウイルスカプシドおよびその使用 | |
| JP7303816B2 (ja) | Aavベクター | |
| JP2023011865A (ja) | MeCP2発現カセット | |
| US20210371480A1 (en) | Compositions and methods for treating age-related macular degeneration and other diseases | |
| TW202003052A (zh) | 用於治療黃斑部失養症之組成物及方法 | |
| KR20230117731A (ko) | 청력 상실의 치료를 위한 변이체 아데노-연관된 바이러스(aav) 캡시드 폴리펩티드 및 이의 유전자 치료제 | |
| JP2021510301A (ja) | 網膜障害を治療するための組成物及び方法 | |
| JP2024531138A (ja) | 筋ジストロフィーを処置するための組成物および方法 | |
| CN114127296B (zh) | Ube3a基因和表达盒及其应用 | |
| RU2816963C2 (ru) | МОДИФИЦИРОВАННАЯ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК), СОДЕРЖАЩАЯ СИММЕТРИЧНЫЕ МОДИФИЦИРОВАННЫЕ ИНВЕРТИРОВАННЫЕ КОНЦЕВЫЕ ПОВТОРЫ | |
| CN118401667A (zh) | 用于治疗cdkl5缺乏症(cdd)的组合物 | |
| WO2023178311A1 (en) | Methods for treating disorders under hypothermia and compositions relating to the same | |
| JP2024515612A (ja) | 球脊髄性筋萎縮症(sbma)の治療に有用な組成物 | |
| WO2023034966A1 (en) | Compositions and methods of using the same for treating disorders associated with thymosin βeta 4 | |
| NZ713958A (en) | Promoters, expression cassettes, vectors, kits, and methods for the treatment of achromatopsia and other diseases | |
| NZ753155B2 (en) | Promoters, expression cassettes, vectors, kits, and methods for the treatment of achromatopsia and other diseases | |
| NZ713958B2 (en) | Promoters, expression cassettes, vectors, kits, and methods for the treatment of achromatopsia and other diseases | |
| NZ612375B2 (en) | Promoters, expression cassettes, vectors, kits, and methods for the treatment of achromatopsia and other diseases |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |