CN108601774B - 用于治疗rsv的组合产品 - Google Patents
用于治疗rsv的组合产品 Download PDFInfo
- Publication number
- CN108601774B CN108601774B CN201780009640.0A CN201780009640A CN108601774B CN 108601774 B CN108601774 B CN 108601774B CN 201780009640 A CN201780009640 A CN 201780009640A CN 108601774 B CN108601774 B CN 108601774B
- Authority
- CN
- China
- Prior art keywords
- compound
- rsv
- combination
- pharmaceutically acceptable
- compounds
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 claims abstract description 208
- 206010061603 Respiratory syncytial virus infection Diseases 0.000 claims abstract description 25
- 229940126062 Compound A Drugs 0.000 claims abstract description 16
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 claims abstract description 16
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 claims abstract description 12
- 229960000329 ribavirin Drugs 0.000 claims abstract description 12
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 claims abstract description 12
- 150000003839 salts Chemical class 0.000 claims description 42
- 241000725643 Respiratory syncytial virus Species 0.000 claims description 34
- 239000003814 drug Substances 0.000 claims description 20
- 230000002195 synergetic effect Effects 0.000 claims description 14
- 239000008194 pharmaceutical composition Substances 0.000 claims description 13
- 230000000840 anti-viral effect Effects 0.000 claims description 6
- 238000004519 manufacturing process Methods 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 4
- 208000015181 infectious disease Diseases 0.000 claims description 4
- 238000000034 method Methods 0.000 abstract description 18
- 230000002401 inhibitory effect Effects 0.000 abstract description 7
- 239000000825 pharmaceutical preparation Substances 0.000 abstract description 6
- 229940127557 pharmaceutical product Drugs 0.000 abstract description 6
- 230000003993 interaction Effects 0.000 description 37
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 24
- 230000009467 reduction Effects 0.000 description 19
- 230000003612 virological effect Effects 0.000 description 18
- 230000000694 effects Effects 0.000 description 14
- -1 YM-543403 Chemical compound 0.000 description 12
- 238000009097 single-agent therapy Methods 0.000 description 12
- 230000008485 antagonism Effects 0.000 description 11
- 241000700605 Viruses Species 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- 229960000402 palivizumab Drugs 0.000 description 10
- BLUJRJMLDHEMRX-UHFFFAOYSA-N 2-[[2-hydroxy-5-[(5-methyltetrazol-1-yl)iminomethyl]phenyl]-(4-hydroxyphenyl)methyl]-4-[(5-methyltetrazol-1-yl)iminomethyl]phenol Chemical compound Cc1nnnn1N=Cc1ccc(O)c(c1)C(c1ccc(O)cc1)c1cc(C=Nn2nnnc2C)ccc1O BLUJRJMLDHEMRX-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 230000004044 response Effects 0.000 description 9
- 239000002253 acid Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 230000000996 additive effect Effects 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- GOFXWTVKPWJNGD-UWJYYQICSA-N n-[2-[(2s)-2-[5-[(3s)-3-aminopyrrolidin-1-yl]-6-methylpyrazolo[1,5-a]pyrimidin-2-yl]piperidine-1-carbonyl]-4-chlorophenyl]methanesulfonamide Chemical compound CC1=CN2N=C([C@H]3N(CCCC3)C(=O)C=3C(=CC=C(Cl)C=3)NS(C)(=O)=O)C=C2N=C1N1CC[C@H](N)C1 GOFXWTVKPWJNGD-UWJYYQICSA-N 0.000 description 6
- UHHHWFCTIQAQKF-UHFFFAOYSA-N n-cyclopropyl-6-[4-[[2-(2-oxa-7-azaspiro[3.5]nonan-7-yl)pyridine-3-carbonyl]amino]benzoyl]-4,5-dihydrothieno[3,2-d][1]benzazepine-2-carboxamide Chemical compound C=1C=2CCN(C(=O)C=3C=CC(NC(=O)C=4C(=NC=CC=4)N4CCC5(COC5)CC4)=CC=3)C3=CC=CC=C3C=2SC=1C(=O)NC1CC1 UHHHWFCTIQAQKF-UHFFFAOYSA-N 0.000 description 6
- 230000010076 replication Effects 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- MTPVBMVUENFFLL-HXUWFJFHSA-N 1-(2-fluorophenyl)-3-[(3s)-2-oxo-5-phenyl-1,3-dihydro-1,4-benzodiazepin-3-yl]urea Chemical compound FC1=CC=CC=C1NC(=O)N[C@@H]1C(=O)NC2=CC=CC=C2C(C=2C=CC=CC=2)=N1 MTPVBMVUENFFLL-HXUWFJFHSA-N 0.000 description 5
- OPRZZDKUMMSNLY-UHFFFAOYSA-N 4-amino-8-[3-[2-(3,4-dimethoxyphenyl)ethylamino]propyl]-6,6-dimethyl-2-(4-methyl-3-nitrophenyl)-3h-imidazo[4,5-h]isoquinoline-7,9-dione Chemical compound C1=C(OC)C(OC)=CC=C1CCNCCCN1C(=O)C(C)(C)C(C=C(N)C2=C3NC(=N2)C=2C=C(C(C)=CC=2)[N+]([O-])=O)=C3C1=O OPRZZDKUMMSNLY-UHFFFAOYSA-N 0.000 description 5
- VTCJNYICQADBJD-UHFFFAOYSA-N N-(2-fluoro-6-methylphenyl)-6-[4-[[5-methyl-2-(7-oxa-2-azaspiro[3.5]nonan-2-yl)pyridine-3-carbonyl]amino]benzoyl]-4,5-dihydrothieno[3,2-d][1]benzazepine-2-carboxamide Chemical compound FC1=C(C(=CC=C1)C)NC(=O)C1=CC2=C(C3=C(N(CC2)C(C2=CC=C(C=C2)NC(C2=C(N=CC(=C2)C)N2CC4(C2)CCOCC4)=O)=O)C=CC=C3)S1 VTCJNYICQADBJD-UHFFFAOYSA-N 0.000 description 5
- 239000000654 additive Substances 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 230000005764 inhibitory process Effects 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- GTQTUABHRCWVLL-UHFFFAOYSA-N C(CCN1C(=CC2=CC(=CC=C12)Cl)CN1C2=C(N(C1=O)CC(F)(F)F)C=CN=C2)S(=O)(=O)C Chemical compound C(CCN1C(=CC2=CC(=CC=C12)Cl)CN1C2=C(N(C1=O)CC(F)(F)F)C=CN=C2)S(=O)(=O)C GTQTUABHRCWVLL-UHFFFAOYSA-N 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- ZKHQWZAMYRWXGA-KQYNXXCUSA-J ATP(4-) Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)[C@H]1O ZKHQWZAMYRWXGA-KQYNXXCUSA-J 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- ZKHQWZAMYRWXGA-UHFFFAOYSA-N Adenosine triphosphate Natural products C1=NC=2C(N)=NC=NC=2N1C1OC(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)C(O)C1O ZKHQWZAMYRWXGA-UHFFFAOYSA-N 0.000 description 3
- 206010013710 Drug interaction Diseases 0.000 description 3
- 241000711920 Human orthopneumovirus Species 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 230000003042 antagnostic effect Effects 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000006143 cell culture medium Substances 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- 238000003570 cell viability assay Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000007405 data analysis Methods 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- QZSZPSDRJPPZDZ-OAQYLSRUSA-N (9bs)-9b-(4-chlorophenyl)-1-(pyridine-3-carbonyl)-2,3-dihydroimidazo[5,6]pyrrolo[1,2-a]pyridin-5-one Chemical compound C1=CC(Cl)=CC=C1[C@]1(C2=CN=CC=C2C2=O)N2CCN1C(=O)C1=CC=CN=C1 QZSZPSDRJPPZDZ-OAQYLSRUSA-N 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 2
- KSHJXDWYTZJUEI-UHFFFAOYSA-N 1-cyclopropyl-3-[[1-(4-hydroxybutyl)benzimidazol-2-yl]methyl]imidazo[4,5-c]pyridin-2-one Chemical compound N=1C2=CC=CC=C2N(CCCCO)C=1CN(C1=O)C2=CN=CC=C2N1C1CC1 KSHJXDWYTZJUEI-UHFFFAOYSA-N 0.000 description 2
- DKORMNNYNRPTBJ-UHFFFAOYSA-N 2-[[6-[[2-(3-hydroxypropyl)-5-methylanilino]methyl]-2-(3-morpholin-4-ylpropylamino)benzimidazol-1-yl]methyl]-6-methylpyridin-3-ol Chemical compound CC1=CC=C(CCCO)C(NCC=2C=C3N(CC=4C(=CC=C(C)N=4)O)C(NCCCN4CCOCC4)=NC3=CC=2)=C1 DKORMNNYNRPTBJ-UHFFFAOYSA-N 0.000 description 2
- CKCODSNUWCBRIS-UHFFFAOYSA-N 5-[[4,6-bis[3-[bis(3-amino-3-oxo-propyl)sulfamoyl]anilino]-1,3,5-triazin-2-yl]amino]-2-[4-[[4,6-bis[3-[bis(3-amino-3-oxo-propyl)sulfamoyl]anilino]-1,3,5-triazin-2-yl]amino]-2-sulfo-phenyl]benzenesulfonic acid Chemical compound NC(=O)CCN(CCC(N)=O)S(=O)(=O)C1=CC=CC(NC=2N=C(NC=3C=C(C(C=4C(=CC(NC=5N=C(NC=6C=C(C=CC=6)S(=O)(=O)N(CCC(N)=O)CCC(N)=O)N=C(NC=6C=C(C=CC=6)S(=O)(=O)N(CCC(N)=O)CCC(N)=O)N=5)=CC=4)S(O)(=O)=O)=CC=3)S(O)(=O)=O)N=C(NC=3C=C(C=CC=3)S(=O)(=O)N(CCC(N)=O)CCC(N)=O)N=2)=C1 CKCODSNUWCBRIS-UHFFFAOYSA-N 0.000 description 2
- SWWRPROUTDGFFV-UHFFFAOYSA-N CCS(=O)(=O)CCc1c(CN2C(=O)N(C3CC3)c4ccncc24)nc5cc(Cl)ccn15 Chemical compound CCS(=O)(=O)CCc1c(CN2C(=O)N(C3CC3)c4ccncc24)nc5cc(Cl)ccn15 SWWRPROUTDGFFV-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 229920002683 Glycosaminoglycan Polymers 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- ALMZSKFFZDETDT-UHFFFAOYSA-N O=S(=O)(C)CCCN1C2=C(C=C(Cl)C=C2)N=C1CN1C2=C(N(C1=O)C1CC1)C=CN=C2 Chemical compound O=S(=O)(C)CCCN1C2=C(C=C(Cl)C=C2)N=C1CN1C2=C(N(C1=O)C1CC1)C=CN=C2 ALMZSKFFZDETDT-UHFFFAOYSA-N 0.000 description 2
- 241001432884 Orthopneumovirus Species 0.000 description 2
- 241000282320 Panthera leo Species 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- 241000242739 Renilla Species 0.000 description 2
- 108010052090 Renilla Luciferases Proteins 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 231100000135 cytotoxicity Toxicity 0.000 description 2
- 230000003013 cytotoxicity Effects 0.000 description 2
- 230000003111 delayed effect Effects 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 238000004020 luminiscence type Methods 0.000 description 2
- 239000001630 malic acid Substances 0.000 description 2
- 235000011090 malic acid Nutrition 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 239000013643 reference control Substances 0.000 description 2
- 208000030925 respiratory syncytial virus infectious disease Diseases 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 230000019635 sulfation Effects 0.000 description 2
- 238000005670 sulfation reaction Methods 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 238000004448 titration Methods 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 230000029812 viral genome replication Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- UNNCHYARSNZOPF-UHFFFAOYSA-L way-154641 Chemical compound [Na+].[Na+].NC(=O)CN(CC(N)=O)S(=O)(=O)C1=CC=CC(NC=2N=C(NC=3C=C(C(C=4C(=CC(NC=5N=C(NC=6C=C(C=CC=6)S(=O)(=O)N(CC(N)=O)CC(N)=O)N=C(NC=6C=C(C=CC=6)S(=O)(=O)N(CC(N)=O)CC(N)=O)N=5)=CC=4)S([O-])(=O)=O)=CC=3)S([O-])(=O)=O)N=C(NC=3C=C(C=CC=3)S(=O)(=O)N(CC(N)=O)CC(N)=O)N=2)=C1 UNNCHYARSNZOPF-UHFFFAOYSA-L 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- 125000003762 3,4-dimethoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Chemical class 0.000 description 1
- 244000286893 Aspalathus contaminatus Species 0.000 description 1
- 241000711895 Bovine orthopneumovirus Species 0.000 description 1
- 238000003734 CellTiter-Glo Luminescent Cell Viability Assay Methods 0.000 description 1
- 102000002004 Cytochrome P-450 Enzyme System Human genes 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical class CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 101150066002 GFP gene Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229940125776 JNJ-53718678 Drugs 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 208000004852 Lung Injury Diseases 0.000 description 1
- 208000019693 Lung disease Diseases 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Chemical class NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Chemical class 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 241000711904 Pneumoviridae Species 0.000 description 1
- 239000012979 RPMI medium Substances 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 206010069363 Traumatic lung injury Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 206010047924 Wheezing Diseases 0.000 description 1
- OCBFFGCSTGGPSQ-UHFFFAOYSA-N [CH2]CC Chemical compound [CH2]CC OCBFFGCSTGGPSQ-UHFFFAOYSA-N 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000012615 aggregate Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229960004909 aminosalicylic acid Drugs 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Chemical class OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 238000012054 celltiter-glo Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229940000425 combination drug Drugs 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 229940124301 concurrent medication Drugs 0.000 description 1
- 239000000625 cyclamic acid and its Na and Ca salt Substances 0.000 description 1
- HCAJEUSONLESMK-UHFFFAOYSA-N cyclohexylsulfamic acid Chemical compound OS(=O)(=O)NC1CCCCC1 HCAJEUSONLESMK-UHFFFAOYSA-N 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 241001493065 dsRNA viruses Species 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 238000013100 final test Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000007902 hard capsule Substances 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical class C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 229960001438 immunostimulant agent Drugs 0.000 description 1
- 239000003022 immunostimulating agent Substances 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 238000012482 interaction analysis Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 208000030500 lower respiratory tract disease Diseases 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000003670 luciferase enzyme activity assay Methods 0.000 description 1
- 231100000515 lung injury Toxicity 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 201000009240 nasopharyngitis Diseases 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 150000003833 nucleoside derivatives Chemical class 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 235000019371 penicillin G benzathine Nutrition 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 235000012431 wafers Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/52—Purines, e.g. adenine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/7056—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing five-membered rings with nitrogen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/42—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum viral
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1027—Paramyxoviridae, e.g. respiratory syncytial virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Abstract
本发明涉及用于治疗或改善RSV感染的RSV抑制化合物A(3‑({5‑氯‑1‑[3‑(甲基磺酰基)丙基]‑1H‑吲哚‑2‑基}甲基)‑1‑(2,2,2‑三氟乙基)‑1,3‑二氢‑2H‑咪唑并[4,5‑c]吡啶‑2‑酮)和RSV抑制化合物B(利巴韦林)的组合。本发明进一步涉及化合物A和化合物B的组合产品、包含化合物A和化合物B的药用产品、化合物A和化合物B的组合或包含化合物A和化合物B的药用产品用于治疗RSV感染的用途、以及治疗或改善有需要的受试者的RSV感染的方法,该方法包括将化合物A和化合物B的组合以有效量给予所述受试者。
Description
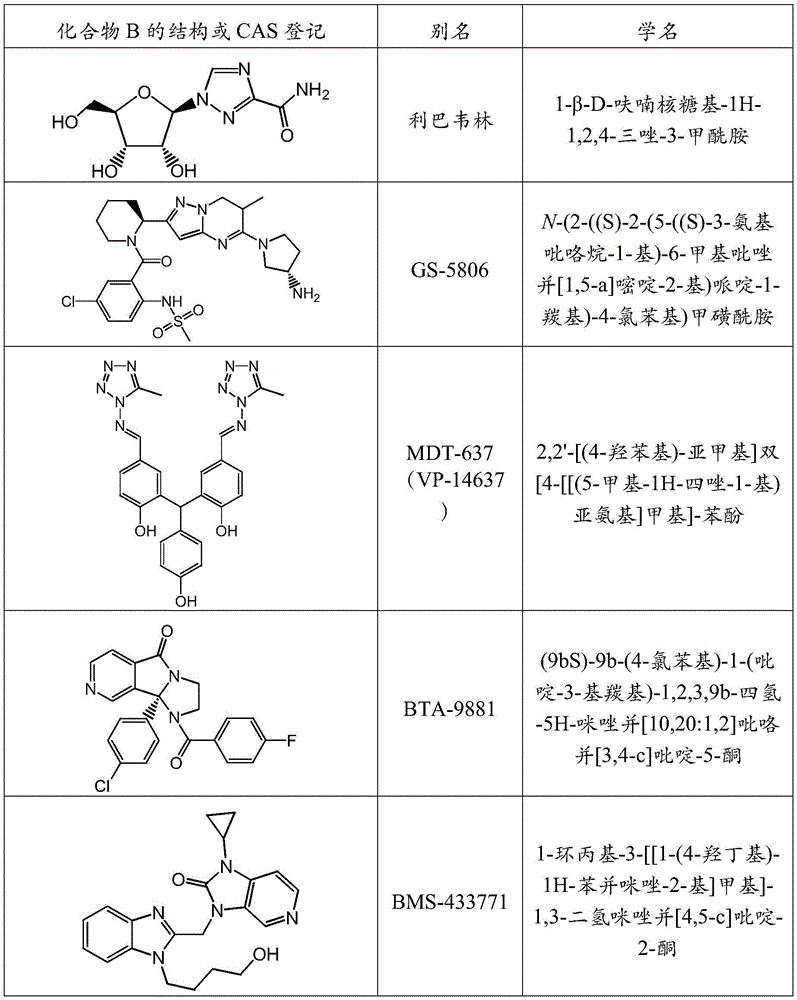
本发明涉及用于治疗或改善RSV感染的RSV抑制化合物A(即,3-({5-氯-1-[3-(甲基磺酰基)丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮)和一种或多种选自以下的RSV抑制化合物B的组合:利巴韦林、GS-5806、MDT-637、BTA-9881、BMS-433771、YM-543403、A-60444、TMC-353121、RFI-641、CL-387626、MBX-300、AZ-27、MEDI8897、CR9501、帕利珠单抗、3-({5-氯-1-[3-(甲基磺酰基)丙基]-1H-苯并咪唑-2-基}甲基)-1-环丙基-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮、3-[[7-氯-3-(2-乙基磺酰基乙基)咪唑并[1,2-a]吡啶-2-基]甲基]-1-环丙基-咪唑并[4,5-c]吡啶-2-酮、N-(2-氟-6-甲基苯基)-6-(4-(5-甲基-2-(7-氧杂-2-氮杂螺[3.5]壬-2-基)烟酰胺基)苯甲酰基)-5,6-二氢-4H-苯并[b]噻吩并[2,3-d]氮杂卓-2-甲酰胺、以及4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮。本发明进一步涉及化合物A和一种或多种化合物B的组合产品、包含化合物A和一种或多种化合物B的药用产品、化合物A和一种或多种化合物B的组合或包含化合物A和一种或多种化合物B的药用产品用于治疗RSV感染的用途、以及治疗或改善有需要的受试者的RSV感染的方法,该方法包括将化合物A和一种或多种化合物B的组合以有效量给予所述受试者。
人RSV或呼吸道合胞病毒是一种大的RNA病毒,连同牛RSV病毒一起是肺病毒科(pneumoviridae)正肺病毒属(Orthopneumovirus)的成员。人RSV是造成全世界所有年龄的人群中一系列呼吸道疾病的原因。它是婴儿期和儿童期下呼吸道疾病的主要原因。超过一半的婴儿在他们出生后第一年遭遇RSV,并且几乎所有婴儿在他们出生后头两年内遭遇RSV。幼儿中的感染可能引起持续多年的肺损伤,并且在以后的生活中可能引起慢性肺疾病(慢性喘息、哮喘)。大龄儿童和成人在RSV感染时经常患有(重)普通感冒。在晚年,易感性再次增加,并且RSV已经牵涉到了老年人中许多肺炎的爆发,导致显著的死亡率。
当今仅有三种药被批准用于对抗RSV感染。第一种是利巴韦林(一种核苷类似物),它提供用于住院儿童严重RSV感染的气溶胶治疗。其他两种药(RSV-IG)和(帕利珠单抗)(多克隆和单克隆抗体免疫刺激剂)旨在以预防性方式使用。两者均很昂贵,并且需要肠胃外给予。用于治疗RSV感染的大量化合物处于临床开发中。那些化合物之一是作为化合物P55在WO-2012/080447中披露的3-({5-氯-1-[3-(甲基磺酰基)-丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮。
现在已经发现,3-({5-氯-1-[3-(甲基磺酰基)-丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮(在下文中被称为化合物A)和一种或多种化合物B的组合提供了治疗RSV感染的改进疗法,其中化合物B具有RSV复制抑制特性。
在此披露的一些实施例涉及化合物A和一种或多种化合物B的组合以及这种组合用于治疗或改善有需要的受试者的RSV感染的用途。
其他实施例涉及包含化合物A和一种或多种化合物B的组合的药用产品以及所述药用产品用于治疗或改善RSV感染的用途。
又其他实施例涉及治疗或改善有需要的受试者的RSV感染的方法,该方法包括将化合物A和一种或多种化合物B的组合以有效量给予所述受试者。
化合物A是作为化合物P55在WO-2012/080447中披露的3-({5-氯-1-[3-(甲基磺酰基)-丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮,其具有以下结构:
一种或多种RSV抑制化合物B单独地选自利巴韦林、GS-5806、MDT-637、BTA-9881、BMS-433771、YM-543403、A-60444、TMC-353121、RFI-641、CL-387626、MBX-300、AZ-27、MEDI8897、CR9501、帕利珠单抗、3-({5-氯-1-[3-(甲基磺酰基)丙基]-1H-苯并咪唑-2-基}甲基)-1-环丙基-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮、3-[[7-氯-3-(2-乙基磺酰基乙基)咪唑并[1,2-a]吡啶-2-基]甲基]-1-环丙基-咪唑并[4,5-c]吡啶-2-酮、N-(2-氟-6-甲基苯基)-6-(4-(5-甲基-2-(7-氧杂-2-氮杂螺[3.5]壬-2-基)烟酰胺基)苯甲酰基)-5,6-二氢-4H-苯并[b]噻吩并[2,3-d]氮杂卓-2-甲酰胺、以及4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮。
每当在下文中使用时,术语化合物A、化合物B、一种或多种化合物B、化合物B或类似的术语意在包括处于其游离碱形式及其药学上可接受的盐形式的化合物A和/或化合物B。
化合物A或化合物B能以药学上可接受的盐形式或以游离(即非盐)形式使用。盐形式可以通过用酸或碱处理游离形式获得。令人感兴趣的是药学上可接受的酸和碱加成盐,其意在包括这些化合物能够形成的治疗活性的无毒酸和碱加成盐形式。可以方便地通过用这种适当的酸来处理游离形式而获得化合物A或化合物B的药学上可接受的酸加成盐。适当的酸包括例如无机酸,如氢卤酸(如氢溴酸或特别是盐酸)、或硫酸、硝酸、磷酸以及类似酸;或有机酸,例如像乙酸、丙酸、羟基乙酸、乳酸、丙酮酸、草酸、丙二酸、琥珀酸、马来酸、富马酸、苹果酸(即,羟基丁二酸)、酒石酸、柠檬酸、甲磺酸、乙磺酸、苯磺酸、对甲苯磺酸、环拉酸、水杨酸、对氨基水杨酸、扑酸以及类似酸。化合物A或化合物B还可以通过用适当的有机或无机碱处理而转化为药学上可接受的金属或胺加成盐形式。适当的碱盐形式包括例如:铵盐、碱金属及碱土金属盐,例如锂、钠或钾盐;或镁或钙盐;有机碱的盐,例如苄星青霉素、N-甲基-D-葡糖胺、海巴明(hydrabamine)盐,以及氨基酸例如像精氨酸、赖氨酸等的盐。术语加成盐形式意在还包括化合物A或化合物B及其盐可以形成的任何溶剂化物。这样的溶剂化物是例如水合物、醇化物(例如乙醇化物)等。
第一组化合物B是其中化合物B选自利巴韦林、GS-5806、MDT-637、A-60444、AZ-27、CR9501、帕利珠单抗、N-(2-氟-6-甲基苯基)-6-(4-(5-甲基-2-(7-氧杂-2-氮杂螺[3.5]壬-2-基)烟酰胺基)苯甲酰基)-5,6-二氢-4H-苯并[b]噻吩并[2,3-d]氮杂卓-2-甲酰胺、以及4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮。
第二组化合物B是其中化合物B选自单克隆抗体MEDI8897、CR9501、和帕利珠单抗;特别地,化合物B是帕利珠单抗。
第三组化合物B是其中化合物B选自利巴韦林、GS-5806、MDT-637、A-60444和AZ-27。
第四组化合物B是其中化合物B选自N-(2-氟-6-甲基苯基)-6-(4-(5-甲基-2-(7-氧杂-2-氮杂螺[3.5]壬-2-基)烟酰胺基)-苯甲酰基)-5,6-二氢-4H-苯并[b]噻吩并[2,3-d]氮杂卓-2-甲酰胺、以及4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮。
在一个实施例中,根据本发明的组合中的化合物A的量和化合物B的量使得获得针对RSV的协同抗病毒效应。
在本发明的组合中,化合物A的每日给予量可以从约10mg至约2500mg、约50mg至约1000mg、或从约50mg至约500mg变化。
在本发明的组合中,一种或多种化合物B的每日给予量可以对于该一种或多种化合物B的总量从约10mg至约2500mg、约50mg至约1000mg、或从约50mg至约500mg变化。
在本段和以下段落中提及的所有量指的是游离形式(即非盐形式)。以上值表示游离形式的等效物,即犹如游离形式将会被给予的数量。如果给予盐,其量需要以盐和游离形式之间的分子量比率的函数来计算。
以上提及的每日剂量对于平均体重约70kg来计算,并且在儿科应用、或者当被具有实质性不同体重的患者使用时的情况下应该重新计算。
剂量可以表示为在一天中以适当时间间隔给予一、二、三或四个或更多个亚剂量。使用的剂量优选地对应于以上提及的化合物A和一种或多种化合物B的每日量、或其亚剂量(如其1/2、1/3、或1/4)。剂型能以相当于在前面段落提及的范围或数量的量以分开的配制品或以组合的配制品含有化合物A和一种或多种化合物B。优选这种组合的配制品。
在每日一次给予化合物A和一种或多种化合物B的情况下,这可以通过给予含有化合物A和一种或多种化合物B的组合的固定剂量组合来完成。可以被给予的剂型在下文描述,口服剂型、特别是口服溶液是优选的。
活性成分可以在药物组合物中分开地或作为组合的药物组合物来配制。在后一情况下,提供了药物组合物,该药物组合物包含治疗有效量的化合物A或其药学上可接受的盐和一种或多种化合物B或其药学上可接受的盐以及药学上可接受的载体。在这种背景下,治疗有效量是在已被感染的受试者中足以稳定或减少RSV感染的量。治疗有效量可以具体地对应于以上提及的每日给予量,或为方便每日多次给予的其亚剂量。
在另一个方面,本发明涉及制备如在此所指定的药物组合物的方法,该方法包括紧密混合药学上可接受的载体与治疗有效量的化合物A或其药学上可接受的盐和有效量的一种或多种化合物B或其药学上可接受的盐。
在此提供的组合还可以被配制为组合制剂而用于同时或顺序地在RSV疗法中使用。在这样一种情形下,化合物A被配制于含有其他药学上可接受的赋形剂的药物组合物中,并且一种或多种化合物B被分开地配制于含有其他药学上可接受的赋形剂的药物组合物中。便利地,这些分开的药物组合物可以是同时或顺序使用的试剂盒的一部分。
本发明的组合的单独成分可以在治疗过程中同时地给予或在不同的时间分开地给予或以分散的或单一的组合形式并行给予。
因此,单独地或组合地,化合物A和一种或多种化合物B可以被配制成适合于给予目的的各种药物组合物。在这些中,将治疗有效量的具体化合物A和B中的每一种与药学上可接受的载体组合,根据所希望给予的制剂形式,该载体可以采取多种形式。药物组合物可以被制备为经口、肠胃外(包括皮下、肌内和静脉内)、经直肠、经颊或经鼻给予的药剂。适合于口服给予的组合物包括粉剂、颗粒剂、聚集体、片剂、经压缩的或包衣的丸剂、糖衣丸、药囊、硬或明胶胶囊、糖浆剂以及悬浮液。适合于肠胃外给予的组合物包括水性或非水溶液或乳液,而对于直肠给予来说,适合于给予的组合物包括具有亲水或疏水媒介物的栓剂。对于经鼻递送,可以使用适合的气溶胶递送系统。
例如,在制备用于口服给予的组合物中,可以使用任何常见药物介质,在口服液体组合物(如悬浮液、糖浆剂、酏剂、乳液以及溶液)的情况下,例如像水、二醇类、油类、醇类等;或在固体组合物的情况下,固体载体如淀粉、糖、髙岭土、润滑剂、粘合剂、崩解剂等。对于肠胃外组合物来说,载体通常将包括至少呈大部分的无菌水,但也可以向其中添加其他成分,如增溶剂、乳化剂或另外的助剂。可以制备可注射溶液,其中载体包括生理盐水溶液、葡萄糖溶液或两者的混合物。也可以制备可注射悬浮液,在这种情况下可以采用适当的液体载体、助悬剂等。还包括预期在使用之前不久将其转化为液体形式制剂的固体形式制剂,如用于重构的粉剂。
药物组合物可以方便地以单位剂型呈现以便给予和使剂量均一。实例包括片剂(包括刻痕片剂或包衣片剂)、胶囊剂、丸剂、栓剂、粉剂包、糯米纸囊剂(wafer)、可注射溶液或混悬液等,及其分离多倍剂。
如在此所指定的化合物A和一种或多种化合物B的组合在被RSV感染的温血动物、特别是人的治疗中是有用的。
本发明还涉及用于治疗或改善有需要的受试者的RSV感染的方法,该方法包括将化合物A和一种或多种化合物B、或前述任一项的药学上可接受的盐的组合以治疗有效量给予所述受试者。化合物A的量可以在从5mg/kg至50mg/kg的范围,并且化合物B的量可以在从5mg/kg至50mg/kg的范围。
在一个实施例中,本发明进一步涉及用于治疗或改善有需要的受试者的RSV感染的方法,该方法包括给予化合物A和一种或多种化合物B、或前述任一项的药学上可接受的盐的组合,其中化合物A的量和化合物B的量使得获得针对RSV的协同抗病毒效应。
其他实施例涉及用于治疗或改善RSV感染的方法,该方法包括使被RSV病毒感染的细胞与有效量的化合物A和一种或多种化合物B、或前述任一项的药学上可接受的盐的组合接触。
如在此使用的,术语“治疗(treat/treating/treatment)”、“治疗的”和“疗法”不一定意指疾病或病情的完全治愈或消失。病毒载量的任何减少或疾病或病情的任何不希望的体征或症状的缓解到任何程度可以被认为是治疗和/或疗法。
术语“治疗有效量”和“有效量”用来表示引起所指出的生物或药物响应的活性化合物、或药物试剂的量。例如,化合物的治疗有效量可以是预防、缓解或改善疾病的症状,减少病毒载量,或延长所治疗的受试者的存活所需要的量。这一响应可以出现在组织、系统、动物或人中,并且包括病毒载量的减少、所治疗的疾病的体征或症状的缓解。鉴于在此提供的披露,有效量的确定完全处于本领域技术人员的能力之内。作为剂量所需的在此披露的化合物的治疗有效量将取决于给予途径、包括人在内的所治疗的动物类型、以及所考虑的特定动物的物理特征。可以定制剂量以实现希望的效果,但是将取决于医药领域的技术人员将认识到的像重量、饮食、同时用药以及其他因素等这些因素。
用于确定治疗呼吸道合胞病毒(RSV)感染的方法的有效性的各种指示物是本领域技术人员已知的。合适的指示物的实例包括但不限于病毒载量的减少、病毒复制的减少、血清转化时间的减少(患者血清中不可检测的病毒)、临床结果中发病率或死亡率的降低、和/或疾病响应的其他指示物。
在一些实施例中,化合物A和一种或多种化合物B、或前述项的药学上可接受的盐的组合可以将病毒滴度降低到不可检测的水平,例如小于1.7log10噬斑形成单位当量(PFUe)/mL、或小于0.3log10噬斑形成单位当量(PFUe)/mL。在一些实施例中,在此描述的化合物的组合可以与给予该组合之前的病毒载量相比减少病毒载量(例如,在接受初始剂量的该组合后60小时)。在一些实施例中,在此描述的化合物的组合可以将病毒载量减少至低于1.7log10(PFUe)/mL、或低于0.3log10(PFUe)/mL。在一些实施例中,在此描述的化合物的组合可以实现与给予该组合之前的病毒载量相比在约1.5-log至约2.5-log减少、约3-log至约4-log减少、或大于约5-log减少范围内的在受试者血清中的病毒滴度的减少。例如,在给予该组合之前、以及在接受初始剂量的该组合后若干小时(例如,在接受初始剂量的该组合后60小时)测量病毒载量。
在一些实施例中,化合物A和一种或多种化合物B、或前述项的药学上可接受的盐的组合可以产生相对于受试者中预处理水平的至少1、2、3、4、5、10、15、20、25、50、75、100倍或更多的RSV复制的减少,如在接受初始剂量的该组合后若干小时(例如,在接受初始剂量的该组合后60小时)所测定的。在一些实施例中,如在此描述的组合可以产生相对于预处理水平的在约2至约5倍、约10至约20倍、约15至约40倍、或约50至约100倍范围内的RSV复制的减少。在一些实施例中,如在此描述的组合可以产生与通过使用作为单一疗法给予的一种抗-RSV试剂实现的RSV复制的减少相比在1log至1.5log、1.5log至2log、2log至2.5log、2.5log至3log、3log至3.5log或3.5log至4log多的RSV复制的减少的范围内的RSV复制的减少,或者可以在一段更短的时间内实现相同的减少。
在一段时间后,感染性病原体可以显露出对一种或多种治疗剂的耐受性。如在此使用的术语“耐受性”是指病毒株显示出对于一种或多种治疗剂延迟的、减弱的响应和/或没有响应。例如,在用抗病毒剂治疗之后,被耐受的病毒感染的受试者的病毒载量可以减少至与由被非耐受的株感染的受试者所表现出的病毒载量减少的量相比更少的程度。在一些实施例中,可以将化合物A和一种或多种化合物B、或前述项的药学上可接受的盐的组合给予被RSV感染的受试者,RSV对于一种或多种不同的抗RSV剂(例如,利巴韦林)是耐受的。在一些实施例中,与耐受作为单一疗法给予的其他抗RSV剂的RSV株的发展相比,当用在此描述的化合物的组合治疗受试者时,耐受的RSV株的发展可能延迟。
在一些实施例中,与经历用一种抗RSV剂治疗的并发症的受试者的百分比相比,化合物A和一种或多种化合物B、或前述项的药学上可接受的盐的组合可以降低经历来自RSV病毒感染的并发症的受试者的百分比。例如,与仅用作为单一疗法给予的一种抗RSV剂治疗的受试者相比,经历并发症的用在此描述的化合物的组合治疗的受试者的百分比可以少5%、10%、25%、40%、50%、60%、70%、80%和90%。
利用化合物A和一种或多种化合物B、或前述项的药学上可接受的盐的组合的潜在优势可以是,与当一种或多种化合物(B)或其药学上可接受的盐和/或化合物A或其药学上可接受的盐作为单一疗法给予时实现相同的治疗结果所需的量相比,在治疗RSV感染上有效的化合物A或其药学上可接受的盐和/或一种或多种化合物B或其药学上可接受的盐的所需的量的减少。例如,与作为单一疗法给予时实现相同的病毒载量减少所需的前述化合物的量相比,化合物A或其药学上可接受的盐和/或一种或多种化合物B或其药学上可接受的盐的量可以更少。利用在此描述的组合的另一个潜在优势是使用具有不同作用机理的两种或更多种化合物可以产生与当作为单一疗法给予化合物时对于耐受病毒株的发展的障碍相比更高的障碍。利用在此描述的组合的另外的优势可以包括在该组合的化合物之间很少至没有交叉耐受性;用于消除该组合的化合物的途径不同;在该组合的化合物之间很少至没有重叠毒性;对于细胞色素P450很少至没有显著作用;和/或在该组合的化合物之间很少至没有药物动力学相互作用。
实例
以下实例旨在说明本发明而非对其进行限制。
实例1:RSV测定
将黑色384孔透明底微量滴定板(康宁公司(Corning),阿姆斯特丹,荷兰)经由声滴喷射(acoustic drop ejection)使用回声液体处理器(Labcyte公司,森尼维尔市,加利福尼亚州)进行填装。将200nL的化合物母液(100%DMSO)转移到测定板中。将化合物(A)或其药学上可接受的盐在384孔板中“水平地”连续稀释(1:3)至12个不同浓度,并且将化合物(B)或其药学上可接受的盐在384孔板中“竖直地”连续稀释(1:3)至12个不同浓度。还为作为参比对照物单独使用的每种化合物的滴定留出空间。通过向每个孔里添加10μL的培养基(不含酚红的RPMI培养基,10%FBS-热灭活,0.04%庆大霉素(50mg/mL))来起始测定。所有添加步骤通过使用多支路分液器(赛默科技公司(Thermo Scientific),埃伦博德海姆(Erembodegem),比利时)来完成。接下来,将在培养基中稀释的rgRSV224病毒(MOI=1)加入这些板中。rgRSV224病毒是一种工程病毒,其包括另外的GFP基因(Hallak LK,SpillmannD,Collins PL,Peeples ME.Glycosaminoglycan sulfation requirements forrespiratory syncytial virus infection[呼吸道合胞病毒感染的糖胺聚糖硫酸化要求];Journal of virology[病毒学杂志](2000),74(22),10508-13)并且是从NIH(贝塞斯达,马里兰州,美国)得到授权。最后,将20μL的海拉(Hela)细胞悬浮液(3,000个细胞/孔)进行铺板。每个测试中包括培养基、病毒感染的和假感染的对照。这些孔每体积含有0.05%DMSO。将细胞在5%CO2气氛中在37℃下进行孵育。病毒暴露三天后,通过内部开发的MSM激光显微镜(蒂博泰克公司(Tibotec),贝尔塞,比利时)测量细胞中的GFP表达而对病毒复制进行定量。EC50被定义为针对GFP表达的50%抑制浓度。
细胞活力测定
平行地,将化合物在一组白色384孔微量滴定板(康宁公司)中孵育三天,并且通过根据制造商的说明书使用ATPlite试剂盒(铂金埃尔默公司(PerkinElmer),扎芬特姆(Zaventem),比利时)来测量细胞的ATP含量而确定海拉细胞中的化合物的细胞毒性。CC50被定义为针对细胞毒性的50%浓度。
数据分析
对于抗RSV活性和细胞活力两者,每个实验以N=3进行。从3个实验产生复制子值的平均抑制百分比,并且对于抗RSV活性,联合指数(CI)通过Program CalCuSyn(Biosoft软件(拜柔公司(Biosoft),英国))进行计算:CI=[(D)1/(Dx)1]+[(D)2/(Dx)2]。将组合定义为:CI<1:协同;CI>1:拮抗作用;CI=1:累加。在下表中提供了CI的更详细的范围。
| CI的范围 | 描述 | 符号 |
| <0.1 | 非常强的协同作用 | ++++++ |
| 0.1-0.3 | 强协同作用 | ++++ |
| 0.3-0.7 | 协同作用 | +++ |
| 0.7-0.85 | 中等协同作用 | ++ |
| 0.85-0.90 | 轻微协同作用 | + |
| 0.90-1.10 | 几乎累加 | +/- |
| 1.10-1.20 | 轻微拮抗作用 | - |
| 1.20-1.45 | 中等拮抗作用 | -- |
| 1.45-3.3 | 拮抗作用 | --- |
| 3.3-10 | 强拮抗作用 | ---- |
| >10 | 非常强的拮抗作用 | ---- |
实例2:组合研究-RSV与海肾报告子(Renilla Reporter)
美国佐治亚州亚特兰大的埃默里大学的Martin Moore博士得到了表达海肾荧光素酶的RSV(A2-RL-line19F)。A2-RL-line19F的体外病毒动力学与野生型RSV的病毒动力学相似。宿主细胞HEp-2购买自ATCC(目录号CCL-23),并且在含有L-谷氨酰胺和15mM的HEPES(Mediatech公司,目录号10-092-CM)的DMEM/Ham's F-1250/50lx中培养细胞。进一步用5%(v/v)FBS(Mediatech公司,目录号35-010-CV)和1%(v/v)青霉素/链霉素(Mediatech公司,目录号30-002-CI)补充该培养基。将HEp-2细胞维持在37℃下在潮湿5%CO2气氛中。
药物治疗和病毒给药
为了确定化合物的组合的作用,遵循以下程序。在第一天,在96孔板中每个孔铺上20,000个HEp-2细胞。在第二天,在100%DMSO中溶解测试品至200x所希望的最终测试浓度。随后,将化合物(A)或其药学上可接受的盐在96孔板中“水平地”连续稀释(1:3)至9个不同浓度,并且将化合物(B)或其药学上可接受的盐在96孔板中“竖直地”连续稀释(1:3)至7个不同浓度。然后将连续稀释的200x测试品以1:10稀释到细胞培养基中以得到20x测试品。将5μL等份的20x测试品以方格棋盘方式加入细胞与90μL现有培养基中。还为作为参比对照物单独使用的每种化合物的滴定留出空间。在预孵育测试品12小时后,以0.5的MOl将A2-RL-line19F加入板中,并且在37℃下在5%CO2中进一步培育2天。
抗RSV活性的测定
使用海肾萤光素酶测定系统(普洛麦格公司(Promega),目录号E2820)测量抗RSV复制子活性。如上所述建立测定板。使用Perkin Elmer多标记计数器Victor3V记录发光。
细胞活力测定
使用Promega CellTiter-Glo发光细胞活力测定(目录号G7572)来测量细胞活力。CellTiter-发光细胞活力测定是基于所存在的三磷酸腺苷(ATP)的定量的确定培养基中的活细胞数的均相法,三磷酸腺苷表示代谢活性细胞的存在。以与抗RSV测定相同的形式建立测定板,除了没有将病毒加入细胞活力测定中。将100-μL等份的CellTiter-Glo试剂加入每个孔中,并且在室温下孵育8分钟。使用Perkin Elmer多标记计数器Victor3V记录发光。
数据分析
对于抗RSV活性和细胞活力两者,每个实验以N=5进行。从5个实验产生复制子值的平均抑制百分比,并且对于抗RSV活性,使用两种药物相互作用分析模型对其进行分析:等效线图分析(Isobologram Analysis)和/或Prichard模型(Prichard's Model)。
等效线图分析
药物-药物组合的效应通过Loewe加性模型进行评估,在该模型中使用CalcuSyn(拜柔公司,弗格森,密苏里州)(基于Chou和Talalay的方法的计算机程序)分析实验数据。计算每个实验组合的联合指数(CI)值和等效线图。<1、1、和>1的CI值分别表示协同、累加效应、以及拮抗作用。在协同范畴下,CI<0.1被认为是非常强的协同作用;CI 0.1-0.3被认为是强协同作用;CI 0.3-0.7被认为是协同作用并且CI 0.7-0.85被认为是中等协同作用。用图表表示累加、协同和拮抗药物效应的等效线图分析也用来模拟抗病毒活性的相互作用。在此表示法中,一种药物的有效浓度(EC)值在一条轴上绘制,并且第二种药物的相应的EC值在第二条轴上绘制;假定其效应是累加的,连接这两个点的线表示达到等EC值所需的组合中每种药物的量。
Prichard模型(MacSynergyII)
MacSynergy II软件由M.Prichard博士(密歇根大学)友善提供。此程序允许用Bliss独立性模型三维检查由两种抑制剂的方格棋盘组合产生的所有数据点的药物相互作用。由重复数据测定置信界限。如果95%置信限(CL)不与理论累加表面重叠,那么在两种药物之间的相互作用与累加显著不同。协同或拮抗作用的量(volume)可以测定,并且用图表以三维描绘并且表示在两种药物浓度上的每个变化的协同作用或拮抗作用的相对量。协同和拮抗作用量是基于Bliss独立性模型,其假设两种化合物独立作用于不同目标。在Bliss独立性模型下,一组预期分数响应faAB以faAB=faA+faB-faA·faB计算,其中faA和faB表示化合物A和B分别在dA和dB量下有可能响应的分数,例如抑制%,并且描述了在量(dA+dB)下的化合物A和B的组合的抑制%。如果faAB>faA+faB-faA·faB,那么有Bliss协同;如果faAB<faA+faB-faA·faB,那么有Bliss拮抗作用。95%协同/拮抗作用量是在所观察的抑制与关于在Bliss独立性模型下预测faAB的95%置信限之间的差异的总和。表1示出了Bliss独立性分析的结果的量以及相应的量描述。将MacSynergy II用于数据分析。
表1:MacSynergy II量描述
实例3:RSV测定组合实验
为了评估其针对RSV的组合抗病毒作用,用JNJ-53718678(“化合物A”)和具有不同作用机制的各种化合物(“化合物B”)进行体外组合研究。简言之,将9个浓度的化合物A与6或7个浓度的某种化合物B组合。在各个浓度的化合物A和化合物B单独或组合存在下海拉细胞被编码eGFP的rgRSV224(RSV工程株)感染(Hallak LK,Spillmann D,Collins PL,Peeples ME.Glycosaminoglycan sulfation requirements for respiratory syncytialvirus infection[呼吸道合胞病毒感染的糖胺聚糖硫酸化要求];Journal of virology[病毒学杂志](2000),74(22),10508-13)。
化合物母液是在100%DMSO中5mM,以下是例外:利巴韦林,20mM;A 60444,10mM;CR9501,在PBS中141μM;帕利珠单抗,在PBS中156μM;MDT 637,在甲醇中100μM。首先,将这些化合物以3倍稀释系列在DMSO中连续稀释;CR9501和帕利珠单抗在细胞培养基中并且MDT637在甲醇中连续稀释。将浓度系列在细胞培养基中稀释100倍以获得组合基质。将10μL的这些化合物溶液转移到黑色384孔透明底组织培养处理的板中。接着,加入10μL的海拉细胞悬浮液(150000个细胞/mL)以达到每孔3000个细胞。最后,加入10μL的稀释的病毒母液以达到1的MOI。所有孔的最终DMSO浓度是0.5%DMSO,除了MDT 637实验,在该实验中它是0.25%DMSO+0.25%甲醇。化合物浓度的每个组合以4次重复在3个分开的板上进行测试,产生总计12个重复。将这些板在37℃下在潮湿5%CO2气氛中孵育3天。用PerkinElmer EnVision仪器使用405nm滤器测量GFP信号。
对于统计分析,观察到的GFP信号使用相应板上的病毒对照物(VC)和细胞对照物(CC)进行标准化:响应=(GFP-CC)/(VC-CC),其中CC作为所有空白孔(无病毒)的中值GFP进行计算,并且VC作为所有对照孔(无化合物)的中值GFP进行计算。
使用Harbron的方法(Statistics in Medicine[医学统计学],2010,DOI:10.1002/sim3916)来评估协同。使用Loewe定义,通过以下将两种化合物表征为累加、协同或拮抗:
其中d1和d2表示组合产生效应y的两种化合物的剂量,并且Dy,1和Dy,2表示当作为单一疗法给予时产生相同效应y的两种化合物的剂量。3PL模型(3参数log逻辑模型)用于单一疗法剂量-响应数据,其中将基线响应固定在1处。
遵循Harbron的方法,将以下模型拟合到数据:
“累加”:假设在两种化合物之间没有相互作用
“一致”:假设跨所有剂量组合有恒定的相互作用指数τ
“线性A”:假设相互作用指数线性地依赖于化合物A的log10剂量:τ=τ1+τ2log 10(dA)
“分开的A”:假设相互作用指数τ采用化合物A的每个剂量的分开的值对于化合物B也考虑后两种模型:
“线性B”:假设相互作用指数τ线性性依赖于化合物B的log10剂量:τ=τ1+τ2log10(dB)
“分开的B”:假设相互作用指数τ采用化合物B的每个剂量的分开的值
基于Akaike信息准则(AIC),针对所有测试的组合选择“分开的A”模型。化合物A与各种化合物B的组合的测试结果在下文报告。
组合:化合物A和作为化合物B的pulmocide化合物(N-(2-氟-6-甲基苯基)-6-(4-(5-甲基-2-(7-氧杂-2-氮杂螺[3.5]壬-2-基)烟酰胺基)苯甲酰基)-5,6-二氢-4H-苯并[b]噻吩并[2,3-d]氮杂卓-2-甲酰胺)
表2:与pulmocide化合物组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 0.94 | 0.96 | 0.92 | 0.78 | 0.56 | 0.43 | 0.36 | 0.20 | 0.11 | 0.06 |
| B=0.058 | 0.99 | 0.99 | 0.93 | 0.81 | 0.56 | 0.39 | 0.28 | 0.17 | 0.08 | 0.04 |
| B=0.17 | 0.99 | 0.99 | 0.91 | 0.74 | 0.51 | 0.37 | 0.23 | 0.16 | 0.08 | 0.04 |
| B=0.52 | 1.04 | 0.96 | 0.87 | 0.70 | 0.45 | 0.31 | 0.23 | 0.14 | 0.07 | 0.04 |
| B=1.6 | 0.91 | 0.87 | 0.75 | 0.46 | 0.27 | 0.18 | 0.11 | 0.06 | 0.04 | 0.02 |
| B=4.7 | 0.20 | 0.14 | 0.12 | 0.06 | 0.03 | 0.01 | 0.01 | -0.00 | -0.00 | -0.00 |
| B=14 | 0.02 | 0.01 | -0.00 | -0.01 | -0.01 | -0.01 | -0.02 | -0.01 | -0.01 | -0.01 |
| B=42 | 0.02 | 0.01 | 0.01 | 0.00 | -0.00 | -0.01 | -0.01 | -0.00 | -0.00 | -0.00 |
表3示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。允许协同度随化合物A的剂量改变显示出对于0.57nM以及更高的剂量的显著协同度。总体上,协同度随剂量水平增加而增加,平稳区在约5.1至139nM。
表3:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
| 剂量(nM) | 估值 | 95%CI | |
| τ1 | 0.19 | 1.013 | (0.955,1.075) |
| τ2 | 0.57 | 0.93 | (0.875,0.989) |
| τ3 | 1.7 | 0.636 | (0.601,0.674) |
| τ4 | 5.1 | 0.479 | (0.449,0.51) |
| τ5 | 15 | 0.484 | (0.443,0.528) |
| τ6 | 46 | 0.544 | (0.479,0.618) |
| τ7 | 139 | 0.51 | (0.412,0.632) |
| τ8 | 417 | 0.234 | (0.198,0.277) |
| τ9 | 1250 | 0.073 | (0.06,0.088) |
| τEC50 | 9.79 | 0.481 | (NA,NA) |
组合:化合物A和作为化合物B的帕利珠单抗
表4:与作为化合物B的帕利珠单抗组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.11 | 1.04 | 0.98 | 0.86 | 0.57 | 0.38 | 0.28 | 0.17 | 0.09 | 0.05 |
| B=0.0061 | 1.05 | 0.99 | 0.93 | 0.77 | 0.51 | 0.34 | 0.26 | 0.15 | 0.08 | 0.04 |
| B=0.018 | 1.01 | 0.94 | 0.88 | 0.74 | 0.44 | 0.30 | 0.19 | 0.12 | 0.06 | 0.03 |
| B=0.055 | 0.97 | 0.90 | 0.84 | 0.69 | 0.42 | 0.26 | 0.20 | 0.12 | 0.06 | 0.03 |
| B=0.165 | 1.01 | 0.93 | 0.82 | 0.64 | 0.32 | 0.16 | 0.11 | 0.06 | 0.03 | 0.02 |
| B=0.494 | 0.89 | 0.78 | 0.61 | 0.25 | 0.08 | 0.04 | 0.02 | 0.00 | 0.00 | 0.00 |
| B=1.482 | 0.33 | 0.13 | 0.08 | 0.02 | 0.01 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
| B=4.447 | 0.06 | 0.03 | 0.02 | 0.01 | 0.01 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
表5示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。注意,通过在从合适的单一疗法获得的估值处固定针对化合物B的3PL模型中的斜率来拟合该模型。允许协同度随化合物A的剂量改变显示出对于所考虑的所有剂量水平的显著协同度。总体上,协同度随剂量水平增加而增加,平稳区在约5.1至139nM。
表5:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
| 剂量(nM) | 估值 | 95%CI | |
| τ1 | 0.19 | 0.788 | (0.726,0.855) |
| τ2 | 0.57 | 0.626 | (0.579,0.678) |
| τ3 | 1.7 | 0.386 | (0.357,0.418) |
| τ4 | 5.1 | 0.248 | (0.224,0.273) |
| τ5 | 15 | 0.237 | (0.206,0.273) |
| τ6 | 46 | 0.31 | (0.253,0.38) |
| τ7 | 139 | 0.274 | (0.185,0.407) |
| τ8 | 417 | 0.101 | (0.044,0.232) |
| τ9 | 1250 | 0.036 | (0.018,0.076) |
| τEC50 | 7.6 | 0.245 | (NA,NA) |
组合:化合物A和作为化合物B的AZ-27
表6:与作为化合物B的AZ-27组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 0.99 | 0.98 | 0.96 | 0.89 | 0.71 | 0.45 | 0.25 | 0.17 | 0.07 | 0.04 |
| B=17 | 1.03 | 0.98 | 0.97 | 0.86 | 0.60 | 0.34 | 0.20 | 0.12 | 0.05 | 0.03 |
| B=51 | 1.00 | 0.93 | 0.90 | 0.72 | 0.45 | 0.23 | 0.13 | 0.07 | 0.03 | 0.02 |
| B=154 | 0.53 | 0.43 | 0.38 | 0.22 | 0.10 | 0.05 | 0.03 | 0.02 | 0.01 | 0.01 |
| B=463 | 0.07 | 0.05 | 0.04 | 0.03 | 0.00 | -0.01 | -0.00 | -0.01 | -0.01 | -0.00 |
| B=1389 | 0.01 | 0.00 | 0.00 | -0.01 | -0.01 | -0.01 | -0.00 | -0.00 | -0.00 | -0.00 |
| B=4167 | 0.00 | 0.00 | 0.00 | -0.00 | -0.01 | -0.01 | -0.00 | 0.00 | -0.00 | 0.00 |
表7示出了对于“分开的A”模型的相互作用指数(τ)估值与95%CI。允许协同度随化合物A的剂量改变显示出对于所考虑的所有剂量水平的显著协同度。总体上,协同度随剂量水平增加而增加,平稳区在约5.1至139nM。
表7:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
| 剂量(nM) | 估值 | 95%CI | |
| τ1 | 0.19 | 0.922 | (0.896,0.949) |
| τ2 | 0.57 | 0.894 | (0.867,0.923) |
| τ3 | 1.7 | 0.755 | (0.724,0.788) |
| τ4 | 5.1 | 0.609 | (0.579,0.642) |
| τ5 | 15 | 0.537 | (0.499,0.578) |
| τ6 | 46 | 0.582 | (0.515,0.658) |
| τ7 | 139 | 0.57 | (0.43,0.755) |
| τ8 | 417 | 0.312 | (0.171,0.57) |
| τ9 | 1250 | 0.126 | (0.093,0.17) |
| τEC50 | 11.99 | 0.559 | (NA,NA) |
组合:化合物A和作为化合物B的GS-5806
表8:与作为化合物B的GS-5806组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.06 | 0.99 | 0.93 | 0.83 | 0.47 | 0.30 | 0.21 | 0.11 | 0.06 | 0.03 |
| B=0.051 | 0.99 | 0.96 | 0.91 | 0.71 | 0.44 | 0.23 | 0.17 | 0.09 | 0.05 | 0.03 |
| B=0.15 | 0.98 | 0.91 | 0.87 | 0.68 | 0.39 | 0.22 | 0.17 | 0.08 | 0.05 | 0.02 |
| B=0.46 | 0.83 | 0.82 | 0.74 | 0.50 | 0.32 | 0.21 | 0.13 | 0.08 | 0.04 | 0.01 |
| B=1.4 | 0.36 | 0.39 | 0.27 | 0.21 | 0.18 | 0.17 | 0.13 | 0.08 | 0.04 | 0.01 |
| B=4.2 | 0.19 | 0.13 | 0.09 | 0.07 | 0.06 | 0.08 | 0.12 | 0.08 | 0.04 | 0.02 |
| B=12.5 | 0.06 | 0.05 | 0.06 | 0.03 | 0.03 | 0.04 | 0.04 | 0.04 | 0.04 | 0.03 |
| B=37.5 | 0.05 | 0.03 | 0.03 | 0.03 | 0.03 | 0.02 | 0.02 | 0.03 | 0.04 | 0.03 |
表9示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。允许协同度随化合物A的剂量改变显示出对于0.57至15nM的剂量的显著协同度。注意,在最高浓度下的相互作用指数是不可估计的。
表9:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
| 剂量(nM) | 估值 | 95%CI | |
| τ1 | 0.19 | 1.063 | (0.985,1.148) |
| τ2 | 0.57 | 0.895 | (0.832,0.963) |
| τ3 | 1.7 | 0.728 | (0.678,0.78) |
| τ4 | 5.1 | 0.678 | (0.621,0.74) |
| τ5 | 15 | 0.783 | (0.684,0.897) |
| τ6 | 46 | 1.321 | (1.091,1.598) |
| τ7 | 139 | 0.938 | (0.469,1.878) |
| τ8 | 417 | 0.037 | (0.007,0.204) |
| τ9 | 1250 | 0 | (NA,NA) |
| τEC50 | 5.17 | 0.679 | (NA,NA) |
组合:化合物A和作为化合物B的MDT-637
表10:与作为化合物B的MDT-637组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.01 | 0.98 | 0.97 | 0.85 | 0.43 | 0.26 | 0.16 | 0.06 | 0.02 | -0.00 |
| B=0.038 | 1.01 | 0.98 | 0.90 | 0.76 | 0.41 | 0.22 | 0.11 | 0.04 | 0.01 | -0.01 |
| B=0.12 | 0.99 | 0.95 | 0.89 | 0.72 | 0.39 | 0.17 | 0.09 | 0.03 | -0.00 | -0.02 |
| B=0.35 | 0.95 | 0.93 | 0.86 | 0.65 | 0.36 | 0.15 | 0.09 | 0.04 | -0.01 | -0.01 |
| B=1 | 0.93 | 0.89 | 0.80 | 0.58 | 0.30 | 0.16 | 0.07 | 0.03 | -0.00 | -0.02 |
| B=3.1 | 0.75 | 0.69 | 0.59 | 0.38 | 0.23 | 0.12 | 0.07 | 0.03 | 0.00 | -0.01 |
| B=9.3 | 0.14 | 0.11 | 0.10 | 0.10 | 0.11 | 0.11 | 0.08 | 0.04 | 0.00 | -0.01 |
| B=28 | 0.01 | 0.00 | -0.00 | -0.01 | 0.04 | 0.08 | 0.08 | 0.05 | 0.02 | 0.00 |
注意,对于分离的A模型,在两个最高浓度处的相互作用指数是不可估计的(τ8和τ9),并且这些结果是基于局部最优值。表11示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。允许协同度随化合物A的剂量改变显示出对于0.19至15nM的剂量的显著协同度。
表11:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
组合:化合物A和作为化合物B的4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)-乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮
表12:与作为化合物B的4-氨基-8-[3-[[2-(3,4-二甲氧基苯基)-乙基]氨基]丙基]-6,6-二甲基-2-(4-甲基-3-硝基苯基)-3H-咪唑并[4,5-h]异喹啉-7,9(6H,8H)-二酮组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.02 | 0.99 | 0.96 | 0.83 | 0.50 | 0.31 | 0.19 | 0.10 | 0.06 | 0.04 |
| B=1.9 | 0.99 | 0.96 | 0.89 | 0.74 | 0.47 | 0.24 | 0.16 | 0.09 | 0.05 | 0.01 |
| B=5.7 | 0.97 | 0.94 | 0.85 | 0.73 | 0.43 | 0.24 | 0.13 | 0.08 | 0.04 | 0.02 |
| B=17 | 0.89 | 0.84 | 0.79 | 0.64 | 0.35 | 0.20 | 0.15 | 0.05 | 0.04 | 0.01 |
| B=51 | 0.74 | 0.65 | 0.60 | 0.47 | 0.22 | 0.18 | 0.09 | 0.05 | 0.02 | 0.01 |
| B=154 | 0.38 | 0.38 | 0.34 | 0.22 | 0.11 | 0.05 | 0.03 | 0.02 | 0.01 | 0.01 |
| B=463 | 0.05 | 0.03 | 0.04 | 0.03 | 0.01 | 0.01 | 0.01 | -0.00 | -0.00 | -0.00 |
| B=1389 | 0.01 | 0.01 | 0.00 | 0.00 | -0.00 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
注意,在对应于化合物B的单一疗法数据的第3个板的第1列处有制造误差,并且在分析中忽略这些数据(导致10个而非12个重复)。表13示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。允许协同度随化合物A的剂量改变显示出对于0.57至46nM的浓度的显著协同度。
表13:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
| 剂量(nM) | 估值 | 95%CI | |
| τ1 | 0.19 | 0.954 | (0.878,1.037) |
| τ2 | 0.57 | 0.89 | (0.821,0.964) |
| τ3 | 1.7 | 0.72 | (0.668,0.776) |
| τ4 | 5.1 | 0.49 | (0.449,0.534) |
| τ5 | 15 | 0.512 | (0.453,0.579) |
| τ6 | 46 | 0.682 | (0.57,0.816) |
| τ7 | 139 | 0.762 | (0.548,1.061) |
| τ8 | 417 | 0.847 | (0.454,1.583) |
| τ9 | 1250 | 0.85 | (0.34,2.129) |
| τEC50 | 5.39 | 0.49 | (NA,NA) |
组合:化合物A和作为化合物B的单克隆抗体CR9501
表14:与作为化合物B的CR9501组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.06 | 1.05 | 1.01 | 0.89 | 0.64 | 0.41 | 0.28 | 0.21 | 0.10 | 0.06 |
| B=0.002 | 1.06 | 0.98 | 0.94 | 0.80 | 0.51 | 0.37 | 0.26 | 0.17 | 0.06 | 0.04 |
| B=0.0061 | 0.99 | 0.94 | 0.89 | 0.73 | 0.43 | 0.30 | 0.21 | 0.13 | 0.05 | 0.04 |
| B=0.018 | 0.93 | 0.88 | 0.79 | 0.67 | 0.39 | 0.26 | 0.18 | 0.10 | 0.04 | 0.02 |
| B=0.055 | 0.99 | 0.92 | 0.80 | 0.52 | 0.24 | 0.15 | 0.07 | 0.04 | 0.02 | 0.01 |
| B=0.164 | 0.77 | 0.66 | 0.49 | 0.26 | 0.07 | 0.03 | 0.01 | 0.00 | 0.00 | 0.00 |
| B=0.493 | 0.28 | 0.18 | 0.09 | 0.03 | 0.01 | -0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
| B=1.48 | 0.04 | 0.02 | 0.01 | 0.01 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
表15示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。允许协同度随化合物A的剂量改变显示出对于所有浓度的显著协同度。
表15:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
组合:化合物A和作为化合物B的利巴韦林
表16:与作为化合物B的利巴韦林组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 1.01 | 0.97 | 0.95 | 0.87 | 0.63 | 0.39 | 0.25 | 0.15 | 0.08 | 0.04 |
| B=69 | 1.00 | 0.99 | 0.93 | 0.81 | 0.54 | 0.33 | 0.23 | 0.15 | 0.07 | 0.05 |
| B=206 | 0.98 | 0.95 | 0.85 | 0.77 | 0.51 | 0.34 | 0.23 | 0.14 | 0.07 | 0.04 |
| B=617 | 0.98 | 0.88 | 0.86 | 0.72 | 0.49 | 0.29 | 0.20 | 0.13 | 0.06 | 0.04 |
| B=1852 | 0.97 | 0.91 | 0.83 | 0.69 | 0.46 | 0.22 | 0.16 | 0.11 | 0.05 | 0.03 |
| B=5556 | 0.94 | 0.91 | 0.83 | 0.63 | 0.34 | 0.16 | 0.13 | 0.07 | 0.04 | 0.03 |
| B=16667 | 0.83 | 0.72 | 0.62 | 0.39 | 0.17 | 0.08 | 0.06 | 0.04 | 0.03 | 0.02 |
| B=50000 | 0.13 | 0.12 | 0.09 | 0.05 | 0.02 | 0.01 | 0.02 | 0.02 | 0.01 | 0.01 |
表17示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。注意,将具有固定在0处的下界的2PL模型拟合到化合物B的单一疗法数据。允许协同度随化合物A的剂量改变显示出对于从0.19至139nM的浓度的显著协同度。
表17:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
组合:化合物A和作为化合物B的A-60444
表18:与作为化合物B的A-60444组合的化合物A的标准化数据(跨12个重复的平均值)。
| A=0 | A=0.19 | A=0.57 | A=1.7 | A=5.1 | A=15 | A=46 | A=139 | A=417 | A=1250 | |
| B=0 | 0.97 | 0.96 | 0.95 | 0.83 | 0.55 | 0.38 | 0.28 | 0.14 | 0.07 | 0.04 |
| B=34 | 1.00 | 0.97 | 0.92 | 0.82 | 0.59 | 0.36 | 0.23 | 0.15 | 0.09 | 0.04 |
| B=103 | 1.00 | 0.96 | 0.87 | 0.82 | 0.58 | 0.34 | 0.23 | 0.14 | 0.07 | 0.04 |
| B=309 | 0.96 | 0.93 | 0.88 | 0.75 | 0.52 | 0.30 | 0.22 | 0.16 | 0.07 | 0.04 |
| B=926 | 0.93 | 0.92 | 0.86 | 0.73 | 0.55 | 0.30 | 0.22 | 0.16 | 0.08 | 0.03 |
| B=2778 | 0.93 | 0.92 | 0.83 | 0.71 | 0.52 | 0.27 | 0.17 | 0.12 | 0.07 | 0.03 |
| B=8333 | 0.75 | 0.72 | 0.62 | 0.45 | 0.16 | 0.08 | 0.05 | 0.03 | 0.02 | 0.01 |
| B=25000 | 0.39 | 0.31 | 0.24 | 0.12 | 0.04 | 0.01 | 0.01 | 0.01 | 0.00 | 0.00 |
表19示出了对于“分开的A”模型的相互作用指数(τ)估值与95%置信区间(CI)。注意,将具有固定在0处的下界的2PL模型拟合到化合物B的单一疗法数据。允许协同度随化合物A的剂量改变显示出对于从0.57至139nM的浓度的显著协同度。
表19:对于“分开的A”模型的相互作用指数的估计值与95%CI。在EC50值处的相互作用指数通过tau估值的线性插入来粗略估计。
Claims (8)
1.一种组合药物,包含
作为化合物A的3-({5-氯-1-[3-(甲基磺酰基)-丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮或其药学上可接受的盐,以及
作为化合物B的利巴韦林或其药学上可接受的盐;
用于在治疗呼吸道合胞病毒(RSV)感染中使用,其中化合物A的量和化合物B的量使得获得针对RSV的协同抗病毒效应。
2.一种组合药物,包含
作为化合物A的3-({5-氯-1-[3-(甲基磺酰基)-丙基]-1H-吲哚-2-基}甲基)-1-(2,2,2-三氟乙基)-1,3-二氢-2H-咪唑并[4,5-c]吡啶-2-酮或其药学上可接受的盐,以及
作为化合物B的利巴韦林或其药学上可接受的盐;
用于在改善RSV感染中使用,其中化合物A的量和化合物B的量使得获得针对RSV的协同抗病毒效应。
3.根据权利要求1或2所述的供使用的组合药物,其中化合物A的量范围是从10 mg至2500 mg,并且化合物B的量范围是从10 mg至2500 mg。
4.一种药物组合物,包含如权利要求1至3中任一项所述的组合药物以及药学上可接受的载体。
5.如权利要求1至3中任一项所述的组合药物用于制造用于在治疗RSV感染中使用的药物的用途。
6.如权利要求1至3中任一项所述的组合药物用于制造用于在改善RSV感染中使用的药物的用途。
7.如权利要求4所述的药物组合物用于制造用于在治疗RSV感染中使用的药物的用途。
8.如权利要求4所述的药物组合物用于制造用于在改善RSV感染中使用的药物的用途。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010988991.4A CN112245429A (zh) | 2016-02-03 | 2017-02-02 | 用于治疗rsv的组合产品 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16154035.6 | 2016-02-03 | ||
| EP16154035 | 2016-02-03 | ||
| PCT/EP2017/052201 WO2017134133A1 (en) | 2016-02-03 | 2017-02-02 | Combination products for the treatment of rsv |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202010988991.4A Division CN112245429A (zh) | 2016-02-03 | 2017-02-02 | 用于治疗rsv的组合产品 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108601774A CN108601774A (zh) | 2018-09-28 |
| CN108601774B true CN108601774B (zh) | 2021-09-21 |
Family
ID=55304886
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780009640.0A Active CN108601774B (zh) | 2016-02-03 | 2017-02-02 | 用于治疗rsv的组合产品 |
| CN202010988991.4A Pending CN112245429A (zh) | 2016-02-03 | 2017-02-02 | 用于治疗rsv的组合产品 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202010988991.4A Pending CN112245429A (zh) | 2016-02-03 | 2017-02-02 | 用于治疗rsv的组合产品 |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US10363253B2 (zh) |
| EP (2) | EP3411028B1 (zh) |
| JP (1) | JP7065030B2 (zh) |
| KR (1) | KR20180108598A (zh) |
| CN (2) | CN108601774B (zh) |
| AU (2) | AU2017214246B2 (zh) |
| BR (1) | BR112018014958A2 (zh) |
| CA (1) | CA3006488A1 (zh) |
| CL (3) | CL2018001808A1 (zh) |
| EA (3) | EA037206B1 (zh) |
| ES (1) | ES2877808T3 (zh) |
| IL (2) | IL259669B (zh) |
| MX (2) | MX2020012592A (zh) |
| MY (1) | MY197217A (zh) |
| PH (2) | PH12018501649B1 (zh) |
| SG (1) | SG11201806581TA (zh) |
| UA (1) | UA124099C2 (zh) |
| WO (1) | WO2017134133A1 (zh) |
| ZA (1) | ZA201805205B (zh) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112017005104B1 (pt) | 2014-10-10 | 2022-08-23 | Pulmocide Limited | Derivados de 5,6-di-hidro-4h-benzotieno-[2,3-d]azepina, seus usos, composição farmacêutica e processo para a preparação dos mesmos |
| US10160772B2 (en) | 2014-12-18 | 2018-12-25 | Pulmocide Limited | 5,6-dihydro-4H-benzo[b]thieno-[2,3-d]azepine derivatives |
| US10626126B2 (en) | 2016-04-08 | 2020-04-21 | Pulmocide Limited | Compounds |
| TW201936193A (zh) * | 2017-12-05 | 2019-09-16 | 愛爾蘭商健生科學愛爾蘭無限公司 | 使用組合產品治療rsv |
| US20240109894A1 (en) * | 2019-10-30 | 2024-04-04 | Janssen Sciences Ireland Unlimited Company | Synthesis of 3-({5-chloro-1-[3-(methylsulfonyl)propyl]-1h-indol-2-yl} methyl)-1-(2,2,2-trifluoroethyl)-1,3-dihydro-2h-imidazo[4,5-c]pyridin-2-one |
| CN114014856B (zh) * | 2021-11-26 | 2023-12-22 | 嘉兴安谛康生物科技有限公司 | 作为呼吸道合胞病毒抗病毒剂的咪唑并吡啶类衍生物 |
| CN116077494A (zh) * | 2023-01-11 | 2023-05-09 | 黑龙江中医药大学 | 一种治疗呼吸道合胞病毒的药物组合物及其制备方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012080447A1 (en) * | 2010-12-16 | 2012-06-21 | Janssen R&D Ireland | Indoles as respiratory syncytial virus antiviral agents |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PT2988780T (pt) | 2013-04-25 | 2019-03-25 | Janssen Vaccines & Prevention Bv | Polipeptídeos f de pré-fusão do rsv solúveis estabilizados |
| CN114716426A (zh) | 2013-08-21 | 2022-07-08 | 詹森生物制药有限公司 | 抗病毒化合物 |
| BR112017005104B1 (pt) * | 2014-10-10 | 2022-08-23 | Pulmocide Limited | Derivados de 5,6-di-hidro-4h-benzotieno-[2,3-d]azepina, seus usos, composição farmacêutica e processo para a preparação dos mesmos |
-
2017
- 2017-02-02 MY MYPI2018001388A patent/MY197217A/en unknown
- 2017-02-02 EA EA201891655A patent/EA037206B1/ru unknown
- 2017-02-02 EP EP17702125.0A patent/EP3411028B1/en active Active
- 2017-02-02 UA UAA201809060A patent/UA124099C2/uk unknown
- 2017-02-02 MX MX2020012592A patent/MX2020012592A/es unknown
- 2017-02-02 AU AU2017214246A patent/AU2017214246B2/en active Active
- 2017-02-02 MX MX2018009422A patent/MX2018009422A/es unknown
- 2017-02-02 EA EA202092251A patent/EA202092251A1/ru unknown
- 2017-02-02 KR KR1020187020776A patent/KR20180108598A/ko not_active Application Discontinuation
- 2017-02-02 EP EP21170919.1A patent/EP3892273A3/en active Pending
- 2017-02-02 EA EA202092250A patent/EA202092250A1/ru unknown
- 2017-02-02 SG SG11201806581TA patent/SG11201806581TA/en unknown
- 2017-02-02 ES ES17702125T patent/ES2877808T3/es active Active
- 2017-02-02 CN CN201780009640.0A patent/CN108601774B/zh active Active
- 2017-02-02 WO PCT/EP2017/052201 patent/WO2017134133A1/en active Application Filing
- 2017-02-02 JP JP2018540796A patent/JP7065030B2/ja active Active
- 2017-02-02 CN CN202010988991.4A patent/CN112245429A/zh active Pending
- 2017-02-02 CA CA3006488A patent/CA3006488A1/en active Pending
- 2017-02-02 US US16/075,103 patent/US10363253B2/en active Active
- 2017-02-02 BR BR112018014958A patent/BR112018014958A2/pt not_active Application Discontinuation
-
2018
- 2018-05-29 IL IL259669A patent/IL259669B/en active IP Right Grant
- 2018-06-29 CL CL2018001808A patent/CL2018001808A1/es unknown
- 2018-08-02 PH PH12018501649A patent/PH12018501649B1/en unknown
- 2018-08-02 ZA ZA2018/05205A patent/ZA201805205B/en unknown
-
2019
- 2019-05-29 CL CL2019001454A patent/CL2019001454A1/es unknown
- 2019-05-29 CL CL2019001455A patent/CL2019001455A1/es unknown
-
2020
- 2020-09-10 IL IL277281A patent/IL277281B/en active IP Right Grant
- 2020-09-29 PH PH12020551598A patent/PH12020551598A1/en unknown
-
2022
- 2022-03-25 AU AU2022202070A patent/AU2022202070A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012080447A1 (en) * | 2010-12-16 | 2012-06-21 | Janssen R&D Ireland | Indoles as respiratory syncytial virus antiviral agents |
Non-Patent Citations (2)
| Title |
|---|
| COMBINATION THERAPY WITH AEROSOLIZED RIBAVIRIN AND INTRAVENOUS IMMUNOGLOBULIN FOR RESPIRATORY SYNCYTIAL VIRUS-DISEASE IN ADULT BONE-MARROW TRANSPLANT RECIPIENTS;WHIMBEY E et al.;《BONE MARROW TRANSPLANTATION》;19950930;第16卷(第3期);393-399 * |
| Comparison of the inhibition of human metapneumovirus and respiratory syncytial virus by ribavirin and immune serum globulin in vitro;Wyde, PR et al.;《ANTIVIRAL RESEARCH》;20030930;第60卷(第1期);51-59 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108601774B (zh) | 用于治疗rsv的组合产品 | |
| US11129834B2 (en) | Combinations and methods comprising a capsid assembly inhibitor | |
| AU2011209788B2 (en) | Antiviral therapy | |
| US20160022724A1 (en) | Methods for treating paramyxoviruses | |
| KR20190071765A (ko) | 코로나 바이러스에 연관된 감염의 치료를 위한 항바이러스 조성물 | |
| US20180117042A1 (en) | Methods for treating respiratory syncytial virus infection | |
| TW202139987A (zh) | 維多氟地莫司(Vidofludimus)用於治療或預防病毒性疾病 | |
| EP3720440B1 (en) | Treatment of rsv with combination product | |
| EA040061B1 (ru) | Комбинация для лечения и ослабления rsv инфекции и фармацевтическая композиция на ее основе | |
| EA040090B1 (ru) | Комбинация для лечения и ослабления rsv инфекции и фармацевтическая композиция на ее основе | |
| WO2018222774A1 (en) | Methods for treating pneumoviruses | |
| AU2014202404C1 (en) | Antiviral therapy | |
| MXPA01002673A (en) | Antiviral combinations |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1258631 Country of ref document: HK |
|
| GR01 | Patent grant | ||
| GR01 | Patent grant |