CN108129552B - 一种海参来源的抗氧化活性肽及提取方法 - Google Patents
一种海参来源的抗氧化活性肽及提取方法 Download PDFInfo
- Publication number
- CN108129552B CN108129552B CN201711399569.XA CN201711399569A CN108129552B CN 108129552 B CN108129552 B CN 108129552B CN 201711399569 A CN201711399569 A CN 201711399569A CN 108129552 B CN108129552 B CN 108129552B
- Authority
- CN
- China
- Prior art keywords
- sea cucumber
- peptide
- active peptide
- derived
- free radical
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 48
- 241000251511 Holothuroidea Species 0.000 title claims abstract description 31
- 230000003078 antioxidant effect Effects 0.000 title claims abstract description 24
- 239000003963 antioxidant agent Substances 0.000 title claims abstract description 18
- 238000000605 extraction Methods 0.000 title abstract description 10
- 125000003275 alpha amino acid group Chemical group 0.000 claims abstract description 5
- 230000003064 anti-oxidating effect Effects 0.000 claims description 6
- 230000000694 effects Effects 0.000 claims description 5
- 239000000843 powder Substances 0.000 claims description 5
- 230000002292 Radical scavenging effect Effects 0.000 claims 1
- MGJZITXUQXWAKY-UHFFFAOYSA-N diphenyl-(2,4,6-trinitrophenyl)iminoazanium Chemical compound [O-][N+](=O)C1=CC([N+](=O)[O-])=CC([N+]([O-])=O)=C1N=[N+](C=1C=CC=CC=1)C1=CC=CC=C1 MGJZITXUQXWAKY-UHFFFAOYSA-N 0.000 claims 1
- TUJKJAMUKRIRHC-UHFFFAOYSA-N hydroxyl Chemical compound [OH] TUJKJAMUKRIRHC-UHFFFAOYSA-N 0.000 claims 1
- 241000965254 Apostichopus japonicus Species 0.000 abstract description 23
- 239000004365 Protease Substances 0.000 abstract description 20
- 108091005804 Peptidases Proteins 0.000 abstract description 15
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 abstract description 14
- 102000004169 proteins and genes Human genes 0.000 abstract description 13
- 108090000623 proteins and genes Proteins 0.000 abstract description 13
- 150000001875 compounds Chemical class 0.000 abstract description 12
- -1 DPPH free radical Chemical class 0.000 abstract description 9
- 102000007079 Peptide Fragments Human genes 0.000 abstract description 9
- 108010033276 Peptide Fragments Proteins 0.000 abstract description 9
- 238000000034 method Methods 0.000 abstract description 6
- 102000004196 processed proteins & peptides Human genes 0.000 abstract description 6
- 238000002360 preparation method Methods 0.000 abstract description 5
- 230000002000 scavenging effect Effects 0.000 abstract description 5
- 108010038807 Oligopeptides Proteins 0.000 abstract description 4
- 102000015636 Oligopeptides Human genes 0.000 abstract description 4
- 229920001184 polypeptide Polymers 0.000 abstract description 3
- 235000019658 bitter taste Nutrition 0.000 abstract description 2
- 235000015872 dietary supplement Nutrition 0.000 abstract description 2
- 230000009465 prokaryotic expression Effects 0.000 abstract description 2
- 238000001308 synthesis method Methods 0.000 abstract description 2
- 239000007788 liquid Substances 0.000 description 17
- 239000012528 membrane Substances 0.000 description 13
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 235000019419 proteases Nutrition 0.000 description 12
- 239000002002 slurry Substances 0.000 description 12
- 238000000926 separation method Methods 0.000 description 9
- 238000012163 sequencing technique Methods 0.000 description 9
- 238000000909 electrodialysis Methods 0.000 description 8
- 238000001728 nano-filtration Methods 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 238000010438 heat treatment Methods 0.000 description 6
- 239000012466 permeate Substances 0.000 description 6
- 238000001694 spray drying Methods 0.000 description 6
- 108090000145 Bacillolysin Proteins 0.000 description 5
- 102000004190 Enzymes Human genes 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 5
- 102000035092 Neutral proteases Human genes 0.000 description 5
- 108091005507 Neutral proteases Proteins 0.000 description 5
- 108090000526 Papain Proteins 0.000 description 5
- 150000001413 amino acids Chemical class 0.000 description 5
- 238000005520 cutting process Methods 0.000 description 5
- 229940088598 enzyme Drugs 0.000 description 5
- 108010007119 flavourzyme Proteins 0.000 description 5
- 229940055729 papain Drugs 0.000 description 5
- 235000019834 papain Nutrition 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 239000000498 cooling water Substances 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 235000013372 meat Nutrition 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 239000002994 raw material Substances 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 238000003860 storage Methods 0.000 description 4
- 241000237502 Ostreidae Species 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 230000033228 biological regulation Effects 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 235000020636 oyster Nutrition 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- CAVKXZMMDNOZJU-UHFFFAOYSA-N Gly-Pro-Ala-Gly-Pro Natural products C1CCC(C(O)=O)N1C(=O)CNC(=O)C(C)NC(=O)C1CCCN1C(=O)CN CAVKXZMMDNOZJU-UHFFFAOYSA-N 0.000 description 2
- QSQXZZCGPXQBPP-BQBZGAKWSA-N Gly-Pro-Cys Chemical compound C1C[C@H](N(C1)C(=O)CN)C(=O)N[C@@H](CS)C(=O)O QSQXZZCGPXQBPP-BQBZGAKWSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- 230000009849 deactivation Effects 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 230000007760 free radical scavenging Effects 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 230000000415 inactivating effect Effects 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 239000007791 liquid phase Substances 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 230000035790 physiological processes and functions Effects 0.000 description 2
- 238000004537 pulping Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 241000965253 Apostichopus Species 0.000 description 1
- 208000035404 Autolysis Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 206010057248 Cell death Diseases 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000003276 anti-hypertensive effect Effects 0.000 description 1
- 230000002785 anti-thrombosis Effects 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- HHEAADYXPMHMCT-UHFFFAOYSA-N dpph Chemical compound [O-][N+](=O)C1=CC([N+](=O)[O-])=CC([N+]([O-])=O)=C1[N]N(C=1C=CC=CC=1)C1=CC=CC=C1 HHEAADYXPMHMCT-UHFFFAOYSA-N 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000013376 functional food Nutrition 0.000 description 1
- 235000019589 hardness Nutrition 0.000 description 1
- 239000012510 hollow fiber Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000007365 immunoregulation Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 229910001410 inorganic ion Inorganic materials 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000028043 self proteolysis Effects 0.000 description 1
- 230000009759 skin aging Effects 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 235000019640 taste Nutrition 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/06—Preparation of peptides or proteins produced by the hydrolysis of a peptide bond, e.g. hydrolysate products
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biophysics (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
- Seasonings (AREA)
- Peptides Or Proteins (AREA)
Abstract
本发明属于抗氧化活性肽制备及鉴定领域,特别涉及一种海参来源的抗氧化活性肽段及提取方法。所述肽段的氨基酸序列为NH2‑Gly‑Pro‑Ala‑Gly‑Pro‑Cys,利用复合蛋白酶制剂酶解获得,对DPPH自由基、羟自由基和超氧阴离子自由基具有良好的清除作用。本发明方法制得的海参低聚肽分子量400‑800占比57%~68%;本发明方法制得的海参低聚肽无苦味、腥味,可作为蛋白营养补充剂直接食用;本发明获得肽段来源于仿刺参,抗氧化活性强,序列明确,可以采用原核表达或多肽合成法等进行批量生产。
Description
技术领域
本发明属于抗氧化活性肽制备及鉴定领域,特别涉及一种海参来源的抗氧化活性肽及提取方法。
背景技术
由于海洋存在许多极端环境,如高压(深海)、低温(极地、深海)、高温(海底火山口)和高盐等。为了适应这些极端的海洋生境,海洋生物蛋白质无论氨基酸的组成或序列都与陆地生物蛋白有很大的不同。种类繁多的海洋蛋白氨基酸序列中,潜在着许多具有生物活性的氨基酸序列,用特异的蛋白酶水解,就释放出有活性的肽段。这些活性的肽段生物学意义主要体现在其吸收机制优于氨基酸和具有氨基酸不可比拟的生理功能两个方面,其生理功能主要有类吗啡样活性、激素和调节激素的作用,对生物体内的酶具有调节和抑制功能,免疫调节,抗血栓,抗高血压,降胆固醇,抑制细菌、病毒,抗癌作用,抗氧化和清除自由基作用,改善元素吸收和矿物质运输,促进生长,调节食品风味、口味和硬度等。生物活性肽是世界上药物及保健品研究的热点。
海参纲仿刺参属,又称刺参,主要分布于中国的黄渤海和俄罗斯、朝韩和日本等东北亚海域。由于刺参特殊的进化地位、独特的繁殖生活史以及夏眠、排脏与再生、自溶等生物学现象,使其具有重要的科学研究价值,同时,针对其活性肽段的研究相对较少,目前主要以蛋白酶酶解海参蛋白制备的海参混合多肽,分子量为5000Da以上,不利于人体吸收,同时也是各种功能的肽段混合在一起。若通过肽段的鉴定把海参不同功能的肽段分离,有助于开发医疗用途精准肽段产品。
发明内容
本发明的目的在于提供一种海参来源的抗氧化活性肽及提取方法,为食品、保健品、化妆品提供高活性和安全的功能性原料。
本发明为实现上述目的所采取的技术方案为:一种海参来源的抗氧化活性肽,其特征在于,所述肽的氨基酸序列为NH2-Gly-Pro-Ala-Gly-Pro-Cys。
所述肽利用复合蛋白酶制剂酶解获得,对DPPH自由基、羟自由基和超氧阴离子自由基具有良好的清除作用。
所述复合蛋白酶的质量配比为:中性蛋白酶:木瓜蛋白酶:风味蛋白酶=(2~4):(3~5):(3~5)。
一种海参来源的抗氧化活性肽的提取方法,其特征在于,包括以下步骤:
S1、原料预处理:取新鲜仿刺参体壁粉碎、制浆,得到仿刺参浆液;
S2、向步骤S1制得的仿刺参浆液中加入所述仿刺参浆液2~5倍质量的水,升温至40~55℃后,加入2.5mol/L的NaOH溶液调节PH至8.0~9.0;加入占所述仿刺参浆液质量0.1~0.2%的复合蛋白酶,搅拌酶解3~6h后,升温至80~95℃灭酶10~25min,得到酶解液;将所述酶解液离心分离,收集液相;
S3、将步骤S2得到的液相采用切割分子量2000~5000Da的纳滤膜分离,收集透过液;
S4、将步骤S3收集的透过液采用电渗析脱出离子;
S5、将步骤S4制得的精制液通过膜浓缩设备浓缩至可溶性固形物,含量占浓缩液总质量20~40%;
S6、将步骤S5制得浓缩液采用蛋白N端测序法分析肽氨基酸排列顺序;
S7、将步骤S5制得浓缩液进行喷雾干燥,得到海参肽粉进行自由基清除实验。
所述步骤S1具体为:取新鲜仿刺参体壁,利用绞肉机将所述仿刺参体壁绞碎10~20min,得到仿刺参浆液。
所述步骤S1中复合蛋白酶的质量配比为:中性蛋白酶:木瓜蛋白酶:风味蛋白酶=(2~4):(3~5):(3~5)。
所述步骤S2中离心分离的条件为:采用摇摆型管式分离机,转速为10000~16000r/min。
所述步骤S4中电渗析的操作条件为:电压10~100V,进分离液流速1.0~1.55吨/小时,浓水流速1.0~1.60吨/小时,电极冷却水流速0.5~1.0吨/小时。
所述步骤S5中膜浓缩的操作条件为:采用切割分子量为10~100Da的纳滤级、中空纤维膜,操作压力为1.5~1.8Mpa。
所述步骤S7中喷雾干燥的条件为:进风温度140℃,出风温度85℃。
本发明以海参体壁为原料,经过特异性的复合蛋白酶酶解,释放出活性肽。通过测序的方法得到肽的氨基酸组成,鉴定抗氧化活性,相比于现有技术的有益效果在于:
1、本发明方法制得的海参低聚肽分子量400-800占比57%~68%;
2、本发明方法制得的海参低聚肽无苦味、腥味,可作为蛋白营养补充剂直接食用;
3、本发明获得肽来源于仿刺参,抗氧化活性强,序列明确,可以采用原核表达或多肽合成法等进行批量生产。
附图说明
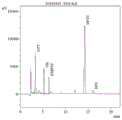
图1为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图一(第一位点)。
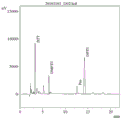
图2为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图二(第二位点)。
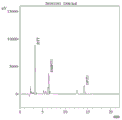
图3为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图三(第三位点)。
图4为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图四(第四位点)。
图5为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图五(第五位点)。
图6为本发明海参来源的抗氧化活性肽的蛋白N段测序峰图六(第六位点)。
实施方式
下面结合附图与实施例对本发明进一步说明,但本发明不局限于具体实施例。
实施例1
一种海参来源的抗氧化活性肽,所述肽的氨基酸序列为NH2-Gly-Pro-Ala-Gly-Pro-Cys。所述肽对DPPH自由基、羟自由基和超氧阴离子自由基具有良好的清除作用。
实施例2
一种实施例1中所述海参来源的抗氧化活性肽的提取方法,具体包括以下步骤:
S1、原料预处理:将仿刺参体壁1000kg用绞肉机粉碎15min,绞碎后进入胶体磨磨浆得浆液;
S2、将浆液导入5m3酶解罐,所述5m3酶解罐为夹层式加热反应釜,加入3倍牡蛎浆液质量的纯水,调整体系温度50℃,用2.5mol/L的NaOH溶液调PH至8.6,加入所述仿刺参浆液总质量0.12%的复合蛋白酶;复合蛋白酶的质量配比为:中性蛋白酶:木瓜蛋白酶:风味蛋白酶=3:4:3;搅拌酶解4h,升温80℃灭酶20min,采用管式离心机16000rpm离心进行固液分离,收集离心清液,导入5m3清液储罐;
S3、5m3分离液储罐与膜分离装置相连,将所得清液经切割分子量5000Da纳滤膜分离装置分离得透过液;
S4、膜分离装置与电渗析装置相连,将所得透过液经电渗析去除无机离子,电渗析的电压为70V,进分离液流速1.5吨/小时,浓水流速1.52吨/小时,电极冷却水流速0.8吨/小时;
S5、所述电渗析装置与膜浓缩设备相连,将精制液经切割分子量50Da纳滤膜浓缩浓缩,使用1.6Mpa压力,浓缩至可溶性固含量占浓缩液质量30%,导入浓缩储罐;
S6、将步骤S5中所制得料液进行蛋白N端测序,结果见图1-图6;
S7、将步骤S5制得浓缩液进行喷雾干燥,得到海参肽粉,进行自由基清除实验。步骤S5中所述浓缩储罐,设置有出料口,将浓缩料液从出料口取出后导入喷雾干燥塔进行喷雾干燥,喷雾干燥时进风温度维持在140℃,出风温度维持在85℃,得海参肽粉;
所得海参肽粉进行清除自由基的抗氧化实验结果表明:
NH2-Gly-Pro-Ala-Gly-Pro-Cys对DPPH自由基(EC50 0.98mg/mL)、羟基自由基(EC50 0.08mg/mL)和超氧阴离子自由基(EC50 0.15mg/mL)具有良好的清除作用。适用于开发功能性食品、保健品、以及防止皮肤衰老的化妆品等。
实施例3
本实施例中所述海参来源的抗氧化活性肽的提取方法与实施例2中相同,不同的技术参数为:
1)步骤S1中将仿刺参体壁用绞肉机粉碎10min;
2)步骤S2中加入2倍牡蛎浆液质量的纯水,调整体系温度40℃,用2.5mol/L的NaOH溶液调PH至8.0,加入所述仿刺参浆液总质量0.1%的复合蛋白酶;复合蛋白酶的质量配比为:中性蛋白酶:木瓜蛋白酶:风味蛋白酶=2:3:4;搅拌酶解3h,升温82℃灭酶10min,采用管式离心机10000rpm离心进行固液分离;
3)步骤S3中将所得清液经切割分子量2000Da纳滤膜分离装置分离得透过液;
4)步骤S4中电渗析的电压为10V,进分离液流速1.0吨/小时,浓水流速1.0吨/小时,电极冷却水流速0.5吨/小时;
5)步骤S5中将精制液经切割分子量10Da纳滤膜浓缩浓缩,使用1.5Mpa压力,浓缩至可溶性固含量占浓缩液质量20%。
实施例4
本实施例中所述海参来源的抗氧化活性肽的提取方法与实施例2中相同,不同的技术参数为:
1)步骤S1中将仿刺参体壁用绞肉机粉碎20min;
2) 步骤S2中加入5倍牡蛎浆液质量的纯水,调整体系温度55℃,用2.5mol/L的NaOH溶液调PH至9.0,加入所述仿刺参浆液总质量0.2%的复合蛋白酶;复合蛋白酶的质量配比为:中性蛋白酶:木瓜蛋白酶:风味蛋白酶=3:4:3;搅拌酶解6h,升温95℃灭酶25min,采用管式离心机13000rpm离心进行固液分离;
3)步骤S3中将所得清液经切割分子量3500Da纳滤膜分离装置分离得透过液;
4)步骤S4中电渗析的电压为100V,进分离液流速1.55吨/小时,浓水流速1.60吨/小时,电极冷却水流速1.0吨/小时;
5)步骤S5中将精制液经切割分子量100Da纳滤膜浓缩浓缩,使用1.8Mpa压力,浓缩至可溶性固含量占浓缩液质量40%。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明披露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
SEQUENCE LISTING
<110> 大连深蓝肽科技研发有限公司
<120> 一种海参来源的抗氧化活性肽及提取方法
<130> 0001S
<160> 1
<170> PatentIn version 3.5
<210> 1
<211> 6
<212> PRT
<213> Apostichopus japonicus
<400> 1
Gly Pro Ala Gly Pro Cys
1 5
SEQUENCE LISTING
<110> 大连深蓝肽科技研发有限公司
<120> 一种海参来源的抗氧化活性肽段及提取方法
<130> 0001S
<160> 1
<170> PatentIn version 3.5
<210> 1
<211> 6
<212> PRT
<213> Apostichopus japonicus
<400> 1
Gly Pro Ala Gly Pro Cys
1 5
Claims (2)
1.一种海参来源的抗氧化活性肽在制备具有抗氧化活性的海参肽粉中的应用,其特征在于,所述抗氧化活性肽的氨基酸序列为NH2-Gly-Pro-Ala-Gly-Pro-Cys。
2.根据权利要求1所述应用,其特征在于,其中所述抗氧化活性肽具有清除DPPH自由基、羟自由基活性。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201711399569.XA CN108129552B (zh) | 2017-12-22 | 2017-12-22 | 一种海参来源的抗氧化活性肽及提取方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201711399569.XA CN108129552B (zh) | 2017-12-22 | 2017-12-22 | 一种海参来源的抗氧化活性肽及提取方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108129552A CN108129552A (zh) | 2018-06-08 |
| CN108129552B true CN108129552B (zh) | 2023-07-07 |
Family
ID=62391408
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201711399569.XA Active CN108129552B (zh) | 2017-12-22 | 2017-12-22 | 一种海参来源的抗氧化活性肽及提取方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN108129552B (zh) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109320589B (zh) * | 2018-10-18 | 2021-07-27 | 大连深蓝肽科技研发有限公司 | 刺参来源的小分子活性肽 |
| CN109400678B (zh) * | 2018-10-18 | 2021-07-27 | 大连深蓝肽科技研发有限公司 | 一种刺参来源的抗氧化和dpp-iv抑制活性肽 |
| CN110256529B (zh) * | 2019-05-30 | 2020-12-04 | 集美大学 | 一种抗氧化肽及其应用 |
| CN110256530B (zh) * | 2019-05-30 | 2020-11-17 | 集美大学 | 一种抗氧化肽及其应用 |
| CN111171138B (zh) * | 2020-01-14 | 2022-11-15 | 大连深蓝肽科技研发有限公司 | 用于检测刺参低聚肽的肽段、单克隆抗体、胶体金试纸条及检测方法 |
| CN113861272B (zh) * | 2021-11-08 | 2023-03-24 | 时代生物科技(深圳)有限公司 | 一种海参活性肽及其制备方法 |
| CN114190562B (zh) * | 2021-12-16 | 2024-05-14 | 吉林国瑞医药有限公司 | 一种含有花胶和轮叶党参低聚肽的抗皮肤衰老组合物及其制备方法和用途 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103987724A (zh) * | 2011-11-04 | 2014-08-13 | 株式会社日皮 | Dpp-4抑制剂 |
| CN104356200A (zh) * | 2014-11-05 | 2015-02-18 | 福州大学 | 一种抗氧化多肽及其制备方法 |
| CN104356201A (zh) * | 2014-11-05 | 2015-02-18 | 福州大学 | 一种海参抗氧化多肽 |
| CN104402972A (zh) * | 2014-11-05 | 2015-03-11 | 福州大学 | 一种海参抗氧化多肽及其制备方法 |
| CN104540960A (zh) * | 2012-07-25 | 2015-04-22 | 株式会社日皮 | 胶原肽组合物的制造方法、dpp-4阻碍剂和血糖值升高抑制剂 |
| CN105177095A (zh) * | 2015-10-14 | 2015-12-23 | 中国科学院海洋研究所 | 一种高效制备海参抗氧化活性肽的方法 |
| CN105368901A (zh) * | 2015-10-24 | 2016-03-02 | 山东好当家海洋发展股份有限公司 | 一种利用仿刺参加工液提取抗菌多肽的方法 |
| CN106107635A (zh) * | 2016-06-29 | 2016-11-16 | 大连深蓝肽科技研发有限公司 | 利用牡蛎鲜肉制备牡蛎低聚肽的方法 |
-
2017
- 2017-12-22 CN CN201711399569.XA patent/CN108129552B/zh active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103987724A (zh) * | 2011-11-04 | 2014-08-13 | 株式会社日皮 | Dpp-4抑制剂 |
| CN104540960A (zh) * | 2012-07-25 | 2015-04-22 | 株式会社日皮 | 胶原肽组合物的制造方法、dpp-4阻碍剂和血糖值升高抑制剂 |
| CN104356200A (zh) * | 2014-11-05 | 2015-02-18 | 福州大学 | 一种抗氧化多肽及其制备方法 |
| CN104356201A (zh) * | 2014-11-05 | 2015-02-18 | 福州大学 | 一种海参抗氧化多肽 |
| CN104402972A (zh) * | 2014-11-05 | 2015-03-11 | 福州大学 | 一种海参抗氧化多肽及其制备方法 |
| CN105177095A (zh) * | 2015-10-14 | 2015-12-23 | 中国科学院海洋研究所 | 一种高效制备海参抗氧化活性肽的方法 |
| CN105368901A (zh) * | 2015-10-24 | 2016-03-02 | 山东好当家海洋发展股份有限公司 | 一种利用仿刺参加工液提取抗菌多肽的方法 |
| CN106107635A (zh) * | 2016-06-29 | 2016-11-16 | 大连深蓝肽科技研发有限公司 | 利用牡蛎鲜肉制备牡蛎低聚肽的方法 |
Non-Patent Citations (3)
| Title |
|---|
| By P. R. DANDO.MEGRIM (LEPIDORHOMBUSWHIFF-IAGONIS) POPULATIONS IN THEENGLISH CHANNEL AND APPROACHES—LACTATE DEHYDROGENASE AND 'GLYCEROL-3-PHOSPHATE DEHYDRO-GENASE POLYMORPHISMS.J. mar. biol. Ass. U.K..1970,第50卷808-818. * |
| 刘志彤等.海参二肽基肽酶 IV 抑制肽的酶解制备及结构鉴定.现代食品科技.第36卷(第36期),全文. * |
| 左爱华等.海参低聚肽的高通量 HPLC MS/MS 分析鉴定和活性筛选.食品工业科技.第41卷(第41期),全文. * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN108129552A (zh) | 2018-06-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108129552B (zh) | 一种海参来源的抗氧化活性肽及提取方法 | |
| CN103992384B (zh) | 一种大黄鱼鱼骨胶原肽及其制备方法和用途 | |
| CN104513843B (zh) | 一种多糖和蛋白肽的联合制备方法 | |
| CN107083413A (zh) | 一种海参内脏制备海参肽和海参多糖的方法 | |
| CN104757252B (zh) | 一种具有抗氧化活性的灰树花蛋白酶解物的制备方法 | |
| CN101942014B (zh) | 一种食品级藻蓝蛋白及其制备方法 | |
| CN111041059B (zh) | 一种具有抗氧化活性南极磷虾肽的制备方法 | |
| CN103073621A (zh) | 一种金枪鱼碎肉蛋白抗氧化肽及其制备方法和用途 | |
| CN110699411B (zh) | 一种蛋壳膜多肽的制备方法 | |
| CN108048518B (zh) | 鸡血球抗氧化肽及其酶解制备方法 | |
| CN106174436A (zh) | 一种复合酶解鱼骨素的制备方法 | |
| CN103103242A (zh) | 一种抗氧化活性肽及其制备方法 | |
| CN106191189A (zh) | 一种金枪鱼皮高保湿活性肽的制备方法及其应用 | |
| CN103627768A (zh) | 鱼皮胶原蛋白生物活性小肽及其制备方法 | |
| CN106387304B (zh) | 一种高压脉冲电场偶联生物酶解制备鲍鱼内脏磷脂的方法 | |
| CN107082807A (zh) | 具有ace抑制功能的牦牛骨蛋白肽及制备方法和应用 | |
| CN103421867A (zh) | 一种海参胶原蛋白的制备方法 | |
| CN106119328A (zh) | 一种适合工业化生产的优质虾低聚肽粉制备方法 | |
| CN103992386A (zh) | 一种大黄鱼鱼鳞抗氧化胶原肽及其制备方法和用途 | |
| KR101647558B1 (ko) | 참치심장으로부터 분리한 항산화 펩타이드의 제조방법 | |
| CN101134773A (zh) | 一种玉米自由基清除剂的提取方法 | |
| CN108101980B (zh) | 一种高纯度藻蓝色素的制备方法 | |
| CN103211145B (zh) | 对酒精性肝损伤具有防护作用的活性多糖肽制备方法及复配 | |
| CN103421871A (zh) | 一种金枪鱼骨胶原蛋白肽的制备方法 | |
| CN106107242A (zh) | 一种无抗水产免疫增强剂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |