CN103517918A - 拮抗性dr3配体 - Google Patents
拮抗性dr3配体 Download PDFInfo
- Publication number
- CN103517918A CN103517918A CN201280011136.1A CN201280011136A CN103517918A CN 103517918 A CN103517918 A CN 103517918A CN 201280011136 A CN201280011136 A CN 201280011136A CN 103517918 A CN103517918 A CN 103517918A
- Authority
- CN
- China
- Prior art keywords
- antibody
- seq
- univalent
- fab
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003446 ligand Substances 0.000 title abstract description 14
- 230000003042 antagnostic effect Effects 0.000 title abstract 2
- 208000027866 inflammatory disease Diseases 0.000 claims abstract description 11
- 102100022203 Tumor necrosis factor receptor superfamily member 25 Human genes 0.000 claims description 272
- 101000679903 Homo sapiens Tumor necrosis factor receptor superfamily member 25 Proteins 0.000 claims description 269
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 47
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 claims description 42
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 claims description 42
- 102000003810 Interleukin-18 Human genes 0.000 claims description 36
- 108090000171 Interleukin-18 Proteins 0.000 claims description 36
- 102000004127 Cytokines Human genes 0.000 claims description 32
- 108090000695 Cytokines Proteins 0.000 claims description 32
- 102000013462 Interleukin-12 Human genes 0.000 claims description 32
- 108010065805 Interleukin-12 Proteins 0.000 claims description 32
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 29
- 150000001413 amino acids Chemical class 0.000 claims description 23
- 235000001014 amino acid Nutrition 0.000 claims description 22
- 208000011231 Crohn disease Diseases 0.000 claims description 21
- 108010074328 Interferon-gamma Proteins 0.000 claims description 21
- 102100037850 Interferon gamma Human genes 0.000 claims description 20
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 claims description 15
- 230000035772 mutation Effects 0.000 claims description 15
- 239000008194 pharmaceutical composition Substances 0.000 claims description 14
- 230000002441 reversible effect Effects 0.000 claims description 13
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 11
- 230000008485 antagonism Effects 0.000 claims description 11
- 102000004889 Interleukin-6 Human genes 0.000 claims description 10
- 108090001005 Interleukin-6 Proteins 0.000 claims description 10
- 102220473254 Emerin_S49A_mutation Human genes 0.000 claims description 9
- 238000010494 dissociation reaction Methods 0.000 claims description 8
- 230000005593 dissociations Effects 0.000 claims description 8
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 7
- 125000006850 spacer group Chemical group 0.000 claims description 7
- 101100112922 Candida albicans CDR3 gene Proteins 0.000 claims description 6
- 210000000936 intestine Anatomy 0.000 claims description 6
- 210000001616 monocyte Anatomy 0.000 claims description 6
- 210000001179 synovial fluid Anatomy 0.000 claims description 6
- 230000001270 agonistic effect Effects 0.000 claims description 5
- 238000001574 biopsy Methods 0.000 claims description 5
- 210000004400 mucous membrane Anatomy 0.000 claims description 5
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims description 4
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 claims description 4
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 4
- 108090000138 Tumor necrosis factor ligand superfamily member 15 Proteins 0.000 claims 5
- 102100024587 Tumor necrosis factor ligand superfamily member 15 Human genes 0.000 claims 5
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 claims 2
- 210000004027 cell Anatomy 0.000 description 127
- 238000000034 method Methods 0.000 description 52
- 108090000623 proteins and genes Proteins 0.000 description 51
- 102000009027 Albumins Human genes 0.000 description 45
- 108010088751 Albumins Proteins 0.000 description 45
- 108090000765 processed proteins & peptides Proteins 0.000 description 44
- 102000004169 proteins and genes Human genes 0.000 description 43
- 235000018102 proteins Nutrition 0.000 description 42
- 241000699666 Mus <mouse, genus> Species 0.000 description 37
- 230000014509 gene expression Effects 0.000 description 31
- 238000003556 assay Methods 0.000 description 27
- 230000000694 effects Effects 0.000 description 24
- 230000004913 activation Effects 0.000 description 22
- 150000001875 compounds Chemical class 0.000 description 22
- 230000035777 life prolongation Effects 0.000 description 22
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 21
- 238000011534 incubation Methods 0.000 description 21
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 20
- 125000003275 alpha amino acid group Chemical group 0.000 description 20
- 238000002474 experimental method Methods 0.000 description 20
- 229940024606 amino acid Drugs 0.000 description 18
- 239000012530 fluid Substances 0.000 description 18
- 238000012216 screening Methods 0.000 description 18
- 239000000370 acceptor Substances 0.000 description 17
- 239000003795 chemical substances by application Substances 0.000 description 17
- 238000013016 damping Methods 0.000 description 17
- 230000027455 binding Effects 0.000 description 16
- 230000008859 change Effects 0.000 description 16
- 239000000203 mixture Substances 0.000 description 16
- 230000028327 secretion Effects 0.000 description 16
- 238000001890 transfection Methods 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 15
- 230000008569 process Effects 0.000 description 15
- 238000012360 testing method Methods 0.000 description 15
- 102000004196 processed proteins & peptides Human genes 0.000 description 14
- 239000006228 supernatant Substances 0.000 description 14
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 13
- 238000005516 engineering process Methods 0.000 description 13
- 210000004408 hybridoma Anatomy 0.000 description 13
- 230000036039 immunity Effects 0.000 description 13
- 239000000523 sample Substances 0.000 description 13
- 239000000126 substance Substances 0.000 description 13
- 239000003643 water by type Substances 0.000 description 13
- 108020004414 DNA Proteins 0.000 description 12
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- 230000006052 T cell proliferation Effects 0.000 description 12
- 230000000903 blocking effect Effects 0.000 description 12
- 238000000684 flow cytometry Methods 0.000 description 12
- 238000013507 mapping Methods 0.000 description 12
- 102100040247 Tumor necrosis factor Human genes 0.000 description 11
- 239000000427 antigen Substances 0.000 description 11
- 230000004927 fusion Effects 0.000 description 11
- 238000004949 mass spectrometry Methods 0.000 description 11
- 239000000463 material Substances 0.000 description 11
- 238000011160 research Methods 0.000 description 11
- 102000010170 Death domains Human genes 0.000 description 10
- 108050001718 Death domains Proteins 0.000 description 10
- 108091007433 antigens Proteins 0.000 description 10
- 102000036639 antigens Human genes 0.000 description 10
- 210000004602 germ cell Anatomy 0.000 description 10
- 230000006698 induction Effects 0.000 description 10
- 210000002966 serum Anatomy 0.000 description 10
- -1 DDR3 Proteins 0.000 description 9
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 9
- 239000011324 bead Substances 0.000 description 9
- 125000004432 carbon atom Chemical group C* 0.000 description 9
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 9
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 9
- 239000012634 fragment Substances 0.000 description 9
- 230000003053 immunization Effects 0.000 description 9
- 238000002649 immunization Methods 0.000 description 9
- 230000004936 stimulating effect Effects 0.000 description 9
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 8
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 8
- 210000004369 blood Anatomy 0.000 description 8
- 239000003153 chemical reaction reagent Substances 0.000 description 8
- 201000006754 cone-rod dystrophy Diseases 0.000 description 8
- 229910052805 deuterium Inorganic materials 0.000 description 8
- 238000010790 dilution Methods 0.000 description 8
- 239000012895 dilution Substances 0.000 description 8
- 230000005764 inhibitory process Effects 0.000 description 8
- 230000002018 overexpression Effects 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 238000005406 washing Methods 0.000 description 8
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 7
- 241000282553 Macaca Species 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 238000004113 cell culture Methods 0.000 description 7
- 239000013604 expression vector Substances 0.000 description 7
- 125000005842 heteroatom Chemical group 0.000 description 7
- 238000006384 oligomerization reaction Methods 0.000 description 7
- 229920001184 polypeptide Polymers 0.000 description 7
- 238000000926 separation method Methods 0.000 description 7
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 7
- 206010061218 Inflammation Diseases 0.000 description 6
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical group OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 238000001514 detection method Methods 0.000 description 6
- 230000029087 digestion Effects 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- 238000002523 gelfiltration Methods 0.000 description 6
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 6
- 230000002209 hydrophobic effect Effects 0.000 description 6
- 230000004054 inflammatory process Effects 0.000 description 6
- 238000002347 injection Methods 0.000 description 6
- 239000007924 injection Substances 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 210000002381 plasma Anatomy 0.000 description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
- 238000004448 titration Methods 0.000 description 6
- 108010032595 Antibody Binding Sites Proteins 0.000 description 5
- 241000894006 Bacteria Species 0.000 description 5
- 241000699802 Cricetulus griseus Species 0.000 description 5
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 5
- 102220520852 Dynein light chain Tctex-type 3_S60A_mutation Human genes 0.000 description 5
- 108060003951 Immunoglobulin Proteins 0.000 description 5
- 102000057297 Pepsin A Human genes 0.000 description 5
- 108090000284 Pepsin A Proteins 0.000 description 5
- 108700008625 Reporter Genes Proteins 0.000 description 5
- 230000003213 activating effect Effects 0.000 description 5
- 238000005804 alkylation reaction Methods 0.000 description 5
- 125000003368 amide group Chemical group 0.000 description 5
- 238000010367 cloning Methods 0.000 description 5
- 230000000295 complement effect Effects 0.000 description 5
- 239000002299 complementary DNA Substances 0.000 description 5
- 235000019621 digestibility Nutrition 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 125000001924 fatty-acyl group Chemical group 0.000 description 5
- 229910052739 hydrogen Inorganic materials 0.000 description 5
- 239000001257 hydrogen Substances 0.000 description 5
- 102000018358 immunoglobulin Human genes 0.000 description 5
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 5
- 210000001672 ovary Anatomy 0.000 description 5
- 229940111202 pepsin Drugs 0.000 description 5
- 239000013612 plasmid Substances 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 125000005629 sialic acid group Chemical group 0.000 description 5
- 230000019491 signal transduction Effects 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 4
- 101100230376 Acetivibrio thermocellus (strain ATCC 27405 / DSM 1237 / JCM 9322 / NBRC 103400 / NCIMB 10682 / NRRL B-4536 / VPI 7372) celI gene Proteins 0.000 description 4
- 206010009900 Colitis ulcerative Diseases 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 4
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 4
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 4
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 4
- 201000006704 Ulcerative Colitis Diseases 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N acetic acid Substances CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 230000029936 alkylation Effects 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000001413 cellular effect Effects 0.000 description 4
- 201000000464 cone-rod dystrophy 2 Diseases 0.000 description 4
- 238000013461 design Methods 0.000 description 4
- 239000000539 dimer Substances 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 239000012636 effector Substances 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 150000004676 glycans Chemical class 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- 229920002674 hyaluronan Polymers 0.000 description 4
- 229960003160 hyaluronic acid Drugs 0.000 description 4
- 230000000527 lymphocytic effect Effects 0.000 description 4
- 241001515942 marmosets Species 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 238000001556 precipitation Methods 0.000 description 4
- 238000000159 protein binding assay Methods 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 102200000024 rs2229317 Human genes 0.000 description 4
- 102220104240 rs879253869 Human genes 0.000 description 4
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical class CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 description 4
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 4
- 241000894007 species Species 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 3
- NHJVRSWLHSJWIN-UHFFFAOYSA-N 2,4,6-trinitrobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O NHJVRSWLHSJWIN-UHFFFAOYSA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 208000023275 Autoimmune disease Diseases 0.000 description 3
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 3
- 241000283707 Capra Species 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 101710177940 IgG receptor FcRn large subunit p51 Proteins 0.000 description 3
- 239000005089 Luciferase Substances 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 230000004988 N-glycosylation Effects 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 208000006440 Open Bite Diseases 0.000 description 3
- 101100070271 Oryza sativa subsp. japonica HDR3 gene Proteins 0.000 description 3
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 3
- 206010039361 Sacroiliitis Diseases 0.000 description 3
- 102000007562 Serum Albumin Human genes 0.000 description 3
- 108010071390 Serum Albumin Proteins 0.000 description 3
- 102220541402 Tumor necrosis factor receptor superfamily member 6_T28A_mutation Human genes 0.000 description 3
- 230000008484 agonism Effects 0.000 description 3
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 3
- 229960000074 biopharmaceutical Drugs 0.000 description 3
- 230000004087 circulation Effects 0.000 description 3
- 238000012937 correction Methods 0.000 description 3
- 230000008878 coupling Effects 0.000 description 3
- 238000010168 coupling process Methods 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- 238000012258 culturing Methods 0.000 description 3
- 238000002022 differential scanning fluorescence spectroscopy Methods 0.000 description 3
- 230000002255 enzymatic effect Effects 0.000 description 3
- 239000013613 expression plasmid Substances 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 238000011207 functional examination Methods 0.000 description 3
- 230000002496 gastric effect Effects 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 230000001939 inductive effect Effects 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 238000007912 intraperitoneal administration Methods 0.000 description 3
- 238000004255 ion exchange chromatography Methods 0.000 description 3
- 208000002551 irritable bowel syndrome Diseases 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 210000004698 lymphocyte Anatomy 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 239000013642 negative control Substances 0.000 description 3
- 230000003472 neutralizing effect Effects 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 102200006011 rs104894295 Human genes 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 238000004904 shortening Methods 0.000 description 3
- 230000009870 specific binding Effects 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 229940104230 thymidine Drugs 0.000 description 3
- 230000010474 transient expression Effects 0.000 description 3
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 3
- 238000000108 ultra-filtration Methods 0.000 description 3
- 206010001497 Agitation Diseases 0.000 description 2
- BPYKTIZUTYGOLE-IFADSCNNSA-N Bilirubin Chemical compound N1C(=O)C(C)=C(C=C)\C1=C\C1=C(C)C(CCC(O)=O)=C(CC2=C(C(C)=C(\C=C/3C(=C(C=C)C(=O)N\3)C)N2)CCC(O)=O)N1 BPYKTIZUTYGOLE-IFADSCNNSA-N 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- BQENDLAVTKRQMS-SBBGFIFASA-L Carbenoxolone sodium Chemical compound [Na+].[Na+].C([C@H]1C2=CC(=O)[C@H]34)[C@@](C)(C([O-])=O)CC[C@]1(C)CC[C@@]2(C)[C@]4(C)CC[C@@H]1[C@]3(C)CC[C@H](OC(=O)CCC([O-])=O)C1(C)C BQENDLAVTKRQMS-SBBGFIFASA-L 0.000 description 2
- 108091035707 Consensus sequence Proteins 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000005720 Glutathione transferase Human genes 0.000 description 2
- 108010070675 Glutathione transferase Proteins 0.000 description 2
- 208000024869 Goodpasture syndrome Diseases 0.000 description 2
- 208000003807 Graves Disease Diseases 0.000 description 2
- 208000015023 Graves' disease Diseases 0.000 description 2
- 102220576062 HLA class I histocompatibility antigen, B alpha chain_Y91C_mutation Human genes 0.000 description 2
- 101000830596 Homo sapiens Tumor necrosis factor ligand superfamily member 15 Proteins 0.000 description 2
- 101000611023 Homo sapiens Tumor necrosis factor receptor superfamily member 6 Proteins 0.000 description 2
- 102000008100 Human Serum Albumin Human genes 0.000 description 2
- 108091006905 Human Serum Albumin Proteins 0.000 description 2
- 108010073807 IgG Receptors Proteins 0.000 description 2
- 102000009490 IgG Receptors Human genes 0.000 description 2
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 2
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 108010050904 Interferons Proteins 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 208000011200 Kawasaki disease Diseases 0.000 description 2
- 108060001084 Luciferase Proteins 0.000 description 2
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 108010060408 Member 25 Tumor Necrosis Factor Receptors Proteins 0.000 description 2
- 239000012124 Opti-MEM Substances 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 108010004729 Phycoerythrin Proteins 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000012564 Q sepharose fast flow resin Substances 0.000 description 2
- 102000007000 Tenascin Human genes 0.000 description 2
- 108010008125 Tenascin Proteins 0.000 description 2
- 108090000901 Transferrin Proteins 0.000 description 2
- 102000004338 Transferrin Human genes 0.000 description 2
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 2
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 2
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 2
- 102100040403 Tumor necrosis factor receptor superfamily member 6 Human genes 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000002152 alkylating effect Effects 0.000 description 2
- 239000012491 analyte Substances 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 230000003139 buffering effect Effects 0.000 description 2
- 244000309466 calf Species 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 125000002843 carboxylic acid group Chemical group 0.000 description 2
- 210000000845 cartilage Anatomy 0.000 description 2
- 238000011210 chromatographic step Methods 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 208000037976 chronic inflammation Diseases 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 210000003104 cytoplasmic structure Anatomy 0.000 description 2
- 230000009849 deactivation Effects 0.000 description 2
- 230000001066 destructive effect Effects 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 230000003828 downregulation Effects 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- 102000043656 human TNFSF15 Human genes 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 230000028993 immune response Effects 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 230000010354 integration Effects 0.000 description 2
- 229940079322 interferon Drugs 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 210000000629 knee joint Anatomy 0.000 description 2
- 238000002372 labelling Methods 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 208000001725 mucocutaneous lymph node syndrome Diseases 0.000 description 2
- 238000002703 mutagenesis Methods 0.000 description 2
- 231100000350 mutagenesis Toxicity 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 238000012510 peptide mapping method Methods 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 2
- 229950004354 phosphorylcholine Drugs 0.000 description 2
- PYJNAPOPMIJKJZ-UHFFFAOYSA-N phosphorylcholine chloride Chemical compound [Cl-].C[N+](C)(C)CCOP(O)(O)=O PYJNAPOPMIJKJZ-UHFFFAOYSA-N 0.000 description 2
- 210000004986 primary T-cell Anatomy 0.000 description 2
- 235000004252 protein component Nutrition 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 239000012146 running buffer Substances 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 238000005070 sampling Methods 0.000 description 2
- 238000007423 screening assay Methods 0.000 description 2
- 238000007789 sealing Methods 0.000 description 2
- 230000009291 secondary effect Effects 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 238000002741 site-directed mutagenesis Methods 0.000 description 2
- FQENQNTWSFEDLI-UHFFFAOYSA-J sodium diphosphate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]P([O-])(=O)OP([O-])([O-])=O FQENQNTWSFEDLI-UHFFFAOYSA-J 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000003153 stable transfection Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 229940124530 sulfonamide Drugs 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 235000019818 tetrasodium diphosphate Nutrition 0.000 description 2
- 239000012096 transfection reagent Substances 0.000 description 2
- 239000012581 transferrin Substances 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- FNKGPXOPDRYAAQ-UHFFFAOYSA-K trisodium;3-bis(3-sulfonatophenyl)phosphanylbenzenesulfonate;hydrate Chemical compound O.[Na+].[Na+].[Na+].[O-]S(=O)(=O)C1=CC=CC(P(C=2C=C(C=CC=2)S([O-])(=O)=O)C=2C=C(C=CC=2)S([O-])(=O)=O)=C1 FNKGPXOPDRYAAQ-UHFFFAOYSA-K 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- 230000003313 weakening effect Effects 0.000 description 2
- OZFAFGSSMRRTDW-UHFFFAOYSA-N (2,4-dichlorophenyl) benzenesulfonate Chemical compound ClC1=CC(Cl)=CC=C1OS(=O)(=O)C1=CC=CC=C1 OZFAFGSSMRRTDW-UHFFFAOYSA-N 0.000 description 1
- GOPWHXPXSPIIQZ-FQEVSTJZSA-N (4s)-4-(9h-fluoren-9-ylmethoxycarbonylamino)-5-[(2-methylpropan-2-yl)oxy]-5-oxopentanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](CCC(O)=O)C(=O)OC(C)(C)C)C3=CC=CC=C3C2=C1 GOPWHXPXSPIIQZ-FQEVSTJZSA-N 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- PXFBZOLANLWPMH-UHFFFAOYSA-N 16-Epiaffinine Natural products C1C(C2=CC=CC=C2N2)=C2C(=O)CC2C(=CC)CN(C)C1C2CO PXFBZOLANLWPMH-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 206010000087 Abdominal pain upper Diseases 0.000 description 1
- 206010069754 Acquired gene mutation Diseases 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- HJCMDXDYPOUFDY-WHFBIAKZSA-N Ala-Gln Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCC(N)=O HJCMDXDYPOUFDY-WHFBIAKZSA-N 0.000 description 1
- 206010064539 Autoimmune myocarditis Diseases 0.000 description 1
- 241001288229 Banchus Species 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 101100007328 Cocos nucifera COS-1 gene Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- KDXKERNSBIXSRK-RXMQYKEDSA-N D-lysine Chemical compound NCCCC[C@@H](N)C(O)=O KDXKERNSBIXSRK-RXMQYKEDSA-N 0.000 description 1
- 101150083174 DR3 gene Proteins 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 101710088341 Dermatopontin Proteins 0.000 description 1
- 206010012735 Diarrhoea Diseases 0.000 description 1
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- OVBJJZOQPCKUOR-UHFFFAOYSA-L EDTA disodium salt dihydrate Chemical compound O.O.[Na+].[Na+].[O-]C(=O)C[NH+](CC([O-])=O)CC[NH+](CC([O-])=O)CC([O-])=O OVBJJZOQPCKUOR-UHFFFAOYSA-L 0.000 description 1
- 238000012286 ELISA Assay Methods 0.000 description 1
- YQYJSBFKSSDGFO-UHFFFAOYSA-N Epihygromycin Natural products OC1C(O)C(C(=O)C)OC1OC(C(=C1)O)=CC=C1C=C(C)C(=O)NC1C(O)C(O)C2OCOC2C1O YQYJSBFKSSDGFO-UHFFFAOYSA-N 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 206010015943 Eye inflammation Diseases 0.000 description 1
- 108010021468 Fc gamma receptor IIA Proteins 0.000 description 1
- LLQPHQFNMLZJMP-UHFFFAOYSA-N Fentrazamide Chemical compound N1=NN(C=2C(=CC=CC=2)Cl)C(=O)N1C(=O)N(CC)C1CCCCC1 LLQPHQFNMLZJMP-UHFFFAOYSA-N 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 102220576057 HLA class I histocompatibility antigen, B alpha chain_Y91S_mutation Human genes 0.000 description 1
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 1
- 101100005713 Homo sapiens CD4 gene Proteins 0.000 description 1
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 1
- 101150106931 IFNG gene Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 208000029523 Interstitial Lung disease Diseases 0.000 description 1
- FFFHZYDWPBMWHY-VKHMYHEASA-N L-homocysteine Chemical compound OC(=O)[C@@H](N)CCS FFFHZYDWPBMWHY-VKHMYHEASA-N 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 108010022337 Leucine Enkephalin Proteins 0.000 description 1
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 108010057466 NF-kappa B Proteins 0.000 description 1
- 102000003945 NF-kappa B Human genes 0.000 description 1
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- QZLYAZMKIKMAGP-UHFFFAOYSA-N O.O.[K].[K] Chemical compound O.O.[K].[K] QZLYAZMKIKMAGP-UHFFFAOYSA-N 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 102000007568 Proto-Oncogene Proteins c-fos Human genes 0.000 description 1
- 108010071563 Proto-Oncogene Proteins c-fos Proteins 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- 238000011530 RNeasy Mini Kit Methods 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 239000005864 Sulphur Substances 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 1
- PZBFGYYEXUXCOF-UHFFFAOYSA-N TCEP Chemical compound OC(=O)CCP(CCC(O)=O)CCC(O)=O PZBFGYYEXUXCOF-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 101710187830 Tumor necrosis factor receptor superfamily member 1B Proteins 0.000 description 1
- 102100033733 Tumor necrosis factor receptor superfamily member 1B Human genes 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 239000003875 Wang resin Substances 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- LPQOADBMXVRBNX-UHFFFAOYSA-N ac1ldcw0 Chemical compound Cl.C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN3CCSC1=C32 LPQOADBMXVRBNX-UHFFFAOYSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 238000001261 affinity purification Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 230000003281 allosteric effect Effects 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 238000012197 amplification kit Methods 0.000 description 1
- 238000005571 anion exchange chromatography Methods 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000005875 antibody response Effects 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 210000000436 anus Anatomy 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000002917 arthritic effect Effects 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 210000001754 blood buffy coat Anatomy 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004063 butyryl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 235000019994 cava Nutrition 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000007969 cellular immunity Effects 0.000 description 1
- 230000004700 cellular uptake Effects 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 238000011097 chromatography purification Methods 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000006020 chronic inflammation Effects 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 206010009887 colitis Diseases 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 208000029078 coronary artery disease Diseases 0.000 description 1
- 238000005336 cracking Methods 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000003412 degenerative effect Effects 0.000 description 1
- 206010061811 demyelinating polyneuropathy Diseases 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 238000010612 desalination reaction Methods 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000006334 disulfide bridging Effects 0.000 description 1
- 125000002228 disulfide group Chemical group 0.000 description 1
- AFOSIXZFDONLBT-UHFFFAOYSA-N divinyl sulfone Chemical compound C=CS(=O)(=O)C=C AFOSIXZFDONLBT-UHFFFAOYSA-N 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000004043 dyeing Methods 0.000 description 1
- 230000005014 ectopic expression Effects 0.000 description 1
- 210000003162 effector t lymphocyte Anatomy 0.000 description 1
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 210000003725 endotheliocyte Anatomy 0.000 description 1
- 238000001976 enzyme digestion Methods 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- WBJINCZRORDGAQ-UHFFFAOYSA-N ethyl formate Chemical compound CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 206010016256 fatigue Diseases 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000005558 fluorometry Methods 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 238000001641 gel filtration chromatography Methods 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 150000002337 glycosamines Chemical group 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000008676 import Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 229960000598 infliximab Drugs 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- URLZCHNOLZSCCA-UHFFFAOYSA-N leu-enkephalin Chemical compound C=1C=C(O)C=CC=1CC(N)C(=O)NCC(=O)NCC(=O)NC(C(=O)NC(CC(C)C)C(O)=O)CC1=CC=CC=C1 URLZCHNOLZSCCA-UHFFFAOYSA-N 0.000 description 1
- 108020001756 ligand binding domains Proteins 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 125000003473 lipid group Chemical group 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 206010025135 lupus erythematosus Diseases 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 210000005075 mammary gland Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- AEMBWNDIEFEPTH-UHFFFAOYSA-N n-tert-butyl-n-ethylnitrous amide Chemical compound CCN(N=O)C(C)(C)C AEMBWNDIEFEPTH-UHFFFAOYSA-N 0.000 description 1
- 229960005027 natalizumab Drugs 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 108010068617 neonatal Fc receptor Proteins 0.000 description 1
- 201000008383 nephritis Diseases 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000000065 osmolyte Effects 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 238000007500 overflow downdraw method Methods 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 238000002161 passivation Methods 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 238000001050 pharmacotherapy Methods 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- 239000013636 protein dimer Substances 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000006432 protein unfolding Effects 0.000 description 1
- 230000001185 psoriatic effect Effects 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 238000002708 random mutagenesis Methods 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000011897 real-time detection Methods 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 238000003571 reporter gene assay Methods 0.000 description 1
- 230000000452 restraining effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 238000011764 rheumatoid arthritis animal model Methods 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 239000012723 sample buffer Substances 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- DCKVNWZUADLDEH-UHFFFAOYSA-N sec-butyl acetate Chemical group CCC(C)OC(C)=O DCKVNWZUADLDEH-UHFFFAOYSA-N 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- 238000012882 sequential analysis Methods 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000010532 solid phase synthesis reaction Methods 0.000 description 1
- 230000037439 somatic mutation Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 210000004988 splenocyte Anatomy 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 150000003463 sulfur Chemical class 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000001502 supplementing effect Effects 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 210000001258 synovial membrane Anatomy 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 238000000954 titration curve Methods 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229960004418 trolamine Drugs 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 230000004304 visual acuity Effects 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 210000004916 vomit Anatomy 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/545—Heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70578—NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Transplantation (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本公开内容涉及炎性疾病的治疗。具体地讲,本公开内容涉及可用于治疗炎性疾病的拮抗性DR3配体。
Description
背景
TL1A是由内皮细胞、树突细胞、单核细胞和其它免疫细胞产生的TNF超家族成员。TL1A通过DR3 (一种由活化T细胞和其它免疫细胞表达的TNF受体超家族成员)发出信号。通过TL1A的受体连接导致通过T辅助效应细胞的增殖和细胞因子产生增加。DR3和TL1A涉及RA和CD,因此在治疗炎性疾病例如RA (类风湿性关节炎)和CD (克罗恩病(Crohns Disease))时会需要拮抗DR3诱导的作用。
WO2011106707公开了DR3特异性抗体(11H08)及其包含插入不同抗体构架的11H08 CDR序列(SEQ
ID NO 14+15)的变体。11H08抗体以相对低的亲和力结合DR3,并且它不与CRD1结构域结合。因此,本领域需要可用于治疗炎性疾病的DR3拮抗剂。
概述
针对DR3产生的二价抗体具有激动作用。这些激动性DR3特异性抗体的几个具有阻断DR3与TL1A间的相互作用的能力。由于激动性抗体导致通过T辅助效应细胞的增殖和细胞因子产生增加,因此在有关炎性病症治疗时不期望使用二价DR3抗体。
本发明提供拮抗性DR3配体,其中所述配体对DR3具有单价特异性,且其中所述配体阻断TL1A与DR3结合。这类配体优选来源于二价激动性抗体,并且任选与半寿期延长部分(例如亲脂部分)缀合。这类配体优选具有高亲和力,和/或优选与DR3的CRD1结构域结合。本发明还涉及这类配体治疗炎性疾病的用途。本文表明本发明的DR3配体能够拮抗通过DR3诱导的作用。
附图简述
图 1:本文提及的序列。
图 2 :通过FCM分析的CHOK1SV上的DR3表达。JD3是市售可获得的DR3抗体。
图 3 :用100
µM MSX培养的CHOK1SV上的稳定DR3表达。通过FCM分析的表达。
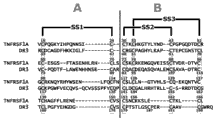
图 4 :TNFR1和DR3胞外域的序列比对。每一行表示富含半胱氨酸的结构域(CRD),该结构域可再被分成A和B亚结构域。突出显示了针对TNFR1测定的CRD中的保守二硫键模式。
图 5 :针对阻断人TL1A与过量表达DR3的CHO细胞结合的能力预筛选的各个小鼠血清。右边条形柱(黑色)是抗TL1A对照(MAB7441 RnD
Biosystems)。
图 6 :通过流式细胞术进行的阻断TL1A:DR3相互作用的抗体的实例。图6A显示与6种阳性DR3抗体的DR3细胞的特异性结合。图6B表示显示4种封闭性抗体和2种非封阻剂(non-blocker)的抑制研究。Y轴表示平均强度荧光。
图 7 :图7A 3种封闭性抗体和作为对照的非封闭DR3特异性ab的滴定曲线——用完全抗体和用Fab表示。
图 8 :在有或没有抗DR3
Fab或mAb时用IL12/IL18
+TL1A刺激的CD4+ T细胞。T细胞增殖在第5天测量。
发明详述
本发明的发明人认识到DR3抗原——其可溶形式及细胞表面表达的形式——的产生被证实是困难的,因为传统方法无一成功。人细胞系中DR3胞外域的重组表达通常导致含有大量寡聚体和高分子量复合物的可溶性蛋白质分泌(另见实施例3)。据推测这些寡聚化蛋白质批次对于免疫而已并不是最优的。与可溶性蛋白质表达最优化(如实施例3所述)的同时,小鼠用过量表达膜结合的DR3的细胞免疫。然而,过量表达DR3的稳定细胞系的产生并不简单。全长DR3中的死亡结构域在稳定转染的过量表达DR3的细胞系中导致细胞死亡,因此必须对全长DR3进行修饰(参见实施例2和5)。已在不同的小鼠品系(BALB/C、RBF和NMRCF1)中进行了免疫以提高抗体库多样性和产生中和性抗DR3
Ab的可能性。
鉴定出几百个DR3结合抗体;这些中仅少数(~2%)能够阻断/抑制DR3:TL1A结合。因此推断具有阻断DR3:TL1A结合的能力的DR3抗体具有拮抗DR3诱导作用的能力。然而,结果的确是所有DR3抗体——不论它们是否具有阻断DR3:TL1A结合的能力——在TL1A存在和不存在时均是激动的(agonistic),它们显然的确在某种程度上模拟TL1A结合诱导的对DR3的作用。
根据这些出人意料的观察结果,本发明人假设,对通过所有DR3抗体发挥的激动作用的解释可能是任何二价DR3抗体可导致DR3群聚,和DR3群聚可能具有诱导胞内DR3信号转导的潜力。这种设想还在有关TNFR家族成员Fas (CD95)和TNFR2的最新出版物(Wang等(2010) Nature
Struc. Mol. Biol. 17,1324-1328;Mukai等(2010) Sci.
Signal. 3,ra83)中得到支持。Wang等人提供了结构数据和解析数据两者,表明了胞内信号转导复合物具有高级次,并含有至少5-7拷贝的受体。类似地,Mukai等人表明受体胞外部分的群聚由配体结合诱导。因此,两种出版物指出,这些TNFR家族成员的高级次群聚可能是信号转导的先决条件。
为了检验该假设,在功能测定法中测定了用木瓜蛋白酶裂解mAb所产生的Fab片段(单价DR3抗体)。来自这些测定法的出人意料的结果是,单价DR3抗体(根据具有阻断/抑制DR3:TL1A结合的能力的DR3抗体制备)在功能测定法中是拮抗性的,即它们具有抑制DR3诱导的作用的能力。因此单价DR3配体/抗体不促进DR3群聚,因此它们不具有激动作用。
不阻止TL1A:DR3相互作用的抗体被用作阴性对照。这种抗体类型在不存在TL1A时在极高浓度下是激动性的,但仅作为mAb。来自这些抗体的相应的Fab不能够阻止TL1A诱导的作用。
定义:
“炎症”是血管组织对有害刺激(例如病原体、受损细胞或刺激物)的复杂的生物反应。炎症是生物消除有害刺激以及启动组织愈合过程的保护性尝试。炎症不是感染的同义词——感染是由外源病原体引起的,而炎症是生物的免疫系统对病原体的反应。
通常,免疫系统能够区分机体正常细胞或“自身”和外来病原体或异常细胞或“异物”。免疫系统丧失识别“自身”为正常的能力并且针对组织或细胞的后续反应的过程,导致耐受性丧失(一种“自身免疫”的状态)。由自身免疫所致病理常常具有严重的临床后果,并且是全世界,尤其是发达国家的主要健康问题之一。
目前可获得生物治疗剂用于治疗某些自身免疫病和/或癌症。例如,类风湿性关节炎患者可用利妥昔单抗(抗CD20)治疗,克罗恩病(Crohn’s disease)患者可用英利昔单抗或那他珠单抗治疗。遗憾的是,接受这些生物制剂任一种的治疗的患者,还会遇到各种副作用和/或是无应答者和/或形成抑制剂。仍然需要特异性靶向病理组织和/或不影响健康组织和/或产生较不严重的副作用和/或产生较少副作用和/或可长期使用和/或不会导致抑制剂形成的备选生物药物。本发明涉及自身免疫病患者和慢性炎性疾病患者中的这些未被满足的需要。
本发明的配体因此适用于治疗炎性疾病和病况例如银屑病、I型糖尿病、格雷夫斯病(Grave’s disease)、炎性肠病(IBD)、克罗恩病、溃疡性结肠炎、肠易激综合征、多发性硬化、类风湿性关节炎(RA)、自身免疫性心肌炎、川崎病(Kawasaki disease)、冠状动脉疾病、慢性阻塞性肺病、间质性肺疾病、自身免疫性甲状腺炎、系统性红斑狼疮(SLE)、硬皮病、全身性硬皮病、银屑病性关节炎、骨关节炎、特应性皮炎、白斑、移植物抗宿主病、斯耶格伦综合征(Sjöogrens’s syndrome)、自身免疫性肾炎、古德帕斯彻综合征(Goodpasture’s syndrome)、慢性炎症性脱髓鞘性多神经病、变态反应、哮喘和其它自身免疫病。
克罗恩病(CD/肉芽肿性/结肠炎)是肠的炎性疾病,可影响胃肠道从口到肛门的任何部位,引起各种症状。其主要引起腹痛、腹泻(其可有血)、呕吐或体重减轻,但还可引起胃肠道以外的并发症例如皮疹、关节炎、眼部炎症、疲劳和注意力缺乏。对于克罗恩病尚无已知的药物或手术疗法。治疗选择局限于控制症状、保持缓解和防止复发。
类风湿性关节炎 (RA) :RA是累及整个身体的全身性疾病,并且是最普通的关节炎形式之一。其特征在于内衬关节的膜的炎症,它引起疼痛、僵硬、发热、发红和肿胀。炎性细胞释放可消化骨和软骨的酶。由于类风湿性关节炎,发炎的关节内衬滑膜可侵入和损害骨和软骨,导致除其它生理作用以外的关节退化和严重疼痛。受累关节可能失去其形状和排列,导致疼痛和运动丧失。
有若干本领域已知的类风湿性关节炎动物模型。例如,在胶原诱发性关节炎(CIA)模型中,小鼠出现十分类似于人类风湿性关节炎的慢性炎性关节炎。由于CIA与RA共享类似的免疫学和病理学特征,因此这使之成为筛选潜在人抗炎化合物的理想模型。
“ DR3 ”有时称为死亡受体3、TRAMP、TNFRSF12、TNFR25、TNFRS25、APO-3、DDR3、LARD、TR3、WSL-1或WSL-LR。人DR3是TNF受体(TNFR)超家族的成员,在胞外域包含4个富含半胱氨酸的基序,在胞质结构域包含“死亡结构域”。人DR3包含SEQ ID 1中规定的氨基酸序列。DR3的胞外域(残基25-199)包含4个富含半胱氨酸的结构域(CRD1、CRD2、CRD3和CRD4)。各CRD通常含有形成3个二硫键的6个半胱氨酸残基。另外,每个CRD可再分为组件A1和B2,其通常在TNFR超家族的常见成员中观察到。
“阻断/抑制/减少DR3与TL1A结合”。本发明的单价配体/抗体具有抑制/阻断/减少DR3:TL1A结合的能力。其可在基于高通量成像的测定法中进行测定。这通过筛选结合DR3转染的CHO细胞的能力和针对野生型细胞的反筛选而在FMAT系统中进行(更多详情描述于实施例4)。如该测定法中测量的一样,如果DR3:TL1A结合降低至少10%、优选至少20%、优选至少25%、优选至少30%、优选至少40%、优选至少50%、优选至少60%、优选至少70%、优选至少75%、优选至少80%、优选至少90%、优选至少95%,最优选约100%,则本发明的单价配体/抗体具有阻断或抑制或减少DR3:TL1A结合的能力。
“延长基团(protractive group)”/“半寿期延长部分”在本文理解为这样的一个或多个化学基团,其与一个或多个氨基酸侧链官能团(例如-SH、-OH、-COOH、-CONH2、-NH2)或者一个或多个N-和/或O-聚糖结构连接并且当与多种治疗性蛋白质/肽缀合时,可延长这些蛋白质/肽的体内循环半寿期。延长基团/半寿期延长部分的实例包括但不限于:生物相容性脂肪酸及其衍生物、羟基烷基淀粉(HAS)例如羟乙基淀粉(HES)、聚乙二醇(Poly Ethylen
Glycol,PEG)、聚(Glyx-Sery)n
(HAP)、透明质酸(HA)、Heparosan聚合物(HEP)、基于磷酰胆碱的聚合物(PC聚合物)、Fleximer、葡聚糖、多聚唾液酸(PSA)、Fc结构域、运铁蛋白、白蛋白、弹性蛋白样肽、XTEN聚合物、白蛋白结合肽、CTP肽及其任何组合。
本发明的“聚二乙醇化DR3配体变体”可具有与DR3配体多肽的任何部分(包括DR3配体多肽的任何氨基酸残基或糖部分)连接的一个或多个PEG分子。可采用化学和/或酶促方法使PEG或其它延长基团与本发明的单价DR3配体上的聚糖缀合。酶促缀合方法的实例描述于例如WO03031464。聚糖可以是天然存在的,或可通过采用本领域众所周知的方法例如插入N联糖基化位点而被插入。本发明“半胱氨酸-聚二乙醇化DR3配体变体”具有与存在于DR3配体中的半胱氨酸的巯基缀合的一个或多个PEG分子。本发明的“半胱氨酸-酰化DR3配体变体”或“半胱氨酸-烷基化DR3配体变体”具有与引入DR3配体的半胱氨酸的巯基缀合的一个或多个疏水半寿期延长部分。此外,有可能使延长性半寿期延长部分与其它氨基酸残基连接。
哺乳动物物种循环血中最丰富的蛋白质组分是血清白蛋白,通常以约3-4.5克/100毫升全血的浓度存在。血清白蛋白是约65,000道尔顿的血液蛋白质,在循环系统中具有若干重要功能。它起血液中存在的各种有机分子的转运蛋白的作用、起整个血液中各种代谢物(例如脂肪酸和胆红素)的主要转运蛋白的作用,并且由于其丰度而起循环血的渗透调节剂的作用。血清白蛋白具有一周以上的半寿期,延长蛋白质的血浆半寿期的一种方法是使蛋白质与结合血清白蛋白的部分缀合。可按J. Med.
Chem., 43, 1986, (2000) (其通过引用结合到本文中)所述来测定白蛋白结合性质。
疏水 / 亲脂半寿期延长部分:本发明的配体优选与性质上主要是亲脂/疏水的半寿期延长部分缀合。在一个优选的实施方案中,疏水半寿期延长部分能够与白蛋白形成非共价复合物(“白蛋白结合剂”),因此促进衍生物随血流循环,还具有延长衍生物的作用时间的作用。因此,整体来看,优选的取代基或部分可称为白蛋白结合部分。
与其与本发明的DR3配体的连接点相比,半寿期延长部分优选位于白蛋白结合部分的相对端或接近白蛋白结合部分的相对端。白蛋白结合部分的其它部分,即半寿期延长部分与肽连接点中间的部分,可称为接头部分、接头、间隔基等。然而,接头的存在是任选的,因此白蛋白结合部分可与半寿期延长部分相同。
在具体的实施方案中,白蛋白结合部分和/或半寿期延长部分是亲脂的,和/或在生理pH (7.4)下带负电荷。
白蛋白结合部分和/或半寿期延长部分可通过缀合化学法例如通过烷基化、酰化或酰胺形成与肽的氨基共价连接;或者例如通过酯化、烷基化与羟基共价连接;或通过肟化与其它基团共价连接。
在一个优选的实施方案中,白蛋白结合部分和/或半寿期延长部分的活性亲硫衍生物与抗DR3
Fab的半胱氨酸残基的巯基共价连接。这类亲硫基团包括但不限于马来酰亚胺、卤代-马来酰亚胺、卤化物(尤其α-卤代乙酰基)、丙烯酰-衍生物(例如丙烯酸酯和丙烯酰胺)、乙烯基砜、反应性二硫基(例如2-吡啶基)。因此,本发明的抗DR3 Fab’优选通过硫醚或二硫键与白蛋白结合部分连接。
可设计本发明的单价抗体,例如Fab’片段,以含有来自构成完整抗体重链硫桥之一的部分的重链的天然存在半胱氨酸残基。该半胱氨酸残基称为C239
(Kabat编号)。半胱氨酸残基还可通过遗传工程插入,但是通过使用天然存在的半胱氨酸残基用于缀合目的,可能有相关安全优势。
在一个优选的实施方案中,在酰胺键形成(该过程称为酰化)的情况下,白蛋白结合部分和/或疏水半寿期延长部分的活性酯与唾液酸残基或唾液酸衍生物的氨基共价连接。
按照本发明十分优选的实施方案,采用酶促方法(例如包括使用唾液酸转移酶的方法),使白蛋白结合部分通过聚糖与配体连接。
对于本发明的目的,术语“白蛋白结合部分”、“半寿期延长部分”和“接头”包括这些分子的未反应以及反应形式。不论是指一种形式还是另一种形式,从使用该术语的上下文来看都是清楚的。
术语“脂肪酸”是指具有4-28个碳原子的脂族一元羧酸,它优选是无支链的,和/或是偶数的,且它可以是饱和的或不饱和的。
术语“脂肪二酸”是指上述定义的但在ω位具有额外羧酸基的脂肪酸。因此,脂肪二酸是二羧酸。
命名法是本领域常用的,例如-COOH和HOOC-是指羧基;-C6H4-是指亚苯基;-CO-和-OC-是指羰基(O=C<);C6H5-O-是指苯氧基;卤化物是指卤素-F、-Cl、-Br、-I和-At。
在一个优选的实施方案中,本发明的白蛋白结合部分包含通过接头和唾液酸残基或唾液酸衍生物与肽或蛋白质连接的脂肪酰基(-(CH2)n-CO-,其中n= 1,2,3,...40)或ω-羧基脂肪酰基(HO2C-(CH2)n-CO-,其中n= 1,2,3,...40)。
在一个优选的实施方案中,本发明的白蛋白结合部分包含通过接头和半胱氨酸残基与肽或蛋白质连接的脂肪酰基(-(CH2)n-CO-,其中n= 1,2,3,...40)或ω-羧基脂肪酰基(HO2C-(CH2)n-CO-,其中n=
1,2,3,...40)。在一个特别优选的实施方案中,n为16或18。
在另一个优选的实施方案中,本发明的白蛋白结合部分包含通过接头和半胱氨酸残基与肽或蛋白质连接的R-(CH2)n-CO-类型的脂肪酰基,其中n= 1,2,3,...40。R是包含酸性基团的基团,例如四唑-5-基或-O-C6H4-COOH。在一个特别优选的实施方案中,n为14或15。
在本发明的情况下,具有-(CH2)12-部分的化合物是可能的白蛋白结合剂。如果这类化合物与蛋白质或肽连接,并导致所述蛋白质或肽的血浆半寿期延长,则要了解白蛋白结合剂可促使血浆半寿期的总体延长。
在一个优选的实施方案中,接头部分如果存在,则具有2-80个C原子,优选5-70个C原子。在其它优选的实施方案中,接头部分如果存在,则具有4-20个杂原子,优选2-40个杂原子,更优选3-30个杂原子。杂原子特别优选的实例为N和O原子。H原子不是杂原子。
在另一个实施方案中,接头包含至少一个OEG分子,和/或至少一个谷氨酸残基,更确切地说相应基团(OEG称为8-氨基-3,6-二氧杂辛酸,即该基团:-NH-(CH2)2-O-(CH2)2-O-CH2-CO-)。
在一个优选的实施方案中,接头部分包含二羧酰胺部分,接头通过硫醚键与半胱氨酸残基连接。在优选的实例中,二羧酰胺部分含有2-30个C原子,优选4-20个C原子,更优选4-10个C原子。
在一个优选的实施方案中,接头部分包含通过酰胺键与唾液酸残基连接的二羧酰胺部分。在优选的实例中,二羧基残基具有2-30个C原子,优选4-20个C原子,更优选4-10个C原子。在其它优选的实例中,二羧基残基具有0-10个杂原子,优选0-5个杂原子。
在另一个优选的实例中,接头部分/间隔基包含含有氨基和通过其远端羧基经由酰胺键与唾液酸残基连接的远端羧基两者的基团。在一个优选的实施方案中,该基团是OEG基团。本文所用术语“亲水间隔基”意指这样的间隔基,其将本发明的单价DR3抗体/配体与白蛋白结合残基用包含至少5个非氢原子(其中30-50%既非N也非O)的化学部分分隔开。优选白蛋白结合残基通过亲水间隔基与Cys残基连接。
氨基酸谷氨酸(Glu)包含2个羧酸基。其γ-羧基优选用于与唾液酸残基或唾液酸衍生物的氨基,或与OEG分子的氨基(如存在的话),或与另一Glu残基的氨基(如存在的话)形成酰胺键。Glu的氨基进而与半寿期延长部分的羧基,或与OEG分子的羧基(如存在的话),或与另一Glu的γ-羧基(如存在的话)形成酰胺键。加入Glu的这种方法偶尔简称为“γ-Glu”。
具有突变的Fc结构域的“Fc融合衍生物”或“Fc融合蛋白”或DR3抗体在本文意指包括与可来源于任何抗体同种型的Fc结构域融合的本发明的DR3配体,但是IgG Fc结构域通常将是优选的,因为IgG抗体的循环半寿期相对较长,优选IgG1和IgG4同种型。此外可对Fc结构域进行修饰以调节某些效应子功能,例如补体结合和/或与某些Fc受体的结合。此外可调节Fc结构域以提高对新生儿Fc受体的亲和力。本发明的DR3配体与具有结合FcRn受体的能力的Fc结构域融合,一般将导致融合蛋白的循环半寿期延长。IgG1 Fc结构域第234、235和237位上的突变一般可导致与FcγRI受体的结合减弱,与FcγRIIa和FcγRIII受体的结合也可能减弱。这些突变不改变与FcRn受体的结合,FcRn受体通过胞吞再循环途径促进长的循环半寿期。优选本发明融合蛋白的修饰IgG1 Fc结构域包含一个或多个下列突变,其分别可导致对某些Fc受体的亲和力降低(L234A、L235E和G237A),和导致C1q介导的补体结合减弱(A330S和P331S)。或者,Fc结构域可以是任选包含S241P/S228P突变的IgG4
Fc结构域。
本文所用术语“抗体”、“单克隆抗体”和“mAb”欲指免疫球蛋白分子及其具有与抗原特异性结合的能力的片段。全长抗体包含4条多肽链,即通过二硫键相互连接的2条重(H)链和2条轻(L)链。每条重链由重链可变区(本文简称为HCVR或VH)和重链恒定区组成。重链恒定区由3个结构域CH1、CH2和CH3组成。每条轻链由轻链可变区(本文简称为LCVR或VL)和轻链恒定区组成。轻链恒定区由一个结构域CL组成。VH和VL区还可再分成超变区,称为互补决定区(CDR),其散布在更保守的称为构架区(FR)的区域内。每个VH和VL由3个CDR和4个FR组成,按以下顺序从氨基端到羧基端排列:FR1、CDR1、FR2、CDR2、FR3、CDR3、FR4。抗体可呈不同同种型的形式;例如IgG (例如IgG1、IgG2、IgG3、IgG4)、IgGA1、IgA2、IgD和IgE。全长抗体通常是二价的(bi-valent/di-valent),即它具有以两个“臂”与抗原结合的能力。相比之下,本发明的单价抗体只包含一个对抗原/DR3有特异性的结合部位。
“Fab区”/“Fab结构域”/“Fab片段”/“Fab”含有界定抗体可结合的特定靶的可变部分。Fab片段是本发明的单特异性/单价DR3配体/DR3抗体的实例。
本发明的单价DR3配体/抗体的实例包括:Fab片段,由VL、VH、CL和CH I结构域组成的单价片段;二价片段,其包含例如通过铰链区的二硫桥连接的两个Fab片段,其中这些Fab片段中仅一个对DR3有特异性;(iii)由VH和CH1结构域组成的Fd片段;(iv)由抗体单臂的VL和VH结构域组成的Fv片段,(v) dAb片段(Ward等(1989) Nature 341:544-546),其由VH结构域组成;(vi)分离的互补决定区(CDR);和(v)对DR3是单价的双特异性抗体。此外,虽然Fv片段的两个结构域VL和VH由不同的基因编码,但可采用重组方法通过使之能够作为单一蛋白质链制备的合成接头将它们连接,其中VL区和VH区配对形成单价分子(称为单链Fv (scFv);参见例如Bird等(1988) Science 242:423-426;以及Huston等(1988) Proc. Natl. Acad. Sci. USA 85:5879-5883)。单链抗体的其它形式(例如双抗体)也包括在术语“单价DR3配体/抗体”内。
“双抗体”是二价双特异性抗体,其中VH和VL结构域在单一多肽链上表达,但使用太短以致于不允许同一链上的两个结构域间配对的接头,从而迫使结构域与另一链的互补结构域配对,并产生两个抗原结合部位(参见例如Hol-liger,P.等(1993) Proc. Natl. Acad. Sci. USA 90:6444-6448;Poljak,R. J.等(1994) Structure 2:1121-1123)。
本文所用术语“人抗体”意指具有来源于人种系免疫球蛋白序列的可变区和恒定区的本发明的单价DR3抗体。本发明的人抗体可例如在CDR中,特别在CDR3中包括非由人种系免疫球蛋白序列编码的氨基酸残基(例如通过体外随机诱变或位点专一诱变或通过体内体细胞突变引入的突变)。
然而,本文所用术语“人抗体”无意包括这样的抗体,其中来源于另一种哺乳动物物种(例如小鼠)种系的CDR序列被移植到人构架序列中,例如所谓的“人源化抗体”或人/小鼠嵌合抗体。人源化单价DR3抗体也是本发明的组成部分。
术语“嵌合单价抗体”是指本发明的单价DR3抗体,其轻链和重链基因通常通过遗传工程从属于不同物种的免疫球蛋白可变区和恒定区基因构建。例如,可将来自小鼠单克隆抗体的基因的可变区段与人恒定区段连接。
本文所用术语“表位”意指单价抗体与之结合的抗原上的任何抗原决定簇。表位决定簇通常由分子(例如氨基酸或糖部分)的化学活性表面群聚组成,常常具有特定的三维结构特征以及特定的电荷特征。用于表征表位的方法的实例包括HX-MS、NMR、X射线、肽步查(peptide walking)、测定法等。术语“抗原互补位”是指识别抗原的抗体的部分。
可根据它们识别或特异性结合的DR3的一个或多个表位或部分,来描述或指定本发明的单价DR3抗体。例如可通过N端和C端位置,或通过连续氨基酸残基的大小来指定一个或多个表位或多肽部分。还可根据其交叉反应性来描述或指定本发明的单价DR3抗体。本文包括不结合多肽的任何其它类似物、直向同源物(ortholog)或同源物的抗体。
“表位框并法(epitope binning)”/”竞争结合测定法”是指利用竞争结合测定法鉴定能够或不能够同时结合DR3的配体/抗体对,从而鉴定结合DR3蛋白上的相同表位或重叠表位(参见实施例10),或因位阻所致不能同时结合的本发明的配体/抗体。框并法(Binning)实验提供存在抗原上完全不同的表位的证据。然而,靠它们自身,它们无法鉴定表位或对表位“作图”至DR3蛋白的特定氨基酸序列或位置。可针对任何配体/抗体或片段对,对结合的竞争进行评价。通常,配体/抗体家族(或框(bin))的有利性质可与由抗体框/竞争基团界定的特定表位的结合相关联。
本文所用术语“免疫反应”或“免疫反应性”意指解离常数Kd低于10-4
M的配体/抗体与其表位的任何结合。适当时,术语“免疫反应”或“免疫反应性”与术语“特异性结合”互换使用。
本文所用术语“亲和力”意指本发明的配体/抗体与表位结合的强度。抗体/配体的亲和力用解离常数Kd测量,解离常数定义为[Ab] x [Ag] /
[Ab-Ag],其中[Ab-Ag]是抗体-抗原复合物的摩尔浓度,[Ab]是未结合抗体的摩尔浓度,[Ag]是未结合抗原的摩尔浓度。亲和常数Ka用1/Kd定义。通过竞争抑制确定抗体特异性和亲和力的优选方法可参见Harlow等,Antibodies:
A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor,
N.Y., 1988);Colligan等主编,
Current Protocols in Immunology, Greene Publishing Assoc. and Wiley
Interscience, N.Y., (1992, 1993);以及Muller,
Meth. Enzymol. 92:589-601 (1983)。
可按本文所述,测量“降低RA患者滑液细胞中的IFN-γ释放”。要了解,在约0.1、0.5、1或5 µg单价抗体/ml的浓度下,采用本文描述的测定条件,RA患者滑液T细胞中的IFN-γ释放降低达至少15%、更优选达至少20%、更优选达至少25%、更优选达至少30%、更优选达至少35%、更优选达至少40%、更优选达至少45%、更优选达至少50%、最优选达至少60%、更优选达至少70%、更优选达至少75%、更优选达至少80%,最优选达至少95%。在反应性患者材料中,本发明的抗体降低RA以及CD患者材料中的干扰素释放(例如IFN-γ)。
可按本文所述,测量“降低来自CD患者肠活检样品的固有层单核细胞(LPMC)中一种或多种细胞因子的释放”。要了解,在约0.1、0.5、1或5 µg单价抗体/ml的浓度下,采用本文描述的测定条件,CD患者LPMC中的细胞因子释放降低达至少15%、更优选达至少20%、更优选达至少25%、更优选达至少30%、更优选达至少35%、更优选达至少40%、更优选达至少45%、更优选达至少50%、最优选达至少60%、更优选达至少70%、更优选达至少75%、更优选达至少80%、最优选达至少95%。在反应性患者材料中,本发明的抗体降低RA以及CD患者材料中的干扰素释放(例如IFN-γ)。
可按本文所述,测量“降低CD4+ T细胞中一种或多种细胞因子的释放”。要了解,在约0.1、0.16、0.5、1或5 µg单价抗体/ml的浓度下,采用本文描述的测定条件,CD4+
T细胞中的细胞因子释放降低达至少15%、更优选达至少20%、更优选达至少25%、更优选达至少30%、更优选达至少35%、更优选达至少40%、更优选达至少45%、更优选达至少50%、最优选达至少60%、更优选达至少70%、更优选达至少75%、更优选达至少80%、最优选达至少95%。
包含本发明的DR3配体的“药物组合物”可以药盒提供,药盒装有包括本发明的配体的容器。治疗性多肽可以用于单剂量或多剂量的注射溶液的形式提供,或作为可在注射前复溶的无菌粉针剂提供。包含本发明配体的药物组合物适于皮下和/或IV给药。本发明的药物组合物可包含一种或多种药学上可接受的载体。
本文所用术语“治疗”是指有需要的任何人或其它动物受试者的药物疗法。预期医学或兽医学从业人员已对所述受试者进行了身体检查,所述从业人员给出了表明采用所述具体治疗有益于所述人或其它动物受试者的健康的试验性或决定性诊断。根据受试者的健康现状,所述治疗的时机和目的可在一个个体与另一个间变化。因此,所述治疗可以是预防性的、治标性的、针对症状的和/或治疗性的。
就本发明而言,预防性、治标性、针对症状的和/或治疗性治疗可代表本发明的各个方面。
本发明的配体可连同其它药物(例如甲氨蝶呤、地塞米松和泼尼松)和/或其它生物药物一起给予。
单价DR3抗体/配体可用重组技术产生。通常将编码本发明的单价DR3抗体/配体的DNA序列插入重组载体。载体优选为表达载体,其中DNA序列与DNA转录所需要的额外区段以及能够指导克隆基因或cDNA在所需宿主细胞中转录的启动子有效连接。
在细胞摄取DNA后,使它们在合适的生长培养基中生长,通常为1-2天,以开始表达目标基因。向其中导入编码单价DR3抗体/配体的DNA序列的宿主细胞可以是任何细胞,包括酵母、真菌、细菌和高级真核细胞。用于本发明的哺乳动物细胞系的实例为COS-1、幼仓鼠肾(BHK)和293。优选的BHK细胞系为tk-ts13 BHK细胞系,其可称为BHK 570细胞。另外,本发明内可使用多种其它细胞系,包括大鼠Hep I、大鼠Hep II、TCMK、NCTC 1469、CHO和DUKX细胞。
然后在允许单价DR3抗体/配体表达的条件下,将上述转化或转染的宿主细胞在合适的营养培养基中培养,之后可从培养物中回收所得肽的全部或部分。然后可通过常规方法(包括通过离心或过滤从培养基中分离宿主细胞;通过盐(例如硫酸铵)沉淀上清液或滤液的蛋白质性组分;根据所述多肽的类型,通过多种层析法(例如离子交换层析法、凝胶过滤层析法、亲和层析法等)纯化),从培养基中回收由细胞产生的单价DR3抗体/配体。
可采用转基因动物技术以产生本发明的单价DR3抗体/配体。优选在宿主雌性哺乳动物(优选绵羊、山羊或牛)乳腺内产生蛋白质。也可采用在转基因植物中的产生。表达可定向于特定器官,例如结节。
还可在上述产生的二价抗体的基础上获得单价DR3抗体,随后进行肽酶消化和所得Fab片段的分离。
随后可对单价DR3抗体/配体进行翻译后修饰以获得体内循环半寿期延长的蛋白质。
实施方案列表:
以下是本发明实施方案的列表。该实施方案列表并非限制性的,要了解本发明包括下列实施方案的任何组合。
实施方案 1 :一种单价拮抗性DR3抗体,其中所述单价抗体阻断DR3与TL1A结合,其中呈其二价形式的所述单价抗体是阻断DR3与TL1A结合的激动性抗体。
实施方案 2 :实施方案1的单价抗体,其中所述单价抗体不是具有WO2011106707所示11H08抗体的CDR序列(SEQ ID NO 14-15)的抗体。
实施方案 3 :实施方案1-2中任一个的单价抗体,其中所述单价抗体与亲脂部分缀合。
实施方案 4 :实施方案3的单价抗体,其中所述亲脂部分包含-(CH2)n-CO-脂肪酰基,其中n为16-18。
实施方案 5 :实施方案3的单价抗体,其中所述亲脂部分包含-(CH2)n-CO-脂肪酰基,其中n为15。
实施方案 6 :实施方案3-5中任一个的单价抗体,其中所述抗体与选自以下式(I)、(II)、(III)、(IV)、(V)和(VI)的亲脂部分缀合:
(VI)
实施方案 7 :实施方案3-6中任一个的单价抗体,其中所述亲脂部分通过亲水间隔基与抗体重链中的天然存在的半胱氨酸残基、优选C239
(Kabat编号)半胱氨酸残基连接。
实施方案 8 :前述实施方案中任一个的单价抗体,其中所述抗体与DR3上的表位结合,其中所述表位包含SEQ
ID NO 1的I43和/或L45。
实施方案 9 :前述实施方案中任一个的单价抗体,其中所述抗体与DR3上的表位结合,其中所述表位包含SEQ
ID NO 1所示氨基酸G37-L45的至少一个和氨基酸L57-A59的至少一个。
实施方案 10 :实施方案9的单价抗体,其中所述表位包含SEQ ID NO 1所示的氨基酸G37-L45和氨基酸L57-A59。
实施方案 11 :前述实施方案中任一个的单价抗体,其中所述配体是Fab片段。
实施方案 12 :前述实施方案中任一个的单价抗体,其中所述单价抗体以低于1 nM的解离常数结合DR3。
实施方案 13 :实施方案12的单价抗体,其中所述单价抗体以低于500
pM、优选低于300 pM、优选低于100
pM、最优选低于30 pM的解离常数结合DR3。
实施方案 14 :前述实施方案中任一个的单价抗体,其中所述抗体与人DR3的CRD1结构域结合。
实施方案 15 :一种单价抗体,或者二价抗体,其包含SEQ ID NO 16所示的3个CDR序列和SEQ ID NO 17所示的3个CDR序列。在另一个实施方案中,本发明的单价抗体包含SEQ
ID NO 10所示的3个CDR序列和SEQ ID NO 11所示的3个CDR序列。
实施方案 16 :一种单价抗体或者二价抗体,其中所述抗体包含人构架、SEQ ID NO 16所示CDR3序列和SEQ ID NO 17所示CDR3序列以及重链中的“S49A”回复突变。
实施方案 17 :实施方案16的单价抗体,其中所述抗体包含SEQ ID NO 16所示的3个CDR序列和SEQ ID NO 17所示的3个CDR序列。在另一个实施方案中,本发明的单价抗体包含分别由SEQ
ID NO 16和17所示的重链和轻链。
实施方案 18 :实施方案15-17中任一个的单价抗体,其中所述抗体是IgG4同种型。
实施方案 19 :前述实施方案中任一个的单价抗体,其中所述抗体与单价抗体“0228”竞争结合人DR3,其中0228重链的氨基酸序列如SEQ ID NO 16所示,0228轻链的氨基酸序列如SEQ ID NO 17所示。在另一个实施方案中,抗体与0228抗体结合相同的表位。
实施方案 20 :实施方案1-14中任一个的单价抗体,其中所述抗体包含SEQ
ID NO 12所示的3个CDR序列和SEQ ID NO 13所示的3个CDR序列。
实施方案 21 :本发明的单价抗体,其中所述抗体与单价抗体0124竞争结合人DR3,其中0124重链的氨基酸序列如SEQ ID NO 12所示,轻链的氨基酸序列如SEQ ID NO 13所示。在另一个实施方案中,抗体与0124抗体结合相同的表位。
实施方案 22 :一种单价抗体或者二价抗体,其中所述抗体包含SEQ ID NO 18所示的3个CDR序列和SEQ ID NO 19所示的3个CDR序列。
实施方案 23 :本发明的单价抗体,其中所述抗体与单价抗体0130竞争结合人DR3,其中0130重链的氨基酸序列如SEQ ID NO 18所示,0130轻链的氨基酸序列如SEQ ID NO 19所示。在另一个实施方案中,抗体与0130抗体结合相同的表位。
实施方案 24 :一种单价抗体或者二价抗体,其中所述抗体包含SEQ ID NO 20所示的3个CDR序列和SEQ ID NO 21所示的3个CDR序列。(0143)。
实施方案 25 :本发明的单价抗体,其中所述抗体与单价抗体0143竞争结合人DR3,其中0143重链的氨基酸序列如SEQ ID NO 20所示,0143轻链的氨基酸序列如SEQ ID NO 21所示。在另一个实施方案中,所述抗体与0143抗体结合相同的表位。
实施方案 26 :一种单价抗体或者二价抗体,其中所述抗体包含SEQ ID NO 22所示的3个CDR序列和SEQ ID NO 23所示的3个CDR序列。(0152)。
实施方案 27 :本发明的单价抗体,其中所述抗体与单价抗体0152竞争结合人DR3,其中0152重链的氨基酸序列如SEQ ID NO 22所示,0152轻链的氨基酸序列如SEQ ID NO 23所示。在另一个实施方案中,所述抗体与0152抗体结合相同的表位。
实施方案 28 :本发明的单价抗体,其中所述抗体降低RA患者滑液细胞中的IFN-γ释放,其中所述滑液细胞用TL1A共刺激。优选细胞是IL-12/IL-18活化的。
实施方案 29 :本发明的单价抗体,其中所述抗体降低CD患者肠活检样品固有层单核细胞(LPMC)的一种或多种细胞因子的释放,其中所述细胞因子选自:IL-6、TNF-α、GM-CSF和IFN-γ,且其中所述LPMC用TL1A、IL-12和IL-18共刺激。优选细胞是IL-12/IL-18活化的。
实施方案 30 :本发明的单价抗体,其中所述抗体降低CD4+ T细胞中一种或多种细胞因子的释放,其中所述细胞因子选自:TNF-α、IL-6、GM-CSF和IFN-γ,且其中所述T细胞用TL1A共刺激。优选细胞是IL-12/IL-18活化的。
实施方案 31 :前述实施方案中任一个的单价抗体,其中所述抗体是IgG4型抗体。
实施方案 32 :前述实施方案中任一个的单价抗体,其中所述抗体与选自以下一种或多种的一个或多个半寿期延长部分缀合:脂肪酸及其衍生物、羟乙基淀粉(HES)、聚乙二醇(PEG)、透明质酸(HA)、heparosan聚合物、基于磷酰胆碱的聚合物、fleximer、葡聚糖、多聚唾液酸(PSA)、Fc结构域、运铁蛋白、白蛋白、弹性蛋白样肽、XTEN聚合物、白蛋白结合肽及其任何组合。由此得出结论,本发明的单价抗体可与两种或更多种不同类型的半寿期延长部分缀合。
实施方案 33 :本发明的单价抗体,其中所述单价抗体包含效应子功能降低的Fc结构域或稳定性提高的Fc结构域。优选Fc结构域是包含1、2、3、4个或所有下列突变的IgG1 Fc结构域:L234A、L235E、G237A、A330S和P331S)。或者,Fc结构域可以是优选包含S241P/S228P突变的IgG4
Fc结构域。
实施方案 34 :本发明的单价抗体,其中所述单价抗体通过聚糖、优选通过唾液酸与半寿期延长部分缀合。
实施方案 35 :本发明的单价抗体,其中所述抗体是人抗体。
实施方案 36 :本发明的单价抗体,其中所述抗体是人源化抗体。
实施方案 37 :本发明的单价抗体,其中所述抗体阻断一个或多个DR3配体的结合。似乎可能的是DR3与TL1A以外的其它配体结合。然而,尚未鉴定出这类配体。
实施方案 38 :本发明的单价抗体(优选包含与27F16A1抗体基本相同的抗原互补位),其中所述抗体包含SEQ ID NO 8中的CDR序列的至少一个和SEQ ID NO 9所示CDR序列的至少一个。优选所述抗体包含SEQ
ID NO 8所示CDR序列的2个和SEQ ID NO 9所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的3个和SEQ ID NO 9所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的至少一个和SEQ ID NO 9所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的至少一个和SEQ ID NO 9所示CDR序列的3个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的1个和SEQ ID NO 9所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的2个和SEQ ID NO 9所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 8所示CDR序列的3个和SEQ ID NO 9所示CDR序列的3个。本发明的这类抗体的任一种可包含这类CDR序列的1、2、3、4、5或6个,其中该CDR序列或这些CDR序列的一个或两个氨基酸已缺失或添加,或突变成不同的氨基酸残基——因此导致与SEQ ID NO 8和SEQ ID NO 9所示CDR序列相比,在一个或多个位置上不同的一个或多个CDR序列。
实施方案 39 :本发明的单价抗体,其中所述抗体与单价抗体27F16A1竞争结合人DR3,其中27F16A1重链的氨基酸序列如SEQ ID NO 8所示,27F16A1轻链的氨基酸序列如SEQ ID NO 9所示。在另一个实施方案中,本发明涉及与27F16A1抗体结合相同表位的抗体。
实施方案 40 :本发明的单价抗体(优选包含与27F44A2抗体基本相同的抗原互补位),其中所述抗体包含SEQ ID NO 10中CDR序列的至少一个和SEQ ID NO 11所示CDR序列的至少一个。优选所述抗体包含SEQ
ID NO 10所示CDR序列的2个和SEQ ID NO 11所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 10所示CDR序列的3个和SEQ ID NO 11所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 10所示CDR序列的至少一个和SEQ ID NO 11所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 10所示CDR序列的至少一个和SEQ ID NO 11所示的3个CDR序列。更优选所述抗体包含SEQ ID NO 10所示CDR序列的1个和SEQ ID NO 11所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 10所示CDR序列的2个和SEQ ID NO 11所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 10所示CDR序列的3个和SEQ ID NO 11所示CDR序列的3个。本发明的这类抗体的任一种可包含这类CDR序列的1、2、3、4、5或6个,其中该CDR序列或这些CDR序列的一个或两个氨基酸已缺失或添加,或突变成不同的氨基酸残基——因此导致与SEQ ID NO 10和SEQ ID NO 11所示CDR序列相比,在一个或多个位置上不同的一个或多个CDR序列。
实施方案 41 :本发明的单价抗体,其中所述抗体与单价抗体27F44A2竞争结合人DR3,其中27F44A2重链的氨基酸序列如SEQ ID NO 10所示,轻链的氨基酸序列如SEQ ID NO 11所示。在另一个实施方案中,本发明的抗体与27F44A2抗体结合相同的表位。
实施方案 42 :本发明的单价抗体(优选包含与28F26A3抗体基本相同的抗原互补位),其中所述抗体包含SEQ ID NO 12中CDR序列的至少一个和SEQ ID NO 13所示CDR序列的至少一个。优选所述抗体包含SEQ
ID NO 12所示CDR序列的2个和SEQ ID NO 13所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 12所示CDR序列的3个和SEQ ID NO 13所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 12所示CDR序列的至少一个和SEQ ID NO 13所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 12所示CDR序列的至少一个和SEQ ID NO 13所示的3个CDR序列。更优选所述抗体包含SEQ ID NO 12所示CDR序列的1个和SEQ ID NO 13所示CDR序列的1个。更优选所述抗体包含SEQ ID NO 12所示CDR序列的2个和SEQ ID NO 13所示CDR序列的2个。更优选所述抗体包含SEQ ID NO 12所示CDR序列的3个和SEQ ID NO 13所示CDR序列的3个。本发明的这类抗体的任一种可包含这类CDR序列的1、2、3、4、5或6个,其中该CDR序列或这些CDR序列的一个或两个氨基酸——因此导致与SEQ ID NO 12和SEQ ID NO 13所示CDR序列相比,在一个或多个位置上不同的一个或多个CDR序列。
实施方案 43 :本发明的单价抗体,其中所述抗体与单价抗体28F26A3竞争结合人DR3,其中28F26A3重链的氨基酸序列如SEQ ID NO 12所示,28F26A3轻链的氨基酸序列如SEQ ID NO 13所示。在另一个实施方案中,抗体与28F26A3抗体结合相同的表位。
实施方案 44 :一种编码本发明的单价抗体或配体的DNA分子。
实施方案 45 :一种表达载体,其包含实施方案44的DNA分子。
实施方案 46 :一种宿主细胞,其包含实施方案45的表达载体或实施方案44的DNA分子。
实施方案 47 :一种用于制备本发明的配体或抗体的方法,其中所述方法包括实施方案46的宿主细胞的温育。
实施方案 48 :一种药物组合物,其包含本发明的化合物。所述组合物任选包含至少一种药学上可接受的载体/赋形剂。
实施方案 49 :本发明的配体或本发明的药物组合物作为药物的用途。
实施方案 50 :用于治疗炎性疾病的本发明的配体或本发明的药物组合物的用途。
实施方案 51 :用于治疗RA的本发明的配体或本发明的药物组合物的用途。
实施方案 52 :用于治疗克罗恩病(CD)的本发明的配体或本发明的药物组合物的用途。
实施方案 53 :用于治疗溃疡性结肠炎(UC)的本发明的配体或本发明的药物组合物的用途。
实施方案 54 :一种治疗炎性疾病的方法,其中所述方法包括将本发明的配体或本发明的药物组合物给予有需要的人。炎性疾病优选为RA、克罗恩病或溃疡性结肠炎。
虽然本文举例说明和描述了本发明的某些特征,但是本领域普通技术人员可以马上想起许多修改、取代、变化和等同内容。因此要了解,随附权利要求书欲涵盖落入本发明真实精神内的所有这类修改和变化。
实施例
实施例
1
免疫和杂交瘤产生
如下列实施例所述,由于该蛋白质富含半胱氨酸的性质,因此难以产生高品质的可溶形式的全长DR3。DR3的可溶形式趋于高度聚集,这可能导致屏蔽重要的配体结合区,使之在免疫时难以产生所需要的抗体应答。使用可溶性全长DR3蛋白、仅含DR3的ECD的部分(像例如仅用CRD1结构域免疫)的DR3蛋白衍生物两者和DR3表达细胞(如实施例3所述)用于免疫,进行了全面的免疫方案以获得稳固的抗DR3抗体(Ab)血清效价。免疫在不同的小鼠品系(BALB/C、RBF和NMRCF1)中进行,以提高抗体库多样性和产生中和性抗DR3
Ab的可能性。在一个实例中,在有或没有不完全弗氏佐剂(IFA)的情况下,用5x106 DR3表达CHO细胞腹膜内(IP)给BALB/C小鼠免疫8次,接着用含纯化的hDR3-Fc (参见实施例3)的IFA IP免疫6次。按实施例4所述,通过FACS,针对DR3/hTL1A封闭性抗体,对小鼠血清进行筛选。具有DR3/hTL1A封闭性Ab效价的小鼠接受最终的加强免疫,加强免疫由使用DR3-mFc在尾静脉中的单次静脉内注射(i.v.)组成。加强免疫后3天,处死小鼠,通过标准电融合方法,使脾细胞与X63Ag8653骨髓瘤细胞融合。将融合细胞接种在96孔板中,并在补充FCS
(Hyclone)的DMEM (Invitrogen)和HAT选择培养基中培养一周,然后筛选DR3/hTL1A封闭性mAb。
实施例
2
用于筛选和免疫的细胞
使过量表达跨膜(TM) DR3的细胞开发成用于基于细胞的筛选测定法和用于小鼠免疫的基本工具。
过量表达TM DR3的稳定细胞系的产生并不简单。将包括TM和死亡结构域(DD)的最初的全长DR3 (有关完整AA序列参见SEQ ID NO 1)克隆至pcDNA3.1表达载体(Invitrogen),使用该载体转染Ba/F3细胞。然而,全长DR3中的DD导致稳定细胞系的细胞死亡。完全不可能表达具有活性DD的全长DR3。为了使DR3中的DD钝化,且仍能够表达跨膜DR3蛋白,设计并开发出两种新的构建体。按照Itoh和Nagata,JBC (268) 第10932-10937页,1993的SEQ ID NO 1中的突变(L356N),Itoh和Nagata描述了CD95的类似突变形式,其中突变导致受体失活。SEQ ID NO 1中DD的缺失(△M339-P417)按照Screaton等,PNAS (94) 第4615-4619页,1997来测定。将截短形式和突变形式两者克隆至pcDNA3.1,并在Ba/F3中表达。这产生过量表达表面DR3的两个稳定细胞系。从流式细胞术(FCM)分析来看,发现DR3的表达水平在用DR3的截短形式开发的细胞系中最高。然而,表达水平对用于筛选测定法的细胞系而言仍太低。因此决定研究来自Lonza的GS-CHO系统(Basel,Switzerland)是否可用于表达DR3的截短形式。将pcDNA3.1的编码cDNA转移至Lonza表达载体pEE14.4中。
按照Lonzas生产商的方案,建立稳定的CHOK1SV细胞。CHOK1SV细胞通过电穿孔转染。在转染前,通过用AcII限制性内切酶消化,使pEE14.4质粒线性化。通过电穿孔,使用10 µg的AcII消化的pEE14.4质粒转染1x107个CHOK1SV细胞。将细胞接种至T75培养瓶中。转染后当天,通过在不含glutamax
(Invitrogen)的CD-CHO培养基中加入L-甲硫氨酸亚砜亚胺(MSX)至50 µM的最终浓度,开始选择。转染后3周,细胞通过使用lympholyte-mammal
(Cedarlane)进行纯化,转移至摇瓶中,在37℃、8% CO2和125 rpm下的培养箱振荡器中培养。选择压力从该点下降至25 µM
MSX。通过FCM分析DR3表达。然而,DR3表达水平极低,决定通过荧光激活细胞分选法(FACS)分选该库以提高表达水平。FACS后4天,通过FCM针对DR3表达对该库进行测试,首次DR3表达良好(图2)。遗憾的是,在2-3周后,DR3表达水平开始降低,细胞不能再用于筛选。
在提高DR3水平和使该库更稳定的尝试中,通过提高至50 µM和100 µM来对MSX选择压力进行研究,另外,在4 X 96W板中用½细胞/孔亚克隆该库。亚克隆产生通过FCM分析的具有高DR3表达水平的两种克隆。然而1-3周后,克隆开始再次丧失表达并显得不稳定,因此不能用于筛选。对于该库提高MSX选择至100 µM导致极好的高表达水平,另外这可随时间推移保持高的表达水平(图3)。
因此,用于筛选和免疫的所得细胞系是用截短的DR3转染并在CD-CHO
+ 100 µM MSX中培养的CHOK1SV。
实施例
3
可溶性
DR3
的表达和纯化
人DR3是极富含半胱氨酸的蛋白质,在胞外域(ECD,残基25-199)中包含4个富含半胱氨酸的结构域(CRD1、CRD2、CRD3和CRD4),在胞质结构域中包含“死亡结构域” (DD)。按照Banner等,Cell (73) 第431-445页,(1993),各CRD通常含有形成3个二硫键的6个半胱氨酸残基。另外,各CRD可再分成在TNFR超家族的常规成员中观察到的组件A1和B2 (J.H.Naismith等,Trends Biochem. Sci. (23) 第74-79页,1998)。具有预测的CRD及组件A1和B2的DR3的序列见图4。
可溶性DR3的产生非常困难,这可能是因为蛋白质的高半胱氨酸含量所致。由于分子间二硫键的形成,人细胞系中DR3的ECD的重组表达通常导致含有大量寡聚体和高分子量复合物的可溶性蛋白质的分泌。这些蛋白质批次不结合TL1A,且在细胞测定中无活性。
采取不同方法解决聚集问题。最初,使DR3的完整ECD
(25-199)与小鼠IgG1或人IgG4的Fc结构融合。在HEK293中的瞬时产生导致低的产量(<10 mg/L)和高的聚集度。凝胶过滤允许富集预期的二聚体,但是由于低产量和高寡聚度,最初不可能获得纯流分。还测定了其它纯化标签例如生物素化、FLAG-标签或三聚肽、生腱蛋白C (TNC),但是未改进结果。
另外,对仅含DR3 ECD的部分的DR3-Fc融合蛋白进行了改造,以确定负责寡聚化的蛋白质的部分。如下设计了4种蛋白质:
DR3 (CRD1)-Fc (SEQ ID NO 2)
DR3 (CRD1+ A1)-Fc (SEQ ID NO 3)
DR3 (CRD1+CRD2)-Fc (SEQ ID NO 4)
DR3 (CRD1+CRD2+A1)-Fc (SEQ ID NO 5)
分子间二硫键的形成和由此产生的错折叠与DR3 ECD长度增加相关,可能反映出半胱氨酸数增加。同时,蛋白质表达的收率随DR3 EC结构域长度增加而降低。对于所有的这些构建体,凝胶过滤允许主要二聚体部分的纯化;然而,蛋白质没有生物活性。除该构建体以外,还制备了多种截短和cys缺失构建体,以试图准确找出负责寡聚化的单个半胱氨酸或小区域。然而,无单一区域或特定的半胱氨酸似乎负有责任,整个DR3序列似乎难以按可溶性形式表达。
另外,产生了谷胱甘肽S-转移酶(GST)与DR3的CRD1间的融合蛋白,其是同基因的(SEQ ID NO 6)。
DR3-Fc
(其包含DR3的ECD、含有TEV切割位点的接头和人IgG4的Fc部分),在中国仓鼠卵巢(CHO)细胞中的稳定表达提高表达水平,并允许主要二聚体的蛋白质(SEQ
ID NO 7)分离。在测量TL1A诱导的DR3信号转导的报道基因测定法中,该部分可与TL1A竞争结合DR3。
使用多种这类蛋白质免疫小鼠。一些蛋白质批次被进一步纯化以分离出少量的非寡聚化DR3。这些批次被用于表面等离子共振(SPR)结合测定法。
HEK293
细胞中的瞬时表达
载体:
通过使用基于CMV启动子的表达载体(pTT载体),表达了DR3蛋白的所有变体。制备pTT载体用于在Yves Durocher
(Durocher等Nucleic Acid Research,2002)开发的基于HEK293-6E EBNA的表达系统中瞬时表达。
细胞维持:
使HEK293-6E细胞在补充25 μg/ml遗传霉素(Gibco)、1% v/v表面活性剂Pluronic F-68
(Gibco)和1% v/v青霉素-链霉素(Gibco)的FreeStyle™ 293表达培养基(Gibco)中悬浮生长。在振荡培养箱中在37℃、8% CO2和125 rpm下,将细胞在Erlenmeyer摇瓶中培养,保持细胞密度介于0.1-1.5 x 106个细胞/ml之间。
DNA转染:
• 用于转染的培养物的细胞密度为0.9-1.1 x 106细胞/ml。
• 每ml细胞培养物使用1 μg DNA。
• 将DNA在Opti-MEM培养基(Gibco)中稀释成30μl培养基/μg DNA,混合,并在室温(23-25℃)温育5分钟。
• 浓度为1 μl/μg DNA的293Fectin™ (Invitrogen)用作转染试剂。
• 将293Fectin™在Opti-MEM培养基(Gibco)中稀释30X,混合,并在室温(23-25℃)下温育5分钟。
• 将DNA和293Fectin溶液混合,置于室温(23-25℃)下温育25分钟。
• 然后将DNA-293Fectin混合物直接加入细胞培养物中。
• 将转染的细胞培养物转移至37℃、8% CO2和125 rpm的振荡培养箱中。
• 转染后5-6天,通过离心,接着经0.22 μm PES过滤器(Corning)过滤,来收获细胞培养上清液。
• 如有可能,采用ForteBio Octet系统和A蛋白生物传感器,通过Biolayer干涉测量法,对蛋白质产生进行定量分析。
DR3-Fc
蛋白质的纯化
将细胞上清液直接上样至具有A蛋白亲和珠粒(MAbelect
Sure;GE Healthcare)的柱上,以20mM Tris/HCl,pH
8.5为缓冲液。结合的蛋白质用10 mM、50 mM和100 mM甲酸钠(pH 3.5)逐步洗脱。洗脱的流分经浓缩,通过超滤转移至PBS缓冲液。凝胶过滤在Superdex200柱(GE
Healthcare)中进行,以PBS为缓冲液。合并含有二聚体蛋白质的流分,通过超滤浓缩。所有层析步骤用Äkta
Explorer FPLC仪器(GE Healthcare)进行。
实施例
4
阻断
TL1A:DR3
相互作用的抗体的筛选
小鼠血清的预筛选
证明在进行融合前针对阻断作用对小鼠血清进行预筛选是必需的,因为小鼠在血清中的阻断作用程度上具有极大的差异。
小鼠用过量表达DR3的细胞系和DR3蛋白两者免疫。进行了全面的免疫方案,以获得具有不同抗体库的不同小鼠。与单一抗原免疫不同,完整细胞免疫包括注射多种抗原。之前已表明,当使用完整细胞免疫时,需要更多的免疫优化,因为不同的免疫方案产生不同的抗体库。针对阻断作用筛选小鼠血清已成为针对融合选择小鼠的重要工具(图5)。
杂交瘤上清液的筛选
为了选出具有阻断TL1A结合的能力的针对DR3的抗体,筛选计划如下:
作为DR3特异性抗体的初步试验,建立了基于高通量成像的测定法。这通过针对结合DR3转染的CHO细胞的能力进行筛选和针对野生型细胞进行反筛选在FMAT系统中进行(有关DR3细胞系的产生参见实施例2)。
通过将50 μl细胞制备物(50000个细胞/孔,50 μl)与25 μl滴定中稀释的单克隆抗体或未稀释的杂交瘤上清液一起在96孔板(Greiner,目录号65021)中标记,并在4℃下温育1小时来进行测定。温育和洗涤(含5%胎牛血清的PBS缓冲液,在200g下离心5分钟)后,每孔加入50 μl第二抗体(在PBS缓冲液中1:400稀释),在4℃下另温育1小时。当从RBF小鼠或Balb/c小鼠Jacksons #
115-136-071 1:400筛选时,使用APC抗小鼠。
最后,细胞经洗涤,并转移到黑色FMAT板中,在测量荧光的PerkinElmer
Envision Turbo (FMAT)上读数。
初始筛选的下一部分是测定阻断DR3配体(TL1A)结合的能力。这通过针对阻断TL1A-flag标签结合DR3转染细胞的能力筛选阳性杂交瘤上清液,而在选定的DR3特异性杂交瘤上清液中进行。作为对照,使用未转染细胞无关抗体或上清液。
通过将50 μl在滴定中稀释的单克隆抗体或未稀释的杂交瘤上清液加入DR3阳性细胞(50000个细胞/孔)中,并在4℃下温育1小时,来进行基于FCM的抑制测定。在温育和洗涤(含5%胎牛血清的PBS缓冲液,在200g下离心5分钟)后,将TL1A-flag标签(浓缩,总体积为50 μl)加入96孔板(Greiner,目录号65021)中。再次在温育和洗涤后,加入第二抗体(APC抗FLAG标签ab,得自Perkin Elmer,最终浓度5 µg/ml) (在PBS缓冲液中1:400稀释),在4℃下另温育1小时。
平行地,如实施例5中所述进行报道基因测定,以检测抗体的激动或拮抗功能性。
内部产生的TL1A是TL1A的成熟胞外域。TL1A含有N端FLAG-HIS-TEV标签。在FACS/FMAT中,FLAG-标签用于检测,HIS-标签用于纯化,而TEV位点允许任选的TEV切割并除去标签。在大肠杆菌中产生的TL1A是市售的,可获自R&D
Systems。内部TL1A在HEK细胞中产生,含有两个N->Q点突变以破坏可能的N-糖基化位点。类似地产生重组弥猴TL1A。
实施例
5
DR3
报道基因测定
Chinnaiyan等人1996 (Science
1996年, 第274卷, 第5289期第990-992页)报告了DR3通过NFκB发出信号,并且当DR3在MCF7细胞中异位表达时诱导细胞凋亡。我们希望利用NFκB信号转导作为报道分子,并使用降低的DR3表达以避免凋亡的细胞。
HEK293细胞系用人DR3表达质粒和NFκB-萤光素酶报道质粒稳定转染。DR3表达质粒以pcDNA3.1 (hygro)+为基础,并且含有受SV40启动子调节的潮霉素抗性基因,除去CMV启动子,插入2个热激元件(HSE),最小c-fos启动子和人DR3编码序列。报道分子以pGL3-basic为基础,Luc+反应受3个NFκB位点和最小干扰素启动子调节。将受SV40启动子调节的新霉素抗性基因插入载体。
在40 ng/ml TL1A (R&D Systems)刺激时,名为I5的DR3/HEK293报道基因细胞,在萤光素酶活性方面产生20-25倍反应。检测TL1A、激动抗体和拮抗抗体/Fab的作用的方法如下。以20,000个细胞/孔将I5细胞接种在聚D-赖氨酸包被的黑色视野96孔板中。次日,将TL1A或培养基加入各孔中,在4小时温育后,使用Steady-GLO试剂盒(Promega),通过TopCount NXT (Perkin Elmer)仪器监测发光。为了测定中和作用,将抗体或Fab与细胞一起预孵育15分钟后,加入TL1A。
对于杂交瘤上清液的筛选,至少一式两份,并使用0 ng/ml、10
ng/ml TL1A和50 ng/ml TL1A,来测定所有样品。
实施例
6
阻断
TL1A:DR3
相互作用的抗体和
Fab
鉴定出对DR3有特异性且对于阻断TL1A与DR3相互作用被测定为阳性的单克隆抗体(mAb)。在至少50次融合后,从主要用表达DR3的细胞免疫的小鼠中,选出总共几百个特异性DR3 mAb。针对TL1A抑制/阻断进一步测定DR3特异性克隆得到74个克隆。图6显示一些阻断DR3抗体的阳性抗体。还包括2个没有这种阻断作用的阳性DR3特异性克隆。
选出所有mAb以及mAb的Fab形式用于进一步的研究。表1概括了所进行的研究,并提供mAb和Fab编号与杂交瘤克隆编号间的关联性。
表 1. 选择用于进一步研究的mAb和Fab列表及mAb和Fab编号与杂交瘤克隆编号间的关联性。
发现抗体0072、0073和0076以剂量依赖性方式阻断TL1A:DR3相互作用。相应的Fab分子(0087、0088和0089)也以剂量依赖性方式保持这种能力(图7)。相对地,来源于不能够抑制TL1A:DR3相互作用的DR3结合mAb的Fab,也不具有这种能力(化合物0077和0091,图7)。
表2显示Fab特征的实例:我们针对结合、阻断TL1A-DR3相互作用的能力、TL1A诱导的T细胞活化、结合共表征了46种Fab (其它实施例中有更详尽的资料)。表中显示了多种选定的Fab以及对照:
表 2 :Fab特征
实施例
7
DR3
抗体和衍生
Fab
的功能作用
针对DR3产生和针对TL1A与DR3相互作用的阻断测定为阳性的单克隆抗体(mAb)是DR3信号转导的潜在中和剂。
将人DR3报道基因细胞系与抗体一起温育15分钟,接着用TL1A刺激或加入培养基。抗体的确仅在极高浓度下具有TL1A作用的适度中和作用,相比之下它们本身在较低剂量下是有效的激活剂。
表3显示0072抗体的作用。在不加入TL1A时0072的活化图是钟形的,表明二价抗体通过交叉结合受体而激活DR3。活化增强直到某种浓度,然后其降低DR3活化,包括TL1A介导的活化。在较高的抗体浓度下,所有抗原互补位不再被受体占据,但是抗体仍阻断TL1A结合和活化,并且观察到抑制作用。TL1A特异性抗体MAB7441
(R&D Systems)包括在内以强调DR3的活化是TL1A特异性的。
表
3
:
根据这些数据,我们假设对DR3具有亲和力的单价抗体,例如Fab (片段ab),可能不会使受体群聚,但仍可抑制TL1A结合。用木瓜蛋白酶切割抗体,纯化出Fab片段。在人DR3报道分子测定中,测定了Fab片段抑制DR3的TL1A活化的能力。测定了来自4种不同DR3抗体的Fab片段,其中3种(0072、0073和0076对应于Fab 0087、0088、0089)可阻断TL1A活化(表4)。
表
4:
第4种Fab
0097 (来自mAb 0077)不抑制,这与mAb
0077不阻断TL1A与DR3结合一致(图6和7)。表5显示在没有TL1A时4种mAb (-0072、-0073、-0076和-0077)激活DR3基因报道分子测定的能力,同样在此证实-0077是极差的激动剂。
表
5
在“I5”人DR3报道细胞系测定中,测定了重组Fab,并且在使用40微克/ml TL1A时,测定了IC50,参见表6。还包括来自专利WO2011/106707的11H08抗DR3-Fab的两种形式H1L2和H1L4。H1L2 (0227-0000-0230)和H1L4
(0227-0000-0231)分别具有3.7 nM和2.8 nM的IC50,而0227-0000-0228是1/10倍,320 pM。
表
6
制备类似于人报道细胞系的弥猴DR3报道细胞系。稳定的弥猴DR3报道细胞系称为Lyda20,通过加入40 ng/ml人(0227-0000-0011)或弥猴(0227-0000-0141)可溶性TL1A,得到10-14倍反应。表7中,显示了弥猴DR3的0123和0228活化数据。
表
7:
绒猴DR3报道细胞测定是瞬时测定法,在用TL1A刺激前2天,使用FuGene 6转染试剂(Roche),将NFκB-报道质粒和受两个热激元件和最小cFos启动子调节的绒猴DR3表达载体转染至HEK293细胞。表8中,显示了用于Fab选择的来自3个物种的DR3活化。
表
8
:
如表8所示,当在瞬时弥猴DR3报道细胞中测定时,来源于27F44抗体的Fab分子具有极差的IC50,为99和73 nM。然而,瞬时绒猴DR3报道细胞测定显示类似于瞬时人DR3测定的IC50值。
11H08/H1L2
(0227-0000-0230)和11H08/H1L4
(0227-0000-0231) Fab在瞬时人DR3报道分子测定中的IC50为4.2和4.3 nM,在瞬时弥猴DR3报道分子测定中具有3倍高的IC50,为14和13 nM,最后在瞬时绒猴DR3报道基因测定中具有50倍高的IC50,为219和377 nM。表8中列出了所有数值。
实施例
8
通过流式细胞术测定的与活化人细胞的结合
血沉棕黄层获自Copenhagen University Hospital的正常健康志愿者。通过磁珠分离,分离出CD4+ T细胞。细胞用2
ng/ml IL-12、50 ng/ml IL-18和100 ng/ml TL1A (在Novo
Nordisk A/S产生的Flag-HIS-TEV-TL1A)激活,并培养5天。在第5天,细胞用10、5、1、0.5、0.1或0.0001 µg/ml的抗DR3 mAb克隆0072、0073或0077,或用Fab片段克隆0087、0088和0091染色。第二PE缀合的山羊-抗小鼠(H+L)用于检测。
结果:单克隆IgG克隆0077及其相应的Fab克隆0091显示与细胞仅弱结合。单克隆IgG克隆0072和0073显示与细胞因子活化CD4+ T细胞强结合,在1ug/ml的浓度或更低浓度下观察到最大结合。相应的Fab克隆(0087和0088)以类似效价与细胞因子活化细胞结合,但是在结合饱和上记录到略微较低的MFI值。预期与Fab处理的细胞相比,IgG处理的细胞有较大的MFI观测值,因为第二(检测)抗体(抗IgG重链和轻链)与全长IgG抗体克隆的Fab和Fc部分两者结合,但仅与Fab克隆的Fab部分结合(表9)。
| 抗体或Fab片段 | 用于测定的浓度 | MFI |
| 0072 | 1 µg/ml | 1300 |
| 0073 | 1 µg/ml | 1300 |
| 0077 | 1 µg/ml | 100 |
| 0087 | 1 µg/ml | 500 |
| 0088 | 1 µg/ml | 500 |
| 0091 | 1 µg/ml | 100 |
表 9:显示了第5天IL-12/IL-18/TL1A活化细胞的平均荧光强度(MFI)值。以单一(singlet)活的CD4+ T细胞对细胞进行门控选择。
功能测定法:
采用CD4 Rosettesep (Stem cell technologies)和Histopaque (Sigma),通过磁珠分离从血沉棕黄层中分离出CD4+
T细胞。在含和不含抗TL1A (1000 ng/ml;MAB7441;RnDSystems)和DR3 mAb或DR3 Fab (5或10 µg/ml)时,用2 ng/ml IL-12、50 ng/ml IL-18和100
ng/ml TL1A (Flag-HIS-TEV-TL1A;Novo Nordisk)激活T细胞(2 x105个细胞/孔,96孔板) 5天。所用DR3 mAb为0072、0073和0077。所用DR3 Fab为0087、0088和0091。在活化5天后,细胞用[3H]胸苷脉冲,16小时后收获。或者激活细胞3天,随后测量细胞因子的产生(参见实施例6、15、18)。
表 10 :T细胞测定:来自用IL-12/IL18+TL1A激活的健康供体的CD4+
T细胞
通过用TL1A共刺激,T细胞增殖增加3倍。这种TL1A依赖性增加通过与抗TL1A中和性对照抗体共温育而被阻断。10 µg/ml下的所有抗DR3 mAb以及Fab 0091略微地抑制增殖,而Fab 0087和0088甚至用该测定法所用最低浓度均完全阻断增殖。综上所述,Fab 0087和0088在减量调节CD4阳性T细胞增殖的TL1A依赖性共刺激中是非常有效的。
实施例
9
小鼠
27F16A1
、
27F44A2
和
28F26A3
mAb
的克隆和测序。
抗DR3抗体的鼠重链和轻链序列从以下杂交瘤克隆:27F16A1、27F44A2和28F26A3。使用得自Qiagen的RNeasy-Mini Kit由杂交瘤细胞提取的总RNA用作cDNA合成的模板。使用得自Clontech的SMARTer™ RACE cDNA扩增试剂盒,在5’-RACE反应中合成cDNA。使用Phusion High-Fidelity PCR Master混合物(Finnzymes)和作为正向引物的SMARTer™ RACE试剂盒中所包括的通用引物混合物(UPM),通过PCR进行HC和LC序列的后续靶扩增。
PCR产物通过凝胶电泳分离,使用得自GE Healthcare Life Sciences的GFX PCR DNA和Gel
Band Purification Kit提取,并使用得自Invitrogen的Zero Blunt TOPO PCR Cloning Kit和化学感受态TOP10大肠杆菌克隆用于测序。使用得自Applied
Biosystems的AmpliTaq Gold Master Mix和13uni/M13rev引物,对选定菌落进行菌落PCR
(Colony PCR)。使用ExoSAP-IT酶混合物(USB)进行菌落PCR提纯。使用任一T3/T7测序引物,在Eurofins MWG Operon,Ebersberg,Germany进行测序。
应用VectorNTI程序,对序列进行分析和注释。按照生产商的说明书,使用所有的试剂盒和试剂。从杂交瘤27F16A1和27F44A2中,鉴定出单一独特的鼠LC κ型和单一独特的鼠HC,IgG1亚类(SEQ ID NO 8-11)。从28F26A3中,鉴定出单一独特的鼠LC κ型和单一独特的鼠HC,IgG2a亚类(SEQ ID NO
12-13)。不包括前导肽序列。
BLAST
检索
使用翻译的抗DR3 27F16A1、27F44A2和28F26A3 VL和VH氨基酸序列作为查询序列。应用BLASTp程序,在GeneSeqP专利数据库(内部数据库,具有自外部数据库输入的序列,但不访问外部各方)中,针对序列进行BLAST检索。在100分最高同一性得分中,VH的最高同一性得分为87.4 (28F26A3),VL的最高同一性得分为97.3 (27F44A2)。综上所述,抗DR3的VH和VL序列代表新的序列。
实施例
10
通过流式细胞术进行抗体结合的评价
采用CD4 Rosettesep (Stem cell technologies)和Histopaque (Sigma),从血沉棕黄层纯化人CD4阳性T细胞。在T75培养瓶中,在含2 mio CD4 T细胞/ml的RPMI (补充10% fcs)中,将T细胞用1:1比率的CD3/CD28 Dynabeads (Invitrogen)刺激4天。用磁体除去珠粒,洗涤细胞2次后,以抗体对500,000个细胞/染色进行滴定。在与山羊-抗小鼠藻红蛋白(Jackson
ImmunoResearch)温育后,测量结合饱和度,随后在BD LSRII上通过流式细胞术分析细胞。所有抗体在3 µg/ml达到饱和。表11中给出了荧光强度中值,而表12中显示染色指数(MFI Ab/MFI同种型)。Ab 0070、0072、0073和0076显示比0071和0077强的结合
表 11 :荧光强度中值
| Ab | 荧光强度中值 |
| 0070 | 2329 |
| 0071 | 406 |
| 0072 | 2650 |
| 0073 | 2844 |
| 0076 | 2645 |
| 0077 | 645 |
| IgG1同种型 | 222 |
表 12 :染色指数
| Ab | 染色指数 |
| 0070 | 10.49 |
| 0071 | 1.83 |
| 0072 | 11.94 |
| 0073 | 12.81 |
| 0076 | 11.91 |
| 0077 | 2.91 |
| IgG1同种型 | 1 |
使用藻红蛋白标记试剂盒lightening link (Innova Biosciences),使所有抗体的等分样品缀合。如上所述刺激CD4 T细胞,并用磁体除去珠粒后,洗涤细胞。对未标记的抗体自0至50 µg/ml终浓度进行滴定,加至细胞中后,在4℃下温育30分钟。洗涤细胞,加入2 µg/ml直接标记的抗体。在30分钟温育后,细胞经洗涤,并在流式细胞仪中流动。测定了标记和未标记抗体的所有组合,并记录荧光强度中值。将竞争标记抗体的结合的未标记抗体分组成结合同一框。
仅Ab 0070、0072、0073、0076能够使活化T细胞充分染色以使之分框。如表13所述,0070、0072、0073、0076能够彼此竞争,因此分在同一框。这些mAb最可能结合相同表位、重叠表位,或者由于位阻所致而不能同时结合。
表13:“框1”抗体
实施例
11
抗体和
Fab
片段的
SPR
分析
与
DR3
的不同结构域结合
DR3的胞外部分位于DR3的氨基端部分,由4个TNF受体的富含半胱氨酸的结构域组成。表达并纯化几种融合蛋白,其含有与人IgG4的Fc结构域融合的渐增长度的DR3胞外域的部分。用于SPR分析的DR3蛋白经纯化以排除寡聚化物质。采用胺偶联化学法,将这些蛋白质固定在CM5传感器芯片上。在Biacore
T100仪器(GE Healthcare)中,通过等离子体表面结合测定法(plasmon surface binding measurements),测定了称为0070、0072、0073和0076的抗DR3抗体与不同DR3-Fc融合蛋白的结合。在FACS测定中,所有这些抗体均抑制TL1A与DR3结合。这4种抗体与只含由DR3氨基酸25-71组成的氨基端CRD的重组DR3 (CRD1)-Fc蛋白(SEQ ID NO 2)结合。另一种抗体0077不抑制TL1A与DR3结合,不与DR3 (CRD1)-Fc (SEQ ID NO 2)结合,但与DR3 (CRD1 + A1)-Fc (SEQ ID NO 3)结合,其含有DR3的氨基酸25-90,表明了其表位或至少其表位的部分位于氨基酸77与90之间。
针对一些Fab片段也进行了相同分析。Fab片段0123、0124、0130、0143、0152、0219和0228全部与DR3(CRD1)-Fc (SEQ
ID NO 2)结合。
还通过SPR测定了Fab片段230和231与DR3-Fc的结合。两种Fab与含DR3的完整胞外域的DR3 (ECD)-Fc (SEQ
ID NO 7)结合,但既不与DR3 (CRD1)-Fc (SEQ ID NO 2)也不与DR3 (CRD1 + A1)-Fc (SEQ ID NO 3)结合,表明了这2种现在技术的Fab片段不与DR3 CRD1结构域结合。
通过
SPR
测量抗
DR3
Fab
片段的结合动力学
实验在Biacore T200仪器(GE Healhtcare)上进行,并用Biacore
T200评价软件进行分析。按照生产商的说明书,将抗人IgG抗体(得自GE Healthcare的人IgG俘获试剂盒)固定在CM5传感器芯片的所有流动池中。使用含0.1%人血清白蛋白的HBS-EP (GE Healthcare)作为运行缓冲液。以介于14与45 RU之间的低表面密度,将DR3(CRD1)-Fc (SEQ
ID NO 2)俘获在芯片上。将Fab片段稀释成介于90和0.037 nM之间的浓度,随后注入达360 s。标准解离时间为900 s,然而由于高亲和力所致,对于最高浓度,应用长达13
000 s的长解离时间以测定正确的k d值。在25℃下以介于30和60 µL/分钟之间的流速,测量结合曲线。
用3 M CaCl2进行再生2 x
20 s。通过减去无俘获配体的参比流动池和缓冲液空白的信号,对原始数据进行双重参比。通过应用Biacore
T200评价软件(GE Healthcare)以1:1结合模型进行拟合,来进行动力学参数测定。计算获自DR3(CRD1)-Fc
(SEQ ID NO 2)的3个不同表面密度的平均值,并陈述于表14中。
表 14 :KD值
| Fab | k a [M-1s-1] | k d [s-1] | K D [M] |
| 124 | 7.52E+05 | 2.01E-04 | 2.67E-10 |
| 130 | 1.74E+06 | 2.08E-04 | 1.20E-10 |
| 143 | 3.49E+06 | 5.10E-06 | 1.47E-12 |
| 219 | 3.20E+06 | 3.06E-05 | 9.55E-12 |
| 228 | 3.97E+06 | 3.19E-05 | 8.05E-12 |
Fab
竞争测定法
实验在Biacore T200仪器(GE Healthcare)中进行。按照生产商的说明书,将抗人IgG抗体(得自GE Healthcare的人IgG俘获试剂盒)固定在CM5传感器芯片的所有流动池中。使用含0.1%人血清白蛋白的HBS-EP (GE Healthcare)作为运行缓冲液。以介于700和1200 RU之间的表面密度俘获DR3 (ECD)-Fc (SEQ
ID NO 7)。使用浓度为20 µg/mL的Fab片段。进行2种Fab片段的双重注入,分别为300和150 s,接着用3 M CaCl2再生2 x
20 s。用Scrubber (BioLogic Software)分析Fab片段的结合反应。
无法同时与DR3 (ECD)-Fc结合的Fab片段被视为属于相同的表位框。如表15所示,全部针对CRD1结构域的Fab片段124、130、143和228,落入同一表位框。同样地,具有相同CDR结构域的Fab片段230和231,也属于不同于CRD1的相同表位框。Fab片段148和163不与其它Fab的任一种竞争,因此落入不同的表位框。当作为2.抗体注入时,Fab片段148不与124、130、143和228竞争,表明了它属于不同的框。然而,当148首先结合时,130、143或228均不再结合,这就表明存在妨碍其它Fab片段结合的位阻或DR3-Fc的构象变化。
表 15 :通过SPR测量的竞争结合DR3-Fc的Fab
| 1. Fab\2. Fab | 124 | 130 | 143 | 148 | 163 | 228 | 230 | 231 |
| 124 | - | - | - | + | + | - | + | n. t. |
| 130 | - | - | - | + | + | - | + | n. t. |
| 143 | - | - | - | + | + | - | + | n. t. |
| 148 | n. t. | - | - | - | + | - | + | + |
| 163 | n. t. | n. t. | + | + | - | + | + | + |
| 228 | n. t. | n. t. | - | + | + | - | + | + |
| 230 | + | + | + | + | + | + | - | - |
| 231 | n. t. | n. t. | + | + | + | + | - | - |
+:两种Fab的同时结合;-:2. Fab无结合;n. t.:未测定
竞争测定
如表16所示,在FACS上,针对阻断0107 (0228的Mab)和0121 (148的Mab)结合DR3表达细胞的Mab结合,对Fab片段228、231、230和148进行了测定。Fab片段230和231不与任何Mab竞争,而可同时与Mab 017和Mab 0121结合。
表 16 :通过FACS进行的竞争测定
实施例
12
通过
DR3
诱变对
Fab-0228
的表位作图
为了确定人DR3的CRD1中哪个氨基酸负责与-0123 Fab相互作用,制备了几种DR3突变体。通过位点定向诱变(Quikchange,Stratagene)产生3种突变R29Q、I43N和L45V。使突变的DR3表达质粒和NFκB-Luc报道质粒瞬时转染至HEK293细胞,使细胞与抗DR3抗Fab-0228短暂预温育,随后用人TL1A刺激4小时。通过使用Steady-GLO (Promega)测定萤光素酶活性,并在TopCount
NXT (Perkin Elmer)上进行监测。R29Q比人野生型稍好地被中和,而I43N、L45V两种和组合突变体I43N/L45V低效得多地被中和,参见表17。
还测定了抗Fab-0123,顺序与-0228类似;R29Q>WT>L45V>I43N>I43N-L45V。因此,残基I43和L45对维持0228与DR3的结合亲和力是非常重要的。这些残基因此最可能是结合表位的部分。相比之下,R29对0228与DR3的结合似乎不是必需的,因为当该残基突变时,亲和力仍保持,甚至略为改进。然而,因为该位置影响0228结合,因此其对结合表位具有结构重要性。
表
17
:
实施例
13
抗
DR3
人源化
0072的序列获自杂交瘤27F44A2的克隆。用于该实施例的所有编号是指Kabat编号方案。
>0072VH
(CDR用黑体字标记) (SEQ ID NO 10)
>0072VL (CDR用黑体字标记) (SEQ ID NO
11)
0072的序列分析揭示在人源化期间必须除去的重链91位处的游离半胱氨酸。
采用MOE [可获自www.chemcomp.com]中的标准技术,构建0072的3D模型,有效CDR区域4.5 Å内的全部残基(VH:31-35B、50-58、95-102;VL:24-34、50-56、89-97)定义为掩蔽残基(mask residue)。掩蔽残基对维持CDR中的结合均可能是重要的。
掩蔽残基包括重链的2、4、27-37、47、50-59、69-71、78、91-103位和轻链的3-5、7、23-36、46-60、62、65、67、69-71、87-98位。
利用种系检索和手工检查,将VH3_13和JH4鉴定为对重链合适的人种系组合,而VKI_02和JK4鉴定为对轻链合适的人种系组合。
现可按照下列规则进行人源化:
- 掩蔽以外的残基视为人的。
- 掩蔽以内且Kabat CDR以内的残基视为鼠的。
- 具有小鼠/种系共有序列的掩蔽以内且Kabat CDR以外的残基视为共有序列。
- 具有小鼠/种系差异的掩蔽以内且Kabat CDR以外的残基易遭受潜在的回复突变。
将0072的有效CDR区移植入种系形成0072的基础人源化构建体hz0072。
1.
>hz0072VH (SEQ ID NO 28)
2.EVQLVESGGGLVQPGGSLRLSCAASGFTFSNYDMSWVRQATGKGLEWVSAFSSDGYTFYP
3.GSVKGRFTISRENAKNSLYLQMNSLRAGDTAVYYCARHADYANYPVMDYWGQGTLVTVSS
4.
5.>hz0072VL (SEQ ID NO 29)
6.DIQMTQSPSSLSASVGDRVTITCRASKSVSTSGYSYMHWYQQKPGKAPKLLIYLASNLES
7.GVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHSRELPLTFGGGTKVEIK
与鼠CDR相比的唯一差异位于CDR_H2。
掩蔽残基中0072和hz0072之间的任何偏差可产生潜在回复突变,名单包括
hz0072VH:T28A,S49A,Y91C
hz0072VL:Q3V,M4L,T5M,S60A
为了研究所有潜在的人源化mAb,必须制备上述突变体的所有组合。
使表18所列Fab蛋白在HEK293 6E细胞中表达,如通过SDS-PAGE凝胶所评价的,对每个变体的表达水平进行比较。表18的结果显示,与在重链91位处含有其它置换即Cys (化合物0172)或Ser (化合物0173或0174)的变体相比,在该位置含有种系Tyr的所有变体(化合物0169、1070和0171)具有显著提高的表达水平。同样从表18来看,轻链4位处的人形式的Met或鼠形式的Leu对表达水平没有明显作用。这表明了重链中的Y91对0072的完全移植形式的表达水平的改进是决定性的。
表 18 :通过在重链91位或轻链4位处具有突变的抗DR3 Fab的变体进行的Fab表达水平的比较。对人源化抗DR3 0072产生具有HC_T28A_S49A和LC_Q3A_T5A_S60A回复突变的变体。HC_Y91是人源化形式;Y91C是鼠形式;Y91S是使Y91突变成无关氨基酸Ser。LC_M4是人源化形式;LC_M4L是鼠形式。通过SDS-PAGE凝胶评价表达水平;“++++”表示>50 mg/L的高表达水平,“+”表示表达水平低下。
回复突变的选择
根据表达、效价和亲和力筛选以及通过生物物理表征,对插入回复突变的可能优势进行了评价。
表达模式:在HEK293-6E中,对0072的各种人源化形式(包括各种回复突变(BM))的表达水平进行了瞬时评价(有关HEK293-6E中的瞬时表达参见实施例3)。
除hz0072以外,就表达而言,还对下列BM分别进行了评价:
LC:T5A和S60A
HC:T28A和S49A
实验以一式三份进行。转染后使细胞生长5天。收获培养基,使用G蛋白传感器,通过forteBIO´s Octet测量表达水平。
结果表明,与hz0072表达相比,HC上的BM S49A导致约2倍增加。其它BM中无一种具有提高表达水平的能力(表19)。
表 19 :与设置为100%表达水平的野生型(WT)相比较的具有回复突变的重链(HC)和具有回复突变的轻链(LC)的相对表达水平。
| 平均值(%) | 标准偏差 | |
| hz0072 | 100 | 0.06 |
| hz0072 T28A(VH) | 91.7 | 6.02 |
| hz0072 S49A(VH) | 251.2 | 4.58 |
| hz0072 T5A(VL) | 45.7 | 1.26 |
| hz0072 S60A(VL) | 63.6 | 2.17 |
生物物理表征
采用示差扫描荧光测定法(differential scanning fluorimetry,DSF),测量了人源化Fab的热稳定性。采用MyiQ实时PCR检测系统(Biorad Laboratories,Inc),进行了DSF。将PBS (pH 7.4)中终浓度为0.3 mg/ml的样品加入密封的96孔PCR板和染料Sypro Orange的2000倍稀释的储液中,所述染料被用来监测蛋白质解折叠转换。用激发/发射波长:480/575 nm测量荧光强度。表20显示人源化Fab的热稳定性。结果表明,具有回复突变的两种Fab
(228和229)具有相同的热稳定性(Tm),为71℃,而没有回复突变的人源化Fab (227)热稳定性降低,为66℃
| Fab | m (℃) |
| hz0072 (227) | 6 |
| hz0072 S49A(VH) (228) | 1 |
| hz0072 S49A(VH) S60A(VL) (229) | 1 |
表 20 :显示人源化Fab的Tm (变性温度)值。
利用生物物理评价选择
IgG4
骨架
采用生物分析仪,对PBS (pH 7.4)中的3 mg/ml人源化Fab的IgG1和IgG4同种型进行了测定以查明断裂方式。采用Agilent 2100生物分析仪查明断裂方式。试剂盒为Agilent Protein 230,所用标志物是具有7个峰的Protein 230梯。用2 µl样品、2 µl Mill-Q水、2 µl样品缓冲液和1 µl 0.5 M N-乙基马来酰亚胺(溶于CH3CN的NEM)制备非还原样品。将所有样品加热至100℃达最多5分钟。
表21显示非还原条件下Fab的游离LC的积分量的生物分析仪数据。结果表明,与IgG1
Fab相比,所有IgG4 Fab在非还原条件下均具有较少的游离LC。
| Fab | gG1 | gG4 |
| hz0072 | 1.9 | .0 |
| hz0072S49A(VH) | .6 | .6 |
| hz0072S49A(VH) S60A (VL) | .2 | .7 |
表 21 :非还原条件下IgG1和IgG4人源化Fab的游离LC的积分峰值。
在上述广泛的效价和亲和力筛选、表达分析和稳定性研究后,选择最终的人源化候选物作为具有以下序列的hz0072VH S49A,
hz0072VL的IgG4形式:
该候选物在可变结构域中没有游离的半胱氨酸。
实施例
14
重组
Fab
片段的纯化:
采用Äkta Explorer FPLC系统(GE Healthcare),通过层析步骤纯化重组Fab片段。将含有重组小鼠Fab的细胞培养上清液稀释,以将电导率降至2 mS以下。根据Fab片段的理论pH,采用MonoQ或MonoS柱(GE Healthcare),进行阳离子或阴离子交换层析。使Fab片段与低离子强度缓冲液(pH值介于5和8.5之间)中的柱结合,用最高1 M NaCl的盐梯度洗脱。进行具有Superdex200柱(GE Healthcare)和PBS作为缓冲液的凝胶过滤以除去寡聚体Fab复合物。
按照生产商的说明书,用KappaSelect (GE Healthcare)通过亲和纯化,对含有人κ免疫球蛋白轻链的恒定部分的嵌合Fab片段进行纯化,接着凝胶过滤除去高分子量复合物。
通过木瓜蛋白酶切割
mAb
产生
Fab
按照生产商的说明书,使用Pierce Fab制备试剂盒(Thermo Scientific),通过切割mAb来产生Fab片段。在一些情况下,进行具有Superdex200柱(GE Healthcare)和PBS作为缓冲液的凝胶过滤以除去高分子量形式。
实施例
15
原代人
T
细胞的细胞因子释放或增殖。
使用CD4 Rosettesep (Stem cell technologies)和Histopaque(Sigma)通过磁珠分离自血沉棕黄层分离的CD4 +
T细胞,在不存在TCR活化时,在有和没有100
ng/ml TL1A (Flag-His-TEV-TL1A;Novo Nordisk)时,用细胞因子IL-12 (2 ng/ml)、IL-18
(50 ng/ml)刺激。测量T细胞增殖和细胞因子释放。收获经刺激48小时的CD4+ T细胞(2x105个细胞/孔)的上清液,并通过Bioplex分析细胞因子释放。5天后测量T细胞增殖。
与IL-12/IL-18处理的T细胞相比,IL-12 (2 ng/ml)、IL-18
(50 ng/ml)和100 ng/ml TL1A (Flag-His-TEV-TL1A;Novo Nordisk)处理的CD4+
T细胞表明T细胞增殖增加6倍。0123和0124 Fab早在0.16 μg/ml的Fab浓度下就完全阻断诱导的T细胞增殖,而相应的mAb 0072和0108不影响T细胞增殖(图8)。
通过TL1A在48小时后,均诱导IL-12/IL-18处理的CD4+
T细胞的细胞因子IL-6、IFNγ、GM-CSF和TNFα释放。与DR3结合性非阻断性Fab 0091相比,TNFα被抗DR3 Fab 0124显著(p=*)阻断(表22)。
表
22:
| 细胞因子 | +TL1A (与IL12/IL18活化T细胞相比的上调倍数) | +TL1A+抗DR3 Fab (与IL12/IL18活化T细胞相比的下调倍数) |
| IL-6 | 16 (p=0.051) | 13.3 (p=0.08) |
| IFNγ | 1.2 (p=0.025) | 1.1 (p=0.08) |
| GM-CSF | 7.5 (p=0.04) | 7.9 (p=0.08) |
| TNFα | 4.4 (p=0.0007= | 5 (p=0.025) |
实施例
16
脂质部分与
Fab
的缀合
NAP-25柱,目录号17-0852-02,来自GE
Healthcare
Hitrap Q-sepharose FF柱(代码:17-5156-01),来自GE
Healthcare
TSPP:三苯膦-3,3',3''-三磺酸三钠盐水合物,目录号39538,来自Alfa Aesar
TDSPP:双(对磺基苯基)苯膦二水合物二钾盐,目录号151888-20-9,来自Strem
Chemicals
TEA:三乙醇胺,产品号:90279,来自Sigma
乙二醇,目录号1.00949.1000,来自MERCK
NaCl:编号:207790010,来自Acros
Organics
EDTA,二钠盐,二水合物,目录号SC-29092,来自ChemCruz
PBS片,目录号18912-014,来自GIBCO
Vivaspin 20,10000 MWCO,PES膜,目录号VS2001,来自Sartorius
PD10 G-25柱,目录号17-0851-01,来自Ge
Healthcare
缩略语
CV:柱体积
FLD:荧光检测
MQ:MilliQ水(高纯净水)
m/z:质荷比
MS:质谱法
M+H:单质子化物类的质量
HPLC:高压液相色谱法
RP:反相
LC-MS:液相色谱-质谱法
NMR:核磁共振光谱法
rt或RT:室温
Boc:叔丁氧基羰基
O-t-Bu:叔丁基酯
t-Bu:叔丁基
DCM:二氯甲烷,CH2Cl2,亚甲基氯
DIC:二异丙基碳二亚胺
DIPEA:N,N-二异丙基乙胺
DMF:N,N-二甲基甲酰胺
DMSO:二甲亚砜
Fmoc:9H-芴-9-基甲氧基羰基
Lys(Mtt)-OH:(S)-6-[(二苯基-对甲苯基-甲基)-氨基]-2-氨基-己酸
Thx:反式-4-氨基甲基环己基甲酸
NMP:N-甲基吡咯烷-2-酮
OEG:(2[2-(氨基)乙氧基]乙氧基)乙酸
TFA:三氟乙酸
THF:四氢呋喃
TIS:三异丙基甲硅烷
TNBS:三硝基苯磺酸
HC:重链
LC:轻链
wt:野生型
氨基酸缩略语遵照IUPAC惯例。
缓冲液缩略语遵照Stoll, V. S.和Blanchard,
J. S., Methods of Enzymology, 182, 1990, Academic Press, 24-38。
缀合,总则
构建在重链(HC) C端上或附近具有不成对半胱氨酸的Fab用于与疏水延长基团缀合。该半胱氨酸目的在于与具有例如马来酰亚胺或卤素-乙酰基的亲硫烷基化试剂缀合。Fab作为具有针对突变Cys的二硫键键合的半胱氨酰化的分子表达。为了释放出用于与烷基化试剂反应的突变Cys,使用膦试剂使之还原。在还原后,将蛋白质与还原试剂相分离,并通过加入烷基化试剂进行烷基化。最后,缀合物通过标准低压色谱法纯化。
4-(1H-四唑 -16- 基 - 十六酰氨磺酰 ) 丁酰基 -OEG-γGlu-γGlu-OEG-N ε (C(O)CH2Br)Lys-OH( 白蛋白结合剂 I):
(化合物I)
按照方案1,采用标准Fmoc-肽化学法,在ABI433合成仪(Applied
Biosystems),以1 mM规模,在固相支持体上合成化合物I。使用Fmoc-OEG-OH和Fmoc-Glu-OtBu保护的氨基酸,使肽在Fmoc-Lys(MTT)-Wang树脂上装配。使用2当量含DIC/NHS的DCM/NMP,对4-(16-1H-四唑-5-基-十六酰氨磺酰)丁酸进行手工偶联过夜,TNBS试验显示反应完成。树脂然后用50 mL
DCM/TFA/TIS/水(94:2:2:2)以流过方式处理,直到黄色消失,约20分钟,接着洗涤,并用DIPEA/DMF中和。含溴乙酸(4
mM)的DCM/NMP (1:1)用1 mM NHS和DIC的混合物激活,过滤,随着更多1 mM DIPEA的加入而加到树脂中。1小时后,反应完成。树脂用80 mL TFA/TIS/水(95:2.5:2.5)处理1小时。用N2流蒸发,通过加入Et2O沉淀,用Et2O洗涤后干燥。粗产物用制备型HPLC纯化(2轮),梯度为30-80% 0.1
TFA/MeCN相对于含0.1% TFA的水溶液。收集流分,用~50%
MeCN冻干,得到化合物 I。
TOF-MS:质量1272.52 (M+1)
上述实施例表明,采用固相合成可能制备高纯度的白蛋白结合剂化合物I。
方案
1
Fab 0120
与白蛋白结合剂
I
的缀合
将含Fab 0120 (25 mg,0.53 umol,4.2 mg/ml)的PBS缓冲液与三苯基膦-3,3',3''三磺酸三钠盐水合物(TSPP,40 mg/ml,350 ul,终浓度3.7 mM)在20 mM三乙醇胺、2 mM EDTA中的溶液(pH 8.5)混合。使反应混合物在室温下温育150分钟的时间。然后通过在用20 mM三乙醇胺、2 mM
EDTA、400 mM NaCl,pH 8.5平衡和洗脱的3个NAP-25柱中进行缓冲液交换来除去小分子量物质。然后将缓冲液交换的还原Fab溶液与白蛋白结合剂I (490 ul,16 mM,终浓度:0.8 mM)在20 mM三乙醇胺、2 mM EDTA、400 mM NaCl中的溶液(pH 8.5)混合。使反应混合物(约9.5 ml)在室温下温育20小时的时间,然后用10 ml缓冲液20 mM三乙醇胺、10%乙二醇(pH 8.0)稀释。随后,使混合物在用20 mM三乙醇胺、10%乙二醇(pH 8.0)平衡的4个NAP25柱中进行缓冲液交换。采用Äkta Puifier 100系统(GE Healthcare),将缓冲液交换的物质上样到用20 mM三乙醇胺、10%乙二醇(pH 8.0)平衡的5 ml Hitrap Q-sepharose FF柱中。用该缓冲液冲洗出未结合的物质(包括未缀合的Fab),在1.5小时的时间内,使用20 mM三乙醇胺、10%乙二醇、1 M NaCl (pH 8.0)的线性梯度洗脱产物。产物在约380
mM NaCl处洗脱,其具有对称峰谱分布。合并相关流分,使用Vivaspin 20装置在3500 g下通过超滤浓缩(10000 MWCO,Sartorius),最后交换缓冲液为PBS缓冲液。在通过A280测定的1.7 mg/ml的浓度下,最后分离的产物为11.9 mg (48%)。SDS-PAGE和MS分析证实产物的身份(实测为m/z 49919 (M+H),计算为49917
(M+H))。
上述实施例显示成功的Fab与白蛋白结合剂I的位点特异性缀合。缀合产生良好收率和高纯度的产物。
Fab
与白蛋白结合剂
II-VI
的缀合
白蛋白结合剂II-VI具有如下所示结构
按照上述化合物I所述的相同方法使白蛋白结合剂I-VI缀合。在白蛋白结合剂IV和VI的情况下,在加入Fab溶液前,化合物是非完全可溶解的。在一些情况下,加入有机溶剂以促进溶解。由于白蛋白结合剂II-VI上较少数目的酸性基团所致,缀合物不与AIEX柱结合,除非pH提高至8.6。在白蛋白结合剂II-VI的情况下,纯的单取代产物被不同量的多重修饰的Fab污染。这些难以通过离子交换层析法除去。
通过表23所示SDS-page和LC-MS实施例,证实了所有缀合物的身份。对于与II、III和V的缀合物,测定纯度为>90%,而与IV和VI的缀合物含有约30%基于未缀合Fab的杂质。
表 23 :与计算质量相比,与各种白蛋白结合剂缀合的2种不同Fab的LC-MS数据。
上述实施例表明,各种不同的白蛋白结合剂可以良好收率和纯度与IgG1和IgG4两种来源的Fab缀合。
上述实施例表明,各种不同的白蛋白结合剂可以良好收率和纯度与IgG1和IgG4两种来源的Fab缀合。
各种
Fab
与白蛋白结合剂
I
的缀合
下列Fab是缀合的:0118、0119、0127和0147 (参见表25)。这些Fab在C端或在0157情况下紧接C端含有不成对的半胱氨酸残基。Fab来源于IgG1或IgG4,且对应于全部结合DR3受体的不同克隆。当按照上述方法反应时,根据LC-MS数据,以良好收率形成缀合物。获得了下列MS数据(表24)
表 24 :与计算质量相比,与白蛋白结合剂I缀合的各种Fab的LC-MS数据
| 与以下Fab缀合 | 实测m/z (M+H) | 计算m/z (M+H) |
| 118 | 49947 | 49947 |
| 119 | 49408 | 49408 |
| 127 | 49712 | 49712 |
| 134 | 49975 | 49975 |
| 147 | 49409 | 49409 |
| 157 | 50169 | 50169 |
上述实施例表明各种Fab可以良好的产率和纯度与不同的白蛋白结合剂分子缀合。
表 25 :用于PK研究的抗DR3 Fab白蛋白结合剂缀合物的列表
实施例
17
主要目标是在iv和sc两种方式给予DBA/1小鼠后表征药代动力学参数,主要重点集中在终末半寿期,以评价修饰Fab片段后延长的程度。
研究设计和方法
在本概要中包括了2项研究的结果(DKPF111105和DKPF110703)。两项研究在雄性DBA/1小鼠中进行,在尾静脉静脉内(i.v.)或在腹股沟皮下(s.c.)给予小鼠。剂量对于Fab为5 mg/kg,对于修饰的Fab为1 mg/kg。使用稀疏采样设计,在每个采样点收集3个血样,从给药前直到给药后7天收集样品,这取决于化合物(例如当测定Fab时,只收集样品直到给药后7小时,而当测定缀合的Fab时,收集样品直到给药后7天)。
采用ELISA测定法,对所收集的血浆样品均进行了分析,简单地说,将板用hDR3-Fc融合蛋白(SEQ ID NO 7)包被,加入稀释的血样,而分析物(Fab或缀合的Fab)可与hDR3结合,然后通过过氧化物酶标记的抗Fab抗体检测结合的分析物,并采用标准方法测量吸光度。根据所测量的血浆浓度值,应用市售软件Phoenix
WinNonlin (Pharsight Corp.),采用标准非区室方法,对药代动力学参数进行了评价。
结果
对延长Fab的终末半寿期的几个不同的接头进行了评价,根据白蛋白结合技术,对于几个分子,可能延长Fab的终末半寿期超过20小时(表 26)。估计Fab的半寿期低于1小时,这说明了Fab较之于全都显示半寿期长得多的缀合Fab (表 26)的差异。
表 26 :iv或sc给予小鼠后的药代动力学参数
实施例
18
:
读取干扰素
-
γ释放作为测定抗
DR3
活性的方法
通过在Ficoll (GE Healthcare,目录号17-5442-02)中以2000
rpm离心20分钟,从血液血沉棕黄层(中国北京解放军307医院血液中心)分离新鲜的人外周血单核细胞(PBMC)。在DPBS中洗涤后,吸取细胞沉淀,以1x106/ml重新悬浮于培养瓶中预热的测定培养基(RPMI
1640、10%热灭活FBS、1%青霉素/链霉素)中培养过夜。然后取出未贴壁淋巴细胞,用于T细胞共刺激测定。
对于共刺激测定,将作为共刺激剂的重组人TL1A (12 µg/mL)以50 µl/孔加入干燥的96孔U底测定板(Corning costar
3799),该测定板除边缘以外的所有孔中用0.3 µg/mL的初级刺激物抗CD3 mAb (BD Pharmingen目录号555336)在37℃培养箱中预先包被3小时。在96孔深孔板(Nunc 278743)中以1.5mL/孔1:3连续滴定范围为0.012-12 µg/mL的4X浓度后,将试验性抗DR3 Fab (0170、0171、0173、0169和0118)以50 µL/孔一式两份转移至测定板中。然后用0.1mL富集的淋巴细胞以2 x
105个细胞/孔加入测定板中,使最终体积达到0.2
mL/孔。在含5% CO2的37℃培养箱中进行细胞培养40小时后,从培养板各孔中收获120mL上清液,以用IFN-γ ELISA试剂盒(eBioscience 目录号88-7316-88)测量细胞因子分泌。按照生产商的建议,将试验上清液1:20稀释,以测量在T细胞测定中分泌的细胞因子的完整范围。
针对其阻断TL1A共刺激的来自健康供体外周血的原代T细胞的细胞因子分泌的能力,对含(173、170和169)或不含(171)回复突变的多种人源化抗DR3 Fab进行了评价。
如表27所示,抗CD3初敏引起中等水平(~50 ng/mL)的IFN-γ分泌,通过重组TL1A共刺激,该分泌提高至超过3倍(~159 ng/mL);而仅TL1A处理只导致最低量的细胞因子释放(1.2 ng/mL)。在TL1A共刺激条件下,所有试验性人源化抗DR3 Fab以剂量依赖性且完全的方式抑制IFN-γ分泌(IC50 ~ 0.01-0.03 ug/mL),其对抗CD3初敏具有最小作用。作为自用多个供体的多项实验鉴定的阴性对照,如对T淋巴细胞的TL1A共刺激所预期,非配体阻断性嵌合抗DR3
Fab 0118不显示显著作用。在用不同供血者的另一项实验中,对第二批的0171和0170 Fab获得类似结果。
表 27 :人源化抗DR3
Fab对TL1A共刺激的健康供血者T淋巴细胞的IFN-γ分泌的作用
实施例
19
抗
DR3
抗体
Fab
阻断类风湿性关节炎患者滑液中
效应
T
细胞的
TL1A
共刺激
在前述实施例中显示了人源化抗DR3 Fab抑制自健康个体外周血分离的原代T细胞的活性。另外,针对其阻断来源于类风湿性关节炎(RA)患者的滑液T细胞的效应子功能的能力,还对一些Fab进行了评价。T细胞的效应子功能包括但不限于在本实施例分析的IFN-γ分泌。用与实施例18所述相同的ELISA试剂盒,测量了分泌的IFN-γ水平。
通过在2000 rpm下离心10分钟,自RA患者膝关节液作为DMARD关节内注射的副产品(废物)分离新鲜的人滑液(SF)细胞(中国北京大学人民医院)。吸取细胞沉淀,以1x106/mL重新悬浮于预热的测定培养基(RPMI 1640、10%热灭活FBS、1%青霉素/链霉素)中。通过FACS分析,针对T淋巴细胞的存在(%),检查滑液细胞的少量样品(~105/0.1mL)。将> 5-10%淋巴细胞群的RA/SF细胞样品用于T细胞共刺激实验。
对于共刺激测定,将重组人TL1A (12µg/mL)作为共刺激剂以50µl/孔加入干燥的96孔U底测定板(Corning costar 3799),该板除边缘以外的所有孔中用0.3µg/mL的初级刺激物抗CD3 mAb (BD目录号555336)在37℃培养箱中预先包被3小时。在96孔深孔板(Nunc 278743)中以1.5mL/孔1:3连续滴定范围为0.012-4µg/mL的4X浓度后,将试验性抗DR3 Fab (0170、0171、0173和0118)以50µL/孔一式两份转移到测定板中。然后用0.1mL
RA/SF细胞以2 x 105个细胞/孔加入测定板,使最终体积达到0.2mL/孔。在含5% CO2的37℃培养箱中进行细胞培养40小时后,从培养板各孔中收获120mL上清液,以用IFN-γ ELISA试剂盒(eBioscience目录号88-7316-88)测量细胞因子分泌。按照生产商的建议,对试验上清液测定合适的稀释因子,以测量在T细胞测定中分泌的细胞因子的完整范围。
针对其阻断TL1A共刺激的RA患者膝关节滑液T细胞的细胞因子分泌的能力,对人源化抗DR3
Fab (171)及其骨架突变的变体(173和170)进行了评价。
如表28所示,抗CD3初敏诱导中等水平(~1228 pg/mL)的IFN-γ分泌,通过重组TL1A共刺激提高该分泌至约2倍(~2188pg/ml);而仅TL1A处理显示无可检出的细胞因子释放。在TL1A共刺激条件下,3种试验的人源化抗DR3 Fab以剂量依赖性且完全方式抑制IFN-γ分泌(IC100 ~ 0.1ug/mL),其对抗CD3初敏具有最小作用。作为阴性对照,如对T淋巴细胞的TL1A共刺激所预期,非配体阻断性嵌合抗DR3
Fab 0118不显示显著作用。在用不同RASF样品的5项实验中,不同批次的0171 (3个批次)和0170 (2个批次) Fab得到类似结果。
表 28 :人源化抗DR3
Fab抑制TL1A共刺激的RA患者SF细胞的IFN-γ分泌
实施例
20
通过抗
DR3 Fab
的
HX-MS
进行表位作图
HX-MS技术利用蛋白质氢交换(HX)可容易地后紧质谱法(MS)。通过用含有氘的水性溶剂替换含有氢的水性溶剂,在蛋白质的给定部位掺入氘原子将引起1 Da的质量增加。在交换反应的猝灭样品中,可通过质谱法监测随时间变化的这种质量增加。可在猝灭条件下通过胃蛋白酶消化,并按照所得肽的质量增加,将氘标记信息亚定位于(sub-localized)蛋白质的区域。
HX-MS的一种应用是通过鉴定在蛋白质-蛋白质复合物形成时氢交换减少的区域,来探测参与分子相互作用的部位。通常可通过因溶剂的空间排阻引起的氢交换显著减少,来揭示结合界面。可仅仅通过测量在各自的结合配偶体存在和不存在时随时间变化掺入任一蛋白质成员的氘总量,通过HX-MS检测蛋白质-蛋白质复合物形成。HX-MS技术使用天然成分,即蛋白质和抗体或Fab片段,并且在溶液中进行。因此HX-MS提供模拟体内条件的可能性(有关HX-MS技术的最近综述参见Wales和Engen, Mass
Spectrom. Rev. 25, 158 (2006))。
所用蛋白质批次为:
hDR3:与Fc融合的hDR3的完整胞外域(SEQ ID NO 7)。该分子是因Fc二聚化引起的相对于hDR3的二聚体。表达批次还含有蛋白质的寡聚化形式,但仅纯化的二聚体部分用于HX-MS实验。
Fab分子:0120、0130、0143、0148、0163、0228、0230和0231 (参见表29)。实验前,将所有蛋白质进行缓冲液交换至PBS
pH 7.4。
仪器和数据记录
在与Synapt G2质谱仪(Waters
Inc.) 耦合的具有HDX技术的nanoACQUITY
UPLC System (Waters Inc.)中进行HX实验。Waters HDX系统包括由LeapShell软件(Leap Technologies Inc/Waters Inc.)操作的Leap机器人(H/D-x PAL;Waters Inc.),其执行氘交换反应的启动、反应时间控制、猝灭反应、向UPLC系统的注入和消化时间控制。Leap机器人配备了分别保持在20℃下用于缓冲液贮存和HX反应以及保持在2℃下用于蛋白质和猝灭溶液贮存的2个控温管组(stack)。此外Waters HDX系统包括控温室,其保持前置柱和分析柱及LC管和开关阀在1℃下。单独的控温室保持胃蛋白酶柱在25℃下。对于联机胃蛋白酶消化,使用100 µL/分钟(0.1%甲酸:CH3CN 95:5)的等度流速(isocratic
flow rate),使含有200 pmol hDR3的100 µL猝灭样品上样并通过置于25℃下的Poroszyme®固定化胃蛋白酶柱体(Immobilized
Pepsin Cartridge) (2.1 × 30 mm (Applied
Biosystems))。将所得肽在VanGuard前置柱BEH
C18 1.7 µm (2.1 × 5 mm (Waters
Inc.))中截留并脱盐。随后,打开阀门使前置柱与分析柱UPLC-BEH C18 1.7
µm (1 × 100 mm (Waters Inc.))联通,并使用以200 μl/分钟递送的10-40% B的9分钟梯度从nanoAQUITY UPLC系统(Waters
Inc.)分离肽。流动相由A:0.1%甲酸和B:含0.1%甲酸的CH3CN组成。采用Synapt
G2质谱仪(Waters Inc.),以阳离子模式获取ESI MS数据和各高能(MSE)实验。亮氨酸-脑啡肽用作锁定质量(lock mass) (m/z
556.2771的[M+H]+离子),以连续模式收集数据(有关进一步的描述参见Andersen和Faber,
Int. J. Mass Spec., 302, 139-148(2011))。
数据分析
采用标准MSE方法,在各个实验中鉴定出消化性肽,其中利用Synapt G2 (Waters Inc.)的离子移动性质,对肽和片段作进一步比对。应用ProteinLynx Global Server 2.5版(Waters Inc.)处理MSE数据。以DynamX软件(Waters Inc.)处理HX-MS原始数据文件。DynamX自动执行锁定质量校正和氘掺入测定,即氘化肽的质心测定。此外,用该软件手工检查所有肽以确保正确的峰和氘化分配。
表位作图实验
在Fab 0120、0130、0143、0148、0163、0228、0230或0231存在或不存在时,通过将hDR3 7倍稀释于相应的氘化缓冲液(即在D2O中制备的PBS,最终为96% D2O,pH
7.4 (未校正值))中,来启动酰胺氢/氘交换(HX)。所有HX反应在20℃下进行,在10 μM Fab不存在或存在时含有2 μM hDR3,因此得到5倍摩尔过量的Fab。在范围为10秒至3000秒的合适时间间隔,50 μl等分量的HX反应物通过50 μl冰冷的猝灭缓冲液(1.35M TCEP)猝灭,导致最终pH为2.5 (未校正值)。
结果与讨论
在0120、0130、0143、0148、0163、0228、0230或0231 Fab不存在或存在时,监测20种消化性肽(涵盖hDR3胞外域一级结构的75%)的HX时程10-3000秒。hDR3在N67和N106位含有2个N-糖基化位点,因此肽图谱在这些区域上具有空位。
在Fab 0120、0130、0143、0148、0163、0228、0230或0231存在或不存在时,在早期时间点(< 300秒)观察到的交换方式可分为两个不同的组别:一组肽显示不受Fab结合影响的交换方式。相比之下,hDR3的另一组肽显示在Fab结合时受保护免于交换(表29)。肽中所观察到的交换保护表示该区参与Fab结合。因此表位部分位于或可能甚至全部位于特定肽所限定的区域内。然而,由于HX-MS的分辨率以消化性肽为基础,给定区域内的交换保护并非意味着该区域内的每个残基都必须参与Fab结合。
0148
和
0163
的表位作图
Fab 0148和0163表示结合hDR3但不阻断TL1A结合的Fab分子。研究中包括了这些Fab分子用于对照。在Fab 0148的CRD3中的P140-L153区域中观察到表位信号(表29)。用5x过量的Fab进行当前的实验,然而,利用0148与hDR3等摩尔比(equimolar ration)的HX-MS实验证实,可在标准等摩尔条件下对该Fab作图。
在CRD4区的G163-F169区域和Y170-L184区域中部分观察到Fab 0163的弱表位信号。
0120
、
0130
、
0143
和
0228
的表位作图
使用3-5x过量的Fab分子,在几项实验中对Fab 0228作图。在CRD1的R32-G54、G37-L45和F46-A59区域观察到表位信号。然而,根据消化性肽中交换保护的相对水平和F46-Y56区域中的弱交换保护或不存在交换保护,可得出结论,0228的表位在G37-L45和L57-A59区域中最强。G37-L45区域还涵盖通过诱变发现对0228/0123与hDR3结合是重要的残基,这些实验的数据因此完全一致(实施例12,表16)。出人意料的是,需要使用相对于hDR3极过量的0228 Fab。通常,当通过HX-MS进行表位作图时,使用等摩尔比的mAb或Fab便足够。如果使用等摩尔比的0228与hDR3,则未观察到表位信号(数据未显示),即使0228具有非常高的亲和力(实施例11,表14)。这些观察结果指出,0228表位位于在实验条件下并非完全溶剂可达到的区域。因此尽管0228的高亲和力,但低的交换保护可能是fab分子必须位于hDR3自我相互作用之上或与hDR3自我相互作用竞争的结果。hDR3自我相互作用可能是非特异性聚集的结果或如例如对TNFR超家族其它成员所述的胞外域群聚的结果(Mukai等(2010) Sci. Signal. 3,ra83)。此外,可在C端区域中观察到弱的作用。由于当与只含有CRD1的蛋白质结合时,0228和0120具有充分的亲和力(实施例11,表14),因此C端作用最可能是在Fab结合时构象重排的结果,并且可能是融合DR3与Fc的铰链区运动的结果。
从SPR实验来看,已经证实0120、0130和0143均与0228竞争并相互竞争与hDR3结合(实施例11,表15)。因此,这些Fab部分或完全共享表位。
一致的是,对这些Fab的HX-MS还显示在相同区域G37-L45中的表位信号。然而交换保护幅度较弱。根据上述观察结果,可以推测,为了使HX-MS在群聚界面显示交换保护,需要高度过量的结合分子,而且它应是高亲和力相互作用。
0230
和
0231
的表位作图
对Fab 0230和0231
(来自WO2011106707的11H08)的表位作图不显示任何表位。鉴于上述观察结果,即为了成功,对hDR3的表位作图需要良好的亲和力,可推测这些Fab (WO2011106707)相对较弱的亲和力妨碍通过HX-MS进行成功的表位作图。
表 29 :产生 Fab 分子的表位信息的 DR3 的 HXMS 分析。在氘交换反应后,DR3用胃蛋白酶消化,产生经分析的下列消化性肽区域。N67和N106位置是糖基化的,因此肽图谱在这些区域上具有空位。DR3残基的编号遵循SEQ ID NO 1 。
不止一种的分配表明,两项或更多项实验给出有关交换保护的幅度方面略微不同的结果。
实施例
21
本文提及抗体的概述
表30提供本文所提及抗体的概述,其命名取决于所使用的不同mAb/Fab形式。命名注释:表30利用4位数标识(例如0228)。然而,对于相同化合物可观察到不同的命名。例如化合物0228亦称为0227-0000-0228、0227-0228、00228或228。所有这些命名表示同一化合物。该规则适用于所有化合物。
表 30 :选用于研究的抗DR3
mAb和Fab化合物的列表。该表给出mAb、Fab和杂交瘤克隆编号间的关系。同一行的化合物具有相同的CDR区,并且来源于相同的鼠mAb,但以不同的形式制备。同一栏的化合物共有相同的分子形式,例如化合物的种类或同种型,但制备自不同的鼠mAb。
实施例
22
结合实验
材料与方法:血沉棕黄层获自哥本哈根医院的正常健康志愿者。通过磁珠分离,分离出CD4+
T细胞。细胞用2 ng/ml IL-12、50 ng/ml IL-18和100
ng/ml TL1A (在Novo Nordisk A/S产生的Flag-HIS-TEV-TL1A)激活,并培养5天。在第5天,细胞用10、5、1、0.5、0.1或0.0001 µg/ml抗DR3
mAb克隆0072、0073或0077,或用Fab片段克隆0087、0088或0091染色。第二PE缀合的山羊-抗小鼠(H+L)用于检测。样品为一式两份。通过FACS评价染色强度。
结果:对于单克隆IgG克隆0077及其相应的Fab克隆0091,无法检测到与细胞结合。单克隆IgG克隆0072和0073显示与细胞因子活化CD4+ T细胞强结合,在1ug/ml的浓度或更低浓度下观察到最大结合。相应的Fab克隆(0087和0088)以类似效价与细胞因子活化细胞结合,但是在结合饱和上记录到略微较低的MFI值。预期与Fab处理的细胞相比,全长抗体处理的细胞有较大的MFI观测值,因为第二(检测)抗体(抗IgG重链和轻链)与全长IgG抗体克隆的Fab和Fc部分两者结合,但仅与Fab克隆的Fab部分结合(表31)。
| 抗体或Fab片段 | 用于测定的浓度 | MFI |
| 0072 | 1 µg/ml | 1300b |
| 0073 | 1 µg/ml | 1300 |
| 0077 | 1 µg/ml | 100 |
| 0087 | 1 µg/ml | 500 |
| 0088 | 1 µg/ml | 500 |
| 0091 | 1 µg/ml | 100 |
表 31 :显示了在第5天IL-12/IL-18/TL1A活化细胞的平均荧光强度(MFI)值。以单一活的CD4+ T细胞对细胞进行门控选择。
实施例
23
T
细胞增殖:
采用CD4 Rosettesep (Stem cell technologies)和Histopaque (Sigma),通过磁珠分离,从血沉棕黄层中分离出CD4+
T细胞。在含和不含抗TL1A (1000 ng/ml;MAB7441;RnDSystems)或DR3 mAb或DR3 Fab (5或10 µg/ml)时,用2 ng/ml IL-12、50 ng/ml IL-18和100
ng/ml TL1A (Flag-HIS-TEV-TL1A;Novo Nordisk)激活T细胞(2*105个细胞/孔,96孔板中)达5天。所用的DR3 mAb为0072、0073和0077。所用的DR3 Fab为0087、0088和0091。所有样品以一式三份进行。通过胸苷掺入,测量细胞增殖。在活化5天后,细胞用[3H]胸苷脉冲,16小时后收获。通过Top Counter以每分钟计数(cpm)测定掺入的胸苷。
结果:通过用TL1A共刺激,T细胞增殖增加3倍。这种TL1A依赖性增加通过与抗TL1A中和性对照抗体共温育而被阻断。在10
µg/ml下,所有抗DR3 mAb以及Fab
0091略微抑制增殖,而Fab 0087和0088甚至用该测定法所用最低浓度都完全阻断增殖。综上所述,Fab 0087和0088在减量调节CD4阳性T细胞增殖的TL1A依赖性共刺激中是非常有效的。
在类似的实验中,与IL-12/IL-18处理的T细胞相比,IL-12 (2 ng/ml)、IL-18
(50 ng/ml)和100 ng/ml TL1A (Flag-His-TEV-TL1A;Novo Nordisk)处理的CD4+ T细胞显示T细胞增殖有6倍增加。0123和0124 Fab早在0.16 μg/ml Fab的浓度下便完全阻断所诱导的T细胞增殖,而相应的mAb 0072和0108不影响T细胞增殖。表2中显示了mAb 0072和相应Fab 0123对的数据。通过胸苷掺入而检测的增殖以每分钟计数(cpm)给出。
表
32:
| 处理 | mAb 0072 | Fab 0123 |
| IL-12/IL-18 | 1629±109 cpm | 1629±109 cpm |
| IL-12/IL-18+TL1A | 10439±689 cpm | 10439±689 cpm |
| IL-12/IL-18+TL1A+0.00128 μg/ml mAb或Fab | 10434±1132 cpm | 5492±1330 cpm |
| IL-12/IL-18+TL1A+0.16 μg/ml mAb或Fab | 11886±984 cpm | 2329±336 cpm |
| IL-12/IL-18+TL1A+10 μg/ml mAb或Fab | 10139±689 cpm | 1619±109 cpm |
标准偏差用±后的数值表示。
受抗
DR3 Fab
影响的细胞因子释放
在不存在TCR活化时,使用CD4
Rosettesep (Stem cell technologies)和Histopaque(Sigma)通过磁珠分离自血沉棕黄层分离的CD4 + T细胞用含和不含100
ng/ml TL1A (Flag-His-TEV-TL1A;Novo Nordisk)的细胞因子IL-12 (2 ng/ml)、IL-18
(50 ng/ml)刺激。48小时后,收获活化CD4+
T细胞(2x105个细胞/孔)的上清液,并通过Bioplex分析细胞因子释放。
通过TL1A在48小时后均诱导IL-12/IL-18处理的CD4+
T细胞的细胞因子IL-6、IFNγ、GM-CSF和TNFα的释放。通过TL1A诱导的IL-6、IFNγ、GM-CSF、TNFα是较之于IL-12/IL-18活化细胞的16倍(p=0.05)、1.2 (p=0.02)、7.5倍 (p=0.04)、4.4 (p=0.0007)。当与DR3结合非阻断性Fab 0091相比时,IL-6 (p=0.04)、GM-CSF
(p=0.04)和TNFα
(p=0.0008)均被抗DR3 Fab 0124显著阻断(表33)。
表
33:
| 细胞因子(平均值+/-SEM) | IL-12/IL-18活化CD4+ T细胞(平均值±SEM) | IL-12/IL-18活化CD4+ T细胞+ TL1A(平均值±SEM) | IL-12/IL-18活化CD4+ T细胞+ TL1A+0124(平均值±SEM) | IL-12/IL-18活化CD4+ T细胞+ TL1A+0091(平均值±SEM) |
| IL-6 | 361±145 | 5981±1918 | 698±282 | 9268±3564 |
| IFNγ | 4207±270 | 4893±400 | 4388±195 | 4945±516 |
| GM-CSF | 45±11 | 336±101 | 55±17 | 437±167 |
| TNFα | 23±2.3 | 102±3 | 24±2.5 | 121±21 |
标准偏差用±之后的数值表示。
实施例
24
使用自克罗恩病患者的肠活检样品分离的固有层单核细胞进行的功能研究
在含和不含抗DR3 Fab 0124和非阻断性对照0091时,将自克罗恩病患者肠活检样品分离的固有层单核细胞(LPMC)与非IBD对照用IL-12 (2 ng/ml)、IL-18 (50 ng/ml)和100
ng/ml TL1A (Flag-His-TEV-TL1A;Novo Nordisk)激活。
来自炎性克罗恩病患者的LPMC能够通过诱导IFNγ而对IL-12/IL-18 + TL1A起反应,且TL1A诱导的IFNγ水平被0124显著阻断(p=0.0001,n=4),表34。此外,DR3 Fab 0124和0228抑制IL-12/IL-18刺激、TL1A处理的克罗恩病患者的LPMC的GM-CSF、TNF-a和IFNg分泌。
表
34:
。
Claims (25)
1. 一种单价拮抗性DR3抗体,其中所述单价抗体阻断DR3与TL1A结合,且其中呈其二价形式的所述单价抗体是阻断DR3与TL1A结合的激动性抗体。
2. 权利要求1的单价抗体,其中所述单价抗体不是具有WO2011106707所示11H08抗体的CDR序列(SEQ ID NO 14+15)的抗体。
3. 前述权利要求中任一项的单价抗体,其中所述单价抗体与亲脂部分缀合。
4. 权利要求3的单价抗体,其中所述亲脂部分包含-(CH2)n-CO-脂肪酰基,其中n为16-18。
5. 权利要求3的单价抗体,其中所述亲脂部分包含-(CH2)n-CO-脂肪酰基,其中n为15。
7. 权利要求3-6中任一项的单价抗体,其中所述亲脂部分通过亲水间隔基与抗体重链中的天然存在的C239 (Kabat编号)半胱氨酸残基连接。
8. 前述权利要求中任一项的单价抗体,其中所述抗体与DR3上的表位结合,其中所述表位包含SEQ ID NO 1的I43和/或L45。
9. 前述权利要求中任一项的单价抗体,其中所述抗体与DR3上的表位结合,其中所述表位包含SEQ ID NO 1所示氨基酸G37-L45的至少一个和氨基酸L57-A59的至少一个。
10. 权利要求9的单价抗体,其中所述表位包含SEQ ID NO 1所示的氨基酸G37-L45和氨基酸L57-A59。
11. 前述权利要求中任一项的单价抗体,其中所述配体是Fab片段。
12. 前述权利要求中任一项的单价抗体,其中所述单价抗体以低于1 nM的解离常数结合DR3。
13. 前述权利要求中任一项的单价抗体,其中所述抗体与人DR3的CRD1结构域结合。
14. 一种单价抗体,其包含SEQ ID NO 10所示的3个CDR序列和SEQ ID NO
11所示的3个CDR序列。
15. 一种单价抗体,其中所述抗体包含人构架、SEQ ID NO 16所示CDR3序列和SEQ ID NO
17所示CDR3序列以及重链的“S49A”回复突变。
16. 权利要求15的单价抗体,其中所述抗体包含SEQ ID NO 16所示的3个CDR序列和SEQ ID NO
17所示的3个CDR序列。
17. 前述权利要求中任一项的单价抗体,其中所述抗体与“0228”单价抗体竞争结合人DR3,其中0228重链的氨基酸序列如SEQ
ID NO 16所示,0228轻链的氨基酸序列如SEQ ID NO 17所示。
18. 前述权利要求中任一项的单价抗体,其中所述抗体降低RA患者滑液细胞中的IFN-γ释放,其中所述滑液细胞用TL1A共刺激。
19. 前述权利要求中任一项的单价抗体,其中所述抗体降低CD患者肠活检样品固有层单核细胞(LPMC)的一种或多种细胞因子的释放,其中所述细胞因子选自:TNF-α、IL-6、GM-CSF和IFN-γ,且其中所述LPMC用TL1A、IL-12和IL-18共刺激。
20. 前述权利要求中任一项的单价抗体,其中所述抗体降低CD4+ T细胞中一种或多种细胞因子的释放,其中所述细胞因子选自:TNF-α、IL-6、GM-CSF和IFN-γ,且其中所述T细胞用TL1A共刺激。
21. 前述权利要求中任一项的单价抗体,其中所述抗体是IgG4型抗体。
22. 一种药物组合物,其包含权利要求1-21中任一项的抗体。
23. 用于治疗炎性疾病的权利要求1-21中任一项的单价抗体或权利要求22的药物组合物的用途。
24. 用于治疗克罗恩病(CD)的权利要求1-21中任一项的单价抗体或权利要求22的药物组合物的用途。
25. 用于治疗类风湿性关节炎(RA)的权利要求1-21中任一项的单价抗体或权利要求22的药物组合物的用途。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11156416 | 2011-03-01 | ||
| EP11156416.7 | 2011-03-01 | ||
| US201161448827P | 2011-03-03 | 2011-03-03 | |
| US61/448,827 | 2011-03-03 | ||
| PCT/EP2012/053539 WO2012117067A1 (en) | 2011-03-01 | 2012-03-01 | Antagonistic dr3 ligands |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103517918A true CN103517918A (zh) | 2014-01-15 |
Family
ID=44210048
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201280011136.1A Pending CN103517918A (zh) | 2011-03-01 | 2012-03-01 | 拮抗性dr3配体 |
Country Status (12)
| Country | Link |
|---|---|
| US (4) | US9737612B2 (zh) |
| EP (1) | EP2681237A1 (zh) |
| JP (1) | JP6215056B2 (zh) |
| KR (1) | KR20140043720A (zh) |
| CN (1) | CN103517918A (zh) |
| BR (1) | BR112013022052A2 (zh) |
| CA (1) | CA2828464A1 (zh) |
| IL (1) | IL227535A0 (zh) |
| MX (1) | MX2013009859A (zh) |
| RU (1) | RU2013141079A (zh) |
| WO (1) | WO2012117067A1 (zh) |
| ZA (1) | ZA201306110B (zh) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106536548A (zh) * | 2014-04-28 | 2017-03-22 | 国家生物技术研究所公司 | Dr3变体及其用途 |
| CN107001462A (zh) * | 2014-04-04 | 2017-08-01 | 协和发酵麒麟株式会社 | 激动活性降低的抗死亡受体3(dr3)拮抗性抗体 |
| CN111808183A (zh) * | 2020-07-25 | 2020-10-23 | 北京吉尔麦迪生物医药科技有限公司 | 一种靶向CD47的高亲和力SIRPα突变体及其融合蛋白 |
| CN116223818A (zh) * | 2023-05-09 | 2023-06-06 | 四川大学华西医院 | Dr3蛋白检测试剂在制备筛查aecopd的试剂盒的用途及筛查aecopd的试剂盒 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20160033504A1 (en) * | 2013-03-15 | 2016-02-04 | Alder Biopharmaceuticals, Inc. | Protocol for identifying and isolating antigen-specific b cells and producing antibodies to desired antigens |
| WO2015036553A1 (en) | 2013-09-16 | 2015-03-19 | Novo Nordisk Health Care Ag | Thiol functionalized polymers |
| CA2924520C (en) * | 2013-11-01 | 2023-09-26 | Ibc Pharmaceuticals, Inc. | Bispecific antibodies that neutralize both tnf-alpha and il-6: novel therapeutic agent for autoimmune disease |
| WO2018135646A1 (ja) | 2017-01-20 | 2018-07-26 | 国立大学法人京都大学 | CD8α+β+細胞傷害性T細胞の製造方法 |
| WO2020070288A1 (en) | 2018-10-05 | 2020-04-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and systems for controlling the agonistic properties of antibody variable domains by light |
| WO2023198851A1 (en) | 2022-04-14 | 2023-10-19 | Institut National de la Santé et de la Recherche Médicale | Methods for controlling the tumor cell killing by light |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000064465A1 (en) * | 1999-04-22 | 2000-11-02 | Human Genome Sciences, Inc. | Death domain containing receptors |
| WO2001035995A2 (en) * | 1999-11-19 | 2001-05-25 | Tittle Thomas V | Tr3-specific binding agents and methods for their use |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU690474B2 (en) | 1995-09-11 | 1998-04-23 | Kyowa Hakko Kirin Co., Ltd. | Antibody againts alpha-chain of human interleukin 5 receptor |
| WO1997033904A1 (en) | 1996-03-12 | 1997-09-18 | Human Genome Sciences, Inc. | Death domain containing receptors |
| EP1500702A1 (en) | 1996-04-01 | 2005-01-26 | Genentech, Inc. | APO-2LI and APO-3 apoptosis polypeptides from the TNFR1 familiy |
| EP1073683B1 (en) | 1998-04-30 | 2005-12-28 | Tanox, Inc. | G-csf receptor agonist antibodies and screening method therefor |
| FR2780062B1 (fr) | 1998-06-17 | 2000-07-28 | Rhone Poulenc Rorer Sa | Anticorps monoclonaux diriges contre la proteine g3bp, et leurs utilisations |
| US6638906B1 (en) * | 1999-12-13 | 2003-10-28 | Nobex Corporation | Amphiphilic polymers and polypeptide conjugates comprising same |
| CA2399388A1 (en) | 2000-02-11 | 2001-08-16 | Michael J. Lenardo | Identification of a domain in the tumor necrosis factor receptor family that mediates pre-ligand receptor assembly and function |
| WO2002040680A2 (en) | 2000-11-17 | 2002-05-23 | The Burnham Institute | Death domain proteins |
| CN100469793C (zh) | 2001-04-05 | 2009-03-18 | 株式会社免疫生物研究所 | 抗骨桥蛋白抗体及其用途 |
| CN102180944A (zh) | 2001-10-10 | 2011-09-14 | 诺和诺德公司 | 肽的重构和糖缀合 |
| KR100499989B1 (ko) | 2002-12-27 | 2005-07-07 | 네오바이오다임 주식회사 | 아사이알로 α1-산 당단백질에 대한 단일클론 항체, 이 항체를 포함하는 아사이알로 α1-산 당단백질에 대한 단일클론 항체, 이 항체를 포함하는 면역크로마토그래피 스트립 및 이 스트립를 이용한 아사이알로 α1-산 당단백질 측정방법 |
| WO2006127900A2 (en) * | 2005-05-25 | 2006-11-30 | Biogen Idec Ma Inc. | Tl1a in the treatment of disease |
| ES2611307T3 (es) | 2005-08-30 | 2017-05-08 | University Of Miami | Inmunomodulación de agonistas, antagonistas e inmunotoxinas del receptor del factor de necrosis tumoral 25 (TNFR25) |
| US20110195048A1 (en) | 2008-10-08 | 2011-08-11 | Podack Eckhard R | Regulation of lymphocytes and uses therefor |
| WO2011106707A2 (en) | 2010-02-26 | 2011-09-01 | Human Genome Sciences, Inc. | Antibodies that specifically bind to dr3 |
-
2012
- 2012-03-01 CN CN201280011136.1A patent/CN103517918A/zh active Pending
- 2012-03-01 EP EP12707996.0A patent/EP2681237A1/en not_active Withdrawn
- 2012-03-01 WO PCT/EP2012/053539 patent/WO2012117067A1/en active Application Filing
- 2012-03-01 US US13/982,617 patent/US9737612B2/en not_active Expired - Fee Related
- 2012-03-01 KR KR1020137021269A patent/KR20140043720A/ko not_active Application Discontinuation
- 2012-03-01 RU RU2013141079/10A patent/RU2013141079A/ru unknown
- 2012-03-01 MX MX2013009859A patent/MX2013009859A/es unknown
- 2012-03-01 BR BR112013022052A patent/BR112013022052A2/pt not_active IP Right Cessation
- 2012-03-01 CA CA2828464A patent/CA2828464A1/en not_active Withdrawn
- 2012-03-01 JP JP2013555876A patent/JP6215056B2/ja not_active Expired - Fee Related
-
2013
- 2013-07-18 IL IL227535A patent/IL227535A0/en unknown
- 2013-08-14 ZA ZA2013/06110A patent/ZA201306110B/en unknown
- 2013-08-23 US US13/974,275 patent/US8765130B2/en active Active
-
2014
- 2014-05-01 US US14/267,028 patent/US9713644B2/en not_active Expired - Fee Related
-
2017
- 2017-07-05 US US15/641,611 patent/US20170305994A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000064465A1 (en) * | 1999-04-22 | 2000-11-02 | Human Genome Sciences, Inc. | Death domain containing receptors |
| WO2001035995A2 (en) * | 1999-11-19 | 2001-05-25 | Tittle Thomas V | Tr3-specific binding agents and methods for their use |
Non-Patent Citations (1)
| Title |
|---|
| LENG WEN 等: "TL1A-induced NF-kB Activation and c-IAP2 Production Prevent DR3-mediated Apoptosis in TF-1 Cells", 《JOURNAL OF BIOLOGICAL CHEMISTRY》, vol. 278, no. 40, 25 July 2003 (2003-07-25), pages 39251 - 39258 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107001462A (zh) * | 2014-04-04 | 2017-08-01 | 协和发酵麒麟株式会社 | 激动活性降低的抗死亡受体3(dr3)拮抗性抗体 |
| CN106536548A (zh) * | 2014-04-28 | 2017-03-22 | 国家生物技术研究所公司 | Dr3变体及其用途 |
| CN111808183A (zh) * | 2020-07-25 | 2020-10-23 | 北京吉尔麦迪生物医药科技有限公司 | 一种靶向CD47的高亲和力SIRPα突变体及其融合蛋白 |
| CN116223818A (zh) * | 2023-05-09 | 2023-06-06 | 四川大学华西医院 | Dr3蛋白检测试剂在制备筛查aecopd的试剂盒的用途及筛查aecopd的试剂盒 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9713644B2 (en) | 2017-07-25 |
| ZA201306110B (en) | 2014-04-30 |
| IL227535A0 (en) | 2013-09-30 |
| JP6215056B2 (ja) | 2017-10-18 |
| US20130336984A1 (en) | 2013-12-19 |
| CA2828464A1 (en) | 2012-09-07 |
| US20130330360A1 (en) | 2013-12-12 |
| US20140294853A1 (en) | 2014-10-02 |
| JP2014509325A (ja) | 2014-04-17 |
| KR20140043720A (ko) | 2014-04-10 |
| RU2013141079A (ru) | 2015-04-10 |
| MX2013009859A (es) | 2014-02-28 |
| BR112013022052A2 (pt) | 2016-11-22 |
| US8765130B2 (en) | 2014-07-01 |
| US9737612B2 (en) | 2017-08-22 |
| WO2012117067A1 (en) | 2012-09-07 |
| EP2681237A1 (en) | 2014-01-08 |
| US20170305994A1 (en) | 2017-10-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103517918A (zh) | 拮抗性dr3配体 | |
| CN107614529B (zh) | Pd-l1抗体、其抗原结合片段及其医药用途 | |
| US10472414B2 (en) | Antibodies specific to pyroglutamated Aβ | |
| CN105001333B (zh) | 抗人nkg2d抗体及其用途 | |
| CN103214577B (zh) | 特异性结合cd154的包括抗体、抗体衍生物和抗体片段在内的结合蛋白及其用途 | |
| CN103874501B (zh) | Cd40l-特异性tn3-衍生的支架及其使用方法 | |
| CN110997712A (zh) | 特异性结合pd-1的抗体及其使用方法 | |
| CN106459216A (zh) | 多特异性抗体构建体 | |
| BR112021004723A2 (pt) | anticorpos de receptor anti-il4 para uso veterinário | |
| KR20230007545A (ko) | FcRn 항체 및 이의 사용 방법 | |
| CN104245736B (zh) | 抗人死亡受体5胞外区的人源化单克隆抗体 | |
| CN110407941A (zh) | Cd39的高亲和力抗体及其用途 | |
| CN108712908A (zh) | 自交联抗体 | |
| CN109476742A (zh) | Tl1a抗体及其用途 | |
| CN107849135A (zh) | 与分拣蛋白结合并抑制颗粒蛋白前体的结合的抗体 | |
| CN104203977A (zh) | 结合肽聚糖识别蛋白1的抗体 | |
| US20210009706A1 (en) | Anti-CD27 Antibody, Antigen-binding Fragment Thereof, and Medical Use Thereof | |
| CN106661104B (zh) | 抗硬骨素抗体、其抗原结合片段及其医药用途 | |
| CN104768975A (zh) | 用于增强或抑制胰岛素-样生长因子1(igf-1)的单克隆抗体 | |
| CN110114370A (zh) | 能够与人白细胞介素-6受体结合的抗体或其抗原结合片段 | |
| US20200131263A1 (en) | Anti-gitr antibody, antigen-binding fragment thereof, and pharmaceutical use thereof | |
| CN108473549A (zh) | 单链gitr受体激动剂蛋白 | |
| CN104011206A (zh) | 新型抗人ctgf抗体 | |
| WO2021112185A1 (ja) | 抗gdf15抗体 | |
| CN109890845A (zh) | 抗rankl抗体及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20140115 |
|
| WD01 | Invention patent application deemed withdrawn after publication |