CN101475552B - 羟基黄酮衍生物及其抗血小板聚集的用途 - Google Patents
羟基黄酮衍生物及其抗血小板聚集的用途 Download PDFInfo
- Publication number
- CN101475552B CN101475552B CN200910010319.1A CN200910010319A CN101475552B CN 101475552 B CN101475552 B CN 101475552B CN 200910010319 A CN200910010319 A CN 200910010319A CN 101475552 B CN101475552 B CN 101475552B
- Authority
- CN
- China
- Prior art keywords
- hydroxyflavone
- white solid
- dmso
- chloro
- nmr
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Pyrane Compounds (AREA)
Abstract
本发明属于医药技术领域,涉及羟基黄酮衍生物及其抗血小板聚集的用途。其结构通式如下所示:羟基黄酮衍生物及其类似物药学上适用的酸加成的盐作为血小板聚集抑制剂。在结构式I和结构式II中,R1,R2,R3,R4,R5相同或不同,是H,卤素,OH,CF3,NO2,NH2,CH3,OCH3;R’,R”相同或不同,是H,卤素,CH2OH,COOH,CH2Cl。本发明的这类化合物的合成方法使用Baker Venkataraman重排及浓硫酸环合等方法制备。本发明的这类化合物的合成方法简单,适应工业化生产,相对于天然的类似物更加稳定,生物活性测试显示此类化合物具有镇痛、抗炎、抗凝血活性,是一种抗血小板聚集药物。
Description
技术领域
本发明属于医药技术领域,涉及羟基黄酮衍生物及其抗血小板聚集的用途。
背景技术
临床研究表明,临床上常见的心脑血管疾病如高血压、糖尿病、心绞痛、心肌梗塞、脑梗塞及脑出血等疾病,均与血小板功能变化和血液流变学异常有关(天津医药,1992,20(11):684)。因此,防止血小板聚集具有重要意义。
血小板是由骨髓中成熟的巨核细胞裂解产生的,初生成的血小板体积较大,具有合成蛋白质的能力,黏着力强,易于聚集和发生释放反应,具有止血功能。目前认为血小板的生理活动主要有粘附,聚集和释放反应三个方面。在正常的生理条件下,血小板并不会粘附在血管内皮上,但当血管受损,血流改变或受到外界化学物质刺激时,血小板则发生三种相关联的反应,即粘附,释放和聚集,而抗血小板聚集药物又分为(1)抑制血小板花生四稀酸代谢的药物;(2)增加血小板内Camp含量的药物;(3)TXA2受体阻断剂和合成酶抑制剂;(4)一氧化氮供体;(5)阻碍ADP介导血小板活化的药物;(6)凝血酶抑制剂;(7)具有抑制血小板聚集作用的其他药物。由于影响血小板聚集的因素很多,有些药物尚存在疗效不确切,稳定性不足,具有毒副作用等缺点,但随着人们对血小板聚集的生理过程和抗血小板聚集药物的作用机制的进一步研究,寻找疗效强,对多种诱导剂均有抑制作用的广谱血小板聚集抑制剂仍是当今研究方向。
黄酮类化合物广泛存在于自然植物中,可分为黄酮、黄酮醇、异黄酮、黄烷、黄烷酮等及其甙类,具有抗肿瘤,抗炎和心脑血管疾病等多种生理活性。(Harborne JB Flavonoids(Chinese Edition),Beijing:Science Press,1983:322;Hogale MB,Pawar BN,Nikai BP.J Indian Chem Soc,1987,64:486)。也有文献(中国中药杂志,2003,28(5),420-422)报道,瓜蒌薤白白酒汤中的天然黄酮类化合物具有抗血小板聚集活性。但是天然黄酮类化合物含量低,我们设计并合成了一系列的黄酮类化合物,以克服天然黄酮类化合物的上述缺点。
发明内容
本发明的一个目的是提供新的抗血小板聚集药物。
本发明的另一个目的是提供一种药用组合物,该组合物包含有效量的所述新的抗血小板聚集化合物或其药学上可接受的盐及其药学上配伍可接受的载体。
本发明的另外一个目的是提供一种在受治疗者体内产生抗血小板聚集效应的方法,该方法包括给予受治疗者足以产生所述效应量的,所述新的抗血小板聚集化合物或其药学上可接受的盐。
本发明涉及以下通式的化合物:
其中R1,R2,R3,R4,R5相同或不同,是
H,卤素,OH,CF3,NO2,NH2,CH3,OCH3
R’,R”相同或不同,是
H,卤素,CH2OH,COOH,CH2Cl
另外,本发明还提供以下通式的化合物:
其中R1,R2,R3,R4,R5相同或不同,是
H,卤素,OH,CF3,NO2,NH2,CH3,OCH3
R’,R”相同或不同,是
H,卤素,CH2OH,COOH,CH2Cl
本发明的这类化合物的合成方法使用Baker Venkataraman重排及浓硫酸环合等方法制备这类化合物。
本发明的这类化合物的合成方法简单,适应工业化生产,相对于天然的类似物更加稳定,生物活性测试显示此类化合物具有镇痛,抗炎,抗凝血活性,是一种抗血小板聚集药物。
具体实施方式
通过下述实施例将有助于理解本发明,但并不影响本发明的内容。
实施例1:2’-氟-7-羟基黄酮
将0.03mol 2’,4’-二羟基苯乙酮,0.22mol无水碳酸钾,150mL干燥丙酮置于250mL圆底烧瓶中,常温下缓慢滴加0.06mol邻氟苯甲酰氯。滴毕后,加热至回流反应12小时。冷却,抽滤,滤饼用少量丙酮洗涤。将滤饼用稀盐酸酸化至pH4-5,抽滤,洗涤,干燥。用丙酮做重结晶。将重结晶后0.022mol1-[2-羟基-4-(2-氟苯甲酰氧基)苯基]-3-(2-氟苯基)]-1,3-丙二酮加到100mL锥形瓶中,加入36mL浓硫酸,冰浴,搅拌4小时。停止反应,将反应液倒入大量的冰水中,析出淡白色固体。抽滤,再将滤饼加入到150mL 5%的碳酸钾溶液中,煮沸后冷却,析出的固体用乙酸乙酯和乙醇重结晶,得白色固体。收率21.0%。MS m/z(M):256.23。1H-NMR(DMSO),δ(ppm):6.66(1H,s),6.95(1H,s),7.48(2H,m),7.66(2H,m),7.98(2H,m),10.89(1H,s)。
实施例2:2’-甲基-7-羟基黄酮
按照实施例1的方法,由2’,4’-二羟基苯乙酮、邻甲基苯甲酰氯反应得到白色固体。收率:38.4%。MS m/z(M):252.26。1H-NMR(DMSO),δ(ppm):2.54(3H,s),6.62(1H,s),6.89(1H,s),7.44(2H,m),7.67(2H,m),7.92(2H,m),10.92(1H,s)。
实施例3:2’-氯-7-羟基黄酮
按照实施例1的方法,由2’,4’-二羟基苯乙酮、邻氯苯甲酰氯反应得到白色固体。收率:27.6%。MS m/z(M):272.68。1H-NMR(DMSO),δ(ppm):6.49(1H,s),6.88(1H,s),6.89-6.98(1H,m),7.51-7.69(4H,m),7.76-7.79(1H,d),10.94(1H,s)。
实施例4:2’-硝基-7-羟基黄酮
按照实施例1的方法,由2’,4’-二羟基苯乙酮、邻硝基苯甲酰氯反应得到白色固体。收率:20.5%。MS m/z(M):283.24。1H-NMR(DMSO),δ(ppm):6.47(1H,s),6.83(1H,s),6.84-6.90(1H,m),7.49-7.66(4H,m),7.72-7.77(1H,d),10.91(1H,s)。
实施例5:4’-甲氧基-7-羟基黄酮
按照实施例1的方法,由2’,4’-二羟基苯乙酮、对甲氧基苯甲酰氯反应得到白色固体。收率:22.7%。MS m/z(M):268.26。1H-NMR(DMSO),δ(ppm):3.82(3H,s),6.47(1H,s),6.87(1H,s),7.39(2H,s),7.62(2H,s),7.88(2H,m),10.90(1H,s)。
实施例6:4’-氯-7-羟基黄酮
按照实施例1的方法,由2’,4’-二羟基苯乙酮、对氯苯甲酰氯反应得到白色固体。收率:21.6%。MS m/z(M):272.68。1H-NMR(DMSO),δ(ppm):6.43(1H,s),6.85(1H,s),7.42(2H,s),7.59(2H,s),7.90(2H,m),10.88(1H,s)。
实施例7:2’-氟-8-溴-7-羟基黄酮
3mmol 2’-氟-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率21.5%。MS m/z(M):335.12。1H-NMR(DMSO),δ(ppm):6.76(1H,s),7.28(1H,d),7.48(2H,m),7.68(1H,m),7.91(1H,d),8.07(1H,t),11.66(1H,s)。
实施例8:2’-甲基-8-溴-7-羟基黄酮
3mmol 2’-甲基-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率22.3%。MS m/z(M):331.16。1H-NMR(DMSO),δ(ppm):2.51(3H,s),6.48(1H,s),7.12(1H,d),7.40(2H,m),7.47(1H,m),7.63(1H,d),7.93(1H,d),11.59(1H,s)。
实施例9:2’-氯-8-溴-7-羟基黄酮
3mmol 2’-氯-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率28.2%。MS m/z(M):351.58。1H-NMR(DMSO),δ(ppm):6.68(1H,s),7.20(1H,d),7.43(2H,m),7.59(1H,m),7.82(1H,d),7.98(1H,d),11.62(1H,s)。
实施例10:2’-硝基-8-溴-7-羟基黄酮
3mmol 2’-硝基-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率19.8%。MS m/z(M):362.13。1H-NMR(DMSO),δ(ppm):6.59(1H,s),7.18(1H,d),7.42(2H,m),7.49(1H,m),7.72(1H,d),7.89(1H,d),11.54(1H,s)。
实施例11:4’-甲氧基-8-溴-7-羟基黄酮
3mmol 4’-甲氧基-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率22.8%。MS m/z(M):347.16。1H-NMR(DMSO),δ(ppm):3.87(3H,s),6.93(1H,s),7.08-7.17(3H,m),7.88(1H,d),8.10(2H,d),11.61(1H,s)。
实施例12:4’-氯-8-溴-7-羟基黄酮
3mmol 4’-氯-7-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率25.5%。MS m/z(M):351.58。1H-NMR(DMSO),δ(ppm):7.06(1H,s),7.10(2H,d,m),7.68(2H,d),7.88(1H,d),8.14(2H,d),11.67(1H,s)。
实施例13:2’-氟-6,8-二溴-7-羟基黄酮
4mmol 2’-氟-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率27.3%。MS m/z(M):414.02。1H-NMR(DMSO),δ(ppm):6.81(1H,s),7.45-7.52(2H,m),7.68(1H,m),8.06(1H,t),8.12(1H,s)。
实施例14:2’-甲基-6,8-二溴-7-羟基黄酮
4mmol 2’-甲基-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率30.1%。MS m/z(M):410.06。1H-NMR(DMSO),δ(ppm):2.50(3H,s),6.54(1H,s),7.41(2H,m),7.49(1H,t),7.63(1H,d),8.14(1H,s)。
实施例15:2’-氯-6,8-二溴-7-羟基黄酮
4mmol 2’-氯-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率33.4%。MS m/z(M):430.48。1H-NMR(DMSO),δ(ppm):6.67(1H,s),7.54-7.65(2H,m),7.69(1H,m),7.82(1H,d),8.15(1H,s)。
实施例16:2’-硝基-6,8-二溴-7-羟基黄酮
4mmol 2’-硝基-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率31.5%。MS m/z(M):441.03。1H-NMR(DMSO),δ(ppm):6.79(1H,s),7.42-7.49(2H,m),7.63(1H,m),7.98(1H,t),8.09(1H,s)。
实施例17:4’-甲氧基-6,8-二溴-7-羟基黄酮
4mmol 4’-甲氧基-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率41.3%。MS m/z(M):426.06。1H-NMR(DMSO),δ(ppm):3.84(3H,s),6.52(1H,s),7.39(2H,m),7.50(1H,t),7.59(1H,d),8.07(1H,s)。
实施例18:4’-氯-6,8-二溴-7-羟基黄酮
4mmol 4’-氯-7-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率19.8%。MS m/z(M):430.48。1H-NMR(DMSO),δ(ppm):7.11(1H,s),7.69(2H,d),8.15(3H,m)。
实施例19:2’-氟-8-氯-7-羟基黄酮
3mmol 2’-氟-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:23.2%。MS m/z(M):290.67。1H-NMR(DMSO),δ(ppm):6.72(1H,s),7.19(1H,d),7.40(2H,m),7.63(1H,m),7.88(1H,d),8.02(1H,t),11.56(1H,s)。
实施例20:2’-甲基-8-氯-7-羟基黄酮
3mmol 2’-甲基-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:31.3%。MS m/z(M):286.71。1H-NMR(DMSO),δ(ppm):2.53(3H,s),6.41(1H,s),7.10(1H,d),7.42(2H,m),7.52(1H,m),7.66(1H,d),7.89(1H,d),11.52(1H,s)。
实施例21:2’-氯-8-氯-7-羟基黄酮
3mmol 2’-氯-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:28.5%。MS m/z(M):307.13。1H-NMR(DMSO),δ(ppm):6.62(1H,s),7.18(1H,d),7.39(2H,m),7.54(1H,m),7.78(1H,d),7.93(1H,d),11.53(1H,s)。
实施例22:2’-硝基-8-氯-7-羟基黄酮
3mmol 2’-硝基-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:24.6%。MS m/z(M):317.68。1H-NMR(DMSO),δ(ppm):6.57(1H,s),7.13(1H,d),7.30(2H,m),7.49(1H,m),7.72(1H,d),7.90(1H,d),11.49(1H,s)。
实施例23:4’-甲氧基-8-氯-7-羟基黄酮
3mmol 4’-甲氧基-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:30.7%。MS m/z(M):302.71。1H-NMR(DMSO),δ(ppm):3.85(3H,s),6.95(1H,s),7.12-7.19(3H,m),7.92(1H,d),8.14(2H,d),11.67(1H,s)。
实施例24:4’-氯-8-氯-7-羟基黄酮
3mmol 4’-氯-7-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:33.8%。MS m/z(M):307.13。1H-NMR(DMSO),δ(ppm):7.12(1H,s),7.20(2H,d,m),7.72(2H,d),7.90(1H,d),8.17(2H,d),11.67(1H,s)。
实施例25:2’-氟-6,8-二氯-7-羟基黄酮
4mmol 2’-氟-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:34.2%。MS m/z(M):325.12。1H-NMR(DMSO),δ(ppm):6.77(1H,s),7.40-7.49(2H,m),7.62(1H,m),7.98(1H,t),8.02(1H,s)。
实施例26:2’-甲基-6,8-二氯-7-羟基黄酮
4mmol 2’-甲基-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:33.1%。MS m/z(M):321.15。1H-NMR(DMSO),δ(ppm):2.53(3H,s),6.52(1H,s),7.39(2H,m),7.43(1H,t),7.60(1H,d),8.04(1H,s)。
实施例27:2’-氯-6,8-二氯-7-羟基黄酮
4mmol 2’-氯-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:26.3%。MS m/z(M):341.57。1H-NMR(DMSO),δ(ppm):6.62(1H,s),7.52-7.60(2H,m),7.63(1H,m),7.79(1H,d),8.12(1H,s)。
实施例28:2’-硝基-6,8-二氯-7-羟基黄酮
4mmol 2’-硝基-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:28.5%。MS m/z(M):352.13。1H-NMR(DMSO),δ(ppm):6.59(1H,s),7.46-7.55(2H,m),7.59(1H,m),7.72(1H,d),8.07(1H,s)。
实施例29:4’-甲氧基-6,8-二氯-7-羟基黄酮
4mmol 4’-甲氧基-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:23.1%。MS m/z(M):337.15。1H-NMR(DMSO),δ(ppm):3.82(3H,s),6.50(1H,s),7.32(2H,m),7.47(1H,t),7.52(1H,d),8.02(1H,s)。
实施例30:4’-氯-6,8-二氯-7-羟基黄酮
4mmol 4’-氯-7-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:19.3%。MS m/z(M):341.57。1H-NMR(DMSO),δ(ppm):7.07(1H,s),7.63(2H,d),8.07(3H,m)。
实施例31:2’-氟-6-羟基黄酮
将0.03mol 2’,5’-二羟基苯乙酮,0.22mol无水碳酸钾,150mL干燥丙酮置于250mL圆底烧瓶中,常温下缓慢滴加0.06mol邻氟苯甲酰氯。滴毕后,加热至回流反应12小时。冷却,抽滤,滤饼用少量丙酮洗涤。将滤饼用稀盐酸酸化至pH4-5,抽滤,洗涤,干燥。用丙酮做重结晶。将重结晶后0.022mol1-[2-羟基-4-(2-氟苯甲酰氧基)苯基]-3-(2-氟苯基)]-1,3-丙二酮加到100mL锥形瓶中,加入36mL浓硫酸,冰浴,搅拌4小时。停止反应,将反应液倒入大量的冰水中,析出淡白色固体。抽滤,再将滤饼加入到150mL 5%的碳酸钾溶液中,煮沸后冷却,析出的固体用乙酸乙酯和乙醇重结晶,得白色固体。收率21.2%。MS m/z(M):256.23。1H-NMR(DMSO),δ(ppm):6.62(1H,s),6.88(1H,s),7.44(2H,m),7.61(2H,m),7.90(2H,m),10.79(1H,s)。
实施例32:2’-甲基-6-羟基黄酮
按照实施例31的方法,由2’,5’-二羟基苯乙酮、邻甲基苯甲酰氯反应得到白色固体。收率:37.8.%。MS m/z(M):252.26。1H-NMR(DMSO),δ(ppm):2.51(3H,s),6.67(1H,s),6.93(1H,s),7.56(2H,m),7.73(2H,m),7.98(2H,m),10.96(1H,s)。
实施例33:2’-氯-6-羟基黄酮
按照实施例31的方法,由2’,5’-二羟基苯乙酮、邻羟基苯甲酰氯反应得到白色固体。收率:33.5%。MS m/z(M):272.68。1H-NMR(DMSO),δ(ppm):6.42(1H,s),6.83(1H,s),6.80-6.92(1H,m),7.46-7.54(4H,m),7.67-7.72(1H,d),10.84(1H,s)。
实施例34:2’-硝基-6-羟基黄酮
按照实施例31的方法,由2’,5’-二羟基苯乙酮、邻硝基苯甲酰氯反应得到白色固体。收率:35.2%。MS m/z(M):283.24。1H-NMR(DMSO),δ(ppm):6.59(1H,s),6.78(1H,s),7.39(2H,m),7.54(2H,m),7.82(2H,m),10.68(1H,s)。
实施例35:4’-甲氧基-6-羟基黄酮
按照实施例31的方法,由2’,5’-二羟基苯乙酮、对甲氧基苯甲酰氯反应得到白色固体。收率:39.8%。MS m/z(M):268.26。1H-NMR(DMSO),δ(ppm):3.79(3H,s),6.43(1H,s),6.77(1H,s),7.31(2H,s),7.58(2H,s),7.80(2H,m),10.81(1H,s)。
实施例36:4’-氯-6-羟基黄酮
按照实施例31的方法,由2’,5’-二羟基苯乙酮、对氯基苯甲酰氯反应得到白色固体。收率:33.7%。MS m/z(M):272.68。1H-NMR(DMSO),δ(ppm):6.40(1H,s),6.69(1H,s),7.28(2H,s),7.51(2H,s),7.74(2H,m),10.67(1H,s)。
实施例37:2’-氟-5-溴-6-羟基黄酮
3mmol 2’-氟-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率31.5%。MS m/z(M):335.12。1H-NMR(DMSO),δ(ppm):6.68(1H,s),7.16(1H,d),7.42(2H,m),7.59(1H,m),7.88(1H,d),8.02(1H,t),11.58(1H,s)。
实施例38:2’-甲基-5-溴-6-羟基黄酮
3mmol 2’-甲基-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率25.6%。MS m/z(M):331.16。1H-NMR(DMSO),δ(ppm):2.52(3H,s),6.68(1H,s),7.16(1H,d),7.43-7.62(4H,m),7.32(1H,d),11.49(1H,s)。
实施例39:2’-氯-5-溴-6-羟基黄酮
3mmol 2’-氯-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率35.8%。MS m/z(M):351.58。1H-NMR(DMSO),δ(ppm):6.92(1H,s),7.26(1H,d),7.52(2H,m),7.63(1H,m),7.92(1H,d),8.15(1H,t),11.73(1H,s)。
实施例40:2’-硝基-5-溴-6-羟基黄酮
3mmol 2’-硝基-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率41.3%。MS m/z(M):362.13。1H-NMR(DMSO),δ(ppm):6.63(1H,s),7.16(1H,d),7.47(2H,m),7.59(1H,m),7.87(1H,d),8.07(1H,t),11.63(1H,s)。
实施例41:4’-甲氧基-5-溴-6-羟基黄酮
3mmol 4’-甲氧基-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率44.9%。MS m/z(M):347.16。1H-NMR(DMSO),δ(ppm):3.80(3H,s),6.53(1H,s),6.72(1H,s),7.33(2H,s),7.63(2H,s),7.84(2H,m),10.76(1H,s)。
实施例42:4’-氯-5-溴-6-羟基黄酮
3mmol 4’-氯-6-羟基黄酮溶于200mL冰醋酸中,加入3mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率35.8%。MS m/z(M):351.58。1H-NMR(DMSO),δ(ppm):6.64(1H,s),6.76(1H,s),7.37(2H,s),7.69(2H,s),7.92(2H,m),10.83(1H,s)。
实施例43:2’-氟-5,7-二溴-6-羟基黄酮
4mmol 2’-氟-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率42.6%。MS m/z(M):414.02。1H-NMR(DMSO),δ(ppm):6.92(1H,s),7.49-7.59(2H,m),7.68-7.93(2H,m),8.15(1H,s)。
实施例44:2’-甲基-5,7-二溴-6-羟基黄酮
4mmol 2’-甲基-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率28.5%。MS m/z(M):410.06。1H-NMR(DMSO),δ(ppm):2.56(3H,s),6.58(1H,s),7.52(2H,m),7.43(1H,t),7.68(1H,d),8.12(1H,s)。
实施例45:2’-氯-5,7-二溴-6-羟基黄酮
4mmol 2’-氯-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率34.7%。MS m/z(M):430.48。1H-NMR(DMSO),δ(ppm):6.62(1H,s),7.49-7.56(2H,m),7.63(1H,m),7.78(1H,d),8.06(1H,s)。
实施例46:2’-硝基-5,7-二溴-6-羟基黄酮
4mmol 2’-硝基-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率42.3%。MS m/z(M):441.03。1H-NMR(DMSO),δ(ppm):6.59(1H,s),7.39-7.46(2H,m),7.53(1H,m),7.68(1H,d),7.96(1H,s)。
实施例47:4’-甲氧基-5,7-二溴-6-羟基黄酮
4mmol 4’-甲氧基-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率43.6%。MS m/z(M):426.06。1H-NMR(DMSO),δ(ppm):3.85(3H,s),6.54(1H,s),7.42(2H,m),7.67(1H,t),7.62(1H,d),8.09(1H,s)。
实施例48:4’-氯-5,7-二溴-6-羟基黄酮
4mmol 4’-氯-6-羟基黄酮溶于200mL冰醋酸中,加入9mmol液溴,室温下搅拌24小时,将反应液倒入大量水中,析出白色固体,用无水乙醇重结晶,得到白色固体,产率44.7%。MS m/z(M):430.48。1H-NMR(DMSO),δ(ppm):6.74(1H,s),7.63(2H,m),7.87(1H,t),7.94(1H,d),8.13(1H,s)。
实施例49:2’-氟-5-氯-6-羟基黄酮
3mmol 2’-氟-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:45.8%。MS m/z(M):290.67。1H-NMR(DMSO),δ(ppm):6.72(1H,s),7.19(1H,d),7.42(2H,m),7.60(1H,m),7.87(1H,d),8.02(1H,t),11.56(1H,s)。
实施例50:2’-甲基-5-氯-6-羟基黄酮
3mmol 2’-甲基-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:26.8%。MS m/z(M):286.71。1H-NMR(DMSO),δ(ppm):2.49(3H,s),6.38(1H,s),7.08(1H,d),7.38(2H,m),7.42(1H,m),7.57(1H,d),7.81(1H,d),11.49(1H,s)。
实施例51:2’-氯-5-氯-6-羟基黄酮
3mmol 2’-氯-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:37.1%。MS m/z(M):307.13。1H-NMR(DMSO),δ(ppm):6.53(1H,s),6.92(1H,s),6.91-7.04(1H,m),7.65-7.73(4H,m),7.82-7.88(1H,d),10.96(1H,s)。
实施例52:2’-硝基-5-氯-6-羟基黄酮
3mmol 2’-硝基-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:28.8%。MS m/z(M):317.68。1H-NMR(DMSO),δ(ppm):6.52(1H,s),7.18(1H,d),7.34(2H,m),7.57(1H,m),7.83(1H,d),7.96(1H,d),11.53(1H,s)。
实施例53:4’-甲氧基-5-氯-6-羟基黄酮
3mmol 4’-甲氧基-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:35.7%。MS m/z(M):302.71。1H-NMR(DMSO),δ(ppm):3.82(3H,s),6.88(1H,s),7.02-7.13(3H,m),7.86(1H,d),8.03(2H,d),11.62(1H,s)。
实施例54:4’-氯-5-氯-6-羟基黄酮
3mmol 4’-氯-6-羟基黄酮和3mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:29.1%。MS m/z(M):307.13。1H-NMR(DMSO),δ(ppm):7.02(1H,s),7.17(2H,d,m),7.69(2H,d),7.83(1H,d),8.13(2H,d),11.60(1H,s)。
实施例55:2’-氟-5,7-二氯-6-羟基黄酮
4mmol 2’-氟-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:33.2%。MS m/z(M):325.12。1H-NMR(DMSO),δ(ppm):6.78(1H,s),7.42-7.50(2H,m),7.63(1H,m),7.98(1H,t),8.05(1H,s)。
实施例56:2’-甲基-5,7-二氯-6-羟基黄酮
4mmol 2’-甲基-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:45.0%。MS m/z(M):321.15。1H-NMR(DMSO),δ(ppm):2.51(3H,s),6.67(1H,s),7.59(2H,m),7.52(1H,t),7.70(1H,d),8.10(1H,s)。
实施例57:2’-氯-5,7-二氯-6-羟基黄酮
4mmol 2’-氯-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:40.8%。MS m/z(M):341.57。1H-NMR(DMSO),δ(ppm):6.67(1H,s),7.52-7.60(2H,m),7.71(1H,m),7.84(1H,d),8.12(1H,s)。
实施例58:2’-硝基-5,7-二氯-6-羟基黄酮
4mmol 2’-硝基-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:29.5%。MS m/z(M):352.13。1H-NMR(DMSO),δ(ppm):6.68(1H,s),7.49-7.58(2H,m),7.66(1H,m),7.80(1H,d),8.06(1H,s)。
实施例59:4’-甲氧基-5,7-二氯-6-羟基黄酮
4mmol 4’-甲氧基-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:38.6%。MS m/z(M):337.15。1H-NMR(DMSO),δ(ppm):3.77(3H,s),6.58(1H,s),7.52(2H,m),7.77(1H,d),7.74(1H,d),8.15(1H,s)。
实施例60:4’-氯-5,7-二氯-6-羟基黄酮
4mmol 4’-氯-6-羟基黄酮和9mmol氯代硫酰氯溶于100mL二氯甲烷中,回流24小时,抽滤,水洗,干燥后蒸除溶剂得到固体,用无水乙醇重结晶,得到白色固体,产率:41.3%。MS m/z(M):341.57。1H-NMR(DMSO),δ(ppm):6.91(1H,s),7.82(2H,m),7.90(1H,d),7.98(1H,d),8.07(1H,s)。
实施例61
下述实验说明本发明化合物对二磷酸腺苷(ADP)诱导血小板聚集的抑制作用。
动物:家兔,3-5kg,雌雄兼用;
仪器:SHANDA PA-196型血小板聚集仪;
药品配置方法:取40mL甲醇,60M10.9%生理盐水混合配成标准溶液,精确秤取1mg样品(精确至0.01mg),用标准溶液稀释至浓度为1mg/mL左右的溶液备用。ADP溶解在生理盐水(250uM)。
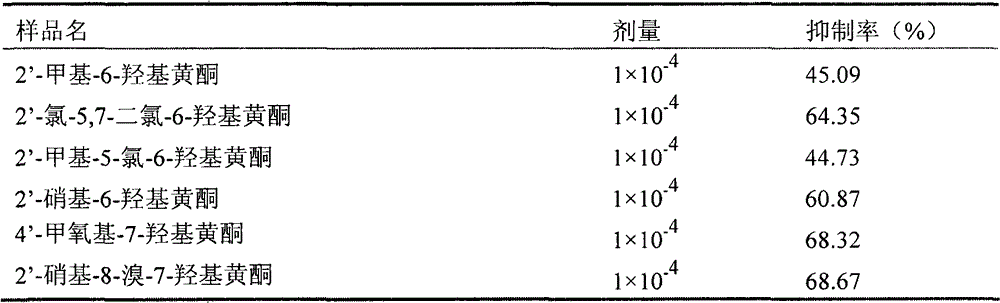
实验方法:在50mL塑料试管中加入4mL3.8%枸橼酸钠水溶液,用酒精仔细擦洗兔耳,再用二甲苯擦洗兔耳,待血管膨胀后在耳缘处涂抹凡士林,割开血管,用预备试管收集36mL血,使血混合均匀,以900转/min离心8-10min,分离出上清血浆PRP(富含血小板血浆),继而以3500转/min离心8-10min,分离出上清血浆PPP(贫含血小板血浆)。精密吸取250uLPRP加入聚集管中,向聚集管中加入含有药品的40%甲醇水溶液20uL,将分别注有250uL的PPP和PRP血浆的聚集管在37±0.01℃预热5min,以PPP250uL调零,再向比色杯中加入10uL二磷酸腺苷(ADP)诱导血小板聚集,于37℃搅拌条件下,绘制曲线,测定血小板最大聚集率,并以空白溶剂做对照,计算血小板聚集抑制率。聚集抑制率=(空白对照聚集抑制率-样品聚集抑制率)/空白对照聚集抑制率×100%。
本发明的化合物进行该实验时,表明有抑制ADP诱导血小板聚集的作用。部分样品抑制率列表如下:
实施例62
下述实验说明本发明化合物对胶原诱导血小板聚集的抑制作用。
动物:家兔,3-5kg,雌雄兼用。
药品配置方法:取90mL甲醇、10mLDMSO混合配成标准溶液I。取80mL甲醇、20mLDMSO混合配成标准溶液。精确秤取样品(精确至0.001g),用标准溶液I溶解,分别配成浓度为30umol/mL、10umol/mL、3umol/mL、1umol/mL的溶液备用,对于在标准溶液I中难溶的样品用标准溶液II溶解,配成浓度为10umol/mL、3umol/mL、1umol/mL的溶液备用。阳性对照:阿司匹林也用标准溶液I和标准溶液II分别配成如上浓度。
实验方法:在10mL塑料试管中加入1mL3.8%枸橼酸钠水溶液,用酒精仔细擦洗兔耳,再用二甲苯擦洗兔耳,待血管膨胀后在耳缘处涂抹凡士林,割开血管,用预备试管收集9mL血,使血混合均匀,以900转/min离心8-10min,分离出上清血浆PRP(富含血小板血浆),继而以3500转/min离心8-10min,分离出上清血浆PPP(贫含血小板血浆)。以PPP调零,精密吸取200uLPRP加入比色杯中,向比色杯中加入样品溶液20uL,在37±0.01℃孵育2min后,再向比色杯中加入20uL胶原诱导血小板聚集,于37℃搅拌条件下,绘制曲线,测定血小板最大聚集率,并以空白溶剂做对照,以阿司匹林为阳性对照,计算样品抗血小板聚集活性的IC50值。
本发明的化合物进行该实验时,表明有抑制胶原诱导血小板聚集的作用。
Claims (5)
1.羟基黄酮衍生物,选自
2’-氯-5,7-二氯-6-羟基黄酮;
2’-甲基-5-氯-6-羟基黄酮;
2’-硝基-8-溴-7-羟基黄酮;
2’-氯-8-溴-7-羟基黄酮;
2’-氟-8-溴-7-羟基黄酮;
4’-氯-8-氯-7-羟基黄酮。
2.一种药物组合物,其特征在于:该组合物含有效量的权利要求1的化合物或与其药学上可接受的盐,及其药学上可接受的载体。
3.权利要求1所述的化合物在制备抗血小板聚集药物中的应用。
4.权利要求2所述的药物组合物在制备抗血小板聚集药物中的应用。
5.2’-甲基-6-羟基黄酮,2’-硝基-6-羟基黄酮,4’-甲氧基-7-羟基黄酮在制备抗血小板聚集药物中的应用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN200910010319.1A CN101475552B (zh) | 2009-02-09 | 2009-02-09 | 羟基黄酮衍生物及其抗血小板聚集的用途 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN200910010319.1A CN101475552B (zh) | 2009-02-09 | 2009-02-09 | 羟基黄酮衍生物及其抗血小板聚集的用途 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101475552A CN101475552A (zh) | 2009-07-08 |
| CN101475552B true CN101475552B (zh) | 2014-03-12 |
Family
ID=40836336
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN200910010319.1A Expired - Fee Related CN101475552B (zh) | 2009-02-09 | 2009-02-09 | 羟基黄酮衍生物及其抗血小板聚集的用途 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN101475552B (zh) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102993149A (zh) * | 2012-12-17 | 2013-03-27 | 江南大学 | 一种微波辅助合成b-环取代黄酮化合物的方法 |
| CN105622562B (zh) * | 2016-03-01 | 2017-12-29 | 张田 | 一种治疗心脑血管疾病的药物组合物 |
| AU2024317564A1 (en) * | 2023-08-03 | 2026-02-19 | Huiankai (Xiamen) Pharmaceutical Technology Co., Ltd. | Modified flavone compounds and use thereof |
-
2009
- 2009-02-09 CN CN200910010319.1A patent/CN101475552B/zh not_active Expired - Fee Related
Non-Patent Citations (7)
| Title |
|---|
| Medicinal Chemistry Letters》.2004,第14卷1165-1167. * |
| Michael S.Y. Huen et al.Naturally occurring 2’-hydroxyl-substituted flavonoids as high-affinity benzodiazepine site ligands.《Biochemical Pharmacology》.2003,第66卷2397-2407. * |
| Raffaele Landolfi et al.Modification of platelet function and arachidonic acid metabolism by bioflavonoids structure-activity relations.《Biochemical Pharmacology》.1984,第33卷(第9期),1525-1530. * |
| Tran Thanh Dao et al.Synthesis and inhibitory activity against COX-2 catalyzed prostaglandin production of chrysin derivatives.《Bioorganic & Medicinal Chemistry Letters》.2004,第14卷1165-1167. |
| Tran Thanh Dao et al.Synthesis and inhibitory activity against COX-2 catalyzed prostaglandin production of chrysin derivatives.《Bioorganic & * |
| Y. B. Vibhute.Toxicity to fish of some halogeno-flavones and flavanones.《Indian J. Exp. Biol.》.1976,第14卷(第4期),489-490. * |
| 闫炳双等.7-乙酰水杨酰氧基黄酮衍生物的合成.《中国药物化学杂志》.1994,第4卷(第1期),36-40. * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101475552A (zh) | 2009-07-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101255169B (zh) | 普拉格雷盐及其制备方法 | |
| TWI471325B (zh) | Indole (Indolizine) derivatives and their pharmaceutical use | |
| EP2243772B1 (en) | Novel P2X7R antagonists and their use | |
| CN111171035B (zh) | 4-苯氧基苯基吡唑并嘧啶酰胺衍生物的制备方法和应用 | |
| CN102149384A (zh) | 作为ep4受体拮抗剂的杂环酰胺衍生物 | |
| TW201412737A (zh) | 吡唑並[3,4-c]吡啶類衍生物、其製備方法及其在醫藥上的應用 | |
| IL209004A (en) | Tetrazole compounds to reduce uric acid levels | |
| CN104387375A (zh) | 硫化氢供体型异色满酮类衍生物、其制备方法及用途 | |
| WO2017198122A1 (zh) | 抗流感小分子化合物及其制备方法和用途 | |
| CN104628661A (zh) | 一类喹喔啉酮衍生物作为醛糖还原酶抑制剂的结构、制备方法及用途 | |
| WO2020107500A1 (zh) | 2-(1-酰氧正戊基)苯甲酸与碱性氨基酸或氨基胍形成的盐、其制备方法及用途 | |
| CN101475552B (zh) | 羟基黄酮衍生物及其抗血小板聚集的用途 | |
| CN109280032B (zh) | 一种哒嗪酮母核结构的组蛋白去乙酰化酶抑制剂及其制备方法和用途 | |
| CN115381827B (zh) | 苯骈三氮唑烷基衍生物在制备治疗或预防心血管疾病的药物中的应用 | |
| CN107973788A (zh) | Bbi608衍生物及其制备与用途 | |
| CA2503674A1 (en) | Quinazolin-4-one derivatives | |
| CN106146419A (zh) | 黄嘌呤氧化酶抑制剂 | |
| CN101230049A (zh) | 氧肟酸类组蛋白去乙酰化酶抑制剂及其制备方法和用途 | |
| CN110172058B (zh) | 7-氮杂螺[5.6]十二烷-10-酮类化合物及其制备方法与用途 | |
| CN115947716B (zh) | 一种靶向Nur77的吲哚衍生物及其应用 | |
| WO2012125533A1 (en) | 3-benzyloxyphenyloxoacetic acid compounds for reducing uric acid | |
| CN102516219A (zh) | 卤代多羟基山酮衍生物及其制备方法与用途 | |
| CN104211682B (zh) | 吡啶类化合物及其用途 | |
| CN1989090B (zh) | 顺式-1,2-取代的二苯乙烯衍生物及其用于制备治疗和/或预防糖尿病的药物的用途 | |
| CN101973925A (zh) | 具有抗炎活性的2-吲哚酮类化合物、其制备方法及医药用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20140312 Termination date: 20190209 |