REFERÊNCIA CRUZADA A PEDIDO RELACIONADO
Esse pedido reivindica o benefício dos Pedidos Provisórios U.S. Nos. de Série 60/910.373, depositado em 05 de abril de 2007, e 60/910.381 depositado em 05 de abril de 2007, cujas revelações são aqui incorporadas em sua totalidade por referência.
Campo da Invenção
A presente invenção relaciona-se de modo geral ao campo de ensaios diagnósticos e de detecção. Mais particularmente, a presente invenção fornece métodos, e reagentes que incluem biochips para detecção da presença, ou para distinguir entre um ou mais analitos em uma amostra.
Fundamento da invenção
Os detalhes bibliográficos das referências fornecidas na atual especificação são listados no final da especificação.
Referência a qualquer técnica anterior nessa especificação não é, e não deve ser considerada como, uma afirmação de qualquer forma de sugestão que essa técnica prévia faz parte do conhecimento comum geral em qualquer país.
A necessidade por métodos de rastreamento rápidos e confiáveis para a detecção de múltiplos analitos em um ensaio único é vital não apenas nos campos de diagnóstico clínico, mas também para uso no rastreamento, por exemplo, para rastreamento de toxinas ambientais e fármacos.
Uma área que necessita desesperadamente de métodos aperfeiçoados de rastreamento e reagentes é no campo de doenças infecciosas. Por exemplo, uma estimativa conservadora do uso mundial de testes diagnósticos para doenças sexualmente transmitidas como Papiloma Vírus Humano (HPV), é de aproximadamente 20.000,000 testes por ano.
Vários dos testes existentes para o rastreamento das causas de doenças infecciosas são demorados, trabalhosos, dispendiosos, freqüentemente específicos para apenas um patógeno específico e/ou ao podem diferenciar entre diferentes cepas de patógenos.
HPV é o principal patógeno causador de câncer cervical. No entanto, o grupo taxonômico de HPV compreende várias “cepas” do patógeno, apenas algumas das quais são associadas ao desenvolvimento de câncer cervical e de outros carcinomas. Portanto, as cepas de HPV são tipicamente classificadas como cepas de “alto risco” incluindo as 13 cepas que respondem aproximadamente por 98% dos casos cervicais, ou cepas de “de baixo risco” que não são tipicamente associadas com o desenvolvimento de câncer cervical.
Atualmente, o câncer cervical é detectado por um teste de Papanicolau. Nessa técnica, as células são coletados do cérvix por raspagem ou lavagem. Essas células são então colocadas em uma lamina de microscópio de vidro e para produzir o “esfregaço”. Um patologista então examina a lâmina, buscando células aberrantes. O teste de Papanicolaou, no entanto, é um ensaio um tanto insatisfatório para a determinação inequivocada do risco de câncer cervical, uma vez que a técnica tem uma taxa de falso negativo de aproximadamente 20% e a técnica não pode distinguir grupo taxonômico de “alto risco” e de “baixo risco”.
Vários dos reagentes e/ou métodos para a detecção de HPV sofrem de altos custos associados e/ou consomem quantidades significativas de tempo para a finalização. Análises mais rápidas e/ou simplificadas que tenham menos custos gerais e que sejam de aplicação mais fácil são necessárias. A presente invenção é direcionada para esses e outros fins importantes.
Sumário da Invenção
A presente invenção fornece ensaios que permitem a detecção de um ou mais analitos e/ou que diferenciam entre membros em uma classe de analitos. Em particular, análise de multiplexação com base nas propriedades dos analitos e dos componentes do ensaio é empregada para identificar ou distinguir entre os analitos.
Portanto, certos aspectos da presente invenção fornecem conjuntos de esferas para a detecção de um ou mais analitos e/ou para a diferenciação entre dois ou mais membros em uma classe de analitos, em que o conjunto de esferas compreende uma pluralidade de famílias ou subconjuntos de esferas em que: (a) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (b) as esferas em cada subconjunto são ligadas a um reagente que reagirá especificamente com um analito dado de interesse em uma amostra a ser testada; (c) o reagente em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que têm uma diferente intensidade fluorescente para criar uma mistura heterogênea de subconjuntos de esferas com base na intensidade fluorescente; e (d) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto o reagente ao qual a esfera foi ligada é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de analito.
Em outros aspectos, a presente invenção contempla métodos para a detecção e/ou diferenciação entre dois ou mais analitos em uma amostra, que compreende as etapas de: (a) contato da amostra com um conjunto de esferas específico para os analitos de interesse; (b) incubação do referido conjunto de esferas com a referida amostra por um tempo e sob condições suficientes para permitir que o referido analito(s) na referida amostra reaja especificamente com um reagente em uma esferas no referido conjunto de esferas; e (c) detecção e/ou diferenciação de analitos na amostra que são ligados a um reagente na referida esfera.
Em alguns outros aspectos, o reagentes pode ser rotulado com um ou mais fluorcromos que também permitem diferenciação entre membros em uma classe de analitos. Em certos aspectos preferidos, a presente invenção fornece métodos e conjuntos de esferas que são capazes de detectar e/ou distinguir entre analitos em uma amostra biológica, em que os analitos são específicos para um patógeno infeccioso.
As amostra biológicas aqui contempladas incluem sangue, soro, saliva, fezes, urina, fluido tecidual, sêmen, exsudato, pús, e fluido e muco respiratório e esfregaços de ferimentos tópicos, cânceres e lesões.
O termo “patógeno” refere-se a um microorganismo ou vírus que infecta ou coloniza uma amostra. Exemplos de patógenos incluem vírus, bactérias, fungos e microorganismos eucarióticos. Um vírus inclui um Lentivírus (por exemplo vírus da AIDS, HIV-I, HIV-II, HTLV-IV), Retrovírus e vírus da gripe aviária. Em algumas modalidade preferidas, “patógeno” inclui um microorganismo ou vírus que infecta um organismo multicelular como um animal ou planta. Portanto, em algumas modalidades, o analito pode ser visto como um patógeno de animal ou planta. No entanto, a presente invenção engloba a detecção e/ou diferenciação de entidades não patogênicas que colonizam organismos multicelulares como simbiontes, endófitos, colonizadores gastrointestinais e outros. Os métodos da presente invenção são também aplicáveis à detecção de analitos em uma amostra que são indicativas da presença de agentes terapêuticos ou substâncias de vício. Os métodos e reagentes da presente invenção também podem ser usados na detecção de um analito em uma amostra que não é derivada de uma amostra biológica isolada de um animal ou uma planta. Como tal, os reagentes e métodos da presente invenção também se estendem à detecção de um ou mais analitos e/ou diferenciação entre analitos em amostras ambientais, que incluem amostras de ar, água e solo, incluindo solo extraterrestre, poeira ou amostras similares, amostras industriais e outras, além das amostras biológicas acima listadas.
Em certas modalidades, a presente invenção fornece métodos diagnósticos e reagentes para HPV em seres humanos e é capaz de detectar e se diferenciar entre diferentes cepas para distinguir grupo taxonômico de HPV de “alto risco” de grupo taxonômico de HPV de “baixo risco”. Portanto, em algumas modalidade preferidas, a presente invenção fornece conjuntos de esferas que são capazes de distinguir entre pluralidades de diferentes cepas de HPV. Como tal, em um aspecto, os analitos são específicos para uma pluralidade de grupos taxonômicos de HPV e os métodos e/ou reagentes são específicos para a detecção de ácido nucleico ou antígenos ou anticorpos que são específicos para a pluralidade de grupos taxonômicos de HPV.
Ainda mais preferidos, iniciadores ou marcadores de ácido nucleico capazes de ligação a uma porção específica de cepa de um genoma de HPV são imobilizados em esferas em cada subconjunto de esferas. Iniciadores direcionados a regiões conservadas em um genoma de HPV que flanqueia uma região específica para cepa são então usados para amplificar o genoma de HPV. Famílias de esferas ou subconjuntos de esferas, cada um para qualquer cepa de HPV são então usados para detectar ou distinguir a cepa de HPV.
Outros aspectos da presente invenção são direcionados a conjuntos de esferas para a detecção de uma ou mais cepas de HPV e/ou para diferenciação entre duas ou mais cepas de HPV, em que os conjuntos de esferas compreendem várias famílias ou subconjuntos de esferas em que: (a) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (b) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (c) o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (d) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de seqüência.
Outros aspectos da presente invenção contemplam métodos para a detecção e/ou diferenciação entre duas ou mais cepas de HPV em uma amostra, que compreende as etapas de: (a) contato da amostra com um conjunto de esferas que compreende várias famílias ou subconjuntos de esferas em que: (i) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (ii) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (iii)o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (iv) pelo menos dois subconjuntos de esferas são misturados para produzir um, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade e discriminação de seqüência; (b) incubação do referido conjunto de esferas com a referida amostra por um tempo e sob condições suficientes para permitir que os referidos marcadores se liguem ao genoma de HPV amplificado para gerar um réplicon que compreende uma região específica para cepa; (c) detecção e/ou diferenciação dos amplicons gerados na amostra que são ligados às referidas esferas para assim identificar ou distinguir entre as duas ou mais cepas de HPV.
Em alguns aspectos preferidos, as esferas nos conjuntos de esferas são distinguíveis com base no tamanho, no nível de intensidade fluorescente, no tipo de fluorcromo e o reagente que é capaz de reagir com um analito específico.
Em outros aspectos, a presente invenção é direcionada a conjuntos de esferas para a detecção de uma cepa de HPV e/ou para diferenciação entre duas ou mais cepas de HPV, em que os conjuntos de esferas compreendem várias famílias ou vários subconjuntos de esferas que têm: (a) pelo menos dois subconjuntos de esferas, em que cada subconjunto de esferas é fisiologicamente distinguível de qualquer outro subconjunto de esfera com base em pelo menos o tamanho; ou (b) pelo menos um subconjunto de esferas que tem pelo menos duas famílias, em que as esferas em um subconjunto de esferas são homogêneas em tamanho com relação uma à outra, e são fisiologicamente distinguíveis em duas ou mais famílias de esferas com base no nível de rotulagem que cada um contém, ou (c) uma combinação das referidas famílias de esferas e referidos subconjuntos de esferas; e em que: as esferas em cada família de esfera de um subconjunto são ligadas a um marcador de captura de ácido nucleico opcionalmente rotulado capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, a pelo menos uma de uma seqüência de ácidos nucleicos de controle, desde que qualquer marcador de captura de ácido nucleico ou seqüência de ácidos nucleicos de controle é rotulado com o mesmo rótulo como outros marcadores de captura rotulados ou seqüência de ácidos nucleicos de controle no subconjunto de esfera, e em qualquer subconjunto único de esferas, cada família de esferas desses tem uma diferente intensidade fluorescente; e cada família de esferas é específica para a detecção de uma cepa de HPV diferente de qualquer outra família de esfera no conjunto de esferas; em que o referido conjunto de esferas é capaz de identificar uma ou mais cepas específicas de HPV através de análise do tamanho da esfera, intensidade fluorescente, ou discriminação de seqüência de pelo menos uma família de esferas ou subconjunto de esferas, com o uso de citometria de fluxo.
A invenção é também direcionada em parte a métodos para a preparação de um conjunto de esferas para diferenciação entre duas ou mais cepas de HPV, o método compreende a seleção de várias famílias ou subconjuntos de esferas com base no tamanho, intensidade fluorescente, ou ambos, que compreende o fornecimento de: (a) pelo menos dois subconjuntos de esferas, em que cada subconjunto de esferas é fisiologicamente distinguível de qualquer outro subconjunto de esferas com base pelo menos no tamanho; ou (b) pelo menos um subconjunto de esferas que tem pelo menos duas famílias, em que as esferas em um subconjunto de esfera são homogêneas em tamanho com relação uma à outra, e são fisiologicamente distinguíveis em duas ou mais famílias de esferas com base no nível de rotulagem que cada um contém, ou (c) uma combinação das referidas famílias de esferas e referidos subconjuntos de esferas; e em que: as esferas em cada família de esfera de um subconjunto são ligadas a um marcador de captura de ácido nucleico opcionalmente rotulado capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, a pelo menos uma de uma seqüência de ácidos nucleicos de controle, desde que qualquer marcador de captura de ácido nucleico ou seqüência de ácidos nucleicos de controle seja rotulado com o mesmo rótulo que outros marcadores de captura rotulados ou seqüência de ácidos nucleicos de controle no subconjunto de esfera, e que em qualquer subconjunto único de esferas, cada família de esferas desses tem uma diferente intensidade fluorescente; e cada família de esferas é específica para a detecção de uma cepa de HPV diferente de qualquer outra família de esfera nos conjuntos de esferas; em que o referido conjunto de esferas é capaz de identificar uma ou mais cepas de HPV específicas através da análise do tamanho da esfera, intensidade fluorescente, ou discriminação de seqüência de pelo menos uma família de esfera ou subconjunto de esfera, com o uso de citometria de fluxo.
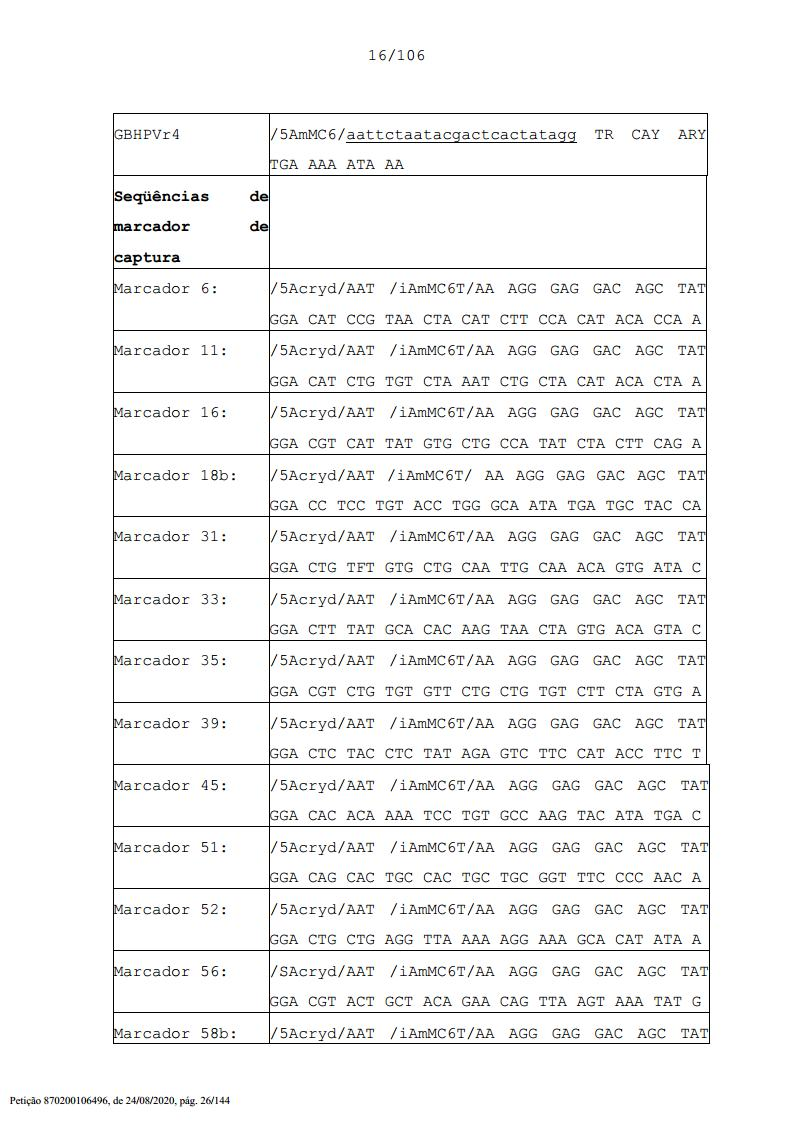
Os métodos da presente invenção em relação a detecção de HPV podem ser usados para distinguir entre de 2 e 16 cepas de HPV incluindo entre 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 e 16 cepas. Em vista da utilidade de um controle, a presente invenção pode usar portanto de 2-17 diferentes esferas ou conjuntos de esferas. Em outra modalidade, os conjuntos de esferas compreendem pelo menos 16 subconjuntos de esferas para as cepas de HPV 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 e 68, e tipicamente um conjunto de esferas de controle. Marcadores de captura adequados são aqueles listados na Tabela 2.
Pode ser desejável testar mais de 16 cepas de um analito. Assim, a presente invenção também inclui conjuntos de esferas com 2-30 diferentes esferas ou conjuntos de esferas, que incluem 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, e 30 esferas ou conjuntos de esferas.
A presente invenção é direcionada em parte a certos pares de iniciadores para uso em qualquer uma das numerosas técnicas de PCR para amplificação de seqüências de ácidos nucleicos, em que os iniciadores adiante e reverso têm opcionalmente pontas (“heels”) conjugadas ao terminal 5' do iniciador. Em certas modalidades a invenção é direcionada a pares de iniciadores de amplificação de oligonucleotídeo para direcionamento de HPV oncogênico, o iniciador direto do par, selecionado do grupo que consiste em: TR TTT GTT ACT GTK GTD GAT ACY A; CAR YTR TTT GTT ACT GTK GTD GAT A; CAR YTR TTT GTT ACT GTK GTD GA; AAY CAR YTR TTT GTT ACT GTK GT; TTT GTT ACT GTK GTD GAT ACY AC HCG; TTT GTT ACT GTK GTD GAT ACY AC HCG YAG; GTK GTD GAT ACY AC HCG YAG TAC e GTD GAT ACY AC HCG YAG TAC HAA; e o iniciador reverso do par de iniciadores é selecionado do grupo que consiste em: TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG; CAY ARY TGA AAA ATA AAY TGY AAA TC; TR CAY ARY TGA AAA ATA AAY TG; e TR CAY ARY TGA AAA ATA AA; em que os iniciadores adiante e reverso são opcionalmente conjugados a uma ponta no terminal 5’ do iniciador.
A determinação de se a ligação ocorreu entre um analito e um reagente presente em uma esfera pode ser feita com o uso de qualquer metodologia que permita a diferenciação entre diferentes esferas no conjunto de esferas. Em certas modalidades particularmente preferidas, os métodos de diferenciação entre diferentes esferas nos conjuntos de esferas utilizam citometria de fluxo.
A presente invenção também contempla kits diagnósticos para uso de acordo com os reagentes e métodos da presente invenção. Em particular, a presente invenção estende-se a biochips e a miniaturização dos componentes de fase sólida do ensaio para gerar reagentes de nanoensaio. Em uma modalidade, o conjunto de esferas ou parte desse ou outros reagentes são imobilizados a uma fase sólida como um biochip. O biochip também pode ser visto como um “biolab” em que pelo menos parte do ensaio é realizada e/ou os resultados são registrados.
Uma lista de abreviações aqui usadas é fornecida na 15 Tabela 1.
Um resumo das seqüências aqui usadas é mostrado na Tabela 2. Tabela 2-Seqüências (5' sendo na esquerda, 3' na direita)
* em que as bases sombreadas correspondem às diferenças.
As seguintes variáveis são aqui usadas: “K” é uma variável para G ou T; “H” é uma variável para os nucleotídeos T, A, ou C; “M” é uma variável para os nucleotídeos A ou C; “Y” é uma variável para os nucleotídeos T ou C; “R” é uma variável para os nucleotídeos A ou G; “W” é uma variável para os nucleotídeos A ou T; “D” é uma variável para os nucleotídeos A, T, ou G; 3Phos é um grupo 3' fosfato; 5Phos é um grupo 5' fosfato; e, 5AmMC6 é um grupo 5' H2N-(CH2)6- anexado por meio de um grupo fosfato.
Breve descrição das figuras
A Figura 1 é uma representação gráfica que mostra um esquema de um exemplo de um protocolo de extração de DNA usado no método diagnóstico para HPV.
A Figura 2 é uma representação gráfica que mostra um protocolo de PCR que pode ser usado para amplificar HPV e DNA humano a partir de uma amostra de DNA. GP5+ e GP6+ referem=se a iniciadores universais de HPV que se ligam a seqüências conservadas (Y) em HPV e geram um amplicon que compreende uma região que é variável entre cepas de HPV (X1.16). Iniciadores LCl_F e LC1_R amplificam uma região de DNA genômico humano (Z) que serve como um controle nas etapas posteriores de hibridização. Iniciadores GP6+ e LC 1_R compreendem um rótulo fluorescente que é incorporado no amplicon gerado.
A Figura 3 é uma representação gráfica que mostra a diferenciação de microesferas com base no tamanho. Seis grupos que correspondem a microesferas que compreendem diâmetros de 3,0 μm, 3,5 μm, 4,1 μm, 5,0 μm, 5,6 μm e 6,8 μm são mostrados.
A Figura 4 é uma representação gráfica que mostra a diferenciação de microesferas do mesmo tamanho com base na intensidade do rótulo fluorescente. Intensidades relativas de TMR de 0%, 4%, 20% and 100% podem ser claramente distintas.
A Figura 5 é um diagrama esquemático que mostra um exemplo dos agentes de ligação que podem ser usados no arranjo. O arranjo compreende microesferas que compreendem diâmetros de 3,0 μm, 3,5 μm, 4,1 μm, 5,0 μm, 5,6 μm e 6,8 μm e intensidades de sinal de rótulo fluorescente de 0%, 4%, 20% e 100%. In No caso dos tamanhos menores de esfera, ou seja, 3,0 μm, 3,5 μm, e 4,1 μm, intensidades de TMR de 0% e 100% foram usadas; para as microesferas de 5,0 μm intensidades de TMR de 0%, 20% e 100% foram usadas; e para as microesferas maiores, o diâmetro de 5,6 μm e 6,8 μm, todas as intensidades de sinal foram usadas.
A Figura 6 mostra um exemplo de um conjunto de esferas da presente invenção.
A Figura 7 é uma representação gráfica que mostra um exemplo do arranjo do agente de ligação ao qual um amplicon foi ligado. Os resultados mostram ligação à seqüência viral conservada, Y, a seqüência de controle humana Z, e a seqüência específica para cepa viral X16.
Descrição detalhada da invenção
A presente invenção fornece ensaios e reagentes que incluem biochips que permitem a detecção de um ou mais analitos e/ou para diferenciar entre membros em uma classe de analitos. Em particular, os analitos são identificados ou distinguidos por métodos de análise de multiplexação com base nas propriedades dos analitos e dos componentes do ensaio. Os ensaios diagnósticos e de detecção e reagentes da presente invenção têm aplicação particular no diagnóstico de infecções por patógeno em seres eucarióticos multicelulares. Em uma modalidade particular, a presente invenção fornece um ensaio diagnóstico para HPV em seres humanos e é capaz de diferenciar entre grupos taxonômicos de HPV para distinguir as infecções por HPV de “alto risco” das infecções por HPV de “baixo risco”. Além, disso, a presente invenção também fornece métodos de diagnóstico ou avaliação do risco de desenvolvimento de uma doença associada a uma infecção por um analito em um ser eucariótico multicelular que incluem, entre outros, câncer cervical em um ser humano.
Deve-se compreender que a menos que indicado de outro modo, a atual invenção não é limitada a protocolos específicos de diagnóstico ou ensaio, uma vez que esses podem variar. Também deve-se entender que a terminologia aqui usada é para objetivos de descrição de modalidade particular apenas e não pretende ser limitante.
Deve ser observado que, como usado na atual especificação, as formas singulares “um”, “uma” e “o/a” incluem aspectos no plural a menos que o contexto já dite em contrário. Portanto, por exemplo, referência a “um analito” inclui um analito único bem como dois ou mais analitos; um “substrato fisiologicamente distinguível” inclui um substrato único bem como dois ou mais substratos; referência a “um alvo” inclui um alvo único, bem como dois ou mais alvos; referência a “uma amplificação” inclui uma amplificação única, bem como múltiplas etapas de amplificação; referência “ao amplicon” inclui um complexo de amplicons único ou múltiplos; e assim por diante.
Portanto, em um aspecto, a presente invenção fornece conjuntos de esferas que são capazes de detectar, e/ou diferenciar entre dois ou mais analitos em uma amostra, os referidos compreendem: (a) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (b) as esferas em cada subconjunto são ligadas a um reagente que reagirá especificamente com um dado analito de interesse em uma amostra a ser testada; (c) o reagente em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de subconjuntos de esferas com base na intensidade fluorescente; e (d) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto o reagente ao qual a esfera foi ligada é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de analito.
Em algumas modalidades, o reagentes também pode ser diferencialmente rotulado para criar subpopulações adicionais de esferas com base na incorporação de diferentes fluorcromos.
Em outra modalidade, a presente invenção fornece métodos ou conjuntos de esferas para a detecção e/ou diferenciação de um analito.
Em certos aspectos preferidos, os métodos ou conjuntos de esferas da presente invenção são capazes de detectar e/ou diferenciar analitos patogênicos.
A presente invenção também fornece métodos para a detecção e/ou diferenciação de entre um ou mais analitos em uma amostra que compreende as etapas de: (a) contato da amostra com um conjunto de esferas específico para os analitos de interesse; (b) incubação do referido conjunto de esferas com a referida amostra por um tempo e sob condições suficientes para permitir que o referido analito(s) na referida amostra reaja especificamente com um reagente em uma esfera no referido conjunto de esferas; e (c) detecção e/ou diferenciação de analitos na amostra que são ligados a um reagente na referida esfera.
Como aqui usado, o termo “analito patogênico” refere- se a um microorganismo ou vírus que supostamente infecta, coloniza ou contaminou a amostra. Exemplos de analitos patogênicos incluem vírus, bactérias, fungos e microorganismos eucarióticos. Em uma modalidade preferida, “analito” inclui um microorganismo ou vírus que infecta i, organismo multicelular como um animal ou planta. Portanto, em algumas modalidades os analitos patogênicos podem ser considerados como um patógeno para o animal ou planta. Entretanto, a presente invenção engloba uma detecção e diferenciação de analitos não patogênicos que colonizam organismos multicelulares como micróbios simbiontes de animais (por exemplo, Lactobacillus spp., bactérias de ruminantes), micróbios simbiontes de insetos (por exemplo, Streptomyces, spp., Wolbachia spp.), micróbios simbiontes de esponjas (por exemplo, alga verde, dinoflagelados, cianobactérias) e outros; endófitos de plantas (por exemplo, Mycorrhiza, Rhizobium spp., Frankia spp., Streptomyces spp.); e outros. Além disso, o analito pode ser um analito que não é associado a um organismo multicelular. Tais analitos incluem bactérias, fungos, vírus, protistas, nematódeos e outros que colonizam ambientes particulares que incluem ambientes “naturais” como solo, oceanos, água fresca, gelo, pedra, descargas hidrotermais e ar; ambientes de cuidados com a saúde que incluem hospitais, equipamento hospitalar, equipamento cirúrgico, vestimentas dos profissionais de saúde e outros; ambientes “industriais” que incluem instalações de produção, instalações farmacêuticas, cervejarias, caves e outros; ambientes “laboratoriais” que incluem fermentadores, cultura, bancadas, equipamento e outros.
Consequentemente, as amostras contempladas pela presente invenção incluem amostras industriais como ar, água, e solo, e outras, e amostra biológicas como sangue, soro, saliva, fezes, urina, fluido tecidual, sêmen, exsudato, pus, fluido e muco respiratório e esfregaços de ferimentos tópicos, cânceres e lesões. Além disso, a amostra pode ser uma amostra extraterrestre como de um meteorito ou de um outro planeta. Em relação ao último, o ensaio da presente invenção pode ser adaptados para uso em um veículo remoto interplanetário para teste de solo ou poeira ou amostras de gelo ou para teste de material de núcleo em um planeta.
Em algumas modalidade preferidas, o analito compreende uma bactéria, fungo, vírus e/ou parasita eucariótico que infecta um animal. “Animal” aqui contemplado inclui qualquer animal, preferivelmente um mamífero e mais preferivelmente um primata que inclui um primata inferior e ainda mais preferivelmente, um humano. Para fins de conveniência, um “animal” também inclui especificamente espécies como gado, cavalos, carneiros, porcos, cabras e mulas bem como animais de laboratório que incluem camundongos, ratos, coelhos, porquinhos da Índia e hamsters.
Exemplos de analitos humanos que podem ser detectados com o uso dos reagentes e métodos da presente invenção incluem vírus como Papiloma Vírus Humano (HPV), coronavírus que incluem o vírus da SARS, vírus influenza, vírus da gripe aviária, HIV incluindo HIV-1, HIV- II ou HLTV-IV, Lentivírus em geral, vírus da hepatite e outros, os agentes patogênicos de doenças sexualmente transmitidas como Clamídia, Gonorréia, Mycoplasma spp. e Sífilis; patógenos com origem em alimentos como Listeria spp., Salmonella spp., E. coli (particularmente E. coli HO 567), Shigella spp., Brucella spp., Staphylococcus aureus;patógenos nosocomiais como S. aureus incluindo S. Aureus resistente à meticilina (MRSA) e enterococcos incluindo Enterococos resistentes à vancomicina (VRE); patógenos ambientalmente adquiridos como Legionella spp., Giardia spp., Crytospiridium spp., Bacillus anthacis (antraz) e outros.
Em outros aspectos, a amostra em que o analito é detectado é preferivelmente uma amostra derivada de um ser multicelular que é supostamente infectado ou colonizado pelo analito. Portanto, em um aspecto, a amostra é preferivelmente uma “amostra biológica”. Exemplos de amostras biológicas que não limitam a presente invenção incluem amostras de tecido ou célula como célula de raspagem, biópsias e outros e amostras de fluido corporal que incluem sangue, urina, linfa, fluido amniótico, fluido cefalorraquidiano e outros.
Em outros aspectos, os métodos da presente invenção são também aplicáveis a um detecção de um “analito” em uma amostra que não é exclusivamente derivada de um organismo eucariótico multicelular. Como tal, a presente invenção estende-se à detecção, e/ou diferenciação entre um ou mais grupos taxonômicos particulares ou cepas de analitos em amostras como amostras ambientais (incluindo ar, água e amostras de solo), amostras industriais, amostras laboratoriais e outras. Por exemplo, os métodos da presente invenção podem ser usados para avaliar a microflora procariótica, microflora eucariótica e/ou carga viral de uma amostra de solo, água ou ar ou uma amostra derivada de um objeto feito pelo homem ou superfície.
Em algumas modalidades particularmente preferidas da presente invenção, o analito a ser detectado é HPV ou uma cepa desse e a amostra é preferivelmente uma amostra biológica derivada de um ser humano. Em uma modalidade também preferida, a amostra biológica compreende uma ou mais células do indivíduo, sangue ou urina. Mais preferivelmente, a amostra biológica compreende células cervicais coletadas do indivíduo. HPV é descrito em detalhes por Gearhart e cols. (www.emedicine.com/MED/topic1037.htm, 2004) que é reproduzido em parte abaixo. HPVs produzem tumores epiteliais da pele e membranas mucosas. Mais de 100 tipos de HPV foram detectados, e os genomas de quase 70 foram seqüenciados completamente. O sistema atual de classificação, que é baseado em similaridades em suas seqüências genômicas, geralmente está correlacionado com as 3 categorias usadas para descrever HPV clinicamente: anogenital e/ou mucoso, não genital cutâneo, e epidermodisplasia verruciforme (EV). Um base de dados de seqüências genômicas de HPV e uma árvore filogenética são disponíveis na Internet em bases de dados de Seqüência de HPV.
As infecções mucosas por HPV são classificadas como latentes (assintomáticas), subclínicas, ou clínicas. As lesões clínicas são excessivamente aparentes, enquanto as infecções latentes são detectadas apenas por testes para o DNA viral. As lesões subclínicas são identificadas por aplicação de ácido acético a 5% e inspeção sob aumento. A maior parte das infecções por HPV são latentes; as infecções clinicamente aparentes comumente resultam em verrugas em vez de malignidades.
Os tipos 6 e 11 de HPV são tipicamente rotulados como de baixo risco porque a infecção com esses tipos tem baixo potencial oncogênico e comumente resulta na formação de condilomas e lesões pré-cancerosas de baixo grau. Os tipos 16 e 18 de HPV surgiram como os tipos de alto risco de HPV porque elas são responsáveis pala maioria das lesões intra- epiteliais de alto grau que podem progredir para carcinomas, particularmente aqueles na categoria anogenital e/ou mucosa.
A infecção por HPV isoladamente não causa transformação maligna do tecido infectado. Cofatores, como 5 uso de tabaco, radiação ultravioleta, gravidez, deficiência de folato e supressão imune estão envolvidos nesse processo. A Tabela 3 lista uma variedade de doenças e s subtipos de HPV associados.
Os Papilomavírus são espécies altamente específicas e não infectam outras espécies, mesmo sob condições laboratoriais. Humanos são o único reservatório conhecido para HPV.
Os Papilomavírus são vírus não envelopados de simetria icosaédrica com 72 capsômeros que circundam um genoma que contém DNA circular de duplo filamento com aproximadamente 8.000 pares de base.
Acredita-se que os Papilomavírus tenham dois modos de replicação, ou seja, replicação do genoma epissomal em células basais e descontrolada, ou vegetativa, replicação em células mais diferenciadas para gerar progênie do vírus. Embora todas as células de uma lesão contenham o genoma viral, a expressão de genes virais é fortemente ligada ao estado da diferenciação celular. A maior parte dos genes virais não é ativada até que o queratinócito infectado deixe a camada basal. A produção de partículas virais pode ocorrer apenas em queratinócitos altamente diferenciados; portanto, a produção do vírus ocorre apenas na superfície epitelial em que as células finalmente entram em contato com o ambiente.
Acredita-se que as lesões por HPV surjam da proliferação de queratinócitos basais infectados. A infecção ocorre tipicamente quando as células basais são expostas ao vírus infeccioso através de uma barreira epitelial rompida como ocorre durante o intercurso sexual ou depois de pequenas abrasões cutâneas. As infecções por HPV não são citolíticas, um tanto de partículas virais são liberadas como um resultado da degeneração de células em descamação. Além disso, o vírus HPV pode sobreviver por vários meses e em baixas temperaturas sem um hospedeiro.
A multiplicação do vírus é geralmente confinada ao núcleo. Conseqüentemente, as células infectadas comumente exibem um alto grau de atipia nuclear. Coilocitose (do grego koilos, significando vazio) descreve uma uma combinação de halo perinuclear com um núcleo picnótico ou encolhido (rasinoide) e é uma característica de infecção produtiva por papilomavírus.
O genoma de HPV existe como um DNA circular epissomal separado do núcleo da célula hospedeira em lesões por HPV benignas ou de baixo risco, como aquelas tipicamente associadas aos tipos 6 e 11 de HPV. Os genomas dos tipos de alto risco de HPV 16 e 18 são tipicamente integrados no Dna da célula hospedeira em lesões malignas. A presente invenção, no entanto, estende-se a qualquer cepa de HPV incluindo, sem limitação, as cepas 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 e 68. A integração do genoma viral no genoma da célula hospedeira é considerada um marco da transformação maligna. As proteínas de HPV E6 e E7 de sorotipos de alto risco mostraram inativar as proteínas supressora de tumor do hospedeiro p53 e Rb, assim resultando em proliferação desregulada da célula hospedeira e transformação maligna.
Portanto, em outros aspectos, a presente invenção fornece métodos para a detecção de, e/ou diferenciação entre, uma ou mais cepas particulares de HPV em uma amostra biológica, os referidos métodos compreendendo as etapas de: (i) obtenção de uma amostra biológica que supostamente compreende HPV de um ser humano; (ii) isolação de ácido nucleico da referida amostra; (iii) amplificação do ácido nucleico da referida amostra com o uso de iniciadores que geram um amplicon que é distinto para cada cepa de HPV; (iv) opcionalmente amplificação de uma seqüência de ácidos nucleicos de controle; (v) efetuar a rotulagem do amplicon(s) citado nas etapas (iii) e/ou (iv); (vi) hibridizar o amplicon(s) rotulado a um conjunto de esferas revestido com reagentes em que cada membro dos conjuntos de esferas compreendem uma molécula de ácido nucleico complementaridade a uma seqüência de nucleotídeos de uma cepa particular de HPV ou uma seqüência de nucleotídeos de controle, ligada ou associada a uma esfera fisiologicamente distinguível; e (vii) determinar a qual dos reagentes um amplicon foi ligado; em que a associação de um amplicon com um reagente particular é indicativa da presença de uma cepa particular de HPV na amostra.
Ainda em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeo de sinal.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeo de bloqueio.
A presente invenção permite a detecção de DNA amplificado de HPV ou, com o uso de uma transcriptase reversa, RNA correspondente. Portanto, a presente invenção contempla esferas com RNA ou DNA ou análogos químicos desses.
Os métodos da presente invenção são baseados, em parte, na detecção e/ou diferenciação entre uma ou mais cepas particular de um analito em uma amostra. Aqui referência a “cepas particulares de um analito” inclui quaisquer variantes da espécie ou grupo taxonômico do analito. Exemplos de “cepas” de um analito incluem subespéciesdo analito, variantes do analito com níveis diferentes de virulência, variantes do analito que indicam diferentes prognósticos quando da infecção ou colonização de um hospedeiro, variantes bioquímicas do analito e outros.
Em algumas modalidade preferidas, os métodos da presente invenção podem ser adaptados para a detecção e/ou diferenciação entre cepas particulares de HPV que são associada a maior risco ou maior potencial oncogênico em humanos (cepas de alto risco) e aquelas que são associadas a risco menor de carcinoma ou baixo potencial oncogênico (cepas de baixo risco). Portanto, o termo cepa de HPV de “alto risco” inclui qualquer cepa de HPV que seja associada ao desenvolvimento de carcinoma, incluindo câncer cervical, em seres humanos. Como acima indicado, exemplos de cepas de HPV de alto risco, que de modo alguma limitam a invenção, incluem HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 e 68. Os marcadores de captura adequados nas esferas para essas cepas de HPV são mostrados na Tabela 2. O termo “marcador” e “iniciador” pode ser usado de modo intercambiável nesse contexto. Cepas de “baixo risco” de HPV incluem aquelas que não são associadas ou apenas fracamente associada a risco aumentado de carcinoma em indivíduos humanos. Tipicamente, as cepas de HPV de baixo risco são as cepas eu formam verrugas, incluindo HPV 6 e HPV 11.
As esferas da presente invenção são ligadas a reagentes que interagirão especificamente com um dado analito de interesse em uma amostra. Em alguns aspectos, os reagentes da presente invenção são ácidos nucleicos e o analitos na amostra que reage especificamente com o reagente são também ácidos nucleicos.
Portanto, esse aspecto da atual invenção usa iniciadores que são direcionados a regiões conservadas de uma cepa de HPV mas que flanqueiam seqüências genômicas específicas para a cepa. As seqüências específicas para a cepa são referidas como seqüências “variáveis” uma vez que elas variam entre cepas comparadas às seqüências conservadas que são constantes entre cepas. Após amplificação, os amplicons são colocados em contato com subconjuntos de esferas no conjunto de esferas em que cada esfera de cada subconjunto carrega um iniciador ou marcador de ácido nucleico de captura capaz de hibridizar a amplicons específicos para cepa. Multiplexação que usa tamanho de esfera, intensidade de fluorescência e especificidade de ligação de DNA permite a identificação, distribuição e distinção das cepas de HPV.
Conseqüentemente, outros aspectos da presente invenção contemplam conjuntos de esferas para a detecção de uma ou mais cepas de HPV e/ou para diferenciação entre duas ou mais cepas de HPV, em que o conjunto de esferas compreende várias famílias ou subconjuntos de esferas em que: (a) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (b) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (c) o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (d) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de seqüência.
Ainda outros aspectos da presente invenção contemplam um métodos para a detecção e/ou diferenciação de entre duas ou mais cepas de HPV em uma amostra, que compreende as etapas de: (a) contato da amostra com um conjunto de esferas que compreende várias famílias ou subconjuntos de esferas em que: (i) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (ii) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (iii) o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (iv) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de seqüência; (b) incubação do referido conjunto de esferas com a referida amostra por um tempo e sob condições suficientes para permitir que os referidos iniciadores se liguem ao genoma de HPV amplificado para gerar um réplicon que compreende uma região específica para cepa; (c) detecção e/ou diferenciação dos amplicons gerados na amostra que são ligados às referidas esferas para assim identificar ou distinguir entre as duas ou mais cepas de HPV.
Os amplicons aos quais os marcadores de captura de ácidos nucleico são específicos também podem ser rotulados com uma molécula repórter fluorescente.
Ácidos nucleicos podem ser isolados da amostra do indivíduo com o uso de qualquer método que seja conveniente com relação à natureza da amostra em si e o analito. Como aqui usado, o termo “ácido nucleico” refere-se a DNA e/ou RNA. Tipicamente, DNA é isolado, embora sob algumas circunstâncias que podem ser evidentes para pessoa habilitada na técnica, possa ser mais preferível isolar RNA, por exemplo, quando o analito de interesse é um RNA vírus. Se RNA é isolado, o RNA pode ser amplificado, ou o RNA pode ser transcrito de modo reverso em cDNA com o uso de métodos padrão, para subseqüente amplificação e análise.
Preferivelmente, o “ácido nucleico” é DNA. DNA pode ser isolado da amostra com o uso de qualquer meio conveniente. Por exemplo, no caso de um vírus como HPV em uma amostra de célula humana, guanidina ou um agente funcionalmente equivalente pode ser usado para lisar as células. Um exemplo de método com base em guanidina para lise de célula e extração de DNA é o método de Nelson e Krawetz (Anal. Biochem. 207(1):97-201, 1992). Soluções de lise com base em guanidina são também comercialmente disponíveis de fornecedores como Qiagen, por exemplo, QIAamp, PAXgene, e outros. No entanto, os métodos de lise podem mudar dependendo da natureza da amostra e analito. Por exemplo, para a detecção de um analito em uma amostra ambiental como amostra de solo ou sedimento, um sistema de libe baseado em esfera de vidro pode ser mais adequado, como o método de Kuske e cols., (Appl. Environ. Microbiol. 64(7):2463-2472, 1998). Em qualquer evento, o protocolo de lise adequados para um dado analito e amostra deve ser facilmente determinado por pessoa de habilidade comum na técnica sem experimentação indevida.
Depois da lise das células, o DNA pode ser purificado por qualquer meio conveniente que pode ser facilmente evidente para pessoa habilitada na técnica (por exemplo, veja kits comercialmente disponíveis acima). Em certas modalidade preferidas da invenção, o DNA é purificado com o uso de uma quantidade limitante de um agente de ligação de DNA como, sem limitação, sílica. Pelo uso de uma quantidade limitante do agente de ligação de DNA, uma quantidade uniforme de DNA pode ser isolada de diferentes amostras uma vez que a quantidade de DNA recuperada em cada caso é igual à quantidade de DNA Máxima que pode ser ligada pela quantidade limitante de agente de ligação de DNA. O DNA ligado ao agente de ligação de DNA pode ser então recuperado ou eluído do agente de ligação de DNA com o uso de qualquer meio conveniente.
Embora o DNA seja um ácido preferido, RNA também pode ser isolado da amostra com o uso de qualquer protocolo padrão de isolação de RNA. A isolação de RNA envolve tipicamente uma etapa de rompimento da célula e uma etapa de isolação de RNA. Exemplos de técnicas de rompimento de célula que são adequadas para a isolação de RNA incluem aquelas apresentadas em “Ambion Technical Bulletin #183” (www.ambion.com/techlib/tb/tb_183.html). Além disso, uma faixa de exemplos de kits de isolação de RNA que são adequados para uma escala de tipos de amostra são apresentados em www.ambion.com/techlib/basics/produtos/maisol_ compchart.html. Entretanto, deve ser compreendido que a presente invenção não é em qualquer sentido limitada por esses métodos e kits específicos para isolação e purificação de RNA e a presente invenção é compatível com quaisquer métodos de isolação de RNA que são evidentes para pessoa habilitada na técnica.
Os conjuntos de esferas podem compreender, em relação à detecção de HPV tantos subconjuntos de esferas quanto cepas de HPV. Portanto, o ensaio pode empregar 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 ou 16 subconjuntos de esferas cada um para as cepas de HPV 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 e 68. Esferas adicionais também podem ser usadas para controles. Marcadores de captura adequados são revelados na Tabela 2.
Portanto, outros aspectos da presente invenção são direcionados a conjuntos de esferas para a detecção de uma ou mais cepas de HPV e/ou para diferenciação entre duas ou mais cepas de HPV, em que os conjuntos de esferas compreendem várias famílias ou subconjuntos de esferas em que: (a) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (b) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico selecionado da lista na Tabela 2 que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (c) o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas tendo uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (d) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de seqüência.
Ainda outro aspecto da presente invenção contempla métodos para a detecção e/ou diferenciação entre duas ou mais cepas de HPV em uma amostra, que compreende as etapas de: (a) contato da amostra com um conjunto de esferas que compreende várias famílias ou subconjuntos de esferas em que: (i) as esferas de cada subconjunto são homogêneas com relação ao tamanho; (ii) as esferas em cada subconjunto são ligadas a um marcador de captura de ácido nucleico selecionado da lista na Tabela 2 que é capaz de se ligar a uma região específica de cepa de HPV de um genoma de HPV ou, opcionalmente, uma seqüência de ácidos nucleicos de controle; (iii) o marcador de captura em cada esfera é rotulado com o mesmo rótulo com cada subconjunto de esferas que tem uma diferente intensidade fluorescente para criar uma mistura heterogênea de esferas com base na intensidade fluorescente; e (iv) pelo menos dois subconjuntos de esferas são misturados para produzir um conjunto de esferas, em que a identidade do subconjunto e portanto a cepa de HPV é identificável por citometria de fluxo com base no tamanho, intensidade fluorescente e discriminação de seqüência; (b) incubação do referido conjunto de esferas com a referida amostra por um tempo e sob condições suficientes para permitir que os referidos marcadores se liguem ao genoma de HPV amplificado para gerar um réplicon que compreende uma região específica para cepa; e (c) detecção e/ou diferenciação dos amplicons gerados na amostra que são ligados às referidas esferas para assim identificar ou distinguir entre as duas ou mais cepas de HPV.
Portanto, os conjuntos de esferas podem compreender 2, 3, 4, 5, 6, 7, 8, 10, 11, 12, 13, 14, 15, 16 subconjuntos de esferas cada um dom uma molécula de ácido nucleico selecionada da listagem na Tabela 2. Referência a essas seqüências específicas para cepa de HPV na Tabela 2 incluem moléculas de ácido nucleico que têm pelo menos 90% de identidade a essas seqüências ou são capazes de hibridizar a elas ou suas formas complementares sob condições de baixo rigor. Referência a pelo menos 90% inclui 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 e100%.
Os métodos da presente invenção se baseiam, em parte, na amplificação de um ácido nucleico a partir de uma amostra que usa iniciadores que se ligam a seqüências conservadas entre diferentes cepas do analito em questão, mas que geram um amplicon que compreende uma seqüência de nucleotídeos distinta para cada cepa do analito. De fato, os iniciadores usados na presente invenção se ligam às seqüências que são conservadas entre as cepas do analito em questão que flanqueiam regiões que são pelo menos parcialmente não conservadas ou polimórficas entre cepas. Esquematicamente, a região amplificada no analito tem a estrutura geral de: C-X-C' em que: C é uma seqüência de nucleotídeos que é conservada entre duas ou mais cepas do analito e é o sítio de ligação do iniciador “adiante”; X é uma seqüência de nucleotídeos, parte ou toda dela compreende variação entre diferentes cepas do analito; C'é uma seqüência de nucleotídeos que é conservada entre duas ou mais cepas do analito e é o sítio de ligação do iniciador “reverso”.
Em certas modalidades é desejável incorporar pontas em um ou mais dos iniciadores para modificar o processo de amplificação de ácido nucleico. Preferivelmente, essas pontas são conjugadas ao terminal 5' do iniciador. Mais preferivelmente, um ou mais pontas são opcionalmente também conjugadas a uma porção 5 Phos ou 5AmMC6 no terminal 5’ da ponta. Em certas modalidades preferidas, as pontas conjugadas a iniciadores adiante são selecionadas de: caatcagc, acaat, ggaac, cagctt, attacc e ctgtt, mais preferivelmente acaat e ctgtt. Em outra modalidade preferida, as pontas conjugadas a iniciadores reversos são selecionadas de: actcactatagg, aatacgactcactatagg, tctaatacgactcactatagg, e aattctaatacgactcactatagg mais preferivelmente actcactatagg e tctaatacgactcactatagg.
Em certas modalidades relacionadas a pares de iniciadores de amplificação de oligonucleotídeos para direcionamento de HPV oncogênico, o iniciador direto do par de iniciadores é selecionado do grupo que consiste em: /5Phos/caatcagc TR TTT GTT ACT GTK GTD GAT ACY A; /5Phos/acaat CAR YTR TTT GTT ACT GTK GTD GAT A; /5Phos/acaat CAR YTR TTT OTT ACT GTK GTD GA; /5Phos/ggaac AAY CAR YTR TIT GTT ACT GTK GT; /5Phos/cagctt TTT GTT ACT GTK GTD GAT ACY AC HCG; /5Phos/cagctt TTT GTT ACT GTK GTD GAT ACY AC HCG YAG; /5Phos/attacc GTK GTD GAT ACY AC HCG YAG TAC; e /5Phos/ctgtt GTD GAT ACY AC HCG YAG TAC HAA; e o iniciador reverso de um par de iniciadores é selecionado do grupo que consiste em: /5AmMC6/actcactatagg TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG; /5AmMC6/aatacgactcactataggCAY ARY TGA AAA ATA AAY TGY AAA TC; /5AmMC6/tctaatacgactcactatagg TR CAY ARY TGA AAA ATA AAY TG; e /5AmMC6/aattctaatacgactcactatagg TR CAY ARY TGA AAA ATA AA.
Como mostrado, um iniciador é indicado em letras maiúsculas e uma ponta opcional em cada caso é mostrada em letras minúsculas sublinhadas. Preferivelmente, o iniciador direto de um par de iniciadores é selecionado de: /5Phos/acaatCAR YTR TTT GTT ACT GTK GTD GA e /5Phos/ctgtt GTD GAT ACY AC HCG YAG TAC HAA. Em outra modalidade preferível, o iniciador reverso de um par de iniciadores é selecionado de /5AmMC6/actcactatagg TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG e /5AmMC6/tctaatacgactcactatagg TR CAY ARY TGA AAA ATA AAY TG.
Em certos aspectos da invenção, os iniciadores incorporam uma seqüência de nucleotídeos extrínseca 5' de região de ligação de não iniciador conjugada à extremidade 5' de uma região de iniciador de ligação de modelo 3'. A seqüência de nucleotídeos extrínseca 5' é convenientemente referida aqui como “ponta”, “gancho de ponta”, “seqüência de ponta” ou “seqüência de ponta extrínseca” mas isso não pretende limitar de qualquer modo a invenção.
Em certas modalidade preferidas, pelo menos um dos iniciadores adiante e reverso é conjugado a uma pontaa no terminal 5’ do iniciador. Preferivelmente, quando o iniciador direto é conjugados a uma ponta no terminal 5' do iniciador direto, a ponta do iniciador direto é selecionada do grupo que consiste em: CAATCAGC, ACAAT, GGAACAAT, GGAAC, CAGCTT, ATTACC, CTGTT, /5Phos/CAATCAGC, /5Phos/ACAAT, /5Phos/GGAACAAT, /5Phos/GGAAC, /5Phos/CAGCTT, 5Phos/ATTACC, e/5Phos/CTGTT. Preferivelmente quando iniciador reverso é conjugados a uma ponta no terminal 5’ do iniciador reverso, a ponta do iniciador reverso é selecionada do grupo que consiste em: ACTCACTATAGG, AATACGACTCACTATAGG, TCTAATACGACTCACTATAGG, AATTCTAATACGACTCACTATAGG, /5AmMC6/ACTCACTATAGG, /5AmMC6/AATACGACTCACTATAGG, /5AmMC6/TCTAATACGACTCACTATAGG, e /5AmMC6/AATTCTAATACGACTCACTATAGG. Em algumas modalidades mais preferidas de pares de iniciadores de amplificação de oligonucleotídeo que contêm uma seqüência de ácido nucleico de ponta opcional, o iniciador direto do par de iniciadores é selecionado do grupo que consiste em: CAR YTR TTT GTT ACT GTK GTD GA, opcionalmente tendo um ACAAT, /5Phos/ACAAT, GGAACAAT, ou um /5Phos/GGAACAAT conjugado ao terminal 5’ do iniciador; e GTD GAT ACY AC HCG YAG TAC HAA, opcionalmente tendo um CTGTT ou /5Phos/CTGTT conjugado ao terminal 5’ do iniciador. Em algumas modalidades mais preferidas de pares de iniciadores de amplificação de oligonucleotídeo que contêm uma seqüência de ácido nucleico de ponta opcional, o iniciador reverso do par de iniciadores é selecionado do grupo que consiste em: TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG, opcionalmente tendo um ACTCACTATAGG ou /5AmMC6/ACTCACTATAGG conjugado ao terminal 5’ do iniciador, TR CAY ARY TGA AAA ATA AAY TG, opcionalmente tendo um TCTAATACGACTCACTATAGG ou /5AmMC6/TCTAATACGACTCACTATAGG conjugado ao terminal 5’ do iniciador; e TR CAY ARY TGA AAA ATA AAY TG, opcionalmente tendo um TCTAATACGACTCACTATAGG ou /5AmMC6/TCTAATACGACTCACTATAGG conjugado ao terminal 5’ do iniciador.
A região de iniciador de ligação de modelo 3’ refere- se a um iniciador cuja porção 3' se liga a um modelo (por exemplo, durante a primeira etapa de anelamento para iniciar a polimerização). O desenho do iniciador acima mencionado resulta na incorporação da seqüência de ponta em produtos de amplificação depois do evento inicial de iniciação. Subsequentemente, a seqüência de ponta 5' age como uma garra para uniformizar a eficiência da amplificação por todos os homólogos do amplicon.
A seqüência de ponta extrínseca pode estar no iniciador direto ou no iniciador reverso ou ambos.
Portanto, certos aspectos da presente invenção contemplam métodos para amplificação de uma molécula alvo de ácido nucleico os referidos métodos compreendendo submissão de um modelo de ácido nucleico do referido alvo de ácido nucleico à amplificação com o uso de um iniciador direto e reverso em que pelo menos um iniciador contém uma seqüência de nucleotídeos extrínseca de região de ligação de não iniciador 5' conjugada a uma região de iniciador de ligação de modelo 3’ em que a referida seqüência de nucleotídeos extrínseca é incorporada em um produto de amplificação depois da iniciação.
Como acima indicado o iniciador direto ou reverso pode compreende a seqüência extrínseca ou ambos podem carregar a seqüência. Quando ambos carregam a seqüência extrínseca, a ponta pode ser a mesma ou diferente.
A presente invenção é particularmente aplicável a iniciadores que são potencialmente capazes de iniciar um conjunto de homólogos de ácido nucleico alvo.
A presente invenção também contempla melhores métodos de amplificação de uma molécula de ácido nucleico incluída em uma população de moléculas de ácido nucleico relacionadas por amplificação com um iniciador direto e reverso, que compreende: a seleção de um ou ambos dos iniciadores adiante ou reverso de modo que um ou ambos contenham uma seqüência extrínseca de nucleotídeos 5’ de região de ligação não iniciadora conjugada a uma região de iniciador de ligação de modelo 3’ em que a referida seqüência extrínseca de nucleotídeos é incorporada na produção de amplificação após a iniciação.
Portanto, referência a uma “molécula de ácido nucleico” inclui a família de moléculas de ácido nucleico relacionadas como um grupo de moléculas de ácido nucleico homólogas.
Kits para reduzir a amplificação também formam parte da presente invenção.
Todas as citações científicas, patentes, pedidos de patente e especificações técnicas do produtor citadas ou descritas nesse documento são aqui incorporadas em sua totalidade por referência.
Entende-se que a menos que indicado de outro modo, a atual invenção não é limitada a reagentes, etapas de processo, e aplicações específicos ou outros, uma vez que eles podem variar. Deve ser também entendido que a terminologia aqui usada é para o objetivo de descrição de modalidade particulares apenas e não pretende ser limitante.
Termos e símbolos de química de ácido nucleico, bioquímica, genética, e biologia molecular aqui usados seguem aqueles de pesquisa e textos padrão no campo, por exemplo, Kornberg and Baker, DNA Replication, Segunda edição (W.H. Freeman, New York, 1992); Lehninger, Biochemistry, Segunda edição (Worth Publishers, New York, 1975); Strachan and Read, Human Molecular Genetics, Segunda edição (Wiley-Liss, New York, 1999); Eckstein Ed, Oligonucleotídeos and Analogs: A Practical Approach (Oxford University Press, New York, 1991); Gait Ed, Oligonucleotídeo Synthesis: A Practical Approach (IRL Press, Oxford, 1984); e outros. “Amplicon” significa o produto de uma reação de amplificação de polinucleotídeo. Ou sejas, ele é uma população de polinucleotídeos, comumente mas não necessariamente de duplo filamento, que são replicados a partir de uma ou mais seqüências de iniciação. Uma ou mais seqüências de iniciação podem ser uma ou mais cópias das mesma seqüência, ou elas podem ser uma mistura de diferentes seqüências. Os amplicons pdoem ser produzidos por várias reações de amplificação cujos produtos são replicados múltiplos de um ou mais ácidos nucleicos alvo.
Geralmente, as reações de amplificação que produzem amplicons são “dirigidas por modelo” uma vez que o pareamento de base de reagentes, nucleotídeos ou oligonucleotídeos, tem complementos em um polinucleotídeo modelo que são necessários para a criação de produtos da reação. Em um aspecto, as reações dirigidas por modelo são extensões de iniciador com uma polimerase de ácido nucleico ou ligações de oligonucleotídeo com uma ligase de ácido nucleico. Tais reações incluem, sem limitação, reações de polimerase linear de PCR, NASBAs, amplificações “rolling circle”, e outras, reveladas nas seguintes referências que são aqui incorporadas por referência: Mullis e cols., Patente U.S. Nos. 4.683.195; 4.965.188; 4.683.202; 4.800.159 (PCR); Gelfand e cols., Patente U.S. No. 5.210.015 (PCR em tempo real com marcadores “Taqman” ou “Taq” [marcas comerciais registradas]); Wittwer e cols., Patente U.S. No. 6.174.670; Kacian e cols., Patente U.S. No. 5.399.491 (“NASBA”); Lizardi, Patente U.S. 5.854.033; Aono e cols., Publ. de Patente Japonesa No. JP 4262799 (amplificação “rolling circle”); e outros.
Uma reação de amplificação pode ser uma amplificação “em tempo real” em que a química de detecção permite que o produto da reação seja medido à medida que a reação de amplificação progride.
A presente invenção é particularmente relacionada com a redução da tendência da amplificação por uma faixa de moléculas de ácido nucleico relacionadas ou homólogas. Exemplos de moléculas de ácido nucleico homólogas incluem homólogos virais, polimorfismos, células relacionadas ao câncer, homólogos bacterianos, homólogos de célula tronco entre vários outros. Um aspecto da presente invenção é a seleção de iniciadores em pontos potenciais de diferença entre os homólogos. Os iniciadores carregam uma seqüência extrínseca de nucleotídeos 5’ de região de ligação não iniciadora conjugada a uma região de iniciador de ligação de modelo 3’ que é incorporada em um produto de amplificação depois da iniciação.
A ponta ou seqüência extrínseca 5' pode ser de cerca de 1 a cerca de 400 bases de comprimento e todas as combinações e subcombinações desses. Preferivelmente a ponta é de cerca de 3 a cerca de 100, mais preferivelmente de cerca de 4 a cerca de 80 bases de comprimento, ainda mais preferivelmente de cerca de 5 a cerca de 40, e ainda mais preferivelmente cerca de 5 a cerca de 25, com cerca de 10 a cerca de 20 sendo mais preferido.
De fato, a seqüência extrínseca 5’ tem opcionalmente um nível de complementaridade à seqüência alvo, e ela não contribui substancialmente para as etapas de ligação iniciais do iniciador. É desejável que a ponta tenha menos que 95% de complementaridade ao iniciador de núcleo. Exemplos adicionais dos níveis de complementaridade podem incluir menos que 90%, 85%, 80%, 75%, 70%, 65%, e 60%. A complementaridade é determinada com o uso de algoritmos padrão.
Como aqui usado, o termo “amplificação” significa realizar uma reação de amplificação. Uma “mistura de reação” ou “frasco de reação” significa uma solução ou compartimento que contém todos os reagentes necessários para realizar a reação, que pode incluir, sem limitação, agentes de tamponamento para manter o pH em um nível selecionado durante a reação, sais, co-fatores, scavengers, e outros.
“Complementar ou substancialmente complementar” refere-se à hibridização ou pareamento de base ou à formação de um duplex entre nucleotídeos ou ácidos nucleicos, como, por exemplo, entre os dois filamentos de uma molécula de dsDNA ou entre um iniciador de oligonucleotídeo e um sítio de ligação de iniciador em um ácido nucleico de filamento único. Os nucleotídeos complementares são, geralmente, A e T (ou A e U), ou C e G. Duas moléculas de RNA ou DNA de filamento únicos são ditas como sendo substancialmente complementares quando os nucleotídeos de um filamento, otimamente alinhados e comparados e com inserções ou deleções de nucleotídeo adequadas, forma par com pelo menos cerca de 80% dos nucleotídeos do outro filamento, comumente pelo menos cerca de 90% a 95%, e mais preferivelmente de cerca de 98 a 100%. Alternativamente, existe complementaridade substancial quando, por exemplo, um filamento de DNA hibridiza sob condições seletivas de hibridização a seu complemento. Tipicamente, a hibridização seletiva ocorre quando existe pelo menos cerca de 65% de complementaridade em uma extensão de pelo menos 14 a 25 nucleotídeos, preferivelmente pelo menos cerca de 75%, mais preferivelmente pelo menos cerca de 90% de complementaridade. Veja, Kanehisa Nucleic Acids Res. 12:203, 1984, aqui incorporado em sua totalidade por referência.
“Duplex” significa que pelo menos dois oligonucleotídeos e/ou polinucleotídeos que são totalmente ou parcialmente complementares sofrem pareamento de base tipo Watson-Crick entre todos ou a maioria de seus nucleotídeos de modo que um complexo estável é formado. Os termos “anelamento” e “hibridização” são usados de modo intercambiável para significar a formação de um duplex estável. “Perfeitamente combinado” em referência a um duplex significa que os filamento do poli- ou oligonucleotídeo que compõem o duplex formam uma estrutura de filamento duplo um com o outro de modo que todo e qualquer nucleotídeo em cada filamento sofre pareamento de base de Watson-Crick com um nucleotídeo no outro filamento.
“Lócus genético” ou “lócus” em referência a um genoma ou polinucleotídeo alvo, significa uma subregião contígua ou segmento do genoma ou polinucleotídeo alvo. Como aqui usado, lócus genético, ou lócus, pode referir-se à posição de um gene ou porção de um gene em um genoma, ou ele pode referir-se a qualquer porção contígua da seqüência genômica esteja ou não em, ou associada a, um gene. Preferivelmente, um lócus genético refere-se a qualquer porção da seqüência genômica de algumas dezenas de nucleotídeos, por exemplo, 10-30, ou 10-100, de comprimento, a algumas centenas de nucleotídeos, por exemplo, 100-1000 ou 100-500 de comprimento, a alguns milhares de nucleotídeo de comprimento, por exemplo, 1.000-10.000 ou 1.000-3.000 de comprimento. Em alguns contextos, os lócus genéticos podem referir-se à localização de um nucleotídeo em um genoma.
“Kit” refere-se a qualquer sistema de liberação para a liberação de materiais ou reagentes para realizar um método da atual invenção. No contexto de ensaios de reação, tais sistemas de liberação incluem sistemas que permitam a estocagem, transporte, ou liberação de reagentes de reação (por exemplo, marcadores, enzimas etc., nos recipientes adequados) e/ou materiais de suporte (por exemplo, tampões, instruções escritas para a realização do ensaio etc.) de uma localização para outra. Por exemplo, os kits incluem uma ou mais embalagens (por exemplo, caixas) que contêm os reagentes de reação relevantes e/ou materiais de suporte. Tal conteúdo pode ser liberado ao receptor junto ou separadamente. Por exemplo, um primeiro recipiente pode conter uma enzima para uso em um ensaio, enquanto um segundo recipiente contém marcadores. Os kits tambem podem conter compartimentos adaptados para conter os reagentes. Em um exemplo, um compartimento compreende uma matriz sólida que tem oligonucleotídeos ou iniciadores ou polinucleotídeos imobilizados nela que participam na reação de amplificação. Um exemplo de uma matriz sólida é um microarranjo. Umkit, portanto, pode ser parte de um sistema de amplificação geral que tem um componente de reagente, um componente de ácido nucleico, um componente de hardware e um componente instrucional.
“Microarranjo” refere-se a um suporte de fase sólida que tem uma superfície plana, que carrega um arranjo de ácidos nucleicos, cada membro do arranjo compreende cópias idênticas de um oligonucleotídeo ou polinucleotídeo imobilizado a uma região ou sítio espacialmente definido, que não sobrepõe com aqueles de outros membros do arranjo; ou seja, as regiões ou sítios são espacialmente distintos. Sítios de hibridização espacialmente definido podem ser adicionalmente “acessíveis” porque a localização e a identidade de seu oligonucleotídeo imobilizado são conhecidos ou predeterminados, por exemplo, antes do uso. Tipicamente, os oligonucleotídeos ou polinucleotídeos são de filamento único e são covalentemente anexados ao suporte de fase sólida, comumente por uma extremidade 5' ou uma extremidade 3'. A densidade de regiões de não sobreposição que contêm ácidos nucleicos em um microarranjo é tipicamente maior que 100 por cm2, e mais preferivelmente, maior que 1.000 por cm2. a tecnologia de microarranjo é revelada nas seguintes referências que são incorporadas em sua totalidade por referência: Schena, Ed, Microarrays: A Practical Approach (IRL Press, Oxford, 2000); Southern, Current Opin. Chem. Biol., 2:404-410, 1998.
Um “microarranjo aleatório” refere-se a um microarranjo cujas regiões espacialmente distintas de oligonucleotídeos ou polinucleotídeos não são espacialmente direcionadas. Ou seja, a identidade dos oligonucleotídeos ou polinucleotídeos anexados não é discernível, pelo menos inicialmente, de sua localização. Em um aspecto, microarranjos aleatórios são arranjos planos de microesferas em que cada microesfera tem anexado um tipo único de complemento de rótulo de hibridização, como a partir de um conjunto de hibridização minimamente cruzado dos oligonucleotídeos. Do mesmo modo, depois da formação, microesferas, ou oligonucleotídeos desses, em um arranjo aleatório podem ser identificados em uma variedade de formas, incluindo por rótulos óticos, por exemplo, proporções de corante fluorescente ou quantum dots, formato, análise de seqüência ou outros.
“Nucleosídeo” como aqui usado inclui os nucleosídeos naturais, que incluem formas 2'-desoxi e T-hidroxil, por exemplo, como descrito em Kornberg e Baker, DNA Replication,2aEd. (Freeman, San Francisco, 1992).
“Reação em cadeia de polimerase”, ou “PCR”, significa uma reação para a amplificação in vitro de seqüências de DNA específicas pela extensão simultânea de iniciador de filamentos complementares de DNA. Em outras palavras, a PCR é uma reação para a produção de múltiplas cópias ou replicas de um ácido nucleico-alvo flanqueado por sítios de ligação de iniciador, esta reação compreendendo uma ou mais repetições das seguintes etapas: (i) desnaturação do ácido nucleico-alvo, (ii) anelamento de iniciadores aos sítios de ligação de iniciador, e (iii) extensão dos iniciadores por uma ácido nucleico polimerase na presença de trifosfatos do nucleosídeo. Normalmente, a reação é ciclada por meio de temperaturas diferentes otimizadas para cada etapa em um instrumento de ciclagem térmico. Temperaturas, durações particulares em cada etapa, e taxas de alteração entre etapas, dependem de muitos fatores bem conhecidos por aqueles habilitados na técnica, por exemplo, exemplificados pelas referências: McPherson e cols., (Eds), “PCR: A Practical Approach” e “PCR2: A Practical Approach” (IRL Press, Oxford, 1991 e 1995, respectivamente). Por exemplo, em uma PCR convencional com o uso de Taq DNA polimerase, um ácido nucleico-alvo de filamento duplo pode ser desnaturado em uma temperatura >90°C, iniciadores anelados em uma temperatura na faixa de 35-90°C. O termo “PCR” engloba formas derivadas da reação, incluindo, sem limitação, RT- PCR, PCR em tempo real, PCR abrigada, PCR quantitativa, PCR multiplexada, PCR de fase sólida aprimorada, e semelhantes. Para mais detalhes de PCR de fase sólida aprimorada, veja, por exemplo, Park, e cols., Analytical Biochemistry, 375 (2008), pp. 391-393, cuja totalidade é aqui incorporada por referência em sua totalidade. O uso de PCR de fase sólida aprimorada é preferido em certas modalidades da presente invenção para a geração e/ou amplificação de moléculas de ácido nucleico relacionadas, por exemplo, às cepas de HPV. Ainda mais preferido é o uso de um ou mais pares de iniciadores diretos/reversos aqui observados em amplificação por PCR de fase sólida aprimorada de moléculas de ácido nucleico relacionadas às cepas de HPV.
Com o uso do formato de ESP-PCR, fosfatos 5-primesão opcionais, já que amplicon de filamento simples não é necessário como um produto de PCR. Os grupos funcionais amina 5-primetambém são opcionais nesse formato, e podem ser usados como um meio preferido de rotulagem com um fluoróforo para a geração de sinal. No entanto, também são empregados muitos meios alternativos de geração de sinal nos quais não há necessidade de qualquer grupo funcional ou de um grupo funcional alternativo. Por exemplo, iniciadores de PCR podem ser não rotulados com flúor, e “oligonucleotídeos sinalizadores” separados, que são conjugados a um sinal, podem ser empregados. Em outro exemplo, com o uso do formato de ESP-PCR, todos os iniciadores de PCR “aquosos” podem ser usados sem grupos funcionais e o sinal poderia alternativamente ser introduzido por meio da incorporação de análogo de nucleotídeo rotulado. Em outra modalidade, com o uso do formato de ESP-PCR, todos os iniciadores de PCR “aquosos” podem ser usados sem grupos funcionais, e o sinal poderia ser introduzido por meio de um iniciador de suporte sólido rotulado de tal forma que o sinal aumente no contexto do produto de filamento duplo.
Meios alternativos para a geração de amplicon de filamento simples incluem a conversão de DNA de filamento duplo em DNA de filamento simples por separação dos filamentos ou por remoção de um filamento do duplex. Os filamentos do duplex podem ser separados por meios térmicos ou químicos de ruptura das ligações interfilamentos. A remoção de um filamento permite a recuperação do filamento desejado e a eliminação de seu complemento, por exemplo, Nikiforov e cols. (Patente U.S. N° 5.518.900), que descrevem a modificação de um entre dois iniciadores usados para amplificação por incorporação de derivados de fosforotioato nucleotídeo na extremidade 5' do iniciador modificado, tornando-o resistente à digestão por exonuclease. Após amplificação de seqüências-alvo usando a reação em cadeia de polimerase (PCR), o dsDNA é submetido à digestão por exonuclease. O filamento não protegido é preferencialmente digerido por uma exonuclease 5' a 3', deixando um produto de filamento simples que consistem no outro filamento. Estratégias similares utilizaram iniciadores ramificados resistentes à exonuclease (Shchepinov e cols., Nuc. Acids. Res. 25: 4.447-4.454 1997) ou preferência de substrato que abriga 5' fosfato de exonuclease Lambda (Higuchi e cols., Nucl. Acids Res. 25: 5.685, 1989).
A PCR assimétrica (Gyllensten e Erlich, Proc. Natl. Acad. Sci. USA 85: 7.652-7.656 1998; Patente U.S. N° 5.066.584) gera ssDNA durante ciclagem térmica pelo emprego de uma concentração desequilibrada de par de iniciadores, de tal forma que um iniciador esteja em uma concentração limitante. Isso favorece o produto de ssDNA iniciado pelo iniciador em excesso.
A PCR assimétrica por iniciador competidor (Gillespie, 1997; Pedido de Patente U.S. N° 08/628.417) emprega a adição separada de um iniciador competidor após a ciclagem térmica da PCR e antes da ciclagem térmica adicional para gerar ssDNA. Kaltenboeck e cols., Biotechniques 12: 164171, 1992, descrevem um método de produção de ssDNA realizando-se, inicialmente, uma PCR para gerar dsDNA, seguida por uma reação separada que usa o produto da primeira PCR como modelo para uma segunda amplificação linear que emprega um iniciador. Veja também a Patente U.S. 6.887.664 para exemplos de PCR assíncrona.
Os volumes de reação variam de poucas centenas de nanolitros, por exemplo, 200 nL, até poucas centenas de μL, por exemplo, 200 μL. “PCR por transcrição reversa”, ou “RT- PCR”, significa uma PCR que é precedida por uma reação de transcrição reversa que converte um RNA-alvo em um DNA de filamento simples complementar, que é então amplificado, por exemplo, Tecott e cols., Patente U.S. N° 5.168.038, cuja patente é aqui incorporada por referência em sua totalidade. “PCR em tempo real” significa uma PCR para a qual uma quantidade de produto de reação, ou seja, amplicon, é monitorada à medida que a reação evolui. Há muitas formas de PCR em tempo real que diferem principalmente nas químicas de detecção usadas para o monitoramento do produto de reação, por exemplo, Gelfand e cols., Patente U.S. N° 5.210.015 (“taqman”); Wittwer e cols., Patentes U.S. Nos6.174.670 e 6.569.627 (corantes intercalados); Tyagi e cols., Patente U.S. N° 5.925.517 (marcadores moleculares); cujas patentes são aqui incorporadas por referência em sua totalidade. As químicas de detecção para PCR em tempo real são revisadas em Mackay e cols., Nucleic Acid Research, 30: 1.292-1.305, 2002, que também é aqui incorporado por referência em sua totalidade. “PCR abrigada” significa uma PCR em dois estágios em que o amplicon de uma primeira PCR se torna a amostra para uma segunda PCR que usa um novo conjunto de iniciadores, pelo menos um dos quais se liga em uma localização interior do primeiro amplicon.
É proposto que os eventos de iniciação iniciais sejam feitos com iniciadores diretos e reversos, em que um ou ambos carregam uma seqüência de nucleotídeos extrínseca 5’ de região de ligação não iniciadora conjugada uma região do iniciador de ligação de modelo 3’, em que a seqüência de nucleotídeos extrínseca é incorporada em um produto de amplificação após iniciação inicial.
O uso de seqüência de ponta 5’ da região de ligação não iniciadora conjugada a uma região iniciadora de ligação de modelo 3’ como o design do iniciador resulta na incorporação da seqüência de ponta em produtos de amplificação após o evento de ligação inicial do iniciador. Subseqüentemente, a seqüência de ponta 5' atua como um grampo para igualar a eficiência de amplificação através de homólogos. Dessa forma, a tendência da amplificação é restrita aos eventos de ligação iniciais do iniciador. O “gancho de ponta” pode ser colocado nos iniciadores diretos e reversos ou em um deles, dependendo da necessidade. Há uma grande liberdade de design em relação a qual seqüência da seqüência do “gancho de ponta” será a mais adequada àquela aplicação em particular. A seqüência iniciadora da ligação do modelo 3' poderia assumir a forma de seqüência degenerada, seqüência de consenso ou um híbrido de seqüências de consenso e degeneradas. Um pool de seqüências de interesse com combinação exata também poderia ser empregado. Em todos esses casos, o princípio do “gancho de ponta” 5' pode ser empregado.
“Polinucleotídeo” e “oligonucleotídeo” são usados de forma intercambiável, e cada um significa um polímero linear de monômeros de nucleotídeos. Monômeros que constituem polinucleotídeos e oligonucleotídeos são capazes de se ligar especificamente a um polinucleotídeo natural por meio de um padrão regular de interações monômero-a- monômero como, por exemplo, o tipo Watson-Crick de pareamento de bases, empilhamento de bases, os tipos Hoogsteen ou Hoogsteen reverso de pareamento de bases, ou semelhantes.
Sempre que um polinucleotídeo ou oligonucleotídeo for representado por uma seqüência de letras (maiúsculas ou minúsculas), por exemplo, “ATGCCTG”, será subentendido que os nucleotídeos estão na ordem 5'^ 3' da esquerda para a direita e que “A” representa desoxiadenosina, “C” representa desoxicitidina, “G” representa desoxiguanosina, e “T” representa timidina, “I” representa desoxiinosina, “U” representa uridina, a menos que indicado de forma diferente ou que fique óbvio pelo contexto.
“Iniciador” significa um oligonucleotídeo, natural ou sintético, que é capaz, mediante a formação de um duplex com um modelo de polinucleotídeo, de atuar como um ponto de iniciação da síntese de ácido nucleico e de ser estendido da sua extremidade 3' juntamente com o modelo, de forma que seja formado um duplex.
A extensão de um iniciador é normalmente realizada com uma ácido nucleico polimerase, por exemplo, uma DNA ou RNA polimerase. A seqüência de nucleotídeos adicionada no processo de extensão é determinada pela seqüência do polinucleotídeo de modelo. Normalmente, os iniciadores são estendidos por uma DNA polimerase. Iniciadores normalmente possuem um comprimento na faixa de 14 a 40 nucleotídeos, ou na faixa de 18 a 36 nucleotídeos. Iniciadores são empregados em diversas reações de amplificação de ácidos nucleicos, por exemplo, reações de amplificação lineares que usam um único iniciador, ou PCRs, que empregam dois ou mais iniciadores. Diretrizes para a seleção dos comprimentos e seqüências de iniciadores para aplicações específicas são bem conhecidas por aqueles habilitados na técnica, como evidenciado pelas seguintes referências que são incorporadas por referência em sua totalidade: Dieffenbach (Ed), “PCR Primer: A Laboratory Manual”, 2a Edição (Cold Spring Harbor Press, New York, 2003).
“Amostra” significa uma quantidade de material de uma fonte biológica, ambiental, médica ou de pacientes na qual se busca a detecção ou medida de ácidos nucleicos-alvo. Por um lado essa definição visa incluir um espécime ou cultura (por exemplo, culturas microbiológicas). Por outro lado, visa incluir amostras tanto biológicas quanto ambientais. Uma amostra pode incluir um espécime de origem sintética. As amostras biológicas podem ser de animais, incluindo humanas, líquidas, sólidas (por exemplo, fezes) ou tecido, bem como alimentos e produtos alimentícios líquidos e sólidos e ingredientes como, por exemplo, laticínios, vegetais, carne e subprodutos da carne, e dejetos. Amostras biológicas podem incluir materiais retirados de um paciente, incluindo, sem limitação, culturas, sangue, saliva, líquido cefalorraquidiano, líquido pleural, leite, linfa, escarro, sêmen, aspirados por agulha, e semelhantes. As amostras biológicas podem ser obtidas de todas as várias famílias de animais domésticos, bem como animais selvagens, incluindo, sem limitação, animais como ungulados, ursos, peixes, roedores etc. Amostras ambientais incluem material ambiental como, por exemplo, matéria de superfície, solo, água e amostras industriais, bem como amostras obtidas de instrumentos, aparelhos, equipamentos, utensílios, itens descartáveis e não descartáveis para o processamento de alimentos e laticínios. Esses exemplos não devem ser considerados como limitantes dos tipos de amostra aplicáveis à presente invenção.
Dessa forma, alguns aspectos da presente invenção fornecem métodos para a amplificação de uma molécula de ácido nucleico-alvo, que compreende: a submissão de um modelo de filamento simples do referido ácido nucleico-alvo à amplificação com o uso de iniciadores diretos e reversos, em que pelo menos um iniciador contém uma seqüência de nucleotídeos extrínseca 5’ da região de ligação não iniciadora conjugada a uma região iniciadora de ligação de modelo 3’, em que a referida seqüência de nucleotídeos extrínseca é incorporada em um produto de amplificação após iniciação inicial.
Outros aspectos da presente invenção contemplados aprimoram métodos de amplificação de uma molécula de ácido nucleico dentro de uma população de moléculas de ácido nucleico relacionadas por amplificação com um iniciador direto e reverso, que compreende: a seleção de um ou ambos os iniciadores, diretos ou reversos, de tal forma que um ou ambos contenham uma seqüência de nucleotídeos extrínseca 5’ da região de ligação não iniciadora conjugada a uma região iniciadora de ligação de modelo 3’, em que a referida seqüência de nucleotídeos extrínseca é incorporada na produção de amplificação após iniciação inicial. Exemplos de seqüências de ponta incluem: Seqüência promotora T7a de 25-mer: AAT TCT AAT ACG ACT CAC TAT AGG G; Iniciador de seqüenciamento M13/pUC (-40) GTT TTC CCA GTC ACG AC; Iniciador de seqüenciamento M13/pUC (-20), de 17-mer GTA AAA CGA CGG CCA GT; Iniciador reverso de seqüenciamento M13/pUC (-26), de 17-mer CAG GAA ACA GCT ATG AC; Iniciador de seqüenciamento M13/pUC (-40), de 17-mer GTT TTC CCA GTC ACG AC; Iniciador de seqüenciamento M13/pUC (-46), de 22-mer GCC AGG GTT TTC CCA GTC ACG A; Iniciador reverso de seqüenciamento M13/pUC (-46), de 24-mer GAG CGG ATA ACA ATT TCA CAC AGG; Iniciador de seqüenciamento de promotor SP6, de 18-mer ATT TAG GTG ACA CTA TAG; Iniciador de seqüenciamento de promotor SP6, de 24-mer CAT ACG ATT TAG GTG ACA CTA TAG; Iniciador de seqüenciamento de promotor T7, de 20-mer TAA TAC GAC TCA CTA TAG GG; Iniciador de seqüenciamento de promotor T3, de 17-mer ATT AAC CCT CAC TAA AG; e, Iniciador de seqüenciamento de promotor T3, de 24-mer GCG CGA AAT TAA CCC TCA CTA AAG.
A amplificação a partir de sítios do iniciador como aqueles descritos acima permite efetivamente o uso de um conjunto de iniciadores “universais”, que se ligam em C e C' para amplificar X de uma gama de cepas do analito. Além disso, deve-se observar que o amplicon amplificado com o uso dos iniciadores universais pode compreender regiões tanto conservadas quanto variáveis.
Em algumas modalidades, são usados iniciadores que amplificam seqüências de HPV. Mais preferivelmente, esses iniciadores são GP5+ é 5' TTT GTT ACT GTG GTA GAT ACT AC 3' e GP6+ é 5' GAA AAA TAA ACT GTA AAT CAT ATT C 3'. Esses iniciadores geram um amplicon de HPV que compreende tanto uma região conservada (definida como Y na Figura 2), quanto uma região que é variável entre diferentes cepas de HPV (definida como X na Figura 2).
Em outra modalidade, esses iniciadores são GP5d2+ é 5' TTT KTT ACH GTK GTD GAT ACH AC 3' e T7aGP6d+ é 5' AAT TCT AAT ACG ACT CAC TAT AGG GGA AAH ATA AAY TGY AAD TCA TAY TC 3'.
Em outra modalidade, esses iniciadores são GP5d3+ é 5' 5Phos TTT GTT ACH GTD GTD GAY ACH AC 3' e T7aGP6d+* é 5'/5AmMC6/AAT TCT AAT ACG ACT CAC TAT AGG GGA AAH ATA AAY TGY ARD TCA WAY TC 3'.
Em outra modalidade, os iniciadores diretos de um par de iniciadores são selecionados do grupo que consiste em: TR TTT GTT ACT GTK GTD GAT ACY A, opcionalmente tendo um caatcagc ou /5Phos/caatcagc conjugado ao terminal 5’ do iniciador; CAR YTR TTT GTT ACT GTK GTD GAT A, opcionalmente tendo um acaat ou /5Phos/acaat conjugado ao terminal 5’ do iniciador; CAR YTR TIT GTT ACT GTK GTD GA, opcionalmente tendo um acaat ou /5Phos/acaat conjugado ao terminal 5’ do iniciador; AAY CAR YTR TTT GTT ACT GTK GT, opcionalmente tendo um ggaac ou /5Phos/ggaac conjugado ao terminal 5’ do iniciador; TCT GTT ACT GTK GTD GAT ACY AC HCG, opcionalmente tendo um cagctt ou /5Phos/cagctt conjugado ao terminal 5’ do iniciador; TTT GTT ACT GTK GTD GAT ACY AC HCG YAG, opcionalmente tendo um cagctt /5Phos/cagctt conjugado ao terminal 5’ do iniciador; GTK GTD GAT ACY AC HCG YAG TAC, opcionalmente tendo um /5Phos/attacc conjugado ao terminal 5’ do iniciador; e GTD GAT ACY AC HCG YAG TAC HAA, opcionalmente tendo um attacc ou /5Phos/ctgtt conjugado ao terminal 5’ do iniciador; e Os iniciadores reversos de um par de iniciadores são selecionados do grupo que consiste em: TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG, opcionalmente tendo um actcactatagg ou /5AmMC6/actcactatagg conjugado ao terminal 5’ do iniciador; CAY ARY TGA AAA ATA AAY TGY AAA TC, opcionalmente tendo um aatacgactcactatagg ou /5AmMC6/aatacgactcactatagg conjugado ao terminal 5’ do iniciador; TR CAY ARY TGA AAA ATA AAY TG, opcionalmente tendo um tctaatacgactcactatagg ou /5AmMC6/tctaatacgactcactatagg conjugado ao terminal 5’ do iniciador; e TR CAY ARY TGA AAA ATA AA, opcionalmente tendo um aattctaatacgactcactatagg ou /5AmMC6/ aattctaatacgactcactatagg conjugado ao terminal 5’ do iniciador. Alternativamente, os iniciadores diretos e reversos são selecionados de um grupo de iniciadores similares àqueles aqui descritos anteriormente, mas que podem diferir dos iniciadores diretos ou reversos aqui descritos anteriormente de 0 a cerca de 5 substituições de nucleotídeos, preferivelmente 0 a cerca de 2 substituições, em sítios onde ocorrem substituições de nucleotídeos entre diferentes cepas de HPV, mas com a exclusão de substituições dois últimos dois nucleotídeos na extremidade 3'. A invenção também contempla substituições similares às seqüências de ponta opcionais, como aquelas para iniciadores diretos ou reversos aqui descritas anteriormente, as referidas pontas opcionais conjugadas ao terminal 5’ de qualquer um dos iniciadores diretos ou reversos descritos acima. Em certas modalidades preferidas, o iniciador direto é selecionado de CAR YTR ITT GTT ACT GTK GTD GA, opcionalmente tendo um acaat ou /5Phos/acaat conjugado ao terminal 5’ do iniciador e GTD GAT ACY AC HCG YAG TAC HAA, opcionalmente tendo um ctgtt ou /5Phos/ctgtt conjugado ao terminal 5’ do iniciador. El algumas outras modalidades preferidas, o iniciador reverso é selecionado de TGA AAA ATA AAY TGY AAA TCA TAT TCY TCM MCA TG, opcionalmente tendo um actcactatagg ou /5AmMC6/actcactatagg conjugado ao terminal 5’ do iniciador e TR CAY ARY TGA AAA ATA AAY TG, opcionalmente tendo um tctaatacgactcactatagg ou /5AmMC6/tctaatacgactcactatagg conjugado ao terminal 5’ do iniciador.
As descrições acima mostram exemplos de pares de iniciadores úteis na presente invenção. Pares de iniciadores adicionais podem ser formados por pareamento de diferentes iniciadores diretos (por exemplo, GP5+, GP5d2+ etc.) e reversos (por exemplo, GP6+, T7aGP6d+) entre eles.
Certas modalidades da invenção são dirigidas aos fragmentos de qualquer um dos iniciadores aqui revelados, incluindo todas as combinações e subcombinações dos referidos fragmentos de iniciador, até um limite inferior de cerca de fragmentos centrais de 20-mer 3-prime de qualquer um dos iniciadores revelados. Como aqui usado, um “fragmento” refere-se a uma seqüência oligomérica de ácidos nucleicos de iniciador ou sonda truncada formada por eliminação de um ou mais nucleotídeos do iniciador original.
A presente invenção também contempla a amplificação de seqüências de controle. Em uma modalidade, a seqüência de controle pode incluir uma região do genoma do indivíduo do qual uma amostra biológica é derivada. No entanto, a presente invenção não se limita, de forma alguma, a essas seqüências de controle em particular, e outras seqüências de controle que poderiam ser evidentes para aqueles habilitados na técnica também são contempladas. Além disso, os métodos da presente invenção também podem ser realizados sem a amplificação de uma seqüência de controle.
Em algumas modalidades, a seqüência de controle é amplificada do genoma de um ser humano com o uso do iniciador MLC1_F, que compreende a seqüência de nucleotídeos 5' TAC ACA CAG GTG TAC ACA GA 3' e MLC1_R, que compreende a seqüência 5' ACC AAG TAC TCT ACG TGT TG 3'.
Em outra modalidade, a seqüência de controle é amplificada do genoma de um ser humano usando o iniciador miel_95f, que compreende a seqüência de nucleotídeos 5' GGC ACC CAG ACA TAC AC 3' e T7amlcl_275r (HeelMLCR), que compreende a seqüência 5' AAT TCT AAT ACG ACT CAC TAT AGG GGA AAH ATA AAY TGY AAD TCA TAY TC 3'.
DNA isolado pode ser amplificado com o uso de qualquer protocolo de amplificação de DNA. Vários métodos exemplares para a amplificação de DNA que não limitam, de forma alguma, a invenção são apresentados em “DNA Amplification: Current Technologies and Applications” (Demidov e Broude Eds., Horizon Bioscience, 2004).
O RNA isolado pode ser amplificado com o uso de quaisquer métodos de RNA conhecidos na técnica e foram desenvolvidas diversas tecnologias de amplificação de RNA. Duas categorias principais destas são: (i) aquelas que utilizam ciclagem térmica como, por exemplo, RT—PCR e (ii) ensaios isotérmicos como, por exemplo, amplificação baseada em seqüência de ácidos nucleicos (NASBA) (Compton, Nature 350: 91-92, 1991; Kievits e cols., J. Virol. Methods 35: 273-286, 1991) e amplificação mediada por transcrição (TMA) (Hill, J. Clin. Ligand Assay 19: 43-51, 1996). Os ensaios isotérmicos pode ser subdivididos com base em se: (i) eles copiam e amplificam a seqüência-alvo, por exemplo, TMA,
NASBA e replicação de seqüência auto-sustentada (3SR) (Guatelli e cols., Proc. Natl. Acad. Sci. USA 87: 1.874-1.878, 1990; Chadwick e cols., J. Virol. Mehods 70: 59-70, 1998; para uma revisão, veja Chan e Fox, Rev. Med. Microbiol. 10: 185-196, 1999), ou (ii) eles geram um sinal alvo-dependente que pode ainda ser amplificado, por exemplo, ensaios de invasor (Lyamichev e cols., Nat. Biotechnol. 17: 292-296, 1999; Ryan e cols., Mol. Diagn. 4: 135-144, 1999). Há várias outras tecnologias de amplificação que não se encaixam facilmente nessas categorias, por exemplo, Q beta replicase (Lizardi e cols., Biotechnology 6: 1.197-1.202, 1988) e DNA ramificado (Todd e cols., J. AIDS Hum. Retrovirol. 10: S35— S44, 1995; Pawlotsky e cols., J. Virol. Methods 79: 227-235, 1999). No entanto, deve-se observar que a presente invenção contempla qualquer método de amplificação d RNA que seria evidente para aqueles habilitados na técnica. Além disso, deve-se observar que a presente invenção também contempla o uso de transcriptase reversa ou um equivalente funcional destas para converter RNA em DNA, o qual pode então ser subseqüentemente amplificado.
De acordo com a presente invenção, os amplicons citados nas etapas (iii) e/ou (iv) dos métodos descritos suprasão rotulados. Os amplicons da presente invenção podem ser rotulados com o uso de qualquer meio conveniente. Métodos exemplares incluem métodos tanto pré- quanto pós- síntese. Métodos de rotulagem pré-síntese incluem a rotulagem de um iniciador de PCR que é subseqüentemente usado para amplificação e, dessa forma, incorporado em um amplicon por meio de PCR. Nesse método, o rótulo é tipicamente anexado à extremidade 5' de um iniciador adequado à amplificação do amplicon, embora a rotulagem em outras posições dentro do iniciador, por exemplo, rotulagem 3' ou rotulagem não terminal, também seja contemplada.
Um vinculador químico também pode ser usado entre o rótulo e o polinucleotídeo que é rotulado. Seqüências vinculadoras apropriadas serão facilmente evidentes para aqueles habilitados na técnica, e provavelmente incluirão vinculadores como, por exemplo, modificadores amino C6, C2 e C12 e vinculadores que compreendem grupos tiol. Como será facilmente verificado, um iniciador pode compreender o vinculador e rótulo, ou somente o vinculador, ao qual o rótulo pode ser anexado em um estágio posterior.
Métodos de rotulagem pós-amplificação incluem sistemas de rotulagem nick, nos quais um polinucleotídeo rotulado é sintetizado a partir do amplicon com o uso de polimerase de Klenow, ou um equivalente funcional desta, por iniciadores aleatórios. Os nucleotídeos rotulados, ou nucleotídeos que compreendem um grupo vinculador, podem ser incorporados no polinucleotídeo sintetizado por polimerase de Klenow durante a síntese.
Em qualquer evento, outros métodos de rotulagem devem ser facilmente evidentes para aqueles habilitados na técnica e deve-se observar que a presente invenção não é definida ou limitada pela escolha do método de rotulagem.
Preferivelmente, o rótulo usado é um “marcador fluorescente” ou “fluoróforo”. Muitos marcadores fluorescentes diferentes serão familiares àqueles habilitados na técnica, e a escolha do marcador fluorescente não limita, de forma alguma, a invenção. Em uma modalidade preferida da presente invenção, os marcadores fluorescentes da presente invenção compreendem qualquer marcador fluorescente que possa ser anexado a um polinucleotídeo e que seja é excitável com o uso de uma fonte luminosa selecionada do grupo abaixo: (i) Lasers de íon argônio: compreendem uma linha azul, de 488 nm, que é adequada à excitação de muitos corantes e fluorcromos que fluorescem na região do verde ao vermelho. Também estão disponíveis lasers de argônio ajustáveis que emitem uma gama de comprimentos de onda (458 nm, 488 nm, 496 nm, 515 nm e outros). (ii) Lasers de diodo: possuem um comprimento de onda de emissão de 635 nm. Outros lasers de diodo agora disponíveis operam a 532 nm. Curiosamente, esse comprimento de onda excita iodeto de propídio (PI) otimamente. A coloração com PI é amplamente usada para análise de DNA, contagem de células vivas/mortas e determinação de ploidia. Lasers de diodo azuis que emitem luz em torno de 476 nm também estão disponíveis (iii) Lasers de gás HeNe: operam com a linha do vermelho de 633 nm. (iv) Lasers de HeCd: operam a 325 nm. (v) Lâmpada de arco de mercúrio de 100 W: a fonte luminosa mais eficiente for excitação de corantes UV como Hoechst e DAPI.
Em modalidades mais preferidas da presente invenção, os marcadores fluorescentes são selecionados de: hidroxicumarina, aminocumarina, metoxicumarina, azul cascata, amarelo Lucifer, NBD, Ficoeritrina (PE), PerCP, aloficocianina, Hoechst 33342, DAPI, Azul SYTOX, Hoechst 33258, cromomicina A3, mitramicina, YOYO-1, verde SYTOX, laranja SYTOX, 7-AAD, laranja acridina, TOTO-1, To-PRO-1, laranja tiazol, TOTO-3, TO-PRO-3, LDS 751, corantes Alexa Flúor, incluindo Alexa Flúor-350, -430, -488, - 532, -546, -555, -556, -594, -633, -647, -660, -680, -700 e -750; corantes BoDipy, incluindo BoDipy 630/650 e BoDipy 650/665; corantes CY, particularmente Cy2, Cy3, Cy3.5, Cy5, Cy 5.5 e Cy7; 6-FAM (Fluoresceína); PE-Cy5, PE-Cy7, Fluoresceína dT; Hexaclorofluoresceína (Hex); 6-carboxi-4', 5'-dicloro-2', 7'-dimetoxifluoresceína (JOE); corantes verdes Oregon, incluindo 488-X e 514; corantes Rodamina, incluindo X- Rodamina, Lissamina Rodamina B, Verde Rodamina, Vermelho Rodamina e ROX; TRITC, Tetrametilrodamina (TMR); Carboxitetrametilrodamina (TAMRA); Tetraclorofluoresceína (TET); Vermelho 6B, Flúor-X, BODIPY-FL, Corante Verde SYBR Green I e Vermelho Texas. Em modalidades particularmente preferidas da presente invenção, o marcador é Cy5, que é particularmente conveniente para a prática da presente invenção.
No entanto, em modalidades alternativas da invenção, podem ser usados marcadores radioativos ou não radioativos para rotular o amplicon. Rótulos radioativos convenientes incluem 32P e 3H. Esses rótulos podem ser incorporados no amplicon e/ou iniciador com o uso de meios convenientes. Uma gama de métodos de rotulagem não radioativa também pode ser usada. Métodos de rotulagem não radioativa exemplares que, de modo algum, limitam a presente invenção são apresentados em Speel (Histochem. Cell Biol. 112: 89-113, 1999).
O termo “reagente”, como aqui usado, visa compreender um polinucleotídeo imobilizado em uma esfera. Mais particularmente, cada reagente compreende um polinucleotídeo que compreende uma seqüência que é complementar a um amplicon gerado de acordo com os métodos aqui descritos, que é ligado ou de algum outro modo associado a uma esfera fisiologicamente distinguível. Um reagente também pode compreender uma seqüência que é complementar a uma seqüência de controle, como aqui definida anteriormente, ou seja, uma seqüência amplificada do genoma de um organismo multicelular (Z) ou do amplicon de uma seqüência de nucleotídeos que é conservada entre cepas do analito (Y).
Conseqüentemente, um conjunto de esferas de reagentes pode compreender: [B1-cX1, B2-cX2, B3-cX3...Bn-cXn, BY-cY, BZ-cZ] em que: B1...Bn, By, BZ são, cada um, esferas fisiologicamente distinguíveis; CXn é um polinucleotídeo imobilizado a uma esfera, em que o referido polinucleotídeo compreende uma seqüência de nucleotídeos que é complementar a uma seqüência de ácidos nucleicos em particular que é específica para um analito ou a uma cepa em particular de um analito em questão e em que n é o número de analitos ou cepas particulares de um analito em questão a ser detectado com o uso do conjunto de esferas; cY é um membro opcional do conjunto de esferas e é um polinucleotídeo imobilizado a uma esfera, em que o referido polinucleotídeo compreende uma seqüência de nucleotídeos que é complementar a uma seqüência que é conservada entre os analitos ou cepas de um analito em questão; cZ é um membro opcional do conjunto de esferas e é um polinucleotídeo imobilizado a uma esfera, em que o referido polinucleotídeo compreende uma seqüência de nucleotídeos que é complementar a uma seqüência de controle que é amplificada a partir de um indivíduo multicelular.
Preferivelmente, o analito em questão é HPV e a seqüência de controle de DNA é uma seqüência genômica de DNA humana.
O termo “complementar”, visa significar que o polinucleotídeo imobilizado do reagente deve hibridizar para um amplicon gerado de acordo com os métodos aqui descritos sob condições de baixa estringência. Preferivelmente, o polinucleotídeo imobilizado deve se ligar à amostra e ao padrão sob condições de estringência média e, mais preferivelmente ainda, o polinucleotídeo imobilizado deve se ligar à amostra e ao padrão sob condições de alta estringência.
Aqui, a referência à baixa estringência inclui e engloba de pelo menos cerca de 0 a pelo menos cerca de 15% v/v de formamida (incluindo 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10% 11%, 12%, 13% e 14% v/v de formamida) e de pelo menos cerca de 1 M a pelo menos cerca de 2 M de sal para hibridização, e pelo menos cerca de 1 M a pelo menos cerca de 2 M de sal para condições de lavagem. Geralmente, a baixa estringência é a partir de cerca de 25-30°C a cerca de 52°C, por exemplo, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 e 52°C. A temperatura pode ser alterada, e temperaturas maiores podem ser usadas para substituir formamida e/ou para gerar condições de estringência alternativas. Condições de estringência alternativas podem ser aplicadas, quando necessário, por exemplo, estringência média, que inclui e engloba de pelo menos cerca de 16% v/v a pelo menos cerca de 30% v/v de formamida, incluindo 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 24%, 26%, 27%, 28%, 29% e 30% v/v de formamida, e de pelo menos cerca de 0,5 M a pelo menos cerca de 0,9 M de sal para hibridização, e pelo menos cerca de 0,5 M a pelo menos cerca de 0,9 M de sal para condições de lavagem, ou alta estringência, que inclui e engloba de pelo menos cerca de 31% v/v a pelo menos cerca de 50% v/v de formamida e de pelo menos cerca de 0,01 M a pelo menos cerca de 0,15 M de sal para hibridização, e pelo menos cerca de 0,01 M a pelo menos cerca de 0,15 M de sal para condições de lavagem. Em geral, a lavagem é realizada em Tm = 69,3 + 0,41 (G+C)% (Marmur e Doty, J. Mol. Biol. 5: 109, 1962). No entanto, a Tm de um DNA duplex diminui em 1°C a cada aumento de 1% no número de pares de bases não compatíveis (Bonner e Laskey, Eur. J. Biochem. 46: 83, 1974). A formamida é opcional nessas condições de hibridização. Conseqüentemente, níveis particularmente preferidos de estringência são definidos da seguinte forma: baixa estringência é 6 x tampão SSC, 0,1% p/v de SDS a 25-42°C; uma estringência moderada é 2 x tampão SSC, 0,1% p/v de SDS em uma temperatura na faixa de 20°C a menos de 65°C; alta estringência é 0,1 x tampão SSC, 0,1% p/v de SDS em uma temperatura de pelo menos 65°C.
As esferas, B1...Bn, By, BZ, do conjuntos de esferas de reagente são, cada uma, esferas fisiologicamente distinguíveis. O termo “fisiologicamente distinguível” refere-se a qualquer característica física ou química que permita que uma esfera, por exemplo, B1, seja diferenciada de outra esfera, por exemplo, B2. Conseqüentemente, as esferas fisiologicamente distinguíveis permitem a diferenciação de reagentes específicos.
Em certas modalidades preferidas, a esfera compreende uma “micropartícula”. Como ficará evidente para aqueles habilitados na técnica, todos os materiais, homogêneos ou no, podem ser usados para a micropartícula. As micropartículas aqui contempladas também podem compreender mais de uma substância e, dessa forma, podem compreender conchas, ligas ou misturas de substâncias orgânicas e/ou inorgânicas. Particularmente materiais úteis que podem ser usados de acordo com a presente invenção e que representam modalidades preferidas da presente invenção incluem materiais selecionados da lista que consiste em: sílica (por exemplo: quartzo ou vidro), látex, titânia, dióxido de estanho, ítria, alumina, e outros óxidos de metal binário (por exemplo, ZnO), perovskites e outros óxidos de metais piezelétricos (por exemplo, BaTiO3), ZnS, sacarose, agarose e outras esferas poliméricas. Em uma modalidade particularmente preferida, a micropartícula compreende sílica.
Em algumas modalidades preferidas, o termo “fisioquimicamente distinguível” refere-se a uma diferença mensurável em qualquer tamanho de esfera, à presença ou ausência de um rótulo opticamente detectável em particular e/ou à intensidade de um rótulo opticamente detectável.
As esferas contempladas pela presente invenção podem ser produzidas em qualquer formato tridimensional regular ou irregular conveniente. No entanto, é geralmente prático sintetizar pequenas esferas ou partículas esferoidais. Essas esferas ou partículas esferoidais também são aqui denominadas “esferas”. Conseqüentemente, em modalidades preferidas da presente invenção, as “micropartículas” da presente invenção são substancialmente esféricas ou esferoidais ou compreendem uma “microesfera”.
Embora as esferas da presente invenção possam ser denominadas “microesferas”, o tamanho real das partículas depende de diversos fatores, e as partículas podem ou não realmente compreender medidas na faixa de micrômetros. Em algumas modalidades preferidas, a esfera compreende um diâmetro (ou medida equivalente em uma partícula não esferoidal) de cerca de 300 nm a cerca de 30 μ m, incluindo 300 nm, 350 nm, 400 nm, 450 nm, 500 nm, 550 nm, 600 nm, 650 nm, 700 nm, 750 nm, 800 nm, 850 nm, 900 nm, 950 nm, 1,0 μm, 1,1 μm, 1,2 μm, 1,3 μm, 1,4 μm, 1,5 μm, 1,6 μm, 1,7 μm, 1,8 μm, 1,9 μm, 2,0 μm, 2,1 μm, 2,2 μm, 2,3 μm, 2,4 μm, 2,5 μm, 2,6 μm, 2,7 μm, 2,8 μm, 2,9 μm, 3,0 μm, 3,1 μm, 3,2 μm, 3,3 μm, 3,4 μm, 3,5 μm, 3,6 μm, 3,7 μm, 3,8 μm, 3,9 μm, 4,0 μm, 4,1 μm, 4,2 μm, 4,3 μm, 4,4 μm, 4,5 μm, 4,6 μm, 4,7 μm, 4,8 μm, 4,9 μm, 5,0 μm, 5,1 μm, 5,2 μm, 5,3 μm, 5,4 μm, 5,5 μm, 5,6 μm, 5,7 μm, 5,8 μm, 5,9 μm, 6,0 μm, 6,1 μm, 6,2 μm, 6,3 μm, 6,4 μm, 6,5 μm, 6,6 μm, 6,7 μm, 6,8 μm, 6,9 μm, 7,0 μm, 7,1 μm, 7,2 μm, 7,3 μm, 7,4 μm, 7,5 μm, 7,6 μm, 7,7 μm, 7,8 μm, 7,9 μm, 8,0 μm, 8,1 μm, 8,2 μm, 8,3 μm, 8,4 μm, 8,5 μm, 8,7 μm, 8,8 μm, 8,9 μm, 9,0 μm, 9,1 μm, 9,2 μm, 9,3 μm, 9,4 μm, 9,5 μm, 9,6 μm, 9,7 μm, 9,8 μm, 9,9 μm, 10 μm, 11 μm, 12 μm, 13 μm, 14 μm, 15 μm, 16 μm, 17 μm, 18 μm, 19 μm, 20 μm, 21 μm, 2 2 μm, 2 3 μm, 2 4 μm, 2 5 μm, 2 6 μm, 2 7 μm, 2 8 μm, 29 μm, 30 μm. Mais preferivelmente, a esfera compreende um diâmetro (ou medida equivalente em uma partícula não esferoidal) entre 1 μm e 10 μm.
Em uma modalidade particularmente preferida, as esferas são AmpaSand (Nome comercial: Genera Biosystems) esferas produzidas por Genera Biosystems. Essas esferas são comercialmente disponíveis e são descritas em www.generabiosystems.com/generabiosystems/technology/AmpaSa ndBeads/. No entanto, a presente invenção não se limita ao uso desses esferas especificamente.
As esferas podem ser distinguidas com base na presença ou ausência de um ou mais “rótulos opticamente detectáveis”. Tipicamente, uma esfera particular pode compreender 0, 1, 2, 3, 4, 5 rótulos opticamente detectáveis. Como aqui usado, o termo “rótulo opticamente detectável” refere-se a qualquer molécula, átomo ou íon que emita fluorescência, fosforescência e/ou incandescência. Os rótulos opticamente detectáveis convenientes incluem aqueles que emitem na faixa de ultravioleta (faixa de comprimento de onda de cerca de 350 nm a cerca de 3nm), visível (faixa de comprimento de onda de cerca de 350 nm a cerca de 800 nm), próxima do infravermelho (NIR) (faixa de comprimento de onda de cerca de 800 nm a cerca de 1500 nm) e/ou infravermelho (IR) (faixa de comprimento de onda de cerca de 1500 nm a cerca de 10μm). No entanto, devido à facilidade de detecção, em uma modalidade particularmente preferida, o rótulo opticamente detectável é detectável na de comprimento de onda visível.
Em uma modalidade também preferida da atual invenção, o rótulo opticamente detectável compreende um ou mais rótulos selecionados da lista que consiste em: um fluoróforo, uma partícula semicondutora, uma partícula de fósforo, uma partícula dopada, ou um nanocristal ou quantum dot.
Em certas modalidades particularmente preferidas da presente invenção, o rótulo opticamente detectável é um fluoróforo. Como aqui usado, o termo “fluoróforo” refere-se a qualquer molécula que exiba a propriedade de fluorescência. Para os objetivos dessa, o termo “fluorescência” pode ser definido como a propriedade de uma molécula de absorver luz de um comprimento de onda particular e re-emitir luz de um comprimento de onda mais longo. A mudança do comprimento de onda está relacionada a uma perda de energia que ocorre no processo. O termo “fluoróforo” pode englobar um faixa de rótulos opticamente detectáveis como fluoróforos químicos e corantes bem como pontos quânticos.
Os rótulos opticamente detectáveis particularmente convenientes que podem ser usados de acordo com a presente invenção são partículas fluorescentes inseridas de semicondutores. Essas partículas de rótulo opticamente detectável podem ser tão pequenas que suas propriedades e emissão tornam-se dependentes do tamanho. Tais partículas pequenas de rótulo opticamente detectável são referidas na técnica como nanopartículas semicondutoras, pontos quânticos, quantum wires, quantum rods ou nanocristais ou partículas Q. No entanto, como aqui usado, o termo “Quantum Dot” ou “QD” deve englobar todas essas partículas. Além disso, os rótulos opticamente detectáveis que compreendem
QDs podem compreender partículas aproximadamente esféricas ou partículas esferoidais, ou partículas esféricas ou esferoidais revestidas. No entanto, o termo QD não deve ser considerado de qualquer modo como sendo limitado a uma morfologia esférica, esferoidal, circular, cilíndrica ou qualquer outra morfologia de um “dot”. Por exemplo, como aqui usado QDs também podem compreender outra morfologias que incluem, entre outras, semelhante a haste, elipsoidal, ou partículas semelhantes a haste ou elipsoidais revestidas.
QDs consistem em núcleo cristalino de escala nanômetro de material semicondutor; versões biologicamente ativas são tipicamente circundadas por uma casca protetora e revestimento externo. Por exemplo, QDs podem compreender cristalitos semicondutores que têm cerca de 2 nm a cerca de 30 nm de diâmetro e podem conter aproximadamente 50-500.000 átomos no cristal, incluindo cristais luminescentes que compreendem materiais como ZnS, ZnSe, ZnTe, CdS, CdSe, CdTe, PbS, PbSe, PbTe, HgS, HgSe, HgTe, Si, ZnO.
QDs fluoresce com um amplo espectro de absorção e um espectro estreito de emissão. Diferente de alguns outros fluoróforos, que têm espetros de absorção distintos, QDs absorvem luz por uma ampla faixa de espectro, que permitem que os pontos quânticos sejam excitados com uma faixa de fontes luminosas, como lasers, lâmpadas em arco, ou LEDs. Além disso, uma coleção de diferentes QDs pode ser usada em aplicações de multiplex que usam uma fonte única de excitação. No entanto, o espectro de emissão para cada ponto é tipicamente muito estreito, na ordem de cerca de 30 nm, a cor exata dependendo do diâmetro da partícula e composição. Além disso, o espectro de emissão estreito de QDs permite resolução de espectro de pontos adjacentes. Além do benefício acima, QDs são também relativamente foto- estáveis, mesmo durante excitação intensa, e são mais brilhantes que os fluoróforos.
Em vista do anterior, deve ser também entendido que a presente invenção engloba o uso QDs de diferentes tamanhos.
Além disso, a presente invenção contempla QDs que são tratados com procedimentos como tratamento térmico, modificação de superfície, liga de metais, passivação de superfície ou cobertura com revestimento de superfície para permite que o QD emita com alto rendimento e para melhorar a fotoestabilidade por longos períodos de tempo.
QDs são também comercialmente disponíveis a partir de companhias como Quantum Dot Corp. (QDC), que produz QDs como o Qdot [Marca Registrada] 605 conjugado de estreptavidina, que contém um núcleo de cádmio-selenito que emite a 605 nm. Os conjugados de Qdot que emitem a 525, 565, 585, e 655 nm são também disponíveis. No entanto, deve-se compreender que a presente invenção não é limitada de qualquer modo pela composição particular do QD (ou qualquer outro rótulo opticamente detectável) e qualquer QD (comercial ou de outros modo) pode ser compatível com a presente invenção.
Há também vários corantes fluorescentes que são disponíveis na técnica que podem ser usados como fluoróforos de acordo com a presente invenção. Uma importante propriedade de um corante fluorescente ou outro fluoróforo, que determina seu potencial para uso é o comprimento de onda de excitação do fluoróforo; ele deve estar de acordo com os comprimentos de onda disponíveis da fonte luminosa. No entanto, vários diferentes corantes fluorescentes e outros fluoróforos serão familiares para aqueles habilitados na técnica, e a escolha do marcador fluorescente, de modo algum, limita a atual invenção. Corantes fluorescentes particularmente convenientes que podem ser usados para a rotulagem de um substrato incluem aqueles discutidos acima com relação à rotulagem do amplicon de PCR. No entanto, quando da escolha de rótulos fluorescentes, o espectro de emissão do rotulo fluorescente usado para o agente de ligação deve ser distinto do espectro de emissão do rótulo usado para o amplicon(s).
Duas técnicas de coloração são comumente usadas para esferas e microesferas de rotulados de modo fluorescente — coloração interna e coloração externa (superfície- rotulagem). As duas técnicas produzem esferas com propriedades únicas, cada um benéfico para diferentes aplicações. A coloração interna produz partículas extremamente estáveis com emissões de fluorescência tipicamente estreitas. Essas esferas frequentemente apresentam uma maior resistência ao fotobranqueamento. Uma vez que o fluoróforo está no interior das esferas, grupos de superfície são disponíveis para uso em ligantes de conjugação (proteínas, anticorpos, ácidos nucleicos etc.) à superfície da esfera. Por essa razão, esferas internamente rotuladas são tipicamente usadas na detecção de analito e aplicações de imunoensaio. A rotulagem de superfície envolve a conjugação do fluoróforo à superfície da esfera. Pelo fato de os fluoróforos estarem sobre a superfície da esfera, eles são capazes de interagir com seu ambiente de modo similar aos fluoróforos em uma célula corada. O resultado é uma esfera padrão que exibe a mesma excitação e propriedades de emissão que as amostras de célula corada, sob uma variedade de diferentes condições, como a presença de contaminantes ou mudanças no pH. A natureza “ambientalmente responsiva” das esferas rotuladas na superfície as torna idealmente adequadas para imitar amostras biológicas. Esferas externamente rotuladas são frequentemente usadas como controles e padrões em inúmeras aplicações que utilizam detecção de fluorescência. No entanto, a presente invenção contempla a associação de uma esfera com um rótulo fluorescente por qualquer meio.
Os termos “esferas fosforescentes”, “esferas de fósforo” e “fósforo” são usados de modo intercambiável nessa. O que constitui um rótulo fosforescente opticamente detectável deve ser prontamente compreendido por pessoa habilitada na técnica. no entanto, por via de exemplo, que não limita a invenção, fósforos adequados incluem pequenas partículas de ZnS, ZnS:Cu, óxido de Eu e outros fósforos usados em dispositivos de apresentação.
Um rótulo opticamente detectável que compreende a um “esfera dopada” pode incluir uma partícula que compreende quantidades obscuras de um ou mais íons terrosos raros, como Eu, Y, Yb, Sm e outros.
Como aqui usado, o termo “rótulo opticamente detectável” deve ser entendido como também englobando múltiplos rótulos opticamente detectáveis, misturas de rótulos opticamente detectáveis, nanocristais revestidos, ligas e outras misturas complexas que podem ser evidentes para o profissional habilitado. O uso de todos esses rótulos opticamente detectáveis deve ser considerado como estando dentro do escopo dos métodos e agentes aqui descritos.
Além disso, o rótulo opticamente detectável do reagente pó compreender um rótulo opticamente detectável incorporado na seqüência de polinucleotídeos imobilizada que é ligada ou associada à esfera, em vez de ser um rótulo diretamente associado à esfera por si.
As esferas são geralmente rotuladas pelo oligonucleotídeo de “rotulagem” ou marcador imobilizado. Esse rótulo carrega uma amina interna (NH2) que é então modificada por conjugação com um succinimidil éster de um corante. No conjunto atual, o corante usado é BODIPY-TMR. Por mistura de rótulos rotulados e não rotulados e então conjugação dessa mistura às esferas, uma pessoa pode produzir classes de esferas com diferentes níveis do marcador fluorescente. As proporções convenientemente usadas estão em uma série de 1:5x; ou seja, as diferentes classes são produzidas pelo uso da proporção de rótulos não rotulados:rotulados. Isso é genericamente exemplificado abaixo na Tabela 4.
Tabela 4 - Proporção de rótulos não rotulados para rotulados
O rótulo opticamente detectável pode ser aplicado a uma esfera em uma faixa de concentrações ou intensidades, assim fornecendo outra base em que as esferas particulares podem ser “fisiologicamente distinguíveis”. Por exemplo, se a intensidade máxima detectável do sinal de um opticamente detectável particular é considerada como sendo 100%, o rótulo pode ser aplicado a uma faixa de esferas para gerar intensidades de 0%, 2%, 4%, 6%, 8%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 100%.
Em uma modalidade, os conjuntos de esferas de reagentes compreendem esferas de 3,0 μm, 3,5 μm, 4,1 μm, 5,0 μm, 5,6 μm e 6,8 μm, em que as esferas de diâmetro de 3,0 μm, 3,5 μm e 4,1 μm são rotuladas a 0% e 100%, as esferas de diâmetro de 5,0 μm são rotuladas a 0%, 100% e 20% e as esferas de diâmetro de 5,6 μm e 6,8 μm são rotuladas a 0%, 100%, 20% e 4%.
Em outra modalidade, os conjuntos de esferas de reagentes compreendem esferas de 3,0 μm, 3,5 μm, 3,77 μm, 5,0 μm, 5,6 μm e 6,8 μm. Todos os tamanhos de esfera, (exceto pelo de 3,0 μm que é dividido por nível zero e alto nível de TMR), são divididos de acordo com seu respectivo nível zero, nível médio, e alto nível de TMR.
Em outra modalidade, os níveis de TMR são ajustados de modo que durante a conjugação da esfera ao oligo, os oligos com proporções definidas totais de oligo para flúor- rotulado são usados para determinar agrupamentos distintos de TMR. Por exemplo, nível zero de TMR tem oligos não rotulados incluídos em conjugação; altos níveis de TMR têm uma proporção total de 3:1 de oligo para flúor-rotulado de oligos incluído em conjugação; e níveis médios de TMR têm uma proporção total de 150:1 a uma de 80:1 de oligo para flúor-rotulado de oligos incluído em conjugação, dependendo do tamanho da esfera.
O componente do polinucleotídeo imobilizado do reagente, por exemplo, cXn, cY e/ou cZ pode ser ligado a uma esfera com o uso de qualquer meio conveniente.
O polinucleotídeo imobilizado pode ser encapsulado em esferas durante sua produção ou pode ser anexado a sua superfície pós-produção. O método de escolha usado para associar o polinucleotídeo com a esfera dependerá do material usado, como será prontamente determinado pelo profissional habilitado. Em adição, tratamentos adicionais, incluindo silanização (revestimento do substrato com silanos), podem ser realizados nas esferas antes da anexação do polinucleotídeo para aumentar a ligação do referido polinucleotídeo à esfera.
Geralmente, as esferas podem ser revestidas com qualquer composto que se anexará de modo covalente, ou adsorverá, à superfície da esfera, e o reagente deve também ter uma porção química para a anexação de um polinucleotídeo, como um grupo tiol, amina ou carboxila. Exemplos não limitantes de compostos com essas características incluem silanos terminados em amino como amino-propiltrimetoxissilano e aminopropiltrietoxissilano, bem como silanos terminados em tiol como tiopropiltrimetoxissilano e tio-propiltrietoxissilano. Além dos silanos, compostos como poli-L-lisina que se anexam não covalentemente à superfície de vidro e adsorve eletrostaticamente os grupos fosfato do polinucleotídeo estão também dentro do escopo da presente invenção.
Portanto, outros compostos, incluindo outros silanos adequados para anexação de um polinucleotídeo a uma superfície são prontamente identificados pelo profissional habilitado, e a presente invenção não é limitada pela escolha do composto.
O polinucleotídeo pode ser anexado à esfera com o uso de qualquer meio conveniente; tipicamente isso é feito por adsorção física ou ligação química. Em adição, as esferas podem ser também revestidas com um agente que promova ou aumente a adsorção ou ligação do polinucleotídeo à superfície da esfera, como amino-silanos. Entretanto, outros agentes que realizam essa função serão prontamente identificados por pessoa habilitada na técnica. em algumas outras modalidade, o polinucleotídeo é covalentemente conjugado à esfera por um grupo oligo acredita que reage com um grupo tiol da esfera.
Em outra modalidade, a molécula de ácido nucleico é ligada à esfera via o Sistema Universal de Ancoragem (UAS) (marca registrada: Genera Biosystems). Resumidamente, esse sistema envolve o uso de uma molécula de ácido nucleico “de ponte” para ligar uma seqüência de “rótulo” de ácido nucleico no substrato com uma seqüência alvo. A seqüência “em ponte” é parcialmente complementar à seqüência de rótulo e parcialmente complementar à seqüência alvo, de modo que a seqüência de ponte pode ser ligar a ambas seqüências de rótulo e alvo e mantê-las em alinhamento de modo que as seqüências de rótulo e alvo possam ser ligadas com o uso de uma ligase. O UAS é também comercialmente disponíveis e é descrito em detalhes em www.generabiosystems.com/generabiosystems/technology/UAS/.
No entanto, a presente invenção não deve ser considerada de qualquer modo limitada a esse método particular de ligação de uma molécula de ácido nucleico a um substrato.
A determinação de se ocorreu a ligação entre um amplicon e um reagente pode ser feita com o uso de qualquer metodologia que permita a localização de um rótulo de amplicon ligado a um reagente particular fisiologicamente distinguível. Em uma modalidade particularmente preferida, a citometria de fluxo é usada.
A citometria de fluxo pode ser definida como uma tecnologia para medir as propriedades das partículas ou células à medida que elas se movem, ou fluem, em suspensão líquida. Uma analogia pode ser feita com um item mais familiar de equipamento laboratorial, o microscópio, para também descrever essa tecnologia. A maioria dos microscópios tem os seguintes componentes:
Uma fonte de luz
O microscópio típico usa um bulbo de luz para iluminar o objeto. No citômetro de fluxo, a fonte de luz é freqüentemente um laser. Lasers são usados porque eles fornecem um feixe muito concentrado e intenso de luz monocromática. O caráter monocromático da luz é especialmente importante na confecção de medições de fluorescência.
A posição
Em um microscópio, a posição é móvel de modo a permitir a passagem do objeto ao campo visual de uma lente objetiva. No citômetro de fluxo, as células ou partículas existem em suspensão líquida. O líquido flui em resposta a pressão do ar, além de uma lente objetiva, assim carregando as células ou partículas através do campo visual.
A lente
Tanto no microscópio quanto no citômetro de fluxo, a lente coleta luz a partir do objeto.
Os filtros
Alguns microscópios têm filtros para selecionar aquelas características da luz que são mais importantes para o observador. Isso é particularmente verdadeiro em microscópios de fluorescência. Em fluorescência, as moléculas do corante são excitadas por luz de um comprimento de onda característico que então produz luz emitida de um comprimento de onda mais longo. Os filtros removem a luz de excitação para permitir que a luz de emissão seja observada ou medida.
Os detectores
Em um microscópio, o detector de luz é o observador. O citômetro de fluxo usa detectores de luz altamente sensíveis chamados tubos fotomultiplicadores (PMT's). Os detectores devem ser capazes de medir os breves lampejos de luz emitida a partir de células ou partículas que se movem uma de cada vez através do campo visual da lente objetiva em taxas de até vários milhares por segundo.
A maior parte dos citômetros de fluxo pode medir tanto a dispersão de luz quanto fluorescência.
Em certas modalidades preferidas, as esferas são detectadas e/ou classificadas de acordo com os métodos da presente invenção com o uso de citometria de fluxo. A presente invenção, no entanto, não é limitada ao método de citometria de fluxo particular ou aparelho anteriormente descrito. Esse exemplo foi fornecido apenas para objetivos ilustrativos, e a presente invenção não deve ser limitada a um instrumento ou método de acordo com o exemplo fornecido.
Com o uso de citometria de fluxo, o tamanho de uma esfera dado pode ser determinado pela dispersão de luz do objeto.
A dispersão de luz é a interação da luz e matéria. Todos os materiais, incluindo esferas, dispersarão a luz. Ela é composta principalmente de luz que é refletida ou refratada. A posição da qual um objeto é visto freqüentemente determina o que se pode dizer a respeito dele. No citômetro de fluxo, os detectores de dispersão de luz são comumente localizados em oposição ao laser (em relação à célula ou partícula), e a um lado do laser, em linha com a interseção do feixe de fluido-fluxo/laser. As medições feitas por esses detectores são chamadas dispersão de luz direta e dispersão de luz lateral, respectivamente.
A dispersão de luz direta fornece alguma informação sobre o tamanho relativo das células individuais ou partículas, enquanto a dispersão de luz lateral fornece alguma informação sobre a granulação relativa de esferas individuais. Eles são frequentemente usados em combinação para distinguir as diferentes categorias principais de células brancas em sangue de mamífero não separado, mas são úteis em uma ampla variedade de outros ensaios também, como a determinação do tamanho de uma micropartícula.
Os presentes inventores determinaram que a citometria de fluxo é capaz de distinguir entre esferas de cerca de 3,0 μm, cerca de 3,5 μm, cerca de 4,1 μm, cerca de 5,0 μm, cerca de 5,6 μm e cerca de 6,8 μm de diâmetro. Os presentes inventores também determinaram que a citometria de fluxo é capaz de distinguir entre esferas de cerca de 3,0 μm, cerca de 3,5 μm, cerca de 3,7 μm, cerca de 5,0 μm, cerca de 5,6 μm e cerca de 6,8 μm de diâmetro. Ainda outras classes de esferas podem ser distinguidas, como entre 5,0 e 5,6 e 5,6 e 6,8. Portanto, os presentes inventores identificaram que a citometria de fluxo pode diferenciar até pelo menos 6 diferentes tamanhos de esferas.
Em adição à detecção de tamanho, os citômetros de fluxo tipicamente têm um ou mais lasers e detectores para a detecção de fluorescência em uma amostra. A fluorescências é a propriedade de uma molécula de absorver luz de um comprimento de onda em particular e re-emitir luz de um comprimento de onda mais longo. A mudança do comprimento de onda está relacionada a uma perda de energia que ocorre no processo. Ela é uma característica que torna a fluorescência extremamente útil: podem ser usados filtros para excluir a luz de excitação do detector de luz ou do observador. Assim, a única luz medida ou observada se origina do fluoróforo. Interferência de segundo plano ou reflexão difusa evidente nos detectores é extremamente baixa.
Há vários corantes fluorescentes que são úteis para citometria de fluxo. Eles se ligam a vários componentes citoquímicos, como ácidos nucleicos; proteínas; receptores de membrana específicos para célula, nucleares, e citoplasmáticos; moléculas de íon intracelular; e vários outros. Uma propriedade chave de um corante fluorescente que determina seu potencial para uso em um ensaio de citometria de fluxo é o comprimento de onda de excitação, ou seja, ele deve combinar com os comprimentos de onda disponíveis da fonte de luz.
Em outros aspectos, a presente invenção fornece métodos para o diagnóstico de uma infecção por um analito patogênico em um indivíduo, o referido método compreende: (i) a obtenção de uma amostra biológica do ser humano que compreende supostamente o referido analito patogênico; (ii) isolação de ácido nucleico a partir da referida amostra; (iii) amplificação do ácido nucleico a partir da referida amostra com o uso de iniciadores que geram um amplicon que é distinto para o referido analito ou uma cepa particular do referido analito; (iv) opcionalmente amplificação de uma seqüência de ácidos nucleicos de controle do indivíduo; (v) opcionalmente efetuar a rotulagem do amplicon(s) citada nas etapas (iii) e/ou (iv); (vi) hibridizar o amplicon(s) rotulado a um conjunto de esferas de reagentes em que cada membro dos conjuntos de esferas compreende uma molécula de ácido nucleico que tem complementaridade a uma seqüência de nucleotídeos do analito ou uma cepa particular do analito ou uma seqüência de nucleotídeos de controle, ligada ou associada a uma esfera fisiologicamente distinguível; e (vii) determiner a qual reagente um amplicon foi ligado; em que a associação de um amplicon com um reagente particular é indicativa de infecção pelo analito no indivíduo.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos 91/106 sinalizadora.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos de bloqueio.
Como aqui usado o termo “indivíduo” refere-se a qualquer organismo que possa ser suscetível à infecção por outro analito. Assim, um “indivíduo” inclui, sem limitação, animais, plantas, fungos e bactérias (que podem ser infectados por bacteriófago). Como aqui usado o termo “animal” inclui preferivelmente um mamífero e mais preferivelmente um primata que inclui um primata inferior e ainda mais preferivelmente, um humano. no entanto, o termo “animal” também inclui especificamente espécies como gado bovino, cavalos, carneiros, porcos, cabras e mulas bem como animais de laboratório. Exemplos de animais de laboratório de teste incluem camundongos, ratos, coelhos, porquinhos da Índia e hamsters. Coelhos e roedores, como ratos e camundongos, fornecem um sistema de teste conveniente ou modelo animal assim como primatas e primatas inferiores. Animais não mamíferos como espécies de ave, peixe zebra, anfíbios (incluindo sapos) e espécies de Drosophila como Drosophila melanogastersão também contemplados.
O “indivíduo” também pode ser um não animal como uma planta. O termo “planta” inclui especificamente plantas de valor agrícola como plantas de cereal (por exemplo, trigo, cevada, aveia, centeio, triticale e milho), arroz, árvores frutíferas (por exemplo, maçãs, bananas, mangas e laranjas), cana de açúcar, plantas de safra horticultural (por exemplo, batatas, cenouras e cebolas) e outras.
No entanto, em certas modalidades preferidas, a presente invenção fornece métodos para o diagnóstico de infecção por HPV em um ser humano, o referido método compreende: (i) a obtenção de uma amostra biológica do ser humano que compreende supostamente HPV; (ii) isolação de ácido nucleico a partir da referida amostra; (iii) amplificação do ácido nucleico a partir da referida amostra com o uso de iniciadores que geram um amplicon que é distinto do referido analito ou uma cepa particular do referido analito; (iv) opcionalmente amplificação de uma seqüência de ácidos nucleicos de controle do DNA genômico do ser humano; (v) opcionalmente efetuar a rotulagem do amplicon(s) citada nas etapas (iii) e/ou (iv); (vi) hibridizar o amplicon(s) rotulado a um conjunto de esferas de reagentes em que cada membro dos conjuntos de esferas compreende uma molécula de ácido nucleico que tem complementaridade a uma seqüência de nucleotídeos de HPV ou uma cepa de HPV particular ou uma seqüência de nucleotídeos de controle, ligada ou associada a um substrato fisiologicamente distinguível; e (vii) determinar a qual reagente um amplicon foi ligado; em que a associação de um amplicon com um reagente particular é indicativa de infecção por HPV no ser humano.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos sinalizadora.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos de bloqueio.
Em alguns aspectos, a presente invenção também contempla métodos para a determinação do risco de um ser humano desenvolver uma doença associada a uma ou mais cepas de HPV o referido método compreende: (i) a obtenção de uma amostra biológica do ser humano que compreende supostamente HPV; (ii) isolação de ácido nucleico a partir da referida amostra; (iii) amplificação do ácido nucleico a partir da referida amostra com o uso de iniciadores que geram um amplicon que é distinto do referido analito ou uma cepa particular do referido analito; (iv) opcionalmente amplificação de uma seqüência de ácidos nucleicos de controle do DNA genômico do ser humano; (v) opcionalmente efetuar a rotulagem do amplicon(s) citada nas etapas (iii) e/ou (iv); (vi) hibridizar o amplicon(s) rotulado a um conjunto de esferas de reagentes em que cada membro dos conjuntos de esferas compreende uma molécula de ácido nucleico que tem complementaridade a uma seqüência de nucleotídeos de HPV ou uma cepa de HPV particular ou uma seqüência de nucleotídeos de controle, ligada ou associada a um substrato fisiologicamente distinguível; e (vii) determinar a qual reagente um amplicon foi ligado; em que a associação de um amplicon com um reagente particular que compreende um polinucleotídeo que é complementar a uma cepa de HPV associada a uma doença particular, é indicativa de um risco aumentado da referida doença no ser humano.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos sinalizadora.
Em outros aspectos, a hibridização ocorre na presença de pelo menos uma seqüência de oligonucleotídeos de bloqueio.
Quando a rotulagem dos amplicons como apontado na parte (v) ocorre, tanto os amplicons quanto as esferas são rotuladas.
Exemplos de doenças associadas a uma ou mais cepas particulares de HPV incluem aquelas apresentadas na Tabela 3. Portanto, em alguns aspectos, a presente invenção fornece métodos para o diagnóstico de um risco aumentado de um indivíduo desenvolver uma doença particular por identificação especificamente de qual cepa de HPV infecta o indivíduo. Em certas modalidades particularmente preferidas, os métodos são adaptados para a determinação do risco de um ser humano desenvolver câncer cervical.
A presente invenção também contempla kits diagnósticos para uso de acordo com os métodos aqui descritos, que incluem o diagnóstico de infecção por HPV em um ser humano e/ou avaliação do risco de um ser humano de desenvolver uma doença associada ao HPV, que inclui câncer cervical. Os kits compreendem um conjunto de esferas de reagentes que compreende cada, um polinucleotídeo que é complementar a uma seqüência de nucleotídeos de uma cepa particular de HPV, ligado ou associado a um substrato fisiologicamente distinguível. Opcionalmente, os kits também podem compreender iniciadores que se ligam a seqüências conservadas entre diferentes cepas de HPV, mas geram um amplicon que compreende seqüências de nucleotídeos distintas para cada cepa de HPV em que o amplicon gerado é supostamente complementar a um polinucleotídeo ligado ou associado com uma ou mais esferas fisiologicamente distinguíveis do kit.
Em algumas modalidade, os conjuntos de esferas dos reagentes compreendem pelo menos um grupo de esferas, cada um compreendendo um diâmetro de qualquer um de cerca de 3,0 μm, cerca de 3,5 μm, cerca de 4,1 μm, cerca de 5,0 μm, cerca de 5,6 μm e cerca de 6,8 μm. Em uma modalidade também preferida, cada grupo de tamanho de esferas compreende um ou mais subgrupos de microesferas cada uma com um rótulo fluorescente em uma escala de diferentes intensidades. O rótulo fluorescente é TMR e pode ser aplicado em intensidades de cerca de 0%, cerca de 4%, cerca de 20% e cerca de 100%.
Em outra modalidade, os conjuntos de esferas de reagentes compreendem pelo menos um grupo de esferas, cada um compreendendo um diâmetro de qualquer um de cerca de 3,0 μm, cerca de 3,5 μm, cerca de 3,7 μm, cerca de 5,0 μm, cerca de 5,4 μm e cerca de 6,8 μm. Os níveis de TMR são ajustados de modo que durante a conjugação da esfera ao oligo, os oligos com proporções totais definidas de oligo para flúor-rotulado são usados para determinar agrupamentos distintos de TMR. Por exemplo, níveis zero de TMR têm oligos não rotulados incluídos em conjugação; altos níveis de TMR têm uma proporção total de 3:1 de oligo para flúor- rotulado de oligos incluídos na conjugação; e níveis médios de TMR têm uma proporção total de 150:1 a 80:1 de oligo para flúor-rotulado de oligos incluídos em conjugação, dependendo do tamanho da esfera.
Em modalidade adicional, os kits compreendem os iniciadores GP5+ e GP6+ e opcionalmente iniciadores MLC1_F e MLC1_R.
Ainda outra modalidade, os kits compreendem os iniciadores GP5d2+ e T7aGP6d+ e opcionalmente iniciadores mlcl_95f e T7amlcl_275r.
Ainda em outra modalidade, os kits compreendem os iniciadores GP5d3+ e T7aGP6d+* e opcionalmente iniciadores mlcl_95f e T7amlcl_275r.
A presente invenção inclui modalidades adicionais de pares de iniciadores em que os iniciadores individuais direto (por exemplo, GP5+, GP5d2+ etc.) e reverso (por exemplo, GP6+, T7aGP6d+) aqui descritos são combinados um com o outro.
Os kits também podem estar na forma de chips ou suportes de fase sólida, comumente referidos como biochips. Todos ou parte dos reagentes usados no atual ensaio podem ser incorporados em um biochip ou miniaturizado em um nanoensaio. Embora a citometria de fluxo seja particularmente útil na medição de resultados do atual ensaio, os biochips podem ser usados para medir ou automatizar outros sinais como aqueles associados a ensaios de modo “whispering gallery”.
Nas obstante as intensidades fluorescentes em um aspecto preferido do método de multiplexação, outras formas de identificação são englobadas pela presente invenção. Um tal método alternativo inclui a detecção de modo “whispering gallery” (WGM). Nessa modalidade, um marcador fluorescente é incorporado nas esferas de um subconjunto ou incorporado ou ligado a DNA na superfície das esferas. Esse marcador fluorescente pode excitar os WGMs com a laser ou fonte de luz branca não focada ou com fonte de luz branca não focada filtrada.
WGMs permitem que apenas certos comprimentos de onda de luz sejam emitidos a partir da partícula. O resultado desse fenômeno é que as bandas de emissão ampla comuns (10100 nm ampla) de, por exemplo, um fluoróforo torna-se restrita e aparece como uma série de picos agudos que correspondem de modo eficaz a padrões de modo de repouso de luz na partícula. De acordo com a presente invenção, foi determinado que o perfil de WGM é extremamente sensível a mudanças na superfície da partícula micro-esferoidal e que o perfil de WGM muda quando a partícula micro-esferoidal interage com analitos ou moléculas em seu ambiente.
Portanto, outros aspectos da presente invenção contemplam métodos de detecção de um analito como um amplicon a partir de uma cepa de HPV que compreende uma seqüência específica para cepa, o referido método compreendendo o contato de pelo menos um conjunto de partículas micro-esferoidais com uma amostra que supostamente compreende o referido analito, em que cada partícula em um conjunto de partículas micro-esferoidais compreende um rótulo opticamente detectável e um parceiro de ligação suposto imobilizado do referido analito (por exemplo, um iniciador ou marcador capaz de ligação, captura ou imobilização de um amplicon a partir de uma cepa de HPV) em que cada conjunto de partícula tem um perfil de WGM definido, em que a ligação do referido analito ao referido parceiro de ligação imobilizado resulta em uma mudança no referido perfil de WGM do referido pelo menos um conjunto de partículas micro-esferoidais que é indicativo da presença do referidos analito.
Os métodos da presente invenção podem ser aplicados para detectar modulação no perfil de WGM de uma partícula micro-esferoidal em que a referida modulação resulta da detecção de ligação ou outra associação de moléculas em uma amostra a potencial ligação de partículas imobilizadas à superfície da partícula micro-esferoidal. A detecção de reações de ligação entre um analito e seu parceiro de ligação com base em mudanças sensíveis nos perfis de WGM permite a identificação e isolação dos analitos.
Uma característica da presente invenção é que as partículas micro-esferoidais podem ser excitadas com uma ampla faixa de fontes de luz, facilitando a medição em vários perfis diferentes de WGM.
Um “rótulo opticamente detectável” pode ser qualquer molécula, átomo ou íon que emita fluorescência, fosforescência e/ou incandescência. Em algumas outras modalidades preferidas da presente invenção, o rótulo opticamente detectável é a fluoróforo, que pode englobar uma faixa de rótulos opticamente detectáveis como fluoróforo químicos e corantes bem como quantum dots.
Em algumas modalidades, a presente invenção fornece pelo menos uma partícula micro-esferoidal que compreende uma partícula de látex ou sílica que tem 1 μm a 100 μm de diâmetro, rotulada com um rótulo opticamente detectável, como um a fluoróforo ou quantum dot, a partícula também compreende um parceiro de ligação suposto de um analito para ser detectado. Um exemplo é uma molécula de ácido nucleico de captura capaz de se ligar a um amplicon de HPV gerado pela amplificação com o uso de dois iniciadores para uma região conservada do genoma de HPV que flanqueia uma região específica para cepa. O rótulo opticamente detectável é detectável em comprimentos de onda visíveis e a partícula micro-esferoidal exibe um ou mais perfis de WGM. Um ou mais dos perfis de WGM da partícula micro- esferoidal modula de modo detectável quando os analitos interagem com o parceiro de ligação imobilizado na partícula. Qualquer mudança no perfil de WGM é indicativa da presença de um analito que se ligou a seu parceiro de ligação.
Oligos de bloqueio podem ser incluídos com as esferas durante a hibridização do amplicon de filamento único às esferas. Os oligos de bloqueio têm pontos deliberados de diferença das regiões de ligação esfera-marcador correspondente dos amplicons de filamento único. Pode haver um oligo de bloqueio para cada esfera-marcador na mistura. Os oligos de bloqueio devem agir como filtros adequadamente fixados. No contexto de uma desnaturação térmica seguida por lenta diminuição na temperatura, os eventos de hibridização mais eficientes ocorrem primeiro. Os amplicons específicos para tipo se ligam à esfera-marcador combinado de acordo com o tipo inicialmente. Os oligos de bloqueio podem se ligar e saturar à esferas-marcadores para abaixo do perfil térmico. Isso pode evitar que ocorram eventos de hibridização tipo cruzada (em que entre os tipos há mais pontos de diferença em regiões de ligação de marcador comparadas com os oligos de bloqueio) ou outras hibridizações não específicas como outros amplicons, incluindo produtos de iniciador-dímero. Um oligo de bloqueio pode estar presente para controle humano bem como os tipos de HPV. Exemplos de oligos de bloqueio são descritos na Tabela 2 acima. O nível de similaridade entre os oligos de bloqueio e a seqüência complementar à região de esfera marcador específica para tipo (para a qual é designada para bloquear) pode ser entre 40% e 95%. Outro exemplo do nível de similaridade é entre 75% e 85%.
Oligos de sinalização podem ser usados como alternativas para o uso de iniciadores de PCR rotulados com flúor diretamente para geração de sinal. Oligos de sinalização são marcadores rotulados com flúor que se liga aos produtos do amplicon em um local diferente da região da esfera-marcador para gerar um complexo esfera- marcador/amplicon/oligo de sinalização após hibridização. As vantagens de seu uso devem ser: excluir a necessidade por iniciador de PCR de rotulagem com flúor (e manuseio excessivo) durante a produção, uso de muito menos oligo rotulado com flúor para sensibilidade equivalente (e benefícios de custo), redução do valor de base de flúor de modo que maior sensibilidade pode ser atingida sem etapas de lavagem (benefícios ao manuseio e risco), sensibilidade aumentada na ausência de oligos de bloqueio devido ao nível extra de aninhamento (“nesting”) no complexo de hibridização, e uso potencial de mais produtos de PCR nas etapas de “detecção”. Todos esses benefícios devem facilitar uma abordagem de “tubo único”. Exemplos de oligos de sinalização são descritos na Tabela 2 acima.
Alternativamente, um corante específico para DNA de filamento duplo, como corante SYBR Verde I pode ser usado como um modo de anexação de sinal ao amplicon na esfera junto ou em vez de oligos de sinal.
A presente invenção é também descrita pelos seguintes exemplos não limitantes.
EXEMPLO 1
Diagnóstico de HPV - isolação e amplificação de DNA
Uma revisão do protocolo de extração de DNA usado para isolar DNA para o método de diagnóstico de HPV é mostrado na Figura 1.
Como mostrado na Figura 2, PCR foi usada para amplificar a amostra de DNA. Os iniciadores GP5d2+ e T7aGP6d+ foram usados para gerar um amplicon para qualquer cepa de HPV que estivesse presente na amostra de DNA. O iniciador T7aGP6d+ compreendia um rótulo fluorescente, especificamente A647 para permitir posterior visualização da ligação do amplicon aos agentes de ligação. Os amplicons virais gerados compreendiam ambas regiões conservadas (Y) que são conservadas entre todas as cepas de HPV examinadas e uma região que é variável (ou seja, específicas para cepa) entre cepas de HPV, Xn, em que n representa uma região variável associada a cada cepa de HPV. Os parceiros de ligação imobilizados em esferas se ligam especificamente a um genoma específico para cepa de HPV.
Além disso, um amplicon do DNA genômico humano foi também gerado com o uso dos iniciadores mlc1_95f and T7amlcl_275r para servir como um controle. Nesse caso, o iniciador T7amlcl_275r também carregava um rótulo de A647.
EXEMPLO 2
Diagnóstico de HPV — Detecção Multiplex
Os amplicons gerados nos Exemplo 1 foram hibridizados a um arranjo de agentes de ligação, cada um carregando um polinucleotídeo que é complementar à região variável do amplicon viral suposto gerado a partir de cada cepa de HPV 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 67 e 68 (X1 até X16). Veja a Tabela 2 para as seqüências de nucleotídeos dos ácidos nucleicos de captura imobilizada às esferas. Além disso, o arranjo pode compreender opcionalmente um agente de ligação que compreende um polinucleotídeo que é complementar à região conservada dos amplicons virais de HPV (Y). Finalmente, um agente de ligação que compreende um polinucleotídeo que é complementar à seqüência do amplicon de controle humano é incluído. O ácido nucleico de captura pode ser DNA ou RNA. Se for usado RNA, uma transcriptase reversa pode ser necessária para gerar RNA a partir do amplicon de DNA.
Cada um dos agentes de ligação no arranjo compreende uma microesfera ou esfera com um tamanho distinto e intensidade de rótulo fluorescente (TMR) distinto. As esferas que compreendem diâmetros de 3,0 μm, 3,5 μm, 3,77 μm, 5,0 μm, 5,6 μm e 6,8 μm pode ser diferenciados um do outro com o uso de citometria de fluxo, como mostrado na Figura 4.
Para cada tamanho dado de microesfera, um rótulo fluorescente (TMR) foi incorporado em intensidades relativas de 0%, aproximadamente 150-80;1 (média), e aproximadamente 3:1 (alta). Essas intensidades de rótulo podem ser claramente distintas co o uso de citometria de fluxo.
EXEMPLO 3
Comparação do método de detecção Multiplex com diagnóstico de HPV tradicional
A Tabela 5, abaixo, fornece uma revisão que compara o método de detecção de HPV Multiplex da presente invenção com o método histológico atual para diagnóstico de HPV.
Análise eletroforética com gel de agarose de produtos de PCR após amplificação a partir de plasmídeo que contém inserção específico para tipo de HPV com o uso de várias combinações de iniciadores.
Cinco microlitros de cada produto foram carregados nas linhas que contêm 5 microlitros de “HyperladderIV DNA ladder’. As reações foram copiadas com 4.0000 cópias de plasmídeo específico para tipo (os números nas linhas indicam o tipo) e submetidas a 40 ciclos de amplificação com o uso de uma temperatura de anelamento de 44°C. Um “x” nas linhas indica reações não analisadas devido à perda evaporativa durante PCR. Um “-“ nas linhas indica nenhum controle de modelo. 200 ou 100 cópias de plasmídeos específicos para tipo junto com 10 ng de DNA genômico humano de Jurkat foram usados para copiar PCRs com o emprego de GBHPVf3+ e GBHPVr1 multiplexado com MLC1_95f e T7aMLC1_275r. Quarenta e oito ciclos de amplificação foram realizados com o uso de uma temperatura de anelamento de 44°C. A análise foi realizada por citometria de fluxo depois de digestão com lambda exonuclease e hibridização às esferas marcadores PapType. Nenhum controle de modelo gerou resultados negativos em todos os tipos. Todos os tipos testados: 6, 11, 16, 18, 31, 45, 51, 52, 56, 58, 59, 66 e 68 geraram resultados positivos com o uso de 200 cópias de plasmídeos específicos para tipo. Todos os tipos acima exceto tipos 51 e 59 geraram resultados positivos que usam 100 cópias de plasmídeos específicos para tipo, indicando um sistema muito sensível e relativamente imparcial.
Quando são aqui usadas faixas para propriedades físicas, como temperatura ou número de nucleotídeos em uma seqüência, todas as combinações e subcombinações de faixas e modalidades específicas nessas estão incluídas.
Aqueles habilitados na técnica perceberão que a invenção aqui descrita é suscetível a variações e modificações diferentes daquelas especificamente descritas. Deve-se compreender que a invenção inclui todas essas variações e modificações. A invenção também inclui todas as etapas, características, composições e compostos referidos ou indicados nessa especificação, individualmente ou coletivamente, e quaisquer e todas combinações de qualquer uma ou mais das referidas etapas ou características.
BIBLIOGRAFIA
Bonner and Laskey, Eur. J. Biochem. 46:83, 1974 Chadwick e cols., J. Virol. Methods 70:59-70, 1998 Chan and Fox, Rev. Med. Microbiol. 10:185-196, 1999 Compton, Nature 350:91-92, 1991 Demidov and Broude (Eds.), “DNA Amplification: Current Technologies and Applications”, Horizon Bioscience, 2004 Gearhart e cols., www.emedicine.com/MED/topic1037.htm, 2004 Guatelli e cols., Proc. Natl Acad. Sci. USA 87:1874-1878, 1990 Hill, J. Clin. Ligand Assay 19:43-51, 1996 Kievits e cols., J. Virol. Methods 35:273-286, 1991 Kuske e cols., Appl. Environ. Microbiol. 64(7):2463- 2472, 1998 Lizardi e cols., Biotechnology 6:1197-1202, 1988 Lyamichev e cols., Nat. Biotechnol. 17:292-296, 1999 Marmur and Doty, J. Mol. Biol. 5:109, 1962 Nelson and Krawetz, Anal. Biochem. 207(1):97-201, 1992 Pawlotsky e cols., J. Virol. Methods 79:227-235, 1999 Ryan e cols., Mol. Diagn. 4:135-144, 1999 Speel, Histochem. Cell Biol. 112:89-113, 1999 5 Todd e cols., J. AIDS Hum. Retrovirol. 10:S35—S44, 1995