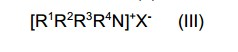BRPI0708613B1 - Uso de compostos de amônio quaternário, e composição farmacêutica - Google Patents
Uso de compostos de amônio quaternário, e composição farmacêutica Download PDFInfo
- Publication number
- BRPI0708613B1 BRPI0708613B1 BRPI0708613-0A BRPI0708613A BRPI0708613B1 BR PI0708613 B1 BRPI0708613 B1 BR PI0708613B1 BR PI0708613 A BRPI0708613 A BR PI0708613A BR PI0708613 B1 BRPI0708613 B1 BR PI0708613B1
- Authority
- BR
- Brazil
- Prior art keywords
- acid
- chloride
- pradofloxacin
- quaternary ammonium
- pharmaceutical composition
- Prior art date
Links
- 150000003856 quaternary ammonium compounds Chemical class 0.000 title claims abstract description 16
- 239000008194 pharmaceutical composition Substances 0.000 title claims 6
- 238000001556 precipitation Methods 0.000 claims abstract description 10
- LZLXHGFNOWILIY-APPDUMDISA-N pradofloxacin Chemical compound C12=C(C#N)C(N3C[C@H]4NCCC[C@H]4C3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 LZLXHGFNOWILIY-APPDUMDISA-N 0.000 claims description 24
- 229960001248 pradofloxacin Drugs 0.000 claims description 24
- 229960000686 benzalkonium chloride Drugs 0.000 claims description 19
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 claims description 19
- 239000002253 acid Substances 0.000 claims description 11
- 229940027983 antiseptic and disinfectant quaternary ammonium compound Drugs 0.000 claims description 10
- UREZNYTWGJKWBI-UHFFFAOYSA-M benzethonium chloride Chemical compound [Cl-].C1=CC(C(C)(C)CC(C)(C)C)=CC=C1OCCOCC[N+](C)(C)CC1=CC=CC=C1 UREZNYTWGJKWBI-UHFFFAOYSA-M 0.000 claims description 9
- 229960001950 benzethonium chloride Drugs 0.000 claims description 7
- 229910001425 magnesium ion Inorganic materials 0.000 claims description 5
- JLVVSXFLKOJNIY-UHFFFAOYSA-N Magnesium ion Chemical compound [Mg+2] JLVVSXFLKOJNIY-UHFFFAOYSA-N 0.000 claims description 4
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 claims description 4
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 claims description 4
- 150000001768 cations Chemical class 0.000 claims description 3
- 229910052751 metal Inorganic materials 0.000 claims description 3
- 239000002184 metal Substances 0.000 claims description 3
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 claims description 2
- 239000002260 anti-inflammatory agent Substances 0.000 claims description 2
- IVUMCTKHWDRRMH-UHFFFAOYSA-N carprofen Chemical compound C1=CC(Cl)=C[C]2C3=CC=C(C(C(O)=O)C)C=C3N=C21 IVUMCTKHWDRRMH-UHFFFAOYSA-N 0.000 claims description 2
- 229960003184 carprofen Drugs 0.000 claims description 2
- 229940120889 dipyrone Drugs 0.000 claims description 2
- NOOCSNJCXJYGPE-UHFFFAOYSA-N flunixin Chemical compound C1=CC=C(C(F)(F)F)C(C)=C1NC1=NC=CC=C1C(O)=O NOOCSNJCXJYGPE-UHFFFAOYSA-N 0.000 claims description 2
- 229960000588 flunixin Drugs 0.000 claims description 2
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 claims description 2
- 229960000991 ketoprofen Drugs 0.000 claims description 2
- 229960001929 meloxicam Drugs 0.000 claims description 2
- LVWZTYCIRDMTEY-UHFFFAOYSA-N metamizole Chemical compound O=C1C(N(CS(O)(=O)=O)C)=C(C)N(C)N1C1=CC=CC=C1 LVWZTYCIRDMTEY-UHFFFAOYSA-N 0.000 claims description 2
- 230000003637 steroidlike Effects 0.000 claims description 2
- 230000000202 analgesic effect Effects 0.000 claims 2
- 125000000218 acetic acid group Chemical group C(C)(=O)* 0.000 claims 1
- 229940124307 fluoroquinolone Drugs 0.000 abstract description 31
- 239000003814 drug Substances 0.000 abstract description 14
- 229940079593 drug Drugs 0.000 abstract description 8
- -1 for example Chemical class 0.000 description 33
- 241001465754 Metazoa Species 0.000 description 29
- 239000000243 solution Substances 0.000 description 26
- 239000002904 solvent Substances 0.000 description 24
- 239000000203 mixture Substances 0.000 description 22
- 238000009472 formulation Methods 0.000 description 20
- 238000002347 injection Methods 0.000 description 20
- 239000007924 injection Substances 0.000 description 20
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 20
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 18
- 239000000126 substance Substances 0.000 description 18
- 239000001257 hydrogen Substances 0.000 description 17
- 229910052739 hydrogen Inorganic materials 0.000 description 17
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 17
- 150000003839 salts Chemical class 0.000 description 17
- 230000015572 biosynthetic process Effects 0.000 description 16
- 238000005755 formation reaction Methods 0.000 description 15
- 229940050906 magnesium chloride hexahydrate Drugs 0.000 description 14
- DHRRIBDTHFBPNG-UHFFFAOYSA-L magnesium dichloride hexahydrate Chemical compound O.O.O.O.O.O.[Mg+2].[Cl-].[Cl-] DHRRIBDTHFBPNG-UHFFFAOYSA-L 0.000 description 14
- 239000002245 particle Substances 0.000 description 14
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 12
- 150000004684 trihydrates Chemical class 0.000 description 12
- 241000282326 Felis catus Species 0.000 description 10
- 241000282472 Canis lupus familiaris Species 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 150000007660 quinolones Chemical class 0.000 description 9
- 210000002966 serum Anatomy 0.000 description 9
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 8
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 8
- 239000013543 active substance Substances 0.000 description 7
- 229910021645 metal ion Inorganic materials 0.000 description 7
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 6
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- 150000001875 compounds Chemical class 0.000 description 6
- 150000004677 hydrates Chemical class 0.000 description 6
- 239000012669 liquid formulation Substances 0.000 description 6
- 229920001223 polyethylene glycol Polymers 0.000 description 6
- 239000003755 preservative agent Substances 0.000 description 6
- SPFYMRJSYKOXGV-UHFFFAOYSA-N Baytril Chemical compound C1CN(CC)CCN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1CC1 SPFYMRJSYKOXGV-UHFFFAOYSA-N 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 5
- 239000002202 Polyethylene glycol Substances 0.000 description 5
- 125000004432 carbon atom Chemical group C* 0.000 description 5
- 229910052736 halogen Inorganic materials 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 4
- PMNLUUOXGOOLSP-UHFFFAOYSA-N 2-mercaptopropanoic acid Chemical compound CC(S)C(O)=O PMNLUUOXGOOLSP-UHFFFAOYSA-N 0.000 description 4
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- 241000283690 Bos taurus Species 0.000 description 4
- 241000700198 Cavia Species 0.000 description 4
- 241000699670 Mus sp. Species 0.000 description 4
- 241000282887 Suidae Species 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 244000309466 calf Species 0.000 description 4
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 229960000740 enrofloxacin Drugs 0.000 description 4
- LZCLXQDLBQLTDK-UHFFFAOYSA-N ethyl 2-hydroxypropanoate Chemical compound CCOC(=O)C(C)O LZCLXQDLBQLTDK-UHFFFAOYSA-N 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 150000002367 halogens Chemical group 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- 239000004310 lactic acid Substances 0.000 description 4
- 235000014655 lactic acid Nutrition 0.000 description 4
- 230000007935 neutral effect Effects 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical class CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 3
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 3
- 241000283086 Equidae Species 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 3
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 3
- 241000700159 Rattus Species 0.000 description 3
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 150000001298 alcohols Chemical class 0.000 description 3
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 239000002585 base Chemical class 0.000 description 3
- 229910001424 calcium ion Inorganic materials 0.000 description 3
- YMKDRGPMQRFJGP-UHFFFAOYSA-M cetylpyridinium chloride Chemical compound [Cl-].CCCCCCCCCCCCCCCC[N+]1=CC=CC=C1 YMKDRGPMQRFJGP-UHFFFAOYSA-M 0.000 description 3
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 235000011187 glycerol Nutrition 0.000 description 3
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 229940091250 magnesium supplement Drugs 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 229920001983 poloxamer Polymers 0.000 description 3
- 230000008961 swelling Effects 0.000 description 3
- 235000002906 tartaric acid Nutrition 0.000 description 3
- 239000011975 tartaric acid Substances 0.000 description 3
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 2
- CTPDSKVQLSDPLC-UHFFFAOYSA-N 2-(oxolan-2-ylmethoxy)ethanol Chemical compound OCCOCC1CCCO1 CTPDSKVQLSDPLC-UHFFFAOYSA-N 0.000 description 2
- VTDOEFXTVHCAAM-UHFFFAOYSA-N 4-methylpent-3-ene-1,2,3-triol Chemical compound CC(C)=C(O)C(O)CO VTDOEFXTVHCAAM-UHFFFAOYSA-N 0.000 description 2
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 2
- 241000251468 Actinopterygii Species 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- 241000272517 Anseriformes Species 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 2
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- LZZYPRNAOMGNLH-UHFFFAOYSA-M Cetrimonium bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](C)(C)C LZZYPRNAOMGNLH-UHFFFAOYSA-M 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 229920000858 Cyclodextrin Polymers 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- 201000004624 Dermatitis Diseases 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 241000287828 Gallus gallus Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical class Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 2
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- 241000286209 Phasianidae Species 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical class OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 229930003427 Vitamin E Natural products 0.000 description 2
- 150000005840 aryl radicals Chemical group 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 235000019445 benzyl alcohol Nutrition 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 238000009395 breeding Methods 0.000 description 2
- 230000001488 breeding effect Effects 0.000 description 2
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 2
- 210000002421 cell wall Anatomy 0.000 description 2
- 229960001927 cetylpyridinium chloride Drugs 0.000 description 2
- 235000013330 chicken meat Nutrition 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 229960003405 ciprofloxacin Drugs 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- CVSVTCORWBXHQV-UHFFFAOYSA-N creatine Chemical compound NC(=[NH2+])N(C)CC([O-])=O CVSVTCORWBXHQV-UHFFFAOYSA-N 0.000 description 2
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 2
- UFULAYFCSOUIOV-UHFFFAOYSA-O cysteaminium Chemical compound [NH3+]CCS UFULAYFCSOUIOV-UHFFFAOYSA-O 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- 229960002433 cysteine Drugs 0.000 description 2
- 239000000645 desinfectant Substances 0.000 description 2
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 229940093499 ethyl acetate Drugs 0.000 description 2
- 229940116333 ethyl lactate Drugs 0.000 description 2
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- MNQZXJOMYWMBOU-UHFFFAOYSA-N glyceraldehyde Chemical compound OCC(O)C=O MNQZXJOMYWMBOU-UHFFFAOYSA-N 0.000 description 2
- 239000001087 glyceryl triacetate Substances 0.000 description 2
- 235000013773 glyceryl triacetate Nutrition 0.000 description 2
- 229940102223 injectable solution Drugs 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 239000000787 lecithin Substances 0.000 description 2
- 235000010445 lecithin Nutrition 0.000 description 2
- 229960003376 levofloxacin Drugs 0.000 description 2
- 244000144972 livestock Species 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 229960003151 mercaptamine Drugs 0.000 description 2
- 229960001699 ofloxacin Drugs 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 2
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000010254 subcutaneous injection Methods 0.000 description 2
- 239000007929 subcutaneous injection Substances 0.000 description 2
- CWERGRDVMFNCDR-UHFFFAOYSA-N thioglycolic acid Chemical compound OC(=O)CS CWERGRDVMFNCDR-UHFFFAOYSA-N 0.000 description 2
- 229960002622 triacetin Drugs 0.000 description 2
- 235000019165 vitamin E Nutrition 0.000 description 2
- 239000011709 vitamin E Substances 0.000 description 2
- 229940046009 vitamin E Drugs 0.000 description 2
- 239000008215 water for injection Substances 0.000 description 2
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- 125000006702 (C1-C18) alkyl group Chemical group 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 1
- QKDHBVNJCZBTMR-LLVKDONJSA-N (R)-temafloxacin Chemical compound C1CN[C@H](C)CN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1F QKDHBVNJCZBTMR-LLVKDONJSA-N 0.000 description 1
- FZTHHIGKHFQAKY-UHFFFAOYSA-N 1-octanoyloxypropan-2-yl decanoate Chemical compound CCCCCCCCCC(=O)OC(C)COC(=O)CCCCCCC FZTHHIGKHFQAKY-UHFFFAOYSA-N 0.000 description 1
- 125000004215 2,4-difluorophenyl group Chemical group [H]C1=C([H])C(*)=C(F)C([H])=C1F 0.000 description 1
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 1
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- SFPKVQYQVWWFKE-UHFFFAOYSA-N 4,5-dihydro-1,3-thiazol-3-ium iodide Chemical compound [I-].C1C[NH+]=CS1 SFPKVQYQVWWFKE-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- XBHBWNFJWIASRO-UHFFFAOYSA-N 6-fluoro-1-(4-fluorophenyl)-4-oxo-7-(1-piperazinyl)-3-quinolinecarboxylic acid Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1=CC=C(F)C=C1 XBHBWNFJWIASRO-UHFFFAOYSA-N 0.000 description 1
- UBGCCYGMLOBJOJ-UHFFFAOYSA-N 7-(1,4-diazabicyclo[3.2.2]nonan-4-yl)-1-ethyl-6-fluoro-4-oxoquinoline-3-carboxylic acid Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN2CCC1CC2 UBGCCYGMLOBJOJ-UHFFFAOYSA-N 0.000 description 1
- WUWFMDMBOJLQIV-UHFFFAOYSA-N 7-(3-aminopyrrolidin-1-yl)-1-(2,4-difluorophenyl)-6-fluoro-4-oxo-1,4-dihydro-1,8-naphthyridine-3-carboxylic acid Chemical compound C1C(N)CCN1C(C(=C1)F)=NC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1F WUWFMDMBOJLQIV-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 241000030939 Bubalus bubalis Species 0.000 description 1
- 241000282832 Camelidae Species 0.000 description 1
- 229930186147 Cephalosporin Natural products 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 241000700114 Chinchillidae Species 0.000 description 1
- 241000272201 Columbiformes Species 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 241000938605 Crocodylia Species 0.000 description 1
- CKLJMWTZIZZHCS-UHFFFAOYSA-N D-OH-Asp Natural products OC(=O)C(N)CC(O)=O CKLJMWTZIZZHCS-UHFFFAOYSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- SNPLKNRPJHDVJA-ZETCQYMHSA-N D-panthenol Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCCO SNPLKNRPJHDVJA-ZETCQYMHSA-N 0.000 description 1
- 239000011703 D-panthenol Substances 0.000 description 1
- 235000004866 D-panthenol Nutrition 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- RUPBZQFQVRMKDG-UHFFFAOYSA-M Didecyldimethylammonium chloride Chemical compound [Cl-].CCCCCCCCCC[N+](C)(C)CCCCCCCCCC RUPBZQFQVRMKDG-UHFFFAOYSA-M 0.000 description 1
- RPWFJAMTCNSJKK-UHFFFAOYSA-N Dodecyl gallate Chemical compound CCCCCCCCCCCCOC(=O)C1=CC(O)=C(O)C(O)=C1 RPWFJAMTCNSJKK-UHFFFAOYSA-N 0.000 description 1
- 241001331845 Equus asinus x caballus Species 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- DSLZVSRJTYRBFB-UHFFFAOYSA-N Galactaric acid Natural products OC(=O)C(O)C(O)C(O)C(O)C(O)=O DSLZVSRJTYRBFB-UHFFFAOYSA-N 0.000 description 1
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 1
- 101000693916 Gallus gallus Albumin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical class NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- LEVWYRKDKASIDU-IMJSIDKUSA-N L-cystine Chemical compound [O-]C(=O)[C@@H]([NH3+])CSSC[C@H]([NH3+])C([O-])=O LEVWYRKDKASIDU-IMJSIDKUSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- BPFYOAJNDMUVBL-UHFFFAOYSA-N LSM-5799 Chemical compound C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN3N(C)COC1=C32 BPFYOAJNDMUVBL-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241000699673 Mesocricetus auratus Species 0.000 description 1
- 241000282339 Mustela Species 0.000 description 1
- KWIUHFFTVRNATP-UHFFFAOYSA-O N,N,N-trimethylglycinium Chemical group C[N+](C)(C)CC(O)=O KWIUHFFTVRNATP-UHFFFAOYSA-O 0.000 description 1
- QIPQASLPWJVQMH-DTORHVGOSA-N Orbifloxacin Chemical compound C1[C@@H](C)N[C@@H](C)CN1C1=C(F)C(F)=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1F QIPQASLPWJVQMH-DTORHVGOSA-N 0.000 description 1
- 241000282941 Rangifer tarandus Species 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-N Sulfurous acid Chemical compound OS(O)=O LSNNMFCWUKXFEE-UHFFFAOYSA-N 0.000 description 1
- AOBORMOPSGHCAX-UHFFFAOYSA-N Tocophersolan Chemical compound OCCOC(=O)CCC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C AOBORMOPSGHCAX-UHFFFAOYSA-N 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- XAKBSHICSHRJCL-UHFFFAOYSA-N [CH2]C(=O)C1=CC=CC=C1 Chemical group [CH2]C(=O)C1=CC=CC=C1 XAKBSHICSHRJCL-UHFFFAOYSA-N 0.000 description 1
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 125000001539 acetonyl group Chemical group [H]C([H])([H])C(=O)C([H])([H])* 0.000 description 1
- 229960004308 acetylcysteine Drugs 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- IAJILQKETJEXLJ-RSJOWCBRSA-N aldehydo-D-galacturonic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-RSJOWCBRSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000008051 alkyl sulfates Chemical class 0.000 description 1
- 229940045714 alkyl sulfonate alkylating agent Drugs 0.000 description 1
- 150000008052 alkyl sulfonates Chemical class 0.000 description 1
- 239000004411 aluminium Substances 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- MDFFNEOEWAXZRQ-UHFFFAOYSA-N aminyl Chemical group [NH2] MDFFNEOEWAXZRQ-UHFFFAOYSA-N 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960001574 benzoxonium chloride Drugs 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 229950011614 binfloxacin Drugs 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 235000021466 carotenoid Nutrition 0.000 description 1
- 150000001747 carotenoids Chemical class 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 229940124587 cephalosporin Drugs 0.000 description 1
- 150000001780 cephalosporins Chemical class 0.000 description 1
- 229960000800 cetrimonium bromide Drugs 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 229960004621 cinoxacin Drugs 0.000 description 1
- VDUWPHTZYNWKRN-UHFFFAOYSA-N cinoxacin Chemical compound C1=C2N(CC)N=C(C(O)=O)C(=O)C2=CC2=C1OCO2 VDUWPHTZYNWKRN-UHFFFAOYSA-N 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 229960003624 creatine Drugs 0.000 description 1
- 239000006046 creatine Substances 0.000 description 1
- 229940109239 creatinine Drugs 0.000 description 1
- 150000001896 cresols Chemical class 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 229960003067 cystine Drugs 0.000 description 1
- 229960003949 dexpanthenol Drugs 0.000 description 1
- NOCJXYPHIIZEHN-UHFFFAOYSA-N difloxacin Chemical compound C1CN(C)CCN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1 NOCJXYPHIIZEHN-UHFFFAOYSA-N 0.000 description 1
- 229950001733 difloxacin Drugs 0.000 description 1
- 229960001760 dimethyl sulfoxide Drugs 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- WBZKQQHYRPRKNJ-UHFFFAOYSA-L disulfite Chemical compound [O-]S(=O)S([O-])(=O)=O WBZKQQHYRPRKNJ-UHFFFAOYSA-L 0.000 description 1
- 239000000555 dodecyl gallate Substances 0.000 description 1
- 235000010386 dodecyl gallate Nutrition 0.000 description 1
- 229940080643 dodecyl gallate Drugs 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- IDYZIJYBMGIQMJ-UHFFFAOYSA-N enoxacin Chemical compound N1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 IDYZIJYBMGIQMJ-UHFFFAOYSA-N 0.000 description 1
- 229960002549 enoxacin Drugs 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- XBJBPGROQZJDOJ-UHFFFAOYSA-N fleroxacin Chemical compound C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN(CCF)C2=C1F XBJBPGROQZJDOJ-UHFFFAOYSA-N 0.000 description 1
- 229960003306 fleroxacin Drugs 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- DSLZVSRJTYRBFB-DUHBMQHGSA-N galactaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O DSLZVSRJTYRBFB-DUHBMQHGSA-N 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229930182478 glucoside Natural products 0.000 description 1
- 150000008131 glucosides Chemical class 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 210000005256 gram-negative cell Anatomy 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 150000004820 halides Chemical group 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- DXKRGNXUIRKXNR-UHFFFAOYSA-N ibafloxacin Chemical compound C1CC(C)N2C=C(C(O)=O)C(=O)C3=C2C1=C(C)C(F)=C3 DXKRGNXUIRKXNR-UHFFFAOYSA-N 0.000 description 1
- 229950007954 ibafloxacin Drugs 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N iron oxide Inorganic materials [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 1
- 235000013980 iron oxide Nutrition 0.000 description 1
- VBMVTYDPPZVILR-UHFFFAOYSA-N iron(2+);oxygen(2-) Chemical class [O-2].[Fe+2] VBMVTYDPPZVILR-UHFFFAOYSA-N 0.000 description 1
- 239000002085 irritant Substances 0.000 description 1
- 231100000021 irritant Toxicity 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 229960002531 marbofloxacin Drugs 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229940057917 medium chain triglycerides Drugs 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 229960004452 methionine Drugs 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 1
- MHWLWQUZZRMNGJ-UHFFFAOYSA-N nalidixic acid Chemical compound C1=C(C)N=C2N(CC)C=C(C(O)=O)C(=O)C2=C1 MHWLWQUZZRMNGJ-UHFFFAOYSA-N 0.000 description 1
- 229960000210 nalidixic acid Drugs 0.000 description 1
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- NRPKURNSADTHLJ-UHFFFAOYSA-N octyl gallate Chemical group CCCCCCCCOC(=O)C1=CC(O)=C(O)C(O)=C1 NRPKURNSADTHLJ-UHFFFAOYSA-N 0.000 description 1
- 239000000574 octyl gallate Substances 0.000 description 1
- 235000010387 octyl gallate Nutrition 0.000 description 1
- 229960004780 orbifloxacin Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000003867 organic ammonium compounds Chemical class 0.000 description 1
- 150000002892 organic cations Chemical class 0.000 description 1
- 125000003431 oxalo group Chemical group 0.000 description 1
- 238000002559 palpation Methods 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 229960004236 pefloxacin Drugs 0.000 description 1
- FHFYDNQZQSQIAI-UHFFFAOYSA-N pefloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 FHFYDNQZQSQIAI-UHFFFAOYSA-N 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 229920001987 poloxamine Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- PXGPLTODNUVGFL-JZFBHDEDSA-N prostaglandin F2beta Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)C[C@@H](O)[C@@H]1C\C=C/CCCC(O)=O PXGPLTODNUVGFL-JZFBHDEDSA-N 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 239000003542 rubefacient Substances 0.000 description 1
- 229950007734 sarafloxacin Drugs 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 150000003378 silver Chemical class 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 229960005480 sodium caprylate Drugs 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- SRRKNRDXURUMPP-UHFFFAOYSA-N sodium disulfide Chemical compound [Na+].[Na+].[S-][S-] SRRKNRDXURUMPP-UHFFFAOYSA-N 0.000 description 1
- BYKRNSHANADUFY-UHFFFAOYSA-M sodium octanoate Chemical compound [Na+].CCCCCCCC([O-])=O BYKRNSHANADUFY-UHFFFAOYSA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 229960004954 sparfloxacin Drugs 0.000 description 1
- DZZWHBIBMUVIIW-DTORHVGOSA-N sparfloxacin Chemical compound C1[C@@H](C)N[C@@H](C)CN1C1=C(F)C(N)=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1F DZZWHBIBMUVIIW-DTORHVGOSA-N 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L sulfate group Chemical group S(=O)(=O)([O-])[O-] QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 150000004763 sulfides Chemical class 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-L sulfite Chemical class [O-]S([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-L 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229960004576 temafloxacin Drugs 0.000 description 1
- UEUXEKPTXMALOB-UHFFFAOYSA-J tetrasodium;2-[2-[bis(carboxylatomethyl)amino]ethyl-(carboxylatomethyl)amino]acetate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]C(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O UEUXEKPTXMALOB-UHFFFAOYSA-J 0.000 description 1
- CBDKQYKMCICBOF-UHFFFAOYSA-N thiazoline Chemical compound C1CN=CS1 CBDKQYKMCICBOF-UHFFFAOYSA-N 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 229940035024 thioglycerol Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 235000019149 tocopherols Nutrition 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 229950008187 tosufloxacin Drugs 0.000 description 1
- JATLJHBAMQKRDH-UHFFFAOYSA-N vebufloxacin Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)CCC3=C1N1CCN(C)CC1 JATLJHBAMQKRDH-UHFFFAOYSA-N 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 150000003712 vitamin E derivatives Chemical class 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
- QUEDXNHFTDJVIY-UHFFFAOYSA-N γ-tocopherol Chemical class OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1 QUEDXNHFTDJVIY-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/186—Quaternary ammonium compounds, e.g. benzalkonium chloride or cetrimide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/472—Non-condensed isoquinolines, e.g. papaverine
- A61K31/4725—Non-condensed isoquinolines, e.g. papaverine containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Dermatology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
medicamento contendo fluoroquinolona. a presente invenção refere-se ao uso de compostos de amônio quaternário para impedir precipitações de fluoroquinolonas de suas soluções, bem como medicamentos toleráveis, estáveis, especialmente adequados para a aplicação parenteral, que em forma dissolvida contêm uma fluoroquinolona e um composto de amônio quaternário.
Description
[001] A presente invenção se refere ao uso de compostos de amônio quaternários para impedir precipitações de fluorquinolonas de suas soluções, bem como medicamentos toleráveis, estáveis, especialmente adequados para a aplicação parenteral, que em forma dissolvidacontêm uma fluorquinolona e um composto de amônio quaternário.
[002] Há uma extensa pesquisa científica no campo da solubili- zação de fluorquinolonas de ação antibiótica. Dessa maneira, na DE- OS-3 831 514 são descritas soluções com quinolonas através da aplicação de íons de metais, especialmente através de íons de cálcio. Uma melhor solubilidade de quinolonas é descrita também na JP 02264724, bem como por M. Nakano, M. Yamamoto, T. Arita em Chem. Pharm. Bull, Interactions of Aluminium, Magnesium and Calcium ions with Nalidixic acid, 26 (5) 1505-1510 (1978) através do uso de íons de metais, especialmente de íons de magnésio. Na EP-A 507 851 são descritos complexos de quinolonas com íons de metais bem como ácido; nesses complexos a solubilidade das quinolonas deve ser melhor. A melhor solubilidade de uma fluorquinolona através da adição de íons de metais, bem como co-solventes está fundamentada na US 5,811,130. A tolerância desses complexos é apresentada em vitelas. Complexos de quinolonas com íons de metais e especialmente com íons de magnésio também são descritos no WO 99/29322, pelo que deve ser obtida uma melhor solubilidade das quinolonas. Os complexos aqui descritos são descritos como sendo bem-toleráveis e estáveis ao armazenamento, sendo que a tolerância foi pesquisada em vitelas e ratos.
[003] Soluções para fins farmacêuticos devem ser livres de preci- pitações. Nas soluções, que são determinadas para a aplicação parenteral, isso é particularmente importante e também precipitações em pequena escala, designadas como formação de partículas, não são aceitáveis. Isso vale para toda a durabilidade de um produto farmaceu- ticamente utilizado. Por isso, há muitas publicações em relação ao tema do impedimento de formação de partículas, respectivamente, pre-cipitação de medicamentos das soluções. Por exemplo, o WO 98/18492 descreve o impedimento de formações de partículas em soluções com cefalosporinas através do uso de fosfolipídios.
[004] A EP-A 287 026 descreve um processo de purificação deta lhado especialmente para a síntese de fluorquinolonas, para que não ocorra formação de partículas na produção de soluções (injetáveis).
[005] Do mesmo modo, o WO 01/10408 descreve que para a produção de soluções injetáveis de uma fluorquinolona, devem ser usadas substâncias de aplicação com uma fração particularmente pequena de impurezas devido aos íons de metais, para assegurar que as soluções continuem livres de partículas.
[006] A liofilização de soluções representa, por exemplo, uma al ternativatambém freqüentemente selecionada para o problema da formação de partículas.
[007] De modo geral, sabe-se que substâncias tensoativas não são bem-toleráveis na administração parenteral. Isso é atribuído, entre outros, à afinidade das substâncias tensoativas em relação aos componentes das paredes celulares. Por isso, as substâncias tensoativas com uma afinidade particularmente pronunciada em relação às paredes celulares são usadas, entre outras, também como desinfetantes ou como conservantes. Isso vale também para conservantes do grupo dos compostos de amônio quaternário, tal como, por exemplo, cloreto de benzalcônio.
[008] Do mesmo modo, sabe-se de modo geral que o grupo dos compostos de amônio quaternário são irritantes da pele e da mucosa. Dessa maneira, K.H. Wallhauser (em Praxis der Sterilisation, Desin- fektion-Konservierung, Thieme Verlag, 1995, 5a edição, página 586598) descreve o efeito rubefaciente do cloreto de benzalcônio na pele de coelho sadio; também é descrita a formação de dermatites em camundongos (J. Amer. Ver. Med. Ass., 1972, 161 (6), 652-655. Dermatitis and death in mice accidentially exposed to quaternary ammonium disinfectants). Em J. Gen. Microbiol., 1967, 48 (3), 391-400 ("Effects of organic cations on the gram-negative cell wall and their bactericidal activity with EDTA and surface active agents") é apresentado o mecanismo do efeito de compostos de amônio quaternário, sendo explicitamente descrita a interação com as membranas celulares e o aumento daí resultante da permeabilidade para outras substâncias.
[009] Na verdade, a melhora da solubilidade de fluorquinolonas através da adição de íons de metais, tais como, por exemplo, de íons de magnésio ou íons de cálcio, em princípio, é descrita na literatura. Contudo, em alguns casos, as soluções de fluorquinolona, ao serem armazenadas, apresentam as precipitações conhecidas na forma de formações de partículas. Isso ocorre também com o uso de substâncias geralmente comuns para impedir precipitações ou cristalizações. Dessa maneira, por exemplo, a formação de partículas em soluções de pradofloxacina não é impedida através da aplicação de co- solventes descritos na US 5,811,130 ou também através de formulações contendo ácido, tais como descritas na EP-A 507 851.
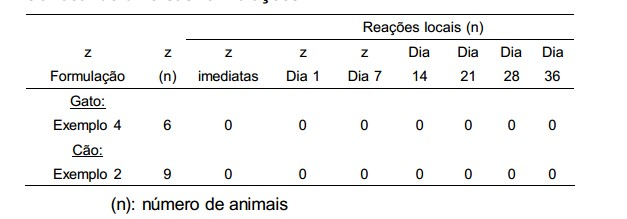
[0010] Além disso, formulações de fluorquinolonas não são bem- toleráveis do mesmo modo nas diversas espécies animais, de maneira que não se pode partir de uma tolerância, que foi determinada em vitelas, para uma tolerância, por exemplo, em porcos ou cães ou mesmo gatos. Isso vale também para o caso inverso; soluções injetáveis, que são toleráveis por cães, não são obrigatoriamente toleráveis por gatos ou vitelas.
[0011] Diferentemente do campo dos animais domésticos (por exemplo, bovinos), além dos resultados locais objetivos, a avaliação da tolerância local de soluções injetáveis em animais de recreação (por exemplo, cães ou gatos) é mais crítica. Dessa maneira, a aceitação dos proprietários de animais em relação às leves intolerâncias locais (por exemplo, intumescimentos, algesia) no campo dos animais de recreação, é nitidamente inferior ao campo dos animais domésticos.Além disso, particularmente as variantes de criação a serem atingidas no campo dos animais de recreação, reagem muitas vezes de maneira mais sensível às injeções subcutâneas comparadas com os animais domésticos. Aqui mencionam-se particularmente os gatos como espécie animal muito sensível. Por conseguinte, também não é supreendente que a maioria das soluções injetáveis com fluorquinolo- nas, entre outras, com base nas tolerâncias deficientes, não estão à disposição de cães ou gatos.
[0012] Para formular a tolerância da melhor maneira possível, re comenda-se manter o pH das soluções o mais neutro possível (cerca de 7,4), mas o que contraria a solubilidade das fluorquinolonas, visto que geralmente essas têm uma solubilidade particularmente baixa na escala de pH neutro. Isso vale especialmente para sistemas aquosos preferivelmente empregados nas quinolonas, sendo que, devido à má solubilidade das quinolonas com pH em torno do ponto neutro, recorre- se a aditivos, tais como co-solventes. Na escala de pH neutro observa- se com freqüência uma formação de partículas da forma betaína das fluorquinolonas, razão pela qual soluções, quando já deveriam ser toleráveis, freqüentemente não são armazenáveis por muito tempo e ocorre a formação de partículas. Na prática, por exemplo, isso é con-tornado pelo fato de se desviar de produtos liofilizados. Mas o manuseio desses produtos liofilizados é complicado e a solução reconsti- tuinte apresenta, via de regra, uma curta durabilidade (por exemplo, de 4 semanas) após a reconstituição ou deve ser diretamente rejeitada devido a possível formação de partículas. Portanto, tais produtos têm claras desvantagens em relação a uma solução injetável pronta, dire-tamenteaplicável.
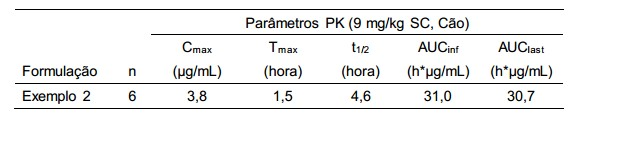
[0013] Por conseguinte, uma solução pronta para o uso é vantajo sa como solução injetável, também designada como "formulação ready to use". Além disso, é necessário que após a aplicação, tal como também descrito no WO 99/29322, a fluorquinolona converta-se no soro na quantidade correspondente. Isso também não é evidente com formulações injetáveis de fluorquinolonas e do mesmo modo pode depender das respectivas espécies animais.
[0014] Foi encontrada uma possibilidade de manter fluorquinolo- nas com substâncias aditivas farmaceuticamente aceitáveis em solução. Dessa maneira, é possível preparar formulações com fluorquino- lonas diretamente aplicáveis (ready to use), que após aplicação parenteral em diversas espécies animais, são localmente bem-toleráveis, que são estáveis em condições de armazenamento farmacêuticas, bem como são livres de formação de partículas e que apresentam um perfil cinético de soro vantajoso.
[0015] A invenção se refere:
[0016] ao uso de compostos de amônio quaternário para impedir precipitações de fluorquinolonas de suas soluções.
[0017] Além disso, a invenção se refere:
[0018] a um medicamento contendo em forma dissolvida: (a) uma fluorquinolona eventualmente na forma de um sal farmaceuticamente utilizável e (b) um composto de amônio quaternário.
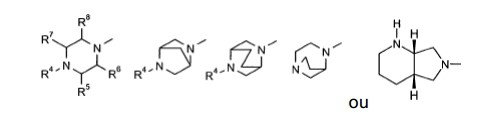
[0019] Fluorquinolonas são compostos, tais como são publicadas, entre outras, nos seguintes documentos: US 4,670,444 (Bayer AG), US 4,472,405 (Riker Labs), US 4,730,000 (Abbott), US 4,861,779 (Pfizer), US 4,382,892 (Daiichi), US 4,704,459 (Toyama), como exemplos concretos sejam mencionados: benofloxacina, binfloxacina, cinoxaci- na, ciprofloxacina, danofloxacina, difloxacina, enoxacina, enrofloxaci- na, fleroxacina, ibafloxacina, levofloxacina, lomefloxacina, marbofloxa- cina, moxifloxacina, norfloxacina, ofloxacina, orbifloxacina, pefloxacina, temafloxacina, tosufloxacina, sarafloxacina, sparfloxacina.
[0021] na qual
[0022] X representa hidrogênio, halogênio, C1-4-alquila, C1-4- alcóxi, NH2,
[0024] sendo que
[0025] R4 representa C1-4-alquila em cadeia linear ou ramificada eventualmente substituída por hidróxi ou metóxi, ciclopropila, acila com 1 a 3 átomos de carbono,
[0026] R5 representa hidrogênio, metila, fenila, tienila ou piridila,
[0027] R6 representa hidrogênio ou C1-4-alquila,
[0028] R7 representa hidrogênio ou C1-4-alquila,
[0029] R8 representa hidrogênio ou C1-4-alquila,
[0030] bem como
[0031] R1 representa um radical alquila com 1 a 3 átomos de car bono, ciclopropila, 2-fluoroetila, metóxi, 4-fluorofenila, 2,4-difluorofenila ou metilamino,
[0032] R2 representa hidrogênio ou alquila com 1 a 6 átomos de carbono eventualmente substituída por metóxi ou 2-metoxietóxi, bem como ciclohexila, benzila, 2-oxopropila, fenacila, etoxicarbonilmetila, pivaloiloximetila,
[0033] R3 representa hidrogênio, metila ou etila e
[0034] A representa nitrogênio, =CH-, =C(halogênio)-, =C(OCH3)-, =C (CH3)- ou =C(CN),
[0035] B representa oxigênio, =NH ou =CH2 eventualmente substi tuída por metila ou fenila,
[0036] Z representa =CH- ou =N-
[0037] e seus sais e hidratos farmaceuticamente utilizáveis.
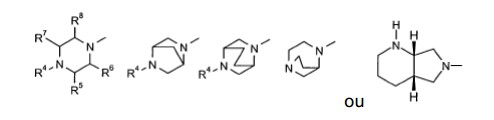
[0038] São preferidos compostos da Fórmula (I),
[0039] na qual
[0040] A representa =CH- ou =C-CN,
[0041] R1 representa C1-C3-alquila eventualmente substituída por halogênio ou ciclopropila,
[0042] R2 representa hidrogênio ou C1-4-alquila,
[0044] sendo que
[0045] R4 representa C1-C3-alquila em cadeia linear ou ramificada eventualmente substituída por hidróxi, oxalila com 1 a 4 átomos de carbono,
[0046] R5 representa hidrogênio, metila ou fenila,
[0047] R6 representa hidrogênio ou metila,
[0048] R7 representa hidrogênio ou metila,
[0049] R8 representa hidrogênio ou metila,
[0050] e seus hidratos e sais farmaceuticamente utilizáveis.
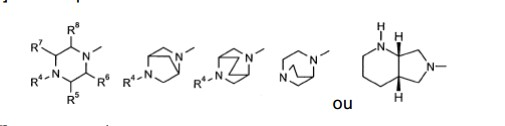
[0051] Particularmente, são preferidos compostos da Fórmula (I),
[0052] em que
[0053] A representa =CH- ou =C-CN,
[0054] R1 representa ciclopropila,
[0055] R2 representa hidrogênio, metila ou etila,
[0057] nas quais
[0058] R4 representa metila, etila eventualmente substituída por hidróxi,
[0059] R5 representa hidrogênio ou metila,
[0060] R6 representa hidrogênio,
[0061] R7 representa hidrogênio ou metila,
[0062] R8 representa hidrogênio,
[0063] e seus sais e hidratos farmaceuticamente utilizáveis.
[0064] Como exemplo preferido de uma fluorquinolona da Fórmula (II) seja mencionada a marbofloxacina:
[0065] Como fluorquinolonas particularmente preferidas sejam mencionados os compostos descritos no WO 97/31001, especialmente ácido 8-ciano-1-ciclopropil-7-((1S,6S)-2,8-diazabiciclo[4.3.0]nonan-8- il)-6-flúor-1,4-dihidro-4-oxo-3-quinolinocarboxílico (pradofloxacina) com a Fórmula
[0066] Além disso, a enrofloxacina é usada de modo particular mente preferido:
[0067] ácido 1-ciclopropil-7-(4-etil-1-piperazinil)-6-flúor-1,4-dihidro- 4-oxo -3-quinolinocarboxílico
[0068] Do mesmo modo, é concebível o uso da substância ativa ciprofloxacina usada, ademais, na medicina humana.
[0069] As fluorquinolonas podem estar presentes na forma de seus racematos ou em formas enantioméricas. Tanto os enantiômeros puros, como também suas misturas podem ser usados de acordo com a invenção.
[0070] Como sais tomam-se em consideração os sais de adição de ácidos farmaceuticamente utilizáveis e sais básicos.
[0071] Como sais farmaceuticamente utilizáveis entendem-se, por exemplo, os sais do ácido clorídrico, ácido sulfúrico, ácido acético, áci-doglicólico, ácido lático, ácido succínico, ácido cítrico, ácido tartárico, ácido metanossulfônico, ácido 4-toluenossulfônico, ácido galacturôni- co, ácido glucônico, ácido embônico, ácido glutamínico ou ácido aspa- ragínico. Além disso, os compostos de acordo com a invenção podem ser ligados aos trocadores de íons ácidos ou básicos. Como sais básicos farmaceuticamente utilizáveis sejam mencionados, por exemplo, os sais de metais alcalinos, por exemplo, os sais de sódio ou potássio, os sais de metais alcalino-terrosos, por exemplo, os sais de magnésio ou cálcio; os sais de zinco, os sais de prata e os sais de guanidínio.
[0072] Por hidratos entendem-se tanto os hidratos das próprias fluorquinolonas, como também os hidratos de seus sais. Como exemplo seja mencionada a pradofloxacina, que forma um trihidrato estável (vide o WO 2005/097789).
[0073] Sob determinadas circunstâncias, as fluorquinolonas po dem formar, como sólido, diversas modificações cristalinas. Modificações vantajosas para os medicamentos da presente invenção são aquelas que têm propriedades de solubilidade correspondentes.
[0074] Nos medicamentos de acordo com a invenção, a fluorquino- lona para animais com um peso corporal de até aproximadamente 80 kg é tipicamente usada em uma proporção de 0,1 até 15 %, preferivelmente 0,5 até 15 % e de modo particularmente preferido, com 1 até 15 %. No caso de animais com um peso corporal a partir de aproximadamente 80 kg, a fluorquinolona é tipicamente usada em uma proporção de 1 até 30 %, preferivelmente 3 até 25 % e de modo particularmente preferido, com 4 até 20 %. Aqui e a seguir - desde que não indicado de outro modo - entende-se por dados de porcentagem, porcento (M/V). Isso significa: massa da respectiva substância em grama para 100 mL de solução pronta.
[0075] Os medicamentos de acordo com a invenção podem conter outras substâncias ativas adequadas, tais como, por exemplo, analgésicos, especialmente NSAID’s (substâncias não esteroidais, antiinfla- matórias). Tais NSAID’s podem ser, por exemplo: meloxicam, flunixina, cetoprofeno, carprofeno, metamizol ou ácido (acetil)-salicílico.
[0076] Compostos de amônio quaternário no sentido desta inven ção são compostos de amônio usualmente orgânicos, que apresentam substituintes apolares e que podem ter diversos contraíons, tais como, por exemplo, cloreto, brometo, iodeto ou fluoreto. Preferivelmente, esses são compostos da Fórmula Geral (II):
[0077] na qual
[0078] R1 a R4 são iguais ou diferentes e representam C1-18- alquila, que pode ser eventualmente interrompida uma ou mais vezes por oxigênio e pode ser eventualmente substituída com hidroxila ou com um radical arila eventualmente substituído com um ou mais átomos de halogênio ou radicais C1-8-alquila ou
[0079] R1 a R4 através de ciclização de três radicais formam radi cais heterocíclicos com 5 ou 6 membros, tais como, por exemplo, piri- dina ou tiazolina, que por seu lado são eventualmente substituídos uma ou mais vezes com C1-4-alquila ou C1-4-alquenila, que portam eventualmente um radical arila, que por seu lado, pode ser substituído com halogênio, especialmente cloro, amino ou dimetilamino e
[0080] X representa sulfato, halogeneto, especialmente cloreto, brometo ou iodeto ou um contra-íon semelhante.
[0081] Pelo menos um dos radicais R1 a R4 apresenta preferivel mente um comprimento de cadeia de 8 a 18, de modo particularmente preferido, 12 a 16 átomos de carbono.
[0082] Arila representa preferivelmente um radical fenila, que é eventualmente substituído com 1 ou 2 radicais selecionados de halo- gênio, especialmente cloro e C1-8-alquila.
[0083] São exemplos os cloretos de alquil-dimetil-benzilamônio, especialmente cloreto de benzalcônio [cloreto de (C8-18)-alquil-dimetil- benzil-amônio] ou cloreto de n-(C12-C18)-alquil-benzildimetilamônio com pesos moleculares médios de cerca de 380, cloreto de benzetônio (cloreto de diisobutil-fenoxietoxietil-dimetilbenzil-amônio), cloreto de diclorobenzil-dimetil-alquil-amônio, cloreto de benzoxônio (cloreto de benzil-dodecil-bis-(2-hidroxietil)-amônio, brometo de cetrimônio, brometo de (N-hexadecil-N,N-trimetil-amônio, cloreto de di-(C8-C18)- alquil-dimetil-amônio, tal como, por exemplo, cloreto de dioctil-dimetil- amônio ou cloreto de di-n-decil-dimetil-amônio, cloreto de cetilpiridínio (cloreto de 1-hexadecil-piridínio) bem como iodeto de tiazolínio (iodeto de 3-heptil-2-(3-heptil-4-metil-4-tiazolin-2-iliden-metil)-4-metil- tiazolínio). Desses, preferem-se particularmente o cloreto de benzetô- nio e cloreto de benzalcônio.
[0084] Os compostos de amônio quaternário são usualmente apli cados em concentrações de 0,001 até 10 %, preferivelmente de 0,005 até 6 % e de modo particularmente preferido, de 0,005 até 3 %. Os dados de porcentagem significam % (M/V).
[0085] Os medicamentos de acordo com a invenção podem conter outras substâncias adicionalmente aos compostos de amônio quaternário, que podem impedir a formação de partículas; por exemplo, po- loxâmeros, lecitinas, polivinilpirrolidonas, co-solventes, antioxidantes ou formadores de complexos. Também esses são usualmente aplicados em concentrações de 0,001 até 20 %, preferivelmente de 0,01 até 10 % e de modo particularmente preferido, de 0,05 até 3 %. Os dados de porcentagem significam % (M/V).
[0086] As formulações líquidas podem conter substâncias, que melhoram a tolerância local da aplicação. Como exemplos sejam men-cionados: captadores de radicais ou antioxidantes, tais como, por exemplo, vitamina E, ésteres de vitamina E hidrossolúveis ou vitamina C, butilhidroxianisol, butilhidroxitolueno, cisteamina, cisteína, glutation, tioglicol, ácido tiolático, dissulfeto de sódio ou também acetilcisteína. Formadores de complexos, tais como, por exemplo, ciclodextrinas (por exemplo, hidroxipropil-ciclodextrina), sódio-EDTA (ácido etilenodiami- notetraacético), polivinilpirrolidona, dexpantenol, sais de ácidos graxos, tais como, por exemplo, caprilato de sódio, sais de cátions de metais polivalentes (por exemplo, Me2+ ou Me3+), especialmente os metais alcalino-terrosos e aqui especialmente o magnésio e sua forma de sal, aminoácidos e entre estes, particularmente, arginina ou lisina, poloxâ- meros, poloxaminas, co-solventes, tais como, por exemplo, n-butanol, glicerina, polietilenoglicol, propilenoglicol ou dimetilacetamida, dextra- nos, creatina, creatinina, ácidos, tais como, por exemplo, o ácido glu- conolactônico, ácido lático, ácido embônico, ácido cítrico, ácido tartári- co, ácido múcico ou ácido hialurônico, lecitinas com um teor de fosfati- dilcolina de 70-100 % de soja ou albumina de galinha. Das substâncias mencionadas acima, aplicam-se preferivelmente os sais de cátions de metais polivalentes e, na verdade, preferivelmente os sais de metais alcalino-terrosos, especialmente sais de magnésio.
[0087] Substâncias, que melhoram a tolerância, são usualmente aplicadas em concentrações de 0,05 até 10 %, preferivelmente com 0,1 até 8 % e de modo particularmente preferido, com 0,5 até 5 %. Os dados de porcentagem significam % (M/V).
[0088] Como solventes, a formulação líquida pode conter água ou substâncias hidromiscíveis. Como exemplos são mencionados: glicerina, propilenoglicol, polietilenoglicol, álcoois toleráveis bem como eta- nol, álcool benzílico ou n-butanol, lactato de etila, acetato de etila, triacetina, N-metil-pirrolidona, propileno carbonato, glicofurol, dimetilace- tamida, 2-pirrolidona, isopropilideno glicerol, glicerinformal. Combinações dos solventes são também imagináveis. formulações preferidas à base de água, são contidas nesses outros solventes ou co-solventes naturais.
[0089] Como solventes, a formulação líquida, além de água ou substâncias hidromiscíveis, também pode conter óleos em forma de uma emulsão. Entre esses, sejam mencionados óleos vegetais, animais e sintéticos, tais como óleo de semente de algodão, óleo de sésamo,óleo de soja, triglicerídeos de cadeia média com um comprimento de cadeia de C12-C18, decanoato de propilenoglicoloctanoato ou também parafina.
[0090] O solvente está usualmente contido em concentrações de até 98,5 %, preferivelmente de até 97 %, de modo particularmente preferido, de até 96,5 %. Via de regra, as concentrações do solvente encontram-se acima de 50 %, preferivelmente acima de 60 %, de modo particularmente preferido, acima de 70 %. Os dados de porcentagem significam % (M/V).
[0091] As formulações de acordo com a invenção também podem conter co-solventes e, na verdade, preferivelmente, quando as formulações contêm água; os co-solventes podem melhorar a solubilidade de certos componentes da formulação. Os co-solventes são usualmente aplicados em proporções de 1 a 10 %, preferivelmente de 3 a 8 % (em cada caso os dados de porcentagem são M/V). Como co- solventes sejam mencionados, por exemplo: álcoois farmaceuticamen- te toleráveis, dimetilsulfóxido, etillactato, acetato de etila, triacetina, N- metilpirrolidona, propilenocarbonato, propilenoglicol, glicofurol, dimeti- lacetamida, 2-pirrolidona, isopropilidenoglicerol, glicerinformal, glicerina e polietilenoglicóis. Como co-solventes prestam-se especialmente álcoois farmaceuticamente toleráveis, tais como, por exemplo, etanol, álcool benzílico ou n-butanol. Misturas dos solventes mencionados acima também podem ser aplicados como co-solventes.
[0092] Conservantes podem estar contidos nas formulações líqui das. Os compostos de amônio quaternário mencionados acima têm, via de regra, efeito conservante, por exemplo, cloreto de benzalcônio, cloreto de benzetônio ou cloreto de cetilpiridínio. Como exemplos de outros conservantes utilizáveis sejam mencionados: álcoois alifático, tais como álcool benzílico, etanol, n-butanol, fenol, cresóis, clorobuta- nol, éster de ácido para-hidroxibenzóico (especialmente os ésteres metílico e propílico), sais ou os ácidos livres dos ácidos carboxílicos, tais como ácido sórbico, ácido benzóico, ácido lático ou ácido propiô- nico.
[0093] Dependendo do tipo de formulação e forma de aplicação, os medicamentos de acordo com a invenção, podem conter outros aditivos e coadjuvantes farmaceuticamente toleráveis. Como exemplos mencionam-se: • antioxidantes, tais como, por exemplo, sulfitos (sulfito de Na, metabissulfito de Na), sulfetos orgânicos (cistina, cisteína, cistea- mina, metionina, tioglicerol, ácido tioglicólico, ácido tiolático), fenóis (tocoferóis, tais como também vitamina E e vitamina E-TPGS (d-alfa- tocoferilpolietilenoglicol-1000-succinato)), butilhidroxianisol, butilhidro- xitolueno, octil- e dodecilgalato), ácidos orgânicos (ácido ascórbico, ácido cítrico, ácido tartárico, ácido lático) e seus sais e ésteres. • Umectantes, tais como, por exemplo, sais de ácido gra- xo, alquilsulfatos graxos, alquilsulfonatos graxos, alquilbenzenossulfo- natos lineares, sulfatos de éter alquilpolietilenoglicólico graxo, éter al- quilpolietilenoglicólico graxo, éter alquilfenolpolietilenoglicólico, alquil- poliglicosídeos, N-metilglucamidas de ácido graxo, polissorbatos, éster de ácido sorbitanograxo e poloxâmeros. • Substâncias para a isotonização, tais como, por exemplo, cloreto de sódio, glicose ou glicerina. • Corantes farmaceuticamente aceitáveis, tais como, por exemplo, óxidos de ferro, carotenóides e outros.
[0094] O pH das formulações líquidas importa em 2-11, preferi velmente 3-8 e de modo particularmente preferido, 4-7,6.
[0095] Os medicamentos de acordo com a invenção podem ser fabricados, em que a fluorquinolona é dispersa no solvente, as substâncias para melhorar a tolerância e eventualmente para impedir a formação de partículas são igualmente complementadas. Co- solventes, tais como outras substâncias constitutivas, tais como, por exemplo, conservantes, já podem ser acrescentados ao solvente ou misturados mais tarde.
[0096] Alternativamente, os co-solventes, conservantes, substân cias que influenciam na tolerância ou formação de partículas também podem ser inicialmente dissolvidos no solvente e em seguida, complementados primeiro à fluorquinolona.
[0097] As preparações farmacêuticas de acordo com a invenção, prestam-se geralmente para a aplicação no ser humano e animal. Pre-ferivelmente, elas são aplicadas na zootecnia e pecuária em animais domésticos, animais de criação, de zoológico, de laboratório, cobaias e de recreação.
[0098] Nos animais domésticos e pecuária incluem-se mamíferos, tais como, por exemplo, bovinos, eqüinos, ovinos, porcinos, caprinos, camelos, búfalos de água, muares, coelhos, caça, renas, animais que fornecem pele, tais como, por exemplo, martas, chinchilas, urso lavadeiro, bem como pássaros, tais como, por exemplo, codorniz, galinhas, gansos, perus, patos, pombos e espécies de pássaros para a criação doméstica ou zoológica.
[0099] Nos animais de laboratório e cobaias incluem-se camun dongos, ratos, porquinhos-da-Índia, hamster dourado, coelhos, macacos, cães e gatos.
[00100] Nos animais de recreação incluem-se coelhos, hamster, ratos, porquinhos-da-Índia, camundongos, cavalos, répteis, espécies de pássaros correspondentes, cães e gatos.
[00101] Além disso, sejam mencionados peixes e, na verdade, pei-xesdomésticos, de criação, de aquário e ornamentais de todos os es- tágios de idade, que vivem em água doce ou salgada.
[00102] Preferivelmente, as preparações de acordo com a invenção são usadas em animais de recreação, tais como cavalos, coelhos, gatos e cães. Elas são especialmente adequadas para a aplicação em gatos e cães.
[00103] Exemplos de animais domésticos preferidos são bovinos, ovinos, porcinos, caprinos, peru e galinha. Animais domésticos particularmente preferidos são bovinos e porco.
[00104] A aplicação pode ser efetuada tanto profilaticamente, meta- filaticamente, como também terapeuticamente.
[00105] Preferivelmente, as formulações líquidas de acordo com a invenção são administradas como soluções ou emulsão, as soluções homogêneas são particularmente preferidas.
[00106] As formulações aqui descritas podem ser administradas ao organismo-alvo (ser humano ou animal) de diferentes maneiras. Elas podem ser aplicadas, por exemplo, via parenteral, especialmente através de injeção (por exemplo, subcutânea, intramuscular, intravenosa, intramamária, intraperitonial), dérmica, oral, retal, vaginal ou nasal, sendo preferida a aplicação parenteral - especialmente através de injeção.
[00107] O uso com as substâncias mencionadas leva a medicamentos com boa solubilidade da substância ativa e boa estabilidade da formulação, especialmente em relação às precipitações. Além disso, o medicamento de acordo com a invenção destaca-se por boa tolerância e cinética de soro adequada nas diversas espécies animais mencionadas, especialmente após administração parenteral.
[00108] As formulações dos seguintes exemplos são preparadas, em que as substâncias de aplicação são misturadas ou dissolvidas em água por injeção. O valor de pH das soluções pode ser ajustado atra- vés da adição de ácidos ou bases. As soluções para a injeção são fil-tradasestéreis e transferidas para recipientes adequados. Pradofloxa- cina pode ser usado como anidrato ou como trihidrato; os valores numéricos são calculados em cada caso para o anidrato.
[00109] (Dados de porcentagem em % em peso, em relação ao volume total do preparado pronto [M/V]). EXEMPLO 1 1 % de enrofloxacina 3,0 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio quantum satis hidróxido de potássio ad 100 % de água por injeção.
[00110] 0,5 g de enrofloxacina, 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de potássio. EXEMPLO 2 3,0 % de pradofloxacina (trihidrato) 3,0 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio quantum satis hidróxido de sódio ad 100 % de água por injeção
[00111] 1,5 g de pradofloxacina (calculado como pradofloxacina pu ra, usada como trihidrato), 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 3 1,5 % de pradofloxacina 3 % de hexahidrato de cloreto de magnésio 0,01 % de cloreto de benzetônio ad 100 % de água por injeção.
[00112] 0,75 g de pradofloxacina, 1,5 g de hexahidrato de cloreto de magnésio e 0,005 g de cloreto de benzetônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 4 1,5 % de pradofloxacina (trihidrato) 3 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio ad 100 % de água por injeção
[00113] 0,75 g de pradofloxacina (calculado como pradofloxacina pura, usada como trihidrato), 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 5 5 % de pradofloxacina (trihidrato) 0,02 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de água por injeção
[00114] 80 g de água por injeção são misturados com 0,02 g de clo reto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 5 g de pradofloxacina (calculado como prado- floxacina pura; usado como trihidrato). Com a água por injeção restante ajusta-se para o peso final para 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio. EXEMPLO 6 1,5 % de pradofloxacina (trihidrato) 0,015 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de água por injeção
[00115] 80 g de água por injeção são misturados com 0,015 g de cloreto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 1,5 g de pradofloxacina (calculado como pra- dofloxacina pura; usado como trihidrato). Com a água por injeção restante completa-se para o peso final de 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio. EXEMPLO 7 1,5 % de pradofloxacina (trihidrato) 0,01 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de Aqua pro injection
[00116] 80 g de Aqua pro injection são misturados com 0,01 g de cloreto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 1,5 g de pradofloxacina (calculado como pra- dofloxacina pura; usado como trihidrato). Com a Aqua pro injection restante completa-se para o peso final de 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio.
[00117] No ensaio clínico, as formulações aqui descritas demonstraram um melhor tolerância local em relação a outras formulações. Irritações de tecidos e intumescimentos causados pela substância ativa no local da injeção manifestam-se de acordo com as formulações usadas. Exemplos para esse fim são relacionados na seguinte tabela.
[00118] O sistema de teste aplicado consiste em uma prova combinada de tolerância local inicial e durante 36 dias e farmacocinética do soro de 0 - 72 horas. Cada formulação é testada em 6 animais cada das duas espécies cão e gato após injeção subcutânea única. As amostras de soro (n = 11/animal) são testadas para sua concentração de substância por meio de HPLC e dessas são calculados os parâme-trosfarmacocinéticos. A tolerância local é avaliada com base nos parâmetros intumescimento, algesia, rubefação e irritação/modificação da pele e avaliada por apalpação. TABELA 1. Resultados selecionados do teste clínico para tolerância local de diversas formulações
[00119] Além das diversas tolerâncias, a formulação tem também uma influência sobre o perfil farmacocinético do soro (PK). Diversas formulações apresentam nítidas diferenças na curva do tempo da concentração de soro. Para as quinolonas, preferem-se curvas com rápida absorção, altas concentrações de pico e fases de eliminação lentas. A tabela abaixo mostra o perfil PK de uma formulação de acordo com a invenção. O sistema de teste usado foi descrito no parágrafo "tolerância local". TABELA 2. Resultados da farmacocinética do soro
Claims (6)
1. Uso de compostos de amônio quaternário selecionado do grupo consistindo em cloreto de benzalcônio [cloreto de (C8-18-alquil- dimetil-benzil-amônio] e cloreto de benzetônio (cloreto de diisobutilfenoxietoxietil-dimetilbenzil-amônio) o referido uso sendo caracterizado pelo fato de que é para prevenção de precipitações de pradofloxacina de soluções das mesmas, em que a pradofloxacina está presente em uma quantidade de 1 a 30% (p/v).
2. Composição farmacêutica, caracterizada pelo fato de que contém, em forma dissolvida: (a) pradofloxacina, e (b) um composto de amônio quaternário selecionado do grupo consistindo em cloreto de benzalcônio e cloreto de benzetônio, como definido na reivindicação 1.
3. Composição farmacêutica, de acordo com reivindicação 2, caracterizada pelo fato de que contém cátions de metais bi- ou trivalentes.
4. Composição farmacêutica, de acordo com a reivindicação 2 ou 3, caracterizada pelo fato de que contém Mg2+.
5. Composição farmacêutica, de acordo com qualquer uma das reivindicações 2 a 4, caracterizada pelo fato de que contém ainda um analgésico.
6. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de que o analgésico é uma substância não esteroidal anti-inflamatória (NSAID), em que a NSAID pode ser meloxicam, flunixina, cetoprofeno, carprofeno, metamizol ou ácido (acetil)-salicílico.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102006010643.1 | 2006-03-08 | ||
| DE102006010643A DE102006010643A1 (de) | 2006-03-08 | 2006-03-08 | Arzneimittel enthaltend Fluorchinolone |
| PCT/EP2007/001569 WO2008025380A1 (de) | 2006-03-08 | 2007-02-23 | Arzneimittel enthaltend fluorchinolone |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0708613A2 BRPI0708613A2 (pt) | 2011-06-07 |
| BRPI0708613B1 true BRPI0708613B1 (pt) | 2021-10-19 |
Family
ID=38171208
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0708613-0A BRPI0708613B1 (pt) | 2006-03-08 | 2007-02-23 | Uso de compostos de amônio quaternário, e composição farmacêutica |
Country Status (31)
| Country | Link |
|---|---|
| US (1) | US10231925B2 (pt) |
| EP (2) | EP1993510A1 (pt) |
| JP (1) | JP5584418B2 (pt) |
| KR (2) | KR20150046367A (pt) |
| CN (2) | CN104208064A (pt) |
| AR (1) | AR059696A1 (pt) |
| AU (1) | AU2007291622B2 (pt) |
| BR (1) | BRPI0708613B1 (pt) |
| CA (1) | CA2645037C (pt) |
| CR (1) | CR10270A (pt) |
| DE (1) | DE102006010643A1 (pt) |
| DK (1) | DK2340809T3 (pt) |
| EC (1) | ECSP088716A (pt) |
| ES (1) | ES2542206T3 (pt) |
| GT (1) | GT200800173A (pt) |
| HU (1) | HUE025044T2 (pt) |
| IL (1) | IL193429A0 (pt) |
| MX (1) | MX2008011344A (pt) |
| MY (1) | MY152885A (pt) |
| NZ (1) | NZ571046A (pt) |
| PE (1) | PE20071021A1 (pt) |
| PL (1) | PL2340809T3 (pt) |
| PT (1) | PT2340809E (pt) |
| RU (1) | RU2527327C2 (pt) |
| SI (1) | SI2340809T1 (pt) |
| SV (1) | SV2008003014A (pt) |
| TW (1) | TWI494105B (pt) |
| UA (1) | UA96753C2 (pt) |
| UY (1) | UY30191A1 (pt) |
| WO (1) | WO2008025380A1 (pt) |
| ZA (1) | ZA200807484B (pt) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7304008B2 (en) | 2001-05-15 | 2007-12-04 | Eurokera | Thermochromic material |
| DE102006010642A1 (de) * | 2006-03-08 | 2007-09-27 | Bayer Healthcare Aktiengesellschaft | Arzneimittelformulierungen, enthaltend Fluorchinolone |
| WO2010069493A1 (de) * | 2008-12-18 | 2010-06-24 | Bayer Animal Health Gmbh | Verbesserte wirkstoffkombination enthaltend ein antibiotikum und einen nichtsteroidalen entzündungshemmer (nsaid) |
| EP2332916A3 (en) | 2009-11-19 | 2011-08-03 | Krka Tovarna Zdravil, D.D., Novo Mesto | A process for a preparation of marbofloxacin and intermediate thereof |
| CN101716141B (zh) * | 2010-01-20 | 2011-11-30 | 白求恩医科大学制药厂 | 一种氟罗沙星注射液及其制备方法 |
| GB2480276A (en) * | 2010-05-11 | 2011-11-16 | Michael Hilary Burke | Process for the preparation of an aqueous injectable enrofloxacin antimicrobial formulation |
| RU2682171C2 (ru) * | 2016-10-11 | 2019-03-15 | Закрытое Акционерное Общество "Биологические Исследования И Системы" (Зао "Бис") | Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) |
| BR112019009132A2 (pt) * | 2016-11-07 | 2019-07-16 | Jubilant Life Sciences Ltd | composições antimicrobianas sinergísticas |
| MX2019009572A (es) * | 2017-02-13 | 2019-10-02 | Bayer Animal Health Gmbh | Composicion liquida que contiene pradofloxacina. |
| WO2019023842A1 (en) | 2017-07-31 | 2019-02-07 | Dow Silicones Corporation | MOISTURE CURING COMPOSITIONS |
| JP2020529490A (ja) | 2017-07-31 | 2020-10-08 | ダウ シリコーンズ コーポレーション | 湿分硬化性組成物 |
| CN111620901B (zh) * | 2020-06-08 | 2023-03-21 | 蚌埠医学院第二附属医院 | 一种含硅氧烷基的氟喹诺酮化合物、其制备方法及用途 |
Family Cites Families (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5746986A (en) | 1980-09-02 | 1982-03-17 | Dai Ichi Seiyaku Co Ltd | Pyrido(1,2,3-de)(1,4)benzoxazine derivative |
| US4670444B1 (en) | 1980-09-03 | 1999-02-09 | Bayer Ag | and-naphthyridine-3-carboxylic acids and antibacte7-amino-1-cyclopropyl-4-oxo-1,4-dihydro-quinoline-rial agents containing these compounds |
| US4472405A (en) | 1982-11-12 | 1984-09-18 | Riker Laboratories, Inc. | Antimicrobial 6,7-dihydro-5,8-dimethyl-9 fluoro-1-oxo-1H, 5H-benzo (ij) quinolizine-2-carboxylic acid and derivatives |
| US4730000A (en) | 1984-04-09 | 1988-03-08 | Abbott Laboratories | Quinoline antibacterial compounds |
| US4551456A (en) * | 1983-11-14 | 1985-11-05 | Merck & Co., Inc. | Ophthalmic use of norfloxacin and related antibiotics |
| AT392789B (de) | 1985-01-23 | 1991-06-10 | Toyama Chemical Co Ltd | Verfahren zur herstellung von 1-substituierten aryl-1,4-dihydro-4-oxonaphthyridinderivaten |
| IN166416B (pt) | 1985-09-18 | 1990-05-05 | Pfizer | |
| DE3713672A1 (de) * | 1987-04-24 | 1988-11-17 | Bayer Ag | Verfahren zur herstellung von parenteral verabreichbaren chinoloncarbonsaeuren |
| US5225413A (en) * | 1988-09-16 | 1993-07-06 | Bayer-Aktiengesellschaft | pH-neutral aqueous solutions of quinolone-carboxylic acids |
| DE3831514A1 (de) | 1988-09-16 | 1990-03-22 | Bayer Ag | Ph-neutrale waessrige loesungen von chinoloncarbonsaeuren |
| JP2832535B2 (ja) | 1989-04-04 | 1998-12-09 | 富山化学工業株式会社 | キノロンカルボン酸またはその塩の可溶化法 |
| WO1991009616A1 (en) * | 1989-12-22 | 1991-07-11 | Yale University | Quinolone antibiotics encapsulated in lipid vesicles |
| DK0507851T3 (da) | 1989-12-29 | 1997-08-25 | Abbott Lab | Quinoloncarboxylsyre-matalion-syrekomplekser |
| FR2665635A1 (fr) * | 1990-08-10 | 1992-02-14 | Merck Sharp & Dohme | Composition pharmaceutique fluide a base d'un complexe metallique et son procede de preparation. |
| DE69224071T2 (de) * | 1991-09-17 | 1998-05-07 | Alcon Lab Inc | Chinolan-antibiotika und polystyrolsulfonat enthaltende zusammensetzungen |
| SK284412B6 (sk) | 1995-12-21 | 2005-03-04 | Pfizer Inc. | Vodný farmaceutický roztok vhodný na injekčné podávanie hostiteľovi |
| RU2173318C2 (ru) | 1996-02-23 | 2001-09-10 | Байер Акциенгезелльшафт | 8-циан-1-циклопропил-7-(2,8-диазабицикло(4.3.0)-нонан-8-ил)-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновые кислоты, их производные и фармацевтическая композиция, обладающая антибактериальной активностью |
| WO1998018492A1 (fr) | 1996-10-25 | 1998-05-07 | Yoshitomi Pharmaceutical Industries Ltd. | Procede pour empecher la precipitation de medicaments |
| GB9714218D0 (en) * | 1997-07-04 | 1997-09-10 | Allied Therapeutics Ltd | Peritoneal dialysis fluid |
| DE19729879C2 (de) * | 1997-07-11 | 1999-07-08 | Mann Gerhard Chem Pharm Fab | Lagerstabile ophthalmische Zusammensetzungen, umfassend Diclofenac und Ofloxacin |
| BR9812644B1 (pt) * | 1997-09-15 | 2010-07-13 | quinolonas antimicrobianas, composição farmacêutica e uso das mesmas. | |
| US6387928B1 (en) * | 1997-09-15 | 2002-05-14 | The Procter & Gamble Co. | Antimicrobial quinolones, their compositions and uses |
| US6605751B1 (en) * | 1997-11-14 | 2003-08-12 | Acrymed | Silver-containing compositions, devices and methods for making |
| ID21415A (id) | 1997-12-05 | 1999-06-10 | Upjohn Co | Senyawa-senyawa antibiotik magnesium quinolon |
| DE19918324A1 (de) * | 1999-04-22 | 2000-10-26 | Mann Gerhard Chem Pharm Fab | Pharmazeutische Zusammensetzung wirksam gegen durch Bakterien, Viren, Pilze, Hefen und Protozoen verursachte Krankheitszustände |
| US6482799B1 (en) * | 1999-05-25 | 2002-11-19 | The Regents Of The University Of California | Self-preserving multipurpose ophthalmic solutions incorporating a polypeptide antimicrobial |
| DE19937115A1 (de) | 1999-08-06 | 2001-02-08 | Bayer Ag | Wäßrige Arzneimittelformulierung von Moxifloxacin oder Salzen davon |
| AU776609B2 (en) * | 1999-09-24 | 2004-09-16 | Novartis Ag | Topical suspension formulations containing ciprofloxacin and dexamethasone |
| EP1596823A2 (en) * | 2003-02-21 | 2005-11-23 | Sun Pharmaceuticals Industries Ltd. | A stable ophthalmic composition |
| DE10312346A1 (de) * | 2003-03-20 | 2004-09-30 | Bayer Healthcare Ag | Kontrolliertes Freisetzungssystem |
| RU2248199C1 (ru) * | 2003-06-02 | 2005-03-20 | Открытое Акционерное Общество "Акционерное Курганское общество медицинских препаратов и изделий "Синтез" (ОАО "Синтез") | Глазные капли и способ их получения |
| DE10337191A1 (de) * | 2003-08-13 | 2005-03-17 | Bayer Healthcare Ag | Neue Verwendung von Chinolon-Antibiotika |
| DE102004001558A1 (de) * | 2004-01-10 | 2005-08-18 | Bayer Healthcare Ag | Arzneimittel zur topischen Applikation bei Tieren |
| DE102004015981A1 (de) | 2004-04-01 | 2005-10-20 | Bayer Healthcare Ag | Neue kirstalline Form von 8-Cyan-1-cyclopropyl-7-(1S,6S-2,8-diazabicyclo[4.3.0]nonan-8-yl)-6-fluor-1,4-dihydro-4-oxo-3-chinolincarbonsäure |
| JP4792032B2 (ja) * | 2004-08-13 | 2011-10-12 | シェーリング−プラウ・リミテッド | 抗生物質、トリアゾールおよびコルチコステロイドを含む薬学的処方物 |
-
2006
- 2006-03-08 DE DE102006010643A patent/DE102006010643A1/de not_active Withdrawn
-
2007
- 2007-02-23 CN CN201410443858.5A patent/CN104208064A/zh active Pending
- 2007-02-23 UA UAA200811959A patent/UA96753C2/ru unknown
- 2007-02-23 HU HUE11151745A patent/HUE025044T2/en unknown
- 2007-02-23 CA CA2645037A patent/CA2645037C/en active Active
- 2007-02-23 BR BRPI0708613-0A patent/BRPI0708613B1/pt active IP Right Grant
- 2007-02-23 NZ NZ571046A patent/NZ571046A/en unknown
- 2007-02-23 RU RU2008139635/15A patent/RU2527327C2/ru not_active IP Right Cessation
- 2007-02-23 AU AU2007291622A patent/AU2007291622B2/en active Active
- 2007-02-23 ES ES11151745.4T patent/ES2542206T3/es active Active
- 2007-02-23 WO PCT/EP2007/001569 patent/WO2008025380A1/de active Application Filing
- 2007-02-23 DK DK11151745.4T patent/DK2340809T3/en active
- 2007-02-23 EP EP07846476A patent/EP1993510A1/de not_active Withdrawn
- 2007-02-23 PL PL11151745T patent/PL2340809T3/pl unknown
- 2007-02-23 KR KR20157009314A patent/KR20150046367A/ko not_active Application Discontinuation
- 2007-02-23 MX MX2008011344A patent/MX2008011344A/es not_active Application Discontinuation
- 2007-02-23 CN CN200780008116.8A patent/CN101394836B/zh active Active
- 2007-02-23 MY MYPI20083457 patent/MY152885A/en unknown
- 2007-02-23 US US12/280,448 patent/US10231925B2/en active Active
- 2007-02-23 SI SI200731666T patent/SI2340809T1/sl unknown
- 2007-02-23 EP EP11151745.4A patent/EP2340809B1/de active Active
- 2007-02-23 JP JP2008557622A patent/JP5584418B2/ja active Active
- 2007-02-23 PT PT111517454T patent/PT2340809E/pt unknown
- 2007-02-23 KR KR1020087022334A patent/KR20080106253A/ko active Application Filing
- 2007-03-01 AR ARP070100842A patent/AR059696A1/es unknown
- 2007-03-07 UY UY30191A patent/UY30191A1/es not_active Application Discontinuation
- 2007-03-07 PE PE2007000249A patent/PE20071021A1/es not_active Application Discontinuation
- 2007-03-07 TW TW096107754A patent/TWI494105B/zh not_active IP Right Cessation
-
2008
- 2008-08-13 IL IL193429A patent/IL193429A0/en unknown
- 2008-08-28 SV SV2008003014A patent/SV2008003014A/es unknown
- 2008-09-01 ZA ZA200807484A patent/ZA200807484B/xx unknown
- 2008-09-03 GT GT200800173A patent/GT200800173A/es unknown
- 2008-09-03 CR CR10270A patent/CR10270A/es not_active Application Discontinuation
- 2008-09-04 EC EC2008008716A patent/ECSP088716A/es unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0708613B1 (pt) | Uso de compostos de amônio quaternário, e composição farmacêutica | |
| US9610297B2 (en) | Stabilization of vitamin B12 | |
| JP4863867B2 (ja) | 制御放出システム | |
| CA2644981C (en) | Pharmaceutical formulation comprising fluoroquinolones |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25A | Requested transfer of rights approved |
Owner name: BAYER INTELLECTUAL PROPERTY GMBH (DE) |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] |
Free format text: NOTIFICACAO DE ANUENCIA RELACIONADA COM O ART 229 DA LPI |
|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 23/02/2007, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |