INSTRUMENTO PARA INSERÇÃO DE UM IMPLANTE NO CANAL DE SCHLEMM DO OLHO
Fundamentos da Invenção
[001] O glaucoma é uma condição doentia dos olhos em que a pressão intraocular aumentada (IOP) é criada mediante o bloqueio do mecanismo de drenagem do fluido aquoso produzido na parte anterior dos olhos. Tais condições de fluxo de saída aquoso são geralmente tratadas por drogas tópicas na forma de colírios, mas pode resultar em tratamento cirúrgico se o tratamento de droga se torne ineficaz devido à perda de resposta à droga ou fraca submissão do paciente.
[002] Pesquisa oftálmica tem indicado que a maior resistência ao fluxo de saída aquoso é a rede trabecular, mais especificamente, o tecido justacanalicular na parede interna do canal de Schlemm (Grant, M.W., Arch. Ophthal. 1963; 69:783-801). A cirurgia tradicional do glaucoma tal como trabeculectomia, envolve uma dissecação do retalho do olho e a remoção de uma parte do tecido esclerótico e da rede trabecular para desviar o trajeto do fluxo de saída aquoso normal e formar um trajeto de fluxo de saída direto a partir da câmara anterior. O fluido aquoso é direcionado posteriormente sob o retalho cirúrgico e a um lago sub-conjuntival conhecido como uma vesícula. As complicações pós-cirúrgicas e o manejo da vesícula são questões significativas com a trabeculectomia e procedimentos similares.
[003] Os tratamentos cirúrgicos recentemente desenvolvidos para o glaucoma envolvem o acesso cirúrgico do canal de Schlemm pela maneira de um ou mais retalhos cirúrgicos e subseqüentemente dilatação do canal para aumentar a drenagem do humor aquoso no trajeto de drenagem natural em lugar de uma vesícula. Os mecanismos envolvidos na dilatação do canal de Schlemm para auxiliar o fluxo de saída aquoso não são completamente elucidados. A dilatação ou expansão do canal pode causar uma comunicação direta entre o canal de Schlemm e o espaço justacanalicular e pode intensificar o fluxo de saída aquoso (Smit, B.A., Johnstone, M.A., Ophthalmology, 2002; 109:786-792). Além disso, a dilatação do canal pode também limitar a capacidade da parede interna ser distendida externamente mediante o aumento da pressão intraocular e comprimir contra a parede externa para aumentar a resistência do fluxo de saída aquoso (Ellingsen, B.A., Grant, W.M., Investigative Ophthalmology, 1972; 11(1): 21-8).
[004] Vários métodos e dispositivos para a cirurgia de glaucoma que envolve o canal de Schlemm foram descritos na técnica anterior. Stegmann, et al. na US 5.486.165 apresentam uma microcânula designada para a liberação de substâncias no canal de Schlemm durante a cirurgia de glaucoma. Na US 2002/0013546, Grieshaber, et al. apresentam um dispositivo para sustentar um lúmen expandido do canal de Schlemm em uma posição permanentemente expandida. Lynch, et al. na US 6.464.724 descrevem um dispositivo de stent para expandir e manter a desobstrução do canal de Schlemm. Neuhann na US 6.494.857 descreve um dispositivo tubular longitudinalmente curvado.
[005] Outros métodos para melhorar a drenagem do humor aquoso no canal de Schlemm envolvem a colocação de um desvio que forma uma passagem de fluido entre a câmara anterior e o canal. Ver Lynch et al. Na US 6.450.984, Hill na US 6.533.768 e Gharib et al. Na US 20020165478.
[006] As drogas colinérgicas tais como pilocarpina são o tratamento médico mais antigo para o glaucoma. Estas drogas funcionam por uma ação mecânica mediante o aumento do tônus muscular ciliar que extrai o esporão escleral adjavente adjacente à rede trabecular voltado para uma direção posterior e interior. A tração é desse modo aplicada à rede trabecular, abrindo os espaços intertrabecular, aumentando o fluxo de saída aquoso, e reduzindo a pressão intraocular. A presente invenção descreve um implante que reside dentro do canal de Schlemm do olho e fornece tração à rede trabecular similar à ação das drogas colinérgicas ou mióticas. O uso de um implante fornece tração contínua e aumento no fluxo de saída aquoso sem re-administração de uma droga e sem os efeitos colaterais da droga. Além disso, visto que o implante aplica tração à rede trabecular diretamente, os efeitos óticos nos olhos tais como deslocamento miópico flutuante e visão diminuída na iluminação obscurecida produzida por drogas colinérgicas são evitados.
[007] Embora a técnica anterior descreva vários meios de desviar ou sondar o lúmen do canal de Schlemm, não ensina um meio de aumentar o fluxo de saída aquoso mediante a aplicação de tração não induzida por droga à rede trabecular na parede interna do canal. A presente invenção descreve um novo método no tratamento cirúrgico de glaucoma mediante a colocação de um implante no canal de Schlemm que é designado para transmitir tração mecânica à rede trabecular de interface sobre a parede interna do canal, desse modo aumentando o fluxo de saída aquoso e reduzindo a pressão intraocular.
[008] Esta invenção é direcionada a um implante oftálmico, que pode ser diretamente inserido no canal de Schlemm para melhorar o fluxo de saída aquoso através do trajeto trabeculocanalicular durante um período de tempo prolongado. A invenção é direcionada às formas de realização e materiais de um tal implante, e também aos instrumentos para a colocação do implante por métodos minimamente invasivos.
Sumário da Invenção
[009] A invenção é direcionada a um implante para o tratamento de glaucoma que compreende um elemento alongado com extremidades distais e próximas posicionáveis dentro do canal de Schlemm do olho de modo a fornecer uma força de tracionamento à parede interna do canal para desse modo aumentar a permeabilidade de fluido da parede interna do canal. A força de tracionamento pode ser axialmente aplicada. A tração axial é distinguível da tração radial. A matriz estende o canal de Schlemm em seu eixo longitudinal. Esta radialmente estende o canal. A força de tracionamento pode ser fornecida através de um elemento de preensão em dita uma ou ambas extremidades do implante e é incorporável a um elemento de tração que fornece a força de fracionamento. Em uma forma de realização, o elemento de tração pode ser uma mola que pode ser acomodada em um alojamento de proteção. Em uma outra forma de realização, o elemento de tração pode ser um elemento de frisamento para prender o implante em uma posição tracionada. O implante pode ser fornecido com uma extremidade expandida ou forma de seção transversal com uma força de tracionamento na faixa de cerca de 1 a 11 gramas.
[0010] O implante pode ser fornecido com rigidez mecânica suficiente para transmitir a força de tracionamento à parede interna após a colocação dentro do canal.
[0011] Em algumas formas de realização, o implante pode compreender um filamento helicoidal ou pelo menos dois filamentos entrelaçados entre si em uma maneira helicoidal ou fixados em uma maneira paralela.
[0012] Em algumas formas de realização, o implante pode compreender um filamento em serpentina tendo um aspecto de seção transversal circular ou oval.
[0013] Em uma outra forma de realização, o implante pode compreender as primeiras regiões de uma primeira dimensão da seção transversal interespaçada com as segundas regiões de uma segunda dimensão da seção transversal em que a primeira dimensão da seção transversal é maior do que a segunda dimensão da seção transversal. Em algumas formas de realização, as primeiras regiões compreendem esferas ou segmentos cilíndricos e podem livremente girar em relação às segundas regiões.
[0014] Em outra forma de realização o implante pode compreender alças conectadas a um elemento axial ou conectadas nas extremidades alternantes.
[0015] O implante pode ser fornecido com uma forma para promover o fluxo de humor aquoso a partir da parede interna do canal até os canais coletores sobre a parede externa do canal. Em algumas formas de realização, o implante pode compreender múltiplas esferas angulares que se parecem com um perfil denteado, perfis semicirculares em repetição, um filamento helicoidal ou um tubo com canais internos.
[0016] O implante pode compreender um metal, um polímero biocompatível e/ou um agente biologicamente ativo. O agente biologicamente ativo pode ser um agente anti-trombogênico, agente anti-microbial, agente anti-inflamatório, agente anti-fibrótico, agente anti-proliferativo celular ou agente anti-aderência.
[0017] A invenção é também direcionada a um instrumento para inserção de um implante no canal de Schlemm do olho que compreende um implante compreendendo um elemento alongado com extremidades distais e proximais posicionáveis dentro de dito canal de modo a fornecer uma força de tracionamento à parede interna do canal para desse modo aumentar a permeabilidade de fluido da parede interna do canal, o implante ligado a uma cânula flexível ou fio de guia. O instrumento pode ainda compreender um elemento mecânico sobre a cânula para a ligação do implante na cânula. Em algumas formas de realização, o elemento mecânico pode compreender um orifício, fenda ou uma área de diâmetro aumentado em uma ponta da cânula.
[0018] O instrumento pode também compreender um elemento guia para a localização do instrumento durante a colocação e avanço dentro do canal de Schlemm. Em uma forma de realização, o elemento guia pode ser um sinalizador ótico de fibra. O instrumento pode também compreender um elemento mecânico dilatável para a dilatação do canal, um lúmen para injeção de materiais viscosos, um revestimento lúbrico e/ou uma ponta arredondada.
[0019] Um método é fornecido para aumentar o fluxo de saída do fluido através do canal de Schlemm que é útil para o tratamento de glaucoma. O implante é colocado no canal de Schlemm mediante o uso de um instrumento de liberação flexível ligado ao implante. O método compreende posicionar o instrumento e o implante dentro do canal, liberar o implante e conectar as extremidades distais e proximais do implante para aplicar força de tracionamento suficiente sobre a parede interna do canal para aumentar a permeabilidade de fluido. Um método é também fornecido para aumentar o fluxo de saída aquoso de fluido através do canal de Schlemm no olho mediante o posicionamento no canal de um instrumento de liberação ligado ao implante que prende uma das extremidades distais ou proximais do implante dentro do canal, ajustando o implante para fornecer força de tracionamento suficiente sobre a parede interna do canal para aumentar a permeabilidade de fluido da parede interna do canal, e prender a outra das extremidades distais e proximais dentro de dito canal para manter a força de tracionamento sobre a parede interna do canal.
Descrição dos Desenhos
[0020] A Figura 1 é uma vista em corte transversal da parte anterior do olho humano indicando a localização do canal de Schlemm e outras estruturas relevantes.
[0021] A Figura 2 é uma vista seccional em 3-D indicando a transversal do canal de Schlemm ao redor do limbo.
[0022] A Figura 3 é uma vista em corte transversal de um implante filamentoso colocado dentro do canal de Schlemm e que fornece tração sobre a parte da parede interna (rede trabecular) do canal.
[0023] As Figs. 4a e 4b apresentam duas formas de realização de um implante filamentoso que compreende uma seção transversal não uniforme. A Fig. 4 a mostra um formato de “esferas em um fio”. A Fig. 4b mostra uma série de segmentos cilíndricos de diâmetro variável.
[0024] As Figs. 5a e 5b apresentam duas formas de realização de filamentos de tração dispostos em um padrão axial. A Fig. 5a mostra uma série de alças ovais conectadas em extremidades alternantes. A Fig. 5b mostra uma série de alças conectadas ao longo de uma estrutura.
[0025] As Figs. 6a e 6b apresentam duas formas de realização de dispositivos de tração em uma configuração de múltiplas esferas designadas para colocar a parede interna do canal de Schlemm em tração. A Fig. 6a mostra um dispositivo configurado em um padrão denteado. A Fig. 6b mostra um dispositivo configurado com esferas semi-circulares em série.
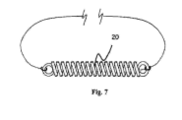
[0026] A Figura 7 mostra um implante filamentoso com um dispositivo de preensão compreendendo um elemento de molas para fornecer tração sobre o filamento in situ no olho.
[0027] As Figs 8a e 8b apresentam um implante filamentoso em posição expandida e contraída com um dispositivo de preensão que compreende um elemento de molas em um alojamento de proteção para fornecer tração sobre o filamento in situ no olho.
[0028] A Figura 9 mostra um implante filamentoso com um elemento de preensão que compreende um acoplamento pregueado para ligar as duas extremidades do filamento entre si sob tração.
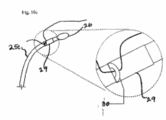
[0029] As Figs. 10a-10c apresentam instrumentos de liberação com características sobre a ponta distal para ligação de um implante filamentoso. A Fig. 10a mostra um instrumento de liberação com uma ponta distal de diâmetro maior do que a haste.A Fig 10b mostra um instrumento de liberação com uma ponta distal maior, um segmento curto de haste e depois um segmento expandido de haste. A Fig. 10c mostra um instrumento de liberação com um ponto de ligação tabulado como um componente do instrumento.
[0030] As Figs. 11a e 11b apresentam um implante que compreende uma série de alças redondas ligeiramente sobrepostas da maneira de uma mola em espiral achatada. A Fig. 11a mostra a vista lateral quando comprimido.
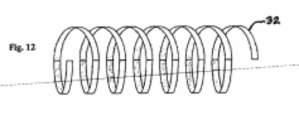
[0031] A Fig. 12 mostra um implante da invenção na forma de um filamento helicoidal.
[0032] A Fig. 13 mostra um implante de acordo com a invenção que é tubular na forma com canais internos direcionados a partir da superfície de interface da parede interna do canal de Schlemm até a superfície de interface da parede externa.
[0033] A Figura 14 é um gráfico de fluxo de saída de fluido vs tração aplicada em um implante filamentoso de prolene como descrito de acordo com o Exemplo 2.
[0034] A Figura 15 é um gráfico de fluxo de saída de fluido como uma função da tração sobre um implante filamentoso de prolene em três diferentes pressões intraoculares como descrito de acordo com o Exemplo 3.
[0035] A Figura 16 é um gráfico de barras que resume o fluxo de saída em testes de tração descritos no Exemplo 4.
Descrição das Formas de Realização
[0036] A invenção fornece um implante oftálmico que compreende um elemento alongado flexível com extremidades distais (o mais distante do instrumento de inserção) e proximais (o mais próximo do instrumento de inserção), e dimensões da seção transversal menores do que o canal de Schlemm, que pode ser inserido no canal e posicionado para fornecer força de tracionamento suficiente à rede trabecular de interface sobre a parede interna do canal para melhorar o fluxo de saída do humor aquoso. Referindo-se às Figs. 1 e 2, o canal de Schlemm 10 é um canal em forma de arco no olho adjacente à rede trabecular. O humor aquoso se drena da câmara anterior através da rede trabecular na parede interna do canal de Schlemm e dentro do canal. A partir do canal, o humor aquoso é guiado para dentro dos canais coletores e eventualmente para dentro das veias aquosas e do sistema venoso. O canal de Schlemm possui um raio na faixa de aproximadamente 5 a 7 mm e dimensões típicas em corte transversal oval de 200 mícrons por 50 mícrons. O acesso cirúrgico ao canal de Schlemm pode ser executado pela dissecação de um retalho esclerótico, como executado nos procedimentos cirúrgicos de viscocanalostomia e de esclerectomia profunda, ou por uma incisão radial esclerótica. Assim que o acesso cirúrgico é alcançado, o implante é colocado dentro do canal de Schlemm e é guiado ao longo da circunferência do canal de Schlemm. O canal pode ser pré-dilatado por tal meio como injeção de um viscoelástico de modo a facilitar a colocação do implante.
[0037] Referindo-se à fig. 3, em uma forma de realização a extremidade distal do implante 11 pode então ser prendida na extremidade proximal e aproximada em uma maneira para aplicar tração ao longo do eixo longitudinal do implante, e desse modo transmitir uma força radialmente intrínseca 12 à parede interna do canal de Schlemm. Embora não pretendendo ser limitado por qualquer teoria particular, além de aumentar o fluxo de saída aquoso através da parede interna do canal pela aplicação de tração, a força radialmente intrínseca pode também atuar para limitar a distração da parede interna. A distração da parede interna pode diminuir o fluxo de saída aquoso através do canal devido ao contato da parede interna com a parede externa.
[0038] Em uma forma de realização, o implante compreende um filamento que é colocado dentro e inteiramente ao longo da circunferência do canal de Schlemm. As extremidades proximais e distais do filamento são atadas entre si para aplicar uma força mecânica intrínseca sobre a parede interna do canal. O filamento pode compreender material elástico ou não elástico ou uma combinação de materiais elásticos e não elásticos. A tração pode ser executada mediante o uso de um implante elástico que possui a vantagem de aplicar tração uniformemente sobre a circunferência do canal pelo estiramento do implante antes de unir as extremidades. Esta forma de realização particular do implante aplica uma força e tração mecânica à parede interna do canal e à rede trabecular, mas não entra em contato ou aplica força mecânica às outras paredes do canal. O filamento pode ser tão pequeno quanto 10 mícrons de diâmetro ou tão grande quanto o canal, aproximadamente 200 mícrons. Além disso, se o canal for dilatado antes da implantação ou estirado durante a implantação, os filamentos de dimensões muito maiores, até 350 mícrons de diâmetro, podem ser implantados. O filamento pode ou não pode ter um lúmen ou canais internos ou externos para o transporte de humor aquoso. O filamento pode ter uma seção transversal uniforme ou não uniforme para intensificar o fluxo de saída aquoso no canal. O filamento pode compreender qualquer material que seja não tóxico e não inflamatório aos tecidos de interface. A reação mínima do tecido é desejada para minimizar a formação do tecido fibroso na interface implante-tecido, que pode comprometer o fluxo de saída de humor aquoso. O implante pode também compreender um ou mais filamentos enrolados entre si ou dispostos em uma maneira paralela.
[0039] Em uma forma de realização alternativa, o implante compreende um filamento compreendendo as primeiras regiões de uma primeira dimensão da seção transversal interespaçadas com as segundas regiões de uma segunda dimensão da seção transversal tal que a primeira dimensão da seção transversal é maior do que a segunda dimensão da seção transversal. Este corte transversal não uniforme, tal como as áreas uniformemente espaçadas de forma relativa da seção transversal maior, resulta em um implante que se parece com um cordão de esferas ou segmentos cilíndricos, tal como mostrado nas duas formas de realização da Fig. 4a e Fig 4b. As esferas ou áreas de dimensão da seção transversal maior, 13, 14, podem compreender o mesmo material como as regiões de filamento menor ou alternativamente podem compreender um outro material. As esferas ou áreas de seção transversal maior podem ser mecanicamente integrais com as regiões de filamento menores ou fabricadas tais que as esferas sejam atravessadas pelo filamento menor através de um canal nas esferas. Os canais de esfera e as dimensões do filamento podem ser feitos sob medida para permitir a rotação livre da esfera ao longo do eixo formado pelo canal para minimizar a irritação mecânica aos tecidos de interface durante o movimento.
[0040] Em uma outra forma de realização alternativa, o implante pode compreender um ou mais elementos de tração axialmente alinhados. Os elementos de tração podem ser filamentos, incluindo fios, tendo um aspecto de seção transversal circular ou oval. Os elementos podem ser conectados entre si, como mostrado na Fig. 5 a, em uma configuração de filamento em curva para formar uma série de curvas de filamento oval 15 ligada entre si alternativamente na parte de cima e na parte de baixo das curvas, criando um padrão de estilo “espinha de peixe”. Referindo-se à Fig. 5b, os elementos 16 podem ser uma série de curvas filamentosas conectadas ao longo de um elemento de estrutura axial 17. Alternativamente, referindo-se à Fig. 11, o implante pode compreender uma série de curvas redondas 31, adjacentes uma a outra ou ligeiramente sobrepostas, da maneira de uma mola em espiral achatada. Os elementos podem ser componentes separados que podem ser serialmente colocados dentro do canal. A força mecânica pode ser aplicada ao longo do eixo do implante para aplicar tração axial somente na parede interna do canal. Além disso, os elementos de tração pode ser dispostos dentro do canal para colocar a parede interna do canal em tração por força mecânica entre a parede interna e externa, isto é, o eixo de seção transversal curto do canal; ou entre as paredes anteriores e posteriores do canal, isto é, o eixo de seção transversal longo do canal ou uma combinação destes. Desta maneira, os elementos de tração podem ser designados a não apenas fornecer força de tracionamento apropriada à parede interna do canal, mas também fornecer uma força de expansão secundária para separar as paredes do canal ou dilatar o canal.
[0041] Em outra forma de realização alternativa, o implante pode compreender um filamento de tração com uma forma para promover o fluxo de saída de humor aquoso a partir da parede interna do canal de Schlemm até os canais coletores sobre a parede externa do canal. Referindo-se à Fig. 6a, o filamento é fornecido em uma configuração com múltiplas misturas angulares 18a para se parecer com um perfil denteado. Os perfis semi-circulares de repetição 18b podem ser fornecidos como mostrado na Fig. 6b. Referindo-se à Fig. 12, um filamento helicoidal 32 pode também ser usado. O implante 33 pode também ser tubular na forma como exemplificado na Fig. 13 com canais internos 34 direcionados a partir da interface superficial da parede interna do canal até a interface superficial da parede externa. Estas formas de realização formam trajetos de fluxo radialmente externos a partir da parede interna até a parede externa do canal enquanto se aplica tração à parede interna.
[0042] O implante é preferível tendo rigidez mecânica suficiente para transmitir tração à parede interna do canal de Schlemm. O implante pode também ter complacência suficiente para permitir algum movimento da parede interna do canal de Schlemm devido à função normal dos olhos. O implante pode também ser usado em seções para fornecer a mesma funcionalidade como um implante único colocado ao longo da circunferência inteira do canal. Por exemplo, em lugar de completamente atravessar o comprimento circunferencial do canal para permitir a conexão da extremidade proximal do implante com a extremidade distal, o implante pode ocupar um segmento da circunferência. Em uma forma de realização, uma extremidade do implante pode ser fixada no tecido próximo ou dentro do canal e a outra estendida no canal e fixada no tecido em alguma distância ao longe após transmitir tração suficiente do implante entre as duas extremidades para fornecer a força intrínseca desejada sobre a parede interna do canal. Desta maneira, um olho de paciente pode ser tratado em segmentos, por exemplo, na situação onde a cirurgia anterior dos olhos tornou uma parte do canal inacessível a um implante completamente circunferencial.
[0043] O implante pode adicionalmente compreender um dispositivo de preensão para facilitar a ligação à outra extremidade do implante ou aos tecidos. O dispositivo de preensão pode ser ligado a uma extremidade do implante ou pode ser um componente separado que leva em conta a ligação e tração de ambas as extremidades do implante. O dispositivo de preensão pode compreender o mesmo material como o filamento, um material diferente ou uma pluralidade de materiais. Por exemplo, um anel pequeno pode ser fabricado sobre a extremidade proximal de um filamento de implante para facilitar a ligação da extremidade distal do filamento em uma curva. O dispositivo de preensão pode compreender um mecanismo de ligação para a extremidade distal do implante tal que a extremidade distal pode ser diretamente ligada ao dispositivo de preensão e submetido à tração com um mecanismo tipo lingüeta de catraca.
[0044] Alternativamente, como mostrado na Fig. 9, um grampo tal como um elemento plissado 19, que pode ser um componente separado ou pode ser fabricado em uma extremidade do implante, pode ser usado para prender a outra extremidade do implante ou ao tecido próximo.
[0045] O dispositivo de preensão pode compreender um elemento de tração tal como um material elástico ou mola. Na Fig. 7 e Fig. 8, uma mola 20 é mostrada a qual permite a tração sobre o implante a ser ajustada durante a colocação cirúrgica ou em um segundo procedimento subseqüente após a implantação. A mola 20 pode também levar em conta a mudança elástica do comprimento de implante para acomodar o movimento do tecido e desse modo minimizar o movimento na interface implante-tecido e irritação mecânica resultante. A mola pode ser configurada para residir dentro de um estojo ou alojamento de proteção 21 para impedir a restrição do movimento da mola pelo tecido de interface assim como proteger o tecido de ser invadido pelo elemento de mola. A mola pode também ser fornecida com um aspecto para medir a tração colocada sobre o implante, tal como um indicador de extração de mola configurado no estojo de proteção externo 21. A mola pode ser visualizada in situ por gonioscopia através da córnea para avaliar pós operativamente o funcionamento do implante. Tipicamente, uma mola ou outro material de tração elástico deve fornecer cerca de 4 a 6 gramas força por mm de mudança no comprimento.
[0046] Em geral, o implante é colocado no canal de Schlemm mediante o uso de um instrumento de liberação flexível ligado ao implante. Isto pode ser executado pelo posicionamento do instrumento e implante dentro do canal, liberando o implante e conectando as extremidades distais e proximais do implante para aplicar força de tracionamento suficiente sobre a parede interna do canal para aumentar a permeabilidade de fluido. Se a rigidez mecânica do implante posicionado isoladamente for suficiente para transmitir força de tracionamento suficiente sobre a parede interna do canal, então a conexão das extremidades do implante pode não ser necessária. Alternativamente, uma extremidade do implante pode ser ancorada ao tecido, depois a extremidade pode ser ancorada no tecido após o ajuste do implante para ter a tração apropriada. Desta maneira, as duas extremidades do implante não necessitam ser atadas uma a outra ou o implante não necessita atravessar o comprimento circunferencial inteiro do canal.
[0047] O implante é preferivelmente colocado no canal de Schlemm mediante o uso de um instrumento de liberação flexível que é usado para entrar no canal tal como descrito pela PCT/US02/37572, aqui incorporada por referência. O implante é progressivamente avançado ao longo do canal de Schlemm na localidade desejada pelo instrumento de liberação, tal como uma cânula, opcionalmente com dilatação anterior ou concorrente do canal. O implante pode ser atado ao instrumento de liberação e liberado do instrumento assim que colocado na posição desejada dentro do canal de Schlemm ou após atravessar a circunferência do canal.
[0048] Alternativamente, o instrumento de liberação pode ser colocado na posição desejada dentro do canal, e o implante fixado em uma extremidade do instrumento, tal como uma cânula ou fio de guia, e puxado para dentro do canal durante a retirada do instrumento flexível. Como mostrado nas Figs. 10a-10c o instrumento de liberação 25a, 25b e 25c pode ter aspectos para auxiliar a ligação e liberação do implante ou seu dispositivo de preensão. O instrumento pode ter um segmento de diâmetro aumentado 26 ou segmentos 27, 28 na extremidade distal para facilitar a ligação de uma extremidade do implante. Alternativamente, tais aspectos podem incluir projetos tais como um orifício ou fenda apropriadamente feito sob medida em uma extremidade do instrumento para inserir e ligar uma parte do implante. O instrumento de liberação pode ter elemento mecânico ativo tal como colar 29 que acomoda uma ponta de ilhó 30 para ligar o implante e/ou para liberar o implante ligado assim que colocado apropriadamente no canal de Schlemm. O instrumento de liberação pode também conter aspectos tais como um lúmen de liberação para permitir a liberação de um fluido em dilatação ao canal de Schlemm antes da, ou concorrente com a, colocação do implante. Uma vez no local desejado, os aspectos mecânicos no membro do instrumento de liberação podem ser usados para liberar o implante na posição apropriada.
[0049] O instrumento de liberação pode compreender um fio de guia flexível ou uma microcânula flexível designado para a canulação de 360o do canal de Schlemm. O instrumento de liberação tipicamente será fabricado tendo um diâmetro na faixa de cerca de 50 a 350 mícrons para ajustar-se dentro do canal. O instrumento de liberação flexível pode ter uma extremidade distal curvada em uma maneira para aproximar o raio da curvatura do canal de Schlemm, tipicamente de 5 a 7 mm. O instrumento pode também compreender um elemento guia para efetuar o avanço apropriado da parte distal tal como descrito na PCT/US02/37572. Tal elemento guia pode compreender marcações ou um dispositivo de transmissão luminosa tal como um sinalizador de fibra ótica na ponta distal do instrumento de liberação que permite o cirurgião identificar e localizar a ponta distal através dos tecidos escleróticos em excesso mediante a visualização direta ou formação de imagem não invasiva durante a inserção e avanço do instrumento dentro do canal.
[0050] A dilatação do canal de Schlemm durante o avanço do instrumento de liberação foi observada para facilitar a colocação atraumática do instrumento de liberação e implante. A dilatação pode ser executada mediante a injeção de um fluido com viscosidade elevada tal como um material viscoelástico cirúrgico na ponta distal do instrumento através de um lúmen no instrumento. Alternativamente, o instrumento pode compreender elementos dilatáveis na ponta distal que pode ser repetidamente expandida e contraída para dilatar o canal durante o avanço do dispositivo. Uma ponta distal redonda e um tratamento superficial lúbrico pode facilitar a inserção e avanço progressivo do instrumento de liberação.
[0051] Para verificar o posicionamento do instrumento de liberação no canal de Schlemm vários métodos são úteis, incluindo o uso de uma ponta sinalizadora de fibra ótica incorporado no instrumento de liberação, localização visual direta durante a dissecção cirúrgica ou pelo guia de imagem externa tal como formação de imagem por ultra-som ou tomografia de coerência ótica. O posicionamento acurado dentro do canal pode ser auxiliado pelas características do instrumento tais como marcações para indicar o comprimento dentro do canal, revestimentos ou maçadores para auxiliar a formação de imagem, e marcações para indicar o alinhamento rotacional. Além disso, o instrumento ou implante pode incorporar marcadores para assistir na determinação de sua localização tais como revestimentos fluorescentes ou ultrassonicamente refletivos ou marcadores rádio-opacos.
[0052] Em uma forma de realização alternativa, o implante pode ser colocado sob visualização direta da câmara anterior do olho. O implante atado em um instrumento de liberação pode ser colocado através de uma incisão da córnea na câmara anterior e através da rede trabecular do olho dentro do canal de Schlemm.
[0053] O implante pode compreender uma variedade de materiais com biocompatibilidade adequada e propriedades mecânicas, incluindo meais tais como aços inoxidáveis, titânio, tungstênio, ligas de níquel-titânio, ligas de cobalto-cromo, polímeros biocompatíveis tais como polimetilmetacrilato, poliimida, náilon, policarbonato, poliestireno, polímero fluorados, polieteretercetona, polissulfona, polietileno, polipropileno, poliésteres, poliuretano, polidimetilsiloxano, tereftalato de polibutileno, tereftalato de polietileno, parileno, cerâmicas flexíveis, carbono, materiais biodegradáveis tais como ácido poliláctico, ácido poliglicólico, poliidroxibuturato, polidioxanona, carbonato de politrimetileno, biopolímeros tais como seda, colágeno, gelatina, glicosoaminoglicanos, quitina, derivados de quitina e elastina, e compósitos de tais materiais. Um implante filamentoso pode ser circular, oval, retangular ou em uma variedade de outras formas em corte transversal. O implante pode ser configurado de um pedaço de filamento ou fio, cortado de um comprimento de material com a configuração em corte transversal desejado, quimicamente cauterizado, mecanicamente ou trabalhado à máquina com laser, extrusado ou moldado.
[0054] O implante pode também compreender agentes biologicamente ativos para promover a resposta biológica favorável pelos tecidos de interface tais como a minimização de coágulos sangüíneos (agentes anti-trombóticos), inflamação, infecção e fibrose (agentes anti-fibróticos). Tais agentes incluem agentes de anti-coagulação tais como heparina, TPA, agentes anti-microbianos tais como antibióticos, agentes anti-inflamatórios tais como esteróides, agentes anti-aderência tais como ácido hialurônico e anti-proliferação celular ou agentes anti-fibróticos tais como rapamicina, 5-fluorouracila, mitomicina, metotrexato ou paclitaxol. Os agentes biologicamente ativos podem ser incorporados no implante ou aplicados como um revestimento.
[0055] Uma outra função do implante é que ele pode servir como um marcador e assim ser visualizado e avaliado da câmara anterior para ser usado de modo preso como um alvo de alinhamento para o tratamento a laser da rede trabecular. Por exemplo, o material de implante de construção e projeto pode permitir o tratamento a laser do tecido adjacente como um meio de aumentar o fluxo de saída do humor aquoso na região do implante. O tratamento a laser pode ser usado para aumentar a permeabilidade da rede trabecular ou qualquer tecido fibrótico que possa se desenvolver na região do implante. O laser pode ser direcionado para a área desejada de tratamento através da córnea por métodos não invasivos ou pela inserção de uma fibra ótica na câmara anterior. O implante pode ter geometria ou revestimentos opticamente ativos para auxiliar na visualização e tratamento a laser do tecido adjacente.
[0056] Os seguintes exemplos são fornecidos para ilustrar a invenção, mas não são destinados a limitar a invenção de qualquer maneira.
Exemplo 1
[0057] Globos inteiros humanos foram obtidos de um banco de tecido qualificado. Os olhos foram inflados em aproximadamente 10 mm Hg de pressão da câmara anterior e colocados em um recipiente em forma de taça. Uma dissecação esclerótica de retalho único foi executada e o canal de Schlemm foi exposto, permitindo o acesso ao óstio do canal. Uma microcânula oftálmica de diâmetro de 20 mícrons (microcânula iTRACK™, iScience Surgical Corp.) foi usada para canular a circunferência inteira do canal. A microcânula foi designada a fornecer um meio de expandir o canal de Schlemm através da injeção dos materiais viscoelásticos, e compreendia uma ponta sinalizadora iluminada para fornecer indicação visual da localização da microcânula quando no canal.
[0058] A microcânula foi preparada com viscoelástico (Healon GV, Advanced Medical Optics, Inc) e inserida no óstio do canal. Usando uma quantidade mínima de injeção de viscoelástico para abrir o canal e fornecer ambiente lúbrico, a microcânula foi avançada completamente ao redor do canal. A ponta distal foi arrancada do sítio cirúrgico em uma distância suficiente para fixar o dispositivo de implante. Um filamento de polipropileno de aproximadamente 28 microns de diâmetro (Prolene, Ethicon, Inc.) foi fixado na extremidade distal da microcânula, que foi depois retirado puxando o filamento de dentro e ao redor do canal. O filamento foi removido da ponta da microcânula e as duas extremidades fixadas em um nó cirúrgico com tração na curva, desse modo aplicando tração à parede interna do canal de Schlemm e da rede trabecular.
Exemplo 2
[0059] Um globo inteiro humano foi preparação similar ao Exemplo 1 acima. O globo foi colocado em um banho na temperatura ambiente de salina tamponanda de fosfato, e uma agulha de infusão de calibre 30 colocada através da córnea para fornecer entrada de fluido. A agulha foi ligada a um reservatório contendo salina tamponada de fosfato fixado em uma altura de 5,4 polegadas (13,7 cm) sobre a altura da Câmara Anterior para fornecer uma infusão em pressão constante de 10 mm Hg. O circuito de fluido também compreendeu um medidor de fluxo digital (Sensiron, Inc) para registrar as vazões em um computador PC. Uma leitura de fluxo de linha de base estável foi tomada antes da dissecção cirúrgica. O acesso cirúrgico e colocação de implante como descrito no Exemplo 1 acima foi executado, com as exceções de que um acesso de dois retalhos foi usado similar à cirurgia de viscocanalostomia e esclerectomia profunda, e o filamento não foi fixado. As extremidades do filamento foram apresentadas sob o retalho cirúrgico e o retalho cirúrgico foi cuidadosamente selado com adesivo de cianoacrilato sem aderir o filamento nos tecidos. As extremidades do filamento foram fixadas nas pontas de um par de hemostatos. Esta disposição levou em conta a aplicação e liberação de tração à curva do filamento no canal mediante a abertura e fechamento dos hemostatos.
[0060] O globo voltou ao sistema de perfusão e foi deixado se aproximar do equilíbrio de fluxo de saída sem tração sobre o filamento. A tração foi depois aplicada ao filamento mediante a abertura dos hemostatos, e novamente o fluxo de saída foi deixado se estabilizar. A tração e liberação alternadas foram executadas em um intervalo de 15 minutos enquanto se registra as vazões. A vazão mudou de um valor não tensionado de 1,22 ± 0,05 ul/min para um valor tensionado de 1,93 ± 0,01 ul/min, um aumento de 58 %. Ver a Fig. 14.
Exemplo 3
[0061] Em uma outra série de experiências, cada extremidade do filamento de diâmetro de 28 mícrons implantada no cadal de Schlemm foi ligada a níveis de força mecânica de 30 gramas (Wagner Instruments) em uma fixação tal que as forças de tração podem ser aplicadas às extremidades do filamento. As medições de fluxo de saída foram tomadas em três diferentes valores de pressão intraoculares e com tração variável. O valor do Recurso de fluxo de saída foi calculado mediante a divisão da vazão em ul/min pela pressão em mm Hg. Os resultados experimentais indicam um valor ideal para aumentar o recurso de fluxo de saída em uma faixa de tração de aproximadamente 6 a 10 gramas força ao longo do comprimento inteiro do eixo todo de implante, ou de 0,159 a 0,265 grama por mm de comprimento de arco do canal para um diâmetro de 12 mm nominal da curvatura do canal. O fluxo de saída foi significativamente aumentado na faixa de tração de 1 a 11 gramas força ou de 0,027 a 0,292 grama força por mm de comprimento de arco do canal para um diâmetro de 12 mm nominal da curvatura do canal. Outro aumento na tração levaria a um decréscimo no recurso de fluxo de saída até o ponto de falência dos tecidos. Ver a Fig. 15.
Exemplo 4
[0062] Em uma série de experiências, um dispositivo de tração para o filamento foi testado. O dispositivo de tração consistia de uma micro mola de extração fabricada de liga de níquel-titânio (Nitinol). O elemento de molar era compreendido de fio de 38 mícrons de diâmetro, enrolado em uma hélice acondicionada fechada (molar) com um diâmetro externo de 175 mícrons e um comprimento de espiral ativa de 1,1 mm. As extremidades da mola foram configuradas em curvas fechadas em ângulos retos ao eixo da molar, para a ligação ao implante filamentoso. A mola foi designada para funcionar na região superelástica linear de Nitinol para fornecer uma força de mola linear na faixa de 4 a 6 gramas força/mm. O elemento de mola foi encaixado em um tubo de poliimida de parede fina com extremidades abertas. A mola foi estendida em um comprimento de aproximadamente 4 mm e depois mantida em extração com prendedores de fio pequenos repousando entre uma curva de mola e o alojamento de tubo de poliimida. Desta maneira, a mola pode ser ligada a uma curva do filamento enquanto se estende e após a liberação dos prendedores de fio, a mola deve comprimir desse modo colocando tração sobre a curva proporcional à quantidade de deflexão da mola. A tração no filamento pode ser determinada pelo exame visual da quantidade de extração da mola.
[0063] Os globos inteiros humanos enucleados foram preparados como no Exemplo 2 acima. As experiências comparativas foram trabalhadas usando o filamento de polipropileno por si mesmo como o grupo de controle e o dispositivo de tração como o grupo de teste. No grupo de controle, o filamento foi separado em uma curva usando um nó deslizante e aplicada tanta tração quanto possa ser razoavelmente obtida com técnicas manuais. No grupo de teste, a mola estendida do dispositivo de tração foi ligada em cada extremidade do filamento, o afrouxamento foi removido da curva e os prendedores liberados removidos permitindo a mola retrair e tensionar o filamento.
[0064] A experiência foi repetida quatro vezes com um aumento significativo no fluxo de saída (aproximadamente duas vezes os valores de controle) observado em 3 das 4 experiências. A quarta experiência não indicou nenhuma mudança aparente. Ver a Fig. 16. Além de tudo, um aumento médio no fluxo de saída de aproximadamente 75 % foi demonstrado pelo uso do filamento com um dispositivo de tração.
Exemplo 5
[0065] Uma experiência foi preparada como no Exemplo 3 acima. Nesta experiência, um filamento de aço inoxidável de 25 mícrons de diâmetro foi colocado na e ao redor da circunferência do canal de Schlemm e depois ligado aos níveis de força mecânica para medir a tração aplicada no filamento e na parede interna do canal. Um sistema de formação de imagem por ultra-som de alta resolução (iVIEW™ imaging system, iScience Surgical Corp) foi usado para tirar imagens em corte transversal do canal com o filamento implantado sob diferentes tensões. As imagens foram tiradas em 0, 5, 10, 15 e 20 gramas de tração sobre o filamento. As imagens indicam uma distração crescente do canal de Schlemm com tração crescente do filamento. Foi observado que o canal de Schlemm era visível com um lúmen aberto em todas as tensões aplicadas, incluindo em tensões de filamento que demonstraram pouco ou nenhum aumento no fluxo de saída aquoso ou recurso aquoso (0, 20 gramas de tração aplicada). Estes resultados indicam a importância da quantidade apropriada de tração aplicada à parede interna do canal de Schlemm e da rede trabecular para aumentar o fluxo de saída aquoso.
[0066] A descrição precedente das formas de realização específicas revela a natureza geral da invenção para que outros possam facilmente modificar e/ou adaptar as várias aplicações de tais formas de realização específicas sem divergir do conceito geral. Portanto, tais adaptações e modificações devem ser e são destinadas a serem compreendidas dentro do significado e faixa de equivalentes das formas de realização divulgadas. Deve ficar compreendido que a fraseologia ou terminologia aqui empregada é para o propósito de descrição e não de limitação.