WO2023113300A1 - 신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 - Google Patents
신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 Download PDFInfo
- Publication number
- WO2023113300A1 WO2023113300A1 PCT/KR2022/019093 KR2022019093W WO2023113300A1 WO 2023113300 A1 WO2023113300 A1 WO 2023113300A1 KR 2022019093 W KR2022019093 W KR 2022019093W WO 2023113300 A1 WO2023113300 A1 WO 2023113300A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- proline
- amino acid
- trans
- group
- macular degeneration
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Ophthalmology & Optometry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
본 발명은 신규한 펩타이드를 포함하는 황반변성의 예방 또는 치료용 조성물에 관한 것이다. 구체적으로, 본 발명의 펩타이드는 황반변성의 주요 발병 원인인 맥락막 혈관신생을 억제하는 우수한 효과를 가지고, 우수한 안정성 및 용해도를 나타내기 때문에, 우수한 황반변성 치료제로 개발이 가능하다.
Description
본 발명은 신규한 펩타이드를 포함하는 황반변성의 예방 또는 치료용 조성물에 관한 것이다. 구체적으로, 본 발명의 펩타이드는 황반변성의 주요 발병 원인인 맥락막혈관신생을 억제하는 효과를 가지며, 우수한 안정성 및 용해도를 갖는다.
황반은 망막이라는 안구 내 신경층에서 가장 중요한 역할을 수행하는 부위로, 약 1.5mm의 반지름을 가지는 망막의 중심부위이며, 이 부위에는 빛을 느낄 수 있는 광수용체가 밀집되어 있다. 따라서 황반은 망막의 중심부로 시력의 대부분을 담당한다. 황반변성은 이러한 황반이 노화, 유전적인 요인, 독성, 염증 등에 의해 변성되는 질환이다. 황반이 변성되면서 시력이 감소되고, 심할 경우 시력을 완전히 잃기도 한다.
황반변성은 크게 비삼출성(건성)과 삼출성(습성)으로 구분하게 되는데, 비삼출성 황반변성은 전체 황반변성의 80-90%를 차지하고 있으며 망막 및 맥락막 위축이 나타나는 후기를 제외하고는 대부분 시력에 큰 영향을 주지 않는다. 그러나 삼출성 황반변성으로 진행할 수 있어 주의가 필요하다. 삼출성 황반변성은 전체 황반변성의 10-20% 정도를 차지하지만, 치료하지 않고 그대로 방치해두면 시력이 빠르게 저하되어 많은 환자들이 진단 후 2년 내에 실명에 이르게 된다.
삼출성 황반변성은 맥락막 신생혈관이 발생한 단계로, 시력 예후가 매우 나빠서 65세 이상 인구에서 실명의 빈도가 가장 높은 질환이다. 맥락막이라 불리는 혈관층은 망막층에 영양물질을 공급하고 망막세포에서 나오는 대사물질을 제거하는 역할을 한다. 그러나 노화 등의 원인으로 인해 맥락막의 혈관이 망막세포 부분까지 뚫고 나와 비정상적으로 생성되는 경우가 있는데, 이 때의 비정상적인 혈관들을 맥락막 신생혈관이라고 한다. 이 혈관은 비정상적인 혈관이기 때문에 매우 약하고 터지기 쉬워 삼출물과 혈액이 흘러나와 황반 부위에 손상을 입히게 된다.
황반변성의 치료는 비삼출성 황반변성의 경우 황반변성의 진행을 낮추는 것으로 알려진 항산화 비타민제의 복용과 황반변성의 위험인자인 고혈압, 고지혈증 등에 대한 치료를 한다. 삼출성 황반변성의 경우 열레이저광응고술, 광역학치료, 항체주사, 유리체절제술 등이 있으나, 아직까지 완전한 치료법은 없고 이에 관한 활발한 연구가 진행 중이다. 최근에는 애플리버셉트, 라니비주맙, 베바시주맙과 같은 항혈관내피성장인자 항체(Anti-VEGF antibody)를 눈 속으로 주사하는 방법이 주로 사용되고 있으나, 반복적인 투여해야 하고 고가의 비용 등의 단점이 있다.
이에, 본 발명자들은 황반변성을 효과적으로 치료할 수 있는 물질에 대한 연구 결과, 우수한 안정성 및 용해도뿐만 아니라 맥락막 혈관신생을 억제하는 우수한 효과를 갖는 신규한 펩타이드 확인하여, 본 발명을 완성하였다.
[선행기술문헌]
[특허문헌]
(특허문헌 1) 한국공개특허 제10-2020-0060397호
본 발명은 화학식 1로 표시되는 펩타이드를 포함하는 황반변성의 예방 또는 치료용 약학 조성물을 제공하는 것을 목적으로 한다.
또한, 본 발명은 서열번호 1 내지 45의 아미노산 서열로 이루어진 펩타이드를 포함하는 황반변성의 예방 또는 치료용 약학 조성물을 제공하는 것을 목적으로 한다.
본 발명은 하기 화학식 1로 표시되는 펩타이드를 포함하는 것을 특징으로 하는 황반변성 예방 또는 치료용 약학 조성물을 제공한다.
[화학식 1]
X1-X2-X3-X4-X5-X6-X7
상기 식에서, X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 비극성 아미노산(non-polar amino acid)이고,
X6은 없거나, 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 없거나, 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산이고,
여기서, X6이 없는 경우, X7도 없다.
일 실시태양에서, 상기 식에서 X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 글리신(Glycine), 페닐-글리신(phenyl-Glycine), 알라닌(Alanine), 발린(Valine), 류신(Leucine), tert-류신(tert-Leucine) 및 2-아미노이소부티르산(2-aminoisobutyric acid)으로 이루어진 군에서 선택된 아미노산이고,
X6은 없거나, 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 없거나, 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산일 수 있고, 여기서, X6이 없는 경우, X7도 없다.
일 실시태양에서, 상기 식에서 X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 비극성 아미노산(non-polar amino acid)이고,
X6은 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산일 수 있다.
일 실시태양에서, 상기 식에서 X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 글리신(Glycine), 페닐-글리신(phenyl-Glycine), 알라닌(Alanine), 발린(Valine), 류신(Leucine), tert-류신(tert-Leucine) 및 2-아미노이소부티르산(2-aminoisobutyric acid)으로 이루어진 군에서 선택된 아미노산이고,,
X6은 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산일 수 있다.
일 실시태양에서, 상기 식에서 X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 글루타메이트(Glutamate) 또는 D-글루타메이트(D-Glutamate)이고,
X5는 2-아미노이소부티르산(2-aminoisobutyric acid)이고,
X6은 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산일 수 있다.
본 발명의 조성물은 서열번호 1 내지 45의 아미노산 서열로 이루어진 군에서 선택된 어느 하나의 펩타이드를 포함할 수 있으며, 바람직하게는 서열번호 43의 아미노산 서열로 이루어진 펩타이드를 포함할 수 있다.
본 발명의 펩타이드는 맥락막 혈관신생(CNV)을 억제하는 효과를 갖는다.
본 발명의 황반변성은 습성 황반변성, 건성 황반변성 및 노인성 황반변성으로 이루어진 군으로부터 선택된 하나 이상일 수 있다.
본 발명은 하기 화학식 1로 표시되는 펩타이드를 황반변성 질환을 갖는 대상에 투여하는 것을 포함하는 황반변성의 치료방법을 제공한다.
[화학식 1]
X1-X2-X3-X4-X5-X6-X7
상기 식에서, X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 비극성 아미노산(non-polar amino acid)이고,
X6은 없거나, 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 없거나, 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산이고,
여기서, X6이 없는 경우, X7도 없다.
본 발명은 상기 화학식 1로 표시되는 펩타이드를 포함하는 황반변성의 치료 또는 예방의 용도를 위한 조성물을 제공한다.
본 발명은 상기 화학식 1로 표시되는 펩타이드를 포함하는 황반변성의 치료 또는 예방을 위한 조성물의 용도를 제공한다.
본 발명의 펩타이드는 우수한 안정성 및 용해도를 가지며, 황반변성의 주요 발병 원인인 맥락막 혈관신생을 억제하는 우수한 효과를 가짐으로써, 황반변성의 예방 또는 치료를 위해 유용하게 사용될 수 있다.
도 1 및 도 2는 본 발명의 펩타이드의 CNV에 대한 FFA(Fundus Fluorescein Angiogrpahy) 측정 및 CTF(Corrected Total Fluorescence) 산출 결과를 나타낸다.
도 3 및 도 4는 본 발명의 펩타이드의 CNV에 대한 OCT(Optical coherence tomography) 측정 및 CNV 병변 크기 산출 결과를 나타낸다.
도 5는 본 발명의 펩타이드의 CNV에 대한 망막전위도검사(Electroretinography) 결과를 나타낸다.
도 6 및 도 7은 본 발명의 실시예 43(002-175)의 펩타이드 및 이를 포함하는 점안액의 CNV에 대한 FFA(Fundus Fluorescein Angiogrpahy) 측정 및 혈관누수(vascular leakage) 정량화 결과를 나타낸다.
도 8 및 도 9는 본 발명의 실시예 43(002-175)의 펩타이드 및 이를 포함하는 점안액의 CNV에 대한 OCT(Optical coherence tomography) 측정 및 CNV 병변 크기 산출 결과를 나타낸다.
도 10 및 도 11은 본 발명의 실시예 43(002-175)의 펩타이드를 포함하는 점안액의 CNV에 대한 FFA(Fundus Fluorescein Angiogrpahy) 측정 및 신생혈관 부위 산출 결과를 나타낸다.
이하, 첨부한 도면을 참조하여 본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자가 용이하게 실시할 수 있도록 본원의 실시태양 및 실시예를 상세히 설명한다. 그러나 본원은 여러 가지 형태로 구현될 수 있으며 여기에서 설명하는 실시태양 및 실시예에 한정되지 않는다.
본원 명세서 전체에서, 어떤 부분이 어떤 구성 요소를 "포함" 한다고 할 때, 이는 특별히 반대되는 기재가 없는 한 다른 구성 요소를 제외하는 것이 아니라 다른 구성 요소를 더 포함할 수 있는 것을 의미한다.
본 발명은 하기 화학식 1로 표시되는 펩타이드를 포함하는 것을 특징으로 하는 황반변성의 예방 또는 치료용 약학 조성물을 제공한다.
[화학식 1]
X1-X2-X3-X4-X5-X6-X7
상기 식에서, X1은 프롤린(Proline), 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline), 트랜스-4-하이드록시-D-프롤린(Trans-4-hydroxy-D-proline), 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline), 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline), 4-메틸렌-L-프롤린(4-methylene-L-proline), 4,4-디메틸-L-프롤린(4,4-dimethyl-L-proline), 및 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)으로 이루어진 군에서 선택된 아미노산이고,
X2는 글리신(Glycine)이고,
X3은 글루타민(Glutamine) 또는 D-글루타민(D-Glutamine)이고,
X4는 아스파르테이트(Aspartate), D-아스파르테이트(D-Aspartate), 글루타메이트(Glutamate), 및 D-글루타메이트(D-Glutamate)로 이루어진 군에서 선택된 아미노산이고,
X5는 비극성 아미노산(non-polar amino acid)이고,
X6은 없거나, 류신(Leucine) 또는 D-류신(D-Leucine)이고,
X7은 없거나, 알라닌(Alanine), D-알라닌(D-Alanine), 및 알라닌-이소프로필에스테르(Alanine-isopropyl ester)로 이루어진 군에서 선택된 아미노산이고,
여기서, X6이 없는 경우, X7도 없다.
본 발명의 펩타이드는 하기 표 1의 펩타이드로 이루어진 군으로부터 선택된 펩타이드일 수 있다.
| 실시예 | 펩타이드 번호 | 아미노산 서열 | 서열번호 | ||||||
| 1 | 002-053 | Hyp | Gly | Gln | Asp | Val | 1 | ||
| 2 | 002-074 | Hyp | Gly | Gln | Asp | Leu | 2 | ||
| 3 | 002-075 | Hyp | Gly | Gln | Asp | Ala | 3 | ||
| 4 | 002-103 | Hyp | Gly | D-Gln | Asp | Gly | 4 | ||
| 5 | 002-104 | Hyp | Gly | Gln | D-Asp | Gly | 5 | ||
| 6 | 002-085 | D-Hyp | Gly | Gln | Asp | Gly | 6 | ||
| 7 | 002-076 | Hyp | Gly | Gln | Asp | Val | Leu | 7 | |
| 8 | 002-077 | Hyp | Gly | Gln | Asp | Leu | Leu | 8 | |
| 9 | 002-078 | Hyp | Gly | Gln | Asp | Ala | Leu | 9 | |
| 10 | 002-105 | Hyp | Gly | D-Gln | Asp | Gly | Leu | 10 | |
| 11 | 002-106 | Hyp | Gly | Gln | D-Asp | Gly | Leu | 11 | |
| 12 | 002-107 | Hyp | Gly | Gln | Asp | Gly | D-Leu | 12 | |
| 13 | 002-090 | D-Hyp | Gly | Gln | Asp | Gly | Leu | 13 | |
| 14 | 002-055 | Hyp | Gly | Gln | Asp | Val | Leu | Ala | 14 |
| 15 | 002-080 | Hyp | Gly | Gln | Asp | Leu | Leu | Ala | 15 |
| 16 | 002-081 | Hyp | Gly | Gln | Asp | Ala | Leu | Ala | 16 |
| 17 | 002-084 | Hyp | Gly | Gln | Asp | Gly | Leu | Ala-IPE | 17 |
| 18 | 002-108 | Hyp | Gly | D-Gln | Asp | Gly | Leu | Ala | 18 |
| 19 | 002-109 | Hyp | Gly | Gln | D-Asp | Gly | Leu | Ala | 19 |
| 20 | 002-110 | Hyp | Gly | Gln | Asp | Gly | D-Leu | Ala | 20 |
| 21 | 002-111 | Hyp | Gly | Gln | Asp | Gly | Leu | D-Ala | 21 |
| 22 | 002-086 | cis-4F-Pro | Gly | Gln | Asp | Gly | 22 | ||
| 23 | 002-087 | trans-4NH2-Pro | Gly | Gln | Asp | Gly | 23 | ||
| 24 | 002-088 | 4,4-difluoro-Pro | Gly | Gln | Asp | Gly | 24 | ||
| 25 | 002-089 | 4-methylene-Pro | Gly | Gln | Asp | Gly | 25 | ||
| 26 | 002-100 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | 26 | ||
| 27 | 002-091 | cis-4F-Pro | Gly | Gln | Asp | Gly | Leu | 27 | |
| 28 | 002-092 | trans-4NH2-Pro | Gly | Gln | Asp | Gly | Leu | 28 | |
| 29 | 002-093 | 4,4-difluoro-Pro | Gly | Gln | Asp | Gly | Leu | 29 | |
| 30 | 002-094 | 4-methylene-Pro | Gly | Gln | Asp | Gly | Leu | 30 | |
| 31 | 002-101 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | Leu | 31 | |
| 32 | 002-095 | D-Hyp | Gly | Gln | Asp | Gly | Leu | Ala | 32 |
| 33 | 002-096 | cis-4F-Pro | Gly | Gln | Asp | Gly | Leu | Ala | 33 |
| 34 | 002-099 | 4-methylene-Pro | Gly | Gln | Asp | Gly | Leu | Ala | 34 |
| 35 | 002-102 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | Leu | Ala | 35 |
| 36 | 002-130 | Hyp | Gly | Gln | Glu | Gly | 36 | ||
| 37 | 002-170 | Hyp | Gly | Gln | Glu | Val | 37 | ||
| 38 | 002-167 | Hyp | Gly | Gln | Glu | Leu | Leu | 38 | |
| 39 | 002-168 | Hyp | Gly | Gln | Glu | Val | Leu | 39 | |
| 40 | 002-132 | Hyp | Gly | Gln | Glu | Gly | Leu | Ala | 40 |
| 41 | 002-165 | Hyp | Gly | Gln | Glu | Leu | Leu | Ala | 41 |
| 42 | 002-166 | Hyp | Gly | Gln | Glu | Val | Leu | Ala | 42 |
| 43 | 002-175 | Hyp | Gly | Gln | Glu | Aib | Leu | Ala | 43 |
| 44 | 002-176 | Hyp | Gly | Gln | Glu | tert-Leu | Leu | Ala | 44 |
| 45 | 002-177 | Hyp | Gly | Gln | Glu | phenyl-Gly | Leu | Ala | 45 |
본 발명에서 사용된 용어 "황반변성(macular degeneration)"은 황반이 노화, 유전적인 요인, 독성, 염증 등에 의해 기능이 떨어지면서 시력이 감소되고, 심할 경우 시력을 완전히 잃기도 하는 질환을 의미한다.
본 발명에서 상기 황반변성은 습성 및 건성 황반변성, 노인성 황반변성일 수 있으며, 이에 한정되는 것은 아니다.
본 발명에서 사용된 용어 "맥락막 혈관신생(choroidal neovascularization; CNV)"은 새로운 맥락막 모세혈관이 생성되는 과정을 의미하는 것이다. 맥락막은 안구의 고혈관막으로 이들이 발견되는 주변부에 위치한 홍채 및 망막에 영양을 공급하는 미세한 모세관의 복잡한 망상구조를 말하는데, 병리학적으로 맥락막 혈관신생은 맥락막으로부터 줄기가 형성된 비정상적인 혈관 및 부르크막의 구조 변형 및 파괴로 인해 망막 밑 공간이 침해되는 것을 의미한다.
본 발명에서 사용된 용어 "혈관신생"은 혈관이 새로 형성되는 과정, 즉, 새로운 혈관이 세포, 조직 또는 기관 내로 발생되는 것을 의미하며, "신생혈관"은 혈관신생 과정을 통해 새로 생성된 혈관을 의미한다. 본원에서 "혈관신생"과 "신생혈관"은 서로 바꾸어 기재할 수 있다.
본 발명에서 사용한 CNV 동물모델은 레이저 슬릿 시스템(Laser slit system)을 이용하여 C57BL/6 마우스의 맥락막에 레이저(laser)를 조사하여 병변을 유도한 마우스 모델이다. 1979년 처음 기술된 레이저 유도 CNV 모델은 광응고법(photocoagulation)을 사용하여 부르크(Bruch)의 막을 교란시켜 맥락막 신생혈관의 성장을 망막 영역으로 유도한 것으로, 신생혈관이 맥락막에서부터 발생한다는 점에서 사람 망막 내에서 발생되는 신생혈관 질병, 즉 습성 황반변성(wet AMD)과 발생 형태가 유사하다. 또한, 상기 레이저 유도 CNV 모델은 신생혈관 AMD에 대한 항혈관 내피 성장 인자(VEGF) 치료의 임상 효능을 예측하는 데 성공했으며, 기존 치료제들의 개발 단계에서 활용되는 동물모델이다(Gong Y, Li J, Sun Y, Fu Z, Liu C-H, Evans L, et al. (2015) Optimization of an Image-Guided Laser-Induced Choroidal Neovascularization Model in Mice. PLoS ONE 10(7)).
본 발명에서, Pro는 프롤린(Proline)이고,
Hyp는 트랜스-4-하이드록시-L-프롤린(Trans-4-hydroxy-L-proline)이고,
D Hyp는 트랜스-4-하이드록시-D-프롤린(Trans-4-Hydroxy-D-proline)이고,
cis-4F-Pro는 시스-4-플루오로-L-프롤린(Cis-4-fluoro-L-proline)이고,
4,4-difluoro-Pro는 4,4,-디플루오로-L-프롤린(4,4-difluoro-L-proline)이고,
4-methylene-Pro는 4-메틸렌-L-프롤린(4-methylene-L-proline)이고,
4,4-dimethyl Pro는 4,4-디메틸-L-프롤린(4,4-Dimethyl-L-proline)이고,
trans-4NH2-Pro는 트랜스-4-아미노-L-프롤린(Trans-4-amino-L-proline)이고,
Gly는 글리신(Glycine)이고,
Gln은 글루타민(Glutamine)이고,
D-Gln는 D-글루타민(D-Glutamine)이고,
Ala는 알라닌(Alanine)이고,
D-Ala는 D-알라닌(D-Alanine)이고,
Val은 발린(Valine)이고,
Leu는 류신(Leucine)이고,
D-Leu는 D-류신(D-Leucine)이고,
Ile는 이소류신(Isoleucine)이고,
Met는 메티오닌(Methionine)이고,
Tert-Leu은 tert-류신(Tert-Leucine)이며, L-알파-tert-부틸글리신(L-α-tert-Butylglycine)이고,
Aib는 2-아미노이소부티르산(2-aminoisobutyric acid)이고,
Isopropyl ester (IPE)는 아미노산 말단기에 이소프로필 에스테르(Isopropyl ester)로 치환된 유도체이고,
Ser은 세린(Serine)이고,
Thr은 트레오닌(Threonine)이고,
Cys는 시스테인(Cycteine)이고,
Asn는 아스파라긴(Asparagine)이고,
Phe는 페닐알라닌(Phenylalanine)이고,
Tyr은 티로신(Tyrosine)이고,
Trp는 트립토판(Tryptophan)이고,
Lys는 리신(Lysine)이고,
Arg는 아르기닌(Arginine)이고,
His는 히스티딘(Histidine)이고,
Asp는 아스파르테이트(Aspartate) 또는 아스파르트산(Aspartic acid)이고,
D-Asp는 D-아스파르테이트(D-Aspartate) 또는 D-아스파르트산(D-Aspartic acid)이고,
Glu는 글루타메이트(Glutamate) 또는 글루탐산(Glutamic acid)이고,
D-Glu는 D-글루타메이트(Glutamate) 또는 D-글루탐산(Glutamic acid)이다.
본 발명에서 극성 아미노산(polar amino acid)은 아미노산의 화학구조상 그 곁사슬이 극성을 갖는 아미노산을 의미하며, Thr, Ser, Cys, Asn, Gln, Asp, Glu, His, Lys, Arg가 포함되며 이에 한정되지 않는다.
본 발명에서 비극성 아미노산(non-polar amino acid)은 아미노산의 화학구조상 그 곁사슬이 극성을 갖지 않는 아미노산을 의미하며, Met, Leu, Pro, Ala, Gly, Val, Ile, Aib가 포함되며, 이에 한정되지 않는다.
본 발명에 사용된 용어 "예방"은 조성물의 투여에 의해 질환의 발병을 억제 또는 지연시키는 모든 행위를 의미하고, "치료"는 조성물의 투여에 의해 질환의 의심 및 발병 개체의 증상이 호전되거나 이롭게 변경되는 모든 행위를 의미한다.
이하 실시예를 통하여 본 발명을 더욱 상세하게 설명하고자 하나, 하기의 실시예는 단지 설명의 목적을 위한 것이며 본원 발명의 범위를 한정하고자 하는 것은 아니다.
[제조예]
본 발명의 펩타이드는 기존에 공지된 고체상 펩타이드 합성법(Solid Phase Peptide Synthesis, SPPS)을 기반으로 합성하였고, 제조공정은 하기의 단계를 포함하였다.
단계 1: 레진 불림 및 로딩
단계 2: 고체상 펩타이드 합성법(Solid Phase Peptide Synthesis, SPPS)
단계 3: 탈 보호화 된 펩타이드 합성(Global cleavage)
단계 4: 1차 정제 및 농축/ 2차 정제 및 농축
단계 5: 동결건조
상기 고체상 펩타이드 합성법(SPPS)은 첫번째 아미노산을 레진에 로딩하여 아미노산 N- 말단의 Fmoc 탈 보호 후 아미노산 서열에 따라 아미노산 커플링을 하고, 상기 보호화 된 펩타이드는 고상반응기에서 합성되는 단계를 포함한다. 또한, 상기 아미노산 커플링은 첫번째 아미노산을 레진에 로딩 후 아미노산 N-말단의 Fmoc을 제거하는 단계; 반응 완료 후 용매를 제거하고 레진을 세척하는 단계; 서열에 따라 다음 아미노산의 커플링을 진행하는 단계; 반응 완료 후 용매를 제거하고 레진을 세척하는 단계; 이후 최종 아미노산 서열이 생성될 때까지 위의 과정을 반복하는 단계를 포함하였다.
각 아미노산의 알파 아민 그룹은 염기에 약한 Fmoc 그룹으로 보호화 되어있고, 곁사슬의 작용기는 산에 약한 그룹으로 보호화 되어있다. Gly, Aib를 제외한 모든 아미노산은 L-configuration이며, 그 중 다음과 같이 몇 가지 아미노산 Hyp(tBu), Glu(tBu), Gln(Trt)는 특유의 보호그룹을 가지고 있다. 그리고 Ala, Leu, Aib, Gly과 같은 아미노산들은 곁사슬의 보호기를 가지고 있지 않다. 따라서 시퀀스에 따라 아미노산 커플링 완료 후 Crude 펩타이드를 얻기 위해 펩타이드에서 레진과 보호기를 제거하였다. 그 후 정제 및 농축과 동결건조를 통하여 실시예 1 내지 45의 펩타이드 화합물을 수득하였다.
[시험예 1]
펩타이드의 맥락막혈관신생 억제 효능 평가: CNV 부위의 형광값(CTF; Corrected total fluorescence) 측정
본 발명의 펩타이드의 맥락막혈관신생(CNV; choroidal neovascularization) 억제 효능을 평가하기 위해 하기와 같이 실험을 수행하였다.
7-8주령의 C57BL/6 마우스에 산동제를 점안하여 동공을 확장하고 Ketamine(50 mg/Kg)와 Rompun(23.32 mg/Kg)을 복강 내 주사하여 마취하였다. Slit-lamp laser injection system을 이용하여 레이저를 마우스의 각 안구의 맥락막에 12시, 3시, 6시, 9시 방향으로 4번씩 조사하였다. 이때 레이저 조사 조건은 532 nm, 80 msec, 240mW로 하였다. 레이저 조사 직후 시린지를 이용하여 PBS에 녹인 10 mg/mL 농도의 펩타이드, 또는 20 mg/mL 농도의 애플리버셉트(aflibercept)를 유리체 내에 각각 1 ul씩 주사하였다. 약물 투여 10일 후 마우스를 마취하고 복강에 2% fluorescein을 투여하여 혈관을 염색하였다. Fluorescein 투여 2~3분후 망막을 촬영하였다. 레이저에 의하여 유도된 CNV 병변은 imageJ program을 이용하여 크기 및 형광값을 측정하였고 개체간 차이를 줄이기 위하여 background를 제거해 줌으로써 CTF(Corrected total fluorescence)을 산출하여 각 군의 값을 비교하였다. 모든 시험의 결과는 평균 ± 표준편차로 나타내고, one-way ANOVA 및 Kruskal-wallis test를 이용하여 유의성을 검증하였다.
상기 실험 결과를 하기 표 2, 및 도 1 및 2에 나타내었다.
| 실시예 | 펩타이드 번호 | 아미노산 서열 | CTF* | |||||||
| 1 | 002-053 | Hyp | Gly | Gln | Asp | Val | +++ | |||
| 2 | 002-074 | Hyp | Gly | Gln | Asp | Leu | + | |||
| 3 | 002-075 | Hyp | Gly | Gln | Asp | Ala | + | |||
| 4 | 002-103 | Hyp | Gly | D-Gln | Asp | Gly | + | |||
| 5 | 002-104 | Hyp | Gly | Gln | D-Asp | Gly | + | |||
| 6 | 002-085 | D-Hyp | Gly | Gln | Asp | Gly | + | |||
| 7 | 002-076 | Hyp | Gly | Gln | Asp | Val | Leu | ++ | ||
| 8 | 002-077 | Hyp | Gly | Gln | Asp | Leu | Leu | ++ | ||
| 9 | 002-078 | Hyp | Gly | Gln | Asp | Ala | Leu | ++ | ||
| 10 | 002-105 | Hyp | Gly | D-Gln | Asp | Gly | Leu | + | ||
| 11 | 002-106 | Hyp | Gly | Gln | D-Asp | Gly | Leu | + | ||
| 12 | 002-107 | Hyp | Gly | Gln | Asp | Gly | D-Leu | + | ||
| 13 | 002-090 | D-Hyp | Gly | Gln | Asp | Gly | Leu | ++ | ||
| 14 | 002-055 | Hyp | Gly | Gln | Asp | Val | Leu | Ala | ++ | |
| 15 | 002-080 | Hyp | Gly | Gln | Asp | Leu | Leu | Ala | ++ | |
| 16 | 002-081 | Hyp | Gly | Gln | Asp | Ala | Leu | Ala | + | |
| 17 | 002-084 | Hyp | Gly | Gln | Asp | Gly | Leu | Ala-IPE | ++ | |
| 18 | 002-108 | Hyp | Gly | D-Gln | Asp | Gly | Leu | Ala | + | |
| 19 | 002-109 | Hyp | Gly | Gln | D-Asp | Gly | Leu | Ala | + | |
| 20 | 002-110 | Hyp | Gly | Gln | Asp | Gly | D-Leu | Ala | + | |
| 21 | 002-111 | Hyp | Gly | Gln | Asp | Gly | Leu | D-Ala | + | |
| 22 | 002-086 | cis-4F-Pro | Gly | Gln | Asp | Gly | + | |||
| 23 | 002-087 | trans-4NH2-Pro | Gly | Gln | Asp | Gly | ++ | |||
| 24 | 002-088 | 4,4-difluoro-Pro | Gly | Gln | Asp | Gly | + | |||
| 25 | 002-089 | 4-methylene-Pro | Gly | Gln | Asp | Gly | + | |||
| 26 | 002-100 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | + | |||
| 27 | 002-091 | cis-4F-Pro | Gly | Gln | Asp | Gly | Leu | +++ | ||
| 28 | 002-092 | trans-4NH2-Pro | Gly | Gln | Asp | Gly | Leu | + | ||
| 29 | 002-093 | 4,4-difluoro-Pro | Gly | Gln | Asp | Gly | Leu | + | ||
| 30 | 002-094 | 4-methylene-Pro | Gly | Gln | Asp | Gly | Leu | + | ||
| 31 | 002-101 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | Leu | + | ||
| 32 | 002-095 | D-Hyp | Gly | Gln | Asp | Gly | Leu | Ala | + | |
| 33 | 002-096 | cis-4F-Pro | Gly | Gln | Asp | Gly | Leu | Ala | + | |
| 34 | 002-099 | 4-methylene-Pro | Gly | Gln | Asp | Gly | Leu | Ala | + | |
| 35 | 002-102 | 4,4-dimethyl Pro | Gly | Gln | Asp | Gly | Leu | Ala | + | |
| 36 | 002-130 | Hyp | Gly | Gln | Glu | Gly | + | |||
| 37 | 002-170 | Hyp | Gly | Gln | Glu | Val | + | |||
| 38 | 002-167 | Hyp | Gly | Gln | Glu | Leu | Leu | + | ||
| 39 | 002-168 | Hyp | Gly | Gln | Glu | Val | Leu | + | ||
| 40 | 002-132 | Hyp | Gly | Gln | Glu | Gly | Leu | Ala | + | |
| 41 | 002-165 | Hyp | Gly | Gln | Glu | Leu | Leu | Ala | + | |
| 42 | 002-166 | Hyp | Gly | Gln | Glu | Val | Leu | Ala | + | |
| 43 | 002-175 | Hyp | Gly | Gln | Glu | Aib | Leu | Ala | ++ | |
| 44 | 002-176 | Hyp | Gly | Gln | Glu | tert-Leu | Leu | Ala | + | |
| 45 | 002-177 | Hyp | Gly | Gln | Glu | phenyl-Gly | Leu | Ala | + | |
| PBS | - | |||||||||
| 애플리버셉트(aflibercept) | + | |||||||||
| *CTF 값 | + | : 300,000 ~ 800,000 | ||||||||
| ++ | : 200,000 ~ 300,000 | |||||||||
| +++ | : 100,000 ~ 200,000 | |||||||||
상기 표 2, 및 도 1 및 2에 나타낸 바와 같이, CNV 부위의 형광값을 측정한 결과, 본 발명의 펩타이드는 CNV 억제 효과를 갖는 것을 확인하였고, 특히 실시예 1(002-053), 실시예 7(002-076), 실시예 8(002-077), 실시예 9(002-078), 실시예 13(002-090), 실시예 14(002-055), 실시예 15(002-080), 실시예 17(002-084), 실시예 23(002-087), 실시예 27(002-091), 및 실시예 43(002-175)의 펩타이드가 매우 우수한 억제 효능을 나타내었다.
따라서 본 발명의 펩타이드는 우수한 CNV 억제 효능을 갖는 것을 알 수 있다.
[시험예 2]
펩타이드의 맥락막혈관신생 억제 효능 평가: 광간섭단층영상(Optical Coherence Tomography)
본 발명의 펩타이드의 CNV(choroidal neovascularization; 맥락막혈관신생) 억제 효능을 평가하기 위해 하기와 같이 실험을 수행하였다.
7-8주령의 C57BL/6 마우스에 산동제를 점안하여 동공을 확장하고 Ketamine(50 mg/Kg)와 Rompun(23.32 mg/Kg)을 복강 내 주사하여 마취하였다. Slit-lamp laser injection system을 이용하여 레이저를 마우스의 각 안구의 맥락막에 12시, 3시, 6시, 9시 방향으로 4번씩 조사하였다. 이때 레이저 조사 조건은 532 nm, 80 msec, 240mW로 하였다. 레이저 조사 직후 시린지를 이용하여 PBS에 녹인 10 mg/mL 농도의 펩타이드, 또는 20 mg/mL 농도의 애플리버셉트(aflibercept)를 유리체 내에 각각 1 ul씩 주사하였다. 약물 투여 10일 후 마우스를 마취하고, 레이저에 의하여 유도된 CNV 병변은 각 화상(burn)당 OCT beam을 투과시켜 ImageJ program을 이용하여 μm2으로 산출하여 나타내었다. 모든 시험의 결과는 평균 ± 표준편차로 나타내고, one-way ANOVA 및 Kruskal-wallis test를 이용하여 유의성을 검증하였다.
상기 실험 결과를 하기 표 3, 및 도 3 및 4에 나타내었다.
| 실시예 | 펩타이드 번호 | 아미노산 서열 | 병변의 크기 (μm2) |
||||||
| 1 | 002-053 | Hyp | Gly | Gln | Asp | Val | 5,636 | ||
| 3 | 002-075 | Hyp | Gly | Gln | Asp | Ala | 6,491 | ||
| 7 | 002-076 | Hyp | Gly | Gln | Asp | Val | Leu | 6,046 | |
| 13 | 002-090 | D-Hyp | Gly | Gln | Asp | Gly | Leu | 6,395 | |
| 14 | 002-055 | Hyp | Gly | Gln | Asp | Val | Leu | Ala | 5,407 |
| 15 | 002-080 | Hyp | Gly | Gln | Asp | Leu | Leu | Ala | 6,672 |
| 17 | 002-084 | Hyp | Gly | Gln | Asp | Gly | Leu | Ala-IPE | 5,978 |
| 34 | 002-099 | 4-methylene-Pro | Gly | Gln | Asp | Gly | Leu | Ala | 8,603 |
| 37 | 002-170 | Hyp | Gly | Gln | Glu | Val | 5,775 | ||
| 41 | 002-165 | Hyp | Gly | Gln | Glu | Leu | Leu | Ala | 4,960 |
| 42 | 002-166 | Hyp | Gly | Gln | Glu | Val | Leu | Ala | 6,102 |
| 43 | 002-175 | Hyp | Gly | Gln | Glu | Aib | Leu | Ala | 5,393 |
| PBS | 10,428 | ||||||||
| 애플리버셉트(aflibercept) | 5,437 | ||||||||
상기 표 3, 및 도 3 및 4에 나타낸 바와 같이, CNV 병변의 크기를 측정한 결과, 본 발명의 펩타이드를 주사한 경우 CNV 병변의 크기가 감소하는 것을 확인하였다. 따라서 본 발명의 펩타이드는 우수한 CNV 억제 효능을 갖는 것을 알 수 있다.
[시험예 3]
펩타이드의 맥락막혈관신생 억제 효능 평가: 망막전위도검사(Electroretinography)
본 발명의 펩타이드의 CNV(choroidal neovascularization; 맥락막혈관신생) 억제 효능을 평가하기 위해 하기와 같이 실험을 수행하였다.
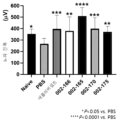
7-8주령의 C57BL/6 마우스에 산동제를 점안하여 동공을 확장하고 Ketamine(50 mg/Kg)와 Rompun(23.32 mg/Kg)을 복강 내 주사하여 마취하였다. Slit-lamp laser injection system을 이용하여 레이저를 마우스의 각 안구의 맥락막에 12시, 3시, 6시, 9시 방향으로 4번씩 조사하였다. 이때 레이저 조사 조건은 532 nm, 80 msec, 240mW로 하였다. 레이저 조사 직후 시린지를 이용하여 PBS에 녹인 10 mg/mL 농도의 펩타이드, 또는 20 mg/mL 농도의 애플리버셉트(aflibercept)를 유리체 내에 각각 1 μL씩 주사하였다. 망막전위도 분석을 위하여 12시간이상 암순응을 시켰다. 암실에서 마우스를 산동하고 마취한 후 Ground electrode는 꼬리, Reference electrode는 머리 그리고 Corneal electrode는 각막에 각각 접촉시켜 망막전위도 검사를 시행하였다. 0.9 cdㆍsec/m2 Flash intensity의 단일백색광으로 망막을 자극하여 반응값을 얻고 a-wave의 골에서부터 b-wave의 정점까지로 정한 진폭을 측정하여 이를 망막 기능의 지표로 평가하였다. 모든 시험의 결과는 평균 ± 표준편차로 나타내고, one-way ANOVA 및 Kruskal-wallis test를 이용하여 유의성을 검증하였다.
상기 실험 결과를 하기 표 4 및 도 5에 나타내었다.
| 실시예 | 펩타이드 번호 | 아미노산 서열 | b-파 진폭(μV) | ||||||
| 37 | 002-170 | Hyp | Gly | Gln | Glu | Val | 400 | ||
| 41 | 002-165 | Hyp | Gly | Gln | Glu | Leu | Leu | Ala | 510 |
| 42 | 002-166 | Hyp | Gly | Gln | Glu | Val | Leu | Ala | 380 |
| 43 | 002-175 | Hyp | Gly | Gln | Glu | Aib | Leu | Ala | 371 |
| Naive | 353 | ||||||||
| PBS | 240 | ||||||||
| 애플리버셉트(aflibercept) | 398 | ||||||||
상기 표 4 및 도 5에 나타낸 바와 같이, b-파 진폭을 측정한 결과, 본 발명의 펩타이드를 주사한 경우 b-파 진폭이 증가하는 것을 확인하였다. 따라서 본 발명의 펩타이드는 우수한 CNV 억제 효능을 갖는 것을 알 수 있다.
[시험예 4]
펩타이드의 안정성 평가
본 발명의 펩타이드의 안정성을 평가하기 위해 하기와 같이 실험을 수행하였다.
해당 펩타이드를 수용액 상태에서 40 ℃, 습도 75%, 가혹 조건하에서 함량 분석을 통해 안정성을 확인하였으며, 하기와 같은 조건으로 HPLC를 이용하여 분석하였다.
분석 칼럼: C18 (4.6 Υ 250 mm, 5 μm, YMC Hydrosphere)
분석파장: 자외부흡광광도계 (210 nm)
주입량/유속: 10 μL / 0.8 mL/min
칼럼 온도: 45 ℃
이동상: 0.1M 인산염완충액메탄올 혼합액 (83:17)
상기 실험 결과를 하기 표 5에 나타내었다.
| 실시예 | 펩타이드 번호 | 초기 함량(%) | 7일 후 함량(%) | 감소율(%) |
| 40 | 002-132 | 96.123 | 95.685 | 0.438 |
| 41 | 002-165 | 98.155 | 97.555 | 0.600 |
| 43 | 002-175 | 96.917 | 96.562 | 0.355 |
| 44 | 002-176 | 98.390 | 97.785 | 0.605 |
| 45 | 002-177 | 98.586 | 98.147 | 0.439 |
상기 표 5에 나타낸 바와 같이, 안정성을 평가한 결과, 본 발명의 펩타이드 모두 7일 후의 함량이 약 95% 이상으로 유지되었고, 7일 후의 감소율 또한 약 1% 미만으로, 안정성이 매우 우수한 것을 확인하였다. 특히 실시예 43(002-175)이 가장 우수한 안정성을 나타내었다. 따라서 본 발명의 펩타이드는 우수한 안정성을 갖는 것을 알 수 있다.
[시험예 5]
펩타이드의 용해도 평가
본 발명의 펩타이드의 용해도를 평가하기 위해 하기와 같이 실험을 수행하였다.
용해도 시험은 대한민국약전 방법을 기반으로 진행하였으며, 용해도는 펩타이드 0.1 g을 물 10 mL에 넣고 20 ± 5 ℃에서 5분간마다 30초간씩 세게 흔들어 섞을 때 30분 이내에 녹는 정도로 판단하였다.
상기 실험 결과를 하기 표 6에 나타내었다.
| 실시예 | 펩타이드 번호 | 용해도(mg/ml) |
| 40 | 002-132 | 330.0 |
| 43 | 002-175 | 500.0 |
| 44 | 002-176 | 100.0 |
상기 표 6에 나타낸 바와 같이, 용해도를 측정한 결과, 본 발명의 펩타이드는 우수한 용해도를 나타내었고, 특히 실시예 43(002-175)이 가장 우수한 용해도를 나타내었다. 따라서 본 발명의 펩타이드는 우수한 용해성을 갖는 것을 알 수 있다.
[시험예 6]
펩타이드를 포함하는 점안액의 맥락막혈관신생 억제 효능 평가
상기 시험예를 통해 우수한 펩타이드로 확인된 실시예 43(002-175)을 포함하는 점안액의 CNV(choroidal neovascularization; 맥락막혈관신생) 억제 효능을 평가하기 위해 하기와 같이 실험을 수행하였다.
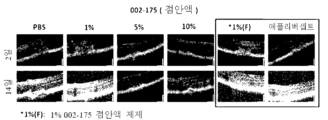
7-8주령의 C57BL/6 마우스에 산동제를 점안하여 동공을 확장하고 Ketamine(50 mg/Kg)와 Rompun(23.32 mg/Kg)을 복강 내 주사하여 마취하였다. Slit-lamp laser injection system을 이용하여 레이저를 마우스의 각 안구의 맥락막에 12시, 3시, 6시, 9시 방향으로 4번씩 조사하였다. 이때 레이저 조사 조건은 532 nm, 80 msec, 240mW로 하였다. 레이저 조사 3일 후 약물 투여 전 시린지를 이용하여 PBS에 녹인 20 mg/mL 농도의 애플리버셉트(aflibercept)를 유리체 내에 각각 1 μL씩 주사하였으며, 농도별로 조제한 약물은 1일 2회(5 μL/eye, AM: 9:00 FM 04:00)씩 11일간 양안에 점안하였다. 레이저 유도 6, 10, 14일 후에 마우스를 마취하고 복강에 2% fluorescein을 투여하여 혈관을 염색하였다. Fluorescein 투여 2~3분후 망막을 촬영하였다. 레이저에 의하여 유도된 CNV 병변은 imageJ program을 이용하여 크기 및 형광값을 측정하였고 개체간 차이를 줄이기 위하여 background를 제거해 줌으로써 CTF(Corrected total fluorescence)을 산출하여 각 군의 값을 비교하였다. 또한, 레이저 유도 6, 10, 14일 후에 마우스를 마취하고, 레이저에 의하여 유도된 CNV 병변은 각 화상(burn)당 OCT beam을 투과시켜 ImageJ program을 이용하여 μm2으로 산출하여 나타내었다. 모든 시험의 결과는 평균 ± 표준편차로 나타내고, one-way ANOVA 및 Kruskal-wallis test를 이용하여 유의성을 검증하였으며, 실험 결과를 도 6 내지 9에 나타내었다.
도 6 및 7에 나타낸 바와 같이, CNV 부위의 형광값을 측정한 결과, 본 발명의 실시예 43(002-175) 펩타이드를 포함하는 점안액은 우수한 CNV 억제 효능을 나타내었으며, 특히 투여 14일 후에는 양성대조군인 애플리버셉트와 비교하여 더욱 우수한 억제 효능을 나타내었다.
또한, 도 8 및 9에 나타낸 바와 같이, CNV 병변의 크기를 측정한 결과, 본 발명의 실시예 43(002-175) 펩타이드를 포함하는 점안액을 투여한 경우 CNV 병변의 크기가 감소하는 것을 확인하였으며, 특히 양성대조군인 애플리버셉트와 비교하여 유사한 수준을 나타내었다.
따라서, 본 발명의 실시예 43(002-175)의 펩타이드를 포함하는 점안액은 우수한 CNV 억제 효능을 갖는 것을 알 수 있다.
[시험예 7]
펩타이드를 포함하는 점안액의 신생혈관 억제 효능 평가
신생혈관성 황반변성의 증상은 망막혈관종 증식(retinal angiomatous proliferation; RAP)이며, 이는 신규 진단된 신생혈관성 황반변성 환자의 약 12~15%에서 나타난다. 한편, Vldlr이 인간 황반변성의 기능적 후보 유전자 중 하나로 알려졌으며, 상기 Vldlr가 녹아웃(knockout(-/-))된 마우스에서 망막하 혈관신생과 함께 망막혈관종 증식이 나타난다. 따라서, 신생혈관성 황반변성 질환 동물 모델인 Vldlr knockout (-/-) 마우스를 대상으로 상기 시험예를 통해 우수한 펩타이드로 확인된 실시예 43(002-175)을 포함하는 점안액의 신생혈관 억제 효능을 평가하기 위해 하기와 같이 실험을 수행하였다.
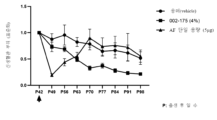
6주령(P42)부터 14주령(P98)까지 Vldlr-/- 마우스에 실시예 43(002-175)을 포함하는 펩타이드 점안액을 1일 2회 점안하였으며, 양성대조군으로 20 mg/mL 농도의 애플리버셉트(aflibercept)를 6주령의 마우스 유리체 내에 각각 1 μL씩 1회 안구 내 주사하였다. 마우스의 안구에 산동제를 점안하여 동공을 확장시킨 후 Ketamine(50 mg/Kg)와 Rompun(23.32 mg/Kg)을 복강 내 주사하여 마취하고 2% fluorescein을 복강 내 주사하여 혈관을 염색하였다. 망막형광촬영을 통하여 이미지를 획득하고, imageJ program을 이용하여 병변 영역을 산출하였으며, 실험 결과를 도 10 및 11에 나타내었다.
도 10 및 11에 나타낸 바와 같이, 신생혈관 부위를 산출한 결과, 양성대조군인 애플리버셉트(AF)를 투여한 군은 투여 1주 후 병변의 크기가 급격히 감소하였으나(P49), 2주차부터 서서히 다시 증가하여 8주 후 음성대조군인 vehicle 투여군과 유사한 크기를 나타내었다(P98). 반면, 본 발명의 실시예 43(002-175) 펩타이드를 포함하는 점안액을 투여한 군은 병변의 크기가 서서히 감소하였으며, 투여 8주 후 병변의 크기가 억제되고 있는 것으로 나타났다(P98).
따라서, 본 발명의 실시예 43(002-175)의 펩타이드를 포함하는 점안액은 우수한 신생혈관 억제 효능을 갖는 것을 알 수 있다.
Claims (9)
- 하기 화학식 1로 표시되는 펩타이드를 포함하는 것을 특징으로 하는 황반변성 예방 또는 치료용 약학 조성물:[화학식 1]X1-X2-X3-X4-X5-X6-X7상기 식에서, X1은 프롤린, 트랜스-4-하이드록시-L-프롤린, 트랜스-4-하이드록시-D-프롤린, 시스-4-플루오로-L-프롤린, 4,4,-디플루오로-L-프롤린, 4-메틸렌-L-프롤린, 4,4-디메틸-L-프롤린, 및 트랜스-4-아미노-L-프롤린으로 이루어진 군에서 선택된 아미노산이고,X2는 글리신이고,X3은 글루타민 또는 D-글루타민이고,X4는 아스파르테이트, D-아스파르테이트, 글루타메이트, 및 D-글루타메이트로 이루어진 군에서 선택된 아미노산이고,X5는 비극성 아미노산이고,X6은 없거나, 류신 또는 D-류신이고,X7은 없거나, 알라닌, D-알라닌, 및 알라닌-이소프로필에스테르로 이루어진 군에서 선택된 아미노산이고,여기서, X6이 없는 경우, X7도 없음.
- 제1항에 있어서,상기 식에서, X1은 프롤린, 트랜스-4-하이드록시-L-프롤린, 트랜스-4-하이드록시-D-프롤린, 시스-4-플루오로-L-프롤린, 4,4,-디플루오로-L-프롤린, 4-메틸렌-L-프롤린, 4,4-디메틸-L-프롤린, 및 트랜스-4-아미노-L-프롤린으로 이루어진 군에서 선택된 아미노산이고,X2는 글리신이고,X3은 글루타민 또는 D-글루타민이고,X4는 아스파르테이트, D-아스파르테이트, 글루타메이트, 및 D-글루타메이트로 이루어진 군에서 선택된 아미노산이고,X5는 글리신, 페닐-글리신, 알라닌, 발린, 류신, tert-류신 및 2-아미노이소부티르산으로 이루어진 군에서 선택된 아미노산이고,X6은 없거나, 류신 또는 D-류신이고,X7은 없거나, 알라닌, D-알라닌, 및 알라닌-이소프로필에스테르로 이루어진 군에서 선택된 아미노산인 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서,상기 식에서, X1은 프롤린, 트랜스-4-하이드록시-L-프롤린, 트랜스-4-하이드록시-D-프롤린, 시스-4-플루오로-L-프롤린, 4,4,-디플루오로-L-프롤린, 4-메틸렌-L-프롤린, 4,4-디메틸-L-프롤린, 및 트랜스-4-아미노-L-프롤린으로 이루어진 군에서 선택된 아미노산이고,X2는 글리신이고,X3은 글루타민 또는 D-글루타민이고,X4는 아스파르테이트, D-아스파르테이트, 글루타메이트, 및 D-글루타메이트로 이루어진 군에서 선택된 아미노산이고,X5는 비극성 아미노산이고,X6은 류신 또는 D-류신이고,X7은 알라닌, D-알라닌, 및 알라닌-이소프로필에스테르로 이루어진 군에서 선택된 아미노산인 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서,상기 식에서, X1은 프롤린, 트랜스-4-하이드록시-L-프롤린, 트랜스-4-하이드록시-D-프롤린, 시스-4-플루오로-L-프롤린, 4,4,-디플루오로-L-프롤린, 4-메틸렌-L-프롤린, 4,4-디메틸-L-프롤린, 및 트랜스-4-아미노-L-프롤린으로 이루어진 군에서 선택된 아미노산이고,X2는 글리신이고,X3은 글루타민 또는 D-글루타민이고,X4는 아스파르테이트, D-아스파르테이트, 글루타메이트, 및 D-글루타메이트로 이루어진 군에서 선택된 아미노산이고,X5는 글리신, 페닐-글리신, 알라닌, 발린, 류신, tert-류신 및 2-아미노이소부티르산으로 이루어진 군에서 선택된 아미노산이고,X6은 류신 또는 D-류신이고,X7은 알라닌, D-알라닌, 및 알라닌-이소프로필에스테르로 이루어진 군에서 선택된 아미노산인 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서,상기 식에서, X1은 프롤린, 트랜스-4-하이드록시-L-프롤린, 트랜스-4-하이드록시-D-프롤린, 시스-4-플루오로-L-프롤린, 4,4,-디플루오로-L-프롤린, 4-메틸렌-L-프롤린, 4,4-디메틸-L-프롤린, 및 트랜스-4-아미노-L-프롤린으로 이루어진 군에서 선택된 아미노산이고,X2는 글리신이고,X3은 글루타민 또는 D-글루타민이고,X4는 글루타메이트 또는 D-글루타메이트이고,X5는 2-아미노이소부티르산이고,X6은 류신 또는 D-류신이고,X7은 알라닌, D-알라닌, 및 알라닌-이소프로필에스테르로 이루어진 군에서 선택된 아미노산인 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서, 서열번호 1 내지 45의 아미노산 서열로 이루어진 군에서 선택된 어느 하나의 펩타이드를 포함하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서, 서열번호 43의 아미노산 서열로 이루어진 펩타이드를 포함하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항 내지 제7항 중 어느 한 항에 있어서, 상기 펩타이드는 맥락막 혈관신생(CNV)을 억제하는 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
- 제1항에 있어서, 상기 황반변성은 습성 황반변성, 건성 황반변성 및 노인성 황반변성으로 이루어진 군으로부터 선택된 하나 이상인 것을 특징으로 하는, 황반변성 예방 또는 치료용 약학 조성물.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20210178126 | 2021-12-13 | ||
| KR10-2021-0178126 | 2021-12-13 | ||
| KR10-2022-0119589 | 2022-09-21 | ||
| KR1020220119589A KR102593936B1 (ko) | 2021-12-13 | 2022-09-21 | 신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023113300A1 true WO2023113300A1 (ko) | 2023-06-22 |
Family
ID=86773096
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/KR2022/019093 WO2023113300A1 (ko) | 2021-12-13 | 2022-11-29 | 신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2023113300A1 (ko) |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120076787A1 (en) * | 2009-05-28 | 2012-03-29 | Peter Adamson | Combination of a tnf-alpha antagonist and a vegf antagonist for use in the treatment or prevention of diseases of the eye |
| KR101721059B1 (ko) * | 2014-12-26 | 2017-03-30 | 주식회사 아이바이오코리아 | 안구 표면 질환 예방 또는 치료용 약학조성물 |
| KR20170115731A (ko) * | 2016-04-08 | 2017-10-18 | 주식회사 아이바이오코리아 | 황반변성 예방 또는 치료용 약학조성물 |
| KR20180126406A (ko) * | 2017-05-17 | 2018-11-27 | 주식회사 유유제약 | 신규한 펩타이드 및 이를 유효성분으로 포함하는 안구질환 치료용 약학 조성물 |
| KR20200134175A (ko) * | 2019-05-21 | 2020-12-01 | 주식회사 아이바이오코리아 | 신규한 펩타이드 화합물 또는 이의 약제학적으로 허용 가능한 염 |
-
2022
- 2022-11-29 WO PCT/KR2022/019093 patent/WO2023113300A1/ko unknown
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120076787A1 (en) * | 2009-05-28 | 2012-03-29 | Peter Adamson | Combination of a tnf-alpha antagonist and a vegf antagonist for use in the treatment or prevention of diseases of the eye |
| KR101721059B1 (ko) * | 2014-12-26 | 2017-03-30 | 주식회사 아이바이오코리아 | 안구 표면 질환 예방 또는 치료용 약학조성물 |
| KR20170115731A (ko) * | 2016-04-08 | 2017-10-18 | 주식회사 아이바이오코리아 | 황반변성 예방 또는 치료용 약학조성물 |
| KR20180126406A (ko) * | 2017-05-17 | 2018-11-27 | 주식회사 유유제약 | 신규한 펩타이드 및 이를 유효성분으로 포함하는 안구질환 치료용 약학 조성물 |
| KR20200134175A (ko) * | 2019-05-21 | 2020-12-01 | 주식회사 아이바이오코리아 | 신규한 펩타이드 화합물 또는 이의 약제학적으로 허용 가능한 염 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2016105086A1 (ko) | 안질환 치료 펩티드 및 이를 포함하는 안질환 치료용 조성물 | |
| WO2017078440A1 (ko) | 신경세포 손실 예방 및 재생 효능을 가지는 펩티드 및 이를 포함하는 조성물 | |
| WO2014073845A1 (en) | A composition for treating diabetes or diabesity comprising oxyntomodulin analog | |
| WO2016137162A1 (ko) | 청력 손상 방어용 펩타이드 및 이를 포함하는 조성물 | |
| WO2018169282A2 (ko) | Atpif1을 함유하는 당뇨 치료용 약학조성물 | |
| WO2017175963A1 (ko) | 연골세포 세포외기질 유래 펩타이드 | |
| WO2018155997A1 (ko) | 에리스로포이에틴 유래 펩티드의 세포손상방지에 효과를 통한 활용 | |
| WO2023113300A1 (ko) | 신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 | |
| WO2012134187A2 (ko) | 황반변성 예방 또는 치료용 약학 조성물 | |
| WO2019045477A1 (ko) | 비멘틴 유래 펩타이드에 특이적으로 결합하는 물질을 포함하는 피부질환 예방 및 치료용 조성물 | |
| WO2013051767A1 (ko) | 안지오제닌의 신규 용도 | |
| WO2023090686A1 (en) | Pentapeptide and use thereof | |
| WO2022050778A1 (en) | Improved cell-permeable modified parkin recombinant protein for treatment of neurodegenerative diseases and use thereof | |
| WO2018147685A1 (ko) | 우르소데옥시콜산을 함유하는 시각장애 예방 또는 치료용 조성물 | |
| WO2018021778A1 (ko) | Lrg1 당단백질을 포함하는 융합 단백질을 함유하는 발기부전, 허혈성 질환 또는 말초 신경질환의 예방 또는 치료용 조성물 | |
| WO2023234703A1 (ko) | 신규의 d-아미노산 유도체 및 이를 포함하는 약학 조성물 | |
| KR102593936B1 (ko) | 신규한 펩타이드를 포함하는 황반변성의 치료용 조성물 | |
| WO2019107964A1 (ko) | 아데노신 유도체를 포함하는 망막 질환 또는 시신경 질환 예방 및 치료용 약학적 조성물 | |
| US10435444B2 (en) | Agent for prevention or treatement of corneal disorders | |
| WO2023013993A1 (en) | Composition or method containing an alk5 inhibitor, ew-7197 | |
| WO2022250470A1 (ko) | Asm 단백질에 특이적으로 결합하는 항체를 유효성분으로 포함하는 뇌질환 치료용 약학적 조성물 | |
| WO2022010273A1 (ko) | 보체 경로 억제제를 포함하는 융합단백질 및 이의 용도 | |
| KR102662922B1 (ko) | 신규의 d-아미노산 유도체 및 이를 포함하는 약학 조성물 | |
| WO2023132698A1 (ko) | 글루카곤-유사 펩타이드-1 및 인터루킨-1 수용체 길항제를 포함하는 퇴행성 뇌질환 예방 또는 치료용 약학 조성물 | |
| WO2021162460A1 (ko) | 신규 비알코올성 간질환의 치료용 약학적 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22907769 Country of ref document: EP Kind code of ref document: A1 |