WO2021065105A1 - イムノクロマトグラフィー - Google Patents
イムノクロマトグラフィー Download PDFInfo
- Publication number
- WO2021065105A1 WO2021065105A1 PCT/JP2020/024691 JP2020024691W WO2021065105A1 WO 2021065105 A1 WO2021065105 A1 WO 2021065105A1 JP 2020024691 W JP2020024691 W JP 2020024691W WO 2021065105 A1 WO2021065105 A1 WO 2021065105A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antigen
- monoclonal antibody
- solution
- magnetic particles
- modified
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54313—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals the carrier being characterised by its particulate form
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54386—Analytical elements
- G01N33/54387—Immunochromatographic test strips
- G01N33/54388—Immunochromatographic test strips based on lateral flow
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/40—Concentrating samples
- G01N1/405—Concentrating samples by adsorption or absorption
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54313—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals the carrier being characterised by its particulate form
- G01N33/54326—Magnetic particles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54393—Improving reaction conditions or stability, e.g. by coating or irradiation of surface, by reduction of non-specific binding, by promotion of specific binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/551—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals the carrier being inorganic
- G01N33/553—Metal or metal coated
Definitions
- the present invention relates to immunochromatography.
- Immunochromatography is frequently used these days because it is easy to operate and can be measured in a short time.
- an antigen such as influenza virus
- immunochromatography the following operation is performed.
- a label modified with an antibody (labeled antibody) is prepared and mixed with a sample containing an antigen.
- the labeled antibody binds to the antigen to form a complex.
- the complex is developed on an insoluble carrier having a detection line coated with an antibody that specifically reacts with an antigen, the complex is captured by reacting with the antibody on the detection line (test line) and detected visually or the like. Is confirmed.
- Examples of such immunochromatography include the methods disclosed in Patent Document 1.
- the present inventors have found that the above problems can be solved by performing a predetermined pretreatment using magnetism and changing the type of monoclonal antibody used in each step. It came to. That is, the present inventors have found that the above problems can be solved by the following configuration.
- a dissociation solution which is an acidic or alkaline solution
- the modified magnetic particles are dissociated from the magnetic particle composite to obtain an antigen-containing solution.
- the antigen in a state in which a gold particle complex which is a complex of the antigen in the neutralizing antigen-containing liquid and the modified gold particles which are gold particles modified with a monoclonal antibody Y capable of binding to the antigen is formed.
- the monoclonal antibody X and the monoclonal antibody Y are different from each other. Immunochromatography in which the monoclonal antibody X and the monoclonal antibody Z are different from each other.
- the neutralizing solution contains HCl and at least one selected from the group consisting of tricine, tris, HEPES, acetoamide glycine, glycinamide and bicine, or NaOH and tricine, tris, HEPES.
- immunochromatography with high detection sensitivity can be provided.
- the immunochromatography of the present invention will be described below.
- the numerical range represented by using “-" in the present specification means a range including the numerical values before and after "-" as the lower limit value and the upper limit value.
- each component may be used alone or in combination of two or more.
- the content of the component means the total content unless otherwise specified.
- the detection sensitivity and the S / N ratio (signal / noise ratio) are further improved is also referred to as "the effect of the present invention is more excellent”.
- the immunochromatography of the present invention (hereinafter, also referred to as "the method of the present invention") is By mixing a sample that can contain an antigen with modified magnetic particles that are magnetic particles modified with a monoclonal antibody X that has a specific affinity for the antigen, a complex of the antigen and the modified magnetic particles can be obtained.
- a mixing step and A collection step of collecting magnetic particles in a mixture containing the above magnetic particle composite using magnetism and a collection step.
- a dissociation solution which is an acidic or alkaline solution
- the modified magnetic particles are dissociated from the magnetic particle composite to obtain an antigen-containing solution.
- the antigen in a state in which a gold particle complex which is a complex of the antigen in the neutralizing antigen-containing liquid and the modified gold particles which are gold particles modified with a monoclonal antibody Y capable of binding to the antigen is formed.
- the monoclonal antibody X and the monoclonal antibody Y are different from each other. Immunochromatography in which the monoclonal antibody X and the monoclonal antibody Z are different from each other.
- a predetermined pretreatment (mixing step, collection step, divergence step, neutralization step) using magnetism is performed, and the type of monoclonal antibody used in a specific step is different. I'm making it. Since the method of the present invention has such a configuration, it is presumed that the above-mentioned effects can be obtained. In particular, it is considered that the monoclonal antibody X used in the pretreatment and the monoclonal antibody Y and / or the monoclonal antibody Z used in the developing step are different from each other.
- an antigen is reacted with a magnetic particle (modified magnetic particle) modified with a monoclonal antibody, and after an operation such as concentration, the modified magnetic particle is dissociated to prepare an antigen-containing solution (particularly, an antigen concentrate).
- an antigen-containing solution particularly, an antigen concentrate
- the modified magnetic particles separated from each other may remain in the liquid and inhibit the antigen-antibody reaction of immunochromatography.
- the method of the present invention is based on the above findings and the like. That is, in the method of the present invention, the monoclonal antibody used in the above pretreatment and the monoclonal antibody used in immunochromatography (development step) are different.
- the process from the mixing process to the neutralization process is also referred to as a "magnetic particle process”.
- the antigen and the modified magnetic particles are mixed by mixing a sample that can contain the antigen and the modified magnetic particles that are magnetic particles modified with the monoclonal antibody X having a specific affinity for the antigen.
- This is a step of obtaining a mixture containing a magnetic particle composite which is a composite of the above.
- the sample used in the mixing step is not particularly limited as long as it is a sample that can contain an antigen.
- samples include, for example, biological samples, especially animal (particularly human) body fluids (eg, blood, serum, plasma, spinal fluid, tears, sweat, urine, pus, runny nose, or sputum) or Examples include excrement (eg, urine), organs, tissues, mucous membranes and skin, scraped specimens (swabs) that are believed to contain them, snot, or animals and plants themselves or their dried bodies.
- antigen examples include bacteria, bacteria (for example, Mycobacterium tuberculosis, lipoarabinomannan (LAM) contained in Mycobacterium tuberculosis), bacteria, viruses (for example, influenza virus), and their nucleoproteins.
- LAM is a major antigen in tuberculosis and a glycolipid which is a major constituent of cell membranes and cell walls.
- the antigen is preferably a virus or LAM, more preferably a virus, and even more preferably an influenza virus, for the reason that the effects of the present invention are more excellent.
- the above sample is in the form of an extract obtained by extracting the sample as it is or by extracting the antigen with an appropriate extraction solvent, and further, a diluent obtained by diluting the extract with an appropriate diluent.
- the extract can be used in a concentrated form by an appropriate method.
- a solvent used in a usual immunological analysis method for example, water, physiological saline, buffer solution, etc.
- a direct antigen-antibody reaction is carried out by diluting with such a solvent. It is also possible to use a water-miscible organic solvent that can be used.
- the modified magnetic particles are magnetic particles modified with a monoclonal antibody X having a specific affinity for the antigen.
- the material of the magnetic particles is not particularly limited as long as it is a magnetic material, and specific examples thereof include iron, cobalt, nickel, oxides thereof, ferrites, and alloys thereof. Of these, iron oxide is preferable because the effects of the present invention are more excellent.
- the magnetic particles may be particles obtained by molding a magnetic material into particles by themselves, particles having a magnetic material as a core and whose surface is coated with a polymer (for example, polystyrene, silica gel, etc.), or particles. , The particles may be particles whose surface is coated with a polymer or the like as a core using a magnetic material.
- the particle size of the magnetic particles is not particularly limited, but is preferably 0.05 ⁇ m to 10 ⁇ m, more preferably 0.1 ⁇ m to 5 ⁇ m, for the reason that the effects of the present invention are more excellent.
- the particle size can be measured with a commercially available particle size distribution meter or the like.
- a measurement method of the particle size distribution optical microscopy, confocal laser microscopy, electron microscopy, atomic force microscopy, static light scattering, laser diffraction, dynamic light scattering, centrifugal sedimentation, electric pulse Measurement methods, chromatography methods, ultrasonic attenuation methods, etc. are known, and devices corresponding to each principle are commercially available.
- a dynamic light scattering method can be preferably used because of the particle size range and ease of measurement.
- Nanotrack UPA Nikkiso Co., Ltd.
- dynamic light scattering particle size distribution measuring device LB-550 HORIBA, Ltd.
- the monoclonal antibody X is a monoclonal antibody having a specific affinity for the above antigen, and is a monoclonal antibody different from the monoclonal antibody Y and the monoclonal antibody Z described later.
- the monoclonal antibody for example, a monoclonal antibody obtained by cell fusion using animal spleen cells immunized with an antigen, or a fragment thereof [for example, F (ab') 2, Fab, Fab', or Fv] is used. be able to. Preparation of these antibodies can be carried out by a conventional method.
- the method for producing the modified magnetic particles is not particularly limited, and a known method can be used.
- a method of activating the magnetic particles with EDC (1-ethyl-3- (3-dimethylaminopropyl) carbodiimide) to support the monoclonal antibody X on the magnetic particles can be mentioned.
- the sample and the modified magnetic particles are mixed.
- the antigen in the sample reacts with the monoclonal antibody X having a specific affinity for the antigen of the modified magnetic particles, and the antigen and the modified magnetism in the sample react. A complex with the particles is formed.
- the sample does not contain an antigen, no complex is formed.
- the collection step is a step of collecting magnetic particles in the mixture containing the magnetic particle composite after the above-mentioned mixing step by using magnetism.
- collecting the magnetic particles in the mixture means “collecting the magnetic particle composite in the mixture, and the magnetic particles (unmodified magnetic particles) and the modified magnetic particles remaining in the mixture.” It means “to do”.
- the method of collecting the magnetic particles in the mixture after the mixing step by using magnetism is not particularly limited.
- the mixture after the mixing step is placed in a conical tube installed on a magnetic stand and magnetically. Examples thereof include a method of collecting the above magnetic particle composite and then extracting a surplus sample.
- the magnetic particles collected in the collection step described above are mixed with a dissociation solution which is an alkaline or acidic solution to dissociate the modified magnetic particles from the magnetic particle composite and contain an antigen. This is the process of obtaining liquid.
- the dissociation liquid dissociates the modified magnetic particles from the magnetic particle composite (complex of the antigen and the modified magnetic particles), and separates the antigen and the modified magnetic particles. As a result, an antigen-containing solution which is an antigen-containing divergent solution is obtained.
- the divergent liquid is not particularly limited as long as it is an alkaline or acidic liquid.
- the alkaline solution is not particularly limited, and specific examples thereof include an aqueous NaOH solution and an aqueous KOH solution. Of these, an aqueous NaOH solution is preferable because the effects of the present invention are more excellent.
- the acidic liquid is not particularly limited, and specific examples thereof include an aqueous HCl solution, an aqueous H 2 SO 4 solution, and an aqueous HNO 3 solution. Of these, an aqueous HCl solution is preferable because the effects of the present invention are more excellent.
- the divergent liquid is preferably an alkaline liquid for the reason that the effect of the present invention is more excellent.
- the divergent liquid preferably contains NaOH or HCl, more preferably contains NaOH, and even more preferably an aqueous NaOH solution, for reasons such as the effects of the present invention being more excellent.
- the amount of the divergent liquid is not particularly limited, but for the reason that the effect of the present invention is more excellent, the amount of the divergent liquid is preferably smaller than the amount of the "sample containing an antigen" used in the above-mentioned mixing step.
- the concentration of the antigen in the divergence solution is in the "antigen-containing sample” used in the above-mentioned mixing step. It will be higher than the concentration of the antigen. That is, the antigen-containing liquid obtained by the dissociation step is a liquid in which the concentration of the antigen is concentrated (antigen concentrate).
- the ratio of the divergent liquid to the "sample containing an antigen" used in the above-mentioned mixing step is preferably 1/5 or less, preferably 1/10 or less, in terms of mass ratio, for the reason that the effect of the present invention is more excellent. Is more preferable, and 1/20 or less is further preferable.
- the neutralization step is a step of obtaining a neutralized antigen-containing solution by neutralizing the antigen-containing solution obtained in the above-mentioned divergence step using a neutralizing solution.
- the dissociation liquid is an alkaline or acidic liquid, so that the antigen-containing liquid obtained in the dissociation step is usually alkaline or acidic.
- the neutralizing solution is used to neutralize the antigen-containing solution.
- the neutralizing solution is not particularly limited, but for example, a known buffer solution can be used.
- a known buffer solution can be used.
- the diverging solution used in the above-mentioned divergence step is an alkaline solution, HCl (particularly, 1M HCl), tricine, tris, HEPES ( It is preferable to contain at least one selected from the group consisting of 4- (2-hydroxyethyl) -1-piperazineethanesulphonic acid), acetamidoglycin, glycinamide and bicine, and the divergence solution used in the above-mentioned divergence step is preferably contained.
- an acidic liquid it is preferable to contain NaOH (particularly 1M NaOH) and at least one selected from the group consisting of tricine, tris, HEPES, acetoamide glycin, glycinamide and bicine.
- the developing step is gold, which is a complex of the antigen in the neutralizing antigen-containing liquid obtained in the above-mentioned neutralizing step and the modified gold particles which are gold particles modified with the monoclonal antibody Y capable of binding to the above-mentioned antigen.
- This is a step of developing a monoclonal antibody Z capable of binding to the antigen on an insoluble carrier having an immobilized reaction site in a state where a particle complex is formed.
- Gold particle composite As described above, in the developing step, first, the antigen in the neutralizing antigen-containing liquid obtained in the neutralizing step described above, and the modified gold particles which are gold particles modified with the monoclonal antibody Y capable of binding to the antigen. A gold particle complex, which is a complex of the above, is formed.
- the modified gold particles are gold particles modified with a monoclonal antibody Y capable of binding to the above antigen.
- Gold particles are not particularly limited. The gold particles act as a catalyst for reducing silver ions in the silver amplification step described later.
- the particle size of the gold particles is preferably 100 nm or less, more preferably 50 nm or less, further preferably 30 nm or less, still more preferably 15 nm or less, for the reason that the effects of the present invention are more excellent. Is particularly preferable.
- the lower limit of the particle size of the gold particles is not particularly limited, but for the reason that the effect of the present invention is more excellent, it is preferably 1 nm or more, more preferably 2 nm or more, and further preferably 5 nm or more. ..
- the particle size of the gold particles can be determined by the same method as for the magnetic particles described above.
- the monoclonal antibody Y is a monoclonal antibody capable of binding to the above-mentioned antigen, and is not particularly limited as long as it is a monoclonal antibody different from the above-mentioned monoclonal antibody X. Specific examples and preferred embodiments of the monoclonal antibody Y are the same as those of the monoclonal antibody X described above.
- the method for producing the modified gold particles is not particularly limited, and a known method can be used.
- a known method can be used.
- the SH bond is cleaved when approaching the gold particles to form an Au-S bond on the Au surface.
- Examples include chemical bonding methods such as immobilization.
- the insoluble carrier is an insoluble carrier having a reaction site (test line) on which a monoclonal antibody Z capable of binding to the antigen is immobilized.
- the insoluble carrier may have a plurality of test lines depending on the type of antigen (for example, a test line for influenza A virus and a test line for influenza B virus).
- the insoluble carrier may have a control line on the downstream side of the test line in order to confirm the development of the gold particle composite.
- a color-developing reagent immobilization line may be provided on the downstream side of the test line in order to detect the reducing agent solution.
- the insoluble carrier for example, as shown in FIG. 1, a nitrocellulose membrane having a gold colloid holding pad 10, a test line 20, a control line 30, and a coloring reagent immobilization line 40 from the upstream side. 100 is mentioned.
- the gold colloid holding pad 10 is a pad for holding gold particles (modified gold particles) modified with the monoclonal antibody Y
- the test line 20 is a line on which the monoclonal antibody Z is immobilized
- the control line 30 is. It is a line for confirming the development
- the color-developing reagent immobilization line 40 is a line for detecting a reducing agent solution described later.
- the upstream side and the downstream side mean a description intended to be developed from the upstream side to the downstream side when the gold particle composite is developed.
- Specific embodiments of the insoluble carrier include, for example, the insoluble carrier and the immunochromatographic kit described in Japanese Patent No. 5728453.
- all the contents described in Japanese Patent No. 5728453 regarding insoluble carriers and immunochromatographic kits are incorporated herein by reference as a part of the disclosure of the present specification.
- the insoluble carrier is preferably a porous carrier.
- nitrocellulose membrane nitrocellulose membrane
- cellulose membrane cellulose membrane
- acetylcellulose membrane polysulfone membrane
- polyethersulfone membrane nylon membrane
- glass fiber glass fiber
- non-woven fabric cloth, thread, etc.
- a nitrocellulose membrane is more preferable.
- the monoclonal antibody Z is a monoclonal antibody capable of binding to the above-mentioned antigen, and is not particularly limited as long as it is a monoclonal antibody different from the above-mentioned monoclonal antibody X. Specific examples and preferred embodiments of the monoclonal antibody Z are the same as those of the monoclonal antibody X described above.
- the method of developing the gold particle composite on an insoluble carrier having a test line is not particularly limited, and for example, a nitrocellulose membrane 100 (or an immunochromatographic kit having the same) as shown in FIG. 1 described above).
- a nitrocellulose membrane 100 or an immunochromatographic kit having the same as shown in FIG. 1 described above.
- the neutralizing antigen-containing solution obtained in the above-mentioned neutralizing step is dropped onto a gold colloid-holding pad, and the solution is moved from the upstream side to the downstream side by using the capillary phenomenon as shown in FIG. And so on.
- the capture step is a step of capturing the gold particle composite at the reaction site of the insoluble carrier.
- the gold particle complex composite of the antigen and the modified gold particles developed on the insoluble carrier in the above developing step.
- the body is captured at the reaction site (test line) of the insoluble carrier. If the sample does not contain an antigen, the gold particle complex is not formed, so that the gold particle complex is not captured at the reaction site of the insoluble carrier.
- the silver amplification step is a step of silver-amplifying the gold particle composite captured in the capture step.
- the silver amplification step is a step of forming large silver particles in the gold particle composite captured at the reaction site of the insoluble carrier by imparting silver ions to the insoluble carrier after the capture step. More specifically, it is a step in which silver ions are reduced using the gold particles of the gold particle composite as a catalyst to form silver particles (for example, a diameter of 10 ⁇ m or more). This significantly improves the detection sensitivity of the captured gold particle composite.
- the method of imparting silver ions to the insoluble carrier after the capture step is not particularly limited, but a method of using the following reducing agent solution and the following silver amplification solution is preferable for the reason that the effects of the present invention are more excellent. Further, in addition to the reducing agent solution and the silver amplification solution, a washing solution may be used to wash the complex remaining on the insoluble carrier other than the specific binding reaction.
- the reducing liquid may also serve as a cleaning liquid.
- the reducing agent solution contains a reducing agent capable of reducing silver ions.
- the reducing agent capable of reducing silver ions can be used in any inorganic or organic material or a mixture thereof as long as silver ions can be reduced to silver.
- As the inorganic reducing agent a reducing metal salt whose valence can be changed by metal ions such as Fe 2+ , V 2+ , and Ti 3+, and a reducing metal complex salt can be preferably mentioned.
- an inorganic reducing agent it is necessary to complex or reduce oxidized ions to remove or detoxify them.
- citric acid or ethylenediaminetetraacetic acid (EDTA) can be used to form a complex of Fe 3+ , which is an oxide, to make it harmless.
- EDTA ethylenediaminetetraacetic acid
- the developer used in the wet silver halide photographic photosensitive material for example, methyl gallic acid, hydroquinone, substituted hydroquinone, 3-pyrazolidones, p-aminophenols, p-phenylenediamines, hindered phenols, amidoxime).
- Adins, catechols, pyrogallols, ascorbic acid (or derivatives thereof), and leuco pigments and other materials apparent to those skilled in the art, such as US Pat. No. 6,
- the materials described in Nos. 020 and 117 can also be used as reducing agents.
- Ascorbic acid reducing agent is also preferable as the reducing agent.
- Useful ascorbic acid reducing agents include ascorbic acid and its analogs, isomers and derivatives thereof, such as D- or L-ascorbic acid and sugar derivatives thereof (eg, ⁇ -lactoascorbic acid, glucoascorbic acid, fucoascorbic acid).
- Acid glucoheptascorbic acid, maltoascorbic acid
- sodium salt of ascorbic acid potassium salt of ascorbic acid
- isoascorbic acid or L-erythroascorbic acid
- salts thereof eg alkali metal salt, ammonium salt or the present technology Salts known in the art
- endiol type ascorbic acid enaminol type ascorbic acid, thioenoal type ascorbic acid and the like
- endiol type ascorbic acid enaminol type ascorbic acid, thioenoal type ascorbic acid and the like
- D, L or D, L-ascorbic acid And the alkali metal salt) or isoascorbic acid (or the alkali metal salt thereof) is preferable, and the sodium salt is a preferable salt.
- a mixture of these reducing agents can be used.
- the reducing agent solution is preferably flown so that the angle between the developing direction in the developing step and the developing direction of the reducing agent solution is 0 to 150 degrees for the reason that the effect of the present invention is more excellent. It is more preferable to flow the reducing agent solution so that the angle between the developing direction and the developing direction of the reducing agent liquid is 0 to 135 degrees. Examples of the method for adjusting the angle between the developing direction and the developing direction of the reducing agent liquid in the developing step include the methods described in Examples of JP-A-2009-150869.
- the silver amplification liquid is a liquid containing a compound containing silver ions.
- a compound containing silver ions for example, an organic silver salt, an inorganic silver salt, or a silver complex can be used.
- silver nitrate, silver acetate, silver lactate, silver butyrate, silver thiosulfate and the like which are silver ion-containing compounds having high solubility in a solvent such as water, can be mentioned.
- Particularly preferred is silver nitrate.
- a silver complex coordinated with a ligand having a water-soluble group such as a hydroxyl group or a sulfone group is preferable, and hydroxythioether silver and the like can be mentioned.
- the organic silver salt, the inorganic silver salt, or the silver complex is 0.001 mol / L to 5 mol / L, preferably 0.005 mol / L to 3 mol / L, and further 0.01 mol / L to 1 mol in the silver amplification solution as silver. It is preferably contained at a concentration of / L.
- auxiliary agent for the silver amplification liquid examples include buffers, preservatives, for example, antioxidants or organic stabilizers, speed regulators and the like.
- buffers include acetic acid, citric acid, sodium hydroxide or one of these salts, a buffer using tris (hydroxymethyl) aminomethane, and other buffers used in general chemical experiments. Can be used. These buffers can be appropriately used to adjust the pH to the optimum pH for the amplified solution.
- alkylamine can be used as an auxiliary agent as an antifog agent, and dodecylamine is particularly preferable.
- a surfactant can be used, and particularly preferably C 9 H 19- C 6 H 4- O- (CH 2 CH 2 O) 50 H.
- the silver amplification liquid is preferably flowed from the direction opposite to the development step described above because the effect of the present invention is more excellent, and the angle between the development direction in the development step and the development direction of the reducing agent solution is 45 degrees or more. It is more preferable to flow at 180 degrees.
- Examples of the method for adjusting the angle between the developing direction and the developing direction of the silver amplification liquid in the developing step include the methods described in Examples of JP-A-2009-150869.
- the monoclonal antibody X and the monoclonal antibody Y are different from each other, and the monoclonal antibody X and the monoclonal antibody Z are different from each other.
- the monoclonal antibody Y and the monoclonal antibody Z may be the same or different, but are preferably different for the reason that the effects of the present invention are more excellent.
- the monoclonal antibody X, the monoclonal antibody Y, and the monoclonal antibody Z are all different monoclonal antibodies.
- the epitope of the monoclonal antibody X and the epitope of the monoclonal antibody Y are preferably different from each other because the effects of the present invention and the like are more excellent.
- the epitope of the monoclonal antibody X and the epitope of the monoclonal antibody Z are preferably different from each other because the effects of the present invention and the like are more excellent.
- the epitope of the monoclonal antibody Y and the epitope of the monoclonal antibody Z may be the same or different, but they are preferably different because the effects of the present invention are more excellent.
- the epitope of the monoclonal antibody X, the epitope of the monoclonal antibody Y, and the epitope of the monoclonal antibody Z are all different. It should be noted that that the epitopes of the monoclonal antibodies are different can be confirmed by, for example, ELISA (Enzyme-Linked Immuno Solvent Assay).
- sample solution (sample containing an antigen) was prepared using Quick S-Influenza A / B "Seiken" negative / positive control solution (product number: 322968, manufactured by Denka Seiken Co., Ltd.). Specifically, the above positive control solution is diluted 10-fold with PBS (Phosphate buffered salts) buffer containing 1% by mass BSA (Bovine Serum Albumin), and the sample solution at each dilution rate (sample containing an antigen). And said.
- the detection limit minimum detection sensitivity
- by the commercially available immunochromatographic detection kit "Capilia FluA + B" manufactured by Alfresa Pharma Corporation was 1/40 for both types A and B.
- Example 1 Immunochromatography of Example 1 was performed as follows.
- ThermoFiser magnetic particles (DynabeadsMyOne-COOH, particle size: 1 ⁇ m, Thermofiser) are activated with EDC (1-ethyl-3- (3-dimethylaminopropyl) carbodiimide) to activate an anti-influenza A monoclonal antibody (Funakoshi). , # GTX629544) was carried on magnetic particles to obtain modified magnetic particles which are magnetic particles modified with an anti-influenza A type monoclonal antibody (monoclonal antibody X).
- a nitrocellulose membrane 100 having a gold colloid holding pad 10, a test line 20, a control line 30, and a coloring reagent immobilization line 40 was prepared from the upstream side.
- the gold colloid holding pad 10 is a pad that holds gold colloid (modified gold particles) modified with an anti-influenza A type monoclonal antibody (Anti-Influenza A SPTN-5 7307, Medix Biochemica) (monoclonal antibody Y).
- test line 20 is a line on which an anti-influenza A monoclonal antibody (Anti-Influenza A SPTN-5 7307, Medix Biochemica) (monoclonal antibody Z) is immobilized, and the control line 30 confirms the development.
- the color-developing reagent immobilization line 40 is a line for detecting a reducing liquid, which will be described later.
- the above neutralized influenza A virus-containing solution was dropped onto a colloidal gold holding pad.
- a gold particle complex which is a complex of influenza A virus in a liquid and gold colloid particles (modified gold particles) modified with an anti-influenza A monoclonal antibody (monoclonal antibody Y) in a gold colloid holding pad. was formed. In this state, it was developed on the downstream side of the nitrocellulose membrane.
- the silver amplification step was carried out as follows.
- Example 2 Example 1 except that an anti-influenza A monoclonal antibody (Anti-Influenza A SPTN-5 7307, Medix Biochemica) was used instead of the anti-influenza A monoclonal antibody (Funakoshi, # GTX629544) as the monoclonal antibody X. Immunochromatography was performed and evaluated according to the same procedure as above. The results are shown in Table 1. In Comparative Example 2, the monoclonal antibody X and the monoclonal antibody Y are the same as each other, and the monoclonal antibody X and the monoclonal antibody Z are the same as each other.
- Example 1 in which the magnetic particle process was performed and the monoclonal antibody X and the monoclonal antibody Y were different from each other and the monoclonal antibody X and the monoclonal antibody Z were different from each other showed high detection sensitivity as compared with a certain Comparative Example 2.
- monoclonal antibody X monoclonal antibody Y
- monoclonal antibody Z monoclonal antibody Z
Landscapes
- Health & Medical Sciences (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Inorganic Chemistry (AREA)
- Peptides Or Proteins (AREA)
Abstract
イムノクロマトグラフィーは、抗原を含み得る試料とモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで磁性粒子複合体を含有する混合物を得る混合工程と、磁気を用いて磁性粒子を捕集する捕集工程と、捕集された磁性粒子と乖離液とを混合することで修飾磁性粒子を乖離させ抗原含有液を得る乖離工程と、中和抗原含有液を得る中和工程と、中和抗原含有液中の抗原とモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、モノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する展開工程と、反応部位において金粒子複合体を捕捉する捕捉工程と、金粒子複合体を銀増幅する銀増幅工程と、を備え、抗体Xと抗体Yが互いに異なり抗体Xと抗体Zが互いに異なる。
Description
本発明は、イムノクロマトグラフィーに関する。
イムノクロマトグラフィーは、操作が簡便であり短時間で測定可能であることから、昨今頻繁に利用されている。
例えば、インフルエンザウイルス等の抗原をイムノクロマトグラフィーで検出する場合、以下のような操作が行われる。
まず、抗体で修飾された標識(標識抗体)を用意し、抗原を含む試料と混合する。標識抗体は抗原と結合し、複合体を形成する。この状態で、抗原と特異的に反応する抗体が塗布された検出ラインを有する不溶性担体に展開させると、複合体は検出ライン(テストライン)上で抗体と反応して捕捉され、目視等により検出が確認される。
このようなイムノクロマトグラフィーとしては、例えば、特許文献1に開示される方法が挙げられる。
例えば、インフルエンザウイルス等の抗原をイムノクロマトグラフィーで検出する場合、以下のような操作が行われる。
まず、抗体で修飾された標識(標識抗体)を用意し、抗原を含む試料と混合する。標識抗体は抗原と結合し、複合体を形成する。この状態で、抗原と特異的に反応する抗体が塗布された検出ラインを有する不溶性担体に展開させると、複合体は検出ライン(テストライン)上で抗体と反応して捕捉され、目視等により検出が確認される。
このようなイムノクロマトグラフィーとしては、例えば、特許文献1に開示される方法が挙げられる。
昨今、より高感度の免疫診断法が望まれるなか、イムノクロマトグラフィーに対しても従来の方法(例えば、特許文献1に開示される方法)よりもさらに高感度な方法が求められている。
そこで、本発明は、上記実情を鑑みて、検出感度の高いイムノクロマトグラフィーを提供することを目的とする。
本発明者らは、上記課題について鋭意検討した結果、磁気を用いた所定の前処理を行うとともに、各工程で使用されるモノクローナル抗体の種類を変えることで上記課題が解決できることを見出し、本発明に至った。
すなわち、本発明者らは、以下の構成により上記課題が解決できることを見出した。
すなわち、本発明者らは、以下の構成により上記課題が解決できることを見出した。
(1) 抗原を含み得る試料と、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、上記抗原と上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る、混合工程と、
磁気を用いて、上記磁性粒子複合体を含有する混合物中の磁性粒子を捕集する、捕集工程と、
上記捕集工程で捕集された磁性粒子と、酸性又はアルカリ性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る、乖離工程と、
中和液を用いて、上記抗原含有液を中和することで、中和抗原含有液を得る、中和工程と、
上記中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する、展開工程と、
上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する、捕捉工程と、
上記捕捉工程で捕捉された金粒子複合体を銀増幅する、銀増幅工程とを備え、
上記モノクローナル抗体Xと上記モノクローナル抗体Yが互いに異なり、
上記モノクローナル抗体Xと上記モノクローナル抗体Zが互いに異なる、イムノクロマトグラフィー。
(2) 上記モノクローナル抗体X、上記モノクローナル抗体Y及び上記モノクローナル抗体Zが全て異なる、上記(1)に記載のイムノクロマトグラフィー。
(3) 上記乖離液が、上記抗原を含み得る試料よりも少ない量の、酸性又はアルカリ性の液である乖離液である、上記(1)又は(2)に記載のイムノクロマトグラフィー。
(4) 上記抗原を含み得る試料に対する、上記乖離液の割合が、質量比で、1/5以下である、上記(3)に記載のイムノクロマトグラフィー。
(5) 上記乖離液が、NaOH又はHClを含有する、上記(1)~(4)のいずれかに記載のイムノクロマトグラフィー。
(6) 上記中和液が、HClと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、又は、NaOHと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、上記(1)~(5)のいずれかに記載のイムノクロマトグラフィー。
(7) 修飾される前の上記磁性粒子の粒子径が、0.05μm~10μmである、上記(1)~(6)のいずれかに記載のイムノクロマトグラフィー。
磁気を用いて、上記磁性粒子複合体を含有する混合物中の磁性粒子を捕集する、捕集工程と、
上記捕集工程で捕集された磁性粒子と、酸性又はアルカリ性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る、乖離工程と、
中和液を用いて、上記抗原含有液を中和することで、中和抗原含有液を得る、中和工程と、
上記中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する、展開工程と、
上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する、捕捉工程と、
上記捕捉工程で捕捉された金粒子複合体を銀増幅する、銀増幅工程とを備え、
上記モノクローナル抗体Xと上記モノクローナル抗体Yが互いに異なり、
上記モノクローナル抗体Xと上記モノクローナル抗体Zが互いに異なる、イムノクロマトグラフィー。
(2) 上記モノクローナル抗体X、上記モノクローナル抗体Y及び上記モノクローナル抗体Zが全て異なる、上記(1)に記載のイムノクロマトグラフィー。
(3) 上記乖離液が、上記抗原を含み得る試料よりも少ない量の、酸性又はアルカリ性の液である乖離液である、上記(1)又は(2)に記載のイムノクロマトグラフィー。
(4) 上記抗原を含み得る試料に対する、上記乖離液の割合が、質量比で、1/5以下である、上記(3)に記載のイムノクロマトグラフィー。
(5) 上記乖離液が、NaOH又はHClを含有する、上記(1)~(4)のいずれかに記載のイムノクロマトグラフィー。
(6) 上記中和液が、HClと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、又は、NaOHと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、上記(1)~(5)のいずれかに記載のイムノクロマトグラフィー。
(7) 修飾される前の上記磁性粒子の粒子径が、0.05μm~10μmである、上記(1)~(6)のいずれかに記載のイムノクロマトグラフィー。
以下に示すように、本発明によれば、検出感度の高いイムノクロマトグラフィーを提供することができる。
以下に、本発明のイムノクロマトグラフィーについて説明する。
なお、本明細書において「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
また、本明細書において各成分は、1種を単独で用いても、2種以上を併用して用いてもよい。ここで、各成分について2種以上を併用する場合、その成分について含有量とは、特段の断りが無い限り、合計の含有量を指す。
また、本明細書において「検出感度及びS/N比(信号/ノイズ比)がより向上する」ことを「本発明の効果等がより優れる」とも言う。
なお、本明細書において「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
また、本明細書において各成分は、1種を単独で用いても、2種以上を併用して用いてもよい。ここで、各成分について2種以上を併用する場合、その成分について含有量とは、特段の断りが無い限り、合計の含有量を指す。
また、本明細書において「検出感度及びS/N比(信号/ノイズ比)がより向上する」ことを「本発明の効果等がより優れる」とも言う。
本発明のイムノクロマトグラフィー(以下、「本発明の方法」とも言う)は、
抗原を含み得る試料と、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、上記抗原と上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る、混合工程と、
磁気を用いて、上記磁性粒子複合体を含有する混合物中の磁性粒子を捕集する、捕集工程と、
上記捕集工程で捕集された磁性粒子と、酸性又はアルカリ性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る、乖離工程と、
中和液を用いて、上記抗原含有液を中和することで、中和抗原含有液を得る、中和工程と、
上記中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する、展開工程と、
上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する、捕捉工程と、
上記捕捉工程で捕捉された金粒子複合体を銀増幅する、銀増幅工程とを備え、
上記モノクローナル抗体Xと上記モノクローナル抗体Yが互いに異なり、
上記モノクローナル抗体Xと上記モノクローナル抗体Zが互いに異なる、イムノクロマトグラフィーである。
抗原を含み得る試料と、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、上記抗原と上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る、混合工程と、
磁気を用いて、上記磁性粒子複合体を含有する混合物中の磁性粒子を捕集する、捕集工程と、
上記捕集工程で捕集された磁性粒子と、酸性又はアルカリ性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る、乖離工程と、
中和液を用いて、上記抗原含有液を中和することで、中和抗原含有液を得る、中和工程と、
上記中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する、展開工程と、
上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する、捕捉工程と、
上記捕捉工程で捕捉された金粒子複合体を銀増幅する、銀増幅工程とを備え、
上記モノクローナル抗体Xと上記モノクローナル抗体Yが互いに異なり、
上記モノクローナル抗体Xと上記モノクローナル抗体Zが互いに異なる、イムノクロマトグラフィーである。
上述のとおり、本発明の方法では、磁気を用いた所定の前処理(混合工程、捕集工程、乖離工程、中和工程)を行うとともに、特定の工程で使用されるモノクローナル抗体の種類を異なるものにしている。
本発明の方法はこのような構成をとるため、上述した効果が得られるものと推測される。特に、上記前処理で使用されるモノクローナル抗体Xと展開工程で使用されるモノクローナル抗体Y及び/又はモノクローナル抗体Zが異なる点に特徴があると考えられる。
本発明者らの検討から、モノクローナル抗体で修飾された磁性粒子(修飾磁性粒子)に抗原を反応させ、濃縮等の操作後に修飾磁性粒子を乖離させて抗原含有液(特に、抗原濃縮液)を得た場合、液中に乖離した修飾磁性粒子が残存して、イムノクロマトグラフィーの抗原抗体反応を阻害する場合があることが分かっている。
本発明の方法は上記知見等に基づくものである。すなわち、本発明の方法においては、上記前処理で使用されるモノクローナル抗体とイムノクロマトグラフィー(展開工程)で使用されるモノクローナル抗体が異なる。このため、乖離した修飾磁性粒子(モノクローナル抗体で修飾された磁性粒子)が抗原と再度反応したとしても、イムノクロマトグラフィーの抗原抗体反応を阻害することなく、高い検出感度が得られるものと推測される。
本発明の方法はこのような構成をとるため、上述した効果が得られるものと推測される。特に、上記前処理で使用されるモノクローナル抗体Xと展開工程で使用されるモノクローナル抗体Y及び/又はモノクローナル抗体Zが異なる点に特徴があると考えられる。
本発明者らの検討から、モノクローナル抗体で修飾された磁性粒子(修飾磁性粒子)に抗原を反応させ、濃縮等の操作後に修飾磁性粒子を乖離させて抗原含有液(特に、抗原濃縮液)を得た場合、液中に乖離した修飾磁性粒子が残存して、イムノクロマトグラフィーの抗原抗体反応を阻害する場合があることが分かっている。
本発明の方法は上記知見等に基づくものである。すなわち、本発明の方法においては、上記前処理で使用されるモノクローナル抗体とイムノクロマトグラフィー(展開工程)で使用されるモノクローナル抗体が異なる。このため、乖離した修飾磁性粒子(モノクローナル抗体で修飾された磁性粒子)が抗原と再度反応したとしても、イムノクロマトグラフィーの抗原抗体反応を阻害することなく、高い検出感度が得られるものと推測される。
以下、本発明の方法が備える各工程について説明する。なお、混合工程から中和工程までを合わせて「磁性粒子プロセス」とも言う。
[混合工程]
混合工程は、抗原を含み得る試料と、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、上記抗原と上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る工程である。
混合工程は、抗原を含み得る試料と、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、上記抗原と上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る工程である。
〔試料〕
混合工程で使用される試料は、抗原を含み得る試料であれば特に制限されない。そのような試料としては、例えば、生物学的試料、特には動物(特にヒト)の体液(例えば、血液、血清、血漿、髄液、涙液、汗、尿、膿、鼻水、又は喀痰)若しくは排泄物(例えば、糞便)、臓器、組織、粘膜や皮膚、それらを含むと考えられる擦過検体(スワブ)、うがい液、又は動植物それ自体若しくはそれらの乾燥体を挙げることができる。
混合工程で使用される試料は、抗原を含み得る試料であれば特に制限されない。そのような試料としては、例えば、生物学的試料、特には動物(特にヒト)の体液(例えば、血液、血清、血漿、髄液、涙液、汗、尿、膿、鼻水、又は喀痰)若しくは排泄物(例えば、糞便)、臓器、組織、粘膜や皮膚、それらを含むと考えられる擦過検体(スワブ)、うがい液、又は動植物それ自体若しくはそれらの乾燥体を挙げることができる。
<抗原>
抗原としては、例えば、菌、細菌(例えば、結核菌、結核菌に含まれるリポアラビノマンナン(LAM))、バクテリア、ウイルス(例えば、インフルエンザウイルス)や、それらの核タンパク質等が挙げられる。なお、LAMは、結核における主要な抗原であり、細胞膜および細胞壁の主要構成成分である糖脂質である。
抗原は、本発明の効果等がより優れる理由から、ウイルス又はLAMであることが好ましく、ウイルスであることがより好ましく、インフルエンザウイルスであることがさらに好ましい。
抗原としては、例えば、菌、細菌(例えば、結核菌、結核菌に含まれるリポアラビノマンナン(LAM))、バクテリア、ウイルス(例えば、インフルエンザウイルス)や、それらの核タンパク質等が挙げられる。なお、LAMは、結核における主要な抗原であり、細胞膜および細胞壁の主要構成成分である糖脂質である。
抗原は、本発明の効果等がより優れる理由から、ウイルス又はLAMであることが好ましく、ウイルスであることがより好ましく、インフルエンザウイルスであることがさらに好ましい。
<試料の前処理>
上記試料は、試料をそのままで、又は、抗原を適当な抽出用溶媒を用いて抽出して得られる抽出液の形で、更には、抽出液を適当な希釈剤で希釈して得られる希釈液の形、若しくは抽出液を適当な方法で濃縮した形で、用いることができる。
上記抽出用溶媒としては、通常の免疫学的分析法で用いられる溶媒(例えば、水、生理食塩液、又は緩衝液等)、あるいは、かかる溶媒で希釈することにより直接抗原抗体反応を実施することができる水混和性有機溶媒を用いることもできる。
上記試料は、試料をそのままで、又は、抗原を適当な抽出用溶媒を用いて抽出して得られる抽出液の形で、更には、抽出液を適当な希釈剤で希釈して得られる希釈液の形、若しくは抽出液を適当な方法で濃縮した形で、用いることができる。
上記抽出用溶媒としては、通常の免疫学的分析法で用いられる溶媒(例えば、水、生理食塩液、又は緩衝液等)、あるいは、かかる溶媒で希釈することにより直接抗原抗体反応を実施することができる水混和性有機溶媒を用いることもできる。
〔修飾磁性粒子〕
上記修飾磁性粒子は、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である。
上記修飾磁性粒子は、上記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である。
<磁性粒子>
上記磁性粒子の材料は磁性を有する材料であれば特に制限されないが、具体例としては、鉄、コバルト、ニッケル、これらの酸化物、フェライト、及び、これらの合金等が挙げられる。なかでも、本発明の効果等がより優れる理由から、酸化鉄が好ましい。
磁性粒子は磁性を有する材料を単独で粒子状に成形した粒子であってもよいし、磁性を有する材料をコアとしてその表面を高分子(例えば、ポリスチレン、シリカゲル等)等で被覆した粒子、又は、磁性を有する材料を用いて高分子等をコアとしたその表面を被覆した粒子であってもよい。
上記磁性粒子の材料は磁性を有する材料であれば特に制限されないが、具体例としては、鉄、コバルト、ニッケル、これらの酸化物、フェライト、及び、これらの合金等が挙げられる。なかでも、本発明の効果等がより優れる理由から、酸化鉄が好ましい。
磁性粒子は磁性を有する材料を単独で粒子状に成形した粒子であってもよいし、磁性を有する材料をコアとしてその表面を高分子(例えば、ポリスチレン、シリカゲル等)等で被覆した粒子、又は、磁性を有する材料を用いて高分子等をコアとしたその表面を被覆した粒子であってもよい。
(粒子径)
磁性粒子の粒子径は特に制限されないが、本発明の効果等がより優れる理由から、0.05μm~10μmであることが好ましく、0.1μm~5μmであることがより好ましい。
磁性粒子の粒子径は特に制限されないが、本発明の効果等がより優れる理由から、0.05μm~10μmであることが好ましく、0.1μm~5μmであることがより好ましい。
なお、粒子径は、市販の粒度分布計等で計測することができる。粒度分布の測定法としては、光学顕微鏡法、共焦点レーザー顕微鏡法、電子顕微鏡法、原子間力顕微鏡法、静的光散乱法、レーザー回折法、動的光散乱法、遠心沈降法、電気パルス計測法、クロマトグラフィー法、超音波減衰法等が知られており、それぞれの原理に対応した装置が市販されている。粒子径の測定方法としては、粒子径範囲および測定の容易さから、動的光散乱法を好ましく用いることができる。動的光散乱を用いた市販の測定装置としては、ナノトラックUPA(日機装(株))、動的光散乱式粒径分布測定装置LB-550((株)堀場製作所)、濃厚系粒径アナライザーFPAR-1000(大塚電子(株))等が挙げられ、本発明においては、25℃の測定温度で測定したメジアン径(d=50)の値として求める。
<モノクローナル抗体X>
モノクローナル抗体Xは、上記抗原と特異的に親和性を有するモノクローナル抗体であって、後述するモノクローナル抗体Y及びモノクローナル抗体Zと異なるモノクローナル抗体である。
モノクローナル抗体は、例えば、抗原によって免疫された動物の脾臓細胞を用いる細胞融合によって得られるモノクローナル抗体、あるいは、それらの断片[例えば、F(ab’)2、Fab、Fab’、又はFv]を用いることができる。これらの抗体の調製は、常法により行うことができる。
モノクローナル抗体Xは、上記抗原と特異的に親和性を有するモノクローナル抗体であって、後述するモノクローナル抗体Y及びモノクローナル抗体Zと異なるモノクローナル抗体である。
モノクローナル抗体は、例えば、抗原によって免疫された動物の脾臓細胞を用いる細胞融合によって得られるモノクローナル抗体、あるいは、それらの断片[例えば、F(ab’)2、Fab、Fab’、又はFv]を用いることができる。これらの抗体の調製は、常法により行うことができる。
<修飾磁性粒子の製造方法>
上記修飾磁性粒子を製造する方法は特に制限されず、公知の方法を用いることができる。例えば、磁性粒子をEDC(1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド)で活性化し、モノクローナル抗体Xを磁性粒子上に担持させる方法等が挙げられる。
上記修飾磁性粒子を製造する方法は特に制限されず、公知の方法を用いることができる。例えば、磁性粒子をEDC(1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド)で活性化し、モノクローナル抗体Xを磁性粒子上に担持させる方法等が挙げられる。
〔混合〕
上記混合工程では、上記試料と上記修飾磁性粒子とを混合する。
これにより、上記試料が抗原を含む場合には、試料中の抗原と上記修飾磁性粒子の上記抗原と特異的に親和性を有するモノクローナル抗体Xとが反応し、上記試料中で抗原と上記修飾磁性粒子との複合体が形成される。一方、上記試料が抗原を含まない場合には、複合体は形成されない。
上記混合工程では、上記試料と上記修飾磁性粒子とを混合する。
これにより、上記試料が抗原を含む場合には、試料中の抗原と上記修飾磁性粒子の上記抗原と特異的に親和性を有するモノクローナル抗体Xとが反応し、上記試料中で抗原と上記修飾磁性粒子との複合体が形成される。一方、上記試料が抗原を含まない場合には、複合体は形成されない。
[捕集工程]
捕集工程は、磁気を用いて、上述した混合工程後の磁性粒子複合体を含有する混合物中の磁性粒子を捕集する工程である。
ここで、「混合物中の磁性粒子を捕集する」とは「混合物中の磁性粒子複合体、並びに、混合物中に残存した、磁性粒子(修飾されなかった磁性粒子)及び修飾磁性粒子を捕集する」ことを意味する。
磁気を用いて上記混合工程後の混合物中の磁性粒子を捕集する方法は特に制限されず、例えば、磁気スタンドに設置したコニカル(円錐形)チューブに上記混合工程後の混合物を入れ、磁気で上記磁性粒子複合体を集めてから、余剰の試料を抜き取る方法等が挙げられる。
捕集工程は、磁気を用いて、上述した混合工程後の磁性粒子複合体を含有する混合物中の磁性粒子を捕集する工程である。
ここで、「混合物中の磁性粒子を捕集する」とは「混合物中の磁性粒子複合体、並びに、混合物中に残存した、磁性粒子(修飾されなかった磁性粒子)及び修飾磁性粒子を捕集する」ことを意味する。
磁気を用いて上記混合工程後の混合物中の磁性粒子を捕集する方法は特に制限されず、例えば、磁気スタンドに設置したコニカル(円錐形)チューブに上記混合工程後の混合物を入れ、磁気で上記磁性粒子複合体を集めてから、余剰の試料を抜き取る方法等が挙げられる。
[乖離工程]
乖離工程は、上述した捕集工程で捕集された磁性粒子と、アルカリ性又は酸性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る工程である。
乖離工程では、乖離液によって磁性粒子複合体(抗原と修飾磁性粒子との複合体)から修飾磁性粒子が乖離し、抗原と修飾磁性粒子とに分離する。結果として、抗原を含有する乖離液である抗原含有液が得られる。
乖離工程は、上述した捕集工程で捕集された磁性粒子と、アルカリ性又は酸性の液である乖離液とを混合することで、上記磁性粒子複合体から上記修飾磁性粒子を乖離させ、抗原含有液を得る工程である。
乖離工程では、乖離液によって磁性粒子複合体(抗原と修飾磁性粒子との複合体)から修飾磁性粒子が乖離し、抗原と修飾磁性粒子とに分離する。結果として、抗原を含有する乖離液である抗原含有液が得られる。
〔乖離液〕
乖離液は、アルカリ性又は酸性の液であれば特に制限されない。
上記アルカリ性の液は特に制限されないが、具体例としては、NaOH水溶液、KOH水溶液等が挙げられる。なかでも、本発明の効果等がより優れる理由から、NaOH水溶液が好ましい。
上記酸性の液は特に制限されないが、具体例としては、HCl水溶液、H2SO4水溶液、HNO3水溶液等が挙げられる。なかでも、本発明の効果等がより優れる理由から、HCl水溶液が好ましい。
乖離液は、本発明の効果等がより優れる理由から、アルカリ性の液であることが好ましい。
乖離液は、本発明の効果等がより優れる理由から、NaOH又はHClを含有するのが好ましく、NaOHを含有するのがより好ましく、NaOH水溶液であるのがさらに好ましい。
乖離液は、アルカリ性又は酸性の液であれば特に制限されない。
上記アルカリ性の液は特に制限されないが、具体例としては、NaOH水溶液、KOH水溶液等が挙げられる。なかでも、本発明の効果等がより優れる理由から、NaOH水溶液が好ましい。
上記酸性の液は特に制限されないが、具体例としては、HCl水溶液、H2SO4水溶液、HNO3水溶液等が挙げられる。なかでも、本発明の効果等がより優れる理由から、HCl水溶液が好ましい。
乖離液は、本発明の効果等がより優れる理由から、アルカリ性の液であることが好ましい。
乖離液は、本発明の効果等がより優れる理由から、NaOH又はHClを含有するのが好ましく、NaOHを含有するのがより好ましく、NaOH水溶液であるのがさらに好ましい。
<量>
乖離液の量は特に制限されないが、本発明の効果等がより優れる理由から、上述した混合工程で用いられる「抗原を含み得る試料」の量よりも少ない乖離液の量であることが好ましい。乖離液の量が上述した混合工程で用いられる「抗原を含み得る試料」の量よりも少ない場合、乖離液中の抗原の濃度は上述した混合工程で用いられる「抗原を含み得る試料」中の抗原の濃度よりも高くなる。すなわち、乖離工程によって得られる抗原含有液は、抗原の濃度が濃縮された液(抗原濃縮液)となる。
上述した混合工程で用いられる「抗原を含み得る試料」に対する乖離液の割合は、本発明の効果等がより優れる理由から、質量比で、1/5以下であることが好ましく、1/10以下であることがより好ましく、1/20以下であることがさらに好ましい。
乖離液の量は特に制限されないが、本発明の効果等がより優れる理由から、上述した混合工程で用いられる「抗原を含み得る試料」の量よりも少ない乖離液の量であることが好ましい。乖離液の量が上述した混合工程で用いられる「抗原を含み得る試料」の量よりも少ない場合、乖離液中の抗原の濃度は上述した混合工程で用いられる「抗原を含み得る試料」中の抗原の濃度よりも高くなる。すなわち、乖離工程によって得られる抗原含有液は、抗原の濃度が濃縮された液(抗原濃縮液)となる。
上述した混合工程で用いられる「抗原を含み得る試料」に対する乖離液の割合は、本発明の効果等がより優れる理由から、質量比で、1/5以下であることが好ましく、1/10以下であることがより好ましく、1/20以下であることがさらに好ましい。
[中和工程]
中和工程は、中和液を用いて、上述した乖離工程で得られた抗原含有液を中和することで、中和抗原含有液を得る工程である。
上述した乖離工程ではアルカリ性又は酸性の液である乖離液で乖離させるため、乖離工程で得られた抗原含有液は通常アルカリ性又は酸性である。一方、アルカリ性又は酸性の液を後述する展開工程に用いた場合、後述するモノクローナル抗体Yやモノクローナル抗体Zが変性して、検出感度の低下に繋がる場合がある。そのため、中和工程では、中和液を用いて抗原含有液を中和する。
中和工程は、中和液を用いて、上述した乖離工程で得られた抗原含有液を中和することで、中和抗原含有液を得る工程である。
上述した乖離工程ではアルカリ性又は酸性の液である乖離液で乖離させるため、乖離工程で得られた抗原含有液は通常アルカリ性又は酸性である。一方、アルカリ性又は酸性の液を後述する展開工程に用いた場合、後述するモノクローナル抗体Yやモノクローナル抗体Zが変性して、検出感度の低下に繋がる場合がある。そのため、中和工程では、中和液を用いて抗原含有液を中和する。
〔中和液〕
中和液は特に制限されないが、例えば、公知の緩衝液を用いることができる。
中和液は、本発明の効果等がより優れる理由から、上述した乖離工程で使用された乖離液がアルカリ性の液である場合は、HCl(特に、1M HCl)と、トリシン、トリス、HEPES(4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid)、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有するのが好ましく、上述した乖離工程で使用された乖離液が酸性の液である場合は、NaOH(特に、1M NaOH)と、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有するのが好ましい。
中和液は特に制限されないが、例えば、公知の緩衝液を用いることができる。
中和液は、本発明の効果等がより優れる理由から、上述した乖離工程で使用された乖離液がアルカリ性の液である場合は、HCl(特に、1M HCl)と、トリシン、トリス、HEPES(4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid)、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有するのが好ましく、上述した乖離工程で使用された乖離液が酸性の液である場合は、NaOH(特に、1M NaOH)と、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有するのが好ましい。
[展開工程]
展開工程は、上述した中和工程で得られた中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する工程である。
展開工程は、上述した中和工程で得られた中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する工程である。
〔金粒子複合体〕
上述のとおり、展開工程では、まず、上述した中和工程で得られた中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させる。
上述のとおり、展開工程では、まず、上述した中和工程で得られた中和抗原含有液中の抗原と、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させる。
<修飾金粒子>
修飾金粒子は、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である。
修飾金粒子は、上記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である。
(金粒子)
金粒子は特に制限されない。
金粒子は、後述する銀増幅工程において銀イオンを還元する触媒として働く。
金粒子は特に制限されない。
金粒子は、後述する銀増幅工程において銀イオンを還元する触媒として働く。
上記金粒子の粒子径は、本発明の効果等がより優れる理由から、100nm以下であることが好ましく、50nm以下であることがより好ましく、30nm以下であることがさらに好ましく、15nm以下であることが特に好ましい。
上記金粒子の粒子径の下限は特に制限されないが、本発明の効果等がより優れる理由から、1nm以上であることが好ましく、2nm以上であることがより好ましく、5nm以上であることがさらに好ましい。
なお、金粒子の粒子径は上述した磁性粒子と同様の方法で求めることができる。
上記金粒子の粒子径の下限は特に制限されないが、本発明の効果等がより優れる理由から、1nm以上であることが好ましく、2nm以上であることがより好ましく、5nm以上であることがさらに好ましい。
なお、金粒子の粒子径は上述した磁性粒子と同様の方法で求めることができる。
(モノクローナル抗体Y)
モノクローナル抗体Yは、上記抗原と結合し得るモノクローナル抗体であって、上述したモノクローナル抗体Xと異なるモノクローナル抗体であれば特に制限されない。
モノクローナル抗体Yの具体例及び好適な態様は、上述したモノクローナル抗体Xと同じである。
モノクローナル抗体Yは、上記抗原と結合し得るモノクローナル抗体であって、上述したモノクローナル抗体Xと異なるモノクローナル抗体であれば特に制限されない。
モノクローナル抗体Yの具体例及び好適な態様は、上述したモノクローナル抗体Xと同じである。
(修飾金粒子の製造方法)
上記修飾金粒子を製造する方法は特に制限されず、公知の方法を用いることができる。例えば、金とSH基とが化学結合することを利用し、モノクローナル抗体YにSH基を導入後、金粒子と接近するときにSH結合が開裂してAu表面上に生成するAu-S結合で固定化させる等の化学的な結合方法が挙げられる。
上記修飾金粒子を製造する方法は特に制限されず、公知の方法を用いることができる。例えば、金とSH基とが化学結合することを利用し、モノクローナル抗体YにSH基を導入後、金粒子と接近するときにSH結合が開裂してAu表面上に生成するAu-S結合で固定化させる等の化学的な結合方法が挙げられる。
〔不溶性担体〕
上記不溶性担体は、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位(テストライン)を有する不溶性担体である。不溶性担体は、抗原の種類に合わせて複数のテストラインを有していてもよい(例えば、インフルエンザA型ウイルス用のテストラインとインフルエンザB型用のテストライン)。また、不溶性担体は、上記金粒子複合体の展開を確認するために、テストラインより下流側にコントロールラインを有していてもよい。また、後述する銀増幅工程において還元剤液を用いる場合には、還元剤液を検出するために、テストラインより下流側に発色試薬固定化ラインを有していてもよい。
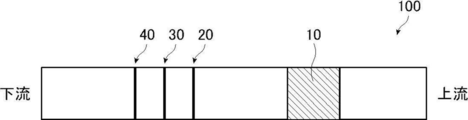
上記不溶性担体の具体的な態様としては、例えば、図1に示されるような、上流側から、金コロイド保持パッド10、テストライン20、コントロールライン30、発色試薬固定化ライン40を有するニトロセルロースメンブレン100が挙げられる。ここで、金コロイド保持パッド10はモノクローナル抗体Yで修飾された金粒子(修飾金粒子)を保持するパッドであり、テストライン20はモノクローナル抗体Zが固定化されたラインであり、コントロールライン30は展開を確認するためのラインであり、発色試薬固定化ライン40は後述する還元剤液を検出するためのラインである。ここで上流側、下流側とは、金粒子複合体が展開する際、上流側から下流側に向けて展開することを意図した記載を意味する。
上記不溶性担体(又はこれを有するイムノクロマトグラフキット)の具体的な態様としては、例えば、特許第5728453号公報に記載の不溶性担体及びイムノクロマトグラフキットが挙げられる。また、不溶性担体及びイムノクロマトグラフキットに関する特許第5728453号公報に記載の内容はすべて本明細書の開示の一部として本明細書中に援用される。
上記不溶性担体は、上記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位(テストライン)を有する不溶性担体である。不溶性担体は、抗原の種類に合わせて複数のテストラインを有していてもよい(例えば、インフルエンザA型ウイルス用のテストラインとインフルエンザB型用のテストライン)。また、不溶性担体は、上記金粒子複合体の展開を確認するために、テストラインより下流側にコントロールラインを有していてもよい。また、後述する銀増幅工程において還元剤液を用いる場合には、還元剤液を検出するために、テストラインより下流側に発色試薬固定化ラインを有していてもよい。
上記不溶性担体の具体的な態様としては、例えば、図1に示されるような、上流側から、金コロイド保持パッド10、テストライン20、コントロールライン30、発色試薬固定化ライン40を有するニトロセルロースメンブレン100が挙げられる。ここで、金コロイド保持パッド10はモノクローナル抗体Yで修飾された金粒子(修飾金粒子)を保持するパッドであり、テストライン20はモノクローナル抗体Zが固定化されたラインであり、コントロールライン30は展開を確認するためのラインであり、発色試薬固定化ライン40は後述する還元剤液を検出するためのラインである。ここで上流側、下流側とは、金粒子複合体が展開する際、上流側から下流側に向けて展開することを意図した記載を意味する。
上記不溶性担体(又はこれを有するイムノクロマトグラフキット)の具体的な態様としては、例えば、特許第5728453号公報に記載の不溶性担体及びイムノクロマトグラフキットが挙げられる。また、不溶性担体及びイムノクロマトグラフキットに関する特許第5728453号公報に記載の内容はすべて本明細書の開示の一部として本明細書中に援用される。
<不溶性担体>
不溶性担体は、多孔性担体が好ましい。特に、本発明の効果等がより優れる理由から、ニトロセルロース膜(ニトロセルロースメンブレン)、セルロース膜、アセチルセルロース膜、ポリスルホン膜、ポリエーテルスルホン膜、ナイロン膜、ガラス繊維、不織布、布、または糸等が好ましく、ニトロセルロース膜がより好ましい。
不溶性担体は、多孔性担体が好ましい。特に、本発明の効果等がより優れる理由から、ニトロセルロース膜(ニトロセルロースメンブレン)、セルロース膜、アセチルセルロース膜、ポリスルホン膜、ポリエーテルスルホン膜、ナイロン膜、ガラス繊維、不織布、布、または糸等が好ましく、ニトロセルロース膜がより好ましい。
<モノクローナル抗体Z>
モノクローナル抗体Zは、上記抗原と結合し得るモノクローナル抗体であって、上述したモノクローナル抗体Xと異なるモノクローナル抗体であれば特に制限されない。
モノクローナル抗体Zの具体例及び好適な態様は、上述したモノクローナル抗体Xと同じである。
モノクローナル抗体Zは、上記抗原と結合し得るモノクローナル抗体であって、上述したモノクローナル抗体Xと異なるモノクローナル抗体であれば特に制限されない。
モノクローナル抗体Zの具体例及び好適な態様は、上述したモノクローナル抗体Xと同じである。
〔展開〕
金粒子複合体を形成させた状態でテストラインを有する不溶性担体に展開する方法は特に制限されないが、例えば、上述した図1に示されるようなニトロセルロースメンブレン100(又はこれを有するイムノクロマトグラフキット)を準備して、上述した中和工程で得られた中和抗原含有液を金コロイド保持パッドに滴下し、図1に示されるように上流側から下流側に毛細管現象を利用して移動させる方法等が挙げられる。
金粒子複合体を形成させた状態でテストラインを有する不溶性担体に展開する方法は特に制限されないが、例えば、上述した図1に示されるようなニトロセルロースメンブレン100(又はこれを有するイムノクロマトグラフキット)を準備して、上述した中和工程で得られた中和抗原含有液を金コロイド保持パッドに滴下し、図1に示されるように上流側から下流側に毛細管現象を利用して移動させる方法等が挙げられる。
[捕捉工程]
捕捉工程は、上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する工程である。
上述のとおり、不溶性担体の反応部位には抗原と結合し得るモノクローナル抗体Zが固定化されているため、上記展開工程で不溶性担体に展開された金粒子複合体(抗原と修飾金粒子との複合体)は、不溶性担体の反応部位(テストライン)で捕捉される。
なお、試料が抗原を含まない場合には上記金粒子複合体が形成されないため、金粒子複合体は不溶性担体の反応部位で捕捉されない。
捕捉工程は、上記不溶性担体の反応部位において、上記金粒子複合体を捕捉する工程である。
上述のとおり、不溶性担体の反応部位には抗原と結合し得るモノクローナル抗体Zが固定化されているため、上記展開工程で不溶性担体に展開された金粒子複合体(抗原と修飾金粒子との複合体)は、不溶性担体の反応部位(テストライン)で捕捉される。
なお、試料が抗原を含まない場合には上記金粒子複合体が形成されないため、金粒子複合体は不溶性担体の反応部位で捕捉されない。
[銀増幅工程]
銀増幅工程は、上記捕捉工程で捕捉された金粒子複合体を銀増幅する工程である。
銀増幅工程は、上記捕捉工程後の不溶性担体に銀イオンを付与することで、不溶性担体の反応部位で捕捉された金粒子複合体に大きな銀粒子を形成する工程である。より詳細には、上記金粒子複合体の金粒子を触媒として銀イオンが還元され、銀粒子(例えば、直径10μm以上)が形成される工程である。
これにより、捕捉された金粒子複合体の検出感度が著しく向上する。
銀増幅工程は、上記捕捉工程で捕捉された金粒子複合体を銀増幅する工程である。
銀増幅工程は、上記捕捉工程後の不溶性担体に銀イオンを付与することで、不溶性担体の反応部位で捕捉された金粒子複合体に大きな銀粒子を形成する工程である。より詳細には、上記金粒子複合体の金粒子を触媒として銀イオンが還元され、銀粒子(例えば、直径10μm以上)が形成される工程である。
これにより、捕捉された金粒子複合体の検出感度が著しく向上する。
〔好適な態様〕
上記捕捉工程後の不溶性担体に銀イオンを付与する方法は特に制限されないが、本発明の効果等がより優れる理由から、下記還元剤液及び下記銀増幅液を使用する方法が好ましい。
また、還元剤液及び銀増幅液に加えて、特異的な結合反応以外で不溶性担体に残存している複合体を洗浄するために洗浄液を使用してもよい。上記還元液は洗浄液を兼ねていてもよい。
上記捕捉工程後の不溶性担体に銀イオンを付与する方法は特に制限されないが、本発明の効果等がより優れる理由から、下記還元剤液及び下記銀増幅液を使用する方法が好ましい。
また、還元剤液及び銀増幅液に加えて、特異的な結合反応以外で不溶性担体に残存している複合体を洗浄するために洗浄液を使用してもよい。上記還元液は洗浄液を兼ねていてもよい。
<還元剤液>
上記還元剤液は、銀イオンを還元し得る還元剤を含有する。銀イオンを還元し得る還元剤は、銀イオンを銀に還元することができれば、無機・有機のいかなる材料、またはその混合物でも用いることができる。無機還元剤としては、Fe2+、V2+、Ti3+、などの金属イオンで原子価の変化し得る還元性金属塩、還元性金属錯塩を好ましく挙げることができる。無機還元剤を用いる際には、酸化されたイオンを錯形成するか還元して、除去するか無害化する必要がある。例えば、Fe2+を還元剤として用いる系では、クエン酸やエチレンジアミン四酢酸(EDTA)を用いて酸化物であるFe3+の錯体を形成し、無害化することができる。本発明ではこのような無機還元剤を用いることが好ましく、本発明のより好ましい態様としては、Fe2+の金属塩を還元剤として用いることが好ましい。
上記還元剤液は、銀イオンを還元し得る還元剤を含有する。銀イオンを還元し得る還元剤は、銀イオンを銀に還元することができれば、無機・有機のいかなる材料、またはその混合物でも用いることができる。無機還元剤としては、Fe2+、V2+、Ti3+、などの金属イオンで原子価の変化し得る還元性金属塩、還元性金属錯塩を好ましく挙げることができる。無機還元剤を用いる際には、酸化されたイオンを錯形成するか還元して、除去するか無害化する必要がある。例えば、Fe2+を還元剤として用いる系では、クエン酸やエチレンジアミン四酢酸(EDTA)を用いて酸化物であるFe3+の錯体を形成し、無害化することができる。本発明ではこのような無機還元剤を用いることが好ましく、本発明のより好ましい態様としては、Fe2+の金属塩を還元剤として用いることが好ましい。
なお、湿式のハロゲン化銀写真感光材料に用いられる現像主薬(例えばメチル没食子酸塩、ヒドロキノン、置換ヒドロキノン、3-ピラゾリドン類、p-アミノフェノール類、p-フェニレンジアミン類、ヒンダードフェノール類、アミドキシム類、アジン類、カテコール類、ピロガロール類、アスコルビン酸(またはその誘導体)、およびロイコ色素類)、および本分野での技術に熟練しているものにとって明らかなその他の材料、例えば米国特許第6,020,117号に記載されている材料も還元剤として用いることができる。
還元剤としては、アスコルビン酸還元剤も好ましい。有用なアスコルビン酸還元剤は、アスコルビン酸とその類縁体、異性体とその誘導体を含み、例えば、D-またはL-アスコルビン酸とその糖誘導体(例えばγ-ラクトアスコルビン酸、グルコアスコルビン酸、フコアスコルビン酸、グルコヘプトアスコルビン酸、マルトアスコルビン酸)、アスコルビン酸のナトリウム塩、アスコルビン酸のカリウム塩、イソアスコルビン酸(又はL-エリスロアスコルビン酸)、その塩(例えばアルカリ金属塩、アンモニウム塩又は当技術分野において知られている塩)、エンジオールタイプのアスコルビン酸、エナミノールタイプのアスコルビン酸、チオエノ-ルタイプのアスコルビン酸等を好ましく挙げることができ、特にはD、LまたはD,L-アスコルビン酸(そして、そのアルカリ金属塩)若しくはイソアスコルビン酸(またはそのアルカリ金属塩)が好ましく、ナトリウム塩が好ましい塩である。必要に応じてこれらの還元剤の混合物を用いることができる。
還元剤液は、本発明の効果等がより優れる理由から、展開工程における展開方向と還元剤液の展開方向との間の角度が0度~150度になるように流すのが好ましく、展開工程における展開方向と還元剤液の展開方向との間の角度が0度~135度になるように流すのがより好ましい。
なお、展開工程における展開方向と還元剤液の展開方向との間の角度を調節する方法としては、例えば、特開2009-150869号公報の実施例に記載の方法等が挙げられる。
なお、展開工程における展開方向と還元剤液の展開方向との間の角度を調節する方法としては、例えば、特開2009-150869号公報の実施例に記載の方法等が挙げられる。
<銀増幅液>
上記銀増幅液は、銀イオンを含む化合物を含有する液である。銀イオンを含む化合物としては、例えば、有機銀塩、無機銀塩、もしくは銀錯体を用いることができる。好ましくは、水などの溶媒に対して溶解度の高い銀イオン含有化合物である、硝酸銀、酢酸銀、乳酸銀、酪酸銀、チオ硫酸銀などが挙げられる。特に好ましくは硝酸銀である。銀錯体としては、水酸基やスルホン基など水溶性基を有する配位子に配位された銀錯体が好ましく、ヒドロキシチオエーテル銀等が挙げられる。
上記銀増幅液は、銀イオンを含む化合物を含有する液である。銀イオンを含む化合物としては、例えば、有機銀塩、無機銀塩、もしくは銀錯体を用いることができる。好ましくは、水などの溶媒に対して溶解度の高い銀イオン含有化合物である、硝酸銀、酢酸銀、乳酸銀、酪酸銀、チオ硫酸銀などが挙げられる。特に好ましくは硝酸銀である。銀錯体としては、水酸基やスルホン基など水溶性基を有する配位子に配位された銀錯体が好ましく、ヒドロキシチオエーテル銀等が挙げられる。
有機銀塩、無機銀塩、もしくは銀錯体は、銀として銀増幅液に0.001mol/L~5mol/L、好ましくは0.005mol/L~3mol/L、更には0.01mol/L~1mol/Lの濃度で含有されることが好ましい。
銀増幅液の助剤としては、緩衝剤、防腐剤、例えば酸化防止剤または有機安定剤、速度調節剤等が挙げられる。緩衝剤としては、例えば、酢酸、クエン酸、水酸化ナトリウムまたはこれらの塩のうちの一つ、又はトリス(ヒドロキシメチル)アミノメタンを用いた緩衝剤、その他一般的化学実験に用いられる緩衝剤を用いることができる。これら緩衝剤を適宜用いて、その増幅溶液に最適なpHに調整することができる。また、カブリ防止剤としてアルキルアミンを助剤として用いることができ、特に好ましくはドデシルアミンである。またこれら助剤の溶解性向上のため、界面活性剤を用いることができ、特に好ましくはC9H19-C6H4-O-(CH2CH2O)50Hである。
銀増幅液は、本発明の効果等がより優れる理由から、上述した展開工程と逆方向から流すのが好ましく、展開工程における展開方向と還元剤液の展開方向との間の角度が45度~180度になるように流すのがより好ましい。
なお、展開工程における展開方向と銀増幅液の展開方向との間の角度を調節する方法としては、例えば、特開2009-150869号公報の実施例に記載の方法等が挙げられる。
なお、展開工程における展開方向と銀増幅液の展開方向との間の角度を調節する方法としては、例えば、特開2009-150869号公報の実施例に記載の方法等が挙げられる。
[モノクローナル抗体]
上述のとおり、モノクローナル抗体Xとモノクローナル抗体Yは互いに異なり、モノクローナル抗体Xとモノクローナル抗体Zは互いに異なる。
モノクローナル抗体Yとモノクローナル抗体Zは同じであっても異なってもよいが、本発明の効果等がより優れる理由から、異なるのが好ましい。この場合、モノクローナル抗体Xとモノクローナル抗体Yとモノクローナル抗体Zはいずれも異なるモノクローナル抗体となる。
上述のとおり、モノクローナル抗体Xとモノクローナル抗体Yは互いに異なり、モノクローナル抗体Xとモノクローナル抗体Zは互いに異なる。
モノクローナル抗体Yとモノクローナル抗体Zは同じであっても異なってもよいが、本発明の効果等がより優れる理由から、異なるのが好ましい。この場合、モノクローナル抗体Xとモノクローナル抗体Yとモノクローナル抗体Zはいずれも異なるモノクローナル抗体となる。
モノクローナル抗体Xのエピトープとモノクローナル抗体Yのエピトープは、本発明の効果等がより優れる理由から、互いに異なるのが好ましい。
モノクローナル抗体Xのエピトープとモノクローナル抗体Zのエピトープは、本発明の効果等がより優れる理由から、互いに異なるのが好ましい。
モノクローナル抗体Yのエピトープとモノクローナル抗体Zのエピトープは同じであっても異なってもよいが、本発明の効果等がより優れる理由から、異なるのが好ましい。この場合、モノクローナル抗体Xのエピトープとモノクローナル抗体Yのエピトープとモノクローナル抗体Zのエピトープはいずれも異なることになる。
なお、モノクローナル抗体のエピトープが異なることは、例えば、ELISA(Enzyme-Linked Immuno Sorbent Assay)によって確認することができる。
モノクローナル抗体Xのエピトープとモノクローナル抗体Zのエピトープは、本発明の効果等がより優れる理由から、互いに異なるのが好ましい。
モノクローナル抗体Yのエピトープとモノクローナル抗体Zのエピトープは同じであっても異なってもよいが、本発明の効果等がより優れる理由から、異なるのが好ましい。この場合、モノクローナル抗体Xのエピトープとモノクローナル抗体Yのエピトープとモノクローナル抗体Zのエピトープはいずれも異なることになる。
なお、モノクローナル抗体のエピトープが異なることは、例えば、ELISA(Enzyme-Linked Immuno Sorbent Assay)によって確認することができる。
以下、実施例により、本発明についてさらに詳細に説明するが、本発明はこれらに限定されるものではない。
[検体液の調製]
クイックS-インフルA・B「生研」陰性/陽性コントロール液(品番;322968、デンカ生研社製)を用いて検体液(抗原を含み得る試料)を調製した。
具体的には、上記陽性コントロール液を、1質量%BSA(Bovine Serum Albumin)を含むPBS(Phosphate buffered salts)バッファーで、10倍ずつ希釈し、各希釈率の検体液(抗原を含み得る試料)とした。
なお、市販のイムノクロマト検出キット「キャピリアFluA+B」(アルフレッサファーマ社製)による検出限界(最小検出感度)はA型B型共に1/40であった。
クイックS-インフルA・B「生研」陰性/陽性コントロール液(品番;322968、デンカ生研社製)を用いて検体液(抗原を含み得る試料)を調製した。
具体的には、上記陽性コントロール液を、1質量%BSA(Bovine Serum Albumin)を含むPBS(Phosphate buffered salts)バッファーで、10倍ずつ希釈し、各希釈率の検体液(抗原を含み得る試料)とした。
なお、市販のイムノクロマト検出キット「キャピリアFluA+B」(アルフレッサファーマ社製)による検出限界(最小検出感度)はA型B型共に1/40であった。
[実施例1]
以下のとおり、実施例1のイムノクロマトグラフィーを行った。
以下のとおり、実施例1のイムノクロマトグラフィーを行った。
〔混合工程〕
ThermoFisher社製の磁性粒子(DynabeadsMyOne-COOH、粒子径:1μm、Thermofisher社製)をEDC(1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド)で活性化し、抗インフルエンザA型モノクローナル抗体(Funakoshi、#GTX629544)を磁性粒子上に担持させ、抗インフルエンザA型モノクローナル抗体(モノクローナル抗体X)で修飾された磁性粒子である修飾磁性粒子を得た。
ThermoFisher社製の磁性粒子(DynabeadsMyOne-COOH、粒子径:1μm、Thermofisher社製)をEDC(1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド)で活性化し、抗インフルエンザA型モノクローナル抗体(Funakoshi、#GTX629544)を磁性粒子上に担持させ、抗インフルエンザA型モノクローナル抗体(モノクローナル抗体X)で修飾された磁性粒子である修飾磁性粒子を得た。
15mLのコニカルチューブに上述した検体液(6mL)を入れ、そこに上記修飾磁性粒子を1mg入れて、40分間撹拌を行いつつ反応させた。このようにして、インフルエンザA型ウイルスと上記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得た。
〔捕集工程〕
反応後、コニカルチューブを磁石スタンドに設置して、10分間、磁性粒子(修飾されなかった磁性粒子、修飾磁性粒子、磁性粒子複合体)を集磁した。エッペンドルフ(ピペット)でコニカルチューブから余剰の検体液を抜きとることで、上記磁性粒子(修飾されなかった磁性粒子、修飾磁性粒子、磁性粒子複合体)を捕集した。
反応後、コニカルチューブを磁石スタンドに設置して、10分間、磁性粒子(修飾されなかった磁性粒子、修飾磁性粒子、磁性粒子複合体)を集磁した。エッペンドルフ(ピペット)でコニカルチューブから余剰の検体液を抜きとることで、上記磁性粒子(修飾されなかった磁性粒子、修飾磁性粒子、磁性粒子複合体)を捕集した。
〔乖離工程〕
即座に、50mM NaOH水溶液(アルカリ性の液)を200μL添加した。添加後5分間超音波処理して、60分間静置した。このようにして、磁性粒子複合体から修飾磁性粒子を乖離させた。静置後、再びコニカルチューブを磁石スタンドに設置して、10分間、乖離した修飾磁性粒子を集磁し、上澄み液(インフルエンザA型ウイルス含有液)(抗原含有液)を回収した。
即座に、50mM NaOH水溶液(アルカリ性の液)を200μL添加した。添加後5分間超音波処理して、60分間静置した。このようにして、磁性粒子複合体から修飾磁性粒子を乖離させた。静置後、再びコニカルチューブを磁石スタンドに設置して、10分間、乖離した修飾磁性粒子を集磁し、上澄み液(インフルエンザA型ウイルス含有液)(抗原含有液)を回収した。
〔中和工程〕
10mM トリスHCl 10μLを中和液として用いて、上記インフルエンザA型ウイルス含有液を中和して、中和インフルエンザA型ウイルス含有液(中和抗原含有液)を得た。
10mM トリスHCl 10μLを中和液として用いて、上記インフルエンザA型ウイルス含有液を中和して、中和インフルエンザA型ウイルス含有液(中和抗原含有液)を得た。
〔展開工程〕
図1に示されるように、上流側から、金コロイド保持パッド10、テストライン20、コントロールライン30、発色試薬固定化ライン40を有するニトロセルロースメンブレン100を準備した。なお、金コロイド保持パッド10は、抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)(モノクローナル抗体Y)で修飾された金コロイド(修飾金粒子)を保持するパッドであり、テストライン20は、抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)(モノクローナル抗体Z)が固定化されたラインであり、コントロールライン30は、展開を確認するためのラインであり、発色試薬固定化ライン40は、後述する還元液を検出するためのラインである。
図1に示されるように、上流側から、金コロイド保持パッド10、テストライン20、コントロールライン30、発色試薬固定化ライン40を有するニトロセルロースメンブレン100を準備した。なお、金コロイド保持パッド10は、抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)(モノクローナル抗体Y)で修飾された金コロイド(修飾金粒子)を保持するパッドであり、テストライン20は、抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)(モノクローナル抗体Z)が固定化されたラインであり、コントロールライン30は、展開を確認するためのラインであり、発色試薬固定化ライン40は、後述する還元液を検出するためのラインである。
上記中和インフルエンザA型ウイルス含有液を金コロイド保持パッドに滴下した。これにより、液中のインフルエンザA型ウイルスと金コロイド保持パッド中の抗インフルエンザA型モノクローナル抗体(モノクローナル抗体Y)で修飾された金コロイド粒子(修飾金粒子)との複合体である金粒子複合体が形成された。この状態で、上記ニトロセルロースメンブレンの下流側に展開した。
〔捕捉工程〕
展開工程で展開された金粒子複合体はテストラインで捕捉される。
展開工程で展開された金粒子複合体はテストラインで捕捉される。
〔銀増幅工程〕
以下のとおり、銀増幅工程を実施した。
以下のとおり、銀増幅工程を実施した。
<還元剤液の調製>
水290gに、硝酸鉄(III)九水和物(富士フイルム和光純薬社製)を水に溶解して作製した1mol/Lの硝酸鉄水溶液23.6mL、及び、クエン酸(富士フイルム和光純薬社製)13.1gを溶解させた。全て溶解した後、スターラーで攪拌しながら硝酸(10質量%)を36ml加え、硫酸アンモニウム鉄(II)六水和物(富士フイルム和光純薬社製)を60.8g加え、これを還元剤液とした。
水290gに、硝酸鉄(III)九水和物(富士フイルム和光純薬社製)を水に溶解して作製した1mol/Lの硝酸鉄水溶液23.6mL、及び、クエン酸(富士フイルム和光純薬社製)13.1gを溶解させた。全て溶解した後、スターラーで攪拌しながら硝酸(10質量%)を36ml加え、硫酸アンモニウム鉄(II)六水和物(富士フイルム和光純薬社製)を60.8g加え、これを還元剤液とした。
<銀増幅液の調製>
水66gに、硝酸銀溶液8mL(10gの硝酸銀を含む)と1mol/Lの硝酸鉄水溶液24mLを加えた。さらに、この溶液と、硝酸(10質量%)5.9mL、ドデシルアミン(富士フイルム和光純薬社製)0.1g、界面活性剤C12H25-C6H4-O-(CH2CH2O)50H 0.1gをあらかじめ47.6gの水に溶解した溶液を混合し、これを銀増幅液とした。
水66gに、硝酸銀溶液8mL(10gの硝酸銀を含む)と1mol/Lの硝酸鉄水溶液24mLを加えた。さらに、この溶液と、硝酸(10質量%)5.9mL、ドデシルアミン(富士フイルム和光純薬社製)0.1g、界面活性剤C12H25-C6H4-O-(CH2CH2O)50H 0.1gをあらかじめ47.6gの水に溶解した溶液を混合し、これを銀増幅液とした。
<還元剤液の展開>
ニトロセルロースメンブレンにおいて、上述した展開工程と同じ方向から(より上流側から)、上述のとおり調製した還元剤液を流した。
ニトロセルロースメンブレンにおいて、上述した展開工程と同じ方向から(より上流側から)、上述のとおり調製した還元剤液を流した。
<銀増幅液の展開>
発色試薬固定化ラインが変色した後、展開工程における展開方向と逆方向から(下流側から)、上述のとおり調製した銀増幅液を流した。このようにして、テストラインで捕捉された金粒子複合体を銀増幅した。
発色試薬固定化ラインが変色した後、展開工程における展開方向と逆方向から(下流側から)、上述のとおり調製した銀増幅液を流した。このようにして、テストラインで捕捉された金粒子複合体を銀増幅した。
〔評価〕
テストラインの着色を目視により確認し、着色が確認された最も小さい希釈率(最小検出感度)を調べた。結果を表1に示す。最小検出感度が小さいほど、抗原の濃度が薄い試料でも抗原を検出できることを意味し、検出感度が高いことを意味する。
テストラインの着色を目視により確認し、着色が確認された最も小さい希釈率(最小検出感度)を調べた。結果を表1に示す。最小検出感度が小さいほど、抗原の濃度が薄い試料でも抗原を検出できることを意味し、検出感度が高いことを意味する。
[比較例1]
混合工程から中和工程までを行わずに、展開工程において中和インフルエンザA型ウイルス含有液の代わりに上述した検体液自体を用いた点以外は、実施例1と同様の手順にしたがって、イムノクロマトグラフィーを実施し、評価した。結果を表1に示す。
混合工程から中和工程までを行わずに、展開工程において中和インフルエンザA型ウイルス含有液の代わりに上述した検体液自体を用いた点以外は、実施例1と同様の手順にしたがって、イムノクロマトグラフィーを実施し、評価した。結果を表1に示す。
[比較例2]
モノクローナル抗体Xとして、抗インフルエンザA型モノクローナル抗体(Funakoshi、#GTX629544)の代わりに抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)を使用した点以外は、実施例1と同様の手順に従って、イムノクロマトグラフィーを実施し、評価した。結果を表1に示す。比較例2において、モノクローナル抗体Xとモノクローナル抗体Yは互いに同じであり、モノクローナル抗体Xとモノクローナル抗体Zは互いに同じである。
モノクローナル抗体Xとして、抗インフルエンザA型モノクローナル抗体(Funakoshi、#GTX629544)の代わりに抗インフルエンザA型モノクローナル抗体(Anti-Influenza A SPTN-5 7307、Medix Biochemica社)を使用した点以外は、実施例1と同様の手順に従って、イムノクロマトグラフィーを実施し、評価した。結果を表1に示す。比較例2において、モノクローナル抗体Xとモノクローナル抗体Yは互いに同じであり、モノクローナル抗体Xとモノクローナル抗体Zは互いに同じである。
表1から分かるように、磁性粒子プロセスを行わなかった比較例1、並びに、磁性粒子プロセスを行ったが、モノクローナル抗体Xとモノクローナル抗体Yが同じであり、モノクローナル抗体Xとモノクローナル抗体Zが同じである比較例2と比較して、磁性粒子プロセスを行い、且つ、モノクローナル抗体Xとモノクローナル抗体Yが互いに異なり、モノクローナル抗体Xとモノクローナル抗体Zが互いに異なる実施例1は、高い検出感度を示した。
なお、モノクローナル抗体(モノクローナル抗体X、モノクローナル抗体Y、モノクローナル抗体Z)として抗インフルエンザA型モノクローナル抗体の代わりに抗インフルエンザB型モノクローナル抗体を用いた点以外は上述した実施例1及び比較例1~2と同様にイムノクロマトグラフィーを実施したところ、表1と同様の傾向が見られた。
10 金コロイド保持パッド
20 テストライン
30 コントロールライン
40 発色試薬固定化ライン
100 ニトロセルロースメンブレン
20 テストライン
30 コントロールライン
40 発色試薬固定化ライン
100 ニトロセルロースメンブレン
Claims (7)
- 抗原を含み得る試料と、前記抗原と特異的に親和性を有するモノクローナル抗体Xで修飾された磁性粒子である修飾磁性粒子とを混合することで、前記抗原と前記修飾磁性粒子との複合体である磁性粒子複合体を含有する混合物を得る、混合工程と、
磁気を用いて、前記磁性粒子複合体を含有する混合物中の磁性粒子を捕集する、捕集工程と、
前記捕集工程で捕集された磁性粒子と、酸性又はアルカリ性の液である乖離液とを混合することで、前記磁性粒子複合体から前記修飾磁性粒子を乖離させ、抗原含有液を得る、乖離工程と、
中和液を用いて、前記抗原含有液を中和することで、中和抗原含有液を得る、中和工程と、
前記中和抗原含有液中の抗原と、前記抗原と結合し得るモノクローナル抗体Yで修飾された金粒子である修飾金粒子との複合体である金粒子複合体を形成させた状態で、前記抗原と結合し得るモノクローナル抗体Zが固定化された反応部位を有する不溶性担体に展開する、展開工程と、
前記不溶性担体の反応部位において、前記金粒子複合体を捕捉する、捕捉工程と、
前記捕捉工程で捕捉された金粒子複合体を銀増幅する、銀増幅工程とを備え、
前記モノクローナル抗体Xと前記モノクローナル抗体Yが互いに異なり、
前記モノクローナル抗体Xと前記モノクローナル抗体Zが互いに異なる、イムノクロマトグラフィー。 - 前記モノクローナル抗体X、前記モノクローナル抗体Y及び前記モノクローナル抗体Zが全て異なる、請求項1に記載のイムノクロマトグラフィー。
- 前記乖離液が、前記抗原を含み得る試料よりも少ない量の、酸性又はアルカリ性の液である乖離液である、請求項1又は2に記載のイムノクロマトグラフィー。
- 前記抗原を含み得る試料に対する、前記乖離液の割合が、質量比で、1/5以下である、請求項3に記載のイムノクロマトグラフィー。
- 前記乖離液が、NaOH又はHClを含有する、請求項1~4のいずれか1項に記載のイムノクロマトグラフィー。
- 前記中和液が、HClと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、又は、NaOHと、トリシン、トリス、HEPES、アセトアミドグリシン、グリシンアミド及びビシンからなる群より選択される少なくとも1種とを含有する、請求項1~5のいずれか1項に記載のイムノクロマトグラフィー。
- 修飾される前の前記磁性粒子の粒子径が、0.05μm~10μmである、請求項1~6のいずれか1項に記載のイムノクロマトグラフィー。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20871388.3A EP4040154A4 (en) | 2019-09-30 | 2020-06-24 | IMMUNOCHROMATOGRAPHY |
| JP2021550332A JP7148738B2 (ja) | 2019-09-30 | 2020-06-24 | イムノクロマトグラフィー |
| CN202080062167.4A CN114341642A (zh) | 2019-09-30 | 2020-06-24 | 免疫层析法 |
| US17/690,177 US20220196647A1 (en) | 2019-09-30 | 2022-03-09 | Immunochromatography |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019178730 | 2019-09-30 | ||
| JP2019-178730 | 2019-09-30 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US17/690,177 Continuation US20220196647A1 (en) | 2019-09-30 | 2022-03-09 | Immunochromatography |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021065105A1 true WO2021065105A1 (ja) | 2021-04-08 |
Family
ID=75336954
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/024691 WO2021065105A1 (ja) | 2019-09-30 | 2020-06-24 | イムノクロマトグラフィー |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220196647A1 (ja) |
| EP (1) | EP4040154A4 (ja) |
| JP (1) | JP7148738B2 (ja) |
| CN (1) | CN114341642A (ja) |
| WO (1) | WO2021065105A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021164160A (ja) * | 2020-03-30 | 2021-10-11 | パナソニックIpマネジメント株式会社 | ハンズフリー装置、ハンズフリーシステムおよびデータ転送方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5728453B2 (ja) | 1976-12-09 | 1982-06-16 | ||
| US6020117A (en) | 1998-09-30 | 2000-02-01 | Eastman Kodak Company | Thermally processable imaging element |
| JP2007085929A (ja) * | 2005-09-22 | 2007-04-05 | Jsr Corp | 特異捕捉用磁性粒子およびその製造方法 |
| JP2009150869A (ja) | 2007-11-29 | 2009-07-09 | Fujifilm Corp | イムノクロマトグラフ方法 |
| WO2010092958A1 (ja) * | 2009-02-10 | 2010-08-19 | 株式会社日立ハイテクノロジーズ | 質量分析技術を用いた免疫分析方法および免疫分析システム |
| WO2012173002A1 (ja) * | 2011-06-15 | 2012-12-20 | 三洋化成工業株式会社 | 磁性シリカ粒子を用いた測定方法及び該測定方法用試薬 |
| JP5728453B2 (ja) * | 2012-09-27 | 2015-06-03 | 富士フイルム株式会社 | クロマトグラフ方法及びクロマトグラフキット |
| JP2016090570A (ja) * | 2014-11-04 | 2016-05-23 | 三洋化成工業株式会社 | 磁性シリカ粒子を用いた対象物質の分離方法 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5683543B2 (ja) * | 2011-09-29 | 2015-03-11 | 富士フイルム株式会社 | クロマトグラフキット及びクロマトグラフ方法 |
-
2020
- 2020-06-24 JP JP2021550332A patent/JP7148738B2/ja active Active
- 2020-06-24 CN CN202080062167.4A patent/CN114341642A/zh active Pending
- 2020-06-24 WO PCT/JP2020/024691 patent/WO2021065105A1/ja active Application Filing
- 2020-06-24 EP EP20871388.3A patent/EP4040154A4/en active Pending
-
2022
- 2022-03-09 US US17/690,177 patent/US20220196647A1/en active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5728453B2 (ja) | 1976-12-09 | 1982-06-16 | ||
| US6020117A (en) | 1998-09-30 | 2000-02-01 | Eastman Kodak Company | Thermally processable imaging element |
| JP2007085929A (ja) * | 2005-09-22 | 2007-04-05 | Jsr Corp | 特異捕捉用磁性粒子およびその製造方法 |
| JP2009150869A (ja) | 2007-11-29 | 2009-07-09 | Fujifilm Corp | イムノクロマトグラフ方法 |
| WO2010092958A1 (ja) * | 2009-02-10 | 2010-08-19 | 株式会社日立ハイテクノロジーズ | 質量分析技術を用いた免疫分析方法および免疫分析システム |
| WO2012173002A1 (ja) * | 2011-06-15 | 2012-12-20 | 三洋化成工業株式会社 | 磁性シリカ粒子を用いた測定方法及び該測定方法用試薬 |
| JP5728453B2 (ja) * | 2012-09-27 | 2015-06-03 | 富士フイルム株式会社 | クロマトグラフ方法及びクロマトグラフキット |
| JP2016090570A (ja) * | 2014-11-04 | 2016-05-23 | 三洋化成工業株式会社 | 磁性シリカ粒子を用いた対象物質の分離方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4040154A1 (en) | 2022-08-10 |
| EP4040154A4 (en) | 2022-12-07 |
| US20220196647A1 (en) | 2022-06-23 |
| JPWO2021065105A1 (ja) | 2021-04-08 |
| JP7148738B2 (ja) | 2022-10-05 |
| CN114341642A (zh) | 2022-04-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5132664B2 (ja) | イムノクロマトグラフ方法 | |
| WO2021065300A1 (ja) | 免疫検査方法及び濃縮用治具 | |
| JP7141458B2 (ja) | クロマトグラフキットおよびクロマトグラフ方法 | |
| US20120252004A1 (en) | Highly sensitive immunochromatography method | |
| US20230341398A1 (en) | SARS-CoV-2 DETECTION KIT AND SARS-CoV-2 DETECTION METHOD | |
| KR20120139543A (ko) | 고감도의 면역크로마토그래프 방법 및 면역크로마토그래프용 키트 | |
| JP2005291783A (ja) | 免疫測定に供する検体浮遊液調製用媒体組成物及びそれを用いる免疫測定方法 | |
| WO2021065105A1 (ja) | イムノクロマトグラフィー | |
| US20210208138A1 (en) | Composite particle for immunochromatography, method for manufacturing the same, and immunochromatography | |
| JP5066498B2 (ja) | アッセイ方法 | |
| JP5782533B2 (ja) | クロマトグラフ方法及びクロマトグラフキット | |
| KR20110134445A (ko) | 검사 시약 및 그것을 사용한 피검 시료 중의 피측정물의 측정 방법 | |
| WO2021065144A1 (ja) | イムノクロマトグラフィー | |
| WO2021153127A1 (ja) | 免疫検査方法 | |
| WO2021152966A1 (ja) | イムノクロマトグラフィー | |
| JP7350100B2 (ja) | イムノクロマトグラフィー | |
| WO2020203228A1 (ja) | イムノクロマトグラフィー | |
| WO2024005055A1 (ja) | 検査方法、検査試薬、及び検査キット | |
| JP5265423B2 (ja) | クロマトグラフ方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20871388 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2021550332 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2020871388 Country of ref document: EP Effective date: 20220502 |