WO2013017559A1 - N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide - Google Patents
N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide Download PDFInfo
- Publication number
- WO2013017559A1 WO2013017559A1 PCT/EP2012/064863 EP2012064863W WO2013017559A1 WO 2013017559 A1 WO2013017559 A1 WO 2013017559A1 EP 2012064863 W EP2012064863 W EP 2012064863W WO 2013017559 A1 WO2013017559 A1 WO 2013017559A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- alkyl
- heterocyclyl
- cycloalkyl
- heteroaryl
- cor
- Prior art date
Links
- 0 *[n]1nbnc1N Chemical compound *[n]1nbnc1N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/80—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,2
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
- A01N43/647—Triazoles; Hydrogenated triazoles
- A01N43/653—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/713—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with four or more nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
- C07D249/10—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D249/14—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
- C07D257/06—Five-membered rings with nitrogen atoms directly attached to the ring carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- the invention relates to the technical field of herbicides, in particular that of herbicides for the selective control of weeds and weeds in
- N- (tetrazol-5-yl) - and N- (triazol-5-yl) benzamides and their pharmacological activity are known. From the earlier priority, not pre-published EP101748937 certain N- (tetrazol-5-yl) - and N- (triazol-5-yl) benzamides and nicotinamides are known as herbicides. It has now been found that (tetrazole-5-yl) - and N- (triazol-5-yl) arylcarbonklareamide and
- nicotinamides which carry special substituents in the 1-position of the tetrazole or triazole ring, are particularly suitable as herbicides.
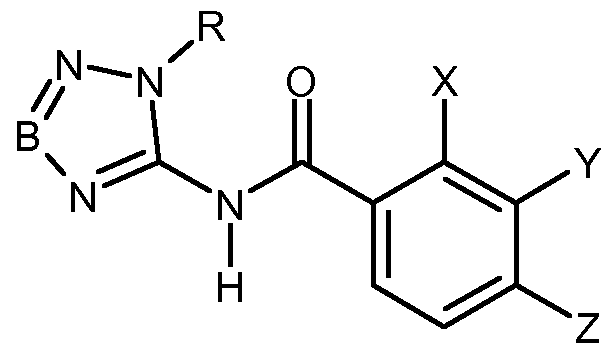
- An object of the present invention are thus N- (tetrazol-5-yl) - and N- (triazol-5-yl) arylcarbonklareamide of formula (I) or salts thereof
- A is N or CY
- B is N or CH
- X is nitro, halogen, cyano, formyl, thiocyanato, (Ci-C6) alkyl, halo (Ci- C6) alkyl, (C2-C6) alkenyl, halo (C2-C6) alkenyl , (C2-C6) alkynyl, halo (C 3 -C 6) - alkynyl, (C3-C6) cycloalkyl, halo (C3-C6) cycloalkyl, (C3-C6) cycloalkyl (C 1 -C 6 ) -alkyl, halogeno (C 3 -C 6 ) -cycloalkyl- (C 1 -C 6 ) -alkyl, COR 1 , COOR 1 , OCOOR 1 , NR 1 COOR 1 , C (O) N (R 1 ) 2 , NR 1 C (O) N
- Z represents halogen, cyano, rhodano, halo (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl, halogeno (C 2 -C 6 ) -alkenyl, (C 2 -C 6 ) -alkynyl, halogeno (C 2 -C 6 ) -alkynyl, -C 6) -alkynyl, (C3-C6) cycloalkyl, halo (C3-C6) cycloalkyl, (C3-C6) cycloalkyl (Ci-C 6) alkyl, halo (C 3 - C 6 ) - cycloalkyl- (C 1 -C 6 ) -alkyl, COR 1 , COOR 1 , OCOOR 1 , NR 1 COOR 1 , C (O) N (R 1 ) 2 , NR 1 C (O)
- R is CH 2 R 6 ,
- Cycloalkyl, heteroaryl, heterocyclyl, phenyl, Q-heteroaryl, Q-heterocyclyl, Q-phenyl and Q-benzyl are each substituted by s substituents selected from the group consisting of methyl, ethyl, methoxy, cyano, nitro, trifluoromethyl and halo, and wherein Heterocyclyl and cycloalkyl carry n oxo groups,
- Q is O, S or NR 3 ,
- R 1 represents hydrogen, (Ci-C 6) -alkyl, (Ci-C 6) -haloalkyl, (C 2 -C 6) alkenyl, (C 2 - C 6) haloalkenyl, (C 2 -C 6) -alkynyl, (C 2 -C 6) -haloalkynyl, (C3-C6) -cycloalkyl, (C 3 - C 6) cycloalkenyl, (C3-C 6) halocycloalkyl, (Ci-C6) alkyl-O - (Ci-C 6) alkyl, (C 3 -C 6) - cycloalkyl, (Ci-C 6) alkyl, phenyl, phenyl (Ci-C 6) alkyl, heteroaryl, (Ci-Ce) - alkyl heteroaryl, Heterocycl, (Ci-C 6) alkyl-heterocycl
- R 3 is hydrogen, (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl, (C 2 -C 6 ) -alkynyl, (C 3 -C 6 ) -cycloalkyl or (C 3 -C 6 ) - Cycloalkyl- (C 1 -C 6 ) -alkyl,
- R 4 is (Ci-C 6) -alkyl, (C 2 -C 6) -alkenyl or (C 2 -C 6) -alkynyl, (C3-C6) -cycloalkyl or (C3-C6) -cycloalkyl- ( C 1 -C 6 ) -alkyl,
- R 5 is (C 1 -C 4 ) -alkyl
- R 6 is OCOOR 4 , NR 4 COOR 4 , S (O) n - (C 1 -C 6 ) -alkyl, S (O) n - (C 1 -C 6 ) -haloalkyl, nitro, cyano, SiR 5 3, PO (OR 5 ) 2 , heterocyclyl or cycloalkyl, where the last two radicals m bear oxo or hydroxy groups, m is 1 or 2,
- n 0, 1 or 2
- s 0, 1, 2 or 3
- t 1, 2, 3 or 4
- alkyl radicals having more than two carbon atoms may be straight-chain or branched.
- Alkyl radicals are, for example, methyl, ethyl, n- or i-propyl, n-, i-, t- or 2-butyl, pentyls, hexyls, such as n-hexyl, i-hexyl and 1,3-dimethylbutyl.
- alkenyl is, for example, allyl, 1-methylprop-2-en-1-yl,
- Alkynyl means e.g. Propargyl, but-2-yn-1-yl, but-3-yn-1-yl, 1-methyl-but-3-yn-1-yl.
- the multiple bond can each be in any position of the unsaturated radical.
- Cycloalkyl means a carbocyclic saturated ring system having three to six C atoms, e.g. Cyclopropyl, cyclobutyl, cyclopentyl or cyclohexyl.
- cycloalkenyl is a monocyclic alkenyl group having three to six carbon ring members, e.g. Cyclopropenyl, cyclobutenyl,
- Cyclopentenyl and cyclohexenyl, wherein the double bond may be in any position.
- Halogen is fluorine, chlorine, bromine or iodine.
- Heterocyclyl means a saturated, partially saturated or fully unsaturated cyclic radical containing from 3 to 6 ring atoms, of which from 1 to 4 are from the group oxygen, nitrogen and sulfur, and additionally by a
- heterocyclyl is piperidinyl, pyrrolidinyl, tetrahydrofuranyl, dihydrofuranyl and oxetanyl.
- Heteroaryl means an aromatic cyclic radical containing from 3 to 6 ring atoms, of which from 1 to 4 are from the group consisting of oxygen, nitrogen and sulfur, and may additionally be fused by a benzo ring.
- heteroaryl stands for
- Benzimidazol-2-yl furanyl, imidazolyl, isoxazolyl, isothiazolyl, oxazolyl, pyrazinyl, pyrimidinyl, pyridazinyl, pyridinyl, benzisoxazolyl, thiazolyl, pyrrolyl, pyrazolyl, thiophenyl, 1, 2,3-oxadiazolyl, 1, 2,4-oxadiazolyl, 1, 2,5-oxadiazolyl, 1, 3,4-oxadiazolyl, 1, 2,4-triazolyl, 1, 2,3-triazolyl, 1, 2,5-triazolyl, 1, 3,4-triazolyl, 1, 2,4-triazolyl, 1, 2,4-thiadiazolyl, 1, 3,4-thiadiazolyl, 1, 2,3-thiadiazolyl, 1, 2,5-thiadiazolyl, 2H-1,2,3,4-tetrazolyl, 1 H-1, 2,
- the compounds of the general formula (I) can exist as stereoisomers. For example, if one or more asymmetric carbon atoms are present, then enantiomers and
- stereoisomers can be prepared by using stereoselective reactions using optically active starting materials and / or
- the invention also relates to all stereoisomers and mixtures thereof, which are of the general formula (I) but are not specifically defined.
- A is N or CY
- B is N or CH
- X is nitro, halogen, cyano, rhodano, (C 1 -C 6 ) -alkyl, halogeno (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl, halogeno (C 2 -C 6 ) -alkenyl, (C 2 -C 4 ) -alkenyl -C 6) alkynyl, halo (C3-C6) -alkynyl, (C 3 - C 6) cycloalkyl, halo (C3-C6) cycloalkyl, Ci-C6) alkyl-O- (C -C 6) alkyl, (C 3 -C 6) - cycloalkyl, (Ci-C 6) alkyl, halo (C3-C6) cycloalkyl- (Ci-C 6) alkyl, COR 1, OR 1 , OCOR 1 ,
- Y is hydrogen, nitro, halogen, cyano, rhodano, (C 1 -C 6 ) -alkyl, halogeno (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl, or halogen- (C 2 -C 6 ) -alkenyl , (C 2 -C 6 ) -alkynyl, halogeno (C 3 -C 6 ) -alkynyl, (C 3 -C 6 ) -cycloalkyl, (C 3 -C 6 ) -cycloalkenyl, halogeno (C 3 -C 6 ) -cycloalkyl, (C 3 -C 6 ) -cycloalkyl, C 6 ) -cycloalkyl, C 6 ) -cycloalkyl- (C 1 -C 6 ) -alkyl, halogeno (C 3 -
- Heterocyclyl where the six last-mentioned radicals each substituted by s radicals selected from the group halogen, nitro, cyano, (Ci-C 6) alkyl, halo (Ci-C 6) alkyl, (C 3 -C 6) - cycloalkyl, S (O) n - (Ci-C 6) -alkyl, (Ci-Ce) alkoxy, halo (Ci-C 6) alkoxy, (Ci-C6) - alkoxy- (Ci-C4) - substituted alkyl and cyanomethyl, and wherein heterocyclyl n carries oxo groups,
- Z represents halogen, cyano, thiocyanato, halo (Ci-C6) alkyl, (C 2 -C 6) alkenyl, halo (C 2 -C 6) alkenyl, (C 2 -C 6) alkynyl, halogen - (C 3 -C 6 ) -alkynyl, (C 3 -C 6 ) -cycloalkyl, halogeno (C 3 -C 6 ) -cycloalkyl, (C 3 -C 6 ) -cycloalkyl- (C 1 -C 6 ) -alkyl, halogeno- (C 3 -C 6 ) -alkyl C 3 -C 6) - cycloalkyl- (Ci-C 6) alkyl, COR 1, COOR 1, C (O) N (R 1) 2, C (O) NR 1 OR 1, OSO 2 R 2, S (O) n R 2 , SO 2 OR 1
- Z can also be hydrogen, (C 1 -C 6) -alkyl or (C 1 -C 6) -alkoxy, if Y is the radical S (O) n R 2 ,
- R is CH 2 R 6 ,
- Cycloalkyl, heteroaryl, heterocyclyl, phenyl, Q-heteroaryl, Q-heterocyclyl, Q-phenyl and Q-benzyl are each substituted by s substituents selected from the group consisting of methyl, ethyl, methoxy, cyano, nitro, trifluoromethyl and halo, and wherein Heterocyclyl and cycloalkyl carry n oxo groups, Q is O, S or NR 3 ,
- R 1 represents hydrogen, (Ci-C 6) -alkyl, (C2-C6) alkenyl, (C2-C6) -alkynyl, (C 3 -C 6) - cycloalkyl, (C3-C6) cycloalkyl (C 1 -C 6 ) -alkyl, (C 1 -C 6 ) -alkyl-O- (C 1 -C 6 ) -alkyl, phenyl, phenyl (C 1 -C 6 ) -alkyl, heteroaryl, (C 1 -C 6 ) - Alkyl-heteroaryl, heterocyclyl, (C 1 -C 6 ) -alkyl-heterocyclyl, (C 1 -C 6 ) -alkyl-O-heteroaryl, (C 1 -C 6 ) -alkyl-O-heterocyclyl, (C 1 -C 4) -alkyl-
- R 2 is (Ci-C6) -alkyl, (C 2 -C 6) -alkenyl, (C 2 -C 6) -alkyl kinyl, (C 3 -C 6) -Cycloal alkyl, (C 3 - C 6 ) -cycloalkyl- (C 1 -C 6 ) -alkyl, (C 1 -C 6 ) -alkyl-O- (C 1 -C 6 ) -alkyl, phenyl, phenyl (C 1 -C 6 ) -alkyl, heteroaryl, (C 1 -C 4) -alkyl C 6 ) -alkyl heteroaryl, heterocyclyl, (C 1 -C 6 ) -alkyl heterocyclyl, (C 1 -C 6 ) -alkyl heterocyclyl, (C 1 -C 6 ) -alkyl heterocyclyl, (C 1 -C 6
- R 3 is hydrogen, (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkynyl, (C 2 -C 6 ) -alkynyl, (C 3 -C 6 ) -cycloalkyl or (C 3 -C 6 ) Cycloalkyl- (C 1 -C 6 ) -alkyl,
- R 4 is (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkynyl or (C 2 -C 6 ) -alkynyl, R 5 is methyl or ethyl, R 6 is OCOOR 4 , NR 4 COOR 4 , S (O) n - (C 1 -C 6 ) -alkyl, S (O) n - (C 1 -C 6 ) -haloalkyl, nitro, cyano, SiR 5 3, PO (OR 5 ) 2 or heterocyclyl, the m is oxo, m is 1 or 2,
- n 0, 1 or 2
- s 0, 1, 2 or 3
- u is 1, 2, 3, 4 or 5.
- A is N or CY
- B is N or CH
- X is nitro, halo, cyano, (Ci-C 6) alkyl, halo (Ci-C 6) alkyl, (C 3 -C 6) - cycloalkyl, OR 1, S (O ) n R 2 , (C 1 -C 6 ) -alkyl-S (O) n R 2 , (C 1 -C 6 ) -alkyl-OR 1 , (C 1 -C 6 ) -alkyl-CON (R 1 ) 2 , (C 1 -C 6 ) -alkyl-SO 2 N (R 1 ) 2 , (C 1 -C 6 ) -alkyl-NR 1 COR 1 , (C 1 -C 6 ) -alkyl-NR 1 SO 2 R 2 , (Ci -C 6) -alkyl heteroaryl, (C 1 -C 6) -alkyl heterocyclyl, where the latter two
- Heterocyclyl carries n oxo groups
- Y is hydrogen, nitro, halogen, cyano, (Ci-C 6) -alkyl, (Ci-C 6) -haloalkyl, OR 1, S (O) n R 2, SO 2 N (R 1) 2, N (R 1) 2, NR 1 SO 2 R 2, NR 1 COR 1, (Ci-C 6) alkyl-S (O) n R 2, (Ci-C 6) - alkyl-OR 1, (Ci-C 6 ) -Alkyl-CON (R 1 ) 2 , (C 1 -C 6 ) -alkyl-SO 2 N (R 1 ) 2 , (C 1 -C 6 ) -alkyl-NR 1 COR 1 , (C 1 -C 6 ) - Alkyl-NR 1 SO 2 R 2 , (C 1 -C 6 ) -alkyl-phenyl, (C 1 -C 6 ) -alkyl-heteroaryl, (C 1 -C
- Z represents halogen, cyano, halo (Ci-C 6) alkyl, (C3-C6) -cycloalkyl, S (O) n R 2, 1, 2,4-triazol-1-yl, or Z may also be Is hydrogen, methyl, methoxy or ethoxy, if Y is the radical S (O) n R 2 ,
- R is CH 2 R 6 ,
- heterocyclyl m carries oxo groups, in each case by u radicals from the group consisting of nitro, cyano, hydroxyl, oxo, SiR 5 3 , PO (OR 5 ) 2 , S (O) n - (C 1 -C 6 ) -alkyl, (C 1 -C 6 ) - alkoxy, halo (Ci-C 6) -alkoxy, N (R 3) 2, COR 3, OCOR 3, NR 3 COR 3, NR 3 SO 2 R 4, (C 3 -C 6) -cycloalkyl, heteroaryl, Heterocyclyl, phenyl, Q-heteroaryl, Q-heterocyclyl, Q-phenyl and Q-benzyl substituted (C 2 -C 6 ) -alkyl, (C 3 -C 7 ) -cycloalkyl, halo (C 2 -C 6 )
- Q is O, S or NR 3 ,
- R 1 represents hydrogen, (Ci-C 6) -alkyl, (C2-C6) alkenyl, (C2-C6) -alkynyl, (C 3 -C 6) - cycloalkyl, (C3-C6) cycloalkyl (C 1 -C 6 ) -alkyl, (C 1 -C 6 ) -alkyl-O- (C 1 -C 6 ) -alkyl, phenyl,
- R 2 is (C 1 -C 6 ) -alkyl, (C 3 -C 6 ) -cycloalkyl or (C 3 -C 6 ) -cycloalkyl- (C 1 -C 6 ) -alkyl, where these three radicals mentioned above are each represented by s radicals from the group consisting of Group consisting of halogen and OR 3 are substituted,
- R 3 is hydrogen or (C 1 -C 6 ) -alkyl, is (C 1 -C 6 ) -alkyl,
- R 5 is methyl or ethyl
- R 6 is OCOOR 4 , NR 4 COOR 4 , S (O) n- (C 1 -C 6 ) -alkyl, S (O) n- (C 1 -C 6 ) -haloalkyl, nitro, cyano, SiR 5 3 , PO (OR 5 ) 2 , m is 1 or 2,
- n 0, 1 or 2
- s 0, 1, 2 or 3
- u is 1, 2, 3, 4 or 5.
- benzoic acid chlorides of the formula (II) or the benzoic acids on which they are based are known in principle and can be synthesized, for example, according to the processes described in US Pat. No. 6,376,429 B1, EP 1 585 742 A1 and EP 1 202 978 A1
- dehydrating reagents commonly used for amidation reactions such as B. 1, ⁇ -carbonyldiimidazole (CDI), dicyclohexylcarbodiimide (DCC), 2,4,6-tripropyl-1, 3,5,2,4,6-trioxatriphosphinane 2,4,6-trioxide (T3P) etc . are used.
- CDI ⁇ -carbonyldiimidazole
- DCC dicyclohexylcarbodiimide
- T3P 3,5,2,4,6-trioxatriphosphinane 2,4,6-trioxide
- alkylating agents such as alkyl halides, sulfonates or dialkyl sulfates can be used in the presence of a base. It may be convenient to change reaction steps in order. Thus, benzoic acids carrying a sulfoxide are not readily converted into their acid chlorides. Here it is advisable to first produce the amide on the thioether stage and then to oxidize the thioether to the sulfoxide.
- the 5-amino-1H-tetrazoles of the formula (III) can be prepared analogously to those known from the literature
- 5-amino-1-R-tetrazoles may be added after in Amino-tetrazole method described in Journal of the American Chemical Society (1954), 76, 923-924:
- R is, for example, an alkyl radical.
- 5-amino-1-R-tetrazoles can be synthesized as described in Journal of the American Chemical Society (1954) 76, 88-89:
- the 5-amino-1H-triazoles of the formula (III) can be prepared analogously to those known from the literature
- Aminotriazole be prepared:
- 5-Amino-1-R-triazoles can also be synthesized, for example, as described in Chemische Berichte (1964), 97 (2), 396-404:
- 5-amino-1-R-triazoles can also be used, for example, as in Angewandte Chemie
- the listed equipment leads to a modular procedure, in which the individual work steps are automated, but between the work steps, manual operations must be performed.
- This can be circumvented by the use of partially or fully integrated automation systems in which the respective automation modules are operated, for example, by robots.
- Such automation systems can be obtained, for example, from Caliper, Hopkinton, MA 01748, USA.
- the implementation of single or multiple synthetic steps can be supported by the use of polymer-supported reagents / Scavanger resins.
- Synthesis methods allow a number of protocols known from the literature, which in turn can be carried out manually or automatically.
- the reactions can be carried out, for example, by means of IRORI technology in microreactors (microreactors) from Nexus Biosystems, 12140 Community Road, Poway, CA92064, USA.
- the preparation according to the methods described herein provides compounds of formula (I) and their salts in the form of substance collections called libraries.
- the present invention also provides libraries containing at least two compounds of formula (I) and their salts.
- the compounds of the formula (I) (and / or salts thereof) according to the invention have a excellent herbicidal activity against a broad spectrum of important mono- and dicotyledonous weed plants. Also difficult to control perennial harmful plants that expel from rhizomes, rhizomes or other permanent organs are well detected by the active ingredients.
- the present invention therefore also provides a method for controlling unwanted plants or for regulating the growth of plants, preferably in plant crops, wherein one or more of the present invention
- Compound (s) on the plants e.g., weeds such as mono- or dicotyledons
- the compounds of the invention may be e.g. in pre-sowing (possibly also by incorporation into the soil), pre-emergence or Nachauflaufmaschine be applied.
- some representatives of the monocotyledonous and dicotyledonous weed flora can be mentioned, which can be controlled by the compounds according to the invention, without the intention of limiting them to certain species.
- the compounds according to the invention are applied to the surface of the earth prior to germination, either the emergence of the weed seedlings is completely prevented or the weeds grow up to the cotyledon stage, but then stop their growth and finally die after three to four weeks
- Ipomoea Lactuca, Linum, Lycopersicon, Nicotiana, Phaseolus, Pisum, Solanum, Vicia, or monocotyledonous cultures of the genera Allium, Pineapple, Asparagus, Avena,
- Crops such as agricultural crops or ornamental plantings.
- the active compounds can also be used to control harmful plants in crops of genetically engineered or conventional mutagenized plants.
- the transgenic plants are usually characterized by particular advantageous properties, for example by resistance to certain pesticides, especially certain herbicides, resistance to plant diseases or pathogens of plant diseases such as certain insects or microorganisms such as fungi, bacteria or viruses.
- Other special special traits for example by resistance to certain pesticides, especially certain herbicides, resistance to plant diseases or pathogens of plant diseases such as certain insects or microorganisms such as fungi, bacteria or viruses.
- transgenic crops Preferred with respect to transgenic crops is the use of the compounds of the invention in economically important transgenic crops of useful and ornamental plants, eg. As cereals such as wheat, barley, rye, oats, millet, rice and corn or even crops of sugar beet, cotton, soy, rape, potato, tomato, pea and other vegetables.
- the compounds according to the invention can be used as herbicides in crops which are resistant to the phytotoxic effects of the herbicides or
- the application of the compounds of the invention or their salts in economically important transgenic crops of useful and ornamental plants eg.
- cereals such as wheat, barley, rye, oats, millet, rice, cassava and corn or cultures of sugar beet, cotton, soy, rape, potato, tomato, pea and other vegetables.
- the compounds according to the invention can preferably be employed as herbicides in crops which are resistant to the phytotoxic effects of the herbicides or have been made genetically resistant. Conventional ways of producing new plants that have modified properties compared to previously occurring plants exist
- Glufosinate see, for example, EP-A-0242236, EP-A-242246) or glyphosate
- transgenic crops for example cotton, with the ability
- Bacillus thuringiensis toxins Bacillus thuringiensis toxins (Bt toxins) to produce, which the
- transgenic crops characterized by a combination z. B. the o. G.
- nucleic acid molecules can be used in any genetic manipulations.
- nucleic acid molecules can be used in any genetic manipulations.
- Plasmids are introduced which allow mutagenesis or a sequence change by recombination of DNA sequences. With the help of standard methods z. For example, base substitutions are made, partial sequences are removed, or natural or synthetic sequences are added. For the connection of the DNA fragments with one another adapters or linkers can be attached to the fragments.
- the production of plant cells having a reduced activity of a gene product can be achieved, for example, by the expression of at least one
- DNA molecules may be used which comprise the entire coding sequence of a gene product, including any flanking sequences that may be present, as well as DNA molecules which comprise only parts of the coding sequence, which parts must be long enough to be present in the cells to cause an antisense effect. It is also possible to use DNA sequences which have a high degree of homology to the coding sequences of a gene product, but are not completely identical.
- the synthesized protein may be located in any compartment of the plant cell. But to achieve the localization in a particular compartment, z.
- the coding region can be linked to DNA sequences that ensure localization in a particular compartment. Such sequences are known in the art (see, for example, Braun et al., EMBO J. 1 1 (1992), 3219-3227, Wolter et al., Proc. Natl. Acad., U.S.A. 85 (1988), 846-850, Sonnewald et al., Plant J. 1 (1991), 95-106). Expression of the nucleic acid molecules can also be found in the
- Organelles of the plant cells take place.
- the transgenic plant cells can be regenerated to whole plants by known techniques.
- the transgenic plants may, in principle, be plants of any plant species, that is, both monocotyledonous and dicotyledonous plants.
- transgenic plants are available, the altered properties by
- the compounds of the invention can be used in transgenic cultures which are resistant to growth factors, such as. B. Dicamba or against
- Herbicides containing essential plant enzymes e.g. As acetolactate synthases (ALS), EPSP synthases, glutamine synthases (GS) or Hydroxyphenylpyruvat dioxygenases (HPPD) inhibit or herbicides from the group of sulfonylureas, the glyphosate, glufosinate or benzoylisoxazole and analogues, resistant.
- ALS acetolactate synthases
- EPSP synthases glutamine synthases
- HPPD Hydroxyphenylpyruvat dioxygenases
- Harmful plants often have effects that are specific for application in the particular transgenic culture, such as altered or specially extended weed spectrum that can be controlled
- Expense amounts that can be used for the application, preferably good compatibility with the herbicides to which the transgenic culture is resistant, and influencing the growth and yield of transgenic crops.
- the invention therefore also relates to the use of the compounds according to the invention as herbicides for controlling harmful plants in transgenic crop plants.
- the compounds according to the invention can be used in the form of wettable powders, emulsifiable concentrates, sprayable solutions, dusts or granules in the customary formulations.
- the invention therefore also relates to herbicidal and plant growth-regulating agents which contain the compounds according to the invention.
- the compounds according to the invention can be formulated in various ways, depending on which biological and / or chemical-physical parameters are predetermined. Possible formulation options are, for example: wettable powder (WP), water-soluble powders (SP), water-soluble concentrates,
- EC emulsifiable concentrates
- EW emulsions
- Water-in-oil emulsions sprayable solutions, suspension concentrates (SC), oil- or water-based dispersions, oil-miscible solutions, capsule suspensions (CS), dusts (DP), mordants, granules for litter and soil application, granules (GR) in the form of micro, spray, elevator and adsorption granules, water-dispersible granules (WG), water-soluble granules (SG),
- the necessary formulation auxiliaries such as inert materials, surfactants, solvents and other additives are also known and are, for example
- Injectable powders are preparations which are uniformly dispersible in water and contain surfactants of the ionic and / or nonionic type (wetting agent, dispersing agent) in addition to the active ingredient, apart from a diluent or inert substance.
- surfactants of the ionic and / or nonionic type wetting agent, dispersing agent
- Formulation aids mixed.
- Emulsifiable concentrates are made by dissolving the active ingredient in one
- organic solvents e.g. Butanol, cyclohexanone, dimethylformamide, xylene or higher-boiling aromatics or hydrocarbons or mixtures of organic solvents with the addition of one or more surfactants of ionic and / or nonionic type (emulsifiers).
- emulsifiers which may be used are: alkylarylsulfonic acid calcium salts, such as
- Ca-dodecylbenzenesulfonate or nonionic emulsifiers such as
- Fatty acid polyglycol esters alkylaryl polyglycol ethers, fatty alcohol polyglycol ethers,
- Propylene oxide-ethylene oxide condensation products alkyl polyethers, sorbitan esters, e.g. Sorbitan fatty acid esters or polyoxethylenesorbitan esters such as e.g.
- Dusts are obtained by grinding the active substance with finely divided solid substances, for example talc, natural clays, such as kaolin, bentonite and pyrophyllite, or diatomaceous earth.
- Suspension concentrates may be water or oil based. You can, for example, by wet grinding using commercially available bead mills and optionally added surfactants, such as the above with the other
- Emulsions e.g. Oil-in-water emulsions (EW) can be prepared, for example, by means of stirrers, colloid mills and / or static mixers using aqueous organic solvents and optionally surfactants, as described e.g. listed above for the other formulation types.
- Granules can be prepared either by spraying the active ingredient on adsorptive, granulated inert material or by applying
- Active substance concentrates by means of adhesives, e.g. Polyvinyl alcohol, polyacrylic acid sodium or mineral oils, on the surface of carriers such as sand, kaolinites or granulated inert material. It is also possible to granulate suitable active ingredients in the manner customary for the production of fertilizer granules, if desired in admixture with fertilizers.
- adhesives e.g. Polyvinyl alcohol, polyacrylic acid sodium or mineral oils
- carriers such as sand, kaolinites or granulated inert material. It is also possible to granulate suitable active ingredients in the manner customary for the production of fertilizer granules, if desired in admixture with fertilizers.
- Water-dispersible granules are generally prepared by the usual methods such as spray drying, fluidized bed granulation, plate granulation, mixing with high-speed mixers and extrusion without solid inert material.
- the agrochemical preparations generally contain from 0.1 to 99% by weight, in particular from 0.1 to 95% by weight, of compounds according to the invention.
- the drug concentration is e.g. about 10 to 90 wt .-%, the balance to 100 wt .-% consists of conventional formulation ingredients. at
- the active substance concentration can be about 1 to 90,
- Dust-like formulations contain 1 to 30 wt .-% of active ingredient, preferably usually 5 to 20 wt .-% of active ingredient, sprayable solutions contain about 0.05 to 80, preferably 2 to 50 wt .-% of active ingredient.
- the active ingredient content depends, in part, on whether the active compound is liquid or solid and which
- Granulation aids, fillers, etc. are used. In the water
- the content of active ingredient is for example between 1 and 95 wt .-%, preferably between 10 and 80 wt .-%.
- the active substance formulations mentioned optionally contain the customary adhesive, wetting, dispersing, emulsifying, penetrating, preserving,
- Mixture formulations or in the tank mix are, for example, known active substances which are based on an inhibition of, for example, acetolactate synthase, acetyl-CoA carboxylase, cellulose synthase, enolpyruvylshikimate-3-phosphate synthase,
- Glutamine synthetase, p-hydroxyphenylpyruvate dioxygenase, phytoene desaturase, photosystem I, photosystem II, protoporphyrinogen oxidase can be used, as described, for example, in Weed Research 26 (1986) 441-445 or "The Pesticide Manual", 15th edition, The British Crop Protection Council and the Royal Soc. of Chemistry, 2009 and There cited literature are described. As known herbicides or
- Plant growth regulators which can be combined with the compounds of the invention are e.g. the following active ingredients (the compounds are denoted either by the "common name” according to the International Organization for Standardization (ISO) or the chemical name or with the code number) and always include all forms of use such as acids, salts, esters and isomers such as stereoisomers and optical isomers.
- active ingredients the compounds are denoted either by the "common name” according to the International Organization for Standardization (ISO) or the chemical name or with the code number
- ISO International Organization for Standardization
- isomers such as stereoisomers and optical isomers.
- One and in part also several application forms are mentioned by way of example: acetochlor, acibenzolar, acibenzolar-S-methyl, acifluorfen, acifluorfen-sodium,
- Flufenpyr Flufenpyr-ethyl, Flumetralin, Flumetsulam, Flumiclorac, Flumiclorac-pentyl, Flumioxazin, Flumipropyn, Fluometuron, Fluorodifen,
- Fluoroglycofen Fluoroglycofen, fluoroglycofen-ethyl, flupoxam, flupropacil, flupropanate,
- Flupyrsulfuron flupyrsulfuron-methyl-sodium, flurenol, flurenol-butyl, fluridone, flurochloridone, fluroxypyr, fluroxypyr-meptyl, flurprimidol, flurtamone, fluthiacet, fluthiacet-methyl, fluthiamide, fomesafen, foramsulfuron, förch lorfenuron,
- Haloxyfop Haloxyfop-P, Haloxyfopethoxyethyl, Haloxyfop-P-ethoxyethyl, Haloxyfop- methyl, Haloxyfop-P-methyl, Hexazinone, HW-02, d. H. 1- (dimethoxyphosphoryl) ethyl (2,4-dichlorophenoxy) acetate, imazamethabenz, imazamethabenz-n-ethyl,
- Imazamox imazamoxammonium, imazapic, imazapyr, imazapyrisopropylammonium, imazaquin, imazaquin-amnunnonium, imazethapyr, imazethapyrammonium, imazosulfuron, inabenfide, indanofan, indaziflam, indoleacetic acid (IAA), 4-indol-3-yl-butyric acid (IBA), iodosulfuron, iodosulfuron-methyl-sodium, loxynil, isoparbazone, isocarbamide, isopropalin, isoproturon, isourone, isoxaben,
- Metamifop metamitron, metazachlor, metazasulfuron, methazole, methiopyrsulfuron, methiozoline, methoxyphenones, methyldymron, 1-methylcyclopropene,
- Methylisothiocyanate metobenzuron, metobromuron, metolachlor, S-metolachlor, metosulam, metoxuron, metribuzin, metsulfuron, metsulfuron-methyl, molinates,
- Nonanoic acid pendimethalin, pendalkin, penoxsulam, pentanochlor, pentoxazone, perfluidone, pethoxamide, phenisopham, phenmedipham, phenmediphamethyl, picloram, picolinafen, pinoxaden, piperophos, pirifenop, pirifenoputyl, pretilachlor, primisulfuron, primisulfuron-methyl, probenazoles, Profluazole, Procyazine, Prodiamine, Prifluralin, Profoxydim, Prohexadione, Prohexadione-calcium, Prohydrojasmone, Prometon, Prometry, Propachlor, Propanil, Propaquizafop, Propazine, Propam, Propisochlor, Propoxycarbazone, Propoxycarbazone-nathum, Propyrisulfuron,
- Triafamon triallate, triasulfuron, triaziflam, triazofenamide, tribenuron, tribenuronmethyl, trichloroacetic acid (TCA), triclopyr, tridiphane, trietazine, trifloxysulfuron, trifloxysulfuron sodium, trifluralin, triflusulfuron, triflusulfuron-methyl, trimeturon, trinexapac, trinexapac-ethyl, tritosulfuron , Tsitodef, Uniconazole, Uniconazole-P, Vernolate, ZJ-0862, d. H. 3,4-Dichloro-N- ⁇ 2 - [(4,6-dimethoxypyrimidin-2-yl) oxy] benzyl ⁇ aniline, and the following compounds:
- the formulations present in commercial form are optionally diluted in a customary manner, e.g. for wettable powders, emulsifiable concentrates, dispersions and water-dispersible granules by means of water. Dusty preparations, ground or spreading granules and sprayable
- Compounds of the formula (I) can vary within wide limits, e.g. between 0.001 and 1.0 kg / ha or more of active substance, but is preferably between 0.005 and 750 g / ha.
- Table 3 Compounds according to the invention of the formula (I) in which A is N.
- a dust is obtained by mixing 10 parts by weight of a compound of formula (I) and / or salts thereof and 90 parts by weight of talc as an inert material and comminuting in a hammer mill.
- a readily dispersible, water-wettable powder is obtained by: 25 parts by weight of a compound of the formula (I) and / or salts thereof, 64
- a dispersion concentrate readily dispersible in water is obtained by reacting 20 parts by weight of a compound of the formula (I) and / or salts thereof with 6 parts by weight of alkylphenol polyglycol ether ( ⁇ Triton X 207), 3 parts by weight
- Mineral oil (boiling range, for example, about 255 to about 277 C) mixed and ground in a ball mill to a fineness of less than 5 microns.
- An emulsifiable concentrate is obtained from 15 parts by weight of a
- a water-dispersible granule is also obtained by
- the compounds according to the invention formulated in the form of wettable powders (WP) or as emulsion concentrates (EC) are then used as aqueous suspension or
- 1-16, 1-44, 1-60, 1-125, 1-154, 1-162, 1-163, 1-174, 1-187, 1-191, 1-197 show , 1-200, 1-204, 1-215, 1-245, 1-246, 1-248, 1-343, 1-345, 1-361, 1-366, 1-368, 1-417, 1 -450, 1-452, 1-453, 1-456, 1-458, 1-460, 1-463, 1-464, 1-465, 1-468, 1-475, 1-476, 1-488 , 1 -494, 1-517, 1-572, 1-583, 2-2, 2-4, 2-5, 2-6, 2-7, 2-19, 3-2 and 3-16 at one Application rate of 320 g / ha each having at least 90% action against Abutilon theophrasti, Amaranthus retroflexus, Matricara inodora, Stellaria media, Veronica persica and Viola tricolor.
- test plants Greenhouse under good growth conditions. 2 to 3 weeks after sowing, the test plants are treated in the single leaf stage.
- the compounds according to the invention formulated in the form of wettable powders (WP) or as emulsion concentrates (EC) are then used as aqueous suspension or
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
Claims
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES12745447.8T ES2542681T3 (es) | 2011-08-03 | 2012-07-30 | Amidas del ácido N-(tetrazol-5-il)- y N-(triazol-5-il)arilcarboxílico y su uso como herbicidas |
| EP20120745447 EP2739611B1 (de) | 2011-08-03 | 2012-07-30 | N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide |
| PL12745447T PL2739611T3 (pl) | 2011-08-03 | 2012-07-30 | Amidy kwasu N-(tetrazol-5-ilo)- i N-(terazol-5-ilo)arylokarboksylowego i ich zastosowanie jako herbicydy |
| JP2014523298A JP6078065B2 (ja) | 2011-08-03 | 2012-07-30 | N−(テトラゾール−5−イル)アリールカルボキサミド類及びn−(トリアゾール−5−イル)アリールカルボキサミド類並びに除草剤としてのそれらの使用 |
| CN201280038161.9A CN103717581B (zh) | 2011-08-03 | 2012-07-30 | N-(四唑-5-基)芳基甲酰胺和n-(三唑-5-基)芳基甲酰胺及其作为除草剂的用途 |
| US14/233,298 US8822378B2 (en) | 2011-08-03 | 2012-07-30 | N-(tetrazol-5-yl)- and N-(triazol-5-yl)arylcarboxamides and use thereof as herbicides |
| IN176DEN2014 IN2014DN00176A (de) | 2011-08-03 | 2012-07-30 | |
| BR112014002191A BR112014002191B1 (pt) | 2011-08-03 | 2012-07-30 | Amidas de ácido n-(tetrazol-5-il)- ou n-(triazol-5-il) arilcarboxílico, seu uso, composição herbicida, e processo para combate de plantas indesejadas |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11176378.5 | 2011-08-03 | ||
| EP11176378 | 2011-08-03 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2013017559A1 true WO2013017559A1 (de) | 2013-02-07 |
Family
ID=46640008
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2012/064863 WO2013017559A1 (de) | 2011-08-03 | 2012-07-30 | N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US8822378B2 (de) |
| EP (1) | EP2739611B1 (de) |
| JP (1) | JP6078065B2 (de) |
| CN (1) | CN103717581B (de) |
| AR (1) | AR087385A1 (de) |
| BR (1) | BR112014002191B1 (de) |
| ES (1) | ES2542681T3 (de) |
| IN (1) | IN2014DN00176A (de) |
| PL (1) | PL2739611T3 (de) |
| WO (1) | WO2013017559A1 (de) |
Cited By (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013092834A1 (en) * | 2011-12-21 | 2013-06-27 | Syngenta Limited | Herbicidal compounds |
| WO2013072528A3 (en) * | 2012-04-27 | 2013-07-04 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)pyridin-3-yl-carboxamide compounds and their use as herbicides |
| WO2013076316A3 (en) * | 2012-04-27 | 2013-09-26 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)hetarylcarboxamide compounds and their use as herbicides |
| EP2773208A1 (de) * | 2011-11-03 | 2014-09-10 | Bayer Intellectual Property GmbH | Herbizid-safener-zusammensetzungen enthaltend n-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide |
| WO2014184017A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)pyridin-3-yl-carboxamide compounds and their use as herbicides |
| WO2014184073A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)arylcarboxamide compounds and their use as herbicides |
| WO2014184074A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)hetarylcarboxamide compounds and their use as herbicides |
| WO2014192936A1 (ja) | 2013-05-31 | 2014-12-04 | 日産化学工業株式会社 | 複素環アミド化合物 |
| JP2015508766A (ja) * | 2012-02-21 | 2015-03-23 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツングBayer Intellectual Property GmbH | 除草3−(スルフィン−/スルホンイミドイル)−ベンズアミド |
| JP2016523831A (ja) * | 2013-05-15 | 2016-08-12 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | 置換型n−(テトラゾール−5−イル)−およびn−(トリアゾール−5−イル)アリールカルボキサミド化合物ならびに除草剤としてのそれらの使用 |
| WO2017042259A1 (en) | 2015-09-11 | 2017-03-16 | Bayer Cropscience Aktiengesellschaft | Hppd variants and methods of use |
| JP2017523235A (ja) * | 2014-06-30 | 2017-08-17 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 除草活性を有するアリールカルボン酸アミド類 |
| JP2017523236A (ja) * | 2014-06-30 | 2017-08-17 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 除草活性を有する安息香酸アミド類 |
| US9867376B2 (en) | 2012-05-24 | 2018-01-16 | Bayer Cropscience Ag | Herbicidal compositions comprising N-tetrazol-5-yl)- or N-(triazol-5-yl)arylcarboxamides |
| JP2018531236A (ja) * | 2015-09-28 | 2018-10-25 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | アシル化n−(1,2,5−オキサジアゾール−3−イル)−、n−(1,3,4−オキサジアゾール−2−イル)−、n−(テトラゾール−5−イル)−およびn−(トリアゾール−5−イル)−アリールカルボキサミド、および除草剤としてのそれらの使用 |
| WO2018219936A1 (en) | 2017-05-30 | 2018-12-06 | Basf Se | Benzamide compounds and their use as herbicides ii |
| WO2018219935A1 (en) | 2017-05-30 | 2018-12-06 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019016385A1 (en) | 2017-07-21 | 2019-01-24 | Basf Se | BENZAMIDE COMPOUNDS AND THEIR USE AS HERBICIDES |
| WO2019025540A1 (de) * | 2017-08-04 | 2019-02-07 | Bayer Aktiengesellschaft | 3-acyl-benzamide und ihre verwendung als herbizide |
| WO2019105995A1 (en) | 2017-11-29 | 2019-06-06 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019122345A1 (en) | 2017-12-22 | 2019-06-27 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019122347A1 (en) | 2017-12-22 | 2019-06-27 | Basf Se | N-(1,2,5-oxadiazol-3-yl)-benzamide compounds and their use as herbicides |
| EP3508480A1 (de) | 2018-01-08 | 2019-07-10 | Basf Se | Benzamidverbindungen und deren verwendung als herbizide |
| WO2019162308A1 (en) | 2018-02-21 | 2019-08-29 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019162309A1 (en) | 2018-02-21 | 2019-08-29 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2020147705A1 (zh) | 2019-01-14 | 2020-07-23 | 青岛清原化合物有限公司 | 4-吡啶基甲酰胺类化合物或其衍生物、制备方法、除草组合物和应用 |
| WO2020148175A1 (de) | 2019-01-14 | 2020-07-23 | Bayer Aktiengesellschaft | Herbizide substituierte n-tetrazolylarylcarboxamide |
| WO2021080330A1 (ko) | 2019-10-21 | 2021-04-29 | 한국화학연구원 | 니코틴아마이드 화합물 및 이 화합물을 포함하는 제초제 조성물 |
| DE112019005943T5 (de) | 2018-11-30 | 2021-08-26 | Qingdao Kingagroot Chemical Compound Co., Ltd. | N-(1, 3, 4-Oxadiazol-2-yl)arylcarboxamide oder deren Salze, Herstellungsverfahren, Herbizidzusammensetzungen und Verwendungen dieser |
| WO2021204665A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide |
| WO2021204669A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide |
| WO2021204666A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide und ihre verwendung als herbizide |
| US11180770B2 (en) | 2017-03-07 | 2021-11-23 | BASF Agricultural Solutions Seed US LLC | HPPD variants and methods of use |
| KR20220144779A (ko) | 2021-04-20 | 2022-10-27 | 한국화학연구원 | 옥사졸리디논 유도체 및 이 화합물을 포함하는 제초제 조성물 |
| RU2827438C1 (ru) * | 2019-11-15 | 2024-09-26 | Сингента Кроп Протекшн Аг | Гербицидные соединения |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9035064B2 (en) * | 2011-03-15 | 2015-05-19 | Bayer Intellectual Property Gmbh | N-(1,2,5-oxadiazol-3-yl)pyridinecarboxamides and use thereof as herbicides |
| UA111193C2 (uk) * | 2011-03-25 | 2016-04-11 | Баєр Інтеллекчуел Проперті Гмбх | Застосування n-(тетразол-4-іл)- або n-(триазол-3-іл)арилкарбоксамідів або їх солей для контролю небажаних рослин на площах трансгенних культур, що толерантні до гербіцидів, що є інгібіторами hppd |
| BR112014006208B1 (pt) * | 2011-09-16 | 2018-10-23 | Bayer Intellectual Property Gmbh | método de indução de respostas reguladoras do crescimento nas plantas aumentando o rendimento de plantas úteis ou plantas de cultura e composição de aumento do rendimento da planta compreendendo isoxadifen-etilo ou isoxadifeno e combinação de fungicidas |
| EP2589598A1 (de) * | 2011-11-03 | 2013-05-08 | Bayer CropScience AG | 5-Phenylsubstituierte N-(Tetrazol-5-yl)- und N-(Triazol-5-yl)arylcarbonsäureamide und ihre Verwendung als Herbizide |
| UA113545C2 (xx) | 2012-05-03 | 2017-02-10 | Солі n-(тетразол-5-іл)арилкарбоксаміду і їх застосування як гербіцидів | |
| CA2990985A1 (en) * | 2015-07-03 | 2017-01-12 | Bayer Cropscience Aktiengesellschaft | N-(tetrazole-5-yl)- and n-(triazole-5-yl)aryl carboxamide derivatives with herbicidal action |
| KR20180095901A (ko) * | 2015-12-17 | 2018-08-28 | 바스프 에스이 | 벤즈아미드 화합물 및 제초제로서 그들의 용도 |
| BR112020017570A2 (pt) * | 2018-02-28 | 2020-12-22 | Bayer Aktiengesellschaft | Benzamidas bicíclicas herbicidamente ativas |
| AR120445A1 (es) * | 2019-11-15 | 2022-02-16 | Syngenta Crop Protection Ag | N-tetrazolil o n-1,3,4-oxadiazolil benzamidas como herbicidas |
| CN114957217A (zh) * | 2022-06-10 | 2022-08-30 | 华中师范大学 | 含有2-三氟甲基吡啶酰胺结构的化合物及其制备方法和应用、除草剂及其应用 |
| WO2024074126A1 (zh) * | 2022-10-05 | 2024-04-11 | 江苏中旗科技股份有限公司 | 一种4-甲磺酰基苯甲酰胺类化合物、制备方法、除草组合物及用途 |
| CN117561242A (zh) * | 2022-10-05 | 2024-02-13 | 江苏中旗科技股份有限公司 | 一种4-甲磺酰基苯甲酰胺类化合物、制备方法、除草组合物及用途 |
Citations (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0131624A1 (de) | 1983-01-17 | 1985-01-23 | Monsanto Co | Plasmide zur transformation von pflanzenzellen. |
| EP0142924A2 (de) | 1983-09-26 | 1985-05-29 | Mycogen Plant Science, Inc. | Insektresistente Pflanzen |
| EP0193259A1 (de) | 1985-01-18 | 1986-09-03 | Plant Genetic Systems N.V. | Modifikation von Pflanzen auf pentechnologischem Wege zur Bekämpfung oder zur Kontrolle von Insekten |
| EP0221044A1 (de) | 1985-10-25 | 1987-05-06 | Monsanto Company | Pflanzenvektoren |
| EP0242246A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| EP0305398A1 (de) | 1986-05-01 | 1989-03-08 | Honeywell Inc | Verbindungsanordnung für mehrere integrierte schaltungen. |
| EP0309862A1 (de) | 1987-09-30 | 1989-04-05 | Bayer Ag | Stilbensynthase-Gen |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| WO1991013972A1 (en) | 1990-03-16 | 1991-09-19 | Calgene, Inc. | Plant desaturases - compositions and uses |
| WO1991019806A1 (en) | 1990-06-18 | 1991-12-26 | Monsanto Company | Increased starch content in plants |
| EP0464461A2 (de) | 1990-06-29 | 1992-01-08 | Bayer Ag | Stilbensynthase-Gene aus Weinrebe |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| WO1992011376A1 (en) | 1990-12-21 | 1992-07-09 | Amylogene Hb | Genetically engineered modification of potato to form amylopectin-type starch |
| WO1992014827A1 (en) | 1991-02-13 | 1992-09-03 | Institut Für Genbiologische Forschung Berlin Gmbh | Plasmids containing dna-sequences that cause changes in the carbohydrate concentration and the carbohydrate composition in plants, as well as plant cells and plants containing these plasmids |
| US6376429B1 (en) | 1998-10-10 | 2002-04-23 | Hoechst Schering Agrevo Gmbh | Benzoylcyclohexanediones, process for their preparation and their use as herbicides and plant growth regulators |
| EP1202978A1 (de) | 1999-07-27 | 2002-05-08 | Aventis CropScience GmbH | Isoxazolyl- und isoxazolinyl-substituierte benzoylcyclohexandione, verfahren zu ihrer herstellung und ihre verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2003010153A1 (en) | 2001-07-26 | 2003-02-06 | Samsung Electronics Co. Ltd. | N-alkyl-n-phenylhydroxylamine compounds containing metal chelating groups, their preparation and their therapeutic uses |
| WO2003010143A1 (en) | 2001-07-26 | 2003-02-06 | Samsung Electronics Co., Ltd. | Dialkylhydroxybenzoic acid derivatives containing metal chelating groups and their therapeutic uses |
| WO2004101532A1 (en) * | 2003-05-13 | 2004-11-25 | Bayer Cropscience Ag | Substituted triazolecarboxamides |
| EP1585742A1 (de) | 2003-01-09 | 2005-10-19 | Bayer CropScience GmbH | Substituierte benzoylderivate als herbizide |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1196237B (it) * | 1984-08-29 | 1988-11-16 | Enichimica Secondaria | Composti eterociclici ad attivita' erbicida |
| JPS649978A (en) * | 1987-07-02 | 1989-01-13 | Shionogi & Co | Perfluoroalkylisoxazole derivative |
| DE3809053A1 (de) * | 1988-03-18 | 1989-09-28 | Bayer Ag | Substituierte 5-amino-4h-1,2,4-triazol-3-yl-carbonsaeureamide, verfahren zu ihrer herstellung und ihre verwendung als herbizide |
| JPH0341072A (ja) * | 1989-07-07 | 1991-02-21 | Hokko Chem Ind Co Ltd | トリアゾールカルボン酸アミド誘導体および除草剤 |
| DE4124150A1 (de) * | 1991-07-20 | 1993-01-21 | Bayer Ag | Substituierte triazole |
| JPH10204066A (ja) * | 1997-01-28 | 1998-08-04 | Nippon Bayer Agrochem Kk | 1−フエニル−5−アニリノテトラゾール類及び農薬としてのその利用 |
| DE10031825A1 (de) * | 2000-06-30 | 2002-01-10 | Bayer Ag | Selektive Herbizide auf Basis von Arylsulfonylaminocarbonyltriazolinonen |
| JP2003034685A (ja) * | 2001-05-14 | 2003-02-07 | Nippon Nohyaku Co Ltd | チアジアゾール誘導体及び農園芸用薬剤並びにその使用方法 |
| ITMI20031855A1 (it) * | 2003-09-29 | 2005-03-30 | Isagro Ricerca Srl | Derivati di 1,3-dioni aventi attivita' erbicida. |
| JP5918124B2 (ja) * | 2009-05-12 | 2016-05-18 | ロマーク ラボラトリーズ エル.シー. | ハロアルキルヘテロアリールベンズアミド化合物 |
| UA109150C2 (xx) * | 2010-09-01 | 2015-07-27 | Аміди n-(тетразол-5-іл)- або n-(триазол-5-іл)арилкарбонової кислоти та їх застосування як гербіцидів | |
| UA111193C2 (uk) * | 2011-03-25 | 2016-04-11 | Баєр Інтеллекчуел Проперті Гмбх | Застосування n-(тетразол-4-іл)- або n-(триазол-3-іл)арилкарбоксамідів або їх солей для контролю небажаних рослин на площах трансгенних культур, що толерантні до гербіцидів, що є інгібіторами hppd |
-
2012
- 2012-07-30 IN IN176DEN2014 patent/IN2014DN00176A/en unknown
- 2012-07-30 AR ARP120102774A patent/AR087385A1/es active Pending
- 2012-07-30 EP EP20120745447 patent/EP2739611B1/de active Active
- 2012-07-30 ES ES12745447.8T patent/ES2542681T3/es active Active
- 2012-07-30 WO PCT/EP2012/064863 patent/WO2013017559A1/de active Application Filing
- 2012-07-30 BR BR112014002191A patent/BR112014002191B1/pt active IP Right Grant
- 2012-07-30 JP JP2014523298A patent/JP6078065B2/ja active Active
- 2012-07-30 PL PL12745447T patent/PL2739611T3/pl unknown
- 2012-07-30 CN CN201280038161.9A patent/CN103717581B/zh active Active
- 2012-07-30 US US14/233,298 patent/US8822378B2/en active Active
Patent Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0131624A1 (de) | 1983-01-17 | 1985-01-23 | Monsanto Co | Plasmide zur transformation von pflanzenzellen. |
| EP0142924A2 (de) | 1983-09-26 | 1985-05-29 | Mycogen Plant Science, Inc. | Insektresistente Pflanzen |
| EP0193259A1 (de) | 1985-01-18 | 1986-09-03 | Plant Genetic Systems N.V. | Modifikation von Pflanzen auf pentechnologischem Wege zur Bekämpfung oder zur Kontrolle von Insekten |
| EP0221044A1 (de) | 1985-10-25 | 1987-05-06 | Monsanto Company | Pflanzenvektoren |
| EP0242246A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0242236A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0305398A1 (de) | 1986-05-01 | 1989-03-08 | Honeywell Inc | Verbindungsanordnung für mehrere integrierte schaltungen. |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| EP0309862A1 (de) | 1987-09-30 | 1989-04-05 | Bayer Ag | Stilbensynthase-Gen |
| WO1991013972A1 (en) | 1990-03-16 | 1991-09-19 | Calgene, Inc. | Plant desaturases - compositions and uses |
| WO1991019806A1 (en) | 1990-06-18 | 1991-12-26 | Monsanto Company | Increased starch content in plants |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| EP0464461A2 (de) | 1990-06-29 | 1992-01-08 | Bayer Ag | Stilbensynthase-Gene aus Weinrebe |
| WO1992011376A1 (en) | 1990-12-21 | 1992-07-09 | Amylogene Hb | Genetically engineered modification of potato to form amylopectin-type starch |
| WO1992014827A1 (en) | 1991-02-13 | 1992-09-03 | Institut Für Genbiologische Forschung Berlin Gmbh | Plasmids containing dna-sequences that cause changes in the carbohydrate concentration and the carbohydrate composition in plants, as well as plant cells and plants containing these plasmids |
| US6376429B1 (en) | 1998-10-10 | 2002-04-23 | Hoechst Schering Agrevo Gmbh | Benzoylcyclohexanediones, process for their preparation and their use as herbicides and plant growth regulators |
| EP1202978A1 (de) | 1999-07-27 | 2002-05-08 | Aventis CropScience GmbH | Isoxazolyl- und isoxazolinyl-substituierte benzoylcyclohexandione, verfahren zu ihrer herstellung und ihre verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2003010153A1 (en) | 2001-07-26 | 2003-02-06 | Samsung Electronics Co. Ltd. | N-alkyl-n-phenylhydroxylamine compounds containing metal chelating groups, their preparation and their therapeutic uses |
| WO2003010143A1 (en) | 2001-07-26 | 2003-02-06 | Samsung Electronics Co., Ltd. | Dialkylhydroxybenzoic acid derivatives containing metal chelating groups and their therapeutic uses |
| EP1585742A1 (de) | 2003-01-09 | 2005-10-19 | Bayer CropScience GmbH | Substituierte benzoylderivate als herbizide |
| WO2004101532A1 (en) * | 2003-05-13 | 2004-11-25 | Bayer Cropscience Ag | Substituted triazolecarboxamides |
Non-Patent Citations (34)
| Title |
|---|
| "Combinatorial Chemistry - Synthesis, Analysis, Screening (Herausgeber Günther Jung", 1999, VERLAG WILEY |
| "Combinatorial Chemistry - Synthesis, Analysis, Screening (Herausgeber Günther Jung", 1999, VERLAG WILEY, pages: 1,34 |
| "Organic and Medicinal Chemistry (Herausgeber C. O. Kappe und a. Stadler", 2005, VERLAG WILEY |
| "Perry's Chemical Engineer's Handbook, 5th Ed.,", 1973, MCGRAW-HILL, pages: 8 - 57 |
| "The Pesticide Manual,15th edition,", 2009, THE BRITISH CROP PROTECTION COUNCIL AND THE ROYAL SOC. OF CHEMISTRY |
| "Trends in Plant Science", vol. 1, 1996, SPRINGER VERLAG BERLIN, pages: 423 - 431 |
| ANGEWANDTE CHEMIE, vol. 75, 1963, pages 918 |
| BARRY A. BUNIN: "The Combinatorial Index", 1998, ACADEMIC PRESS |
| BRAUN ET AL., EMBO J., vol. 11, 1992, pages 3219 - 3227 |
| C. MARSDEN: "Solvents Guide, 2nd Ed.,", 1963, INTERSCIENCE |
| CHEMFILES, vol. 4, no. 1 |
| CHEMIE, vol. 30, no. 12, 1990, pages 436 - 437 |
| CHEMISCHE BERICHTE, vol. 97, no. 2, 1964, pages 396 - 404 |
| G.C. KLINGMAN: "Weed Control as a Science", 1961, JOHN WILEY AND SONS, INC., pages: 81 - 96 |
| H.V. OLPHEN: "Introduction to Clay Colloid Chemistry, 2nd Ed.,", J. WILEY & SONS |
| J.D. FREYER; S.A. EVANS: "Weed Control Handbook,5th Ed.,", 1968, pages: 101 - 103 |
| J.E. BROWNING: "Chemical and Engineering", 1967, article "Agglomeration" |
| JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 76, 1954, pages 88 - 89 |
| JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 76, 1954, pages 923 - 924 |
| K. MARTENS: "Spray Drying, 3rd Ed.", 1979, G. GOODWIN LTD. |
| MCCUTCHEON'S: "Detergents and Emulsifiers Annual", MC PUBL. CORP. |
| POTRYKUS UND G. SPANGENBERG: "Gene Transfer to Plants", 1995, SPRINGER LAB MANUAL |
| SAMBROOK ET AL.: "Molecular Cloning, A Laboratory Manual, 2. Aufl.", 1989, COLD SPRING HARBOR LABORATORY PRESS |
| SCHÖNFELDT: "Grenzflächenaktive Äthylenoxidaddukte", 1976, WISS. VERLAGSGESELL. |
| SISLEY; WOOD: "Encyclopedia of Surface Active Agents", 1964, CHEM. PUBL. CO. INC. |
| SONNEWALD ET AL., PLANT J., vol. 1, 1991, pages 95 - 106 |
| VERFAHREN: "Spray-Drying Handbook" 3rd ed.", 1979, G. GOODWIN LTD. |
| WADE VAN VALKENBURG: "Pesticide Formulations", 1973, MARCEL DEKKER |
| WATKINS: "Handbook of Insecticide Dust Diluents and Carriers, 2nd Ed.,", DARLAND BOOKS |
| WEED RESEARCH, vol. 26, 1986, pages 441 - 445 |
| WINNACKER: "Gene und Klone", 1996, VCH WEINHEIM |
| WINNACKER-KÜCHLER: "Chemische Technologie", vol. 7, C. HANSER VERLAG |
| WINNACKER-KUCHLER: "Chemische Technologie, 4. Aufl.", vol. 7, 1986 |
| WOLTER ET AL., PROC. NATL. ACAD. SCI. USA, vol. 85, 1988, pages 846 - 850 |
Cited By (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2773208A1 (de) * | 2011-11-03 | 2014-09-10 | Bayer Intellectual Property GmbH | Herbizid-safener-zusammensetzungen enthaltend n-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide |
| WO2013092834A1 (en) * | 2011-12-21 | 2013-06-27 | Syngenta Limited | Herbicidal compounds |
| US9375012B2 (en) | 2011-12-21 | 2016-06-28 | Syngenta Limited | Herbicidal compounds |
| JP2015508766A (ja) * | 2012-02-21 | 2015-03-23 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツングBayer Intellectual Property GmbH | 除草3−(スルフィン−/スルホンイミドイル)−ベンズアミド |
| US20150111750A1 (en) * | 2012-04-27 | 2015-04-23 | Basf Se | Substituted N-(tetrazol-5-yl)- and N-(triazol-5-yl)hetarylcarboxamide compounds and their use as herbicides |
| WO2013076316A3 (en) * | 2012-04-27 | 2013-09-26 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)hetarylcarboxamide compounds and their use as herbicides |
| US9398768B2 (en) | 2012-04-27 | 2016-07-26 | Basf Se | Substituted N-(tetrazol-5-yl)- and N-(triazol-5-yl)pyridin-3-yl-carboxamide compounds and their use as herbicides |
| WO2013072528A3 (en) * | 2012-04-27 | 2013-07-04 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)pyridin-3-yl-carboxamide compounds and their use as herbicides |
| US9867376B2 (en) | 2012-05-24 | 2018-01-16 | Bayer Cropscience Ag | Herbicidal compositions comprising N-tetrazol-5-yl)- or N-(triazol-5-yl)arylcarboxamides |
| WO2014184017A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)pyridin-3-yl-carboxamide compounds and their use as herbicides |
| WO2014184073A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)arylcarboxamide compounds and their use as herbicides |
| WO2014184074A1 (en) * | 2013-05-15 | 2014-11-20 | Basf Se | Substituted n-(tetrazol-5-yl)- and n-(triazol-5-yl)hetarylcarboxamide compounds and their use as herbicides |
| JP2016523831A (ja) * | 2013-05-15 | 2016-08-12 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | 置換型n−(テトラゾール−5−イル)−およびn−(トリアゾール−5−イル)アリールカルボキサミド化合物ならびに除草剤としてのそれらの使用 |
| WO2014192936A1 (ja) | 2013-05-31 | 2014-12-04 | 日産化学工業株式会社 | 複素環アミド化合物 |
| JPWO2014192936A1 (ja) * | 2013-05-31 | 2017-02-23 | 日産化学工業株式会社 | 複素環アミド化合物 |
| US9708314B2 (en) | 2013-05-31 | 2017-07-18 | Nissan Chemical Industries, Ltd. | Heterocyclic amide compound |
| KR20160015211A (ko) | 2013-05-31 | 2016-02-12 | 닛산 가가쿠 고교 가부시키 가이샤 | 복소환 아미드 화합물 |
| AU2014271662B2 (en) * | 2013-05-31 | 2018-03-01 | Nissan Chemical Corporation | Heterocyclic amide compound |
| KR20210029300A (ko) | 2013-05-31 | 2021-03-15 | 닛산 가가쿠 가부시키가이샤 | 복소환 아미드 화합물 |
| JP2017523235A (ja) * | 2014-06-30 | 2017-08-17 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 除草活性を有するアリールカルボン酸アミド類 |
| JP2017523236A (ja) * | 2014-06-30 | 2017-08-17 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 除草活性を有する安息香酸アミド類 |
| WO2017042259A1 (en) | 2015-09-11 | 2017-03-16 | Bayer Cropscience Aktiengesellschaft | Hppd variants and methods of use |
| JP2018531236A (ja) * | 2015-09-28 | 2018-10-25 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | アシル化n−(1,2,5−オキサジアゾール−3−イル)−、n−(1,3,4−オキサジアゾール−2−イル)−、n−(テトラゾール−5−イル)−およびn−(トリアゾール−5−イル)−アリールカルボキサミド、および除草剤としてのそれらの使用 |
| US11180770B2 (en) | 2017-03-07 | 2021-11-23 | BASF Agricultural Solutions Seed US LLC | HPPD variants and methods of use |
| WO2018219936A1 (en) | 2017-05-30 | 2018-12-06 | Basf Se | Benzamide compounds and their use as herbicides ii |
| WO2018219935A1 (en) | 2017-05-30 | 2018-12-06 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019016385A1 (en) | 2017-07-21 | 2019-01-24 | Basf Se | BENZAMIDE COMPOUNDS AND THEIR USE AS HERBICIDES |
| AU2018309334B2 (en) * | 2017-08-04 | 2022-07-21 | Bayer Aktiengesellschaft | 3-acyl-benzamides and their use as herbicides |
| WO2019025540A1 (de) * | 2017-08-04 | 2019-02-07 | Bayer Aktiengesellschaft | 3-acyl-benzamide und ihre verwendung als herbizide |
| IL272164B1 (en) * | 2017-08-04 | 2023-03-01 | Bayer Ag | 3-Acyl-benzamides and their use as herbicides |
| US11051515B2 (en) | 2017-08-04 | 2021-07-06 | Bayer Aktiengesellschaft | 3-acyl-benzamides and their use as herbicides |
| IL272164B2 (en) * | 2017-08-04 | 2023-07-01 | Bayer Ag | 3-Acyl-benzamides and their use as herbicides |
| WO2019105995A1 (en) | 2017-11-29 | 2019-06-06 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019122347A1 (en) | 2017-12-22 | 2019-06-27 | Basf Se | N-(1,2,5-oxadiazol-3-yl)-benzamide compounds and their use as herbicides |
| WO2019122345A1 (en) | 2017-12-22 | 2019-06-27 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019134993A1 (en) | 2018-01-08 | 2019-07-11 | Basf Se | Benzamide compounds and their use as herbicides |
| EP3508480A1 (de) | 2018-01-08 | 2019-07-10 | Basf Se | Benzamidverbindungen und deren verwendung als herbizide |
| WO2019162309A1 (en) | 2018-02-21 | 2019-08-29 | Basf Se | Benzamide compounds and their use as herbicides |
| WO2019162308A1 (en) | 2018-02-21 | 2019-08-29 | Basf Se | Benzamide compounds and their use as herbicides |
| DE112019005943T5 (de) | 2018-11-30 | 2021-08-26 | Qingdao Kingagroot Chemical Compound Co., Ltd. | N-(1, 3, 4-Oxadiazol-2-yl)arylcarboxamide oder deren Salze, Herstellungsverfahren, Herbizidzusammensetzungen und Verwendungen dieser |
| WO2020148175A1 (de) | 2019-01-14 | 2020-07-23 | Bayer Aktiengesellschaft | Herbizide substituierte n-tetrazolylarylcarboxamide |
| WO2020147705A1 (zh) | 2019-01-14 | 2020-07-23 | 青岛清原化合物有限公司 | 4-吡啶基甲酰胺类化合物或其衍生物、制备方法、除草组合物和应用 |
| KR20210047264A (ko) | 2019-10-21 | 2021-04-29 | 한국화학연구원 | 니코틴아마이드 화합물 및 이 화합물을 포함하는 제초제 조성물 |
| WO2021080330A1 (ko) | 2019-10-21 | 2021-04-29 | 한국화학연구원 | 니코틴아마이드 화합물 및 이 화합물을 포함하는 제초제 조성물 |
| RU2827438C1 (ru) * | 2019-11-15 | 2024-09-26 | Сингента Кроп Протекшн Аг | Гербицидные соединения |
| WO2021204666A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide und ihre verwendung als herbizide |
| WO2021204669A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide |
| WO2021204665A1 (de) | 2020-04-07 | 2021-10-14 | Bayer Aktiengesellschaft | Substituierte isophtalsäurediamide |
| CN115768752A (zh) * | 2020-04-07 | 2023-03-07 | 拜耳公司 | 取代的间苯二酸二酰胺 |
| KR20220144779A (ko) | 2021-04-20 | 2022-10-27 | 한국화학연구원 | 옥사졸리디논 유도체 및 이 화합물을 포함하는 제초제 조성물 |
Also Published As
| Publication number | Publication date |
|---|---|
| AR087385A1 (es) | 2014-03-19 |
| PL2739611T3 (pl) | 2015-09-30 |
| JP2014521676A (ja) | 2014-08-28 |
| EP2739611B1 (de) | 2015-05-13 |
| BR112014002191B1 (pt) | 2018-07-17 |
| IN2014DN00176A (de) | 2015-07-10 |
| EP2739611A1 (de) | 2014-06-11 |
| BR112014002191A2 (pt) | 2017-03-07 |
| ES2542681T3 (es) | 2015-08-10 |
| CN103717581A (zh) | 2014-04-09 |
| US20140179527A1 (en) | 2014-06-26 |
| US8822378B2 (en) | 2014-09-02 |
| JP6078065B2 (ja) | 2017-02-08 |
| CN103717581B (zh) | 2016-04-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2773625B1 (de) | 5-phenylsubstituierte n-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| WO2013017559A1 (de) | N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| EP2791119B1 (de) | N-(1,2,5-oxadiazol-3-yl)-, n-(1,3,4-oxadiazol-2-yl)-, n-(tetrazol-5-yl)- und n-(triazol-5-yl)-arylcarbonsäureamide und ihre verwendung als herbizide | |
| TWI554211B (zh) | N-(四唑-5-基)-和n-(三唑-5-基)芳基羧醯胺類及其在充作除草劑上的用途 | |
| EP2691379B1 (de) | Herbizid und fungizid wirksame 3-phenylisoxazolin-5-carboxamide und 3- phenylisoxazolin-5-thioamide | |
| EP2686315B1 (de) | N-(1,2,5-oxadiazol-3-yl)-, n-(tetrazol-5-yl)- und n-(triazol-5-yl)bicycloaryl-carbonsäureamide und ihre verwendung als herbizide | |
| WO2013124245A1 (de) | Herbizid wirksame 4-nitro substituierte n-(tetrazol-5-yl)-, n-(triazol-5-yl)- und n-(1,3,4-oxadiazol-2-yl)arylcarbonsäureamide | |
| EP2773626B1 (de) | Herbizid wirksame oximether substituierter benzoylamide | |
| EP2686316A1 (de) | N-(1,2,5-oxadiazol-3-yl)pyridincarboxamide und ihre verwendung als herbizide | |
| EP2688885A1 (de) | N-(1,3,4-oxadiazol-2-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| EP3601242A1 (de) | Substituierte n-(1,3,4-oxadiazol-2-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| EP2475646A1 (de) | 4- (3-alkylthiobenzoyl) pyrazole und ihre verwendung als herbizide | |
| WO2009149806A2 (de) | Herbizid wirksame 4- (3-alkylsulfinylbenzoyl) pyrazole | |
| EP2802569B1 (de) | Tetrazol-5-yl- und triazol-5-yl-arylverbindungen und ihre verwendung als herbizide | |
| EP2459528A1 (de) | 2-(3-alkylthiobenzoyl)cyclohexandione und ihre verwendung als herbizide | |
| EP2260027B1 (de) | Herbizid wirksame 4- (3-aminobenzoyl) -5-cyclopropylisoxazole | |
| WO2011012248A2 (de) | 2-(3-aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre verwendung als herbizide | |
| WO2012010575A1 (de) | (4-halogenalkyl-3-thiobenzoyl)cyclohexandione und ihre verwendung als herbizide | |
| EP2480522A1 (de) | 3-amino-2-nitro-substituierte benzoylderivate und ihre verwendung als herbizide | |
| WO2013124246A1 (de) | Herbizid wirksame 4-dialkoxymethyl-2-phenylpyrimidine |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201280038161.9 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 12745447 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2012745447 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 2014523298 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14233298 Country of ref document: US |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112014002191 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 112014002191 Country of ref document: BR Kind code of ref document: A2 Effective date: 20140129 |