WO2011012248A2 - 2-(3-aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre verwendung als herbizide - Google Patents
2-(3-aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre verwendung als herbizide Download PDFInfo
- Publication number
- WO2011012248A2 WO2011012248A2 PCT/EP2010/004446 EP2010004446W WO2011012248A2 WO 2011012248 A2 WO2011012248 A2 WO 2011012248A2 EP 2010004446 W EP2010004446 W EP 2010004446W WO 2011012248 A2 WO2011012248 A2 WO 2011012248A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- alkyl
- cycloalkyl
- phenyl
- alkynyl
- alkenyl
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C317/00—Sulfones; Sulfoxides
- C07C317/44—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton
- C07C317/48—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton the carbon skeleton being further substituted by singly-bound nitrogen atoms, not being part of nitro or nitroso groups
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/34—Nitriles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N41/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a sulfur atom bound to a hetero atom
- A01N41/02—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a sulfur atom bound to a hetero atom containing a sulfur-to-oxygen double bond
- A01N41/10—Sulfones; Sulfoxides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/01—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms
- C07C255/32—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms having cyano groups bound to acyclic carbon atoms of a carbon skeleton containing at least one six-membered aromatic ring
- C07C255/42—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms having cyano groups bound to acyclic carbon atoms of a carbon skeleton containing at least one six-membered aromatic ring the carbon skeleton being further substituted by singly-bound nitrogen atoms, not being further bound to other hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/02—Systems containing only non-condensed rings with a three-membered ring
Definitions
- the invention relates to the technical field of herbicides, in particular that of herbicides for the selective control of weeds and weeds in
- the object of the present invention is therefore to provide herbicidally active compounds with improved herbicidal properties compared with the compounds known from the prior art
- An object of the present invention are 2- (3-aminobenzoyl) -3-cyclopropyl-3-oxopropanenitriles of the formula (I) or salts thereof
- X and Y are independently nitro, halogen, cyano, thiocyanato, (C r C6) alkyl, (dC 6) -haloalkyl, (C 2 -C 6) alkenyl, (C 2 -C 6) haloalkenyl, (C 2 - C 6) alkynyl, (C 3 -C 6) -haloalkynyl, (C 3 -C 6) -cycloalkyl, (C 3 -C 6) halocycloalkyl, (C 3 -C 6) cycloalkyl (C 1 -C 6) alkyl, (C 3 -C 6) -Halogencycloalkyl- (CrC 6) alkyl, COR 1, OR 1, OCOR 1, OSO 2 R 2, S (O) n R 2, SO 2 OR 1 , SO 2 N (R 1 ) 2 1 NR 1 SO 2 R 2 , NR 1 COR 1 , (C
- R 1 is hydrogen, (C r C6) alkyl, (C 2 -C 6) alkenyl, (C 2 -C 6) -alkynyl, (C 3 -C 6) - cycloalkyl, (C 3 -C 6 ) -Cycloalkyl- (C 1 -C 6 ) -alkyl, phenyl or phenyl- (C 1 -C 6 ) -alkyl, where the seven last-mentioned radicals are represented by s radicals from the group consisting of cyano, halogen, nitro, rhodano, OR 3 , S ( O) n R 4 , N (R 3 ) 2 , NR 3 OR 3 , COR 3 , OCOR 3 , SCOR 3 , NR 3 COR 3 , CO 2 R 3 , COSR 3 , CON (R 3 ) 2 and (dC 4 ) Alkoxy- (C 2 -C 6 ) al
- R 2 is (dC 6) alkyl, (C 2 -C 6) alkenyl, (C 2 -C 6) -alkynyl, (C 3 -C 6) cycloalkyl, (C 3 -C 6) cycloalkyl (C 1 -C 6 ) -alkyl, phenyl or phenyl (C 1 -C 6 ) -alkyl, where the seven last-mentioned radicals are represented by s radicals from the group consisting of cyano,
- R 4 is (dC 6) alkyl, (C 2 -C 6) -alkenyl or (C 2 -C 6) alkynyl, n is O, 1 or 2, s is 0, 1, 2 or 3rd
- alkyl radicals having more than two carbon atoms may be straight-chain or branched.
- Alkyl radicals are, for example, methyl, ethyl, n- or i-propyl, n-, i-, t- or 2-butyl, pentyls, hexyls, such as n-hexyl, i-hexyl and 1,3-dimethylbutyl.
- Halogen is fluorine, chlorine, bromine or iodine.
- the compounds of the general formula (I) can exist as stereoisomers.
- stereoisomers For example, if one or more asymmetrically substituted carbon atoms are present, enantiomers and diastereomers may occur. Similarly, stereoisomers occur when n is 1 (sulfoxides).
- Stereoisomers can be obtained from the mixtures obtained in the preparation by customary separation methods, for example by chromatographic separation methods. Similarly, stereoisomers can be selectively prepared by using stereoselective reactions using optically active sources and / or adjuvants.
- the invention also relates to all stereoisomers and mixtures thereof, which are of the general formula (I), but are not specifically defined.
- X and Y are independently nitro, halogen, cyano, (CrC 6) - alkyl, (Ci-C 6) -haloalkyl, (C 2 -C 6) alkenyl, (C 2 -C 6) -haloalkenyl, (C 2 -C 6) -alkynyl, (C 3 -C 6) -haloalkynyl, (C 3 -C 6) -cycloalkyl, (C 3 -C 6) halocycloalkyl, (C 3 -C 6) - cycloalkyl (CrC 6 ) -alkyl, (C 3 -C 6 ) -halocycloalkyl- (C 1 -C 6 ) -alkyl, COR 1 , OR 1 , OCOR 1 , OSO 2 R 2 , S (O) n R 2 , SO 2 OR 1 , (C 1 -C 6 ) -
- R 1 is hydrogen, (C r C6) alkyl, (C 2 -C 6) alkenyl, (C 2 -C 6) -alkynyl, (C 3 -C 6) - cycloalkyl, (C 3 -C 6 ) -Cycloalkyl- (C 1 -C 6 ) -alkyl, phenyl or phenyl- (C 1 -C 6 ) -alkyl, where the seven last-mentioned radicals are substituted by s radicals from the group consisting of halogen and OR 3 ,
- R 2 is (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl, (C 2 -C 6 ) -alkynyl, (C 3 -C 6 ) -cycloalkyl, (C 3 -C 6 ) - cycloalkyl (C 1 -C 6) alkyl, phenyl or phenyl- (Ci-C 6) -alkyl, where these abovementioned radicals are substituted by s radicals selected from the group consisting of cyano, halogen and oR 3,
- R 3 is hydrogen, (C r C6) alkyl, (C r C6) -haloalkyl, (C2 -Ce) -alkenyl or (C 2 -C 6) alkynyl
- R 4 is (C 1 -C 6 ) -alkyl, (C 2 -C 6 ) -alkenyl or (C 2 -C 6 ) -alkynyl, n is 0, 1 or 2, s is 0, 1, 2 or 3.
- X is nitro, fluorine, chlorine, bromine, iodine, cyano, methyl, ethyl, methoxy, ethoxy, trifluoromethyl, methylsulfonyl, ethylsulfonyl, methylsulfenylmethyl,
- Methylsulfinylmethyl, methylsulfonylmethyl, Y is nitro, fluorine, chlorine, bromine, iodine, cyano, methoxy, ethoxy,
- Trifluoromethyl methylsulfonyl, ethylsulfonyl.
- Benzoic acids are synthesized. Such syntheses are described in EP 0 625 505 A1. The preparation of the benzoic acids (IIIa) and the associated acid chlorides (IM) is described, for example, in WO 94/14782, WO 95/16678 and US Pat
- Chromatographieapparaturen available, for example, the company ISCO, Inc., 4700 Superior Street, Lincoln, NE 68504, USA.
- the listed equipment leads to a modular procedure, in which the individual work steps are automated, but between the work steps, manual operations must be performed.
- This can be circumvented by the use of partially or fully integrated automation systems in which the respective automation modules are operated, for example, by robots.
- Such automation systems can be obtained, for example, from Caliper, Hopkinton, MA 01748, USA.
- Solid-phase assisted methods are used. For this purpose, individual intermediates or all intermediates of the synthesis or one for the
- Literature-known protocols which in turn can be performed manually or automatically.
- the reactions can be carried out, for example, by means of IRORI technology in microreactors (microreactors) from Nexus Biosystems, 12140 Community Road, Poway, CA92064, USA. Both solid and liquid phases can be supported by the implementation of single or multiple synthetic steps through the use of microwave technology.
- IRORI technology in microreactors (microreactors) from Nexus Biosystems, 12140 Community Road, Poway, CA92064, USA. Both solid and liquid phases can be supported by the implementation of single or multiple synthetic steps through the use of microwave technology.
- a number of experimental protocols are described in the specialist literature, for example in Microwaves in Organic and Medicinal Chemistry (publishers C. O. Kappe and A. Stadler), Verlag Wiley, 2005.
- the preparation according to the methods described herein provides compounds of formula (I) and their salts in the form of substance collections called libraries.
- the present invention also provides libraries containing at least two compounds of formula (I) and their salts.
- Root sticks or other permanent organs are well detected by the active ingredients.
- the present invention therefore also provides a process for
- Compound (s) of the invention eg harmful plants such as mono- or dicotyledonous weeds or unwanted crops
- the seed eg
- the compounds of the invention may be e.g. in Vorsaat- (possibly also by incorporation into the soil), pre-emergence or
- Monocotyledonous harmful plants of the genera Aegilops, Agropyron, Agrostis,
- Crops harmful weed competition is eliminated very early and sustainably.
- Crops of economically important crops e.g. dicotyledonous cultures of
- Plant growth in crops such as agricultural crops or ornamental plantings.
- the transgenic plants are usually characterized by particular advantageous properties, for example by resistance to certain pesticides, especially certain herbicides, resistance to plant diseases or pathogens of plant diseases such as certain insects or microorganisms such as fungi, bacteria or viruses.
- z. B the crop in terms of quantity, quality, shelf life, composition and special ingredients.
- transgenic plants with increased starch content or altered quality of the starch or those with other fatty acid composition of the crop are known.
- transgenic cultures Preferred with respect to transgenic cultures is the use of the compounds of the invention in economically important transgenic crops of useful and
- Ornamental plants z.
- cereals such as wheat, barley, rye, oats, millet, rice and corn or cultures of sugar beet, cotton, soybeans, rape, potato, tomato, pea and other vegetables.
- the compounds of the invention can be used as herbicides in crops which are resistant to the phytotoxic effects of the herbicides or
- the application of the compounds of the invention or their salts in economically important transgenic crops of useful and ornamental plants eg.
- cereals such as wheat, barley, rye, oats, millet, rice, cassava and corn or cultures of sugar beet, cotton, soy, rape, potato, tomato, pea and other vegetables.
- the compounds according to the invention can be used as herbicides in crops which are resistant to the phytotoxic effects of the herbicides or
- Glufosinate see, for example, EP-A-0242236, EP-A-242246) or glyphosate
- transgenic crops for example cotton, with the ability
- Bacillus thuringiensis toxins Bacillus thuringiensis toxins (Bt toxins) to produce, which the
- transgenic crops characterized by a combination z.
- Numerous molecular biological techniques that can be used to produce new transgenic plants with altered properties are known in principle;
- nucleic acid molecules can be introduced into plasmids that allow mutagenesis or sequence alteration by recombination of DNA sequences.
- Standard methods can z. For example, base substitutions are made, partial sequences are removed, or natural or synthetic sequences are added.
- adapters or linkers can be attached to the fragments, see, for example, US Pat. Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2nd ed. CoId Spring Harbor Laboratory Press, ColD Spring Harbor, NY; or Winnacker "Genes and Clones", VCH Weinheim 2nd edition 1996
- Gene product can be obtained, for example, by the expression of at least one corresponding antisense RNA, a sense RNA to obtain a
- Cosuppressions canes or the expression of at least one appropriately engineered ribozyme, specifically transcripts of the above
- DNA molecules may be used which comprise the entire coding sequence of a gene product, including any flanking sequences that may be present, as well as DNA molecules which comprise only parts of the coding sequence, which parts must be long enough to be present in the cells to cause an antisense effect. It is also possible to use DNA sequences which have a high degree of homology to the coding sequences of a gene product, but are not completely identical.
- the synthesized protein may be located in any compartment of the plant cell. But to achieve the localization in a particular compartment, z.
- the coding region can be linked to DNA sequences that ensure localization in a particular compartment. Such sequences are the See, for example, Braun et al., EMBO J. 11 (1992), 3219-3227; Wolter et al., Proc. Natl. Acad., U.S.A. 85 (1988), 846-850; Sonnewald et al. Plant J. 1 (1991), 95-106).
- the expression of the nucleic acid molecules can also take place in the organelles of the plant cells.
- the transgenic plant cells can be regenerated to whole plants by known techniques.
- the transgenic plants may, in principle, be plants of any plant species, that is, both monocotyledonous and dicotyledonous plants.
- transgenic plants are available, the altered properties by
- the compounds of the invention can be used in transgenic cultures which are resistant to growth factors, such as. B. Dicamba or against herbicides, the essential plant enzymes, eg. Acetolactate synthases (ALS), EPSP synthases, glutamine synthases (GS) or hydroxyphenylpyruvate dioxygenases (HPPD) inhibit, respectively against herbicides from the group of
- growth factors such as. B. Dicamba or against herbicides
- the essential plant enzymes eg. Acetolactate synthases (ALS), EPSP synthases, glutamine synthases (GS) or hydroxyphenylpyruvate dioxygenases (HPPD) inhibit, respectively against herbicides from the group of
- Sulfonylureas the glyphosate, glufosinate or benzoylisoxazole and analogues, are resistant.
- Harmful plants often have effects that are specific for application in the particular transgenic culture, such as altered or specially extended weed spectrum that can be controlled
- the invention therefore also relates to the use of
- the compounds of the invention may be in the form of wettable powders, emulsifiable concentrates, sprayable solutions, dusts or
- Granules are used in the usual preparations.
- the invention therefore also relates to herbicidal and plant growth-regulating agents which contain the compounds according to the invention.
- the compounds according to the invention can be formulated in various ways, depending on which biological and / or chemical-physical parameters are predetermined. As formulation options come
- wettable powder WP
- water-soluble powder SP
- EC emulsifiable concentrates
- EW emulsions
- SC Suspension concentrates
- CS capsule suspensions
- DP dusts
- mordants granules for litter and soil application
- granules GR
- WG water-dispersible granules
- SG water-soluble granules
- the necessary formulation auxiliaries such as inert materials, surfactants,
- Solvents and other additives are also known and are described, for example, in Watkins, Handbook of Insecticides Dust Diluents and Carriers, 2nd Ed., Darland Books, Caldwell NJ, Hv Olphen, "Introduction to Clay Colloid Chemistry”; 2nd Ed., J. Wiley & Sons, NY; C. Marsden, “Solvent Guide”; 2nd Ed., Interscience, NY 1963; McCutcheon's "Detergents and Emulsifiers
- Fungicides as well as with safeners, fertilizers and / or growth regulators, e.g. in the form of a ready-made formulation or as a tank mix.
- Injectable powders are preparations which are uniformly dispersible in water and contain surfactants of the ionic and / or nonionic type (wetting agents, dispersants) in addition to the active ingredient except a diluent or inert substance.
- surfactants of the ionic and / or nonionic type wetting agents, dispersants
- the herbicidal active ingredients are finely ground, for example, in conventional apparatus such as hammer mills, blower mills and air-jet mills and simultaneously or subsequently with the
- Emulsifiable concentrates are made by dissolving the active ingredient in one
- organic solvents e.g. Butanol, cyclohexanone, dimethylformamide, xylene or else higher-boiling aromatics or hydrocarbons or mixtures of the organic solvents with the addition of one or more ionic and / or nonionic surfactants (emulsifiers).
- emulsifiers are: alkylarylsulfonic acid calcium salts such as calcium dodecylbenzenesulfonate or nonionic emulsifiers such as
- Fatty acid polyglycol esters alkylaryl polyglycol ethers, fatty alcohol polyglycol ethers, Propylene oxide-ethylene oxide condensation products, alkyl polyethers, sorbitan esters such as sorbitan fatty acid esters or Polyoxethylensorbitanester such as
- Dusts are obtained by milling the active ingredient with finely divided solids, e.g. Talc, natural clays such as kaolin, bentonite and pyrophyllite, or diatomaceous earth.
- finely divided solids e.g. Talc, natural clays such as kaolin, bentonite and pyrophyllite, or diatomaceous earth.
- Suspension concentrates may be water or oil based. They can be prepared, for example, by wet grinding using commercially available bead mills and, if appropriate, addition of surfactants, as described, for example, in US Pat. upstairs with the others
- Emulsions e.g. Oil-in-water emulsions (EW) can be prepared, for example, by means of stirrers, colloid mills and / or static mixers using aqueous organic solvents and optionally surfactants, as described e.g. listed above for the other formulation types.
- EW Oil-in-water emulsions
- Granules can be prepared either by spraying the active ingredient on adsorptive, granulated inert material or by applying
- Active substance concentrates by means of adhesives, e.g. Polyvinyl alcohol, polyacrylic acid sodium or mineral oils, on the surface of carriers such as sand, kaolinites or granulated inert material. It is also possible to granulate suitable active ingredients in the manner customary for the production of fertilizer granules, if desired in admixture with fertilizers.
- adhesives e.g. Polyvinyl alcohol, polyacrylic acid sodium or mineral oils
- carriers such as sand, kaolinites or granulated inert material. It is also possible to granulate suitable active ingredients in the manner customary for the production of fertilizer granules, if desired in admixture with fertilizers.
- Water-dispersible granules are generally prepared by the usual methods such as spray drying, fluidized bed granulation, plate granulation, mixing with high-speed mixers and extrusion without solid inert material.
- the agrochemical preparations generally contain from 0.1 to 99% by weight, in particular from 0.1 to 95% by weight, of compounds according to the invention.
- the drug concentration is e.g. about 10 to 90 wt .-%, the balance to 100 wt .-% consists of conventional formulation ingredients.
- the active ingredient concentration may be about 1 to 90, preferably 5 to 80 wt .-%.
- Dust-like formulations contain 1 to 30 wt .-% of active ingredient, preferably usually 5 to 20 wt .-% of active ingredient, sprayable solutions contain about 0.05 to 80, preferably 2 to 50 wt .-% of active ingredient.
- the active ingredient content depends, in part, on whether the active compound is liquid or solid and which
- Granulation aids, fillers, etc. are used. In the water
- the content of active ingredient is for example between 1 and 95 wt .-%, preferably between 10 and 80 wt .-%.
- the active substance formulations mentioned optionally contain the customary adhesion, wetting, dispersing, emulsifying, penetrating, preserving, antifreeze and solvent, fillers, carriers and dyes, antifoams,
- Fungicides as well as with safeners, fertilizers and / or growth regulators, e.g. in the form of a ready-made formulation or as a tank mix.
- acetolactate synthase As a combination partner for the compounds of the invention in Mixture formulations or in the tank mix are, for example, known active ingredients which are based on inhibition of, for example, acetolactate synthase, acetyl-CoA carboxylase, cellulose synthase, enolpyruvylshikimate-3-phosphate synthase, glutamine synthetase, p-hydroxyphenylpyruvate dioxygenase, phytoene desaturase , Photosystem I 1 photosystem II, protoporphyrinogen oxidase, can be used, as described, for example, in Weed Research 26 (1986) 441-445 or "The Pesticide Manual", 14th edition, The British Crop Protection Council and the Royal Soc. of Chemistry, 2003 and cited therein.
- Known herbicides or plant growth regulators which can be combined with the compounds according to the invention are, for example, the following active substances (which
- Flucetosulfuron Fluchloralin, Flufenacet (Thiafluamide), Flufenpyr, Flufenpyr-ethyl, Flumetralin, Flumetsulam, Flumiclorac, Flumiclorac-pentyl, Flumioxazin,
- Methylisothiocyanate metobenzuron, metobenzuron, metobromuron, metolachlor, S-metolachlor, metosulam, metoxuron, metribuzin, metsulfuron, metsulfuron-methyl, molinates, monalides, monocarbamides, monocarbamide dihydrogen sulfate,
- Nonanoic acid pendimethalin, pendalkin, penoxsulam, pentanochlor, pentoxazone, perfluidone, pethoxamide, phenisopham, phenmedipham, phenmediphamethyl, picloram, picolinafen, pinoxaden, piperophos, pirifenop, pirifenoputyl, pretilachlor, primisulfuron, primisulfuron-methyl, probenazoles, Profluazole, Procyazine,
- the formulations present in commercially available form are optionally diluted in the customary manner, for example in the case of wettable powders, emulsifiable concentrates, dispersions and water-dispersible granules by means of water. Dusty preparations, ground or spreading granules and sprayable
- herbicides used i.a. varies the required application rate of
- Step 2 Synthesis of 2- (3-Fluoro-4- (trifluoromethyl) phenyl) -4,4-dimethyl-4,5-dihydro-1,3-oxazole
- Step 3 Synthesis of 2- (3-Fluoro-2-methyl-4- (trifluoromethyl) phenyl) -4,4-dimethyl-4,5-dihydro-1,3-oxazole
- Step 4 Synthesis of N- (3- (4,4-dimethyl-4,5-dihydro-1,3-oxazol-2-yl) -2-methyl-6- (trifluoromethyl) phenyl) formamide
- Step 7 Synthesis of 1- (3-amino-2-methyl-4- (trifluoromethyl) phenyl) -3-cyclopropylpropane-1,3-dione
- Step 8 Synthesis of 1- (3-amino-2-methyl-4- (trifluoromethyl) phenyl) -3-cyclopropyl-2 - [(dimethylamino) methylene] propane-1,3-dione
- Step 9 Synthesis of 4- (3-amino-2-methyl-4- (trifluoromethyl) benzoyl) -5-cyclopropylisoxazole
- the aqueous phase was extracted once with EA, and the combined organic phases were washed once with 1 M hydrochloric acid, dried and freed from the solvent. Finally, the crude product was purified by chromatography to yield 80 mg of the product having a purity of about 90% by weight.
- Step 10 Synthesis of 2- (3-amino-2-methyl-4- (trifluoromethyl) benzoyl) -3-cyclopropyl-3-oxo-propanenitrile (# 3)
- a dusting agent is obtained by mixing 10 parts by weight of a compound of the formula (I) and / or salts thereof and 90 parts by weight of talc as an inert material and comminuting in a hammer mill.
- a wettable powder readily dispersible in water is obtained by reacting 25 parts by weight of a compound of the formula (I) and / or its salts, 64 parts by weight of kaolin-containing quartz as inert material, 10 parts by weight
- a dispersion concentrate readily dispersible in water is obtained by reacting 20 parts by weight of a compound of the formula (I) and / or salts thereof with 6 parts by weight of alkylphenol polyglycol ether ( ⁇ Triton X 207), 3
- Nonylphenol as emulsifier e) A water-dispersible granules are obtained by
- a water-dispersible granule is also obtained by adding 25 parts by weight of a compound of formula (I) and / or salts thereof, 5 parts by weight of sodium 2,2'-dinaphthylmethane-6,6'-disulfonate
- the compounds according to the invention formulated in the form of wettable powders (WP) or as emulsion concentrates (EC) are then treated as aqueous
- the compounds Nos. 1, 3 and 25 at an application rate of 80 g / ha each have an at least 90% activity against Amaranthus retroflexus, Echinochloa crus galli and Veronica persica. 2. Herbicidal action against harmful plants in postemergence
- WP wettable powders
- EC emulsion concentrates
- Formulated compounds of the invention are then as aqueous
Abstract
Es werden 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile der allgemeinen Formel (I) als Herbizide beschrieben. In dieser Formel (I) stehen X und Y für organische Reste wie Alkyl und andere Reste wie Halogen, Nitro und Cyano.
Description
Beschreibung 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre Verwendung als Herbizide
Die Erfindung betrifft das technische Gebiet der Herbizide, insbesondere das der Herbizide zur selektiven Bekämpfung von Unkräutern und Ungräsern in
Nutzpflanzenkulturen.
Aus verschiedenen Schriften ist bereits bekannt, daß bestimmte 2-Benzoyl-3- oxopropannitrile herbizide Eigenschaften besitzen. So werden in EP 213 892, WO 97/28136 und EP 625 505 2-Benzoyl-3-oxopropannitrile beschrieben, die am Phenylring durch verschiedene Reste substituiert sind.
Die aus diesen Schriften bekannten Verbindungen zeigen jedoch häufig eine nicht ausreichende herbizide Wirksamkeit. Aufgabe der vorliegenden Erfindung ist daher die Bereitstellung von herbizid wirksamen Verbindungen mit - gegenüber den aus dem Stand der Technik bekannten Verbindungen - verbesserten herbiziden
Eigenschaften.
Es wurde nun gefunden, daß 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannithle als Herbizide besonders gut geeignet sind.
Ein Gegenstand der vorliegenden Erfindung sind 2-(3-Aminobenzoyl)-3-cyclopropyl- 3-oxopropannitrile der Formel (I) oder deren Salze
worin
X und Y bedeuten unabhängig voneinander Nitro, Halogen, Cyano, Rhodano, (CrC6)-Alkyl, (d-C6)-Halogenalkyl, (C2-C6)-Alkenyl, (C2-C6)-Halogenalkenyl, (C2- C6)-Alkinyl, (C3-C6)-Halogenalkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Halogencycloalkyl, (C3-C6)-Cycloalkyl-(C1-C6)-alkyl, (C3-C6)-Halogencycloalkyl-(CrC6)-alkyl, COR1, OR1, OCOR1, OSO2R2, S(O)nR2, SO2OR1, SO2N(R1)2l NR1SO2R2, NR1COR1, (d- C6)-Alkyl-S(O)nR2, (d-C6)-Alkyl-OR1, (d-C6)-Alkyl-OCOR1, (Ci-C6)-Alkyl-OSO2R2, (d-C6)-Alkyl-COOR1, (CrC6)-Alkyl-SO2OR1, (d-C6)-Alkyl-CON(R1)2, (d-C6)-Alkyl- SO2N(R1)2, (d-C6)-Alkyl-NR1COR1 oder (d-C6)-Alkyl-NR1SO2R2,
R1 bedeutet Wasserstoff, (CrC6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)- Cycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, Phenyl oder Phenyl-(d-C6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Cyano, Halogen, Nitro, Rhodano, OR3, S(O)nR4, N(R3)2, NR3OR3, COR3, OCOR3, SCOR3, NR3COR3, CO2R3, COSR3, CON(R3)2 und (d-C4)-Alkoxy-(C2-C6)- alkoxycarbonyl substituiert sind,
R2 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, Phenyl oder Phenyl-(d-C6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Cyano,
Halogen, Nitro, Rhodano, OR3, S(O)nR4, N(R3)2, NR3OR3, COR3, OCOR3, SCOR3, NR3COR3, CO2R3, COSR3, CON(R3)2 und (d-C4)-Alkoxy-(C2-C6)-alkoxycarbonyl substituiert sind, R3 bedeutet Wasserstoff , (CrC6)-Alkyl, (d-C6)-Haloalkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl,
R4 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl, n bedeutet O, 1 oder 2, s bedeutet 0, 1 , 2 oder 3.
In der Formel (I) und allen nachfolgenden Formeln können Alkylreste mit mehr als zwei Kohlenstoffatomen geradkettig oder verzweigt sein. Alkylreste bedeuten z.B. Methyl, Ethyl, n- oder i-Propyl, n-, i-, t- oder 2-Butyl, Pentyle, Hexyle, wie n-Hexyl, i-Hexyl und 1 ,3-Dimethylbutyl. Halogen steht für Fluor, Chlor, Brom oder lod.
Ist eine Gruppe mehrfach durch Reste substituiert, so ist darunter zu verstehen, daß diese Gruppe durch ein oder mehrere gleiche oder verschiedene der genannten Reste substituiert ist.
Die Verbindungen der allgemeinen Formel (I) können je nach Art und Verknüpfung der Substituenten als Stereoisomere vorliegen. Sind beispielsweise ein oder mehrere asymmetrisch substituierte Kohlenstoffatome vorhanden, so können Enantiomere und Diastereomere auftreten. Ebenso treten Stereoisomere auf, wenn n für 1 steht (Sulfoxide). Stereoisomere lassen sich aus den bei der Herstellung anfallenden Gemischen nach üblichen Trennmethoden, beispielsweise durch chromatographische Trennverfahren, erhalten. Ebenso können Stereoisomere durch Einsatz stereoselektiver Reaktionen unter Verwendung optisch aktiver Ausgangs- und/oder Hilfsstoffe selektiv hergestellt werden. Die Erfindung betrifft auch alle Ste- reoisomeren und deren Gemische, die von der allgemeinen Formel (I) umfasst, jedoch nicht spezifisch definiert sind.
Die Verbindungen der allgemeinen Formel (I) liegen in Abhängigkeit von äußeren Bedingungen, wie Druck, Temperatur, pH-Wert und Lösungsmittel, in verschiedenen tautomeren Strukturen vor, die durch die oben genannte Formel (I) umfasst sein sollen:
Bevorzugt sind Verbindungen der allgemeinen Formel (I), worin
X und Y bedeuten unabhängig voneinander Nitro, Halogen, Cyano, (CrC6)- Alkyl, (Ci-C6)-Halogenalkyl, (C2-C6)-Alkenyl, (C2-C6)-Halogenalkenyl, (C2-C6)-Alkinyl, (C3-C6)-Halogenalkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Halogencycloalkyl, (C3-C6)- Cycloalkyl-(CrC6)-alkyl, (C3-C6)-Halogencycloalkyl-(C1-C6)-alkyl, COR1, OR1, OCOR1, OSO2R2, S(O)nR2, SO2OR1, (Ci-C6)-Alkyl-S(O)nR2, (CrC6)-Alkyl-OR1, (C1- C6)-Alkyl-OCOR1, (CrC6)-Alkyl-OSO2R2, (Ci-C6)-Alkyl-COOR1, (Ci-C6)-Alkyl- SO2OR1, (Ci-C6)-Alkyl-CON(R1)2 oder (CrC6)-Alkyl-NR1SO2R2,
R1 bedeutet Wasserstoff, (CrC6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)- Cycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, Phenyl oder Phenyl-(CrC6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Halogen und OR3 substituiert sind,
R2 bedeutet (Ci-C6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Cycloalkyl-(C1-C6)-alkyl, Phenyl oder Phenyl-(Ci-C6)-alkyl, wobei diese vorstehend genannten Reste durch s Reste aus der Gruppe bestehend aus Cyano, Halogen und OR3 substituiert sind,
R3 bedeutet Wasserstoff , (CrC6)-Alkyl, (CrC6)-Haloalkyl, (C2-Ce)-Al kenyl oder (C2-C6)-Alkinyl,
R4 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl, n bedeutet 0, 1 oder 2, s bedeutet 0, 1 , 2 oder 3.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel (I), worin
X bedeutet Nitro, Fluor, Chlor, Brom, lod, Cyano, Methyl, Ethyl, Methoxy, Ethoxy, Trifluormethyl, Methylsulfonyl, Ethylsulfonyl, Methylsulfenylmethyl,
Methylsulfinylmethyl, Methylsulfonylmethyl, Y bedeutet Nitro, Fluor, Chlor, Brom, lod, Cyano, Methoxy, Ethoxy,
Trifluormethyl, Methylsulfonyl, Ethylsulfonyl.
In allen nachfolgend genannten Formeln haben die Substituenten und Symbole, sofern nicht anders definiert, dieselbe Bedeutung wie unter Formel (I) beschrieben.
Erfindungsgemäße Verbindungen können beispielsweise nach dem in Schema 1 angegebenen und grundsätzlich aus EP 0 625 505 A1 bekannten Verfahren durch Reaktion eines Säurechlorids der Formel (III) mit einem beta-Ketonitril der Formel (M) in einem geeigneten Lösungsmittel, wie Acetonitril, unter Katalyse einer Base, wie Triethylamin, sowie in einem zweiten Schritt unter Katalyse von Cyanid hergestellt werden.
Schema 1
(II) (III) (I)
Erfindungsgemäße Verbindungen können auch beispielsweise nach dem in Schema 2 angegebenen Verfahren durch basenkatalysierte Ringöffnung aus Isoxazolen (IV) hergestellt werden. Die Isoxazole (II) können aus den entsprechenden
Benzoesäuren (lila) synthetisiert werden. Solche Synthesen werden in EP 0 625 505 A1 beschrieben. Die Herstellung der Benzoesäuren (lila) sowie der zugehörigen Säurechloride (IM) ist beispielsweise in WO 94/14782, WO 95/16678 und
WO95/31446 beschrieben.
(lila) (IV) (I)
Kollektionen aus Verbindungen der Formel (I) und/oder deren Salzen, die nach den oben genannten Reaktionen synthetisiert werden können, können auch in
parallelisierter Weise hergestellt werden, wobei dies in manueller, teilweise automatisierter oder vollständig automatisierter Weise geschehen kann. Dabei ist es beispielsweise möglich, die Reaktionsdurchführung, die Aufarbeitung oder die Reinigung der Produkte bzw. Zwischenstufen zu automatisieren. Insgesamt wird hierunter eine Vorgehensweise verstanden, wie sie beispielsweise durch D. Tiebes in Combinatorial Chemistry - Synthesis, Analysis, Screening (Herausgeber Günther Jung), Verlag Wiley 1999, auf den Seiten 1 bis 34 beschrieben ist.
Zur parallelisierten Reaktionsdurchführung und Aufarbeitung können eine Reihe von im Handel erhältlichen Geräten verwendet werden, beispielsweise Calpyso- Reaktionsblöcke (Caylpso reaction blocks) der Firma Barnstead International, Dubuque, Iowa 52004-0797, USA oder Reaktionsstationen (reaction stations) der Firma Radleys, Shirehill, Saffron Waiden, Essex, CB 11 3AZ, England oder
MultiPROBE Automated Workstations der Firma Perkin Elmar, Waltham,
Massachusetts 02451 , USA. Für die parallelisierte Aufreinigung von Verbindungen der allgemeinen Formel (I) und deren Salzen beziehungsweise von bei der
Herstellung anfallenden Zwischenprodukten stehen unter anderem
Chromatographieapparaturen zur Verfügung, beispielsweise der Firma ISCO, Inc., 4700 Superior Street, Lincoln, NE 68504, USA.
Die aufgeführten Apparaturen führen zu einer modularen Vorgehensweise, bei der die einzelnen Arbeitsschritte automatisiert sind, zwischen den Arbeitsschritten jedoch manuelle Operationen durchgeführt werden müssen. Dies kann durch den Einsatz von teilweise oder vollständig integrierten Automationssystemen umgangen werden, bei denen die jeweiligen Automationsmodule beispielsweise durch Roboter bedient werden. Derartige Automationssysteme können zum Beispiel von der Firma Caliper, Hopkinton, MA 01748, USA bezogen werden.
Die Durchführung einzelner oder mehrerer Syntheseschritte kann durch den Einsatz von Polymer-supported reagents/Scavanger-Harze unterstützt werden. In der Fachliteratur sind eine Reihe von Versuchsprotokollen beschrieben, beispielsweise in ChemFiles, Vol. 4, No. 1 , Polymer-Supported Scavengers and Reagents for Solution-Phase Synthesis (Sigma-Aldrich).
Neben den hier beschriebenen Methoden kann die Herstellung von Verbindungen der allgemeinen Formel (I) und deren Salzen vollständig oder partiell durch
Festphasen unterstützte Methoden erfolgen. Zu diesem Zweck werden einzelne Zwischenstufen oder alle Zwischenstufen der Synthese oder einer für die
entsprechende Vorgehensweise angepassten Synthese an ein Syntheseharz gebunden. Festphasen- unterstützte Synthesemethoden sind in der Fachliteratur
hinreichend beschrieben, z.B. Barry A. Bunin in "The Combinatorial Index", Verlag Academic Press, 1998 und Combinatorial Chemistry - Synthesis, Analysis,
Screening (Herausgeber Günther Jung), Verlag Wiley, 1999. Die Verwendung von Festphasen- unterstützten Synthesemethoden erlaubt eine Reihe von
literaturbekannten Protokollen, die wiederum manuell oder automatisiert ausgeführt werden können. Die Reaktionen können beispielsweise mittels IRORI-Technologie in Mikroreaktoren (microreactors) der Firma Nexus Biosystems, 12140 Community Road, Poway, CA92064, USA durchgeführt werden. Sowohl an fester als auch in flüssiger Phase kann die Durchführung einzelner oder mehrerer Syntheseschritte durch den Einsatz der Mikrowellen-Technologie unterstützt werden. In der Fachliteratur sind eine Reihe von Versuchsprotokollen beschrieben, beispielsweise in Microwaves in Organic and Medicinal Chemistry (Herausgeber C. O. Kappe und a. Stadler), Verlag Wiley, 2005.
Die Herstellung gemäß der hier beschriebenen Verfahren liefert Verbindungen der Formel (I) und deren Salze in Form von Substanzkollektionen, die Bibliotheken genannt werden. Gegenstand der vorliegenden Erfindung sind auch Bibliotheken, die mindestens zwei Verbindungen der Formel (I) und deren Salzen enthalten.
Die erfindungsgemäßen Verbindungen der Formel (I) (und/oder deren Salze), im folgenden zusammen als„erfindungsgemäße Verbindungen" bezeichnet, weisen eine ausgezeichnete herbizide Wirksamkeit gegen ein breites Spektrum
wirtschaftlich wichtiger mono- und dikotyler annueller Schadpflanzen auf. Auch schwer bekämpfbare perennierende Schadpflanzen, die aus Rhizomen,
Wurzelstöcken oder anderen Dauerorganen austreiben, werden durch die Wirkstoffe gut erfaßt.
Gegenstand der vorliegenden Erfindung ist daher auch ein Verfahren zur
Bekämpfung von unerwünschten Pflanzen oder zur Wachstumsregulierung von Pflanzen, vorzugsweise in Pflanzenkulturen, worin eine oder mehrere
erfindungsgemäße Verbindung(en) auf die Pflanzen (z.B. Schadpflanzen wie mono-
oder dikotyle Unkräuter oder unerwünschte Kulturpflanzen), das Saatgut (z.B.
Körner, Samen oder vegetative Vermehrungsorgane wie Knollen oder Sprossteile mit Knospen) oder die Fläche, auf der die Pflanzen wachsen (z.B. die Anbaufläche), ausgebracht werden. Dabei können die erfindungsgemäßen Verbindungen z.B. im Vorsaat- (ggf. auch durch Einarbeitung in den Boden), Vorauflauf- oder
Nachauflaufverfahren ausgebracht werden. Im einzelnen seien beispielhaft einige Vertreter der mono- und dikotylen Unkrautflora genannt, die durch die
erfindungsgemäßen Verbindungen kontrolliert werden können, ohne dass durch die Nennung eine Beschränkung auf bestimmte Arten erfolgen soll.
Monokotyle Schadpflanzen der Gattungen: Aegilops, Agropyron, Agrostis,
Alopecurus, Apera, Avena, Brachiaria, Bromus, Cenchrus, Commelina, Cynodon, Cyperus, Dactyloctenium, Digitaria, Echinochloa, Eleocharis, Eleusine, Eragrostis, Eriochloa, Festuca, Fimbristylis, Heteranthera, Imperata, Ischaemum, Leptochloa, Lolium, Monochoria, Panicum, Paspalum, Phalaris, Phleum, Poa, Rottboellia, Sagittaria, Scirpus, Setaria, Sorghum.
Dikotyle Unkräuter der Gattungen: Abutilon, Amaranthus, Ambrosia, Anoda,
Anthemis, Aphanes, Artemisia, Atriplex, BeIMs, Bidens, Capsella, Carduus, Cassia, Centaurea, Chenopodium, Cirsium, Convolvulus, Datura, Desmodium, Emex,
Erysimum, Euphorbia, Galeopsis, Galinsoga, Galium, Hibiscus, Ipomoea, Kochia, Lamium, Lepidium, Lindernia, Matricaria, Mentha, Mercurialis, Mullugo, Myosotis, Papaver, Pharbitis, Plantago, Polygonum, Portulaca, Ranunculus, Raphanus, Rorippa, Rotala, Rumex, Salsola, Senecio, Sesbania, Sida, Sinapis, Solanum, Sonchus, Sphenoclea, Stellaria, Taraxacum, Thlaspi, Trifolium, Urtica, Veronica, Viola, Xanthium.
Werden die erfindungsgemäßen Verbindungen vor dem Keimen auf die
Erdoberfläche appliziert, so wird entweder das Auflaufen der Unkrautkeimlinge vollständig verhindert oder die Unkräuter wachsen bis zum Keimblattstadium heran, stellen jedoch dann ihr Wachstum ein und sterben schließlich nach Ablauf von drei bis vier Wochen vollkommen ab.
Bei Applikation der Wirkstoffe auf die grünen Pflanzenteile im Nachauflaufverfahren tritt nach der Behandlung Wachstumsstop ein und die Schadpflanzen bleiben in dem zum Applikationszeitpunkt vorhandenen Wachstumsstadium stehen oder sterben nach einer gewissen Zeit ganz ab, so dass auf diese Weise eine für die
Kulturpflanzen schädliche Unkrautkonkurrenz sehr früh und nachhaltig beseitigt wird.
Obgleich die erfindungsgemäßen Verbindungen eine ausgezeichnete herbizide Aktivität gegenüber mono- und dikotylen Unkräutern aufweisen, werden
Kulturpflanzen wirtschaftlich bedeutender Kulturen z.B. dikotyler Kulturen der
Gattungen Arachis, Beta, Brassica, Cucumis, Cucurbita, Helianthus, Daucus,
Glycine, Gossypium, Ipomoea, Lactuca, Linum, Lycopersicon, Nicotiana, Phaseolus, Pisum, Solanum, Vicia, oder monokotyler Kulturen der Gattungen Allium, Ananas, Asparagus, Avena, Hordeum, Oryza, Panicum, Saccharum, Seeale, Sorghum, Triticale, Triticum, Zea, insbesondere Zea und Triticum, abhängig von der Struktur der jeweiligen erfindungsgemäßen Verbindung und deren Aufwandmenge nur unwesentlich oder gar nicht geschädigt. Die vorliegenden Verbindungen eignen sich aus diesen Gründen sehr gut zur selektiven Bekämpfung von unerwünschtem
Pflanzenwuchs in Pflanzenkulturen wie landwirtschaftlichen Nutzpflanzungen oder Zierpflanzungen.
Darüberhinaus weisen die erfindungsgemäßen Verbindungen (abhängig von ihrer jeweiligen Struktur und der ausgebrachten Aufwandmenge) hervorragende
wachstumsregulatorische Eigenschaften bei Kulturpflanzen auf. Sie greifen regulierend in den pflanzeneigenen Stoffwechsel ein und können damit zur gezielten Beeinflussung von Pflanzeninhaltsstoffen und zur Ernteerleichterung wie z.B. durch Auslösen von Desikkation und Wuchsstauchung eingesetzt werden. Desweiteren eignen sie sich auch zur generellen Steuerung und Hemmung von unerwünschtem vegetativen Wachstum, ohne dabei die Pflanzen abzutöten. Eine Hemmung des vegetativen Wachstums spielt bei vielen mono- und dikotylen Kulturen eine große Rolle, da beispielsweise die Lagerbildung hierdurch verringert oder völlig verhindert werden kann.
Aufgrund ihrer herbiziden und pflanzenwachstumsregulatorischen Eigenschaften können die Wirkstoffe auch zur Bekämpfung von Schadpflanzen in Kulturen von gentechnisch oder durch konventionelle Mutagenese veränderten Pflanzen eingesetzt werden. Die transgenen Pflanzen zeichnen sich in der Regel durch besondere vorteilhafte Eigenschaften aus, beispielsweise durch Resistenzen gegenüber bestimmten Pestiziden, vor allem bestimmten Herbiziden, Resistenzen gegenüber Pflanzenkrankheiten oder Erregern von Pflanzenkrankheiten wie bestimmten Insekten oder Mikroorganismen wie Pilzen, Bakterien oder Viren.
Andere besondere Eigenschaften betreffen z. B. das Erntegut hinsichtlich Menge, Qualität, Lagerfähigkeit, Zusammensetzung und spezieller Inhaltsstoffe. So sind transgene Pflanzen mit erhöhtem Stärkegehalt oder veränderter Qualität der Stärke oder solche mit anderer Fettsäurezusammensetzung des Ernteguts bekannt.
Bevorzugt bezüglich transgener Kulturen ist die Anwendung der erfindungsgemäßen Verbindungen in wirtschaftlich bedeutenden transgenen Kulturen von Nutz- und
Zierpflanzen, z. B. von Getreide wie Weizen, Gerste, Roggen, Hafer, Hirse, Reis und Mais oder auch Kulturen von Zuckerrübe, Baumwolle, Soja, Raps, Kartoffel, Tomate, Erbse und anderen Gemüsesorten.Vorzugsweise können die erfindungsgemäßen Verbindungen als Herbizide in Nutzpflanzenkulturen eingesetzt werden, welche gegenüber den phytotoxischen Wirkungen der Herbizide resistent sind bzw.
gentechnisch resistent gemacht worden sind.
Bevorzugt ist die Anwendung der erfindungsgemäßen Verbindungen oder deren Salze in wirtschaftlich bedeutenden transgenen Kulturen von Nutz-und Zierpflanzen, z. B. von Getreide wie Weizen, Gerste, Roggen, Hafer, Hirse, Reis, Maniok und Mais oder auch Kulturen von Zuckerrübe, Baumwolle, Soja, Raps, Kartoffel, Tomate, Erbse und anderen Gemüsesorten. Vorzugsweise können die erfindungsgemäßen Verbindungen als Herbizide in Nutzpflanzenkulturen eingesetzt werden, welche gegenüber den phytotoxischen Wirkungen der Herbizide resistent sind bzw.
gentechnisch resistent gemacht worden sind.
Herkömmliche Wege zur Herstellung neuer Pflanzen, die im Vergleich zu bisher vorkommenden Pflanzen modifizierte Eigenschaften aufweisen, bestehen
beispielsweise in klassischen Züchtungsverfahren und der Erzeugung von Mutanten. Alternativ können neue Pflanzen mit veränderten Eigenschaften mit Hilfe
gentechnischer Verfahren erzeugt werden (siehe z. B. EP-A-0221044, EP-A- 0131624). Beschrieben wurden beispielsweise in mehreren Fällen
- gentechnische Veränderungen von Kulturpflanzen zwecks Modifikation der in den Pflanzen synthetisierten Stärke (z. B. WO 92/11376, WO 92/14827,
WO 91/19806),
transgene Kulturpflanzen, welche gegen bestimmte Herbizide vom Typ
Glufosinate (vgl. z. B. EP-A-0242236, EP-A-242246) oder Glyphosate
(WO 92/00377) oder der Sulfonylharnstoffe (EP-A-0257993, US-A-5013659) resistent sind,
transgene Kulturpflanzen, beispielsweise Baumwolle, mit der Fähigkeit
Bacillus thuringiensis-Toxine (Bt-Toxine) zu produzieren, welche die
Pflanzen gegen bestimmte Schädlinge resistent machen (EP-A-0142924, EP-A-0193259).
transgene Kulturpflanzen mit modifizierter Fettsäurezusammensetzung (WO
91/13972).
gentechnisch veränderte Kulturpflanzen mit neuen Inhalts- oder
Sekundärstoffen z. B. neuen Phytoalexinen, die eine erhöhte
Krankheitsresistenz verursachen (EPA 309862, EPA0464461 )
gentechnisch veränderte Pflanzen mit reduzierter Photorespiration, die höhere Erträge und höhere Stresstoleranz aufweisen (EPA 0305398).
Transgene Kulturpflanzen, die pharmazeutisch oder diagnostisch wichtige
Proteine produzieren („molecular pharming")
- transgene Kulturpflanzen, die sich durch höhere Erträge oder bessere
Qualität auszeichnen
transgene Kulturpflanzen die sich durch eine Kombinationen z. B. der o. g. neuen Eigenschaften auszeichnen („gene stacking") Zahlreiche molekularbiologische Techniken, mit denen neue transgene Pflanzen mit veränderten Eigenschaften hergestellt werden können, sind im Prinzip bekannt;
siehe z. B. I. Potrykus und G. Spangenberg (eds.) Gene Transfer to Plants, Springer
Lab Manual (1995), Springer Verlag Berlin, Heidelberg, oder Christou, "Trends in Plant Science" 1 (1996) 423-431).
Für derartige gentechnische Manipulationen können Nucleinsäuremoleküle in Plasmide eingebracht werden, die eine Mutagenese oder eine Sequenzveränderung durch Rekombination von DNA-Sequenzen erlauben. Mit Hilfe von
Standardverfahren können z. B. Basenaustausche vorgenommen, Teilsequenzen entfernt oder natürliche oder synthetische Sequenzen hinzugefügt werden. Für die Verbindung der DNA-Fragmente untereinander können an die Fragmente Adaptoren oder Linker angesetzt werden, siehe z. B. Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2. Aufl. CoId Spring Harbor Laboratory Press, CoId Spring Harbor, NY; oder Winnacker "Gene und Klone", VCH Weinheim 2. Auflage 1996
Die Herstellung von Pflanzenzellen mit einer verringerten Aktivität eines
Genprodukts kann beispielsweise erzielt werden durch die Expression mindestens einer entsprechenden antisense-RNA, einer sense-RNA zur Erzielung eines
Cosuppressionseffektes oder die Expression mindestens eines entsprechend konstruierten Ribozyms, das spezifisch Transkripte des obengenannten
Genprodukts spaltet. Hierzu können zum einen DNA-Moleküle verwendet werden, die die gesamte codierende Sequenz eines Genprodukts einschließlich eventuell vorhandener flankierender Sequenzen umfassen, als auch DNA-Moleküle, die nur Teile der codierenden Sequenz umfassen, wobei diese Teile lang genug sein müssen, um in den Zellen einen antisense-Effekt zu bewirken. Möglich ist auch die Verwendung von DNA-Sequenzen, die einen hohen Grad an Homologie zu den codiereden Sequenzen eines Genprodukts aufweisen, aber nicht vollkommen identisch sind.
Bei der Expression von Nucleinsäuremolekülen in Pflanzen kann das synthetisierte Protein in jedem beliebigen Kompartiment der pflanzlichen Zelle lokalisiert sein. Um aber die Lokalisation in einem bestimmten Kompartiment zu erreichen, kann z. B. die codierende Region mit DNA-Sequenzen verknüpft werden, die die Lokalisierung in einem bestimmten Kompartiment gewährleisten. Derartige Sequenzen sind dem
Fachmann bekannt (siehe beispielsweise Braun et al., EMBO J. 11 (1992), 3219- 3227; Wolter et al., Proc. Natl. Acad. Sei. USA 85 (1988), 846-850; Sonnewald et al., Plant J. 1 (1991), 95-106). Die Expression der Nukleinsäuremoleküle kann auch in den Organellen der Pflanzenzellen stattfinden.
Die transgenen Pflanzenzellen können nach bekannten Techniken zu ganzen Pflanzen regeneriert werden. Bei den transgenen Pflanzen kann es sich prinzipiell um Pflanzen jeder beliebigen Pflanzenspezies handeln, d.h., sowohl monokotyle als auch dikotyle Pflanzen.
So sind transgene Pflanzen erhältlich, die veränderte Eigenschaften durch
Überexpression, Suppression oder Inhibierung homologer (= natürlicher) Gene oder Gensequenzen oder Expression heterologer (= fremder) Gene oder Gensequenzen aufweisen.
Vorzugsweise können die erfindungsgemäßen Verbindungen in transgenen Kulturen eingesetzt werden, welche gegen Wuchsstoffe, wie z. B. Dicamba oder gegen Herbizide, die essentielle Pflanzenenzyme, z. B. Acetolactatsynthasen (ALS), EPSP Synthasen, Glutaminsynthasen (GS) oder Hydroxyphenylpyruvat Dioxygenasen (HPPD) hemmen, respektive gegen Herbizide aus der Gruppe der
Sulfonylharnstoffe, der Glyphosate, Glufosinate oder Benzoylisoxazole und analogen Wirkstoffe, resistent sind.
Bei der Anwendung der erfindungsgemäßen Wirkstoffe in transgenen Kulturen treten neben den in anderen Kulturen zu beobachtenden Wirkungen gegenüber
Schadpflanzen oftmals Wirkungen auf, die für die Applikation in der jeweiligen transgenen Kultur spezifisch sind, beispielsweise ein verändertes oder speziell erweitertes Unkrautspektrum, das bekämpft werden kann, veränderte
Aufwandmengen, die für die Applikation eingesetzt werden können, vorzugsweise gute Kombinierbarkeit mit den Herbiziden, gegenüber denen die transgene Kultur resistent ist, sowie Beeinflussung von Wuchs und Ertrag der transgenen
Kulturpflanzen.
Gegenstand der Erfindung ist deshalb auch die Verwendung der
erfindungsgemäßen Verbindungen als Herbizide zur Bekämpfung von
Schadpflanzen in transgenen Kulturpflanzen.
Die erfindungsgemäßen Verbindungen können in Form von Spritzpulvern, emulgierbaren Konzentraten, versprühbaren Lösungen, Stäubemitteln oder
Granulaten in den üblichen Zubereitungen angewendet werden. Gegenstand der Erfindung sind deshalb auch herbizide und pflanzenwachstumsregulierende Mittel, welche die erfindungsgemäßen Verbindungen enthalten.
Die erfindungsgemäßen Verbindungen können auf verschiedene Art formuliert werden, je nachdem welche biologischen und/oder chemisch-physikalischen Parameter vorgegeben sind. Als Formulierungsmöglichkeiten kommen
beispielsweise in Frage: Spritzpulver (WP), wasserlösliche Pulver (SP),
wasserlösliche Konzentrate, emulgierbare Konzentrate (EC), Emulsionen (EW), wie Öl-in-Wasser- und Wasser-in-ÖI-Emulsionen, versprühbare Lösungen,
Suspensionskonzentrate (SC), Dispersionen auf Öl- oder Wasserbasis, ölmischbare Lösungen, Kapselsuspensionen (CS), Stäubemittel (DP), Beizmittel, Granulate für die Streu- und Bodenapplikation, Granulate (GR) in Form von Mikro-, Sprüh-, Aufzugs- und Adsorptionsgranulaten, wasserdispergierbare Granulate (WG), wasserlösliche Granulate (SG), ULV-Formulierungen, Mikrokapseln und Wachse. Diese einzelnen Formulierungstypen sind im Prinzip bekannt und werden
beispielsweise beschrieben in: Winnacker-Küchler, "Chemische Technologie", Band 7, C. Hanser Verlag München, 4. Aufl. 1986; Wade van Valkenburg, "Pesticide Formulations", Marcel Dekker, N.Y., 1973; K. Martens, "Spray Drying" Handbook, 3rd Ed. 1979, G. Goodwin Ltd. London.
Die notwendigen Formulierungshilfsmittel wie Inertmaterialien, Tenside,
Lösungsmittel und weitere Zusatzstoffe sind ebenfalls bekannt und werden beispielsweise beschrieben in: Watkins, "Handbook of Insecticide Dust Diluents and Carriers", 2nd Ed., Darland Books, Caldwell N.J., H.v. Olphen, "Introduction to Clay Colloid Chemistry"; 2nd Ed., J. Wiley & Sons, N.Y.; C. Marsden, "Solvente Guide";
2nd Ed., Interscience, N.Y. 1963; McCutcheon's "Detergents and Emulsifiers
Annual", MC Publ. Corp., Ridgewood N.J.; Sisley and Wood, "Encyclopedia of Surface Active Agents", Chem. Publ. Co. Inc., N.Y. 1964; Schönfeldt,
"Grenzflächenaktive Äthylenoxidaddukte", Wiss. Verlagsgesell., Stuttgart 1976;
Winnacker-Küchler, "Chemische Technologie", Band 7, C. Hanser Verlag München, 4. Aufl. 1986.
Auf der Basis dieser Formulierungen lassen sich auch Kombinationen mit anderen Pestizid wirksamen Stoffen, wie z.B. Insektiziden, Akariziden, Herbiziden,
Fungiziden, sowie mit Safenern, Düngemitteln und/oder Wachstumsregulatoren herstellen, z.B. in Form einer Fertigformulierung oder als Tankmix.
Spritzpulver sind in Wasser gleichmäßig dispergierbare Präparate, die neben dem Wirkstoff außer einem Verdünnungs- oder Inertstoff noch Tenside ionischer und/oder nichtionischer Art (Netzmittel, Dispergiermittel), z.B. polyoxyethylierte Alkylphenole, polyoxethylierte Fettalkohole, polyoxethylierte Fettamine,
Fettalkoholpolyglykolethersulfate, Alkansulfonate, Alkylbenzolsulfonate,
ligninsulfonsaures Natrium, 2,2'-dinaphthylmethan-6,6'-disulfonsaures Natrium, dibutylnaphthalin-sulfonsaures Natrium oder auch oleoylmethyltaurinsaures Natrium enthalten. Zur Herstellung der Spritzpulver werden die herbiziden Wirkstoffe beispielsweise in üblichen Apparaturen wie Hammermühlen, Gebläsemühlen und Luftstrahlmühlen feingemahlen und gleichzeitig oder anschließend mit den
Formulierungshilfsmitteln vermischt. Emulgierbare Konzentrate werden durch Auflösen des Wirkstoffes in einem
organischen Lösungsmittel z.B. Butanol, Cyclohexanon, Dimethylformamid, XyIoI oder auch höhersiedenden Aromaten oder Kohlenwasserstoffen oder Mischungen der organischen Lösungsmittel unter Zusatz von einem oder mehreren Tensiden ionischer und/oder nichtionischer Art (Emulgatoren) hergestellt. Als Emulgatoren können beispielsweise verwendet werden: Alkylarylsulfonsaure Calzium-Salze wie Ca-Dodecylbenzolsulfonat oder nichtionische Emulgatoren wie
Fettsäurepolyglykolester, Alkylarylpolyglykolether, Fettalkoholpolyglykolether,
Propylenoxid-Ethylenoxid-Kondensationsprodukte, Alkylpolyether, Sorbitanester wie z.B. Sorbitanfettsäureester oder Polyoxethylensorbitanester wie z.B.
Polyoxyethylensorbitanfettsäureester. Stäubemittel erhält man durch Vermählen des Wirkstoffes mit fein verteilten festen Stoffen, z.B. Talkum, natürlichen Tonen, wie Kaolin, Bentonit und Pyrophyllit, oder Diatomeenerde.
Suspensionskonzentrate können auf Wasser- oder Ölbasis sein. Sie können beispielsweise durch Naß-Vermahlung mittels handelsüblicher Perlmühlen und gegebenenfalls Zusatz von Tensiden, wie sie z.B. oben bei den anderen
Formulierungstypen bereits aufgeführt sind, hergestellt werden.
Emulsionen, z.B. ÖI-in-Wasser-Emulsionen (EW), lassen sich beispielsweise mittels Rührern, Kolloidmühlen und/oder statischen Mischern unter Verwendung von wäßrigen organischen Lösungsmitteln und gegebenenfalls Tensiden, wie sie z.B. oben bei den anderen Formulierungstypen bereits aufgeführt sind, herstellen.
Granulate können entweder durch Verdüsen des Wirkstoffes auf adsorptionsfähiges, granuliertes Inertmaterial hergestellt werden oder durch Aufbringen von
Wirkstoffkonzentraten mittels Klebemitteln, z.B. Polyvinylalkohol, polyacrylsaurem Natrium oder auch Mineralölen, auf die Oberfläche von Trägerstoffen wie Sand, Kaolinite oder von granuliertem Inertmaterial. Auch können geeignete Wirkstoffe in der für die Herstellung von Düngemittelgranulaten üblichen Weise - gewünschtenfalls in Mischung mit Düngemitteln - granuliert werden.
Wasserdispergierbare Granulate werden in der Regel nach den üblichen Verfahren wie Sprühtrocknung, Wirbelbett-Granulierung, Teller-Granulierung, Mischung mit Hochgeschwindigkeitsmischern und Extrusion ohne festes Inertmaterial hergestellt.
Zur Herstellung von Teller-, Fließbett-, Extruder- und Sprühgranulate siehe z.B.
Verfahren in "Spray-Drying Handbook" 3rd ed. 1979, G. Goodwin Ltd., London; J.E.
Browning, "Agglomeration", Chemical and Engineering 1967, Seiten 147 ff; "Perry's Chemical Engineer's Handbook", 5th Ed., McGraw-Hill, New York 1973, S. 8-57.
Für weitere Einzelheiten zur Formulierung von Pflanzenschutzmitteln siehe z.B. G. C. Klingman, "Weed Control as a Science", John Wiley and Sons, Inc., New York,
1961 , Seiten 81-96 und J. D. Freyer, S.A. Evans, "Weed Control Handbook", 5th Ed., Blackwell Scientific Publications, Oxford, 1968, Seiten 101-103.
Die agrochemischen Zubereitungen enthalten in der Regel 0.1 bis 99 Gew.-%, insbesondere 0.1 bis 95 Gew.-%, erfindungsgemäße Verbindungen.
In Spritzpulvern beträgt die Wirkstoffkonzentration z.B. etwa 10 bis 90 Gew.-%, der Rest zu 100 Gew.-% besteht aus üblichen Formulierungsbestandteilen. Bei emulgierbaren Konzentraten kann die Wirkstoffkonzentration etwa 1 bis 90, vorzugsweise 5 bis 80 Gew.-% betragen. Staubförmige Formulierungen enthalten 1 bis 30 Gew.-% Wirkstoff, vorzugsweise meistens 5 bis 20 Gew.-% an Wirkstoff, versprühbare Lösungen enthalten etwa 0.05 bis 80, vorzugsweise 2 bis 50 Gew.-% Wirkstoff. Bei wasserdispergierbaren Granulaten hängt der Wirkstoffgehalt zum Teil davon ab, ob die wirksame Verbindung flüssig oder fest vorliegt und welche
Granulierhilfsmittel, Füllstoffe usw. verwendet werden. Bei den in Wasser
dispergierbaren Granulaten liegt der Gehalt an Wirkstoff beispielsweise zwischen 1 und 95 Gew.-%, vorzugsweise zwischen 10 und 80 Gew.-%.
Daneben enthalten die genannten Wirkstofformulierungen gegebenenfalls die jeweils üblichen Haft-, Netz-, Dispergier-, Emulgier-, Penetrations-, Konservierungs-, Frostschutz- und Lösungsmittel, Füll-, Träger- und Farbstoffe, Entschäumer,
Verdunstungshemmer und den pH-Wert und die Viskosität beeinflussende Mittel.
Auf der Basis dieser Formulierungen lassen sich auch Kombinationen mit anderen Pestizid wirksamen Stoffen, wie z.B. Insektiziden, Akariziden, Herbiziden,
Fungiziden, sowie mit Safenern, Düngemitteln und/oder Wachstumsregulatoren herstellen, z.B. in Form einer Fertigformulierung oder als Tankmix.
Als Kombinationspartner für die erfindungsgemäßen Verbindungen in
Mischungsformulierungen oder im Tank-Mix sind beispielsweise bekannte Wirkstoffe, die auf einer Inhibition von beispielsweise Acetolactat-Synthase, Acetyl- CoA-Carboxylase, Cellulose-Synthase, Enolpyruvylshikimat-3-phosphat-Synthase, Glutamin-Synthetase, p-Hydroxyphenylpyruvat-Dioxygenase, Phytoendesaturase, Photosystem I1 Photosystem II, Protoporphyrinogen-Oxidase beruhen, einsetzbar, wie sie z.B. aus Weed Research 26 (1986) 441-445 oder "The Pesticide Manual", 14th edition, The British Crop Protection Council and the Royal Soc. of Chemistry, 2003 und dort zitierter Literatur beschrieben sind. Als bekannte Herbizide oder Pflanzenwachstumsregulatoren, die mit den erfindungsgemäßen Verbindungen kombiniert werden können, sind z.B. folgende Wirkstoffe zu nennen (die
Verbindungen sind entweder mit dem "common name" nach der International Organization for Standardization (ISO) oder mit dem chemischen Namen oder mit der Codenummer bezeichnet) und umfassen stets sämtliche Anwendungsformen wie Säuren, Salze, Ester und Isomere wie Stereoisomere und optische Isomere. Dabei sind beispielhaft eine und zum Teil auch mehrere Anwendungsformen genannt:
Acetochlor, Acibenzolar, Acibenzolar-S-methyl, Acifluorfen, Acifluorfen-sodium, Aclonifen, Alachlor, Allidochlor, Alloxydim, Alloxydim-sodium, Ametryn,
Amicarbazone, Amidochlor, Amidosulfuron, Aminocyclopyrachlor, Aminopyralid, Amitrole, Ammoniumsulfamat, Ancymidol, Anilofos, Asulam, Atrazine, Azafenidin, Azimsulfuron, Aziprotryn, BAH-043, BAS-140H, BAS-693H, BAS-714H, BAS-762H, BAS-776H, BAS-800H, Beflubutamid, Benazolin, Benazolin-ethyl, Bencarbazone, Benfluralin, Benfuresate, Bensulide, Bensulfuron-methyl, Bentazone, Benzfendizone, Benzobicyclon, Benzofenap, Benzofluor, Benzoylprop, Bicyclopyrone, Bifenox, Bilanafos, Bilanafos-natrium, Bispyribac, Bispyribac-natrium, Bromacil, Bromobutide, Bromofenoxim, Bromoxynil, Bromuron, Buminafos, Busoxinone, Butachlor,
Butafenacil, Butamifos, Butenachlor, Butralin, Butroxydim, Butylate, Cafenstrole, Carbetamide, Carfentrazone, Carfentrazone-ethyl, Chlomethoxyfen, Chloramben, Chlorazifop, Chlorazifop-butyl, Chlorbromuron, Chlorbufam, Chlorfenac, Chlorfenac- natrium, Chlorfenprop, Chlorflurenol, Chlorflurenol-methyl, Chloridazon, Chlorimuron, Chlorimuron-ethyl, Chlormequat-chlorid, Chlornitrofen, Chlorophthalim, Chlorthal- dimethyl, Chlorotoluron, Chlorsulfuron, Cinidon, Cinidon-ethyl, Cinmethylin,
Cinosulfuron, Clethodim, Clodinafop Clodinafop-propargyl, Clofencet, Clomazone, Clomeprop, Cloprop, Clopyralid, Cloransulam, Cloransulam-methyl, Cumyluron, Cyanamide, Cyanazine, Cyclanilide, Cycloate, Cyclosulfamuron, Cycloxydim, Cycluron, Cyhalofop, Cyhalofop-butyl, Cyperquat, Cyprazine, Cyprazole, 2,4-D, 2,4- DB, Daimuron/Dymron, Dalapon, Daminozide, Dazomet, n-Decanol, Desmedipham, Desmetryn, Detosyl-Pyrazolate (DTP), Diallate, Dicamba, Dichlobenil, Dichlorprop, Dichlorprop-P, Diclofop, Diclofop-methyl, Diclofop-P-methyl, Diclosulam, Diethatyl, Diethatyl-ethyl, Difenoxuron, Difenzoquat, Diflufenican, Diflufenzopyr, Diflufenzopyr- natrium, Dimefuron, Dikegulac-sodium, Dimefuron, Dimepiperate, Dimethachlor, Dimethametryn, Dimethenamid, Dimethenamid-P, Dimethipin, Dimetrasulfuron,
Dinitramine, Dinoseb, Dinoterb, Diphenamid, Dipropetryn, Diquat, Diquat-dibromide, Dithiopyr, Diuron, DNOC, Eglinazine-ethyl, Endothal, EPTC, Esprocarb, Ethalfluralin, Ethametsulfuron-methyl, Ethephon, Ethidimuron, Ethiozin, Ethofumesate, Ethoxyfen, Ethoxyfen-ethyl, Ethoxysulfuron, Etobenzanid, F-5331 , d.h. N-[2-Chlor-4-fluor-5-[4- (3fluorpropyl)-4,5-dihydro-5-oxo-1 H-tetrazol-1 -yl]-phenyl]-ethansulfonamid,
Fenoprop, Fenoxaprop, Fenoxaprop-P, Fenoxaprop-ethyl, Fenoxaprop-P-ethyl, Fenoxasulfone, Fentrazamide, Fenuron, Flamprop, Flamprop-M-isopropyl,
Flamprop-M-methyl, Flazasulfuron, Florasulam, Fluazifop, Fluazifop-P, Fluazifop- butyl, Fluazifop-P-butyl, Fluazolate, Flucarbazone, Flucarbazone-sodium,
Flucetosulfuron, Fluchloralin, Flufenacet (Thiafluamide), Flufenpyr, Flufenpyr-ethyl, Flumetralin, Flumetsulam, Flumiclorac, Flumiclorac-pentyl, Flumioxazin,
Flumipropyn, Fluometuron, Fluorodifen, Fluoroglycofen, Fluoroglycofen-ethyl, Flupoxam, Flupropacil, Flupropanate, Flupyrsulfuron, Flupyrsulfuron-methyl-sodium, Flurenol, Flurenol-butyl, Fluridone, Flurochloridone, Fluroxypyr, Fluroxypyr-meptyl, Flurprimidol, Flurtamone, Fluthiacet, Fluthiacet-methyl, Fluthiamide, Fomesafen, Foramsulfuron, Forchlorfenuron, Fosamine, Furyloxyfen, Gibberellinsäure,
Glufosinate, L-Glufosinate, L-Glufosinate-ammonium, Glufosinate-ammonium, Glyphosate, Glyphosate-isopropylammonium, H-9201 , Halosafen, Halosulfuron, Halosulfuron-methyl, Haloxyfop, Haloxyfop-P, Haloxyfop-ethoxyethyl, Haloxyfop-P- ethoxyethyl, Haloxyfop-methyl, Haloxyfop-P-methyl, Hexazinone, HNPC-9908, HOK- 201 , HW-02, Imazamethabenz, Imazamethabenz-methyl, Imazamox, Imazapic, Imazapyr, Imazaquin, Imazethapyr, Imazosulfuron, Inabenfide, Indanofan,
Indaziflam, Indolessigsäure (IAA), 4-lndol-3-ylbuttersäure (IBA), lodosulfuron, lodosulfuron-methyl-natrium, loxynil, Ipfencarbazone.lsocarbamid, Isopropalin, Isoproturon, Isouron, Isoxaben, Isoxachlortole, Isoxaflutole, Isoxapyrifop, IDH-100, KUH-043, KUH-071 , Karbutilate, Ketospiradox, Lactofen, Lenacil, Linuron,
Maleinsäurehydrazid, MCPA, MCPB, MCPB-methyl, -ethyl und -natrium, Mecoprop, Mecoprop-natrium, Mecoprop-butotyl, Mecoprop-P-butotyl, Mecoprop-P- dimethylammonium, Mecoprop-P-2-ethylhexyl, Mecoprop-P-kalium, Mefenacet, Mefluidide, Mepiquat-chlorid, Mesosulfuron, Mesosulfuron-methyl, Mesotrione, Methabenzthiazuron, Metam, Metamifop, Metamitron, Metazachlor, Metazosulfuron, Methazole, Methiozolin, Methoxyphenone, Methyldymron, 1-Methylcyclopropen,
Methylisothiocyanat, Metobenzuron, Metobenzuron, Metobromuron, Metolachlor, S- Metolachlor, Metosulam, Metoxuron, Metribuzin, Metsulfuron, Metsulfuron-methyl, Molinate, Monalide, Monocarbamide, Monocarbamide-dihydrogensulfat,
Monolinuron, Monosulfuron, Monuron, MT 128, MT-5950, d. h. N-[3-Chlor-4-(1- methylethyl)-phenyl]-2-methylpentanamid, NGGC-011 , Naproanilide, Napropamide, Naptalam, NC-310, d.h. 4-(2,4-dichlorobenzoyl)-1-methyl-5-benzyloxypyrazole, Neburon, Nicosulfuron, Nipyraclofen, Nitralin, Nitrofen, Nitrophenolat-natrium
(Isomerengemisch), Nitrofluorfen, Nonansäure, Norflurazon, Orbencarb,
Orthosulfamuron, Oryzalin, Oxadiargyl, Oxadiazon, Oxasulfuron, Oxaziclomefone, Oxyfluorfen, Paclobutrazol, Paraquat, Paraquat-dichlorid, Pelargonsäure
(Nonansäure), Pendimethalin, Pendralin, Penoxsulam, Pentanochlor, Pentoxazone, Perfluidone, Pethoxamid, Phenisopham, Phenmedipham, Phenmedipham-ethyl, Picloram, Picolinafen, Pinoxaden, Piperophos, Pirifenop, Pirifenop-butyl, Pretilachlor, Primisulfuron, Primisulfuron-methyl, Probenazole, Profluazol, Procyazine,
Prodiamine, Prifluraline, Profoxydim, Prohexadione, Prohexadione-calcium,
Prohydrojasmone, Prometon, Prometryn, Propachlor, Propanil, Propaquizafop, Propazine, Propham, Propisochlor, Propoxycarbazone, Propoxycarbazone-natrium, Propyrisulfuron, Propyzamide, Prosulfalin, Prosulfocarb, Prosulfuron, Prynachlor, Pyraclonil, Pyraflufen, Pyraflufen-ethyl, Pyrasulfotole, Pyrazolynate (Pyrazolate), Pyrazosulfuron-ethyl, Pyrazoxyfen, Pyribambenz, Pyribambenz-isopropyl,
Pyribenzoxim, Pyributicarb, Pyridafol, Pyridate, Pyriftalid, Pyriminobac, Pyriminobac- methyl, Pyrimisulfan, Pyrithiobac, Pyrithiobac-natrium, Pyroxasulfone, Pyroxsulam,
Quinclorac, Quinmerac, Quinoclamine, Quizalofop, Quizalofop-ethyl, Quizalofop-P, Quizalofop-P-ethyl, Quizalofop-P-tefuryl, Rimsulfuron, Saflufenacil, Secbumeton, Sethoxydim, Siduron, Simazine, Simetryn, SN-106279, Sulcotrione, Sulfallate (CDEC), Sulfentrazone, Sulfometuron, Sulfometuron-methyl, Sulfosate (Glyphosate- trimesium), Sulfosulfuron, SYN-523, SYP-249, SYP-298, SYP-300, Tebutam, Tebuthiuron, Tecnazene, Tefuryltrione, Tembotrione, Tepraloxydim, Terbacil, Terbucarb, Terbuchlor, Terbumeton, Terbuthylazine, Terbutryn, TH-547,
Thenylchlor, Thiafluamide, Thiazafluron, Thiazopyr, Thidiazimin, Thidiazuron, Thiencarbazone, Thiencarbazone-methyl, Thifensulfuron, Thifensulfuron-methyl, Thiobencarb, Tiocarbazil, Topramezone, Tralkoxydim, Triallate, Triasulfuron, Triaziflam, Triazofenamide, Tribenuron, Tribenuron-methyl, Trichloressigsäure (TCA)1 Triclopyr, Tridiphane, Trietazine, Trifloxysulfuron, Trifloxysulfuron-natrium, Trifluralin, Triflusulfuron, Triflusulfuron-methyl, Trimeturon, Trinexapac, Trinexapac- ethyl, Tritosulfuron, Tsitodef, Uniconazole, Uniconazole-P, Vernolate, ZJ-0166, ZJ- 0270, ZJ-0543, ZJ-0862 sowie die folgenden Verbindungen
Zur Anwendung werden die in handelsüblicher Form vorliegenden Formulierungen gegebenenfalls in üblicher weise verdünnt z.B. bei Spritzpulvern, emulgierbaren Konzentraten, Dispersionen und wasserdispergierbaren Granulaten mittels Wasser. Staubförmige Zubereitungen, Boden- bzw. Streugranulate sowie versprühbare
Lösungen werden vor der Anwendung üblicherweise nicht mehr mit weiteren inerten Stoffen verdünnt.
Mit den äußeren Bedingungen wie Temperatur, Feuchtigkeit, der Art des
verwendeten Herbizids, u.a. variiert die erforderliche Aufwandmenge der
Verbindungen der Formel (I). Sie kann innerhalb weiter Grenzen schwanken, z.B. zwischen 0,001 und 1 ,0 kg/ha oder mehr Aktivsubstanz, vorzugsweise liegt sie jedoch zwischen 0,005 und 750 g/ha. Die nachstehenden Beispiele erläutern die Erfindung.
A. Chemische Beispiele
Herstellung von 2-(3-Amino-2-methyl-4-(trifluormethyl)benzoyl)-3-cyclopropyl-3- oxopropannitril (Tabellenbeispiel Nr. 3) Schritt 1 : Synthese von 3-Fluor-N-(1-hydroxy-2-methylpropan-2-yl)-4-(trifluormethyl)- benzamid
10.0 g (48.0 mmol) 3-Fluor-4-(trifluormethyl)benzoesäure wurden in 40 ml CH2CI2 vorgelegt und mit fünf Tropfen DMF versetzt. 7.93 g (62.4 mmol) Oxalylchlorid wurden langsam bei Raumtemperatur (RT) zugetropft, und das Gemisch nach Ende der Gasabspaltung unter Rückfluss erhitzt bis die Reaktion vollständig war. Das
Gemisch wurde eingeengt, anschließend wurde nochmals mit Toluol nachdestilliert. In einem Temperatur-Bereich von 5 - 25 °C wurde eine Lösung dieses rohen Säurechlorids in 40 ml CH2CI2 zu einer Lösung von 8.57 g (96.1 mmol) 2-Amino-2- methylpropanol in 20ml CH2CI2 zugetropft. Danach wurde das Gemisch 1.5 h im Eisbad gerührt, anschließend taute es über einen Zeitraum von 16 h auf RT auf. Das ausgefallene Hydrochlorid wurde abgetrennt, der Rückstand mit viel CH2CI2 gewaschen, und das Filtrat bis zur Trockene eingeengt. Es wurden 8.40 g des
Produkts mit einer Reinheit von ca. 80 % erhalten. Weiterhin wurde der zu Beginn der Aufarbeitung abgetrennte Rückstand mit Wasser verrührt und erneut filtriert. Als Rückstand wurden zusätzlich 4.60 g sauberes Produkt erhalten. Schritt 2: Synthese von 2-(3-Fluor-4-(trifluormethyl)phenyl)-4,4-dimethyl-4,5-dihydro- 1 ,3-oxazol
9.60 g (85 Gew.-% Reinheit; 29.2 mmol) 3-Fluor-N-(1-hydroxy-2-methylpropan-2-yl)- 4-(trifluormethyl)benzamid wurden in 80 ml CHbCI2 vorgelegt und mit 4.17 g (35.0 mmol) Thionylchlorid versetzt. Das Gemisch wurde bei RT 5 h gerührt und dann zur Aufarbeitung auf Eiswasser gegossen. Der Inhalt wurde mit 1 M Natronlauge alkalisiert, und die wässrige Phase wurde zweimal mit CH2CI2 extrahiert. Die vereinigten organischen Phasen wurden getrocknet und eingeengt. Schließlich wurde das Rohprodukt chromatographisch gereinigt, wobei 5.05 g sauberes Produkt erhalten wurden.
Schritt 3: Synthese von 2-(3-Fluor-2-methyl-4-(trifluormethyl)phenyl)-4,4-dimethyl- 4,5-dihydro-1 ,3-oxazol
30.3 g (116 mmol) 2-[3-Fluor-4-(trifluormethyl)phenyl]-4,4-dimethyl-4,5-dihydro-1 ,3- oxazol wurden unter Schutzgas in 350 ml trockenem THF vorgelegt und auf -70 0C gekühlt. Bei einer Temperatur von -62 0C bis -66 0C wurden langsam 7.80 g (122 mmol) n-Butyllihium als 2.50 M Lösung in Heptan langsam zugetropft. Der Inhalt wurde noch 1.75 h bei ca. -70 0C gerührt. Anschließend wurde eine Lösung von 20.6 g (145 mmol) lodmethan in 50 ml trockenem THF zugetropft. Das Gemisch wurde 30 min. bei ca. -70 0C gerührt, dann wurde es 16 h stehen gelassen, wobei es auf RT auftaute. Zur Aufarbeitung wurde der Inhalt mit 300 ml 1 M Salzsäure bei 10 0C - 15 0C versetzt, und danach wurde Wasser zugegeben. Das Gemisch wurde zweimal mit Diethylether extrahiert, die vereinigten organischen Phasen wurden mit wässriger 10proz. Natriumbisulfitlösung gewaschen, getrocknet und vom
Lösungsmittel befreit. Das Rohprodukt wurde schließlich chromatographisch gereinigt, wobei 9.20 g sauberes Produkt erhalten wurden.
Schritt 4: Synthese von N-(3-(4,4-Dimethyl-4,5-dihydro-1 ,3-oxazol-2-yl)-2-methyl-6- (trifluormethyl)phenyl)formamid
8.51 g (189 mmol) Formamid und 10.6 g (94.5 mmol) Kalium-tert.-butylat wurden in 90 ml N,N-Dimethylacetamid vorgelegt, gerührt und nach 5 min. mit 5.20 g (18.9 mmol) 2-[3-Fluor-2-methyl-4-(trifluormethyl)phenyl]-4,4-dimethyl-4,5-dihydro-1 ,3- oxazol versetzt. Das Gemisch wurde 45 min. auf 140 0C erhitzt und anschließend unter Hochvakuum eingeengt. Der Rückstand wurde mit 400 ml einer 1 M Lösung von HCl in Ethanol versetzt und anschließend eingeengt. Der Rückstand wurde in CH2Cb aufgenommen und filtriert. Der Rückstand wurde mit CH2CI2
nachgewaschen, und das Filtrat wurde anschließend vom Lösungsmittel befreit. Schließlich wurde das Rohprodukt chromatographisch gereinigt, wobei 4.30 g sauberes Produkts erhalten wurden.
Schritt 5: Synthese von 3-Amino-2-methyl-4-(trifluormethyl)benzoesäure
3.90 g (13.0 mmol) N-[3-(4,4-Dimethyl-4,5-dihydro-1 ,3-oxazol-2-yl)-2-methyl-6-
(trifluormethyl)phenyl]formamid wurden mit 80 ml konzentrierter Salzsäure versetzt und unter Rückfluss erhitzt. Nach 4 h wurde das Gemisch abgekühlt, filtriert, der Rückstand wurde mit Wasser nachgewaschen anschließend trocken gesaugt. Als Rückstand wurden 1.40 g sauberes Produkt erhalten. Das Filtrat wurde dreimal mit Essigsäureethylester (EE) extrahiert, die vereinigten organischen Phasen wurden getrocknet und anschließend vom Lösungsmittel befreit. Der Rückstand wurde in wenig 1 M Salzsäure verrührt und filtriert, wobei als Rückstand nochmals 800 mg sauberes Produkt isoliert wurden. Schritt 6: Synthese von tert.-Butyl-2-(3-amino-2-methyl-4-(trifluormethyl)benzoyl)-3- cyclopropyl-3-oxopropanoat
500 mg (2.28 mmol) 3-Amino-2-methyl-4-(trifluormethyl)benzoesäure wurden in 10 ml trockenem Tetra hydrofu ran vorgelegt und im Eisbad auf 0 0C bis 5 0C abgekühlt. Nach Zugabe von 481 mg (2.51 mmol) N-(3-Dimethylaminopropyl)-N'-ethyl- carbodiimid und 339 mg (2.51 mmol) 1-Hydroxybenzotriazol wurde das Gemisch 6 h im Eisbad bei 0 0C bis 5 0C gerührt und anschließend auf RT aufgetaut. Das
Gemisch wurde 16 h bei RT stehen gelassen. Zur Aufarbeitung wurde der Inhalt
filtriert, das Filtrat wurde in einem Folgeschritt weiter umgesetzt. 630 mg (3.42 mmol) tert.-Butyl-S-cyclopropyl-S-oxopropanoat wurden in 10 ml trockenem THF gelöst und vorsichtig mit 137 mg (60 proz.; 3.42 mmol) Natriumhydrid versetzt. Das Gemisch wurde 2 h bei RT gerührt. Danach wurde zu diesem Gemisch bei RT die oben hergestellte Lösung der aktivierten 3-Amino-2-methyl-4-(trifluormethyl)benzoesäure in Tetrahydrofuran zugetropft. Die entstehende Suspension wurde 2 h bei RT gerührt. Zur Aufarbeitung wurde das Lösungsmittel entfernt, der Rückstand wurde in Wasser aufgenommen, der Inhalt wurde mit 1 M Salzsäure angesäuert, und das Gemisch wurde zweimal mit CH2Cb extrahiert. Die vereinigten organischen Phasen wurden vom Lösungsmittel befreit, und der Rückstand (1.40 g) wurde als
Rohprodukt ohne weitere Reinigung direkt für die nächste Synthesestufe eingesetzt.
Schritt 7: Synthese von 1-(3-Amino-2-methyl-4-(trifluormethyl)phenyl)-3-cyclopropyl- propan-1 ,3-dion
1 40 g des in Schritt 6 hergestellten Rohprodukts tert.-Butyl-2-(3-amino-2-methyl-4- (trifluormethyl)benzoyl)-3-cyclopropyl-3-oxopropanoat wurden mit 5.0 ml
Trifluoressigsäure versetzt und dann unter Rückfluss erhitzt. Als eine HPLC-Analyse vollständigen Umsatz anzeigte wurde das Gemisch eingeengt, und der Rückstand wurde chromatographisch gereinigt. Es wurden 300 mg des Produkts mit einer Reinheit von ca. 83 Gew.-% erhalten.
Schritt 8: Synthese von 1-(3-Amino-2-methyl-4-(trifluormethyl)phenyl)-3-cyclopropyl- 2-[(dimethylamino)methylen]propan-1 ,3-dion
340 mg (80 Gew.-% Reinheit; 0.95 mmol) 1-[3-Amino-2-methyl-4- (trifluormethyl)phenyl]-3-cyclopropylpropan-1 ,3-dion wurden mit 3.0 ml N1N-
Dimethylforrnamiddimethylacetal versetzt und 16 h bei RT gerührt. Zur Aufarbeitung wurde zweimal n-Heptan zugegeben und anschließend abdekantiert. Der Rückstand wurde getrocknet. Es wurden 268 mg sauberes Produkt erhalten. Schritt 9: Synthese von 4-(3-Amino-2-methyl-4-(trifluormethyl)benzoyl)-5- cyclopropylisoxazol
268 mg (0.79 mmol) 1-[3-Amino-2-methyl-4-(trifluormethyl)phenyl]-3-cyclopropyl-2- [(dimethylamino)methylen]propan-1 ,3-dion wurden in 25 ml Ethanol gelöst. 66 mg
(0.95 mmol) Hydroxlammoniumchlorid wurden zugegeben, nach 5 min. wurden 77.5 mg (0.95 mmol) Natriumacetat zugegeben. Das Reaktionsgemisch wurde so lange bei RT gerührt, bis eine HPLC-Kontrolle die Vollständigkeit der Umsetzung anzeigte. Der Inhalt wurde vom Lösungsmittel befreit, und der Rückstand wurde in EE und Wasser aufgenommen. Die wässrige Phase wurde einmal mit EE extrahiert, die vereinigten organischen Phasen wurden einmal mit 1 M Salzsäure gewaschen, getrocknet und vom Lösungsmittel befreit. Schließlich wurde das Rohprodukt chromatographisch gereinigt, wobei 80 mg des Produkts mit einer Reinheit von ca. 90 Gew.-% gewonnen wurden.
Schritt 10: Synthese von 2-(3-Amino-2-methyl-4-(trifluormethyl)benzoyl)-3- cyclopropyl-3-oxopropannitril (Nr. 3)
40.0 mg (0.13 mmol) 4-[3-Amino-2-methyl-4-(trifluormethyl)benzoyl]-5- cyclopropylisoxazol wurden in 5 ml Dichlormethan vorgelegt und nach der Zugabe von 26 mg (0.26 mmol) Triethylamin 16 h bei RT gerührt. Zur Aufarbeitung wurden 3 ml 1 M Salzsäure zugegeben, und die organische Phase wurde vom Lösungsmittel befreit. Es wurden 37.8 mg des Produkts mit einer Reinheit von ca. 90 Gew.-% erhalten.
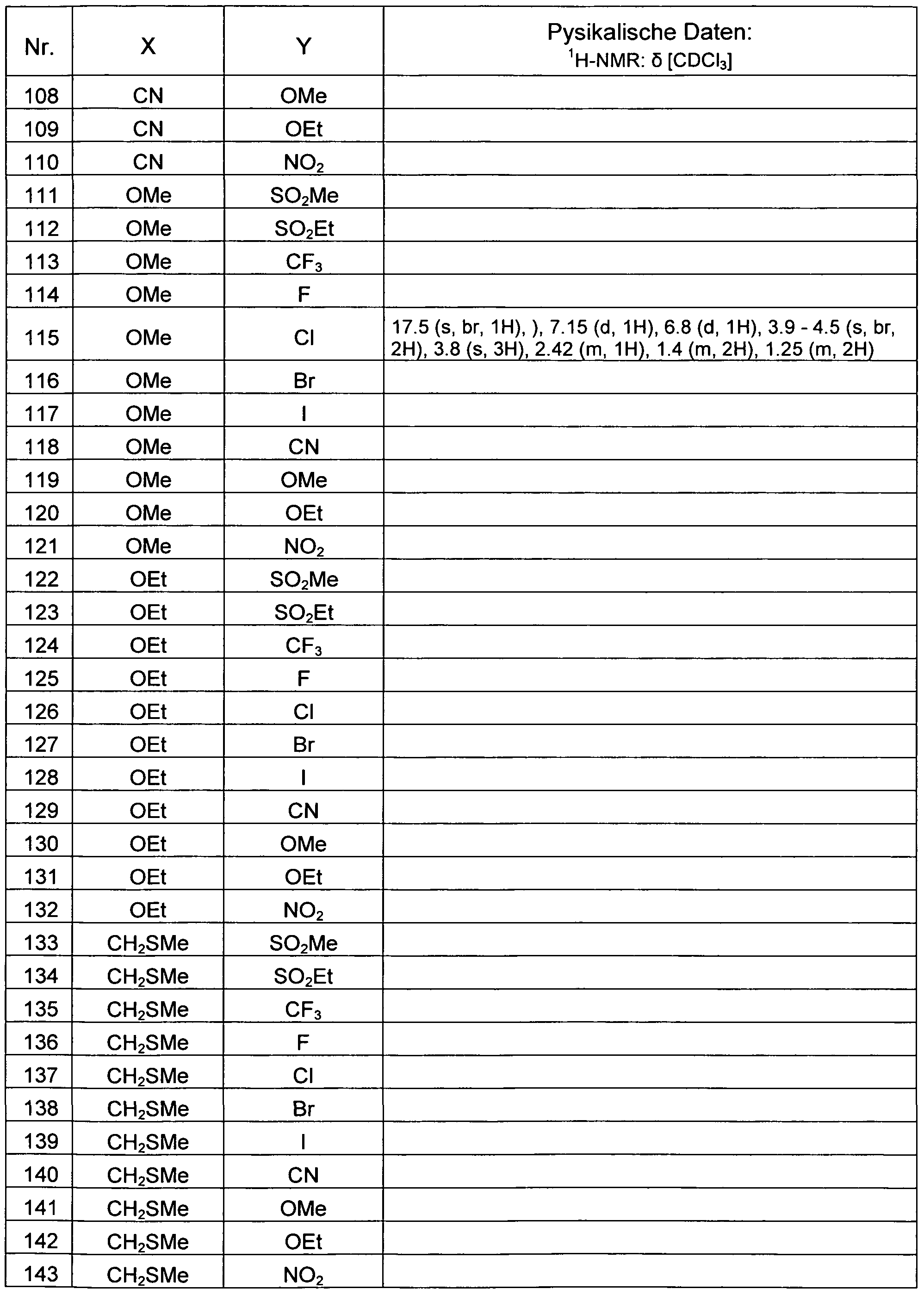
Die in nachfolgenden Tabellen aufgeführten Beispiele wurden analog oben genannten Methoden hergestellt beziehungsweise sind analog oben genannten Methoden erhältlich. Diese Verbindungen sind ganz besonders bevorzugt. Die verwendeten Abkürzungen bedeuten:
Et = Ethyl Me = Methyl
Tabelle: Erfindungsgemäße Verbindungen der allgemeinen Formel (I)
B. Formulierungsbeispiele a) Ein Stäubemittel wird erhalten, indem man 10 Gew. -Teile einer Verbindung der Formel (I) und/oder deren Salze und 90 Gew.-Teile Talkum als Inertstoff mischt und in einer Schlagmühle zerkleinert. b) Ein in Wasser leicht dispergierbares, benetzbares Pulver wird erhalten, indem man 25 Gewichtsteile einer Verbindung der Formel (I) und/oder deren Salze, 64 Gew.-Teile kaolinhaltigen Quarz als Inertstoff, 10 Gewichtsteile
ligninsulfonsaures Kalium und 1 Gew.-Teil oleoylmethyltaurinsaures Natrium als Netz- und Dispergiermittel mischt und in einer Stiftmühle mahlt. c) Ein in Wasser leicht dispergierbares Dispersionskonzentrat wird erhalten, indem man 20 Gew.-Teile einer Verbindung der Formel (I) und/oder deren Salze mit 6 Gew. -Teilen Alkylphenolpolyglykolether (©Triton X 207), 3
Gew.-Teilen Isotridecanolpolyglykolether (8 EO) und 71 Gew.-Teilen paraffinischem Mineralöl (Siedebereich z.B. ca. 255 bis über 277 C) mischt und in einer Reibkugelmühle auf eine Feinheit von unter 5 Mikron vermahlt. d) Ein emulgierbares Konzentrat wird erhalten aus 15 Gew.-Teilen einer
Verbindung der Formel (I) und/oder deren Salze, 75 Gew.-Teilen
Cyclohexanon als Lösungsmittel und 10 Gew.-Teilen oxethyliertes
Nonylphenol als Emulgator. e) Ein in Wasser dispergierbares Granulat wird erhalten indem man
75 Gew.-Teile einer Verbindung der Formel (I) und/oder deren Salze, 10 Gew.-Teile ligninsulfonsaures Calcium,
5 Gew.-Teile Natriumlaurylsulfat,
3 Gew.-Teile Polyvinylalkohol und
7 Gew.-Teile Kaolin
mischt, auf einer Stiftmühle mahlt und das Pulver in einem Wirbelbett durch Aufsprühen von Wasser als Granulierflüssigkeit granuliert.
f) Ein in Wasser dispergierbares Granulat wird auch erhalten, indem man 25 Gew. -Teile einer Verbindung der Formel (I) und/oder deren Salze, 5 Gew.-Teile 2,2'-dinaphthylmethan-6,6'-disulfonsaures Natrium
2 Gew.-Teile oleoylmethyltaurinsaures Natrium,
1 Gew.-Teil Polyvinylalkohol,
17 Gew.-Teile Calciumcarbonat und
50 Gew.-Teile Wasser
auf einer Kolloidmühle homogenisiert und vorzerkleinert, anschließend auf einer Perlmühle mahlt und die so erhaltene Suspension in einem Sprühturm mittels einer Einstoffdüse zerstäubt und trocknet.
C. Biologische Beispiele
1. Herbizide Wirkung gegen Schadpflanzen im Vorauflauf
Samen von mono- bzw. dikotylen Unkraut- bzw. Kulturpflanzen werden in
Holzfasertöpfen in sandiger Lehmerde ausgelegt und mit Erde abgedeckt. Die in Form von benetzbaren Pulvern (WP) oder als Emulsionskonzentrate (EC) formulierten erfindungsgemäßen Verbindungen werden dann als wäßrige
Suspension bzw. Emulsion mit einer Wasseraufwandmenge von umgerechnet 600 bis 800 l/ha unter Zusatz von 0,2% Netzmittel auf die Oberfläche der Abdeckerde appliziert. Nach der Behandlung werden die Töpfe im Gewächshaus aufgestellt und unter guten Wachstumsbedingungen für die Testpflanzen gehalten. Die visuelle Bonitur der Schäden an den Versuchspflanzen erfolgt nach einer Versuchszeit von 3 Wochen im Vergleich zu unbehandelten Kontrollen (herbizide Wirkung in Prozent (%): 100% Wirkung = Pflanzen sind abgestorben, 0 % Wirkung = wie
Kontrollpflanzen). Dabei zeigen beispielsweise die Verbindungen Nr. 1 , 3 sowie 25 bei einer Aufwandmenge von 80 g/ha jeweils eine mindestens 90 %-ige Wirkung gegen Amaranthus retroflexus, Echinochloa crus galli und Veronica persica.
2. Herbizide Wirkung gegen Schadpflanzen im Nachauflauf
Samen von mono- bzw. dikotylen Unkraut- bzw. Kulturpflanzen werden in
Holzfasertöpfen in sandigem Lehmboden ausgelegt, mit Erde abgedeckt und im •*>- Gewächshaus unter guten Wachstumsbedingungen angezogen. 2 bis 3 Wochen nach der Aussaat werden die Versuchspflanzen im Einblattstadium behandelt. Die in Form von benetzbaren Pulvern (WP) oder als Emulsionskonzentrate (EC)
formulierten erfindungsgemäßen Verbindungen werden dann als wäßrige
Suspension bzw. Emulsion mit einer Wasseraufwandmenge von umgerechnet 600 bis 800 l/ha unter Zusatz von 0,2% Netzmittel auf die grünen Pflanzenteile gesprüht. Nach ca. 3 Wochen Standzeit der Versuchspflanzen im Gewächshaus unter optimalen Wachstumsbedingungen wird die Wirkung der Präparate visuell im
Vergleich zu unbehandelten Kontrollen bonitiert (herbizide Wirkung in Prozent (%): 100% Wirkung = Pflanzen sind abgestorben, 0 % Wirkung = wie Kontrollpflanzen). Dabei zeigen beispielsweise die Verbindungen Nr. 1 , 3 sowie 25 bei einer
Aufwandmenge von 80 g/ha jeweils eine mindestens 80 %-ige Wirkung gegen Echinochloa crus galli, Matricaria inodora, Stellaria media und Veronica persica.
Claims
1. 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile der Formel (I) oder deren Salze
X und Y bedeuten unabhängig voneinander Nitro, Halogen, Cyano, Rhodano, (Ci-C6)-Alkyl, (Ci-C6)-Halogenalkyl, (C2-C6)-Alkenyl, (C2-C6)-Halogenalkenyl, (C2- C6)-Alkinyl, (C3-C6)-Halogenalkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Halogencycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, (C3-C6)-Halogencycloalkyl-(Ci-C6)-alkyl, COR1, OR1, OCOR1, OSO2R2, S(O)nR2, SO2OR1, SO2N(R1)2, NR1SO2R2, NR1COR1, (C1- C6)-Alkyl-S(O)nR2, (Ci-C6)-Alkyl-OR1, (d-CeO-Alkyl-OCOR1, (C1-C6)-Alkyl-OSO2R2, (CrC6)-Alkyl-COOR1, (C1-C6)-Alkyl-SO2OR1, (C1-C6)-Alkyl-CON(R1)2, (CrC6)-Alkyl- SO2N(R1)2, (d-C^-Alkyl-NR^OR1 oder (C1-C6)-Alkyl-NR1SO2R2, R1 bedeutet Wasserstoff, (CrC6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)- Cycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, Phenyl oder Phenyl-(d-C6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Cyano, Halogen, Nitro, Rhodano, OR3, S(O)nR4, N(R3)2, NR3OR3, COR3, OCOR3, SCOR3, NR3COR3, CO2R3, COSR3, CON(R3)2 und (C1-C-O-AIkOXy-(C2-C6)- alkoxycarbonyl substituiert sind,
R2 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Cycloalkyl-(C1-C6)-alkyl, Phenyl oder Phenyl-(C1-C6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Cyano,
Halogen, Nitro, Rhodano, OR3, S(O)nR4, N(R3)2, NR3OR3, COR3, OCOR3, SCOR3, NR3COR3, CO2R3, COSR3, CON(R3)2 und (C1-C4)-Alkoxy-(C2-C6)-alkoxycarbonyl substituiert sind, R3 bedeutet Wasserstoff, (d-C6)-Alkyl, (Ci-C6)-Haloalkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl,
R4 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl, n bedeutet 0, 1 oder 2, s bedeutet 0, 1 , 2 oder 3. 2. 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile nach Anspruch 1 , worin X und Y bedeuten unabhängig voneinander Nitro, Halogen, Cyano, (CrC6)- Alkyl, (C1-C6)-Halogenalkyl, (C2-C6)-Alkenyl, (C2-C6)-Halogenalkenyl, (C2-C6)-Alkinyl, (C3-C6)-Halogenalkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Halogencycloalkyl, (C3-C6)- Cycloalkyl-(Ci-C6)-alkyl, (C3-C6)-Halogencycloalkyl-(d-C6)-alkyl, COR1, OR1, OCOR1, OSO2R2, S(O)nR2, SO2OR1, (d-C6)-Alkyl-S(O)nR2, (d-C6)-Alkyl-OR1, (C1- C6)-Alkyl-OCOR1, (d-C6)-Alkyl-OSO2R2, (CrC6)-Alkyl-COOR1, (d-C6)-Alkyl- SO2OR1, (Ci-C6)-Alkyl-CON(R1)2 oder (d-C6)-Alkyl-NR1SO2R2,
R1 bedeutet Wasserstoff, (Ci-C6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)- Cycloalkyl, (C3-C6)-Cycloalkyl-(Ci-C6)-alkyl, Phenyl oder Phenyl-(d-C6)-alkyl, wobei die sieben letztgenannten Reste durch s Reste aus der Gruppe bestehend aus Halogen und OR3 substituiert sind,
R2 bedeutet (d-C6)-Alkyl, (C2-C6)-Alkenyl, (C2-C6)-Alkinyl, (C3-C6)-Cycloalkyl, (C3-C6)-Cycloalkyl-(d-C6)-alkyl, Phenyl oder Phenyl-(d-C6)-alkyl, wobei diese vorstehend genannten Reste durch s Reste aus der Gruppe bestehend aus Cyano, Halogen und OR3 substituiert sind,
R3 bedeutet Wasserstoff, (d-C6)-Alkyl, (d-C6)-Haloalkyl, (C2-C6)-Alkenyl oder (C2-C6)-Alkinyl, n bedeutet O, 1 oder 2, s bedeutet e 1 ,
2 oder 3.
3. 2-(3-Aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile nach Anspruch 1 oder 2, worin
X bedeutet Nitro, Fluor, Chlor, Brom, lod, Cyano, Methyl, Ethyl, Methoxy, Ethoxy, Trifluormethyl, Methylsulfonyl, Ethylsulfonyl, Methylsulfenylmethyl,
Methylsulfinylmethyl, Methylsulfonylmethyl, Y bedeutet Nitro, Fluor, Chlor, Brom, lod, Cyano, Methoxy, Ethoxy,
Trifluormethyl, Methylsulfonyl, Ethylsulfonyl.
4. Herbizide Mittel, gekennzeichnet durch einen herbizid wirksamen Gehalt an mindestens einer Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 3.
5. Herbizide Mittel nach Anspruch 4 in Mischung mit Formulierungshilfsmitteln.
6. Verfahren zur Bekämpfung unerwünschter Pflanzen, dadurch
gekennzeichnet, daß man eine wirksame Menge mindestens einer Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 3 oder eines herbiziden Mittels nach Anspruch 4 oder 5 auf die Pflanzen oder auf den Ort des unerwünschten
Pflanzenwachstums appliziert.
7. Verwendung von Verbindungen der Formel (I) gemäß einem der Ansprüche 1 bis 3 oder von herbiziden Mitteln nach Anspruch 4 oder 5 zur Bekämpfung
unerwünschter Pflanzen.
8. Verwendung nach Anspruch 7, dadurch gekennzeichnet, daß die
Verbindungen der Formel (I) zur Bekämpfung unerwünschter Pflanzen in Kulturen von Nutzpflanzen eingesetzt werden.
9. Verwendung nach Anspruch 8, dadurch gekennzeichnet, daß die Nutzpflanzen transgene Nutzpflanzen sind.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US22937709P | 2009-07-29 | 2009-07-29 | |
| EP09009776 | 2009-07-29 | ||
| EP09009776.7 | 2009-07-29 | ||
| US61/229,377 | 2009-07-29 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2011012248A2 true WO2011012248A2 (de) | 2011-02-03 |
| WO2011012248A3 WO2011012248A3 (de) | 2011-04-28 |
Family
ID=41338610
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2010/004446 WO2011012248A2 (de) | 2009-07-29 | 2010-07-21 | 2-(3-aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre verwendung als herbizide |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20110053778A1 (de) |
| AR (1) | AR079403A1 (de) |
| WO (1) | WO2011012248A2 (de) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013010882A2 (de) | 2011-07-15 | 2013-01-24 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2013104705A1 (de) | 2012-01-11 | 2013-07-18 | Bayer Intellectual Property Gmbh | Tetrazol-5-yl- und triazol-5-yl-arylverbindungen und ihre verwendung als herbizide |
| WO2015052178A1 (en) | 2013-10-10 | 2015-04-16 | Basf Se | 1,2,5-oxadiazole compounds and their use as herbicides |
| WO2015052173A1 (en) | 2013-10-10 | 2015-04-16 | Basf Se | Tetrazole and triazole compounds and their use as herbicides |
| WO2019080226A1 (zh) * | 2017-10-24 | 2019-05-02 | 青岛清原化合物有限公司 | 取代的苯甲酰基二酮腈类化合物或其互变异构体、盐、制备方法、除草组合物及应用 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10532976B2 (en) * | 2015-06-23 | 2020-01-14 | National Institute Of Biological Sciences, Beijing | FTO inhibitors |
| CN111087294A (zh) * | 2019-12-18 | 2020-05-01 | 浙江工业大学 | 一种高纯调环酸钙的制备方法 |
Citations (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0131624A1 (de) | 1983-01-17 | 1985-01-23 | Monsanto Co | Plasmide zur transformation von pflanzenzellen. |
| EP0142924A2 (de) | 1983-09-26 | 1985-05-29 | Mycogen Plant Science, Inc. | Insektresistente Pflanzen |
| EP0193259A1 (de) | 1985-01-18 | 1986-09-03 | Plant Genetic Systems N.V. | Modifikation von Pflanzen auf pentechnologischem Wege zur Bekämpfung oder zur Kontrolle von Insekten |
| EP0213892A2 (de) | 1985-08-27 | 1987-03-11 | Rohm And Haas Company | Enole mit herbizider Wirkung |
| EP0221044A1 (de) | 1985-10-25 | 1987-05-06 | Monsanto Company | Pflanzenvektoren |
| EP0242236A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| EP0305398A1 (de) | 1986-05-01 | 1989-03-08 | Honeywell Inc | Verbindungsanordnung für mehrere integrierte schaltungen. |
| EP0309862A1 (de) | 1987-09-30 | 1989-04-05 | Bayer Ag | Stilbensynthase-Gen |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| WO1991013972A1 (en) | 1990-03-16 | 1991-09-19 | Calgene, Inc. | Plant desaturases - compositions and uses |
| WO1991019806A1 (en) | 1990-06-18 | 1991-12-26 | Monsanto Company | Increased starch content in plants |
| EP0464461A2 (de) | 1990-06-29 | 1992-01-08 | Bayer Ag | Stilbensynthase-Gene aus Weinrebe |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| WO1992011376A1 (en) | 1990-12-21 | 1992-07-09 | Amylogene Hb | Genetically engineered modification of potato to form amylopectin-type starch |
| WO1992014827A1 (en) | 1991-02-13 | 1992-09-03 | Institut Für Genbiologische Forschung Berlin Gmbh | Plasmids containing dna-sequences that cause changes in the carbohydrate concentration and the carbohydrate composition in plants, as well as plant cells and plants containing these plasmids |
| WO1994014782A1 (en) | 1992-12-18 | 1994-07-07 | Rhone-Poulenc Agriculture Ltd. | 4-benzoyl isoxazoles derivatives and their use as herbicides |
| EP0625505A2 (de) | 1993-05-18 | 1994-11-23 | Rhone Poulenc Agriculture Ltd. | 2-Cyan-1,3-dion-Derivate und ihre Verwendung als Herbizid |
| WO1995016678A1 (en) | 1993-12-15 | 1995-06-22 | Rhone Poulenc Agriculture Limited | 4-benzoylisoxazoles and their use as herbicides |
| WO1995031446A1 (en) | 1994-05-17 | 1995-11-23 | Rhone Poulenc Agriculture Ltd. | 4-benzoylisoxazole derivatives and their use as herbicides |
| WO1997028136A1 (en) | 1996-01-30 | 1997-08-07 | Rhone-Poulenc Agriculture Ltd. | Benzoylisoxazoles and 2-cyano-1,3-dione derivatives and their use as herbicides |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9310203D0 (en) * | 1993-05-18 | 1993-06-30 | Rhone Poulenc Agriculture | Compositions of new matter |
| US5804532A (en) * | 1991-01-25 | 1998-09-08 | Rhone-Poulenc Agriculture Limited | Herbicidal 2-cyano-1,3-diones |
-
2010
- 2010-07-21 WO PCT/EP2010/004446 patent/WO2011012248A2/de active Application Filing
- 2010-07-27 AR ARP100102709A patent/AR079403A1/es unknown
- 2010-07-27 US US12/844,103 patent/US20110053778A1/en not_active Abandoned
Patent Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0131624A1 (de) | 1983-01-17 | 1985-01-23 | Monsanto Co | Plasmide zur transformation von pflanzenzellen. |
| EP0142924A2 (de) | 1983-09-26 | 1985-05-29 | Mycogen Plant Science, Inc. | Insektresistente Pflanzen |
| EP0193259A1 (de) | 1985-01-18 | 1986-09-03 | Plant Genetic Systems N.V. | Modifikation von Pflanzen auf pentechnologischem Wege zur Bekämpfung oder zur Kontrolle von Insekten |
| EP0213892A2 (de) | 1985-08-27 | 1987-03-11 | Rohm And Haas Company | Enole mit herbizider Wirkung |
| EP0221044A1 (de) | 1985-10-25 | 1987-05-06 | Monsanto Company | Pflanzenvektoren |
| EP0242236A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0242246A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0305398A1 (de) | 1986-05-01 | 1989-03-08 | Honeywell Inc | Verbindungsanordnung für mehrere integrierte schaltungen. |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| EP0309862A1 (de) | 1987-09-30 | 1989-04-05 | Bayer Ag | Stilbensynthase-Gen |
| WO1991013972A1 (en) | 1990-03-16 | 1991-09-19 | Calgene, Inc. | Plant desaturases - compositions and uses |
| WO1991019806A1 (en) | 1990-06-18 | 1991-12-26 | Monsanto Company | Increased starch content in plants |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| EP0464461A2 (de) | 1990-06-29 | 1992-01-08 | Bayer Ag | Stilbensynthase-Gene aus Weinrebe |
| WO1992011376A1 (en) | 1990-12-21 | 1992-07-09 | Amylogene Hb | Genetically engineered modification of potato to form amylopectin-type starch |
| WO1992014827A1 (en) | 1991-02-13 | 1992-09-03 | Institut Für Genbiologische Forschung Berlin Gmbh | Plasmids containing dna-sequences that cause changes in the carbohydrate concentration and the carbohydrate composition in plants, as well as plant cells and plants containing these plasmids |
| WO1994014782A1 (en) | 1992-12-18 | 1994-07-07 | Rhone-Poulenc Agriculture Ltd. | 4-benzoyl isoxazoles derivatives and their use as herbicides |
| EP0625505A2 (de) | 1993-05-18 | 1994-11-23 | Rhone Poulenc Agriculture Ltd. | 2-Cyan-1,3-dion-Derivate und ihre Verwendung als Herbizid |
| WO1995016678A1 (en) | 1993-12-15 | 1995-06-22 | Rhone Poulenc Agriculture Limited | 4-benzoylisoxazoles and their use as herbicides |
| WO1995031446A1 (en) | 1994-05-17 | 1995-11-23 | Rhone Poulenc Agriculture Ltd. | 4-benzoylisoxazole derivatives and their use as herbicides |
| WO1997028136A1 (en) | 1996-01-30 | 1997-08-07 | Rhone-Poulenc Agriculture Ltd. | Benzoylisoxazoles and 2-cyano-1,3-dione derivatives and their use as herbicides |
Non-Patent Citations (6)
| Title |
|---|
| BRAUN ET AL., EMBO J., vol. 11, 1992, pages 3219 - 3227 |
| CHEMFILES, vol. 4, no. 1 |
| CHRISTOU, TRENDS IN PLANT SCIENCE, vol. 1, 1996, pages 423 - 431 |
| SONNEWALD ET AL., PLANT J., vol. 1, 1991, pages 95 - 106 |
| WEED RESEARCH 26, 1986, pages 441 - 445 |
| WOLTER ET AL., PROC. NATL. ACAD. SCI. USA, vol. 85, 1988, pages 846 - 850 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013010882A2 (de) | 2011-07-15 | 2013-01-24 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2013104705A1 (de) | 2012-01-11 | 2013-07-18 | Bayer Intellectual Property Gmbh | Tetrazol-5-yl- und triazol-5-yl-arylverbindungen und ihre verwendung als herbizide |
| WO2015052178A1 (en) | 2013-10-10 | 2015-04-16 | Basf Se | 1,2,5-oxadiazole compounds and their use as herbicides |
| WO2015052173A1 (en) | 2013-10-10 | 2015-04-16 | Basf Se | Tetrazole and triazole compounds and their use as herbicides |
| WO2019080226A1 (zh) * | 2017-10-24 | 2019-05-02 | 青岛清原化合物有限公司 | 取代的苯甲酰基二酮腈类化合物或其互变异构体、盐、制备方法、除草组合物及应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2011012248A3 (de) | 2011-04-28 |
| US20110053778A1 (en) | 2011-03-03 |
| AR079403A1 (es) | 2012-01-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2791119B1 (de) | N-(1,2,5-oxadiazol-3-yl)-, n-(1,3,4-oxadiazol-2-yl)-, n-(tetrazol-5-yl)- und n-(triazol-5-yl)-arylcarbonsäureamide und ihre verwendung als herbizide | |
| CN103596946B (zh) | N-(1,3,4-噁二唑-2-基)芳基甲酰胺及其作为除草剂的用途 | |
| EP2691379B1 (de) | Herbizid und fungizid wirksame 3-phenylisoxazolin-5-carboxamide und 3- phenylisoxazolin-5-thioamide | |
| EP2379508B1 (de) | Herbizid und insektizid wirksame 4-phenylsubstituierte pyridazinone | |
| EP2773625B1 (de) | 5-phenylsubstituierte n-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| EP2686315B1 (de) | N-(1,2,5-oxadiazol-3-yl)-, n-(tetrazol-5-yl)- und n-(triazol-5-yl)bicycloaryl-carbonsäureamide und ihre verwendung als herbizide | |
| WO2012123416A1 (de) | N-(1,2,5-oxadiazol-3-yl)pyridincarboxamide und ihre verwendung als herbizide | |
| EP2739611A1 (de) | N-(tetrazol-5-yl)- und n-(triazol-5-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| TWI478907B (zh) | 4-(3-取代的苯甲醯基)吡唑類及其作為除草劑之用途 | |
| WO2013124245A1 (de) | Herbizid wirksame 4-nitro substituierte n-(tetrazol-5-yl)-, n-(triazol-5-yl)- und n-(1,3,4-oxadiazol-2-yl)arylcarbonsäureamide | |
| WO2009149806A2 (de) | Herbizid wirksame 4- (3-alkylsulfinylbenzoyl) pyrazole | |
| EP2260027B1 (de) | Herbizid wirksame 4- (3-aminobenzoyl) -5-cyclopropylisoxazole | |
| EP3601242A1 (de) | Substituierte n-(1,3,4-oxadiazol-2-yl)arylcarbonsäureamide und ihre verwendung als herbizide | |
| WO2011012248A2 (de) | 2-(3-aminobenzoyl)-3-cyclopropyl-3-oxopropannitrile und ihre verwendung als herbizide | |
| EP2802569B1 (de) | Tetrazol-5-yl- und triazol-5-yl-arylverbindungen und ihre verwendung als herbizide | |
| EP2459528A1 (de) | 2-(3-alkylthiobenzoyl)cyclohexandione und ihre verwendung als herbizide | |
| EP2480522B1 (de) | 3-amino-2-nitro-substituierte benzoylderivate und ihre verwendung als herbizide | |
| EP2536277B1 (de) | 3-aminocarbonyl substituierte benzoylcyclohexandione und ihre verwendung als herbizide | |
| EP2595955A1 (de) | (4-halogenalkyl-3-thiobenzoyl)cyclohexandione und ihre verwendung als herbizide | |
| WO2013124246A1 (de) | Herbizid wirksame 4-dialkoxymethyl-2-phenylpyrimidine |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10737776 Country of ref document: EP Kind code of ref document: A2 |
|
| DPE1 | Request for preliminary examination filed after expiration of 19th month from priority date (pct application filed from 20040101) | ||
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 10737776 Country of ref document: EP Kind code of ref document: A2 |